DOI: 10.31146/1682-8658-ecg-171-11-100-134
Проект рекомендаций российского общества детских гастроэнтерологов, гепатологов и нутрициологов по диагностике и лечению болезни Крона у детей
Корниенко Е. А.1, Хавкин А. И.2, Федулова Е. Н.3, Волынец Г. В.2, Габрусская Т. В.1, Скворцова Т. А.4, Никитин А. В.4, Сорвачева Т. Н.5, Цимбалова Е. Г.2, Щербакова О. В.2
1 Санкт-Петербургский Государственный педиатрический медицинский университет МЗ РФ
2 Российский национальный исследовательский медицинский университет им. Н. И. Пирогова МЗ РФ
3 Приволжский исследовательский медицинский университет МЗ РФ
4 Морозовская детская городская клиническая больница ДЗ гор. Москвы
5 Российская медицинская академия непрерывного профессионального образования МЗ РФ
Draft recommendations of the russian society of pediatric gastroenterology, hepatology and nutrition on diagnosis and treatment of Crohn's disease in children
Elena A. Kornienko1, Anatoly I. Khavkin2, Elvira N. Fedulova3, Galina V. Volynets2, Tatyana V. Gabruskaya1, Tamara A. Skvortsova4, Artem V. Nikitin4, Tatyana N. Sorvacheva5, Ekaterina G. Tsimbalova2, Olga V. Shcherbakova2
1 St. Petersburg State Pediatric Medical University of the Ministry of Health of the Russian Federation.
2 Pirogov Russian National Research Medical Universityof the Ministry of Health of the Russian Federation.
3 Volga Research Medical University of the Ministry of Health of the Russian Federation.
4 Morozov Children’s City Clinical Hospital, Moscow
5 Russian Medical Academy of Continuing Professional Education, Ministry of Health of the Russian Federation
Для цитирования: Корниенко Е. А., Хавкин А. И., Федулова Е. Н., Волынец Г. В., Габрусская Т. В., Скворцова Т. А., Никитин А. В., Сорвачева Т. Н., Цимбалова Е. Г., Щербакова О. В. Проект рекомендаций российского общества детских гастроэнтерологов, гепатологов и нутрициологов по диагностике и лечению болезни Крона у детей. Экспериментальная и клиническая гастроэнтерология. 2019;171(11): 100–134. DOI: 10.31146/16828658-ecg-171-11-100-134
For citation: Kornienko Elena A., Khavkin Anatoly I., Fedulova Elvira N., Volynets Galina V., Gabruskaya Tatyana V., Skvortsova Tamara A., Nikitin Artem V., Sorvacheva Tatyana N., Tsimbalova Ekaterina G., Shcherbakova Olga V. Draft recommendations of the russian society of pediatric gastroenterology, hepatology and nutrition on diagnosis and treatment of Crohn's disease in children. Experimental and Clinical Gastroenterology. 2019;171(11): 100–134. (In Russ.)
DOI: 10.31146/1682-8658-ecg-171-11-100-134
Корниенко Елена Александровна, д.м.н., профессор кафедры детских болезней им. проф. И. М. Воронцова;
ORCID ID: 0000–0003–2743–1460
Хавкин Анатолий Ильич, д.м.н., профессор, руководитель отдела гастроэнтерологии Научно-исследовательского клинического института педиатрии имени академика Ю. Е. Вельтищева; ORCID: 0000–0001–7308–7280
Федулова Эльвира Николаевна, д.м.н., главный научный сотрудник отдела «Ревматологических и других системных заболеваний»; ORCID: 0000–0002–1774–0692
Волынец Галина Васильевна, д.м.н., главный научный сотрудник отдела гастроэнтерологии Научноисследовательского клинического института педиатрии им. Академика Ю. Е. Вельтищева; ORCID ID: 0000–0002–5413–9599 Габрусская Татьяна Викторовна, к.м.н. врач 5 отделения гастроэнтерологии клиники; ORCID ID: 0000–0002–7931–2263 Скворцова Тамара Андреевна, к.м.н., врач-гастроэнтеролог, заведующая гастроэнтерологическим отделением;
ORCID ID: 0000–0002–6525–8665
Никитин Артём Вячеславович, к.м.н., врач-гастроэнтеролог гастроэнтерологического отделения;
ORCID: 0000–0001–8837–9243
Сорвачева Татьяна Николаевна, д.м.н., заведующая кафедрой диетологии и нутрициологии; ORCID: 0000–0001–5587–3560
Цимбалова Е. Г., к.м.н., заведующая отделением гастроэнтерологии; ORCID: 0000–0001–7388–2006
Щербакова Ольга Вячеславовна, к.м.н., Заведующая хирургическим отделением № 1 (колопроктология); ORCID https:// orcid.org/0000–0002–8514–3080
Elena A. Kornienko, MD, PhD, Dr Sci, professor of the department of childhood diseases named after prof. IM. Vorontsov;
ORCID ID: 0000–0003–2743–1460
Anatoly I. Khavkin, MD, PhD, Dr Sci, Prof, Chief Researcher, Head of the Department of Gastroenterology, Veltishev Scientific Research Clinical Pediatric Institute; ORCID: 0000–0001–7308–7280
Elvira N. Fedulova, MD, PhD, Dr Sci, Chief Researcher at the Department of Rheumatological and Other Systemic Diseases of the Ministry of Health of Russia; ORCID: 0000–0002–1774–0692
Galina V. Volynets,MD,PhD, Dr Sci, Chief Researcher, department of gastroenterology, Veltishev Scientific Research Clinical Pediatric Institute; ORCID ID: 0000–0002–5413–9599
Tatyana V. Gabruskaya, MD, PhD, gastroenterologist 5 of the Department of Gastroenterology; ORCID ID: 0000–0002–7931–2263
Tamara A. Skvortsova,MD, PhD, Head of the Department of Gastroenterology; ORCID ID: 0000–0002–6525–8665
Artem V. Nikitin, MD, gastroenterologist of the gastroenterological department; ORCID: 0000–0001–8837–9243
Tatyana N. Sorvacheva, MD, PhD, Dr Sci, Head of the Department of Dietetics and Nutritionology; ORCID: 0000–0001–5587–3560
Ekaterina G. Tsimbalova, MD, PhD, Head of the Department of Gastroenterology; ORCID: 0000–0001–7388–2006
Olga V. Shcherbakova, MD, PhD, Head of the Department of Coloproctolology; ORCID https://orcid.org/0000–0002–8514–3080
Резюме
В статье представлен финальный вариант проект протокола по диагностике и лечению болезни Крона у детей, разработанный экспертами Российского общества детских гастроэнтерологов, гепатологов и нутрициологов. Данный проект неоднократно обсуждался детскими гастроэнтерологами — специалистами в области изучения воспалительных заболеваний кишечника у детей во время круглых столов на XXV-м и XXVI-м Конгрессах детских гастроэнтерологов России и, после окончательного утверждения, будет представлен в виде клинических рекомендаций.
Ключевые слова: Болезнь Крона у детей, проект рекомендаций по диагностике и лечению, клинические рекомендации
Summary
The final version of the draft protocol for the diagnosis and treatment of Crohn’s disease in children, developed by experts of the Russian Society of Pediatric Gastroenterology, Hepatology and Nutrition, is presented in the article. This project has been repeatedly discussed by pediatric gastroenterologists — specialists in the study of IBD in children during round tables at the XXV-th and XXVI-th Congres of Pediatric Gastroenterologists of Russia and, after final approval, will be presented in the form of clinical recommendations.
Keywords: Crohn’s disease in children, draft recommendations for diagnosis and treatment, clinical recommendations
1. Введение
Во всем мире наблюдается рост частоты воспалительных заболеваний кишечника (ВЗК) у детей, в частности – болезни Крона (БК), заболеваемость которой варьирует от 1,5 до 11,4 на 100000[1, 2], при этом расчетное значение распространенности БК составляет 58/100000. Точных данных о распространенности БК у детей в России нет, но отдельные региональные наблюдения указывают на аналогичную тенденцию. Так, в Санкт-Петербурге заболеваемость БК возросла за последние 10 лет более чем в 10 раз и составила 5,5 на 100000, а распространенность– 20 на 100000 детей и подростков [3]. Примерно у 25% больных БК впервые манифестирует в возрасте до 18 лет, за последние 10 лет ВЗК с началом в детском возрасте возросли в 3 раза [4]. В детском возрасте ВЗК характеризуются более агрессивным течением, чем у взрослых, процесс име-
1.1. Термины и определение
Болезнь Крона (БК) – хроническое, рецидивирующее заболевание желудочно-кишечного тракта
ет более распространенный характер, склонен к прогрессирующему нарастанию тяжести. Заболевание сопряжено с высоким риском развития осложнений и требует интенсивной терапии, в частности, назначения глюкокортикостероидов, иммуносупрессоров и антицитокиновых препаратов [5,6].У пациентов с дебютом БК в детском возрасте также более высока вероятность осложнений, требующих хирургического вмешательства. Риск резекции части кишки при данной патологии к 30 годам составляет 48 ± 5% по сравнению с 14 ± 2% у взрослых [7].
Своевременная диагностика и адекватная терапия способны существенно повлиять на течение БК. Выбор терапии должен осуществляться с учетом локализации и активности процесса, индивидуальных особенности пациента (возраст и имеющиеся факторы риска).
неясной этиологии, характеризующееся трансмуральным, сегментарным, гранулематозным
воспалением с развитием местных и системных осложнений.
Обострение (рецидив, атака) БК – это появление типичных симптомов заболевания впервые или у больных БК в стадии клинической ремиссии, спонтанной или медикаментозно поддерживаемой.
1.2. Этиология и патогенез
Этиология воспалительных заболеваний кишечника (ВЗК), в том числе БК, точно не установлена. Заболевание развивается в результате сочетанного влияния нескольких факторов, включающих генетическую предрасположенность, дефекты врожденного и приобретенного иммунитета, нарушение состояния микробиоты и влияние неблагоприятных факторы окружающей среды. Кишечная микробиота у всех больных с БК характеризуются уменьшением видового разнообразия, уменьшением числа толерогенных видов (например, Faecalibacteriumprausnitzii, Bacteroidesthetaiotaomicron), увеличением жгутиковых бактерий и микробов, пенетрирующих слизистый слой, изменением вирома, усилением проницаемости слизистой. [9].
Выявлено более 100 генов, предрасполагающих к ВЗК, большинство из которых контролирует взаимодействие иммунной системы с внешними антигенами. С большей частотой встречаются мутации NOD2, IL23R, ATG16L1, IRGM, NKX2–3, 1q24,
5p13, HERC2, CCNY, 10q21. Более 50% генов, определяющих риск к развитию ВЗК, ассоциированы и с другими воспалительными и аутоиммунными заболеваниями, что может объяснить развитие внекишечных проявлений ВЗК [10]. При этом каких-либо специфических генетических особенностей, свойственных детям (за исключением детей раннего возраста) обнаружено не было.
Хроническое воспаление при ВЗК является следствием аномальной и пролонгированной активации иммунной системы кишечника.
Ремиссия БК – исчезновение типичных проявлений заболевания:
• клиническая – отсутствие симптомов БК (соответствует значению Педиатрического Индекса активности БК (PCDAI) <10 (см. ниже);
• эндоскопическая – отсутствие видимых макроскопических признаков воспаления при эндоскопическом исследовании [8].
Многочисленные исследования продемонстрировали, что нарушения имеют место практически во всех звеньях иммунного ответа [11], начиная от барьерных функций эпителия и распознавания антигена паттерн-распознающими рецепторами, передачи сигнала дендритными клетками и сигнальными молекулами, презентации антигена HLA, и заканчивая функциями моноцитов-макрофагов, Ти В-лимфоцитов. Образование инфламмасом, активация каспазы-1 и секреции провоспалительных цитокинов: IL-1, IL-17, IL-23, IL-6, TNF-a обусловливают развитие трансмуральной воспалительной инфильтрации стенки кишки. Младенческие формы ВЗК могут быть обусловлены нарушением формирования иммунологической толерантности к собственной микробиоте кишечника вследствие мутации отдельных генов, например, IL-10, FOXP3, XIAP и др [12].
Каскад гуморальных и клеточных реакций при БК приводит к трансмуральному воспалению кишечной стенки с образованием характерных для БК саркоидных гранулем, состоящих из эпителиоидных гистиоцитов без очагов некроза и гигантских клеток.
При БК могут поражаться любые отделы желудочно-кишечного тракта – от полости рта до ануса. Тем не менее, в подавляющем большинстве случаев у детей доминирует поражение илеоцекального отдела (70%), изолированное поражение толстой кишки встречается в 30%, аноректальной области – у 20%, поражение верхних отделов ЖКТ– у 5–15% [3].
1.3. Целевая аудитория клинических рекомендаций:
1. Гастроэнтерологи
2. Врачи педиатры
3. Врачи общей практики (семейные врачи)
4. Колопроктологи
5. Детские хирурги
6. Эндоскописты
7. Медицинские работники со средним медицинским образованием
8. Организаторы здравоохранения
9. Врачи-эксперты медицинских страховых организаций (в том числе при проведении медико-экономической экспертизы).
1.4. Методология составления клинических рекомендаций
Рекомендации составлены на основании: данных Европейского доказательного консенсуса по диагностике и лечению БК у детей [2], представленного совместнос Европейским обществом по изучению язвенного колита и болезни Крона и Европейским обществом педиатров гастроэнтерологов, гепатологов и нутрициологов (ESPGHAN, 2014), рекомендаций Всемирной Организации Здравоохранения по воспалительным заболеваниям кишечника (2015г)
[4] данных литературы и Российских рекомендаций
по диагностике и лечению болезни Крона у взрослых пациентов (2017г) [8].
Клинические рекомендации отражают мнение экспертов по ключевым вопросам. В клинической практике могут возникать ситуации, выходящие за рамки представленных рекомендаций, поэтому окончательное решение о тактике ведения каждого пациента должен принимать лечащий врач, на котором лежит ответственность за адеватность проводимого лечения.
Уровень Диагностическое исследование Терапевтическое исследование
Систематический обзор гомогенных диагности- Систематический обзор гомогенных РКИ
ческих исследований 1 уровня
Таблица 1.
Уровни достоверности доказательств (Оксфорд-
Валидизирующее когортное исследование с каче1b ственным «золотым» стандартом
Специфичность или чувствительность столь вы1с соки, что положительный или отрицательный ре-
зультата позволяет исключить/установить диагноз
Отдельное РКИ (с узким ДИ) Исследование «Все или ничего»
ский центр доказательной медицины) [95]
Систематический обзор гомогенных диагностических исследований >2 уровня
Разведочное когортное исследование с каче2b ственным «золотым» стандартом
Систематический обзор (гомогенных) когортных исследований
Отдельное когортное исследование (включая РКИ низкого качества; т.е. с <80% пациентов, прошедших контрольное наблюдение)
нет Исследование «исходов»; экологические исследования
Систематический обзор гомогенных исследований уровня 3b и выше
Исследование с непоследовательным набором 3b или без проведения исследования «золотого
стандарта у всех испытуемых
Исследование случай-контроль или исследо-
4 вание с некачественным или не независимым
«золотым» стандартом
Мнение экспертов без тщательной критической оценки или основанное на физиологии, лабораторные исследования на животных или разработка «первых принципов»
Систематический обзор гомогенных исследований «случай-контроль»
Отдельное исследование «случай-контроль»
Серия случаев (и когортные исследования или исследования «случай-контроль» низкого качества)
Мнение экспертов без тщательной критической оценки, лабораторные исследования на животных или разработка «первых принципов»
2. Классификация
В педиатрической практике рекомендуется использовать международную классификацию болезни Крона, принятую в 2010г в Париже.
Для верификации периода заболевания (обострение или ремиссия), оценки тяжести обострения, а также для динамической оценки эффективности лечения рекомендуется расчет Педиатрического индекса активности болезни Крона (PCDAI) [2].
Интерпретация PCDAI:
▷ <10: отсутствие активности (ремиссия)
▷ 11–30: легкая или среднетяжелая форма
▷ 30–100: тяжелая форма
• Клинический ответ на лечение:
▷ Снижение индекса PCDAI ≥ 15 баллов по сравнению с исходным; суммарный индекс PCDAI
≤ 30 баллов
• Клиническая ремиссия:
▷ PCDAI ≤ 10 баллов
• Утрата ответа на лечение:
▷ Увеличение PCDAI ≥ 15 баллов или PCDAI> 30 баллов
Критерий Градации Сочетания Таблица 2.
Возраст
До 16л – А1
А1а – до 10 лет
А1b – от 10 до 17 лет 17–40л – А2
Go – нет нарушений роста, G1 – есть нарушения роста
Классификация болезни
Крона
Старше 40л – А3
Локализация
Терминальный илеит – L1 Изолированный колит – L2 Илеит и колит – L3 Верхние отделы – L4:
L4a – поражение выше связки Трейца
L4b – поражение ниже связки Трейца, но выше дистальной 1/3 подвздошной кишки
L1+L4 L2+L4 L3+L4
L4ab
Перианальные изменения – р
Форма
Нестенозирующая и
Непенетрирующая (воспалительная) –В1 Стенозирующая – В2
Пенетрирующая – В3
B2B3 – сочетание стеноза и пенетрации
Сочетание с перианальным поражением В1р, В2р, В3р
Таблица 3.
Педиатрический индекс
Критерии балл
нет 0
активности болезни Крона PCDAI
Боли в животе
Стул, частота, консистенция
Самочувствие, активность
Масса тела
Рост
Болезненность в животе
Малой интенсивности 5 Сильной интенсивности 10
0–1 раза в день, жидкий без примесей крови 0
2–5 раза в день, с небольшой примесью крови 5 Более 6 раза в день 10
Нет ограничения активности 0
Умеренное ограничение активности 5 Значительное ограничение активности 10
Нет снижения массы тела 0
Снижение массы тела на 1–9% 5 Снижение массы тела более 10% 10
Ниже одного центеля 0
От 1–2 центелей 5 Ниже двух центелей 10
Нет болезненности 0
Болезненность, отмечается уплотнение 5 Выраженная болезненность 10
Параректальные проявления нет 0
Активная фистула, болезненность, абсцесс 10
нет 0
Внекишечные проявления
Гематокрит у детей до 10 лет
Гематокрит (девочки 11–18 лет)
Гематокрит (мальчики 11–14 лет)
Гематокрит (мальчики 15–18 лет)
СОЭ (мм/час)
Альбумин (г/дл)
одно 5
Более двух 10
>33 0
28–32 2,5
<28 5
>34 0
29–34 2.5
<29 5
>35 0
30–34 2,5
<30 5
>37 0
32–36 2,5
<32 5
<20 0
20–50 2,5
>50 5
>3.5 0
3.1–3.4 5
<3.0 10
3. Диагностика
Однозначных диагностических критериев БК не существует, и диагноз ставится на основании сочетания данных анамнеза, клинической картины и типичных эндоскопических и гистологических изменений [13, 14].
Существуют критерии достоверного диагноза БК по Lennard-Jones, включающие определение шести ключевых признаков заболевания [15].
1. Поражение любого отдела ЖКТ от полости рта до анального канала: хроническое гранулематозное поражение слизистой оболочки губ или щек; пилородуоденальное поражение, поражение тонкой кишки, хроническое перианальное поражение;
3.1. Клиника
К наиболее частым клиническим симптомам БК у детей относятся [2]:
2. Прерывистый характер поражения ЖКТ;
3. Трансмуральный характер поражения: афтозные язвы, язвы-трещины, абсцессы, свищи;
4. Фиброз: стриктуры;
5. Лимфоидное: трансмуральное воспаление, лимфоидные скопления;
6. Муцин: нормальное содержание муцина в зоне активного воспаления слизистой оболочки толстой кишки;
7. Обнаружение неказеозной гранулемы.
Диагноз БК считается достоверным при наличии трех любых признаков или при обнаружении гранулемы в сочетании с любым другим признаком.
• длительная хроническая диарея (более 6 нед), чаще без примеси крови,
Аутоиммунные, связанные с активностью заболевания:
Артропатии (артралгии, артриты) Поражение кожи (узловатая эритема, гангренозная пиодермия) Поражение слизистых (афтозный стоматит)
Поражение глаз (увеит, ирит, иридоциклит, эписклерит)
Аутоиммунные, не связанные с активностью заболевания:
Анкилозирующий спондилит (сакроилеит)
Первичный склерозирующий холангит (редко)
Остеопороз, остеомаляция Псориаз
Обусловленные длительным воспалением иметаболическими нарушениями:
Холелитиаз
Стеатоз печени, стеатогепатит Тромбоз периферических вен, тромбоэмболия легочной артерии Амилоидоз
Таблица 4. Внекишечные проявления болезни Крона
• боль в животе упорного характера с четкой локализацией,
• потеря массы, значительный дефицит массы тела, отставание в росте
• длительная лихорадка неясного генеза
• анемия, чаще железодефицитная
• перианальные осложнения (хронические анальные трещины, парапроктит, свищи прямой кишки).
Практические аспекты:
Клиническая картина на ранних этапах развития БК может быть стертой, симптоматика неспецифичной, что затрудняет своевременную диагностику. Иногда БК протекает латентно, проявляясь лишь задержкой физического развития ребенка, иногда первыми симптомами могут быть осложнения. К осложнениям БК относят: наружные свищи (кишечно-кожные), внутренние свищи (межкишечные, кишечнопузырные, ректо-вагинальные), инфильтрат брюшной полости, межкишечные или интраабдоминальные абсцессы, стриктуры ЖКТ (с нарушением кишечной проходимости и без таковой), анальные трещины, парапроктит (при аноректальном поражении), кишечное кровотечение (редко).
Примерно у четверти детей с БК обнаруживаются внекишечные проявления болезни [2] (табл. 4).
Аутоиммунные проявления, связанные с активностью воспалительного процесса, появляются вместе с основными кишечными симптомами обострения и исчезают вместе с ними на фоне лечения. Аутоиммунные проявления, не связанные с активностью процесса (сопутствующими аутоиммунными заболеваниями), имеют тенденцию к прогрессированию независимо от фазы основного заболевания (обострение или ремиссия) и часто определяют неблагоприятный прогноз болезни.
3.2. Лабораторная диагностика
Практические аспекты:
Изменения в лабораторных данных при БК имеют неспецифический характер. В общем анализе крови могут быть обнаружены анемия (чаще железодефицитная или анемии хронического заболевания, реже В-12или фолиеводефицитная), лейкоцитоз (на фоне хронического воспаления, при наличии абсцесса или на фоне стероидной терапии), ускорение СОЭ. Биохимическое исследование позволяет выявить повышение С-реактивного белка (СРБ), диспротеине-
мию (в частности, гипоальбуминемию и повышение a2и γ-глобулинов). При поражении печени может быть повышен уровень АЛТ, АСТ, ГГТП, билирубина. При остром начале диареи выполняется анализ кала для исключения острой кишечной инфекции, исследование токсинов А и В Cl.difficile (при недавно проведенном курсеантибиотикотерапии или пребывании в стационаре для исключения псевдомембранозного колита). Исключаются паразитарные инвазии.
3.3. Инструментальная диагностика
3.4. Иная диагностика
Дополнительные инструментальные и лабораторные исследования выполняются преимущественно с целью проведения дифференциальной диагностики
с рядом заболеваний. К ним относят: язвенный колит, острые кишечные инфекции (дизентерия, сальмонеллез, кампилобактериоз, йерсиниоз, амебиаз, парази-
Таблица 5. Макроскопические Микроскопические
Макрои микроскопические
признаки болезни Крона у детей
Специфические:
• Афтозные язвы
• Щелевидные линейные или извитые язвы
• Булыжная мостовая в терминальном илеуме
• Стеноз с престенотической дилатацией
• Утолщение стенки кишки с сужением просвета
• Перианальные поражения (свищи, абсцессы, язвы или стеноз анального канала)
• Язвы в тощей или подвздошной кишках
Неспецифические:
• Отек
• Гиперемия
• Ранимость
• Гранулярность
• Локальная потеря сосудистого рисунка
Специфические:
• Неказеозные гранулемы на расстоянии от крипт
• Очаговость и неравномерность воспаления
• Трансмуральный характер инфильтрата
• Подслизистый фиброз
Неспецифические:
• Гранулема, прилежащая к разрыву крипты
• Слабый воспалительный инфильтрат в собственной пластинке СОК
• Эрозии и поверхностные язвы СОК
• Нрушение архитектоники крипт, уменьшение бокаловидных клеток, метаплазия клеток Панета
тозы), Cl. difficile-ассоциированная диарея, цитомегаловирусный колит, туберкулез кишечника, системные васкулиты, неоплазии толстой и тонкой кишки, бо-
лезнь Бехчета, аппендицит, синдром раздраженного кишечника, целиакия, эозинофильные поражения, первичные иммунодефицитные состояния.
4. Лечение
4.1. Цель лечения БК у детей – это:
• Максимально быстрое достижение «глубокой» ремиссии, под которой подразумевается не только клиническая, но и морфологическая (эндоскопическая и гистологическая) ремиссия.
• Как можно более длительное поддержание ремиссии.
• Профилактика осложнений.
• Улучшение качества жизни.
• Обеспечение нормальных темпов роста и развития ребенка.
Выбор терапии должен проводиться с учетом факторов риска неблагоприятного течения БК. По мнению экспертов ESPGHAN [2], это:
• глубокое язвенное поражение толстой кишки при эндоскопическом исследовании
• сохраняющееся тяжелое течение заболевания, несмотря на адекватную индукционную терапию
4.2. Индукция ремиссии
4.2.1. Лечебное питание
• распространенное поражение (тотальное поражение тонкой кишки)
• значительное замедление линейного роста (показатель отклонения роста Z > –2,5)
• тяжелый остеопороз
• стенозирующее и (или) пенетрирующее течение на момент дебюта заболевания (течение заболевания B2 и/или B3)
• тяжелое поражение перианальной области.
Наличие даже одного из этих факторов позволяет предположить неблагоприятный исход заболевания, что должно послужить основанием для оптимизации проводимой терапии и применения препаратов, которые, как было установлено, изменяют естественное течение заболевания, таких как иммуносупрессоры и биологические препараты, а при осложнениях – соответствующей операции.
Практические аспекты:
1. При лечении всех детей с воспалительным поражением кишечника, включая поражение толстой кишки, для достижения заживления слизистой оболочки, нормализации минеральной плотности костной ткани и роста должно отдаваться предпочтение ПЭП, а НЕ глюкокортикостероидам. Однако в отношении эффективности ПЭП у пациентов с тяжелым изолированным панколитом при болезни Крона достоверные данные отсутствуют. Также отсутствуют данные о пользе применения ПЭП при изолированном поражении ротовой полости или перианальной области.
2. Продолжительность ПЭП при его применении для индукции ремиссии обычно составляет 6–10 недель. Большинство детей нуждается в среднем в 120% от нормы потребности поступления нутриентов, тем не менее, содержание пищевых веществ в рационе должно учитывать индивидуальные особенности ребенка. Обычные
продукты питания могут быть осторожно повторно применены во времяпервой и третьей недели курса лечебного питания. Это зависит от симптомов заболевания и состояния пациента в данный период времени
3. Выбор смеси для ПЭП осуществляется между специализированными полимерными, содержащими специальные противовоспалительные факторы (например, ModulenIBD с противовосполительным трансформирующим фактором роста β-2), полимерными, полуэлементными (например, Пептамен Юниор) или элементными (EO28 и др.) видами смесей в зависимости от степени и уровня поражения.
Питательные смеси следует вводить через рот (сиппинг), дробно в течение дня. Предпочтительны специализированные для данной патологии смеси, содержащие противовосполительный трансформирующий фактор роста. Полуэлементные
и элементные смеси имеют преимущество при непереносимости белка коровьего молока.
Кормление через назогастральный зонд или гастротому, в том числе и в режиме ночной алиментации, может применяться при непереносимости вкуса или невозможности достижения адекватного объема смеси при ее введении через рот. Однако решение о применении данного пути введения или альтернативных мето-
дов лечения следует принимать индивидуально с учетом качества жизни пациента.
4.2.1.1. Эффективность ПЭП
До настоящего времени не было проведено ни одного рандомизированного плацебо-контролируемого исследования (РКИ) полного энтерального питания (ПЭП) с использованием только жидких питательных смесей у детей, страдающих БК, однако было проведено несколько РКИ, в которых сравнивали ПЭП со стандартным лечением. Анализ результатов этих исследований был проведен в трех мета-анализах [17–19] при этом суммарная частота достижения ремиссии составила 73% (относительный риск (ОР) 0,95, 95% доверительный интервал (ДИ) 0,67–1,3428 и ОР 0,97, 95% ДИ 0,7–1,4). В послед-
ний мета-анализ было включено семь РКИ с общим количеством пациентов, равным 204 (100 в группе глюкокортикостероидов, 104 в группе энтерального питания; возраст от 4 до 18,6 лет), в которых проводилось сравнительное применение элементных (аминокислотных) [20–22], полуэлементных (гидролизованных) [23–24] или полимерных жидких смесей [25] и терапии глюкокортикостероидами. В данных исследованиях наблюдались существенные различия в отношении продолжительности лечения (варьировала от 3 до 10 недель), локализации и продолжительности заболевания (впервые выявленное заболевание или рецидив заболевания), а также в отношении сопутствующей терапии. Тем не менее, общий вывод заключался в том, что ПЭП и глюкокортикостероиды обладают примерно равной эффективностью в достижении индукции ремиссии у детей с БК [18, 19].
Информация о продолжительности ремиссии после применения ПЭП, представленная в литературных источниках, противоречива, при этом в некоторых исследованиях период времени до возникновения рецидива был более коротким [20,22]. по сравнению с глюкокортикостероидами, а в некоторых – более продолжительным [34]. В течение 10 месяцев после ПЭП у 39% пациентов наблюдался рецидив заболевания.
Помимо индукции ремиссии, отмечено влияние ПЭП на заживление слизистой оболочки
4.2.1.2. Варианты лечения
При проведении РКИ [26–28], открытых исследований у детей [29] и мета-анализов данных, полученных в исследованиях у взрослых, не было доказано, что источник белка (т.е. полимерные или элементные смеси) оказывает влияние на эффективность. Кроме того, полимерные смеси лучше переносятся, более экономичны, и реже возникает необходимость их введения через назогастральный зонд [29].
4. Если клинически ответ при использовании ПЭП в течение 2 недель отсутствует, следует решить вопрос о применении альтернативных методов лечения.
5. Доказательная база в отношении перехода к обычному питанию после завершения применения ПЭП отсутствует. Эксперты ESPGHANпредлагают постепенное введение обычной пищи одновременно с уменьшением объема питательной смеси каждые 2–3 дня в течение 2–3 недель.
кишечника, восстановление минерализации костной ткани и улучшений показателей роста и массы тела без характерных для кортикостероидов побочных эффектов терапии [234].
Исследовательская группа Европейского общества энтреального и парентерального питания (ESPEN), Porto IBD Group, провела анализ 7 исследований, из которых 3 были проведены на разных полимерных продуктах [235, 236, 34], а 4 были выполнены на специализированной полимерной формуле с трансформирующим фартором роста β-2 (ТФР β-2, Modulen® IBD) [231, 232, 36, 233]. Во всех исследованиях показано улучшение состояния слизистой, показатели полного заживления варьировались от 19 до 87% [234]. В одном исследоавнии, помимо полного трансмурального заживления слизистой у 21% детей (3 из 14), было показан ранний эндоскопический результат ПЭП (полное или практичеки полное заживление слизистой оболочки), с которым были связаны уменьшение обострений, госпитализаций и потребности в противо-TNF лечении на протяжении года наблюдения [234, 235]. ECCO/ESPGHAN особенно отметили рандомизированное контролируемое исследование, в котором сравнивали ПЭП полимерной формулой с трансформирующим фартором роста β-2 (ТФР β-2, Modulen® IBD) и кортикостероиды. Исследование показало яное преимущество ПЭП после 10 недель применения в отношении заживления слизистой (74% vs. 33%, соответствено) [36, 234]
Важным пактическим выводом, сделанным ECCO/ESPGHAN в резултате анализа имеющихся на сегодня результатов исследований, стало заключение о том, что благодаря положительному влиянию на заживление слизистой оболочки кишечника, восстановленияю минерализации костной ткани и улучшения роста, ПЭП должно иметь преимущества перед кортикостероидами для всех детей с воспалительными заболеваниями кишечника [234].
Введение смесей для ПЭП через рот, по-видимому, так же эффективно, как и непрерывное их введение через назогастральный зонд. По этой причине лечение следует начинать с введения через рот полимерных смесей, а переходить к введению смеси через назогастральный зонд нужно только в случае невозможности достижения достаточной энергетической ценности потребляемой смеси, которая
должна составлять примерно 120% от суточной потребности [30]. Сравнительных исследований
для оценки сроков применения ПЭП не проводилось, но чаще использовались сроки 6–8 недель [31].
4.2.1.3. Эффективность в зависимости от локализации и течения заболевания
По данным мета-анализа, подтверждена эффективность применения ПЭП для индукции ремиссии у всех пациентов с воспалительной формой заболевания независимо от зоны поражения [17, 32, 33]. Тем не менее, сравнительного исследования с эффективностью глюкокортикостероидов в случае
4.2.2. Глюкокортикостероиды
изолированного тяжелого колита у пациентов с болезнью Крона не проводилось. Отсутствуют также данные, подтверждающие эффективность применения ПЭП при активном артрите и других внекишечных проявлениях заболевания, а также при пенетрирующем течении заболевания.
Практические аспекты
1. Рекомендуемая доза преднизолона (или аналогичного препарата) для приема внутрь при обострении БК для большинства пациентов детского возраста составляет 1 мг/кг (максимальная доза 40 мг/сутки) однократно в сутки утром. При недостаточном эффекте может потребоваться увеличение дозы до 1,5 мг/кг (максимальная доза 60 мг/сутки).
2. При отсутствии эффекта от перорального применения глюкокортикостероидов у некоторых пациентов может быть эффективным внутривенное введение глюкокортикостероидов.
4.2.2.1. Эффективность глюкокортикостероидов В связи с тем, что только в нескольких исследованиях сообщалось о применении глюкокортикостероидов у детей, страдающих ВЗК, стратегия лечения у детей в основном основана на опыте лечения взрослых пациентов [37]. Было проведено два РКИ у детей [38,39], в которых проводилось сравнение преднизолона и будесонида, и одно исследование [40], в котором проводилось сравнение преднизолона и комбинации преднизолон с 6-меркаптопурином у детей с впервые установленным диагнозом БК. Кроме того, допол-
3. Начальная доза будесонида – 9 мг, препарат в дозе до 12 мг используется у детей в течение первых 4-х недель для индукции ремиссии. Постепенное уменьшение дозы будесонида можно проводить в течение 10–12 недель.
4. Рекомендуется назначение первоначальной дозы в течение 2 недель с последующим постепенным снижением и отменой не позднее 12 недель. Схема снижения дозы преднизолона приведена в таблице 6.
нительные данные были получены из регистров детей, страдающих ВЗК, и из популяционных исследований. Значения частоты достижения ремиссии в течение тридцати дней после начала лечения для преднизолона в исследованиях у детей колебались от 57% [34] до 79% [40] в РКИ и 62% в популяционном исследовании [41]. В исследованиях использовалась схема снижения дозы глюкокортикостероидов продолжительностью от восьми до 12 недель. В клинической практике начало применения и снижение дозы
Таблица 6.
Схема снижения дозы преднизолона при проведении индукционной терапии БК у детей (в соответствии с ре-
2014) [2]
глюкокортикостероидов не стандартизировано и осуществляется на основании опыта врача. Однократный прием суточной дозы в утреннее время уменьшает потенциальное негативное вли-
яние препаратов, связанное с замедлением роста [42]. Внутривенное введение глюкокортикостероидов применяется только для лечения тяжелого обострения заболевания.
4.2.2.2. Глюкокортикостероиды и заживление слизистой оболочки
Клинический ответ при лечении болезни Крона не коррелирует с эндоскопическим улучшением [43], а оценка эндоскопического ответа на применение глюкокортикостероидов у детей, страдающих БК, была проведена только в двух исследованиях: Berni Canani [34] установил, что эндоскопическое улучшение наблюдалось у 4 из 10 пациентов, однако ни у одного пациента не было зарегистрировано заживления слизистой оболочки через 8 недель после начала лечения. В исследовании, проведенном
Borrelli и соавт.[36], наблюдалось частичное заживление слизистой оболочки у 6 из 18 (33%) пациентов, получавших глюкокортикостероиды, на 10 неделе. В исследовании поддерживающей терапии в течение года полное заживление слизистой оболочки при эндоскопическом исследовании было достигнуто при монотерапии будесонидом у 24% пациентов, а при его комбинации с азатиоприном – у 83% пациентов [44].
4.2.2.3. Варианты лечения и эффективность в зависимости от локализации и течения заболевания
У пациентов с легкой или среднетяжелой формой БК с локализацией патологического процесса в подвздошной кишке или восходящей ободочной кишке применение будесонид предпочтителен [38,39, 45]. В исследовании, проведенным Levine и соавт. [46], были зарегистрированы лучшие показатели достижения ремиссии и ответа в течение 7 недель при использовании дозы 12 мг, по сравнению со стандартной дозой 9 мг (66% и 74% по сравнению
с 42% и 51% соответственно) через 7 недель. При
поражении дистальных отделов толстой кишки, также, как и у взрослых пациентов, могут быть использованы клизмы с глюкокортикостероидами. У маленьких детей доза будесонида должна подбираться в соответствии с возрастом и массой тела.
Поддержание ремиссии с использованием глюкокортикостероидов не рекомендуется, а в случае развития стероидозависимости обязателен переход на другую терапию (иммуносупрессоры, биологическая терапия).
4.2.2.4. Безопасность глюкокортикостероидов и нежелательные эффекты
Подавление функции надпочечников может развиваться даже через одну неделю после начала лечения системными глюкокортикостероидами [47]. Риски развития нежелательных эффектов зависят от дозы и продолжительности лечения [48]. однако чувствительность у различных пациентов может существенно различаться. Одной из важнейших
4.2.3. Антибиотики
проблем, возникающих при лечении глюкокортикостероидами детей с БК, является замедление роста. В связи с этим, длительные курсы глюкокортикостероидов у детей не допустимы.
На фоне лечение глюкокортикостероидами рекомендуется назначение препаратов кальция и витамина Д для снижения риска остеопороза.
Практические аспекты
1. При поражении перианальной области наблюдается хороший кратковременный эффект от лечения метронидазолом/ ципрофлоксацином, которое может служить переходным этапом к дальнейшему назначению иммуносупрессивной или биологической терапии.
4.2.3.1. Эффективность антибиотиков
4.2.3.1.1. Пенетрирующая форма заболевания. До настоящего времени не было проведено ни одного исследования у детей по оценке эффективности антиботиков при пенетрирующей форме БК. Мета-анализ трех исследований, включавших 123 взрослых пациента, страдающих БК, с наличием свища в перианальной области [49] продемонстрировал статистически значимый эффект
2. Стандартная суточная доза метронидазола составляет 10–20 мг/кг, а ципрофлоксацина – 20 мг/кг.
3. Азитромицин и рифаксимин могут использоваться для индукции ремиссии у детей с воспалительной формой болезни Крона легкой или средней тяжести.
в отношении уменьшения количества отделяемого из свища после курса ципрофлоксацина или метронидазола (ОР=0,8; 95% ДИ=0,66–0,98). Монотерапия антибиотиками при наличии абсцессов брюшной полости у больных БК эффективна при небольших абсцессах, но лишь у пациентов, ранее не получавших иммуносупрессоры. Во всех остальных случаях более
эффективно хирургическое лечение, хотя у некоторых пациентов чрескожное дренирование абсцесса может позволить избежать оперативного вмешательства. Bermejo и соавт. [50] наблюдали 128 взрослых пациентов, страдающих БК, с абсцессами в брюшной полости. Максимальная эффективность в течение 1 года наблюдалась при использовании хирургического лечения (91%) по сравнению с применением только антибактериальной терапии (63%) и антибиотиков в комбинации с чрескожным дренированием (30%). Неэффективность первоначальной антибиотикотерапии была связана с использованием иммуносупрессоров на момент постановки диагноза (ОР 8,45; 95% ДИ 1,16–61,5; P=0,03), наличием
свища (ОР 5,43; 95% ДИ 1,18–24,8; P=0,02) и разме-
рами абсцесса (ОР 1,65; 95% ДИ 1,07–2,54; P=0,02).
4.2.3.1.2. Воспалительная форма заболевания.
К сожалению, РКИ эффективности антибиотиков у детей для контроля активности воспалительного процесса в кишечнике при БК отсутствуют. Мета-анализ 10 РКИ у взрослых (1160 пациентов) [49] показал статистически значимое превосходство эффективности антибиотиков по сравнению с плацебо (ОР =0,85, при 95% ДИ 0,73–0,99, P = 0,03). Применялись различные антибиотики (противотуберкулезные
4.3. Поддерживающая терапия
4.3.1. Тиопурины
препараты, макролиды, фторхинолоны, 5-нитроимидазол и рифаксимин) в виде монотерапии или в комбинации. Было установлено, что применение производных рифамицина в виде монотерапии и в комбинации с другими антибиотиками оказывало статистически значимый эффект в отношении индукции ремиссии при обострении БК.
Levine и Turner [51] провели ретроспективный анализ данных о 32 детей с обострением БК, которые получали 8-недельный курс комбинации азитромицина и метронидазола. Азитромицин назначался в дозе 7,5–10 мг/кг однократно в сутки (максимальная доза: 500 мг) 5 дней в неделю в течение 4-х недель, а затем 3 раза в неделю в течение последующих 4-х недель совместно с метронидазолом. Через 8 недель после начала лечения у 21/32 (66%) пациентов была достигнута полная клиническая ремиссия, а у 54% из них наблюдалась нормализация концентрации C-реактивного белка (CРБ). Эффект был более выраженным при легкой степени тяжести заболевания. При проведении ретроспективного анализа данных у 23 детей с ВЗК (12 с БК) было установлено, что у 12 пациентов (60%) наблюдалось улучшение симптомов при применении рифаксимина в дозе 10–30 мг/кг в течение 4-х недель.
Практические аспекты
1. Тиопурины эффективны в поддержании ремиссии БК, достигнутой на фоне глюкокортикостероидов. Для получения максимального эффекта от тиопуринов может потребоваться от 8 до 14 недель, поэтому начинать терапию ими следует на фоне снижения дозы преднизолона.
2. У пациентов без нарушений метаболизма тиопуринов рекомендуется применение азатиоприна в дозе 2,0–2,5 мг/кг или 6-меркаптопурина в дозе 1,0–1,5 мг/кг в сутки.
3. Исследование активности тиопуринметилтрансферазы (ТПМТ) перед началом терапии тиопуринами (норма 230–450 ед/мл) позволяет выявить пациентов с высоким риском миелосупрессии. Если проведение этого исследования невозможно, в начале лечения может быть назначена половинная доза тиопурина с контролем общего анализа крови еженедельно в течение 2 недель [4], если миелосупрессии не отмечается, рекомендуется постепенное увеличения дозы тиопурина до полной. Снижение дозы тиопурина в 2 раза рекомендуется при снижении лейкоцитов в крови ниже 3000/мм3, тиопурины
противопоказаны в редких случаях, когда абсолютное количество лейкоцитов снижается ниже 1500/мм3.
4. В течение первого месяца после начала лечения обязателен контроль общего анализа крови и активности печеночных ферментов, первоначально – каждые 1–2 недели с последующим уменьшением частоты; а в дальнейшем на протяжении всего лечения тиопуринами необходим контроль этих показателей каждые 3 месяца у всех пациентов (независимо от активности ТПМТ).
5. Панкреатит может развиваться независимо от дозы в ранние сроки после начала применения тиопуринов, при его развитии обычно требуется отмена препарата. Необходимо уделить особое внимание дифференциальной диагностике истинной токсичности, связанной с применением тиопуринов, и внекишечными проявлениями ВЗК в форме панкреатита.
6. Решение о переводе с азатиоприна (AZA) на 6-меркаптопурин (6-MP) и наоборот может быть принято у пациентов с гриппоподобным
синдромом или острыми симптомами со стороны желудочно-кишечного тракта.
7. Увеличение активности трансаминаз более двух норм может носить транзиторный характер или потребовать снижения дозы препарата или его отмены. При повышении активности ТПМТ и уровня трансаминаз рекомендуется снижение дозы тиопурина и назначение аллопуринола.
8. При добавлении к лечению аллопуринола доза тиопурина должна быть снижена до 25–33% от
4.3.1.1. Эффективность тиопуринов
У детей с БК проведено одно плацебо-контролируемое и семь наблюдательных исследований, в которых оценивалось применение тиопуринов для поддержания ремиссии. В РКИ, проведенном Markowitz [40], частота рецидивов составила 4 и 9% в группе 6меркаптопурина (n = 27 пациентов) и 26 и 47% в группе плацебо (n = 28 пациентов) через 6 и 18 месяцев соответственно после индукции ремиссии с использованием преднизолона у пациентов с впервые диагностированной среднетяжелой и тяжелой БК. В ретроспективных исследованиях серий случаев при использовании азатиоприна наблюдался более длительный период поддержания ремиссии, более низкая частота госпитализаций, повторного назначения глюкокортикостероидов и выполнения хирургических вмешательств [52, 53].Применение азатиоприна в более высокой дозе 2,5 мг/кг/сутки было более эффективным по сравнению с более низкими дозами 1,0 или 2,0 мг/кг/
первоначальной дозы. Стандартная доза аллопуринола для взрослых составляет 100 мг/сутки, доза аллопуринола для детей должна быть уменьшена (50–75 мг в зависимости от массы тела).
9. Всем пациентам, которые применяют или ранее применяли тиопурины, рекомендуется избегать воздействия солнечных лучей в течение всей жизни, а также проходить регулярное дерматологическое обследование в связи с повышенным риском опухолей кожи.
сутки. При проведении наблюдательных исследований у взрослых было отмечено уменьшение необходимости в выполнении хирургических вмешательств, а также профилактический эффект в отношении поражения перианальной области, в особенности в случае раннего начала лечения [54, 55], однако в более поздних исследованиях эффективность тиопуринов в отношении поддержания ремиссии была поставлена под сомнение [56, 57]. В исследовании SONIC были получены данные проспективного анализа заживления слизистой оболочки, проведенного у максимального количества взрослых пациентов с БК; из 115 пациентов, получавших азатиоприн, заживление слизистой оболочки (заживление язв) наблюдалось у 16,5% [58]. В случае применения азатиоприна в дозе 3 мг/ кг наблюдалась стабилизация или улучшение значения показателя отклонения роста (Z-показателя) у 36% детей, страдающих БК [59].
4.3.1.2. Безопасность и побочные эффекты тиопуринов
Побочные реакции при применении тиопуринов были зарегистрированы у 15–46% пациентов[60–62]. В 8%–28% случаев они стали причиной снижения дозы препарата, а в 18%–43% случаев лечение было прекращено. Применение азатиоприна в более высокой дозе 3 мг/кг/сутки у детей, страдающих ВЗК, приводит к отмене препарата у 30% пациентов[59]. Дозозависимая токсичность может проявиться как спустя несколько недель, так и несколько лет после начала лечения и включает в себя гепатотоксичность и миелосупрессию. При применении препаратов в стандартных дозах гематологическая токсичность наблюдается у 1,8%-13,7% пациентов [60–62]. Риск развития инфекций составляет ~ 8% [62], однако при анализе данных, полученных из последних крупных регистров детей DEVELOP и взрослых TREAT, было установлено что применение иммуносупрессоров не было связано с повышенным риском инфекций, в то время как применение биологических препаратов более чем удваивало риск инфекций [63, 64].
Токсичность, не зависящая от дозы препарата, обычно проявляется в течение первых недель после начала лечения. Панкреатит относится к наиболее частым проявлениям реакции гиперчувствительности и наблюдается у 3–4% пациентов. Другие нежелательные лекарственные реакции, не зависящие от дозы препарата, включают диспепсические расстройства (5–8%), лихорадку, гриппоподобные симптомы, миалгию, артралгию
и сыпь (наблюдается ~ 9% пациентов). Замена препарата на 6меркаптопурин может быть успешной примерно у 50% пациентов с непереносимостью азатиоприна, в особенности при миалгии или артралгии, но также может быть эффективной в случае гепатоксичности, симптомов со стороны желудочно-кишечного тракта, гриппоподобных проявлений и сыпи [61]. Результаты недавнего небольшого исследования серии случаев позволяют предположить, что попытка применения 6-меркаптопурина может быть успешной и безопасной у некоторых пациентов с панкреатитом, индуцированным применением азатиоприна [65]. Примерно 9% пациентов с ВЗК не отвечают на применение тиопуринов [66], а у пациентов с высокой активностью ТПМТ (>14 Ед/мл эритроцитов) наблюдается меньшая эффективность лечения [67].
На основании долгосрочных наблюдений было установлено, что риск развития лимфомы у пациентов с ВЗК, получающих тиопурины, особенно у мужчин, увеличивается примерно в четыре раза, однако абсолютный риск у детей и подростков был меньшим [68, 69]. Было рассчитано, что у детей риск составляет 4,5 случаев/10000 пациенто-лет [70], он был задокументирован в детском регистре DEVELOP [71]. Кроме того, примерно у 40 подростков и взрослых пациентов, страдающих ВЗК, была зарегистрирована Т-клеточная лимфома печени и селезёнки с летальным исходом; практически все пациенты были мужского пола, и у 50% пациентов
опухоль возникла в возрасте до 20 лет. Примерно половина этих пациентов получала в течение длительного времени только тиопурины, а другая половина получала длительное время тиопурины в комбинации с препаратами антител к фактору некроза опухоли, длительность экспозиции анти-ФНО терапии при этом существенно варьировала [72]. Применение тиопуринов также было связано с 4–5 кратным увеличением риска развития немеланомного рака кожи даже в возрасте до 50 лет [73,74].
4.3.2. Метотрексат
Интересно отметить, что в недавних исследованиях было выявлено, что применение тиопуринов приводит к снижению риска развития новообразований колоректальной области, как у пациентов с БК, так и с ЯК, и данный профилактический эффект, по-видимому, более выражен, чем у препаратов 5-АСК [75]. Следует избегать назначения тиопуринов во время инфекции, вызванной вирусом ЭпштейнБарр (ВЭБ), в связи с риском развития лимфом, ассоциированных с ВЭБ.
Практические аспекты:
1. Метотрексат следует назначать в дозе 15 мг/м2 1 раз в неделю; максимальная доза – 25 мг.
2. Если у пациента в течение нескольких месяцев наблюдается стойкая полная ремиссия с нормальными значениями маркеров воспаления, может быть предпринята попытка снижения дозы до 10 мг/м2 один раз в неделю (максимальная доза – 15 мг).
3. Метотрексат обычно назначается в виде подкожных инъекций, эффективность которых аналогична эффективности внутримышечных инъекций.
4. На фоне терапии метотрексатом рекомендуется прием внутрь фолиевой кислоты (5 мг через
4.3.2.1. Эффективность метотрексата
Результаты, полученные в 7 ретроспективных когортных исследованиях у детей, позволяют предположить, что эффективность метотрексата у детей, у которых лечение тиопуринами было неэффективным или наблюдалась их плохая переносимость, составляет от 50 до 80% [76–82]; при этом частота ремиссии через 6 и 12 месяцев составила 37–62% и 25–33% соответственно, а частота ремиссии в течение всего первого года – 15–35%. В двух небольших исследованиях (n=50) не было выявлено различий между метотрексатом и 6-меркаптопурином в отношении поддержания ремиссии БК (ОР 2,63;
25–72 часа после введения метотрексата или 1 мг однократно в сутки 5 дней в неделю).
5. У пациентов со стойкой ремиссией необходим периодический контроль общего анализа крови и активности АЛТ.
6. Метотрексат строго противопоказан при беременности, а также его применение противопоказано половым партнерам женщины при планировании беременности, при необходимости следует использовать эффективный метод контрацепции.
7. При плохой переносимости метотрексата (тошнота) рекомендуется введение ондансетрона за час до инъекции в начале курса лечения.
95%ДИ 0,74–9,37; P=0,14). У детей, ответивших на лечение [76], отмечена нормализация линейного роста, что может быть косвенным признаком эффективного контроля воспаления слизистой оболочки. Оценка эффективности метотрексата заживлять слизистую оболочку не проводилась, за исключением одного исследования у взрослых, в котором оно достигнуто у 2 из 11 пациентов, получавших метотрексат, 8 из 18, получавших азатиоприн (p = 0,011 по сравнению с метотрексатом) и 9 из 16 пациентов, получавших инфликсимаб (p = 0,008 по сравнению с метотрексатом) [83].
4.3.2.2. Безопасность и нежелательные эффекты метотрексата
Побочные реакции сдерживают широкое применение метотрексата. К ним относятся тошнота/рвота, гриппоподобные симптомы, поражение печени и, значительно реже, миелосупрессия. Проблема тошноты и рвоты может быть особенно неприятной, и данные явления часто становятся причиной прекращения применения препарата [84]; в исследовании, проведенном Uhlen и соавт.[77], тошнота/рвота наблюдалась у 7/61 (11%) пациентов, а в исследовании, проведенном Turner и соавт.[76], у 4/17 (24%) детей, принимавших препарат внутрь, и у 6/39 (15%) пациентов из группы, получавшей
препарат подкожно. Появление тошноты и рвоты можно предотвратить путем превентивного применения антагониста рецептора 5-гидрокситриптамина (HT)3 типа ондансетрона [85]. Токсическое влияние на органы дыхания относится к очень серьезным, но крайне редким осложнениям применения метотрексата; ни одного случая данного явления у детей с БК зарегистрировано не было. Повышение активности печеночных ферментов может наблюдаться у 30% пациентов и обычно проходит после временного прекращения применения метотрексата и/или снижения дозы.
4.3.3. Лечение биологическими препаратами (антитела к фактору некроза опухолей (анти-ФНО)
Практические аспекты:
1. Решение о применении антиФНО в качестве препарата первой линии для индукции ремиссии может быть принято у отдельных пациентов детского возраста при наличии факторов риска неблагоприятного исхода заболевания (см. выше).
2. Решение о раннем начале применения анти-ФНО должно быть принято у пациентов с тяжелыми внекишечными проявлениями заболевания (например, тяжелый артрит, гангренозная пиодермия).
3. Оценка первоначальной эффективности лечения ингибитором ФНО должна проводиться после введения второй или третьей дозы препарата, и при отсутствии значимого эффекта к 12–14 неделе лечения применение препарата должно быть прекращено (первичная неэффективность лечения).
4. У пациентов, ранее не получавших анти-ФНО (наивные к анти-ФНО терапии), инфликсимаб и адалимумаб имеют равную эффективность и профиль побочных реакций. Выбор препарата проводят в соответствии с доступностью, способом введения, предпочтением пациента, стоимостью и местными нормативными требованиями.
5. Данных для оценки риска/пользы комбинированной или монотерапии детей с БК недостаточно. По-видимому, комбинированная терапия в течение первых 6 месяцев может снижать образование антител и обусловленную ими утрату ответа на лечение. Но это преимущество следует оценивать с учетом увеличения со временем риска развития лимфомы на фоне тиопуринов, поэтому данный вопрос следует решать индивидуально (учитывая факторы неблагоприятного прогноза заболевания). Одновременное применение метотрексата в низких дозах может быть более безопасным, чем тиопуринов, но эта комбинация имеет меньшую доказательную базу.
6. Рутинная премедикация ацетаминофеном, глюкокортикостероидами или антигистаминными препаратами перед введением анти-ФНО не показана.
7. Перед началом анти-ФНО терапии обязательно проведение исследования на туберкулез:
рентгенография органов грудной клетки, кожная проба с очищенным туберкулином и/или тест с высвобождением гамма-интерферона лимфоцитами (квантифероновый тест).
8. Для индукции ремиссии инфликсимаб назначают в дозе 5 мг/кг, 3 дозы в течение 6 недель (недели 0–2–6) с последующей поддерживающей терапией с введением препарата в дозе 5 мг/кг каждые 8 недель. У больных, у которых наблюдается уменьшение эффективности препарата или при низкой концентрации препарата может потребоваться применение более высоких доз препарата до 10 мг/кг и/или сокращение продолжительности интервалов между введениями до 4-х недель. Уменьшение дозы инфликсимаба показано, если его остаточная концентрация превышает 8–10 мкг/мл.
9. Для индукции ремиссии адалимумаб назначают в дозе 2,4 мг/кг (максимальная доза 160 мг) на первую инъекцию, 1,2 мг/кг (максимальная доза 80 мг) через 2 недели, с последующим введением препарата в дозе 0,6 мг/кг (максимальная доза 40 мг) каждые 2 недели. В качестве альтернативы можно использовать следующую схему: у пациентов с массой тела до 40 кг была предложена схема 80–40–20 мг, а для пациентов с массой тела более 40 кг – 160–80–40 мг. Еженедельное введение показано при снижении эффективности и низкой остаточной концентрацией препарата.
10. В случае недостаточного ответа или снижения эффективности лечения для установления причины целесообразно определение остаточной концентрации инфликсимаба и адалимумаба, а также антител к ним в сыворотке крови.
11. Переход с одного антиФНО препарата на другой возможен у пациента при непереносимости одного препарата или утратой его эффекта; однако вероятность хорошего ответа на лечение в этом случае ниже, чем у больных, ранее не получавших антиФНО терапии.
12. Биосимиляры являются последующими версиями оригинальных биофармацевтических препаратов, произведенных другой компанией
после истечения срока действия патента на оригинальный препарат. Стремительно разрабатываются биосимиляры таких препаратов, как инфликсимаб и адалимумаб, и начинают
4.3.3.1. Эффективность анти-ФНО терапии
4.3.3.1.1. Воспалительная форма заболевания. Эффективность инфликсимаба для индукции и поддержания ремиссии у детей с БК доказана в нескольких РКИ. В рандомизированном исследовании REACH [86] дети в возрасте от 6 до 17 лет с активной БК после предшествующего недостаточно эффективного лечения глюкокортикостероидами и иммуносупрессорами получали инфликсимаб по схеме 0, 2 и 6 недель. У 98 (88%) из 112 пациентов был достигнут ответ на лечение, у 59% через 10 недель наблюдалась клиническая ремиссия. Пациенты, ответившие на лечение через 10 недель, были рандомизированы для дальнейшего лечения инфликсимабом (5 мг/кг) каждые 8 недель или каждые 12 недель при продолжающемся лечением иммуносупрессорами (обычно тиопурином). Введение препарата с интервалом 8 недель было более эффективным. Применение инфликсимаба на ранних стадиях заболевания может привести к лучшим результатам у отдельных пациентов из группы высокого риска [87].
Исследование IMAgINE было первым двойным слепым рандомизированным исследованием [88], в котором была проведена оценка эффективности адалимумаба у 192 детей в возрасте 6–17 лет с умеренно тяжелой и тяжелой активной БК (PCDAI>30), несмотря на применение пероральных глюкокортикостероидов и/или иммуносупрессоров. В исследование включались пациенты, ранее отвечавшие на лечение инфликсимабом, у которых эффективность данного препарата была утрачена, и пациенты, которые не переносили данный препарат. После открытой фазы индукции дети были рандомизированы для лечения высокой или низкой дозой адалимумаба. Через 54 недели у 31/93 детей (33,3%), получавших высокую дозу препарата, наблюдалась клиническая ремиссия. В ретроспективном многоцентровом исследовании, проведенном у 115 пациентов детского возраста, страдающих БК, которые получили, как минимум, 1 дозу адалимумаба (95% из них ранее получали инфликсимаб), частота без-стероидной ремиссии в течение 1 года составила 42% [89]. Данные, полученные у детей, были
4.3.3.2. Внекишечные проявления БК
У взрослых показано, что инфликсимаб может быть эффективным для лечения внекишечных проявлений БК [95]. Применение инфликсимаба у детей с внекишечными проявлениями было описано в исследовании серии случаев пациентов с гангренозной пио-
4.3.3.3. Заживление слизистой оболочки
В недавнем исследовании, проведенном в Польше [101], наблюдалось полное заживление слизистой оболочки через 10 недель у 23% из 66 получавших лечение анти-ФНО детей с БК. Заживление слизистой
регистрироваться в МЗ России для лечения ВЗК. В настоящее время, однако, имеются данные по оценке эффективности биосимиляров только в ревматологии.
сравнимы с данными, полученными в исследованиях адалимумаба у взрослых.
4.3.3.1.2. Пенетрирующая форма заболевания. Данные, подтверждающие эффективность инфликсимаба у детей с БК, протекающей с формированием свищей, малочисленны. При ретроспективном анализе эффективности инфликсимаба при сопутствующем поражении перианальной области в у 31 пациента в исследовании REACH (28%), было установлено, что через 2 недели после однократной инфузии препарата у 41% было достигнуто частичное или полное закрытие свища [90].В недавнем исследовании серии случаев у детей GETAID [91] было установлено, что частота ответа на лечение инфликсимабом через 12 месяцев составила 75% (75/101 пациента с БК), при этом у 54% наблюдалось полное закрытие свища.
Данные, касающиеся закрытия свищей у детей с БК, получавших адалимумаб, ограничены. При проведении анализа подгрупп в исследовании IMAgINE было установлено, что закрытие свища было достигнуто через 52 недели у 23,8% пациентов (5/21) в группе, получавшей низкую дозу препарата, и у 40% – высокую дозу. У взрослых было установлено существенное преимущество инфликсимаба перед плацебо (55% пациентов с закрытием всех свищей по сравнению с 13% в группе плацебо) (P=0,002) [92]. Медиана времени до получения ответа на лечение инфликсимабом составила 14 дней. Что касается адалимумаба, частота закрытия свищей через 12 недель составила 48% у пациентов, ранее не получавших антиФНО, и 26% у пациентов, ранее получавших инфликсимаб [93]. На 24 неделе частота закрытия свищей была значительно выше в группе пациентов, ранее не получавших антиФНО (60% и 20%, P<0,01). В недавнем рандомизированном исследовании у взрослых (ADAFI) было установлено, что при применении адалимумаба в комбинации с ципрофлоксацином была достигнута более высокая частота закрытия свищей перианальной области, чем при применении адалимумаба в комбинации с плацебо, через 12 недель соответственно 65% и 33% [94].
дермией, поражением лица и полости рта, эритемой, метастатическим поражением кожи полового члена и кожи мошонки при БК, увеитом, первичным поражением легких, первичным склерозирующим холангитом всочетании с панкреатитом иостеомиелитом [96–100].
оболочки сопряжено с увеличением скорости роста и формирования костной ткани. Malik и соавт.
[102] описали когорту пациентов, в которой у 42%, получавших адалимумаб, наблюдалось улучшение
линейного роста, в особенности у детей, у которых была достигнута ремиссия. При определении концентрации маркеров образования костной ткани в сыворотке крови наблюдалось быстрое
их улучшение после лечения антиФНО как у детей, так и у взрослых с БК [103–106]. Применение анти-ФНО снижает необходимость выполнения хирургических вмешательств [55].
4.3.3.4. Оптимизация (интенсификация) лечения ингибиторами ФНО
Для достижения стойкой клинической ремиссии в детской гастроэнтерологической клинической практике иногда требуется оптимизация (интенсификация лечения анти-ФНО). Увеличивается доза препарата (с 5 мг/кг до 10 мг/кг инфликсимаба) и/или сокращаются интервалы между введениями (переход на введение каждые 4 недели для
4.3.3.5. Комбинированная терапия
Вопрос о том, следует ли применять ингибиторы ФНО в виде монотерапии или в комбинации с иммуносупрессором, вызывал особенно много споров в детской практике. В исследовании SONIC, проведенном у взрослых пациентов [108], ранее не получавших ни иммуносупрессоры, ни инфликсимаб, было выявлено умеренное увеличение эффективности инфликсимаба в случае его комбинации с азатиоприном.Однако в исследовании SONIC не рассматривался вопрос о преимуществе комбинированной терапии перед монотерапией инфликсимабом, если предшествующее лечение азатиоприном было неэффективным. Как в исследовании ACCENT I, так и в исследовании ACCENT II не было выявлено никаких различий в отношении достижения ремиссии и ответа на лечение между пациентами на монотерапии инфликсимабом и комбинированной терапии [109]. Сходные результаты были получены в отношении адалимумаба в исследовании CHARM [110]. Но было выявлено незначительное преимущество комбинированной терапии, в особенности в течение первых 6 месяцев лечения [111, 112].Были зарегистрированы более высокие значения концентрации антител к инфликсимабу и более низкие остаточные концентрации анти-ФНО препарата у больных, получавших монотерапию инфликсимабом, что сопровождалось большей частотой инфузионных реакций и менее благоприятным исходом лечения. В недавнем мета-анализе было установлено, что применение комбинированной терапии с использованием азатиоприна дает лучшие клинические результаты, чем монотерапия инфликсимабом, даже в случае отсутствия эффекта от азатиоприна в анамнезе.
Что касается адалимумаба, в исследовании IMAGINE не было выявлено достоверной разницы достижения клинического ответа и ремиссии у детей, получавших монотерапию адалимумабом по сравнению с комбинацией с иммуносупрессором на 4-й и 26-й неделях. Клинический ответ 79,5% vs 87,3%, клиническая ремиссия 26,5% vs 29,6% на 4-й и клинический ответ 59,0% vs 45,1%, клиническая ремиссия 35,9% vs 29,6% на 26-й неделе соответственно у детей, получавших и не получавших иммуносупрессоры, ни в одном случае разница не достигала статистической достоверности [88]. Также сопутствующее лечение иммуносупрессором не приводило к достоверному повышению средней остаточной концентрации адалимумаба
инфликсимаба и на еженедельное введение для адалимумаба). Оптимизацию проводят в случае неэффективности лечения или утраты ответа на лечение. Важно поддерживать минимальную остаточную концентрацию препарата в сыворотке крови на определяемом уровне (3–8 мкг/мл) [107].
на 26-й и 52-й неделе, концентрация была лишь нумерически выше у детей, получавших адалимумаб в комбинации с иммуносупрессором [229]. Однако в данное исследование включались пациенты, у которых уже отмечалась предшествующая неудача лечения иммуносупрессорами. В проспективном раздомизированном контролируемом исследовании, проведенном у взрослых пациентов с БК, наивных к лечению иммуносупрессорами, с адалимумабом по типу исследования SONIC, не было показано преимущества комбинированной терапии с азатиоприном по сравнению с монотерапией адалимумабом [230]. Частота клинической ремиссии к 26-й неделе составила 71,8% в группе монотерапии адалимумабом и 68,1% в группе комбинированной терапии с азатиоприном (разница недостоверна). Вероятно, в случае с адалимумабом комбинация с иммуносупрессором не имеет столь критического значения, как в случае с инфликсимабом, для достижения потенциала эффективности терапии.
Негативным моментом комбинированной терапии антиФНО и азатиоприном является повышенный риск развития лимфомы [113]. Комбинация с метотрексатом является более привлекательной в связи с отсутствием доказательств повышения риска развития лимфомы, и наличием данных, показавших пользу сочетания метотрексата и инфликсимаба у ревматологических больных. В клиническом исследовании COMMIT взрослые пациенты, страдающие БК в качестве индукционной терапии получали инфликсимаб и глюкокортикостероиды в сочетании с метотрексатом или плацебо [114]. Никаких различий в клиническом ответе выявлено не было, но назначение метотрексата сопровождалось более высокой концентрацией инфликсимаба и уменьшением частоты образования антител к нему. При проведении ретроспективного анализа в исследовании BSPGHAN у 70 детей, страдающих БК и получавших лечение адалимумабом [115], частота достижения ремиссии была выше у тех больных, которые одновременно получали иммуносупрессоры (34/46 (74%) против 9/24 (37%), p=0,003). С учетом этого, можно сделать вывод о допустимости одновременного применения азатиоприна в течение первых 6 месяцев терапии инфликсимабом, а затем лучше отменить азатиоприн, в особенности у мальчиков, однако тактика лечения должна быть индивидуальной и основываться на оценке прогностических факторов.
Прекращение комбинированной терапии является обоснованным только у пациентов, у которых была достигнута глубокая ремиссия (заживление
4.3.3.6. Сравнение инфликсимаба и адалимумаба В ретроспективном когортном исследовании [116] было проведено сравнение результатов, полученных у 100 взрослых пациентов, страдающих БК, получавших инфликсимаб, и 100 пациентов, получавших адалимумаб, не было выявлено никаких
слизистой оболочки). Роль метотрексата в комбинированной терапии у детей с БК должна быть определена в клинических исследованиях.
различий в достижении клинического ответа; ответ на лечение через 1 и 2 года наблюдался у 62% и 41% пациентов, получавших адалимумаб, и 65% и 49% пациентов, получавших инфликсимаб, соответственно.
4.3.3.7. Безопасность анти-ФНО и нежелательные эффекты
Образование антител к антиФНО может привести к развитию острых инфузионных реакций, отсроченных реакций гиперчувствительности, снижению концентрации препаратов в сыворотке крови, а также потере ответа на лечение [117–119]. Нерегулярное введение препаратов может привести к увеличению риска образования антител [119]. В трех небольших исследованиях, проведенных у детей, антитела к инфликсимабу были выявлены у трети пациентов, страдающих БК [118, 119,120]. При проведении мета-анализа 18 исследований (включающих 3326 взрослых пациентов, страдающих БК и получавших инфликсимаб)
[121] было установлено, что частота образование антител к инфликсимабу составила 45,8% при использовании эпизодических инфузий и 12,4% при проведении регулярной поддерживающей терапии. В исследовании IMAgINE только у 2,3% пациентов в группе, получающей высокую дозу препарата, и у 4,4% пациентов в группе, получающей низкую дозу препарата, обнаружены антитела к адалимумабу.
Наиболее распространенные симптомы острой инфузионной реакции: одышка, приливы, тошнота, головная боль, гипоксемия и тахикардия. Анализ 18 исследований у детей показал, что острая инфузионная реакция была зарегистрирована у 168 из 1100 пациентов, получавших инфликсимаб (15%) [2]. Большинство реакций были легкими, и наблюдался быстрый ответ на лечение в виде временного прекращения инфузии препарата или уменьшения скорости инфузии. Применение премедикации (антигистаминных, жаропонижающих препаратов или глюкокортикостероидов), по-видимому, не предотвращает развития острой инфузионной реакции [122–125]. Частота инфузионных реакций у детей была аналогичной таковой у взрослых [109, 126]. Тяжелые инфузионные реакции в виде гипоксии, гипотензии или затруднения дыхания являются противопоказанием для дальнейшего применения инфликсимаба.
Отсроченные реакции гиперчувствительности могут наблюдаться минимум через день после инфузии препарата и характеризуются развитием артралгии и отеком суставов, которые могут сопровождаться лихорадкой и/или сыпью. Частота возникновения данных реакций у детей, получающих инфликсимаб, достигает 8% [86], аналогичная ситуация наблюдается и у взрослых [109, 126]. У 20–29% детей при этом обнаружены антинуклеарные антитела (АНА). Клиническая значимость положительных АНА после лечения антагонистами ФНО-α до сих пор остается неясной.
Серьезные инфекции, таких как сепсис, менингит, пневмония, абсцессы, опоясывающий лишай или инфекция, вызванная вирусом ветряной оспы, гемофагоцитарный лимфогистиоцитоз, обусловленный вирусом Эпштейн-Барр, дерматомикозы и оппортунистические грибковые инфекции, были зарегистрированы у 49 из 1483 пациентов, получавших инфликсимаб (3,3%) [127]. У детей, страдающих БК и получавших адалимумаб из когорты BSPGHN, частота зарегистрированных серьезных нежелательных явлений составила 6%, включая два случая смерти от сепсиса у пациентов, получавших также иммуносупрессоры и домашнее парентеральное питание [115].
Риск развития оппортунистических инфекций (инвазивные грибковые инфекции, реактивация латентного туберкулеза) увеличивается у пациентов, получающих комбинированную терапию с использованием иммуносупрессоров, а также у пациентов с недостаточностью питания [128]. Если пациент не болел ветряной оспой и у него отсутствуют антитела к данному вирусу, целесообразна вакцинация против ветряной оспы, если возможна отсрочка начала лечения (так как необходим 4–6-недельный интервал между иммунизацией и началом иммуносупрессивной терапии).
При изучении долгосрочной безопасности схем лечения, включающих антиФНО, был выявлен повышенный риск новообразований: гепатолиенальной Т-клеточной лимфомы – у 30 пациентов, страдающих ВЗК и получавших лечения с использованием анти-ФНО в комбинации с тиопуринами [129], что позволяет предположить, что развитие лимфомы связано с применением тиопуринов, а комбинация с инфликсимабом является катализатором [130].206 У детей, получавших биологические препараты, по данным FDA на апрель 2008 года было зарегистрировано 48 случаев злокачественных новообразований, включая лимфому и злокачественные новообразования кожи, в том числе меланому (31 случай после применения инфликсимаба, 2 случая после применения адалимумаба и 15 случаев после применения этанерцепта) [131].
Появление симптомов со стороны кожи, таких как экзема или псориазоподобные поражения, было зарегистрировано у 20% взрослых пациентов, страдающих ВЗК [126], увеличивается их частота и у детей с ВЗК. Псориаз, индуцированный применением инфликсимаба, наблюдался у 8% (6/73) пациентов детского возраста, страдающих ВЗК [132].
4.3.3.8. Утрата ответа на лечение
Первичное отсутствие ответа на лечение – это отсутствие ответа на индукционный курс в течение первых 6 месяцев после начала лечения. Утрата ответа на лечение – это ситуация, когда у пациента, который ранее отвечал на лечение биологическим препаратом, ухудшилось течение заболевания или возник рецидив, несмотря на регулярное введение биологического препарата, что сопровождается укорочением интервала времени ремиссии после инфузии. Определение минимальной остаточной концентрации препарата может помочь выяснить причину утраты ответа на лечение и решить вопрос о дальнейшей тактике лечения в случае сохранения утраты ответа на лечение.
Неиммунные факторы, ведущие к утрате ответа на лечение, включают усиление воспаления, возникновение воспалительных процессов, на которые не могут подействовать применяемые препараты, осложнения заболевания (стеноз или пенетрация). Возможны проблемы, связанные с приверженностью, субоптимальные схемы лечения и уменьшение концентрации препарата или его метаболитов. Часто встречаются факторы, не связанные с ВЗК, такие как оппортунистические и другие инфекции или синдром раздраженного кишечника, не связанный с воспалительными изменениями. Таким образом, всегда необходимо проводить повторное обследование пациента в случае утраты эффективности лечения, и убедиться в том, что симптомы действительно обусловлены активностью данного заболевания. В настоящее время для лечения пациентов с утратой ответа используется тактика увеличения дозы препарата, которая заключается в применении удвоенной дозы или укорочения интервала между инфузиями /инъекциями, которая может быть эффективной у детей с низкой остаточной концентрацией препарата даже при наличии антител в невысоких титрах. При проведении ретроспективных исследований в Израиле [133] и Бельгии [134] не было выявлено преимуществ использования удвоенной дозы инфликсимаба
4.3.5. Аминосалицилаты
по сравнению с укорочением интервала между введениями, но по причинам, связанным с затратами на лечение и удобством пациента, предпочтительнее первоначально использовать удвоение дозы препарата. В целом, у 47% пациентов наблюдался устойчивый ответ в течение 1 года после увеличения дозы или укорочения интервала между введениями [133].У десяти пациентов с наличием антител к инфликсимабу использовалась более интенсивная схема лечения, при этом клинический ответ наблюдался у 6 (60%) пациентов. После применения более интенсивной схемы лечения концентрация антител к инфликсимабу снизилась у пяти пациентов.
В последнее время появились доказательства, позволяющие предположить, что добавление тиопуринов или метотрексата к схеме лечения пациентов, получавших инфликсимаб в виде монотерапии и утративших ответ на лечение по причине образования антител к инфликсимабу, может привести к исчезновению антител и восстановлению уровня остаточной концентрации, а также клинического ответа [135]. При выявлении соответствующих титров антител к инфликсимабу может быть как назначена более интенсивная схема, так и добавлен иммуносупрессор. При отсутствии эффекта от использования более интенсивной схемы лечения и комбинированной терапии или при высоком титре антител к инфликсимабу может быть принято решение о переходе на другой биологический препарат. Karmiris и соавт. [136] провели анализ 168 пациентов, которые начали получать адалимумаб по причине утраты ответа на лечение, обусловленной образованием антител к инфликсимабу. Клинический ответ был достигнут у 93% пациентов и был устойчивым у 62% пациентов; медиана периода наблюдения составила 20 месяцев. Такая тактика не будет успешной у пациентов с активным заболеванием и достаточной концентрацией препарата в крови; в данном случае показан переход на биологическую терапию молекулами другого класса.
Практические аспекты:
1. Препараты 5-АСК могут использоваться для индукции ремиссии БК у детей с локализацией в толстой кишке и легкой тяжестью воспалительного процесса, при этом может быть использован сульфасалазин или месалазин в гранулах.
2. Выбор препарата 5-АСК зависит от локализации процесса: при легкой БК илеальной локализации (L1) показано назначение месалазина в таблетках с рН-зависимым покрытием; при локализации в тонкой кишке (L4b) – в капсулах с рН-независимым механизмом раскрытия.
3. Доза 5-АСК для приема внутрь детям с БК аналогична таковой для пациентов детского возраста с ЯК и составляет 40–80 мг/кг/сутки до 4 г в сутки.
4. Доказательства того, что применение 5-АСК индуцирует заживление слизистой оболочки, отсутствуют, и в связи с этим данные препараты должны использоваться при легких формах при отсутствии глубоких язвенных дефектов. Для подтверждения полной ремиссии необходим тщательный контроль таких показателей, как концентрация CРБ, СОЭ и концентрация фекального кальпротектина, а также должен быть установлен низкий порог для необходимости усиления терапии.
4.3.5.1. Эффективность 5-АСК
Хотя эффективность 5-АСК при лечении ЯК четко задокументирована, роль аминосалицилатов в лечении БК остается спорной. Данные, основанные на принципах доказательной медицины, указывающие на четкие преимущества использования 5-АСК в качестве индукционной терапии у пациентов с БК, отсутствуют [137]. В единственном плацебо-контролируемом перекрестном исследовании,
4.3.6. Пробиотики
проведенном у детей [138], не было выявлено преимуществ применения 5-АСК для индукции ремиссии у 14 детей с активной БК с поражением тонкой кишки. В единственном клиническом исследовании поддерживающей терапии у 122 детей с БК в стадии ремиссии выявлено двукратное уменьшение риска рецидива на фоне приема месалазина [139].
5. Хирургическое лечение болезни Крона у детей
Прогрессирующее течение заболевания приводит к развитию кишечных осложнений у каждого второго больного за десятилетний период наблюдения, кроме того до 90% пациентов с БК подвергаются в течение жизни одной или нескольким операциям [140]. Невозможность радикального излечения БК нередко приводит к повторным вмешательствам, увеличивая риск синдрома короткой кишки [141]. Современная стратегия хирургического лечения
БК направлена на выполнение экономных резекций кишки, применение малоинвазивных методик и органосохраняющих вмешательств [142]. Оперативное вмешательство может изменить течение заболевания у детей с БК, которые растут физически и интеллектуально, поэтому решение о хирургическом лечении должно быть принято после тщательного рассмотрения показаний и оценки целесообразности операции.
5.1. Показания к хирургическому лечению БК
Данный раздел подготовлен на основе данных литературы, доказательного консенсуса по лечению детей с БК и клинических рекомендаций международных и национальных Обществ детских гастроэнтерологов, гепатологов и нутрициологов – Европейского [2], Британского [143] и Североамериканского [144], а также на основе доказательного консенсуса Всемирной Организации Здравоохранения по лечению ВЗК [4] и лечению
5.1.1. Острые кишечные осложнения
К ним относят кишечное кровотечение, перфорацию кишки и токсическую дилатацию ободочной кишки.
При кишечном кровотечении экстренное хирургическое вмешательство показано в случае массивной кровопотери, на фоне проведения адекватной медикаментозной терапии БК, при ухудшении состояния или отсутствии положительной динамики в течение 24–48 часов, несмотря на интенсивную гемостатическую терапию и заместительные гемотрансфузии эритроцитарной массы (у детей важными критериями продолжающегося кишечного кровотечения являются – учащенный более 6 раз в сутки стул с примесью крови, примесь крови в стуле более 10–15% объема циркулирующей крови, тахикардия, снижение гемоглобина менее 80 г/л) [152]. В случае кишечного кровотечения
перианальной формы БК [145]; клинических рекомендаций по лечению взрослых пациентов с БК – Европейских [146, 147] и Российских Ассоциаций колопроктологов и гастроэнтерологов [8].
Показаниями к хирургическому лечению являются острые и хронические кишечные осложнения БК, а также неэффективность консервативной терапии с задержкой физического развития [148, 149, 150, 151].
при БК выполняют экономную резекцию кишки с наложением анастомоза и/или формированием кишечной стомы; кроме того, с целью выявления дополнительных источников кровотечения, желательно проведение интраоперационной колонои энтероскопии [153].
Перфорация тонкой кишки в свободную брюшную полость является достаточно редким осложнением и обычно возникает в области патологического участка кишки со стриктурой [154]. При клинико-рентгенологических признаках перитонита (абдоминальный болевой синдром, положительные симптомы раздражения брюшины, свободный газ в брюшной полости – по данным обзорной R-графии органов брюшной полости) показано экстренное хирургическое вмешательство, которое в данной ситуации может быть ограничено
резекцией пораженного отдела кишки с формированием стомы или анастомоза. В случае экстренной операции рекомендуется избегать формирования первичного кишечного анастомоза без наложения
превентивной кишечной стомы. Перфорация толстой кишки при БК встречается крайне редко, операцией выбора является резекция ободочной кишки с формированием стомы [155].
Токсическая дилатация ободочной кишки (токсический мегаколон) является редким осложнением при БК толстой кишки и представляет собой не связанное с обструкцией расширение кишки на фоне симптомов интоксикации [156]. По данным обзорной рентгенографии органов брюшной полости отмечают увеличение диаметра поперечно-ободочного отдела толстой кишки: у подростков и взрослых пациентов более 60мм, у детей старше 11 лет – более 55мм, младше 11 лет – более 40мм. К факторам риска токсической дилатации относятся гипокалиемия, гипомагниемия, подготовка кишки к колоноскопии при помощи осмотических слабительных,
5.1.2. Хронические кишечные осложнения
Включают стриктуры кишки, внутрибрюшные инфильтраты и абсцессы, внутренние и наружные
применение антидиарейных препаратов. О развитии токсического мегаколон свидетельствует нарастание симптомов интоксикации (тахикардия, артериальная гипотония, фебрилитет), вздутие живота, резкое сокращение частоты стула (на фоне ранее имевшейся диареи) и уменьшение болей в животе [157]. При неэффективности интенсивной консервативной терапии в течении 24–48 часов, с применением эндоскопической декомпрессии кишечника, показано проведение экстренной операции с наложением илеостомы и отключением толстой кишки, либо экстренной субтотальной колэктомии с формированием терминальной илеостомы.
кишечные свищи, дисплазию эпителия высокой степени [8].
5.1.3. Неэффективность консервативной терапии и задержка физического развития
О неэффективности консервативной терапии свидетельствует наличие гормональной зависимости и резистентности; кроме того проявлением неадекватной лекарственной терапии также может являться задержка физического развития [2, 8, 158]. Отставание в росте имеется практически у каждого четвертого ребенка с БК [148].Своевременность хирургического вмешательства при БК демонстрировало прибавку роста у детей [159]. У детей с рефрактерной БК задержка роста является основным
показанием к хирургии, поскольку «окно возможностей» терапии может быть небольшим [2]. У детей с тяжелым течением БК, при неэффективности консервативного лечения, особенно в препубертатном или пубертатном возрасте, либо с задержкой роста и локальным поражением кишечника, может быть полезным выполнение резекции кишки для обеспечения практически здорового интервала в 2–3 года, и в этих случаях первичный кишечный анастомоз обычно безопасен [160].
5.2. Хирургическое лечение стриктурирующей и пенетрирующей БК
БК в детском возрасте часто представлена более тяжелыми осложненными формами, чем у взрослых, непредсказуемым прогнозом, и нередко приводит к необратимым изменениям не только в результате естественного течения заболевания,
но и вследствие перенесенных хирургических вмешательств [161, 162, 163]. Вероятность повторной резекции кишечника у детей с БК составляет до 29% в течение 10 лет после первого вмешательства [164].
5.2.1. Хирургическое лечение БК тонкой кишки и илеоцекальной зоны
При стриктурирующем фенотипе илеоцекальной БК формируется стриктура терминального отдела подвздошной кишки или илеоцекальной области [165]. Выявленное супрастенотическое расширение подвздошной кишки более чем на 3см в диаметре у детей с БК, значительно ассоциировано
с необратимыми фиброзными изменениями кишки и может являться показанием к хирургическому вмешательству [166]. Операцией выбора является илеоцекальная резекция с формированием илео-асцендоанастомоза [160, 167]. Предпочтительной методикой формирования тонкокишечного ана-
стомоза является наложение аппаратного анастомоза по типу «бок-в-бок», что уменьшает веро-
ятность его несостоятельности и последующего развития стриктуры [168, 169].
При отсутствии инфильтрата и абсцесса предпочтительней выполнение хирургического вмешательства на тонкой кишке и илеоцекальной зоне лапароскопическим способом [170, 171, 172]. Лапароскопические вмешательства в последнее десятилетие получили большое распространение у детей и взрослых пациентов с БК, как минимальная инвазивная процедура, с хорошим
косметическим результатом, более ранним восстановлением в послеоперационном периоде и коротким пребыванием в стационаре [173, 174]. После лапароскопических операций реже возникают такие осложнения, как спаечная непроходимость и раневая инфекция, однако частота послеоперационного рецидива БК сравнима с открытыми вмешательствами [175, 176 177, 178].
При осложненном течении БК с образованием стриктур тощей или подвздошной кишки, включая стриктуры анастомоза после предшествовавшей операции, альтернативой кишечной резекции является выполнение органосохраняющих стриктуропластик или создание обходных анастомозов, позволяющих избежать синдрома короткого кишечника [147]. При коротких стриктурах менее 10 см длиной наиболее общепринятой методикой является стриктуропластика по ХайнекеМикуличу (продольное рассечение кишки в области стриктуры с поперечным анастомозом), при
стриктурах кишки длиной 10–25 см используют методику Финнея (наложение широкого анастомоза по типу «бок-в-бок» на петле кишки со стриктурой), а в случае более протяженного поражения – операцию Мичеласси (пересечение кишки проксимальнее стриктуры и создание кишечного анастомоза по типу «бок-в-бок» по всей длине измененного участка) [179]. Противопоказаниями к стриктуропластике являются инфильтраты, абсцессы, злокачественные новообразования кишки или активное кровотечение и выраженное воспаление в области пораженного участка [167].
При БК осложненной формированием внутрибрюшного абсцесса требуется назначение антибактериальной терапии, а также проведение дренирования абсцесса или резекции пораженного участка кишки [180, 181]. Дополнительно к антибиотикам и дренированию абсцесса должна быть усилена специфическая противовоспалительная терапия БК, снижена доза глюкокортикоидных гормонов, проведена оптимизация энтерального питания. Внутрибрюшные абсцессы у детей с БК
в 90% случаев могут быть успешно дренированы чрезкожным доступом [162]. У пациентов с абсцессами, которые не могут быть дренированы (менее 2см в диаметре), должны использоваться максимальные дозы антибактериальных препаратов. Радикальное оперативное вмешательство показано в случае внутрибрюшных абсцессов, невосприимчивых к комбинации антимикробной и специфической терапии БК и невозможности проведения дренирования [182].
При выявлении межкишечных или кишечно-пузырных свищей у пациентов с БК основной целью
является разобщение свища с ограниченной кишечной резекцией, сохраняющей длину кишки [142].
5.2.2. Хирургическое лечение БК толстой кишки Ограниченное поражение толстой кишки при БК (менее трети ободочной кишки) не требует проведения колэктомии [183]. В этом случае можно ограничиться резекцией пораженного сегмента с формированием кишечного анастомоза в пределах здоровых тканей [184]. При выявлении
непротяженной стриктуры толстой кишки возможно выполнение эндоскопической дилатации стриктуры [185], однако данная манипуляция связана с более высоким риском рецидива заболевания по сравнению с резекцией пораженного участка кишечника [186].
При выявлении стриктуры восходящей и/или поперечно-ободочной кишки возможно выполнение правосторонней гемиколэктомии с илео-асцендоили илео-трансверзоанастомозом. При левостороннем поражении выполняется резекция левых отделов с формированием колоректального анастомоза. При вовлечении в патологический процесс всей ободочной кишки, при минимальной активности воспалительных изменений в прямой кишке, с адекватной функцией анального
сфинктера и отсутствии перианальных поражений, возможно формирование илео-ректоанастомоза [161]. Операция «отключения» транзита кишечного содержимого по толстой кишке путем формирования илеостомы показана только у крайне истощенных пациентов на фоне тяжелого активного колита [170]. Данный вид хирургического лечения является временным. Хирургическое вмешательство возможно безопасно выполнить с использованием лапароскопической техники [171, 187].
Возможность формирования тонкокишечного резервуарного анастомоза при БК толстой кишки является спорной, учитывая высокий риск
осложнений и частую необходимость удаления резервуара в связи с развитием перианальных поражений и БК резервуара [188].
У пациентов с длительным анамнезом БК толстой кишки (хотя в большей степени это касается язвенного колита) существенно повышается риск колоректального рака [189]. Важными факторами развития рака являются начало ВЗК в детском и подростковом возрасте и длительность анамнеза. Так, 10-тилетний анамнез заболевания повышает
риск развития рака до 2%; а 20-летний анамнез – уже до 8% [190]. Скрининг колоректального рака должен быть обязательным у пациентов с длительным анамнезом БК. Показанием к тотальной колэктомии является дисплазия эпителия высокой степени, выявленная в неизмененной слизистой оболочке, либо выявленные участки неоплазии.
5.2.3. Хирургическое лечение БК с поражением верхних отделов ЖКТ
Вовлечение в воспалительный процесс верхних отделов ЖКТ у детей с БК встречается чаще, чем у взрослых (до 30%), и является хорошо известной
фенотипической особенностью детского возраста [16,191]и обусловливает неблагоприятный прогноз, особенно при стриктурирующей фенотипе [147].
В качестве хирургического лечения возможно проведение эндоскопической баллонной дилатации стриктуры, формирование обходного анастомоза, выполнение стриктуропластики или резекция пораженного участка [165]. Прибегать
к формированию обходного тонкокишечного анастомоза на изолированной петле следует лишь в исключительных случаях (например, при стриктурах двенадцатиперстной кишки) из-за высокого риска развития синдрома избыточного бактериального
роста в отключенной части тонкой кишки и малигнизации. Стриктуры гастродуоденальной зоны (как правило, 12-перстной кишки) поддаются баллонной дилатации. Также эффективным является выполнение стриктуропластики [179]. Обширные
резекции способствуют формированию синдрома короткой тонкой кишки [146]. При наличии единичных или множественных непротяженных стриктур тощей кишки операцией выбора может быть стриктуропластика [192].
5.2.4. Медикаментозная и нутритивная поддержка в периоперационный период
В значительной степени изучено влияние предоперационной консервативной терапии БК на послеоперационные хирургические осложнения [193]. Преднизолон 20 мг ежедневно или его эквивалент в течение более шести недель до операции является значительным фактором риска для хирургических осложнений [194, 195]. Поэтому лечение стероидными гормонами рекомендуется прекратить, как только это возможно. Напротив, тиопурины можно безопасно использовать в периоперационный
период, отмены препарата до операции не требуется [196, 197]. В то время как лечение анти-ФНО-препаратами до операции может увеличивать частоту послеоперационных осложнений. Недавние исследования и мета-анализы показали повышенный риск развития послеоперационного сепсиса, раневых инфекций, внутрибрюшных абсцессов и несостоятельности анастомоза у пациентов с БК [198, 199, 200, 201, 202]. Сочетание стероидов и анти-ФНО повышает риск осложнений.
Недостаточное питание является значительным фактором риска послеоперационных осложнений, включая несостоятельность анастомоза, поскольку адекватное питание обеспечивает трофические свойства тканей, помогая заживлению ран [203]. Потеря 10% массы тела или более в течение 3-месячного периода, считается выраженным дефицитом веса, сопровождается задержкой физического развития. Такие дети и подростки должны получать
предоперационную нутритивную поддержку путем энтерального или сочетанного энтерально – парентерального питания [204, 205]. Уровень сывороточного альбумина не является основным маркером нарушения нутритивного статуса, так как уровень альбумина может зависеть от множества факторов, включая острый или хронический сепсис; в дополнение к уровню альбумина следует использовать другие показатели и инструментальные оценки [206].
5.3. Лечение БК с перианальными поражениями.
Перианальные поражения развиваются у 13–67% детей, могут встречаться при любой локализации БК
[207] и представлены гипертрофированными кожными подвесками (воспаленными анальными бахромка-
ми), анальными трещинами, параректальными абсцессами и свищами, стенозами ануса и прямой кишки [145]. У 10–12% детей с БК перианальные поражения являются первыми проявлениями заболевания [208].
Во многих клинических рекомендациях по лечению перианальной БК отмечена важная роль мануальной ревизии промежности под наркозом (“exam under anesthesia”), которая является не только ценным диагностическим мероприятием (т.н. «золотым
стандартом» в руках опытного хирурга), но и может сопровождаться хирургическим вмешательством – вскрытием и дренированием парапроктита, с проведением дренирующей непересекающей лигатуры, т.н. дренажа-сетона [209, 210, 211].
При БК с перианальными поражениями назначаются иммуносупрессоры и/или биологические анти-ФНО препараты, кроме того требуется
проведение антибактериальной терапии общим курсом не менее 3 мес. Подход к хирургическому вмешательству на перианальной области должен
быть индивидуален для каждого пациента [212, 213, 214]. При наличии трещин анального канала хирургическое вмешательство не рекомендуется, а отдается предпочтение местной противовоспалительной терапии и гигиеническому уходу [215]. В последние годы встратегию лечения пациентов с перианальными поражениями при БК были внесены изменения, сопряженные с новыми целями – 1) использовать простые эффективные процедуры; 2) минимизировать боль; 3) отдавать
предпочтение паллиативной помощи против агрессивного хирургического вмешательства [145].
Простые свищи, не сопровождающиеся какими-либо симптомами, не требуют хирургического вмешательства. Показано динамическое наблюдение на фоне адекватной консервативной терапии. При наличии симптомов возможно проведение фистулотомии или адекватного дренирования свища при помощи дренажа-сетона [211].
Лечение сложных свищей включает установку дренажей-сетонов в комбинации с агрессивной медикаментозной терапией. Показанием к установке дренирующих лигатур в большинстве случаев
является вовлечение части сфинктера в свищевой ход. Время удаления дренажа зависит от медикаментозной терапии [207].
Учитывая высокую эффективность биологической терапии при надлежащем дренировании
сложных свищей оправдано раннее назначение анти-ФНО терапии [2].
Тем не менее, сложные перианальные свищи, особенно с активной БК прямой кишки, с высокой частотой приводящие к развитию гнойно-септических осложнений, являются показанием к отключению пассажа кишечного отделяемого по толстой кишке путем формирования двуствольной илеостомы [171]. Однако, прекращение пассажа по кишечнику не приводит к заживлению свища
(только уменьшает симптоматику), но позволяет с успехом оперировать в условиях «отключенной» толстой кишки.
При отсутствии воспаления в дистальном отделе толстой кишки возможно выполнение низведения слизисто-мышечного лоскута прямой кишки с пластикой внутреннего свищевого отверстия [183,216].
Ректо-вестибулярные свищи у девочек с БК (ректо-вагинальные – у женщин) в подавляющем большинстве случаев требуют хирургического вмешательства. Лишь в отдельных ситуациях при наличии низкого свища между прямой кишкой и преддверием влагалища возможно проведение только консервативного лечения [217]. В осталь-
ных случаях показано оперативное лечение под прикрытием стомы [218]. Спонтанного закрытия ректо-вестибулярных свищей не происходит. При наличии активного воспаления в прямой кишке адекватная противовоспалительная терапия до операции увеличивает эффективность вмешательства.
Наличие стриктуры нижне-ампулярного отдела прямой кишки или стеноза анального канала является наиболее неблагоприятным фактором, повышающим вероятность формирования постоянной кишечной стомы [219, 220]. Формирование постоян-
ной стомы у детей с перианальными поражениями потребовалось в 10% случаев по данным ретроспективного объединенного обзора из двух центров [221]. В большинстве случаев данные осложнения требуют выполнения резекции прямой кишки [222].
В отдельных ситуациях, при отсутствии активного воспаления в вышележащих отделах кишки, возможно использование малоинвазивных способов коррекции дистальных стриктур, включающих инъекции стероидов и анти-ФНО-препаратов в область стриктуры, использование
баллонной дилатации, бужирование стриктуры расширителями Гегара (при стриктуре анального канала до зубчатой линии), до более травматичных хирургических методов, таких как стриктуропластика или резекция прямой кишки [145, 223].
5.4. Противорецидивная терапия после хирургического лечения БК
Даже при полном удалении всех макроскопически измененных отделов кишечника, хирургическое вмешательство не приводит к полному исцелению: в течение 5 лет клинически значимый рецидив отмечается у 28–45% пациентов, а в течение 10 лет – у 36–61%, что диктует необходимость проведения противорецидивной терапии после операции [164]. Потенциальными факторами риска
послеоперационного рецидива у пациентов с БК являются курение, предшествующая резекция кишки, генетические маркеры, перфорирующее течение БК, протяженность поражения (>40см тонкой кишки), перианальные поражения, две и более резекции кишки в анамнезе и короткая продолжительность болезни перед первой операцией [175, 224, 225].
В детском возрасте послеоперационный рецидив выявляется в первые годы после операции до 38% наблюдений, а через 5 лет после резекции до 50%
случаев, и его частота зависит от первичной локализации и распространенности БК [226].
Противорецидивную терапию рекомендуется начинать через 2 недели после оперативного вмешательства. В течение 3 мес. после операции рекомендуется проводить антибактериальную терапию: метронидазол, ципрофлоксацин (возможна смена антибиотиков каждые 2 недели). Смена антибиотиков позволяет снизить риск периферической нейропатии, которая развивается при длительных курсах метронидазола.
Спустя 6–12 месяцев всем оперированным пациентам с БК показано проведение контрольного обследования, в первую очередь, эндоскопического с оценкой эндоскопической активности в области анастомоза по шкале Rutgeerts (Табл. 7). При невозможности визуализировать зону анастомоза следует констатировать наличие или отсутствие рецидива, основываясь на сочетании данных рентгенологического
Оценка Определение
0 Нет признаков воспаления
1 <5 афтозных язв
>5 афтозных язв с нормальной слизистой оболочкой между ними или протяженные участки здоро-
Таблица 7.
Шкала эндоскопической активности послеоперационного рецидива болезни Крона по Rutgeerts [227]
2 вой слизистой оболочки между более выраженными изъязвлениями или поражения, ограниченные подвздошно-толстокишечным анастомозом.
3 Диффузный афтозный илеит с диффузно воспаленной слизистой оболочкой
4 Диффузное воспаление с крупными язвами, «булыжной мостовой» и/или сужением просвета.
обследования (как правило, КТ) и неинвазивных маркеров воспаления – С-реактивного белка, фекального кальпротектина и др.
При отсутствии признаков воспаления или обнаружении минимальных воспалительных изменений проводимая терапия должна быть продолжена. Наличие более выраженных воспалительных изменений (2–4) указывает на неэффективность проводимой терапии и должно служить показанием к усилению терапии: подключению
иммуносупрессоров у пациентов, ранее их не получавших или к проведению биологической терапии анти-ФНО у пациентов, находящихся на поддерживающей терапии азатиоприном/6-меркаптопурином. В дальнейшем, вне зависимости от характера течения заболевания и клинической манифестации БК, следует не реже раза в 1–3 года выполнять контрольное эндоскопическое исследование, следуя этому же алгоритму выбора противорецидивного средства [228].
Выбор терапии БК должен проводиться в соответствии с ее локализацией, распространенностью и тяжестью (табл. 8). Недостаточная эффективность
индукционной терапии требует интенсификации лечении. По достижении ремиссии проводится дальнейшая поддерживающая терапия.
6. Профилактика и диспансерное наблюдение
В связи с прогрессирующим характером заболевания пациенты, страдающие БК, должны получать постоянную (пожизненную терапию) и проходить регулярный (пожизненный) мониторинг активности заболевания. Контроль активности заболевания позволяют не только инструментальные методы исследования, но и лабораторные методы
анализа маркеров воспаления, в первую очередь, уровня фекального кальпротектина, концентрация которого в стуле коррелирует со степенью активности воспалительного процесса в кишечнике.
Периодичность и объем диспансерного наблюдения определяется индивидуально, но у большинства пациентов целесообразно:
Таблица 8.
Выбор терапии в зависимости от фенотипа БК
Фенотип Степень тяжести
Индукция ремиссии Интенсификация при
неэффективности
Поддержание ремиссии
L1 терминальный илеит
Месалазин в таблет-
Легкая ках с рН-зависимым
высвобождением
Будесонид в таблетках (9 мг/сут)
Месалазин или тиопурины
Средней тяжести
ПЭП или
Будесонид в таблетках (9–12 мг/сут)
Преднизолон 1 мг/кг/с Тиопурины
Сульфасалазин или месалазин в гранулах
Преднизолон 1 мг/кг/с Месалазин или тиопу-
Средней тяжести
ПЭП Преднизолон 1 мг/кг/с Тиопурины
Тяжелая Преднизолон 1–2 мг/кг/с Анти-ФНО Тиопурины или ан-
L2,3 -илеоколит (распространенный)
Средней тяжести
Преднизолон 1 мг/кг/с Анти-ФНО или мето-
Тиопурины, метотрексат или анти-ФНО
L2,3 +L4
(+верхние отделы)
Преднизолон 1–2 мг/кг Тяжелая peros или в/в + анти-
биотики
Преднизолон 1–2 мг/кг Тяжелая peros или в/в + анти-
биотики
Анти-ФНО
Анти-ФНО
Тиопурины или анти-ФНО
Тиопурины или анти-ФНО
+р (перианальная) Средней
Антибиотики + местное лечение
Анти-ФНО Тиопурины или ан-
В3 – свищевая форма
Тяжелая
Средней тяжести или тяжелая
Анти-ФНО + антибиотики + хирургическое лечение
Анти-ФНО + антибиотики + хирургическое лечение
Повышение дозы или сокращение интервалов между введением анти-ФНО
Повышение дозы или сокращение интервалов между введением анти-ФНО
Анти-ФНО или комбинация с тиопуринами или метотрексатом
Комбинация анти-ФНО с тиопуринами или метотрексатом





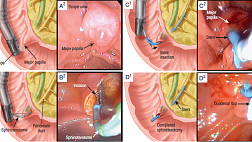







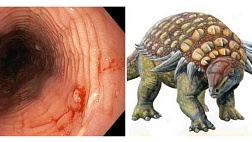





.jpg)





.png)
















Комментарии