- Компании
- Takeda. О компании, буклеты, каталоги, контакты
- Olympus. О компании, буклеты, каталоги, контакты
- Boston Scientific. О компании, буклеты, каталоги, контакты
- Pentax. О компании, буклеты, каталоги, контакты
- Fujifilm & R-Farm. О компании, буклеты, каталоги, контакты
- Erbe. О компании, буклеты, каталоги, контакты
- Еще каталоги
- Мероприятия
- Информация
- Обучение
- Классификации
- Атлас
- Quiz
- Разделы
- Пациенту
QR-код этой страницы

Для продолжения изучения на мобильном устройстве ПРОСКАНИРУЙТЕ QR-код с помощью спец. программы или фотокамеры мобильного устройства
Документы и приказы: Язвенный колит - клинические рекомендации 2024

Полный текст статьи:
Кодирование по Международной статистической
классификации болезней и проблем, связанных со здоровьем:K51
Год утверждения (частота пересмотра):2024
Возрастная категория:Взрослые
Пересмотр не позднее:2026
ID:193
Разработчик клинической рекомендации
Общероссийская общественная организация "Ассоциация колопроктологов России"
Российская Гастроэнтерологическая Ассоциация
Одобрено Научно-практическим Советом Минздрава РФ
Клинические рекомендации
Язвенный колит
Кодирование по Международной статистической
классификации болезней и проблем, связанных со здоровьем:K51
Год утверждения (частота пересмотра):2024
Возрастная категория:Взрослые
Пересмотр не позднее:2026
ID:193
Разработчик клинической рекомендации
- Общероссийская общественная организация "Ассоциация колопроктологов России"
- Российская Гастроэнтерологическая Ассоциация
Одобрено Научно-практическим Советом Минздрава РФ
Оглавление
- Список сокращений
- Термины и определения
- 1. Краткая информация по заболеванию или состоянию (группы заболеваний или состояний)
- 1.1 Определение заболевания или состояния (группы заболеваний или состояний)
- 1.2 Этиология и патогенез заболевания или состояния (группы заболеваний или состояний)
- 1.3 Эпидемиология заболевания или состояния (группы заболеваний или состояний)
- 1.4 Особенности кодирования заболевания или состояния (группы заболеваний или состояний) по Международной статистической классификации болезней и проблем, связанных со здоровьем
- 1.5 Классификация заболевания или состояния (группы заболеваний или состояний)
- 1.6 Клиническая картина заболевания или состояния (группы заболеваний или состояний)
- 2. Диагностика заболевания или состояния (группы заболеваний или состояний) медицинские показания и противопоказания к применению методов диагностики
- 2.1 Жалобы и анамнез
- 2.2 Физикальное обследование
- 2.3 Лабораторные диагностические исследования
- 2.4 Инструментальные диагностические исследования
- 2.5 Иные диагностические исследования
- 3. Лечение, включая медикаментозную и немедикаментозную терапии, диетотерапию, обезболивание, медицинские показания и противопоказания к применению методов лечения
- 4. Медицинская реабилитация и санаторно-курортное лечение, медицинские показания и противопоказания к применению методов медицинской реабилитации, в том числе основанных на использовании природных лечебных факторов
- 5. Профилактика и диспансерное наблюдение, медицинские показания и противопоказания к применению методов профилактики
- 6. Организация оказания медицинской помощи
- 7. Дополнительная информация (в том числе факторы, влияющие на исход заболевания или состояния)
- Критерии оценки качества медицинской помощи
- Список литературы
- Приложение А1. Состав рабочей группы по разработке и пересмотру клинических рекомендаций
- Приложение А2. Методология разработки клинических рекомендаций
- Приложение А3. Справочные материалы, включая соответствие показаний к применению и противопоказаний, способов применения и доз лекарственных препаратов, инструкции по применению лекарственного препарата
- Приложение Б. Алгоритмы действий врача
- Приложение В. Информация для пациента
- Приложение Г1-ГN. Шкалы оценки, вопросники и другие оценочные инструменты состояния пациента, приведенные в клинических рекомендациях
Список сокращений
АЛТ– аланинаминотрансфераза
АСТ– аспартатаминотрансфераза
5-АСК – 5-аминосалициловая кислота
АЗА – азатиоприн
Анти-ФНО – антитела к фактору некроза опухоли альфа
БК – болезнь Крона
БОС – биологическая обратная связь
ВЗК – воспалительные заболевания кишечника
Гамма-ГТ – гамма-глютамилтранспептидаза
ГИБП – генно-инженерный биологический препарат
ГКС – глюкокортикоиды
ДИ – доверительный интервал
ЖКТ – желудочно-кишечный тракт
ИАРА – илеоанальный резервуарный анастомоз
ИМТ– индекс массы тела
КТ – компьютерная томография
ЛДГ – лактатдегидрогеназа
ММХ – мультиматриксная оболочка
МП – меркаптопурин
МРТ – магнитно-резонансная томография
НПВС – нестероидные противовоспалительные и противоревматические препараты
РКИ – рандомизированное контролируемое испытание
СОЭ– скорость оседания эритроцитов
СРБ – С-реактивный белок
ТИС – таргетные иммуносупрессоры
ФНО-альфа – фактор некроза опухоли-альфа
ЯК – язвенный колит
Термины и определения
Язвенный колит (ЯК) – хроническое заболевание толстой кишки, характеризующееся иммунным воспалением ее слизистой оболочки.
Обострение (рецидив, атака) ЯК – появление типичных симптомов заболевания у больных ЯК в стадии клинической ремиссии, спонтанной или медикаментозно поддерживаемой. На практике признаками клинического обострения являются увеличение частоты дефекаций с выделением крови и/или характерные изменения, обнаруживаемые при эндоскопическом исследовании толстой кишки.
Ремиссия ЯК – исчезновение основных клинических симптомов заболевания [1] и заживление слизистой оболочки толстой кишки («глубокая ремиссия») [2].
Ремиссия ЯК, клиническая – отсутствие примеси крови в стуле, отсутствие императивных/ложных позывов при частоте дефекаций не более 3 раз в сутки.
Ремиссия ЯК, эндоскопическая – отсутствие видимых макроскопических признаков воспаления при эндоскопическом исследовании толстой кишки.
Ремиссия ЯК, гистологическая – отсутствие микроскопических признаков воспаления.
Стероидорезистентность – в случае тяжелой атаки – отсутствие положительной динамики со стороны клинических и лабораторных показателей, несмотря на применение системных ГКС в дозе, эквивалентной 2 мг/кг массы тела преднизолона** в сутки, в течение более чем 7 дней;
В случае среднетяжелой атаки – сохранение активности заболевания при пероральном приеме ГКС в дозе, эквивалентной 1 мг/кг массы тела преднизолона**, в течение 2 недель [3,4].
Стероидозависимость – увеличение активности болезни, возникшее при уменьшении дозы ГКС после достижения исходного улучшения в течение 3 месяцев от начала лечения;
Возникновение рецидива болезни в течение 3 месяцев после окончания лечения ГКС.
Бионаивный пациент – пациент, не получавший ранее генно-инженерных биологических препаратов (ГИБП) или таргетных иммуносупрессоров (ТИС).
Колэктомия – хирургическая операция по удалению слепой и всей ободочной кишки от илецекального клапана до ректосигмоидного перехода.
1. Краткая информация по заболеванию или состоянию (группы заболеваний или состояний)
1.1 Определение заболевания или состояния (группы заболеваний или состояний)
Язвенный колит (ЯК) – хроническое заболевание толстой кишки, характеризующееся иммунным воспалением ее слизистой оболочки.
При ЯК поражается только толстая кишка (за исключением ретроградного илеита), в процесс обязательно вовлекается прямая кишка, воспаление чаще всего ограничивается слизистой оболочкой (за исключением острого тяжелого колита) и носит диффузный характер.
1.2 Этиология и патогенез заболевания или состояния (группы заболеваний или состояний)
Этиология воспалительных заболеваний кишечника (ВЗК), в том числе ЯК, не установлена. Заболевание развивается в результате сочетания нескольких факторов, включающих генетическую предрасположенность, дефекты врожденного и приобретенного иммунитета, нарушения кишечной микрофлоры и влияние факторов окружающей среды. Описано около 100 генетических полиморфизмов, ассоциированных с ЯК. Генетическая детерминированность приводит к изменениям врожденного иммунного ответа, аутофагии, нарушению механизмов распознавания микроорганизмов, нарушению эпителиального барьера и, как результат, извращению адаптивного иммунитета. Ключевым дефектом, предрасполагающим к развитию ВЗК является нарушение распознавания бактериальных молекулярных маркеров (паттернов) дендритными клетками, что приводит к гиперактивации сигнальных провоспалительных путей. Также при ВЗК отмечается уменьшение разнообразия кишечной микрофлоры за счет снижения доли анаэробных бактерий, преимущественно Bacteroidetes и Firmicutes. На этом фоне развитие ВЗК происходит под действием пусковъых факторов, к которым относят курение, нервный стресс, дефицит витамина D, питание с пониженным содержанием пищевых волокон и повышенным содержанием животного белка, кишечные инфекции, особенно инфекция Clostridioides difficile и цитомегаловирусная инфекция.
Результатом взаимного влияния генетических и предрасполагающих факторов является активация различных субпопуляций Т-лимфоцитов: Т-хелперов 1, 2, 17 типов и регуляторных Т-лимфоцитов на разных этапах воспаления, что ведет к гиперэкспрессии провоспалительных цитокинов, таких как фактор некроза опухоли-альфа (ФНОα), интерлекинов 1, 12, 23, 17 (ИЛ 1, ИЛ 12, ИЛ 23, ИЛ 17) и других и молекул клеточной адгезии. Вследствие этих нарушений формируется воспалительная лимфоплазмоцитарная инфильтрация и деструкция слизистой оболочки толстой кишки с характерными для ЯК макроскопическими изменениями.
1.3 Эпидемиология заболевания или состояния (группы заболеваний или состояний)
Максимальная распространенность ЯК в мире в настоящее время составляет 505/100000 населения (в Европе), а заболеваемость в разных регионах колеблется в интервале от 0,6 до 24,3 на 100000 населения. Самая высокая заболеваемость ЯК 24,3/100000 отмечена в Европе, 19,2/100000 в Северной Америке [4,5,6,7,8].
Данные о распространенности ЯК в Российской Федерации ограничены [9,10]. Распространенность ЯК выше в северных широтах и в западных регионах. Заболеваемость и распространенность ЯК в Азии ниже, однако, в настоящее время увеличивается. Европеоиды страдают заболеванием чаще, чем представители негроидной и монголоидной рас. Пик заболеваемости приходится на возрастной интервал 20-30 лет, в некоторых странах отмечен второй пик заболеваемости в возрасте 60-70 лет. Заболеваемость среди мужчин и женщин приблизительно одинакова.
1.4 Особенности кодирования заболевания или состояния (группы заболеваний или состояний) по Международной статистической классификации болезней и проблем, связанных со здоровьем
K51.0 – Язвенный (хронический) энтероколит
K51.1 – Язвенный (хронический) илеоколит
K51.2 – Язвенный (хронический) проктит
K51.3 – Язвенный (хронический) ректосигмоидит
K51.4 – Псевдополипоз ободочной кишки
K51.5 – Мукозный проктоколит
K51.8 – Другие язвенные колиты
K51.9 – Язвенный колит неуточненный
1.5 Классификация заболевания или состояния (группы заболеваний или состояний)
Существующая классификация ЯК по протяженности поражения, характеру течения, тяжести атаки и наличию осложнений определяет выбор медикаментозной терапии, показания и выбор вида операции, а также периодичность скрининга на колоректальный рак [11].
Для описания протяженности поражения применяется Монреальская классификация (табл. 1), оценивающая протяженность макроскопических изменений при эндоскопическом исследовании толстой кишки.
Таблица 1. Монреальская классификация ЯК по протяженности поражения [12].
|
Протяженность воспаления |
Обозначение по Монреальской классификации |
Характеристика |
|
Проктит |
Е1 |
Дистальный ЯК, ограниченный прямой кишкой |
|
Левосторонний колит |
Е2 |
Поражение толстой кишки от анального сфинктера до левого изгиба ободочной кишки |
|
Тотальный колит (панколит) |
Е3 |
Поражение распространяется проксимальнее левого изгиба, захватывая всю толстую кишку, иногда в сочетании с ретроградным илеитом (вовлечением в воспалительный процесс 10–15 см подвздошной кишки) |
Особо следует отметить, что проктосигмоидит включен в понятие левостороннего ЯК, а тотальный колит включает и субтотальное поражение ободочной кишки проксимальнее левого изгиба.
По характеру течения выделяют:
1. Острое течение (менее 6 месяцев от дебюта заболевания);
2. Хроническое непрерывное течение (длительность ремиссии менее 6 месяцев на фоне адекватной терапии);
3. Хроническое рецидивирующее течение (длительность ремиссии более 6 месяцев).
Для правильного формулирования диагноза и определения тактики лечения следует оценивать тяжесть текущего обострения (атаки), для чего используются простые критерии Truelove-Witts, как правило, применяемые в повседневной клинической практике, и индекс активности ЯК (индекс Мейо; DAI), как правило, применяемый в клинических испытаниях. Однако, для оценки прогноза заболевания и определения социального статуса пациента, включая получение инвалидности, льготного лекарственного обеспечения, бесплатного санаторно-курортного лечения и других социальных льгот необходимо учитывать тяжесть заболевания в целом, что определяется тяжестью текущей атаки, наличием внекишечных проявлений и осложнений, рефрактерностью к лечению, в частности, развитием стероидной зависимости и резистентности. Выделяют легкую, среднетяжелую и тяжелую атаки ЯК (табл. 2 и 3).
Таблица 2. Тяжесть атаки ЯК согласно критериям Truelove-Witts [3,4].
|
Показатель |
Легкая атака |
Среднетяжелая атака |
Тяжелая атака |
|
Частота стула с кровью в сутки |
<4 |
≥4, если: |
≥6 и: |
|
ЧСС в 1мин |
<90 уд/мин |
≤90 уд/мин |
>90 уд/мин или |
|
Температура |
<37,5°С |
≤37,8°С |
>37,8°С или |
|
Гемоглобин |
> 115 г/л |
≥105 г/л |
<105 г/л или |
|
СОЭ или CРБ |
≤ 20 мм/ч Норма |
≤30 мм/ч ≤ 30 мг/л |
>30 мм/ч или >30 мг/л |
В клинической практике нередко встречается так называемая «сверхтяжелая или крайне тяжелая атака» ЯК, характеризующаяся диареей более 10-15 раз в сутки, нарастающим падением гемоглобина, лихорадкой выше 38°С, тяжелой гипопротеинемией и электролитными сдвигами, высоким уровнем С-реактивного белка (СРБ) [13,14,15]. Подходы к лечению такого колита отличаются от обычных. В англоязычной литературе такое состояние называется «острый тяжелый ЯК» (acute severe UC) [16].
Таблица 3. Тяжесть атаки согласно индексу активности ЯК (индекс Мейо).
|
Значение индекса (баллы) |
0 |
1 |
2 |
3 |
|
Частота стула |
Обычная |
На 1–2 в день больше обычной |
На 3–4 в день больше обычной |
На 5 в день больше обычной |
|
Примесь крови в стуле |
Нет |
Прожилки |
Видимая кровь |
Преимущественно кровь |
|
Состояние слизистой оболочки |
Норма |
Минимальная активность (1 балл по Schroeder) |
Умеренная активность (2 балла по Schroeder) |
Выраженная активность (3 балла по Schroeder) |
|
Общая оценка состояния врачом |
Норма |
Удовлетворительное состояние |
Состояние средней тяжести |
Тяжелое состояние |
|
Тяжесть атаки ЯК устанавливается по сумме баллов 4 параметров из таблицы: 0–2 баллов: ремиссия (при этом оценка параметров ректального кровотечения и эндоскопического состояния слизистой = 0 баллов); 3–5 баллов: легкая атака ЯК; 6–9 баллов: среднетяжелая атака ЯК 10–12 баллов: тяжелая атака ЯК | ||||
|
Частичный (неполный) индекс Мейо без данных эндоскопии: 0–1 балл: клиническая ремиссия (при этом параметр «ректальное кровотечение» = 0 баллов) 1–2 балла: легкая атака 3–5 баллов: среднетяжелая атака ≥6 баллов: тяжелая атака
| ||||
Используемая в индексе Мейо шкала оценки состояния слизистой оболочки по Schroeder приведена в Таблице 4 и применяется для оценки эндоскопической активности ЯК.
Таблица 4. Классификация ЯК в зависимости от эндоскопической активности (по Schroeder) [17].
|
0 |
1 (минимальная активность) |
2 (умеренная активность) |
3 (выраженная активность) |
|
Норма или неактивное заболевание |
Легкая гиперемия, смазанный сосудистый рисунок. Легкая контактная ранимость. |
Выраженная гиперемия, отсутствие сосудистого рисунка, умеренная контактная ранимость, эрозии). |
Спонтанная ранимость, изъязвления. |
Классификация ЯК в зависимости от ответа на глюкокортикостероиды (ГКС) облегчает выбор рациональной лечебной тактики, поскольку целью консервативного лечения является достижение стойкой ремиссии с прекращением терапии ГКС. Для этих целей выделяются [3,4]:
1. Стероидорезистентность:
а. в случае тяжелой атаки – отсутствие положительной динамики со стороны клинических и лабораторных показателей, несмотря на применение кортикостероидов системного действия (код АТХ H02A), глюкокортикоидов (код АТХ H02AB) в дозе, эквивалентной 2 мг/кг массы тела преднизолона** в сутки, в течение более чем 7 дней;
б. в случае среднетяжелой атаки – сохранение активности заболевания при пероральном приеме ГКС в дозе, эквивалентной 1 мг/кг массы тела преднизолона, в течение 2 недель.
2. Стероидозависимость:
а. увеличение активности болезни, возникшее при уменьшении дозы ГКС после достижения исходного улучшения в течение 3 месяцев от начала лечения;
б. возникновение рецидива болезни в течение 3 месяцев после окончания лечения ГКС.
При формулировании диагноза следует отразить характер течения заболевания, протяженность поражения, тяжесть текущей атаки или наличие ремиссии, наличие стероидной зависимости или резистентности, а также наличие внекишечных проявлений или кишечных осложнений ЯК. Ниже приведены примеры формулировок диагноза:
1. «Язвенный колит, хроническое рецидивирующее течение, проктит, среднетяжелая атака».
2. «Язвенный колит, хроническое непрерывное течение, левостороннее поражение, среднетяжелая атака. Стероидная зависимость. Внекишечные проявления (периферическая артропатия)».
3. «Язвенный колит, хроническое рецидивирующее течение, тотальное поражение, тяжелая атака. Стероидная резистентность. Токсический мегаколон».
1.6 Клиническая картина заболевания или состояния (группы заболеваний или состояний)
Клиническая картина ЯК включает четыре клинических синдрома:
Кишечный синдром. Типичные кишечные симптомы включают диарею, преимущественно в ночное время (65 % случаев), кровь в стуле (95-100% случаев), тенезмы (чаще при проктитах и проктосигмоидитах), иногда тенезмы в сочетании с запором при дистальном ограниченном поражении. При проктитах и проктосигмоидитах диарея может отсутствовать, в клинической картине преобладают тенезмы. Для ЯК, в отличие от БК, боль в животе не характерна. Может быть умеренно выраженный болевой абдоминальный синдром спастического характера, чаще перед стулом.
Эндотоксемия – признаки системного воспаления, обусловленные высокой активностью воспалительного процесса в толстой кишке. Эндотоксемия в разной степени сопутствует среднетяжелым и тяжелым формам ЯК. Основные симптомы – общая интоксикация, лихорадка, тахикардия, анемия, увеличение СОЭ, лейкоцитоз, тромбоцитоз, повышение уровня острофазных белков: СРБ, фибриногена.
Метаболические расстройства являются следствием диареи, токсемии, избыточной потери белка с калом вследствие экссудации и нарушением всасывания воды и электролитов. Клинические симптомы типичны: потеря массы тела (иногда до степени истощения), обезвоживание, гипопротеинемия, гипоальбуминемия с развитием отечного синдрома, гипокалиемия и другие электролитные нарушения, гиповитаминоз.
Внекишечные системные проявления (ВКП) встречаются в 20-25% случаев ЯК и обычно сопровождают тяжелые формы болезни [18] (табл. 5).
Таблица 5. Основные внекишечные (системные) проявления язвенного колита.
|
Аутоиммунные, связанные с активностью заболевания |
Аутоиммунные, не связанные с активностью заболевания |
Обусловленные длительным воспалением и метаболическими нарушениями |
|
Артропатии (артралгии, артриты) Поражение кожи (узловатая эритема, гангренозная пиодермия) Поражение слизистых (афтозный стоматит) Поражение глаз (увеит, ирит, иридоциклит, эписклерит) Поражение печени (аутоиммунный гепатит) |
Первичный склерозирующий холангит Анкилозирующий спондилит (сакроилеит) Остеопороз, остеомаляция Псориаз, псориатический артрит |
Холелитиаз Стеатоз печени, стеатогепатит Тромбоз периферических вен, тромбоэмболия легочной артерии Амилоидоз |
Аутоиммунные проявления, связанные с активностью воспалительного процесса, появляются вместе с основными кишечными симптомами обострения и исчезают вместе с ними на фоне лечения. Аутоиммунные проявления, не связанные с активностью процесса (в англоязычной литературе их часто называют «сопутствующими аутоиммунными заболеваниями»), имеют тенденцию к прогрессированию независимо от фазы основного заболевания (обострение или ремиссия) и часто определяют негативный прогноз болезни.
Кишечные осложнения ЯК включают кишечное кровотечение, токсическую дилатацию и перфорацию толстой кишки, а также колоректальный рак. Поскольку эти осложнения в большей степени требуют хирургического лечения, подробно они рассматриваются в Разделе 3.2 «Хирургическое лечение».
2. Диагностика заболевания или состояния (группы заболеваний или состояний) медицинские показания и противопоказания к применению методов диагностики
Критерии установления диагноза/состояния на основании патогномоничных данных:
1) анамнестических данных;
2) физикального обследования;
3) лабораторных исследований;
4) инструментального обследования.
Однозначных диагностических критериев ЯК не существует. Диагноз выставляется на основании сочетания данных анамнеза, клинической картины и типичных эндоскопических и гистологических изменений.
2.1 Жалобы и анамнез
- У всех пациентов при подозрении на ЯК рекомендуется сбор анамнеза и жалоб для верификации диагноза [19-22].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 4)
- В том числе при сборе анамнеза рекомендуется уточнить наличие факта курения для сужения круга диагностического поиска и верификации диагноза [23].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 3)
Комментарий: следует обратить внимание на частоту и характер стула (жидкий многократный стул, тенезмы), оценить суточный объем стула, длительность указанных симптомов, наличие примеси крови в каловых массах, характер болей в животе; поездки в южные страны; принимаемые лекарственные препараты (в частности, антибиотики и нестероидные противовоспалительные и противоревматическиие препараты (НПВП)); курение; наличие воспалительных и злокачественных заболеваний кишечника у родственников [24,25].
2.2 Физикальное обследование
- У всех пациентов с подозрением на ЯК в обязательном порядке рекомендуется физикальное обследование с целью сужения круга диагностического поиска и верификации диагноза:
- осмотр перианальной области;
- пальцевое исследование прямой кишки [26].
Уровень убедительности рекомендаций – C (уровень достоверности доказательств – 5)
Комментарий: при физикальном осмотре могут быть обнаружены различные проявления ЯК, включая лихорадку, периферические отеки, дефицит питания, наличие признаков перфорации или токсической дилатации толстой кишки, а также внекишечных проявлений.
2.3 Лабораторные диагностические исследования
- Рекомендуется всем пациентам при подозрении на ЯК общий (клинический) анализ крови развернутый для диагностики анемии, сопутствующей патологии, а также определения степени активности ЯК [27-32].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 4)
Комментарий: при клиническом анализе крови могут быть диагностированы анемии (железодефицитная, анемия хронического заболевания, В12- или фолиеводефицитная анемия), лейкоцитоз (на фоне хронического воспаления или на фоне стероидной терапии), тромбоцитоз, увеличение СОЭ.
- Рекомендуется всем пациентам при подозрении на ЯК анализ крови биохимический общетерапевтический (исследованиие уровня общего белка, альбумина, глюкозы, общего билирубина, холестерина, калия (К+), натрия (Na+), хлоридов (Сl-), , фибриногена в крови, исследование уровня С-реактивного белка в сыворотке крови, определение активности АЛТ, АСТ, гамма-ГТ, ЛДГ, щелочной фосфатазы в крови,) для диагностики сопутствующей патологии [29,32-36].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 4)
Комментарий: биохимическое исследование позволяет выявить электролитные нарушения, гипопротеинемию (в частности, гипоальбуминемию), а также повышение щелочной фосфатазы, что является возможным проявлением ассоциированного с ЯК первичного склерозирующего холангита.
- Рекомендуется пациентам с острым течением ЯК (первой атаке заболевания) проводить дифференциальную диагностику с острой кишечной инфекцией [37].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 4)
- Рекомендуется пациентам с обострением ЯК выполнить исследование кала на токсины А и В Clostridioides difficile для исключения клостридиальной инфекции [38-41].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 4)
- Рекомендуется выполнение лабораторного исследования кала на налиичие токсина клостридии диффициле (Clostridioides difficile) методами: иммуноферментного анализа с определением токсинов А и В и/или иммунохемилюминесцентного анализа с определением токсинов А и В и/или полимеразной цепной реакции [38-40].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 4)
- Всем пациентам при подозрении на ЯК, среднетяжелой и тяжелой атаках ЯК, при стероидорезистентности или резистентности к биологической терапии рекомендуется патолого-анатомическое исследование биопсийного (операционного) материала и/или проведение ПЦР в материале биоптатов слизистой оболочки толстой кишки (из очагов поражения) на наличие цитомегаловируса (ЦМВ) [42,43].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 4)
2.4 Инструментальные диагностические исследования
- Рекомендуется всем пациентам с легкой и умеренной активностью ЯК проведение илеоколоноскопии для верификации диагноза. Пациентам с выраженной активностью ЯК рекомендуется проведение сигмоидоскопии [25,44].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 4)
Комментарий: колоноскопия обязательна для установления диагноза ЯК и оценки активности ЯК, а также для решения вопроса о колэктомии. Эндоскопическое исследование толстой кишки является основным методом диагностики ЯК, однако, специфичные эндоскопические признаки отсутствуют. Наиболее характерными являются диффузное воспаление, ограниченное слизистой оболочкой, начинающееся в прямой кишке и распространяющееся проксимальнее, с четкой границей воспаления. Эндоскопическую активность ЯК наилучшим образом отражают контактная ранимость (выделение крови при контакте с эндоскопом), отсутствие сосудистого рисунка и наличие эрозий и изъязвлений. Обнаружение стойкого сужения кишки на фоне ЯК требует обязательного исключения колоректального рака.
- Рекомендуется пациентам с тяжелой атакой ЯК обзорная рентгенография органов брюшной полости для исключения перфорации толстой кишки [45].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 4)
- Рекомендуется пациентам с тяжелой атакой ЯК обзорная рентгенография органов брюшной полости для исключения токсической дилатации толстой кишки [25].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 5)
- Всем пациентам с подозрением на ЯК при первичной постановке диагноза, при сомнениях в правильности диагноза, рекомендуется выполнение биопсии слизистой оболочки толстой кишки с целью верификации диагноза [46,47].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 5)
Комментарий: при длительном анамнезе ЯК (более 7-10 лет) целесообразна хромоэндоскопия с прицельной биопсией или ступенчатая биопсия (из каждого отдела толстой кишки) для исключения дисплазии эпителия. Рекомендуемым стандартом биопсии при постановке диагноза является взятие биоптатов слизистой оболочки прямой кишки и не менее чем из 4 других участков толстой кишки, а также слизистой оболочки подвздошной кишки.
К микроскопическим признакам ЯК относятся деформация крипт (разветвленность, разнонаправленность, появление крипт разного диаметра, уменьшение плотности крипт, «укорочение крипт», крипты не достигают подлежащего слоя мышечной пластинки слизистой оболочки), «неровная» поверхность слизистой в биоптате слизистой оболочки, уменьшение числа бокаловидных клеток, базальный плазмоцитоз, инфильтрация собственной пластинки слизистой оболочки моноядерными клетками с примесью сегментоядерных лейкоцитов и эозинофилов, наличие крипт-абсцессов и базальных лимфоидных скоплений. Степень воспалительной инфильтрации обычно уменьшается по мере удаления от прямой кишки.
- Рекомендуется всем пациентам с подозрением на ЯК при первичной постановке диагноза, при сомнениях в правильности ранее выставленного диагноза, при длительном анамнезе ЯК, при подозрении на осложнения ЯК, а также для исключения патологии других органов брюшной полости - ультразвуковое исследование органов брюшной полости (комплексное), забрюшинного пространства, органов малого таза комплексное (трансвагинальное и трансабдоминальное) [48,49].
Уровень убедительности рекомендаций – А (уровень достоверности доказательств – 2)
- Рекомендуется пациентам с подозрением на ЯК, в качестве скрининговой диагностики, а также оценки эффективности проводимой терапии проведение ультразвукового исследования кишечника (ультразвуковое исследование тонкой кишки, ультразвуковое исследование толстой кишки, ультразвуковое исследование сигмовидной и прямой кишки) для оценки протяженности и выраженности поражения толстой кишки [50].
Уровень убедительности рекомендаций – В (уровень достоверности доказательств – 3)
- Рекомендуется всем пациентам с подозрением на ЯК при необходимости дифференциальной диагностики или при невозможности проведения полноценной илеоколоноскопии одно из следующих визуализирующих методов исследования:
- магнитно-резонансная томография (МРТ) толстой кишки с контрастированием [51];
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 4)
- компьютерная томография (КТ) с контрастированием кишечника (компьютерная томография толстой кишки с ретроградным контрастированием, компьютерная томография толстой кишки с двойным контрастированием, компьютерная томография тонкой кишки с контрастированием, компьютерная томография тонкой кишки с двойным контрастированием) (в случае недоступности экспертной оценки или невозможности выполнения МРТ) [52,53].
Уровень убедительности рекомендаций – B (уровень достоверности доказательств – 3)
- Рекомендуется пациентам с подозрением на ЯК при необходимости дифференциальной диагностики или при невозможности проведения полноценной колоноскопии, МРТ и КТ проведение ирригоскопии с двойным контрастированием для оценки протяженности поражения толстой кишки, уточнения наличия образований, стриктур и т.д. [26,54,55].
Уровень убедительности рекомендаций –С (уровень достоверности доказательств – 4)
Комментарий: пациентам с подозрением на ЯК также возможно выполнение дополнительных исследований в зависимости от клинической ситуации.
2.5 Иные диагностические исследования
Дополнительные инструментальные и лабораторные исследования выполняются преимущественно с целью проведения дифференциальной диагностики с рядом заболеваний. Это инфекционные, сосудистые, медикаментозные, токсические и радиационные поражения, а также дивертикулит и др. На следующем этапе дифференциальной диагностики проводится верификация клинических диагнозов ЯК и БК, относящихся к группе ВЗК. Таким образом, дифференциальный диагноз ЯК проводится с БК толстой кишки, острыми кишечными инфекциями (дизентерия, сальмонеллез, кампилобактериоз, иерсиниоз, амебиаз), паразитозами, поражениями кишечника, ассоциированными с Cl.difficile, в том числе вызванными антибиотиками [56], туберкулезом кишечника, системными васкулитами, раком толстой кишки, дивертикулитом, микроскопическими колитами (коллагеновым и лимфоцитарным) [56], радиационным проктитом.
С целью дифференциальной диагностики и подбора терапии при внекишечных проявлениях ЯК и сопутствующих состояниях может потребоваться консультация:
- врача-психотерапевта или медицинского психолога (невроз, планируемая операция с наличием стомы и т.п.);
- врача-эндокринолога (стероидный сахарный диабет, надпочечниковая недостаточность у пациентов на длительной терапии ГКС);
- врача-дерматовенеролога (дифференциальный диагноз узловатой эритемы, пиодермии и т.п.);
- врача-ревматолога (артропатии, сакроилеит и т.п.);
- врача-акушера-гинеколога (беременность).
3. Лечение, включая медикаментозную и немедикаментозную терапии, диетотерапию, обезболивание, медицинские показания и противопоказания к применению методов лечения
3.1 Консервативное лечение
3.1.1 Цели и принципы терапии
Лечебные мероприятия при ЯК включают в себя назначение лекарственных препаратов, хирургическое лечение, психосоциальную поддержку и диетические рекомендации.
Глобально цели лечения ЯК в настоящее время определены стратегией «Treat-to-target (Т2Т)», что означает «Лечение до достижения цели». Эта концепция направлена на достижение долгосрочного эффекта лечения, профилактики осложнений, уменьшение частоты госпитализаций, снижение риска операций и колоректального рака, улучшение качества жизни и снижение частоты инвалидизации у пациентов с хроническими заболеваниями [57,58]. С точки зрения ежедневной клинической практики целями терапии ЯК являются достижение и поддержание долговременной бесстероидной клинико-эндоскопической ремиссии (прекращение приема ГКС в течение 12 недель после начала терапии) [59].
В соответствии со стратегией «Т2Т» при ЯК первоочередной целью терапии должно быть полное купирование клинических симптомов (отсутствие крови в стуле и нормализация стула), о которых сообщает сам пациент. Обязательным является достижение эндоскопической ремиссии.
При прогрессировании процесса и/или развитии опасных для жизни осложнений конкретной целью является своевременное проведение хирургического лечения.
В рамках стратегии «Т2Т» предусмотрен непрерывный мониторинг эффективности лечения путем регулярного исследования биологических маркеров (СРБ, ФК) и проведения эндоскопического исследования [58].
Выбор вида консервативного или хирургического лечения определяется тяжестью атаки, протяженностью поражения толстой кишки, наличием ВКП, длительностью анамнеза, эффективностью и безопасностью ранее проводившейся терапии, а также риском развития осложнений ЯК [59,60] и наличием факторов риска негативного прогноза течения ЯК [61-64].
Факторы риска негативного прогноза течения ЯК
Предикторы агрессивного течения и предикторы риска колэктомии.
· Возраст установления диагноза ≤ 40 лет (ассоциирован с более тяжелым течением заболевания, коротким периодом ремиссий и более высоким риском колэктомии);
· возраст ≥ 65 лет на момент установления диагноза (ассоциирован с риском ранней колэктомии);
· распространенное поражение;
· высокая активность по данным эндоскопии (большие и/или глубокие язвы);
· наличие внекишечных проявлений;
· ранняя потребность в системных ГКС (назначение в дебюте заболевания) или потребность хотя бы в одном курсе ГКС;
· тяжелое обострение по Truelove-Witts (количество критериев дополнительно к частоте стула с кровью >6 раз/сутки коррелирует с прогнозом: частотой колэктомии в исходе текущего обострения) [65];
· сверхтяжелая атака ЯК с диареей более 10-15 раз в сутки, прогрессирующей анемией, лихорадкой выше 38°С, гипоальбуминемией ≤ 27г/л, высоким уровнем СРБ и глубокими обширными язвами слизистой оболочки толстой кишки ассоциирована с высоким риском колэктомии в первые дни обострения [13,15];
· повышенные уровни маркеров воспаления;
· некурящие и бывшие курильщики имеют тенденцию к большей протяженности воспаления и к более медленному заживлению. У курильщиков отмечены более редкие обострения и госпитализации.
Поскольку полное излечение пациентов ЯК достигается только путем удаления толстой кишки (колпроктэктомии), при достижении ремиссии неоперированный пациент должен оставаться на постоянной поддерживающей (противорецидивной) терапии. Следует особо отметить, что ГКС не могут применяться в качестве поддерживающей терапии. Ниже представлены рекомендации по выбору препаратов для индукции и поддержания ремиссии в зависимости от протяженности поражения и тяжести атаки [26].
3.1.2 Проктит. Легкая и среднетяжелая атака
- Группе пациентов с легким и среднетяжелым проктитом рекомендовано местное лечение препаратами месалазина** (код АТХ A07EC02) [26,66,67].
Уровень убедительности рекомендации B (уровень достоверности доказательств – 2)
Комментарий: в данной ситуации целесообразно назначение суппозиториев с месалазином** (1 г/сут, при необходимости дозу можно увеличить до дозы #месалазина** 2 г/сутки) или ректальной пены месалазина (1 г 1 раз/сутки, при необходимости дозу можно увеличить до дозы #месалазина 2 раз/сутки) [26,66,67,263]. Оценка терапевтического ответа проводится через 2 недели [66], при положительном ответе лечение в указанных дозах пролонгируется до 6-8 недель.
- Рекомендуется пациентам при неэффективности лечения ректальными формами месалазина** назначение ректальных форм ГКС (кортикостероиды для местного применения (Код АТХ A07EA) [68].
Уровень убедительности рекомендации А (уровень достоверности доказательств – 1)
Комментарий: в данной ситуации целесообразно назначать ректальную пену будесонида 2 мг в сутки или суппозитории с преднизолоном 10 мг (extempore) 2 раза в сутки с оценкой ответа через 2 недели для достижения ремиссии [26,68,69].
- Рекомендуется при достижении ремиссии поддерживающая терапия – ректальное введение #месалазина** (свечи или ректальная пена) 1 г 3 раза в неделю в виде монотерапии не менее 2 лет для поддержания ремиссии [26,70].
Уровень убедительности рекомендации В (уровень достоверности доказательств – 2)
- Рекомендуется при неэффективности местного лечения подключить пероральные формы месалазина** (гранулы, таблетки, таблетки кишечнорастворимые с пролонгированным высвобождением, покрытые пленочной оболочкой (ММХ)) в терапевтической дозе согласно инструкции по применению для достижения ремиссии [71].
Уровень убедительности рекомендации А (уровень достоверности доказательств – 2)
Комментарий. Допустимо назначение сульфасалазина** вместо месалазина** [74,77].
- Рекомендуется пациентам при отсутствии эффекта от пероральных форм месалазина** назначение ГКС для достижения ремиссии [26,69].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 5)
Комментарий: в данной клинической ситуации ГКС назначаются в таблетках в дозе эквивалентной преднизолону** 0,5-0,75 мг/кг массы тела в сутки для достижения ремиссии.
- Рекомендуется в случае рецидива, требующего повторного назначения ГКС, комбинировать ГКС с азатиоприном** (АЗА) или #меркаптопурином** (МП) для достижения ремиссии [26,72,229,230,231,232,233].
Для азатиоприна** (АЗА) - Уровень убедительности рекомендации А (уровень достоверности доказательств – 1)
Для #меркаптопурина** (МП) - Уровень убедительности рекомендации С (уровень достоверности доказательств – 4)
Комментарий: АЗА** назначается по 2-2,5 мг/кг, а #МП** по 1,5 мг/кг. Местная терапия (ректальная пена будесонида 2 мг в сутки, свечи с преднизолоном 10 мг х 1-2 раза в сутки (extempore)) может быть продолжена.
- Рекомендуется при достижении ремиссии, индуцированной ГКС, проводить поддерживающую терапию АЗА** 2-2,5 мг/кг (или #МП** 1,5 мг/кг) не менее 2 лет для сохранения ремиссии [71,72].
Уровень убедительности рекомендации А (уровень достоверности доказательств – 2)
- Рекомендуется пациентам, у которых обнаружена ДНК цитомегаловируса в слизистой оболочке толстой кишки терапия #ганцикловиром** в дозе 5мг/кг 2 раза в сутки в течение 14-21 дней для элиминации возбудителя [26,73].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 4)
Комментарий: на период проведения лечения #ганцикловиром** отмена базисной терапии не требуется.
3.1.3 Проктит. Тяжёлое течение (развивается крайне редко)
- Рекомендуется пациентам при тяжелом язвенном проктите внутривенное введение ГКС в дозе, эквивалентной #преднизолону** 1-1,5 мг/кг массы тела в сутки в комбинации с местной терапией месалазином** (суппозитории ректальные, ректальная пена) или в комбинации с ГКС ректально (пена будесонида 2 мг в сутки, свечи с преднизолоном 10 мг х 2 раза в сутки (extempore)) для достижения ремиссии [26,69, 234].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 5)
- В случае первой атаки ЯК при достижении ремиссии для ее поддержания пациентам рекомендуется терапия местными формами препаратов месалазина** (суппозитории ректальные, ректальная пена) 1 г х 3 раза в неделю в виде монотерапии или в комбинации с пероральным месалазином** (гранулы, таблетки, таблетки кишечнорастворимые с пролонгированным высвобождением, покрытые пленочной оболочкой ММХ) в дозе 2-2,4 г – не менее 2 лет для поддержания ремиссии [26,67,70,71,74,75,76].
Уровень убедительности рекомендации А (уровень достоверности доказательств – 1)
Комментарий. Допустимо назначение сульфасалазина** 2 г/сут вместо месалазина** [74,77].
- Рекомендуется в случае рецидива, требующего повторного назначения ГКС (системных или топических), одновременно с ГКС назначать АЗА** 2-2,5 мг/кг (или #МП** 1,5 мг/кг) и затем продолжать поддерживающую терапию иммуносупрессорами (АЗА** или #МП**) не менее 2 лет для сохранения ремиссии [72, 229, 230,231,232,233].
Для азатиоприна** (АЗА) - Уровень убедительности рекомендации А (уровень достоверности доказательств – 1)
Для #меркаптопурина** (МП) - Уровень убедительности рекомендации С (уровень достоверности доказательств – 4)
- Рекомендуется пациентам, у которых обнаружена ДНК цитомегаловируса в слизистой оболочке толстой кишки терапия #ганцикловиром** в дозе 5мг/кг 2 раза в сутки в течение 14-21 дней для элиминации возбудителя [26,73].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 4)
Комментарий: на период проведения лечения #ганцикловиром** отмена базисной терапии не требуется.
3.1.4 Левосторонний и тотальный язвенный колит. Легкая атака
- Рекомендуется пациентам при первой атаке или рецидиве назначение месалазина** внутрь (гранулы, таблетки, таблетки кишечнорастворимые с пролонгированным высвобождением, покрытые пленочной оболочкой ММХ) в максимальных терапевтических дозах в соответствии с инструкциями по применению в комбинации с месалазином** в клизмах 4 г/сут для достижения ремиссии [26,70,78,79].
Уровень убедительности рекомендации B (уровень достоверности доказательств – 3)
Комментарий: терапевтический ответ оценивается через 2 недели. При улучшении клинической картины и положительной лабораторной динамике терапия продолжается до 6-8 недель.
- Рекомендуется при отсутствии эффекта от комбинированной терапии препаратами месалазина** назначение ректальных форм ГКС [79,80].
Уровень убедительности рекомендации А (уровень достоверности доказательств – 2)
Комментарий: целесообразно назначение ректальной пены будесонида 2 мг в сутки или суспензии #гидрокортизона ацетата + лидокаин 125-250 мг 1 раз в сутки в виде клизм или ректального капельного введения для достижения ремиссии [235, 236,267,268,269 ].
- Рекомендуется пациентам при достижении ремиссии проводить поддерживающую терапию пероральным месалазином** (гранулы, таблетки, таблетки кишечнорастворимые с пролонгированным высвобождением, покрытые пленочной оболочкой ММХ) 2-2,4 г/сут для сохранения ремиссии [81].
Уровень убедительности рекомендации А (уровень достоверности доказательств – 1)
Комментарий: дополнительное введение месалазина** в клизмах по 2 г х 2 раза в неделю («терапия выходного дня») увеличивает вероятность долгосрочной ремиссии.
- Рекомендуется пациентам при отсутствии ответа на комбинированную терапию пероральными препаратами месалазина** в сочетании с любым ректальным лекарственным средством назначение кортикостероидов для местного применения (топических ГКС) (код АТХ A07EA) (будесонид (таблетки кишечнорастворимые с пролонгированным высвобождением, покрытые пленочной оболочкой) MMX) или кортикостероидов системного действия (код АТХ H02A) (см. раздел 3.1.4) для индукции ремиссии [82].
Уровень убедительности рекомендации В (уровень достоверности доказательств – 3)
- Рекомендуется пациентам, у которых обнаружена ДНК цитомегаловируса в слизистой оболочке толстой кишки терапия #ганцикловиром** в дозе 5мг/кг 2 раза в сутки в течение 14-21 дня для элиминации возбудителя [26,73].
Уровень убедительности рекомендации C (уровень достоверности доказательств – 4)
Комментарий: на период проведения лечения #ганцикловиром** отмена базисной терапии не требуется.
3.1.5 Левосторонний и тотальный язвенный колит. Среднетяжелая атака
- Рекомендуется пациентам при первой атаке или рецидиве ЯК назначение перорального месалазина** (гранулы, таблетки, таблетки ММХ) в максимальной терапевтической дозе (в соответствии с инструкцией по применению) в комбинации с месалазином** в клизмах 4 г/сут для достижения ремиссии [26,75,76].
Уровень убедительности рекомендации А (уровень достоверности доказательств – 1)
Комментарий: терапевтический ответ оценивается через 2 недели. При улучшении клинической картины и положительной лабораторной динамике терапия продолжается до 6-8 недель.
- Рекомендуется пациентам при достижении ремиссии поддерживающая терапия препаратами месалазина** (гранулы, таблетки, таблетки ММХ) 2,0-2,4 г/сут внутрь + месалазин** в клизмах по 4 г х 2 раза в неделю для сохранения ремиссии [26,75,76,79].
Уровень убедительности рекомендации А (уровень достоверности доказательств – 1)
Комментарий: допустимо назначение сульфасалазина** 2 г/сут вместо месалазина** [74,77].
- Рекомендуется пациентам без ответа на месалазин** в течение 2 недель, но при отсутствии признаков системного воспаления назначение топических ГКС (будесонид (таблетки кишечнорастворимые с пролонгированным высвобождением, покрытые пленочной оболочкой ММХ) . глюкокортикостероид для местного применения (топический) ГКС (код АТХ A07EA06) назначают в дозе 9 мг/сут [243]. После 8 недельного приема будесонида (таблетки кишечнорастворимые с пролонгированным высвобождением, покрытые пленочной оболочкой ММХ), снижение дозы проводится через день в течение 1-2 недель до полной отмены [46,83,84,85.
Уровень убедительности рекомендации А (уровень достоверности доказательств – 2)
- Рекомендуется пациентам при неэффективности месалазина** в течение 2 недель и при признаках системного воспаления назначение кортикостероиды системного действия (код АТХ H02A), глюкокортикоиды (код АТХ H02AB) для достижения терапевтического эффекта [46,82,86,87,88].
Уровень убедительности рекомендации А (уровень достоверности доказательств – 1)
Комментарий: системные ГКС назначают в дозе, эквивалентной преднизолону** 1 мг/кг массы тела в сутки до достижения клинического ответа с последующим снижением по 5 мг в 5-7 дней до полной отмены, в течение не более 12 недель.
- Рекомендуется пациентам при снижении дозы ГКС до эквивалентной 35-45 мг преднизолона**, назначить дополнительно месалазин** (гранулы, таблетки, таблетки кишечнорастворимые с пролонгированным высвобождением, покрытые пленочной оболочкой (ММХ) в максимальной терапевтической дозе в соответствии с инструкциями к препаратам для поддержания терапевтического эффекта (в том случае, если пациент не получает иммуносупрессоров (противоопухулевые препараты и иммуномодуляторы, Азатиоприн** код АТХ L04AX01, #Меркаптопурин** код АТХ L01BB02) и ГИБТ- ингибиторы фактора некроза опухоли альфа (ФНО-альфа) (инфликсимаб** (код АТХ L04AB02), адалимумаб** (код АТХ L04AB04), голимумаб** (код АТХ L04AB06), селективные иммунодепрессанты – ведолизумаб** (код АТХ L04AA33), тофацитиниб** (код АТХ L04AA29), упадацитиниб** (код АТХ L04AA44), озанимод (код АТХ L04AA38), ингибиторы интерлейкина устекинумаб** (код АТХ L04AC05)[78].
Уровень убедительности рекомендации B (уровень достоверности доказательств – 3)
Комментарий: дальнейшее снижение ГКС следует проводить на фоне месалазина** с последующим переходом на поддерживающую терапию месалазином** (гранулы, таблетки, таблетки кишечнорастворимые с пролонгированным высвобождением, покрытые пленочной оболочкой (ММХ) 2,0-2,4 г в сутки.
- Рекомендуется пациентам в случае непереносимости препаратов месалазина** или при необходимости повторного назначения ГКС в течение года и менее комбинировать ГКС с АЗА** 2,0-2,5 мг/кг или #МП** 1,5 мг/кг для достижения терапевтического эффекта [72,89, 229,230,231,232,233].
Для азатиоприна** (АЗА) - Уровень убедительности рекомендации A (уровень достоверности доказательств – 1)
Для #меркаптопурина** (МП) - Уровень убедительности рекомендации С (уровень достоверности доказательств – 4)
- Рекомендуется пациентам при достижении ремиссии продолжение поддерживающей терапии АЗА** 2,0-2,5 мг/кг/сут или #МП** 1,5 мг/кг не менее 2 лет для сохранения ремиссии [72,89].
Уровень убедительности рекомендации А (уровень достоверности доказательств – 2)
- Рекомендуется пациентам при отсутствии эффекта от ГКС в течение 2 недель назначение ГИБП - ингибиторы фактора некроза опухоли альфа (ФНО-альфа) (инфликсимаб**, адалимумаб**, голимумаб**), селективные иммунодепрессанты (ведолизумаб**), ингибиторы интерлейкина (устекинумаб**) или ТИС - селективные иммунодепрессанты (тофацитиниб**, упадацитиниб** или озанимод) для достижения ремиссии в виде индукционного (инициирующего) курса и поддерживающей терапии [90-96, 106, 238].
Уровень убедительности рекомендации А (уровень достоверности доказательств – 2)
Комментарий: Схемы и дозы препаратов для ГИБП и ТИС в рамках индукционного (инициирующего) курса и поддерживающей терапии:
· для инфликсимаба** индукционный (инициирующий) курс предусматривает трехкратное введение на 0, 2 и 6 неделе внутривенно в дозе 5 мг/кг массы тела, затем такая же доза для поддерживающей терапии 1 раз в 8 недель
· для адалимумаба** индукционный (инициирующий) курс состоит из первого подкожного введения в дозе 160 мг, затем второго подкожного введения через 2 недели в дозе 80 мг, затем поддерживающая терапия в дозе 40 мг каждые 2 недели
· для голимумаба** индукционный (инициирующий) курс состоит из первого подкожного введения 200 мг, второго подкожного введения через 2 недели в дозе 100 мг, третьего введения - 100 мг или 50 мг исходя из массы тела пациента, далее поддерживающая терапия проводится в той же дозировке, подкожно каждые 4 недели
· для ведолизумаба** индукционный (инициирующий) курс предусматривает трехкратное введение на 0, 2 и 6 неделе внутривенно в дозе 300 мг, затем поддерживающее лечение по 300 мг внутривенно каждые 8 недель
· для устекинумаба** индукционная (инициирующая) доза вводится внутривенно в первый день с расчетом дозы по массе тела пациента на момент введения, далее через 8 недель первое поддерживающее подкожное введение в дозе 90 мг и далее терапия в дозе 90 мг подкожно каждые 12 или 8 недель (при потере ответа).
· для тофацитиниба** 8-недельный индукционный (инициирующий) курс в дозе 10 мг х 2 раза в сутки, затем 5 мг х 2 раза в сутки в качестве поддерживающей терапии
· для упадацитиниба** 8-недельный индукционный (инициирующий) курс в дозе 45 мг в таблетках 1 раз в сутки и затем 30 мг или 15 мг в таблетках 1 раз в сутки в качестве поддерживающей терапии
· для озанимода индукционный (инициирующий) курс составляет 7 дней с постепенным увеличением дозы перорально (начиная с 0,23 мг в сутки до 0,92 мг в сутки) согласно инструкции по применению, на 8-й день и далее полная доза составляет 0,92 мг 1 раз в сутки.
У бионаивных пациентов любой из указанных препаратов может быть использован в качестве первой линии терапии [203]. Следует иметь в виду, что в первой линии терапии ведолизумаб** эффективнее адалимумаба** [210].
- Рекомендуется пациентам, получающим инфликсимаб**, комбинировать его с другими иммунодепрессантами (код АТХ L04AX) (АЗА** 2,0-2,5 мг/кг) для повышения эффективности лечения [72,97,98].
Уровень убедительности рекомендации А (уровень достоверности доказательств – 2)
Комментарий: допустимо применение #МП** 1,5 мг/кг вместо АЗА** в связи с тем, что МП** является метаболитом АЗА**. Для других ГИБП (адалимумаб** – (код АТХ L04AB04), голимумаб** (код АТХ L04AB06), селективных иммунодепрессантов – ведолизумаб** (код АТХ L04AA33), ингибиторов интерлейкина устекинумаб** (код АТХ L04AC05) тофациниб** ( код АТХ L04AA29), упадацитиниб** (код АТХ L04AA44), озанимод (код АТХ L04AA38), эффективность комбинации с иммуносупрессорами ( другие иммунодепрессанты код АТХ L04AX) не доказана. Совместное применение азатиоприна** и тофацитиниба** противопоказано [99,100].
- Рекомендуется пациентам при эффективности индукционного курса ГИБП и ТИС (Селективные иммунодепрессанты код АТХ L04AA: озанимод, упадацитиниб**, тофацитиниб**) проводить противорецидивную терапию тем же препаратом в соответствии с инструкцией по применению в течение, как минимум, 2 лет для поддержания ремиссии [91,92,93,101,102].
Уровень убедительности рекомендации А (уровень достоверности доказательств – 2)
- Рекомендуется пациентам при первичной неэффективности или потере ответа на любой из ингибиторов фактора некроза опухоли альфа (ФНО-альфа) препаратов смена терапии на ведолизумаб**, тофацитиниб**, устекинумаб**, упадацитиниб** или озанимод для достижения ремиссии [93,95,96,103,104, 239].
Уровень убедительности рекомендации А (уровень достоверности доказательств – 2)
Комментарий: любой из указанных препаратов может быть назначен в качестве 2-ой и последующих линий терапии на фоне ГКС или без них. При выборе ведолизумаба** после ингибиторов фактора некроза опухоли альфа (ФНО-альфа) следует иметь в виду, что его эффективность в качестве препарата 2-ой линии ниже, чем в 1-ой линии [211]. Выбор устекинумаба** в качестве второй линии ГИБП при неэффективности первого ингибитора фактора некроза опухоли альфа (ФНО-альфа) ассоциирован с лучшими результатами (достижением клинического ответа и клинической ремиссии), по сравнению с переводом пациента на другой ингибитор фактора некроза опухоли альфа (ФНО-альфа) или ведолизумаб** [225,226].
- Рекомендуется пациентам при потере ответа на ингибиторы фактора некроза опухоли альфа (ФНО-альфа) препараты в 1-ой линии терапии (рецидив ЯК на фоне ранее достигнутой ремиссии) оптимизация терапии в виде увеличения дозы препарата (10 мг/кг инфликсимаба** каждые 8 недель, 100 мг голимумаба** каждые 4 недели, 80 мг адалимумаба** каждые 2 недели) или сокращения интервалов между введениями (#инфликсимаб** до 4-6 недель, адалимумаб** 40 мг каждую неделю) или назначение препаратов другого механизма действия: ведолизумаба**, тофацитиниба**, устекинумаба**, упадацитиниба** или озанимода для достижения терапевтического эффекта [90, 91,92,93,101,102,104,105, 240, 241, 242].
Уровень убедительности рекомендации А (уровень достоверности доказательств – 3)
Комментарий: смена на другой ингибитор фактора некроза опухоли альфа (ФНО-альфа) препарат возможна, но ее эффективность ниже, чем при переходе на препараты других классов (ведолизумаб**, тофацитиниб**, устекинумаб**, упадацитиниб** или озанимод).
- Рекомендуется пациентам при потере ответа на ведолизумаб** в стандартной дозе 300 мг каждые 8 недель оптимизация терапии в виде сокращения интервалов между введениями до 4 недель или смена на биологический препарат другого класса (ингибитора фактора некроза опухоли альфа (ФНО-альфа), устекинумаб**, тофацитиниб**, упадацитиниб**, озанимод) [106,211, 244,264 ].
Уровень убедительности рекомендации C (уровень достоверности доказательств – 3)
Комментарий: эффективность ингибиторов фактора некроза опухоли альфа (ФНО-альфа) во 2-й линии терапии после потери ответа на ведолизумаб** не снижается по сравнению с их эффективностью в 1-ой линии, т.е. применение ведолизумаба** не влияет на последующую эффективность ингибитров фактора некроза опухоли альфа (ФНО-альфа) [211,212].
- Рекомендуется пациентам при потере ответа на устекинумаб** в стандартном режиме введения каждые 12 недель оптимизация терапии в виде сокращения интервалов между введениями до 8 недель или смена на препарат другого класса ГИБП или ТИС
): ингибиторы фактора некроза опухоли альфа (ФНО-альфа) (инфликсимаб** (код АТХ L04AB02), адалимумаб** (код АТХ L04AB04), голимумаб** (код АТХ L04AB06), селективные иммунодепрессанты (ведолизумаб** код АТХ L04AA33, тофацитиниб** код АТХ L04AA29, упадацитиниб** код АТХ L04AA44, озанимод код АТХ L04AA38) [104, 244,245,246].
Уровень убедительности рекомендации C (уровень достоверности доказательств – 3)
- Рекомендуется пациентам при потере ответа на тофацитиниб** в стандартной дозе 10 мг в день оптимизация терапии до 20 мг в день [107].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 4)
Комментарий: доказательная база о возможности перехода с тофацитиниба** на биологические препараты недостаточна. Смена препаратов возможна и остается на усмотрение лечащего врача. При достижении стабильной клинико-эндоскопической бесстероидной ремиссии длительность биологической терапии определяется лечащим врачом. В большинстве стран лечение проводят в течение многих лет. Ранняя отмена препаратов, как правило, приводит к рецидиву ЯК в короткие сроки. При невозможности пролонгированного использования ГИБП и ТИС, поддерживающая терапия проводится только иммуносупрессорами (Противоопухолевые препараты и иммуномодуляторы: АЗА**, #МП**).
- Рекомендуется пациентам при рецидиве, возникшем на фоне поддерживающей терапии азатиоприном** код АТХ L04AX01 или #меркаптопурином** код АТХ АТХ L01BB026) , назначение ГИБП ингибиторов фактора некроза опухоли альфа (ФНО-альфа) (инфликсимаб** (код АТХ L04AB02), адалимумаб** (код АТХ L04AB04), голимумаб** (код АТХ L04AB06), ведолизумаб** (код АТХ L04AA33) или ингибитора интерлейкина устекинумаб** (код АТХ L04AC05))или селективных иммунодепрессантов (ТИС) (тофацитиниба** код АТХ L04AA29, упадацитиниба** (код АТХ L04AA44) или озанимода (код АТХ L04AA38)),с отменой тиопуринов согласно инструкции по медицинскому применению [91,92,93,94,95,96,101,238].
Уровень убедительности рекомендации А (уровень достоверности доказательств – 2)
Комментарий: любой из указанных препаратов может назначаться в качестве первой линии терапии (см. раздел 3.1.5).
- Рекомендуется пациентам, у которых обнаружена ДНК цитомегаловируса в слизистой оболочке толстой кишки терапия #ганцикловиром** в дозе 5мг/кг 2 раза в сутки в течение 14-21 дня для элиминации возбудителя [26,73].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 4)
Комментарий: на период проведения лечения #ганцикловиром** отмена базисной терапии не требуется.
3.1.6 Левосторонний и тотальный язвенный колит. Тяжелая атака
- Рекомендуется пациентам в качестве первой линии терапии внутривенное введение ГКС для достижения ремиссии [26,108].
Уровень убедительности рекомендации А (уровень достоверности доказательств – 2)
Комментарий: применение ГКС целесообразно в дозе, эквивалентной преднизолону** 2 мг/кг массы тела внутривенно (при высокой массе тела возможно назначение 1,5 мг/кг) в течение 7 дней или применение гидрокортизона** в эквивалентной дозе. Эквивалентность доз и длительность действия ГКС приведена в таблице 6. Ответ оценивается в интервале от 3 до 7 дней. Если в течение трех дней состояние стабильно, то терапию продолжают до 7 дней. Если состояние больного в течение трех дней ухудшается ставится вопрос о «терапии спасения» или о колэктомии. Если через 7 дней отмечено клиническое улучшение, то терапию ГКС можно продолжить до стабильного улучшения и затем переходить на пероральный прием препаратов и медленно снижать дозу по 5 мг в 5-7 дней. В случае отсутствия значимого клинического улучшения через 7 дней состояние расценивается как стероидорезистентность.
- Рекомендуется пациентам дополнительно назначить местную терапию клизмами с месалазином** 4 г в сутки или суспензией #гидрокортизона-ацетата+лидокаином 250 мг х 1 раз в сутки в виде клизм или ректального капельного введения для достижения ремиссии [79,80, 235,236,246,267,268,269].
Уровень убедительности рекомендации C (уровень достоверности доказательств – 5)
- Рекомендуется пациентам при наличии метаболических нарушений проводить инфузионную терапию с целью регидратации, коррекции белково-электролитных нарушений [59].
Уровень убедительности рекомендации C (уровень достоверности доказательств – 5)
Комментарий: гипокалиемия и гипомагниемия повышают риск токсической дилатации ободочной кишки.
- Рекомендуется пациентам при уровне гемоглобина ниже 80 г/л для коррекции анемии в виде гемотрансфузии (эритромасса), при уровне гемоглобина от 80 до 100 г/л – терапия препаратами железа парентерально: железа [III] гидроксид сахарозный комплекс**, железа (III) гидроксид декстран, железа (III) гидроксид олигоизомальтозат**, железа карбоксимальтозат** [109].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 5)
- Рекомендуется госпитализированным пациентам при наличии показаний для снижения риска тромбообразования проведение профилактической терапии низкомолекулярными гепаринами (АХТ В01АВ Группа гепарина), гепарином натрия** подкожно 5000 МЕ 2-3 раза в сутки или #эноксапарином натрия** подкожно 40 мг 1 раз в сутки, или #фондапаринуксом натрия 2,5 мг подкожно 1 раз в сутки [204,205, 247, 257, 258,259, 265].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 4)
- Рекомендуется у пациентов с дефицитом массы тела (ИМТ менее 18) назначение дополнительного энтерального, в том числе зондового, питания для улучшения трофологического статуса [110].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 2)
Комментарий: полное парентеральное питание и/или временное ограничение приема пищи внутрь нецелесообразно.
- При развитии признаков системного воспаления у пациентов рекомендуется назначение антибактериальных препаратов системного действия с целью профилактики септических осложнений:
1 линия – #метронидазол**(500 мг в/в 3 раза в сутки) + фторхинолоны (#ципрофлоксацин** 500 мг в/в 2 раза в сутки), # ципрофлоксацин** 400 мг в/в 2 раза в сутки) [112, 113, 261,262, 270];
Комментарий: При неээфективности антибактериальной терапии 1 линии возможно использование комбинации иных антибактериальных препаратов системного действия с учетом чувствительности микроорганизма [113]
Уровень убедительности рекомендации А (уровень достоверности доказательств – 1)
Таблица 6. Сравнительная характеристика ГКС
|
Препарат |
Длительность действия (t1/2) |
Эквивалентная доза (мг) |
|
Кортизо |
8-12 ч |
20 |
|
Преднизолон** |
12-36 ч |
5 |
|
Метилпреднизолон** |
12-36 ч |
4 |
- Рекомендуется пациентам при клиническом ответе на ГКС через 7 дней перевод на пероральный прием преднизолона** с последующим снижением до полной отмены по 5-10 мг преднизолона** в 5-7 дней для поддержания ремиссии [59].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 5)
Комментарий: схема перехода с внутривенных ГКС на пероральные формы рассматривается индивидуально лечащим врачом в зависимости от скорости достижения эффекта и выраженности терапевтического ответа.
При развитии стероидорезистентности, если нет непосредственной угрозы жизни или тяжелых осложнений, требующих немедленного оперативного вмешательства, показана «терапия спасения» на фоне сохраняющегося лечения ГКС, т.е. усиление консервативной терапии, которая проводится инфликсимабом** в дозе 5 мг/кг в рамках индукционного курса на 0, 2 и 6 неделе или #циклоспорином** в/в в дозе 2-4 мг/кг в течение 7 дней (с мониторированием показателей функции почек и определением концентрации препарата в крови) или тофацитинибом** (20 мг/сут в рамках индукционного курса в течение 8 недель) [103,206,207,208, 256, 260]. Клинический результат такой терапии оценивается через 7 дней. Исследования показали, что эффективность двух схем (с инфликсимабом** и #циклоспорином**) на 8 день лечения идентична, поэтому в настоящее время в зарубежной практике используется в основном инфликсимаб**, как препарат более безопасный и не требующий трудоемкого и дорогостоящего определения концентрации. При отсутствии эффекта через 7-8 дней рассматриваются варианты хирургического лечения. При невозможности назначения инфликсимаба** допустимо назначение тофацитиниба** с учетом скорости достижения эффекта [207,208] (см. раздел 3.1.5).
- Рекомендуется пациентам при достижении ремиссии на инфликсимабе** продолжить поддерживающую противорецидивную терапию этим же препаратом по стандартной схеме в комбинации с АЗА** 2-2,5 мг/кг (или #МП 1,5 мг/кг) или без него [98,102,114,248 ].
Уровень убедительности рекомендации B (уровень достоверности доказательств – 2)
- Рекомендуется пациентам при положительном ответе на в/в #циклоспорин** через 7 дней перейти на пероральный прием препарата в дозе 2 мг/кг веса с дополнительным назначением АЗА** 2 мг/кг (на фоне терапевтической дозы ГКС) с постепенной отменой ГКС в течение 12 недель до момента достижения терапевтической концентрации и начала действия АЗА** для увеличения продолжительности ремиссии у пациента. При достижении ремиссии можно отменять пероральный #циклоспорин**, оставив пациента на поддерживающей терапии АЗА** не менее 2 лет [72,89,115,116, 256, 260].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 5)
Комментарий: Существенный недостаток такой схемы лечения обусловлен одновременным применением сразу трех иммуносупрессивных препаратов с повышением риска нежелательных явлений.
3.1.7 Сверхтяжелый язвенный колит любой протяженности
В такой форме может протекать как первая атака ЯК, так любое из последующих обострений (характеристику см. в разделе «классификация ЯК»). Пациент должен быть госпитализирован в многопрофильный (специализированный) стационар для консервативного лечения с последующим обязательным наблюдением врачом-гастроэнтерологом и врачом-колопроктологом (врачом-хирургом) для решения вопроса о целесообразности выполнения хирургического вмешательства в течение 24 часов.
- Рекомендуется пациентам при сверхтяжелой атаке ЯК назначение в/в ГКС в дозе, эквивалентной преднизолону** 2 мг/кг массы тела для достижения терапевтического эффекта [117].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 4)
Комментарий: эффективность консервативной терапии при сверхтяжелой атаке ЯК не превышает 50%. При этом производят оценку клинической картины и лабораторных параметров каждые 24 часа, а при необходимости – чаще. При ухудшении клинической картины и лабораторных показателей единственным путем спасения жизни пациента при сверхтяжелой атаке ЯК является колэктомия. При существенной положительной динамике со стороны клинической картины и лабораторных показателей с достаточной степенью осторожности можно продолжить в/в терапию ГКС до 14 дней. Если в течение 3 дней положительная динамика отсутствует, то это состояние расценивается как стероидорезистентность.
- В случае стероидорезистентности если нет непосредственной угрозы жизни пациента или развития тяжелых осложнений, требующих немедленного оперативного вмешательства, данной группе пациентов рекомендуется назначение терапии «второй линии» (в англоязычной литературе «терапии спасения»), которая включает следующие варианты лечения:
инфликсимаб** 5 мг/кг (введения в рамках индукционного курса на 0, 2 и 6 неделе) [118,119]
Уровень убедительности рекомендации А (уровень достоверности доказательств – 2)
или
#циклоспорин** (лучше в/в) 2-4 мг/кг в течение 7 дней с мониторированием показателей функции почек [120,121]
Уровень убедительности рекомендации А (уровень достоверности доказательств – 2)
или
Тофацитиниб** 20 мг/сут в рамках индукционного курса в течение 8 недель [103,206,207,208].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 4)
Комментарий: другие биологические препараты в качестве «терапии спасения» не используются. Данной группе пациентов при отрицательной динамике или при отсутствии ответа на 7 день терапии инфликсимабом**, #циклоспорином** или тофацитинибом** показано хирургическое лечение [122].
- Рекомендуется пациентам при достижении ремиссии на инфликсимабе** продолжить поддерживающую противорецидивную терапию этим же препаратом по стандартной схеме в комбинации с АЗА** 2-2,5 мг/кг (или #МП 1,5 мг/кг) или без него [98,102,114].
Уровень убедительности рекомендации B (уровень достоверности доказательств – 4)
- Рекомендуется пациентам при достижении ремиссии на тофацитинибе** продолжить поддерживающую терапию этим же препаратом 10 мг/сут [103].
Уровень убедительности рекомендации C (уровень достоверности доказательств – 4)
- Рекомендуется пациентам при положительном ответе на в/в #циклоспорин** через 7 дней перейти на пероральный прием препарата в дозе 2 мг/кг веса с дополнительным назначением АЗА** 2 мг/кг (на фоне терапевтической дозы стероидов) с постепенной отменой стероидов в течение 12 недель до момента достижения терапевтической концентрации и начала действия АЗА** для увеличения продолжительности ремиссии у пациента. При достижении ремиссии можно отменять пероральный циклоспорин**, оставив пациента на поддерживающей терапии АЗА** не менее 2 лет [72, 89,115,116, 256],260.
Уровень убедительности рекомендации С (уровень достоверности доказательств – 5)
3.1.8 Биосимиляры (Биоаналоги)
Биосимиляры – это биологические лекарственные средства, содержащие версию активного вещества, уже разрешенного оригинального биологического лекарственного средства (эталонного препарата) [213]. В настоящее время рынок биосимиляров постоянно расширяется. Применительно к ВЗК это пока касается биоаналогов на основе моноклональных антител к ФНО-альфа. Только в Европе в последнюю декаду были зарегистрированы 21 биосимиляр, из них 14 на основе адалимумаба и 4 на основе инфликсимаба** [214]. В РФ также зарегистрированы биосимиляры инфликсимаба** и адалимумаба**, недавно появились аналоги тофацитиниба**. Применение биосимиляров снижает экономическую нагрузку на систему здравоохранения и, тем самым, значительно расширяет возможности использования и доступность ГИБП. Сейчас существует достаточная доказательная база по эффективности и безопасности биосимиляров, однако среди клиницистов остается предубеждение против них, как препаратов с более низкой эффективностью [215]. Европейская организация по изучению ВЗК (ЕССО) в 2017 г декларировала позицию по использованию биоаналогов при ВЗК, в которой подчеркивается, что после регистрации биоаналог считается таким же эффективным препаратом, как и оригинальный продукт, а для оценки его долговременной эффективности и безопасности требуются большие наблюдательные исследования [216]. Именно с этих позиций систематический обзор 90 исследований при разных иммуно-воспалительных заболеваниях 2018 года показал, что в подавляющем большинстве исследований не наблюдалось различий в безопасности, эффективности или иммуногенности между биоаналогами и соответствующими оригинальными препаратами, что свидетельствует о сохранении хорошего профиля польза–риск при переходе с оригинального препарата на биоаналог [217]. Реальная клиническая практика европейских стран и США демонстрирует сходную эффективность, безопасность и иммуногенность при переключении пациентов ВЗК с оригинального инфликсимаба** на его биоаналоги [218-222]. Лишь в одном исследовании в 9,9% случаев фиксировали необходимость обратного переключения с биосимиляра на эталонный препарат вследствие нежелательных проявлений со стороны кожи, желудочно-кишечного тракта или из-за потери ответа на препарат. У подавляющего большинства больных ответ на лечение после обратного переключения восстановился [220]. Сравнение адалимумаба и двух его аналогов у больных ВЗК в Италии не показало значимой разницы в эффективности, безопасности и иммуногенности между препаратами после индукционного курса и после 6 мес поддерживающего лечения [223]. Результаты долгосрочного постмаркетингового наблюдения за эффективностью и безопасностью биосимиляров на основе моноклональных антител в течение 7 лет не выявили каких-либо побочных эффектов, специфичных для биосимиляров [224]. ЕССО консенсус подчеркивает, что принятие решения о переходе с оригинального препарата на биоаналог по не медицинским показаниям должно проводиться в соответствии с национальными клиническими рекомендациями и вся информация должна быть доведена до сведения пациента и объяснена ему [216].
Несмотря на достаточно четко сформулированные утверждения относительно биосимиляров, существуют и определенные противоречия в этом вопросе, согласно которым принятые положения основаны на исследованиях с разными методологическими подходами и недостаточным числом наблюдений, что ограничивает их достоверность [227].
Российские публикации свидетельствуют, что частота вторичной потери ответа и нежелательных явлений у пациентов c ВЗК при переводе с оригинального инфликсимаба на его биосимиляр составляет около 30%, что достоверно выше, чем у тех, кто постоянно получает оригинальный препарат. Кроме того, частота нежелательных явлений достоверно выше у больных, получающих препарат по МНН, что ведет к неоправданному и нерегулируемому чередованию оригинального препарата и биоаналогов по сравнению с больными, получающими препараты по торговому наименованию [227, 228].
В Российские клинические рекомендации по ЯК положение о биосимилярах вносится впервые. Поскольку российские биосимиляры не представлены на зарубежном рынке, то международные данные об успешном опыте переключения будут иметь для России ограниченную применимость. Поэтому следует с осторожностью экстраполировать эти данные на отечественную клиническую практику.
- Рекомендуется при показаниях к назначению ГИБП класса ингибиторов фактора некроза опухоли альфа (ФНО-альфа) (инфликсимаба** и адалимумаба**) использовать как оригинальный препарат, так и его биоаналоги, как равноценные лекарственные средства [215,216].
Комментарий: это положение касается в равной мере как первичного назначения фактора некроза опухоли альфа (ФНО-альфа) препаратов у бионаивных пациентов, так и переключения с оригинального препарата на биоаналог по немедицинским показаниям. Однако следует иметь в виду, что неконтролируемое переключение с оригинала на биосимиляр или разные биосимиляры и обратно по МНН может привести к ухудшению течения заболевания, быстрой потере ответа и нежелательным явлениям [228].
Переход с одного фактора некроза опухоли альфа (ФНО-альфа) препарата на другой в рамках одного класса при потере ответа на первый препарат не рекомендуется ни для оригинальных препаратов, ни для биосимиляров (см. раздел 3.1.5). Достаточной доказательной базы для использования биоаналогов лекарственных препаратов других классов для лечения ЯК пока нет.
3.2 Хирургическое лечение
3.2.1 Показания к хирургическому лечению ЯК: неэффективность или невозможность продолжения консервативной терапии.
Показаниями к хирургическому лечению ЯК служат неэффективность консервативной терапии (стероидорезистентность, неэффективность ГИБП) или невозможность их продолжения (стероидозависимость, непереносимость или противопоказания для проведения консервативной терапии), кишечные осложнения ЯК (токсическая дилатация, перфорация кишки, кишечное кровотечение), а также рак толстой кишки или высокий риск его возникновения.
О неэффективности консервативной терапии свидетельствуют (см. раздел 1.5):
· стероидная резистентность;
· стероидная зависимость.
Стероидозависимость удается эффективно преодолеть при помощи ГИБП и/или иммуносупрессоров (АЗА**, #МП**) в 40-55% случаев [78,116], а при стероидорезистентности назначение #циклоспорина** или инфликсимаба** позволяет индуцировать ремиссию в 43-80% случаев [118,119,120]. Однако, у части пациентов с высоким риском осложнений и неэффективностью консервативной терапии при развитии стероидорезистентности или зависимости возможно проведение хирургического лечения без попытки применения ГИБП или противоопухолевых препаратов (иммуносупрессоров) (Азатиоприн** код АТХ L04AX01, Меркаптопурин** код АТХ L01BB02)
3.2.2 Показания к хирургическому лечению ЯК: кишечные осложнения ЯК
- Пациентам с осложнениями ЯК (кишечное кровотечение, перфорация толстой кишки, токсическая дилатация на фоне адекватной инфузионной терапии) рекомендуется экстренная операция в объеме субтотальной колэктомии или тотальной колэктомии или колпроктэктомии (при выраженной активности в прямой кишке) для увеличения продолжительности жизни пациента [123,124,125].
Уровень убедительности рекомендации C (уровень достоверности доказательств – 5)
Комментарий: токсическая дилатация ободочной кишки (токсический мегаколон), представляет собой не связанное с обструкцией расширение ободочной кишки 6 см и более с явлениями интоксикации. К факторам риска токсической дилатации относятся гипокалиемия, гипомагниемия, подготовка кишки к колоноскопии при помощи осмотических слабительных и прием антидиарейных препаратов. Косвенно о развитии токсической дилатации свидетельствует внезапное сокращение частоты стула на фоне имевшейся диареи, вздутие живота, а также внезапное уменьшение или исчезновение болевого синдрома и нарастание симптомов интоксикации (нарастание тахикардии, снижение АД). Перфорация толстой кишки является наиболее опасным осложнением ЯК с почти 50% летальностью.
3.2.3 Показания к хирургическому лечению ЯК: колоректальный рак
У пациентов с длительным анамнезом ЯК существенно повышен риск колоректального рака, что обуславливает необходимость регулярного обследования для выявления дисплазии в эпителии слизистой оболочки толстой кишки. На вероятность развития рака влияют следующие факторы:
а) длительность анамнеза ЯК: риск колоректального рака составляет 2% при 10-летнем, 8% - при 20-летнем и 18% - при 30-летнем анамнезе [126];
б) начало заболевания в детском и подростковом возрасте, хотя этот фактор может лишь отражать длительность анамнеза и не являться независимым предиктором колоректального рака [127];
в) протяженность поражения: риск наиболее повышен у пациентов с тотальным ЯК, в то время как у пациентов с проктитом риск не отличается от среднего в популяции;
г) наличие первичного склерозирующего холангита [128];
д) семейный анамнез колоректального рака;
е) тяжелые обострения ЯК в анамнезе или непрерывное течение ЯК. Последствием высокой активности ЯК может стать воспалительный полипоз, также являющийся фактором риска развития колоректального рака [129].
Контрольная колоноскопия должна проводиться в условиях хорошей подготовки кишки и, желательно, в период ремиссии, поскольку активное воспаление затрудняет выявление дисплазии.
Для скрининга неопластических изменений слизистой оболочки используются уточняющие эндоскопические методики: видеоколоноскопия с хромоскопией в сочетании с красителем или виртуальная (оптическая) хромоскопия с выполнением прицельной биопсии [130,131,132]. При использовании уточняющих эндоскопических методик выполнение поисковой биопсии не требуется.
Результаты скрининговой биопсии влияют на тактику дальнейшего лечения и наблюдения.
- Рекомендуется пациентам с ЯК при обнаружении дисплазии высокой степени в биопсийном материале из макроскопически неизмененной слизистой оболочки хирургическое лечение в объеме тотальной колэктомии [126].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 4)
Комментарий: возможно выполнение колпроктэктомии с формированием постоянной концевой илеостомы или колпроктэктомии с одномоментным формированием тонкокишечного резервуара под прикрытием петлевой илеостомы. Наличие дисплазии в эпителии слизистой оболочки толстой кишки должно быть подтверждено вторым независимым патоморфологом. Объем хирургического лечения обсуждается совместно с пациентом, тем самым учитывается его желание в отношении сохранения анальной дефекации или формирования постоянной илеостомы.
- Рекомендуется при обнаружении дисплазии легкой степени в эпителии макроскопически неизмененной слизистой оболочки, индивидуально обсуждать совместно с пациентом два варианта хирургического лечения – тотальная колэктомия (колпроктэктомия) с формированием постоянной концевой илеостомы и колпроктэктомия с одномоментным формированием тонкокишечного резервуара под прикрытием петлевой илеостомы для улучшения качества жизни пациента или продолжение регулярного эндоскопического скрининга с сокращением интервала между исследованиями в периоде от 6 до 12 месяцев [126,249].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 4)
Комментарий: объем хирургического лечения обсуждается совместно с пациентом, тем самым учитывается его желание в отношении сохранения анальной дефекации или формирования постоянной илеостомы. Пациент вправе воздержаться от оперативного лечения, в таком случае предлагается эндоскопический скрининг.
- Рекомендуется пациентам с ремиссией ЯК, при подтверждении наличия аденоматозного полипа (эндоскопически и по результатам патоморфологического исследования), выполнение стандартной полипэктомии для вторичной профилактики рака [128].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 4)
Комментарий: пациентам с ремиссией ЯК при наличии крупных неопластических образований толстой кишки и отсутствием дисплазии в эпителии слизистой оболочки вне указанных образований возможно выполнение мукозэктомии или диссекции в подслизистом слое [133,134].
- Не рекомендуется колэктомия пациентам с ЯК при наличии аденоматозного полипа с дисплазией тяжелой степени, если в других отделах толстой кишки дисплазия в эпителии слизистой оболочки отсутствует или соответствует легкой степени [128].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 4)
- Рекомендуется пациентам с ЯК при наличии участка сужения в толстой кишке проводить эндоскопическое исследование с биопсией из зоны сужения для исключения колоректального рака [129].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 5)
Комментарий: дисплазия в эпителии слизистой оболочки должна быть подтверждена вторым врачом-патологоанатомом, а затем программа лечения должна обсуждаться врачебным мультидисциплинарным консилиумом. Если колоноскопия не тотальная из-за наличия сужения, необходима КТ с внутривенным и внутрипросветным контрастированием для оценки характера изменений стенки толстой кишки проксимальнее сужения [135]. Всем пациентам с колоректальным раком на фоне язвенного колита, после проведения онкологического консилиума, показано хирургическое лечение в объеме тотальной колэктомии с брюшно-анальной резекцией прямой кишки для исключения риска злокачественной трансформации в оставшихся отделах толстой кишки.
3.2.4 Виды хирургических вмешательств
У большинства пациентов ЯК современная консервативная терапия позволяет контролировать течение воспалительного процесса, однако у 10-30% пациентов в связи с неэффективностью медикаментозного лечения приходится прибегать к хирургическому вмешательству, направленному на удаление толстой кишки [123,124]. До начала 1980-х годов стандартом хирургического лечения являлась колпроктэктомия с концевой илеостомой, несмотря на эпизодическое формирование илеоректального анастомоза. За последние 20 лет новым золотым стандартом стала восстановительно-пластическая операция – тотальная колэктомия с формированием резервуара (колпроктэктомия с илеоанальным резервуарным анастомозом (ИАРА)) [136,137] (Табл.7). При отсутствии осложнений данная операция обеспечивает возможность контролируемой дефекации через задний проход с удовлетворительным качеством жизни [136]: частота дефекации после формирования ИАРА составляет 4 - 8 раз в сутки [138-140], а средний суточный объем полуоформленного/жидкого стула - около 700 мл в сутки (в сравнении с 200 мл/сутки у здорового человека).
Таблица 7. Методы хирургического лечения ЯК
|
С формированием постоянной илеостомы |
С восстановлением дефекации через задний проход | ||
|
Колэктомия с брюшно-анальной резекцией прямой кишки и формированием постоянной концевой илеостомы |
С формированием ИАРА, в 2 этапа: |
С формированием ИАРА, в 3 этапа: |
Субтотальная резекция ободочной кишки с формированием илеоректального анастомоза (в исключительных случаях) |
|
1. Колэктомия с резекцией прямой кишки, формирование ИАРА, петлевая илеостомия; 2. Закрытие петлевой илеостомы |
1. Субтотальная резекция ободочной кишки (субтотальная колэктомия), концевая илеостомия; 2. Проктэктомия, формирование ИАРА, петлевая илеостомия; 3. Закрытие петлевой илеостомы | ||
Всем пациентам, которым предстоит хирургическое вмешательство (тотальная или субтотальная колэктомия или колэктомия с брюшно-анальной резекцией прямой кишки) по поводу неэффективности консервативной терапии язвенного колита, за исключением кишечных осложнений, предпочтительней применять лапароскопические технологии для уменьшения частоты интраоперационных и послеоперационных осложнений, более быстрого восстановления, уменьшения риска развития спаечного процесса в брюшной полости, уменьшения риска снижения фертильности и улучшения косметического результата [141-146].
3.2.5 Выбор вида хирургического лечения
Проведение реконструктивно-пластической операции с формированием ИАРА, несмотря на очевидную привлекательность для пациента, возможно не во всех случаях, поскольку ряд факторов ухудшают функциональный исход операции и увеличивают риск осложнений, приводя к необходимости удаления резервуара у 3,5-10% пациентов [147-149].
У пациентов старших возрастных групп с ЯК, несмотря на более высокую частоту сопутствующих заболеваний, само хирургическое вмешательство с формированием тонкокишечного резервуара безопасно [150]. Функция анального держания, играющая ключевую роль для нормального функционирования ИАРА, как правило, ухудшается у лиц старших возрастных групп [151].
Кроме того, у пациентов старше 60 лет чаще развиваются осложнения, в частности резервуарит и стриктура анастомоза [152,153]. В то же время, какой-либо конкретный возрастной порог для отказа от формирования ИАРА не определен.
Формирование тонкокишечного резервуара (ИАРА) на 30-70% [154-158] повышает риск бесплодия у женщин детородного возраста с ЯК.
Риск бесплодия связан со спаечным процессом, вовлекающим маточные трубы. Планируемая беременность и молодой возраст женщины не являются противопоказаниями к формированию ИАРА, однако, пациентка должна быть предупреждена о потенциальном риске бесплодия. В отдельных случаях возможно рассмотреть вопрос о формировании илеоректального анастомоза в качестве промежуточного этапа хирургического лечения (см.ниже).
У всех пациенток с ЯК, при возникновении показаний к операции, использование лапароскопических технологий снижает риск развития бесплодия на 90% [158].
Приблизительно у 10% пациентов даже при патоморфологическом изучении операционного препарата после колэктомии, не удается провести дифференциальный диагноз между БК и ЯК, в связи с чем им устанавляется диагноз колит неуточненный. Решение о формировании ИАРА в таких случаях принимается индивидуально, при этом пациент должен быть предупрежден о рисках неэффективности реконструктивно-пластической операции и иных осложнениях, связанных с БК.
Пациентам с ЯК при наличии таких сопутствующих заболеваний, как рак прямой кишки и выраженное анальное недержание 2 или 3 степени формирование тонкокишечного резервуара (ИАРА) нецелесообразно.
- Рекомендуется пациентам с тяжелой атакой ЯК, не ответивших на консервативное лечение, а также пациентам с ЯК, у которых к моменту установления показаний к операции, в течение более 6 недель была проведена гормональная терапия преднизолоном** в дозе не менее 20 мг в сутки в течение более чем 6 недель выполнять трехэтапное хирургическое лечение (колэктомия с формированием илеостомы на первом этапе, формирование тонкокишечного резервуара и петлевой илеостомы – на втором этапе, и закрытие петлевой илеостомы – на третьем этапе) для снижения риска послеоперационных осложнений [159-161].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 4)
Комментарий: у всех пациентов с тяжелой или сверхтяжелой атакой язвенного колита, при возникновении показаний к операции, хирургическое вмешательство должно быть в объеме не менее колэктомии с формированием концевой илеостомы, что позволяет улучшить общее состояние пациента, устранить метаболические нарушения, а патоморфологическое исследование операционного препарата исключает БК. Колэктомия является относительно безопасным вмешательством даже у пациентов в критическом состоянии [159-161]. При достаточной квалификации хирурга безопасным является использование лапароскопических технологий [162,163].
Формирование илеоректального анастомоза не приводит к излечению пациента и не исключает возможность рецидива воспаления в прямой кишке и развития рака [164-166]. Данная операция при ЯК может выполняться только в исключительных случаях у женщин, планирующих беременность. Обязательным условием является наличие ремиссии в прямой кишке и согласие пациентки на регулярное обследование прямой кишки с биопсией слизистой оболочки [165,167].
3.2.6 Особенности хирургического вмешательства при формировании тонкокишечного резервуара
Пациентам с ЯК, подвергшимся колэктомии, реконструктивно-пластические операции с формированием тонкокишечного резервуара (ИАРА) выполняются в специализированных стационарах, поскольку частота осложнений и функциональный исход таких вмешательств существенно зависит от личного опыта хирурга [165].
Длина сохраняемой прямой и/или сигмовидной кишки
Пациентам с ЯК при выполнении колэктомии по срочным показаниям, которым в дальнейшем планируется формирование тонкокишечного резервуара, целесообразно сохранить всю прямую кишку и нижние брыжеечные сосуды для улучшения качества жизни. Прямую кишку целесообразно пересекать на уровне мыса крестца или дополнительно сохранять дистальный отдел сигмовидной кишки (решение принимается оперирующим хирургом). При сохранении дистального отдела сигмовидной кишки она выводится на переднюю брюшную стенку в виде концевой сигмостомы. Последний вариант является наиболее безопасным, поскольку при этом в брюшной полости не остается культя кишки. При пересечении прямой кишки на уровне мыса в течение нескольких дней предпочтительней дренирование культи через задний проход для профилактики несостоятельности швов в связи с накоплением слизи. В случае сохранения отключённой прямой или прямой и сигмовидной кишки, возможно развитие вторичных воспалительных изменений слизистой оболочки по типу колита отключенной кишки. Контролируемые испытания лекарственных средств у пациентов после колэктомии не проводились. Эмпирическое лечение заключается в местном применении месалазина [168], стероидов, промывании отключенной прямой кишки растворами антисептиков.
Наложение анастомоза при формировании ИАРА
Пациентам с ЯК, которым планируется хирургическое лечение с формированием тонкокишечного резервуара, с целью улучшения функциональных результатов, целесообразно сохранять дистальный участок прямой кишки длиной не более 2 см выше зубчатой линии. Сохранение протяженного участка прямой кишки (более 2 см выше зубчатой линии) может быть причиной хронического воспаления в ней с дисфункцией резервуара, а также способствует сохранению риска дисплазии и (очень редко) рака [164]. При невозможности сформировать резервуарно-ректальный анастомоз при помощи сшивающего аппарата следует выполнить брюшно-анальную резекцию прямой кишки и наложить ручной илеоанальный анастомоз.
Морфологические изменения эпителиальной выстилки резервуара обычно развиваются через 12-18 месяцев после закрытия илеостомы и характеризуются уплощением и сокращением числа ворсинок и нередко сопровождается развитием толстокишечной метаплазии [169,170], что потенциально связано с риском развития злокачественной трансформации слизистой оболочки резервуара. Кроме того, при наложении аппаратного ИАРА сохраняется небольшой участок слизистой оболочки прямой кишки («манжетка»). Риск развития рака резервуара повышен у пациентов, оперированных по поводу рака или дисплазии на фоне ЯК (и при обнаружении дисплазии в операционном материале), а также у пациентов с первичным склерозирующим холангитом (ПСХ). Научное обоснование частоты контрольных обследований пациентов с ИАРА не выполнялось, однако, у пациентов с наличием вышеуказанных факторов риска целесообразно проведение контрольных эндоскопических исследований (резервуароскопии) с биопсией слизистой оболочки не реже одного раза в 2 года.
3.2.7 Медикаментозная терапия в период хирургического лечения
Влияние лекарственной терапии на риск хирургических вмешательств.
- Рекомендуется с осторожностью проводить медикаментозную терапию (гормональную, иммунодепрессивную, ГИБТ) в период хирургического лечения для снижения риска послеоперационных осложнений [171-176].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 4)
Комментарий: прием преднизолона** в дозе более 20 мг в течение более чем 6 недель увеличивает частоту послеоперационных осложнений [171,172]. Предоперационный прием АЗА** и #МП** не ухудшает исход хирургического лечения [173], в то время как введение инфликсимаба** и циклоспорина** незадолго до операции может увеличивать частоту послеоперационных осложнений [174,175], хотя данные по инфликсимабу** остаются противоречивыми [176]. Резкое прекращение терапии ГКС может вызвать синдром отмены (острую надпочечниковую недостаточность, так называемый Аддисонический криз), что обусловливает необходимость временного продолжения гормональной терапии после операции до полной отмены. На настоящий момент отсутствует надежная научная база для обоснования какой-либо схемы прекращения гормональной терапии после колэктомии по поводу ЯК. Доза ГКС для дальнейшего перорального приема в период отмены гормональной терапии определяется длительностью предшествовавшей терапии и величиной использованных доз. Согласно рекомендациям Европейского общества по изучению ЯК и БК (ECCO) [26], в случае, если гормональная терапия перед операцией проводилась не более месяца, сразу после операции возможно прекращение приема ГКС.
Если перед операцией пациент более месяца получал ГКС, после хирургического вмешательства целесообразно перейти с вышеописанной высокой парентеральной дозы на пероральный прием ГКС в дозе не ниже верхней границы суточной стрессовой продукции кортизола, то есть не ниже 20 мг преднизолона**.
3.2.8 Резервуарит и другие осложнения хирургического лечения при формировании тонкокишечного резервуара
Резервуарит представляет собой неспецифическое воспаление тонкокишечного резервуара и наиболее частое осложнение ИАРА. Частота его возникновения колеблется в широком диапазоне от 15 до 50% в течение 10 лет после формирования ИАРА в крупных специализированных центрах [177-179]. Такие различия могут быть обусловлены существенно большим риском резервуарита при ЯК, превышающим частоту этого осложнения при формировании ИАРА по поводу других заболеваний (в частности, семейного аденоматозного полипоза) [180,181].
У пациентов с признаками и симптомами, характерными для резервуарита, следует выполнить интестиноскопию (резервуароскопию) для оценки степени воспалительных изменений слизистой оболочки резервуара с исследованием биопсийного материала.
Резервуарит сопровождается образованием абсцессов, свищей, стеноза резервуаро-анального анастомоза и риском развития рака в резервуаре. Последнее осложнение встречается исключительно редко и почти всегда – при выявленной дисплазии тяжелой степени или раке в операционном препарате после колэктомии.
Дифференциальный диагноз при подозрении на резервуарит проводится с синдромом раздраженного резервуара (СРР), ишемическими поражениями, БК и другими редкими причинами дисфункции резервуара, такими как коллагенозный, цитомегаловирусный и Clostridioides difficile – ассоциированный резервуарит. Следует учитывать возможность развития неспецифического илеита, вызываемого приемом НПВС, и синдрома избыточного бактериального роста.
Основными препаратами, применяемыми для лечения резервуарита остаются антибиотики, что позволяет классифицировать резервуарит как антибиотикочувствительный, антибиотикозависимый и антибиотикорезистентный.
- Рекомендуется пациентам с резервуаритом первая линия терапии, включающая 14-дневный курс перорального метронидазола** (15-20 мг/кг/сутки) или #ципрофлоксацина** (1000 мг/сут) для достижения терапевтического эффекта [182].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 3)
Комментарий: нежелательные явления значительно чаще отмечаются при приеме метронидазола**. В случаях антибиотикорезистентного резервуарита возможно назначение перорального #будесонида** (9 мг) в течение 8 недель [250].
- Рекомендуется пациентам с резервуаритом при отсутствии эффекта или при развитии зависимости от приема указанных препаратов назначение резервных препаратов – #рифаксимина (2000 мг/сут) и #тинидазола (1000–1500 мг/сут), в том числе в комбинации с #ципрофлоксацином** (1000 мг/сут), ректальных ГКС, ректальных препаратов месалазина**, азатиоприна** для достижения терапевтического эффекта [182].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 5)
- Рекомендуется пациентам с хроническим резистентным к терапии резервуаритом при неэффективности первой линии терапии и резервных лекарственных средств назначение для индукции и поддержания ремиссии ингибиторов фактора некроза опухоли альфа (ФНО – альфа) [183], ведолизумаба** [184] индукционный (инициирующий) курс предусматривает трехкратное введение на 0, 2 и 6 неделе внутривенно в дозе 300 мг, затем поддерживающее лечение по 300 мг внутривенно каждые 8 недель или устекинумаба** [185] индукционная (инициирующая) доза вводится внутривенно в первый день с расчетом дозы по массе тела пациента на момент введения, далее через 8 недель первое поддерживающее подкожное введение в дозе 90 мг и далее терапия в дозе 90 мг подкожно каждые 12 или 8 недель (при потере ответа) [251,252].
Уровень убедительности рекомендации А (уровень достоверности доказательств – 2)
Воспаление слизистой оболочки сохраненного участка прямой кишки.
Другим потенциальным осложнением ИАРА является воспаление слизистой оболочки прямой кишки, сохраняемой при наложении аппаратного анастомоза.
- Рекомендуется пациентам с проктитом после формирования тонкокишечного резервуара, лечение проводить свечами #месалазина** 500 мг 2 раза в сутки и/или ректальными ГКС для достижения терапевтического эффекта [68,266].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 4)
3.2.9 Дисфункция илеостомы после хирургического лечения ЯК
Под дисфункцией илеостомы понимается увеличение объема кишечного отделяемого по илеостоме более 1000 мл в сутки. Данное состояние также сопровождается быстро прогрессирующими метаболическими и водно-электролитными нарушениями [186,187].
- Рекомендуется пациентам с дисфункцией илеостомы для лабораторной диагностики Clostridioides difficile – ассоциированной диареи использовать алгоритм, включающий молекулярно-биологическое исследование фекалий на возбудителя диффициального клостридиоза или иммунохроматографическое экспресс-исследование кала на токсины на токсины А и В клостридии (Clostridium difficile) и бинарный токсин Cl. difficile [186,188].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 5)
Комментарий: помимо обильного жидкого отделяемого по стоме, в клинической картине также отмечается повышение температуры тела до 390С, метеоризм, редко жалобы на тошноту, рвоту, боли в животе спастического характера. При лабораторных исследованиях: анемия, гипопротеинемия, гипоальбуминемия, гипокалиемия, повышение уровня СРБ, редко увеличение концентрации креатинина.
- Рекомендуется пациентам с лёгкой дисфункцией илеостомы диетотерапия, спазмолитики (код АТХ A03D Спазмолитики в комбинации с анальгетиками) и препараты, замедляющие пассаж по ЖКТ (код АТХ A07 Противодиарейные, кишечные противовоспалительные / противомикробные препараты) для достижения терапевтического эффекта и улучшения качества жизни пациента [186-188].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 5)
Комментарий: лёгкая форма заболевания характеризуется увеличением объема кишечного отделяемого по илеостоме, без признаков системного воспаления.
- Рекомендуется пациентам со среднетяжёлой формой дисфункции илеостомы, при подтверждении диагноза клостридиальной инфекции, метронидазол** в дозе 500 мг внутрь три раза в день в течение 7 дней. При отсутствии клинического эффекта от метронидазола** через 5-7 дней производят смену препарата на #ванкомицин** в дозе 2000 мг в день per os в течение 10 дней для достижения терапевтического эффекта и улучшения качества жизни пациента [186,187,189,190,254, 255].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 5)
Комментарий: среднетяжёлая форма характеризуется увеличением объема кишечного отделяемого по илеостоме, повышением температуры тела и изменениями лабораторных показателей: при увеличении уровня лейкоцитов в крови более 15×109/л, креатинина в сыворотке крови выше 115 мкмоль/л, подъёме температуры тела выше 380C и снижении уровня альбумина менее 25 г/л, пациенты должны получать лечение в условиях круглосуточного стационара. В случае подтверждения клостридиальной инфекции показано назначение #ванкомицина** в дозе 1000 мг внутрь в день в течение 10 дней.
- Рекомендуется пациентам с тяжелой формой дисфункции илеостомы при подтверждении диагноза клостридиальной инфекции наряду с инфузионной терапией назначение #ванкомицина** внутрь в дозе 500 мг 4 раза в день в сочетании с метронидазолом** в дозе 500 мг 3 раза в день внутривенно [187,191, 253].
Уровень убедительности рекомендации C (уровень достоверности доказательств – 5)
Комментарий: тяжёлая форма дисфункции илеостомы, помимо увеличения объема кишечного отделяемого по илеостоме, проявляется болями в животе спастического характера, развитием лихорадки вплоть до гектических значений, лейкоцитозом, гипоальбуминемией. При невозможности введения препарата через рот #ванкомицин** назначается внутрикишечно - при этом препарат в дозе 500 мг разводится в 500 мл 0,9% раствора хлорида натрия и вводится в просвет кишки четыре раза в день. Ухудшение состояния пациента с возникновением гипотонии, гипертермия выше 38,5 °C, задержка стула, выраженное вздутие живота, изменение сознания, лейкоцитоз свыше 15 × 10⁹ или лейкопения ниже 2 × 109, повышение уровня лактата в сыворотке крови выше 2,2 ммоль/л, развитие синдрома полиорганной недостаточности требует его перевода в отделение интенсивной терапии для дальнейшего лечения.
4. Медицинская реабилитация и санаторно-курортное лечение, медицинские показания и противопоказания к применению методов медицинской реабилитации, в том числе основанных на использовании природных лечебных факторов
Специфические меры реабилитации пациентов с ЯК отсутствуют.
Поскольку в ряде случаев терапия ЯК сопряжена с применением иммунодепрессантов, основным способом реабилитации пациентов является профилактика оппортунистических инфекций, описанная в разделе 5.
У пациентов, которым потребовалось хирургическое лечение язвенного колита, возможна реабилитация в три этапа.
1-й этап – ранняя реабилитация, осуществляется непосредственно после хирургического лечения со 2-х по 14-е сутки. Основной задачей 1 этапа реабилитации является восстановление нормального функционирования желудочно-кишечного тракта после хирургического вмешательства. Именно на этом этапе чаще всего выявляются и должны быть корригированы нарушения мочеиспускания. Важная роль отводится также контролю гомеостаза, мероприятиям, направленным на заживление послеоперационных ран, купированию послеоперационного болевого синдрома, активизации пациента. В данный период проводится контроль лабораторных показателей путем назначения общего анализа крови, биохимического анализа крови, коагулограммы крови, общего анализа мочи.
2-й этап реабилитации начинается после 15 суток и направлен на окончательное заживление послеоперационных ран с контролем за деятельностью желудочно-кишечного тракта и других систем организма. Данный этап возможно осуществлять как амбулаторно, так и в условиях стационара дневного или круглосуточного пребывания.
3-й этап реабилитации осуществляется в поздний послеоперационный период у пациентов как с постоянной илеостомой, так и перед реконструктивно-восстановительной операцией. Основной задачей на данном этапе является нормализация функции желудочно-кишечного тракта, проведение мероприятий, направленных на выявление и коррекцию нарушений функции запирательного аппарата прямой кишки.
Недостаточность анального сфинктера
Реабилитация возможна на 2 и 3 этапах. У ряда пациентов, у которых оперативное вмешательство по поводу ЯК завершилось формированием тонкокишечного резервуара, отмечается снижение функции держания.
Пациентам ЯК с недостаточностью анального сфинктера перед реконструктивно-восстановительным лечением целесообразно исследование функции запирательного аппарата прямой кишки (сфинктерометрия, профилометрия, исследование проводимости по срамному нерву) с последующей консультаций врача физиотерапевта для проведения лечения, направленного на улучшение функции держания [192].
- Пациентам ЯК при выявлении недостаточности анального сфинктера 2-3 степени, рекомендуется рассмотреть возможность проведения в условиях дневного или круглосуточного стационара 10-дневного цикла электростимуляции, БОС-терапии и тибиальной нейромодуляции, направленной на улучшение сократительной способности мышц наружного сфинктера и тазового дна за счет увеличения как силы, так и длительности произвольного сжатия [192,193].
Уровень убедительности рекомендации C (уровень достоверности доказательств – 4)
Комментарий: БОС-терапия является неинвазивным методом вовлекающим в процесс реабилитации собственные ресурсы организма с выработкой правильных навыков на уровне создания новых условно-рефлекторных связей. Так же эффективным является метод тибиальной нейромодуляции. Нейромодуляция — это процесс, при котором электрический ток по одним нервным путям модулирует существовавшую ранее активность в других нервных путях или центрах. Чрескожная электростимуляция заднего большеберцового нерва применяется при функциональных заболеваниях органов малого таза, так как в составе заднего большеберцового нерва проходят волокна из II и III крестцовых сегментов спинного мозга, играющие значительную роль в иннервации прямой кишки, мочевого пузыря и их сфинктеров. Доказано, что мышечные структуры отключенного запирательного аппарата могут реагировать на проводимую терапию, увеличивая как тонус, так и силу волевых сокращений [192,193]. Стимуляцию тибиального нерва проводят с помощью накожного стимулирующего электрода, что позволяет пациенту после курса предварительного обучения продолжить курс лечения самостоятельно в домашних условиях. В таком случае курс лечения с ежедневными сеансами стимуляции может продлеваться до 1-3 месяцев. Контроль эффективности терапии производится перед началом и по окончании каждого курса процедур путем комплексного физиологического исследования функции запирательного аппарата прямой кишки. При улучшении показателей тонуса и сократительной способности анальных сфинктеров, можно ставить вопрос о выполнении реконструктивно-восстановительной операции, направленной на возобновление естественного пассажа по желудочно-кишечному тракту.
5. Профилактика и диспансерное наблюдение, медицинские показания и противопоказания к применению методов профилактики
Язвенный колит характеризуется хроническим рецидивирующим течением. Диспансерное наблюдение при ЯК проводится пожизненно. Целью диспансерного наблюдения является, в первую очередь, профилактика колоректального рака.
Рекомендуется всем пациентам ЯК в стадии клинической ремиссии выполнение колоноскопии не реже, чем каждые 3 года [271,272].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 4)
У части пациентов периодичность диспансерного наблюдения с проведением колоноскопии может быть иной. К особенностям наблюдения за пациентами, получающими иммунодепрессанты и/или биологические препараты, относится профилактика оппортунистических инфекций. К факторам риска развития оппортунистических инфекций относят: прием преднизолона** 20 мг в сутки и более в течение 2 недель, прием иммуносупрессоров (код АТХ L04AX другие иммунодепрессанты. АЗА**,#МТ** , код АТХ L01BB02#МП**,) и биологических препаратов, возраст старше 50 лет, сопутствующие заболевания (хронические заболевания легких, алкоголизм, органические заболевания головного мозга, сахарный диабет).
Пациентам следует разъяснить необходимость постоянного приема лекарственных препаратов, поскольку соблюдение предписаний по терапии существенно (в 2-2,5 раза) снижает частоту обострений, а сама терапия является методом химиопрофилактики колоректального рака.
- Рекомендуется всем пациентам ЯК обязательная вакцинопрофилактика в соответствии с Европейским консенсусом по профилактике, диагностике и лечению оппортунистических инфекций. Необходимым минимумом вакцинопрофилактики является [194]:
• вакцина для профилактики вирусного гепатита B**;
• вакцина для профилактики пневмококковых инфекций**;
• вакцина для профилактики гриппа [инактивированная]**;
• для женщин до 26 лет, при отсутствии вируса на момент скрининга рекомендуется вакцинация от вируса папилломы человека.
Уровень убедительности рекомендации С (уровень достоверности доказательств – 5)
- Пациентам в период терапии ГКС рекомендуется мониторинг уровня гликемии (исследование уровня глюкозы в крови) для профилактики побочного действия глюкокортикоидов[273,274].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 5)
- Рекомендуется пациентам в период терапии иммунодепрессантами (Азатиоприн** (код АТХ L04AX01), Меркаптопурин** (код L01BB02) ежемесячный контроль уровня лейкоцитов (исследование уровня лейкоцитов в крови (общий анализ крови)) и печёночных ферментов (определение активности АЛТ, АСТ, щелочной фосфатазы и ГГТ в крови, исследование уровня общего билирубина в крови) в начале лечения раз в две недели, далее раз в месяц в течение первых 6 месяцев терапии, далее раз в три месяца для профилактики побочных эффектов от терапии [275].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 4)
- Рекомендуется пациентам перед проведением ГИБП или ТИС и далее каждые 6 месяцев прием (осмотр, консультация) врача-фтизиатра и скрининг на туберкулез (квантифероновый тест, а при невозможности, проведение внутрикожной пробы с туберкулезным аллергеном – проба Манту, аллерген туберкулезный рекомбинантный в стандартном разведении**) для диагностики туберкулеза [195].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 5)
- Пациенткам с ЯК рекомендуется ежегодный прием (осмотр, консультация) врача-акушера-гинеколога и проведение скринига рака шейки матки (мазок по Папаниколау с цитологическим исследованием микропрепарата цервикального канала) для диагностики интраэпителиальной неоплазии шейки матки [209].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 5)
- Рекомендуется пациентам до назначения иммуносупрессивной терапии, включая ГИБП или ТИС и на фоне лечения проводить скрининг для диагностики сопутствующих заболеваний в соответствии с профессиональными клиническими рекомендациями:
1) На наличие маркеров вирусных гепатитов (определение антител к вирусу гепатита C в крови; определение антител к поверхностному антигену (HBsAg) вируса гепатита B (Hepatitis В virus) в крови) [194].
2) На иммунодефицит человека (определение антител классов M, G (IgM, IgG) к вирусу иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV 1) в крови; определение антител классов M, G (IgM, IgG) к вирусу иммунодефицита человека ВИЧ-2 (Human immunodeficiency virus HIV 2) в крови) [194].
3) На сифилис (определение антител к бледной трепонеме (Treponema pallidum) в нетрепонемных тестах (RPR, РМП) (качественное и полуколичественное исследование) в сыворотке крови).
Уровень убедительности рекомендации С (уровень достоверности доказательств – 5)
- Рекомендуется всем пациентам каждые 6 месяцев выполнять исследование уровня кальпротектина в кале и/или ректороманоскопию с целью оценки эффективности проводимой терапии [197-202].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 4)
Комментарий: с точки зрения долгосрочного прогноза течения ЯК целесообразно регулярно оценивать наличие эндоскопической ремиссии (заживления слизистой оболочки).
6. Организация оказания медицинской помощи
Медицинская помощь, за исключением медицинской помощи в рамках клинической апробации, в соответствии с Федеральным законом от 21.11.2011 № 323-ФЗ (ред. от 28.12.2022) «Об основах охраны здоровья граждан в Российской Федерации», постановлением Правительства Российской Федерации от 17.11.2021 № 1968 «Об утверждении Правил поэтапного перехода медицинских организаций к оказанию медицинской помощи на основе клинических рекомендаций, разработанных и утвержденных в соответствии с частями 3, 4, 6 - 9 и 11 статьи 37 Федерального закона «Об основах охраны здоровья граждан в Российской Федерации» организуется и оказывается:
1) в соответствии с положением об организации оказания медицинской помощи по видам медицинской помощи, которое утверждается уполномоченным федеральным органом исполнительной власти;
2) в соответствии с порядками оказания помощи по профилям «гастроэнтерология», «колопроктология», обязательным для исполнения на территории Российской Федерации всеми медицинскими организациями;
3) на основе настоящих клинических рекомендаций;
4) с учетом стандартов медицинской помощи, утвержденных уполномоченным федеральным органом исполнительной власти.
Первичная специализированная медико-санитарная помощь больным ЯК оказывается врачом-гастроэнтерологом, врачом-колопроктологом и иными врачами-специалистами в медицинских организациях, имеющих лицензию на оказание соответствующих видов медицинской деятельности.
При подозрении или выявлении язвенного колита у пациента врачи-терапевты, врачи-терапевты участковые, врачи общей практики (семейные врачи), врачи-специалисты, средние медицинские работники в установленном порядке направляют пациента на консультацию в медицинскую организацию, имеющую в своем составе кабинет врача-гастроэнтеролога, врача-колопроктолога, и/или амбулаторный гастроэнтерологический центр (отделение), и/или амбулаторный колопроктологический центр (отделение), и/или центр диагностики и лечения воспалительных заболеваний кишечника (при наличии в субъекте, организуется на функциональной основе) для оказания ему первичной специализированной медико-санитарной помощи. Консультация в указанных структурных подразделениях медицинской организации должна быть проведена не позднее 14 рабочих дней с даты выдачи направления на консультацию, а в случаях тяжелой формы язвенного колита не позднее 3 рабочих дней с даты выдачи направления на консультацию.
Врач-гастроэнтеролог, врач-колопроктолог медицинской организации, имеющей в своем составе кабинет врача-гастроэнтеролога, врача-колопроктолога, амбулаторный гастроэнтерологический центр (отделение), амбулаторный колопроктологический центр (отделение), центр диагностики и лечения воспалительных заболеваний кишечника, организует своевременное квалифицированное обследование и лечение пациента, включая определение степени выраженности воспалительного процесса, протяженности поражения, наличия кишечных и внекишечных проявлений, в том числе взятие биопсийного материала.
При необходимости лечения и углубленного обследования в стационарных условиях, пациент направляется лечащим врачом в гастроэнтерологическое отделение, колопроктологическое отделение, центр диагностики и лечения воспалительных заболеваний кишечника или иную медицинскую организацию, оказывающую медицинскую помощь в стационарных условиях пациентам по профилю «гастроэнтерология», «колопроктология».
При подозрении и (или) выявлении язвенного колита у пациента в ходе оказания ему скорой медицинской помощи таких пациентов переводят или направляют в медицинские организации, оказывающие медицинскую помощь по профилю «гастроэнтерология», «колопроктология» для определения тактики ведения и необходимости применения дополнительно других методов специализированного лечения, включая проведение таргетной биологической терапии.
Врач-гастроэнтеролог, врач-колопроктолог медицинской организации, имеющей в своем составе кабинет врача-гастроэнтеролога, врача-колопроктолога, амбулаторный гастроэнтерологический центр (отделение), амбулаторный колопроктологический центр (отделение), центр диагностики и лечения воспалительных заболеваний кишечника направляет пациента в медицинские организации, имеющие для оказания медицинской помощи в стационарных условиях в своем составе гастроэнтерологическое отделение и/или колопроктологическое отделение, и/или центр диагностики и лечения воспалительных заболеваний кишечника для уточнения диагноза (в случае невозможности установления диагноза при оказании первичной специализированной медико-санитарной помощи) и оказания специализированной, в том числе высокотехнологичной, медицинской помощи. Срок начала оказания специализированной, за исключением высокотехнологичной, медицинской помощи определяется по решению комиссии по отбору пациентов для госпитализации в зависимости от тяжести язвенного колита, характера течения, распространённости воспалительного процесса, не должен превышать 30 календарных дней с даты выдачи направления на госпитализацию.
Специализированная, в том числе высокотехнологичная, медицинская помощь при язвенном колите оказывается врачами-гастроэнтерологами, врачами-колопроктологами в медицинских организациях, имеющих в своем составе гастроэнтерологическое отделение и/или колопроктологическое отделение, и/или центр диагностики и лечения воспалительных заболеваний кишечника, имеющих лицензию, необходимую материально-техническую базу, сертифицированных специалистов, в стационарных условиях и условиях дневного стационара и включает в себя профилактику, диагностику, лечение язвенного колита, требующих использования специальных методов и сложных уникальных медицинских технологий, а также медицинскую реабилитацию.
Показания для госпитализации в круглосуточный или дневной стационар медицинской организации, оказывающей специализированную, в том числе высокотехнологичную медицинскую помощь при язвенном колите определяются врачом-гастроэнтерологом и/или врачом-колопроктологом с проведением при необходимости мультидисциплинарного консилиума.
Показанием для госпитализации в медицинскую организацию в экстренной или неотложной форме является:
1) наличии осложнений язвенного колита, требующих оказания ему специализированной медицинской помощи в экстренной и неотложной форме;
2) наличие осложнений лечения (хирургическое вмешательство, биологическая терапия, гормональная и цитостатическая терапия и т.д.) язвенного колита.
Показанием для госпитализации в медицинскую организацию в плановой форме является:
1) необходимость выполнения сложных интервенционных диагностических медицинских вмешательств, требующих последующего наблюдения в условиях круглосуточного или дневного стационара;
2) наличие показаний к специализированному лечению язвенного колита (хирургическое вмешательство, гормональная и цитостатическая терапия, биологическая и таргетная терапия), требующему наблюдения в условиях круглосуточного или дневного стационара.
Показанием к выписке пациента из медицинской организации является:
1) завершение курса лечения, или одного из этапов оказания специализированной, в том числе высокотехнологичной медицинской помощи, в условиях круглосуточного или дневного стационара при условии отсутствия осложнений лечения, требующих медикаментозной коррекции и/или медицинских вмешательств в стационарных условиях;
2) отказ пациента или его законного представителя от специализированной, в том числе высокотехнологичной медицинской помощи в условиях круглосуточного или дневного стационара, установленной консилиумом медицинской организации, оказывающей лечение язвенного колита при условии отсутствия осложнений основного заболевания и/или лечения, требующих медикаментозной коррекции и/или медицинских вмешательств в стационарных условиях;
3) необходимость перевода пациента в другую медицинскую организацию по соответствующему профилю оказания медицинской помощи. Заключение о целесообразности перевода пациента в профильную медицинскую организацию осуществляется после предварительной консультации по предоставленным медицинским документам и/или предварительного осмотра пациента врачами специалистами медицинской организации, в которую планируется перевод.
7. Дополнительная информация (в том числе факторы, влияющие на исход заболевания или состояния)
Риск тяжелого обострения ЯК в течение жизни составляет 15%, при этом вероятность тяжелой атаки выше у пациентов с тотальным поражением толстой кишки. При проведении адекватной противорецидивной терапии в течение 5 лет обострений удается избежать у половины пациентов, а в течение 10 лет - у 20% пациентов. В течение первого года после постановки диагноза вероятность колэктомии составляет 4-9% (при тяжелой атаке - около 50%), в дальнейшем с каждым годом заболевания риск колэктомии увеличивается на 1%. Факторами риска агрессивного течения ЯК являются прогрессирование поражения от дистального (проктита) к тотальному, первичный склерозирующий холангит, а также детский и подростковый возраст на момент начала заболевания. Планирование беременности необходимо осуществлять в период ремиссии ВЗК, что позволяет улучшать исходы беременности. Применение беременными большинства препаратов для лечения ВЗК сопряжено с низким риском неблагоприятного воздействия на плод, за исключением метотрексата** и препаратов 5-АСК (код АТХ - A07EC Аминосалициловая кислота и аналогичные препараты (код АТХ A07EC02 Месалазин)) содержащих дибутилфталат. Отмена ингибиторов фактора некроза опухоли альфа (ФНО-альфа) или переход на монотерапию возможны лишь у ограниченного числа пациенток с низким риском реактивации ВЗК. Лечение генно-инженерными биологическими препаратами, не противопоказанными при беременности (см. инструкцию по применению), может быть продолжено, если польза для матери превышает потенциальные риски для плода.
Уменьшение рисков, связанных с назначением ГКС, достигается строгим соблюдением принципов гормональной терапии. ГКС не могут применяться в качестве поддерживающей терапии.
При назначении гормональной терапии необходимо учитывать следующее:
• постепенное снижение дозы стероидов до полной отмены - строго обязательно;
• суммарная продолжительность гормональной терапии не должна превышать 12 недель;
• обязательным является сопутствующий прием препаратов кальция в комбинации с витамином D и/или другими средствами;
• в период лечения необходим регулярный контроль уровня глюкозы в крови.
Пациентам, которым в результате хирургического лечения была сформирована кишечная стома, может потребоваться консультация и наблюдение специалистом по реабилитации стомированных пациентов.
Критерии оценки качества медицинской помощи
Критерии оценки качества первичной медико-санитарной помощи взрослым при язвенном колите
|
№ п/п |
Критерии оценки качества |
Оценка выполнения |
|
1. |
Выполнен прием (осмотр, консультация) врача-гастроэнтеролога и/или врача-колопроктолога с обязательным трансректальным пальцевым исследованием (при установлении диагноза) |
Да/Нет |
|
2. |
Выполнена колоноскопия или (при установлении диагноза) |
Да/Нет |
|
3. |
Выполнено ультразвуковое исследование органов брюшной полости (комплексное) (при установлении диагноза) |
Да/Нет |
|
4. |
Выполнено исследование кала на наличие токсина Clostridioides difficile или иммунохроматографическое экспресс-исследование кала на токсины A и B Clostridioides difficile или определение ДНК возбудителя Clostridioides difficile в образцах фекалий методом ПЦР (при остром течении язвенного колита и/или наличии подозрений на данную патологию) |
Да/Нет |
|
5. |
Назначена терапия препаратами группы аминосалициловая кислота и аналогичные препараты или глюкокортикостероиды для местного применения |
Да/Нет |
Критерии оценки качества специализированной медицинской помощи взрослым при язвенном колите
|
№ п/п |
Критерии оценки качества |
Оценка выполнения |
|
1. |
Выполнен прием (осмотр, консультация) врача-гастроэнтеролога и/или врача-колопроктолога с обязательным трансректальным пальцевым исследованием (при установлении диагноза) |
Да/Нет |
|
2. |
Выполнена колоноскопия (если не была выполнена в амбулаторных условиях ранее в течение предшествующих 12 месяцев) |
Да/Нет |
|
3. |
Выполнено ультразвуковое исследование органов брюшной полости (комплексное) (при установлении диагноза в случае, если не была выполнена в амбулаторных условиях) |
Да/Нет |
|
4. |
Выполнена биопсия слизистой оболочки толстой кишки в зоне поражения (при установлении диагноза в случае, если не была выполнена в амбулаторных условиях или если ранее установленный диагноз сомнителен, кроме стадии очень высокой активности заболевания) |
Да/Нет |
|
5. |
Проведена терапия лекарственными препаратами группы аминосалициловой кислоты и аналогичными препаратами и/или кортикостероидами системного действия и/или другими иммунодепрессантами и/или ингибиторами фактора некроза опухоли альфа (ФНО-альфа) или устекинумабом** или ведолизумабом** или тофацитинибом** или упадацитинибом** или озанимодом и/или хирургическое вмешательство (в зависи-мости от медицинских показаний и при отсутствии медицинских противопоказаний) |
Да/Нет |
Клинические рекомендации по диагностике и лечению Язвенного колита обсуждены на заседании профильной комиссии по специальности «Колопроктология» 8 октября 2022г. в рамках Всероссийской научно-практической конференции с международным участием «Съезд колопроктологов России», на заседании комиссии по хирургическим наукам научного совета ОМедН РАН 25 ноября 2022г в рамках XVI Всероссийской конференции с международным участием «Левитановские чтения»
Список литературы
- Travis S, Dinesen L. Remission intrials of ulcerative colitis: what does it mean? Pract Gastroenterology. 2010;30:17–20.
- D"Haens G, Sandborn W, Feagan B et al. A review of activity indices and efficacy end points for clinical trials of medical therapy in adults with ulcerative colitis. Gastroenterology. 2007;132:763–86.
- Truelove S, Witts L. et al. Cortisone in ulcerative colitis; final report on a therapeutic trial Br Med J. 1955; 2:1041-1048.
- Dignass A, Eliakim R, Magro F et al. Second European evidence-based consensus on the diagnosis and management of ulcerative colitis part 1: definitions and diagnosis J Crohns Colitis. 2012 Dec;6(10):965-90. doi: 10.1016/j.crohns.2012.09.003
- Cosnes J, Gower-Rousseau C, Seksik P et al. Epidemiology and natural history of inflammatory bowel diseases. Gastroenterology. 2011;140:1785–94.
- Molodecky N, Soon I, Rabi D et al. Increasing incidence and prevalence of the inflammatory bowel diseases with time, based on systematic review. Gastroenterology. 2012;142(1):46-54.
- De Groof E, Rossen N, Van Rhijn B et al. Burden of disease and increasing prevalence of inflammatory bowel disease in a populationbased cohort in the Netherlands. Eur. J. Gastroenterol Hepatol. 2016;28:1065–72.
- Qiu Y, Wen Ren W, Liu Y et al. Disease burden of inflammatory bowel disease in China from 1990 to 2017: Findings from the global burden of diseases 2017. E Clinical Medicine. 2020;27:100544. doi: 10.1016/j.eclinm.2020.100544
- Белоусова Е.А., Абдулганиева Д.И., Алексеева О.П. и соавт. Социально-демографическая характеристика, особенности течения и варианты лечения воспалительных заболеваний кишечника в России. Результаты двух многоцентровых исследований. Альманах клинической медицины. 2018;46(5):445-463. https://doi.org/10.18786/2072-0505-2018-46-5-445-463
- Burisch J, Pedersen N, Čuković-Čavka S et al. East-West gradient in the incidence of inflammatory bowel disease in Europe: The ECCO-EpiCom inception cohort. Gut. 2014;63(4):588-97.
- Katsanos KН, Vermeire S, Christodoulou DК et al. Dysplasia and cancer in inflammatory bowel disease 10 years after diagnosis: results of a population-based European collaborative follow-up study. Digestion. 2007;75: 113–21.
- Silverberg M, Satsangi J, Ahmad T et al. Toward an integrated clinical, molecular and serological classification of inflammatory bowel disease: report of a working party of the 2005 Montreal World Congress of Gastroenterology. Can J Gastroenterol. 2005;19:5–36.
- Seah D, De Cruz P. Review article: the practical management of acute severe ulcerative colitis. Aliment Pharmacol Ther. 2016 Feb;43(4):482-513.
- Hindryckx P, Jairath V, D"Haens G. Acute severe ulcerative colitis: from pathophysiology to clinical management. Nat Rev Gastroenterol Hepatol. 2016 Nov;13(11):654-664.
- Ачкасов С.И., Шапина М.В., Веселов В.В., Варданян А.В., Мингазов А.Ф., Пономаренко А.А. Предикторы колэктомии у пациентов со свертяжелым язвенным колитом. Колопроктология. 2020;19(3):37-48. https://doi.org/10.33878/2073-7556-2020-19-3-37-48
- Chen J, Andrews J, Kariyawasam V et al. IBD Sydney Organisation and the Australian Inflammatory Bowel Diseases Consensus Working Group. Review article: acute severe ulcerative colitis - evidence-based consensus statements. Aliment Pharmacol Ther. 2016 Jul;44(2):127-44.
- Schroeder KН, Tremaine W, Ilstrup DМ. Coated oral 5-aminosalicylic acid therapy for mildly to moderately active ulcerative colitis. A randomized study. N Engl J Med. 1987;317:1625–9.
- Григорьева Г.А., Мешалкина Н.Ю. О проблеме системных проявлений воспалительных заболеваний кишечника. Фарматека. 2011; № 15, с. 44-49.
- Sands B. From symptom to diagnosis: clinical distinctions among various forms of intestinal inflammation. Gastroenterology. 2004; 126:1518–32.
- Perler B, Ungaro R, Baird G, Malette M et al. Presenting symptoms in inflammatory bowel disease: descriptive analysis of a community-based inceptive cohort. BMC Gastroenterol. 2019;19:47.
- Fine K, Schiller L. AGA technical review on the evaluation and management of chronic diarrhea. Gastroenterology. 1999;116:1464–86.
- Forrest K, Symmons D, Foster P. Systematic review: is ingestion of paracetamol or non-steroidal anti-inflammatory drugs associated with exacerbations of inflammatory bowel disease? Aliment Pharmacol Ther. 2004;20:1035–43.
- Mahid SS, Minor KS, Soto RE et al. Smoking and inflammatory bowel disease: a meta-analysis. Mayo Clin Proc. 2006;81:1462–71.
- Vermeire S. Review article: genetic susceptibility and application of genetic testing in clinical management of inflammatory bowel disease. Aliment Pharmacol Ther. 2006;24:2–10.
- Mogan G. R. et al. Toxic megacolon in ulcerative colitis complicated by pneumomediastinum: report of two cases //Gastroenterology. – 1980. – Т. 79. – №. 3. – С. 559-562.
- Magro F, Gionchetti P, Eliakim R, Ardizzone S, Armuzzi A, Barreiro-de Acosta M, Burisch J, Gecse KB, Hart AL, Hindryckx P, Langner C, Limdi JK, Pellino G, Zagórowicz E, Raine T, Harbord M, Rieder F; European Crohn’s and Colitis Organisation [ECCO]. Third European Evidence-based Consensus on Diagnosis and Management of Ulcerative Colitis. Part 1: Definitions, Diagnosis, Extra-intestinal Manifestations, Pregnancy, Cancer Surveillance, Surgery, and Ileo-anal Pouch Disorders. J Crohns Colitis. 2017 Jun 1;11(6):649-670. doi: 10.1093/ecco-jcc/jjx008. Erratum in: J Crohns Colitis. 2022 Aug 16;: PMID: 28158501.
- Travis SP, Jewell DP. Ulcerative colitis: clinical presentation and diagnosis. In: Satsangi J, Sutherland LR, editors. Inflammatory Bowel Diseases. London: Churchill Livingstone. 2003:169–81.
- Lucendo AJ, Arias Á, Roncero Ó, Hervías D, et al. Anemia at the time of diagnosis of inflammatory bowel disease: Prevalence and associated factors in adolescent and adult patients. Sao Paulo Med J. 2014;132(3):140-6.
- Irwin JR, Ferguson E, Simms LA, Hanigan K et al. Detectable Laboratory Abnormality Is Present up to 12 Months Prior to Diagnosis in Patients with Crohn"s Disease. Dig Dis Sci. 2019 Feb;64(2):503-517.
- Cherfane CE, Gessel L, Cirillo D, Zimmerman MB, Polyak S. Monocytosis and a Low Lymphocyte to Monocyte Ratio Are Effective Biomarkers of Ulcerative Colitis Disease Activity. Inflamm Bowel Dis. 2015 Aug;21(8):1769-75.
- Feng JR, Qiu X, Wang F, Chen PF, et al. Diagnostic Value of Neutrophil-to-Lymphocyte Ratio and Platelet-to-Lymphocyte Ratio in Crohn"s Disease. Gastroenterol Res Pract. 2017. doi: 10.1155/2017/3526460
- Yoon JY, Park SJ, Hong SP, Kim TI, et al. Correlations of C-reactive protein levels and erythrocyte sedimentation rates with endoscopic activity indices in patients with ulcerative colitis. Dig Dis Sci. 2014 Apr;59(4):829-37.
- Yamamoto-Furusho JK, Sánchez-Osorio M, Uribe M. Prevalence and factors associated with the presence of abnormal function liver tests in patients with ulcerative colitis. Ann Hepatol. 2010 Oct-Dec;9(4):397-401.
- Archampong EQ, Harris J, Clark CG. The absorption and secretion of water and electrolytes across the healthy and the diseased human colonic mucosa measured in vitro. Gut. 1972 Nov;13(11):880-6.
- Maharshak N, Arbel Y, Gal-Oz A, Rogowski O, et al. Comparative analysis of Bayer wide-range C-reactive protein (wr-CRP) and the Dade-Behring high sensitivity C-reactive protein (hs-CRP) in patients with inflammatory bowel disease. J Dig Dis. 2008 Aug;9(3):140-3.
- Weber P, Husemann S, Vielhaber H, Zimmer KP, Nowak-Göttl U. Coagulation and fibrinolysis in children, adolescents, and young adults with inflammatory bowel disease. J Pediatr Gastroenterol Nutr. 1999 Apr;28(4):418-422.
- Axelrad JE1, Joelson A, Green PHR, Lawlor G et al. Enteric Infections Are Common in Patients with Flares of Inflammatory Bowel Disease. Am J Gastroenterol. 2018 Oct;113(10):1530-1539. doi: 10.1038/s41395-018-0211-8
- Issa M, Vikayapal A, Gracham MB et al. Impact of Clostridium difficile in inflammatory bowel disease patients. Clin Gastroenterol Hepatol. 2007;5:345-351.
- Rodeman JF, Dubberke ER, Reske KA et al. Incidence of Clostridium difficile in inflammatory bowel disease. Clin Gastroenterol Hepatol. 2007;5:339-344.
- Issa M, Ananthakrishnan AN, Binion DG. Clostridium difficile and inflammatory bowel disease. Inflamm Bowel Dis. 2008;14:1432-42.
- Nguyen GC, Kaplan GG, Harris ML et al. A national survey of the prevalence and impact of Clostridium difficile infection among hospitalized inflammatory bowel disease patients. Am J Gastroenterol. 2008;103:1443-50.
- Kim JJ, Simpson N, Klipfel N, Debose R, et al. Cytomegalovirus infection in patients with active inflammatory bowel disease. Dig Dis Sci. 2010 Apr;55(4):1059-65. doi: 10.1007/s10620-010-1126-4
- Levin A, Yaari S, Stoff R, Caplan O, Wolf DG, Israeli E. Diagnosis of Cytomegalovirus Infection during Exacerbation of Ulcerative Colitis.Digestion. 2017;96(3):142-148. doi: 10.1159/000479865.
- Lin WC, Chang CW, Chen MJ, Hsu TC, Wang HY. Effectiveness of sigmoidoscopy for assessing ulcerative colitis disease activity and therapeutic response. Medicine (Baltimore). 2019 May;98(21):e15748. doi: 10.1097/MD.0000000000015748
- Bansal J, Jenaw RK, Rao J et al. Effectiveness of plain radiography in diagnosing hollow viscus perforation: study of 1,723 patients of perforation peritonitis. Emerg Radiol. 2012 Apr;19(2):115-9. doi: 10.1007/s10140-011-1007-y.
- Annese V, DapernoM, Rutter MD et al. European evidence based consensus for endoscopy in inflammatory bowel disease. Journal of Crohn’s and Colitis. 2013;7(12):982-1018.
- Tanaka M, Saito H, Fukuda S, Sasaki Y et al. Simple mucosal biopsy criteria differentiating among Crohn disease, ulcerative colitis, and other forms of colitis: measurement of validity. Scand J Gastroenterol. 2000 Mar;35(3):281-6.
- Parente F, Greco S, Molteni M et al. Role of early ultrasound in detecting inflammatory intestinal disorders and identifying their anatomical location within the bowel. Alimentary Pharmacology and Therapeutics. 2003;18:1009-1016.
- Baltarowich O. H., Scoutt L. M., Hamper U. M. Nongynecologic findings on pelvic ultrasound: focus on gastrointestinal diseases //Ultrasound Quarterly. – 2012. – Т. 28. – №. 2. – С. 65-85.
- Smith R., Taylor K, Friedman AB et al. Systematic Review: Clinical Utility of Gastrointestinal Ultrasound in the Diagnosis, Assessment and Management of Patients With Ulcerative Colitis. J Crohns Colitis. 2020 May 21;14(4):465-479. doi: 10.1093/ecco-jcc/jjz163
- Kılıçkesmez O, Soylu A, Yaşar N, Demirbaş T, Dolapçıoğlu C et al. Is quantitative diffusion-weighted MRI a reliable method in the assessment of the inflammatory activity in ulcerative colitis? Diagn Interv Radiol. 2010 Dec;16(4):293-8. doi:10.4261/1305-3825.DIR.2989-09.1
- Jia Y, Li C, Yang X, Dong Z et al. CT Enterography score: a potential predictor for severity assessment of active ulcerative colitis. BMC Gastroenterol. 2018 Nov 9;18(1):173. doi: 10.1186/s12876-018-0890-z
- Gashin L, Villafuerte-Galvez J, Leffler DA et al. Utility of CT in the emergency department in patients with ulcerative colitis. Inflamm Bowel Dis. 2015 Apr;21(4):793-800. doi: 10.1097/MIB.0000000000000321
- Милько В.И., Минцер О.П., Топчий Т.В., Корсуновский А.А. Клиническая оценка данных ирригоскопии при неспецифическом язвенном колите. Вест. Рентгенологии и радиологии. 1983; № 5, с. 46-50.
- Fraser GM, Findlay JM. The double contrast enema in ulcerative and Crohn"s colitis. Clin Radiol. 1976 Jan;27(1):103-12.
- Ивашкин В.Т., Шептулин А.А., Шифрин О.С., Галимова С.Ф., и соавт. Микроскопический колит: клинические формы, диагностика, лечение. Российский журнал гастроэнтерологии, гепатологии, колопроктологии. 2006; т.16, №6, с. 56-60.
- Peyrin-Biroulet L, Sandborn W, Sands B et al. Selecting Therapeutic Targets inflammatory Bowel Disease (STRIDE): determining therapeutic goals for treat-to-target. Am J Gastroenterol. 2015;110(9):1324-1338. https://doi.org/10.1038/ajg.2015.233
- Тurner D, Ricciuto A, Lewis A et al.; International Organization for the Study of IBD. STRIDE-II: An Update on the Selecting Therapeutic Targets in Inflammatory Bowel Disease (STRIDE) Initiative of the International Organization for the Study of IBD (IOIBD): Determining Therapeutic Goals for Treat-to-Target strategies in IBD. Gastroenterology. 2021 Apr;160(5):1570-1583. doi:10.1053/j.gastro.2020.12.031. Epub 2021 Feb 19. PMID: 33359090
- Халиф И.Л. Лечебная тактика при язвенном колите. Российский журнал гастроэнтерологии, гепатологии, колопроктологии. 2006; т.16, №3, с.58-62.
- Белоусова Е.А., Никитина Н.В., Цодикова О.М. Лечение язвенного колита легкого и среднетяжелого течения. Фарматека. 2013; № 2, с.42-46.
- Reinisch W. Reinink A, Higgins P. Factors Associated With Poor Outcomes in Adults With Newly Diagnosed Ulcerative Colitis. Clinical Gastroenterology and Hepatology 2015;13:635-642.
- Dias CC, Rodrigues PP, da Costa-Pereira A et al. Clinical predictors of colectomy in patients with ulcerative colitis: systematic review and meta-analysis of cohort studies. J Crohns Colitis. 2015;9:156–63.
- Annese V, Beaugerie L, Egan L, Biancone L, Bolling C, Brandts C et al. European Evidence-based Consensus: Inflammatory Bowel Disease and Malignancies. J Crohns Colitis. 2015;9(11):945-65.
- Абдулганиева Д.И., Бакулев А.Л., Белоусова Е.А. и соавт. Раннее назначение генно-инженерных биологических препаратов при иммуновоспалительных заболеваниях: возможности и перспективы. Позиция экспертов. // Альманах клинической медицины. - 2020. - Т. 48. - №6. - C. 422-436. doi: 10.18786/2072-0505-2020-48-050
- Dinesen LC, Walsh AJ, Protic MN, Heap G et al. The pattern and outcome of acute severe colitis. J Crohns Colitis. 2010;4(4):431-437. https://doi.org/10.1016/j.crohns.2010.02.001
- Marshall JK, Thabane M, Steinhart AH, Newman JR et al. Rectal 5-aminosalicylic acid for induction of remission in ulcerative colitis. Cochrane Database of Systematic Reviews. 2010, Issue 1. Art. No.: CD004115. doi: 10.1002/14651858.CD004115
- Lamet M. A multicenter, randomized study to evaluate the efficacy and safety of mesalamine suppositories 1 g at bedtime and 500 mg twice daily in patients with active mild-to-moderate ulcerative proctitis. Dig Dis Sci. 2011;56:513–2256,57.
- Marshall JK, Irvine EJ. Rectal corticosteroids versus alternative treatments in ulcerative colitis: a meta-analysis. Gut. 1997;40:775–81.
- Pokrotnieks J, Sitkin S. A proposed treatment algorithm for mild to moderate ulcerative colitis–with an emphasis on budesonide foam and mucosal healing. J Gastroenterol. 2018 Jun;53(6):799–800. doi: 10.1007/s00535-018-1458-y
- Regueiro M, Loftus Jr EV, Steinhart AH, Cohen RD. Medical management of left-sided ulcerative colitis and ulcerative proctitis: critical evaluation of therapeutic trials. Inflamm Bowel Dis. 2006;12:979–94.
- Safdi M, DeMicco M, Sninsky C, Banks P et al. A double-blind comparison of oral versus rectal mesalamine versus combination therapy in the treatment of distal ulcerative colitis. Am J Gastroenterol. 1997;92:1867–71.
- Timmer A, Patton PH, Chande N, McDonald JW, MacDonald JK. Azathioprine and 6-mercaptopurine for maintenance of remission in ulcerative colitis. Cochrane Database Syst Rev. 2016 May 18;(5):CD000478. doi:10.1002/14651858.CD000478.pub4
- Ahmed I, Kassem W, Salam Y, Furnari M, Mehta T. Outcome of Cytomegalovirus Colitis in Inflammatory Bowel Disease with Different Regimes of Ganciclovir. Middle East J DigDis. 2018 Oct;10(4):220-229. doi: 10.15171/mejdd.2018.114
- Sutherland L, Macdonald JK. Oral 5-aminosalicylic acid for induction of remission in ulcerative colitis. Cochrane Database Syst Rev. 2006:CD000543.
- Ford AC, Achkar J-P, Khan KJ, Kane SV, Talley NJ et al. Efficacy of 5-aminosalicylates in ulcerative colitis: systematic review and meta-analysis. Am J Gastroenterol. 2011;106:601–16.
- Ford AC, Khan KJ, Achkar JP et al. Efficacy of oral vs. topical, or combined oral and topical 5-aminosalicylates, in Ulcerative Colitis: systematic review and meta-analysis. The American journal of gastroenterology. 2012;107:167-76.
- Nikfar S et al. A meta-analysis of the efficacy of sulfasalazine in comparison with 5- aminosalicylates in the induction of imp rovement and maintenance of remission in patients with ulcerative colitis. Digestive diseases and sciences. 2009;54(6):1157-1170.
- Kane SV, Bjorkman DJ. The efficacy of oral 5-ASAs in the treatment of active ulcerative colitis: a systematic review. Rev Gastroenterol Disord. 2003;3:210–8.
- Zhang Y, Chen D, Wang F, Li X, Xue X et al. Comparison of the efficiency of different enemas on patients with distal ulcerative colitis. Cell Prolif. 2019 Mar;52(2):e12559. doi: 10.1111/cpr.12559. Epub 2019 Jan 18
- Danielsson A, Löfberg R, Persson T, Salde L et al. A steroid enema, budesonide, lacking systemic effects for the treatment of distal ulcerative colitis or proctitis. Scand J Gastroenterol. 1992;27(1):9-12.
- Nguyen NH, Fumery M, Dulai PS, Prokop LJ et al. Comparative efficacy and tolerability of pharmacological agents for management of mild to moderate ulcerative colitis: a systematic review and network meta-analyses. Lancet Gastroenterol Hepatol. 2018 Nov;3(11):742-753. doi:10.1016/S2468-1253(18)30231-0
- D"Haens G. Systematic review: second-generation vs. conventional corticosteroids for induction of remission in ulcerative colitis. Aliment Pharmacol Ther. 2016;44:1018-1029.
- Hartmann F1, Stein J; BudMesa-Study Group. Clinical trial: controlled, open, randomized multicentre study comparing the effects of treatment on quality of life, safety and efficacy of budesonide or mesalazine enemas in active left-sided ulcerative colitis. Aliment Pharmacol Ther. 2010 Aug;32(3):368-76.
- Gross V1, Bar-Meir S, Lavy A, Mickisch O et al. Budesonide foam versus budesonide enema in active ulcerative proctitis and proctosigmoiditis. Aliment Pharmacol Ther. 2006 Jan 15;23(2):303-12.
- Matzen P. Budesonide enema in distal ulcerative colitis. A randomized dose-response trial with prednisolone enema as positive control. The Danish Budesonide Study Group. Scand J Gastroenterol. 1991 Dec;26(12):1225-30.
- Lichtenstein GR. Budesonide Multi-matrix for the Treatment of Patients with Ulcerative Colitis. Dig Dis Sci. 2016 Feb;61(2):358-70.
- Sherlock ME, MacDonald JK, Griffiths AM, Steinhart AH, Seow CH. Oral budesonide for induction of remission in ulcerative colitis. Cochrane Database Syst Rev. 2015 Oct 26;(10):CD007698.
- Danese S, Siegel CA, Peyrin-Biroulet L. Review article: integrating budesonide-MMX into treatment algorithms for mild-to-moderate ulcerative colitis. Aliment Pharmacol Ther. 2014 May;39(10):1095-103.
- Gisbert JP, Linares PM, McNicholl AG, Mate J, Gomollon F. Meta-analysis: the efficacy of azathioprine and mercaptopurine in ulcerative colitis. Aliment Pharmacol Ther. 2009;30:126–37.
- Rutgeerts P, Sandborn WJ, Feagan BG et al. Infliximab for induction and maintenance therapy for ulcerative colitis. New England Journal of Medicine. 2005;353:2462-2476.
- Sandborn WJ, van Assche G, Reinisch W et al. Adalimumab induces and maintains clinical remission in patients with moderate-to-severe ulcerative colitis. Gastroenterology. 2012;142:257-65 e1-3.
- Sandborn WJ, Feagan BG, Marano C et al. Subcutaneous golimumab induces clinical response and remission in patients with moderate-to-severe ulcerative colitis. Gastroenterology. 2014;146:85-95; quiz e14-5.
- Feagan BG, Rutgeerts P, Sands BE et al. Vedolizumab as induction and maintenance therapy for ulcerative colitis. The New England journal of medicine. 2013;369:699-710.
- Sandborn W SB, D"Haens GR et al. Efficacy and safety of oral tofacitinib as induction therapy in patients with moderate to severe ulcerative colitis: results from two phase 3 randomized controlled trials. Gastroenterology. 2016:S157
- Danese S, Vermeire S et al. Upadacitinib as induction and maintenance therapy for moderately to severely active ulcerative colitis: results from three phase 3, multicentre, double-blind, randomised trials. Lancet. 2022 Jun 4;399(10341):2113-2128. doi: 10.1016/S0140-6736(22)00581-5
- Sandborn W, Feagan BG et al. Ozanimod as Induction and Maintenance Therapy for Ulcerative Colitis N Engl J Med. 2021 Sep 30;385(14):1280-1291. doi: 10.1056/NEJMoa2033617
- Panaccione R, Ghosh S, Middleton S et al. Combination therapy with infliximab and azathioprine is superior to monotherapy with either agent in ulcerative colitis. Gastroenterology. 2014;146:392-400.e3.
- Panaccione R, Ghosh S, Middleton S et al. Infliximab, azathioprine or infliximab + azathioprine for treatment of moderate to severe ulcerative colitis. The UC SUCCESS trial. J Crohns Colitis. 2011;5:1376-1380. doi:10.1002/14651858.CD000478
- Yarur AJ, Rubin DT. Therapeutic Drug Monitoring of Anti-tumor Necrosis Factor Agents in Patients with Inflammatory Bowel Diseases. Inflamm Bowel Dis. 2015 Jul;21(7):1709-18.
- Steenholdt C, Bendtzen K, Brynskov J, Ainsworth MA. Optimizing Treatment with TNF Inhibitors in Inflammatory Bowel Disease by Monitoring Drug Levels and Antidrug Antibodies. Inflamm Bowel Dis. 2016 Aug;22(8):1999-2015.
- Sandborn WJ, Su C, Sands BE et al. OCTAVE Induction 1, OCTAVE Induction 2, and OCTAVE Sustain Investigators. Tofacitinib as induction and maintenance therapy for ulcerative colitis. N Engl J Med. 2017;376:1723–36.
- Reinisch W, Sandborn WJ, Rutgeerts P et al. Long-term infliximab maintenance therapy for ulcerative colitis: the ACT-1 and -2 extension studies. Inflamm Bowel Dis. 2012;18:201–11.
- Danese S, D"Amico F, Bonovas S, Peyrin-Biroulet L. Positioning Tofacitinib in the Treatment Algorithm of Moderate to Severe Ulcerative Colitis. Inflamm Bowel Dis. 2018;24(10):2106-2112. doi:10.1093/ibd/izy076
- Sands BE, Sandborn WJ, Panaccione R et al. Ustekinumab as Induction and Maintenance Therapy for Ulcerative Colitis. N Engl J Med. 2019 Sep 26;381(13):1201-1214. doi: 10.1056/NEJMoa1900750
- Singh S, Fumery M, Sandborn WJ, Murad MH. Systematic review with network meta-analysis: first- and second-line pharmacotherapy for moderate-severe ulcerative colitis. Aliment Pharmacol Ther. 2018 Jan;47(2):162-175. doi:10.1111/apt.14422
- Shmidt E, Kochhar G, Hartke J et al. Predictors and Management of Loss of Response to Vedolizumab in Inflammatory. Inflamm Bowel Dis. 2018;24(11):2461-2467. doi: 10.1093/ibd/izy171
- Sands BE, Armuzzi A, Marshall JK et al. DOP026 Efficacy and safety of dose escalation to tofacitinib 10 mg BID for patients with ulcerative colitis following loss of response on tofacitinib 5 mg BID maintenance therapy: results from OCTAVE open. J Crohns Colitis. 2018;12:49, https://doi.org/10.1093/ecco-jcc/jjx180.063.
- Turner D, Walsh CM, Steinhart AH et al. Response to corticosteroids in severe ulcerative colitis: a systematic review of the literature and a meta-regression. Clin Gastroenterol Hepatol. 2007;5:103-110.
- Dignass AU, Gasche C, Bettenworth D et al. European consensus on the diagnosis and management of iron deficiency and anaemia in inflammatory bowel diseases. J Crohns Colitis. 2015;9:211-22.
- Gonzalez-Huix F, Fernandez-Banares F, Esteve-Comas M et al. Enteral versus parenteral nutrition as adjunct therapy in acute ulcerative colitis. Am J Gastroenterol. 1993;88:227–32.
- Parlak E, Dağli U, Ulker A et al. Comparison of 5-aminosalicylic acid plus glucocorticosteroid with metronidazole and ciprofloxacin in patients with active ulcerative colitis. J Clin Gastroenterol. 200;33(1):85-6.
- Khan KJ, Ullman TA, Ford AC, Abreu MT et al. Antibiotic therapy in inflammatory bowel disease: a systematic review and meta-analysis. Am J Gastroenterol. 2011;106:661–73.
- Ohkusa T, Kato K, Terao S, Chiba T et al. Newly developed antibiotic combination therapy for ulcerativecolitis: a double-blind placebo-controlled multicenter trial. Am J Gastroenterol. 2010;105:1820–9.
- Sokol H, Seksik P, Carrat F, Nion-Larmurier I et al. Usefulness of co-treatment with immunomodulators in patients with inflammatory bowel disease treated with scheduled infliximab maintenance therapy. Gut. 2010;59:1363–8.
- Chebli LA, Chaves LDdM, Pimentel FF, Guerra DM et al. Azathioprine maintains long-term steroid-free remission through 3 years in patients with steroid-dependent ulcerative colitis. Inflamm Bowel Dis. 2010;16:613–9.
- Ardizzone S, Maconi G, Russo A, Imbesi V et al. Randomised controlled trial of azathioprine and 5-aminosalicylic acid for treatment of steroid dependent ulcerative colitis. Gut. 2006;55:47–53.
- Халиф И.Л., Нанаева Б.А., Головенко А.О., Головенко О.В. Отдаленные результаты консервативного лечения больных с тяжелым обострением язвенного колита. Терапевтический архив. 2015;87(2):34-38. https://doi.org/10.17116/terarkh201587234-38.
- Järnerot G, Hertervig E, Friis-Liby I et al. Infliximab as rescue therapy in severe to moderately severe ulcerative colitis: a randomized, placebo-controlled study. Gastroenterology. 2005;128:1805–11.
- Lees CW, Heys D, Ho GT, Noble CL et al. A retrospective analysis of the efficacy and safety of infliximab as rescue therapy in acute severe ulcerative colitis. Aliment Pharmacol Ther. 2007;26:411–9
- Van Assche G, D"Haens G, Noman M, Vermeire S et al. Randomized, double-blind comparison of 4 mg/kg versus 2 mg/kg intravenous cyclosporine in severe ulcerative colitis. Gastroenterology. 2003;125:1025–31.
- Sjoberg M, Walch A, Meshkat M, Gustavsson A et al. Infliximab or cyclosporine as rescue therapy in hospitalized patients with steroid-refractory ulcerative colitis: a retrospective observational study. Inflamm Bowel Dis. 2012;18(2):212-8.
- Головенко А.О., Халиф И.Л., Головенко О.В., Веселов В.В. Предикторы эффективности инфликсимаба у больных с тяжелой атакой язвенного колита. Российский журнал гастроэнтерологии, гепатологии, колопроктологии. 2013.5(23): 65-73.
- Lennard-Jones JE, Ritchie JK, Hilder W, Spicer CC. Assessment of severity in colitis: a preliminary study. Gut. 1975;16:579–84.
- Travis SP, Farrant JM, Ricketts C, Nolan DJ et al. Predicting outcome in severe ulcerative colitis. Gut. 1996;38:905–10.
- Cima R. R. Timing and indications for colectomy in chronic ulcerative colitis: surgical consideration //Digestive diseases. – 2010. – Т. 28. – №. 3. – С. 501-507
- Provenzale D. et al. Prophylactic colectomy or surveillance for chronic ulcerative colitis? A decision analysis //Gastroenterology. – 1995. – Т. 109. – №. 4. – С. 1188-1196.
- Jess T, Loftus Jr EV, Velayos FS, Harmsen WS et al. Risk of intestinal cancer in inflammatory bowel disease: a population-based study from olmsted county, Minnesota. Gastroenterology. 2006;130:1039–46.
- Odze R. D. et al. Long-term follow-up after polypectomy treatment for adenoma-like dysplastic lesions in ulcerative colitis //Clinical Gastroenterology and Hepatology. – 2004. – Т. 2. – №. 7. – С. 534-541.
- Fumery M. et al. Colonic strictures in inflammatory bowel disease: epidemiology, complications, and management //Journal of Crohn"s and Colitis. – 2021. – Т. 15. – №. 10. – С. 1766-1773.
- Feuerstein JD, Rakowsky S, Sattler L et al. Meta-analysis of dye-based chromoendoscopy compared with standard- and high-definition white-light endoscopy in patients with inflammatory bowel disease at increased risk of colon cancer. Gastrointest Endosc. 2019; 90:186– 195.
- Iannone A, Ruospo M, Wong G et al. Chromoendoscopy for surveillance in ulcerative colitis and crohn’s disease: a systematic review of randomized trials. Clin Gastroenterol Hepatol 2017;15:1684–1697.
- Bessissow T, Dulai PS, Restellini S et al. Comparison of endoscopic dysplasia detection techniques in patients with ulcerative colitis: a systematic review and network meta-analysis. Inflamm Bowel Dis 2018;24:2518–2526.
- Alkandari A, Thayalasekaran S, Bhandari M et al. Endoscopic Resections in Inflammatory Bowel Disease: A Multicentre European Outcomes Study. J Crohns Colitis. 2019; 28:13(11):1394-1400.
- Kinoshita S, Uraoka T, Nishizawa T et al. The role of colorectal endoscopic submucosal dissection in patients with ulcerative colitis. Gastrointest Endosc. 2018; 87(4):1079-1084.
- Andersen K, Vogt C, Blondin D et al. Multi-detector CT-colonography in inflammatory bowel disease: prospective analysis of CT-findings to high-resolution video colonoscopy. Eur J Radiol. 2006;58:140–6.
- Richards DM, Hughes SA, Irving MH, Scott NA. Patient quality of life after successful restorative proctocolectomy is normal. Colorectal Dis. 2001;3:223–6.
- McLaughlin SD, Clark SK, Thomas-Gibson S, Tekkis P et al. Guide to endoscopy of the ileo-anal pouch following restorative proctocolectomy with ileal pouch-anal anastomosis; indications, technique, and management of common findings. Inflamm Bowel Dis. 2009;15:1256–63.
- Marcello PW, Roberts PL, Schoetz Jr DJ, Coller JA et al. Long-term results of the ileoanal pouch procedure. Arch Surg. 1993;128:500–3 [discussion 503–4].
- Sagar PM, Pemberton JH. Ileo-anal pouch function and dysfunction. Dig Dis. 1997;15:172–88.
- Meagher AP, Farouk R, Dozois RR, Kelly KA et al. J ileal pouch-anal anastomosis for chronic ulcerative colitis: complications and long-term outcome in 1310 patients. Br J Surg. 1998;85:800–3.
- Fleming FJ, Francone TD, Kim MJ, Gunzler D, Messing S, Monson JR. A laparoscopic approach does reduce short-term complications in patients undergoing ileal pouch-anal anastomosis. Dis Colon Rectum. 2011;54:176–82.
- Colombo F, Pellino G, Selvaggi F et al. Minimally invasive surgery and stoma-related complications after restorative proctocolectomy for ulcerative colitis. A two-centre comparison with open approach. Am J Surg. 2019;217:682–8.
- Ahmed A, Keus F, Heikens J et al. Open versus laparoscopic [assisted] ileo pouch anal anastomosis for ulcerative colitis and familial adenomatous polyposis. Cochrane Database Syst Rev. 2009;1:CD006267.
- Tilney HS, Lovegrove RE, Heriot AG et al. Comparison of short-term outcomes of laparoscopic vs open approaches to ileal pouch surgery. Int J Colorectal Dis. 2007;22:531–42.
- Hull TL, Joyce MR, Geisler DP, Coffey JC. Adhesions after laparoscopic and open ileal pouch-anal anastomosis surgery for ulcerative colitis. Br J Surg. 2012;99:270–5.
- Sofo L, Caprino P, Sacchetti F, Bossola M. Restorative proctocolectomy with ileal pouch-anal anastomosis for ulcerative colitis: a narrative review. World J Gastrointest Surg. 2016;8:556–63.
- Setti-Carraro P, Ritchie JK, Wilkinson KH et al. The first 10 years’ experience of restorative proctocolectomy for ulcerative colitis. Gut. 1994;35:1070–1075.
- Fazio VW, Ziv Y, Church JM et al. Ileal pouch-anal anastomoses complications and function in 1005 patients. Ann Surg. 1995;222:120–127.
- Belliveau P, Trudel J, Vasilevsky CA et al. Ileoanal anastomosis with reservoirs: complications and long-term results. Can J Surg. 1999;42: 345–352.
- Pinto RA, Canedo J, Murad-Regadas S, Regadas SF et al. Ileal pouch-anal anastomosis in elderly patients: is there a difference in morbidity compared with younger patients? Colorectal Dis. 2011;13:177–83.
- Church JM. Functional outcome and quality of life in an elderly patient with an ileal pouch-anal anastomosis: a 10-year follow up. Aust N Z J Surg. 2000;70:906–7.
- Chapman JR, Larson DW, Wolff BG, Dozois EJ et al. Ileal pouch-anal anastomosis: does age at the time of surgery affect outcome? Arch Surg. 2005;140:534–40.
- Delaney CP, Dadvand B, Remzi FH et al. Functional outcome, quality of life, and complications after ileal pouch-anal anastomosis in selected septuagenarians. Dis Colon Rectum. 2002;45:890–4.
- Olsen KO, Joelsson M, Laurberg S, Oresland T. Fertility after ileal pouch-anal anastomosis in women with ulcerative colitis. Br J Surg. 1999;86:493–5.
- Ording OK, Juul S, Berndtsson I, Oresland T et al. Ulcerative colitis: female fecundity before diagnosis, during disease, and after surgery compared with a population sample. Gastroenterology. 2002;122:15–9.
- Gorgun E, Remzi FH, Goldberg JM, Thornton J et al. Fertility is reduced after restorative proctocolectomy with ileal pouch anal anastomosis: a study of 300 patients. Surgery. 2004;136:795–803.
- Johnson P, Richard C, Ravid A, Spencer L et al. Female infertility after ileal pouch-anal anastomosis for ulcerative colitis. Dis Colon Rectum. 2004;47:1119–26.
- Oresland T, Palmblad S, Ellstrom M, Berndtsson I et al. Gynaecological and sexual function related to anatomical changes in the female pelvis after restorative proctocolectomy. Int J Colorectal Dis. 1994;9:77–81.
- Alves A, Panis Y, Bouhnik Y, Maylin V et al. Subtotal colectomy for severe acute colitis: a 20-year experience of a tertiary care center with an aggressive and early surgical policy. J Am Coll Surg. 2003;197:379–85
- Berg DF, Bahadursingh AM, Kaminski DL, Longo WE. Acute surgical emergencies in inflammatory bowel disease. Am J Surg. 2002;184:45–51.
- Hyman NH, Cataldo P, Osler T. Urgent subtotal colectomy for severe inflammatory bowel disease. Dis Colon Rectum. 2005;48: 70–3.
- Holubar SD, Larson DW, Dozois EJ, Pattana-Arun J et al. Minimally invasive subtotal colectomy and ileal pouch-anal anastomosis for fulminant ulcerative colitis: a reasonable approach? Dis Colon Rectum. 2009;52:187–92.
- Marceau C, Alves A, Ouaissi M, Bouhnik Y et al. Laparoscopic subtotal colectomy for acute or severe colitis complicating inflammatory bowel disease: a case-matched study in 88 patients. Surgery. 2007;141:640.
- Annibali R, Oresland T, Hulten L. Does the level of stapled ileoanal anastomosis influence physiologic and functional outcome? Dis Colon Rectum. 1994;37:321–9.
- Burns EM, Bottle A, Aylin P, Clark SK et al. Volume analysis of outcome following restorative proctocolectomy. Br J Surg. 2011;98:408–17.
- Tekkis PP, Fazio VW, Lavery IC, Remzi FH et al. Evaluation of the learning curve in ileal pouch-anal anastomosis surgery. Ann Surg. 2005;241:262–8.
- Lepisto A. Fate of the rectum after colectomy with ileorectal anastomosis in ulcerative colitis. Scand J Surg. 2005;94:40–2.
- Edwards, C.M., George B, Warren F. Diversion colitis: new light through old windows. Histopathology. 1999.35(1):86-7.
- Shepherd NA, Jass JR, Duval I, Moskowitz RL et al. Restorative proctocolectomy with ileal reservoir: pathological and histochemical study of mucosal biopsy specimens. J Clin Pathol. 1987;40:601–7.
- SettiCarraro PG, Talbot IC, Nicholls JR. Patterns of distribution of endoscopic and histological changes in the ileal reservoir after restorative proctocolectomy for ulcerative colitis. A long-term follow-up study. Int J Colorectal Dis. 1998;13:103–7.
- Ferrante M, D"Hoore A, Vermeire S et al. Corticosteroids but not infliximab increase short-term postoperative infectious complications in patients with ulcerative colitis. Inflamm Bowel Dis. 2009;15:1062–70.
- Lake JP, Firoozmand E, Kang JC, Vassiliu P et al. Effect of high-dose steroids on anastomotic complications after proctocolectomy with ileal pouch-anal anastomosis. J Gastrointest Surg. 2004;8:547–51.
- Mahadevan U, Loftus Jr EV, Tremaine WJ, Pemberton JH, Harmsen WS, Schleck CD et al. Azathioprine or 6-mercaptopurine before colectomy for ulcerative colitis is not associated with increased postoperative complications. Inflamm Bowel Dis. 2002;8:311–6.
- Pugliese D, Armuzzi A, Rizzo G et al. Effect of anti-TNF-alpha treatment on short-term post-operative complications in patients with inflammatory bowel disease. Gut. 2010;59(Suppl III):A13.
- Subramanian V, Pollok RC, Kang JY, Kumar D. Systematic review of postoperative complications in patients with inflammatory bowel disease treated with immunomodulators. Br J Surg. 2006;93:793–9.
- Yang Z, Wu Q, Wang F, Wu K, Fan D. Meta-analysis: effect of preoperative infliximab use on early postoperative complications in patients with ulcerative colitis undergoing abdominal surgery. Aliment Pharmacol Ther. 2012 Nov;36(10):922-8. doi: 10.1111/apt.12060. Epub 2012 Sep 24
- Meagher AP, Farouk R, Dozois RR, Kelly KA et al. J ileal pouch-anal anastomosis for chronic ulcerative colitis: complications and long-term outcome in 1310 patients. Br J Surg. 1998;85:800–3.
- Simchuk EJ, Thirlby RC. Risk factors and true incidence of pouchitis in patients after ileal pouch-anal anastomoses. World J Surg. 2000;24:851–6.
- Stahlberg D, Gullberg K, Liljeqvist L, Hellers G et al. Pouchitis following pelvic pouch operation for ulcerative colitis. Incidence, cumulative risk, and risk factors. Dis Colon Rectum. 1996;39:1012–8.
- Penna C, Tiret E, Kartheuser A, Hannoun L et al. Function of ileal J pouch-anal anastomosis in patients with familial adenomatous polyposis. Br J Surg. 1993;80:765–7.
- Tjandra JJ, Fazio VW, Church JM, Oakley JR et al. Similar functional results after restorative proctocolectomy in patients with familial adenomatous polyposis and mucosal ulcerative colitis. Am J Surg. 1993;165:322–5.
- Poo S., Sriranganathan D., Segal J. P. Network meta-analysis: efficacy of treatment for acute, chronic, and prevention of pouchitis in ulcerative colitis //European Journal of Gastroenterology & Hepatology. – 2022. – Т. 34. – №. 5. – С. 518-528
- Viazis N, Giakoumis M, Koukouratos T et al. Long term benefit of one year infliximab administration for the treatment of chronic refractory pouchitis, Journal of Crohn"s and Colitis. 2013;7(10):457–460.
- Travis S, Silverberg MS, Danese S et al. OP04 Vedolizumab intravenous is effective across multiple treatment targets in chronic pouchitis: Results of the randomised, double-blind, placebo-controlled EARNEST trial. Journal Crohns Colitis. 2022;16(Supplement_1):i004–5
- Peter J, Zeitz J, Stallmach A. Ustekinumab Rescue Therapy in a Patient With Chronic Refractory Pouchitis. Journal of Crohn"s and Colitis. 2018;12(8):1008–1009.
- Сухина М.А., Образцов И.В., Михалевская В.И., Ачкасов С.И., Сафин А.Л., Шелыгин Ю.А. Алгоритм лабораторной диагностики clostridium difficile-ассоциированной диареи. Журнал микробиологии, эпидемиологии и иммунобиологии (ЖМЭИ). 2018;(2):45-53.
- Шелыгин Ю.А., Алёшкин В.А., Сухина М.А., Миронов А.Ю., и др. Клинические рекомендации национальной ассоциации специалистов по контролю инфекций, связанных с оказанием медицинской помощи, и общероссийской общественной некоммерческой организации «Ассоциация колопроктологов России» по диагностике, лечению и профилактике Сlostridium difficile-ассоциированной диареи (cdi). Колопроктология. 2018;(3):7-23. https://doi.org/10.33878/2073-7556-2018-0-3-7-23.
- Aguado JM, Anttila VJ, Galperine T, Goldenberg SD et al. Highlighting clinical needs in Clostridium difficile infection: the views of European healthcare professionals at the front line. J Hosp Infect. 2015;2(50):117-125.
- Metan G, Türe Z, Kaynar L. Tigecycline for the treatment of Clostridium difficile infection refractory to metronidazole in haematopoietic stem cell transplant recipients. Journal of Chemotherapy. 2015;6(27):354–357.
- Chiu CY, Sarwal A, Feinstein A, Hennessey K. Effective Dosage of Oral Vancomycin in Treatment for Initial Episode of Clostridioides difficile Infection: A Systematic Review and Meta-Analysis. Antibiotics (Basel). 2019 Oct 1;8(4). pii: E173. doi: 10.3390/antibiotics8040173.
- Tschudin-Sutter S, Braissant O, Erb S et al. Growth Patterns of Clostridium difficile – Correlations with Strains, Binary Toxin and Disease Severity: A Prospective Cohort Study. PLoS One. 2016;9(11):e0161711.
- Фоменко О.Ю., Ачкасов С.И., Титов А.Ю., Алешин Д.В., и соавт. Современные возможности улучшения функционального состояния запирательного аппарата у пациентов с наличием превентивных кишечных стом. Российский журнал гастроэнтерологии, гепатологии, колопроктологии. 2015; №5, с.77-83.
- Фоменко О.Ю., Ачкасов С.И., Титов А.Ю., Джанаев Ю.А., и соавт. Роль аноректальной манометрии, БОС-терапии и тибиальной нейромодуляции в диагностике и консервативном лечении анальной инконтиненции у пожилых. Клиническая геронтология. 2015; №5-6, с.16-20.
- Rahier JF, Magro F, Abreu C, Armuzzi A et al. Second European evidence-based consensus on the prevention, diagnosis and management of opportunistic infections in inflammatory bowel disease. JCrohns Colitis. 2014 Jun;8(6):443-68. doi: 10.1016/j.crohns.2013.12.013. Epub 2014 Mar 6
- American Thoracic Society/Centers for Disease Control and Prevention/Infectious Diseases Society of America: controlling tuberculosis in the United States. Am J Respir Crit Care Med. 2005.172(9):1169-227.
- Franchimont D, Ferrante M, Louis E et al. Belgian IBD research group (BIRD) position statement 2017 on the use of biosimilars in inflammatory bowel diseases (IBD); Acta Gastroenterol Belq 2018;81:49–53.
- Lin WC, Chang CW, Chen MJ, Hsu TC, Wang HY. Effectiveness of sigmoidoscopy for assessing ulcerative colitis disease activity and therapeutic response. Medicine (Baltimore). 2019 May;98(21):e15748. doi: 10.1097/MD.0000000000015748
- Colombel JF, Ordás I, Ullman T, Rutgeerts P et al. Agreement Between Rectosigmoidoscopy and Colonoscopy Analyses of Disease Activity and Healing in Patients With Ulcerative Colitis. Gastroenterology. 2016 Feb; 150(2):389-95.e3. doi: 10.1053/j.gastro.2015.10.016
- Annese V., Daperno M., Rutter MD et al. European evidence based consensus for endoscopy in inflammatory bowel disease. J Crohns Colitis. 2013;7(12):982-1018.
- Puolanne AM, Kolho KL, Alfthan H, Färkkilä M. Is home monitoring of inflammatory bowel disease feasible? A randomized controlled study. Scand J Gastroenterol. 2019 Jul;54(7):849-854. doi: 10.1080/00365521.2019.1618910
- Kato J, Yoshida T, Hiraoka S. Prediction of treatment outcome and relapse in inflammatory bowel disease. Expert Rev Clin Immunol. 2019 Jun;15(6):667-677. doi: 10.1080/1744666X.2019.1593140
- Князев О.В., Каграманова А.В., Корнеева И.А. и соавт. Значение фекального кальпротектина в мониторинге активности воспалительных заболеваний кишечника. Терапевтический архив. 2019; 91 (4): 53–61. DOI: 10.26442/00403660.2019.04.000229
- Trigo-Vicente С., Gimeno-Ballester V et al. Systematic review and network meta‑analysis of treatmentfor moderate‑to‑severe ulcerative colitis. Int J Clin Pharm. 2018 Dec;40(6):1411-1419. doi: 10.1007/s11096-018-0743-4
- Nguyen GC, Bernstein CN, Bitton A et al. Consensus statements on the risk, prevention, and treatment of venous thromboembolism in inflammatory bowel disease: Canadian Association of Gastroenterology. Gastroenterology. 2014;146:835-848.
- Olivera P., Zuily S. International consensus on the prevention of venous and arterial thrombotic events in patients with inflammatory bowel disease. Nat Rev Gastroenterol Hepatol. 2021 Dec;18(12):857-873. doi: 10.1038/s41575-021-00492-8
- Подольская Д.В., Шапина М.В., Баранова Т.А., Тишаева И.А., Александров Т.Л., Князев О.В., Нанаева Б.А. Эффективность тофацитиниба в качестве «терапии спасения» у пациентов с язвенным колитом тяжелой степени. Колопроктология. 2021;20(3):43–50. https://doi.org/10.33878/2073-7556-2021-20-3-43-50
- Kotwani P., Terdiman J, Lewin S. Tofacitinib for Rescue Therapy in Acute Severe Ulcerative Colitis: A Real-world Experience. J CrohnsColitis. 2020 Jul 30;14(7):1026-1028. doi: 10.1093/ecco-jcc/jjaa018
- Xiao Y, Benoit N, Sedano R. Effectiveness of Tofacitinib for Hospitalized Patients with Acute Severe Ulcerative Colitis: Case Series. Dig Dis Sci. 2022. doi: 10.1007/s10620-022-07439-2
- Goetgebuer L et al. Kreijne Increased Risk of High-grade Cervical Neoplasia in Women with Inflammatory Bowel Disease: A Case-controlled Cohort Study. Journal of Crohn"s and Colitis. 2021, 1464–1473. doi:10.1093/ecco-jcc/jjab036
- Sands B, Peyrin-Biroulet L, Loftus E et al. Vedolizumab versus Adalimumab for Moderate-to-Severe Ulcerative Colitis. N Engl J Med. 2019 Sep 26;381(13):1215-1226. doi: 10.1056/NEJMoa1905725
- Bressler B, Yarur A, Silverberg M et al. Vedolizumab and Anti-Tumour Necrosis Factor α Real-World Outcomes in Biologic-Naïve Inflammatory Bowel Disease Patients: Results from the EVOLVE Study. J Crohns Colitis. 2021 Oct 7;15(10):1694-1706. doi: 10.1093/ecco-jcc/jjab058
- Bressler B, Yarur A, Kopylov U et al. Clinical Effectiveness of First-Line Anti-TNF Therapies and Second-Line Anti-TNF Therapy Post-Vedolizumab Discontinuation in Patients with Ulcerative Colitis or Crohn’s Disease. United European Gastroenterol J. 2019;7(8(Supplement)). Poster P1091.
- Guideline on similar biological medicinal products containing biotechnology-derived proteins as active substance: quality issues (revision 1) EMA/CHMP/BWP/247713/2012. Available at: https://www.ema.europa.eu/en/ documents/scientific-guideline/ guideline-similar-biological-medicinal-products-containing-biotechnology-derived-proteins-active_en-2.pdf. Last accessed: September 2022.
- IQVIA. The impact of biosimilar competition in Europe. 2021. Available at: https://www.iqvia. com/-/media/iqvia/pdfs/library/ white-papers/the-impact-of-biosimilar-competition-in-europe-2021.pdf. Last accessed: 17 October 2022.
- Humphry N. The Rise of Anti-TNF Biosimilars: Guidelines, Real-World Evidence, and Challenges to Acceptance. EMJ Gastroenterol. 2022;11[Suppl 7]:2-10. https://doi.org/10.33590/emjgastroenterol/10106137.
- Danese S, Fiorino G, Raine T et al. ECCO position statement on the use of biosimilars for inflammatory bowel disease-an update. J Crohns Colitis. 2017;11:26-34.
- Cohen H, Blauvelt A, Rifkin RM et al. Switching reference medicines to biosimilars: a systematic literature review of clinical outcomes. Drugs. 2018;78:463-78.
- Massimi D, Barberio B, Bertani L et al. Switching from infliximab originator to SB2 biosimilar in inflammatory bowel diseases: a multicentric prospective real-life study. Ther Adv Gastroenterol. 2021;14:1-11.
- Trystram N, Abitbol V, Tannoury J et al. Outcomes after double switching from originator infliximab to biosimilar CT-P13 and biosimilar SB2 inpatients with inflammatory bowel disease: a 12-month prospective cohort study. Aliment Pharmacol Ther. 2021;53:887-99.
- Mahmmod S, Schultheiss JPD, van Bodegraven AA et al. Outcome of reverse switching from CT-P13 to originator infliximab in patients with inflammatory bowel disease. Inflamm Bowel Dis. 2021;27:1954- 62.
- Kaniewska M, Rosolowski M, Moniuzsko A et al. Biosimilar infliximab versus originator in Crohn’s disease anti-TNF-α naïve and non-naïve patients. Prz Gastroenterol. 2021;16:207-12.
- Morris GA, McNikol M, Boyle B et al. Increasing biosimilar utilization at a pediatric inflammatory bowel disease center and associated cost savings: show me the money. Inflamm Bowel Dis. 2022;28:531-8.
- Barberio B. Cingolani L, Canova C et al. A propensity score-weighted comparison between adalimumab originator and its biosimilars, ABP501 and SB5, in inflammatory bowel disease: a multicenter Italian study. Ther Adv Gastroenterol. 2021;14:175-82.
- Kurki P, Barry S., Bourges I et al. Safety, immunogenicity and interchangeability of biosimilar monoclonal antibodies and fusion proteins: a regulatory perspective. Drugs. 2021;81:1881-96.
- 3rd European Evidence-based Consensus on the Diagnosis and Management of Crohn"s Disease 2016: Part 1: Diagnosis and Medical Management. J Crohns Colitis. 2017 Jan;11(1):3-25. doi: 10.1093/ecco-jcc/jjw168. Epub 2016 Sep 22.
- Cordón JP, Arranz EM, Ramírez L, Arranz M. What is the best strategy after failure to anti-TNF? Ustekinumab or other anti-TNF? A. Cerpa Arencibia, C. Suarez Ferrer. Journal of Crohn s and Colitis. January 2020; 14 (Supplement_1):S554-S554.
- Stavem K. Switching from one reference biological to another in stable patients for non-medical reasons: a literature search and brief review. J Mark Access Health Policy. 2021; 9(1):1964792. Published online 2021 Aug 20. DOI: 10.1080/20016689.2021.1964792 https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8381978/
- Князев О.В., Звяглова М.Ю., Каграманова А.В. и соавт. Потеря ответа и частота нежелательных явлений у пациентов с язвенным колитом и болезнью Крона при переходе с оригинального препарата инфликсимаб на его биосимиляры. Терапевтический архив. 2021; 93 (2): 150–157. DOI: 10.26442/00403660.2021.02.200624.
- Gisbert J. P. et al. Meta‐analysis: the efficacy of azathioprine and mercaptopurine in ulcerative colitis //Alimentary pharmacology & therapeutics. – 2009. – Т. 30. – №. 2. – С. 126-137.
- Sood A. et al. Role of azathioprine in severe ulcerative colitis: one-year, placebo-controlled, randomized trial //Indian journal of gastroenterology: official journal of the Indian Society of Gastroenterology. – 2000. – Т. 19. – №. 1. – С. 14-16.
- Kuriyama M. et al. Tolerability and usefulness of mercaptopurine in azathioprine‐intolerant Japanese patients with ulcerative colitis //Digestive Endoscopy. – 2010. – Т. 22. – №. 4. – С. 289-296
- Meier J., Sturm A. Current treatment of ulcerative colitis //World journal of gastroenterology: WJG. – 2011. – Т. 17. – №. 27. – С. 3204.
- Ng S. C., Kamm M. A. Therapeutic strategies for the management of ulcerative colitis //Inflammatory bowel diseases. – 2009. – Т. 15. – №. 6. – С. 935-950
- Абдулхаков С. Р., Абдулхаков Р. А. Неспецифический язвенный колит: современные подходы к диагностике и лечению //Вестник современной клинической медицины. – 2009. – Т. 2. – №. 1. – С. 32-41.
- O. Petitjean, J. L. Wendling, M. Tod, et all/ Pharrnacokinetics and absolute rectal bioavaila bility of hydrocortisone acetate in distal colitis // Aliment. Pharmacol. Ther. (1992) 6, 35 1-357.
- Lloyd R. Sutherland. Topical Treatment of Ulcerative Colitis// Medical Clinics of North America-Vol.74, No. 1, January 1990
- Pleet J. L. et al. The use of pharmacological prophylaxis against venous thromboembolism in hospitalised patients with severe active ulcerative colitis //Alimentary pharmacology & therapeutics. – 2014. – Т. 39. – №. 9. – С. 940-948
- Sands B. E. et al. Ustekinumab as induction and maintenance therapy for ulcerative colitis //New England Journal of Medicine. – 2019. – Т. 381. – №. 13. – С. 1201-1214.
- Sandborn W. J. et al. Tofacitinib as induction and maintenance therapy for ulcerative colitis //New England Journal of Medicine. – 2017. – Т. 376. – №. 18. – С. 1723-1736.
- Gies N. et al. Treatment of ulcerative colitis with adalimumab or infliximab: long‐term follow‐up of a single‐centre cohort //Alimentary pharmacology & therapeutics. – 2010. – Т. 32. – №. 4. – С. 522-528.
- Gemayel N. C. et al. Dose escalation and switching of biologics in ulcerative colitis: a systematic literature review in real-world evidence //Current Medical Research and Opinion. – 2019. – Т. 35. – №. 11. – С. 1911-1923.
- Burr N. E. et al. Efficacy of biological therapies and small molecules in moderate to severe ulcerative colitis: systematic review and network meta-analysis //Gut. – 2022. – Т. 71. – №. 10. – С. 1976-1987.
- Travis S. P. L. et al. Once-daily budesonide MMX in active, mild-to-moderate ulcerative colitis: results from the randomised CORE II study //Gut. – 2014. – Т. 63. – №. 3. – С. 433-441.
- Panaccione R. et al. Dose Escalation Patterns of Advanced Therapies in Crohn’s Disease and Ulcerative Colitis: A Systematic Literature Review //Advances in Therapy. – 2023. – Т. 40. – №. 5. – С. 2051-2081.
- Sofia M. A., Rubin D. T. Current approaches for optimizing the benefit of biologic therapy in ulcerative colitis //Therapeutic advances in gastroenterology. – 2016. – Т. 9. – №. 4. – С. 548-559.
- Ferretti F. et al. An update on current pharmacotherapeutic options for the treatment of ulcerative colitis //Journal of Clinical Medicine. – 2022. – Т. 11. – №. 9. – С. 2302\
- Pleet J. L. et al. The use of pharmacological prophylaxis against venous thromboembolism in hospitalised patients with severe active ulcerative colitis //Alimentary pharmacology & therapeutics. – 2014. – Т. 39. – №. 9. – С. 940-948
- Christophorou D. et al. Systematic review with meta‐analysis: infliximab and immunosuppressant therapy vs. infliximab alone for active ulcerative colitis //Alimentary Pharmacology & Therapeutics. – 2015. – Т. 41. – №. 7. – С. 603-612
- Woolrich A. J., DaSilva M. D., Korelitz B. I. Surveillance in the routine management of ulcerative colitis: the predictive value of low-grade dysplasia //Gastroenterology. – 1992. – Т. 103. – №. 2. – С. 431-438.
- Gionchetti P. et al. Oral budesonide in the treatment of chronic refractory pouchitis //Alimentary pharmacology & therapeutics. – 2007. – Т. 25. – №. 10. – С. 1231-1236.
- Segal J. P. et al. Systematic review with meta‐analysis: the management of chronic refractory pouchitis with an evidence‐based treatment algorithm //Alimentary Pharmacology & Therapeutics. – 2017. – Т. 45. – №. 5. – С. 581-592.
- Khoo E. et al. Systematic Review and Meta-analysis of Immunomodulator and Biologic Therapies for Treatment of Chronic Pouchitis //medRxiv. – 2021. – С. 2021.01. 19.21250059
- Rao K., Higgins P. D. R. Epidemiology, diagnosis, and management of Clostridium difficile infection in patients with inflammatory bowel disease //Inflammatory bowel diseases. – 2016. – Т. 22. – №. 7. – С. 1744-1754.
- Silva J. et al. Treatment of Clostridium difficile colitis and diarrhea with vancomycin //The American Journal of Medicine. – 1981. – Т. 71. – №. 5. – С. 815-822.
- Nitzan O. et al. Clostridium difficile and inflammatory bowel disease: role in pathogenesis and implications in treatment //World journal of gastroenterology: WJG. – 2013. – Т. 19. – №. 43. – С. 7577.
- Bamba S. et al. Factors affecting the efficacy of cyclosporin A therapy for refractory ulcerative colitis //Journal of gastroenterology and hepatology. – 2010. – Т. 25. – №. 3. – С. 494-498.
- Papa A, Gerardi V, Marzo M, Felice C, Rapaccini GL, Gasbarrini A. Venous thromboembolism in patients with inflammatory bowel disease: focus on prevention and treatment. World J Gastroenterol. 2014 Mar 28;20(12):3173-9. doi: 10.3748/wjg.v20.i12.3173.
- Tinsley A, Naymagon S, Enomoto LM, Hollenbeak CS, Sands BE, Ullman TA. Rates of pharmacologic venous thromboembolism prophylaxis in hospitalized patients with active ulcerative colitis: results from a tertiary care center. J Crohns Colitis. 2013 Dec;7(12):e635-40. doi: 10.1016/j.crohns.2013.05.002
- Lightner AL, Sklow B, Click B, Regueiro M, McMichael JJ, Jia X, Vaidya P, Delaney CP, Cohen B, Wexner SD, Steele SR, Holubar SD. Venous Thromboembolism in Patients Admitted for IBD: An Enterprise-Wide Experience of 86,000 Hospital Encounters. Dis Colon Rectum. 2023 Mar 1;66(3):410-418. doi: 10.1097/DCR.0000000000002338
- Hiroshi N., (2022). Acute Severe Ulcerative Colitis: Optimal Strategies for Drug Therapy. Gut and Liver. 17. 10.5009/gnl220017.
- Singh S, Allegretti JR, Siddique SM, Terdiman JP. AGA Technical Review on the Management of Moderate to Severe Ulcerative Colitis. Gastroenterology. 2020 Apr;158(5):1465-1496.e17. doi: 10.1053/j.gastro.2020.01.007. Epub 2020 Jan 13. PMID: 31945351; PMCID: PMC7117094.
- Wenjie Xi , Zongwei Li , Rongrong Ren , Xiao-Yong Sai , Lihua Peng &Yunsheng Yang (2020): Effect of antibiotic therapy in patients with ulcerative colitis: a metaanalysis of randomized controlled trials, Scandinavian Journal of Gastroenterology, DOI:10.1080/00365521.2020.1858958
- Sehgal P. et al. Systematic review: safety of mesalazine in ulcerative colitis //Alimentary pharmacology & therapeutics. – 2018. – Т. 47. – №. 12. – С. 1597-1609.
- Sandborn W. J. et al. Efficacy of upadacitinib in a randomized trial of patients with active ulcerative colitis //Gastroenterology. – 2020. – Т. 158. – №. 8. – С. 2139-2149. e14. – 2В
- Samama MM, Cohen AT, Darmon JY, Desjardins L, Eldor A, Janbon C, Leizorovicz A, Nguyen H, Olsson CG, Turpie AG, Weisslinger N. A comparison of enoxaparin with placebo for the prevention of venous thromboembolism in acutely ill medical patients. Prophylaxis in Medical Patients with Enoxaparin Study Group. N Engl J Med. 1999 Sep 9;341(11):793-800. doi: 10.1056/NEJM199909093411103. PMID: 10477777.
- Gionchetti P. et al. Comparison of mesalazine suppositories in proctitis and distal proctosigmoiditis //Alimentary pharmacology & therapeutics. – 1997. – Т. 11. – №. 6. – С. 1053-1057.
- Д. Д. Тарасова, Л. Н. Шилова, М. В. Королeва, Современные аспекты терапии язвенного колита №2 2019 (74) - "Актуальные вопросы фармакотерапии в гастроэнтерологии. Стр. 28-32
- Marshall JK, Irvine EJ. Rectal corticosteroids versus alternative treatments in ulcerative colitis: a meta-analysis. Gut. 1997 Jun;40(6):775-81. doi: 10.1136/gut.40.6.775. PMID: 9245932; PMCID: PMC1027203.
- Truelove SC. Treatment of ulcerative colitis with local hydrocortisone. Br Med J. 1956 Dec 1;2(5004):1267-72. doi: 10.1136/bmj.2.5004.1267. PMID: 13374319; PMCID: PMC2036121.
- Turunen UM, Färkkilä MA, Hakala K, Seppälä K, Sivonen A, Ogren M, Vuoristo M, Valtonen VV, Miettinen TA. Long-term treatment of ulcerative colitis with ciprofloxacin: a prospective, double-blind, placebo-controlled study. Gastroenterology. 1998 Nov;115(5):1072-8. doi: 10.1016/s0016-5085(98)70076-9. PMID: 9797360.
- Rutter M. D. et al. Thirty-year analysis of a colonoscopic surveillance program for neoplasia in ulcerative colitis //Gastroenterology. – 2006. – Т. 130. – №. 4. – С. 1030-1038.
- Hata K. et al. Earlier surveillance colonoscopy programme improves survival in patients with ulcerative colitis associated colorectal cancer: results of a 23-year surveillance programme in the Japanese population //British journal of cancer. – 2003. – Т. 89. – №. 7. – С. 1232-1236.
- Taylor K., Gibson P. R. Conventional therapy of ulcerative colitis: corticosteroids //Crohn"s Disease and Ulcerative Colitis: From Epidemiology and Immunobiology to a Rational Diagnostic and Therapeutic Approach. – 2017. – С. 399-412.
- Clore J. N., Thurby-Hay L. Glucocorticoid-induced hyperglycemia //Endocrine practice. – 2009. – Т. 15. – №. 5. – С. 469-474.
- Shaye O. A. et al. Hepatotoxicity of 6-mercaptopurine (6-MP) and Azathioprine (AZA) in adult IBD patients //Official journal of the American College of Gastroenterology| ACG. – 2007. – Т. 102. – №. 11. – С. 2488-2494
Приложение А1. Состав рабочей группы по разработке и пересмотру клинических рекомендаций
|
№ |
Ф.И.О. |
Ученая степень |
Ученое звание |
Профессиональная ассоциация |
|
1. |
Абдулганиева Диана Ильдаровна |
Д.м.н. |
Профессор |
Российская гастроэнтерологическая ассоциация |
|
2. |
Алексеева Ольга Поликарповна |
Д.м.н. |
Профессор |
Российская гастроэнтерологическая ассоциация |
|
3. |
Ачкасов Сергей Иванович |
Д.м.н. |
Профессор, член-корр. РАН |
Ассоциация колопроктологов России |
|
4. |
Бакулин Игорь Геннадьевич |
Д.м.н. |
Профессор |
Ассоциация колопроктологов России |
|
5. |
Барышева Ольга Юрьевна |
Д.м.н. |
|
Российская гастроэнтерологическая ассоциация |
|
6. |
Белоусова Елена Александровна |
Д.м.н. |
Профессор |
Российская гастроэнтерологическая ассоциация |
|
7. |
Болихов Кирилл Валерьевич |
К.м.н. |
|
Ассоциация колопроктологов России |
|
8. |
Варданян Армен Восканович |
К.м.н. |
|
Ассоциация колопроктологов России |
|
9. |
Веселов Алексей Викторович |
|
|
Ассоциация колопроктологов России |
|
10. |
Веселов Виктор Владимирович |
Д.м.н. |
Профессор |
Ассоциация колопроктологов России |
|
11. |
Головенко Олег Владимирович |
Д.м.н. |
Профессор |
Российская гастроэнтерологическая ассоциация |
|
12. |
Губонина Ирина Владимировна |
К.м.н. |
Доцент |
Российская гастроэнтерологическая ассоциация |
|
13. |
Денисенко Валерий Ларионович |
Д.м.н. |
Профессор |
Ассоциация колопроктологов России |
|
14. |
Долгушина Анастасия Ильинична |
Д.м.н. |
Профессор |
Российская гастроэнтерологическая ассоциация |
|
15. |
Ивашкин Владимир Трофимович |
Д.м.н. |
Профессор, академик РАН |
Российская гастроэнтерологическая ассоциация |
|
16. |
Кашников Владимир Николаевич |
Д.м.н. |
Доцент |
Ассоциация колопроктологов России |
|
17. |
Князев Олег Владимирович |
Д.м.н. |
|
Российская гастроэнтерологическая ассоциация |
|
18. |
Костенко Николай Владимирович |
Д.м.н. |
Профессор |
Ассоциация колопроктологов России |
|
19. |
Лахин Александр Владимирович |
|
|
Ассоциация колопроктологов России |
|
20. |
Маев Игорь Вениаминович |
Д.м.н. |
Профессор, академик РАН |
Российская гастроэнтерологическая ассоциация |
|
21. |
Макарчук Павел Александрович |
К.м.н. |
|
Российская гастроэнтерологическая ассоциация |
|
22. |
Москалев Алексей Игоревич |
К.м.н. |
|
Ассоциация колопроктологов России |
|
23. |
Нанаева Бэлла Александровна |
К.м.н |
|
Ассоциация колопроктологов России |
|
24. |
Никитина Наталья Васильевна |
К.м.н. |
|
Российская гастроэнтерологическая ассоциация |
|
25. |
Одинцова Альфия Харисовна |
К.м.н |
|
Российская гастроэнтерологическая ассоциация |
|
26. |
Ощепков Андрей Владимирович |
К.м.н. |
|
Ассоциация колопроктологов России |
|
27. |
Павленко Владимир Васильевич |
Д.м.н. |
Профессор |
Российская гастроэнтерологическая ассоциация |
|
28. |
Полуэктова Елена Александровна |
Д.м.н. |
Профессор |
Российская гастроэнтерологическая ассоциация |
|
29. |
Решетов Игорь Владимирович |
Д.м.н. |
Профессор, академик РАН |
Ассоциация колопроктологов России |
|
30. |
Ситкин Станислав Игоревич |
К.м.н. |
Доцент |
Российская гастроэнтерологическая ассоциация |
|
31. |
Сушков Олег Иванович |
Д.м.н. |
|
Ассоциация колопроктологов России |
|
32. |
Тарасова Лариса Владимировна |
Д.м.н. |
Профессор |
Российская гастроэнтерологическая ассоциация |
|
33. |
Ткачев Александр Васильевич |
Д.м.н |
Профессор |
Российская гастроэнтерологическая ассоциация |
|
34. |
Тимербулатов Виль Мамилович |
Д.м.н. |
Профессор, член-корр. РАН |
Ассоциация колопроктологов России |
|
35. |
Успенская Юлия Борисовна |
Д.м.н. |
|
Российская гастроэнтерологическая ассоциация |
|
36. |
Фролов Сергей Алексеевич |
Д.м.н. |
Доцент |
Ассоциация колопроктологов России |
|
37. |
Хлынова Ольга Витальевна
|
Д.м.н. |
Профессор, член-корр. РАН |
Российская гастроэнтерологическая ассоциация |
|
38. |
Чашкова Елена Юрьевна |
К.м.н |
|
Ассоциация колопроктологов России |
|
39. |
Чеснокова Ольга Владимировна |
|
|
Российская гастроэнтерологическая ассоциация |
|
40. |
Шапина Марина Владимировна |
К.м.н. |
|
Ассоциация колопроктологов России |
|
41. |
Шелыгин Юрий Анатольевич |
Д.м.н. |
Профессор, академик РАН |
Ассоциация колопроктологов России |
|
42. |
Шептулин Аркадий Александрович |
Д.м.н. |
Профессор |
Российская гастроэнтерологическая ассоциация |
|
43. |
Шифрин Олег Самуилович |
Д.м.н. |
Профессор |
Российская гастроэнтерологическая ассоциация |
|
44. |
Шкурко Татьяна Всеволодовна |
К.м.н. |
|
Ассоциация колопроктологов России |
|
45. |
Щукина Оксана Борисовна |
Д.м.н. |
|
Российская гастроэнтерологическая ассоциация |
Конфликты интересов у всех перечисленных авторов отсутствуют.
Приложение А2. Методология разработки клинических рекомендаций
Целевая аудитория данных клинических рекомендаций:
1. Врачи -гастроэнтерологи
2. Врачи -колопроктологи
3. Врачи -хирурги
4. Врачи -терапевты
5. Врачи общей практики (семейные врачи)
6. Врачи -эндоскописты
В данных клинических рекомендациях все сведения ранжированы по уровню достоверности (доказательности) в зависимости от количества и качества исследований по данной проблеме.
Таблица П1. Шкала оценки уровней достоверности доказательств (УДД) для методов диагностики (диагностических вмешательств)
|
УДД |
Расшифровка |
|
1 |
Систематические обзоры исследований с контролем референсным методом или систематический обзор рандомизированных клинических исследований с применением мета-анализа |
|
2 |
Отдельные исследования с контролем референсным методом или отдельные рандомизированные клинические исследования и систематические обзоры исследований любого дизайна, за исключением рандомизированных клинических исследований с применением мета-анализа |
|
3 |
Исследования без последовательного контроля референсным методом или исследования с референсным методом, не являющимся независимым от исследуемого метода или нерандомизированные сравнительные исследования, в том числе когортные исследования |
|
4 |
Несравнительные исследования, описание клинического случая |
|
5 |
Имеется лишь обоснование механизма действия или мнение экспертов |
Таблица П2. Шкала оценки уровней достоверности доказательств (УДД) для методов профилактики, лечения и реабилитации (профилактических, лечебных, реабилитационных вмешательств)
|
УДД |
Расшифровка |
|
1 |
Систематический обзор рандомизированных клинических исследований с применением мета-анализа |
|
2 |
Отдельные рандомизированные клинические исследования и систематические обзоры исследований любого дизайна, за исключением рандомизированных клинических исследований, с применением мета-анализа |
|
3 |
Нерандомизированные сравнительные исследования, в том числе когортные исследования |
|
4 |
Несравнительные исследования, описание клинического случая или серии случаев, исследование «случай-контроль» |
|
5 |
Имеется лишь обоснование механизма действия вмешательства (доклинические исследования) или мнение экспертов |
Таблица П3. Шкала оценки уровней убедительности рекомендаций (УУР) для методов профилактики, лечения и реабилитации (профилактических, диагностических, лечебных, реабилитационных вмешательств)
|
УУР |
Расшифровка |
|
А |
Сильная рекомендация (все рассматриваемые критерии эффективности (исходы) являются важными, все исследования имеют высокое удовлетворительное методологическое качество, их выводы по интересующим исходам являются согласованными) |
|
В |
Условная рекомендация (не все рассматриваемые критерии эффективности (исходы) являются важными, не все исследования имеют высокое удовлетворительное методологическое качество и/или их выводы по интересующим исходам не являются согласованными) |
|
С |
Слабая рекомендация (отсутствие доказательств надлежащего качества (все рассматриваемые критерии эффективности (исходы) являются неважными, все исследования имеют низкое методологическое качество и их выводы по интересующим исходам не являются согласованными) |
Порядок обновления клинических рекомендаций
Механизм обновления клинических рекомендаций предусматривает систематическую актуализацию – не реже чем один раз в три года, а также при появлении новых данных с позиции доказательной медицины по вопросам диагностики, лечения, профилактики и реабилитации конкретных заболеваний, наличии обоснованных дополнений/замечаний к ранее утвержденным КР (клинических рекомендации), но не чаще 1 раз в 6 месяцев.
Приложение А3. Справочные материалы, включая соответствие показаний к применению и противопоказаний, способов применения и доз лекарственных препаратов, инструкции по применению лекарственного препарата
Данные клинические рекомендации разработаны с учетом следующих нормативных актов:
Приказу Министерства здравоохранения Российской Федерации от 02.04.2010 № 206н (ред. от 21.02.2020) «Об утверждении Порядка оказания медицинской помощи населению с заболеваниями толстой кишки, анального канала и промежности колопроктологического профиля»;
Приказу Министерства здравоохранения Российской Федерации № 906н от 12 ноября 2012г «Порядка оказания медицинской помощи населению по профилю «гастроэнтерология»;
Приказу Министерства здравоохранения Российской Федерации от 14.12.2021 № 1144н «Об утверждении стандарта медицинской помощи взрослым при язвенном колите (диагностика и лечение)»
Приложение Б. Алгоритмы действий врача
Рисунок 1. Алгоритм диагностической и лечебной тактики при язвенном колите
См.ПДФ
Приложение В. Информация для пациента
Язвенный колит (ЯК) – хроническое воспалительное заболевание, характеризующееся повторяющимися острыми обострениями, после которых следуют периоды ремиссии. Многочисленные исследования показывают, что без лечения у пациентов с ЯК существенно повышается риск колоректального рака и смертность. Несвоевременное и недостаточное лечение может привести к прогрессированию заболевания и не только нарастанию симптомов (диареи с кровью, болей в животе), но и к системным проявлениям: снижению массы тела, лихорадке, анемии. Тяжелое обострение язвенного колита представляет угрозу для жизни из-за риска перфорации (прободения) кишки и развития перитонита. Самое главное, что даже при слабо выраженных симптомах или их отсутствии в кишке может сохраняться воспаление. При неполноценном лечении это постоянное воспаление приводит к развитию колоректального рака, который при ЯК протекает особенно агрессивно. Только постоянная противовоспалительная терапия может уменьшить вероятность развития опухоли.
Язвенный колит – достаточно редкое заболевание, человек с этой болезнью должен по возможности наблюдаться у врача, специализирующегося на лечении именно данной патологии, и строго следовать его рекомендациям по длительной, нередко, пожизненной, лекарственной терапии. Ни уровень физической нагрузки, ни прием конкретных продуктов питания, не влияют на риск обострения язвенного колита так, как влияет на него нерегулярный прием лекарств и несвоевременное обращение к специалисту.
Приложение Г1-ГN. Шкалы оценки, вопросники и другие оценочные инструменты состояния пациента, приведенные в клинических рекомендациях
Нет
.
Рекомендуемые статьи
При эндоскопическом исследовании в случае бронхоэктазов в стадии ремиссии выявляется
частично диффузный бронхит I степени воспаления
Активируйте PUSH уведомления в браузер
Отключите PUSH уведомления в браузер
Содержание
Интернет магазин
Популярное
- О нас
- Правовые вопросы
- Политика
обработки персональных
данных EndoExpert.ru - Связаться с нами
- Стать партнером
© 2016-2022 EndoExpert.ru

Вы находитесь в разделе предназначенном только для специалистов (раздел для пациентов по ссылке). Пожалуйста, внимательно прочитайте полные условия использования и подтвердите, что Вы являетесь медицинским или фармацевтическим работником или студентом медицинского образовательного учреждения и подтверждаете своё понимание и согласие с тем, что применение рецептурных препаратов, обращение за той или иной медицинской услугой, равно как и ее выполнение, использование медицинских изделий, выбор метода профилактики, диагностики, лечения, медицинской реабилитации, равно как и их применение, возможны только после предварительной консультации со специалистом. Мы используем файлы cookie, чтобы предложить Вам лучший опыт взаимодействия. Файлы cookie позволяют адаптировать веб-сайты к вашим интересам и предпочтениям.
Я прочитал и настоящим принимаю вышеизложенное, хочу продолжить ознакомление с размещенной на данном сайте информацией для специалистов.


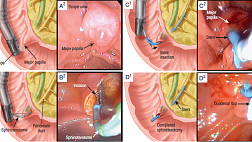












.jpg)





.png)


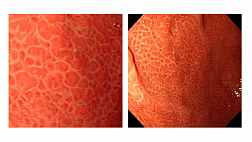














Комментарии