- Компании
- Takeda. О компании, буклеты, каталоги, контакты
- Olympus. О компании, буклеты, каталоги, контакты
- Boston Scientific. О компании, буклеты, каталоги, контакты
- Pentax. О компании, буклеты, каталоги, контакты
- Fujifilm & R-Farm. О компании, буклеты, каталоги, контакты
- Erbe. О компании, буклеты, каталоги, контакты
- Еще каталоги
- Мероприятия
- Информация
- Обучение
- Классификации
- Атлас
- Quiz
- Разделы
- Пациенту
QR-код этой страницы

Для продолжения изучения на мобильном устройстве ПРОСКАНИРУЙТЕ QR-код с помощью спец. программы или фотокамеры мобильного устройства
Документы и приказы: Гастрит и дуоденит у детей. Клинические рекомендации 2024 - 2026

Полный текст статьи:
Кодирование по Международной статистической классификации болезней и проблем, связанных со здоровьем:K29.0, K29.1, K29.3, K29.4, K29.5, K29.6, K29.7, K29.8, K29.9, K31.8
Год утверждения (частота пересмотра):2024
Возрастная категория:Дети
Пересмотр не позднее:2026
Разработчик клинической рекомендации
Союз педиатров России
Автономная некоммерческая организация "Общество детских гастроэнтерологов, гепатологов и нутрициологов"
Клинические рекомендации
Гастрит и дуоденит у детей
Кодирование по Международной статистической
классификации болезней и проблем, связанных со здоровьем:K29.0, K29.1, K29.3, K29.4, K29.5, K29.6, K29.7, K29.8, K29.9, K31.8
Год утверждения (частота пересмотра):2024
Возрастная категория:Дети
Пересмотр не позднее:2026
ID:837
Разработчик клинической рекомендации
· Союз педиатров России
· Автономная некоммерческая организация "Общество детских гастроэнтерологов, гепатологов и нутрициологов"
Одобрено Научно-практическим Советом Минздрава РФ
Оглавление
· Список сокращений
· Термины и определения
· 1. Краткая информация по заболеванию или состоянию (группы заболеваний или состояний)
· 1.1 Определение заболевания или состояния (группы заболеваний или состояний)
· 1.2 Этиология и патогенез заболевания или состояния (группы заболеваний или состояний)
· 1.3 Эпидемиология заболевания или состояния (группы заболеваний или состояний)
· 1.4 Особенности кодирования заболевания или состояния (группы заболеваний или состояний) по Международной статистической классификации болезней и проблем, связанных со здоровьем
· 1.5 Классификация заболевания или состояния (группы заболеваний или состояний)
· 1.6 Клиническая картина заболевания или состояния (группы заболеваний или состояний)
· 2. Диагностика заболевания или состояния (группы заболеваний или состояний) медицинские показания и противопоказания к применению методов диагностики
· 2.1 Жалобы и анамнез
· 2.2 Физикальное обследование
· 2.3 Лабораторные диагностические исследования
· 2.4 Инструментальные диагностические исследования
· 2.5 Иные диагностические исследования
· 3. Лечение, включая медикаментозную и немедикаментозную терапии, диетотерапию, обезболивание, медицинские показания и противопоказания к применению методов лечения
· 4. Медицинская реабилитация и санаторно-курортное лечение, медицинские показания и противопоказания к применению методов медицинской реабилитации, в том числе основанных на использовании природных лечебных факторов
· 5. Профилактика и диспансерное наблюдение, медицинские показания и противопоказания к применению методов профилактики
· 6. Организация оказания медицинской помощи
· 7. Дополнительная информация (в том числе факторы, влияющие на исход заболевания или состояния)
· Критерии оценки качества медицинской помощи
· Список литературы
· Приложение А1. Состав рабочей группы по разработке и пересмотру клинических рекомендаций
· Приложение А2. Методология разработки клинических рекомендаций
· Приложение А3. Справочные материалы, включая соответствие показаний к применению и противопоказаний, способов применения и доз лекарственных препаратов, инструкции по применению лекарственного препарата
· Приложение Б. Алгоритмы действий врача
· Приложение В. Информация для пациента
· Приложение Г1-ГN. Шкалы оценки, вопросники и другие оценочные инструменты состояния пациента, приведенные в клинических рекомендациях
Список сокращений
АИ – аутоиммунный гастрит
АМО** – амоксициллин**
В** – висмута трикалия дицитрат**
ВЭБ – Вирус Эпштейна-Барра
ГЭР – гастроэзофагеальный рефлюкс
ДПК – двенадцатиперстная кишка
ДЭР – дуоденогастральный рефлюкс
ИГХ – иммуногистохимия
ИПН – ингибиторы протонного насоса
КЛА** – кларитромицин**
ЛФК – лечебная физкультура (Лечебная физкультура при заболеваниях пищевода, желудка, двенадцатиперстной кишки)
МЕТ** – метронидазол**
НПВП – нестероидные противовоспалительные препараты
СОДПК – слизистая оболочка двенадцатиперстной кишки
СОЖ – слизистая оболочка желудка
Т – #тетрациклин
ФД – функциональная диспепсия
ХГ – хронический гастрит
ХД – хронический дуоденит
ЭГДС – эзофагогастродуоденоскопия
H. рylori – Helicobacter pylori
OLGA (система) – Operative Link for Gastritis Assessment (оперативная система оценки гастритов)
OLGIM (система) – Operating Link For Gastric Intestinal Metaplasia (оперативная система определения стадии, формы и степени поражения кишечной метаплазией)
Термины и определения
Гастрит – воспалительное заболевание слизистой оболочки желудка.
Дуоденит – воспалительное заболевание слизистой оболочки двенадцатиперстной кишки.
Хронический гастрит – это хроническое воспаление слизистой оболочки желудка, проявляющееся ее клеточной инфильтрацией, нарушением физиологической регенерации и, вследствие этого, атрофией железистого эпителия, кишечной метаплазией, расстройством секреторной, моторной и нередко инкреторной функции желудка.
Хронический дуоденит – заболевание, которое характеризуется хронической воспалительной инфильтрацией слизистой оболочки двенадцатиперстной кишки, желудочной метаплазией эпителия и нарушениями гистоархитектоники и в виде укорочения ворсинок и углубления крипт.
Helicobacter pylori (H.pylori) – подвижная, спирально или S-образно закрученная грамотрицательная бактерия, которая обладает способностью колонизировать слизистую оболочку желудка, а в отдельных случаях и слизистую оболочку двенадцатиперстной кишки, и вызывать их воспаление.
Эрадикация – комплексное лечение, направленное на уничтожение инфекции Helicobacter pylori (H.pylori)
Аутоиммунный гастрит – орган-специфическое хроническое прогрессирующее заболевание, сопровождающееся поражением тела и дна желудка, с развитием атрофии желез и гипохлоргидрии, заканчивающееся пернициозной анемией.
Функциональная диспепсия – это комплекс жалоб, включающий в себя боли, чувство жжения и переполнения в подложечной области после еды, раннее насыщение, которые отмечаются в течение 3 последних месяцев (при общей продолжительности не менее 6 месяцев) и, которые не могут быть объяснены органическими заболеваниями (язвенная болезнь, опухоли, и др.).
OLGA (система) (Operative Link for Gastritis Assessment – оперативная система оценки гастритов) – определяет стадию атрофии (%), степень воспаления (слабая, умеренная, выраженная).
OLGIM (система) (Operating Link For Gastric Intestinal Metaplasia – оперативная система определения стадии, формы и степени поражения кишечной метаплазией. Обе системы вместе оценивают риска развития рака желудка
1. Краткая информация по заболеванию или состоянию (группы заболеваний или состояний)
1.1 Определение заболевания или состояния (группы заболеваний или состояний)
Гастрит (gastritis; греч. gaster желудок + -itis воспаление) – поражение слизистой оболочки желудка с преимущественно воспалительными изменениями при остром развитии процесса и явлениями дисрегенерации, структурной перестройки с прогрессирующей атрофией ее при хроническом течении, сопровождающееся нарушением функций желудка и других систем организма [1]. Различают острый и хронический гастрит. Хронический гастрит составляет большую часть заболеваний желудка [1].
Хронический гастрит (ХГ) – это хроническое воспаление слизистой оболочки желудка (СОЖ) различной этиологии, проявляющееся клеточной инфильтрацией СОЖ, нарушением физиологической регенерации и вследствие этого атрофией железистого эпителия, кишечной метаплазией, расстройством секреторной, моторной и нередко инкреторной функции желудка [2].
Дуоденит – (duodenitis; лат. duodenum двенадцатиперстная кишка + -itis воспаление) – воспалительно-дистрофический процесс, захватывающий все слои стенки двенадцатиперстной кишки или ограничивающийся ее слизистой оболочкой. Различают также бульбит (bulbitis) – воспаление луковицы двенадцатиперстной кишки и оддит (odditis) – воспаление сфинктера общего желчного протока (Одди) – кольцевидной мышцы, охватывающей общий желчный проток перед выходом его в полость двенадцатиперстной кишки [3].
Хронический дуоденит (ХД) – заболевание, которое характеризуется хронической воспалительной инфильтрацией слизистой оболочки двенадцатиперстной кишки, желудочной метаплазией эпителия и нарушениями гистоархитектоники и в виде укорочения ворсинок и углубления крипт [2].
1.2 Этиология и патогенез заболевания или состояния (группы заболеваний или состояний)
Причины, способствующих развитию гастрита, разделяются на экзогенные и эндогенные. Экзогенные гастриты развиваются на фоне погрешностей в питании, курения, приема алкоголя, инфицирования H.pylori, а также других инфекционных заболеваний с поражением желудка, пищевых токсикоинфекций, раздражающего действия некоторых лекарств (салицилаты, нестероидные противовоспалительные препараты (НПВП), преднизолон, препараты наперстянки, хлорид калия, некоторые антибиотики, противотуберкулезные средства и др.), оказывающих неблагоприятное влияние на слизистую оболочку желудка, пищевой аллергии (на землянику, грибы и др.) и т.д. Роль аллергического фактора в этиологии хронического гастрита остается спорной. Участие пищевой аллергии в настоящее время считается доказанным лишь применительно к особой форме хронического гастрита – эозинофильному гастриту.
Эндогенные гастриты в зависимости от причины возникновения подразделяются на нервно-рефлекторные (патологическое рефлекторное воздействие других пораженных органов – кишечника, желчного пузыря, поджелудочной железы), гастрит, связанный с нарушениями вегетативной нервной системы и патологией эндокринных органов (гипофиз, надпочечники, щитовидная железа), гематогенный гастрит (при хронических инфекциях, нарушениях обмена веществ), гипоксемический гастрит (на фоне уменьшения кровотока в слизистой оболочке желудка, например, при ишемической болезни сердца и сосудов), элиминационный гастрит (связан с выделением через слизистую оболочку желудка различных токсических веществ. К этой группе относится, например, уремический гастрит, возникающий при выделении через стенку желудка конечных продуктов азотистого обмена у больных с хронической почечной болезнью продвинутых стадий).
Определенное место в этиологии хронического гастрита занимают и наследственные факторы, хотя их конкретная роль в возникновении заболевания изучена еще недостаточно.
Патогенез развития изменений при гастрите связан в первую очередь в нарушении равновесия между факторами защиты и агрессии в СОЖ, что приводит к формированию не только воспалительного процесса, но в последующем и к дисметаболическим, дисрегенераторным, дистрофическим и атрофическим процессам в слизистой оболочке желудка, которые в итоге способствуют развитию функциональной недостаточности органа. Независимо от причины, вызвавшей воспаление СОЖ, патологический процесс развивается по этапам широко известного каскада Correa: нормальная слизистая – поверхностный гастрит – хронический атрофический гастрит – метаплазия тонкокишечного типа – метаплазия толстокишечного типа – дисплазия – аденокарцинома [4]. Одним из основных этиологических факторов хронического гастрита считается H.pylori, признанный международным агентством по изучению рака канцерогеном первого порядка [5]. Микроб имеет более 40 генов патогенности, собранные в одном из его сегментов – «острове патогенности». Главным фактором патогенности считается высокомолекулярный белок CagA, продукция которого повышает риск развития атрофии в СОЖ в 3 раза [6, 7]. Помимо наличия CagA, риск развития рака желудка возрастает при инфицировании vacA, iceA, babA-позитивными штаммами [8]. Однако, даже при условии успешной эрадикации возбудителя у пациентов с хроническим гастритом далеко не всегда имеет место полное восстановление морфологии слизистой оболочки желудка. Маастрихтский консенсус III ввел термин «точка невозврата», после которой эрадикация H.pylori уже не дает существенного профилактического эффекта в отношении развития рака желудка [9]. Этой «точкой невозврата» считается наличие выраженной атрофии и кишечной метаплазии. В Маастрихтском консенсусе VI утверждается, что после успешной эрадикации H.pylori пациенты с высокой стадией (OLGA/OLGIM III-IV) гастрита и/или обширной эндоскопической атрофией по-прежнему подвержены риску развития рака желудка [10]. Для хронического гастрита у детей в 68% случаев характерно умеренно выраженное поверхностное воспаление с незначительной инфильтрацией, не сопровождающееся развитием атрофии [11]. Атрофические изменения СОЖ чаще встречаются во взрослом возрасте [12].
При инвазии H. pylori в слизистую оболочку желудка в ней развивается специфический воспалительный процесс (гастрит, дуоденит) с участием местных и гуморальных иммунных механизмов (фагоцитоз, бласт-транформация лимфоцитов, синтез иммуноглобулинов и др.), а также индуцируется локальный иммунный ответ, который проявляется не только в изменении уровня sIgA, но и сопровождается изменениями цитокинового (интерлейкинового) статуса [13, 14]. Обнаружение H.pylori в двенадцатиперстной кишке объясняется тем, что при гастритах с повышенной кислотностью приблизительно у 30% взрослых пациентов происходит метаплазия эпителия двенадцатиперстной кишки, а именно, замена его на эпителий, свойственный желудочному, что создает условия для заселения двенадцатиперстной кишки H.pylori [15]. Частота желудочной метаплазии увеличивается с возрастом: до 8 лет частота ЖМ составила 8%, от 8-12 лет – 25%, у детей старше 12 лет – 38% [16]
Патоморфологические данные, а также исследования с применением теста проницаемости сахарозы доказывают, что при гастритах и дуоденитах, как при любом хроническом воспалении пищеварительной трубки, имеет место синдром повышенной эпителиальной проницаемости, выраженность которого коррелирует с активностью воспалительного процесса в слизистой оболочке желудка. H.pylori вносит вклад в возникновение этот синдрома, оказывая негативное влияние на структурные компоненты плотных контактов эпителиоцитов [17].
Более чем у 90% населения присутствует другая инфекция – вирус Эпштейна-Барр (ВЭБ) Имеются исследования, показывающие триггерную роль этого вируса в развитии заболеваний верхнего отдела желудочно-кишечного тракта [18].
Важным этиологическим фактором ХГ, помимо Н.pylori, является аутоиммунное поражение СОЖ [19]. На долю его выявления в популяции приходится 15-18% случаев. АГ у детей явление редкое, чаще всего встречается у европейских женщин пожилого возраста. Но, тем не менее, в литературе описаны случаи выявления АГ в молодом возрасте [20]. Недостаточные знания по АГ у детей приводят к отсроченному времени постановки диагноза [19].
Этиология аутоиммунного гастрита до сих пор полностью не изучена. Среди инфекционных факторов, являющихся триггером аутоиммунного гастрита, безусловно, ведущее место отводится Helicobacter pylori, в геноме которого присутствуют цитотоксинассоциированные гены, способные вызывать различные выраженные патологические процессы в слизистой оболочке желудка, в том числе активацию онкогенных белков [21].
Патогенез АГ связан с образованием антител к H+/К+-АТФазе париетальных клеток СОЖ, к фактору Кастла и нарушением дифференциации эпителия и гибели париетальных клеток. Имеются убедительные доказательства в поддержку механизма молекулярной мимикрии между антигенами H.pylori и H+/К+-АТФазой париетальных клеток [22].
Тем не менее, единого мнения по вопросу роли H. pylori в развитии аутоиммунного гастрита пока не достигнуто. Однако большинством исследователей признается, что роль H.pylori в развитии аутоиммунного гастрита весьма незначительна. У взрослых антитела к париетальным клеткам были обнаружены только среди H.pylori-негативных пациентов [22, 23]. Показано, что у детей инфекция H.pylori может не играть роли в развитии аутоиммунного гастрита [24, 25].
Тригерную роль при аутоиммунном гастрите может играть также инфекция ВЭБ и ее сочетание с H.pylori [26].
В ряде случаев АГ сочетается с другими аутоиммунными заболеваниями (аутоиммунный тиреоидит, сахарный диабет I типа, витилиго и др.) [27, 28, 29]. Н.pylori может предшествовать АГ и играть ведущую роль в запуске аутоиммунных механизмов за счет перекрестной реактивности между антигенами микроорганизма и Н+К+/АТФазой париетальных клеток [30].
Вследствие разрушения париетальных клеток нарушается образование как соляной кислоты, так и внутреннего фактора Кастла, что ведет за собой нарушение всасывания железа с развитием железодефицитной анемии, и всасывания витамина В12 с последующим нарушением эритропоэза и развитием пернициозной анемии. Пернициозная анемия – не единственный симптом заболевания. Витамин В12 также имеет решающее значение в производстве миелина, недостаток которого приводит к таким неврологическим расстройствам как онемение, парестезии, слабость и атаксия, которые могут предшествовать анемии, злокачественная ассоциативная дегенерация спинного мозга [25, 31].
Необходимо концентрировать внимание на том, что заболевание развивается медленно, в течение многих лет. Антитела должны быть стойкими и содержаться в достаточной концентрации, чтобы вместе с аутореактивными T-клетками CD4+ желудка вызвать местную реакцию и способствовать атрофии слизистой оболочки и разрушению париетальных клеток [25]. До настоящего времени четко не определена динамика концентрации антител к париетальным клеткам в зависимости от времени и патологии заболевания. Однако у больных с тяжелым течением аутоиммунного гастрита исчезновение источника антигена вследствие выраженной атрофии слизистой оболочки приводит к снижению титра антител. Примечательно, что антитела к париетальным клеткам желудка присутствуют также у 2,5–9% здоровых взрослых людей [32].
Особые формы гастрита встречаются реже, характеризуются специальными этиологическими факторами или могут сопровождать другие заболевания. Лимфоцитарный гастрит может быть связан с глютеновой энтеропатией, эозинофильный гастрит протекает в рамках эозинофильного гастроэнтерита, гранулематозный гастрит ассоциируют с болезнью Крона, саркоидозом, васкулитами [34].
Дуоденит является гетерогенным заболеванием, вызываемым инфекционными агентами (Н.pylori, микобактерии, Tropheryma whipplei, грибы рода Candida, паразиты: лямблии, анкилостома, анизокидоз; Strongyloides, вирусы, в т.ч. цитомегаловирусы и герпесвирусы), экзогенными воздействиями (алкоголь, химические агенты, радиация, лекарства), другими заболеваниями (Болезнь Крона, саркоидоз, васкулит, пурпура Шенляйн-Геноха, целиакия) [35, 36].
К факторам риска ХД относят также нарушения режима питания, еду всухомятку, употребление грубой, острой, раздражающей слизистую оболочку пищи, интолерантность к отдельным пищевым продуктам. Из лекарственных средств наиболее неблагоприятное влияние оказывают аспирин, преднизолон, нестероидные противовоспалительные препараты при длительном приеме [37]. Употребление алкогольных напитков, особенно крепких, и табакокурение оказывают как непосредственное отрицательное влияние на слизистую оболочку двенадцатиперстной кишки, так и нарушают нейрогуморальные механизмы регуляции процессов репарации, эти факторы наиболее типичны для взрослых, но встречаются и у подростков [38]. Нельзя исключить значение хронического психоэмоционального стресса, нарушающего механизмы, регулирующие морфофункциональное состояние гастродуоденальной зоны [37]. Часто у больных имеет место сочетание нескольких этиологических факторов [39]. Определить этиологический фактор в каждом конкретном случае весьма трудно, поскольку дуоденит и сопутствующие заболевания часто имеют общие факторы риска, а в процессе течения взаимоотягощают друг друга [37].
Хронический дуоденит подразделяют на первичный (изолированный), который встречается редко и вторичный, который рассматривается как сопутствующая патология или осложнение основного заболевания. Хронический вторичный дуоденит наблюдается при язвенной болезни, гастрите, патологии поджелудочной железы, желчевыводящих путей, печени. Патогенез первичного хронического дуоденита не известен. При вторичном ХД разнообразная этиология логично предполагает различия в патогенезе заболевания, однако установлено, что действие этиологических факторов в слизистой оболочке двенадцатиперстной кишки нередко вызывает однотипные морфофункциональные изменения [40]. В патогенезе выделяют пусковой механизм, общие и местные патогенетические реакции. Пусковой механизм связан с непосредственным влиянием агрессивных факторов на слизистую оболочку двенадцатиперстной кишки (СОДПК). Одним из основных этиологических факторов вторичного хронического дуоденита является Н.pylori. Хронический дуоденит развивается, как правило, на фоне хронического гастрита, ассоциированного с Н.pylori, и метаплазии желудочного эпителия в двенадцатиперстной кишке. Очаги метаплазированного эпителия легко повреждаются кислым желудочным содержимым, и в участках метаплазии развиваются эрозии. Дуоденит, обусловленный Н.pylori, как правило, локализуется в луковице двенадцатиперстной кишки [41]. При хроническом гепатите и хроническом панкреатите развитие хронического дуоденита обусловлено повышенной абсорбцией панкреатических ферментов; снижением секреции бикарбонатов, что способствует закислению дуоденального содержимого и действию агрессивных факторов желудочного сока; сниженной резистентностью слизистой оболочки двенадцатиперстной кишки; при заболеваниях легких и сердечно-сосудистой системы развитию хронического дуоденита способствует гипоксия слизистой оболочки двенадцатиперстной кишки [41]. В развитии хронического дуоденита при заболеваниях желчевыводящих путей важную роль играет кишечная микрофлора. Особенно большую роль играет этот фактор при желудочной ахилии. В этих условиях легко развивается дисбактериоз; проксимальные отделы тонкой кишки, включая двенадцатиперстную кишку, заселяет необычная для этих отделов бактериальная флора [42, 43, 44].
Местные механизмы патогенеза хронического дуоденита включают нарушения региональной микроциркуляции, которые приводят к дистрофическим, некротическим и воспалительно-эрозивным поражениям слизистой оболочки двенадцатиперстной кишки, нарушению процессов репарации, включая дифференцировку железистых структур, развитию атрофии и секреторной недостаточности. В области микроциркуляторных расстройств в пораженной ткани появляется нейтрофильная и лимфоплазмоцитарная инфильтрация, возникает иммуновоспалительная реакция, которая при хроническом течении болезни может приобретать аутоиммунный характер.
1.3 Эпидемиология заболевания или состояния (группы заболеваний или состояний)
Распространенность ХГ и ХД в детской популяции точно не установлена, учитывая отсутствие эпидемиологических морфологических исследований. Приводимые в литературе данные основаны на обследовании детей с хроническим гастритом или функциональной диспепсией. По имеющимся данным, доля ХГ среди детей младшего школьного возраста составляет 45%, среди детей среднего школьного возраста 73% и 65% – среди старших школьников, ХГ часто сочетается с дуоденитом, в изолированном виде встречается лишь у 10-15% детей [45, 46].
Исследования распространенности инфекции Н.pylori как одного из важных этиологических факторов развития ХГ среди детей показывают достаточно высокую распространенность H.pylori у детей в 1990-е годы и ее значительное снижение в последнее время. В течение почти двух десятилетий – с 1996 по 2014 г. – в Сибири исследовалась популяция школьников 14-17 лет. За этот период было обследовано 684 ребенка, выявлено снижение распространенности инфекции: в 1996 г. – 62,5%, в 1999 г. – 56,2%, в 2009 г. – 50%, в 2014 г. – 45,1% [47, 48]. В конце 1990-х – начале 2000-х годов в Санкт-Петербурге серологическим методом было проведено обследование детей на H.pylori. В 1995 г. в группе 307 детей в возрасте 2-19 лет распространенность инфекции составила 44%, а в 2005 г. среди детей этой же возрастной группы – 31% [49].
В 2007-2011 гг. также в Санкт-Петербурге проводилось обследование 860 детей 0-17 лет с помощью тест-систем ИФА DRG (Германия) и «ГастроПанель» Biohit (Финляндия). Антитела были обнаружены в 48,95% случаев [50]. В 2017-2018 гг. в Рязани было обследовано 24 ребенка 4-16 лет: серопозитивными оказались 20,8% обследованных [51].
Дуоденит является одним из самых распространенных, если не самым распространенным, заболеванием двенадцатиперстной кишки, а вместе с гастритом – и всего желудочно-кишечного тракта. Гистологическими исследованиями установлено, что у 100% детей с клиническими признаками функциональной диспепсии регистрируется воспалительный процесс в слизистой оболочке двенадцатиперстной кишки различной степени [52]. Среди больных диспепсическим синдромом морфологические признаки острого дуоденита выявляются у 1,5% обследованных, а хронического у 25,6% [45, 53]. По некоторым данным, частота хронического дуоденита при хроническом гастрите (ХГ) также высока и составляет от 75% до 100% [55].
1.4 Особенности кодирования заболевания или состояния (группы заболеваний или состояний) по Международной статистической классификации болезней и проблем, связанных со здоровьем
К29 Гастрит и дуоденит
K29.0 – Острый геморрагический гастрит
K29.1 – Другие острые гастриты
K29.3 – Хронический поверхностный гастрит
K29.4 – Хронический атрофический гастрит
K29.5 – Хронический гастрит неуточненный
K29.6 – Другие гастриты (гипертрофический гигантский, гранулематозный, болезнь Менетрие)
K29.7 – Гастрит неуточненный
K29.8 – Дуоденит
K29.9 – Гастродуоденит неуточненный
K31.8 – Другие уточненные болезни желудка и двенадцатиперстной кишки
1.5 Классификация заболевания или состояния (группы заболеваний или состояний)
Существует несколько классификаций ХГ и ХД. В 1984 году А.В. Мазурин с соавторами разработал классификацию ХГ, которая принята за основу и используется в отечественной педиатрической практике по настоящее время. Постоянно обновляющиеся данные в связи с большим количеством исследований, выполненных с момента открытия Н.pylori в 1983 году, требуют обновления рекомендаций для практической работы врачей терапевтов, гастроэнтерологов, педиатров, врачей общей практики. Как российские, так и международные классификации претерпевают изменения в соответствии с полученными результатами. Классификация А.В. Мазурина была пересмотрена и дополнена Союзом педиатров РФ в 2002 г (табл. 1) [45, 54, 55].
Таблица 1
Классификация хронического гастрита и дуоденита [45, 54, 55]
|
Происхождение |
Первичный (экзогенный) |
|
|
Вторичный (эндогенный) |
|
Этиологический фактор |
Инфекционный: - Нelicobacter pylori - другие бактерии, вирусы, грибы Токсический реактивный (химический, радиационный, лекарственный, стрессовый, алиментарный) |
|
Аутоиммунный (при болезни Крона, гранулематозе, целиакии, саркоидозе, системных заболеваниях и др.) | |
|
Топография |
Гастрит: - антральный - фундальный - пангастрит Дуоденит: - бульбит - постбульбарный - пандуоденит Гастродуоденит |
|
Формы поражения желудка и двенадцатиперстной кишки (эндоскопические) |
Эритематозный/экссудативный Нодулярный Эрозивный (с плоскими или приподнятыми дефектами) Геморрагический |
|
Формы поражения желудка и двенадцатиперстной кишки (морфологические) |
По глубине поражения: - поверхностный - диффузный По характеру поражения: - с оценкой степени воспаления, активности, атрофии, кишечной метаплазии |
|
Периоды заболевания |
Обострение Неполная клиническая ремиссия Полная клиническая ремиссия Клинико-эндоскопическая ремиссия Клинико-эндоскопически-морфологическая ремиссия |
|
Характер кислотной продукции желудка |
Повышенная Неизмененная Пониженная |
В зарубежной практике с 1990 г. пользовались Сиднейской системой классификации, модифицированной в 1996 г.
С 2006 г. диагноз ХГ принято считать исключительно морфологическим. В связи с этим в 2008 г. в помощь Сиднейской классификации разработана система гистологической оценки гастрита – на основании оценки гистологических признаков выраженности воспаления и атрофии в антральном отделе (3 биоптата) и теле желудка (2 биоптата) под названием OLGA (Орегаtive Link for Gastritis Assessment) с определением степеней (выраженность воспалительной инфильтрации) и стадий (выраженность атрофии) ХГ, которую используют в отношении взрослых в настоящее время. Принятой отдельной гистологической классификации ХГ в международной педиатрической практике нет [57].
В 2015 г. принят Киотский глобальный консенсус по ведению Н.pylori-ассоциированного гастрита, который актуализировал имеющуюся информацию и обновил ее через призму рисков развития рака желудка для взрослых пациентов [34].
В 2010 году А.И. Хавкиным и Г.В. Волынец предложена рабочая классификация ХГ у детей, с дополнениями к уже существующей классификации А.В. Мазурина (табл. 4) [45, 54, 55]. В настоящий момент эта классификация проходит научную апробацию и обсуждение. Учитывая расширенную этиологическую характеристику ХГ, представленную в данной классификации, возможно, в будущем, она станет ведущей классификацией ХГ.
На сегодня, для практического использования следует применять классификацию А.В. Мазурина, пересмотренную и дополненную Союзом педиатров РФ в 2002 г.
Этиологическое разнообразие ХД представлено в классификации, предложенной экспертным советом Киотского консенсуса [34] (табл. 5).
Таблица 5
Классификация форм дуоденита, основанная на этиологическом принципе (Киотский консенсус)
|
|
|
1.Инфекционный дуоденит H-pylory-ассоциированный Обусловленный другими бактериями: -Микобактериальный -Обусловленный Tropheryma whipplei (болезнь Уипла) Флегмонозный Грибковый (дуоденальный кандидоз) Паразитарный: -Анкилостомитозный -Анизокидозный -Лямблиозный -Обусловленный Strongyloides Вирусный: -Цитомегаловирусный -Герпетический |
|
2.Дуоденит, обусловленный экзогенными воздействиями: Алкогольный Химический Радиационный Обусловленный другими экзогенными воздействиями Лекарственно-индуцированный |
|
3.Дуоденит специфической этиологии Аллергический Эозинофильный Лимфоцитарный |
|
4.Дуоденит, обусловленный другими заболеваниями: Болезнью Крона Саркоидозом Васкулитом Пурпурой Шенлейна-Геноха Целиакией |
В педиатрической литературе чаще всего описывается дуоденит при хроническом гастрите, ассоциированном с H.pylori [58-61], что, связано с ведущей роли хеликобактерной инфекции в этиологии хронического дуоденита; при лямблиозе [62, 63] и сочетании этих двух этиологических факторов [60]; дуодениты при инфицировании вирусами герпетической группы [64].
Помимо этиологического, существуют еще несколько подходов к классификации дуоденитов. Различают острый и хронический дуоденит [65]. В «Сиднейской системе» классификации хронического гастрита, принятой в 1990 году на IX Международном конгрессе гастроэнтерологов, диагностика ХД отражена в разделе эндоскопических исследований [66].
В разделе эндоскопических исследований приводятся следующие варианты:
- эритематозный дуоденит (по наличию гиперемии слизистой двенадцатиперстной кишки);
- эрозивный дуоденит (по наличию поверхностных дефектов слизистой оболочки);
- геморрагический дуоденит (при геморрагических проявлениях);
- атрофический дуоденит (признаки атрофии слизистой);
- узелковый, или нодулярный дуоденит (при визуально регистрируемых фолликулярных образованиях) [67, 68].
Более подробная классификация дуоденитов по эндоскопической картине представлена в таблице 6 [55, 68].
Таблица 6
Классификация дуоденитов по эндоскопической картине
|
Эндоскопические термины |
Характеристика дуоденитов | |
|
|
Эндоскопическая |
Топографическая |
|
Гиперемия Геморрагии Атрофия Эрозии Фолликулы |
Эритематозный Геморрагический Атрофический Эрозивный Нодулярный (узловой) |
Проксимальный (бульбит) Дистальный (постбульбарный) Локальный (папиллит) Диффузный (тотальный) |
ХД является диагнозом морфологическим. М.Р. Конорев и соавт. (2003) предлагают морфологически выделять следующие виды ХД [68]:
· неатрофические;
· атрофические;
· хеликобактерные;
· нодулярные;
· гранулематозные;
· эозинофильные;
· лимфоцитарные.
1.6 Клиническая картина заболевания или состояния (группы заболеваний или состояний)
ХГ как диагноз морфологический не имеет специфического клинического эквивалента, у большинства детей симптомы отсутствуют.
В Киотском консенсусе отмечено, что инфекция Н.pylori сама по себе может приводить к появлению симптоматики у части больных с диспепсией. В связи с этим, если у Н.pylori-инфицированного пациента с диспепсией при отсутствии морфологических изменений со стороны СОЖ после эрадикационной терапии отмечается стойкое улучшение симптоматики (в течение 6-12 месяцев), то таких пациентов рассматривают как имеющих Н.pylori-ассоциированную диспепсию. В других случаях их рассматривают как пациентов с ФД, требующих другого лечения [34].
К общим проявлениям хронического гастрита у детей относятся слабость, раздражительность, нарушения со стороны сердечно-сосудистой системы – кардиалгия, аритмия; у пациентов с атрофическим хроническим гастритом может развиться симптомокомплекс, схожий с демпинг-синдромом (внезапная слабость, бледность, потливость, сонливость, возникающие вскоре после еды), иногда сочетающихся с расстройствами кишечника, с императивным позывом к стулу. Существует отдельная категория симптомов, которые называются симптомами «тревоги». У детей следует обращать внимание на появление дисфагии, рецидивирующей рвоты, рвоты с кровью, мелены, рецидивирующих диарей, задержка физического и полового развития, длительное повышение температуры. При выявлении этих признаков необходимо расширенное обследование для исключения тяжелой органической патологии желудочно-кишечного тракта, в том числе эрозивного гастрита и дуоденита.
К осложнениям ХГ относят развитие гиповитаминозов, анемий, панкреатитов. При эрозивных поражениях могут возникать кровотечения. Так как в большинстве случаев имеет место сочетание ХГ и ХД, трудно выделить четкие диагностические симптомы изолированного дуоденита [59]. Наиболее типичными симптомами ХД являются – ноющая боль в эпигастрии и околопупочноной областях с ощущением тяжести, распиранием в подложечной области, чувством тошноты и саливацией. Очень часто в пубертатном периоде появляются вегетососудистые расстройства – слабость, потливость, головные боли, головокружения [71].
Осложнения хронического дуоденита достаточно многообразны. К ним относятся [72]:
· Патологический дуоденогастральный рефлюкс: возникает вследствие дискинезии и дуоденостаза, недостаточности пилорического сфинктера, способствует развитию антрального хронического гастрита.
· Дуоденостаз: обусловлен дистрофическими процессами в стенке кишки и нарушением функции энтеральной нервной системы. Приводит к застою и брожению пищевых масс, поступающих из желудка, развитию интоксикации.
· Синдром избыточного бактериального роста: связан с воспалительно-эрозивными изменениями слизистой оболочки двенадцатиперстной кишки, дуоденостазом, нарушением желудочного и дуоденального пищеварения.
· Кишечные кровотечения: чаще возникают при эрозивно-геморрагическом дуодените, редко бывают обильными и приводят к выраженной анемии. Они наблюдаются в различные сроки у 19-25% больных ХД.
· Папиллит: возникает вследствие выраженного воспалительного процесса в области большого дуоденального соска, может приводить к его стенозированию, развитию механической желтухи и холангита.
· Перидуоденит: характеризуется выраженным воспалительным процессом всей стенки двенадцатиперстной кишки, нередко переходящим на прилежащие ткани. Возникает при распространенном эрозивном процессе и папиллите.
· Деформация двенадцатиперстной кишки: является следствием выраженного воспалительно-эрозивного процесса, папиллита.
· Демпинг-синдром: чаще встречается при сочетании дуоденита с язвенной болезнью и хроническим гастритом, наличием у больных ваготонии, ускоренной эвакуации пищевых масс в тонкий кишечник, неадекватном выделении инсулина, недостаточном расщеплении крахмала амилазой панкреатического сока, возникновении гипогликемии, вегетососудистых параксизмов парасимпатического типа.
У детей раннего возраста ХГ и ХД встречаются редко и связаны в первую очередь с другими заболеваниями: целиакией, инфекционными энтеритами и др. Частота регистрации атрофических процессов в СОЖ и СОДПК напрямую зависит от возраста пациентов [73].
2. Диагностика заболевания или состояния (группы заболеваний или состояний) медицинские показания и противопоказания к применению методов диагностики
Критерии установления диагноза/состояния:
Диагноз хронического гастрита и хронического дуоденита – это диагноз морфологический, он основан на выявлении гистологических признаков воспаления слизистой оболочки желудка и/или двенадцатиперстной кишки (лимфоцитарная и нейтрофильная инфильтрация, а также атрофия, кишечная метаплазия и дисплазия). Дополнительные диагностические критерии – объективные изменения, характерные для воспаления слизистой оболочки желудка, выявленные при проведении эндоскопического исследования, (нодулярная гиперплазия и эрозивные изменения). Положительные результаты тестов для выявления H. pylori позволяют установить этиологию гастрита, т.к. данный микроорганизм является важным этиологическим фактором развития воспаления СОЖ [57].
2.1 Жалобы и анамнез
Возможные жалобы у пациентов с гастритом и дуоденитом и их интерпретация представлены в подразделе 1.6. Необходимо обратить внимание на наличие или отсутствие симптомов «тревоги»: постоянная боль в правом верхнем или правом нижнем квадранте, дисфагия, одинофагия, постоянная рвота, признаки желудочно-кишечного кровотечения, непроизвольная потеря массы тела, замедление роста, задержка полового созревания, необъяснимая лихорадка и наличие в семейном анамнезе воспалительных заболеваний кишечника, целиакии или язвенной болезни [74].
При сборе анамнеза следует уточнить, была ли ранее проведена пациенту ЭГДС с биопсией; имелись ли при этом указания на наличие воспалительных изменений слизистой оболочки желудка и двенадцатиперстной кишки, а также атрофии, кишечной метаплазии, эпителиальной дисплазии). Важно уточнить, выявлялась ли ранее инфекция H.pylori, была ли ранее проведена эрадикационная терапия, с помощью какой схемы лечения, проведен ли контроль эффективности эрадикационной терапии.
При подозрении на наличие аутоиммунного гастрита важны указания в анамнезе на наличие других аутоиммунных заболеваний, выявленную ранее атрофию слизистой оболочки тела желудка при относительно сохранной слизистой оболочке антрального отдела, антител к париетальным клеткам желудка и антител к фактору Кастла.
Клинически аутоиммунный гастрит часто ассоциируется с другими аутоиммунными заболеваниями, такими как аутоиммунный тиреоидит, синдром Шегрена и сахарный диабет 1-го типа, поэтому может считаться системным заболеванием. В частности, известны осложнения аутоиммунного тиреоидита, отнесенные к категории 3В полигландулярного аутоиммунного синдрома [25]. Однако аутоиммунный гастрит может быть и самостоятельным заболеванием, не связанным с другими иммунопатологическими процессами.
Клиническая картина аутоиммунного гастрита у детей не связана с какими-либо специфическими признаками или симптомами, характерными для заболеваний желудочно-кишечного тракта [25, 32].
У детей, как и у взрослых, абдоминальные боли более характерны для неаутоиммунного гастрита. Болевой синдром при аутоиммунном гастрите (если имеется) характеризуется длительными болями в животе, которые носят ноющий характер и не имеют определенной локализации. Из диспепсических проявлений для аутоиммунного гастрита по сравнению с неаутоиммунным гастритом более характерны изжога, ощущение горечи и/или кислоты во рту, что специфично для гастроэзофагеальных рефлюксов, а также метеоризм, который свидетельствует о нарушении пищеварения. Однако при аутоиммунном гастрите у детей по сравнению с детьми, имеющими неаутоиммунный гастрит, чаще отмечается синдром хронической неспецифической интоксикации, характеризующийся субфебрилитетом и/или эпизодическими кратковременными немотивированными подъемами температуры тела до фебрильной, а также лимфаденопатией с увеличением преимущественно передне- и/или заднешейной группы лимфатических узлов, может быть гепатолиенальный синдром (табл. 1) [75]. Показатели красной крови у 86,2% детей с аутоиммунным гастритом остаются в пределах возрастной нормы. У 13,8% пациентов отмечается железодефицитная анемия легкой степени. Другой, характерный для взрослых, симптом аутоиммунного гастрита – витамин В12-дефицитная анемия – практически отсутствует у детей [32]. Вероятно, это связано с тем, что пернициозная анемия развивается преимущественно при атрофическом гастрите, развивающемся в более старшем, а часто – в пожилом возрасте, тогда как у детей аутоиммунный гастрит имеет доатрофическую стадию [75].
2.2 Физикальное обследование
Физикальное обследование включает в себя поверхностную и глубокую пальпацию живота (пальпация при заболеваниях пищевода, желудка, двенадцатиперстной кишки), при которой можно выявить болезненность в эпигастральной области, оценку симптомов раздражения брюшины (пальпация при заболеваниях пищевода, желудка, двенадцатиперстной кишки), что важно при выраженном абдоминальном болевом синдроме; перкуссию печени (перкуссия при заболеваниях печени и желчевыводящих путей) для исключения сопутствующей гепатомегалии; аускультацию (аускультация при заболеваниях пищевода, желудка, двенадцатиперстной кишки) для оценки перистальтики пищеварительной трубки.
При физикальном обследовании патогномоничных данных для гастрита и дуоденита нет.
2.3 Лабораторные диагностические исследования
Патогномоничных для гастрита и дуоденита лабораторных маркеров нет. Лабораторные исследования детям проводятся для исключения/подтверждения осложнений, а также с целью онкопревенции у детей старшей подростковой группы.
· Пациентам с гастритом и дуоденитом рекомендуется выполнение общего (клинического) анализа крови развернутого с определением уровня гемоглобина, гематокрита, эритроцитов, цветового показателя, тромбоцитов, лейкоцитов с лейкоцитарной формулой, с целью подтверждения/исключения анемии из-за кровотечения при эрозивном поражении слизистой оболочки гастродуоденальной области, а также анемии как последствия аутоиммунного гастрита [76-80].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: лейкоцитоз может свидетельствовать об инфекционной этиологии заболевания, микроцитарная анемия свидетельствует о скрытых кровопотерях или нарушении всасывания железа, макроцитарная анемия развивается вследствие дефицита витамина В12 при аутоиммунном поражении желудка [76-80]. Исследование проводится в процессе динамического наблюдения, частота назначения определяется клинической ситуацией и выявленными изменениями.
При выявлении анемии диагностика и лечение проводится согласно соответствующим клиническим рекомендациям.
· Всем пациентам с подозрением на аутоиммунный гастрит рекомендуется определение содержания антител к антигенам желудка в крови (антитела к париетальным клеткам желудка) для подтверждения или исключения диагноза [81-85].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Комментарии: Антитела к париетальным клеткам являются эффективным инструментом для скрининга аутоиммунного атрофического гастрита и злокачественной пернициозной анемии. Мишенью для антител к париетальным клеткам является H+/K+ АТФ-аза, при этом данный вид антител нацелен как на альфа-, так и на бета-субъединицы протонного насоса, хотя основным антигеном является альфа-субъединица. Антитела к париетальным клеткам можно обнаружить у 85-90% пациентов с пернициозной анемией, а также у 20,7% пациентов с инфекцией Helicobacter pylori, которая считается одним из возможных возбудителей АГ. Чувствительность определения антител к париетальным клеткам для диагноза аутоиммунного гастрита составляет ~80%, специфичность низкая (обнаруживаются у лиц без аутоиммунного гастрита: встречаются в сыворотке крови пациентов с сахарным диабетом 1 типа, аутоиммунными заболеваниями щитовидной железы, витилиго, целиакией). Антитела к внутреннему фактору Кастла блокируют связывание кобаламина с внутренним фактором. Чувствительность для диагностики аутоиммунного гастрита ~50%, но специфичность достигает 99% [81-86].
Опубликованы случаи сочетания аутоиммунного гастрита с аутоиммунным тиреоидитом, диабетом 1 типа, ревматологическими заболеваниями, иммунодефицитными состояниями, в связи с чем пациентам с аутоиммунным гастритом следует назначить консультации специалистов и обследование согласно соответствующим клиническим рекомендациям [20, 188, 189.].
· Пациентам с гастритом и дуоденитом, у которых выявлена анемия/дефицит железа рекомендовано селективное проведение исследования кала на скрытую кровь с целью диагностики скрытого кровотечения и последующего выбора объема эндоскопического обследования в случае положительного результата [93, 94]
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: при оценке результатов анализа кала на скрытую кровь необходимо учитывать, что положительная реакция может встречаться при многих других заболеваниях, приеме некоторых лекарственных препаратов (висмута трикалия дицитрат**, препараты железа, аскорбиновая кислота**), несоблюдении диетических рекомендаций перед сдачей анализа (употреблении в пищу мяса, свеклы и т.п.).
Исследование, как правило, может быть использовано при невозможности проведения ЭГДС и/или поиска источников скрытого кровотечения в нижних отделах желудочно-кишечного тракта.
2.4 Инструментальные диагностические исследования
· Пациентам детского возраста с подозрением на гастрит и дуоденит рекомендуется выполнять эндоскопическое исследование верхних отделов ЖКТ (эзофагогастродуоденоскопия (ЭГДС)) согласно показаниям и симптомам «тревоги», которыми являются: дисфагия, одинофагия, гастроэзофагеальный рефлюкс, не купируемый медикаментозно, рвота, признаки желудочно- кишечного кровотечения, хронические упорные, стереотипные боли в животе, анорексия, потеря массы и/или задержка роста, анемия, хроническая диарея, анамнез, отягощенный по язвенной болезни или раку желудка, с целью подтверждения диагноза, выявления наличия изменений слизистой оболочки верхних отделов ЖКТ, выполнения биопсии желудка и двенадцатиперстной кишки [95, 96].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Комментарии: выполнение эндоскопического исследования всем пациентам детского возраста при подозрении на гастрит и дуоденит не выполнимо в рутинной медицинской практике, важен дифференцированный подход и определение показаний к проведению данной исследования с учетом современных представлений о патологии верхних отделов ЖКТ [95, 96]. Эндоскопические признаки гастрита у детей в подавляющем большинстве случаев прямо коррелируют с гистологическими (по факту выявления гастрита). Современные методы эндоскопического исследования, в частности, видеоэндоскопия высокой четкости с мультимодальным режимом осмотра и увеличением, предоставляют дополнительные высокоинформативные возможности для диагностики гастрита и дуоденита, поскольку могут использоваться для повышения частоты выявления атрофии/метаплазии на этапе эндоскопической диагностики, для повышения возможностей прицельной биопсии (ЭГДС (с улучшением качества изображения, в т.ч., хромоэндоскопия)) [95].
Эндоскопическая картина хронического гастрита и дуоденита приводится в Приложении А3
· Пациентам детского возраста с подозрением на гастрит и дуоденит, имеющим показания к проведению ЭГДС, рекомендуется выполнение биопсии желудка с помощью эндоскопии, биопсии двенадцатиперстной кишки с помощью эндоскопии (из тела и антрального отдела желудка, луковицы и залуковичной области двенадцатиперстной кишки) с последующим патолого-анатомическим исследованием биопсийного (операционного) материала желудка (в т.ч., патолого-анатомическое исследование биопсийного (операционного) материала желудка с применением гистохимических методов и патолого-анатомическое исследование биопсийного (операционного) материала желудка с применением иммуногистохимических методов, микроскопическое исследование материала желудка на хеликобактер пилори (Helicobacter pylori)) и патолого-анатомическое исследование биопсийного (операционного) материала двенадцатиперстной кишки в т.ч., патолого-анатомическое исследование биопсийного (операционного) материала двенадцатиперстной кишки с применением гистохимических методов и патолого-анатомическое исследование биопсийного (операционного) материала двенадцатиперстной кишки с применением иммуногистохимических методов) позволяющим исключить злокачественный характер язвенного поражения для диагностики инфекции H.pylori и др инфекционных агентов, выявления воспалительных изменений, атрофии, метаплазии для уточнения выраженности гастрита и дуоденита [97-104].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2)
Комментарии: патолого-анатомическое (гистологическое) исследование незаменимо для уточнения особенностей воспалительного процесса в слизистой оболочке желудка (атрофический, неатрофический), степени его активности (активный, неактивный), а также в выявлении, собственно, H.pylori [98]. В отличии от взрослых, единого регламента относительно количества биопсий у детей нет, выполняется прицельная биопсия из поражённых участков слизистой оболочки гастродуоденальной зоны. Биоптаты из разных отделов желудка и двенадцатиперстной кишки необходимо четко маркировать и помещать в отдельные контейнеры. При выявлении язв или эрозий, а также при подозрении на H.pylori-ассоциированный гастрит следует произвести биопсию слизистой оболочки желудка для верификации H.pylori доступными методами. Следует брать биопсию при любой диагностической эндоскопии у детей даже из неизмененных участков. [96, 106]. Для диагностики особых форм гастрита (aутоиммунный атрофический гастрит, атрофически-гиперпластический гастрит, гипертрофический гастрит, полипозный гастрит, лимфоцитарный гастрит, гранулематозный гастрит, эозинофильный гастрит, ригидный (антральный) гастрит) результаты гистологического исследования являются решающими.
Патолого-анатомическая (гистологическая) картина хронического гастрита и дуоденита приводится в Приложении А3.
· Пациентам детского возраста с подозрением на гастрит и дуоденит рекомендуется выполнение Ультразвуковое исследование органов брюшной полости (комплексное) (в т.ч., с водно-сифонной пробой) с целью исключения или подтверждения патологии других органов брюшной полости, в особенности, билиарного тракта [54, 107].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: патология билиарного тракта достаточно часто встречается у детей и может сопутствовать гастриту и дуодениту. Чувствительность и специфичность ультразвуковой диагностики несколько ниже по сравнению с компьютерной томографией и во многом зависит от квалификации специалиста по ультразвуковой диагностике, однако данный метод является неинвазивным, не несет лучевую нагрузку и может применяться повторно, следовательно, может быть использована для скринингового обследования [54, 107, 108].
Также полезно проведение УЗИ желудка с водно-сифонной пробой в связи с необходимостью исключения/подтверждения нарушения моторики: ГЭР и ДЭР.
2.5 Иные диагностические исследования
Отдельного внимания заслуживает вопрос диагностики инфекции H.pylori в детском возрасте, поскольку, в отличие от взрослой популяции, для детей не применяется стратегия «проверь и лечи», когда всем пациентам независимо от наличия или отсутствия жалоб, при обнаружении H.pylori назначается эрадикационная терапия. В детской практике важен более дифференцированный подход, особенно в случае выявления микроорганизма у пациента без симптомов диспепсии, когда вопрос о лечении может быть рассмотрен после тщательного обсуждения с пациентом/родителями [109].
· Пациентам с гастритом и дуоденитом для определения этиологии заболевания и тактики лечения рекомендовано обследование на наличие инфекции H.pylori [10, 15, 34].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Комментарии: Инфекция H.pylori является важным этиологическим фактором гастрита [10, 15, 34], следовательно, при обнаружении воспалительных изменений слизистой оболочки гастродуоденальной зоны показано исключение или подтверждение наличия данного микробного этиологического агента [10, 15, 34].
· Пациентам с гастритом и дуоденитом обследование на H.pylori рекомендовано проводить не ранее, чем через 2 недели после прекращения приема антисекреторных препаратов, в особенности ингибиторов протонногонасоса, и/или 4 недели после прекращения приема противомикробных препаратов системного действия и висмута трикалия дицитрата**, для того, чтобы избежать искаженных результатов [10].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Комментарий: Терапия ингибиторами протонного насоса и антибактериальными препаратами системного действия может дать ложноотрицательные результаты диагностического теста на инфекцию H.pylori из-за подавления репликации микроорганизма [110].
Указанные временные интервалы применимы в случаях первичной диагностики H.pylori, а также для мониторинга эффективности лечения. Они касаются как инвазивных, так и неинвазивных тестов, а именно, бактериологического, патологоанатомического (гистологического) методов, 13С-уреазного дыхательного теста на Helicobacter Pylori (быстрого уреазного теста), Иммунохроматографического экспресс-исследования кала на геликобактер пилори (Helicobacter pylori) [10, 109, 110, 111].
· Пациентам с гастритом и дуоденитом для первичной диагностики инфекции H.pylori рекомендуется использовать инвазивные методы с высокой чувствительностью: 13С-уреазный дыхательный тест на Helicobacter Pylori (быстрый уреазный тест) или Микроскопическое исследование материала желудка на хеликобактер пилори (Helicobacter pylori), а также (при доступности) бактериологическое исследование биоптатов (микробиологическое (культуральное) исследование биоптата стенки желудка на хеликобактер пилори (Helicobacter pylori), Микробиологического (культурального) исследования биоптатов слизистой желудка хеликобактер пилори (Helicobacter pylori)) [10].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Комментарии: в настоящее время основным «критерием–стандартом» для исследования заболеваний, ассоциированных с H.pylori, у детей остается эндоскопия верхних отделов желудочно-кишечного тракта с биопсией для проведения бактериологического, гистологического исследования, 13С-уреазного дыхательного теста на Helicobacter Pylori (быстрого уреазного теста) [112]. Особенности проведения современных сухих быстрых уреазных тестов является возможность провести исследование одного и того же биоптата сначала с помощью непосредственно уреазного теста, а затем патолого-анатомически (гистологически), что позволяет уменьшить количество биопсий при исследовании, а, следовательно, время процедуры, тем самым ускоряя и облегчая диагностику [114]. При использовании гелевых или жидких уреазных тестов, где исследование того же биоптата повторно невозможно, необходимо брать по 2 биоптата из каждого отдела, а при проведении и бактериологического исследования – дополнительно 2 биоптата. В таких случаях целесообразно проводить ЭГДС под наркозом при наличии технических возможностей и отсутствии противопоказаний и брать не менее 4-х (максимально – 6): биоптатов из тела и антрального отдела желудка [115].
В результате обзора Seo и соавторов [116] с обследованием 255 детей с помощью 13С-уреазного дыхательного теста на Helicobacter Pylori (быстрого уреазного теста) было обнаружено, что чувствительность этого метода повышалась с возрастом (она была самой низкой в возрастной группе 0-4 года) и с количеством биопсий [116]. Авторы объясняют свои выводы более низкой плотностью бактерий у детей по сравнению с подростками и взрослыми.
Использование микробиологического (культурального) исследования биоптата стенки желудка на хеликобактер пилори (Helicobacter pylori)/микробиологического (культурального) исследования биоптатов слизистой желудка хеликобактер пилори (Helicobacter pylori)/микробиологическое (культуральное) исследование биоптатов слизистой желудка на хеликобактер пилори (Helicobacter pylori) с определением чувствительности к антибактериальным препаратам (методами: E-test (Определение чувствительности микроорганизмов к антимикробным химиотерапевтическим препаратам методом градиентной диффузии), диско-диффузионный метод (Определение чувствительности микроорганизмов к антимикробным химиотерапевтическим препаратам диско-диффузионным методом), ПЦР в реальном времени (Определение ДНК хеликобактер пилори (Helicobacter pylori) в биоптатах слизистой желудка методом ПЦР), FISH-тест (отсутствует в Номенклатуре, метод флуоресцентной гибридизации in situ (FISH))) и ПЦР для определения мутаций, кодирующих резистентность к кларитромицину**, метронидазолу**, #тетрациклину, желательно, при возможности, при назначении даже первой линии терапии у детей и абсолютно показано при неудачном результате терапии первой и второй линии для индивидуального подбора терапии [10, 54, 109].
При отсутствии технической возможности проведения бактериологического исследования, ПЦР (Определение ДНК хеликобактер пилори (Helicobacter pylori) в биоптатах слизистой желудка методом ПЦР) или FISH-теста (отсутствует в Номенклатуре, метод флуоресцентной гибридизации in situ (FISH), выбор схемы лечения должен быть основан на данных о распространенности устойчивых штаммов H. pylori в конкретном регионе
Первичная диагностика инфекции H.pylori с помощью неинвазивных тестов (например, 13С-уреазного дыхательного теста на Helicobacter Pylori (быстрого уреазного теста), аммиачный дыхательный тест (отсутствует в утвержденной Номенклатуре медицинских услуг)) имеет скрининговый характер, в педиатрии подход «test and treat» не применяется [109]. При положительном результате неинвазивного метода показано проведение ЭГДС для окончательной постановки диагноза с использованием быстрого уреазного теста и гистологии, как описано выше. Сочетание 13С-уреазного дыхательного теста на Helicobacter Pylori (быстрого уреазного теста) и патолого-анатомическое исследования (гистологии) повышает чувствительность и специфичность первичной диагностики практически до 100%. Использование только 13С-уреазного дыхательного теста на Helicobacter Pylori (быстрого уреазного теста) или только патолого-анатомическое исследования (гистологии) снижает точность исследования примерно на 10–15% [117].
· Не рекомендуется применение серологических тестов (Определение антител к хеликобактер пилори (Helicobacter pylori) в крови) для первичной диагностики H.pylori и контроля эрадикации у детей в связи с недостаточной информативностью [109, 111]
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: Клиническое применение теста ограничено тем, что он не позволяет дифференцировать факт инфицирования в анамнезе от наличия H.pylori в настоящий момент и контролировать эффективность эрадикации. Не все серологические тесты равноценны. В рекомендациях ESPGHAN (2018) указано, что определение IgA, IgG к H.pylori в сыворотке, цельной крови, моче и слюне не следует использовать в клинической практике. Исследования уровня антител к H.pylori (методом иммуноферментного анализа) допустимо при проведении популяционных исследований в научных целях, а также при отсутствии других возможностей диагностики H.pylori [109].
Таким образом, серологические тесты не следует применять для диагностики, они не используются и для контроля эрадикации H.pylori, так как IgG в крови могут оставаться длительное время [109, 117].
· Для контроля успешности эрадикации H.pylori через 4-6 недель после окончания лечения рекомендовано применение 13С-уреазного дыхательного теста на Helicobacter Pylori (быстрого уреазного теста) (с мочевиной обычного изотопного состава), или определение антигена хеликобактера пилори в фекалиях (определение антигена H.pylori в кале с помощью моноклональных антител) [10, 118].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарий: Чувствительность 13С-уреазного дыхательного теста на Helicobacter Pylori (быстрого уреазного теста) составляет 94-96%, дыхательного аммиачного теста (отсутствует в утвержденной Номенклатуре медицинских услуг) – 90-92%, а определение антигена H.pylori в фекалиях– 83-92%, а специфичность: 90-93%, 86-93% и 90-100% соответственно [118-120]. Следует помнить, что проведение 13С-уреазного дыхательного теста на Helicobacter Pylori (быстрого уреазного теста) может дать ложноположительный результат у детей младше 6 лет из-за меньшего объема распределения и другой скорости продукции CO2 [113]. При необходимости проведения контрольного эндоскопического обследования после лечения предпочтение следует отдавать инвазивным тестам для верификации НР: патолого-анатомическому исследованию биопсийного (операционного) материала желудка и двенадцатиперстной кишки или 13С-уреазного дыхательного теста на Helicobacter Pylori (быстрого уреазного теста).
· Не рекомендуется обследование на H.pylori детей с жалобами, характерными для функциональной диспепсии (см. раздел 1.6) при отсутствии показаний к ЭГДС и симптомов «тревоги» [74].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Комментарий: ЭГДС не показана при подозрении на функциональные расстройства ЖКТ (если клиническая картина соответствует их критериям) [74, 121-126]. При отсутствии симптомов «тревоги», в соответствии с существующими рекомендациями, следует предположить функциональную диспепсию или иное заболевание функционального характера, назначить лечение и лишь при отсутствии эффекта или при появлении симптомов «тревоги» перейти к более углубленному обследованию, а именно – проведению ЭГДС. Решение о проведении ЭГДС принимается также с учетом семейного анамнеза и отягощенной наследственности по язвенной болезни или раку желудка. Если органические поражения, в том числе гастрит и дуоденит, не подозреваются клинически или не выявляются с помощью ЭГДС, не следует проводить инвазивное диагностическое тестирование с единственной целью выявления инфекции H.pylori. Диагностическое исследование на H.pylori у детей оправдано только в тех случаях, когда ожидаемая польза перевешивает затраты и риски, связанные с тестированием и последующим лечением. Гастрит, ассоциированный с H.pylori, при отсутствии язвенной болезни у ребенка, редко вызывает симптомы или прогрессирует до более серьезного заболевания осложнения в детском возрасте [127]. Более низкий риск осложнений у детей может быть частично объяснен другой иммунной реакцией на инфекцию. По сравнению со взрослыми, биопсия желудка, полученная у детей, инфицированных H.pylori, показывает менее выраженное воспаление. Кроме того, обнаружено увеличение количества иммуносупрессивных Т-регуляторных клеток (Treg) наряду с ответом в виде противовоспалительного цитокина IL-10 вместо провоспалительного IL-17 [128-129]. Исходя из имеющихся данных, лечение, направленное на устранение инфекции H.pylori, как ожидается, не улучшит симптомы у детей, за исключением случаев язвенной болезни [127].
3. Лечение, включая медикаментозную и немедикаментозную терапии, диетотерапию, обезболивание, медицинские показания и противопоказания к применению методов лечения
3.1 Консервативное лечение
3.1.1 Диетотерапия
· Пациентам с гастритом и дуоденитом в стадии обострения рекомендуется диетотерапия с целью минимизации травматизации воспаленной слизистой оболочки гастродуоденальной зоны [95, 130, 131].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарий: показано применение химического, механического и термического ограничения в еде; дробное питание до 5-6 раз в сутки в течение 1 месяца, затем число приемов пищи уменьшается до 4 раз в сутки и через 2-3 месяца, при наступлении стойкой клинико-эндоскопической ремиссии, больной возвращается к обычному питанию. В период обострения гастрита и дуоденита следует исключить жареную и копченую, соленую, маринованную пищу, продукты содержащие экстрактивные вещества (перец, горчица, специи, лук, чеснок), предпочтение отдается продуктам, приготовленным на пару, отварным, тушеным. Также рекомендуются каши, кисели из сладких ягод, муссы, желе, печеные яблоки [95, 130, 131].
3.1.2 Эрадикация H. pylori
· Пациентам детского возраста с гастритом и дуоденитом, у которых выявлена инфекция НР, рекомендуется проведение эрадикационной терапии по абсолютным показаниям (наличие эрозивных и/или атрофических изменений слизистой оболочки гастродуоденальной зоны, указание в анамнезе на наследственную отягощенность по язвенной болезни или раку желудка у родственников) и относительным показаниям (любые HP-ассоциированные варианты хронического гастродуоденита, протекающие с выраженной клинической симптоматикой и/или обширной обсемененностью HP слизистой оболочки желудка по данным гистологического исследования, любые HP-ассоциированные варианты гастродуоденальной патологии у родственников, пожелавших провести курс эрадикационной терапии (после обследования)) с целью дифференцированного подхода к терапии с учетом пользы и рисков проводимого лечения [54, 95, 109].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Комментарий: в отличие от взрослых, для которых эрадикация НР требуется в любом случае, независимо от наличия симптомов или повреждения слизистой оболочки гастродуоденальной зоны [10, 95, 120], для детской популяции используется дифференцированный подход к определению необходимости проведения антихеликобактерной терапии, что особенно актуальной для детей раннего возраста, когда присутствуют ограничения для приема антисекреторных и антибактериальных препаратов системного действия, а также высок риск реинфекции НР. В популяциях с высокой распространенностью инфекции частота повторного заражения среди детей младшего возраста после успешной ликвидации может быть значительной. Исследование, проведенное в Боливии среди населения с высокой распространенностью заболевания и низким уровнем дохода, показало, что частота повторного заражения через 1 год после успешного лечения составляет 20% у детей младше 10 лет и 8% у детей старшего возраста и подростков [133]. В Латинской Америке уровень повторного заражения через 1 год составляет 11% [134], а в Германии (страна с низкой распространённостью НР) – 2,3% в год [135]. Риск развития рака, ассоциированного с H.pylori, или лимфомы слизистой оболочки, ассоциированной с лимфоидной тканью, в детском возрасте в Европе и Северной Америке крайне низок. Соотношение риска и пользы эрадикационной терапии может варьироваться в разных регионах. В регионах с высоким уровнем заболеваемости раком желудка, таких как Китай или Япония, польза от лечения, направленного на снижение риска развития рака желудка, может перевешивать риски, связанные с лечением [137]. В западных странах имеются эпидемиологические данные о том, что инфекция H.pylori, особенно у детей младшего возраста, может быть связана со снижением распространенности аллергических заболеваний, в частности бронхиальной астмы [138-141]. Таким образом, решение о лечении гастрита и дуоденита, ассоциированного с H.pylori, обнаруженного случайно во время проведения ЭГДС, при отсутствии эрозивно-язвенным поражений слизистой оболочки гастродуоденальной зоны, должно быть тщательно обсуждено с пациентом и членами его семьи с учетом потенциального риска и пользы лечения у каждого конкретного пациента.
· Пациентам с гастритом и дуоденитом, инфицированным НР, рекомендуется предварительное микробиологическое (культуральное) исследование биоптатов слизистой желудка на хеликобактер пилори (Helicobacter pylori) с определением чувствительности к антибактериальным препаратам с целью индивидуального подбора схемы лечения и повышения эффективности эрадикации HP (таблица 1) [109].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарий: Использование микробиологического (культурального) исследования биоптатов слизистой желудка на хеликобактер пилори (Helicobacter pylori)с определением чувствительности к антибактериальным препаратам (методом разведений или Е-теста) и ПЦР для определения мутаций, кодирующих резистентность к кларитромицину**, метронидазолу**, #тетрациклину, желательно при назначении даже первой линии терапии у детей и абсолютно показано при неудачном результате терапии первой и второй линии для индивидуального подбора терапии [10, 54, 95, 109].
При отсутствии технической возможности проведения бактериологического исследования, ПЦР (Определение ДНК хеликобактер пилори (Helicobacter pylori) в биоптатах слизистой желудка методом ПЦР) или FISH-теста - метод флуоресцентной гибридизации in situ (FISH) (отсутствует в утвержденной Номенклатуре медицинских услуг), выбор схемы лечения должен быть основан на данных о распространенности устойчивых штаммов H. pylori в конкретном регионе
Таблица 1
Схемы эрадикации с учетом установленной антибиотикорезистентности HР
|
Чувствительность HP |
Выбор схемы терапии |
|
Чувствителен к КЛА** и МЕТ** |
ИПН+АМО**+КЛА** 14 дней |
|
Резистентен к КЛА**, чувствителен к МЕТ** |
ИПН+АМО**+МЕТ** или ИПН+В**+МЕТ**+#Т (с 8 лет) 14дней |
|
Резистентен к МЕТ**, чувствителен к КЛА** |
ИПН+АМО**+КЛА** 14 дней (возможно + В) |
|
Резистентен к КЛА** и к МЕТ** |
ИПН+АМО**+МЕТ** с высокими дозами АМО ** или ИПН+В**+#Т+МЕТ** 14 дней |
|
Неизвестна чувствительность к АБ: |
Высокие дозы ИПН+АМО**+МЕТ** или ИПН+В**+#Т+МЕТ** 14 дней |
Условные обозначения:
АМО – амоксициллин**,
КЛА – кларитромицин**,
МЕТ – метронидазол**,
ИПН – ингибиторы протонного насоса (#омепразол**, #рабепразол, #эзомепразол**),
Т – #тетрациклин,
В** – висмута трикалия дицитрат**
Рекомендуемые дозы препаратов представлены в таблице 2 [95, 109]
|
Препарат |
Код ATX |
Рекомендуемые дозы |
|
#Омепразол** |
A02BC |
1 мг/кг/сут в 2 приема, с 12 лет |
|
#Рабепразол |
A02BC |
1 мг/кг/сут в 2 приема, с 12 лет |
|
#Эзомепразол** |
A02BC |
1-2 мг/кг/с в таблетках или гранулах в 2 приема за 30 мин. до еды (с 1 года; таблетки с 12 лет) |
|
Амоксициллин** |
J01CA |
50 мг/кг до 1 г в 2 приема, с 5 лет возможно увеличение дозы в 1,5 раза |
|
Кларитромицин** |
J01FA |
15 мг/кг в 2 приема, суспензия с 6 мес., таблетки с 12лет |
|
Джозамицин** |
J01FA |
детям весом более 10 кг, в дозировке 40-50 мг/кг в 2-3 приема. |
|
Метронидазол** |
J01XD |
20 мг/кг до 500 мг в 2 приема, с 6 лет |
|
#Тетрациклин |
J01AA |
50 мг/кг до 1 г в 2 приема с 8 лет |
|
#Нифурател |
G01AX |
15-30 мг/кг/сут в 2 приема с 3 лет |
|
Висмута трикалия дицитрат ** |
A02BX |
120 мг 3-4 раза (8 мг/кг/сут.) с 4 лет |
С учетом технических трудностей осуществления индивидуального подбора противомикробных препаратов системного действия для лечения преимущество отдается схеме, назначаемой при неизвестной чувствительности НР к этим препаратам.
· Пациентам с гастритом и дуоденитом, инфицированным НР, в случае невозможности определения чувствительности микроорганизма к противомикробным препаратам системного действия в качестве терапии первой линии рекомендуется использование эмпирически выверенных эффективных схем эрадикационной терапии [95, 109].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Комментарий:
Следует использовать одну из следующих схем:
· ИПН + АМО** + КЛА** (+В**)
· ИПН + КЛА** + МЕТ** (+В**)
· ИПН + АМО** + МЕТ** (+В**)
· ИПН + АМО** или КЛА** + Нифурател
· ИПН + АМО** + Джозамицин** (последовательное назначение антибиотиков по 7 дней) (+В**) (для второй линии терапии)
· ИПН + #Т + В** + МЕТ** (с 8 лет)
Условные обозначения: АМО** – амоксициллин**, КЛА** – кларитромицин**, МЕТ** – метронидазол**, ИПН – ингибиторы протонного насоса (#омепразол**, #рабепразол, #эзомепразол**), Т – #тетрациклин*, В** – висмута трикалия дицитрат**
При отсутствии данных о чувствительности НР к противомикробным препаратам системного действия возможно увеличение стандартной дозы амоксициллина** в 1,5 раза (в соответствии с рекомендациями ESPGHAN) или применение последней схемы (ESPGHAN) [109]. Висмута трикалия дицитрат ** может быть добавлен как компонент в тройные схемы уже на первой линии для детей с 4 лет. Длительность лечения – 14 дней. Прием ИПН (по АТХ-классификации: ингибиторы протонового насоса (A02BC): #омепразол**, #рабепразол, #эзомепразол**) или висмута трикалия дицитрата** не пролонгируется более 14 дней без особых показаний.
#Тетрациклин может быть введен в схемы эрадикации с учетом возрастных ограничений (с 8 лет). Отечественный и зарубежный опыт современных препаратов #тетрациклина показывает его эффективность и безопасность [95, 109].
Хотя фуразолидон является недорогим и высоко эффективным в отношении H.pylori препаратом, к которому, практически не встречается ни первичная, ни вторичная резистентность, высокая частота серьезных побочных эффектов (тошнота, рвота и др.) не позволяет рекомендовать его в педиатрической практике [142, 143]. По данным немногочисленных исследований у взрослых и детей, эффективность 3-х-компонентных схем, включавших нифурател в комбинации с амоксициллином**, ИПН или другие препараты для лечения язвенной болезни желудка и двенадцатиперстной кишки и ГЭРБ (А02ВХ) (препаратов висмута) составляет 82,9-86,0% [144-146]. Следует, однако, отметить отсутствие мета-анализов по данному вопросу.
Имеются данные о возможности применения джозамицина**(таблетки диспергируемые, детям весом >10 кг ) в качестве альтернативы кларитромицину**, у детей – в схемах последовательной терапии [118], показания к применению при хеликобактерной инфекции у детей включены в инструкцию к препарату.
Последовательная терапия, не имеющая преимуществ перед классическими схемами с одновременным приемом препаратов, может быть предложена пациенту исключительно для повышения приемлемости в случаях нежелания родителей или самого пациента по тем или иным соображениям следовать стандартным схемам лечения. Тем не менее ряд авторов рекомендуют последовательную терапию в схемах первой линии [147, 148].
Следует обратить внимание, что не все ингибиторы протонного насоса разрешены у детей и не все из них имеют показания: язвенная болезнь или применение в схемах эрадикации HP.
· Пациентам с гастритом и дуоденитом, инфицированным НР, если после первого курса лечения эрадикация HP не достигнута (контроль следует осуществлять через 4-6 недель после окончания схемы), повторная терапия проводится не сразу, а при последующем обострении с целью обеспечения максимальной безопасности лечения [109].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарий: Выбор схемы терапии, при возможности, должен производиться на основании данных посева HP и индивидуального определения его чувствительности к антибиотикам (см. раздел 2). Если это сделать невозможно, применяется квадротерапия: ИПН с #тетрациклином, метронидазолом** и висмутом, либо схемы с включением производных нитрофурана) [95].
Рекомендуемые схемы терапии (при условии, что они не использовались ранее):
· В** + ИПН + АМО** + КЛА**
· В** + ИПН + АМО** или КЛА** + нифурател
· ИПН + #Т + В** + МЕТ**
Длительность лечения – 14 дней.
Условные обозначения: АМО** – амоксициллин**, КЛА** – кларитромицин**, МЕТ** – метронидазол**, ИПН – ингибиторы протонного насоса, Т – #тетрациклин, В** – висмута трикалия дицитрат**
· Пациентам с гастритом и дуоденитом, являющимися H.рylori-позитивными и имеющими показания для проведения эрадикационной терапии рекомендуется обеспечить приверженность к назначенному лечению (комплаенс), в том числе за счет беседы с родителями/законными представителями с целью достижения максимальной эффективности эрадикации возбудителя [95, 107, 109, 118, 149, 150].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарий: Комплаенс следует рассматривать как ключевой фактор успеха эрадикационной терапии H.pylori. В контролируемом исследовании было показано, что при приеме более 60% назначенных препаратов эрадикация инфекции составила 96%, при приеме менее 60% (низкий комплаенс) – 69% [149]. В широкомасштабном рандомизированном контролируемом исследовании процент эрадикации снизился при низком комплаенсе (принято менее 80% назначенных препаратов) на 34%, причем у некомплаентных пациентов персистенция H.pylori наблюдалась в 59% случаев [150]. Следует уделить время тому, чтобы проконсультировать пациента и/или его родственников, объяснить, как принимать комплексную лекарственную терапию и оценить возможные побочные эффекты антибиотикотерапии. Следует специально отметить необходимость завершения лечения и приема предписанной суммарной дозы лекарственных средств, а также необходимость контрольного обследования для оценки эффективности эрадикации.
· При выявлении у пациента детского возраста инфекции НР и наличии показаний к эрадикации с целью предотвращения реинфекции рекомендуется провести беседу о необходимости обследования на наличие НР всех членов семьи и селективно назначить эрадикационную терапию НР-позитивным детям при наличии показаний (см. выше), взрослые НР-позитивные направляются на консультацию к соответствующему специалисту [151]
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 3)
Комментарий: Повторное заражение H.pylori чаще встречается у детей, чем у взрослых, и общепризнано, что семья играет важную роль в первичном детском заражении. При обследовании пятидесяти семей, в каждой из которых был зарегистрирован основной случай инфицирования H.pylori у детей (средний возраст 9,48 лет) при длительном наблюдении (в среднем 62,2 месяца) частота повторного инфицирования составила 2,4% на пациента в год в группе наблюдения и 0,7% на пациента в год в группе, где проводилась эрадикация всех инфицированных взрослых (р = 0,31) [151].
3.1.3 Медикаментозное лечение
· Пациентам с гастритом и дуоденитом, не ассоциированным с H.pylori, рекомендуется назначение препаратов в зависимости от имеющихся жалоб с целью их купирования [74, 124, 152, 153]
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Комментарий: Все препараты для симптоматического лечения назначаются с учётом возрастных ограничений.
При боли в эпигастральной области пациентам с гастритом и дуоденитом возможно использование средств с антисекреторным эффектом: алюминия фосфат (A02AB03) детям детям старше 6 месяцев до 6 лет – 1/2 пакетика или 2 чайные ложки после каждого из 4 кормлений, детям, старше 6 лет – по 1-2 пак. 2-3 раза в сутки) или алгелдрат+магния гидроксид (A02AX Антациды в комбинации с другими средствами) детям от 10 до 15 лет – по 5 мл 3-4 раза в день или 10 мл 1-2 раза или по 1 пакетику 1-2 раза в день, с 15 лет перорально по 15 мл, через 1-2 ч после приема пищи и перед сном или по мере необходимости (не более 6 столовых ложек в сутки), ингибиторы протонного насоса (дозировки и ограничения такие же как в составе эрадикационной терапии) – предпочтение отдается группе «ингибиторы протонного насоса» в сравнении с блокаторами Н2-гистаминовых рецепторов в связи с более высокой эффективностью первых в устранении клинических симптомов.
При ощущениях тяжести в эпигастриальной области и чувстве раннего насыщения возможно применение стимуляторов моторики желудочно-кишечного тракта (домперидон (A03FA03) детям старше 12 лет при хронических диспепсических явлениях 10 мг 3 раза в сутки, в т.ч. и перед сном в случае необходимости, тримебутин (A03AA05) детям старше 12 лет по 100-200 мг 3 раза в сутки, детям в возрасте 5-12 лет: по 50 мг 3 раза в сутки, детям в возрасте 3-5 лет по 25 мг 3 раза в сутки) [74, 124, 152, 153].
В комплексной терапии гастрита и дуоденита в рутинной практике при симптоматическом лечении болей в животе спастического характера в животе чаще всего назначаются следующее симптоматическое лечение:
дротаверин** (таблетки 40 мг детям с возраста 6 лет: от 6 до 12 лет: по 40 мг на один прием 1-2 раза в день. Максимальная суточная доза – 80 мг (2 таблетки по 40 мг), старше 12 лет: по 40 мг на один прием 1-4 раза в день или по 80 мг на один прием 1-2 раза в день. Максимальная суточная доза – 160 мг (4 таблетки по 40 мг)) и др.
Лечение особых форм гастритов проводится индивидуально с использованием, в основном, симптоматической терапии, а также с обязательным привлечением врачей-детских хирургов для решения вопроса об оперативном вмешательстве.
При стабильном течении заболевания, при отсутствии клинических и лабораторных проявлений пациенты в лечении не нуждаются.
· Для ускорения регресса воспаления и заживления эрозий слизистой оболочки желудка и двенадцатиперстной кишки рекомендуется пациентам с гастритом и дуоденитом применять висмута трикалия дицитрат** [10, 154, 155].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
· В лечении билиарного рефлюкс-гастрита эффективным является использование препаратов урсодезоксихолевой кислоты** в средней дозировке из расчета 250 мг капсула (при весе тела до 47 кг) или 1 мерный стаканчик (5мл – 250 мг) (детям с 4 недель) – или 0,5 табл. (250 мг) (детям с 3 лет -) ежедневно вечером, перед сном (капсулы не разжевывают), запивая небольшим количеством воды. Курс лечения – от 10-14 дней до 6 мес, при необходимости – до 2 лет. [156, 157].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
· В лечении аутоиммунного гастрита рекомендуется лечение основного заболевания, являющегося триггером иммунопатологического процесса в слизистой оболочке желудка, предотвращение дефицита железа и/или витамина B12, оценка риска малигнизации [19, 190].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Комментарий: Этиологическое и патогенетическое лечение аутоиммунного гастрита у детей в настоящее время не разработано. лечение проводится согласно соответствующим рекомендациям. При выявлении инфекции Helicobacter pylori проводится курс эрадикационной терапии с использованием трех или четырехкомпонентной схемы терапии [19].
· Пациентам с гастритом и дуоденитом рекомендуется селективное назначение препаратов группы «Противодиарейные микроорганизмы» с целью снижение риска побочных эффектов и повышения эффективности антихеликобактерной терапии (если она поводится), в первую очередь, ассоциированного с применением антибиотиков кишечного дисбиоза и профилактики антибиотико-ассоциированной диареи, с целью повышения иммунитета, с целью снижения проницаемости эпителиального барьера, с целью коррекции и профилактики нарушений микробиоты желудочно-кишечного тракта [132, 158, 159, 164-170].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Комментарий: Важность коррекции и профилактики нарушений микробиоты желудочно-кишечного тракта в первую очередь относится к лицам с нестабильной кишечной микробиотой, к которым относятся дети.
Эффективность противодиарейных микроорганизмов (пробиотиков) в повышении эффективности и безопасности эрадикации НР, в том числе для профилактики антибиотико-ассоциированной диареи, доказана в проведенных РКИ и подтверждена последующими мета-анализами у взрослых [132, 158, 159].
Наиболее эффективным в настоящее время считается применение Lactobacillus rhamnosus GG и Saccharomyces boulardii CNCM I-745 (250 мг 2 раза в день для детей с 1 года до 3 лет, 500 мг 2 раза в день для детей с 3 лет). Эти штаммы в настоящее время входят в текущие рекомендации ESPGHAN-2024 и WGO (2023 г.) по противодиарейным микроорганизмам (пробиотикам) (зарегистрированный лекарственный препарат Сахаромицеты Буларди). В локальные методические рекомендации НСОИМ и РГА по пробиотикам (2024 г.) также включён пробиотический штамм Lactobacillus acidophilus (NK1, NK2, NK5, NK12) + кефиран (препарат Лактобактерии ацидофильные+Грибки кефирные) для профилактики антибиотико-ассоциированной диареи улучшения исходов эрадикации инфекции H. pylori [70, 71, 72, 73, 74, 132].
Действие противодиарейных микроорганизмов (пробиотиков) как иммуномодуляторов сопряжено с их способностью проявлять прямую антимикробную активность в отношении патогенов, производя антимикробные вещества (бактериоцины), а также со способностью модулировать иммунный ответ через эпителиальные клетки, модулировать и активировать иммунные реакции с помощью макрофагов и дендритных клеток, активировать CD8+Т-лимфоциты и CD4+Т-лимфоциты, модулировать продукцию IgA, стимулировать toll-подобные рецепторы, модифицировать профиль экспрессии цитокинов [164-168].
Позитивное действие противодиарейных микроорганизмов (пробиотиков) для восстановления слизистого барьера связано к с их иммунологическими эффектами, так и со способностью индуцировать регенерацию слизистой оболочки и улучшение выработки муцина, что ингибирует прилипание патогенов к эпителиальным клеткам, а также снижает проницаемость эпителиального барьера [164, 169, 170].
4. Медицинская реабилитация и санаторно-курортное лечение, медицинские показания и противопоказания к применению методов медицинской реабилитации, в том числе основанных на использовании природных лечебных факторов
· Пациентам с гастритом и дуоденитом с целью более быстрого и полного восстановления и профилактики рецидивов рекомендуется селективное проведение по показаниям санаторно-курортного лечения после купирования обострения заболевания, проведения эрадикационной терапии в случае инфицирования НР, как правило, через 3-6 месяцев после начала лечения [171-173].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарий: в настоящее время убедительных доказательств того, что санаторно-курортное лечение, а также лечебная физкультура, улучшает прогноз или влияет на исходы гастрита и дуоденита, нет. Для окончательного вывода о необходимости данного лечения необходимо проведение качественных широкомасштабных исследований. Продолжительность санаторно-курортного лечения – 14-21 день. В ранний период реабилитации предпочтение следует отдавать местным санаториям. Направление на курортное лечение в санатории, удаленные от места проживания возможно при формировании стойкой клинической ремиссии. Следует рассмотреть проведение лечебной физкультуры (лечебная физкультура при заболеваниях пищевода, желудка, двенадцатиперстной кишки), медицинского массажа с целью улучшения крово- и лимфообращения в брюшной полости; нормализации моторики желудка и двенадцатиперстной кишки, секреторной и нейрогуморальной регуляции пищеварительных процессов; создания благоприятных условий для репаративных процессов в слизистой оболочке желудка и двенадцатиперстной кишки при отсутствии противопоказаний [171-173], а также психотерапевтического и физиотерапевтического лечения. На 3-м году наблюдения возможно оздоровление детей в санаторных сменах летних оздоровительных лагерей. На санаторно-курортное лечение не направляют пациентов с противопоказаниями к данному виду лечения, а также к проведению любых бальнеологических процедур (например, пациенты с болезнью Менетрие, с полипозом желудка и новообразованиями желудка).
5. Профилактика и диспансерное наблюдение, медицинские показания и противопоказания к применению методов профилактики
· Пациентам с гастритом и дуоденитом диспансерное наблюдение рекомендовано к проведению совместно врачом-педиатром участковым /врачом общей практики (семейный врач) и/или врачом-гастроэнтерологом в условиях поликлиники, учитывая распределение по группам (I-IV) в зависимости от состояния обострения и ремиссии заболевания с целью проведения противорецидивных и реабилитационных мероприятий, различающихся в группах учета [174].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарий: При стойкой длительной клинико-лабораторной ремиссии через 3 года наблюдения можно поставить вопрос о снятии с диспансерного учета. варианты диспансерного обследования в зависимости от секреторной функции желудка представлены в таблицах 10-11.
Таблица 10
Диспансерное наблюдение детей с ХГ с повышенной секреторной и кислотообразующей функцией
|
Группа |
Исследования |
Осмотр специалистов |
Противорецидивные и реабилитационные мероприятия |
|
III (стадия неполной клинико-лабораторной ремиссии)
|
1. ЭГДС и диагностика НР-инфекции – 1 раз в год (при эрозивном процессе – 2 раза в год) 2. Диагностика НР-инфекции – 1 раз в год (предпочтительно двумя методами) 3. Оценка эрадикации НР через 6-8 недель после окончания антихеликобактерной терапии 4. Микроскопическое исследование кала на яйца и личинки гельминтов и Микроскопическое исследование кала на простейшие, копрограмма, Общий (клинический) анализ крови (КАК) – 2 раза в год 5. Исследование микробиоценоза кишечника (дисбактериоз) – по показаниям |
Врач-педиатр, врач-гастроэнтеролог – 1 раз в 3 месяца |
1. При выявлении НР – повторная терапия (трех/четырехкомпонентная схема) 2. Противорцидивное лечение – 2 раза в год весна/осень (антациды, Н2-блокаторы, средства пленкообразующие, Другие препараты для лечения язвенной болезни желудка и двенадцатиперстной кишки и ГЭРБ (препараты висмута) до 2-4 недель 3. Фитотерапия (с седативным действием) и минеральные воды – 2 раза в год в течение 1 месяца 4. Физиотерапия, лечебная физкультура (ЛФК) (Лечебная физкультура при заболеваниях пищевода, желудка, двенадцатиперстной кишки)) – 2 раза в год 5. Вакцинация – по эпидемиологическим показаниям 6. Группа физкультуры – специальная 7. Селективно назначить лечение в местном санатории через 3 месяца после достижения клинико-лабораторной ремиссии |
|
II (стадия клинико-лабораторной ремиссии) |
1. ЭГДС и диагностика НР-инфекции – 1 раз в год/по показаниям 2. Диагностика НР-инфекции – 1 раз в год/по показаниям (предпочтительно двумя методами) 3. Микроскопическое исследование кала на яйца и личинки гельминтов и Микроскопическое исследование кала на простейшие, копрограмма, Общий (клинический) анализ крови – 2 раза в год |
Врач-педиатр, врач-гастроэнтеролог – 2 раза в год |
1. Противорцидивное лечение – повторная эрадикация НР по желанию пациента не ранее, чем через 6 месяцев после предыдущего лечения после определения чувствительности к антибактериальным препаратам системного действия 2. Фитотерапия и минеральные воды – 2 раза в год в течение 1 месяца 3. Физиотерапия, ЛФК – 1 раз в год 4. Вакцинация – противопоказаний нет 5. Группа физкультуры – подготовительная 6. Селективно назначить лечение в санатории – 1 раз в год |
|
I (стадия стойкой клинико-лабораторной ремиссии) |
1. ЭГДС и диагностика НР-инфекции – 1 раз в год/по показаниям 2. Диагностика НР-инфекции – 1 раз в год/по показаниям (предпочтительно двумя методами) 3. Микроскопическое исследование кала на яйца и личинки гельминтов и Микроскопическое исследование кала на простейшие, соскоб на энтеробиоз, копрограмма, общий (клинический) анализ крови – 1 раз в год |
Врач-педиатр, врач-гастроэнтеролог – 1 раз в год |
1. Противорецидивное лечение (пленкообразующие препараты) – по показаниям 2. Фитотерапия и минеральные воды – 1 раз в год в течение 1 месяца 3. Физиотерапия, ЛФК – по показаниям 4. Вакцинация – противопоказаний нет 5. Группа физкультуры – основная 6. Селективно назначить лечение в санатории – 1 раз в год |
Таблица 11
Диспансерное наблюдение детей с ХГ с пониженной секреторной и кислотообразующей функцией
|
Группа |
Исследования |
Осмотр специалистов |
Противорецидивные и реабилитационные мероприятия |
|
III (стадия неполной клинико-лабораторной ремиссии)
|
1. ЭГДС – 1 раз в год 2. Диагностика НР-инфекции – 1 раз в год (двумя методами) 3. Определение содержания антител к антигенам желудка в крови – 1 раз в год 4. Внутрипищеводная рН-метрия/Внутрипищеводная рН-метрия суточная – 1 раз в год 4. Микроскопическое исследование кала на яйца и личинки гельминтов и Микроскопическое исследование кала на простейшие, копрограмма, Общий (клинический) анализ крови – 2 раза в год 5. Исследование микробиоценоза кишечника (дисбактериоз) – по показаниям 6. Определение антител классов M, G (IgM, IgG) к вирусу Эпштейна-Барра (Epstein-Barr virus) в крови – 1 раз в год |
Врач-педиатр, врач-гастроэнтеролог – 1 раз в 3 месяца |
1. При выявлении НР – эрадикационная терапия (трех/четырехкомпонентная схема) 2. Противорецидивное лечение – 2 раза в год весна/осень (заместительные средства, Ретинол (витамин A), Аскорбиновая кислота (витамин C), Токоферол (витамин E) и Комплекс витаминов группы B, ферментные препараты) 3. При выявлении ВЭБ – противовирусная терапия под контролем инфекциониста 3. Фитотерапия и высокоминерализованные минеральные воды – 2 раза в год в течение 1 месяца 4. Физиотерапия и ЛФК – 2 раза в год 5. Вакцинация – по эпидемиологическим показаниям 6. Группа физкультуры – специальная в течение 1 года после обострения заболевания 7. Селективно назначить лечение в местном санатории через 3 месяца после достижения клинико-лабораторной ремиссии |
|
II (стадия клинико-лабораторной ремиссии) |
1. ЭГДС – 1 раз в год 2. Диагностика НР – инфекции – 1 раз в год (двумя методами) 3. Определение содержания антител к антигенам желудка в крови – 1 раз в год 4. Внутрипищеводная рН-метрия/Внутрипищеводная рН-метрия суточная – 1 раз в год 5. Микроскопическое исследование кала на яйца и личинки гельминтов и Микроскопическое исследование кала на простейшие, копрограмма, Общий клинический) анализ крови – 1 раз в год 5. Определение антител классов M, G (IgM, IgG) к вирусу Эпштейна-Барра (Epstein-Barr virus) в крови – 1 раз в год |
Врач-педиатр, врач-гастроэнтеролог – 2 раза в год |
1. При выявлении НР – эрадикационная терапия (трех/четырехкомпонентная схема) 2. Противорцидивное лечение – 2 раза в год весна/осень (заместительные средства, Ретинол (витамин A), Аскорбиновая кислота (витамин C), Токоферол (витамин E) и Комплекс витаминов группы B, ферментные препараты) 3. При выявлении ВЭБ – противовирусная терапия под контролем инфекциониста 3. Фитотерапия и высокоминерализованные минеральные воды – 1-2 раза в год в течение 1 месяца 4. Физиотерапия и ЛФК – 2 раза в год 5. Вакцинация – противопоказаний нет 6. Группа физкультуры – подготовительная |
|
I (стадия стойкой клинико-лабораторной ремиссии) |
1.ЭГДС – 1 раз в год (по показаниям) 2. Диагностика НР – инфекции – 1 раз в год (неинвазивная) 3. Определение содержания антител к антигенам желудка в крови – 1 раз в год 4. Внутрипищеводная рН-метрия/Внутрипищеводная рН-метрия суточная – 1 раз в год (по показаниям) 4. Микроскопическое исследование кала на яйца и личинки гельминтов и Микроскопическое исследование кала на простейшие, копрограмма, Общий (клинический) анализ крови – 1 раз в год 5. Определение антител классов M, G (IgM, IgG) к вирусу Эпштейна-Барра (Epstein-Barr virus) в крови – 1 раз в год |
Врач-педиатр, врач-гастроэнтеролог – 1 раз в год |
1. Противорцидивное лечение – по показаниям 2. Фитотерапия и минеральные воды – 1 раз в год в течение 1 месяца 3. Физиотерапия, ЛФК – по показаниям 4. Вакцинация – противопоказаний нет 5. Группа физкультуры – основная 6. Санаторий – 1 раз в год |
· Пациентам с гастритом и дуоденитом рекомендовано проведение профилактических мероприятий с целью уменьшения частоты встречаемости и рецидивов заболевания [175, 176, 177].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарий: в качестве профилактики используются образовательные программы для детей и их родителей с информированием о факторах риска и клинических проявлениях ХГ и ХД. Проводят обучение с формированием принципов режима дня, питания, физического воспитания и закаливания, освоение комплексов лечебная физкультура, выполнение противоэпидемических мероприятий. Основное направление профилактики направлено на уменьшение распространения НР-инфекции. Для этого, обязательным является личная гигиена в семье, обследование ближайших родственников на инвазию НР, а также лечение родственников, обсемененных НР.
Для вторичной профилактики возможно применять курсы профилактического лечения, которые включают диетотерапию, прием препаратов, улучшающих обменные процессы, витаминов, минеральные воды, фитотерапию, физиотерапевтические процедуры. Курсы проводятся 2 раза в год весной и осенью (в сентябре-октябре и марте-апреле). Возможно применение, например, фитопрепаратов из цветков ромашки, для уменьшения воспалительного процесса в слизистой оболочке желудка и двенадцатиперстной кишки, лакрицу (солодку), с целью улучшения регенерации. Прием в пищу блюд из капусты также способствует регенерации. [175, 176]. Физиотерапевтические методы также возможно селективно назначить пациентам с ХГ и ХД. Имеются публикации о противовоспалительном, обезболивающем действии, нормализации функции желудка и реактивности организма. У детей преимущественно применяют микроволны дециметрового диапазона (воздействие электромагнитным излучением дециметрового диапазона (ДМВ)) с локализацией воздействия на щитовидной железе, в воротниковой, эпигастральной областях и пилородуоденальной зоне; микроволны сантиметрового диапазона (воздействие электромагнитным излучением сантиметрового диапазона (СМВ-терапия)); ультразвук (воздействие ультразвуком при заболеваниях пищевода, желудка, двенадцатиперстной кишки); переменное магнитное поле (Воздействие переменным магнитным полем (ПеМП)); для местного воздействия применяют гальванизацию при заболеваниях пищевода, желудка, двенадцатиперстной кишки (услуга отсутствует в действующей Номенклатуре услуг) и лекарственный электрофорез (Электорофорез лекарственных препаратов при заболеваниях желудка и двенадцатиперстной кишки) [177].
· Пациентам с атрофией слизистой оболочки гастродуоденальной зоны с целью профилактики прогрессирования гастрита и дуоденита, а также профилактики рака желудка, рекомендуется эндоскопическое наблюдение в зависимости от выраженности атрофии: со слабой и умеренной степенью атрофии слизистой оболочки, ограниченной только антральным отделом желудка эндоскопическое наблюдение не рекомендуется [71, 91, 178-187].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Комментарии: Лица с выраженной атрофией и кишечной метаплазией слизистой оболочки желудка продолжают нуждаться в эндоскопическом наблюдении даже несмотря на ликвидацию инфекции H. pylori в результате успешной ее эрадикации [10, 34, 71, 91, 178]. Популяционное исследование (405172 человека, за период 1979-2011) показало, что у взрослых, которые проходили эндоскопическое исследование с биопсией в связи с неонкологическими показаниями, в течение 20 лет рак желудка развивается в одном случае из 256 при нормальной слизистой оболочке желудка, в 1 из 85 при наличии гастрита, в 1 из 50 – атрофического гастрита, в 1 из 39 – кишечной метаплазии и в 1 случае из 19 – при выявлении дисплазии [178]. Исходя их данных этого исследования, можно предположить, что выраженная атрофия и кишечная метаплазия, выявленные в подростковом возрасте, в отсутствие наблюдения могут привести к формированию рака желудка к 40-45 годам, т.е. в молодом трудоспособном возрасте. По данным, полученным при обследовании 1755 пациентов с диспепсией в среднем в течение 55 месяцев неоплазия была выявлена исключительно у лиц с иcходными стадиями OLGA III-IV, риск неоплазии отсутствовал у пациентов со стадией OLGA 0, I и II, составил 36,5 на 1000 человеко-лет при стадии III и 63,1 на 1000 человеко-лет при стадии IV [184]. Даже незначительно выраженная кишечная метаплазия существенно повышала риск рака желудка [180, 181]. Наличие кишечной метаплазии (как маркера выраженного гастрита) может иметь даже большее значение, чем степень атрофии без кишечной метаплазии, причем неполная кишечная метаплазия является прогностически неблагоприятным фактором развития рака желудка по сравнению с полной кишечной метаплазией, ее следует рассматривать как дополнительное условие определения сроков наблюдения пациентов с гастритом [184, 185]. Дополнительным фактором риска рака желудка служит наличие близких родственников, страдающих раком желудка [186, 187].
Вакцинация
Гастриты и дуодениты не являются противопоказаниями к проведению вакцинации с использованием вакцин любого типа [Приказ Минздрава России от 06.12.2021 №1122н «Об утверждении национального календаря профилактических прививок и календаря профилактических прививок по эпидемическим показаниям», Методические указания МУ 3.3.1.1095—02. Медицинские противопоказания к проведению профилактических прививок препаратами национального календаря прививок], а также для вакцинации против коронавирусной инфекции нового типа (COVID-19), в соответствии с инструкциями к препаратам
6. Организация оказания медицинской помощи
Большинство пациентов с гастритом и дуоденитом подлежат наблюдению и лечению в амбулаторных условиях.
В зависимости от необходимости, может быть оказана медицинская помощь любого вида, условия, формы, предусмотренных законодательством Российской Федерации.
Показания для госпитализации в медицинскую организацию:
1. выраженный абдоминальный болевой синдром (8-10 баллов по десятибалльной шкале)
2. необходимость проведения эрадикационной терапии под врачебным контролем при высоком риске развития аллергических реакций или антибиотико-ассоциированной диареи
3. необходимость выполнения эндоскопического исследования с множественной биопсией под наркозом
4. наличие признаков желудочно-кишечного кровотечения у пациента с подозрением на эрозивный гастрит и/или дуоденит -показание для экстренной госпитализации
5. социальные показания (невозможность проведения обследования /лечения в амбулаторных условиях)
Организация диетического лечебного питания пациентов с гастритами и дуоденитами при стационарном лечении в медицинских организациях проводится в соответствии с приказом Минздрава России от 23 сентября 2020г. №1008н «Об утверждении порядка обеспечения пациентов лечебным питанием» (Приложение 3).
Показания к выписке пациента из медицинской организации:
1. установление клинического диагноза, купирование болевого синдрома и исключение острой хирургической патологии
2. окончание курса эрадикационной терапии H.pylori
3. выполнение эндоскопического исследования
4. остановка желудочно-кишечного кровотечения
7. Дополнительная информация (в том числе факторы, влияющие на исход заболевания или состояния)
При своевременном лечении и отсутствии признаков атрофии высокой степени, метаплазии и дисплазии в слизистой оболочке желудка прогноз благоприятный. По мере усугубления структурных изменений слизистой оболочки желудка прогноз в отношении течения заболевания и риска развития рака желудка ухудшается.
Критерии оценки качества медицинской помощи
|
№ |
Критерии качества |
Оценка выполнения (да/нет) |
|
1. |
Выполнен общий (клинический) анализ крови развернутый с определением уровня гемоглобина, гематокрита, эритроцитов, цветового показателя, тромбоцитов, лейкоцитов с лейкоцитарной формулой |
Да/нет |
|
2. |
Проведена ЭГДС пациентам с подозрением на гастрит и дуоденит, имеющим показания к проведению эндоскопического исследования |
Да/нет |
|
3. |
Выполнено определение инфицированности H.pylori при первичной диагностике – 13С-уреазный дыхательный тест на Helicobacter Pylori (быстрый уреазный тест), Микроскопическое исследование материала желудка на хеликобактер пилори (Helicobacter pylori) или Микробиологическое (культуральное) исследование биоптата стенки желудка на хеликобактер пилори (Helicobacter pylori), Микробиологическое (культуральное) исследование биоптатов слизистой желудка хеликобактер пилори (Helicobacter pylori). |
Да/нет |
|
4. |
Проведена эрадикационная терапия (при выявлении показаний к эрадикации H.pylori ) |
Да/нет |
Список литературы
1. Гастрит. Большая Медицинская Энциклопедия. Главный редактор Б. В. Петровский. издание третье, онлайн версия [электронный ресурс]. URL: https://xn--90aw5c.xn--c1avg/index.php/%D0%93%D0%90%D0%A1%D0%A2%D0%A0%D0%98%D0%A2?ysclid=lymyg9unjq151124601 (дата обращения 15.07.2024). [Gastritis. A Large Medical Encyclopedia. Editor-in-chief B. V. Petrovsky. third edition, online version [electronic resource]. URL: https://xn--90aw5c.xn--c1avg/index.php/%D0%93%D0%90%D0%A1%D0%A2%D0%A0%D0%98%D0%A2?ysclid=lymyg9unjq151124601 (accessed 07/15/2024)].
2. Маев И.В., Самсонов А.А., Андреев Д.Н. Болезни желудка. М., 2015; 976 с. [Mayev I.V., Samsonov A.A., Andreev D.N. Stomach diseases. M., 2015; 976 p.]
3. Дуоденит. Большая Медицинская Энциклопедия. Главный редактор Б. В. Петровский. издание третье, онлайн версия [электронный ресурс]. URL: https://xn--90aw5c.xn--c1avg/index.php/%D0%94%D0%A3%D0%9E%D0%94%D0%95%D0%9D%D0%98%D0%A2?ysclid=lymyzwuyfn133880326 (дата обращения 15.07.2024) [Duodenite. A Large Medical Encyclopedia. Editor-in-chief B. V. Petrovsky. third edition, online version [electronic resource]. URL: https://xn--90aw5c.xn--c1avg/index.php/%D0%94%D0%A3%D0%9E%D0%94%D0%95%D0%9D%D0%98%D0%A2?ysclid=lymyzwuyfn133880326 (accessed 07/15/2024)].
4. Correa P. Gastric cancer: overview. Gastroenterol Clin North Am. 2013;42(2):211-217. doi:10.1016/j.gtc.2013.01.002.
5. International Agency for Research on Cancer. IARC (1994) Schistosomes, Liver Flukes and Helicobacter Pylori (IARC Monographs on the Evaluation of Carcinogenic Risks to Humans, Vol. 61), Lyon, IARC [электронный ресурс]. URL: https://www.iarc.who.int/world-cancer-report-content-overview/ (дата обращения 21.03.2024).
6. Барышникова Н.В., Суворов А.Н., Ткаченко Е.И., Успенский Ю.П. Роль генетических особенностей Helicobacter pylori в патогенезе заболеваний органов пищеварения: от теории к практике. Экспериментальная и клиническая гастроэнтерология. 2009; 1: 12-19. [Baryshnikova N.V., Suvorov A.N., Tkachenko E.I., Uspensky Yu.P. The role of genetic features of Helicobacter pylori in the pathogenesis of diseases of the digestive system: from theory to practice. Experimental and clinical gastroenterology. 2009; 1: 12-19].
7. Farinati F, Cardin R, Russo VM, Busatto G, Franco M, Rugge M. Helicobacter pylori CagA status, mucosal oxidative damage and gastritis phenotype: a potential pathway to cancer? Helicobacter. 2003 Jun;8(3):227-34. doi: 10.1046/j.1523-5378.2003.00149.x.
8. Tran SC, Bryant KN, Cover TL. The Helicobacter pylori cag pathogenicity island as a determinant of gastric cancer risk. Gut Microbes. 2024 Jan-Dec;16(1):2314201. doi: 10.1080/19490976.2024.2314201.
9. Malfertheiner P., Megraud F., O"Morain C. et al. Current concepts in the management of Helicobacter pylori infection: the Maastricht III Consensus Report. Gut. 2007; 56 (6): 772–81. doi: 10.1136/gut.2006.101634.
10. Malfertheiner P, Megraud F, Rokkas T et al. Management of Helicobacter pylori infection: the Maastricht VI/Florence consensus report. Gut. 2022 Aug 8:gutjnl-2022-327745. doi: 10.1136/gutjnl-2022-327745.
11. Сапожников В. Г. Особенности морфологических изменений слизистой оболочки при хроническом хеликобактерассоциированном гастродуодените у детей. Экспериментальная и клиническая гастроэнтерология 2018;149(1): 33–37. [Sapozhnikov VG. [Peculiarities of morphological changes of mucous membrane in chronic helicobacteraceae gastroduodenitis in children]. Eksp Klin Gastroenterol. 2018; 149(1): 33-37. (In Russ.)].
12. Islek A, Yilmaz A, Elpek GO, Erin N. Childhood chronic gastritis and duodenitis: Role of altered sensory neuromediators. World J Gastroenterol 2016; 22(37): 8349-8360 [PMID: 27729741 DOI: 10.3748/wjg.v22.i37.8349] Атрофические изменения СОЖ чаще встречаются во взрослом возрасте.
13. Kivrak Salim D, Sahin M, Köksoy S, Adanir H, Süleymanlar I. Local Immune Response in Helicobacter pylori Infection. Medicine (Baltimore). 2016 May; 95(20):e3713. doi: 10.1097/MD.0000000000003713.
14. Хомерики С.Г. Helicobacter pylori – индуктор и эффектор окислительного стресса в слизистой оболочке желудка: традиционные представления и новые данные. Экспериментальная и клиническая гастроэнтерология. 2006; 1: 37-46. [Khomeriki SG. [Helicobacter pylori as an inductor and effecter of the oxidative stress in the stomach mucosa: traditional views and new data]. Eksp Klin Gastroenterol. 2006; 1: 37-46. (In Russ.)].
15. Исаков В.А., Домарадский И.В. Хеликобактериоз. М.: Медпрактика, 2003, 412 с. [Isakov V.A., Domaradsky I.V. Helicobacteriosis. M.: Medpraktika, 2003, 412 p.].
16. Заблодский А.Н., Крылов Ю.В., Крылов А.Ю. Желудочная метаплазия и язвенная болезнь двенадцатиперстной кишки у детей, инфицированных Helicobacter pylori. ВЕСТНИК ВГМУ, 2003, ТОМ 2, №4, с. 60-66. [Zablodsky A.N., Krylov Yu.V., Krylov A.Yu.. Gastric metaplasia and duodenal ulcer in children infected with Helicobacter pylori.Vitebsk Medical JoUrnal. 2003;1 (4):60-66. (In Russ.)
17. Симаненков В.И., Маев И.В., Ткачева О.Н, Алексеенко С.А., Андреев Д.Н., Бордин Д.С. и соавт. Синдром повышенной эпителиальной проницаемости в клинической практике. Мультидисциплинарный национальный консенсус. Кардиоваскулярная терапия и профилактика. 2021;20(1):2758. doi:10.15829/1728-8800-2021-2758. [Simanenkov V.I., Maev I.V., Tkacheva O.N., Alekseenko S.A., Andreev D.N., Bordin D.S., et al. Syndrome of increased epithelial permeability in clinical practice. Multidisciplinary national Consensus. Cardiovascular Therapy and Prevention. 2021;20(1):2758. (In Russ.) https://doi.org/10.15829/1728-8800-2021-2758].
18. Dursun N., Hacihasanoglu E., Oksu O., et al. Epstein-Barr virus infection in patients with chronic gastritis without Helicobacter pylori infection. Turk J Gastroenterol. 2020;31(3):205-10. Doi: 10.5152/tjg.2020.18850.
19. Волынец Г.В. Клинические и диагностические особенности и принципы терапии аутоиммунного гастрита у детей. Детская гастроэнтерология. 2005; 3: 33–37. URL: http://www.gastroscan.ru/literature/authors/824. [Volynets G.V. Clinical and diagnostic features and principles of therapy of autoimmune gastritis in children. Pediatric gastroenterology. 2005; 3: 33–37. URL: http://www.gastroscan.ru/literature/authors/824].
20. Saglietti C, Sciarra A, Abdelrahman K, Schneider V, Karpate A, Nydegger A, Sempoux C. Autoimmune Gastritis in the Pediatric Age: An Underestimated Condition Report of Two Cases and Review. Front Pediatr. 2018 May 1;6:123. doi: 10.3389/fped.2018.00123.
21. Ikuse T., Blanchard T.G., Czinn S.J. Inflammation, Immunity, and Vaccine Development for the Gastric Pathogen Helicobacter pylori. Curr Top Microbiol Immunol. 2019; 421: 1–19. DOI: 10.1007/978–3–030–15138–6_1 .
22. Malfertheiner P., Camargo M.C., El-Omar E., Liou J.M., Peek R., Schulz C., et al. Helicobacter pylori infection. Nat Rev Dis Primers. 2023;9(1):19. DOI: 10.1038/s41572–023– 00431–8 .
23. Zhang Y., Weck M.N., Schöttker B., Rothenbacher D., Brenner H. Gastric parietal cell antibodies, Helicobacter pylori infection, and chronic atrophic gastritis: evidence from a large population-based study in Germany. Cancer Epidemiol Biomarkers Prev. 2013; 22(5): 821–6. DOI: 10.1158/1055–9965. EPI-12–1343.
24. Demir A.M., Berberoğlu Ateş B., Hızal G., Yaman A., Tuna Kırsaçlıoğlu C., Oğuz A.S., et al. Autoimmune atrophic gastritis: The role of Helicobacter pylori infection in children. Helicobacter. 2020; 25(5): e12716. DOI: 10.1111/hel.12716 .
25. Moreira-Silva H., Silva G., Costa E., Guerra I., Santos-Silva E., Tavares M., et al. Insights Into Pediatric Autoimmune Gastritis: Is There a Role for Helicobacter pylori Infection? J Pediatr Gastroenterol Nutr. 2019; 68(6): e99–e104. DOI: 10.1097/MPG.0000000000002278.
26. Новикова В.П. Этиопатогенетические и клинико-морфологические особенности хронического гастрита в разном возрасте: автореф. дис. … д-ра мед.наук. СПб., 2009, 48 с. [Novikova V.P. Etiopathogenetic and clinical morphological features of chronic gastritis at different ages: abstract. ... Doctor of Medical Sciences. St. Petersburg, 2009, 48 p].
27. Звягин А.А. Аутоиммунный гастрит у детей с аутоиммунными заболеваниями. Педиатр. 2013; IV (4): 44-47. [Zvyagin A.A. Autoimmune gastritis in children with autoimmune diseases. Pediatrician. 2013; IV (4): 44-47].
28. Hall S.N., Appelman H.D. Autoimmune Gastritis. Arch Pathol Lab Med. 2019; 143(11):1327-1331. doi: 10.5858/arpa.2019-0345-RA.
29. Rodriguez-Castro K.I., Franceschi M., Miraglia C., Russo M., Nouvenne A., Leandro G., et al. Autoimmune diseases in autoimmune atrophic gastritis. Acta Biomed. 2018; 89(8-S):100-103. doi: 10.23750/abm.v89i8-S.7919.
30. Veijola LI, Oksanen AM, Sipponen PI, Rautelin HI. Association of autoimmune type atrophic corpus gastritis with Helicobacter pylori infection. World J Gastroenterol. 2010 Jan 7;16(1):83-8. doi: 10.3748/wjg.v16.i1.83.
31. Hall S.N., Appelman H.D. Autoimmune Gastritis. Arch Pathol Lab Med. 2019; 143(11): 1327–1331. DOI: 10.5858/ arpa.2019–0345-RA.
32. Волынец Г.В. Хронический гастрит у детей. LAP LAMBERT, Германия, 2013; 356. [Volynets G.V. Chronic gastritis in children. LAP LAMBERT, Germany, 2013; 356. (in Russ.)] ISBN: 978–3–659–35473–1].
33. Rusak E., Chobot A., Krzywicka A., Wenzlau J. Anti-parietal cell antibodies — diagnostic significance. Adv Med Sci. 2016; 61(2): 175–179. DOI: 10.1016/j.advms.2015.12.004.
34. Sugano K., Tack J., Kuipers E.J., Graham D.Y., El-Omar E.M., Miura S. et al. Kyoto global consensus report on Helicobacter pylori gastritis Gut 2015;64:1353–1367. doi: 10.1136/gutjnl-2015-309252.
35. Маев И.В., Андреев Д.Н., Самсонов А.А., Дичева Д.Т., Парцваниа-Виноградова Е.В. Эволюция представлений о дефиниции, классификации, диагностике и лечении гастрита, ассоциированного с инфекцией helicobacter pylori (по материалам киотского консенсуса, 2015). Фарматека. 2016;6:24–33. [Mayev I.V., Andreev D.N., Samsonov A.A., Dicheva D.T., Partsvania-Vinogradova E.V. Evolution of ideas about the definition, classification, diagnosis and treatment of gastritis associated with helicobacter pylori infection (based on the Kyoto Consensus, 2015). Pharmateca. 2016;6:24–33].
36. Калинина Е.Ю., Крулевский В.А., Новикова В.П., Цех О.М.Этиология хронического гастродуоденита (хгд) у детей и подростков. Гастроэнтерология Санкт-Петербурга. 2011; 4: M13-M13a. [Kalinina E.Yu., Krulevsky V.A., Novikova V.P., Tsekh O.M. Etiology of chronic gastroduodenitis (hcg) in children and adolescents. Gastroenterology of St. Petersburg. 2011; 4: M13-M13a].
37. Чернин В.В. Болезни пищевода, желудка и двенадцатиперстной кишки: Руководство для врачей. М.: ООО «Медицинское информационное агентство»: 2010, 528 с. [Chernin V.V. Diseases of the esophagus, stomach and duodenum: A guide for doctors. M.: LLC "Medical Information Agency": 2010, 528 p.].
38. Калинина Е.Ю., Новикова В.П., Цех О.М. Особенности морфологической перестройки слизистой оболочки двенадцатиперстной кишки при длительном воздействии алкоголя. Профилактическая и клиническая медицина. 2011; 2-1 (39): 80-85. [Kalinina E.Yu., Novikova V.P., Workshop O.M. Features of morphological restructuring of the duodenal mucosa during prolonged exposure to alcohol. Preventive and clinical medicine. 2011; 2-1 (39): 80-85].
39. Мельникова И.Ю., Новикова В.П., Горюнова М.М., Крулевский В.А., Петровский А.Н., Калинина Е.Ю., Цех О.М. Гетерогенность хронического гастродуоденита у детей. Российский вестник перинатологии и педиатрии. 2010; 55 (2): 81-86. [Melnikova I.Yu., Novikova V.P., Goryunova M.M., Krulevsky V.A., Petrovsky A.N., Kalinina E.Yu., Tsekh O.M. Heterogeneity of chronic gastroduodenitis in children. Russian Bulletin of Perinatology and Pediatrics. 2010; 55 (2): 81-86].
40. Новикова В.П., Калинина Е.Ю. Современные представления о хроническом дуодените у детей. В сборнике: Традиции и инновации петербургской педиатрии. Сборник трудов научно-практической конференции. Под редакцией А.С. Симаходского, В.П. Новиковой, Т.М. Первуниной, И.А. Леоновой. 2017. С. 73-94. [Novikova V.P., Kalinina E.Y. Modern ideas about chronic duodenitis in children. In the collection: Traditions and innovations of St. Petersburg pediatrics. Proceedings of the scientific and practical conference. Edited by A.S. Simakhodsky, V.P. Novikova, T.M. Pervukhina, I.A. Leonova. 2017. pp. 73-94].
41. Успенский Ю.П., Суворов А.Н., Барышникова Н.В. -СПб.: ИнформМед, 2011. – 572 с.:ил., 16 с. цв. вкл. ISBN 978-5-904192-46-4. [Uspensky Yu.P., Suvorov A.N., Baryshnikova N.V. -St. Petersburg: InformMed, 2011. – 572 p.:ill., 16 p. color. incl. ISBN 978-5-904192-46-4.].
42. Чернин В.В. Значение Helicobacter pylori в нормомикробиоценозе и дисбактериозе мукозной микрофлоры эзофагогастродуоденальной зоны при ее воспалительно-эрозивно-язвенных поражениях. Верхневолжский медицинский журнал. 2011; 9 (4): 72-78. [Chernin V.V. The importance of Helicobacter pylori in the normomicrobiocenosis and dysbiosis of the mucosal microflora of the esophagogastroduodenal zone in its inflammatory erosive and ulcerative lesions. The Upper Volga Medical Journal. 2011; 9 (4): 72-78].
43. Чернин В.В. Нарушение симбионтного пищеварения и дисбактериоз пищеварительного тракта человека. Экспериментальная и клиническая гастроэнтерология. 2017; 11 (147): 96-100. [Chernin V.V. Violation of symbiotic digestion and dysbiosis of the human digestive tract. Experimental and clinical gastroenterology. 2017; 11 (147): 96-100].
44. Микробиота желудочно-кишечного тракта при хроническом гастрите. под ред. А.Н. Суворова, В.П. Новиковой, И.Ю. Мельниковой. – СПб: ИнформМед, 2014, 210 с. [Microbiota of the gastrointestinal tract in chronic gastritis. edited by A.N. Suvorov, V.P. Novikova, I.Y. Melnikova. – St. Petersburg: InformMed, 2014, 210 p.].
45. Бельмер С.В., Разумовский А.Ю., Хавкин А.И. и др. Болезни желудка и двенадцатиперстной кишки у детей. М., 2017. 536 с. [Belmer S.V., Razumovsky A.Y., Khavkin A.I., et al. Diseases of the stomach and duodenum in children. M: Medpraktika-M, 2017. 536 p. (In Russ.)].
46. Запруднов A.M., Григорьев К.И. Современные особенности подростковой гастроэнтерологии. Педиатрия. 2011; 90(2):6. [Zaprudnov A.M., Grigoriev K.I. Modern features of adolescent gastroenterology. Pediatrics. 2011; 90(2):6].
47. Бордин Д.С., Кузнецова Е.С., Стаувер Е.Е., Никольская К.А., Чеботарева М.В., Войнован И.Н., Неясова Н.А. Эпидемиология инфекции Helicobacter pylori в Российской Федерации с 1990 по 2023 г.: систематический обзор. РМЖ. Медицинское обозрение. 2024;8(5):260-267. DOI: 10.32364/2587-6821-2024-8-5-3. [Bordin D.S., Kuznetsova E.S., Stauver E.E., Nikolskaya K.A., Chebotareva M.V., Voynovan I.N., Neyasova N.A. Epidemiology of Helicobacter pylori infection in the Russian Federation from 1990 to 2023: a systematic review. Medical review. 2024;8(5):260-267. DOI: 10.32364/2587-6821-2024-8-5-3].
48. Reshetnikov O.V., Häivä V.M., Granberg C. et al. Seroprevalence of Helicobacter pylori infection in Siberia. Helicobacter. 2001;6(4):331–336. DOI: 10.1046/j.1523-5378.2001.00045.x.
49. Tkachenko M.A., Zhannat N.Z., Erman L.V. et al. Dramatic changes in the prevalence of Helicobacter pylori infection during childhood: a 10-year follow-up study in Russia. J Pediatr Gastroenterol Nutr. 2007;45(4):428–432. DOI: 10.1097/MPG.0b013e318064589f.
50. Сварваль А.В., Ферман Р.С., Жебрун А.Б. Изучение динамики превалентности инфекции, обусловленной Helicobacter pylori, среди различных возрастных групп населения Санкт-Петербурга в 2007–2011 годах. Инфекция и иммунитет. 2014;2(4):741–746. DOI: 10.15789/2220-7619-2012-4-741-746. [Svarval A.V., Ferman R.S., Zhebrun A.B. Study of the dynamics of the prevalence of infection caused by Helicobacter pylori among various age groups of the population of St. Petersburg in 2007–2011. Infection and immunity. 2014;2(4):741–746 (in Russ.). DOI: 10.15789/2220-7619-2012-4-741-746].
51. Жесткова Т.В., Бутов М.А., Лымарь Ю.Ю., Папков С.В. Распространенность инфекции Helicobacter pylori среди жителей Рязанского региона. Российский медико-биологический вестник им. акад. И.П. Павлова. 2019;27(1):35–40. DOI: 10.23888/PAVLOVJ201927135-40. [Zhestkova T.V., Butov M.A., Lymar Yu.Yu., Papkov S.V. Prevalence of Helicobacter pylori infection among residents of the Ryazan region. Russian Medical and Biological Bulletin named after. acad. I.P. Pavlova. 2019;27(1):35–40 (in Russ.). DOI: 10.23888/PAVLOVJ201927135-40].
52. Blomquist L, Hirata I, Slezak P, Ohshiba S. Duodenitis--distinguishing features in a retrospective endoscopic and histological study. Hepatogastroenterology. 1994 Dec;41(6):537-41.
53. Бельмер С.В., Хавкин А.И. Гастроэнтерология детского возраста. М.: ИД Медпрактика-М, 2008; 360 с. (Belmer SV, Khavkin AI. Gastroenterology childhood. M.: ID Medpraktika-M, 2008; 360).
54. Хавкин А.И., Новикова В.П. Хронический гастрит у детей: новые возможности диетотерапии. Фарматека. 2022; 9: 18-25. DOI: https://dx.doi.org/10.18565/pharmateca.2022.9.18-25 [Хавкин А.И., Новикова В.П. Хронический гастрит у детей: новые возможности диетотерапии. Фарматека. 2022; 9: 18-25. DOI: https://dx.doi.org/10.18565/pharmateca.2022.9.18-25].
55. Бельмер С.В., Гасилина Т.В. Хронический гастродуоденит у детей. Спорные вопросы. Рос. вестн. перинатологии и педиатрии. 2009; 54 (3): 80–83. [Belmer S.V., Gasilina T.V. Chronic gastroduodenitis in children. Controversial issues. Ros. vestn. perinatology and pediatrics. 2009; 54 (3): 80–83].
56. Детская гастроэнтерология: рук. для врачей. Под ред. Н.П. Шабалова. 2-е изд., перераб. и доп. М., 2013. 760 с. [Pediatric gastroenterology: hands. for doctors. Edited by N.P. Shabalov. 2nd ed., reprint. and additional M., 2013. 760 s].
57. Иванов Д.О., Новикова В.П., Алешина Е.И. и др. Руководство по педиатрии. Том 6. Гастроэнтерология детского возраста. СПб.,2022. [Ivanov D.O., Novikova V.P., Aleshina E.I., et al. Guidelines for Pediatrics. Volume 6 – Pediatric Gastroenterology. St. Petersburg, 2022 .
58. Мельникова И.Ю., Новикова В.П., Горюнова М.М., Крулевский В.А., Петровский А.Н., Калинина Е.Ю., Цех О.М. Гетерогенность хронического гастродуоденита у детей. Российский вестник перинатологии и педиатрии. 2010; 55 (2): 81-86. [Melnikova I.Yu., Novikova V.P., Goryunova M.M., Krulevsky V.A., Petrovsky A.N., Kalinina E.Yu., Tsekh O.M. Heterogeneity of chronic gastroduodenitis in children. Russian Bulletin of Perinatology and Pediatrics. 2010; 55 (2): 81-86].
59. Конорев М.Р. Хронический хеликобактерный дуоденит. Медицинские новости. 1999; 8: 82-84. [Konorev M.R. Chronic helicobacter duodenitis. Medical news.1999; 8: 82-84].
60. Новикова В.П., Осмаловская Е.А., Калинина Е.Ю. Хеликобактериоз и лямблиоз при хроническом гастродуодените у детей. РМЖ. 2014; 22 (20): 1448-1451. [Novikova V.P., Osmolovskaya E.A., Kalinina E.Y. Helicobacteriosis and giardiasis in chronic gastroduodenitis in children. BC. 2014; 22 (20): 1448-1451].
61. Цветкова Л.Н., Мельникова И.Ю., Новикова В.П. Хронический гастрит и гастродуоденит у детей. Национальное руководство. Педиатрия. Том 1. Под ред. А.А. Баранова. М.: ГЭОТАР-Медиа, 2009, C. 711-722. [Tsvetkova L.N., Melnikova I.Yu., Novikova V.P. Chronic gastritis and gastroduodenitis in children. National leadership. Pediatrics. Volume 1. Edited by A.A. Baranov. M.: GEOTAR-Media, 2009, pp. 711-722].
62. Бельмер С.В., Бехтерева М.К., Калинина Е.Ю., Новикова В.П., Осмаловская Е.А., Шабалов А.М. Лямблиоз. Учебное пособие для врачей. Под редакцией В. П. Новиковой, М. К. Бехтеревой, С. В. Бельмера. Санкт-Петербург, 2014. (2-е издание, исправленное и дополненное). [Belmer S.V., Bekhtereva M.K., Kalinina E.Yu., Novikova V.P., Osmolovskaya E.A., Shabalov A.M. Giardiasis. A textbook for doctors. Edited by V. P. Novikova, M. K. Bekhtereva, S. V. Belmer. St. Petersburg, 2014. (2nd edition, revised and expanded)].
63. Корниенко Е.А., Минина С.Н., Фадина С.А. Клиника, диагностика и лечение лямблиоза у детей. Педиатр. Фармакология. 2009;.6 (4): 2–7. [Kornienko E.A., Minina S.N. Fadina S.A. Clinic, diagnosis and treatment of lyambliosis in detei. Pediatrician. Pharmacology. 2009;.6 (4): 2–7].
64. Мельникова И.Ю., Крулевский В.А., Горюнова М.М., Петровский А.Н., Новикова В.П., Калинина Е.Ю. Тучные клетки в гастродуоденальной слизистой оболочке у детей с ВЭБ-ассоциированным хроническим гастродуоденитом. Вестник Северо-Западного государственного медицинского университета им. И.И. Мечникова. 2011; 2 (4): 64-68. [Melnikova I.Yu., Krulevsky V.A., Goryunova M.M., Petrovsky A.N., Novikova V.P., Kalinina E.Yu. Mast cells in the gastroduodenal mucosa in children with EBV-associated chronic gastroduodenitis. Bulletin of the I.I. Mechnikov Northwestern State Medical University. 2011; 2 (4): 64-68].
65. Маев И.В., Самсонов А.А. Хронический дуоденит (Алгоритм диагностики и лечебной тактики). Пособие для врачей общей практики, терапевтов, гастроэнтерологов: Учебное пособие. - М:, 2007. 80 с. [Mayev I.V., Samsonov A.A. Chronic duodenitis (Algorithm of diagnosis and therapeutic tactics). A manual for general practitioners, internists, gastroenterologists: A textbook. - Moscow:, 2007. 80 s].
66. Tytgat GN. The Sydney System: endoscopic division. Endoscopic appearances in gastritis/duodenitis. J Gastroenterol Hepatol. 1991 May-Jun;6(3):223-34. doi: 10.1111/j.1440-1746.1991.tb01469.x.
67. Белогурова М.Б., Гончар Н.В., Григович И.Н., Думова Н.Б., Корниенко Е.А., Косенко И.М., Луппова Н.Е., Мельникова И.Ю., Новикова В.П., Приворотский В.Ф., Пронина Е.В., Храмцова Е.Г. Детская гастроэнтерология. Практическое руководство. Под редакцией И.Ю. Мельниковой. Москва, 2018. Сер. Библиотека врача-специалиста. [Belogurova M.B., Gonchar N.V., Grigovich I.N., Dumova N.B., Kornienko E.A., Kosenko I.M., Luppova N.E., Melnikova I.Yu., Novikova V.P., Privorotsky V.F., Pronina E.V., Khramtsova E.G. Pediatric gastroenterology. Practical guide. Edited by I.Y. Melnikova. Moscow, 2018. Ser. Library of a specialist doctor].
68. Конорев М.Р. Принципы современной классификации дуоденитов. / М.Р. Конорев, А.М. Литвяков, М.Е. Матвиенко. Клинич. медицина. 2003; 81 (2): 15–16. [Konorev M.R. Principles of modern classification of duodenites. / M.R. Konorev, A.M. Litvyakov, M.E. Matvienko. Clinic. the medicine. 2003; 81 (2): 15–16].
69. Stanghellini V, Chan FK, Hasler WL, Malagelada JR, Suzuki H, Tack J, Talley NJ. Gastroduodenal Disorders. Gastroenterology. 2016 May;150(6):1380-92. doi: 10.1053/j.gastro.2016.02.011.
70. Король С.М., Колупаева Е.А. Болезни желудка и двенадцатиперстной кишки у детей и подростков: Учебно–методическое пособие. Минск, 2005. С. 10. [Korol S.M., Kolupaeva E.A. Diseases of the stomach and duodenum in children and adolescents: An educational and methodological guide. Minsk, 2005. p. 10].
71. Епимахова Ю.В. Взаимосвязь вегетососудистой дистонии и хронического гастродуоденита у подростков. Тула, 2010. [Епимахова Ю.В. Взаимосвязь вегетососудистой дистонии и хронического гастродуоденита у подростков. Тула, 2010].
72. Чернин В.В. Хронический дуоденит. [электронный ресурс]. URL: Код доступа. https://studfile.net/preview/4106367/ (дата обращения 25.07.2024). [Chernin V.V. Chronic duodenitis. [electronic resource]. URL: The access code. https://studfile.net/preview/4106367 / (accessed 07/25/2024)].
73. Валенкевич Л.Н., Яхонтова О.И. Клиническая энтерология. СПб: Гиппократ, 2001. — 288 с. [Valenkevich L.N., Yakhontova O.I. Clinical enterology. St. Petersburg: Hippocrates, 2001. — 288 p.].
74. Hyams J.S., Di Lorenzo C., Saps M. Shulman RJ, Staiano A, van Tilburg M. Functional disorders: children and adolescents. Gastroenterology. 2016. 150:1456–1468. doi: 10.1053/j.gastro.2016.02.015.
75. Yu H., Robertson E.S. Epstein–Barr Virus History and Pathogenesis. Viruses. 2023;15(3):714. DOI: 10.3390/v15030714.
76. Miceli E., Lenti M.V., Padula D., Luinetti O., Vattiato C., Monti C.M. et al. Common features of patients with autoimmune atrophic gastritis. Clin Gastroenterol Hepatol. 2012 Jul;10(7):812-4. doi: 10.1016/j.cgh.2012.02.018.
77. Pruthi H.S., Sharma S.K., Singh B., Anand A.C. Aetiology of upper gastrointestinal haemorrhagean endoscopic study. Med J Armed Forces India. 2000; 56(3):188-191. doi:10.1016/S0377-1237(17)30162-4.
78. Biecker E. Diagnosis and therapy of non-variceal upper gastrointestinal bleeding. World J Gastrointest Pharmacol Ther. 2015; 6(4):172-82. doi: 10.4292/wjgpt.v6.i4.172.
79. Лосик Е.А., Ивашкин В.Т. Гематологические проявления аутоиммунного гастрита. Рос журн гастроэнтерол гепатол колопроктол. 2016;26(1):37-43. doi:10.22416/1382-4376-2016-26=1-37-43. [Losik Y.A., Ivashkin V.T. Hematological manifestations of autoimmune gastritis. Rus J Gastroenterol Hepatol Coloproctol. 2016;26(1):37-43. (In Russ.) https://doi.org/10.22416/1382-4376-2016-26-1-37-43].
80. Tomizawa M., Shinozaki F., Hasegawa R.et al. Low haemoglobin levels are associated with upper gastrointestinal bleeding. Biomed Rep 2016; vol.5 (3): 349-352.
81. Hall S.N., Appelman H.D. Autoimmune Gastritis. Arch Pathol Lab Med. 2019; 143(11):1327-1331. doi: 10.5858/arpa.2019-0345-RA.
82. Rodriguez-Castro K.I., Franceschi M., Miraglia C., Russo M., Nouvenne A., Leandro G., et al. Autoimmune diseases in autoimmune atrophic gastritis. Acta Biomed. 2018; 89(8-S):100-103. doi: 10.23750/abm.v89i8-S.7919.
83. Лосик Е.А., Селиванова Л.С., Антонова Т.В., Лапина Т.Л., Тертычный А.С., Ивашкин В.Т. Морфологические критерии диагноза аутоиммунного гастрита. Российский журнал гастроэнтерологии, гепатологии, колопроктологии. 2016;26(5):13-20. doi:10.22416/1382-4376-2016-26-5-13-20. [Losik Y.A., Selivanova L.S., Antonova T.V., Lapina T.L., Tertychny A.S., Ivashkin V.T. Morphological diagnostic criteria of autoimmune gastritis. Rus J Gastroenterol Hepatol Coloproctol. 2016;26(5):13-20. (In Russ.) https://doi.org/10.22416/1382-4376-2016-26-5-13-20].
84. Белоусов А.С., Водолагин В.Д., Жаков В.П. Диагностика, дифференциальная диагностика и лечение болезней органов пищеварения. М., 2002. 424 с. [Belousov A.S., Vodolagin V.D., Zhakov V.P. Diagnostics, differential diagnosis and treatment of diseases of the digestive system. M., 2002. 424 p].
85. Rusak E., Chobot A., Krzywicka A., Wenzlau J. Anti-parietal cell antibodies - diagnostic significance. Adv Med Sci. 2016; 61(2):175-179. doi: 10.1016/j.advms.2015.12.004.
86. Lahner E., Norman G.L., Severi C., Encabo S., Shums Z., Vannella L. et al. Reassessment of intrinsic factor and parietal cell autoantibodies in atrophic gastritis with respect to cobalamin deficiency. Am J Gastroenterol. 2009; 104(8):2071-9. doi: 10.1038/ajg.2009.231.
87. Huang Y.K., Yu J.C., Kang W.M., Ma Z.-Q., Ye X., Tian S.-B. et al. Significance of serum pepsinogens as a biomarker for gastric cancer and atrophic gastritis screening: a systematic review and meta-analysis. PLoS One. 2015; 10(11):e0142080. doi: 10.1371/journal.pone.0142080.
88. Zagari R.M., Rabitti S., Greenwood D.C., Eusebi L.H., Vestito A., Bazzoli F. Systematic review with meta-analysis: diagnostic performance of the combination of pepsinogen, gastrin-17 and anti-Helicobacter pylori antibodies serum as- says for the diagnosis of atrophic gastritis. Aliment PharmacolTher. 2017; 46(7):657 – 667. doi: 10.1111/apt.14248.
89. Watabe H., Mitsushima T., Yamaji Y., Okamoto M., Wada R., Kokubo T. et al. Predicting the development of gastric cancer from combining Helicobacter pylori antibodies and serum pepsinogen status: a prospective endoscopic cohort study. Gut. 2005; 54(6):764–8. doi: 10.1136/gut.2004.055400.
90. Kurilovich S., Belkovets A., Reshetnikov O., Openko T., Malyutina S., Ragino Y. et al. Stomach-specific Biomarkers (GastroPanel) Can Predict the Development of Gastric Cancer in a Caucasian Population: A Longitudinal Nested Case-Control Study in Siberia. Anticancer Res. 2016; 36(1):247-53. PMID: 26722050.
91. Pimentel-Nunes P., Libânio D., Marcos-Pinto R., Areia M., Leja M., Esposito G. et al. Management of epithelial precancerous conditions and lesions in the stomach (MAPS II): European Society of Gastrointestinal Endoscopy (ESGE), European Helicobacter and Microbiota Study Group (EHMSG), European Society of Pathology (ESP), and Sociedade Portuguesa de EndoscopiaDigestiva (SPED) guideline update 2019. Endoscopy. 2019; 51(4):365-388. doi: 10.1055/a-0859-1883.
92. Banks M., Graham D., Jansen M., Gotoda T., Coda S., di Pietro M. et al. British Society of Gastroenterology guidelines on the diagnosis and management of patients at risk of gastric adenocarcinoma. Gut. 2019; 68(9):1545-1575. doi: 10.1136/gutjnl-2018-318126.
93. Romano C, Oliva S, Martellossi S, Miele E, Arrigo S, Graziani MG, Cardile S, Gaiani F, de"Angelis GL, Torroni F. Pediatric gastrointestinal bleeding: Perspectives from the Italian Society of Pediatric Gastroenterology. World J Gastroenterol. 2017 Feb 28;23(8):1328-1337 Kim Н. Diagnostic and treatment approaches for refractory ulcers. Clin Endoscop 2015; vol.48 (4): 285-290.
94. Sierra D, Wood M, Kolli S, Felipez LM. Pediatric Gastritis, Gastropathy, and Peptic Ulcer Disease. Pediatr Rev. 2018 Nov;39(11):542-549.
95. Бельмер С. В., Корниенко Е. А., Волынец Г. В., Гурова М. М., Звягин А. А., Камалова А. А., Луппова Н. Е., Нижевич А. А., Новикова В. П., Печкуров Д. В., Приворотский В. Ф., Сатаев В. У., Тяжева А. А., Файзуллина Р. А., Хавкин А. И. Диагностика и лечение хеликобактерной инфекции у детей. Рекомендации общества детских гастроэнтерологов, гепатологов, нутрициологов. Редакция от 15.10.2021 г. Экспериментальная и клиническая гастроэнтерология. 2021;193(9): 119–127. doi: 10.31146/1682-8658-ecg-193-9-119-127. [Belmer S. V., Kornienko E. A., Volynets G. V., Gurova M. M., Zvyagin A. A., Kamalova A. A., Luppova N. E., Nizhevich A. A., Novikova V. P., Pechkurov D. V., Privorotsky V. F., Sataev V. U., Tyazheva A. A., Fayzullina R. A., Khavkin A. I. Diagnosis and treatment of helicobacter pylori infection in children. Recommendations of the Society of Pediatric gastroenterologists, hepatologists, nutritionists. Edition of 10/15/2021 Experimental and clinical gastroenterology. 2021;193(9): 119–127. doi: 10.31146/1682-8658-ecg-193-9-119-127].
96. Tringali A, Thomson M, Dumonceau JM, et al. Pediatric gastrointestinal endoscopy: European Society of Gastrointestinal Endoscopy (ESGE) and European Society for Paediatric Gastroenterology Hepatology and Nutrition (ESPGHAN) Guideline Executive summary. Endoscopy. 2017; 49: 83–91. doi: 10.1055/s-0042–111002.
97. East J.E., Vleugels J.L., Roelandt P., Bhandari P., Bisschops R., Dekker E. et al. Advanced endoscopic imaging: European Society of Gastrointestinal Endoscopy (ESGE) Technology Review. Endoscopy. 2016;48(11):1029-1045. doi: 10.1055/s-0042-118087.
98. Rugge M., Genta R.M., Fassan M., Valentini E., Coati I., Guzzinati S. et al. OLGA Gastritis Staging for the Prediction of Gastric Cancer Risk: A Long-term Follow-up Study of 7436 Patients. Am J Gastroenterol. 2018; 113(11):1621-1628. doi: 10.1038/s41395-018-0353-8.
99. Mao X.Y., Xu S.F., Liu Q., Jiang J.X., Zhang H.H., Sang H.M. et al. Anatomical predilection of intestinal metaplasia based on 78,335 endoscopic cases. Saudi J Gastroenterol. 2016; 22(2):154-60. doi: 10.4103/1319-3767.178528.
100. Kim Y.I., Kook M.C., Cho S.J., Lee J.Y., Kim C.G., Joo J. et al. Effect of biopsy site on detection of gastric cancer high-risk groups by OLGA and OLGIM stages. Helicobacter. 2017; 22(6). doi:10.1111/hel.12442.
101. Isajevs S., Liepniece-Karele I., Janciauskas D., Moisejevs G., Funka K., Kikuste I. et al. The effect of incisura angularis biopsy sampling on the assessment of gastritis stage. Eur J Gastroenterol Hepatol. 2014; 26(5):510 – 513. doi: 10.1097/MEG.0000000000000082.
102. Varbanova M., Wex T., Jechorek D., Röhl F.W., Langner C., Selgradet M. et al. Impact of the angulus biopsy for the detection of gastric preneoplastic conditions and gastric cancer risk assessment. J Clin Pathol. 2016; 69(1):19 – 25. doi: 10.1136/jclinpath-2015-202858
103. Lan H.C., Chen T.S., Li A.F., Chang F.Y., Lin H.C. Additional corpus biopsy enhances the detection of Helicobacter pylori infection in a background of gastritis with atrophy. BMC Gastroenterol. 2012;12:182. doi: 10.1186/1471-230X-12-182.
104. Shin C.M., Kim N., Lee H.S., Lee H.E., Lee S.H., Park Y.S. et al. Validation of diagnostic tests for Helicobacter pylori with regard to grade of atrophic gastritis and/or intestinal metaplasia. Helicobacter. 2009;14(6):512-9. doi: 10.1111/j.1523-5378.2009.00726.x
105. Dixon M.F., Genta R.M., Yardley J.H., Correa P. Classification and grading of gastritis. The updated Sydney System. International Workshop on the Histopathology of Gastritis, Houston 1994. Am. J. Surg. Pathol. 1996; 20(10):1161-81. doi: 10.1097/00000478-199610000-00001
106. Schreiber- Dietrich D., Hocke M., Braden B., Carrara S., Gottschalk U., Dietrich C. F. Pediatric Endoscopy, Update 2020. Applied Sciences. 2019; 9(23):5036. Doi:10.3390/app9235036 .
107. Детская гастроэнтерология. Национальное руководство. Под ред. С.В. Бельмера, А.Ю. Разумовского, А.И. Хавкина. М., 2022. 856 с. [Pediatric gastroenterology. National leadership. Edited by S.V. Belmer, A.Y. Razumovsky, A.I. Khavkin. M., 2022. 856 p].
108. Picone D, Rusignuolo R, Midiri F, Lo Casto A, Vernuccio F, Pinto F, Lo Re G. Imaging Assessment of Gastroduodenal Perforations. Semin Ultrasound CT MR. 2016 Feb;37(1):16-22. doi: 10.1053/j.sult.2015.10.006.
109. Jones NL, Koletzko S, Goodman K, Bontems P, Cadranel S, Casswall T, Czinn S, Gold BD, Guarner J, Elitsur Y, Homan M, Kalach N, Kori M, Madrazo A, Megraud F, Papadopoulou A, Rowland M; ESPGHAN, NASPGHAN. Joint ESPGHAN/NASPGHAN Guidelines for the Management of Helicobacter pylori in Children and Adolescents (Update 2016). J Pediatr Gastroenterol Nutr. 2017 Jun;64(6):991-1003. doi: 10.1097/MPG.0000000000001594.
110. Calvet X. Diagnosis of Helicobacter pylori Infection in the Proton Pump Inhibitor Era. Gastroenterol Clin North Am. 2015 Sep;44(3):507-18. doi: 10.1016/j.gtc.2015.05.001.
111. Bak-Romaniszyn L, Wojtuń S, Gil J, Płaneta-Małecka I. Choroba wrzodowa--etiopatogeneza, rozpoznawanie i leczenie [Peptic ulcer disease etiology, diagnosis and treatment]. Pol Merkur Lekarski. 2004;17 Suppl 1:128-32. Polish.
112. Crowley E, Bourke B, Hussey S. How to use Helicobacter pylori testing in paediatric practice. Arch Dis Child Educ Pract Ed. 2013 Feb;98(1):18-25. doi: 10.1136/archdischild-2012-301642.
113. Leal YA, Flores LL, Fuentes-Pananá EM, Cedillo-Rivera R, Torres J. 13C-urea breath test for the diagnosis of Helicobacter pylori infection in children: a systematic review and meta-analysis. Helicobacter. 2011 Aug;16(4):327-37. doi: 10.1111/j.1523-5378.2011.00863.x.
114. Аронова Е. Б., Коломина Е. О., Дмитриенко М. А., Сварваль А. В., Рощина Н. Г., Кунилова Е. С., Антипова М. В., Зарубова И. А. Быстрый уреазный ХЕЛПИЛ-тест: от моделирования к клинической практике. Гастроэнтерология Санкт-Петербурга. 2017-07-01;(3):25-29. [102. Aronova E. B., Kolomina E. O., Dmitrienko M. A., Svarval A.V., Roshchina N. G., Kunilova E. S., Antipova M. V., Zarubova I. A. Rapid urease HELP test: from modeling to clinical practice. Gastroenterology of St. Petersburg. 2017-07-01;(3):25-29].
115. Dixon MF, Genta RM, Yardley JH, Correa P. Histological classification of gastritis and Helicobacter pylori infection: an agreement at last? The International Workshop on the Histopathology of Gastritis. Helicobacter. 1997 Jul;2 Suppl 1:S17-24. doi: 10.1111/j.1523-5378.1997.06b09.x.
116. Seo JH, Park JS, Yeom JS, Lim JY, Park CH, Woo HO, Baik SC, Lee WK, Cho MJ, Rhee KH, Youn HS. Correlation between positive rate and number of biopsy samples on urease test in childhood Helicobacter pylori infection. J Korean Med Sci. 2014 Jan;29(1):106-9. doi: 10.3346/jkms.2014.29.1.106.
117. Roma E., Miele E. He li co bac ter py lo ri Infection in Pediatrics. Helicobacter. 2015 Sep;20 Suppl 1:47–53. doi: 10.1111/hel.12257.
118. Корниенко Е. А. Инфекция Helicobacter pylori у детей. – ГЭОТАР-медиа, М., 2011, 272 с. [Kornienko E. A. Helicobacter pylori infection in children. Moscow. GEOTAR-media Publ., 2011, 272 p. (in Russ.)].
119. Best LM, Takwoingi Y, Siddique S, Selladurai A, Gandhi A, Low B, Yaghoobi M, Gurusamy KS. Non-invasive diagnostic tests for Helicobacter pylori infection. Cochrane Database Syst Rev. 2018 Mar 15;3(3):CD012080. doi: 10.1002/14651858.CD012080.pub2.
120. Makristathis A., Hirschi A. M., Megraud F., Bessede E. Review: Diagnosis of He li co bac ter py lo ri infection. Helicobacter. 2019; 24(S1): e12641. doi: 10.1111/hel.12641.
121. Emiroglu HH, Sokucu S, Suoglu OD, Gulluoglu M, Gokce S. Is there a relationship between Helicobacter pylori infection and erosive reflux disease in children? Acta Paediatr. 2010 Jan;99(1):121-5. doi: 10.1111/j.1651-2227.2009.01512.x.
122. Llanes R, Millán LM, Escobar MP, Gala A, Capó V, Feliciano O, Gutiérrez O, Llop A, Ponce F, Pérez-Pérez GI. Low prevalence of Helicobacter pylori among symptomatic children from a hospital in Havana, Cuba. J Trop Pediatr. 2012 Jun;58(3):231-4. doi: 10.1093/tropej/fmr060.
123. Mansour MM, Al Hadidi KhM, Omar MA. Helicobacter pylori and recurrent abdominal pain in children: is there any relation? Trop Gastroenterol. 2012 Jan-Mar;33(1):55-61. doi: 10.7869/tg.2012.9.
124. Ganesh M, Nurko S. Functional dyspepsia in children. Pediatr Ann. 2014 Apr;43(4):e101-5. doi: 10.3928/00904481-20140325-12.
125. Thakkar K, Chen L, Tessier ME, Gilger MA. Outcomes of children after esophagogastroduodenoscopy for chronic abdominal pain. Clin Gastroenterol Hepatol. 2014 Jun;12(6):963-9. doi: 10.1016/j.cgh.2013.08.041.
126. Dhroove G, Chogle A, Saps M. A million-dollar work-up for abdominal pain: is it worth it? J Pediatr Gastroenterol Nutr. 2010 Nov;51(5):579-83. doi: 10.1097/MPG.0b013e3181de0639.
127. Sierra MS, Hastings EV, Goodman KJ. What do we know about benefits of H. pylori treatment in childhood? Gut Microbes. 2013 Nov-Dec;4(6):549-67. doi: 10.4161/gmic.27000.
128. Harris PR, Wright SW, Serrano C, Riera F, Duarte I, Torres J, Peña A, Rollán A, Viviani P, Guiraldes E, Schmitz JM, Lorenz RG, Novak L, Smythies LE, Smith PD. Helicobacter pylori gastritis in children is associated with a regulatory T-cell response. Gastroenterology. 2008 Feb;134(2):491-9. doi: 10.1053/j.gastro.2007.11.006.
129. Freire de Melo F, Rocha AM, Rocha GA, Pedroso SH, de Assis Batista S, Fonseca de Castro LP, Carvalho SD, Bittencourt PF, de Oliveira CA, Corrêa-Oliveira R, Magalhães Queiroz DM. A regulatory instead of an IL-17 T response predominates in Helicobacter pylori-associated gastritis in children. Microbes Infect. 2012 Apr;14(4):341-7. doi: 10.1016/j.micinf.2011.11.008.
130. Vomero ND, Colpo E. Nutritional care in peptic ulcer. Arq Bras Cir Dig. 2014 Nov-Dec;27(4):298-302. doi: 10.1590/S0102-67202014000400017.
131. Семенова Н.Н., Боровик Т.Э., Дмитриенко Л.И. Лечебное питание детей при заболеваниях желудка и двенадцатиперстной кишки. Медицинский совет. 2007; 3:64-70. [Semenova N.N., Borovik T.E., Dmitrienko L.I. Therapeutic nutrition of children with diseases of the stomach and duodenum. Medical advice. 2007; 3:64-70].
132. Ивашкин В.Т., Горелов А.В., Абдулганиева Д.И., Алексеева О.П., Алексеенко С.А., Барановский А.Ю. и др. Методические рекомендации Научного сообщества по содействию клиническому изучению микробиома человека (НСОИМ) и Российской гастроэнтерологической ассоциации (РГА) по применению пробиотиков, пребиотиков, синбиотиков, метабиотиков и обогащенных ими функциональных пищевых продуктов для лечения и профилактики заболеваний гастроэнтерологического профиля у взрослых и детей. Российский журнал гастроэнтерологии, гепатологии, колопроктологии. 2024. https:// doi.org/10.22416/1382-4376-2024-117-312. [Ivashkin V.T., Gorelov A.V., Abdulganieva D.I., Alekseeva O.P., Alekseenko S.A., Baranovsky A.Yu., Zakharova I.N.et al. Methodological Guidelines of the Scientific Community for Human Microbiome Research (CHMR) and the Russian Gastroenterology Association (RGA) on the Use of Probiotics, Prebiotics, Synbiotics, Metabiotics and Functional Foods Enriched with Them for the Treatment and Prevention of Gastrointestinal Diseases in Adults and Children. Russian Journal of Gastroenterology, Hepatology, Coloproctology. 2024. https://doi. org/10.22416/1382-4376-2024-117-312].
133. Sivapalasingam S, Rajasingham A, Macy JT, Friedman CR, Hoekstra RM, Ayers T, Gold B, Quick RE. Recurrence of Helicobacter pylori infection in Bolivian children and adults after a population-based "screen and treat" strategy. Helicobacter. 2014 Oct;19(5):343-8. doi: 10.1111/hel.12137.
134. Morgan DR, Torres J, Sexton R, Herrero R, Salazar-Martínez E, Greenberg ER, Bravo LE, Dominguez RL, Ferreccio C, Lazcano-Ponce EC, Meza-Montenegro MM, Peña EM, Peña R, Correa P, Martínez ME, Chey WD, Valdivieso M, Anderson GL, Goodman GE, Crowley JJ, Baker LH. Risk of recurrent Helicobacter pylori infection 1 year after initial eradication therapy in 7 Latin American communities. JAMA. 2013 Feb 13;309(6):578-86. doi: 10.1001/jama.2013.311.
135. Feydt-Schmidt A, Kindermann A, Konstantopoulos N, Demmelmair H, Ballauff A, Findeisen A, Koletzko S. Reinfection rate in children after successful Helicobacter pylori eradication. Eur J Gastroenterol Hepatol. 2002 Oct;14(10):1119-23. doi: 10.1097/00042737-200210000-00013.
136. Ford AC, Yuan Y, Moayyedi P. Helicobacter pylori eradication therapy to prevent gastric cancer: systematic review and meta-analysis. Gut. 2020 Dec;69(12):2113-2121. doi: 10.1136/gutjnl-2020-320839.
137. Blaser MJ, Chen Y, Reibman J. Does Helicobacter pylori protect against asthma and allergy? Gut. 2008 May;57(5):561-7. doi: 10.1136/gut.2007.133462.
138. Serrano CA, Talesnik E, Peña A, Rollán A, Duarte I, Torres J, Majerson D, Einisman H, Viviani P, Harris PR. Inverse correlation between allergy markers and Helicobacter pylori infection in children is associated with elevated levels of TGF-β. Eur J Gastroenterol Hepatol. 2011 Aug;23(8):656-63. doi: 10.1097/MEG.0b013e328347c231.
139. Zevit N, Balicer RD, Cohen HA, Karsh D, Niv Y, Shamir R. Inverse association between Helicobacter pylori and pediatric asthma in a high-prevalence population. Helicobacter. 2012 Feb;17(1):30-5. doi: 10.1111/j.1523-5378.2011.00895.x.
140. Amberbir A, Medhin G, Erku W, Alem A, Simms R, Robinson K, Fogarty A, Britton J, Venn A, Davey G. Effects of Helicobacter pylori, geohelminth infection and selected commensal bacteria on the risk of allergic disease and sensitization in 3-year-old Ethiopian children. Clin Exp Allergy. 2011 Oct;41(10):1422-30. doi: 10.1111/j.1365-2222.2011.03831.x.
141. Arnold IC, Hitzler I, Müller A. The immunomodulatory properties of Helicobacter pylori confer protection against allergic and chronic inflammatory disorders. Front Cell Infect Microbiol. 2012 Feb 16;2:10. doi: 10.3389/fcimb.2012.00010.
142. Graham D.Y., Lu H. Furazolidone in He li co bac ter py lo ri therapy: misunderstood and oft en unfairly maligned drug told in a story of French bread. Saudi J Gastroenterol. 2012; 18:1–2. doi: 10.4103/1319–3767.91724.
143. Mohammadi M., Attaran B., Malekzadeh R., et al. Furazolidone, an Underutilized Drug for H. pylori Eradication: Lessons from Iran. Dig Dis Sci. 2017;62(8):1890–6. doi:10.1007/s10620–017–4628–5.
144. Nijevitch A.A., Sataev V. U., Akhmadeyeva E. N., et al. Nifuratel- containing initial anti He li co bac ter py lo ri triple therapy in children. Helicobacter. 2007 Apr;12(2):132–5. doi: 10.1111/j.1523–5378.2007.00482.x.
145. Дехнич Н.Н,, Тряпышко А. А., Трушин И. В., и др. Нифурател в эрадикации инфекции Helicobacter pylori у взрослых: результаты рандомизированного сравнительного, клинического исследования. Клиническая микробиология и антимикробная химиотерапия. 2020; 22 (2): 119–127 [Dekhnich N.N., Tryapyshko A. A., Trushin I. V., Kuzmenkov A. Yu., Kozlov R. S. Results of an open-label, randomized, comparative clinical trial of nifuratel in the eradication of Helicobac ter pylori infection in adult patients. Clinical Microbiology and Antimicrobial Chemotherapy. 2020; 22(2):119–127. (in Russ.) doi: 10.36488/cmac.2020.2.119–127].
146. Успенский Ю. П., Барышникова Н. В. Использование производных нитрофурана в схемах эрадикационной терапии первой линии. РМЖ, 2012; 35: 169 [Uspensky Yu.P., Baryshnikova N. V. Use of nitrofuran derivatives in first-line eradication therapy regimens. RMZh, 2012; (35): 1694. (in Russ.).].
147. Iwańczak B.M., Borys- Iwanicka A., Biernat M., Gościniak G. Assessment of Sequential and Standard Triple Therapy in Treatment of Helicobacter pylori Infection in Children Dependent on Bacteria Sensitivity to Antibiotics. Adv Clin Exp Med. 2016 Jul- Aug;25(4):701–8. doi: 10.17219/acem/38554.
148. Ахмадеева Э. Н., Нижевич А. А., Кучина Е. С., Сатаев В. У., Арзамасцев А. Г.. Последовательная (sequential) антихеликобактерная терапия у детей с хроническим гастритом: пилотное исследование. Педиатрия. 2013; 92 (6): 85–87. [Ahmadeeva E.N., Nijevich A. A., Kuchina E. S., Sataev V. U., Arzamastsev A. G.. [Sequential anti- Helicobacter pylori therapy in children with chronic gastritis: a pilot study]. Pediatria. 2013; 92 (6): 85–87. (In Russ.)].
149. Graham DY, Lew GM, Malaty HM, Evans DG, Evans DJ Jr, Klein PD, Alpert LC, Genta RM. Factors influencing the eradication of Helicobacter pylori with triple therapy. Gastroenterology. 1992 Feb;102(2):493-6. doi: 10.1016/0016-5085(92)90095-g.
150. Kim B.J., Lee H., Lee Y.C., Jeon S.W., Kim G.H., Kim H.S. et al. Ten-Day Concomitant, 10-Day Sequential, and 7-Day Triple Therapy as First-Line Treatment for Helicobacter pylori Infection: A Nationwide Randomized Trial in Korea. Gut Liver. 2019;13(5):531-540. doi: 10.5009/gnl19136 .
151. Farrell S, Milliken I, Doherty GM, Murphy JL, Wootton SA, McCallion WA. Total family unit Helicobacter pylori eradication and pediatric re-infection rates. Helicobacter. 2004 Aug;9(4):285-8. doi: 10.1111/j.1083-4389.2004.00240.x.
152. Drossman DA. Functional Gastrointestinal Disorders: History, Pathophysiology, Clinical Features and Rome IV. Gastroenterology. 2016 Feb 19:S0016-5085(16)00223-7. doi: 10.1053/j.gastro.2016.02.032.
153. Stanghellini V, Chan FK, Hasler WL, Malagelada JR, Suzuki H, Tack J, Talley NJ. Gastroduodenal Disorders. Gastroenterology. 2016 May;150(6):1380-92. doi: 10.1053/j.gastro.2016.02.011.
154. Хомерики Н.М., Морозов И.А. Особенности цитопротекции в желудке и некоторые аспекты фармакологического действия препаратов висмута. Медицинский совет. 2017;11:112-119. DOI: 10.21518/2079-701X-2017-112-119. [Khomeriki N.M., Morozov I.A. Peculiarities of cytoprotection in the stomach and some aspects of pharmacological action of bismuth drugs. Medical council. 2017;11:112-119. DOI: 10.21518/2079-701X-2017-112-119 (In Russ.)].
155. Bagchi D, McGinn TR, Ye X, Balmoori J, Bagchi M, Stohs SJ, Kuszynski CA, Carryl OR, Mitra S. Mechanism of gastroprotection by bismuth subsalicylate against chemically induced oxidative stress in cultured human gastric mucosal cells. Dig Dis Sci. 1999 Dec;44(12):2419-28. doi: 10.1023/a:1026618501729.
156. Галиев Ш.З., Амиров Н.Б. Дуоденогастральный рефлюкс как причина развития рефлюкс-гастрита. Вестник современной клинической медицины. 2015;8(2):50-61. [Galiev Sh.Z., Amirov N.B. Duodenogastric reflux as a cause of reflux gastritis. Bulletin of Modern Clinical Medicine. 2015;8(2):50-61].
157. McCabe ME 4th, Dilly CK. New Causes for the Old Problem of Bile Reflux Gastritis. Clin Gastroenterol Hepatol. 2018 Sep;16(9):1389-1392. doi: 10.1016/j.cgh.2018.02.034.
158. Shi X., Zhang J., Mo L., Shi J, Qin M, Huang X. Effi cacy and safety of probiotics in eradicating He li co bac ter py lori: a network meta-analysis. Medicine (Baltimore). 2019; v.98(15): e15180. doi: 10.1097/MD.0000000000015180.
159. Zhu R., Chen K., Zheng Y.-Y., et al. Meta-analysis of the effi acy of probiotics in He li co bac ter py lo ri eradication therapy. World J Gastroenterol. 2014; 20 (47): 18013–18021. doi: 10.3748/wjg.v20.i47.18013
160. Yang C, Liang L, Lv P, Liu L, Wang S, Wang Z, Chen Y. Effects of non-viable Lactobacillus reuteri combining with 14-day 390 standard triple therapy on Helicobacter pylori eradication: A randomized double-blind placebo-controlled trial. Helicobacter. 2021 Dec;26(6):e12856. doi: 10.1111/hel.12856.
161. Zhu XL, Liu Z, Wu ZQ, Li D, Jiang AP, Yu GX. [Clinical effects of different therapeutic regimens for Helicobacter pylori infection in children]. Zhongguo Dang Dai Er Ke Za Zhi. 2017 Jun;19(6):672-676. Chinese. doi: 10.7499/j.issn.1008-394 8830.2017.06.012.
162. Francavilla R, Polimeno L, Demichina A, Maurogiovanni G, Principi B, Scaccianoce G, Ierardi E, Russo F, Riezzo G, Di Leo A, Cavallo L, Francavilla A, Versalovic J. Lactobacillus reuteri strain combination in Helicobacter pylori infection: a ran397domized, double-blind, placebo-controlled study. J Clin Gastroenterol. 2014 May-Jun;48(5):407-13. doi:398 10.1097/MCG.0000000000000007.
163. Корниенко Е. А., Паролова Н. И. Микробиота желудка и возможности пробиотиков в эрадикации H. pylori . – Фарматека. 2017; 13: 22–29 [Kornienko E.A., Parolova N. I. Gastric microbiota and potentials of probiotics in the eradication of H. py lo ri. Farmateka. 2017; 13: 22–29. (in Russ.).].
164. Lehtoranta L, Pitkäranta A, Korpela R. Probiotics in respiratory virus infections. Eur J Clin Microbiol Infect Dis. 2014 Aug;33(8):1289-302. doi: 10.1007/s10096-014-2086-y.
165. Shi N., Li N., Duan X., Niu H. Interaction between the gut microbiome and mucosal immune system. Military Medical Research. 2017;4:59. doi: 10.1186/s40779-017-0122-9.
166. Clavel T., Lagkouvardos I., Gomes-Neto J.C., Ramer-Tait A.E. Deciphering interactions between the gut microbiota and the immune system via microbial cultivation and minimal microbiomes. Immunol. Rev. 2017;279(1):8–22. doi: 10.1111/imr.12578.
167. Rios D., Wood M.B., Li J., Chassaing B., Gewirtz A.T., Williams I.R. Antigen sampling by intestinal M cells is the principal pathway initiating mucosal IgA production to commensal enteric bacteria. Mucosal Immunol. 2016;9(4):907–916. doi: 10.1038/mi.2015.121
168. Tilg H., Moschen A.R. Food, immunity, and the microbiome. Gastroenterology. 2015;148(6):1107–1119. doi: 10.1053/j.gastro.2014.12.036
169. Ahrne S, Hagslatt ML. Effect of lactobacilli on paracellular permeability in the gut. Nutrients. 2011 Jan;3(1):104-17. doi: 10.3390/nu3010104.
170. Morais MB, Jacob CM. The role of probiotics and prebiotics in pediatric practice. J Pediatr (Rio J). 2006 Nov;82(5 Suppl):S189-97. doi: 10.2223/JPED.1559.
171. Филимонов Р.М. Курортное лечение заболеваний органов пищеварения. Москва. 2012, 406 с. [Filimonov R.M. Spa treatment of diseases of the digestive system. Moscow. 2012, 406 s].
172. Пархотик И.И. Физическая реабилитация при заболеваниях органов брюшной полости. Киев. Олимпийская литература. 2003, 223 с. [Parkhotik I.I. Physical rehabilitation in diseases of the abdominal cavity. Kyiv. Olympic literature. 2003, 223 p.].
173. Физическая и реабилитационная медицина в педиатрии /Хан М.А., Разумов А.Н., Корчажкина Н.Б., Погонченкова И.В. – М.: ГЭОТАР-Медиа, 2018. – 408 с. [Physical and rehabilitation medicine in pediatrics /Khan M.A., Razumov A.N., Korchazhkina N.B., Pogonchenkova I.V. – M.: GEOTAR-Media, 2018. – 408 p.].
174. Мельникова И.Ю., Новикова В.П. Диспансеризация детей и подростков с патологией пищеварительной системы. СпецЛит, Санкт-Петербург, 2011, С. 26-38. [Melnikova I.Yu., Novikova V.P. Medical examination of children and adolescents with pathology of the digestive system. SpetsLit, St. Petersburg, 2011, pp. 26-38].
175. Корсун В.Ф. и соавт., Лекарственные растения в гепатологии. – М.: Русский врач, 2005. – 278 с. [Korsun V.F. et al., Medicinal plants in hepatology. – M.: Russian doctor, 2005. – 278 p.].
176. Мирович В.М., Привалова Е.Г., Петухова С.А. Применение растительных средств при заболеваниях желудочно-кишечного тракта: учебное пособие. – ФГБОУ ВО ИГМУ Минздрава РФ, кафедра фармакогнозии и фармацевтической технологии. – Иркутск: ИГМУ, 2020. –139 с. [Mirovich V.M., Privalova E.G., Petukhova S.A. The use of herbal remedies for diseases of the gastrointestinal tract: a textbook. – FGBOU VO IGMU of the Ministry of Health of the Russian Federation, Department of Pharmacognosy and Pharmaceutical Technology. – Irkutsk: IGMU, 2020. -139 s].
177. Сичинава И.В. Необходимость совершенствования системы реабилитации детей с хроническими гастродуоденитами. Фарматека. 2012; s2-12: 60-63 [Sichinava I.V. The need to improve the rehabilitation system for children with chronic gastroduodenitis. Pharmateca. 2012; s2-12: 60-63].
178. Song H., Ekheden I.G., Zheng Z. et al. Incidence of gastric cancer among patients with gastric precancerous lesions: observational cohort study in a low risk Western population. BMJ. 2015; 351: h3867. doi: 10.1136/bmj.h4134.
179. Rugge M., Meggio A., Pravadelli C., Barbareschi M., Fassan M., Gentilini M. et al. Gastritis staging in the endoscopic follow-up for the secondary prevention of gastric cancer: a 5-year prospective study of 1755 patients. Gut. 2019; 68(1): 11 – 17. doi: 10.1136/gutjnl-2017-314600.
180. Cho S.J., Choi I..J, Kook M.C., Nam B.-H., Kim C.G., Lee J.Y. et al. Staging of intestinal- and diffuse-type gastric cancers with the OLGA and OLGIM staging systems. Aliment Pharmacol Ther. 2013; 38(10):1292 – 1302. doi: 10.1111/apt.12515.
181. Kodama M., Murakami K., Okimoto T., Abe H., Sato R., Ogawa R. et al. Histological characteristics of gastric mucosa prior to Helicobacter pylori eradication may predict gastric cancer. Scand J Gastroenterol. 2013; 48(11): 1249 – 1256. doi: 10.3109/00365521.2013.838994.
182. Mera R.M., Bravo L.E., Camargo M.C., Bravo J.C., Delgado A.G., Romero-Gallo J. et al. Dynamics of Helicobacter pylori infection as a determinant of progression of gastric precancerous lesions: 16-year follow-up of an eradication trial. Gut. 2018; 67(7):1239 – 1246. doi: 10.1136/gutjnl-2016-311685.
183. Gonzalez C.A., Sanz-Anquela J.M., Companioni O., Bonet C., Berdasco M., López C. et al. Incomplete type of intestinal metaplasia has the highest risk to progress to gastric cancer: results of the Spanish follow-up multicenter study. J Gastroenterol Hepatol. 2016; 31(5): 953 – 958. doi: 10.1111/jgh.13249.
184. Gonzalez C.A., Sanz-Anquela J.M., Gisbert J.P., Correa P. Utility of subtyping intestinal metaplasia as marker of gastric cancer risk. A review of the evidence. Int J Cancer. 2013; 133(5): 1023 – 1032. doi: 10.1002/ijc.28003.
185. Conchillo J.M., Houben G., de Bruine A., Stockbrügger R. Is type III intestinal metaplasia an obligatory precancerous lesion in intestinal-type gastric carcinoma? Eur J Cancer Prev. 2001; 10(4):307 – 312. doi: 10.1097/00008469-200108000-00003.
186. Rokkas T., Sechopoulos P., Pistiolas D., Georgios Margantinis, Koukoulis G. Helicobacter pylori infection and gastric histology in first-degree relatives of gastric cancer patients: a meta-analysis. Eur J Gastroenterol Hepatol. 2010; 22(9):1128 – 1133. doi: 10.1097/MEG.0b013e3283398d37.
187. Marcos-Pinto R., Dinis-Ribeiro M., Carneiro F., Wen X., Lopes C., Figueiredo C. et al. First-degree relatives of early-onset gastric cancer patients show a high risk for gas tric cancer: phenotype and genotype profile. Virchows Arch. 2013; 463(3): 391 – 399. doi: 10.1007/s00428-013-1458-5
188. Segni M, Borrelli O, Pucarelli I, Delle Fave G, Pasquino AM, Annibale B. Early manifestations of gastric autoimmunity in patients with juvenile autoimmune thyroid diseases. J Clin Endocrinol Metab. 2004 Oct;89(10):4944-8. doi: 10.1210/jc.2003-031597. PMID: 15472189
189. Besançon A, Michaud B, Beltrand J, Goncalves T, Jais JP, Polak M, Chatenoud L, Robert JJ. Revisiting autoimmune gastritis in children and adolescents with type 1 diabetes. Pediatr Diabetes. 2017 Dec;18(8):772-776. doi: 10.1111/pedi.12482. Epub 2016 Dec 22. PMID: 28004477
190. Mitsinikos T, Shillingford N, Cynamon H, Bhardwaj V. Autoimmune Gastritis in Pediatrics: A Review of 3 Cases. J Pediatr Gastroenterol Nutr. 2020 Feb;70(2):252-257. doi: 10.1097/MPG.0000000000002547. PMID: 31978028, 20
Приложение А1. Состав рабочей группы по разработке и пересмотру клинических рекомендаций
1. Новикова Валерия Павловна – доктор медицинских наук, профессор, заведующая кафедрой пропедевтики детских болезней с курсом общего ухода ФГОУ ВО СПбГПМУ Минздрава России, заведующая лабораторией Медико-социальных проблем педиатрии НИЦ ФГОУ ВО СПбГПМУ Минздрава России, член Союза педиатров России, член Российского общества детских гастроэнтерологов, гепатологов и нутрициологов
2. Барышникова Наталья Владимировна – кандидат медицинских наук, доцент, старший научный сотрудник лаборатории Медико-социальных проблем педиатрии НИЦ ФГОУ ВО СПбГПМУ Минздрава России
3. Хавкин Анатолий Ильич – доктор медицинских наук, профессор, заведующий кафедрой гастроэнтерологии и диетологии им. А.В. Мазурина, руководитель Московского областного центра детской гастроэнтерологии и гепатологии Научно-исследовательского клинического института детства Министерства здравоохранения Московской области; профессор кафедры педиатрии с курсом детских хирургических болезней Медицинского института Белгородского государственного национального исследовательского университета, председатель Общества детских гастроэнтерологов, гепатологов и нутрициологов России, Член Союза педиатров России.
4. Гурова Маргарита Михайловна – доктор медицинских наук, ведущий научный сотрудник лаборатории Медико-социальных проблем педиатрии НИЦ ФГОУ ВО СПбГПМУ Минздрава России, профессор кафедры пропедевтики детских болезней с курсом общего ухода ФГОУ ВО СПбГПМУ Минздрава России, член Союза педиатров России, член Общества детских гастроэнтерологов, гепатологов и нутрициологов, заместитель главного врача по медицинской части СПб ГБУЗ КДЦД
5. Калинина Елена Юрьевна – кандидат медицинских наук, заведующая кафедрой нормальной анатомии ФГОУ ВО СПбГПМУ
6. Завьялова Анна Никитична – доктор медицинских наук, профессор кафедры пропедевтики детских болезней с курсом общего ухода ФГОУ ВО СПбГПМУ Минздрава России, член Союза педиатров России, член Общества детских гастроэнтерологов, гепатологов и нутрициологов Член Союза педиатров России.
7. Корниенко Елена Александровна – д.м.н., профессор кафедры детских болезней им. профессора И. М. Воронцова ФП и ДПО ФГБОУ ВО СПбГПМУ Минздрава России. Главный внештатный детский гастроэнтеролог Комитета по здравоохранению Правительства Санкт-Петербурга. член Общества детских гастроэнтерологов, гепатологов и нутрициологов Член Союза педиатров России.
8. Волынец Галина Васильевна – д.м.н., профессор кафедры инновационной педиатрии и детской хирургии ФДПО, доцент кафедры педиатрии с инфекционными болезнями у детей ФДПО ФГБОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России. Заведующий отделом, отдел гастроэнтерологии НИКИ педиатрии им.ак. Ю.Е. Вельтищева. член Общества детских гастроэнтерологов, гепатологов и нутрициологов, член союза педиатров России
9. Листопадова Анастасия Павловна – кандидат медицинских наук, ассистент кафедры пропедевтики детских болезней с курсом общего ухода за детьми ФГОУ ВО СПбГПМУ, старший научный сотрудник лаборатории Медико-социальных проблем педиатрии НИЦ ФГОУ ВО СПбГПМУ Минздрава России, член Общества детских гастроэнтерологов, гепатологов и нутрициологов, член союза педиатров России
10. Мельникова Ирина Юрьевна – профессор, доктор медицинских наук, заведующая кафедрой педиатрии и детской кардиологии СЗГМУ им. И.И. Мечникова, член Общества детских гастроэнтерологов, гепатологов и нутрициологов, член союза педиатров России
11. Бельмер Сергей Викторович – профессор, доктор медицинских наук профессор кафедры госпитальной педиатрии №2 ПФ ФГАОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России, сопредседатель Общества детских гастроэнтерологов, гепатологов и нутрициологов, член союза педиатров России
12. Богданова Наталья Михайловна – кандидат медицинских наук, доцент кафедры пропедевтики детских болезней с курсом общего ухода за детьми ФГОУ ВО СПбГПМУ, Минздрава России, член Общества детских гастроэнтерологов, гепатологов и нутрициологов, член союза педиатров России
13. Баранов А.А. – академик РАН, д.м.н., почетный Президент Союза педиатров России, советник руководителя НИИ педиатрии и охраны здоровья детей ЦКБ РАН, главный внештатный специалист педиатр Минздрава России, профессор кафедры педиатрии и детской ревматологии Клинического института детского здоровья имени Н.Ф. Филатова ФГАОУ «Первый МГМУ им. И.М. Сеченова» Минздрава России (Сеченовский Университет)
14. Намазова-Баранова Л.С. – академик РАН, профессор, д.м.н., Президент Союза педиатров России; паст-президент EPA/UNEPSA; руководитель НИИ педиатрии и охраны здоровья детей ЦКБ РАН, заведующая кафедрой факультетской педиатрии педиатрического факультета ФГБОУ ВО «РНИМУ им. Н.И. Пирогова» Минздрава России, главный внештатный детский специалист по профилактической медицине Минздрава России
15. Гундобина О.С. – к.м.н, в.н.с., врач-гастроэнтеролог НИИ педиатрии и охраны здоровья детей ЦКБ РАН член Союза педиатров России
16. Кайтукова Е.В. – кандидат медицинских наук, главный врач НИИ педиатрии и охраны здоровья детей ЦКБ РАН, доцент кафедры факультетской педиатрии педиатрического факультета ФГБОУ ВО «РНИМУ им. Н.И. Пирогова» Минздрава России член Союза педиатров России
17. Комарова Е.В. – доктор медицинских наук, заместитель руководителя НИИ педиатрии и охраны здоровья детей ЦКБ РАН, врач-гастроэнтеролог, член Союза педиатров России
18. Потапов А.С. – д.м.н., профессор, член Союза педиатров России
19. Ревуненков Г.В. – к.м.н., в.н.с., руководитель отдела инновационных диагностических методов исследования, врач ультразвуковой диагностики НИИ педиатрии и охраны здоровья детей ЦКБ РАН, член Союза педиатров России.
20. Сурков А.Н. – доктор медицинских наук, заведующий гастроэнтерологическим отделением с гепатологической группой, главный научный сотрудник лаборатории научных основ детской гастроэнтерологии и гепатологии НИИ Педиатрии им. Г.Н. Сперанского, профессор кафедры педиатрии и общественного здоровья Института подготовки медициснких кадров ФГАУ «НМИЦ здоровья детей» Минздрава России, член Союза педиатров России
Конфликт интересов:
Авторы подтверждают отсутствие финансовой поддержки/конфликта интересов, который необходимо обнародовать.
Приложение А2. Методология разработки клинических рекомендаций
Целевая аудитория данных клинических рекомендаций:
1. Целевая аудитория данных клинических рекомендаций:
2. Врачи-педиатры
3. Врачи общей врачебной практики (семейные врачи)
4. Врачи-гастроэнтерологи
5. Врачи-эндоскописты
6. Студенты медицинских ВУЗов
7. Обучающиеся в ординатуре
Методы, использованные для оценки качества и силы доказательств:
· поиск в электронных базах данных. Описание методов, использованных для оценки качества и силы доказательств: доказательной базой для рекомендаций являются публикации, вошедшие в Кохрейновскую библиотеку, базы данных EMBASE, MEDLINE и PubMed. Глубина поиска – 10 лет.
· консенсус экспертов;
· оценка значимости в соответствии с рейтинговой схемой.
Таблица 1. Шкала оценки уровней достоверности доказательств (УДД) для методов диагностики (диагностических вмешательств)
|
УДД |
Расшифровка |
|
1 |
Систематические обзоры исследований с контролем референсным методом или систематический обзор рандомизированных клинических исследований с применением мета-анализа |
|
2 |
Отдельные исследования с контролем референсным методом или отдельные рандомизированные клинические исследования и систематические обзоры исследований любого дизайна, за исключением рандомизированных клинических исследований, с применением мета-анализа |
|
3 |
Исследования без последовательного контроля референсным методом или исследования с референсным методом, не являющимся независимым от исследуемого метода или нерандомизированные сравнительные исследования, в том числе когортные исследования |
|
4 |
Несравнительные исследования, описание клинического случая |
|
5 |
Имеется лишь обоснование механизма действия или мнение экспертов |
Таблица 2. Шкала оценки уровней достоверности доказательств (УДД) для методов профилактики, лечения и реабилитации (профилактических, лечебных, реабилитационных вмешательств)
|
УДД |
Расшифровка |
|
1 |
Систематический обзор РКИ с применением мета-анализа |
|
2 |
Отдельные РКИ и систематические обзоры исследований любого дизайна, за исключением РКИ, с применением мета-анализа |
|
3 |
Нерандомизированные сравнительные исследования, в т.ч. когортные исследования |
|
4 |
Несравнительные исследования, описание клинического случая или серии случаев, исследования «случай-контроль» |
|
5 |
Имеется лишь обоснование механизма действия вмешательства (доклинические исследования) или мнение экспертов |
Таблица 3. Шкала оценки уровней убедительности рекомендации (УУР) для методов профилактики, диагностики, лечения и реабилитации (профилактических, диагностических, лечебных, реабилитационных вмешательств)
|
УУР |
Расшифровка |
|
A |
Сильная рекомендация (все рассматриваемые критерии эффективности (исходы) являются важными, все исследования имеют высокое или удовлетворительное методологическое качество, их выводы по интересующим исходам являются согласованными) |
|
B |
Условная рекомендация (не все рассматриваемые критерии эффективности (исходы) являются важными, не все исследования имеют высокое или удовлетворительное методологическое качество и/или их выводы по интересующим исходам не являются согласованными) |
|
C |
Слабая рекомендация (отсутствие доказательств надлежащего качества (все рассматриваемые критерии эффективности (исходы) являются неважными, все исследования имеют низкое методологическое качество и их выводы по интересующим исходам не являются согласованными) |
Порядок обновления клинических рекомендаций.
Механизм обновления клинических рекомендаций предусматривает их систематическую актуализацию – не реже чем один раз в три года, а также при появлении новых данных с позиции доказательной медицины по вопросам диагностики, лечения, профилактики и реабилитации конкретных заболеваний, наличии обоснованных дополнений/замечаний к ранее утверждённым КР, но не чаще 1 раза в 6 месяцев.
Приложение А3. Справочные материалы, включая соответствие показаний к применению и противопоказаний, способов применения и доз лекарственных препаратов, инструкции по применению лекарственного препарата
1. Государственный реестр лекарственных средств: https://grls.rosminzdrav.ru
2. Приказ МЗ РФ от 20 декабря 2012г. № 1183н «Об утверждении номенклатуры должностей медицинских работников и фармацевтических работников».
3. Приказ МЗ РФ от 23 июля 2010 г. № 541н. Единый квалификационный справочник должностей руководителей, специалистов и служащих, раздел Квалификационные характеристики должностей работников в сфере здравоохранения.
4. Федеральный закон от 25.12.2018 № 489-ФЗ «О внесении изменений в статью 40 Федерального закона "Об обязательном медицинском страховании в Российской Федерации" и Федеральный закон "Об основах охраны здоровья граждан в Российской Федерации" по вопросам клинических рекомендаций».
5. Приказ Минздрава России № 103н от 28.02.2019 г. «Об утверждении порядка и сроков разработки клинических рекомендаций, их пересмотра, типовой формы клинических рекомендаций и требований к их структуре, составу и научной обоснованности включаемой в клинические рекомендации информации».
6. Приказ Минздрава России от 13.10.2017 № 804н "Об утверждении номенклатуры медицинских услуг".
7. Приказ Министерства здравоохранения РФ от 14 января 2019 г. № 4н «Об утверждении порядка назначения лекарственных препаратов, форм рецептурных бланков на лекарственные препараты, порядка оформления указанных бланков, их учета и хранения»
8. Приказ Министерства здравоохранения и социального развития РФ от 16 апреля 2012 г. № 366н «Об утверждении Порядка оказания педиатрической помощи»
9. Приказ Минздрава России 203н от 10 мая 2017г «Об утверждении критериев оценки качества медицинской помощи»
10. Приказ Минздрава России от 23 сентября 2020г. № 1008н «Об утверждении порядка обеспечения пациентов лечебным питанием».
Приложение А3.1 Эндоскопическая картина гастрита у детей
а) Больной, 10 лет. Нодулярный гастрит с единичной эрозией
б) Больной, 15 лет Геморрагический гастрит.
Эндоскопическая картина дуоденита у детей
Приложение А3.2 Патолого-анатомическая (гистологическая) картина гастрита у детей
а) Больная, 10 лет. Воспаление в слизистой оболочке тела желудка у пациентки с хроническим гастритом Окраска гематоксилином и эозином. Увеличение Х 160.
б) Больной, 8 лет. Воспаление в слизистой оболочке антрального отдела желудка у пациентов с хроническим гастритом Окраска гематоксилином и эозином. Увеличение Х 120.
в) Больная, 14 лет. Тесное расположение НР на поверхности эпителиоцитов антрального отдела желудка. Окраска альциановым синим. Увеличение Х 160.
г) Больной, 12 лет. Биоптат слизистой оболочки антрального отдела желудка. Определяется крупный лимфоидный фолликул со светлым центром. Окраска гематоксилином и эозином. Увеличение Х 120.
д) Больной, 15 лет. Фиброз стромы в слизистой оболочке желудка у пациента с хроническим гастритом Окраска пикрофуксином по Ван-Гизону. Увеличение Х 120.
е) Больной, 7 лет. Атрофия желез в слизистой оболочке желудка у пациента с хроническим гастритом Окраска гематоксилином и эозином. Увеличение Х 120.
ж) Больной, 14 лет. Неполная кишечная метаплазия. Окраска гематоксилином и эозином, альциановым синим. Увеличение Х 120 и Х 160.
з) Больной, 10 лет Хронический аутоиммунный гастрит с начинающейся деструкцией желез. Увеличение× 400. Окраска гематоксилин–эозин.
Приложение А3.3 Патолого-анатомическая (гистологическая) картина дуоденита у детей
|
Слизистая оболочка ДПК с сохранением архитектоники, слабой лимфоплазмоцитарной инфильтрацией. Хронический активный дуоденит I степени по R. Whitеhead (1990). Окраска гематоксилином и эозином, увел.100 |
Слизистая оболочка ДПК с укорочение ворсинок, углублением крипт, нарастанием воспалительной инфильтрации. Хронический активный дуоденит II степени по R. Whitеhead (1990). Окраска гематоксилином и эозином, увел.100 |
|
Слизистая оболочка ДПК с выраженным укорочением ворсинок и углубление крипт, выраженной воспалительной инфильтрацией. Хронический активный субатрофический дуоденит II степени по R. Whitеhead (1990). Окраска гематоксилином и эозином, увел. 100 |
Хронический активный атрофический дуоденит III степени по R. Whitеhead (1990) при целиакии, «Лысая» слизистая оболочка. Лимфо-плазмоцитарная инфильрация, как собственной пластинки, так и подслизистой основы. Окраска гематоксилином и эозином, увел.100 |
|
Хронический активный атрофический дуоденит при целиакии. Интраэпителиальная инфильтрация покровного эпителия (более 40 на 100 эпителиоцитов). Окраска гематоксилином и эозином, увел. 400 |
Хронический активный субатрофический дуоденит при целиакии. Экспрессия CD 8. ИГХ, увел.100 |
|
Хронический активный атрофически-гиперпластический дуоденит с обширным эрозированием при целиакии. Окраска гематоксилином и эозином, увел.100 |
Хронический атрофический дуоденит при целиакии. Выраженная пролиферативная активность эпителия в сохранных удлиненных криптах. Экспрессия KI-67. ИГХ, увел.40 |
|
Хронический неактивный атрофически-гиперпластический дуоденит при целиакии. Неравномерное количество нейроэндокринных клеток, продуцирующих серотонин (рис.А ) и хромогранин А (рис. Б). Экспрессия серотонина и хромогранина А. ИГХ, докраска ядер гемотоксилином, увел 400 | |
|
Хронический активный хеликобактерный дуоденит: резкое нарушение архитектоники за счет выраженной диффузной и нодулярной лимфоплазмоцитарной инфильтрации, уменьшение количества бокаловидных клеток. Окраска гематоксилином и эозином, увел.100 |
Тот же биоптат. Снижение количества бокаловидных клеток, скопление Нelicobacter pylori на поверхности биоптата. Окраска по Романовскому-Гимза, увел. 1000, иммерсия. |
|
Хронический активный дуоденит, ассоциированный с вирусным поражением. Выраженное увеличение тучных клеток в строме. Окраска по Романовскому-Гимза, увел. 400 |
Хронический активный хеликобактерный дуоденит, распространенная желудочная метаплазия эпителия. Экспрессия муцина 5. ИГХ, увел.100 |
|
Хронический активный дуоденит при ревматоидном артрите. На фоне выраженной лимфо-плазмоцитарной инфильтрации диффузного характера отмечается экспрессия Ig E в собственной пластинке. ИГХ, увел. 400 |
Хронический атрофически-гиперпластический активный дуоденит при муковисцидозе, Неравномерное количество бокаловидных клеток, гиперпродукция слизи с расширением крипт и формированием слизистых бухт. Окраска гематоксилином и эозином, альциановым синим, увел. 200 |
|
Хронический активный дуоденит при тропической спру: сочетание атрофических и гиперластических изменений, лимфо-нодулярной гиперплазии и диффузной полиморфноклеточной инфильтрации собственной пластинки. Окраска гематоксилином и эозином, увел.40 |
Хронический активный дуоденит при длительном употреблении нестероидных противовоспалительных препаратов: диффузная лимфоплазмоцитарная инфильтрация и фиброз собственной пластинки, резкое утолщение и сближение ворсинок с эффектом слипания их, гиперплазия покровного эпителия с формированием псевдопапиллярных структур. Окраска гематоксилином и эозином, альциановым синим, увел. 40. |
|
Хронический активный атрофический эозинофильный дуоденит: резко увеличено количество эозинофильных гранулоцитов в воспалительном инфильтрат эозинофильный. Окраска гематоксилином и эозином, альциановым синим, увел. 200 (рис. А) и 400 (рис.Б) | |
|
| |
|
Хронический неактивный атрофический дуоденит (коллагеновое спру): резкое нарушение архитектоники за счет диффузного фиброза собственной пластинки на фоне минимальной клеточной инфильтрации стромы, атрофии и обеднения клеточного состава покровного эпителия. Окраска гематоксилином и эозином (рис. А) и пикрофуксином по методу Ван-Гизона (рис. Б), увел.200 | |
Приложение Б. Алгоритмы действий врача
Алгоритмы диагностики и лечения при гастрите и дуодените
Вариант 1
Вариант 2
Вариант 3
Вариант 4
Схема
Алгоритм выбора лечебной программы исходя из диагностических возможностей, в том числе верификации H. pylori
|
Диагностические возможности |
Решение | ||||
|
№ |
ЭГДС |
Диагности-ческие тесты (инвазивные и неинвазивные) |
Патолого-анатомическое (гистоло-гическое) исследование |
Определение резистентности H.pylori к противо-микробным препаратам системного действия |
|
|
1 |
+ |
+ |
+ |
+ |
Индивидуальная лечебная программа с учетом чувствительности H.pylori |
|
2 |
+ |
+ |
+ |
- |
Стандартная схема 1 линии с учетом региональных данных и индивидуальных особенностей ребенка |
|
3 |
+ |
+ |
- |
- |
Стандартная схема 1 линии при наличии абсолютных показ |
|
4 |
- |
+ |
- |
- |
Направление на ЭГДС |
|
5 |
- |
- |
- |
- |
Направление на ЭГДС |
Приложение В. Информация для пациента
Гастрит и дуоденит являются политологическими заболеваниями, в основе развития которых лежит нарушение баланса факторов агрессии и защиты слизистой оболочки желудка и двенадцатиперстной кишки. Практически всегда при развитии гастрита развивается и сопутствующий дуоденит, изолированный дуоденит встречается крайне редко. Важным фактором, вызывающим гастрит, в настоящее время признан микроорганизм, называемый Helicobacter pylori. Каждый пациент, у которого при проведении эндоскопического исследования верхних отделов желудочно-кишечного тракта выявлен гастрит, должен быть обследован на наличие данной инфекции. При ее подтверждении необходимо по показаниям провести лечение, направленное на уничтожение этого микроорганизма с последующим контролем эффективности лечения через 4-6 недель. При неэффективности проведенного лечения следует провести повторный курс терапии с другой схемой назначения лекарственных средств. Важно соблюдать приверженность к лечению и строго контролировать прием лекарственных препаратов для повышения эффективности лечения, строго соблюдать рекомендации врача. Терапия, приводящая к уничтожению Helicobacter pylori, сейчас считается основной мерой, направленной на оздоровление слизистой оболочки желудка, и профилактику рака желудка. Наличие рака желудка у близких родственников (родители, бабушки и дедушки) служит дополнительным основанием для проведения лечения против Helicobacter pylori. При отсутствии Helicobacter pylori лечение проводится в соответствии с выявленными жалобами и существующими рекомендациями.
Приложение Г1-ГN. Шкалы оценки, вопросники и другие оценочные инструменты состояния пациента, приведенные в клинических рекомендациях
Приложение Г1. Визуально-аналоговая шкала для патолого-анатомической (гистологической) оценки биоптатов желудка и двенадцатиперстной кишки
Название на русском языке: Визуально-аналоговая шкала для патолого-анатомической (гистологической) оценки биоптатов желудка и двенадцатиперстной кишки
Оригинальное название (если есть):
Источник (официальный сайт разработчиков, публикация с валидацией):
Тип (подчеркнуть):
- шкала оценки
- индекс
- вопросник
- другое (уточнить):_____________________________________________________
Назначение: патолого-анатомическая (гистологическая) оценка биоптатов желудка и двенадцатиперстной кишки
Содержание (шаблон), Ключ (интерпретация) и Пояснения:
.
Рекомендуемые статьи
При эндоскопическом исследовании в случае бронхоэктазов в стадии ремиссии выявляется
частично диффузный бронхит I степени воспаления
Активируйте PUSH уведомления в браузер
Отключите PUSH уведомления в браузер
Содержание
Интернет магазин
Популярное
- О нас
- Правовые вопросы
- Политика
обработки персональных
данных EndoExpert.ru - Связаться с нами
- Стать партнером
© 2016-2022 EndoExpert.ru

Вы находитесь в разделе предназначенном только для специалистов (раздел для пациентов по ссылке). Пожалуйста, внимательно прочитайте полные условия использования и подтвердите, что Вы являетесь медицинским или фармацевтическим работником или студентом медицинского образовательного учреждения и подтверждаете своё понимание и согласие с тем, что применение рецептурных препаратов, обращение за той или иной медицинской услугой, равно как и ее выполнение, использование медицинских изделий, выбор метода профилактики, диагностики, лечения, медицинской реабилитации, равно как и их применение, возможны только после предварительной консультации со специалистом. Мы используем файлы cookie, чтобы предложить Вам лучший опыт взаимодействия. Файлы cookie позволяют адаптировать веб-сайты к вашим интересам и предпочтениям.
Я прочитал и настоящим принимаю вышеизложенное, хочу продолжить ознакомление с размещенной на данном сайте информацией для специалистов.

















.jpg)





.png)


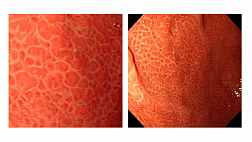


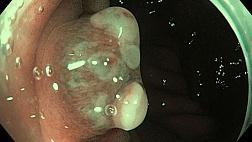











Комментарии