- Компании
- Takeda. О компании, буклеты, каталоги, контакты
- Olympus. О компании, буклеты, каталоги, контакты
- Boston Scientific. О компании, буклеты, каталоги, контакты
- Pentax. О компании, буклеты, каталоги, контакты
- Fujifilm & R-Farm. О компании, буклеты, каталоги, контакты
- Erbe. О компании, буклеты, каталоги, контакты
- Еще каталоги
- Мероприятия
- Информация
- Обучение
- Классификации
- Атлас
- Quiz
- Разделы
- Пациенту
QR-код этой страницы
Для продолжения изучения на мобильном устройстве ПРОСКАНИРУЙТЕ QR-код с помощью спец. программы или фотокамеры мобильного устройства
Статьи: Эндоскопическая подслизистая диссекция аденокарциномы пищеводно-желудочного перехода у пациента после комплексного лечения первичной лимфомы головного мозга. Клинический случай
| Авторы: | Соколов СА, Ленский БС, Москалец МВ, Шипулева ИЮ, Фёдоров ЕД, Каннер ДЮ 1 2020г. |
| Об авторах: |
1. Государственное бюджетное учреждение здравоохранения города Москвы «Московская городская онкологическая больница № 62 Департамента здравоохранения города Москвы» |



Полный текст статьи:
ЭНДОСКОПИЧЕСКАЯ ПОДСЛИЗИСТАЯ ДИССЕКЦИЯ АДЕНОКАРЦИНОМЫ ПИЩЕВОДНО-ЖЕЛУДОЧНОГО ПЕРЕХОДА У ПАЦИЕНТА ПОСЛЕ КОМПЛЕКСНОГО ЛЕЧЕНИЯ ПЕРВИЧНОЙ ЛИМФОМЫ ГОЛОВНОГО МОЗГА. КЛИНИЧЕСКИЙ СЛУЧАЙ.
Соколов С.А., Ленский Б.С., Шипулева И.В., Москалец М.В., Каннер Д.Ю., Федоров Е.Д.
Государственное бюджетное учреждение здравоохранения города Москвы «Московская городская онкологическая больница № 62 Департамента здравоохранения города Москвы»
Введение.
Основным критерием первично-множественного злокачественного заболевания является выявление в организме нескольких независимых друг от друга очагов злокачественного роста. Первично множественные злокачественные заболевания принято разделять на синхронные (опухоли диагностированы одновременно) и метахронные (с интервалом выявления опухолей не менее 6 месяцев). Возникновению опухолей способствуют самые разнообразные факторы: генетические, вирусные, физические, химические, ионизирующее излучение и др.
В последние годы возрастает частота выявления первично-множественных новообразований. В Российской Федерации в 2015г. этот показатель составлял 6,7 %, а в 2018г. уже 8,8 % от всех впервые выявленных злокачественных новообразований [2]. С одной стороны, это можно связать с совершенствованием диагностики, с другой стороны, выявление опухолей новых локализаций может быть связано с увеличением продолжительности жизни онкобольных после эффективного лечения по поводу первичного рака. И если еще несколько десятилетий назад выявление у пациента двух и более злокачественных заболеваний ставило под сомнение эффективность терапии, то сегодня первично-множественные опухоли не являются препятствием для выполнения радикального лечения.
В настоящей статье рассмотрено клиническое наблюдение редкого первично-множественного синхронного злокачественного заболевания: первичной лимфомы головного мозга и аденокарциномы пищеводного-желудочного перехода. В доступной нам литературе встретилось всего одно схожее клиническое наблюдение [8]. Однако, в отличие от нашего случая, пациенту была выполнена гастрэктомия с последующим химиолучевым лечением по поводу лимфомы головного мозга.
Первичная лимфома центральной нервной системы (ПЛЦНС) - редкая опухоль центральной нервной системы (5-7 % от всех первичных опухолей ЦНС), относится к редким формам неходжкинских экстранодальных лимфом [3,4]. ПЛЦНС определяется поражением паренхимы головного или спинного мозга, оболочек мозга, глаза, и в большинстве случаев (более 70%) манифестирует очаговой неврологической симптоматикой. Более чем в 90% случаев лимфома головного мозга представлена В-клеточным вариантом. Пациентам с первичной лимфомой ЦНС рекомендована химиотерапия на основе высокодозного метотрексата. В случае неполного ответа на лечение пациенту с первичной лимфомой ЦНС рекомендовано проведение лучевой терапии [3,4].
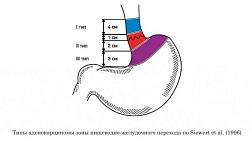
В последние годы во всем мире наблюдается тенденция к росту заболеваемости раком пищеводно-желудочного перехода [6,7,9,10]. Аденокарциномы ПЖП с эпицентром роста выше Z-линии, на уровне Z-линии и до 2,0 см ниже от Z-линии (I-II типы по Siewert) классифицируются и стадируются как рак пищевода и подлежат лечению согласно алгоритмам, соответствующим раку пищевода. Опухоли ПЖП с эпицентром роста дистальнее 2 см от Z-линии (III тип по Siewert) классифицируются и стадируются как рак желудка и подлежат лечению согласно алгоритмам, соответствующим раку желудка [1,5].
При росте опухоли ПЖП в пределах слизистой оболочки (Tis, T1a) признанным методом лечения считается эндоскопическое удаление опухоли методом резекции слизистой оболочки с диссекцией подслизистого слоя. Абсолютными показаниями являются: умеренно- и хорошо-дифференцированные опухоли, отсутствие изъязвлений, размер опухоли до 2 см включительно. Расширенными показаниями для эндоскопической диссекции служат: умеренно- и хорошо-дифференцированные поверхностные опухоли более 2 см, образования до 3 см включительно с изъязвлением или начальной подслизистой инвазией, а также плохо-дифференцированные поверхностные опухоли размером до 2 см включительно [6].
Клинический случай.
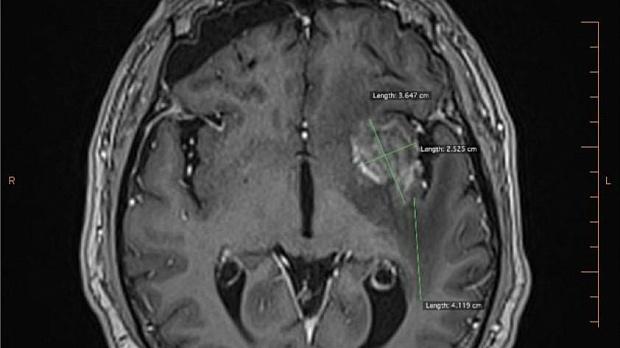
Пациент, 72 лет, по профессии физик-ядерщик, считает себя больным с ноября 2017 г., когда стал отмечать головные боли. Обратился к невропатологу по месту жительства, при обследовании по данным МРТ головного мозга выявлены два образования: в правой лобной и левой височных долях, размерами 31 х 35 х 33 мм и 14 х 12 х 10 мм соответственно, расцененные как очаги вторичного поражения. При комплексном обследовании (включая компьютерную томографию органов грудной клетки и брюшной полости (КТ ОГК и БП), позитронно-эмиссионную томографию совмещенную с КТ (ПЭТ-КТ), эзофагогастродуоденоскопию с биопсией) в области пищеводно-желудочного перехода была выявлена ещё одна опухоль. По результатам планового гистологического исследования - высокодифференцированная аденокарцинома ПЖП.
В связи с увеличением размеров опухоли правой лобной доли и нарастанием неврологической симптоматики, 26.12.2017г. в «НМИЦ нейрохирургии им. академика Н.Н. Бурденко» пациенту была выполнена операция: удаление внутримозговой опухоли правой лобной доли с использованием интраоперационного УЗИ. По данным гистологического исследования операционного материала и результатам иммунофенотипирования: диффузная В-крупноклеточная лимфома головного мозга. В послеоперационном периоде пациенту выполнено 2 курса химиотерапии по схеме темозоломид - ретуксимаб (17.01-21.02.2018г).
В связи с наличием второй синхронной опухоли пищеводно-желудочного перехода, в марте 2018 г. пациент обратился в нашу клинику за консультативной помощью. Пациент предъявлял жалобы на выраженную слабость. Грубой очаговой симптоматики выявлено не было, но сохранялись нарушения в координационной сфере, астенический синдром, присутствовали дизартрия и тремор рук.
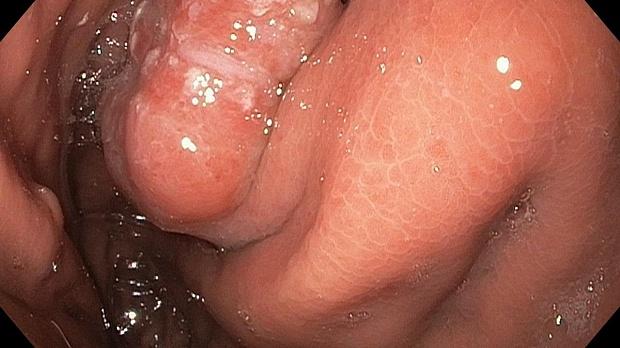
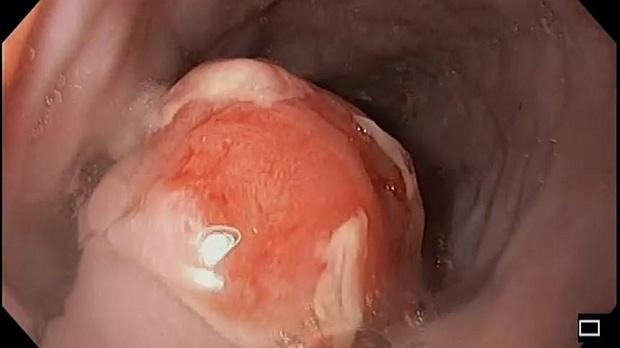
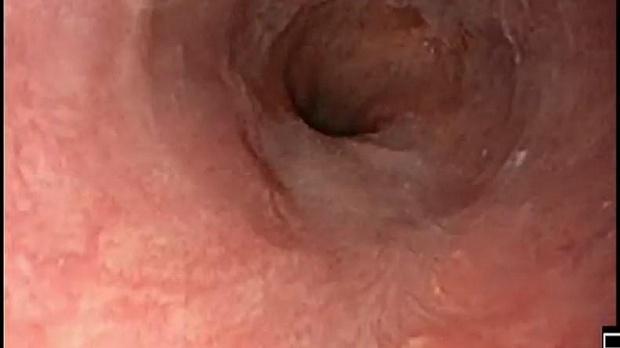
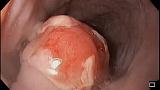
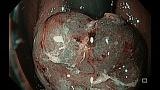
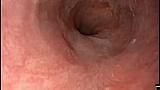
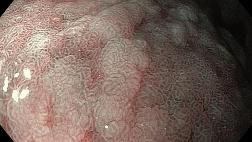
При эндоскопическом осмотре в области ПЖП определялась экзофитная опухоль, размерами 20 х 15 мм, на широком основании, высотой до 5-7 мм, с красной шероховатой поверхностью и налетом фибрина (рис. 1). При инструментальной пальпации опухоль легко смещалась, пролабировала в просвет желудка и пищевода. Аксиальная хиатальная грыжа и особенности расположения опухоли в зоне пищеводно-желудочной перехода не позволили создать необходимую акустическую среду и провести мини-зондовое эндоскопическое ультразвуковое исследование.
При пересмотре стеклопрепаратов и гистологических блоков ранее выполненной биопсии из области ПЖП морфологическая картина соответствовала тубулярной аденоме желудка с признаками интраэпителиальной неоплазии высокой степени с очагами подозрительными в отношении аденокарциномы.
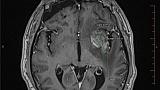
По данным МРТ головного мозга от 21.03.2018г. отмечалась отрицательная динамика в виде увеличения размеров образования в левой височной доле до 36 х 25 мм, увеличения перифокального отека (рис. 2).
Решением общебольничного консилиума удаление опухоли кардиоэзофагеального перехода было отложено в связи с признаками прогрессии опухоли головного мозга, наличием дефицита в неврологической симптоматике, а также высоким риском осложнений после хирургического вмешательства под наркозом. На момент принятия решения опухоль ПЖП, в отличие от опухоли ЦНС, не представляла угрозы для жизни пациента. Было рекомендовано продолжить лечение у гематолога, после стабилизации процесса ЦНС повторно вернуться к вопросу об удалении опухоли ПЖП.
С марта по октябрь 2018г. пациенту проводилось специализированное лечение в гематологическом отделении «ГКБ им. С.П. Боткина ДЗ г. Москвы»: 2 цикла полихимиотерапии (ПХТ) по схеме R-I-R, 5 курсов ПХТ по схеме TMR и 1 курс ПХТ по схеме R-HD-CE. По окончании химиотерапии, по данным МРТ головного мозга от 09.10.2018г. в зоне ранее выявляемого образования в левой височной доле сохранялись отдельные участки слабого накопления контрастного препарата с нечеткими контурами.
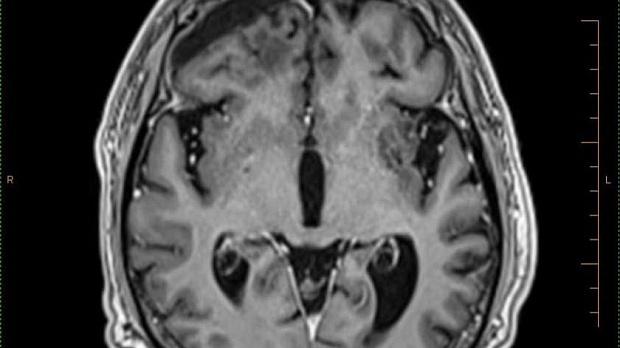
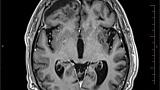
Вторым этапом комплексного лечения лимфомы головного мозга, с 20.11.18г. по 26.12.18г. в ФГАУ «Лечебно-реабилитационный центр» был выполнен курс 3D конформной дистанционной лучевой терапии на весь объем головного мозга в РОД -2 Гр до СОД 36 Гр с последующим увеличением на зону остаточной опухоли в РОД -2Гр до СОД 46 Гр. По данным контрольной МРТ головного мозга от 31.01.2019г: постоперационные кистозно-глиозные изменения в правой лобной доле, уменьшение постоперационной гидромы справа. МР-признаки опухолевого поражения в левой височной доле не обнаружены (рис 3). Таким образом, удалось добиться стабилизации опухолевого процесса в головном мозге. Реабилитационный период продлился три месяца.
В марте 2019г., через один год после первичной консультации, пациент повторно обратился к нам в клинику для дообследования и решения вопроса об удалении аденокарциномы кардиоэзофагеального перехода. На момент обращения у пациента сохранялись жалобы на общую слабость, вялость, повышенную утомляемость, утрату способности к длительному умственному и физическому напряжению, раздражительность, расстройство памяти, нарушение координации движений.
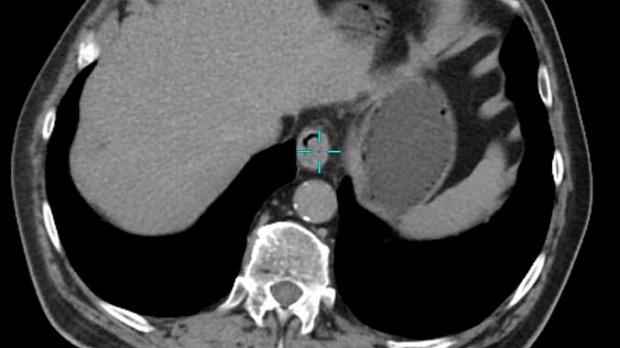
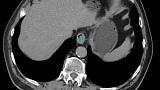
КТ ОГК и БП с контрастным усилением указывала на наличие гиперваскулярного образования по левому контуру области кардиоэзофагеального перехода, размерами 23 х 11 мм, с наличием кратерообразного углубления на поверхности, без признаков инфильтрации окружающей клетчатки (рис 4). Нижние параэзофагеальные лимфоузлы (ЛУ) размером до 7 х 5 мм, кардиальные ЛУ, ЛУ по малой и большой кривизне, пилорические и по ходу левой желудочной артерии размером до 2-4 мм, в области чревного ствола и общей печеночной артерии единичные ЛУ размером до 6 х 11 мм.
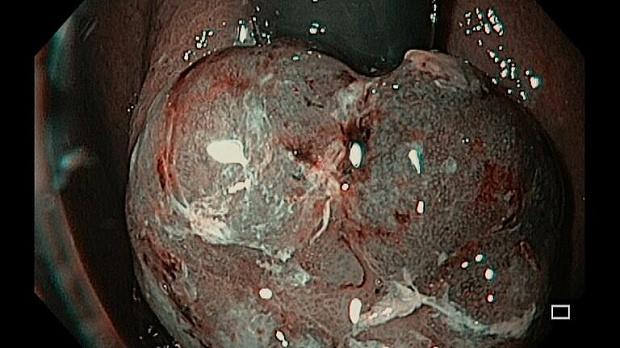
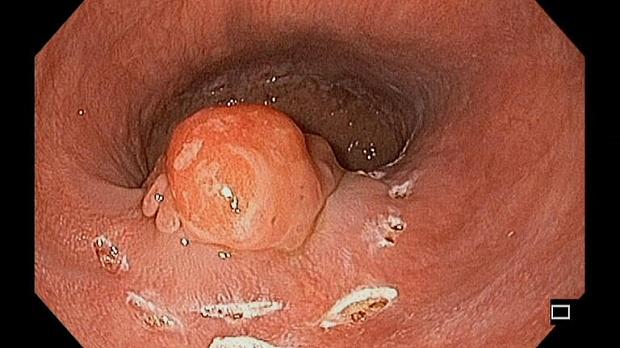
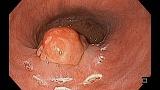
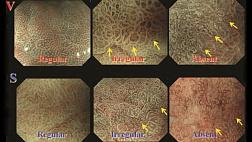
Эндоскопическое исследование пищевода и желудка проводилось в смежном режиме c применением осмотра в белом свете (White Light Endoscopy) и осмотре в узком спектре (Narrow Band Imaging). По результатам эндоскопического осмотра зубчатая линия располагалась по верхнему краю кардиальных складок, на 39 см от резцов, на этом же уровне по задней полуокружности определялся проксимальный край экзофитной опухоли, протяженностью 25-30 мм, шириной до 20 мм, высотой до 12‑14 мм, с контактно ранимой поверхностью покрытой фибрином. Кардия смыкалась не полностью, отмечалось пролабирование кардиальных складок слизистой оболочки с опухолью в просвет пищевода. Уровень пищеводного отверстия диафрагмы определялся на 44 см от резцов. При инверсионном осмотре зоны кардии опухоль смещалась вместе со слизистой оболочкой как в просвет пищевода, так и в просвет желудка. По центру опухоли имелся участок депрессии размерами до 5 х 8 мм, неправильной формы, с четкой демаркационной линией, ямочный и сосудистый рисунок не прослеживались. (рис. 5,6).
Для оценки глубины инвазии опухоли в стенку пищевода и желудка, а также состояния регионарных лимфоузлов была выполнена ультрасонография эхоэндоскопом с радиальным УЗ-датчиком (частота 5-10 МГц). По результатам исследования в области кардиоэзофагеального перехода по задней полуокружности определялось гипоэхогенное образование до 25 х 20 мм, исходящее из слизистого слоя стенки, подслизистый слой прослеживался фрагментарно, мышечный слой был сохранен, интактен, наружный контур стенки пищевода и желудка ровный, четкий (рис. 7). Увеличенные и патологически измененные лимфатические узлы не определялись.
На основании жалоб, анамнеза, данных осмотра и обследований был сформулирован предварительный диагноз: Первично-множественное синхронное злокачественное заболевание: 1) диффузная В-крупноклеточная лимфома с мультифокальным поражением головного мозга, удаление опухоли 26.12.2017г., состояние после двух курсов химиотерапии. Прогрессирование. Состояние после 2 циклов ПХТ по схеме R-I-R. Прогрессирование. Состояние после 5 курсов ПХТ по схеме TMR и 1 курса ПХТ по схеме R-HD-CE. Частичная ремиссия. Состояние после ЛТ в СОД 46 Гр. Стабилизация. 2) кардиоэзофагеальный рак, тип II по Siewert, стадия IА, cT1аN0M0. Сопутствующие заболевания: ишемическая болезнь сердца, гипертоническая болезнь 3 степени, риск 4. Грыжа пищеводного отверстия диафрагмы.
Учитывая данные комплексного предоперационного обследования, а также общее состояние пациента и связанные с этим высокие риски развития тяжёлых операционных и послеоперационных осложнений, на общебольничном консилиуме было принято решение отказаться от хирургического лечения в пользу лечебно-диагностического эндоскопического удаления опухоли ПЖП методом резекции слизистой оболочки с диссекцией подслизистого слоя.
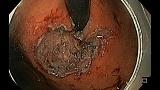
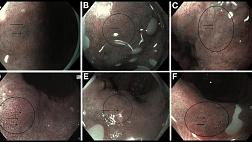
Операция была выполнена 09.04.2019г. через 13 месяцев после диагностики опухоли, под эндотрахеальным наркозом с использованием помпы для подачи воды в дополнительный канал эндоскопа и инсуффляцией углекислого газа. Точечная маркировка слизистой оболочки была выполнена отступя от видимых краев опухоли 4-5 мм с помощью эндоскопического ножа Triangle Knife (рис. 8), циркулярный разрез слизистой оболочки вокруг опухоли (отступя от эндоскопических меток 2‑3 мм) был выполнен с помощью ножей Triangle Knife и IT Knife после введения в подслизистый слой раствора гиалуроновой к‑ты с индигокармином. Далее с помощью эндоскопических ножей была выполнена диссекция подслизистого слоя. Опухоль была удалена единым блоком. Гемостаз видимых сосудов в ложе удаленной опухоли был осуществлён щипцами типа Coagrasper. По окончании операции признаков перфорации, кровотечения не выявлено (рис.9). Операционный препарат (50 х 45 мм) был извлечен, фиксирован и погружен в формалин.
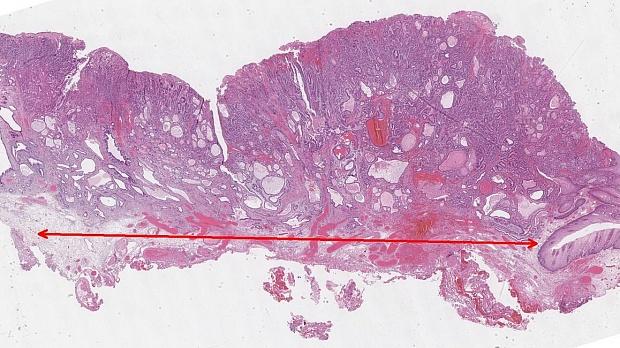
Макроскопическое описание удаленного препарата: фрагмент слизистой оболочки неправильной формы, размерами 48 х 44 х 14 мм. На слизистой определяется изъязвленное экзофитное крупно‑бугристое образование неправильной формы с четкими границами, размерами 30 х 32 х 12 мм, располагающееся на расстоянии 2 мм от проксимального края.
Микроскопической описание: фрагмент слизистой оболочки области пищеводно‑желудочного перехода, представленный слизистой оболочкой пищевода с прилежащими участками слизистой оболочки желудка, с наличием в центральной части, а также ближе к проксимальному краю очагов инвазивного роста аденокарциномы. В области фронта инвазии определяются очаги инвазии лимфатических сосудов. Признаков пищевода Барретта не выявлено. Опухоль прорастает в подслизистый слой. Наибольший горизонтальный размер инвазивного компонента - 25 мм. Во всех исследованных краях препарата признаков опухолевого роста не выявлено.
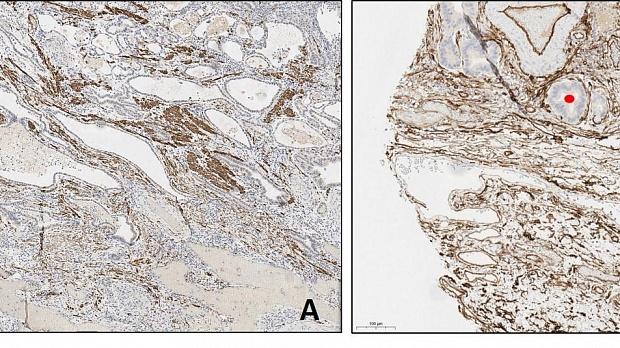
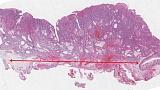
Морфологическое и иммуногистохимическое заключение: умеренно дифференцированная аденокарцинома пищеводно-желудочного перехода, grade II (рис. 10). Опухоль прорастает в подслизистый слой (sm3), в просветах сосудов определяются очаги опухоли (Ly «+», V «+»), в краях препарата признаков опухолевого роста не выявлено, (LM «-», VM «-»), рис. 11.
Учитывая жалобы, анамнез, результаты исследований, интраоперационную картину, результаты морфологического и иммуногистохимического исследований был сформирован окончательный диагноз:
Первично-множественное синхронное злокачественное заболевание: 1) диффузная В-крупноклеточная лимфома с мультифокальным поражением головного мозга, удаление опухоли 26.12.2017г., состояние после двух курсов химиотерапии. Прогрессирование. Состояние после 2 циклов ПХТ по схеме R-I-R. Прогрессирование. Состояние после 5 курсов ПХТ по схеме TMR и 1 курса ПХТ по схеме R-HD-CE. Частичная ремиссия. Состояние после ЛТ в СОД 46 Гр. Стабилизация. 2) кардиоэзофагеальный рак, тип II по Siewert, стадия IB, pT1bN0M0. Эндоскопическое удаление опухоли методом резекции слизистой оболочки с диссекцией подслизистого слоя 09.04.2019г.
Послеоперационный период протекал без осложнений, пациент получал ингибиторы протонной помпы в дозировке 40 мг 2 раза в день внутривенно на протяжении 3 дней, далее по стандартной схеме.
Решением консилиума в послеоперационном периоде дополнительного противоопухолевого лечения назначено не было, пациент оставлен под строгий динамический контроль.
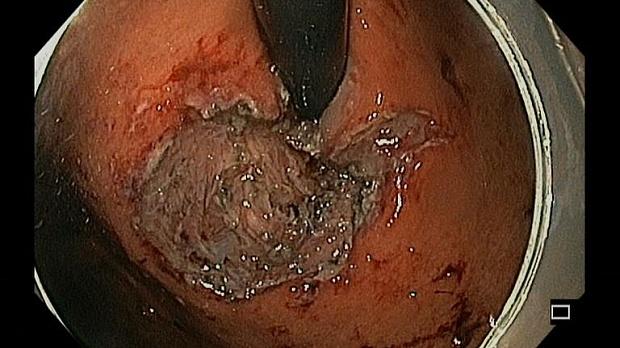
Эзофагогастродуоденоскопия от 03.10.2019г. (через 6 месяцев после операции): на расстоянии 40 см от резцов по задней полуокружности определяется проксимальный край едва заметного плоского белесоватого рубца, протяженностью около 4,0 см, без признаков опухолевого поражения (рис. 12).
КТ ОГК и БП с внутривенным контрастированием от 06.12.19г. (через 8 месяцев после операции): дополнительные образования в пищеводе и желудке не дифференцируются, абдоминальный сегмент пищевода расположен частично выше диафрагмы. КТ данных за мтс-поражение регионарных лимфоузлов и прогрессирование заболевания нет.
МРТ головного мозга от 25.11.19г.: появление мелких опухолевых очагов по оболочкам постоперационной гидромы справа. Зона постоперационных кистозно‑глиозных изменений в правой лобной доле; глиоз в области островка и левой височной доли без динамики.
Таким образом, через 8 месяцев после удаления опухоли кардии, по данным комплексного обследования (включая КТ ОГК и БП с внутривенным контрастированием, эзофагогастродуоденоскопию), признаков местного и отдаленного рецидива кардиоэзофагеального рака не выявлено. Однако, по данным МРТ головного мозга отметилась отрицательная динамика в виде появления мелких опухолевых очагов в зоне удаленной опухоли правой лобной доли. Учитывая исчерпанные резервы химиолучевого лечения лимфомы головного мозга, изменения выявленные при контрольной МРТ головного мозга требуют динамического наблюдения. Пациент чувствует себя удовлетворительно, планируется очередное контрольное обследование.
Список литературы:
Рекомендуемые статьи
При эндоскопическом исследовании в случае бронхоэктазов в стадии ремиссии выявляется
частично диффузный бронхит I степени воспаления
Активируйте PUSH уведомления в браузер
Отключите PUSH уведомления в браузер
Содержание
Интернет магазин
Популярное
- О нас
- Правовые вопросы
- Политика
обработки персональных
данных EndoExpert.ru - Связаться с нами
- Стать партнером
© 2016-2022 EndoExpert.ru

Вы находитесь в разделе предназначенном только для специалистов (раздел для пациентов по ссылке). Пожалуйста, внимательно прочитайте полные условия использования и подтвердите, что Вы являетесь медицинским или фармацевтическим работником или студентом медицинского образовательного учреждения и подтверждаете своё понимание и согласие с тем, что применение рецептурных препаратов, обращение за той или иной медицинской услугой, равно как и ее выполнение, использование медицинских изделий, выбор метода профилактики, диагностики, лечения, медицинской реабилитации, равно как и их применение, возможны только после предварительной консультации со специалистом. Мы используем файлы cookie, чтобы предложить Вам лучший опыт взаимодействия. Файлы cookie позволяют адаптировать веб-сайты к вашим интересам и предпочтениям.
Я прочитал и настоящим принимаю вышеизложенное, хочу продолжить ознакомление с размещенной на данном сайте информацией для специалистов.






.jpg)





.png)


.jpg)















Комментарии