- Компании
- Takeda. О компании, буклеты, каталоги, контакты
- Olympus. О компании, буклеты, каталоги, контакты
- Boston Scientific. О компании, буклеты, каталоги, контакты
- Pentax. О компании, буклеты, каталоги, контакты
- Fujifilm & R-Farm. О компании, буклеты, каталоги, контакты
- Erbe. О компании, буклеты, каталоги, контакты
- Еще каталоги
- Мероприятия
- Информация
- Обучение
- Классификации
- Атлас
- Quiz
- Разделы
- Пациенту
QR-код этой страницы

Для продолжения изучения на мобильном устройстве ПРОСКАНИРУЙТЕ QR-код с помощью спец. программы или фотокамеры мобильного устройства
Документы и приказы: Грыжа пищеводного отверстия диафрагмы. Взрослые. Клинические рекомендации 2024 - 2026

Полный текст статьи:
Министерство
Здравоохранения
Российской Федерации
Клинические рекомендации Грыжа пищеводного отверстия диафрагмы
Год утверждения (частота пересмотра): 2024Пересмотр не позднее:2026
ID: 849_1
Возрастная категория: Взрослые
Разработчик клинической рекомендации Общероссийская общественная организация "Российское общество хирургов"
Одобрены
Оглавление
· 1. Краткая информация по заболеванию или состоянию (группы заболеваний или состояний)
· 1.1 Определение заболевания или состояния (группы заболеваний или состояний)
· 1.2 Этиология и патогенез заболевания или состояния (группы заболеваний или состояний)
· 1.3 Эпидемиология заболевания или состояния (группы заболеваний или состояний)
· 1.4 Особенности кодирования заболевания или состояния (группы заболеваний или состояний) по Международной статистической классификации болезней и проблем, связанных со здоровьем
· 1.5 Классификация заболевания или состояния (группы заболеваний или состояний)
· 1.6 Клиническая картина заболевания или состояния (группы заболеваний или состояний)
· 2. Диагностика заболевания или состояния (группы заболеваний или состояний) медицинские показания и противопоказания к применению методов диагностики
· 2.1 Жалобы и анамнез
· 2.2 Физикальное обследование
· 2.3 Лабораторные диагностические исследования
· 2.4 Инструментальные диагностические исследования
· 2.5 Иные диагностические исследования
· 3. Лечение, включая медикаментозную и немедикаментозную терапии, диетотерапию, обезболивание, медицинские показания и противопоказания к применению методов лечения
· 4. Медицинская реабилитация и санаторно-курортное лечение, медицинские показания и противопоказания к применению методов медицинской реабилитации, в том числе основанных на использовании природных лечебных факторов
· 5. Профилактика и диспансерное наблюдение, медицинские показания и противопоказания к применению методов профилактики
· 6. Организация оказания медицинской помощи
· 7. Дополнительная информация (в том числе факторы, влияющие на исход заболевания или состояния)
· Критерии оценки качества медицинской помощи
· Список литературы
· Приложение А1. Состав рабочей группы по разработке и пересмотру клинических рекомендаций
· Приложение А2. Методология разработки клинических рекомендаций
· Приложение А3. Справочные материалы, включая соответствие показаний к применению и противопоказаний, способов применения и доз лекарственных препаратов, инструкции по применению лекарственного препарата
· Приложение Б. Алгоритмы действий врача
· Приложение В. Информация для пациента
· Приложение Г1-ГN. Шкалы оценки, вопросники и другие оценочные инструменты состояния пациента, приведенные в клинических рекомендациях
Список сокращений
ГПОД – грыжа пищеводного отверстия диафрагмы
ГЭРБ – гастроэзофагеальная рефлюксная болезнь
КТ – компьютерная томография
МО – медицинская организация
МРТ – магнитно-резонансная томография
УЗИ – ультразвуковое исследование
ЭГДС – эзофагогастродуоденоскопия
Термины и определения
Грыжей называют выхождение покрытых брюшиной внутренних органов через естественные или искусственные (возникшие после травмы, хирургических вмешательств) отверстия в брюшной стенке, тазового дна, диафрагмы под наружные покровы тела или в другую полость.
Грыжевые ворота – врожденный или приобретенный дефект в мышечноапоневротическом слое брюшной стенки и/или диафрагме.
Грыжевой мешок – часть париетальной брюшины, выпячивающаяся через грыжевые ворота. Содержимое грыжевого мешка может быть представлено любым органом брюшной полости.
Грыжа пищеводного отверстия диафрагмы – заболевание, связанное со смещением через расширенное пищеводное отверстие диафрагмы в грудную полость абдоминального отдела пищевода, кардии, верхнего отдела желудка (в запущенных случаях - всего желудка), а также других органов, чаще петель кишечника, вызывающее сдавление и смещение органов и структур заднего средостения.
Рецидивная грыжа пищеводного отверстия диафрагмы – грыжа, появившаяся в области ранее выполненного грыжесечения.
1. Краткая информация
1.1 Определение заболевания или состояния (группы заболеваний или состояний)
Грыжа пищеводного отверстия диафрагмы (ГПОД) - заболевание, связанное со смещением через расширенное пищеводное отверстие диафрагмы в грудную полость абдоминального отдела пищевода, кардии, верхнего отдела желудка (в запущенных случаях - всего желудка), а также других органов, чаще петель кишечника, вызывающее сдавление и смещение органов и структур заднего средостения
1.2 Этиология и патогенез заболевания или состояния (группы заболеваний или состояний)
ГПОД могут быть как врожденными, так и приобретенными. В основе врожденных ГПОД лежат аномалии внутриутробного развития. Врожденный короткий пищевод («грудной желудок») – это аномалия эмбриональной закладки кардиальной части пищеварительного тракта вследствие задержки роста пищевода на ранних этапах эмбрионального развития. Согласно теории С.Я. Долецкого (1960), дети нередко рождаются с умеренно выраженным неопущением желудка, однако желудок в дальнейшем перемещается в брюшную полость. Если при этом развивается рефлюкс-эзофагит, сопровождающийся рубцовым процессом, то пищевод может фиксироваться в средостении и, таким образом, формируется врожденная ГПОД.
Ряд авторов (Б.П. Покровский, Н.Н. Каншин и др.) считают, что все ГПОД в детском возрасте необходимо считать врожденными.
Приобретенные ГПОД развиваются во взрослом состоянии, хотя нельзя исключать возможность их развития и в детском возрасте.
Согласно одной из теорий патогенеза ГПОД (В.Я. Бараков, 1957; В.И. Соболев, 1957), развитие грыжи у взрослых людей связано с частичной атрофией мышечных волокон, которая становится более выраженной в пожилом возрасте. В результате атрофии ослабляются межмышечные связи, опускается диафрагма и, как следствие, расширяется пищеводное отверстие диафрагмы. Развитию мышечной атрофии в более молодом возрасте способствует недостаточная физическая нагрузка. Это объясняет тот факт, что ГПОД часто развивается у пациентов, не занимаюшихся физическим трудом и не ведущих активный образ жизни. Опущению диафрагмы способствует эмфизема легких.
Кроме расширения пищеводного отверстия диафрагмы в развитии ГПОД играет роль нарушение фасциальных связей пищевода, растяжение пищеводно-диафрагмальной мембраны. Это связано, с одной стороны, с генетической предрасположенностью в виде так называемой «слабости соединительной ткани». Этим объясняется тот факт, что ГПОД часто сочетается с грыжами других локализаций, плоскостопием, варикозным расширением подкожных вен нижних конечностей, геморроем. С другой стороны, к растяжению пищеводно-диафрагмальной мембраны приводит значительный набор веса или резкое похудание [21].
Расширение пищеводного отверстия диафрагмы и расслабление пищеводно-диафрагмальной мембраны создают анатомические предпосылки для развития ГПОД, а провоцирующим фактором является увеличение разницы давления в брюшной и грудной полостях. Повышение внутрибрюшного давления способствует «выталкиванию» желудка в грудную клетку. Вторым фактором, приводящим к развитию ГПОД, считается подтягивание кардии вверх вследствие интенсивного сокращения продольной мускулатуры пищевода. Впервые выдвинул эту теорию Бергманн в 30-х годах XX века, после того как в эксперименте на собаках, раздражая шейный отдел блуждающего нерва, наблюдал толчкообразный подъем желудка вверх с одновременным резким продольным сокращением пищевода. Этим механизмом можно объяснить развитие ГПОД при сопутствующих заболеваниях, сопровождающихся раздражением блуждающего нерва, например при желчнокаменной болезни, при пенетрирующих в поджелудочную железу язвах и т.д. Сторонники этой теории считают, что все заболевания, которые так или иначе приводят к раздражению блуждающего нерва, способствуют развитию аксиальных скользящих ГПОД.
ГПОД травматического генеза впервые описал Stoianoff (1900). В 1962 году Marchard впервые описал несколько клинических случаев развития клиники ГПОД у пациентов после закрытой травмы живота. При этом посттравматической грыжей такие ГПОД назвать нельзя, так как не было разрыва диафрагмы. Таким образом считается, что развитию ГПОД при наличии соответствующих анатомических предпосылок может способствовать закрытая травма живота.
Операции на желудке и диафрагме также могут приводить к развитию ГПОД. Кроме того, после этих операций могут клинически начать проявляться бессимптомные до этого ГПОД. Причина – поступление в пищевод тонкокишечного содержимого.
Считается, что короткий пищевод формируется в результате рефлюкс-эзофагита, который развивается из-за сопутствующей гастроэзофагеальной рефлюксной болезни (ГЭРБ) при скользящих аксиальных ГПОД. Рефлюкс-эзофагит приводит к воспалительному продольному рубцовому сморщиванию пищевода. Другая теория возникновения укорочения пищевода базируется на упомянутых опытах Бергманна и связана с продольным спастическим сокращением пищевода. Согласно этой теории, спастические сокращения гладкой мускулатуры пищевода сменяются развитием рубцовой ткани, то есть имеет место переход функциональной стадии заболевания в органическую. При этом в результате спастического сокращения пищевода вторично развивается аксиальная скользящая ГПОД, а сопутствующие ГЭРБ и рефлюкс-эзофагит приводят к развитию короткого пищевода.
1.3 Эпидемиология заболевания или состояния (группы заболеваний или состояний)
ГПОД является широко распространенным заболеванием: встречается у 5% всего взрослого населения, причем у 50% пациентов ГПОД не сопровождается клиническими проявлениями и, следовательно, не диагностируется.
В Российской Федерации в 2023 г. по данным главного хирурга МЗ РФ было выполнено 4 680 плановых операций при ГПОД. Преобладали лапароскопические вмешательства (85,9%). Послеоперационная летальность составила 0,18% [111].
1.4 Особенности кодирования заболевания или состояния (группы заболеваний или состояний) по Международной статистической классификации болезней и проблем, связанных со здоровьем
K44.0 Диафрагмальная грыжа с непроходимостью без гангрены
K44.1 Диафрагмальная грыжа с гангреной
K44.9 Диафрагмальная грыжа без непроходимости или гангрены
1.5 Классификация заболевания или состояния (группы заболеваний или состояний)
Общепринятой классификации ГПОД в настоящее время нет.
Ниже приводятся классификации ГПОД, наиболее распространенные в отечественной литературе, которые можно использовать в практической деятельности в отдельности. Целесообразно придерживаться международной классификации, дополняя ее классификацией короткого пищевода Б.В. Петровского и Н.Н. Каншина (1962 г.), поскольку в случае наличия у пациента короткого пищевода, его степень необходимо отражать в диагнозе.
I. Анатомо-рентгенологическая классификация ГПОД (наиболее распространенная классификация в России):
1. Скользящая (аксиальная, осевая) грыжа - характеризуется тем, что абдоминальная часть пищевода, кардия и фундальная часть желудка могут через расширенное пищеводное отверстие диафрагмы свободно проникать в грудную полость и возвращаться обратно в брюшную полость (при перемене положения больного).
2. Параэзофагеальная грыжа - конечная часть пищевода и кардия остаются под диафрагмой, но часть фундального отдела желудка проникает в грудную полость и располагается рядом с грудным отделом пищевода (параэзофагеально).
3. Смешанный вариант грыжи - сочетание аксиальной и параэзофагеальной грыж.
II. Kлассификация ГПОД в зависимости от объема проникновения желудка в грудную полость, в основе которой лежат рентгенологические проявления заболевания (И.Л. Тагер, А.А. Липко, 1965 г.):
ГПОД I степени: в грудной полости (над диафрагмой) находится абдоминальный отдел пищевода, кардия - на уровне диафрагмы, желудок приподнят и непосредственно прилежит к диафрагме.
ГПОД II степени: в грудной полости располагается абдоминальный отдел пищевода, непосредственно в области пищеводного отверстия диафрагмы - часть желудка.
ГПОД III степени: над диафрагмой находятся абдоминальный отдел пищевода, кардия и часть желудка (дно и тело, в тяжелых случаях и антральный отдел).
III. Клиническая классификация В.Х. Василенко и А.Л. Гребенева (1978 г.), которая нередко представлена в сокращенном варианте:
· фиксированные или нефиксированные грыжи (для аксиальных и параэзофагеальных грыж);
· аксиальная грыжа: пищеводная, кардиофундальная, субтотально- и тотально-желудочная;
· параэзофагеальная грыжа (фундальная, антральная);
· врожденный короткий пищевод с «грудным желудком» (аномалия развития);
· грыжи другого типа (тонкокишечные, сальниковые и др.).
В случае применения классификации В.Х. Василенко и А.Л. Гребенева (1978 г.) диагноз следует формулировать в соответствии с полной версией классификации:
1. Тип грыжи:
o фиксированные или нефиксированные (для аксиальных и параэзофагеальных грыж);
o аксиальная: пищеводная, кардиофундальная, субтотально- и тотально-желудочная;
o параэзофагеальная (фундальная, антральная);
o врожденный короткий пищевод с «грудным желудком» (аномалия развития);
o грыжи иного типа (тонкокишечные, сальниковые и др.).
2. Осложнения:
o рефлюкс-эзофагит (морфологическая характеристика: катаральный, эрозивный, язвенный);
o пептическая язва пищевода;
o воспалительно рубцовое стенозирование и/или укорочение пищевода (приобретенное укорочение пищевода), степень их выраженности;
o острое или хроническое пищеводное (пищеводно-желудочное) кровотечение;
o ретроградный пролапс слизистой оболочки желудка в пищевод;
o инвагинация пищевода в грыжевую часть;
o перфорация пищевода;
o рефлекторная стенокардия;
o ущемление грыжи (при параэзофагеальных грыжах).
3. Производящая причина:
o дискинезия пищеварительного тракта;
o повышение внутрибрюшного давления;
o возрастное ослабление соединительнотканных структур и др.
4. Механизм возникновения грыжи:
o пульсионный;
o тракционный;
o смешанный.
5. Сопутствующие заболевания.
6. Степени тяжести рефлюкс-эзофагита:
o легкая степень (слабая выраженность симптоматики, иногда ее отсутствие (в этом случае наличие эзофагита констатируется на основании данных рентгенографии пищевода, эзофагоскопии и прицельной биопсии);
o средняя степень тяжести (симптоматика заболевания выражена, есть ухудшение общего самочувствия и снижение работоспособности);
o тяжелая степень (выраженная симптоматика эзофагита и присоединение осложнений, в первую очередь, пептических стриктур и рубцовых укорочений пищевода).
IV. Классификация ГПОД Б.В. Петровского и Н.Н. Каншина (1962 г.):
I. Грыжи пищеводного отверстия диафрагмы скользящего (аксиального) типа:
1. пищеводная грыжа пищеводного отверстия диафрагмы;
2. кардиальная грыжа пищеводного отверстия диафрагмы;
3. кардиально-фундальная грыжа пищеводного отверстия диафрагмы.
II. Грыжа пищеводного отверстия диафрагмы параэзофагеального типа:
1. фундальная грыжа пищеводного отверстия диафрагмы;
2. антральная грыжа пищеводного отверстия диафрагмы;
3. кишечная грыжа пищеводного отверстия диафрагмы (тонкокишечная и толстокишечная);
4. комбинированная кишечно-желудочная грыжа пищеводного отверстия диафрагмы (сочетание кишечной грыжи с той или иной формой больших грыж, образованных желудком);
5. сальниковая грыжа пищеводного отверстия диафрагмы.
III. Гигантские грыжи пищеводного отверстия диафрагмы:
1. субтотальная желудочная грыжа пищеводного отверстия диафрагмы;
2. тотальная желудочная грыжа пищеводного отверстия диафрагмы.
IV. Короткий пищевод (brachyoesophagus) 1-й и 2-й степени:
1. приобретенный короткий пищевод;
2. врожденный короткий пищевод (грудной желудок).
К 1-й степени авторы относили короткий пищевод, когда кардия фиксирована не выше 4 см над диафрагмой. Ко 2-й степени – кардия находится на 4 см выше диафрагмы.
V. Современная анатомическая классификация, принятая консенсусами большинства европейских стран и США (I-IV типы ГПОД):
Тип I - скользящие ГПОД, когда гастроэзофагеальный переход смещается выше диафрагмы. Желудок располагается в обычном продольном положении, дно желудка остается ниже гастроэзофагеального перехода.
Тип II - параэзофагеальные грыжи; гастроэзофагеальный переход остается в нормальном анатомическом положении, но часть дна желудка, которая прилегает к пищеводу, выходит через диафрагмальное отверстие.
Тип III представляет собой комбинацию I и II типов: гастроэзофагеальный переход и дно желудка выпячиваются через пищеводное отверстие диафрагмы. Дно желудка располагается над гастроэзофагеальным переходом.
Тип IV: тип III + другие органы брюшной полости (толстая кишка, селезенка, поджелудочная железа).
1.6 Клиническая картина заболевания или состояния (группы заболеваний или состояний)
Основными симптомами ГПОД I типа являются проявления гастроэзофагеального рефлюкса, развитие которого связано, в первую очередь, с расширением угла Гисса и, как следствие, сглаживанием клапана Губарева. ГПОД в 80-90% случаев сопровождается ГЭРБ [54], при этом около 60% пациентов с ГПОД предъявляют жалобы на гастроэзофагеальный рефлюкс [64]. Таким образом, не все ГПОД I типа сопровождаются гастроэзофагеальным рефлюксом, что и объясняет наличие так называемых «бессимптомных» ГПОД. У пациентов со сниженной желудочной кислотностью рефлюкс не сопровождается симптомами. Принято считать, что клинические проявления ГПОД всегда обусловлены наличием рефлюкс-эзофагита.
ГПОД является фактором риска развития эрозивного рефлюкс-эзофагита [103].
Следует отметить, что отсутствие при ЭГДС макроскопических признаков эзофагита не исключает его наличие. Так, еще в 1958 году В.И. Савельев, который изучал развитие эзофагита на собаках после формирования пищеводно-желудочных анастомозов, доказал, что на гистологических препаратах поражение слизистой пищевода выявлялось чаще, чем макроскопически. Отсутствие макроскопических изменений со стороны слизистой пищевода при длительно существующем гастроэзофагеальном рефлюксе объясняется неодинаковой устойчивостью слизистой к воздействию соляной кислоты у разных людей. Не последнюю роль в этом играет состояние иннервации пищевода.
Самым частым симптомом при ГПОД является боль, которая локализуется преимущественно в эпигастральной области, но может быть и загрудинно, и в правом, и в левом подреберье. Боль часто носит жгучий характер. Иррадиация боли может быть различной, чаще вверх (загрудинно, в область сердца, лопатку, левое плечо, шею), но также и в левое подреберье, в оба подреберья и даже в поясницу. У большинства пациентов боль возникает спустя некоторое время после приема пищи, особенно в положении лежа. Боль также часто развивается во время физической нагрузки, связанной с наклоном туловища, физическим или психоэмоциональным напряжением. Не всегда можно однозначно связать болевой синдром с ГПОД. Поэтому если проявление боли не типично для рефлюкс-эзофагита, то высока вероятность того, что боль имеет другую причину.
Для рефлюкс-эзофагита характерна жгучая боль на уровне мечевидного отростка за грудиной, которая усиливается после еды и в горизонтальном положении, а также сопровождается другими типичными симптомами гастро-эзофагеального рефлюкса.
Вторым по частоте симптомом при ГПОД является изжога.
Срыгивание, которое часто достигает ротоглотки, является следствием гастроэзофагеального рефлюкса, возникает внезапно в горизонтальном положении, либо при наклонах туловища и не сопровождается тошнотой. Внезапность срыгивания является причиной аспирации, что вызывает приступ кашля и/или неприятное чувство «першения» в горле, а иногда приводит к потере голоса в результате химического воздействия срыгиваемой жидкости на голосовые связки.
Срыгивание, изжога и отрыжка являются признаками несостоятельности кардии, однако одновременно все три симптома у одного пациента встречаются нечасто.
Тошнота и рвота являются редкими симптомами ГПОД.
Дисфагия чаще всего связана с сужением пищевода вследствие развития пептической стриктуры на фоне рефлюкс-эзофагита, либо с онкологией. Дисфагия, связанная непосредственно с ГПОД, встречается редко и как правило выражена незначительно, появляется периодически, часто усиливается при волнении и при спешке во время приема пищи. Клинически задержку пищи при ГПОД пациенты описывают на уровне мечевидного отростка.
Развитие дисфагии может быть связано также с ущемлением параэзофагеальных грыж. В этом случае дисфагия развивается остро и сопровождается интенсивным болевым синдромом.
Одышка и затруднение дыхания при ГПОД возникает преимущественно в горизонтальном положении.
При ГПОД может развиваться так называемая «рефлекторная стенокардия».
Анемия при ГПОД может развиться в силу разных причин. Первая причина – рефлюкс-эзофагит. Кровотечение может происходить как из эрозий слизистой пищевода, так и непосредственно из самой слизистой путем диапедеза. Такие кровотечения чаще бывают незначительные и приводят к развитию анемии в случае длительного персистирования. Однако, кровотечения при эрозивном рефлюкс-эзофагите могут быть и профузными. Вторая причина – кровотечение из слизистой желудка. В частности, при кардио-фундальной ГПОД значительная часть желудка находится выше диафрагмы и в результате некоторого пережатия органа на уровне пищеводного отверстия диафрагмы возникает нарушение венозного оттока. При этом в зоне сдавления из-за механического повреждения легко образуются поверхностные эрозии и язвы. Анемия при ГПОД чаще всего гипохромная, что можно связать как с кровотечениями, так и с нарушением усвоения организмом железа. Согласно одной из теорий, хроническая травматизация стенки желудка (особенно при больших ГПОД) уменьшает его секрецию, что в свою очередь может негативно отражаться на усвоении организмом железа.
Некоторыми авторами отмечается развитие спленомегалии при ГПОД, что связывают со сдавлением, тромбозом селезеночной вены.
Гигантские ГПОД часто проявляются нарушением эвакуации съеденной пищи из желудка. В клинической практике этот симптом связывают с ущемлением желудка в грыжевых воротах, что не совсем верно, так как на самом деле причина заключается в завороте желудка в грыжевом мешке. В англоязычной литературе есть термин «upside-down stomach», то есть перевернутый «вверх ногами» желудок. Поворот желудка осуществляется на 180°, при этом большая кривизна оказывается обращена вправо, а малая - влево. В периоды обострения клиническая картина напоминает симптомы стеноза привратника, но с наслоением симптомов, которые связаны с расположением расширенного, переполненного содержимом желудка не в брюшной полости, а в грудной клетке. В рвотных массах у таких пациентов нередко обнаруживают примесь крови.
При приобретенном коротком пищеводе симптомы ГЭРБ, как правило, значительно выражены и нередко сочетаются с пептической стриктурой.
2. Диагностика
Диагноз устанавливается на основании выявления ГПОД одним из следующих методов: рентгеноскопия пищевода и желудка; ЭФГДС; компьютерная томография.
2.1 Жалобы и анамнез
· При опросе пациента с ГПОД рекомендуется обращать внимание на жалобы, связанные со смещением органов в заднее средостение и жалобы, связанные с гастроэзофагеальным рефлюксом [1, 13, 21, 36, 59].
Уровень убедительности рекомендаций – В (уровень достоверности доказательств – 2).
Комментарий. Жалобы, связанные с самой ГПОД и жалобы, связанные с гастроэзофагеальным рефлюксом, различаются. Из анамнеза уже можно заподозрить наличие у пациента большой ГПОД. Пациенты со скользящими аксиальными ГПОД предъявляют жалобы, связанные с гастроэзофагеальным рефлюксом: жгучие боли без регургитации съеденной пищей. Пациентов с параэзофагеальными ГПОД, смешанными формами больше беспокоят регургитация съеденной пищи, боль после приема пищи, чувство сдавления за грудиной и респираторные симптомы. Наличие синдрома Кемерона приводит к развитию клиники желудочного кровотечения и анемии, что является частым симптомом при больших ГПОД [101].
Развитие пищевода Баррета часто связано с ГПОД [1, 51]. В опубликованном Eusebi L.H. и соавт. (2021) метаанализе выявлена взаимосвязь развития пищевода Баррета и употребления алкоголя, особенно при наличии у пациента ГПОД [51].
2.2 Физикальное обследование
· Всем больным с ГПОД рекомендуется физикальное обследование (осмотр, перкуссия, пальпация, аускультация органов грудной и брюшной полостей) с обязательной оценкой нутритивного статуса. [13, 15, 19, 24].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 5).
Комментарий. При физикальном обследовании необходимо обращать внимание не только на различные клинические проявления ГПОД, включая дефицит питания, но и наличие осложнений заболевания.
2.3 Лабораторные диагностические исследования
Лабораторные исследования не имеют диагностического значения в случае неосложненной ГПОД. Они назначаются при подготовке пациента к операции. Объем лабораторных исследований зависит от наличия у пациента сопутствующих заболеваний, предполагаемого вида анестезии и метода хирургического лечения.
2.4 Инструментальные диагностические исследования
· Обзорная рентгенография органов грудной клетки - не рекомендуется использовать как метод диагностики ГПОД [31, 45, 54].
Уровень убедительности рекомендации – С (уровень достоверности доказательств – 5).
Комментарий. На обзорной рентгенограмме органов грудной клетки возможно предположить наличие у пациента ГПОД в случае, когда грыжевое выпячивание больших размеров и фиксировано в заднем средостении. При этом имеется затемнение мягких тканей в грудной клетке с уровнем жидкости или без него. Наличие ретрокардиального уровня жидкости на рентгенограмме грудной клетки является патогномоничным признаком для параэзофагеальной грыжи пищеводного отверстия диафрагмы. Газовый пузырь в грудной клетке наблюдается в случаях, когда содержимым ГПОД являются петли толстого кишечника.
· В качестве основного метода диагностики ГПОД у пациентов с установленным диагнозом и при подозрении на наличие ГПОД рекомендуется рентгеноскопия пищевода и желудка с барием [70, 81, 86, 88].
Уровень убедительности рекомендации – В (уровень достоверности доказательств – 2).
Комментарии. Рентгеноскопия пищевода и желудка с барием позволяет получить информацию о размере ГПОД, типе ГПОД, наличии/отсутствии нарушения моторики пищевода, пептической стриктуры/стеноза пищевода, вызванных ГЭРБ, а также подтвердить или исключить наличие короткого пищевода и уточнить его степень [86]. Большинство опубликованных результатов исследований указывают на то, что рентгеноскопия пищевода и желудка по-прежнему остается важным методом в диагностике ГПОД [70]. По мнению Siegal S.R. и соавторов (2017), ГПОД можно диагностировать этим методом, если размер аксиальной грыжи больше 2 см [88]. Рекомендуется записывать видеоэзофаграмму, которая позволяет получить дополнительную информацию о продвижении контрастного вещества по пищеводу [81].
· Компьютерная томография (КТ) органов грудной полости в сочетании с КТ органов брюшной полости рекомендуется при гигантских ГПОД, при подозрении на ущемление параэзофагеальной ГПОД и во всех неясных клинических ситуациях, а также с целью выявления сопутствующей патологии [47, 86].
Уровень убедительности рекомендации – В (Уровень достоверности доказательств – 2).
Комментарий. КТ (А06.09.005 и А06.30.005) не рекомендуется к выполнению в обязательном порядке. КТ выполняется для получения дополнительной информации о местоположении и типе ГПОД при ее больших размерах. Нередко ГПОД обнаруживают случайно при выполнении КТ по другим показаниям [86]. Dallemagne et al. (2018) рекомендуют выполнять КТ для исключения перфорации, пневмоперитонеума или пневмомедиастинума [47]. КТ показана также при подозрении на ущемление ГПОД [86].
· Всем пациентам с подозрением ГПОД или с уже установленным диагнозом ГПОД рекомендуется выполнять эзофагогастродуоденоскопию (ЭГДС) [28, 46, 61, 86].
Уровень убедительности рекомендации – В (Уровень достоверности доказательств – 2).
Комментарий. После сбора жалоб, анамнеза и физикального обследования базовой инвазивной диагностикой ГПОД является ЭГДС, которая позволяет осмотреть пищеводно-желудочный переход и исключить онкологическое заболевание. Кроме того, ЭГДС дает важнейшую информацию по наличию/отсутствию ГЭРБ, выраженность которой необходимо описывать по общепринятым для этого классификациям (например, по Лос-Анджелеской классификации), пищевода Барретта, язвы Камерона и поражения, подозрительные на злокачественность[28, 46]. Смещение пищеводно-желудочного перехода выше Z-линии с интерстинальной метаплазией (пищевод Баррета) необходимо описывать согласно пражской классификаци пищевода Баррета (2004 г.) [61]. Roman S. и соавт. (2016) обращают внимание на то, что избыточное нагнетание воздуха в желудок при эндоскопическом исследовании может привести к увеличению размера грыжи [86].
2.5 Иные диагностические исследования
· Пациентам в случае выполнения антирефлюксной операции при ГПОД I типа рекомендуется выполнять суточную внутрипищеводную РН-метрию и манометрию пищевода высокого разрешения с целью исключения заболеваний пищевода, которые сопровождаются нарушением его моторики, например ахалазии кардии [3, 28, 48, 64, 81, 83, 86, 106].
Уровень убедительности рекомендации – В (Уровень достоверности доказательств – 1).
Комментарий. Функциональная хирургия пищевода означает дифференциальную гастроэзофагеальную диагностику. Суточная РН-метрия и манометрия пищевода высокого разрешения являются необходимыми составляющими для принятия решения о хирургическом лечении у пациентов с ГЭРБ в сочетании с ГПОД, как правило, I типа. Суточная РН-метрия не является обязательным методом диагностики ГПОД, но важна для количественного анализа эпизодов рефлюкса [81]. Перед антирефлюксными операциями у пациентов с ГПОД I типа необходимо исключать нарушения моторики пищевода, которые возникают при таких заболеваниях, как, например, ахалазия кардии [3, 28, 64, 83]. Проверить состояние моторики пищевода можно с помощью манометрии высокого разрешения (МВР), поскольку она обеспечивает регистрацию давления в реальном времени [86, 106]. Однако размещение катетера для проведения манометрии является довольно непростой задачей и Dallemagne et al. (2018) сообщили, что метод эффективен менее чем в 50% случаев [48].
· Пациентам с симптоматическими ГПОД (тип II, III, IV) проведение суточной пищеводной РН-метрии и манометрии пищевода высокого разрешения рутинно выполнять не рекомендуется. [24, 28, 31, 72, 94].
Уровень убедительности рекомендации – В (Уровень достоверности доказательств – 2).
Комментарий. Для определния гастроэзофагеального рефлюкса используется многоканальная внутрипросветная импеданс-рН-метрия, которая позволяет в большинстве случаев определить кислый или слабокислый гастроэзофагеальный рефлюкс, а также зафиксировать регургитацию газа из желудка. [24, 28, 31].
При симптоматических ГПОД (тип II, III, IV) часто показания к операции определяются по другим критериям, поэтому проведение суточной РН-метрии и манометрии пищевода высокого разрешения можно не выполнять [72, 94].
Магнитно-резонансную томографию (МРТ) рекомендовано применять при ГПОД только для динамического контроля оперированных пациентов с целью контроля положения сетчатого импланта при наличии для этого клинических показаний [72, 94].
Уровень убедительности рекомендации – В (Уровень достоверности доказательств – 2).
3. Лечение
3.1. Консервативное лечение
· Лечение ГПОД может быть только хирургическим. Консервативного лечения не существует [1, 15, 24, 28, 31 89].
Комментарий. Консервативное лечение заключается в лечении сопутстсвующей ГЭРБ и ее осложнений, прежде всего рефлюкс-эзофагита [89].
3.2. Хирургическое лечение
· Рекомендуется различать показания к антирефлюксным операциям у пациентов с ГПОД I типа и показания к операциям у пациентов с ГПОД II–IV типов [10, 11, 17, 30, 31, 36, 102].
Уровень убедительности рекомендации – В (Уровень достоверности доказательств – 1).
Комментарий. Целью антирефлюксной операции при ГПОД I типа является формирование фундопликационной манжеты в нижней трети пищевода и тем самым ликвидация гастроэзофагеального рефлюкса, при симптоматических ГПОД II–IV типов – коррекция неправильного положения желудка и других органов, сместившихся внутрь грудной клетки. При этом не важно наличие/отсутствие у этих пациентов ГЭРБ [102].
· Хирургическое лечение пациентам с ГПОД I типа при отсутствии осложнений ГЭРБ не рекомендуется [25, 33, 37, 49].
Уровень убедительности рекомендации – В (Уровень достоверности доказательств – 1).
· Хирургическое лечение пациентам с ГПОД I типа рекомендуется при наличии осложнений ГЭРБ, а также при неэффективности консервативного лечения ГЭРБ в течение 6 месяцев, либо в случае отказа пациента от проведения консервативной терапии в течение длительного времени [6, 16, 17, 22, 23, 24, 27, 77, 101].
Уровень убедительности рекомендации – С (Уровень достоверности доказательств – 5).
Комментарий. Показанием к операции по поводу ГПОД I типа является ГЭРБ [16, 17]. Во время операции по поводу ГЭРБ в обязательном порядке выполняется фундопликация и устраняется сама ГПОД.
Показания к хирургическому лечению за прошедшие годы мало изменились [6, 77, 111]. Первым показанием является прогрессирование ГЭРБ, которая проявляется типичными симптомами (изжога, регургитация), наличием функциональных дефектов (несостоятельность кардиоэзофагеального перехода, ГПОД) и/или наличием осложнений ГЭРБ (рефлюкс-эзофагит, пищевод Баррета), а также необходимостью повышать дозы лекарственных средств из-за неэффективности консервативного лечения [22, 23, 24, 27].
Вторым показанием является наличие не связанных с соляной кислотой симптомов, несмотря на проведение медикаментозной терапии. Например, рецидивирующие аспирации, «объемный рефлюкс» или регургитация.
Третим показанием является рецидирование симптомов при попытке отменить медикаментозную терапию. Антирефлюксная операция является альтернативой длительной медикаментозной терапии, например при индивидуальной непереносимости препаратов или при отказе пациента от консервативной терапии [77, 111].
· Пищевод Баррета рекомендуется не считать противопоказанием для хирургического лечения ГПОД [1, 2, 4, 26, 45, 60, 98].
Уровень убедительности рекомендации – С (Уровень достоверности доказательств – 5).
Комментарий. Наличие пищевода Баррета не является противопоказанием для операции при ГПОД [1, 2, 4, 26, 98]. При этом не доказано, что хирургическое лечение при пищеводе Баррета с антирефлюксным компонентом (фундопликация) предотвращает развитие онкологии [45, 98]. Антирефлюксная хирургия в этом случае служит для контроля и улучшения клинической ситуации [60].
· Пациентам с ГПОД II, III и IV типов рекомендуется хирургическое лечение в плановом порядке [18, 31, 41, 47, 52, 75, 80, 109, 110].
Уровень убедительности рекомендации – С (Уровень достоверности доказательств – 5).
Комментарий. Параэзофагеальная ГПОД является показанием к операции, что подтверждается многочисленными исследованиями [31, 41, 47, 75, 80, 109, 110]. Основанием для этого является постепенное увеличение размера ГПОД с увеличением риска ущемления, что сопряжено с высокой вероятностью осложнений и летальности при операциях, выполненных по неотложным показаниям [18]. Однако, watchfull-waiting-концепция (то есть наблюдать и ждать) в некоторых случаях оправдана, так как риск развития ущемления при параэзофагеальной ГПОД, по данным литературы, составляет 1,4% [52]. Показания к операции при ГПОД IV типа выставляются с учетом высокого периоперационного риска (пневмоторакс, пневмония, внутригрудное кровотечение, образование эмпиемы).
При хирургическом лечении ГПОД необходимо добиться следующих целей: 1) безнасильственное возвращение желудка из средостения в брюшную полость; 2) функциональная реконструкция пищеводного отверстия диафрагмы без повреждения переднего и заднего nervus vagus; 3) с одной стороны, устранение гастроэзофагеального рефлюкса, с другой стороны, не допустить развитие дисфагии после формирования парциальной или циркулярной фундопликационной манжеты.
· Пациентов с ГПОД рекомендуется оперировать лапароскопическим доступом [19, 31, 41, 47, 52, 75, 80, 109, 110].
Уровень убедительности рекомендации – С (Уровень достоверности доказательств – 4).
Комментарий. Лапароскопический доступ в хирургии ГПОД в настоящее время является золотым стандартом [19, 31, 41, 47, 52, 75, 80, 109, 110].
· В лечении пациентов с ГПОД применение робото-ассистированных систем рекомендуется по усмотрению оперирующего хирурга [9, 11, 42, 85].
Уровень убедительности рекомендаций – В (Уровень достоверности доказательств – 3).
Комментарий. Применение робото-ассистированных систем в хирургии ГПОД демонстрирует сопоставимые результаты по сравнению с лапароскопическим доступом. При этом показания и методология операций идентичны [9, 11, 42, 85].
· Лапаротомный доступ при хирургическом лечении пациентов с ГПОД рекомендуется в экстренных ситуациях при развитии интраоперационных осложнений, а также в случае перитонита или некроза желудка [7, 8, 12, 23, 25, 31].
Уровень убедительности рекомендации – С (Уровень достоверности доказательств – 5).
Комментарий. Хирургическая конверсия иногда необходима из-за развития кровотечения, травмы селезенки или выраженного спаечного процесса. Хирурги, выполняющие эти операции лапароскопически, должны обладать соответствующими навыками, необходимыми при хирургической конверсии. [7, 8, 12, 23, 25, 31].
· Во время мобилизации пищевода во время операции по поводу ГПОД, как при лапароскопическом доступе, так и при использовании робото-ассистированных технологий рекомендуется сохранять блуждающий нерв [1, 8, 95, 80, 82].
Уровень убедительности рекомендации – В (Уровень достоверности доказательств – 2).
Комментарий. Во время мобилизации пищевода и формирования фундопликационной манжеты необходимо сохранять передний и задний ствол блуждающего нерва из-за риска развития диареи в послеоперационном периоде, демпинг-синдрома и вздутия живота, а также риска развития холецистолитиаза в отдаленном периоде [1, 8, 95, 80, 82].
· Грыжевой мешок во время операции по поводу ГПОД как при лапароскопическом доступе, так и при использовании робото-ассистированных технологий рекомендуется отделять от структур средостения, а затем полностью или частично удалять с целью облегчения формирования фундопликационной манжеты [50, 68, 99, 105].
Уровень убедительности рекомендации – C (Уровень достоверности доказательств – 4).
Комментарии. Медиастинально расположенный грыжевой мешок необходимо выделять при операциях по поводу ГПОД [68].
Результаты научных исследований, сравнивающих полную и неполную диссекцию грыжевого мешка, показали отсутствие различий в послеоперационных осложнениях, за исключением раннего рецидива [50, 99, 105].
· Короткие желудочные сосуды при мобилизации большой кривизны желудка и его дна во время операции по поводу ГПОД как при лапароскопическом доступе, так и при использовании робото-ассистированных технологий не рекомендуется рутинно лигировать и пересекать, если фундопликацию возможно выполнить без натяжения [65, 66, 74].
Уровень убедительности рекомендации – В (Уровень достоверности доказательств – 1).
Комментарий. Полное пересечение всех Vasa gastricae breves сопровождается удлинением времени операции и ухудшением в дальнейшем запирательной функции фундопликационной манжеты. С другой стороны, полное пересечение Vasa gastricae breves по большой кривизне желудка облегчает формирование без натяжения полной циркулярной манжеты по Nissen-Rossetti [65, 66, 74].
· При мобилизации малой кривизны желудка во время операции по поводу ГПОД как при лапароскопическом доступе, так и при использовании робото-ассистированных технологий рекомендуется сохранять аномально идущие или добавочные артерии к печени [96].
Уровень убедительности рекомендации – В (Уровень достоверности доказательств – 3).
Комментарий. При мобилизации желудка по малой кривизне рекомендовано сохранять аномально идущие или добавочные артерии к печени, которые отходят от а. gastrica sinistra в 12% случаев [96].
· Выбор передней или задней пластики пищеводного отверстия диафрагмы рекомендуется на усмотрение оперирующего хирурга.
Уровень убедительности рекомендации – С (Уровень достоверности доказательств – 5).
Комментарий. При выполнении реконструкции пищеводного отверстия диафрагмы пластика ножек диафрагмы имеет решающее значение. Многочисленные публикации на эту тему демонстрируют сопоставимые результаты выполнения передней или задней пластики ножек диафрагмы [74, 99]. Пластика ножек диафрагмы не должна приводить к сужению пищеводного отверстия диафрагмы, чтобы избежать развития дисфагии. Если узкую фундопликационную манжету можно коррегировать с помощью баллонной дилатации, то при узком пищеводном отверстии диафрагмы это не принесет эффекта [48]. Стандартно выполняемое шинирование пищевода с помощью толстого желудочного зонда (32Ch) описывается многими авторами [48], но при соответствующем опыте оперирующего хирурга от этого можно отказаться.
· Аллопластика пищеводного отверстия диафрагмы сетчатым имплантом во время операции по поводу ГПОД - как при лапароскопическом доступе, так и при использовании робото-ассистированных технологий у пациентов с ГПОД II, III и IV типов рекомендуется выбирать индивидуально [20, 25, 33, 34, 35, 37, 57, 58, 59, 68, 69, 77, 79, 87, 90, 92, 102, 104, 107].
Уровень убедительности рекомендаций – А (Уровень достоверности доказательств – 1).
Комментарии. С момента первого описания применения сетчатого импланта в хирургии ГПОД Kuster и Gilroy в 1993 году [69] опубликовано множество вариантов выполнения аллопластики пищеводного отверстия диафранмы при ГПОД [20, 25, 57, 58, 79, 87, 107].
Международные клинические рекомендации, посвященные лечению паховых и послеоперационных грыж, рекомендуют всегда применять сетчатые импланты, за исключением ряда особенных ситуаций [34, 35, 77, 90, 104]. Рутинное применение аллопластики сетчатым имплантом при ГПОД, напротив, является спорным. В частности, Society of American Gastrointestinal and Endoscopic Surgeons (SAGES) считает преимуществом имплантации сетчатого импланта при ГПОД низкую вероятность рецидива. Однако, в связи с небольшим количеством исследований на эту тему, выполненных по правилам доказательной медицины, а также относительно высоким риском развития осложнений, связанных с аллопластикой сетчатыми имплантами (дисфагия и перфорация пищевода), SAGES не рекомендует рутинно проводить аллопластику сетчатыми имплантами [68].
Патогенез ГПОД, как и других грыж, является мультифакторным. Общепринято, что развитию грыж способствует повышенное внутрибрюшное давление. Если в хирургии грыж других локализацией применяют циркулярные и заходящие далеко за границу грыжевого дефекта, крупнопористые со стабильной структурой и монофильные сетчатые импланты, то в хирургии ГПОД на эту тему продолжаются дискуссии [37, 104].
Если при определенном размере грыжевых ворот состояние окружающих мягких тканей не позволяет выполнить пластику без их натяжения, то рекомендовано использовать сетчатые импланты. Предметом дискуссии остаются такие детали, как: вид сетки, операционный доступ, насколько сетка должна перекрывать грыжевой дефект и т.д. [33, 34, 37, 68,77, 78, 90, 104].
Необходимо, во-первых, стандартизировать размер дефекта, при котором выставляются показания для аллопластики сетчатым ипплантом. Во-вторых, необходимо стандартизировать технику мобилизации ножек диафрагмы в области пищеводного отверстия диафрагмы. В-третьих, выбрать безопасный и подходящий для хиатопластики вид сетчатого импланта [58, 59]. МРТ позволяет документировать состояние сетчатого импланта при динамическом наблюдении за пациентом в послеоперационном периоде. Предварительные результаты моноцентрического исследования показали, что рецидив ГПОД после применения аллопластики сетчатым имплантом через 2 года после операции составляет 6% без осложнений, связанных с сетчатым имплантом [102].
Имеются данные о преимуществе аллопластики по сравнению с пластикой пищеводного отверстия диафрагмы узловыми швами в количестве рецидивов после операции, в случае больших или параэзофагеальных ГПОД, и у пациентов с ГЭРБ. Необходимы дальнейшие клинические исследования, которые бы стандартизировали размер грыжевого дефекта, служащим показанием для имплантации сетки, вид сетчатого импланта, форму импланта и методику его вшивания в область грыжевого дефекта. Кроме того, необходимы наблюдения в течение длительного послеоперационного периода для выявления специфических осложнений, связанных с аллопластикой сетчатым имплантом при ГПОД.
Метаанализ Müller-Stich et al. (2015) показал, что при лапароскопических операциях параэзофагеальных ГПОД аллопластика сетчатым имплантом должна выполняться рутинно [79].
Некоторые эксперты рекомендуют использовать биологические импланты для аллопластики. Однако, эти рекомендации основываются, как правило, на личном опыте авторов [92].
· В случае, когда у пациентов с ГПОД II, III и IV типов во время операции по поводу ГПОД, как при лапароскопическом доступе, так и при использовании робото-ассистированных технологий обнаружено грыжевое выпячивание (расхождение ножек диафрагмы) размером более 5 см рекомендуется выполнить аллопластику пищеводного отверстия диафрагмы сетчатым имплантом [15, 23, 53, 58, 68, 76, 80, 87].
Уровень убедительности рекомендаций – А (Уровень достоверности доказательств – 1).
Комментарий. В случае большого размера ГПОД (>5 cm) клинические рекомендации SAGES рекомендуют аллопластику, так как после нее отмечается меньшее количество рецидивов [68]. Недостаточно наблюдений пациентов после аллопластики в отдаленном послеоперационном периоде, что не позволяют сделать достоверные выводы о ее безопасности в свете развития специфических осложнений, связанных с сетчатыми имплантами. Например, имеются данные 6-12 месяцев наблюдения, которые указывают на 22-26% рецидивов ГПОД при узловых швах против 0-8,6% при аллопластике [15, 23, 53, 58, 80]. Метаанализ, опубликованный Memon et al. (2016) показал отсутствие различий в применении аллопластики и узловых швов, за исключением меньшего количества рецидивов при аллопластике [76]. Аналогичные результаты были получены в результате проведения метаанализа Sathasivam R с соавт. (2018) [87].
· Рутинное применение аллопластики при антирефлюксных операциях у пациентов с ГПОД I типа не рекомендуется [15, 23, 53, 58, 80].
Уровень убедительности рекомендации – В (Уровень достоверности доказательств – 2).
Комментарий. Устранение ГПОД в комбинации с пластикой пищеводного отверстия диафрагмы и фундопликацией являются очень эффективными в лечении ГЭРБ [80]. При сочетании ГПОД I типа с ГЭРБ пищеводное отверстие диафрагмы расширено, как правило, незначительно и практически во всех случаях удается выполнить его пластику без натяжения и без применения сетчатого импланта.
· У пациентов с любым типом ГПОД во время операции по поводу ГПОД после ликвидации грыжевого выпячивания и пластики пищеводного отверстия диафрагмы рекомендуется в обязательном порядке дополнительно выполнить фундопликацию [5, 30, 32, 37, 39, 40, 43, 49, 58, 62, 73, 76, 84].
Уровень убедительности рекомендации – А (Уровень достоверности доказательств – 1).
Комментарий. При ГПОД необходимо выполнять фундопликацию независмо от того, сопровождается она ГЭРБ или нет. В проспективном исследовании Granderath FA и соавт. (2007) было показано, что результаты операции в группе пациентов, которым выполнялась аллопластика пищеводного отверстия диафрагмы сетчатым имплантом и фундопликация были лучше по сравнению с группой пациентов, которым была выполнена аллопластика в сочетании с кардиофреникопексией [58].
Несмотря на существующие дискуссии, литературные данные демонстрируют сопоставимые результаты формирования неполной (180°, 270°) и циркулярной (360°) фундопликационной манжеты.
Так, метаанлиз, проведенный Broeders et al. (2013), показал сопоставимые результаты неполных и циркулярных фундопликаций с меньшим количеством дисфагий в послеоперационном периоде в случае нециркулярной фундопликации [37]. Метаанализ Chrysos E. и соавт. охватывает 5 рандомизированных контролируемых исследований в период с 2004 по 2015 гг. [32, 39, 40, 43, 84] и одно рандомизированное контролируемое исследование, переведенное с китайского языка [49]. Был проведен сравнительный анализ 266 пациентов с циркулярной фундопликацией (360°) и 265 пациентов с фундопликационной манжетой на 180°. В послеоперационном периоде не было обнаружено статистически значимых различий в результатах, за исключением того, что в группе с неполной фундопликационной манжетой было больше реопераций в связи с рецидивом ГЭРБ. В группе с циркулярной фундопликацией было больше случаев дисфагии, которые не потребовали повторных операций. В связи с полученными результатами авторы не видят преимуществ между двумя вариантами фундопликационной манжеты, тем более что степень удовлетворенности операциями в каждой из групп была высокой (94,2% и 89,4%).
Так как в этом метаанализе в группе с циркулярной фундопликацией было больше случаев дисфагии, стал обсуждаться вопрос о целесообразности применения 270°-фундопликации по Toupet вместо циркулярной фундопликации. Однако статистически это не доказано [36, 49, 73].
Метаанализ, проведенный Memon et al. (2015), показал, что гастроэзофагеальный рефлюкс развивается чаще после передней фундопликации, но при этом меньше случаев дисфагии. Однако было проведено сравнение только передней и задней неполной фундопликации, принципиальное преимущество неполной фундопликации по сравнению с полной доказано не было [76].
Недостаточно клинических исследований 360°- vs. 270°-фундопликационной манжеты при хирургическом лечении ГПОД III–IV типов [5, 30, 62]. Единственное моноцентровое ретроспективное исследование отдаленных результатов ГПОД III/IV типов показало сопоставимые результаты между группами. Удовлетворенность пациентов была выше в группе с циркулярной фундопликацией [62].
· Гастропексия не рекомендуется как самостоятельный вид операции у пациентов с ГПОД I - IV типов и может использоваться только как дополнение к основной методике операции в ряде клинических ситуаций на усмотрение оперирующего хирурга [32, 39, 40, 43, 84].
Уровень убедительности рекомендации – С (Уровень достоверности доказательств – 5).
Комментарий. Некоторые авторы описали низведение грыжи и гастропексию без крурорафии или удаления грыжевого мешка, особенно у пациентов с ярко выраженными симптомами. Летальность и осложнения были низкими, но рентгенологический рецидив был выявлен у 22% через 3 месяца. Результаты такой хирургической тактики уступают стандартным методам операции, и поэтому изолировано гастропексия не должна быть целью операции [32, 39, 40, 43, 84].
· В случае рецидива ГПОД рекомендуется повторная хирургическая операция только пациентам с наличием симптомов ГПОД и/или ГЭРБ [7, 8, 10, 12, 13, 38, 48, 55, 56, 71, 91, 97, 108].
Уровень убедительности рекомендации – В (Уровень достоверности доказательств – 3).
Комментарий. Не существует стандартизированного определения рецидива после хирургического лечения ГПОД [7, 8, 10, 12]. Рецидив может быть основан исключительно на рентгенологических данных, но часто пациент не имеет симптомов и, следовательно, не имеет рецидивирующих симптомов. Lidor A.O. и соавт. (2015) сопоставили симптомы с рентгенологическими данными на бариевой эзофагограмме. Они определили, что рентгенологически рецидивирующие грыжи >2 см коррелируют с ухудшением симптомов, и, таким образом, определили рецидивирующую грыжу как вертикальное расширение слизистой оболочки желудка над диафрагмой >2 см [71]. Если фундопликация не проводилась, более общее определение рецидива — это любое новое доказательство параэзофагеальной грыжи или проксимальной миграции кардии при контрастном бариевом исследовании или КТ [48]. В рамках дообследования при рентгенологически подтвержденном рецидиве ГПОД целесообразно выполнить суточную рН-метрию, которая позволяет зафиксировать рецидив ГЭРБ при так называемых «бессимптомных» рецидивах.
Показаниями к повторной операции при наличии подтвержденного рецидива ГПОД могут являться рецидивирующий пищеводно-желудочный рефлюкс; дисфагия; разрыв либо смещение фундопликационной манжеты в грудную клетку через дефект пищеводного отверстия диафрагмы, смещение более 30% желудка в грудную клетку (то есть речь идет о параэзофагеальной ГПОД); некупируемый консервативно синдром «gas-bloat» (синдром вздутия); болевой синдром.
При принятии решения о повторной операции следует учитывать, что результаты после повторной операции в случае параэзофагеальной грыжи хуже, чем после первичной операции [56]. После первичной операции симптомы отсутствуют в 85–90% случаев, в то время как после повторной операции - только в 70% [97]. Частота хирургической конверсии выше в случае повторной операции (до 33%) [38, 55, 91]. Продолжительность операции и стационарного лечения также больше в случае повторной операции [38, 108].
Частота интраоперационных осложнений при повторной операции выше: в одном исследовании описывается 13,1% повреждений пищевода или желудка и 3,4% пневмоторакса [56]. В условиях повторной операции резко увеличивается опасность повреждения блуждающих нервов [56]. В случае повреждения блуждающих нервов возможно выполнение пилоропластики. Если рецидив ГПОД сопровождается клинической картиной повреждения обоих блуждающих нервов, которое произошло во время первичной операции по поводу ГПОД (подтверждено нарущение пассажа по желудку, выявлен выраженный гастроптоз во время обследования перед повтороной операцией), то дополнением к фундопликации может стать дистальная резекция желудка, предпочтительно по Ру. Принятие решения о резекционной операции только на основании данных, полученных хирургом интраоперационно во время повторной операции, не обосновано. Выполнение резекции желудка при рецидивах ГПОД также может быть оправдано при наличии у пациента желчного дуодено-гастрального рефлюкса [97, 108].
Показатели качества жизни при сравнении первичной и повторной операций различаются [13, 38, 97, 108]. Одно исследование показало, что пациенты, перенесшие повторную операцию, сообщают о худших показателях качества жизни по таким критериям, как чувство переполнения, отрыжка, тошнота, рефлюкс и общее состояние желудочно-кишечного тракта по сравнению с пациентами, перенесшими первичную операцию [38]. Однако другое исследование не обнаружило разницы в послеоперационном качестве жизни после первичной и повторной операции с использованием нескольких опросников качества жизни [97].
Повторная операция должна проводиться только опытными хирургами в медицинских организациях с большим потоком операций. Повторная операция должна предлагаться только пациентам с симптомами ГПОД и с объективными доказательствами неудачи предыдущего хирургического лечения [108].
Пациентов следует информировать до операции о том, что повторная операция может не привести к полному разрешению симптомов. Тщательное предоперационное обследование для определения вероятной причины первоначальной неудачи и всестороннего анализа текущего состояния пациента имеет решающее значение.
4. Реабилитация
Реабилитация осуществляется в отделениях по профилю оказания специализированной помощи (I этап), в отделениях медицинской реабилитации стационара (II этап) и в реабилитационном отделении поликлиники, реабилитационном отделении дневного стационара, реабилитационном отделении санатория (III этап).
Реабилитация организуется реабилитационной мультидисциплинарной бригадой, в состав которой входят: врач-хирург, врач по лечебной физкультуре, медицинский психолог, специалист по эрготерапии и специалист по физической реабилитации, а также врач-гастроэнтеролог. На первом этапе лечащим врачом является врач-хирург (врач-торакальный хирург) и все мероприятия по реабилитации согласуются с ним и с врачом анестезиологом-реаниматологом (при нахождении пациента в реанимации). При необходимости могут быть привлечены другие специалисты. Нет данных о преимуществе тех или иных методов физиотерапии при ГПОД; физиотерапия может быть рассмотрена как альтернативная и дополнительная методика в дополнении к базисной.
· Медицинская реабилитация рекомендуется всем пациентам с ГПОД, выбор оптимального метода реабилитации зависит от каждого конкретного случая заболевания [2, 8, 47, 103].
Уровень убедительности рекомендации – С (Уровень достоверности доказательств – 5).
· Медицинскую реабилитацию пациентам с ГПОД рекомендуется начинать максимально рано и проводить одновременно с лечением [4, 28, 55, 103].
Уровень убедительности рекомендации – С (Уровень достоверности доказательств – 5).
· В первый день после операции, кроме обезболивания ненаркотическими анальгетиками (в соответствии с АТХ: N02B другие анальгетики и антипиретики), всем пациентам рекомендуется ранняя мобилизация, дыхательная гимнастика и медленная ходьба в пределах палаты [17, 49, 74].
Уровень убедительности рекомендаций – С (Уровень достоверности доказательств – 5).
· Рекомендуется всем пациентам после хирургического лечения ГПОД в день операции голод, с первых суток и в течение двух первых месяцев после – щадящая диета [4, 47, 58, 106].
Уровень убедительности рекомендаций – С (Уровень достоверности доказательств – 5).
· Рекомендуется всем пациентам после хирургического лечения ГПОД ограничение подъема тяжестей в течение 6 месяцев [2, 10, 55, 74].
Уровень убедительности рекомендаций – С (Уровень достоверности доказательств – 5).
· Пациентам после окончания лечения ГПОД рекомендуется санаторно-курортное лечение [4, 8, 103].
Уровень убедительности рекомендаций С (уровень достоверности доказательств–5).
5. Профилактика
Надежных методов профилактики ГПОД не существует, поскольку нет способов влияния на предрасполагающие причины развития заболевания.
С целью профилактики рецидивирования грыжи в послеоперационном периоде пациентам рекомендуется отказ от курения, ограничение длительной и тяжелой физической работы, профилактика и лечение ХОБЛ и запоров [2, 8, 10, 40, 103].
Уровень убедительности рекомендаций – С (Уровень достоверности доказательств – 5).
· Диспансерное наблюдение рекомендуется не оперированным пациентам с ГПОД при наличии выраженных сопутствующих заболеваний или в случае отказа от оперативного вмешательства [10, 55, 106].
Уровень убедительности рекомендаций – С (Уровень достоверности доказательств – 5).
Комментарии. С учетом высокого риска рецидивирования, особую диспансерную группу могут составлять оперированные пациенты с рецидивными грыжами [10, 55, 106].
· Проведение диспансерного осмотра врачом-хирургом пациента после операции по поводу ГПОД рекомендуется через 3 месяца и через 12 месяцев, а затем не менее 1 раза в год в течение 3-х лет [2, 47, 74, 106].
Уровень убедительности рекомендаций – С (Уровень достоверности доказательств – 5).
· Контрольную рентгеноскопию пищевода и желудка с бариевой взвесью рекомендовано проводить пациентам через 3 месяца и через 12 месяцев после операции, а в дальнейшим только по показаниям при наличии подозрения на развитие рецидива ГПОД [10, 58, 84].
Уровень убедительности рекомендаций – С (Уровень достоверности доказательств – 5).
6. Дополнительная информация, влияющая на течение и исход заболевания
Организация оказания медицинской помощи пациентам с ГПОД проводится согласно Порядка оказания медицинской помощи взрослому населению по профилю «хирургия» (Приказ Министерства здравоохранения РФ от 15 ноября 2012 г. № 922н).
Первичная специализированная медико-санитарная помощь оказывается врачом-хирургом. При подозрении или выявлении у пациента ГПОД врачи-терапевты, врачи-терапевты участковые, врачи общей практики (семейные врачи), врачи-специалисты, средние медицинские работники в установленном порядке направляют пациента на консультацию в кабинет врача-хирурга для оказания ему первичной специализированной медико-санитарной помощи. При невозможности оказания медицинской помощи в рамках первичной медико-санитарной помощи и наличии медицинских показаний пациент направляется в медицинскую организацию, оказывающую специализированную медицинскую помощь по профилю «хирургия».
Специализированная медицинская помощь оказывается врачами-хирургами, врачами-торакальными хирургами в стационарных условиях и включает в себя профилактику, диагностику, лечение заболеваний и состояний, требующих использования специальных методов и сложных медицинских технологий, а также медицинскую реабилитацию.
Оперативное лечение пациентов с ГПОД при неотложных ситуациях (ущемление) может проводиться в хирургических и в хирургических торакальных отделениях медицинских организаций всех уровней. Плановое оперативное лечение ГПОД целесообразно проводить в хирургических или хирургических торакальных отделениях медицинских организаций третьего уровня. При сложных ГПОД (ГПОД III и IV типов, рецидивных ГПОД, у пациентов с сопутствующими заболеваниями, в т.ч. сердечно-сосудистой и дыхательной систем, сахарным диабетом или при показаниях для выполнения симультанных операций), оперативное лечение целесообразно проводить в медицинских организаций третьего уровня или федеральных центрах, специализирующихся на лечении данной категории пациентов.
Показания для плановой госпитализации:
· ГПОД II типа;
· ГПОД III типа;
· ГПОД IV типа;
· Рецидив ГПОД;
· ГПОД I типа с наличием осложнений ГЭРБ, а также при отсутствии эффекта от консервативного лечения ГЭРБ в течение 6 месяцев или отказ пациента от длительной консервативной терапии ГЭРБ.
Показания для экстренной госпитализации:
Наличие диагноза ущемленной ГПОД для выполнения экстренного хирургического вмешательства.
Показания к выписке пациента из стационара:
Активизация пациента после операции, отсутствие осложнений со стороны послеоперационной раны, внутренних органов и систем организма.
7. Дополнительная информация (в том числе факторы, влияющие на исход заболевания или состояния)
На исход заболевания или состояния могут оказывать влияние:
· поливалентная аллергия;
· наличие в анамнезе лейкоза, онкологических заболеваний, туберкулеза или положительной реакции на ВИЧ-инфекцию, гепатит В и С, сифилис;
· выраженные врожденные дефекты, подтвержденные данными анамнеза и/или объективным обследованием, ведущие к нарушению нормальной жизнедеятельности и требующие коррекции (врожденные пороки сердца, желудочно-кишечного тракта, мочеполовой системы, скелета; синдром Марфана, синдром Кляйнфельтра, синдром Эдвардса, синдром Опица, синдром Гольденхара и другие);
· заболевания сердечно-сосудистой системы: постинфарктный кардиосклероз, безболевая ишемия миокарда, перикардит, аневризма аорты, гипертоническая болезнь III степени, стенокардия напряжения, нестабильная стенокардия, стенокардия Принцметала;
· клинически значимые нарушения ритма и проводимости (фибрилляция/трепетания предсердий, частая желудочковая экстрасистолия по типу би(три)геминии, желудочковая тахикардия, полная блокада левой ножки пучка Гиса, трехпучковая блокада пучка Гиса, фибрилляция желудочков, синоаурикулярная блокада более I степени, атриовентрикулярная блокада II -III степени, синдром Фредерика);
· хроническая сердечная недостаточность III - IV степени по NYHA;
· хроническое легочное сердце в стадии декомпенсации;
· бронхиальная астма;
· тромбоэмболия легочной артерии;
· острый инфаркт миокарда;
· острое нарушение мозгового кровообращения;
· транзиторная ишемическая атака;
· острая пневмония, плеврит;
· системные заболевания соединительной ткани по данным анамнеза – системная склеродермия, системная красная волчанка, системные васкулиты, антифосфолипидный синдром, дерматомиозит, саркоидоз, ревматизм и другие;
· сахарный диабет I и II типа;
· ожирение c индексом массы тела более 40;
· острая почечная недостаточность;
· хроническая почечная недостаточность со скоростью клубочковой фильтрации менее 30 мл/мин;
· язвенная болезнь желудка и двенадцатиперстной кишки в стадии обострения, цирроз печени;
· рассеянный склероз и другие демиелинизирующие заболевания;
· любые психиатрические заболевания по данным анамнеза;
· гематологические заболевания по данным анамнеза;
· наркомания или хронический алкоголизм по данным анамнеза;
· беременность/периодлактации.
Критерии оценки качества медицинской помощи
|
№ п/п |
Критерии качества |
Оценка выполнения |
|
1. |
Выполнена рентгеноскопия пищевода и желудка с барием |
да/нет |
|
2. |
Выполнена эзофагогастроскопия |
да/нет |
|
3. |
Во время выполнения операции по поводу ГПОД сохранены ветви блуждающего нерва |
да/нет |
|
4. |
Во время выполнения операции по поводу ГПОД грыжевой мешок мобилизован и частично или полностью удален из заднего средостения |
да/нет |
|
5. |
Операция по поводу ГПОД дополнена формированием фундопликационной манжеты |
да/нет |
Список литературы
1. Аллахвердян А.С., Праздников Э.Н. Пищевод Барретта как осложнение гастроэзофагеальной рефлюксной болезни: диагностика и современные методы лечения (взгляд хирурга). Consilium Medicum. 2015; 17 (8): 60–66 с. DOI: 10.26442/2075-1753_2015.8.55-61
2. Аллахвердян А.С., Мазурин В.С., Анипченко Н.Н., Шабаров В.Л. Лапароскопическая фундопликация при лечении пищевода Баррета. Альманах клинической медицины. 2015; 40: 117-120 с.
3. Аллахвердян А.С. Выбор метода лапароскопической фундопликации при скомпрометированной моторике пищевода. Вестник последипломного медицинского образования. 2016; 2: 72-75 с.
4. Анищенко В.В., Платонов П.А. Комплексное лечение пациентов с пищеводом Баррета. Вопросы реконструктивной и пластической хирургии. 2014; Т17, 4 (51): 50-53 с.
5. Анищенко В.В., Ким Д.А., Козлов А.В., Патрушев П.А., Норматов Р.М. Минигастрошунтирование с фундопликацией по Ниссену в лечении пациентов с ожирением и гастроэзофагеальной рефлюксной болезнью. Хирургическая практика. 2023; 8 (3): 43-58 с.
6. Ким Д.А., Анищенко В.В., Патрушев П.А. Лечение гастроэзофагеального рефлюкса у пациентов после продольной резекции желудка в ближайшем послеоперационном периоде. Хирургическая практика. 2022; 2 (45): 26-33 с.
7. Галлямов Э.А., Луцевич О.Э., Кубышкин В.А., Ерин С.А., Агапов М.А., Преснов К.С., Бусырев Ю.Б., Галлямов Э.Э., Гололобов Г.Ю., Зрянин А.М., Старков Г.А., Толстых М.П. Повторные лапароскопические операции при рецидиве гастроэзофагеальной рефлюксной болезни и грыжи пищеводного отверстия диафрагмы. Хирургия. Журнал им. Н.И. Пирогова. 2019; 2: 26-31 с.
8. Галлямов Э.А., Агапов М.А., Луцевич О.М., Кубышкин В.А., Ерин С.А., Преснов К.С., Бусырев Ю.Б., Какоткин В.В., Торосян О.Г. Лапароскопический подход в коррекции рецидивов гастроэзофагеальной рефлюксной болезни и грыж пищеводного отверстия диафрагмы. Хирургическая практика. 2019; 3 (39): 32-40 с.
9. Семенякин И.В., Луцевич О.Э., Галлямов Э.А., Шестаков А.Л., Ерин С.А., Дибиров М.Д., Бобылев А.А., Косяков Н.А., Фомин В.С., Бокарев Ф.А., Гололобов Г.Ю. Сравнительный анализ лапароскопической и робот-ассистированной фундопликации при грыжах пищеводного отверстия диафрагмы. Московский хирургический журнал. 2019; 4 (68): 54-59 с.
10. Гололобов Г.Ю., Ерин С.А., Овчинникова У.Р., Абумуслимов К.К., Хусаинов И.Р., Китиева А.А., Галлямов Э.А. Лапароскопическая коррекция рецидива гастроэзофагеальной рефлюксной болезни и грыжи пищеводного отверстия диафрагмы после дважды провальной фундопликации. Клинический случай. Хирургическая практика. 2023; 8 (4): 6-20 с.
11. Шестаков А.Л., Ерин С.А., Гололобов Г.Ю., Бурмистров А.И., Овчинникова У.Р., Чичерина М.А., Юркулиев Н.А., Гадлевский Г.С., Дибиров М.Д., Галлямов Э.А. Результаты лапароскопических и робот-ассистированных антирефлюксных оперативных вмешательств при грыжах пищеводного отверстия диафрагмы и гастроэзофагеальной рефлюксной болезни. Клиническая и экспериментальная хирургия. Журнал имени академика Б.В. Петровского. 2023; Т. 11. №1 (39): 92-103 с.
12. Ерин С.А., Гололобов Г.Ю., Юркулиев Н.А., Чичерина М.А., Бурмистров А.И., Гадлевский Г.С., Овчинникова У.Р., Горбачева И.В., Галлямов Э.А. Эвентрация диафрагмы под маской рецидивной параэзофагеальной грыжи пищеводного отверстия диафрагмы. Хирургическая практика. 2022; 4 (45): 70-76 с.
13. Оскретков В.И., Ганков В.А., Гурьянов А.А., Климов А.Г., Андреасян А.Р., Овсепян М.А. Качество жизни больных гастроэзофагеальной рефлюксной болезнью с аксиальной грыжей пищеводного отверстия диафрагмы после дозированной эзофагофундопликации. Вестник хирургической гастроэнтерологии. 2016; 4: 11-15 с.
14. Цеймах Е.А., Андреасян А.Р., Ганков В.А., Масликова С.А., Гасымов А.Н., Волженин Д.В. Видеолапароскопическое лечение аксиальной кардиофундальной грыжи пищеводного отверстия диафрагмы при коротком пищеводе с диафрагмохиатопластикой (Клинический случай). Бюллетень медицинской науки. 2023; 1 (29): 128-135 с.
15. Андреасян А.Р., Ганков В.А., Масликова С.А., Багдасарян Г.И., Цеймах Е.А. Видеолапароскопическое лечение параэзофагеальной фиксированной комбинированной кишечно-желудочной гигантской грыжи пищеводного отверстия диафрагмы. Оперативная хирургия и клиническая анатомия (Пироговский научный журнал). 2022; 6 (2): 45-49 с.
16. Оскретков В.И., Ганков В.А., Андреасян А.Р., Климова Г.И., Овсепян М.А. Причины патологического гастроэзофагеального рефлюкса после видеолапароскопической коррекции замыкательной функции кардии у больных аксиальной грыжей пищеводного отверстия диафрагмы. Хирургия. Журнал им. Н.И. Пирогова. 2020; 6: 38-43 с.
17. Цеймах Е.А., Андреасян А.Р., Ганков В.А., Берестенников А.В., Масликова С.А., Григорян М.А., Гасымов А.Н. Отдаленные результаты лечения гастроэзофагеальной рефлюксной болезни у больных грыжей пищеводного отверстия диафрагмы после видеолапароскопического оперативного вмешательства в сочетании с диафрагмохиаотопластикой. Оперативная хирургия и клиническая анатомия (Пироговский научный журнал). 2023; 7 (3): 37-43 с.
18. Ганков В.А., Шестаков Д.Ю., Андреасян А.Р., Цеймах Е.А. Видеолапароскопическое оперативное лечение ущемленной параэзофагеальной грыжи пищеводного отверстия диафрагмы (клиническое наблюдение). Acta Biomedica Scientifica. 2023; 8 (1): 204-210 с.
19. Пучков К.В., Пучков Д.К., Филимонов В.Б. Лапароскопический метод лечения пищеводного отверстия диафрагмы (ГПОД), результаты применения различных методик. Альманах Института хирургии им. А.В.Вишневского. 2015;10 (1): 347-348 с.
20. Пучков К.В., Пучков Д.К. Лапароскопический метод лечения грыж пищеводного отверстия диафрагмы с использованием композитных сетчатых имплантов для герниорафии. Альманах Института хирургии им. А.В.Вишневского. 2017; 1: 1239-1240 с.
21. Черкасов Д.М., Черкасов М.Ф., Татьянченко В.К., Старцев Ю.М., Меликова С.Г. Анатомические особенности и биомеханические свойства диафрагмы в патогенезе развития грыж пищеводного отверстия диафрагмы. Хирургия. Журнал им. Н.И. Пирогова. 2019; 7. С. 29-35.
22. Черкасов Д.М., Черкасов М.Ф., Татьянченко В.К., Старцев Ю.М., Меликова С.Г. Комплексное лечение осложненных форм грыж пищеводного отверстия диафрагмы с учетом индивидуальных особенностей пациента. Медико-фармацевтический журнал Пульс. 2019; 21 (10): 35-41 с.
23. Черкасов Д.М., Черкасов М.Ф., Татьянченко В.К., Старцев Ю.М., Меликова С.Г., Галашокян К.М. Хирургическая тактика при больших и гигантских грыжах пищеводного отверстия диафрагмы. Вестник хирургии им. И.И. Грекова. 2018; 177 (4): 63-66 с.
24. Черкасов Д.М., Черкасов М.Ф., Старцев Ю.М., Меликова С.Г. Современный подход к лечению осложненных грыж пищеводного отверстия диафрагмы. Эндоскопическая хирургия. 2016; 22 (2): 14-17 с.
25. Черкасов Д.М., Черкасов М.Ф., Татьянченко В.К., Старцев Ю.М., Меликова С.Г., Галашокян К.М. Дифференцированный подход к выбору пластики грыж пищеводного отверстия диафрагмы. Эндоскопическая хирургия. 2020; 26 (1): 5-12 с.
26. Черкасов М.Ф., Скуратов А.В., Черкасов Д.М., Старцев Ю.М., Меликова С.Г. Преимущества оригинального способа эндохирургического лечения пищевода Баррета. Эндоскопическая хирургия. 2018; 24 (2): 30-33 с.
27. Черкасов Д.М., Черкасов М.Ф., Старцев Ю.М., Меликова С.Г., Галашокян К.М. Опыт хирургического лечения осложненных форм грыж пищеводного отверстия диафрагмы с учетом конституциональных особенностей пациентов Московский хирургический журнал. 2020; 1 (71): 88-94 с.
28. Andolfi C, Jalilvand A, Plana A, Fisichella PM. Surgical Treatment of Paraesophageal Hernias: A Review. J Laparoendosc Adv Surg Tech A. 2016;26:778–783.
29. Analatos A et al (2020) Tension-free mesh versus suture-alone cruroplasty in antireflux surgery: a randomized, double-blind clinical trial. Br J Surg 107(13):1731–1740. https://doi.org/10.1002/bjs.11917.
30. Analatos A, Lindblad M, Ansorge C, Lundell L, Thorell A, Håkanson BS. Total versus partial posterior fundoplication in the surgical repair of para-oesophageal hernias: randomized clinical trial. BJS Open. 2022 May 2;6(3): zrac034. doi: 10.1093/bjsopen/zrac034.
31. AWMF – Arbeitsgemeinschaft der Wissenschaftlichen Medizinischen Fachgesellschaften e. V. (2015) S2k Leitlinie: Gastroösophageale Refluxkrankheit. Registernummer 021-013. Stand: 31.05. 2014 (gültig bis31.05.2019).
32. BaigrieR, CullisS, NdhluniA, Cariem A (2005) Randomized doubleblind trial of laparoscopic Nissen fundoplication versus anterior partial fundoplication. Br J Surg 92(7):819–823.
33. Berger D, Bientzle M(2007) Laparoscopic repairof parastomal hernias: a single surgeon’s experience in 66 patients. Dis Colon Rectum 50(10):1668–1673.https://doi.org/ 10.1007/s10350-007-9028-z.
34. Bittner R, Arregui M, Bisgaard T, Dudai M, Ferzli G, Fitzgibbons R, Fortelny R, Klinge U, Kockerling F, Kuhry E (2011) Guidelines for laparoscopic (TAPP) and endoscopic (TEP) treatment of inguinal hernia [International Endohernia Society (IEHS). Surg Endosc 25(9):2773 5.
35. Bittner R, Montgomery M, Arregui E, Bansal V, Bingener J, Bisgaard T, Buhck H, Dudai M, Ferzli G, Fitzgibbons R (2015) Update of guidelines on laparoscopic (TAPP) and endoscopic (TEP) treatment of inguinal hernia (International Endohernia Society). Surg Endosc 29(2):289–321 6.
36. Booth M, Stratford J, Jones L, Dehn T(2008) Randomized clinical trialof laparoscopic total (Nissen) versus posterior partial (Toupet) fundoplication for gastro-oesophageal reflux disease based on preoperative oesophageal manometry. Br J Surg95(1):57–63.
37. Broeders JA, Roks DJ, Ali UA, Watson DI, Baigrie RJ, Cao Z, Hartmann J, Maddern GJ (2013) Laparoscopic anterior 180-degree versus nissen fundoplication for gastroesophageal reflux disease: systematic review and metaanalysis of randomized clinical trials. AnnSurg257(5):850–859.
38. Brown AM, Nagle R, Pucci MJ, et al. Perioperative Outcomes and Quality of Life after Repair of Recurrent Hiatal Hernia Are Compromised Compared with Primary Repair. Am Surg 2019; 85:556-60.
39. Cai W, Watson DI, Lally C, Devitt P, GameP, JamiesonG (2008) Ten-year clinical outcome of a prospective randomized clinical trial of laparoscopic Nissen versus anterior 180° partial fundoplication. Br J Surg 95(12):1501–1505.
40. Cao Z, Cai W, Qin M, Zhao H, Yue P, LiY (2012) Randomized clinical trial of laparoscopic anterior 180 partial versus 360 Nissen fundoplication: 5-year results. Dis Esophagus 25(2):114–120.
41. Casaccia M, Torelli P, Panaro F, Cavaliere D, Saltalamacchia L, Troilo BM, Savelli A, Valente U (2005) Laparoscopic tension-free repair of large paraesophageal hiatal hernias with a composite A-shaped mesh: two-year followup. J LaparoendoscAdv SurgTech A 15(3):279–284.
42. Ceccarelli G, Valeri M, Amato L, De Rosa M, Rondelli F, Cappuccio M, Gambale FE, Fantozzi M, Sciaudone G, Avella P, Rocca A. Robotic revision surgery after failed Nissen anti-reflux surgery: a single center experience and a literature review. J Robot Surg. 2023 Aug;17(4):1517-1524. doi: 10.1007/s11701-023-01546-6. Epub 2023 Mar 2.
43. Chrysos E, Athanasakis E, Pechlivanides G, Tzortzinis A, Mantides A, Xynos E (2004) The effect of total and anterior partial fundoplication on antireflux mechanisms of the gastroesophageal junction. Am J Surg188(1):39–44,
44. Clapp B, Kara AM, Nguyen-Lee PJ, Annabi HM, Alvarado L, Marr JD, et al. Does bioabsorbable mesh reduce hiatal hernia recurrence rates? A meta-analysis. Surg Endosc. 2023;37(3):2295–2303. doi: 10.1007/s00464-022-09514-1.
45. Csendes A, Burdiles P, Braghetto I, Korn O (2004) Adenocarcinoma appearing very late after antireflux surgery for Barrett’s esophagus: long-term follow-up, review of the literature, and addition of six patients. J Gastrointest Surg 8(4):434–441.
46. Collet D, Luc G, Chiche L. Management of large para-esophageal hiatal hernias. J Visc Surg. 2013; 150:395–402.
47. Dallemagne B (2013) Operationstechnikund schwierige Situationen (Thoraxmagen). In: Korenkov M, Germer C-T, Lang H (Hrsg) Gastrointestinale Operationen und technische Varianten –Operationstechniken der Experten. Springer, Berlin, Heidelberg, S43–47.
48. Dallemagne B, Quero G, Lapergola A, Guerriero L, Fiorillo C, Perretta S. Treatment of giant paraesophageal hernia: pro laparoscopic approach. Hernia. 2018; 22:909–919.
49. Du X, Wu J-M, Hu Z-W, Wang F, Wang Z-G, Zhang C, Yan C, Chen M-P (2017) Laparoscopic Nissen (total) versus anterior 180° fundoplication for gastroesophageal reflux disease: a metaanalysis and systematic review. Medicine96(37):e8085.
50. Edye MB, Canin-Endres J, Gattorno F, Salky BA. Durability of laparoscopic repair of paraesophageal hernia. Ann Surg. 1998;228(4):528–535. doi: 10.1097/00000658-199810000-00009.
51. Eusebi LH, Telese A, Cirota GG, Haidry R, Zagari RM, Bazzoli F, Ford AC. Systematic review with meta-analysis: risk factors for Barrett's oesophagus in individuals with gastro-oesophageal reflux symptoms. Aliment Pharmacol Ther. 2021 May;53(9):968-976. doi: 10.1111/apt.16321. Epub 2021 Mar 11. PMID: 33705573.
52. Feußner H (2013) Operationstechnik und schwierige Situationen (GERD und Thoraxmagen). In: KorenkovM, GermerC-T, LangH (Hrsg) Gastrointestinale Operationen und technische Varianten –Operationstechniken der Experten. Springer, Berlin, Heidelberg, S47–52.
53. Frantzides CT, Madan AK, Carlson MA, Stavropoulos GP (2002) A prospective, randomized trial of laparoscopic polytetrafluoroethylene (PTFE) patch repair vs simple cruroplasty for large hiatal hernia. ArchSurg137(6):649–652.
54. Fuchs KH, Babic B, Breithaupt W, Dallemagne B, Fingerhut A, Furnee E, Granderath F, Horvath P, Kardos P, Pointner R (2014) EAES recommendations for the management of gastroesophageal reflux disease. SurgEndosc28(6):1753–1773.
55. Funch-Jensen P, Bendixen A, Iversen MG, et al. Complications and frequency of redo antireflux surgery in Denmark: a nationwide study, 1997-2005. Surg Endosc 2008; 22:627-30.
56. Furnée EJ, Draaisma WA, Broeders IA, et al. Surgical reintervention after failed antireflux surgery: a systematic review of the literature. J Gastrointest Surg 2009; 13:1539-49.
57. Geerts JH, de Haas JWA, Nieuwenhuijs VB. Lessons learned from revision procedures: a case series pleading for reinforcement of the anterior hiatus in recurrent hiatal hernia. Surg Endosc. 2024 May;38(5):2398-2404. doi: 10.1007/s00464-024-10703-3. Epub 2024 Apr 2. PMID: 38565689.
58. Granderath FA (2017) Operative Therapie bei Hiatushernie. Chirurg. https://doi.org/10.1007/s00104- 016-0338-3.
59. Granderath F, Schweiger U, PointnerR (2007) Laparoscopic antireflux surgery: tailoring the hiatal closure to the size of hiatal surface area. SurgEndosc21(4):542–548.
60. Hansdotter I, Björ O, Andreasson A, Agreus L, Hellström P, Forsberg A, Talley NJ, Vieth M, Wallner B (2016) Hill classification is superior to the axial length of a hiatal hernia for assessment of the mechanical anti-reflux barrier at the gastroesophageal junction. EndoscInt4(3): E311.
61. Herrero LA, Curvers WL, Van Vilsteren F, Wolfsen H, Ragunath K, Song LWK, Mallant-Hent RC, Van Oijen A, Scholten P, Schoon EJ (2013) Validation of the Prague C&M classification of Barrett’s esophagus in clinical practice. Endoscopy45(11):876–882.
62. Huerta CT, Plymale M, Barrett P, DavenportDL, Roth JS(2018)Longtermefficacy of laparoscopic Nissen versus Toupet fundoplication for the management of types III and IV hiatal hernias. Surg Endosc. https://doi.org/10.1007/s00464- 018-6589-y.
63. Kahrilas P (1999) The role of hiatus hernia in GERD. Yale J Biol Med 72(2–3):101.
64. Kahrilas PJ, Sifrim D (2008) Highresolution manometry and impedance-pH/manometry: valuable tools in clinical and investigational esophagology., S 756–769 https:// doi.org/10.1053/j.gastro.2008.05. 048.
65. Khatri K, Sajid MS, Brodrick R, Baig MK, Sayegh M, Singh KK. Laparoscopic Nissen fundoplication with or without short gastric vessel division: a meta-analysis. Surg Endosc. 2012;26(4):970–978. doi: 10.1007/s00464-011-1979-4.
66. Kinsey-Trotman SP, Devitt PG, Bright T, Thompson SK, Jamieson GG, Watson DI. Randomized trial of division versus nondivision of short gastric vessels during Nissen fundoplication: 20-year outcomes. Ann Surg. 2018;268(2):228–232. doi: 10.1097/SLA.0000000000002648.
67. Köhler G, Wundsam H, PallweinPrettner L, Koch O, Emmanuel K (2015) Magnetic resonance visible 3-Dfunnel meshesfor laparoscopic parastomal hernia prevention and treatment. EurSurg47(3):127–132.
68. Kohn GP, Price RR, DeMeester SR, Zehetner J, Muensterer OJ, Awad Z, et al. Guidelines for the management of hiatal hernia. Surg Endosc. 2013; 27:4409–4428.
69. Kuster GG, Gilroy S (1993) Laparoscopic technique for repair of paraesophageal hiatal hernias. J LaparoendoscSurg3(4):331–338.
70. Lebenthal A, Waterford SD, Fisichella PM. Treatment and controversies in paraesophageal hernia repair. Front Surg. 2015; 2:13.
71. Lidor AO, Steele KE, Stem M, et al. Long-term quality of life and risk factors for recurrence after laparoscopic repair of paraesophageal hernia. JAMA Surg 2015; 150:424-31.
72. Linke GR, Borovicka J, Schneider P, Zerz A, Warschkow R, Lange J, Müller-Stich BP (2008) Is a barium swallow complementary to endoscopy essential in the preoperative assessment of laparoscopic antireflux and hiatal hernia surgery? Surg Endosc22(1):96–100 21.
73. Mardani J, Lundell L, Engström C (2011) Total or posterior partial fundoplication in the treatment of GERD: results of a randomized trial after 2 decades of follow-up. Ann Surg253(5):875–878.
74. Markar SR, Karthikesalingam AP, Wagner OJ, Jackson D, Hewes JC, Vyas S, et al. Systematic review and meta-analysis of laparoscopic Nissen fundoplication with or without division of the short gastric vessels. Br J Surg. 2011;98(8):1056–1062. doi: 10.1002/bjs.7519.
75. Medina L, Peetz M, Ratzer E, Fenoglio M (1998) Laparoscopic paraesophageal hernia repair. J Soc LaparoendoscSurg2(3):269–272.
76. Memon MA, Memon B, Yunus RM, Khan S (2016) Suture cruroplasty versus prosthetic hiatal herniorrhaphy for large hiatal hernia: a meta-analysis and systematic review of randomized controlled trials. Ann Surg 263(2):258–266. https://doi.org/ 10.1097/sla.0000000000001267.
77. Miserez M, Peeters E, Aufenacker T, Bouillot J, Campanelli G, Conze J, Fortelny R, Heikkinen T, Jorgensen L, Kukleta J(2014)Updatewithlevel 1 studies of the European Hernia Societyguidelineson the treatment of inguinal hernia in adult patients. Hernia18(2):151–163.
78. Mittal SK(2013) Operationstechnik und schwierige Situationen(Thoraxmagen). In: Korenkov M, Germer C-T, Lang H (Hrsg) Gastrointestinale Operationen und technische Varianten – Operationstechniken der Experten. Springer, Berlin, Heidelberg, S55–61.
79. Müller-Stich BP, Kenngott HG, Gondan M, Stock C, Linke GR, Fritz F, Nickel F, Diener MK, Gutt CN, Wente M (2015) Use of mesh in laparoscopic paraesophageal hernia repair: a meta-analysis and risk-benefit analysis. PLoS ONE 10(10): e139547.
80. Oelschlager BK, Yamamoto K, Woltman T, Pellegrini C. Vagotomy during hiatal hernia repair: a benign esophageal lengthening procedure. J Gastrointest Surg. 2008;12(7):1155. doi: 10.1007/s11605-008-0520-0.
81. Oleynikov D, Jolley JM. Paraesophageal hernia. Surg Clin North Am. 2015; 95:555–565.
82. Ozdogan M, Kuvvetli A, Das K, Oruc C, Karateke F, Aydin M, et al. Effect of preserving the hepatic vagal nerve during laparoscopic Nissen fundoplication on postoperative biliary functions. World J Surg. 2013;37(5):1060–1064. doi: 10.1007/s00268-013-1958-0.
83. Philpott H, Sweis R. Hiatus Hernia as a Cause of Dysphagia. Curr Gastroenterol Rep. 2017; 19:40.
84. Raue W, Ordemann J, Jacobi C, Menenakos C, Buchholz A, Hartmann J (2011) Nissen versus Dor fundoplication for treatment of gastroesophageal reflux disease: a blinded randomized clinical trial. DigSurg28(1):80–86.
85. Robotic surgery versus Laparoscopic surgery for anti-reflux and hiatal hernia surgery: a short-term outcome and cost systematic literature review and meta-analysis. Gonçalves-Costa D, Barbosa JP, Quesado R, Lopes V, Barbosa J. Langenbecks Arch Surg. 2024 Jun 6;409(1):175. doi: 10.1007/s00423-024-03368-y. PMID: 38842610.
86. Sathasivam R, Bussa G, Viswanath Y, Obuobi RB, Gill T, Reddy A, Shanmugam V, Gilliam A, Thambi P. Mesh hiatal hernioplasty' versus 'suture cruroplasty' in laparoscopic para-oesophageal hernia surgery; a systematic review and meta-analysis. Asian J Surg. 2019 Jan;42(1):53-60. doi: 10.1016/j.asjsur.2018.05.001. Epub 2018 Jun 7.
87. Siegal SR, Dolan JP, Hunter JG. Modern diagnosis and treatment of hiatal hernias. Langenbecks Arch Surg. 2017; 402:1145–1151.
88. Sierra-Arango F, Castaño DM, Forero JD, Pérez-Riveros ED, Ardila Duarte G, Botero ML, Cárdenas A, De la Hoz-Valle J. A Randomized Placebo-Controlled N-of-1 Trial: The Effect of Proton Pump Inhibitor in the Management of Gastroesophageal Reflux Disease. Can J Gastroenterol Hepatol. 2019 Dec 12; 2019:3926051. doi: 10.1155/2019/3926051.
89. Simons M, Aufenacker T, BayNielsen M, Bouillot J, Campanelli G, Conze J, De Lange D, Fortelny R, Heikkinen T, Kingsnorth A (2009) European Hernia Society guidelines on the treatment of inguinal hernia in adult patients. Hernia13(4):343–403 7.
90. Sowards KJ, Holton NF, Elliott EG, et al. Safety of robotic assisted laparoscopic recurrent paraesophageal hernia repair: insights from a large single institution experience. Surg Endosc 2020; 34:2560-6.
91. Tam V, Winger DG, Nason KS (2016) A systematic review and meta-analysis of mesh vs suture cruroplasty in laparoscopic largehiatal hernia repair. Am J Surg 211(1):226–238. https://doi.org/ 10.1016/j.amjsurg.2015.07.007.
92. Temperley HC, Davey MG, O'Sullivan NJ, Ryan ÉJ, Donlon NE, Donohoe CL et al (2022) What works best in hiatus hernia repair, sutures alone, absorbable mesh or non-absorbable mesh? A systematic review and network meta-analysis of randomized clinical trials. Dis Esophagus 36(7): doac101.
93. Tolone S, Savarino E, Zaninotto G, Gyawali CP, Frazzoni M, de Bortoli N, Frazzoni L, del Genio G, Bodini G, FurnariM (2018) High-resolution manometry is superior to endoscopy and radiology in assessing and grading sliding hiatal hernia: A comparison with surgical in vivo evaluation. United European Gastroenterol J 6(7):981. https://doi. org/10.1177/2050640618769160.
94. van Rijn S, Roebroek YG, Conchillo JM, Bouvy ND, Masclee AA. Effect of vagus nerve injury on the outcome of antireflux surgery: an extensive literature review. Dig Surg. 2016;33(3):230–239. doi: 10.1159/000444147.
95. Vansant JH, Baker JW Jr (1976) Complications of vagotomy in the treatment of hiatal hernia. AnnSurg 183(6):629.
96. Vilar A, Priego P, Puerta A, et al. Redo Surgery after Failure of Antireflux Surgery. Am Surg 2018; 84:1819-24.
97. Wang KK, Sampliner RE (2008) Updated guidelines 2008 for the diagnosis, surveillance and therapy of Barrett’s esophagus. Am J Gastroenterol103(3):788.
98. Watson DI, Davies N, Devitt PG, Jamieson GG. Importance of dissection of the hernial sac in laparoscopic surgery for large hiatal hernias. Arch Surg. 1999;134(10):1069–1073. doi: 10.1001/archsurg.134.10.1069.
99. Weber C, Davis C, Shankaran V, Fisichella P (2011) Hiatal hernias: a review of the pathophysiologic theories and implication for research. SurgEndosc25(10):3149].
100. Weyhe D (2016) Netzkomplikationen bei der Hiatushernie. Chir Allg Z17(6):295–299.
101. Weyhe D, Chowbey P (2018) Komplexe Hiatushernien. In: Bittner R et al (Hrsg) Laparo-endoskopische Hernienchirurgie: Evidenzbasierte klinische Praxis. Springer, Berlin, Heidelberg, S435–446.
102. Witarto AP, Witarto BS, Pramudito SL, Ratri LC, Wairooy NAP, Konstantin T, Putra AJE, Wungu CDK, Mufida AZ, Gusnanto A. Risk factors and 26-years worldwide prevalence of endoscopic erosive esophagitis from 1997 to 2022: a meta-analysis. Sci Rep. 2023 Sep 14;13(1):15249. doi: 10.1038/s41598-023-42636-7. PMID: 37709957.
103. Working Group (2018) International guidelines for groin hernia management. Hernia 22(1):1–165. https://doi.org/10.1007/s10029- 017-1668-x.
104. Wu JS, Dunnegan DL, Soper NJ. Clinical and radiologic assessment of laparoscopic paraesophageal hernia repair. Surg Endosc. 1999;13(5):497–502. doi: 10.1007/s004649901021.
105. Yu HX, Han CS, Xue JR, Han ZF, Xin H. Esophageal hiatal hernia: risk, diagnosis and management. Expert Rev Gastroenterol Hepatol. 2018; 12:319–329.
106. Zhang C, Liu D, Li F, Watson DI, Gao X, Koetje JH, Luo T, Yan C, Du X, Wang Z. Systematic review and meta-analysis of laparoscopic mesh versus suture repair of hiatus hernia: objective and subjective outcomes. Surg Endosc. 2017 Dec;31(12):4913-4922. doi: 10.1007/s00464-017-5586-x.
107. Zahiri HR, Weltz AS, Sibia US, et al. Primary versus redo paraesophageal hiatal hernia repair: a comparative analysis of operative and quality of life outcomes. Surg Endosc 2017; 31:5166-74.
108. Zaninotto G, Portale G, Costantini M, Fiamingo P, Rampado S, Guirroli E, Nicoletti L, Ancona E (2007) Objective follow-up after aparoscopic repair of large type III hiatal hernia. Assessment of safety and durability. World J Surg 31(11):2177–2183.
109. Zehetner J, Lipham JC, Ayazi S, Oezcelik A, Abate E, Chen W, DeMeester SR, Sohn HJ, Banki F, Hagen JA (2010) A simplified technique for intrathoracic stomach repair: laparoscopic fundoplication with Vicryl mesh and BioGlue crural reinforcement. Surg Endosc 24(3):675–679.
110. Zullo A, Manta R, De Francesco V, FioriniG, LahnerE, VairaD, Annibale B (2018) Cameron lesions: a still overlooked diagnosis. Case report and systematic review of literature. Clin Res Hepatol Gastroenterol. https://doi.org/10.1016/j.clinre. 2018.05.002.
111. Ревишвили А.Ш. с соавт. Хирургическая помощь в Российской Федерации. - М., 2024. - 192 с.
Приложение А1. Состав рабочей группы
1. Аллахвердян Александр Сергеевич -доктор медицинских наук, профессор, заведующий кафедрой торакальной хирургии ФГБОУ ВО «Российский университет медицины» Минздрава России
2. Анипченко Алексей Николаевич – доктор медицинских наук, заместитель главного врача по хирургической помощи ГБУЗ «Городская клиническая больница имени М. П. Кончаловского Департамента здравоохранения города Москвы»
3. Анищенко Владимир Владимирович – доктор медицинских наук, профессор, заведующий кафедрой хирургии Новосибирского государственного медицинского университета
4. Галлямов Эдуард Абдулхаевич - доктор медицинских наук, доцент, заведующий кафедрой общей хирургии ФГАОУ ВО Первого МГМУ имени И. М. Сеченова Минздрава России (Сеченовский университет)
5. Ганков Виктор Анатольевич – доктор медицинских наук, доцент, профессор кафедры общей хирургии, оперативной хирургии и топографической анатомии лечебного факультета ФГБОУ ВО АГМУ Минздрава России
6. Пучков Константин Викторович – доктор медицинских наук, профессор
7. Сажин Александр Вячеславович – доктор медицинских наук, профессор, член-корреспондент РАН, заведующий кафедрой факультетской хирургии № 1 лечебного факультета ФГАОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России
8. Старков Юрий Геннадьевич – доктор медицинских наук, профессор, заведующий хирургическим эндоскопическим отделением ФГБУ «НМИЦ хирургии им. А.В. Вишневского» Минздрава России
9. Черкасов Денис Михайлович – доктор медицинских наук, профессор кафедры хирургических болезней № 2 ФГБОУ ВО РостГМУ Минздрава России
Приложение А2. Методология разработки клинических рекомендаций
Предлагаемые рекомендации имеют своей целью довести до практических врачей современные представления об этиологии и патогенезе ГПОД, ознакомить их с современными алгоритмами диагностики и лечения основных вариантов течения этого заболевания, но не являются универсальным и всеобъемлющим протоколом оказания помощи.
В ситуациях, не описанных в предлагаемых рекомендациях, а также в критических ситуациях и (или) в условиях ограниченных возможностей целесообразно исходить из положений других согласительных документов, решений локальных этических комитетов и консилиумов, собственного опыта и здравого смысла.
Целевая аудитория данных клинических рекомендаций: врачи-хирурги, врачи - торакальные хирурги, врачи - анестезиологи-реаниматологи, врачи-гастроэнтерологи, врачи-кардиологи, врачи скорой медицинской помощи, врачи приемного отделения, врачи-терапевты, врачи - терапевты участковые, врачи общей практики (семейные врачи), врачи-рентгенологи, врачи ультразвуковой диагностики, врачи функциональной диагностики.
Таблица 1. Шкала оценки уровней достоверности доказательств (УДД) для методов диагностики (диагностических вмешательств)
|
УДД |
Расшифровка |
|
1. |
Систематические обзоры исследований с контролем референсным методом или систематический обзор рандомизированных клинических исследований с применением мета-анализа |
|
2. |
Отдельные исследования с контролем референсным методом или отдельные рандомизированные клинические исследования и систематические обзоры исследований любого дизайна, за исключением рандомизированных клинических исследований, с применением мета-анализа |
|
3. |
Исследования без последовательного контроля референсным методом или исследования с референсным методом, не являющимся независимым от исследуемого метода или нерандомизированные сравнительные исследования, в том числе когортные исследования |
|
4. |
Несравнительные исследования, описание клинического случая |
|
5. |
Имеется лишь обоснование механизма действия или мнение экспертов |
Таблица 2. Шкала оценки уровней достоверности доказательств (УДД) для методов профилактики, лечения и реабилитации (профилактических, лечебных, реабилитационных вмешательств)
|
УДД |
Расшифровка |
|
1. |
Систематический обзор рандомизированных клинических исследований с применением мета-анализа |
|
2. |
Отдельные рандомизированные клинические исследования и систематические обзоры исследований любого дизайна, за исключением рандомизированных клинических исследований, с применением мета-анализа |
|
3. |
Нерандомизированные сравнительные исследования, в том числе когортные исследования |
|
4. |
Несравнительные исследования, описание клинического случая или серии случаев, исследование "случай-контроль" |
|
5. |
Имеется лишь обоснование механизма действия вмешательства (доклинические исследования) или мнение экспертов |
Таблица 3. Шкала оценки уровней убедительности рекомендаций (УУР) для методов профилактики, диагностики, лечения и реабилитации (профилактических, диагностических, лечебных, реабилитационных вмешательств)
|
УУР |
Расшифровка |
|
A |
Сильная рекомендация (все рассматриваемые критерии эффективности (исходы) являются важными, все исследования имеют высокое или удовлетворительное методологическое качество, их выводы по интересующим исходам являются согласованными) |
|
B |
Условная рекомендация (не все рассматриваемые критерии эффективности (исходы) являются важными, не все исследования имеют высокое или удовлетворительное методологическое качество и/или их выводы по интересующим исходам не являются согласованными) |
|
С |
Слабая рекомендация (отсутствие доказательств надлежащего качества (все рассматриваемые критерии эффективности (исходы) являются неважными, все исследования имеют низкое методологическое качество и их выводы по интересующим исходам не являются согласованными) |
Порядок обновления клинических рекомендаций
Механизм обновления клинических рекомендаций предусматривает их систематическую актуализацию – не реже чем один раз в три года, а также при появлении новых данных с позиции доказательной медицины по вопросам диагностики, лечения, профилактики и реабилитации конкретных заболеваний, наличии обоснованных дополнений/замечаний к ранее утверждённым КР, но не чаще 1 раза в 6 месяцев.
Приложение А3. Связанные документы
Данные клинические рекомендации разработаны с учетом следующих нормативно- правовых документов:
1. Федеральный закон от 21 ноября 2011 г. № 323-ФЗ «Об основах охраны здоровья граждан в Российской Федерации», статья 37 и 79;
2. Постановление Правительства РФ от 17.11.2021 № 1968 (ред. от 14.03.2024) «Об утверждении Правил поэтапного перехода медицинских организаций к оказанию медицинской помощи на основе клинических рекомендаций, разработанных и утвержденных в соответствии с частями 3,4,6-9 и 11 ст. 37 Федерального закона «Об основах охраны здоровья граждан в Российской Федерации»;
3. Приказ Министерства здравоохранения Российской Федерации от 15 ноября 2012 г. № 922н «Об утверждении порядка оказания медицинской помощи взрослому населению по профилю «хирургия»;
4. ПриказМинистерстваздравоохраненияРоссийскойФедерацииот10мая2017г.№203н «Обутверждениикритериевоценкикачествамедицинскойпомощи».
Приложение Б. Алгоритмы ведения пациента
Приложение В. Информация для пациентов
Возможные осложнения и последствия хирургического лечения ГПОД.
В случае проведения хирургического лечения ГПОД возможен риск развития следующих осложнений: кровотечение, повреждение во время операции соседних органов и структур, инфекционные осложнения. При всех операциях на пищеводно-желудочном переходе имеется опасность повреждения блуждающего нерва, что может привести к развитию в послеоперационном периоде задержки эвакуации из желудка съеденной пищи. В очень редких случаях из-за фиксации желудка спайками к диафрагме может произойти повреждение стенки желудка во время операции. По данным литературы, частота возникновения выше указанных осложнений при операциях при ГПОД составляет 10-20%.
При выполнении лапароскопических операций по поводу ГПОД результаты лечения в отдаленном послеоперационном периоде неплохие. В течение первых трех лет после операции у 8-12% оперированных пациентов развивается рецидив, то есть ГПОД возникает снова. Однако среди пациентов с рецидивами ГПОД не более 10% нуждаются в повторных операциях. Остальных пациентов длительное время симптомы ГПОД не беспокоят.
Приложение Г.
Нет.
.
Рекомендуемые статьи
При эндоскопическом исследовании в случае бронхоэктазов в стадии ремиссии выявляется
частично диффузный бронхит I степени воспаления
Активируйте PUSH уведомления в браузер
Отключите PUSH уведомления в браузер
Содержание
Интернет магазин
Популярное
- О нас
- Правовые вопросы
- Политика
обработки персональных
данных EndoExpert.ru - Связаться с нами
- Стать партнером
© 2016-2022 EndoExpert.ru

Вы находитесь в разделе предназначенном только для специалистов (раздел для пациентов по ссылке). Пожалуйста, внимательно прочитайте полные условия использования и подтвердите, что Вы являетесь медицинским или фармацевтическим работником или студентом медицинского образовательного учреждения и подтверждаете своё понимание и согласие с тем, что применение рецептурных препаратов, обращение за той или иной медицинской услугой, равно как и ее выполнение, использование медицинских изделий, выбор метода профилактики, диагностики, лечения, медицинской реабилитации, равно как и их применение, возможны только после предварительной консультации со специалистом. Мы используем файлы cookie, чтобы предложить Вам лучший опыт взаимодействия. Файлы cookie позволяют адаптировать веб-сайты к вашим интересам и предпочтениям.
Я прочитал и настоящим принимаю вышеизложенное, хочу продолжить ознакомление с размещенной на данном сайте информацией для специалистов.

















.jpg)





.png)


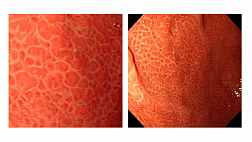















Комментарии