- Компании
- Takeda. О компании, буклеты, каталоги, контакты
- Olympus. О компании, буклеты, каталоги, контакты
- Boston Scientific. О компании, буклеты, каталоги, контакты
- Pentax. О компании, буклеты, каталоги, контакты
- Fujifilm & R-Farm. О компании, буклеты, каталоги, контакты
- Erbe. О компании, буклеты, каталоги, контакты
- Еще каталоги
- Мероприятия
- Информация
- Обучение
- Классификации
- Атлас
- Quiz
- Разделы
- Пациенту
QR-код этой страницы
Для продолжения изучения на мобильном устройстве ПРОСКАНИРУЙТЕ QR-код с помощью спец. программы или фотокамеры мобильного устройства
Документы и приказы: КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ ПО ДИАГНОСТИКЕ И ЛЕЧЕНИЮ БОЛЕЗНИ КРОНА У ВЗРОСЛЫХ (ПРОЕКТ) 2020
Полный текст статьи:
https://doi.org/10.33878/2073-7556-2020-19-2-8-38
КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ ПО ДИАГНОСТИКЕ И ЛЕЧЕНИЮ БОЛЕЗНИ КРОНА У ВЗРОСЛЫХ (ПРОЕКТ)
Ивашкин В.Т., Шелыгин Ю.А., Абдулганиева Д.И., Абдулхаков Р.А., Алексеева О.П., Алексеенко С.А., Ачкасов С.И., Багненко С.Ф., Бакулин И.Г., Барановский А.Ю., Барышева О.Ю., Белоусова Е.А.,
Болихов К.В., Валуйских Е.Ю., Варданян А.В., Веселов А.В., Веселов В.В., Головенко О.В., Губонина И.В., Жигалова Т.Н., Карпухин О.Ю., Кашников В.Н., Кизова Е.А., Князев О.В., Костенко Н.В., Куловская Д.П., Куляпин А.В., Лахин А.В., Макарчук П.А., Москалев А.И., Нанаева Б.А.,
Низов А.А., Никитина Н.В., Николаева Н.Н., Никулина И.В., Одинцова А.Х., Осипенко М.Ф., Павленко В.В., Парфенов А.И., Полуэктова Е.А.,
Румянцев В.Г., Светлова И.О., Ситкин С.И., Тарасова Л.В., Ткачев А.В., Успенская Ю.Б., Фролов С.А., Хлынова О.В., Чашкова Е.Ю., Шапина М.В., Шифрин О.С., Шкурко Т.В., Щукина О.Б.
[Ключевые слова: болезнь Крона, воспалительные заболевания кишечника, консервативная терапия, хирургическое лечение, иммуносупрессоры, глюкокортикостероиды, биологическая терапия, противорецидивная терапия]
СПИСОК СОКРАЩЕНИЙ
АЗА – азатиоприн
БК – болезнь Крона
ВЗК – воспалительные заболевания кишечника
ГКС – глюкокортикостероиды
ДИ – доверительный интервал
ЖКТ – желудочно-кишечный тракт
ИАБК – индекс активности болезни Крона ИАРА – илеоанальный резервуарный анастомоз КТ – компьютерная томография
ММХ – мультиматриксная оболочка
МП – меркаптопурин
МРТ – магнитно-резонансная томография
МТ – метотрексат
НПВС – нестероидные противовоспалительные средства РКИ – рандомизированное контролируемое испытание УЗИ – ультразвуковое исследование
ФНО-альфа – фактор некроза опухоли альфа
ЯК – язвенный колит
ТЕРМИНЫ И ОПРЕДЕЛЕНИЯ
Болезнь Крона (БК) – хроническое, рецидивирующее заболевание желудочно-кишечного тракта (ЖКТ) неясной этиологии, характеризующееся трансмуральным, сегментарным, гранулематозным воспалением с развитием местных и системных осложнений [1].
Обострение БК – появление типичных симптомов заболевания у пациентов с БК в стадии клинической ремиссии, спонтанной или медикаментозно поддерживаемой [1].
Ремиссия БК – исчезновение типичных проявлений заболевания [1].
Ремиссия БК, клиническая – отсутствие симптомов БК (соответствует значению Индекса активности БК (ИАБК) <150) [2].
Ремиссия БК, эндоскопическая – [2]. Соответствие значению упрощенного эндоскопического индекса тяжести БК (SES CD) ≤ 3.
1. КРАТКАЯ ИНФОРМАЦИЯ ПО ЗАБОЛЕВАНИЮ ИЛИ СОСТОЯНИЮ (ГРУППЕ ЗАБОЛЕВАНИЙ
ИЛИ СОСТОЯНИЙ)
1.1 Определение заболевания или состояния (группы заболеваний или состояний)
Болезнь Крона (БК) – хроническое, рецидивирующее заболевание ЖКТ неясной этиологии, характеризующееся трансмуральным, сегментарным, гранулематозным воспалением с развитием местных и системных осложнений [1].
1.2 Этиология и патогенез заболевания или состояния (группы заболеваний или состояний)
Таблица 1. Монреальская классификация БК по локализации поражения
Надпись: L1 Терминальный илеит: болезнь ограничена терминальным отделом подвздошной кишки или илеоцекальной областью (с вовлечением или без вовлечения в процесс слепой кишки) L2 Колит: любая локализация воспалительного очага в толстой кишке между слепой кишкой и анальным сфинктером, без вовлечения тонкой кишки или верхнего отдела ЖКТ L3 Илеоколит: терминальный илеит ( с вовлечением или без вовлечения слепой кишки) в сочетании с одним или несколькими очагами воспаления между слепой кишкой и анальным сфинктером L4 Верхний отдел ЖКТ: поражение проксимальнее терминального отдела (исключая полость рта) По распространенности поражения выделяют: 1. Локализованную БК: • Поражение протяженностью менее 30 см. Чаще используется для описания изолированного поражения илеоцекальной зоны; • Возможно изолированное поражение небольшого участка толстой кишки. 2. Распространенную БК: • Поражение протяженностью более 100 см (сумма всех пораженных участков). По характеру течения выделяют [9]: 1. Острое течение (менее 6 месяцев от дебюта заболевания); 2. Хроническое течение (более 6 месяцев от дебюта заболевания).
Table 1. Montreal Classification for Crohn's Disease (lesion site)
Этиология воспалительных заболеваний кишечника (ВЗК), в том числе БК, не установлена: заболевание развивается в результате сочетания нескольких факторов, включающих генетическую предрасположенность, дефекты врожденного и приобретенного иммунитета, кишечную микрофлору и различные факторы окружающей среды. Описано около
100 однонуклеотидных полиморфизмов, ассоциированных с БК. Данный генетический фон предрасполагает к изменениям врожденного иммунного ответа, аутофагии, механизмов распознавания микроорганизмов, эндоплазматического ретикулоцитарного стресса, функций эпителиального барьера и адаптивного иммунного ответа. Ключевым дефектом иммунитета, предрасполагающим к развитию ВЗК, является нарушение распознавания бактериальных молекулярных маркеров (паттернов) дендритными клетками, что приводит к гиперактивации сигнальных провоспалительных путей [3,4]. Также при ВЗК отмечается снижение разнообразия кишечной микрофлоры за счет снижения доли анаэробных бактерий, преимущественно Bacteroidetes и Firmicutes. При наличии указанных микробиологических и иммунологических изменений ВЗК развивается под действием пусковых факторов, к которым относят курение, нервный стресс, дефицит витамина D, питание с пониженным содержанием пищевых волокон и повышенным содержанием животного белка, кишечные инфекции, особенно инфекции, ассоциированные C. difficile.
Результатом взаимного влияния данных факторов риска является активация Th1и Th17-клеток, гиперэкспрессия провоспалительных цитокинов, в первую очередь, фактора некроза опухоли-альфа (ФНО-альфа), интерлейкинов 12 и 23, молекул клеточной адгезии. Каскад гуморальных и клеточных реакций при БК приводит к трансмуральному воспалению кишечной стенки с образованием характерных для БК, но не для язвенного колита (ЯК),
саркоидных гранулем, состоящих из эпителиоидных гистиоцитов без очагов некроза и гигантских клеток.
При БК могут поражаться любые отделы ЖКТ – от полости рта до ануса. Тем не менее, в подавляющем большинстве случаев БК поражает илеоцекальный отдел. БК, в отличие от ЯК, не может быть излечена ни терапевтическими, ни хирургическими методами [5].
1.3 Эпидемиология заболевания или состояния (группы заболеваний или состояний)
Согласно зарубежным данным, заболеваемость БК составляет от 0,3 до 20,2 на 100 000 человек, распро-
страненность достигает 322 на 100 000 человек [6]. Данные о распространенности БК в Российской Федерации ограничены. Распространенность БК выше в северных широтах и на Западе. Заболеваемость и распространенность БК в Азии ниже, однако, увеличивается. Европеоиды страдают заболеванием чаще, чем представители негроидной и монголоидной рас. Пик заболеваемости отмечается между 20 и 30 годами жизни [7]. Заболеваемость приблизительно одинакова у мужчин и женщин.
1.4 Особенности кодирования заболевания или состояния (группы заболеваний или состояний) по Международной статистической классификации болезней и проблем, связанных со здоровьем K50.0 – Болезнь Крона тонкой кишки
K50.1 – Болезнь Крона толстой кишки
K50.8 – Другие разновидности болезни Крона K50.9 – Болезнь Крона неуточненная
1.5 Классификация заболевания или состояния (группы заболеваний или состояний)
Для классификации БК по локализации поражения применяется Монреальская классификация (Табл. 1) [8].
![]() 9
9
Таблица 2. Внекишечные проявления БК
Table 2. Extrabowel Crohn's Disease Manifestations
|
Аутоиммунные, связанные с активностью заболевания: |
Аутоиммунные, не связанные с активностью заболевания: |
Обусловленные длительным воспалением и метаболическими нарушениями: |
|
Артропатии (артралгии, артриты) |
Анкилозирующий спондилит (сакроилеит) |
Холелитиаз |
|
Поражение кожи (узловатая эритема, |
Первичный склерозирующий холангит (редко) |
Стеатоз печени, стеатогепатит |
|
гангренозная пиодермия) |
Остеопороз, остеомаляция |
Тромбоз периферических вен, |
|
Поражение слизистых (афтозный стоматит) |
Псориаз |
тромбоэмболия легочной артерии |
|
Поражение глаз (увеит, ирит, иридоциклит, |
Псориатический артрит |
Амилоидоз |
|
эписклерит) |
|
|
Тяжесть заболевания, в целом, определяется: тяжестью текущего обострения, наличием внекишечных проявлений и осложнений, протяженностью поражения, рефрактерностью к лечению, в частности, развитием гормональной зависимости и резистентности. Однако, для формулировки диагноза и определения тактики лечения следует определять тяжесть текущего обострения, для чего используются простые критерии, разработанные Обществом по изучению ВЗК [10], индекс Харви-Брэдшоу [11]. Существует также ИАБК (индекс активности БК – индекс Беста [12]; СDAI), как правило, применяемый в клинических испытаниях ввиду сложности его расчета, в соответствии с которым выделяют легкую, среднетяжелую и тяжелую активную БК (Приложения Г1-3). Использование той или иной системы оценки тяжести определяется рутинной практикой конкретного лечебного учреждения.
БК классифицируется в зависимости от фенотипического варианта заболевания:
1. Нестриктурирующая, непенетрирующая (синонимы в русскоязычной литературе – просветная, инфильтративно-воспалительная, неосложненная, в англоязычной литературе –luminal) – воспалительный характер течения заболевания, которое никогда не было осложненным (в любое время в ходе болезни).
2. Стриктурирующая (стенозирующая) – сужение просвета кишки (по данным лучевых и/или эндоскопических методов или по результатам хирургического вмешательства).
3. Пенетрирующая (синонимы: рус. – свищевая, англ. – fistulising) возникновение интраабдоминальных свищей, и/или воспалительного инфильтрата с абсцессом в любое время в течении болезни, исключая послеоперационные интраабдоминальные осложнения.
4. Перианальная (наличие перианальных поражений: свищи, анальные трещины, перианальные абсцессы) могут быть в сочетании с любой из указанных форм, а также быть самостоятельным проявлением перианальной БК.
Классификация БК в зависимости от ответа на гормональную терапию соответствует таковой для ЯК:
1. Гормональная резистентность:
1.1 В случае тяжелой атаки – отсутствие положительной динамики клинических и лабораторных показателей, несмотря на системное введение глюкокортикостероидов (ГКС) в дозе, эквивалентной 2 мг/кг массы тела преднизолона, в течение более чем 7 дней;
1.2 В случае среднетяжелой атаки – сохранение активности заболевания при пероральном приеме ГКС в дозе, эквивалентной 1 мг/кг массы тела преднизолона, в течение 2 недель.
2. Гормональная зависимость:
2.1 Увеличение активности болезни при уменьшении дозы ГКС после достижения исходного улучшения в течение 3 месяцев от начала лечения;
2.2 Возникновение рецидива болезни в течение 3 месяцев после окончания лечения ГКС.
При формулировании диагноза следует отразить:
а) локализацию поражения с перечислением пораженных сегментов ЖКТ;
б) фенотипический вариант;
в) тяжесть текущего обострения или наличие ремиссии заболевания;
г) характер течения заболевания;
е) наличие гормональной зависимости или резистентности;
ж) наличие внекишечных или кишечных и перианальных осложнений.
При наличии у пациента свищей и стриктур одновременно или в разные периоды заболевания диагноз БК, согласно Монреальской классификации, формулируется как «пенетрирующая», так как это более тяжелое осложнение, но в диагнозе также обязательно должна фигурировать стриктура как осложнение.
1.6 Клиническая картина заболевания или состояния (группы заболеваний или состояний)
К наиболее частым клиническим симптомам БК относятся хроническая диарея (более 6 недель), в большинстве случаев, без примеси крови, боль в животе, лихорадка и анемия неясного генеза, симптомы кишечной непроходимости, а также перианальные осложнения (хронические анальные трещины, рецидивирующие после хирургического лечения, парапроктит, свищи прямой кишки).
У больных БК с поражением верхних отделов ЖКТ могут наблюдаться и другие гастроэнтерологические жалобы. Так, при поражении пищевода отмечаются жалобы на боли в грудной клетке, изжогу и срыгивание (напоминающие таковые при гастроэзофагеальной рефлюксной болезни), в более тяжелых случаях – на дисфагию и одинофагию, рвоту и потерю массы тела. При БК с поражением желудка и двенадцатиперстной кишки больные могут предъявлять жалобы на боли, тяжесть и переполнение в подложечной области, тошноту, снижение аппетита [13].
У значительной доли пациентов могут обнаруживаться внекишечные проявления заболевания [14] (Табл. 2).
Аутоиммунные проявления, связанные с активностью воспалительного процесса, которые появляются вместе с основными кишечными симптомами обострения и исчезают вместе с ними на фоне лечения. Аутоиммунные проявления, не связанные с активностью процесса (в англоязычной литературе их часто называют «сопутствующими аутоиммунными заболеваниями»), имеют тенденцию к прогрессированию независимо от фазы основного заболевания (обострение или ремиссия) и часто определяют негативный прогноз болезни.
Клиническая картина на ранних этапах развития заболевания может быть не выражена, что замедляет диагностику. В этой связи при постановке диагноза у значительной части пациентов обнаруживаются симптомы, связанные с осложнениями БК. К осложнениям БК относят: наружные свищи (кишечно-кожные), внутренние свищи (межкишечные, кишечнопузырные, ректо-вагинальные), инфильтрат брюшной полости, межкишечные или интраабдоминальные абсцессы, стриктуры ЖКТ (с нарушением кишечной проходимости и без таковой), анальные трещины, парапроктит (при аноректальном поражении), кишечное кровотечение (редко).
Перианальные проявления развиваются у 26-54% пациентов, страдающих БК [15-17], и чаще встречаются при поражении толстой кишки.
2. ДИАГНОСТИКА ЗАБОЛЕВАНИЯ ИЛИ СОСТОЯНИЯ (ГРУППЫ ЗАБОЛЕВАНИЙ
ИЛИ СОСТОЯНИЙ), МЕДИЦИНСКИЕ ПОКАЗАНИЯ И ПРОТИВОПОКАЗАНИЯ К ПРИМЕНЕНИЮ МЕТОДОВ
ДИАГНОСТИКИ
Однозначных диагностических критериев БК не существует, и диагноз выставляется на основании сочетания данных анамнеза, клинической картины и типичных эндоскопических и гистологических изменений [18-20].
Диагноз должен быть подтвержден: эндоскопическим и морфологическим методом и/или эндоскопическим и лучевым методом диагностики.
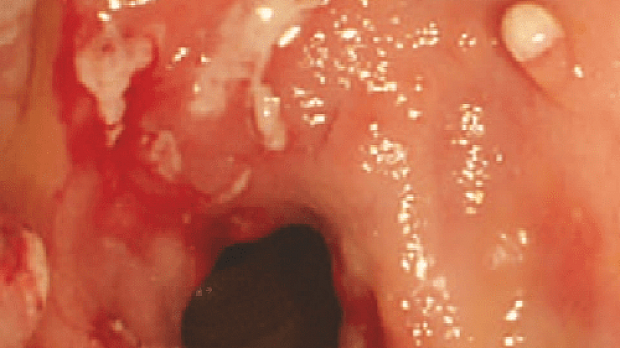
Эндоскопическими критериями диагностики БК являются регионарное (прерывистое) поражение слизистой оболочки, симптом «булыжной мостовой» (сочетание глубоких продольно ориентированных язв и поперечно направленных язв c островками отёчной гиперемированной слизистой оболочкой), линейные язвы (язвы-трещины), афты, а в некоторых случаях – стриктуры и устья свищей.
Рентгенологические проявления БК включают регионарное, прерывистое поражение, стриктуры,
«булыжную мостовую», свищи и межкишечные или внутрибрюшные абсцессы.
Морфологическими признаками БК служат:
• Глубокие щелевидные язвы, проникающие в подслизистую основу или мышечный слой;
• Эпителиоидные гранулемы (скопления эпителиоидных гистиоцитов без очагов некроза и гигантских клеток), которые обычно обнаруживаются в стенке резецированного участка и только в 15-36% случаев – при биопсии слизистой оболочки);
• Фокальная (дискретная) лимфоплазмоцитарная инфильтрация собственной пластинки слизистой оболочки;
• Трансмуральная воспалительная инфильтрация с лимфоидной гиперплазией во всех слоях кишечной стенки;
• Прерывистое поражение – чередование пораженных и здоровых участков кишки (при исследовании резецированного участка кишки).
В отличие от ЯК, крипт-абсцессы при БК формируются редко, а секреция слизи остается нормальной. Диагноз должен быть подтвержден: эндоскопическим и морфологическим методом и/или эндоскопическим и лучевым методом диагностики.
2.1 Жалобы и анамнез
При опросе пациента стоит обратить внимание на частоту и характер стула, длительность данных симптомов, наличие примеси крови, характер болей в животе, наличие эпизодов повышения температуры тела, анемию, симптомы кишечной непроходимости, перианальные осложнения (хронические анальные трещины, рецидивирующие после хирургического лечения, парапроктит, свищи прямой кишки), внекишечные проявления заболевания [14] (Табл. 2).
При сборе анамнеза стоит обратить внимание на наличие аутоиммунных проявлений, связанных и не связанных с активностью воспалительного процесса, и на осложнения БК. Кроме того, следует уточнить характер начала заболевания, информацию о поездках в южные страны, непереносимости пищевых продуктов, приеме лекарственных препаратов (включая антибиотики и нестероидные противовоспалительные средства (НПВС)), курении и семейном анамнезе.
2.2 Физикальное обследование
Физикальное обследование всех пациентов кроме общих методов (осмотр, аускультация, перкуссия и пальпация живота) должно включать:
· осмотр перианальной области;
· пальцевое исследование прямой кишки с целью выявления перианальных проявлений БК [11,21]. Уровень убедительности рекомендации С (уровень достоверности доказательств – 5). Комментарий. При физикальном обследовании могут быть обнаружены различные проявления БК, включая лихорадку, дефицит питания, наличие инфильтрата брюшной полости, наружных кишечных свищей, перианальных проявлений (трещин, свищей), а также внекишечные проявления.
2.3 Лабораторные диагностические исследования
· Рекомендуется всем пациентам при БК развернутый общий анализ крови для диагностики анемии, сопутствующей патологии, а также определения степени активности БК [22-24].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 4).
Комментарий. Лабораторные проявления БК носят неспецифический характер. При клиническом анализе крови могут быть диагностированы анемия (железодефицитная, анемии хронического заболевания, В-12или фолат-дефицитная), лейкоцитоз (на фоне хронического воспаления, при наличии абсцесса или на фоне стероидной терапии), тромбоцитоз. При необходимости дифференциальной диагностики анемии целесообразно исследовать уровень фолиевой кислоты, витамина В12, сывороточного железа, общую железосвязывающую способность сыворотки, ферритина.
· Рекомендуется всем пациентам при БК биохи-
мический анализ крови (общий белок, альбумин, АЛТ, АСТ, общий билирубин, гамма-ГТ, ЛДГ, К, Na, СL, С-реактивный белок, щелочная фосфатаза, фибриноген) для диагностики сопутствующей патологии [23,25-28].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 4).
Комментарий: Биохимическое исследование позволяет выявить электролитные нарушения, гипопротеинемию (в частности, гипоальбуминемию), а также повышение щелочной фосфатазы, что является возможным проявлением ассоциированного с БК первичного склерозирующего холангита.
Пациентам при необходимости оценки или мониторинга активности воспаления в кишечнике рекомендовано выполнять анализ кала на фекальный кальпротектин [29].
Уровень убедительности рекомендации А (уровень достоверности доказательств – 2).
Пациентам при недавно проведенном курсе антибиотикотерапии или пребывании в стационаре рекомендовано выполнять анализ кала для исключения острой кишечной инфекции, исследование клостридиальных токсинов А и В для исключения клостридиальной инфекции [30-35].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 4).
Комментарий. Для выявления инфекции в 90% случаев требуется минимум 4 образца кала. Важным при тяжелой атаке БК является определение ЦМВинфекции в крови и/или слизистой оболочке кишки методом ПЦР.
· Рекомендуется пациентам с обострением БК (или первой атаке заболевания) проводить дифференциальную диагностику с острой кишечной инфекцией [36-37].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 5).
2.4 Иные диагностические исследования Пациентам при первичном осмотре рекомендуется выполнение ректороманоскопии [11,21].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 5).
Пациентам при подозрении на кишечную непроходимость или перфорацию кишечника рекомендуется обзорная рентгенография брюшной полости для подтверждения данного состояния [38, 39].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 5).
Пациентам при необходимости определения локализации, протяженности, степени активности воспалительного процесса рекомендовано проведение илеоколоноскопии [40,41].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 4).
Пациентам при первичной диагностике, подозрении на прогрессирование заболевания или при признаках рецидива рекомендовано проведение эзофагогастродуоденоскопии для исключения/подтверждения поражения верхних отделов ЖКТ [13,42,43].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 4).
Пациентам при необходимости определения локализации, протяженности, степени активности воспалительного процесса, а также для исключения осложнений БК (абдоминальные инфильтраты, межкишечные, межорганные свищи, перфорации, стриктуры) рекомендовано проведение магнитно-резонансной томографии (МРТ) и/или компьютерной томографии (КТ) с контрастированием кишечника [18,44,45].
Уровень убедительности рекомендации А (уровень достоверности доказательств – 1).
Пациентам с перианальными проявлениями БК в виде свищей прямой кишки или при подозрении на них рекомендовано проведение МРТ малого таза с внутривенным контрастированием для подтверждения диагноза, определения локализации, протяженности свищевого хода [18,46.47].
Уровень убедительности рекомендации А (уровень достоверности доказательств – 1).
Комментарий. При невозможности выполнения МРТ таким пациентам рекомендовано выполнение ультразвукового исследования (УЗИ) ректальным датчиком и/или фистулография. Однако чувствительность и специфичность данных методов в настоящее время уступают МРТ. Целью обследования при перианальных проявлениях БК является, в первую очередь, исключение острого гнойного процесса в параректальной области, требующего срочного хирургического лечения.
Пациентам при невозможности проведения КТ или МРТ, после исключения кишечной непроходимости рекомендовано проведение рентгенконтрастного исследования кишечника с бариевой взвесью для подтверждения локализации и протяженности воспалительного процесса, межкишечных, межорганных свищей, стриктур [38,48-50].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 5).
Пациентам с острой атакой или при первом обращении, рекомендовано проведение биопсии слизистой оболочки кишки в зоне поражения для патологоанатомического исследования биопсийного материала [40,51].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 2).
Всем пациентам рекомендовано проведение УЗИ органов брюшной полости, забрюшинного пространства, малого таза для исключения осложнений основного заболевания и сопутствующей патологии [5254].
Уровень убедительности рекомендации В (уровень достоверности доказательств – 2).
Пациентам с подозрением на поражение верхних отделов ЖКТ (при отсутствии участков сужения просвета ЖКТ) и отсутствии признаков воспаления при МРТ, КТ и УЗИ или невозможности их проведения, рекомендовано проведение видеокапсульной эндоскопии для подтверждения диагноза, определения локализации, степени активности воспалительного процесса [55].
Уровень убедительности рекомендации В (уровень достоверности доказательств – 1).
Комментарий. Необходимо помнить, что задержка капсулы в кишечнике наблюдается у 13% пациентов [55].
Пациентам с БК при необходимости проведения капсульной эндоскопии до этого исследования рекомендовано выполнять рентгенологические исследования (КТ-энтерографию или МР-энтерографию) для выявления стриктур тонкой кишки [56,57].
Уровень убедительности рекомендации C (уровень достоверности доказательств – 4).
Пациентам с БК при подозрении на поражение тонкой кишки и невозможности достоверного подтверждения диагноза по данным илеоколоноскопии, КТ и МРТ, невозможности проведения видеокапсульного исследования, рекомендована двубаллонная энтероскопия, для подтверждения диагноза, определения локализации и степени активности воспалительного процесса [58].
Уровень убедительности рекомендации В (уровень достоверности доказательств – 2).
2.5 Иная диагностика
Дополнительные инструментальные и лабораторные исследования выполняются, преимущественно, с целью проведения дифференциальной диагностики с рядом заболеваний [59]. Это инфекционные, сосудистые, медикаментозные, токсические и радиационные поражения, а также дивертикулит и др. На следующем этапе дифференциальной диагностики проводится верификация клинических диагнозов ЯК и БК, относящихся к группе ВЗК. Таким образом, дифференциальный диагноз БК проводится с ЯК, острыми кишечными инфекциями (дизентерия, сальмонеллез, кампилобактериоз, иерсиниоз, амебиаз, паразитозы), антибиотико-ассоциированными поражениями кишечника (в т.ч. инфекцией ассоциированной с C.difficile) [36,37,60], НПВСассоциированными энтеропатиями, туберкулезом кишечника, системными васкулитами, неоплазиями толстой и тонкой кишки, дивертикулитом, аппендицитом, эндометриозом, солитарной язвой прямой кишки, ишемическим колитом, актиномикозом, лучевыми поражениями кишечника и синдромом раздраженного кишечника.
С целью дифференциальной диагностики и подбора терапии при внекишечных проявлениях БК и сопутствующих состояниях может потребоваться консультация:
– врача-психотерапевта или медицинского психолога (невроз, планируемая операция с наличием стомы и т.п.);
– врача-эндокринолога (стероидный сахарный диабет, надпочечниковая недостаточность у пациентов на длительной гормональной терапии);
– врача-дерматовенеролога (дифференциальный диагноз узловатой эритемы, пиодермии и т.п.);
– врача-ревматолога (артропатии, сакроилеит и т.п.);
– врача-акушера-гинеколога (беременность).
3. ЛЕЧЕНИЕ, ВКЛЮЧАЯ МЕДИКАМЕНТОЗНУЮ И НЕМЕДИКАМЕНТОЗНУЮ ТЕРАПИИ,
ДИЕТОТЕРАПИЮ, ОБЕЗБОЛИВАНИЕ, МЕДИЦИНСКИЕ ПОКАЗАНИЯ И ПРОТИВОПОКАЗАНИЯ
К ПРИМЕНЕНИЮ МЕТОДОВ ЛЕЧЕНИЯ
3.1 Консервативное лечение
Принципы лечения.
Лечебные мероприятия при БК включают в себя назначение лекарственных препаратов, хирургическое лечение и диетотерапию [11].
Всем пациентам с БК рекомендовано определять вид консервативного или хирургического лечения на основании тяжести атаки, протяженности и локализации воспаления в ЖКТ, наличию внекишечных проявлений и кишечных осложнений (стриктура, абсцесс, инфильтрат), длительности анамнеза, эффективности и безопасности ранее проводившейся терапии, а также риска развития осложнений БК [11,66]. При выборе терапии необходимо обратить внимание на наличие у пациента факторов неблагоприятного прогноза заболевания на момент установления диагноза (Возраст пациента <40 лет, распространенное (>100 см) поражение тонкой кишки, ранняя потребность в назначении системных стероидов, наличие перианальной болезни Крона, а также пенетрирующая форма (B3), вовлечение верхних отделов ЖКТ (L4), отсутствие заживления слизистой оболочки при достижении клинической ремиссии, статус курильщика, наличие эпителиоидных гранулем, наличие сопутствующих аутоиммунных заболеваний.
Цели терапии соответствуют стратегии «лечения до достижения цели» («Trеat to target»).
Целями терапии БК являются индукция ремиссии и ее поддержание без ГКС, профилактика осложнений, предупреждение операции, а при прогрессировании процесса и развитии опасных для жизни осложнений – своевременное назначение хирургического лечения. Поскольку хирургическое лечение не приводит к полному излечению пациентов с БК даже при радикальном удалении всех пораженных сегментов кишечника, необходимо проведение противорецидивной терапии, которую следует начать не позднее 2 недель после перенесенного оперативного вмешательства [62].
Лекарственные препараты, назначаемые пациентам с БК, условно подразделяются на:
1. Средства для индукции ремиссии: системные ГКС (преднизолон** и метилпреднизолон**) и топические (будесонид**), в комбинации с иммуносупрессорами (азатиоприн** (АЗА), #меркаптопурин** (МП), #метотрексат** (МТ)), биологические генноинженерные препараты: моноклональные антитела к ФНО-альфа (инфликсимаб**, адалимумаб** и цертолизумаба пэгол**), моноклональные антитела
к ИЛ-12/23 (устекинумаб**) и моноклональные антитела к интегрину альфа4-бэта7, селективно действующие только в ЖКТ (ведолизумаб**), а также антибиотики.
2. Средства для поддержания ремиссии (противорецидивные средства): иммуносупрессоры (АЗА**, #МП**), биологические препараты (инфликсимаб**, адалимумаб**, цертолизумаба пэгол** устекинумаб** и ведолизумаб**).
3. Вспомогательные симптоматические средства: препараты для коррекции анемии, препараты для коррекции белково-электролитных нарушений, средства для профилактики остеопороза (препараты кальция) и др.
Следует особо отметить, что системные ГКС не могут применяться в качестве поддерживающей терапии, а также назначаться более 12 недель [63].
3.1.1 БК в форме терминального илеита, легкая степень тяжести
Данной группе пациентов в качестве терапии первой линии рекомендуется назначать будесонид** в капсулах или гранулах в виде саше (при приеме капсул суточная доза составляет 9 мг/сут однократно или по 3 мг 3 раза в день в течение 10 недель с последующим снижением по 3 мг в неделю до полной отмены. При приеме саше суточная доза составляет 9 мг/в сутки однократно в течение 16 недель с последующим снижением по 9 мг через день в течение двух недель) [11,64-66].
Уровень убедительности рекомендации B (уровень достоверности доказательств – 1).
Комментарий. Терапевтический эффект будесонида** следует оценивать через 2-4 недели. При отсутствии терапевтического ответа на будесонид** лечение проводится как при среднетяжёлой атаке БК.
Данной группе пациентов в качестве противорецидивной терапии рекомендуется раннее (одновременно с будесонидом**) назначение иммуносупрессоров (АЗА** 2-2,5 мг/кг в день или #МП** 1,5 мг/кг в день), а при их непереносимости или неэффективности – #МТ** (25 мг/нед. п/к или в/м) [67-69].
Уровень убедительности рекомендации А (уровень достоверности рекомендации – 1).
Комментарий. Поскольку АЗА** начинает действовать через 12 недель, раннее назначение необходимо для того, чтобы АЗА** начал действовать к моменту отмены ГКС.
Данной группе пациентов после отмены будесонида** рекомендуется проводить противорецидивную терапию тиопуринами (АЗА**/#МП**) не менее 4 лет в терапевтических дозах [11,70-72].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 5).
Таблица 3. Сравнительная характеристика ГКС
Table 3. Comparative Characteristics of Glucocorticoids
|
Препарат |
Длительность действия (t1/2) |
Эквивалентная доза (мг) |
|
Гидрокортизон |
8-12 ч |
20 |
|
Преднизолон |
12-36 ч 12-36 ч |
5 |
|
Метилпреднизолон |
4 |
3.1.2 БК илеоцекальной локализации средней тяжести
Данной группе пациентов для индукции ремиссии рекомендованы топические стероиды (будесонид** 9 мг/сут.). Режим дозирования, сроки оценки эффективности как при легкой БК аналогичной локализации [66].
Уровень убедительности рекомендации A (уровень достоверности рекомендации – 1).
Данной группе пациентов для индукции ремиссии БК при неэффективности топических стероидов (будесонида**) или при наличии инфильтрата, воспалительного сужения и/или признаков системного воспаления рекомендуется применять системные ГКС (преднизолон** или эквивалентные дозы других ГКС (Табл. 3) [73-75].
Уровень убедительности рекомендации A (уровень достоверности рекомендации – 1).
Комментарий. Доза преднизолона при данной локализации и тяжести составляет 1 мг/кг массы тела. Эффективность ГКС оценивается через 2-4 недели c дальнейшим снижением дозы ГКС на 5 мг в 5-7 дней до полной отмены на фоне продолжения терапии иммуносупрессорами. Суммарная продолжительность терапии ГКС не должна превышать 12 недель. Данной группе пациентов при признаках активного системного воспаления и/или наличии инфильтрата и/или гнойных осложнений рекомендуется добавить антибиотики [76-79].
Уровень убедительности рекомендации В (уровень достоверности рекомендации – 3).
Комментарий. Рекомендовано назначение метронидазола 1 г/день + фторхинолонов 1 г/день 10–14 дней перорально или парентерально. Возможен дальнейший переход на длительный (до 3 месяцев) пероральный прием препаратов.
Данной группе пациентов в качестве противорецидивной терапии рекомендуется раннее (одновременно с ГКС) назначение иммуносупрессоров (АЗА** 2-2,5 мг/кг или #МП** 1,5 мг/кг), а при их непереносимости или неэффективности – #МТ**(25 мг/нед. п/к или в/м) [67-69].
Уровень убедительности рекомендации А (уровень достоверности рекомендации – 1).
Данной группе пациентов после отмены ГКС рекомендуется проводить поддерживающую терапию тиопуринами (АЗА**/#МП**) длительно не менее 4 лет
[11,70-72].
Уровень убедительности рекомендации A (уровень достоверности доказательств – 1).
Группе пациентов с активной БК со стероидорезистентностью, стероидозависимостью, непереносимостью ГКС или при неэффективности или непереносимости иммуносупрессоров рекомендуется биологическая терапия в виде индукционного курса (инфликсимаб**, адалимумаб**, цертолизумаба пэгол**, устекинумаб** или ведолизумаб**) [80-83]. Уровень убедительности рекомендации C (уровень достоверности доказательств – 3).
Комментарий. Дозы биологических препаратов назначают в соответствии с инструкцией по при-
менению. Отсутствие первичного ответа на биологическую терапию определяется после индукционного курса (в зависимости от препарата). При наличии отрицательной динамики эффективность препарата оценивается раньше. Все биологические препараты примерно одинаковы по эффективности, поэтому с одинаковой вероятностью могут быть назначены в качестве терапии первой линии.
Пациентам, достигшим ремиссии любым из биологических препаратов, рекомендуется перейти к длительной поддерживающей терапии тем же препаратом (с иммуносупрессорами или без них) [87-90].
Уровень убедительности рекомендации A (уровень достоверности доказательств – 1).
Комментарий. Дозы и схемы введения биологических препаратов для поддерживающей терапии назначают в соответствии с инструкцией по применению.
Пациентам с активной БК при назначении инфликсимаба** рекомендуется комбинировать его с тиопуринами для повышения эффективности лечения [87-90].
Уровень убедительности рекомендации A (уровень достоверности доказательств – 1).
Комментарий. Для других биологических препаратов целесообразность такой комбинации не доказана. Назначение комбинированной терапии остается на усмотрение лечащего врача.
· Рекомендуется пациентам при первичной неэффективности любым из биологических препаратов смена терапии на препарат другого класса для достижения ремиссии [91-93].
Уровень убедительности рекомендации A (уровень достоверности доказательств – 1).
Комментарий: смена на препарат того же класса возможна, однако ее эффективность ниже, чем переход на другой класс препаратов.
· Рекомендуется пациентам при потере ответа на терапию любым из биологических препаратов (рецидив БК на фоне ранее достигнутой ремиссии) оптимизация терапии тем же препаратом в виде сокращения интервалов между введениями или увеличения дозы препарата, согласно инструкциям по применению, или смена терапии на другой препарат [80-82,92,94-96].
Уровень убедительности рекомендации A (уровень достоверности доказательств – 1).
Пациентам с активной БК при неэффективности консервативной терапии рекомендовано хирургическое лечение [97-98].
Уровень убедительности рекомендации A (уровень достоверности доказательств – 1).
3.1.3 БК толстой кишки любой локализации Пациентам с легким и среднетяжелым обострением рекомендуется терапия системными ГКС (преднизолон** или эквивалентные дозы других ГКС) перорально [73-75].
Уровень убедительности рекомендации A (уровень достоверности доказательств – 1).
Комментарий. Доза преднизолона при данной локализации и тяжести составляет 1 мг/кг массы тела. Оценка терапевтического эффекта производится через 2-4 недели c дальнейшим снижением дозы ГКС на 5 мг в 5-7 дней до полной отмены на фоне продолжения терапии иммуносупрессорами. Суммарная продолжительность терапии ГКС не должна превышать 12 недель.
Пациентам с тяжелым обострением рекомендуется терапия системными ГКС (преднизолон** или эквивалентные дозы других ГКС) перорально или внутривенно [73-75].
Уровень убедительности рекомендации A (уровень достоверности доказательств – 1).
Комментарий. Доза преднизолона при данной локализации и тяжести составляет 2 мг/кг массы тела. Оценка терапевтического эффекта производится через 2-4 недели c дальнейшим снижением дозы ГКС на 5 мг в 5-7 дней до полной отмены на фоне продолжения терапии иммуносупрессорами. Суммарная продолжительность терапии ГКС не должна превышать 12 недель.
Данной группе пациентов одновременно с ГКС рекомендуется назначить иммуносупрессоры: АЗА** (2-2,5 мг/кг) или #МП** (1,5 мг/кг), а при непереносимости тиопуринов – #МТ** (25 мг/нед. п/к или в/м 1 раз в неделю) [67-69].
Уровень убедительности рекомендации A (уровень достоверности рекомендации – 1).
Данной группе пациентов при признаках активного системного воспаления, угрозе сепсиса и/или наличии инфильтрата и/или гнойных осложнений рекомендуется добавить антибиотики [76-79].
Уровень убедительности рекомендации В (уровень достоверности рекомендации – 3).
Данной группе пациентов, получающих поддерживающую терапию иммуносупрессорами, рекомендуется продолжать её длительно не менее 4 лет для поддержания стойкой ремиссии [11,70-72].
Уровень убедительности рекомендации С (уровень достоверности рекомендации – 5).
Группе пациентов с активной БК со стероидорезистентностью, стероидозависимостью, непереносимостью ГКС или при неэфективности/непереносимости иммуносупрессоров, рекомендуется биологическая терапия в виде индукционного курса (инфликсимаб**, адалимумаб**, цертолизумаба пэгол**, устекинумаб** или ведолизумаб**) [80-83].
Уровень убедительности рекомендации C (уровень достоверности доказательств – 4).
Комментарий. Дозы и схемы введения биологических препаратов назначают в соответствии с инструкцией по применению. Отсутствие первичного ответа на биологическую терапию определяется после индукционного курса (в зависимости от препарата). При наличии отрицательной динамики эффективность препарата оценивается раньше. Все биологические препараты примерно одинаковы по эффективности, поэтому с одинаковой вероятностью могут быть назначены в качестве терапии первой линии.
Пациентам, достигшим ремиссии любым из биологических препаратов, рекомендуется перейти к поддерживающей терапии тем же препаратом (с иммуносупрессорами или без них) [84-86].
Уровень убедительности рекомендации A (уровень достоверности доказательств – 1).
Комментарий. Дозы биологических препаратов для поддерживающей терапии назначают в соответствии с инструкцией по применению.
Пациентам с активной БК при назначении инфликсимаба** рекомендуется комбинировать его с тиопуринами для повышения эффективности лечения [87-89].
Уровень убедительности рекомендации A (уровень достоверности доказательств – 1).
Комментарий. Для других биологических препаратов целесообразность такой комбинации не доказана. Назначение комбинированной терапии остается на усмотрение лечащего врача.
· Рекомендуется пациентам при первичной неэффективности любым из биологических препаратов смена терапии на препарат другого класса для достижения ремиссии [91-93].
Уровень убедительности рекомендации A (уровень достоверности доказательств – 1).
Комментарий: смена на препарат того же класса возможна, однако ее эффективность ниже, чем переход на другой класс препаратов.
· Рекомендуется пациентам при потере ответа на терапию любым из биологических препаратов (рецидив БК на фоне ранее достигнутой ремиссии) оптимизация терапии тем же препаратом в виде сокращения интервалов между введениями или увеличения дозы препарата согласно инструкциям по применению или смена терапии на другой препарат [80-82,92,94-96].
Уровень убедительности рекомендации A (уровень достоверности доказательств – 1).
Пациентам с активной БК при неэффективности консервативной терапии рекомендовано хирургическое лечение [97-98].
Уровень убедительности рекомендации A (уровень достоверности доказательств – 1а).
3.1.4 БК тонкой кишки (кроме терминального илеита)
Пациентам с БК легкого течения с ограниченным поражением рекомендуется терапия месалазином с преимущественным высвобождением в тонкой кишке в дозе 4 г перорально [99,100].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 5).
Комментарий. Оценка терапевтического эффекта производится через 2-4 недели.
Пациентам, достигшим ремиссии на терапии месалазином с преимущественным высвобождением в тонкой кишке, рекомендовано проведение поддерживающей терапии в дозе 4 г перорально [99,100].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 5).
Пациентам с неэффективностью терапии месалазином рекомендуется терапия системными ГКС (преднизолон** или эквивалентные дозы других ГКС) перорально [73-75].
Уровень убедительности рекомендации A (уровень достоверности доказательств – 1).
Комментарий. Доза преднизолона при данной локализации и тяжести составляет 1 мг/кг массы тела. Оценка терапевтического эффекта производится через 2-4 недели.
Пациентам со среднетяжелым течением БК рекомендуется терапия системными ГКС (преднизолон** или эквивалентные дозы других ГКС) перорально[73-75]. Уровень убедительности рекомендации A (уровень достоверности доказательств – 1).
Комментарий. Доза преднизолона при данной локализации и тяжести составляет 1 мг/кг массы тела. Оценка терапевтического эффекта производится через 2-4 недели.
Пациентам с тяжелым течением БК рекомендуется терапия системными ГКС (преднизолон** или эквивалентные дозы других ГКС) внутривенно или перорально [73-75].
Уровень убедительности рекомендации A (уровень достоверности доказательств – 1).
Комментарий. Доза преднизолона при данной локализации и тяжести составляет 2 мг/кг массы тела. Оценка терапевтического эффекта производится через 2-4 недели.
Данной группе пециентов одновременно с ГКС рекомендуется назначить иммуносупрессоры: АЗА** (2-2,5 мг/кг) или #МП** (1,5 мг/кг), а при непереносимости тиопуринов – #МТ** (25 мг/нед. п/к или в/м 1 раз в неделю) [67-69].
Уровень убедительности рекомендации A (уровень достоверности рекомендации – 1).
Данной группе пациентов при признаках системного воспаления, угрозе сепсиса и/или наличии инфильтрата и/или гнойных осложнений рекомендуется добавить антибиотики [76-79].
Уровень убедительности рекомендации В (уровень достоверности рекомендации – 3).
Комментарий. Рекомендовано назначение метронидазола 1 г/день + фторхинолонов 1 г/день 10–14 дней перорально или парентерально. Возможен дальнейший переход на длительный (до 3 месяцев) пероральный прием препаратов.
Данной группе пациентов, получающих противорецидивную терапию иммуносупрессорами, рекомендуется продолжать её длительно не менее 4 лет для поддержания стойкой ремиссии [11,70-72].
Уровень убедительности рекомендации A (уровень достоверности рекомендации – 1).
Группе пациентов с активной БК со стероидорезистентностью, стероидозависимостью, непереносимостью ГКС, или при неэффективности (рецидив через 3-6 месяцев после отмены ГКС на фоне АЗА**/#МП**) или непереносимости иммуносупрессоров рекомендуется биологическая терапия в виде индукционного курса (инфликсимаб**, адалимумаб**, цертолизумаба пэгол**, устекинумаб** или ведолизумаб**) с последующим переходом на длительное (многолетнее) поддерживающее лечение [80-83],
Уровень убедительности рекомендации C (уровень достоверности доказательств – 3).
Комментарий. Дозы и схемы введения биологических препаратов назначают в соответствии с инструкцией по применению. Отсутствие первичного ответа на биологическую терапию определяется после индукционного курса (в зависимости от препарата). При наличии отрицательной динамики эффективность препарата оценивается раньше. Все биологические препараты примерно одинаковы по эффективности, поэтому с одинаковой вероятностью могут быть назначены в качестве терапии первой линии.
Пациентам, достигшим ремиссии любым из биологических препаратов, рекомендуется перейти к поддерживающей терапии тем же препаратом (с иммуносупрессорами или без них) [84-86].
Уровень убедительности рекомендации A (уровень достоверности доказательств – 1).
Комментарий. Дозы биологических препаратов для поддерживающей терапии назначают в соответствии с инструкцией по применению.
Пациентам с активной БК при назначении инфликсимаба** рекомендуется комбинировать его с тиопуринами для повышения эффективности лечения [87-90].
Уровень убедительности рекомендации A (уровень достоверности доказательств – 1).
Комментарий. Для других биологических препаратов целесообразность такой комбинации не доказана. Назначение комбинированной терапии остается на усмотрение лечащего врача.
· Рекомендуется пациентам при первичной неэффективности любым из биологических препаратов смена терапии на препарат другого класса для достижения ремиссии [91-93].
Уровень убедительности рекомендации A (уровень достоверности доказательств – 1).
Комментарий: смена на препарат того же класса возможна, однако ее эффективность ниже, чем переход на другой класс препаратов.
· Рекомендуется пациентам при потере ответа на терапию любым из биологических препаратов (рецидив БК на фоне ранее достигнутой ремиссии) оптимизация терапии тем же препаратом в виде сокращения интервалов между введениями или увеличения дозы препарата, согласно инструкциям по применению, или смена терапии на другой препарат [80-82,92,94-96].
Уровень убедительности рекомендации A (уровень достоверности доказательств – 1).
Пациентам с активной БК при неэффективности консервативной терапии рекомендовано хирургическое лечение [97,98].
Уровень убедительности рекомендации A (уровень достоверности доказательств – 1).
3.1.5. БК с поражением пищевода, желудка и двенадцатиперстной кишки
· Пациентам с активной формой БК с поражением
пищевода, желудка и двенадцатиперстной кишки с целью достижения ремиссии рекомендуется начальная терапия системными ГКС в комбинации с ингибиторами протонного насоса [13].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 5).
Комментарий. Контролируемые исследования, посвященные эффективности применения лекарственных препаратов для лечения БК с поражением верхних отделов ЖКТ, в настоящее время отсутствуют. При рефрактерном течении отмечен хороший эффект биологической терапии [13].
· Данной группе пациентов одновременно с ГКС рекомендуется назначить иммуносупрессоры: АЗА** (2-2,5 мг/кг) или #МП** (1,5 мг/кг), а при непереносимости тиопуринов – #МТ** (25 мг/нед. п/к или в/м 1 раз в неделю) [67-69].
Уровень убедительности рекомендации A (уровень достоверности рекомендации – 1).
· Данной группе пациентов, получающих противо-
рецидивную терапию иммуносупрессорами, рекомендуется продолжать её длительно не менее 4 лет для поддержания стойкой ремиссии [11,70-72].
Уровень убедительности рекомендации A (уровень достоверности рекомендации – 1).
· Группе пациентов с активной БК со стероидорези-
стентностью, стероидозависимостью, непереносимостью ГКС или при неэфективности/непереносимости иммуносупрессоров, рекомендуется биологическая терапия аналогичная ситуациям при других локализациях БК [80-90].
Уровень убедительности рекомендации C (уровень достоверности доказательств – 3).
· Пациентам с активной БК при неэффективности
консервативной терапии рекомендовано хирургическое лечение [97-98].
Уровень убедительности рекомендации A (уровень достоверности доказательств – 1).
3.1.6 Тяжелое течение активной БК любой локализации
Пациентам с тяжелым течением БК рекомендуется терапия системными ГКС (преднизолон** или эквивалентные дозы других ГКС) внутривенно или перорально [73,74].
Уровень убедительности рекомендации A (уровень достоверности доказательств – 1).
Комментарий. Доза преднизолона при данной локализации и тяжести составляет 1-2 мг/кг массы тела. Оценка терапевтического эффекта производится через 2-4 недели.
Данной группе пациентов одновременно с ГКС рекомендуется назначить иммуносупрессоры: АЗА** (2-2,5 мг/кг) или #МП** (1,5 мг/кг), а при непереносимости тиопуринов – #МТ** (25 мг/нед. п/к или в/м 1 раз в неделю) [67-69].
Уровень убедительности рекомендации A (уровень достоверности рекомендации – 1).
Данной группе пациентов при признаках системного воспаления, угрозе сепсиса и/или наличии инфильтрата, и/или гнойных осложнений рекомендуется добавить антибиотики [76-79].
Уровень убедительности рекомендации В (уровень достоверности рекомендации – 3).
Комментарий. Рекомендовано назначение метронидазола 1 г/день + фторхинолонов 1 г/день 10–14 дней перорально или парентерально. Возможен дальнейший переход на длительный (до 3 месяцев) пероральный прием препаратов.
Данной группе пациентов, получающих противорецидивную терапию иммуносупрессорами, рекомендуется продолжать её длительно не менее 4 лет для поддержания стойкой ремиссии [11,70-72].
Уровень убедительности рекомендации С (уровень достоверности рекомендации – 5).
Группе пациентов с активной БК со стероидорезистентностью, стероидозависимостью, непереносимостью ГКС, или при неэффективности (рецидив через 3-6 месяцев после отмены ГКС на фоне АЗА**/#МП**) или непереносимости иммуносупрессоров рекомендуется биологическая терапия в виде индукционного курса (инфликсимаб**, адалимумаб**, цертолизумаба пэгол**, устекинумаб** или ведолизумаб**) [80-83].
Уровень убедительности рекомендации C (уровень достоверности доказательств – 3).
Комментарий. Дозы и схемы введений биологических препаратов назначают в соответствии с инструкцией по применению. Отсутствие первичного ответа на биологическую терапию определяется после индукционного курса (в зависимости от препарата). При наличии отрицательной динамики эффективность препарата оценивается раньше. Все биологические препараты примерно одинаковы по эффективности, поэтому с одинаковой вероятностью могут быть назначены в качестве терапии первой линии.
Данной группе пациентов при раннем рецидиве заболевания в течение 6 месяцев лечение рекомендуется сразу начинать с биологических препаратов в сочетании с системными ГКС в комбинации с иммуносупрессорами или без них [11].
Уровень убедительности рекомендации С (уровень достоверности рекомендации – 5).
Комментарий. Повторные курсы ГКС допустимо назначать только при невозможности применения биологических препаратов.
Пациентам, достигшим ремиссии любым из биологических препаратов, рекомендуется перейти к поддерживающей терапии тем же препаратом (с иммуносупрессорами или без них) [84-86].
Уровень убедительности рекомендации A (уровень достоверности доказательств – 1).
Комментарий. Дозы биологических препаратов для поддерживающей терапии назначают в соответствии с инструкцией по применению.
Пациентам с активной БК при назначении инфликсимаба** рекомендуется комбинировать его с тиопуринами для повышения эффективности лечения [87-90].
Уровень убедительности рекомендации A (уровень достоверности доказательств – 1).
Комментарий. Для других биологических препаратов целесообразность такой комбинации не доказана. Назначение комбинированной терапии остается на усмотрение лечащего врача.
· Рекомендуется пациентам при первичной неэффективности любым из биологических препаратов смена терапии на препарат другого класса для достижения ремиссии [91-93].
Уровень убедительности рекомендации A (уровень достоверности доказательств – 1).
Комментарий: смена на препарат того же класса возможна, однако ее эффективность ниже, чем переход на другой класс препаратов.
· Рекомендуется пациентам при потере ответа на терапию любым из биологических препаратов (рецидив БК на фоне ранее достигнутой ремиссии) оптимизация терапии тем же препаратом в виде сокращения интервалов между введениями или увеличения дозы препарата согласно инструкциям по применению или смена терапии на другой препарат [80-82,92,94-96]. Уровень убедительности рекомендации A (уровень достоверности доказательств – 1). Пациентам с активной БК при неэффективности консервативной терапии рекомендовано хирургическое лечение [97,98].
Уровень убедительности рекомендации A (уровень достоверности доказательств – 1).
3.1.7 БК с перианальными поражениями Перианальные поражения при БК часто требуют хирургического лечения, которое рассматривается в Разделе 3.2.5 «Лечение БК с перианальными поражениями».
У всех пациентов с перианальным поражением БК в случае отсутствия показаний к хирургическому лечению или после него рекомендовано назначение иммуносупрессоров (АЗА**, #МП**, #МТ**) и/или биологических препаратов (инфликсимаб**, адалимумаб**, цертолизумаба пэгол**, устекинумаб** или ведолизумаб) в стандартных дозах [16,101,102].
Уровень убедительности рекомендации С (уровень достоверности рекомендации – 5).
Пациентам с перианальными поражениями БК рекомендовано назначение метронидазола 1 г/сут. и/или ципрофлоксацина 1 г/сут. [16,17,102,103].
Уровень убедительности рекомендации В (уровень достоверности рекомендации – 2).
Комментарий. Антибиотики назначаются длительно (до 6 мес. или до появления побочных эффектов).
У пациентов с перианальными проявлениями БК рекомендовано подключение к терапии метронидазолом в виде свечей и мазей [16,102,104].
Уровень убедительности рекомендации В (уровень достоверности рекомендации – 2).
У пациентов с перианальными проявлениями БК, при наличии трещин анального канала хирургическое вмешательство не рекомендуется, а отдается предпочтение вышеописанной местной консервативной терапии [16,102,104].
Уровень убедительности рекомендации В (уровень достоверности рекомендации – 2).
3.1.8 Мониторинг эффективности и побочных эффектов лекарственной терапии
· Всем пациентам для мониторинга эффективности
лечения любыми препаратами рекомендуется исследование кальпротектина в кале [105-108].
Уровень убедительности рекомендации В (уровень достоверности рекомендации – 2).
Комментарий. Периодичность мониторинга 1 раз в 3 месяца позволяет своевременно (до появления симптомов заболевания) выявить реактивацию воспаления в кишечнике.
· Всем пациентам для мониторинга эффективности лечения любыми препаратами рекомендуется эндоскопия через 6-9 месяцев после назначения терапии [109].
Уровень убедительности рекомендации В (уровень достоверности рекомендации – 3).
· Всем пациентам для мониторинга эффективности
лечения любыми препаратами рекомендуются визуализирующие методы (КТ или МРТ кишечника) для мониторинга эффективности терапии рекомендуется проводить 1 раз в год [110].
Уровень убедительности рекомендации В (уровень достоверности рекомендации – 3).
· Пациентам рекомендовано ежегодно выполнять
местный осмотр перианальной области и пальцевое исследование прямой кишки для исключения перианальных осложнений, а также при необходимости – УЗИ ректальным датчиком (при доступности экспертного исследования) [11,111].
Уровень убедительности рекомендации С (уровень достоверности рекомендации – 5).
· Пациентам при динамическом нарастании уровня
маркеров воспаления (С-реактивного белка, фекального кальпротектина) рекомендуется выполнять (илео)колоноскопию для оценки активности заболевания [112].
Уровень убедительности рекомендации A (уровень достоверности рекомендации – 1).
Комментарий. Рутинное (ежегодное) эндоскопическое исследование при отсутствии клинических показаний (сомнений в диагнозе, необходимости исключения сопутствующих состояний, нарастания клинических проявлений, подозрений на осложнения) в большинстве случаев не требуется. При отсутствии показаний, связанных с БК, периодичность (илео)колоноскопии определяется клиническими
рекомендациями по раннему выявлению злокачественных новообразований толстой кишки.
· Пациентам, получающим иммуносупрессоры, рекомендовано ежемесячно выполнять исследование уровня эритроцитов, лейкоцитов, тромбоцитов крови, свободного и связанного билирубина, креатинина, мочевины, определение активности аланинаминотрансферазы, аспартатаминотрансферазы, щелочной фосфатазы, амилазы в крови для оценки функции печени [11].
Уровень убедительности рекомендации С (уровень достоверности рекомендации – 5).
· Рекомендуется пациентам перед проведением
терапии ГИБП и далее каждые 6 месяцев консультация врача-фтизиатра и скрининг на туберкулез (квантифероновый тест, а при невозможности, проведение внутрикожной пробы с туберкулезным аллергеном – проба Манту, диаскин-тест) для диагностики туберкулеза [113].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 5).
Пациентам до назначения иммуносупрессивной терапии, включая ГИБП и на фоне лечения рекомендуется проводить скрининг на наличие маркеров вирусных гепатитов В (HBsAg, анти-HBc, ДНК качественным методом), С (анти-HCV) и иммунодефицита человека (анти-ВИЧ), а также сифилиса для диагностики сопутствующих заболеваний в соответствии с профессиональными клиническими рекомендациями [114].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 5).
Рекомендовано строгое соблюдение доз и графика введения биологических препаратов. Нерегулярное введение биологических препаратов повышает риск аллергических реакций и неэффективности лечения [115].
Уровень убедительности рекомендации B (уровень достоверности рекомендации – 2).
Комментарий. Недопустимы перерывы в лечении без медицинских показаний.
3.2 Хирургическое лечение БК
Большинство пациентов с БК в течение жизни переносят хотя бы одно оперативное вмешательство на ЖКТ. Невозможность радикального излечения пациентов с БК нередко приводит к повторным резекциям, увеличивая риск синдрома короткой кишки. Современная тактика хирургического лечения БК направлена на выполнение ограниченных резекций, а при возможности – проведение органосохраняющих вмешательств (стриктуропластика, дилатация стриктур) [97-87].
У пациентов с осложненной формой БК, перенесших хирургическое лечение, применение биологической терапии в анамнезе ассоциировано с увеличени-
ем послеоперационных септических осложнений. В связи с этим рекомендовано с осторожностью прибегать к назначению биологической терапии у пациентов, которым планируется хирургическое лечение. При этом безопасный период времени отмены биологического препарата перед оперативным вмешательством неизвестен [116-119].
Уровень убедительности рекомендации А (уровень достоверности доказательств – 2).
Комментарий. Последние результаты исследований и мета-анализов показали увеличение риска возникновения послеоперационных осложнений, таких как несостоятельность анастомоза, возникновение внутрибрюшных абсцессов, плохого заживления ран у пациентов, получавших биологическое лечение перед хирургическим вмешательством [116-119].
3.2.1 Показания к хирургическому лечению БК Показаниями к оперативному вмешательству при БК служат острые и хронические осложнения, а также неэффективность консервативной терапии и задержка физического развития [97,98].
Острые осложнения БК.
К ним относят кишечное кровотечение, перфорацию кишки и токсическую дилатацию ободочной кишки. При кишечном кровотечении экстренное хирургическое вмешательство рекомендуется при невозможности стабилизировать гемодинамику пациента, несмотря на переливания эритроцитарной массы и проведения интенсивной гемостатической терапии [120,121].
Уровень убедительности рекомендации C (уровень достоверности рекомендации – 5).
Комментарий. Кишечное кровотечение констатируют при потере более 100 мл крови/сутки по данным объективных лабораторных методов (сцинтиграфия, определение гемоглобина в каловых массах гемоглобинцианидным методом) или при объеме каловых масс с визуально определяемой примесью крови более 800 мл/сутки. В подобных случаях выполняется резекция пораженного участка кишечника (с наложением анастомоза или без такового, а также с возможным формированием стом) с обязательной интраоперационной энтероили колоноскопией [121].
У пациентов с осложненной формой БК при выявлении угрожающих симптомов (перитонеальные симптомы, свободный газ в брюшной полости по данным обзорной R-графии) рекомендуется экстренное хирургическое вмешательство, которое в подобной ситуации может быть ограничено резекцией пораженного отдела с формированием анастомоза или стомы [122,123].
Уровень убедительности рекомендации C (уровень достоверности рекомендации – 5).
Комментарий. У пациентов с локализацией БК в тонкой кишке ее перфорация в свободную брюшную полость является достаточно редким осложнением и обычно возникает либо дистальнее, либо проксимальнее участка кишки с наличием стриктуры. В случае экстренной операции рекомендовано избегать формирования первичного анастомоза без протекции при помощи двуствольной илеостомы [123].
У пациентов с БК, в случае перфорации толстой кишки, в качестве операции выбора рекомендуется субтотальная резекция ободочной кишки с формированием илеостомы [123].
Уровень убедительности рекомендации C (уровень достоверности рекомендации – 4).
У пациентов с локализацией БК в толстой кишке, при развитии токсической дилатации, операцией выбора рекомендуется субтотальная колэктомия с одноствольной илеостомией [123].
Уровень убедительности рекомендации C (уровень достоверности рекомендации – 4).
Комментарий. Токсическая дилатация ободочной кишки является редким осложнением при БК и представляет собой не связанное с обструкцией расширение ободочной кишки до 6,0 см и более с явлениями интоксикации. К факторам риска токсической дилатации относятся гипокалиемия, гипомагниемия, подготовка кишки к колоноскопии при помощи осмотических слабительных и прием антидиарейных препаратов. О развитии токсической дилатации свидетельствует внезапное сокращение частоты стула на фоне имевшейся диареи, вздутие живота, а также внезапное уменьшение или исчезновение болевого синдрома и нарастание симптомов интоксикации (нарастание тахикардии, снижение АД).
Хронические осложнения БК.
Хронические осложнения включают стриктуры, инфильтрат брюшной полости, внутренние или наружные кишечные свищи и наличие неоплазии [124].
Неэффективность консервативной терапии и задержка физического развития.
О неэффективности консервативной терапии свидетельствует наличие гормональной зависимости и резистентности (см. Раздел 1.5. Классификация БК). Проявлением неадекватной лекарственной терапии является также задержка физического развития, чаще всего возникающая при поражении верхних отделов ЖКТ.
3.2.2 Хирургическое лечение БК в форме терминального илеита или илеоколита
У пациентов данной группы при формировании стриктуры подвздошной кишки или илеоцекального клапана в качестве операции выбора рекомендуется резекция илеоцекального угла с формированием илео-асцендоанастомоза или стомы (при наличии нарушения кишечной проходимости) [125,126].
Уровень убедительности рекомендации С (уровень достоверности рекомендации – 4).
Комментарий. Приблизительно 1/3 всех пациентов с БК имеет подобную локализацию, которая часто осложняется формированием стриктуры подвздошной кишки или илеоцекального клапана. При этом решающим фактором для отказа от выполнения первичного анастомоза является наличие нарушения кишечной проходимости.
У пациентов данной группы, при выявлении стриктуры после первого курса консервативного лечения (т.е. применения ГКС) в качестве первого этапа лечения рекомендуется резекция пораженного участка кишки, а не повторный курс консервативной (гормональной) терапии [127].
Уровень убедительности рекомендации C (уровень достоверности рекомендации – 5).
У пациентов с активной БК с формированием абсцесса брюшной полости рекомендуется назначение антибиотиков, а также дренирование абсцесса или резекция пораженного участка [127].
Уровень убедительности рекомендации C (уровень достоверности рекомендации – 5).
Комментарий. Дренирование может осуществляться хирургическим путем или в специализированных центрах и при наличии достаточной квалификации – путем чрезкожного дренирования. Последний вариант может применяться только при отсутствии стриктуры пораженного участка кишечника, что определяет необходимость резекции пораженного отдела.
У пациентов с осложненной формой БК, при наличии непротяженных стриктур тощей или подвздошной кишки, включая стриктуры анастомоза после предшествовавшей резекции, альтернативой резекции рекомендовано выполнение рассечения рубцовых стриктур тонкой кишки (стриктуропластики), позволяющей избежать обширных резекций тонкой кишки [98].
Уровень убедительности рекомендации С (уровень достоверности рекомендации – 5).
Комментарий. Выполнение данного вмешательства возможно при длине стриктуры не более 10 см. Противопоказаниями к стриктуропластике служат наличие инфильтрата, абсцесса, злокачественных образований в стенке кишки или активное кровотечение и выраженное воспаление пораженного участка.
У пациентов данной группы, при отсутствии инфильтрата и абсцесса предпочтительней выполнение хирургического вмешательства на тонкой кишке и илео-цекальной зоне лапароскопическим способом [128,129].
Уровень убедительности рекомендации С (уровень достоверности рекомендации – 5).
Комментарий. Одномоментное формирование двух анастомозов не приводит к увеличению частоты послеоперационных осложнений и частоты рецидива заболевания [130]. Предпочтительной методикой формирования анастомоза на тонкой кишке является наложение аппаратного анастомоза по типу «бок-в-бок», что уменьшает вероятность его несостоятельности [131] и последующего развития стриктуры.
3.2.3 Хирургическое лечение БК толстой кишки
У пациентов данной группы, при ограниченном поражении толстой кишки рекомендуется резекция пораженного сегмента с формированием кишечного анастомоза в пределах здоровых тканей [132,133].
Уровень убедительности рекомендации В (уровень достоверности рекомендации – 2).
Комментарий. Пациентам с ограниченным поражением толстой кишки (менее трети толстой кишки), при развитии осложнений БК, не требуется колэктомия. При наличии поражения в восходящем отделе ободочной кишки, в силу анатомических особенностей показана правосторонняя гемиколэктомия (с сохранением терминального отдела подвздошной кишки). При поражении левого изгиба и/или нисходящей ободочной кишки выполняется левосторонняя гемиколэктомия с формированием трансверзосигмоидного анастомоза или стомы. При локализации БК в сигмовидной кишке выполняется резекция пораженного участка.
У пациентов с распространенной БК толстой кишки с тяжелыми клиническим проявлениями, операцией выбора рекомендуется субтотальная колэктомия с наложением одноствольной илеостомы [98].
Уровень убедительности рекомендации C (уровень достоверности рекомендации – 5).
Комментарий. Дистальную часть толстой кишки возможно не резецировать при условии отсутствия в ней выраженного воспаления и вывести на переднюю брюшную стенку в виде одноствольной сигмостомы, или ушить культю прямой кишки наглухо.
У пациентов с поражением всей толстой кишки, а также наличием выраженного воспаления в прямой кишке и тяжелыми перианальными поражениями в качестве альтернативной операции рекомендована колэктомия с брюшно-анальной резекцией прямой кишки с формированием концевой одноствольной илеостомы [98].
Уровень убедительности рекомендации C (уровень достоверности рекомендации – 5).
Комментарий. Данное вмешательство выполняется только у пациентов с выраженной активностью воспалительного процесса в прямой кишке или тяжелыми перианальными проявлениями, поскольку делает невозможным дальнейшее восстановление анальной дефекации.
У пациентов с тяжелыми перианальными поражениями, по возможности, не рекомендована брюшно-промежностная экстирпация [98].
Уровень убедительности рекомендации C (уровень достоверности рекомендации – 5).
Комментарий. Экстирпация прямой кишки нецелесообразна в связи с крайне низкими репарационными возможностями и риском формирования обширных промежностных ран, которые в дальнейшем длительно заживают вторичным натяжением, что инвалидизирует пациентов и ограничивает их социальную активность.
У пациентов с тотальным поражением толстой кишки, при отсутствии тяжелых клинических проявлений и минимальной активностью воспалительных изменений в прямой кишке, адекватной функции держания кишечного содержимого и отсутствии перианальных поражений, в качестве операции выбора рекомендована колэктомия с формированием илео-ректального анастомоза [132].
Уровень убедительности рекомендации C (уровень достоверности рекомендации – 5).
Комментарий. Возможность формирования тонкокишечного резервуара (илео-анального резервуарного анастомоза (ИАРА)) при БК толстой кишки является спорной в связи с высокой частотой осложнений и частым возникновением показаний к удалению резервуара. В то же время, средняя продолжительность жизни пациентов после формирования ИАРА без постоянной илеостомы достигает 10 лет, что имеет значение для молодых работоспособных пациентов [133]. Основные проблемы, угрожающие пациенту с ИАРА на фоне БК, это развитие перианальных поражений и БК тонкокишечного резервуара.
У пациентов с локализацией БК в толстой кишке формирование илеостомы (отключающей двуствольной стомы) с целью прекращения транзита кишечного содержимого по толстой кишке рекомендовано только у крайне истощенных пациентов и у беременных женщин [128].
Уровень убедительности рекомендации C (уровень достоверности рекомендации – 5).
Комментарий. Данный вид хирургического лечения является временным. Учитывая, что при БК отключение пассажа по толстой кишке не всегда является эффективным, в последующем необходимо вновь обсуждать вопрос об объеме оперативного вмешательства после проведения точной дифференциальной диагностики между БК толстой кишки и ЯК. Все перечисленные хирургические вмешательства возможно безопасно выполнить с использованием лапароскопических технологий [134,135].
У пациентов с локализацией БК в толстой кишке при выявлении непротяженной стриктуры рекомендовано выполнение баллонной дилатации стенозов толстой кишки (эндоскопическим способом) [136]. Уровень убедительности рекомендации C (уровень достоверности рекомендации – 5).
Комментарий. Данная манипуляция связана с более высоким риском рецидива заболевания по сравнению с резекцией пораженного участка кишечника.
У пациентов с локализацией БК в толстой кишке выполнение рассечения рубцовых стриктур (стриктуропластики) не рекомендуется [127,137,138].
Уровень убедительности рекомендации В (уровень достоверности рекомендации – 2).
3.2.4 Хирургическое лечение БК с поражением верхних отделов ЖКТ
У пациентов данной группы, при выявлении стриктур, инфильтратов и межкишечных свищей в проксимальных отделах тонкой кишки в качестве хирургического лечения рекомендовано формирование обходных анастомозов, рассечение рубцовых стриктур (стриктуропластика) или резекция пораженного участка [98,137,138].
Уровень убедительности рекомендации В (уровень достоверности рекомендации – 2).
Комментарий. Вовлечение в воспалительный процесс участка кишечника проксимальнее терминального отдела подвздошной кишки часто приводит к формированию множественных стриктур и межкишечных свищей, что обусловливает неблагоприятный прогноз БК и требует хирургического лечения.
У пациентов данной группы, прибегать к формированию обходного анастомоза рекомендовано лишь в исключительных случаях, поскольку высок риск развития синдрома избыточного бактериального роста в отключенной части тонкой кишки, а также возможно развитие рака. Вместе с тем, обширные резекции обуславливают развитие синдрома короткого кишечника [139].
Уровень убедительности рекомендации С (уровень достоверности рекомендации – 5).
У пациентов данной группы, при наличии единичных или множественных непротяженных стриктур операцией выбора могут быть различные варианты рассечения рубцовых стриктур тонкой кишки (стриктуропластики) [140].
Уровень убедительности рекомендации С (уровень достоверности рекомендации – 4).
У пациентов данной группы, при выявлении стриктуры гастродуоденальной зоны (как правило, 12-перстной кишки) рекомендована эндоскопическая баллонная дилатация или выполнение рассечения рубцовой стриктуры (стриктуропластики) [140].
Уровень убедительности рекомендации C (уровень достоверности рекомендации – 4).
3.2.5 Лечение БК с перианальными поражениями (перианальная БК)
Подход к хирургическому вмешательству на перианальной области должен быть индивидуален для каждого пациента [101,141].
У пациентов с перианальными проявлениями БК, при наличии наружных перианальных свищей рекомендована ликвидация свища путем его иссечения (при помощи фистулотомии) [142] или его адекватное дренирование при наличии абсцессов (при помощи установки латексных дренажей-сетонов) [143].
Уровень убедительности рекомендации С (уровень достоверности рекомендации – 4).
Комментарий. Простые свищи, не сопровождающиеся какими-либо симптомами, не требуют хирургического вмешательства. Рекомендовано динамическое наблюдение на фоне вышеописанной консервативной терапии. Показанием к установке сетонов в большинстве случаев являются транси экстрасфинктерные свищи. При отсутствии воспалительного процесса в слизистой оболочке прямой кишки возможно выполнение низведения слизисто-мышечного лоскута прямой кишки с пластикой внутреннего свищевого отверстия [143].
У пациентов с перианальными проявлениями БК, при лечении сложных свищей рекомендовано их дренирование (установка латексных дренажей-сетонов) в комбинации с агрессивной медикаментозной терапией [16].
Уровень убедительности рекомендации С (уровень достоверности рекомендации – 5).
Комментарий. Учитывая высокую эффективность биологической терапии при надлежащем дренировании сложных свищей прямой кишки оправдано её раннее назначение (инфликсимаб, адалимумаб, цертолизумаба пэгол, устекинумаб, ведолизумаб). Тем не менее, сложные свищи, с затеками и выраженным гнойным воспалением часто являются показанием к отключению пассажа по толстой кишке путем формирования двуствольной илеостомы.
У пациентов с перианальными проявлениями БК, при ректовагинальном свище рекомендовано его иссечение с ушиванием дефекта влагалища и низведением полнослойного лоскута прямой кишки [16].
Уровень убедительности рекомендации С (уровень достоверности рекомендации – 5).
Комментарий. Ректовагинальные свищи в большинстве случаев требуют хирургического вмешательства. При этом, оперативное лечение показано под прикрытием илеостомы. Лишь в отдельных ситуациях при наличии низкого свища между прямой кишкой и преддверием влагалища рекомендовано
проведение только консервативного лечения. При наличии активного поражения прямой кишки адекватная противовоспалительная терапия до операции увеличивает эффективность вмешательства [16].
У пациентов с перианальными проявлениями БК, при наличии стриктуры нижне-ампулярного отдела прямой кишки или стеноза анального канала рекомендовано выполнение проктосигмоидэктомии (или проктэктомии) или брюшно-анальной резекции прямой кишки [16].
Уровень убедительности рекомендации С (уровень достоверности рекомендации – 5).
Комментарий. Наиболее неблагоприятным фактором, повышающим вероятность постоянной илеостомы или колостомы, является наличие стриктуры нижне-ампулярного отдела прямой кишки или стеноза анального канала. В отдельных ситуациях, при отсутствии активного воспаления в вышележащих отделах кишечника, возможно бужирование стриктуры [16].
3.2.6 Противорецидивная терапия после хирургического лечения БК
Даже при полном удалении всех макроскопически измененных отделов кишечника, хирургическое вмешательство не приводит к полному выздоровлению: в течение 5 лет клинически значимый рецидив отмечается у 28-45% пациентов, а в течение 10 лет – у 36-61%, что диктует необходимость назначения или продолжения противорецидивной терапии после операций по поводу БК [144,145]. К факторам, достоверно повышающим риск послеоперационного рецидива, относятся: курение, две и более резекции кишки в анамнезе, протяженные резекции тонкой кишки в анамнезе (>50 см), перианальные поражения, пенетрирующий фенотип [146].
В зависимости от сочетания факторов риска, а также от эффективности, ранее проводившейся противорецидивной терапии, пациенты после операции должны быть стратифицированы на группы с различным риском послеоперационного рецидива. К высокому риску послеоперационного рецидива относится наличие 2 и более факторов риска:
– курение;
– перианальные поражения БК;
– пенетрирующая БК;
– протяженная резекция (более 50 см) кишечника;
– предыдущее хирургическое вмешательство;
– раннее начало заболевания.
Пациентам из группы низкого риска рекомендовано проведение терапии АЗА** (2,0-2,5 мг/кг/сут.) или #МП** (1,5 мг/кг/сут.) [147].
Уровень убедительности рекомендации B (уровень достоверности доказательств – 2).
Таблица 4. Шкала эндоскопической активности послеоперационного рецидива БК по Rutgeerts [149] (при резекции терминального отдела подвздошной кишки или илеоцекальной резекции)
Table 4. Postoperative Crohn's Disease Recurrence Scale by Rutgeerts [149] after terminal ileum resection or ileocaecal resection
|
Оценка |
Определение |
|
i0 |
Нет признаков воспаления |
|
i1 |
≤5 афтозных язв |
|
i2 |
>5 афтозных язв с нормальной слизистой оболочкой между ними или протяженные участки здоровой слизистой оболочки между более выраженными изъязвлениями или поражения, ограниченные подвздошно-толстокишечным анастомозом |
|
i3 |
Диффузный афтозный илеит с диффузно воспаленной слизистой оболочкой |
|
i4 |
Диффузное воспаление с крупными язвами, «булыжной мостовой» и/или сужением просвета |
Пациентам с высоким риском рецидива рекомендовано еще до проведения контрольного эндоскопического исследования начать курс биологической терапии (инфликсимаб**, адалимумаб**, цертолизумаба пэгол**, устекинумаб**, ведолизумаб**) [148-153]. Уровень убедительности рекомендации C (уровень достоверности доказательств – 3).
Комментарий. Данных по применению устекинума-
ба и ведолизумаба недостаточно, чтобы достоверно судить об их эффективности в качестве послеоперационной противорецидивной терапии.
Пациентам с БК противорецидивную терапию рекомендовано начинать через 4 недели после оперативного вмешательства при отсутствии послеоперационных осложнений [154].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 3).
Спустя 6-12 месяцев всем оперированным пациентам с БК рекомендовано проведение контрольного эндоскопического обследования, а при необходимости МРТ, КТ (табл. 4) [155-157].
Уровень убедительности рекомендации C (уровень достоверности доказательств – 3).
Оперированным пациентам с БК, при невозможности визуализировать зону анастомоза рекомендовано констатировать наличие или отсутствие рецидива, основываясь на сочетании данных рентгенологического обследования (КТ или МРТ) и неинвазивных маркеров воспаления – С-реактивного белка, фекального кальпротектина и др. [18,107, 108,112,155-157].
Уровень убедительности рекомендации C (уровень достоверности доказательств – 3).
У пациентов с БК при отсутствии признаков воспаления или обнаружении минимальных (i1 по шкале Rutgeerts) (Табл. 4) воспалительных изменений проводимую терапию рекомендовано продолжить[149].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 5).
У пациентов с БК при наличии более выраженных воспалительных изменений (i2-i4) рекомендовано усиление терапии: рекомендовано подключение иммуносупрессоров у пациентов, ранее их не получавших или проведение биологической терапии (адалимумабом**, инфликсимабом**, цертолизумаба пэголом**, устекинумабом**, ведолизумабом**) у пациентов, находящихся на поддерживающей терапии АЗА**/#МП** или при невозможности их назначения [147-153].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 5.
Комментарий. Наличие более выраженных воспалительных изменений (i2-i4) указывает на неэффективность проводимой терапии.
В дальнейшем у пациентов с БК, вне зависимости от характера течения заболевания и клинической манифестации БК, рекомендовано не реже одного раза в 1-3 года выполнять контрольное эндоскопическое исследование, следуя этому же алгоритму выбора противорецидивного лечения [158].
Уровень убедительности рекомендации С (уровень достоверности доказательств 4).
3.2.7 Дисфункция илеостомы после хирургического лечения БК
Под дисфункцией илеостомы понимается увеличение объема кишечного отделяемого по илеостоме более 1000 мл в сутки. Ведение пациентов с данным состоянием описано в клинических рекомендациях
«Язвенный колит».
4. МЕДИЦИНСКАЯ РЕАБИЛИТАЦИЯ, МЕДИЦИНСКИЕ ПОКАЗАНИЯ И ПРОТИВОПОКАЗАНИЯ К ПРИМЕНЕНИЮ МЕТОДОВ РЕАБИЛИТАЦИИ
Меры медицинской реабилитации направлены на профилактику осложнений консервативной терапии и нежелательных последствий хирургического лечения.
Легкая и умеренная степень нарушения функционирования требует лечения в амбулаторных условиях. Тяжелая степень нарушения функции, либо абсолютная ее невозможность требуют госпитализации в круглосуточный стационар.
У пациентов, которым потребовалось хирургическое лечение осложнений БК, возможна реабилитация в три этапа.
1- й этап – ранняя реабилитация, осуществляется непосредственно после хирургического лечения со 2-х по 14-е сутки. Основной задачей 1 этапа реабилитации является восстановление нормального функционирования ЖКТ после хирургического вмешательства. Именно на этом этапе чаще всего выявляются и должны быть корригированы нарушения мочеиспускания. Важная роль отводится также контролю гомеостаза, мероприятиям, направленным на заживление послеоперационных ран, купированию послеоперационного болевого синдрома, активизации пациента. В данный период проводится контроль общего анализа крови, биохимического анализа крови, коагулограммы крови, общего анализа мочи.
2- й этап реабилитации начинается после 15 суток и продолжается по мере необходимости в последующем. Направлен на окончательное заживление послеоперационных ран с контролем за деятельностью ЖКТ и других систем организма. Данный этап возможно осуществлять как амбулаторно, так и в условиях стационара дневного или круглосуточного пребывания.
3- й этап реабилитации осуществляется в поздний реабилитационный период у пациентов как с постоянной илеостомой, так и перед реконструктивно-восстановительной операцией. Основной задачей на данном этапе является компенсация функции ЖКТ, мероприятия, направленные на выявление и коррекцию функции запирательного аппарата прямой кишки.
Недостаточность анального сфинктера (НАС) – реабилитация возможна на 2 и 3 этапах. У пациентов после оперативного вмешательства по поводу БК с формированием стомы отмечается снижение функции держания.
Пациентам с недостаточностью анального сфинктера, перед реконструктивно-восстановительным лечением, рекомендуется выполнение патофизиологического исследования (сфинктерометрия, профилометрия, исследование проводимости по срамному нерву) с последующей консультаций физиотерапевта [159].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 5).
Пациентам при выявлении недостаточности анального сфинктера 2-3 степени рекомендуется провести реабилитационное лечение, включающее 10-дневный цикл БОС-терапии и тибиальной нейромодуляции в условиях дневного или круглосуточного стационара [159,160].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 4).
Комментарий. В реабилитации пациентов с недостаточностью анального сфинктера, по данным литературы, широкое применение имеет метод лечения биологической обратной связью (БОСтерапия), направленный на улучшение сократительной способности мышц наружного сфинктера и тазового дна за счет увеличения как силы, так и длительности произвольного сжатия [159,160].
Данный неинвазивный метод вовлекает в процесс реабилитации собственные ресурсы организма с выработкой правильных навыков на уровне создания новых условно-рефлекторных связей. Так же эффективным является метод тибиальной нейромодуляции. Нейромодуляция – это процесс, при котором электрический ток по одним нервным путям модулирует существовавшую ранее активность в других нервных путях или центрах. Чрескожная электростимуляция заднего большеберцового нерва – n.tibialis – применяется при функциональных заболеваниях органов малого таза, так как в составе заднего большеберцового нерва проходят волокна из II и III крестцовых сегментов спинного мозга, играющие значительную роль в иннервации прямой кишки, мочевого пузыря и их сфинктеров. Доказано, что мышечные структуры отключенного запирательного аппарата могут реагировать на БОС-терапию и проведение тибиальной нейромодуляции, увеличивая как тонус, так и силу волевых сокращений [159,160]. Стимуляцию тибиального нерва проводят с помощью накожного стимулирующего электрода, что позволяет пациенту после курса предварительного обучения продолжить курс лечения самостоятельно в домашних условиях. В таком случае курс лечения с ежедневными сеансами стимуляции может продлеваться до 1-3 месяцев. Контроль эффективности БОС-терапии производится перед началом и по окончании каждого курса процедур путем комплексного физиологического исследования функции запирательного аппарата прямой кишки (сфинктерометрия + физиологическое исследование резервуарной функции низведенной кишки). При улучшении показателей тонуса и сократительной способности анальных сфинктеров, можно ставить вопрос о выполнении реконструктивно-восстановительной операции, направленной на возобновление естественного пассажа по ЖКТ.
5. ПРОФИЛАКТИКА И ДИСПАНСЕРНОЕ НАБЛЮДЕНИЕ, МЕДИЦИНСКИЕ ПОКАЗАНИЯ И ПРОТИВОПОКАЗАНИЯ К ПРИМЕНЕНИЮ
МЕТОДОВ ПРОФИЛАКТИКИ
БК характеризуется прогрессирующим поражением кишечника. На момент установления диагноза осложнения (стриктуры, свищи) обнаруживаются лишь у 10-20% пациентов, в то время как в течение 10 лет подобные осложнения развиваются у >90% пациентов. В течение 10 лет хирургическое вмешательство в связи с осложнениями и/или неэффективностью консервативной терапии выполняется у половины пациентов с БК, а у 35-60% в течение 10 лет после операции развивается рецидив заболевания. Гормональная зависимость при БК в течение 10 лет хотя бы раз констатируется у 30% пациентов [161].
В связи с прогрессирующим характером заболевания пациенты, страдающие БК, должны получать постоянную (пожизненную терапию) и проходить регулярный (пожизненный) мониторинг активности заболевания. Контроль активности заболевания позволяют не только инструментальные методы исследования, но и лабораторные методы анализа маркеров воспаления, в первую очередь, уровня фекального кальпротектина, концентрация которого в стуле коррелирует со степенью язвенного поражения ЖКТ.
Периодичность и объем диспансерного наблюдения определяется индивидуально, но у большинства пациентов рекомендовано:
Пациентам при доступности экспертного исследования рекомендовано выполнять УЗИ кишечника каждые 6 месяцев [11,162-165].
Уровень убедительности рекомендации С (уровень достоверности рекомендации – 5).
Пациентам рекомендовано ежегодно выполнять рентгенологическое или МР-исследование кишечника для исключения стриктурирующих и иных осложнений [11,110].
Уровень убедительности рекомендации С (уровень достоверности рекомендации – 5).
Пациентам рекомендовано ежегодно выполнять местный осмотр перианальной области и пальцевое исследование прямой кишки для исключения перианальных осложнений, а также при необходимости – УЗИ ректальным датчиком (при доступности экспертного исследования) [11,111].
Уровень убедительности рекомендации С (уровень достоверности рекомендации – 5).
Пациентам, получающим иммуносупрессоры и/или биологические препараты, рекомендована вакцинация в качестве профилактики оппортунистических инфекций и иных осложнений: рекомбинантная вакцина против HBV, поливалентная инактивированная пневмококковая вакцина, трехвалентная инактивированная вакцина против вируса гриппа и для женщин до 26 лет, при отсутствии вируса на момент скрининга рекомендуется вакцинация от вируса папилломы человека [114].
Уровень убедительности рекомендации С (уровень достоверности рекомендации – 5).
Комментарий. К факторам риска развития оппортунистических инфекций относят: прием преднизолона** 20 мг в сутки и более в течение 2 недель, прием иммуносупрессоров (АЗА**, #МП**, #МТ**) и биологических препаратов, возраст старше 50 лет, сопутствующие заболевания (хронические заболевания легких, алкоголизм, органические заболевания головного мозга, сахарный диабет).
Всем пациентам, получающим биологическую терапию, не рекомендована смена оригинального препарата на биоаналог, или наоборот, более одного раза [166].
Уровень убедительности рекомендации С (уровень достоверности рекомендации – 5).
Комментарий. В настоящее время зарегистрированы биосимиляры (биоаналоги) анти-ФНО препаратов, схожие с оригинальными биологическими лекарственными средствами по эффективности и безопасности, однако их взаимозаменяемость с оригинальными препаратами в настоящее время не доказана. С учетом отсутствия клинических испытаний у пациентов с ВЗК, доказавших безопасность и эффективность чередования или полного переключения с оригинального препарата на биоаналоги и наоборот, подобный терапевтический подход не рекомендован [11].
6. ОРГАНИЗАЦИЯ ОКАЗАНИЯ МЕДИЦИНСКОЙ ПОМОЩИ
Медицинская помощь, за исключением медицинской помощи в рамках клинической апробации, в соответствии с федеральным законом от 21.11.2011 № 323-ФЗ (ред. от 47 25.05.2019) «Об основах охраны здоровья граждан в Российской Федерации», организуется и оказывается:
1) в соответствии с положением об организации оказания медицинской помощи по видам медицинской помощи, которое утверждается уполномоченным федеральным органом исполнительной власти;
2) в соответствии с порядками оказания помощи по профилям «гастроэнтерология», «колопроктология», обязательным для исполнения на территории Российской Федерации всеми медицинскими организациями;
3) на основе настоящих клинических рекомендаций;
4) с учетом стандартов медицинской помощи, утвержденных уполномоченным федеральным органом исполнительной власти.
Первичная специализированная медико-санитарная помощь оказывается врачом-гастроэнтерологом, врачом-колопроктологом и иными врачами-специалистами в медицинских организациях, имеющих лицензию на оказание соответствующие виды медицинской деятельности.
При подозрении или выявлении у пациента БК врачи-терапевты, врачи-терапевты участковые, врачи общей практики (семейные врачи), врачи-специалисты, средние медицинские работники в установленном порядке направляют пациента на консультацию в медицинскую организацию, имеющую в своем составе кабинет врача-гастроэнтеролога, врача-колопроктолога, амбулаторный гастроэнтерологический центр (отделение), амбулаторный колопроктологический центр (отделение), центр диагностики и лечения воспалительных заболеваний кишечника (при наличии в субъекте, организуется на функциональной основе) для оказания ему первичной специализированной медико-санитарной помощи. Консультация в указанных структурных подразделениях медицинской организации должна быть проведена не позднее 15 рабочих дней с даты выдачи направления на консультацию, а в случаях тяжелых форм БК не позднее 3 рабочих дней с даты выдачи направления на консультацию.
Врач-гастроэнтеролог, врач-колопроктолог медицинской организации, имеющей в своем составе кабинет врача-гастроэнтеролога, врача-колопроктолога, амбулаторный гастроэнтерологический центр (отделение), амбулаторный колопроктологический центр (отделение), центр диагностики и лечения воспалительных заболеваний кишечника организуют выполнение диагностических исследований, необходимых для установления диагноза, включая определение степени выраженности воспалительного процесса, протяженности поражения, наличия кишечных и внекишечных проявлений, в том числе взятие биопсийного материала.
В случае невозможности выполнения диагностических исследований, необходимых для установления диагноза, включая определение степени выраженности воспалительного процесса, протяженности поражения, наличия кишечных и внекишечных проявлений, в том числе взятие биопсийного материала, а также при наличии показаний для оказания медицинской помощи в стационарных условиях, пациент направляется лечащим врачом в гастроэнтерологическое отделение, колопроктологическое отделение, центр диагностики и лечения воспалительных заболеваний кишечника или иную медицинскую организацию, оказывающую медицинскую помощь в стационарных условиях пациентам по профилю «гастроэнтерология», «колопроктология».
При подозрении и (или) выявлении у пациента БК в ходе оказания ему скорой медицинской помощи, таких пациентов переводят или направляют в медицинские организации, оказывающие медицинскую помощь по профилю «гастроэнтерология», «колопроктология» для определения тактики ведения и необходимости применения дополнительно других методов специализированного лечения, включая проведение таргетной биологической терапии.
Врач-гастроэнтеролог, врач-колопроктолог медицинской организации, имеющей в своем составе кабинет врача-гастроэнтеролога, врача-колопроктолога, амбулаторный гастроэнтерологический центр (отделение), амбулаторный колопроктологический центр (отделение), центр диагностики и лечения воспалительных заболеваний кишечника направляет пациента в медицинские организации, имеющие для оказания медицинской помощи в стационарных условиях в своем составе гастроэнтерологическое отделение и/или колопроктологическое отделение, и/или центр диагностики и лечения воспалительных заболеваний кишечника для уточнения диагноза (в случае невозможности установления диагноза при оказании первичной специализированной медикосанитарной помощи) и оказания специализированной, в том числе высокотехнологичной, медицинской помощи. Срок начала оказания специализированной, за исключением высокотехнологичной, медицинской помощи определяется по решению комиссии по отбору пациентов для госпитализации в зависимости от тяжести БК, характера течения, распространённости воспалительного процесса. Срок не должен превышать 30 календарных дней с даты выдачи направления на госпитализацию.
Специализированная, в том числе высокотехнологичная, медицинская помощь при БК оказывается врачами-гастроэнтерологами, врачами-колопроктологами в медицинских организациях, имеющих в своем составе гастроэнтерологическое отделение и/или колопроктологическое отделение, и/или центр диагностики и лечения воспалительных заболеваний кишечника, имеющих лицензию, необходимую материальнотехническую базу, сертифицированных специалистов, в стационарных условиях и условиях дневного стационара и включает в себя профилактику, диагностику, лечение БК, требующих использования специальных методов и сложных уникальных медицинских технологий, а также медицинскую реабилитацию.
Показания для госпитализации в круглосуточный или дневной стационар медицинской организации, оказывающей специализированную, в том числе высокотехнологичную медицинскую помощь при БК определяются консилиумом врачей-гастроэнтерологов и врачей-колопроктологов, с привлечением при необходимости других врачей-специалистов.
Показанием для госпитализации пациента в медицинскую организацию в экстренной или неотложной форме является:
1) наличие осложнений БК, требующих оказания ему специализированной медицинской помощи в экстренной и неотложной форме;
2) наличие осложнений лечения БК (хирургическое вмешательство, биологическая терапия, гормональная и цитостатическая терапия и т.д.).
Показанием для госпитализации в медицинскую организацию в плановой форме является:
1) необходимость выполнения сложных интервенционных диагностических медицинских вмешательств, требующих последующего наблюдения в условиях круглосуточного или дневного стационара;
2) наличие показаний к специализированному лечению БК (хирургическое вмешательство, гормональная и цитостатическая терапия, биологическая и тар-
гетная терапия.), требующему наблюдения в условиях круглосуточного или дневного стационара.
Показанием к выписке пациента из медицинской организации является:
1) завершение курса лечения или одного из этапов оказания специализированной, в том числе высокотехнологичной медицинской помощи, в условиях круглосуточного или дневного стационара при условии отсутствия осложнений лечения, требующих медикаментозной коррекции и/или медицинских вмешательств в стационарных условиях;
2) отказ пациента или его законного представителя от специализированной, в том числе высокотехнологичной медицинской помощи в условиях круглосуточного или дневного стационара, установленной консилиумом медицинской организации, оказывающей лечение болезни Крона при условии отсутствия осложнений основного заболевания и/или лечения, требующих медикаментозной коррекции и/или медицинских вмешательств в стационарных условиях;
3) необходимость перевода пациента в другую медицинскую организацию по соответствующему профилю оказания медицинской помощи. Заключение о целесообразности перевода пациента в профильную медицинскую организацию осуществляется после предварительной консультации по предоставленным медицинским документам и/или предварительного осмотра пациента врачами специалистами медицинской организации, в которую планируется перевод.
7. ДОПОЛНИТЕЛЬНАЯ ИНФОРМАЦИЯ (В ТОМ ЧИСЛЕ ФАКТОРЫ, ВЛИЯЮЩИЕ
НА ИСХОД ЗАБОЛЕВАНИЯ ИЛИ СОСТОЯНИЯ)
Прогностически неблагоприятными факторами при БК являются курение, дебют заболевания в детском возрасте, перианальные поражения, пенетрирующий фенотип заболевания и распространенное поражение тонкой кишки. С пациентом-курильщиком в обязательном порядке должна быть проведена беседа о необходимости прекращения табакокурения.
Планирование беременности необходимо осуществлять в период ремиссии ВЗК, что позволяет улучшать исходы беременности. Применение беременными большинства препаратов для лечения ВЗК сопряжено с низким риском неблагоприятного воздействия на плод, за исключением #МТ** и месалазина в таблетках с оболочкой, содержащей дибутилфтолат. Отмена анти-ФНО возможна лишь у ограниченного числа пациенток с низким риском реактивации ВЗК. Лечение генно-инженерными биологическими препаратами, не противопоказанными при беременности (см. инструкцию по применению препарата), может быть продолжено, если польза для матери превышает потенциальные риски для плода.
КОНФЛИКТ ИНТЕРЕСОВ: АВТОРЫ ЗАЯВЛЯЮТ ОБ ОТСУТСТВИИ КОНФЛИКТА ИНТЕРЕСОВ.
The authors declare no conflicts of interest.
.
 Вам может быть интересно:
Вам может быть интересно:
- Образовательный модуль "Воспалительные заболевания кишечника" с Веселовым В.В.
- Проект рекомендаций российского общества детских гастроэнтерологов, гепатологов и нутрициологов по диагностике и лечению болезни Крона у детей
- Статьи: Дифференциальная диагностика НЯК и болезни Крона
- Монреальская классификация болезни Крона
- Шкала эндоскопической активности послеоперационного рецидива болезни Крона по Rutgeerts
- Симптом перетяжек по типу "бамбука" - патогномоничный признак болезни Крона желудка
- Патогенез болезни Крона в стихах
- Статьи: СВЯЗЬ МЕЖДУ АЦЕТАМИНОФЕНОМ И НЕСТЕРОИДНЫМИ ПРОТИВОВОСПАЛИТЕЛЬНЫМИ ПРЕПАРАТАМИ (НПВП) И РИСКОМ ОБОСТРЕНИЯ БОЛЕЗНИ КРОНА И ЯЗВЕННОГО КОЛИТА
Список литературы:
Рекомендуемые статьи
Эластография при эндосонографии (ЭУС или эндоУЗИ)
Эластография (эластосонография) – метод виртуальной пальпации (технология улучшенной визуализации при ЭУС диагностике), позволяющий дифференцировать злокачественные и доброкачественные поражения лимфоузлов. Основана на принципе, что более мягкие ткани при сжатии легче деформируются, это позволяет объективно оценить консистенцию ткани, показать различия в плотности между нормальными и патологически измененными тканями.
При эндоскопическом исследовании в случае бронхоэктазов в стадии ремиссии выявляется
частично диффузный бронхит I степени воспаления
Активируйте PUSH уведомления в браузер
Отключите PUSH уведомления в браузер
Содержание
Интернет магазин
Популярное
- О нас
- Правовые вопросы
- Политика
обработки персональных
данных EndoExpert.ru - Связаться с нами
- Стать партнером
© 2016-2022 EndoExpert.ru

Вы находитесь в разделе предназначенном только для специалистов (раздел для пациентов по ссылке). Пожалуйста, внимательно прочитайте полные условия использования и подтвердите, что Вы являетесь медицинским или фармацевтическим работником или студентом медицинского образовательного учреждения и подтверждаете своё понимание и согласие с тем, что применение рецептурных препаратов, обращение за той или иной медицинской услугой, равно как и ее выполнение, использование медицинских изделий, выбор метода профилактики, диагностики, лечения, медицинской реабилитации, равно как и их применение, возможны только после предварительной консультации со специалистом. Мы используем файлы cookie, чтобы предложить Вам лучший опыт взаимодействия. Файлы cookie позволяют адаптировать веб-сайты к вашим интересам и предпочтениям.
Я прочитал и настоящим принимаю вышеизложенное, хочу продолжить ознакомление с размещенной на данном сайте информацией для специалистов.
.jpg)







.png)


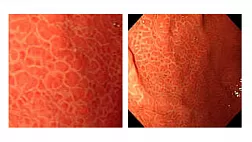
.jpg)
















Комментарии