- Компании
- Takeda. О компании, буклеты, каталоги, контакты
- Olympus. О компании, буклеты, каталоги, контакты
- Boston Scientific. О компании, буклеты, каталоги, контакты
- Pentax. О компании, буклеты, каталоги, контакты
- Fujifilm & R-Farm. О компании, буклеты, каталоги, контакты
- Erbe. О компании, буклеты, каталоги, контакты
- Еще каталоги
- Мероприятия
- Информация
- Обучение
- Дайджест
- QuaCol
- Разделы
- Пациентy
QR-код этой страницы

Для продолжения изучения на мобильном устройстве ПРОСКАНИРУЙТЕ QR-код с помощью спец. программы или фотокамеры мобильного устройства
Документы и приказы: Проект. Механическая желтуха неопухолевого генеза 2023-2024. Клинические рекомендации РОХ.
| Авторы: | РОХ |

Полный текст статьи:
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ
РОССИЙСКОЙ ФЕДЕРАЦИИ
Клинические рекомендации
Механическая желтуха
неопухолевого генеза
Возрастная группа: Взрослая (старше 16 лет)
Кодирование по МКБ 10: В66/ В67/ В67.5/ В77/ С22.0/ С22.1/ С23/ С24.0/ С24.8/
С25/ К80/ К80.3/К80.4/ К80.5/ К83.0/ К83.1/ К83.3/К83.5/ К91.5/ Q44
Год утверждения (частота пересмотра): 202 г. (пересмотр каждые 5 лет)
ID
URL
Разработчик клинических рекомендаций: Общероссийская общественная организация «Российское общество хирургов»
Утверждены Согласованы Российским обществом хирургов Научным советом Министерства на XV съезде хирургов России здравоохранения Российской федерации 25 октября 2023г. «____» ______________202 г.
ОГЛАВЛЕНИЕ …………………………………………………………………………………..
CПИСОК СОКРАЩЕНИЙ ……………………………………………………….…………..
ТЕРМИНЫ И ОПРЕДЕЛЕНИЯ………………………………………………………………
1.КРАТКАЯИНФОРМАЦИЯПОЗАБОЛЕВАНИЮ…………...……..………….....………..
1.1. ОПРЕДЕЛЕНИЕ ЗАБОЛЕВАНИЯ ……………………………,……..................
1.2. ЭТИОЛОГИЯ И ПАТОГЕНЕЗ ЗАБОЛЕВАНИЯ …………………….………......
1.3. ЭПИДЕМИОЛОГИЯ ЗАБОЛЕВАНИЯ …………………………………………
1.4. ОСОБЕННОСТИ КОДИРОВАНИЯ ЗАБОЛЕВАНИЯПО МЕЖДУНАРОДНОЙ
СТАТИСТИЧЕСКОЙКЛАССИФИКАЦИИБОЛЕЗНЕЙ И ПРОБЛЕМ,
СВЯЗАННЫХ СО ЗДОРОВЬЕМ……….………………………………………………
1.5. КЛАССИФИКАЦИЯ ЗАБОЛЕВАНИЯ …………….……………………………………
1.6. КЛИНИЧЕСКАЯ КАРТИНА ЗАБОЛЕВАНИЯ …………………………………………
2. ДИАГНОСТИКА ЗАБОЛЕВАНИЯ. МЕДИЦИНСКИЕ ПОКАЗАНИЯ
И ПРОТИВОПОКАЗАНИЯ К ПРИМЕНЕНИЮ МЕТОДОВ ДИАГНОСТИК…………….
2.1. ЖАЛОБЫ И АНАМНЕЗ…………………………………………………...…………
2.2. ФИЗИКАЛЬНОЕ ОБСЛЕДОВАНИЕ……………………………………………..…
2.3. ЛАБОРАТОРНЫЕМЕТОДЫ ДИАГНОСТИКИ ………………………………........
2.4. ИНСТРУМЕНТАЛЬНЫЕ МЕТОДЫ ДИАГНОСТИКИ ……………………………
3. ЛЕЧЕНИЕ, ВКЛЮЧАЯ МЕДИКАМЕНТОЗНУЮ И НЕМЕДИКАМЕНТОЗНУЮ
ТЕРАПИИ, ДИЕТОТЕРАПИЮ, ОБЕЗБОЛИВАНИЕ, МЕДИЦИНСКИЕ ПОКАЗАНИЯ
И ПРОТИВОПОКАЗАНИЯ К ПРИМЕНЕНИЮ МЕТОДОВ ЛЕЧЕНИЯ………………...
4. МЕДИЦИНСКАЯ РЕАБИЛИТАЦИЯ И САНАТОРНО-КУРОРТНОЕ ЛЕЧЕНИЕ,
МЕДИЦИНСКИЕ ПОКАЗАНИЯ И ПРОТИВОПОКАЗАНИЯ К ПРИМЕНЕНИЮМЕТОДОВ МЕДИЦИНСКОЙ РЕАБИЛИТАЦИИ, В ТОМ ЧИСЛЕОСНОВАННЫХ НА ИСПОЛЬЗОВАНИИ ПРИРОДНЫХ ЛЕЧЕБНЫХ ФАКТОРОВ…………………………………………………………………………………….
5. ПРОФИЛАКТИКА И ДИСПАНСЕРНОЕ НАБЛЮДЕНИЕ, МЕДИЦИНСКИЕ
ПОКАЗАНИЯ И ПРОТИВОПОКАЗАНИЯ К ПРИМЕНЕНИЮ МЕТОДОВ ПРОФИЛАКТИКИ…...………………………………………………………………………......
6. ОРГАНИЗАЦИЯ ОКАЗАНИЯ МЕДИЦИНСКОЙ ПОМОЩИ……………………………
7.ДОПОЛНИТЕЛЬНАЯ ИНФОРМАЦИЯ (В ТОМ ЧИСЛЕ ФАКТОРЫ, ВЛИЯЮЩИЕ НА ИСХОД ЗАБОЛЕВАНИЯ ИЛИ СОСТОЯНИЯ)……………………………………………….
КРИТЕРИИ ОЦЕНКИ КАЧЕСТВА МЕДИЦИНСКОЙ ПОМОЩИ……………………..........
СПИСОК ЛИТЕРАТУРЫ …………………………………………………………………...
ПРИЛОЖЕНИЕ А1. СОСТАВ РАБОЧЕЙ ГРУППЫ ПО РАЗРАБОТКЕ И
ПЕРЕСМОТРУ КЛИНИЧЕСКИХ РЕКОМЕНДАЦИЙ……………………………………
ПРИЛОЖЕНИЕ А2. МЕТОДОЛОГИЯ РАЗРАБОТКИ КЛИНИЧЕСКИХ РЕКОМЕНДАЦИЙ……………………………………………………………………………..
ПРИЛОЖЕНИЕ А3. СПРАВОЧНЫЕ МАТЕРИАЛЫ, ВКЛЮЧАЯ СООТВЕТСТВИЕ
ПОКАЗАНИЙ К ПРИМЕНЕНИЮ И ПРОТИВОПОКАЗАНИЙ, СПОСОБОВ ПРИМЕНЕНИЯИ ДОЗ ЛЕКАРСТВЕННЫХ ПРЕПАРАТОВ, ИНСТРУКЦИИ ПО ПРИМЕНЕНИЮЛЕКАРСТВЕННЫХ ПРЕПАРАТОВ……………….……………...……...
ПРИЛОЖЕНИЕ Б.АЛГОРИТМЫ ДЕЙСТВИЙ ВРАЧА…………………….……….........
ПРИЛОЖЕНИЕ В. ИНФОРМАЦИЯ ДЛЯ ПАЦИЕНТА……………………...……………..
ПРИЛОЖЕНИЕ Г1-Г4. ШКАЛЫ ОЦЕНКИ, ВОПРОСНИКИ И ДРУГИЕ ОЦЕНОЧНЫЕ
ИНСТРУМЕНТЫ СОСТОЯНИЯ ПАЦИЕНТА, ПРИВЕДЕННЫЕ В КЛИНИЧЕСКИХ
РЕКОМЕНДАЦИЯХ……………………………………………………………….…………..
III. Список сокращений
АЛТ – аланинаминотрансфеназа
АСТ –аспартатаминотрансфераза
БСДК - большой сосочек двенадцатиперстной кишки
ГГТП – гамма-глутамилтранспептидаза
ДПК - двенадцатиперстная кишка
ЖВП – желчевыводящие протоки
ЖКБ – желчнокаменная болезнь
КТ – компьютерная томография
ЛХЭ – лапароскопическая холецистэктомия
МЖ – механическая желтуха (синоним – обтурационная желтуха)
МИТ – мини-инвазивные технологии
МРТ – магнитно-резонансная томография
МРХПГ – магнитно-резонансная холангиопанкреатография
МСКТ – мультиспиральная компьютерная томография
ОЖП – общий жёлчный проток
ОПП – общий печёночный проток
ППЖ – проток поджелудочной железы
УЗИ – ультразвуковое исследование
ХС – холедохоскопия
ХЭ – холецистэктомия
ЧЧХГ – чрескожная чреспечёночная холангиография
ЧЧХС – чрескожная чреспечёночная холангиостомия
ЩФ – щелочная фосфатаза
Эндо-УЗИ – эндоскопическое ультразвуковое исследование
ЭПСТ – эндоскопическая папиллосфинктеротомия
ЭРХПГ – эндоскопическая ретроградная холангиопанкреатография
ЭГДС – эзофагогастродуоденоскопия
_____________________________________
[1] Примечание: гепат(о) – относящийся к печени;
гепатико – относящийся к печеночному протоку.
панкреат(о) – относящийся к поджелудочной железе;
панкреатико – относящийся к протоку поджелудочной железы;
холедохо – относящийся к общему жёлчному протоку [1].
IV. Термины и определения
Билиарная гипертензия– повышение давления в желчевыводящих путях, обусловленное каким-либо препятствием оттоку желчи.
Гепатиколитиаз – наличие конкрементов в общем печеночном протоке.
Холангиолитиаз – наличие камней в жёлчных протоках без уточнения анатомической локализации.
Холедохолитиаз– наличие камней в общем жёлчном протоке.
Дистальный блок – нарушение оттока желчи на уровне ниже места слияния (конфлюенса) пузырного и общего печеночного протоков.
Проксимальный блок – нарушение оттока желчи на уровне выше места слияния (конфлюенса) пузырного и общего печеночного протоков.
Острый холангит – острое воспаление жёлчных протоков вследствие проникновения в них инфекции
Острый холецистит– острое воспаление желчного пузыря.
Острый панкреатит– острое воспаление поджелудочной железы.
Холангиогенный сепсис – сепсис, источником которого является воспалительный процесс в желчных протоках.
Острая печёночная недостаточность– любой, быстро развившийся эпизод дисфункции печени, характеризующийся стремительно нарастающим ухудшением биохимических показателей функции печении и может сопровождаться дисфункцией других органов.
V. Краткая информация по заболеванию или состоянию (группе заболеваний или состояний)
1.1. Определение заболевания или состояния (группы заболеваний или состояний).
Механическая желтуха (МЖ, синдром механической желтухи, обтурационная желтуха) – угрожающее жизни состояние, развивающееся вследствие нарушения естественного пассажа желчи из печени по внутри- и внепечёночным желчным протокам в двенадцатиперстную кишку, проявляющееся комплексом симптомов, возникающее вследствие ЖКБ и ее осложнений, осложнений хирургических операций и других доброкачественных заболеваний органов гепатопанкреатобилиарной области, осложнений хирургических операций.
1.2. Этиология и патогенез заболевания или состояния (группы заболеваний или состояний)
По этиологическому принципу причины МЖ могут быть объединены в две основные группы: МЖ неопухолевого генеза (60%) и МЖ опухолевого генеза (20%) [1, 14, 81].
1.2.1 Механическая желтуха неопухолевого генеза: ЖКБ, осложнённая холедохолитиазом, стриктуры желчных протоков, стеноз БСДК.
1.2.2 Воспалительные заболевания: острый холецистит, холангит, панкреатит (острый или хронический), киста головки поджелудочной железы, стеноз БСДК.
1.2.3 Паразитарные заболевания печени и жёлчных протоков: описторхоз, аскаридоз, эхинококкоз, альвеококкоз.
1.2.4 Пороки развития: кисты желчных протоков, парапапиллярный дивертикул и др.
Начальным отделом внутрипеченочной части желчевыводящей системы являются межклеточные желчные капилляры (канальцы), в которые гепатоцитами выделяются компоненты желчи. Из канальцев образуются междольковые, затем сегментарные, долевые, правый и левый печеночные протоки.
В области ворот печени последние сливаются в общий печеночный проток, в который ниже впадает пузырный проток – образуется общий желчный проток (ОЖП), по которому жёлчь поступает в ДПК.
Возникновение МЖ всегда обусловлено нарушением поступления жёлчи в ДПК, жёлчной гипертензией и нарушением пигментного обмена – билирубина. Билирубин образуется из гемоглобина поврежденных (погибших) эритроцитов в ретикуло-эндотелиальной системе – преимущественно в печеночных макрофагах (клетках Купфера) и в меньшей степени в селезенке и костном мозге. Это токсичная и не растворимая в воде непрямая фракция пигмента (несвязанный билирубин, непрямой). Из плазмы крови печеночных капилляров (синусоидов) непрямой билирубин (несвязанный билирубин) поступает в гепатоциты через кровяной полюс клетки.
В гепатоцитах непрямой билирубин связывается с глюкуроновой кислотой благодаря чему превращается в нетоксичный прямой билирубин (связанный билирубин). Последний через жёлчный полюс гепатоцита поступает в желчные канальцы и в конечном итоге в ДПК [1].
При жёлчной гипертензии подавляется секреция билирубина гепатоцитами (холестаз) и расширяются желчные протоки. Желчь при высокой гипертензии диффундирует через эндотелиальные клетки в венозное и лимфатическое русло, где накапливается прямой билирубин, возникает гипербилирубинемия [1, 84].
При отсутствии жёлчи в кишечнике (ахолия) нарушается пищеварение, происходит транслокация бактерий и эндотоксинов из кишечника в кровь воротной вены.
Часто отмечается стеаторрея к соответствующей клинической симптоматикой эндотоксикоза различной степени тяжести. Развивается микрососудистый тромбоз в почках с констрикцией их резистивных сосудов и нарастанием функциональных нарушений, приводящий к гепато-ренальному синдрому, нарастанию уровня мочевины и креатинина в крови, нарушается белковосинтетическая и антитоксическая функция печени, возникают нарушения в системе гемостаза.Эндотоксины проникают через гематоэнцефалический барьер, что проявляется печёночной энцефалопатией.
1.3. Эпидемиология заболевания или состояния (группы заболеваний или состояний).
В Российской федерации ЖКБ страдают примерно 30% лиц старше 70 лет. Опухолевая МЖ может встречаться у лиц моложе 50 – 60 лет. Паразитарные заболевания, которые являются причиной МЖ, чаще встречаются в эндемичных регионах - Сибири, Дальнем востоке, среднеазиатских республиках и в регионах Северного Кавказа [6, 12, 16, 18, 20, 21, 22, 75].
K80.3 – Камни желчного протока с холангитом
K80.4 – Камни желчного протока с холециститом
K80.5 – Камни желчного протока без холангита или холецистита
K83.0 – Холангит
K83.1 – Закупорка желчного протока
1.5. Классификация заболевания или состояния (группы заболеваний или состояний).
§ По уровню блока желчных протоков:
«Высокий» блок – выше места впадения пузырного протока в общий печёночный проток.
«Низкий» блок – ниже места впадения пузырного протока в ОЖП [85].
§ По уровню гипербилирубинемии: лёгкой степени тяжести – до 85 мкмоль/л; средней степени тяжести – 86-169 мкмоль/л; тяжёлой степени тяжести – выше 170 мкмоль/л.
§ Для оценки тяжести МЖ рекомендуется классификацию Гальперина Э.И., 2014. (приложение Г4).
а) Легкая степень (Класс А) - ≤ 5 баллов
б) Средняя (класс В) – 6-15 баллов
в) Тяжелая (класс С) - ˃ 16 баллов
§ Осложнения МЖ: острый холангит, печёночная недостаточность, печеночно-почечная недостаточность, тромбо-геморрагический синдром, апостематоз печени, абсцессы печени [14, 15, 115].
(УУР – С; УДД - 5)
1.6. Клиническая картина заболевания или состояния (группы заболеваний или состояний).
Основные задачи диагностики – установление механического характера желтухи, определение причины нарушения проходимости ЖВП, уровня блока и степени тяжести МЖ.
Поскольку желтуха является не самостоятельной нозологической формой, а синдромом, характерным для ряда заболеваний, то выбор рационального алгоритма диагностических методов затруднен.
Для постановки диагноза желтухи в большинстве случаев бывает достаточно анамнеза и физикального осмотра. Желтуха, вызванная конкрементами общего жёлчного протока (холедохолитиазом), обычно бывает быстро нарастающей, транзиторной, связанной с болью, иногда сопровождается лихорадкой (холангитом – воспалением желчных протоков). Медленное и постепенное начало желтухи без боли (нередко с потерей массы тела) может свидетельствовать о злокачественном новообразовании. Желтуха, возникающая после холецистэктомии (удаления желчного пузыря), предположительно является следствием оставшихся жёлчных камней в протоках (резидуального холедохолитиаза) или повреждения жёлчного протока.
VI. Диагностика заболевания или состояния (группы заболеваний или состояний), медицинские показания и противопоказания к применению методов диагностики.
У пациента с желтухой рекомендуется выполнить анализ жалоб, анамнеза заболевания и анамнеза жизни на этапе поступления в стационар. Сведения из жалоб и анамнеза, физикальное и лабораторное обследование позволяют заподозрить механический характер желтухи примерно у 80% пациентов [1, 9, 17, 26].
Пациенты предъявляют жалобы на боли в животе, желтушность склер и кожных покровов, кожный зуд; повышение температуры тела при наличии воспалительных процессов, общую слабость, выделение тёмной мочи и светлого кала, металлический привкус во рту.
Как правило, при наличии ЖКБ в анамнезе, пациенты отмечают характерные приступы болей в правом подреберье по типу печёночных колик: при погрешностях в диете (употребление алкоголя, жирной, жареной пищи, лекарственных препаратов).
Кожный зуд обусловлен раздражением кожных рецепторов солями желчных кислот, а при холедохолитиазе может возникать до развития внешних признаков МЖ. Он значительно ухудшает качество жизни больных, не дает им покоя, вызывает бессонницу и повышенную раздражительность, часто приводит к многочисленным расчёсам, следы которых видны на коже.
Характерным признаком МЖ неопухолевого генеза является возникновение в начале заболевания резкого болевого приступа в правом подреберье или в зоне Шоффара (чуть правее и выше пупка), боли иррадиируют в поясницу, шею, в правое плечо и область сердца (возможно развитие холецисто-кардиального синдрома).
При ЖКБ механическая желтуха, как правило, обусловлена холедохолитиазом. Характерный для неё симптомокомплекс складывается из интенсивных болей в правом подреберье или эпигастрии, желтушности кожи, склер и слизистых оболочек, возникающих спустя 12-24 часа после приступа болей, с обесцвечиванием кала и потемнением мочи. При полной обтурации просвета ОЖП желтуха быстро нарастает. Когда обтурация не полная или возникает т.н."вентильный" механизм нарушения оттока жёлчи, МЖ носит ремитирующий характер [1, 2, 29, 85].
Предположить острый холангит можно по наличию болей в правом подреберье, лихорадки с ознобом и МЖ (триада Шарко).
(УУР – В; УДД - 5)
Пациенту с признаками желтухи рекомендуется провести обследование при поступлении, включающее оценку всех основных систем организма. При внешнем осмотре больного выявляют иктеричность склер и кожных покровов, следы расчёсов на теле.
У ранее оперированных пациентов имеются послеоперационные рубцы на передней брюшной стенке. Длительно существующая МЖ приводит к нарушениям в системе гомеостаза. Клиническими проявлениями этого тяжёлого осложнения являются кожные гематомы в местах минимальных травм и инъекций, геморрагическая сыпь, возможны холемические кровотечения. При острых воспалительных процессах в органах гепатопанкреатобилиарной зоны (например, при остром холецистите, холангите, осложненных МЖ), отмечается высокая температура тела. При подобных состояниях - брюшная стенка не участвует в акте дыхания, пальпаторно живот болезненный, а при деструктивных формах воспаления желчного пузыря отмечается локальное напряжение в правом подреберье. Там же, в ряде случаев, удается пальпировать увеличенный, напряжённый и резко болезненный жёлчный пузырь. Выявляются положительные симптомы Ортнера-Грекова, Мерфи, Кера, Мюсси-Георгиевского (френикус-симптом) [2, 98].
В то же время, при медленном нарастании безболевой МЖ можно пропальпировать увеличенный безболезненный жёлчный пузырь – синдром Курвуазье, что свидетельствует о низком опухолевом блоке ЖВП.
(УУР – С; УДД - 5)
3. Лабораторные методы диагностики
Основные задачи лабораторной диагностики – определение вероятной причины и уровня гипербилирубинемии, выраженности синдрома холестаза – цитолиза, тяжести поражения печени, почек, других органов, нарушений в системе гемостаза. Важно выявить лабораторные признаки системного воспалительного ответа.
В качестве обязательных исследований рекомендуются: общий анализ крови, общий анализ мочи, биохимический анализ крови с определением билирубина и его фракций (амилазы, трансаминаз (АЛТ, АСТ), щелочной фосфатазы, ГГТП, глюкозы, мочевины, креатинина), группа крови, резус-фактор, коагулограмма.
(УУР – С; УДД – 3а)
Комментарии: в общем анализе крови при воспалительной природе желтухе имеет место лейкоцитоз, высокое содержание палочкоядерных нейтрофилов, повышенный уровень С-реактивного белка, увеличение СОЭ, при интоксикации возможна анемия.
В биохимических анализах крови отмечается увеличение концентрации прямого и непрямого билирубина за счёт прямой, а при её длительном существовании, и непрямой фракции. Концентрация билирубина может достигать высоких цифр – до 850 мкмоль/л и выше, однако если обтурация неполная, его уровень часто не превышает 100 мкмоль/л. [1-6]. Повышается уровень щелочной фосфатазы (ЩФ), при длительной желтухе наблюдается умеренное повышение активности аланинаминотрансфеназы (АЛТ) и аспартатаминотрансферазы (АСТ). Иногда, для дифференциальной диагностики острого гепатита, вычисляется коэффициент Де Ритиса (отношение АСТ/АЛТ), снижение которого ниже 1,0 характерно для вирусного гепатита. Менее информативно увеличение содержания в сыворотке крови желчных кислот, холестерина, липопротеинов, триглицеридов. У ряда больных имеет место повышение активности гамма-глютамилтрансферазы (ГГТП). Содержание фермента увеличивается при поражении печени, его повышенная активность указывает на наличие холестаза, поэтому при МЖ она резко увеличивается и достигает 20 кратного превышения нормы, особенно это характерно при раковом характере желтухи или присоединении гнойного холангита. Содержание креатинина сохраняется на нормальных показателях, при развитии почечной недостаточности возникает повышение его активности [6, 7]. При изучении кислотно-щелочного состояния, величина электролитов крови зависят от степени печеночной и полиорганной недостаточности.
В качестве дополнительных исследований рекомендуются: при паразитарной обтурации ЖВП определение количества эозинофилов в крови, выполнение иммуноферментного анализа (ИФА) и молекулярно-биологического обследования (методом ПЦР) [76, 77].
(УУР – В; УДД – 1с)
Для выяснения этиологической роли аскаридоза в развитии природы механической желтухи рекомендуется, помимо стандартных исследований, использовать:
a) гемограмма: эозинофилия, умеренный лейкоцитоз;
b) обнаружение яиц A.lumbricoideus при копроскопии.
(УУР – С; УДД – 3а)
Комментарии: Феномены при диагностике билиарного аскаридоза представлены в таблице см. Приложение Г1[11].
При подозрении на описторхозную этиологию МЖ рекомендуется использовать клинические, иммунологические, паразитологические и молекулярно-биологические методы диагностики
(УУР – В; УДД – 1c)
Комментарии: Указание на описторхозную инвазию может дать исследование крови (эозинофилия) или иммуноферментный анализ, позволяющий выявлять антитела IgM и IgG. Достоверный диагноз устанавливается только после паразитологического анализа, основанного на нахождения яиц описторхов или их биологических фрагментов в дуоденальном содержимом или в испражнениях. Это становится возможным только на 3-4 недели заболевания, или молекулярно-биологического обследования (методом ПЦР-амплификации), позволяющего дифференцировать вид возбудителя [8, 11-14].
С целью дифференциальной диагностики МЖ и скрининга социально-значимых болезней всем пациентам рекомендуется исследование маркеров гепатита (IgM анти-HAV, IgM анти-HEV, HBsAg, Anti-HBs, анти-HCV, анти-HCV IgG) [78] (Приложение Б).
(УУР – С; УДД - 5)
4. Инструментальные методы исследования
В качестве обязательных исследований рекомендуются: ЭКГ, УЗИ брюшной полости, гепатобилиарной области, рентгенография органов брюшной полости и грудной клетки. [30]
(УУР – С; УДД – 3а)
Комментарии. УЗИ органов брюшной полости – первоочередной скрининговый метод обследования пациентов с желтухой. Диагноз МЖ основывают на визуализации расширенных внепеченочных (более 10мм) или внутрипеченочных (более 4мм) жёлчных протоков (чувствительность метода – 87%, специфичность – 99%). УЗИ также дает достаточно точные данные при идентификации желчных камней, определении размеров печени, жёлчного пузыря, поджелудочной железы, хотя визуализация дистального отдела ОЖП и поджелудочной железы может быть недостаточной. Отсутствие дилатации жёлчного протока при УЗИ зачастую исключает обтурацию, кроме редких случаев [62]\
Чрескожное УЗИ, позволяет выявить расширение жёлчных протоков и уровень блока ЖВП и своевременно провести декомпрессию билиарного тракта. Чувствительность УЗИ при ЖКБ – 98%-99%, при опухолях – 64-70%. [10-12].
В качестве дополнительных исследований рекомендуются: ЭГДС с осмотром БСДК, МРХПГ, Эндо-УЗИ, МСКТ [11, 24, 54, 80].
Для уточнения диагноза холангиолитиаза и уровня блока ЖВП после УЗИ рекомендуется выполнить МРХПГ и эндо-УЗИ. При подозрении на опухолевой процесс рекомендуется выполнить МСКТ [1, 81, 83].
МРХПГ рекомендуется во всех ситуациях, когда трансабдоминальное УЗИ не позволяет установить точный дооперационный диагноз причины и уровня блокады оттока желчи от печени при МЖ: для уточнения характера и уровня поражения ЖВП при наличии подозрений на склерозирующий холангит или стриктуры жёлчных путей; в качестве как метода выбора для оценки состояния ВЖП у пациентов с предшествующим формированием желудочно-кишечных и билиодигестивных анастомозов [33, 34, 92].
(УУР – В; УДД – 2b)
Комментарии: Результаты МРПХГ могут служить «дорожной картой» для последующего ЭРХПГ или реконструктивных вмешательств [7,8]. Следует помнить о возможном завышении протяженности стриктуры или блока желчных путей, так как количества желчи в зоне сужения или обструкции в естественных условиях не всегда достаточно для формирования сигнала и отражения анатомии протоковой системы [2].
При механической желтухе Эндо-УЗИ рекомендуется использовать при дистальном блоке, когда после применения УЗИ, ЭРХПГ, МРХПГ, МСКТ его причина остается неясной.
(УУР – В; УДД – 2b)
Комментарии: Метод демонстрирует высокую диагностическую эффективность при небольших опухолях головки поджелудочной железы, дистального отдела общего желчного протока, микрохоледохолитиазе и других малых поражениях. Эндо-УЗИ и МРТ ЖП для диагностики камней ВЖП являются высоко информативными методами, приоритет применения того или другого метода зависит от доступности его и наличия обученных специалистов [1-9, 13-16].
КТ или МСКТ как правило, дополняют УЗИ органов брюшной полости, что позволяет точнее определить уровень и характер билиарной обструкции. МСКТ (КТ) рекомендуется при незначительных изменениях печени и поджелудочной железы, а также для определения стадии онкологического заболевания, включая вовлечение в процесс сосудов периампулярными образованиями [59].
5. Иные диагностические исследования.
Эндоскопическая ретроградная холангиопанкреатография (ЭРХПГ), чрескожная чреспечёночная холангиография (ЧЧХГ) — не являются самостоятельными диагностическими процедурами, а рекомендуются только как этап хирургического лечения с применением МИТ [55, 56]. При наличии высокоинформативных неинвазивных методов диагностики МЖ: УЗИ, МРТ, КТ, эндоскопическое УЗИ (Эндо-УЗИ) выполнение ЭРХПГ и ЧЧХГ с диагностическими целями не рекомендуется
(УУР – В; УДД – 2b)
Комментарии: РХПГ может использоваться как метод визуализации при выполнении эндоскопических транспапиллярных вмешательств [7, 8, 10, 11].
При желтухе, сопровождаемой расширением жёлчных протоков и наличием конкрементов, обнаруженных с помощью инструментальных методов обследования, рекомендуется применение эндоскопических методов обследования и лечения. Чувствительность ЭРХПГ при обнаружении холедохолитиаза составляет около 90%, при этом есть возможность одновременной папиллосфинктеротомии (ЭПСТ) извлечения камней (литоэкстракция), либо стентирования ОЖП или ОПП [57,62].
Обнаружения расширенных жёлчных протоков при отсутствии жёлчных камней также требует более глубокого исследования. При неинформативности УЗИ и МРХРГ для выявления причины МЖ рекомендуется ЭРХПГ [102,103].
Для определения этиологии стриктуры, ее доброкачественного (вторичная, посттравматическая) или злокачественного характера (холангиокарцинома) рекомендуется браш–биопсия [31].
При проксимальном блоке (уровень ворот печени и выше) рекомендуется ЧЧХГ для определения дальнейшей тактики лечения или установки стента с целью декомпрессии ЖВП [70,71,74,124].
Выполнение чрескожной чреспеченочной холангиографии при описторхозе не рекомендуется
Комментарии: ЧЧХГ при описторхозе является чрезвычайно опасной из-за опасности повреждения холангиоэктазов и развития жёлчного перитонита [12, 13].
Лапароскопия в диагностике МЖ не рекомендуется
Комментарии: лапароскопия позволяет выявить лишь косвенные признаки МЖ: «малахитовый» цвет печени, ее увеличение и закругление края [1-3]. Биопсия новообразований печени, выявленных при лапароскопии, имеет ограниченное применение. Следует помнить о том, что при биопсии гемангиомы высока вероятность интенсивного не контролируемого кровотечения, а паразитарные заболевания в результате биопсии могут дать диссеминацию процесса.
Характер и тяжесть МЖ рекомендуется установить в течение 24 часов для правильной маршрутизации больного и оказания своевременной помощи.
(Приложение Г1, Г2)
Дифференциальную диагностику рекомендуется проводить с МЖ опухолевого генеза, паренхиматозной и гемолитической желтухами (Приложение Б) [23,25].
(УУР – С, УДД – 5)
VII. Лечение, включая медикаментозную и немедикаментозную терапии, диетотерапию, обезболивание, медицинские показания и противопоказания к применению методов лечения.
Пациентов с МЖ рекомендуется госпитализировать в экстренном порядке. Общие подходы в лечении пациентов с синдромом МЖ включают восстановление оттока жёлчи, ликвидацию жёлчной гипертензии, профилактику и лечение осложнений МЖ. Проводится комплексная консервативная терапия (параллельно с диагностическими мероприятиями), которая может служить и предоперационной подготовкой [1, 3, 5].
(УУР – C; УДД – 3a)
Комментарии: методы, объемы и сроки лечения определяются в зависимости от характера заболевания. Главная цель – максимально быстрая ликвидация желтухи, коррекция имеющихся нарушений органов и систем, профилактика послеоперационных осложнений.
Лечение пациентов при тяжелой МЖ рекомендуется проводить в отделении реанимации и интенсивной терапии до стабилизации их состояния, где проводят инфузионную, дезинтаксикационную, антибактериальную, антикоагулянтную, антисекреторную терапию и респираторную, нутритивную поддержку. Осуществляют лабораторный и инструментальный мониторинг для оценки тяжести состояния, выявления осложнений и наличия органной дисфункции. После стабилизации больной переводится в хирургическое отделение.
1. Консервативное лечение.
Консервативное лечение у больных МЖ рекомендуется осуществлять параллельно с диагностическими мероприятиями, оно должно быть непродолжительным и преследовать цель стабилизации общего состояния пациента путем снижения эндогенной интоксикации, нормализации системы гемостаза, другой органной дисфункции, подготовки к операции или минимально инвазивным методам билиарной декомпрессии и устранения МЖ.
Консервативное лечение рекомендуется проводить с учетом тяжести МЖ. Основными задачами инфузионной терапии являются: быстрое и эффективное восстановление центральной и периферической гемодинамики, коррекция реологических параметров крови и системы гемостаза, кислотно-щелочного и электролитного баланса, поддержание и восстановление репаративных процессов печеночной паренхимы, снижение эндогенной интоксикации, обеспечение нутритивной поддержки. С этой целью рекомендуется парентеральное введение жидкости в объеме 1,5-2 л/сут (5-10 мл/кг/сут) при поддержании диуреза 1,5-2 л/сут. Внутривенное введение 5-10% раствора глюкозы как энергетического субстрата для восстановления запаса гликогена в печении и улучшения ее детоксикационной функции. [38,39,40,41].
Для профилактики гипергидратации в течение суток, рекомендуется контролировать (лучше в мониторном режиме) содержание натрия в сыворотке крови, уровень гемоглобина и гематокритное число. [35,36]
Консервативная терапия при МЖ является важным вспомогательным видом лечения и не служит альтернативой декомпрессии ЖВП.
(УУР – С, УДД – 4)
1.1 Антибиотикотерапия
Назначать антибиотики рекомендуется по следующим показаниям:
1. Профилактика вероятных инфекционных осложнений
2. Наличие инфекции: холангит, острый холецистит, холангиогенные абсцессы, сепсис [51,52,53,96].
Комментарии: основной целью антибактериальной терапии у пациентов с МЖ, причинами которой являются острые воспалительные заболевания (острый холецистит, острый холангит, билиарный панкреатит), после восстановления адекватного пассажа жёлчи, является ограничение, как системного воспалительного ответа, так и локального воспаления, профилактика инфекционных осложнений. Одним из основных условий эффективности проводимого лечения, является восстановление проходимости ЖВП, особенно при остром гнойном холангите.
У всех пациентов с МЖ на фоне острой хирургической инфекции рекомендуется бактериологическое исследование жёлчи [43,45,46].
(УУР – A, УДД – 1a)
Комментарии: Для выявления возбудителей, посев желчи должен быть получен в начале любой выполняемой процедуры.
При выборе антибиотиков рекомендуется учитывать их фармакокинетику и фармакодинамику, возможность проникновения в ЖВП, функцию почек и печени, а также наличие аллергии и других побочных эффектов. Эмпирическая антибактериальная терапия проводится до тех пор, пока не будут получены результаты бактериологического исследования и определена чувствительность бактерий к антибиотикам, после этого терапия должна быть скорригирована. Терапия должна продолжаться до нормализации клинических и лабораторных показателей – ма́ркеров воспаления [44,49,50]
У пациентов с МЖ классов В и С рекомендуется использование следующих антибактериальных препаратов: ампициллин/сульбактам в качестве начальной терапии, если чувствительность предполагаемых возбудителей составляет более 80% к данному антибиотику в конкретном регионе с учетом микробиологического мониторинга (локальные данные). На основании этого, возможно использование следующих групп препаратов: цефалоспорины 2 поколения (цефокситин); цефалоспорины 3 поколения (цефтриаксон или цефотаксим + метронидазол или цефоперазон/сульбактам). Группа карбапенемов (эртапенем); группа фторхинолонов (ципрофлоксацин, левофлоксацин + метронидазол или моксифлоксацин).
(УУР – С, УДД – 4)
Для профилактики и лечения кровотечений из желудочно-кишечного тракта у всех больных при МЖ рекомендуется использовать ингибиторы протонной помпы, Н²-блокаторы гистамина и препараты, обволакивающие слизистую оболочку желудка, а также осуществлять полноценную сбалансированную нутритивную поддержку.
При наличии у пациента гнойного холангита и любой степени тяжести МЖ, декомпрессию рекомендуется выполнять в неотложном порядке в течение первых 6-8 часов с момента поступления в хирургический стационар. В остальных случаях, принять решение о декомпрессии жёлчных протоков при МЖ рекомендуется в течение 24 часов после поступления больного в стационар. При легкой степени МЖ декомпрессия может быть выполнена и в более поздние сроки - в течение 48-96 часов на фоне инфузионной терапии [37].
(УУР – С, УДД – 5)
1.2 Коррекцию нарушений в системе гемостаза при МЖ рекомендуется обсудить при подготовке к хирургическому лечению (мини-инвазивному, традиционному) при 2-х кратном увеличении МНО, гипофибриногенемии (˂1,5г/л), тромбоцитопении (<50.109 /л), протромбиновом индексе меньше 70%. Рекомендуется назначать препараты витамина К, ингибитор фибринолиза – транексамовая кислота, переливание тромбоцитарной массы, плазмы и криопреципитата.
1.3 Экстракорпоральные методы детоксикации – гемодиализ рекомендуется при острой почечной (печеночно-почечной )недостаточности (креатинин более 1,1 ммоль/л, мочевина ˃2г/л, калий - ˃ 6 ммоль/л).
При высоком уровне билирубина (˃300 ммоль/л) рекомендуется плазмосорбция и плазмофильтрация [83].
Решение о применении методов экстракорпоральной детоксикации принимается коллегиально на консилиуме.
(УУР – С, УДД – 5)
Лечение аскаридоза.
Консервативное лечение пациентов с аскаридозным холангитом направлено на то, чтобы вызвать паралич червей при пероральном введении противогельминтных препаратов с длительностью лечения 72 часа. Ее результативность оценивается клиническим осмотром и анализом функции печени. Успех консервативного лечения наблюдается в виде купирования желтухи, боли, лихорадки и исчезновения аскарид из желчных протоков. Эффективность такой лечебной технологии составляет 68%-80%. После купирования симптомов в течение 3 дней, рекомендуется назначение антигельминтных препаратов (пирантел, памоат, мебендазол и альбендазол) до тех пор, пока острые симптомы не будут устранены полностью. Спонтанный выход червей из желчных протоков рекомендуется контролировать посредством УЗИ [28].
Эндоскопическая экстракция рекомендуется пациентам, которые не реагируют на консервативное лечение, то есть у которых аскариды сохраняются в желчных протоках в течение 3х недель. Эндоскопическое извлечение червя из ампулярного отверстия БДС успешно может быть проведено у 90-100% пациентов.
Пациентам с аскаридозом не рекомендуется выполнение сфинктеротомии.
Комментарии: выполнение сфинктеротомии ведет у таких пациентов к рецидивирующему заражению билиарного дерева, облегчая прохождение аскарид через ампулу БДС [28].
2. Анестезиологическое пособие определяется исходя из тяжести состояния пациента, объема хирургического вмешательства, наличия у него коморбидных заболеваний. В качестве метода выбора анестезиологического пособия рекомендуется общая анестезия [1,96,97].
3. Хирургические методы лечения неопухолевой МЖ.
Хирургическая тактика определяется тяжестью состояния пациента, уровнем блока желчных протоков, тяжестью желтухи, наличием холангита
и других осложнений механической желтухи. Для выбора хирургической тактики лечения механической желтухи, рекомендуется использовать классификацию по степени ее тяжести, предложенную Э.И. Гальпериным.
Наиболее частой причиной развития билиарной гипертензии неопухолевого генеза является «низкий блок» желчных протоков [1,8,81]. При наличии у пациента гнойного холангита и любой степени тяжести механической желтухи рекомендуется выполнение декомпрессии в срочном порядке в течение первых 6-8 часов с момента поступления в хирургический стационар. В остальных случаях, принять решение о декомпрессии желчных протоков при механической желтухе рекомендуется в течение 24 часов после поступления больного в стационар.
В качестве операции выбора рекомендуется ретроградное эндоскопическое вмешательство на желчных протоках: ЭРХПГ, ЭПСТ, литоэкстракция, стентирование [1,3,5,7,10].
(УУР – С, УДД – 3a)
Комментарии: ЭРХПГ с ЭПСТ на протяжении многих лет остается основным методом эндоскопического лечения холедохолитиаза для ликвидации МЖ. Этот метод позволяет в 85-90% случаев удалить конкременты из общего желчного протока и восстановить желчеотток. Эта процедура возможна даже у пациентов старших возрастных групп с тяжелыми сопутствующими заболеваниями [5, 8-10].
Механическая литотрипсия. В случае наличия крупных конкрементов в холедохе (размером более 10 мм), перед извлечением их рекомендуется фрагментировать.
Комментарии: механическая литотрипсия выполняется при наличии «сложных» конкрементов или в сложных клинических ситуациях при МЖ.. Эффективность механической литотрипсии достигает 80–90% [19].
Показания к выполнению механической литотрипсии при МЖ:
1) Наличие конкремента, размеры которого превышают устье терминального отдела холедоха после ЭПСТ;
2) Холедохолитиаз при стенозе терминального отдела холедоха;
3) Наличие парапапиллярного дивертикула, ограничивающего протяженность рассечения большого дуоденального соска;
4) Расположение камня выше рубцовой стриктуры холедоха или опухолевого стеноза, у пациентов с высоким риском или не подлежащих хирургическому лечению.
Противопоказания кмеханической литотрипсии при МЖ :
1) Наличие острогопанкреатита, холецистита;
2) Тяжелые формы коагулопатии;
3) Камень, когда его размер превышает диаметр корзиныдля литотрипсии;
4) Выраженная дилатация холедоха, требующая наложения билиодигестивного анастомоза для адекватного дренирования.
Механическая литоэкстракция. Для удаления желчных конкрементов из протоков рекомендуется использовать баллонные (типа Фогарти) и корзинчатые (типа Дормиа) экстракторы.
Баллонные экстракторы рекомендуется использовать:
1) при наличии большого количества мелких конкрементов;
2) для контроля окончательной санации желчных протоков;
3) для получения «окклюзионной» холангиографии (при контрольном контрастировании холедоха после ЭПСТ и лечебных манипуляций) [31-33].
Лазерная литотрипсия. Эффективность этого способа интракорпорального разрушения камней составляет 87–95%. Преимуществом лазерного разрушения камней является очень малый размер осколков, что позволяет им спонтанно покидать проток. К отрицательным качествам относятся большие затраты времени, высокая стоимость используемого оборудования и увеличение состава оперирующей бригады.
Эндоскопическая интракорпоральная литотрипсия является достаточно эффективным способом разрушения камней, не поддающихся обычной литоэкстракции [1-5, 7].
В случае наличия крупных конкрементов в холедохе (размером более 10 мм) перед извлечением их рекомендуется фрагментировать [ 1,5,20].
(УУР – С, УДД – 3a)
Комментарии: механическая литотрипсия выполняется при наличии «сложных» конкрементов или в сложных клинических ситуациях при МЖ.. Эффективность механической литотрипсии достигает 80–90% [19].
При невозможности эндоскопической холедохолитоэкстракции рекомендуется установка билиодуоденального пластикового стента (одного или нескольких). При наличии у пациента гнойного холангита рекомендуется установка наружного назобилиарного дренажа.
Декомпрессия желчных протоков рекомендуется пациентам с «высоким блоком» при механической желтухе средней и высокой степени тяжести. При механической желтухой лёгкой степени, отсутствии явлений холангита и «высоким блоком» экстренная билиарная декомпрессия не рекомендуется.
Наиболее частой причиной развития билиарной гипертензии неопухолевого генеза является «низкий блок» желчных протоков. В этом случае в качестве операции выбора рекомендуется ретроградное эндоскопическое вмешательство на желчных протоках - ЭРХПГ, ПСТ. При невозможности эндоскопической холедохолитоэкстракции рекомендуется установка билиодуоденального пластикового стента (одного или нескольких).
При риске развития (травматичная ЭПСТ) постманипуляционного острого панкреатита либо при его возникновении после ретроградного вмешательства — рекомендуется установка пластикового стента (5-7 Fr) в ППЖ на глубину 5–7 см [105].
В случае «проксимального блока» жёлчных протоков рекомендуется использование ретроградного стентирования, либо чрескожного чреспеченочного антеградного дренирования (стентирования) жёлчных протоков под ультразвуковым и рентгенконтролем (ЧЧХГ, ЧЧХС). При технической возможности рекомендуется проведение дренажа ниже уровня стриктуры [27,28,81,106,124]. При наличии после декомпрессии длительно существующего наружного жёлчного свища, рекомендуется возвращение больному потерь жёлчи per os, назначение ферментных препаратов.
С целью декомпрессии желчных протоков, по показаниям, рекомендуется стентирование желчных протоков пластиковыми, либо только покрытыми нитиноловыми стентами. Пластиковые стенты рекомендуются при наличии протяжённой стриктуры терминального отдела ОЖП, крупном и множественном неразрешённом холедохолитиазе, гнойном холангите [111,112,113,117].
(УУР – A, УДД – 1a)
Декомпрессия «покрытым» нитиноловым стентом рекомендуется при стриктуре желчного протока и невозможности выполнения плановой реконструктивной или восстановительной операции из-за тяжелых коморбидных заболеваний.
Применение «непокрытых» нитиноловых стентов при механической желтухе неопухолевого генеза не рекомендуется [82,83,91,94,101,124].
Комбинированные методы дренирования желчевыводящих протоков (Рандеву-технология и др.) позволяют значительно расширить лечебные возможности транспапиллярных вмешательств и рекомендуются у пациентов с МЖ при сложных анатомических вариантах: атипичном положении БСДК, расположении БСДК в дивертикуле, нарушенной анатомии после операции [89, 93].
Дренирование жёлчного пузыря под лапароскопическим или ультразвуковым контролем для лечения МЖ неопухолевого генеза в настоящее время рекомендуется только при наличии у больного явлений острого холецистита или невозможности применения другого способа декомпрессии при дистальном блоке, застойном жёлчным пузыре с проходимым пузырным протоком [65,6,69,83,107,114].
Лечение пациентов рекомендуется продолжить в отделении реанимации и интенсивной терапии до стабилизации их состояния
с последующим переводом в профильные хирургические отделения.
В послеоперационном периоде проводится инфузионная терапия, респираторная поддержка, антибактериальная, антикоагулянтная
и антисекреторная терапия, нутритивная поддержка. По показаниям проводится лабораторный и инструментальный мониторинг для оценки состояния и выявления осложнений.
При невозможности выполнения декомпрессии желчных протоков по технической либо иной причине на II уровне оказания квалифицированной помощи рекомендуется перевести больного в стационар III-го уровня.
(УУР – С, УДД – 3a)
Комментарии: эндоскопические транспапиллярные вмешательства при МЖ выполняются в экстренном, отсроченном и плановом порядке. Они могут быть, как этапом хирургического лечения, так и самостоятельными методами восстановления желчеоттока, становясь альтернативой оперативному вмешательству [6]. Именно в специализированных стационарах многопрофильных больниц имеется достаточное оснащение и опытные специалисты, выполняющие не менее 40-50 процедур в год, способные обеспечить высокую эффективность и низкий уровень осложнений после ЭРХПГ.
При наличии показаний к выполнению плановой реконструктивно-восстановительной операции, после декомпрессии жёлчных протоков больного рекомендуется направить в стационар III-го уровня специализированной помощи.
Вопрос выполнения холецистэктомии после успешного разрешения явлений МЖ на фоне холедохолитиаза решается индивидуально в зависимости от конкретной ситуации: рекомендуется выполнение сочетанной операции (одновременной) – эндоскопической литэкстракции, затем лапароскопической холецистэктомии, либо выполнение холецистэктомии в ближайшие 72 часа или в плановом порядке. Принятие решения о выполнении холецистэктомии в течении одной госпитализации решается индивидуально на междисциплинарном консилиуме.
Всем пациентам при паразитарных МЖ в качестве первого этапа хирургического лечения рекомендуется билиарная декомпрессия. Эндоскопическая экстракция паразитов показана пациентам, которые не реагируют на консервативное лечение, то есть у которых аскариды сохраняются в желчных протоках в течение 3х недель.
Основными показаниями к операции являются: неудачи эндоскопического лечения; расположение аскарид во внутрипеченочных желчных протоках.
Хирургическое лечение включает в себя холецистэктомию (открытую или лапароскопическую), ревизию желчных протоков, удаления камней и аскарид из желчных протоков. В зависимости от ситуации рекомендуется наружное дренирование ОЖП либо формирование билиодигестивного анастомоза [64,67].
Всем пациентам при эхинококкозе печени, осложнённом МЖ, рекомендуется лечение, направленное на обеспечение нормального пассажа желчи в кишечник и воздействие на эхинококковую кисту. После купирования желтухи рекомендуется решить вопрос о лечении заболевания в соответствии с рекомендациями рабочей группы ВОЗ (World Health Organization-Informal Working Group on Echinococcosis (WHO-IWGE). Противорецидивная терапия показана после любого вида оперативноголечения эхинококкоза [22,123].
В случае возникновения жизнеугрожающего осложнения (абсцесс печени) рекомендуется разрешение ситуации путём выполнения билиарной декомпрессии, наружного дренирования гнойного очага с применением мини-инвазивных технологий. После купирования желтухи рекомендуется решить вопрос о возможности радикального или паллиативного вмешательства.
В качестве основных способов декомпрессии при неопухолевой МЖ рекомендуются минимально-инвазивные – ретроградные эндоскопические (ЭРХПГ, ЭПСТ, литэкстракция, стентирование, назобилиарное дренирование) и антеградные чрескожные (ЧЧХС, литэкстракция, стентирование).
При невозможности выполнить декомпрессию в конкретном стационаре 2-го уровня, рекомендуется пациента немедленно направить в стационар 3-го уровня (специализированное лечебное учреждение).
Если пациенту предполагается радикальное хирургическое вмешательство и уровень билирубина менее 80-100 ммоль/л, декомпрессия не рекомендуется [83,86,87,88].
(УУР – С, УДД – 5)
В зависимости от опыта специалиста, оснащённости стационара, характера заболевания, при остром деструктивном холецистите с МЖ в качестве метода выбора рекомендуется лапароскопическая холецистэктомия с одновременным вмешательством на протоках.
(УУР – В, УДД – 4)
При МЖ рекомендуется ограничить употребление мяса, рыбы, жирной и острой пищи. Важно обильное питье, употребление обезжиренного молока, фруктов и овощей.
С целью поддерживающей терапии по показаниям целесообразно принимать гепатопротекторы, витамины и пищеварительные ферменты. (Приложение В)
(УУР – А, УДД – 2)
Трансабдоминальные хирургические вмешательства для разрешения МЖ рекомендуются в случае невозможности выполнения мини-инвазивных вмешательств или возникновении осложнений при их выполнении, которые невозможно разрешить в рамках МИТ [47,48].
Использование МИТ у этой категории пациентов в специализированных стационарах в последние годы сопровождается минимальным числом осложнений. При дистальном блоке предпочтение рекомендуется отдавать ретроградным эндоскопическим МИТ [124].
4. Алгоритм хирургического лечения механической желтухи
5. Послеоперационные осложнения и их лечение
Эндоскопические транспапиллярные вмешательства являются инвазивными вмешательствами, сопровождающиеся в ряде случаев осложнениями. Наиболее частыми осложнениями эндоскопических транспапиллярных операций бывают: кровотечение, панкреатит, ретродуоденальная перфорация, холангит.
При выполнении ЭПСТ с применением высокочастотного тока, существует опасность развития тяжелых постманипуляционных осложнений, частота которых составляет до 10,5% случаев, а летальность – до 2,3%. Использование тока высокой частоты в монополярном режиме при ЭПСТ в 0,8-6,5% случаев приводит к возникновению кровотечения, в 9% случаев к острому панкреатиту и 1-1,5% - ретродуоденальные перфорации.
Для остановки кровотечения при ЭПСТ рекомендуется использовать: эндоскопической диатермокоагуляцией, аргоноплазменной коагуляцией или наложением клипс. В случае рефрактерного кровотечения рекомендовано оперативное лечение: прошивание сосуда в области ЭПСТ [13].
При микроперфорациях ОЖП и ретродуоденальной зоны рекомендуется выполнить эндоскопическое стентирование покрытым стентом, при повреждении стенки ДПК рекомендуется клипирование зоны дефекта и дренирование ДПК [58,104,121]. Частота данного осложнения варьирует от 0,3 до 1,0%.
Причинами ретродуоденальной перфорации являются:
1) отсутствие четких визуальных ориентиров границ допустимого разреза (при локализации БДС в дивертикуле, состояние после резекции желудка по Бильрот-II);
2) предрассечение без селективного контрастирования протока;
3) при выполнении форсированной литоэкстракции (приложение чрезмерно большого усилия для извлечения камня) или баллонной дилатации после ЭПСТ;
4) случаи механической перфорации катетером, папиллотомом при повторных канюляциях или форсированного введения литотриптора.
Наиболее опасным осложнением ЭРХПГ является развитие острого панкреатита, с частотой 1,3%-1,8% и до 5,4% – если выполнялась ЭПСТ.
При травматичных ЭПСТ для профилактики острого панкреатита, а также при развитии ОП рекомендуется выполнить стентирование ППЖ [80,124].
(УУР – А, УДД – 4)
Осложнения чрескожных методов декомпрессии желчевыводящих протоков.
1) Интраоперационные:
a) кровотечение (от 0,5% до 17%), а летальность от этого вида осложнений достигает 3%. К ним относят: внутрибрюшное кровотечение (до 8%), наружное кровотечение по дренажному катетеру, которое происходит вследствие миграции дренажа и гемобилию (2,0–17,7%) для купирования которой необходимо промывание дренажа и гемостатическая терапия (от 10,1 до 16,1%) [1-4].
б. желчеистечение в брюшную полость (от 7,4 до 8,9%), проявляется в течение ближайших нескольких часов после пунктирования и дренирования протоков и может закончиться развитием перитонита, который требует экстренного хирургического вмешательства [1-4];
в. пневмоторакс (от 0,6 до 1,1%) [3-4];
г. аллергические реакции на контрастные вещества (от 0,2 до 0,5%) [3-4];
2) ранние (2-7-е сутки):
a) полная дислокация дренажа, требующая редренирования желчных протоков (от 5,5 до 17,8%) [7-9];
б. частичная дислокация дренажа, требующая коррекцию его положения (от 11,7 до 23,2%) [7-9];
в. подкапсульная гематома печени (от 1,6 до 1,7%) [7-9].
3) Поздние (22-30-е сутки):
a) холангит наблюдается у 0,7-28,0% больных – основной предпосылкой для развития холангита является длительная механическая желтуха [4,5];
б. надпеченочный или подпеченочный абсцесс (от 4,2 до 5,3%) [4,6];
в. желчеистечение в плевральную полость – корректируется дренированием под ультразвуковым контролем (от 1,7% до 2,6%) [6, 11];
г. пневмония (от 0,4 до 0,6%) [7,8];
д. перитонит (от 0,8 до 1,6%) [7,8];
е. ателектаз легкого (от 0,2 до 1,6%) [3];
ж. гидроторакс (от 0,8 до 0,9%) [3].
VIII. Медицинская реабилитация и санаторно-курортное лечение, медицинские показания и противопоказания к применению методов медицинской реабилитации, в том числе основанных на использовании природных лечебных факторов
Медицинскую реабилитацию рекомендуется начинать максимально рано и проводить одновременно с лечением. Реабилитацию рекомендуется осуществлять в отделениях по профилю оказания специализированной помощи (I этап), в отделениях медицинской реабилитации стационара (II этап) и в реабилитационном отделении поликлиники, реабилитационном отделении дневного стационара, реабилитационном отделении санатория (III этап).
Реабилитационные мероприятия рекомендуется направлять на уменьшении боли и ранней активизации, нормализации микрофлоры толстой кишки, улучшению биохимических показателей крови, снижению тревожно-депрессивных проявлений, уменьшению диспептических явлений и улучшению пищеварения [109].
Послеоперационная боль – важнейший фактор, влияющий на длительность послеоперационного пребывания пациента в стационаре. При проведении послеоперационной аналгезии рекомендуется осуществлять мультимодальный подход с комплексным использованием регионарной аналгезии, нейрональных блоков, комбинации ацетаминофена (парацетамола) и нестероидных противовоспалительных препаратов.
Рекомендуется ранняя активизация больных. Постельный режим усугубляет потерю мышечной массы и слабость, ухудшает лёгочные функции, предрасполагает к венозному застою и тромбоэмболии, а также способствует послеоперационному образованию спаек в брюшной полости. Рекомендуется приложить все усилия для ранней послеоперационной активации, которая возможна при адекватной аналгезии (концепция ускоренного восстановления – см. Анналы хирургическогой гепатологии. 2023; (2). https://doi.org/10.16931/1995-5464.2023-2.).
Рекомендуется ранняя пероральная гидратация после прекращения внутривенной инфузии.
При наличии тошноты и рвоты у пациентов в послеоперационном периоде рекомендуется фармакологическая терапия (дроперидол, противорвотные препараты).
Пациентов, перенёсших хирургическое лечение по поводу ЖКБ и её осложнений, рекомендуется направлять в санатории гастроэнтерологического профиля и специализированные реабилитационные отделения через 2-3 недели после операции.
IX. Профилактика и диспансерное наблюдение, медицинские показания и противопоказания к применению методов профилактики.
Основной целью профилактики возникновения МЖ является своевременное лечение заболеваний печени, жёлчных протоков, поджелудочной железы и регулярное диспансерное наблюдение у специалистов соответствующего профиля, а также у семейного врача, терапевта. [99]
Эхинококкоз, альвеококкоз. В максимально короткие сроки после операции рекомендуется назначение химиотерапии – альбендазол 10-15 мг/кг веса, мебендазол 40-50 мг/кг веса – одномесячные курсы с двухнедельным интервалом – 3-6 курсов. Особенно важно назначение химиотерапии при множественном и сочетанном поражении, диссеминированном процессе, при самопроизвольном или случайном нарушении целостности кистозных образований. Вопрос о назначении химиотерапии решается индивидуально совместно хирургом и инфекционистом [22,123].
В послеоперационном периоде всем пациентам рекомендуется лабораторный и инструментальный контроль в течение первого года: общий анализ крови, исследования крови с помощью иммуноферментного анализа, УЗИ печени и ЖВП 3 раза в год, КТ органов брюшной полости через 6 мес. и через год: в последующем – через 12 мес.
Аскаридоз. Рекомендуется регулярное применение антигельминтных препаратов, что препятствует возникновению рецидива кишечного аскаридоза, осложнением которого является аскаридоз желчевыводящих путей.
Описторхоз. Рекомендуется своевременная дегельминтизация, обязательная диспансеризация пациентов с проведением УЗИ не менее одного раза в год и с амбулаторным лечением с применением антипаразитарных препаратов. Важна индивидуальная работа с пациентами по повышению их санитарной культуры с дальнейшим диспансерным наблюдением.
X. Организация оказания медицинской помощи
Догоспитальный этап предусматривает экстренную госпитализацию
в многопрофильный хирургический стационар с круглосуточным дежурством диагностической службы, бригады хирургов и эндоскопистов.
На постгоспитальном этапе проводится дообследование пациента
с целью дальнейшего обязательного выполнения плановой холецистэктомии после разрешения явлений механической желтухи на фоне холедохолитиаза.
XI. Дополнительная информация (в том числе факторы, влияющие на исход заболевания или состояния).
На исход заболевания или состояния могут оказывать влияние:
- Ургентные хирургические заболевания (острый аппендицит, перфорация полого органа, острая ишемия кишечника, мезентеральный тромбоз, ущемлённая грыжа, острая кишечная непроходимость желудочно-кишечное кровотечение и другое);
- Острый инфаркт миокарда;
-Заболевания сердечно сосудистой системы: постинфарктный кардиосклероз, безболевая ишемия миокарда, перикардит, аневризма аорты, гипертоническая болезнь III степени, стенокардия напряжения, нестабильная стенокардия;
- Клинически значимые нарушения ритма и проводимости ( фибрилляция / трепетания предсердий, частая желудочковая экстрасистолия по типу би-, тригеминии, желудочковая тахикардия, полная блокада левой ножки пучка Гиса, трёхпучковая блокада пучка Гиса, фибрилляция желудочков, синоаурикулярная блокада более I степени, атриовентрикулярная блокада II-III степени, синдром Фредерика);
- Хроническая сердечная недостаточность III-IV степени по NYHA;
- Хроническое легочное сердце в стадии декомпенсации;
- Тромбоэмболия легочной артерии;
- Острое нарушение мозгового кровообращения;
- Транзиторная ишемическая атака;
- Острая пневмония, плеврит;
- Острая почечная недостаточность;
- Хроническая почечная недостаточность со скорость юклубочковой фильтрации менее 30мл/мин;
- Бронхиальная астма;
- Сахарный диабет I и II типа;
- Инфекционные и паразитарные заболевания;
- Выраженные врожденные дефекты, подтверждённые данными анамнеза и/или объективным обследованием;
- Язвенная болезнь желудка и двенадцатиперстной кишки в стадии обострения;
- Цирроз печени;
- Системные заболевания соединительной ткани;
- Рассеянный склероз и другие демиелинизирующие заболевания;
- Гематологические заболевания;
- Психиатрические заболевания;
- Наркомания или хронический алкоголизм по данным анамнеза;
- Беременность/период лактации;
- Ожирениеcиндексоммассытелаболее40;
- Наличие в анамнезе онкологических заболеваний, туберкулёза или положительной реакции на ВИЧ-инфекцию, гепатит В и С, сифилис;
- Гиперчувствительность к иммуноглобулинам и другим препаратам крови;
- Поливалентная аллергия.
XII.Критерии оценки качества медицинской помощи
№п/п |
Критерии качества |
УДД |
УУР | |||
1. |
Выполнен осмотр врачом-хирургом не позднее 1 часа от момента поступления в стационар |
2а |
В | |||
2. |
Выполнен анализ крови биохимический общетерапевтический (билирубин, щелочная фосфатаза, аланинаминотрансфераза, аспартатаминотрансфераза, амилаза, мочевина, глюкоза) |
1а |
А | |||
3. |
Выполнено ультразвуковое исследование органов брюшной полости не позднее 2 часов от момента поступления в стационар; лабораторные, эндоскопические и рентген-радиологические исследования для уточнения причины механической желтухи(по показаниям) |
2а |
В | |||
4. |
Выполнена верификация причины механической желтухи до начала лечения, за исключением случаев хирургического лечения |
3 |
C | |||
5. |
Выполнена консультация врача инфекциониста при подозрении или наличия паразитарной причины механической желтухи |
2 b |
В | |||
6. |
Начато проведение предоперационной подготовки не позднее 2-6 часов от момента поступления в стационар (при наличии неотложных показаний) |
2а |
В | |||
7. |
Выполнено хирургическое вмешательство не позднее 6 часов от момента поступления в стационар (при наличии неотложных показаний) |
1в |
А | |||
8. |
Выполнено радикальное устранение причины механической желтухи (при имеющихся условиях) |
1а |
А | |||
9. |
Выполнена декомпрессия желчных ходов с применением эндоскопического, чрескожного и хирургического лечения в объёме, соответствующем указанными в рекомендациях (по показаниям) |
1а |
А | |||
10. |
Выполнено бактериологическое исследование желчи и экссудата из брюшной полости с определением чувствительности возбудителя к антибиотикам и другим лекарственным препаратам (при различных видах вмешательств) |
1в |
А | |||
11. |
Определен конкретный вид завершения оперативного вмешательства |
1а |
А | |||
12 |
Выполнение анестезии в соответствии с объемом оперативного вмешательства и тяжестью состояния пациента |
3 |
C | |||
13. |
Выполнение гистологического исследования удаленного препарата, с указанием параметров в соответствии с рекомендациями (у больных, кому выполнено эндоскопическое и хирургическое лечение) |
3 |
C | |||
14. |
Выполнены адекватная интенсивная и антибактериальная терапия |
1а |
А | |||
15. |
При онкологической причине заболевания выполнено стадирование опухолевого процесса до начала противоопухолевого лечения (классификация TNM) |
2 a |
B | |||
16 |
Выполнена консультация онколога-химиотерапевта при противопоказаниях к хирургическому лечению |
3 |
C | |||
17. |
Выполнение периоперационной антибиотикопрофилактики |
Ia |
A | |||
18. |
Выполнение тромбопрофилактики послеоперационных осложнений (при условии отсутствия противопоказаний к её проведению; у больных, кому выполнено хирургическое лечение) |
Ia |
A | |||
19. |
Отсутствие кровотечений в раннем послеоперационном периоде (у больных, кому выполнено эндоскопическое, чрескожное и хирургическое лечение) |
3 |
C | |||
20 |
Проведение комбинированной химиотерапии больному распространенным неоперабельным опухолевым процессом при удовлетворительном состоянии (после консультации врача онколога) |
1в |
A | |||
21 |
Дренирование, стентирование желчных протоков, наложение билиодигестивных анастомозов при механической желтухе |
2а |
В | |||
22 |
Антибактериальная терапия острого, холангита при дренировании желчных протоков |
1а |
А | |||
23 |
Выполнена профилактика послеоперационных осложнений в период госпитализации |
1в |
А | |||
XIII. Список литературы
1. Руководство по хирургии желчных путей: 2 е изд. Под редакцией Гальперина Э.И., Ветшева П.С. М: Видар М; 2009. 568 с.
2. Дадвани С. А., Ветшев П. С., Шулутко А. М. Прудков М.И. Желчнокаменная болезнь: М: ГЭОТАР-Медиа; 2009.176 с.
3. Taylor A., Stapley S., Hamilton W. Jaundice in primary care: a cohort study of adults–aged more 45 years using electronic medical records. Fam Pract 2012; 29: 416 -420.
4. Williams E., Beckingham I. Sayed G. Et al. Updated guideline on the management of common bile duct stones (CBDS). 2017; № 66 (5):765-782.
5. Center S.A. Diseases of the gallbladder and biliary tree. Vet Clin North Am Small Anim Pract 2009; №39 (3): 543-598.
6. Майстренко Н.А. Стукалов В. В. Холедохолитиаз: СПб: ЭЛБИ-СПб; 2000. 288 с.
7. Нечитайло М.Е., Грубник В.В., Ковальчук А.Л. и др. Минимально инвазивная хирургия патологии желчных протоков: К.: Здоров'я; 2005. 424 с.
8. Bismuth H., Majno P.E. Biliary strictures: classification based on the principles of surgical treatment. World J Surg 2001; №25 (10):1241–1244.
9. Старостина О.Ю. Панюшкина И.И. Сравнительная характеристика методов лабораторной диагностики описторхоза. Клиническая лабораторная диагностика 2014; 4: 44-46.
10. Mendonça E.Q., Bernardo W.M., Moura E.G.et al. Endoscopic versus surgical treatment of ampullary adenomas: a systematic review and meta-analysis. Clinics (Sao Paulo) 2016; 71(1):28-35.
11. Goda K., Kikuchi D., Yamamoto Y. et al. Endoscopic diagnosis of superficial non-ampullary duodenal epithelial tumors in Japan: Multicenter case series. Dig Endosc 2014; №26 (2):23-29.
12. Aine Keating, Obstructive jaundice induced by biliary ascariasis. BMJ Case Reports; 2012, 68-72.
13. Данилов М.В., Зурабиани В.Г., Карпова Н.Б. Осложнения минимально инвазивной хирургии. Хирургическое лечение осложнений минимально инвазивных вмешательств на желчных путях и поджелудочной железе. Руководство для врачей: “Бином”; 2015.
14. Гальперин Э.И. Классификация тяжести механической желтухи. Анналы хир гепатол 2012; 2: 26-34.
15. Гальперин Э.И. Момунова О. Н. Классификация тяжести механической желтухи. Хирургия. Журнал им. Н.И. Пирогова 2014;1: 5-9
16. Альперович Б.И., Мерзликин Н.В., Сало В.Н., Скурлатов М.С. Повторные операции при альвеококкозе. Анналы хирургической гепатологии 2011; № 16:(3): 110¬-115.
17. Курачева Н.А. Ультразвуковая диагностика механической желтухи в хирургии паразитарных заболеваний печени. Автореферат. дисс... канд. мед. наук. Томск. 2013.
18. Паразитарные механические желтухи: Цхай В. Ф. Бражникова Н. А. Альперович Б. И. и др. 2013; 230 с.
19. Higuchi R., TakadaT., Steven M., Strasberg S.V. et al. TG13 miscellaneous etiology of cholangitis and cholecystitis. J Hepatobiliary Pancreat Sci 2013; 20:97–105.
20. Omar J. S. et al. Biliary Ascariasis: A Review. World Journal Surgery 2006; 30: 1500–1506.
21. Бражникова Н.А., Цхай В.Ф. Клиника, диагностика и лечение осложнений описторхоза. Анналы хирургической гепатологии 2004;.№ 9:(2): 40-44.
22. Хирургия эхинококкоза: Ю.Л.Шевченко, Ф.Г.Назыров. М.: «Династия»; 2016. 288 с.
23. Pershina A.G., Ivanov V.V., Efimova L.V. et al. Magnetic resonance imaging and spectroscopy for differential assessment of liver abnormalities induced by Opisthorchis felineus in an animal model. PLoS neglected tropical diseases. Publisher: Public Library of Science (San Francisco, US). 2017; 11(7):e0005778
24. Практическое руководство по ультразвуковой диагностике. Общая ультразвуковая диагностика: Под ред. Митькова В.В. М.: Видар; 2003. 720 с.
25. Gurusamy K.S., Giljaca V., Takwoingi Y. et al. Ultrasound versus liver function tests for diagnosis of common bile duct stones. Cochrane Database Syst Rev 2015;(2): CD011548.
26. Williams E J, Green J, Beckingham I. et al. Guidelines on the management of common bile duct stones (CBDS). Gut 2008;57;1004-1021.
27. Степанова Ю.А., Борсуков А.В.,Панченков Д.Н. Чрескожные вмешательства на органах гепатопанкреатобилиарной зоны и селезенке под контролем ультразвука. Диагностическая интервенционная радиология 2009; №3: (1): 55–77.
28. Shojaiefard A., Esmaeilzadeh M., Ghafouri A., Mehrabi A. Various techniques for the surgical treatment of common bile duct stones: a meta review. Gastroenterol Res Pract 2009; 840208.
29. Tasneem L., Corey A.C., Max P.R. et al. ACR Appropriateness Criteria Jaundice. JACR 2013; №10: (6): 402–409.
30. Кононенко С. Н, Лимончиков С. В. Диагностика механической желтухи и пути повышения эффективности миниинвазивных технологий, направленных на ее ликвидацию. Хирургия. Журнал им. Н.И. Пирогова 2011; 9: 4-10.
31. Park H.S., Lee J.M., Choi J.Y. et al. Preoperative evaluation of bile duct cancer: MRI combined with MR cholangiopancreatography versus MDCT with direct cholangiography. AJR Am J Roentgenol 2008;190: 396-405.
32. Kim T.U., Kim S., Lee J.W. et al. Ampulla of Vater: comprehensive anatomy, MR imaging of pathologic conditions, and correlation with endoscopy. Eur J Radiol 2008;66:48-64.
33. Jovanović P., Salkić N.N., Zerem E. et al. Biochemical and ultrasound parameters may help predict the need for therapeutic endoscopic retrograde cholangiopancreatography (ERCP) in patients with a firm clinical and biochemical suspicion for choledocholithiasis. Eur J Intern Med 2011;22: 110–114.
34. Williams E.J., Taylor S., Fairclough P. et al. Are we meeting the standards set for endoscopy? Results of a large-scale prospective survey of endoscopic retrograde cholangio-pancreatograph practice. Gut 2007;56: 821–829.
35. Church N., Periera S., Hatfield A. et al. Success of initial ERCP following therapeutic failure. Gut 2007; №7(2):A88.
36. Панченко Е.Ф., Пирожков С.В., Теребилина Н.Н. и др. Механизмы антиэндотоксической защиты печени. Пат физиол. и экспер. тер 2012; 3: 62-69.
37. Ступин В.А., Басарболиева Ж.В., Агапов М.А.. и др. Результаты комбинированного лечения больных с механической желтухой доброкачественного генеза. Хирургия. Журнал им. Н.И. Пирогова 2012; 7: 75-79.
38. Карелов А.Е., Пышная И.В., Митрохина М.В. и др. Эффективность ремаксола у онкологических пациентов с послеоперационной дисфункцией печени. Экспер. и клин. фармакол. 2013; 7: 19-23.
39. Хороненко В.Э., Донскова Ю.С., Баскаков Д.С. и др. Профилактика печеночной недостаточности при обширных резекциях печени. Анестезиол. и реаниматол 2014; 4: 33-38.
40. Яковлев А.Ю., Чичканова А.С., Улитин Д.С. и др. Коррекция печеночной дисфункции при подготовке к системной лекарственной терапии больных злокачественными новообразованиями желчевыводящих путей. Вопр. онкол 2012; 14: 555-558.
41. Яковлев А.Ю., Зайцев Р.Р., Семенов В.Б. и др. Лекарственная коррекция желчеоттока у больных со злокачественными новообразованиями желчевыводящих путей. Анналы хирургической гепатологии 2014; 3:.81-85.
42. Mayumi T., Okamoto K., Takada T. et al. Tokyo Guidelines 2018: Мanagement bundles for acute cholangitis and cholecystitis. J Hepatobiliary Pancreat Sci 2018; 25:96–100.
43. Gomi H., Takada T., Hwang T.L. et al. Updated comprehensive epidemiology, microbiology, and outcomes among patients with acute cholangitis. J Hepatobiliary Pancreat Sci 2017; 24:310–318.
44. Tanaka A., Takada T., Kawarada Y. et al. Antimicrobial therapy for acute cholangitis: Tokyo Guidelines. J Hepatobiliary Pancreat Surg 2007;14:59–67.
45. Salvador V., Lozada M., Consunji R. Microbiology and antibiotic susceptibility of organisms in bile cultures from patients with and without cholangitis at an Asian. Academic Medical Center.Surg Infect 2011;12: 105–111.
46. Melzer M., Toner R., Lacey S., Bettany E., Rait G. Biliary tract infection and bacteremia: presentation, structural abnormalities, causative organisms and clinical outcomes. Postgrad Med J 2007;83: 773–776.
47. Mazuski J.E., Tessier J.M., May A.K. et al. The Surgical Infection Society Revised Guidelines on the Management of Intra-Abdominal Infection. Surgical infections 2017; 18:1–76.
48. Rhodes A., Evans L.E., Alhazzani W. et al. Surviving Sepsis Campaign: International Guidelines for Management of Sepsis and Septic Shock: 2016. Intensive Care Med 2017;43: 304–377.
49. Kogure H., Tsujino T., Yamamoto K. et al. Fever-based antibiotic therapy for acute cholangitis following successful endoscopic biliary drainage. J Gastroenterol 2011; 46:1411–1417.
50. Park T.Y., Choi J.S., Song T.J.. et al. Early oral antibiotic switch compared with conventional intravenous antibiotic therapy for acute cholangitis with bacteremia. Dig Dis Sci 2014; 59:2790–2796.
51. Regimbeau J.M., Fuks D., Pautrat K. et al. Effect of postoperative antibiotic administration on postoperative infection following cholecystectomy for acute calculous cholecystitis: a randomized clinical trial. JAMA 2014;312:145–154.
52. 81. Loozen C.S., Kortram K., Kornmann V.N. et al. Randomized clinical trial of extended versus single-dose perioperative antibiotic prophylaxis for acute calculous cholecystitis. Br J Surg 2017; 104: 151–157.
53. Mazeh H., Mizrahi I., Dior U. et al. Role of antibiotic therapy in mild acute calculus cholecystitis: a prospective randomized controlled trial. World J Surg 2012; 36:1750–1759.
54. Choo L., Mishra G.., Conway J. et al. Prospective single blinded study of endoscopic ultrasound prior to endoscopic retrograde cholangiopanctreatography for patients for a positive intraoperative cholangiogram. Gastrointest Endosc 2012; № 75 (4): AB203.
55. Garewal D., Powell S., Milan S.J. et al. Sedative techniques for endoscopic retrograde cholangiopancreatography. Cochrane Database Syst Rev 2012; (6): CD007274.
56. Guidance for the use of propofol sedation for adult patients undergoing endoscopic retrograde cholangiopancreatography (ERCP) and other complex upper GI procedures. On behalf of the Joint Royal College of Anaesthetists and British Society of Gastroenterology Working Party. 2011.
57. Testoni P.A.., Mariani A.., Aabakken L. et al. Papillary cannulation and sphincterotomy techniques at ERCP: European Society of Gastrointestinal Endoscopy (ESGE) Clinical Guideline. Endoscopy 2016; 48:657–683.
58. Dumonceau J-M., Pierre H. Deprez P, Jenssen Ch. et al. Indications, results and clinical impact of endoscopic ultrasound (EUS)-guided sampling in gastroenterology: European Society of Gastrointestinal Endoscopy (ESGE) Clinical Guideline. Endoscopy 2017; №49(7): 695-714.
59. Коков Л.С. Интервенционная радиология: М.: ГЭОТАР-Медиа; 2008. 192 с.
60. Ozcan N., Kahriman G., Mavili E. Percutaneous transhepatic removal of bile duct stones: results of 261 patients. Cardiovasc Intervent Radiol 2012; 35:890–897.
61. Kint J.F., van den Bergh J.E., van Gelder R.E. et al. Percutaneous treatment of common bile duct stones: results and complications in 110 consecutive patients. Dig Surg 2015;№32:(б): 9–15.
62. Кулезнева Ю. М., Израилов Р. Е., Мусаев Г. Х. и др. Чрескожные вмешательства в абдоминальной хирургии: М: ГЭОТАР-Медиа; 2016. 192с
63. Buddingh K.T. The Critical View of Safety and Routine Intraoperative Cholangiography Complement Each Other as Safety Measures During Cholecystectomy. J. Gastrointest. Surg 2011; №15(6):1069-1070.
64. Sheffield К.М., Han Y., Kuo Y.F. et al. Variation in the Use of Intraoperative Cholangiography during Cholecystectomy. J. Am. Coll. Surg 2012;№ 214(4): 668-679.
65. Kenny R., Richardson J., McGlone E.R, et al. Laparoscopic common bile duct exploration versus pre or post-operative ERCP for common bile duct stones in patients undergoing cholecystectomy: is there any difference? Int J Surg 2014; 12: 989–993.
66. Zhang H.W., Chen Y.J., Wu C.H. et al. Laparoscopic common bile duct exploration with primary closure for management of choledocholithiasis: a retrospective analysis and comparison with conventional T-tube drainage. Am Surg 2014; 80:178–181.
67. 99.Gurusamy K.S., Koti R., Davidson B.R. T-tube drainage versus primary closure after laparoscopic common bile duct exploration. Cochrane Database Syst Rev 2013;(6): CD005641.
68. Ragulin-Coyne E., Witkowski E.R., Chau Z. et al. Is routine intraoperative cholangiogram necessary in the twenty-first century? A national view. J Gastrointest Surg 2013; № 17(3):434–442.
69. Scroggie D.L., Jones C. Fluorescent imaging of the biliary tract during laparoscopic cholecystectomy. Ann Surg Innov Res 2014; 8: 5-12.
70. 102.Ford J.A., Soop M., Du J., Loveday B.P., Rodgers M. Systematic review of intraoperative cholangiography in cholecystectomy. Br J Surg 2012;№ 99(2):160–167.
71. Itoi T., Moon J.H., Waxman I. Сurrent status of direct peroral cholangioscopy. Digestive Endoscopy. 2011; № 154–157.
72. Endoscopic versus surgical treatment of ampullary adenomas: a systematic review and meta-analysis. Clinics (Sao Paulo) 2016; №71(1):28-35.
73. 109. Garcea G. Preoperative biliary drainage for distal obstruction: the case against revisited. Pancreas 2010; №39 (2): 119–126.
74. Buddingh K.T. The Critical View of Safety and Routine Intraoperative Cholangiography Complement Each Other as Safety Measures During Cholecystectomy. J. Gastrointest. Surg 2011; №15(6):1069-1070.
75. Земляной В.П., Дарвин В.В., Филенко Б.П., Сингаевский А.Б. и др.Паразитарные заболевания органов брюшной полости. В кн. «Абдоминальная хирургия. Национальное руководство: краткое издание». Москва: 2016. с.834 – 852.
76. Онищенко С.В., Дарвин В.В. Роль папиллита в развитии описторхозного холангита. Анналы хирургической гепатологии 2012; №17(1):66-73.
77. Зайцев И.С. Показания к повторным операциям при альвеококкозе печени. Сибирский медицинский журнал 2013; 8:55-61.
78. Imankulov S.B., Fedotovskikh G.V., Shaymardanova G.M. et al. Treatment of liver echinococcosis high-intensity focused ultrasound (HIFU - therapy). J Clin Med Kaz 2012; №3(26): 43 - 49.
79. Askew J., Connor S. Review of the investigation and surgical management of resectable ampullary adenocarcinoma 2013; №15(11):829-838.
80. Шаповальянц С.Г., Будзинский С.А., Федоров Е.Д. и др. Эндоскопическое лечение послеоперационных рубцовых стриктур желчевыводящих путей (20-летний опыт). Анналы хирургической гепатологии 2011;№16(2):10–17.
81. Шевченко Ю.Л., Ветшев П.С., Стойко Ю.М. и др. Приоритетные направления в лечении больных с механической желтухой. Анналы хирургической гепатологии 2011; 3: 9–15.
82. Group O.L.o.E.W. "The Oxford 2011 Levels of Evidence". Oxford Centre for Evidence-Based Medicine 2011.
83. Российский консенсус по актуальным вопросам диагностики и лечения синдрома механической желтухи. Хирургия. Журнал им. Н.И. Пирогова . 2020; 6:5-17
84. Подлужный В.И. Механическая желтуха: Принципы диагностики и современного хирургического лечения. Фундаментальная и клиническая медицина 2018; 82-92
85. Национальное руководство «Клиническая хирургия». T. 2. M.: ГЭОТАР-Медиа; 2009.
86. Miyazaki M, Yoshitomi H, Miyakawa S, et al. Clinical practice guidelines for the management of biliary tract cancers 2015: the 2nd English edition. J Hepatobiliary Pancreat Sci. 2015;22:249-273.
87. Creditt AB, Tozer J, Joyce M. Biliary Ultrasound. Clinical Ultrasound; 2018;149-165.
88. Badger WR, Borgert AJ, Kallies KJ. Utility of MRCP in clinical decision making of suspected choledocholithiasis: An institutional analysis and literature review. Am J Surg. 2017;214(2):251-255.
89. Нечипай А.М., Орлов С.Ю., Федоров Е.Д. ЭУСбука. Руководство по эндоскопической ультрасонографии. Практическая медицина; 2013.
90. Joo I, Lee JM, Yoon JN. Imaging Diagnosis of Intrahepatic and Perihilar Cholangiocarcinoma: Recent Advances and Challenges. Radiology. 2018 July;288(1):7-13. Epub 2018 Jun 5.
91. Arian MA, Freeman ML, Howell DA, et al. Choledocholithiasis: Clinical manifestations, diagnosis, and management. Literature review current through: Nov 2018.
92. Karlsen TH, Folseraas T, Thorburn D, Vesterhus M. Primary sclerosing cholangitis – a comprehensive review. Journal of Hepatology. 2017; 67:1298-1323.
93. Naess S, Bjornsson E, Anmarkrud JA, et al. Small duct primary sclerosing cholangitis without inflammatory bowel disease is genetically different from large duct disease. Liver Int. 2014;34(10):1488-1495.
94. European Association for the Study of the L. EASL Clinical Practice Guidelines: management of cholestatic liver diseases. Journal of Hepatology. 2009;51(2):237-267.
95. Lee DW, Chan AC, Lam YH, Ng EK, Lau JY, Law BK, et al. Biliary decompression by nasobiliary catheter of biliary stent in acute suppurative cholangitis: a prospective randomized trial. Gastrointest Endosc. 2002;56:361-365.
96. Клинические рекомендации Федерации анестезиологов и реаниматологов России «Периоперационное ведение больных с нарушениями системы гемостаза», 2018 г.
97. Fekaj E, Jankulovski N and Matveeva N. Obstructive Jaundice. Austin Gig Syst. 2017;2(1):1006.
98. Biliary cancer: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up; 2016.
99. LCA Hepato-pancreatobiliary Cancer Clinical Guidelines. Nov 2014.
100.Celotti A, Solaini L, Montori G, et al. Preoperative biliary drainage in hilar cholangiocarcinoma: Systematic review and meta-analysis. Eur J Surg Oncol. 2017;43:1628-1635.
101.Taylor MC, McLeod RS, Langer B. Biliary stenting versus bypass surgery for the palliation of malignant distal bile duct obstruction: a metaanalysis. Liver Transpl. 2000;6:302-308.
102.Martin DJ, Vernon DR, Toouli J. Surgical versus endoscopic treatment of bile duct stones. Cochrane Database Syst Rev. 2006:CD003327.
103.Ryozawa S, Itoi T, Katanuma A, et al. Japan Gastroenterological Endoscopy Society guidelines for endoscopic sphincterotomy. Dig Endosc. 2018 Mar;30(2):149-173. Epud 2018 Jan 18. Review. PubMed PMID:29247546.
104. Singhvi G, Ampara R, Baum J, Gumaste V. ASGE guidelines result in cost-saving in the management of choledocholithiasis. Ann Gastroenterol. 2016 Jan-Mar;29(1):85-90.
105. Dumonceau JM, Tringali A, Papanikolaou IS, et al. Endoscopic biliary stenting: indications, choice of stents, and results: European Society of Gastrointestinal Endoscopy (ESGE) Clinical Guideline – Updated October 2017. Endoscopy. 2018 Sept;50(9):910-930.
106. Kint JF, van den Bergh JE, van Gelder RE, et al. Percutaneous treatment of common bile duct stones: results and complications in 110 consecutive patients. Dig. Surg. 2015; 32:9-15.
107.Deo KB1, Adhikary S1, Khaniya S1, Shakya VC1, Agrawal CS1 Laparoscopic Choledochotomy in a Solitary Common Duct Stone: A Prospective Study. Minim Invasive Surg. 2018 May 14.
108.Testoni PA, Mariani A, Aabakken L, et al. Papillary cannulation and sphincterotomy techniques at ERCP: European Society of Gastrointestinal Endoscopy (ESGE) Clinical Guideline. Endoscopy. 2016;48:657-683.
109.American Society for Gastrointestinal Endoscopy (ASGE) consensus guidelines. THE role of ERCP in begin diseases of the biliary tract. Gastrointest Endosc. 2015;81(4):795-803.
110.Asia-Pacific consensus guidelines for endoscopic management of benign biliary strictures. Gastrointest. Endosc. 2017;86(1):44-58.
111.European Society of Gastrointestinal Endoscopy (ESGE) Clinical Guideline. Endoscopic biliary stenting: indica-tions, choice of stents, and results: Updated October 2017. Endoscopy. 2018;50(9):910-930.
112.Cote GA, Slivka A, Tarnasky P, et al. Effect of covered metallic stents compared with plastic with plastic stents on benign biliary stricture resolution: a randomized clinical trial. JAMA. 2016; 315:1250-1257.
113.Khan MA, Baron TH, Kamal F, et al. Efficacy of self-expandable metal stents in management of benign biliary strictures and comparison with multiple plastic stents: a meta-analysis. Endoscopy. 2017; 49:682-694.
114.Lau WY, Lai EC, Lau SH. Management of bile duct injury after laparoscopic cholecystectomy: a review. Aust N Z J Surg. 2010; 80:75-81.
115.Лекции по гепатопанкреатобилиарный хирургии. Под ред.Э.И.Гальперина и Т.Г.Дюжевой. М.:Видар-М; 2011.
116.Гальперин Э.И., Чевокин А.Ю., Дюжева Т.Г. Особенности симптоматики и хирургического лечения разного типа рубцовых стриктур желчных протоков. Анналы хирургической гепатологии. 2017;22(3):19-28.
117.Вишневский В.А., Ефанов М.Г., Икрамов Р.З., Варава А.Б., Трифонов С.А. Современная хирургическая тактика при рубцовых стриктурах желчных протоков. Тенденции и нерешенные вопросы. Анналы хирургической гепатологии. 2017;22(3):11-18.
118.Pancreatic Adenocarcinoma. NCCN Clinical Practice Guidelines in Oncology. 2015.
119.Pancreatic Adenocarcinoma. NCCN Clinical Practice Guidelines in Oncology. 2015.
120.Al-Kawas F, Aslanian H, Baillie J, et all. Percutaneous transhepatic vs. Endoscopic retrograde biliary drainage for suspected malignant hilar obstruction: study protocol for a randomized controlled trial. Trials. 2018;19:108.
121.БурдюковМ.С., ГусевД.В., ГвоздевА.А. идр. Индивидуальный подход к выбору тактики билиарной декомпрессии у больных с опухолями гепатобилиопанкреатодуоденальной зоны. Доказательная гастроэнтерология. 2014;3:52-56.
122.Кукушкин А.И., Давыдов М.И., Долгушин Б.И., Виршке Э.Р. и др. Осложнения чрескожных чреспеченочных рентгеноэндобилиарных вмешательств у больных с механической желтухой опухолевой этиологии. Вестн. РОНЦ им. Н. Н. Блохина РАМН. 2004;3:108-110
123.Ветшев П.С., Мусаев Г.Х., Шарипов Р.Х. Мини-инвазивные технологии в лечении эхинококкоза печени. Анналы хирургической гепатологии. 2021.26(4): 77-86.
124.Карпов О.Э., Ветшев П.С., Бруслик С.В., Маады А.С., Свиридова Т.И., Алиев Ф. Минимально инвазивные стентовые технологиив гепатопанкреатобилиарной хирургии. Анналы хирургической гепатологии. 2021.26(3): 13-22.
125.Карпов О.Э., Ветшев П.С., Бруслик С.В., Маады А.С. Сочетанное применение ретроградного и антеградного доступов при сложном холедохолитиазе. Анналы хирургической гепатологии. 2013. Т. 18. №1. С. 59-62.
XIV. Приложение А1.Состав рабочей группы по разработке и пересмотру клинических рекомендаций
Рабочая группа:
1. Профессор Гальперин Э.И. – Москва
2. Академик РАН, профессор Хатьков И.Е. - Москва
3. Профессор Вишневский В.А. – Москва
4. Профессор Ветшев П.С. – Москва
5. Профессор Дарвин В.В. – Сургут
6. Профессор Дюжева Т.Г. – Москва
7. Профессор Дибиров М.Д. – Москва
8. Профессор Шулутко А.М. – Москва
9. Профессор Прудков М.И. – Екатеринбург
10. Профессор Буриев И.М. – Москва
11. Профессор Шаповальянц С.Г. – Москва
12. Профессор Ахаладзе Г.Г. – Москва
13. Профессор Парфенов И.П. – Москва
14. Профессор Кулезнева Ю.В. – Москва
15. Профессор Цвиркун В.В. – Москва
16. Абдужалилов М.К. – главный хирург Дагестана
Ни у кого из членов рабочей группы при разработке настоящих клинических рекомендаций не возникло конфликта интересов, а именно персональной заинтересованности в получении лично, либо через представителя компании материальной выгоды или иного преимущества, которое повлияло бы или могло повлиять на надлежащее исполнение им профессиональных обязанностей.
XV.Приложение А2. Методология разработки клинических рекомендаций
Целевая аудитория данных клинических рекомендаций: врачи-хирурги; врачи-анестезиологи-реаниматологи; врачи-эндоскописты.
Шкала оценки уровней достоверности доказательств (УДД) для методов диагностики (диагностических вмешательств).
|
УДД |
Расшифровка |
|
1. |
Систематические обзоры исследований с контролем референсным методом или систематический обзор рандомизированных клинических исследований с применением мета-анализа. |
|
2. |
Отдельные исследования с контролем референсным методом или отдельные рандомизированные клинические исследования и систематические обзоры исследований любого дизайна, за исключением рандомизированных клинических исследований, с применением мета-анализа. |
|
3. |
Исследования без последовательного контроля референсным методом или исследования с референсным методом, не являющимся независимым от исследуемого метода или нерандомизированные сравнительные исследования, в том числе когортные исследования. |
|
4. |
Не сравнительные исследования, описание клинического случая. |
|
5. |
Имеется лишь обоснование механизма действия или мнение экспертов. |
Таблица 2.
Шкала оценки уровней достоверности доказательств (УДД) для методов профилактики, лечения и реабилитации (профилактических, лечебных, реабилитационных вмешательств).
|
УДД |
Расшифровка |
|
1. |
Систематический обзор рандомизированных клинических исследований с применением мета-анализа |
|
2. |
Отдельные рандомизированные клинические исследования и систематические обзоры исследований любого дизайна, за исключением рандомизированных клинических исследований, с применением мета-анализа |
|
3. |
Нерандомизированные сравнительные исследования, в том числе когортные исследования |
|
4. |
Несравнительные исследования, описание клинического случая или серии случаев, исследование "случай-контроль" |
|
5. |
Имеется лишь обоснование механизма действия вмешательства (доклинические исследования) или мнение экспертов |
Таблица 3.
Шкала оценки уровней убедительности рекомендаций (УУР) для методов профилактики, диагностики, лечения и реабилитации (профилактических, диагностических, лечебных, реабилитационных вмешательств).
|
УУР |
Расшифровка |
|
A |
Сильная рекомендация (все рассматриваемые критерии эффективности (исходы) являются важными, все исследования имеют высокое или удовлетворительное методологическое качество, их выводы по интересующим исходам являются согласованными) |
|
B |
Условная рекомендация (не все рассматриваемые критерии эффективности (исходы) являются важными, не всеисследованияимеютвысокоеилиудовлетворительноеметодологическоекачествои/илиихвыводыпоинтересующимисходамнеявляютсясогласованными) |
|
C |
Слабая рекомендация (отсутствие доказательств надлежащего качества (все рассматриваемые критерии эффективности (исходы) являются неважными, все исследования имеют низкое методологическое качество и их выводы по интересующим исходам не являются согласованными) |
Порядок обновления клинических рекомендаций: Механизм обновления клинических рекомендаций предусматривает их систематическую актуализацию – не реже одного раза в три года, а также при появлении новых данных с позиции доказательной медицины по вопросам диагностики, лечения, профилактики и реабилитации, наличии обоснованных дополнений/замечаний к ранее утверждённым КР, но не чаще 1 раза в 6 месяцев.
XVI. Приложение А3. Справочные материалы, включая соответствие показаний к применению и противопоказаний, способов применения и доз лекарственных препаратов инструкции по применению лекарственного препарата
Данные клинические рекомендации разработаны с учётом следующих нормативно-правовых документов:
- Указ Президента Российской Федерации от 07.05.2018 г. №204 «О национальных целях и стратегических задачах развития Российской Федерации на период до 2024 года»;
- Постановление Правительства Российской Федерации от 17.11.2021 г. №1968 «Об утверждении Правил поэтапного перехода медицинских организаций к оказанию медицинской помощи на основе клинических рекомендаций, разработанных и утверждённых в соответствии с частями 3, 4, 6-9 и 11 статьи 37 Федерального Закона «Об основах охраны здоровья граждан в Российской Федерации»»;
- Приказ Министерства здравоохранения Российской Федерации от 15.11.2012 г. №922н"Об утверждении Порядка оказания медицинской помощи взрослому населению по профилю "хирургия";
- Приказ Министерства здравоохранения Российской Федерации от 10.05.2017 г. №203н «Об утверждении и критериев оценки качества медицинской помощи»;
- Приказ Министерства здравоохранения Российской Федерации от 28.02.2019г. №103н «Об утверждении порядка и сроков разработки клинических рекомендаций, их пересмотра, типовой формы клинических рекомендаций и требований к их структуре, составу и научной обоснованности, включаемой в клинические рекомендации информации»;
- Приказ Министерства здравоохранения Российской Федерации от 23.06.2020 г. №617н «О внесении изменений в приложении №1, 2 и 3 к приказу Министерства здравоохранения Российской Федерации от 28.02.2019 г. №103н «Об утверждении порядка и сроков разработки клинических рекомендаций, их пересмотра, типовой формы клинических рекомендаций и требований к их структуре, составу и научной обоснованности включаемой в клинические рекомендации информации»;
- Приказ Министерства здравоохранения Российской Федерации от 19.05.2022 г. №321 «О рабочей группе Министерства здравоохранения Российской Федерации по актуализации методологических подходов к оплате медицинской помощи за счёт средств обязательного медицинского страхования в рамках программы государственных гарантий бесплатного оказания гражданам медицинской помощи»;
- Приказ Министерства здравоохранения Российской Федерации от 05.08.2022 г. № 530н "Об утверждении унифицированных форм медицинской документации, используемых в медицинских организациях, оказывающих медицинскую помощь в стационарных условиях, в условиях дневного стационара и порядков их ведения";
- Письмо Федерального фонда ОМС от 30.12.2014г.№6545/30-5«О целевых экспертизах качества медицинской помощи»;
- Приказ Федерального фонда ОМС от 28.02.2019г. №36 «Об утверждении порядка организации проведения контроля объемов, сроков, качества и условий предоставления медицинской помощи по обязательному медицинскому страхованию».
XVII. Приложение Б. Алгоритмы действий врача
Алгоритм дифференциальной диагностики
|
Показатели |
Гемолитическая |
Паренхиматозная |
Механическая |
|
Анамнез |
Появление желтухи в детском возрасте, подобные заболевания у родственников, усиление желтухи после пребывания на холоде. |
Контакт с токсическими веществами, злоупотребление алкоголем, контакт с больными желтухой, инфекционными заболеваниями (мононуклеоз), инъекции, гемотрансфузии. |
Приступы болей в правом подреберье, нередко сопровождающиеся желтухой, операции на желчных путях, снижение веса. |
|
Тип развития |
Быстрый, с анемией, иногда лихорадка, озноб. |
Начало постепенное после периода тошноты и потери аппетита |
Быстрое прогрессирование после приступа болей при обтурации камнем. Постепенное развитие при новообразовании. |
|
Окраска кожи |
Бледно-желтая с лимонным оттенком |
Оранжевая, желтая |
Зеленый оттенок желтухи, желто-серый |
|
Интенсивность желтухи |
Небольшая |
Умеренно выраженная |
От умеренно выраженной до резкой |
|
Кожный зуд |
Отсутствует |
Неустойчивый |
Устойчивый |
|
Тяжесть в области печени |
Нет |
Часто в ранней стадии болезни |
Редко, исключая острый холецистит |
|
Размер печени |
Нормальный, могут быть умеренное увеличение |
Увеличена, нормальная или уменьшена |
Нормальная или увеличена |
|
Боли в области печени, правом подреберье |
Нет |
Редко |
Часто |
|
Размеры селезенки |
Увеличена |
Часто увеличена |
Обычно не увеличена |
|
Цвет мочи |
Нормальный. Может быть темный при высокой уробилирубинурии |
Темный (наличие связанного билирубина) |
Темный (наличие связанного билирубина) |
|
Содержание уробилина в моче |
Резко повышен |
Может отсутствовать короткий период, в дальнейшем чрезмерно или умеренно повышен |
Отсутствует при полной обтурации |
|
Цвет кала |
Нормальный или темный (повышено содержание стеркобилина) |
Бледный (снижен стеркобилин, повышено количество жира) |
Ахоличный (нет стеркобилина, повышено количество жира) |
|
Функциональные пробы печени |
Повышенное содержание свободного билирубина в крови, осадочные пробы отрицательные, активность щелочной фосфатазы не изменена. |
Повышено содержание связанного и свободного билирубина. Активность щелочной фосфатазы иногда повышена, повышение активности трансаминаз. Осадочные пробы положительны. Повышен коэффициент "железо/медь" сыворотки. |
Высокое содержание связанного билирубина в крови. Повышение активности щелочной фосфатазы. Положительная проба Иргля, осадочные пробы отрицательные |
|
Специальные тесты |
Тесты гемолиза положительные. Реакция Кумбса. Определение резистентности эритроцитов. Выявление тепловых и холодовых антител в сыворотке. Определение гаптоглобина. Электрофорез гемоглобина. |
Биопсия печени, лапароскопия. Радиоизотопное исследование с бенгальским розовым или коллоидным золотом, бромсульфалеиновая проба. |
Рентгенологическое исследование ЖКТ и желчных путей. Лапароскопия. Биопсия печени. ФГДС, ЭРХПГ, ЧЧХГ Сканирование печени. Определение ферментов (амилаза) крови и мочи. |
Алгоритм дифференциальной диагностики на основании инструментальных методов исследования
XVIII. Приложение В. Информация для пациента
После малоинвазивных или открытых хирургических вмешательств течение 1-2 месяцев пациент должен придерживаться относительно простых и выполнимых ограничений. В выполнении они достаточно просты тем более, если учесть, что их игнорирование чревато достаточно неприятными и нежелательными последствиями. При чрескожном дренировании желчных протоков рекомендуется строгий уход за наружным дренажом после операции и на амбулаторном этапе лечения.
Диета: После вмешательств по поводу механической желтухи необходимо придерживаться диетического питания в объеме лечебного стола №5 (по Певзнеру). Он восстанавливает работу печени, желчных путей, положительно влияет на желчеотделение. В основу диеты вложено употребление в основном белков и углеводов, а количество жиров в некоторой степени ограничено. Категорически запрещено использовать продукты с содержанием щавелевой кислоты, холестерина, эфирных масел и азота. В таких случаях необходимо придерживаться следующих правил:
1) употребление одинаковых небольших порций строго пять раз в день;
2) не разрешается есть очень холодную и горячую пищу;
3) приготовление блюд путем запекания, варения и на пару;
4) продукты с грубой клетчаткой, прожилками необходимо измельчать и перетирать.
В течение суток меню диеты по Певзнеру рекомендует употреблять до двух литров жидкости и 10 граммов соли в еде. Калорийность в среднем составляет до 2800 килокалорий. А соотношение белков, жиров и углеводов – 90:90:400 граммов. Больше половины белков имеют животное происхождение, а треть жиров – растительное. Диета номер 5 по Певзнеру положительно относится к овощам, таким как, картофель, огурцы и помидоры, морковь и свекла, перец и краснокочанная капуста. Из круп нужно готовить овсяные, рисовые, гречневые и манные каши, а также макаронные изделия. Со всеми этими продуктами необходимо готовить супы на растительном или сливочном масле. Полезно есть любые сладкие ягоды, бананы и яблоки, клубнику, все сухофрукты. Мясо лучше выбирать нежирное – кроличье, говядину, куриное филе. Приветствуются морепродукты – креветки, кальмары, треска и хек. В день можно съедать только один вареный желток, а омлеты делать из белков. Из молочной продукции можно применять все с небольшим процентом жирности, а сметану использовать как заправку для салатов. Выпечка должна быть несдобной, хлеб печь из пшеничной или ржаной муки 2 сорта. Кроме этого, существуют продукты, полностью исключающиеся из питания. Это маринованные овощи, зелень, белокочанная капуста, чеснок и лук зеленый, грибы и редис. Из круп нельзя употреблять кукурузную, ячневую, пшено, горох, перловку, а также бульоны и супы из них с жирной рыбой и мясом.
Заправлять вторые блюда не разрешается горчицей, перцем либо хреном. Во время лечения исключаются из рациона шоколад, слоеное тесто, свежую и сдобную выпечку. Запрещены напитки с газами, крепкие кофе и чай, и ни в коем случае алкоголь.
Благодаря этим советам по продуктам, в организме быстро происходит обезболивание больных органов и наступает скорейшее выздоровление.
Физическая активность после оперативных вмешательств по поводу механической желтухи: В последующие 6 недель после открытых вмешательств происходит сращение мышц, на фоне чего остается риск образования спаек и грыж. Категорически запрещается поднимание тяжестей и активные физические нагрузки. В то же время отмечается, что ежедневная ходьба небыстрым шагом по 2-3 километра в послеобеденное время способствует предотвращению спаек. Прописывается лечебная гимнастика. Примечательно, что наилучшее восстановление мышечной ткани происходит у тех лиц, кто ранее вел активный образ жизни и поддерживал свое тело в тонусе. Спустя несколько месяцев можно возвращаться к умеренным нагрузкам, постепенно дополняя лечебную гимнастику общими упражнениями:
1) совершать пешие прогулки на небольшие расстояния;
2) после формирования послеоперационного рубца – посещать бассейн и выполнять несложные физические упражнения;
3) тем, кто ведет активный образ жизни, а также пациентам с лишним весом – носить специальный бандаж.
XIX. Шкалы оценки, вопросники и другие оценочные инструменты состояния пациента, приведенные в клинических рекомендациях
Приложение Г1. Феномены при диагностике билиарного аскаридоза.
|
Диагностическая модальность |
Ключевая особенность |
|
УЗИ брюшной полости |
1.Одиночная, длинная линейная или изогнутая эхогенная непрозрачная структура без внутренней трубки (знак полоски); |
|
2.Одиночная толстая длинная линейная или изогнутая неосвещенная эхогенная полоса, содержащая либо центральную трубку или трубчатую структуру (знак внутренней трубки); | |
|
3.Множественные длинные линейные эхогенные структуры (знак Спагетти); | |
|
Компьютерная томография |
Внешний вид «бычьи глаза» при контрастном сканировании; |
|
Магнитно-резонансная холангиопанкреатография |
1.Линейная, слегка гиперинтенсивная трубчатая структура с центральной гипоинтенсивной областью; |
|
2.Линейные гипоинтенсивные дефекты заполнения при массивном билиарном аскаридозе; | |
|
Эндоскопическая ретроградная холангиопанкреатография |
Гладкие длинные линейные дефекты заполнения с сужающимися концами; |
Приложение Г2. Рекомендации рабочей группы ВОЗ (World Health Organization-Informal Working Groupon Echinococcosis (WHO-IWGE) по лечению эхинококковой кисты
|
WHO-IWGE 2001 |
Описание |
Рекомендации по лечению |
|
СЕ1 |
- Однокамерная, простая киста, содержащая анэхогенное содержимое, но может бытьи эхогенным из-за наличия эхинококкового песка, определяемого в виде хлопьев - «снежинок». - Стенка кисты четко визуализируется - Обычно круглая или овальная - Размер вариабельный: CE1s (< 5.0 cm), CE1m (5 – 10 cm), CE1l (> 10cm) - Статус - паразит живой |
Только лекарственная терапия (альбендазол) при размере кисты меньше 5 см. PAIR + Лекарственная терапия (альбендазол) при размере кисты больше 5 см. |
|
СЕ2 |
- Многокамерная киста с «перегородками». Перегородки в кисте могут выглядеть как «спицы колес» - Патогномонично визуализация дочерних цист в виде структур подобных сотам - Дочерние цисты могут частично или полностью заполнять материнскую кисту - Стенка кисты в норме визуализируется - Обычно округлой или овальной формы - Размер вариабельный: CE2s (< 5.0 cm), CE2m (5 – 10 cm), CE2l (> 10cm) - Статус - паразит живой |
Хирургическое лечение + Лекарственная терапия (альбендазол) или Альтернативные пункционные методики+ Лекарственная терапия (альбендазол) |
|
CE3A |
- Однокамерная киста, которая может содержать дочерние цисты - Анэхогенное содержимое с видимой флотацией мембраны кисты (отслоившаяся и неправильно сложившаяся внутренняя оболочка кисты), определяется флотация в виде волн на верхушке кисты. УЗИ симптом «водяной лилии» - отслоившаяся мембрана, плавающая в кистозной жидкости. - Киста может быть неправильной формы, не полностью округлая, в связи со снижением давления внутри кисты. Размер вариабельный: CE3s(< 5.0cm), CE3m (5 – 10 cm), CE3l (> 10cm). - Статус - паразит в переходной, промежуточной фазе. |
Тольколекарственная терапия (альбендазол) при кисте меньше 5 см PAIR+лекарственная терапия (альбендазол) при кисте больше 5 см |
|
CE3B |
- Киста с дочерними кистами с равномерным матриксом - Статус - переходная или промежуточная фаза; наряду с погибшей материнской и дочерними кистами, в жидкости и на оболочках могут находится жизнеспособные протосколексы. Комментарий: подтип CE3B выделен, так как подобный тип, сопровождается более частым рецидивом и худшим ответом на терапию альбендазолом, по сравнению с CE3A |
Хирургическое лечение + Лекарственная терапия (альбендазол) или Альтернативные пункционные методики + Лекарственная терапия (альбендазол) |
|
СЕ4 |
- Гетерогенное гипо(гипер)эхогенное содержимое (признаки дегенеративных изменений). - Не содержит дочерних кист - Визуализируется в виде «клубка шерсти», что говорит о разрушении оболочки. Размер вариабельный:CE4s(< 5.0cm), CE4m (5 – 10 cm), CE4l (> 10cm) - Статус - паразит погибший. |
Наблюдение с регулярным ультразвуковым контролем в течение 10 лет |
|
СЕ5 |
- Киста характеризуется толстой кальцифицированной стенкой в форме арки, за которой образуется коническая эхо-тень. Степень кальцификации от частичной до полной. Размер вариабельный::CE5s (< 5.0 cm), CE5m (5 – 10 cm), CE5l (> 10cm). - Статус - паразит погибший. Комментарий: Диагноз не очевиден, нет патогномоничных симптомов, но подозревается E. granulosus. |
Наблюдение с регулярным ультразвуковым контролем в течение 10 лет |
Приложения Г3. Рекомендуемое выделение вариантов различных видов хирургического лечения при альвеококкозном поражении печени.
1. резектабельный вариант: локальный первичный очаг и удалимые региональные метастазы. Рекомендуется резекция печени и удаление метастазов, которая возможна без сосудистых реконструкций и выполнимая в любом центре хирургии печени;
2. погранично резектабельный вариант: распространенный альвеококкоз с вовлечением афферентных и/или эфферентных сосудов и/или нижней полой вены и удалимые региональные метастазы. Решение о возможности и объеме резекций принимается только в центрах, имеющих опыт обширных резекций и трансплантаций печени;
3. нерезектабельный вариант: поражение критического объема паренхимы, и/или инвазия сосудистых структур с невозможностью их реконструкции, и/или цирроз предполагаемого остатка печени без неудалимых отдаленных метастазов. Радикальным методом лечения является трансплантация печени;
4. неоперабельный вариант: поражение критического объема паренхимы, и/или инвазия сосудистых структур с невозможностью их реконструкции, и/или цирроз предполагаемого остатка печени, неудалимые внепеченочные метастазы. Показано выполнение лишь паллиативных мероприятий.
Приложения Г4. Классификация тяжести механической желтухи (Э.И. Гальперин и соавт., 2014 г.).
Таблица 1
Бальная оценка тяжести печеночной недостаточности при механической желтухе по биохимическим показателям
|
Лабораторные показатели |
Степень тяжести печеночнойнедостаточности | ||
|
1 |
2 |
3 | |
|
Общий билирубин сыворотки крови (мкмоль/л) |
60 |
60-200 |
>200 |
|
Общий белок сыворотки крови (мкмоль/л) |
>65 |
65-55 |
55 |
Комментарии: В соответствии с данной классификацией проводится трехстепенная бальная оценка уровня общего билирубина:
<60 мкмоль/л – 1 балл;
60 – 200 мкмоль/л – 2 балла;
>200 мкмоль/л – 3балла.
Осложнениями, усиливающие тяжесть синдрома МЖ, являются: холангит, почечная недостаточность, печеночная недостаточность, энцефалопатия, желудочно-кишечное кровотечение, сепсис. Эти осложнения синдрома МЖ оцениваются по сравнению с уровнем общего билирубина с коэффициентом 2 и зависят от уровня билирубинемии, т.е. билирубин 1 балл – осложнение 2 балла, билирубин 2 балла – осложнение 4 балла и билирубин 3 балла – осложнение 6 баллов. При соединении двух и более осложнений удваивает или пропорционально увеличивает число баллов. Сепсис оценивается как два и более осложнения. Опухолевый генез МЖ оценивался как 1 осложнение.При такой совокупности оценочных факторов выделяются 3 класса тяжести МЖ (табл. 2)
Таблица 2
Степень тяжести механической желтухи
|
Степень тяжести желтухи |
Количество баллов. |
Послеоперационные осложнения % |
Послеоперационная летальность % |
|
Легкая (класс А) |
≤5 баллов |
16,3 |
0,8 |
|
Средняя (класс В) |
6-15 баллов |
59 |
13,6 |
|
Тяжелая (класс С) |
≥16 баллов |
88,4 |
46,1 |
Механическая желтуха:
Класс «А» (легкая механическая желтуха – больные с числом баллов ≤5);
Класс «В» (Механическая желтуха средней степени тяжести) – больные с числом баллов 6-15;
Класс «С» (тяжелая механическая желтуха) – больные с числом баллов ≥16.
Помимо оценки тяжести МЖ, классификация позволяет определить прогноз оперативного вмешательства: у больных с МЖ класса «А» – прогноз благоприятный, класса «В» – сомнительный, зависящий от общего состояния больного. Однако не стоит забывать, что печеночная недостаточность осложняет МЖ в любой период болезни и определяет прогноз и исход заболевания. Данная классификация не затрагивает прогнозирование печеночной недостаточности при МЖ.
.
Рекомендуемые статьи
Синдром Бергмана
расстройство сердечной деятельности с изменениями ЭКГ при рефлюкс-эзофагите и аксиальной грыже
При эндоскопическом исследовании в случае бронхоэктазов в стадии ремиссии выявляется
частично диффузный бронхит I степени воспаления
Активируйте PUSH уведомления в браузер
Отключите PUSH уведомления в браузер
Содержание
Интернет магазин
Популярное
- О нас
- Правовые вопросы
- Политика
обработки персональных
данных EndoExpert.ru - Связаться с нами
- Стать партнером
© 2016-2022 EndoExpert.ru

Вы находитесь в разделе предназначенном только для специалистов (раздел для пациентов по ссылке). Пожалуйста, внимательно прочитайте полные условия использования и подтвердите, что Вы являетесь медицинским или фармацевтическим работником или студентом медицинского образовательного учреждения и подтверждаете своё понимание и согласие с тем, что применение рецептурных препаратов, обращение за той или иной медицинской услугой, равно как и ее выполнение, использование медицинских изделий, выбор метода профилактики, диагностики, лечения, медицинской реабилитации, равно как и их применение, возможны только после предварительной консультации со специалистом. Мы используем файлы cookie, чтобы предложить Вам лучший опыт взаимодействия. Файлы cookie позволяют адаптировать веб-сайты к вашим интересам и предпочтениям.
Я прочитал и настоящим принимаю вышеизложенное, хочу продолжить ознакомление с размещенной на данном сайте информацией для специалистов.


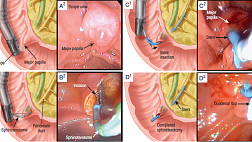





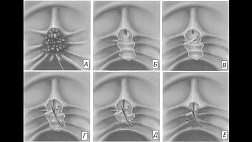

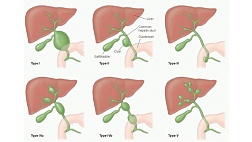




.jpg)





.png)



.jpg)













Комментарии