- Компании
- Takeda. О компании, буклеты, каталоги, контакты
- Olympus. О компании, буклеты, каталоги, контакты
- Boston Scientific. О компании, буклеты, каталоги, контакты
- Pentax. О компании, буклеты, каталоги, контакты
- Fujifilm & R-Farm. О компании, буклеты, каталоги, контакты
- Erbe. О компании, буклеты, каталоги, контакты
- Еще каталоги
- Мероприятия
- Информация
- Обучение
- Классификации
- Атлас
- Quiz
- Разделы
- Пациенту
QR-код этой страницы

Для продолжения изучения на мобильном устройстве ПРОСКАНИРУЙТЕ QR-код с помощью спец. программы или фотокамеры мобильного устройства
Статьи: Диагностика и лечение дивертикулов Ценкера
| Авторы: | Королёв М.П. Федотов Л.Е. Климов А.В. Антипова М.В. Оглоблин А.Л. Мамедов Ш.Д. Габдрахманова Л.А. 2016г. |
Введение:
Лечение дивертикулов пищевода является актуальной проблемой современной хирургии. В настоящее время достигнут значительный успех в лечении рака пищевода [19]. Интерес к лечению доброкачественных заболеваний пищевода, в том числе и дивертикулов, появился с середины прошлого века, несмотря на то, что с момента описания первого дивертикула пищевода (Ludlow, 1764) прошло более 250 лет [4, 19, 24].
Среди больных с дивертикулами пищевода, наиболее выраженные клинические проявления у больных с дивертикулом Ценкера. В настоящее время дивертикул Ценкера является одной из причин развития дисфагии, наряду с такими заболеваниями, как опухоли пищевода, кардиоспазм, ожоговая болезнь пищевода, гастроэзофагеальной рефлюксной болезнью и инородными телами пищевода.
В современной медицине наиболее часто диагноз дивертикул Ценкера выставляют врачи - эндоскописты, что связано с растущим количеством эндоскопических исследований при заболеваниях верхних отделов желудочно- кишечного тракта.
Наша клиника занимается лечением больных дивертикулом пищевода более 30 лет. За данный период времени на лечении в клинике находилось 417 больных с дивертикулом пищевода. По локализации дивертикулы в пищеводе распределились следующим образом: дивертикул Ценкера, средней трети (перибронхиальные) и нижней трети (эпифренальные и поддиафрагмальные) пищевода.
Данные по локализации дивертикула в пищеводе представлены в таблице 1.
Таблица 1 — Локализация дивертикулов пищевода
|
Число больных с дивертикулом пищевода | |
|
Дивертикул Ценкера |
136 (32,6%) |
|
Средней трети пищевода |
257 (61,6%) |
|
Нижней трети пищевода |
24 (5,8%) |
|
Всего: 417 (100%) | |
На 2015 год, выполнено 133 операции больным дивертикулом Ценкера. Изначально, выполнялись открытые операции с эндоскопическим ассистированием. С 2009 года применяются малоинвазивные способы лечения дивертикула Ценкера. Открытыми операциями, в последние годы, мы пользуемся при осложнённых дивертикулах Ценкера. Результаты лечения представлены в таблице 2.
Таблица 2. Результаты хирургического лечения больных дивертикулом Ценкера.
|
Больные дивертикулом Ценкера N (84) |
Количество
|
Всего |
|
Резекция и инвагинация дивертикула с крикофарингеальной миотомией под контролем эндоскопической техники |
56
(42%)
|
133
(100%)
|
|
Эндоскопическая баллонная дилатация с введением препарата «Диспорт» в область крикофарингеальной мышцы |
3
(2%)
| |
|
Эндоскопическое рассечение волокон нижней порции крикофарингеальной мышцы |
74
(56%)
|
Полный текст статьи:
ИСТОРИЯ ВОПРОСА.
Дивертикул Ценкера стали диагностировать со второй половины XVIII столетия. Первое сообщение об обнаружении дивертикула Ценкера принадлежит Ludlow из Бристоля, который в своем письме Hunter’y, датированном 1764 годом, сообщает, что при вскрытии он столкнулся с «противоестественным карманом».
Препарат, о котором рассказывалось в письме, хранится в Гунтеровском музее в Глазго [10, 14, 18, 26].
Первое описание клинических симптомов и патологической анатомии дивертикула пищевода, датировано 1804 годом, принадлежит Deguise.
В 1816 году Bell в своей книге приводит собственное описание нескольких наблюдений «слепых мешков» и рекомендует с целью опорожнения шейного дивертикула наложение свища [10, 14, 26, 53]. Впервые подобная операция была выполнена Nicoladoni, через 40 лет после предложения Bell’а.
Пациент с наложенным свищом скончался от пневмонии на 6-е сутки после операции [10].
В XIX веке редко применялись операции на полостях, тем более на пищеводе, учитывая его расположение и анатомическое соседство с жизненно важными анатомическими образованиями [19].
В 1850 году Kluge предложил радикальную операцию по устранению дивертикула пищевода — дивертикулэктомию. Ее впервые выполнил Niehans в 1884 году. У пациента с зобом и дивертикулом после операции по поводу зоба клинические проявления сохранились, и Niehans предпринял попытку дивертикулэктомии. Пациент скончался от кровотечения из нижней щитовидной артерии [19].
Первый анализ этиопатогенеза дивертикулов пищевода принадлежит Rokitanski. Он разделил дивертикулы на пульсионные и тракционные.
В 1877 году Zenker представил анализ 27 случаев дивертикулов, в том числе 5 собственных наблюдений. Сопоставляя клиническую и патологоанатомическую картину, он подтвердил эти особенности и подробно описал шейные дивертикулы, которые получили его имя [18,19].
Позже Oekonomides (1882) и Tetens (1888) описали глоточно-пищеводные дивертикулы, ими также было введено понятие о комбинированном пульсионно- тракционном дивертикуле.
Первые попытки хирургического лечения дивертикулов предпринимались на шейном отделе пищевода. Это обусловлено большей доступностью и меньшей операционной травмой [18].
Wheeler из Дублина в 1886 году произвел первую удачную дивертикулэктомию, а в 1892 году об успешной операции сообщил Bergman. В том же году две удачные операции с шейными дивертикулами провел Kocher [18].
Французский хирург Girad в конце XIX века предложил оригинальную операцию — инвагинацию дивертикула пищевода с наложением кисетного шва. В 1917 году в работах Bevan’a сообщается о некоторой модификации этого метода: было предложено инвагинировать дивертикул с помощью наложения поперечных и продольных швов [16, 18].
В 1893 году Reichman и Mintz впервые дали патолого- анатомическое описание эпифренальных дивертикулов. Симптоматику дивертикулов данной локализации описал Kienbock.
В отечественной литературе о наблюдении 472 пациентов с дивертикулами различных отделов пищевода сообщил А.В. Судакевич в 1908 году. Все пациенты наблюдались в клинике госпитальной хирургии Московского университета, руководителем которой был профессор П.И. Дьяконов. Он же впервые в отечественной литературе сообщил о 24 эзофагоскопиях, проводимых для диагностики дивертикула пищевода [6, 18, 19].
В 1911 году Н.А. Богораз в монографии «К хирургии пищевода» отразил вопросы этиологии, патогенеза, классификации, клинической картины и лечения дивертикулов пищевода [12, 18, 19, 20].
В многотомном руководстве П.И. Тихова (1916 г.), одна из глав посвящена проблемам диагностики и лечения дивертикулов пищевода.
С целью предотвращения застоя пищевых масс в мешке дивертикула Liebl в 1910 году предложил операцию, смысл которой сводился к фиксации дна мешка к мышцам глотки. Впервые эту операцию провел Hill в 1917 году [18].
В 1911 году Goldmann впервые выполнил двухэтапную операцию при глоточно-пищеводном дивертикуле.
Первый этап операции заключался в выделении мешка дивертикула и перевязке его шейки. Второй этап проводили через две недели, он заключался в удалении мешка дивертикула и ушивании раны. Таким образом, автор пытался избежать развития медиастинита. Однако после первого этапа нередко наступал некроз дивертикула [18].
Murphy и Judd в 1916 и 1919 годах модифицировали операцию Goldmann, предложив более позднюю перевязку мешка, либо его фиксацию без перевязки на первом этапе. Через 14 лет Lahey вновь модифицировал двухмоментную операцию при шейных дивертикулах. Первый этап сводился к выделению дивертикулярного мешка с подшиванием его к коже.
Через 7 дней производилась перевязка дивертикула у шейки с его отсечением. Заживление послеоперационной раны осуществлялось вторичным натяжением. Руководствуясь данным методом, Warren с хорошим результатом выполнил 365 оперативных вмешательств [18].
В период Великой Отечественной войны советские хирурги накопили большой опыт в грудной хирургии, что положительно сказалось на хирургии пищевода. Начиная с 1950-х годов, ряд отечественных хирургов сообщают об успешном лечении дивертикулов пищевода различных локализаций [14, 16].
В 1959 г. Н.Е. Дудко, И.М. Слепуха и В.Ф. Брынко применили сшивающий аппарат УКБ-25 для прошивания шейки дивертикула, при этом дивертикулэктомии не проводили, а накладывали П- образные швы для ликвидации полости дивертикула.
С 1960-х годов Т.Т. Даурова, Т.А. Суворова, А.А. Вишневский, Е.И. Захаров сообщают о применении аллопластики и сетчатой капроновой ткани с целью укрепления мышечной оболочки пищевода после дивертикулэктомии [12].
Параллельно в зарубежной литературе активно обсуждаются вопросы этиологии, патогенеза и хирургического лечения дивертикулов пищевода.
Историю диагностики дивертикулов пищевода можно разделить на дорентгеновский период и период рентгенодиагностики.
До введения рентгенологического метода исследования дивертикулы пищевода чаще всего обнаруживали при аутопсии. Прижизненная диагностика осуществлялась методом слепого зондирования. При слепом зондировании зонд попадал в полость дивертикула или проникал в желудок. Успех зондирования зависел от расположения дивертикула и умелой манипуляции зондом. Дальнейшее развитие методики привело к применению двойного зондирования, смысл которого заключался в введении двух зондов, один из которых оставался в пищеводе, а другой свободно проникал в желудок.
Дальнейшим шагом в распознавании дивертикулов пищевода являлось эндоскопическое исследование, которое улучшило диагностику дивертикулов, но в силу несовершенной технической оснащенности не всегда трактовалось правильно. [11, 18].
Reitzenstein в 1898 году впервые с помощью рентгеновских лучей подтвердил диагноз дивертикула пищевода. При этом были выявлены трудности в диагностике дивертикулов небольших размеров.
Отдельные трудности в диагностике имеют тракционные дивертикулы, направленные вверх.
Э.Н. Ванцян (1964) придавал большое значение рентгенокинематографии, за счет наличия фазы пневморельефа.
АНАТОМИЯ И ФИЗИОЛОГИЯ ГЛОТКИ И ПИЩЕВОДА.
Пищеварительная система начинается с полости рта, (cavitas oris). Она состоит из двух отделов: преддверия рта и собственно полости рта.
Преддверие рта, vestibulum oris, представляет собой щелевидное пространство, расположенное между губами и щеками — снаружи, зубами и деснами — внутри. В преддверие полости рта открывается выводной проток околоушной железы. Его устье находится на слизистой оболочке щеки на уровне второго верхнего большого коренного зуба.
Пища поступает в ротовую полость через ротовую щель, которая ограничена верхней и нижней губами. В толще губ и щек расположены мимические мышцы. Их наружная поверхность покрыта кожей, а внутренняя — слизистой оболочкой. Последняя выстлана многослойным плоским неороговевающим эпителием и содержит многочисленные мелкие слюнные железы.
Слизистая оболочка с внутренней поверхности губ и щек переходит на десны. По средней линии она образует уздечки верхней и нижней губ. Десны, gingivae, — это слизистая оболочка, покрывающая альвеолярные отростки челюстей.
Собственно, полость рта, cavitas oris propria, имеет верхнюю стенку и дно.
Через зев она сообщается с глоткой.
Верхняя стенка представлена твердым и мягким нёбом, отграничивающим ротовую полость от носовой. Твердое нёбо представляет собой костное нёбо (его образуют отростки верхней челюсти и нёбной кости), покрытое слизистой оболочкой. Мягкое нёбо — это продолжение твердого нёба. Его основу образуют поперечно-полосатые мышцы. Передний отдел мягкого нёба расположен почти в горизонтальной плоскости, задний отдел — нёбная занавеска — опускается вниз и заканчивается нёбным язычком. При глотании мягкое нёбо поднимается и препятствует попаданию пищевого комка из ротоглотки в носоглотку и полость носа.
От мягкого нёба в стороны и книзу направляются две пары дужек: нёбно- язычные (передние) и нёбно-глоточные (задние). Дужки представляют собой дупликатуры слизистой оболочки, содержащие одноименные мышцы. Между ними с каждой стороны находится углубление, в котором расположена нёбная миндалина, tonsilla palatina. Со стороны ротовой полости нёбо выстлано многослойным плоским неороговевающим эпителием; со стороны носовой — мерцательным.
Дно полости рта образовано мышцами шеи, лежащими выше подъязычной кости. Они выстланы изнутри слизистой оболочкой.
В полости рта расположены зубы и язык. В нее также открываются протоки слюнных желез. В этом отделе пища находится в среднем 10—20с.
Глотка, (pharynx) — орган воронкообразной формы, в который из полости рта попадает пережеванная и смоченная слюной пища.
Этот орган прикреплен к основанию черепа и переходит в пищевод на уровне седьмого шейного позвонка. В среднем длина глотки составляет 12—14 см. В ней осуществляется перекрест пищеварительного и дыхательного пути. Боковые участки органа граничат с сосудисто-нервным пучком шеи, включающим общую сонную артерию, внутреннюю яремную вену и блуждающий нерв.
Соответственно расположению глотки в ней выделяют три части:
1. носовую (носоглотку), pars nasalis;
2. ротовую (ротоглотку), pars oralis;
3. гортанную (гортаноглотку), pars laryngea.
Глотка имеет следующие стенки: верхнюю (свод), заднюю, переднюю и две боковых. Следует отметить, что передняя стенка выражена только в гортаноглотке. В первых двух отделах она практически отсутствует за счет сообщений с носовой и ротовой полостями.
Носовая часть расположена за носовой полостью и сообщается с последней при помощи хоан. Через них воздух попадает в гортань.
Эпителий носоглотки аналогичен по строению эпителию носовой полости (мерцательный). В носоглотку открывается слуховая (Евстахиева) труба, которая сообщает барабанную полость с глоткой. Она служит для вентиляции последней и выравнивания давления в барабанной полости с атмосферным.
Поэтому носовое дыхание необходимо для нормального функционирования органа слуха. Ротовая часть расположена позади зева, который представляет собой относительно небольшое пространство, ограниченное двумя парами нёбных дужек по бокам, мягким нёбом — сверху и корнем языка — снизу. Пространство ротоглотки ограничено с одной стороны уровнем мягкого нёба, а с другой — входом в гортань. Ее эпителий многослойный, плоский, неороговевающий, такой же как и в ротовой полости. Именно здесь перекрещиваются пищеварительный и дыхательный пути.
Гортанная часть представляет собой самый узкий отдел глотки. Она граничит спереди с задней стенкой гортани, снизу переходит в пищевод. Эпителий гортанной части многослойный плоский неороговевающий. Пища из ротовой полости через ротоглотку и гортаноглотку переходит в пищевод, а воздух из носовой полости идет в носоглотку, ротоглотку и в гортань. Один из хрящей гортани — надгортанник, препятствует попаданию пищи в дыхательные пути. Он играет роль своеобразного клапана.
Стенка глотки состоит из трех оболочек: слизистой, мышечной и адвентициальной. В слизистой оболочке глотки расположены специальные лимфоидные образования, относящиеся к иммунной системе, называемые миндалинами:
– нёбная миндалина, tonsilla palatina (парная), расположена между двумя нёбными дужками;
– трубная миндалина, tonsilla tubaria (парная), находится возле выхода в глотку слуховой трубы;
– язычная миндалина, tonsilla lingualis (непарная), лежит на корне языка;
– глоточная миндалина, tonsilla pharyngealis, seu adenoida (непарная), на верхней стенке глотки.
Все вместе они образуют лимфоэпителиальное глоточное кольцо Пирогова
— Вальдейера. Функция этого кольца — обезвреживание микроорганизмов, попадающих с пищей и воздухом в глотку, а также участие в иммунных процессах. Снаружи эти органы покрыты слизистой оболочкой, которая образует складки (крипты). Лимфоидные узелки расположены в веществе миндалин под эпителием и содержат большое количество иммунных клеток — лимфоцитов. Следует отметить, что с возрастом происходит утрата миндалинами своих функций. Размеры их уменьшаются, вплоть до полного исчезновения (атрофии).
У взрослого человека хорошо заметными остаются только нёбные миндалины.
Под слизистой оболочкой вместо подслизистой основы расположен слой соединительной ткани, носящий название глоточно-базилярной фасции. Благодаря ей глотка прикрепляется к основанию черепа.
Мышечная оболочка глотки представлена поперечно-полосатой мускулатурой, сокращение которой способствует продвижению пищевого комка в пищевод. Различают две группы мышц глотки:
1. мышцы-сжиматели, или констрикторы: верхний, средний и нижний; они расположены циркулярно и покрывают друг друга в виде черепицы;
2. мышцы, поднимающие глотку: шилоглоточная и нёбно-глоточная; они лежат продольно и выражены слабее констрикторов.
Снаружи глотка покрыта адвентицией, которая ограничивает подвижность органа.
Таким образом, глотка выполняет функции проводника пищи из ротовой полости в пищевод и воздуха из носовой полости в гортань. Кроме того, за счет наличия лимфо-эпителиального кольца Пирогова — Вальдейера она обеспечивает защиту организма от проникновения болезнетворных бактерий и вирусов.
Пищевод, (oesophagus) — полый орган длиной 25 — 30 см. Он начинается от глотки на уровне VII шейного позвонка, а заканчивается на уровне XI грудного позвонка, переходя в желудок. Самая большая часть пищевода расположена в грудной полости.
Небольшие, по 2,0—4,5 см, его части находятся в области шеи и в брюшной полости. Следовательно, в пищеводе различают шейную, грудную и брюшную части. Пищевод проходит позади трахеи и граничит с грудной частью аорты. С боков к нему прилежат блуждающие нервы, которые, переплетаясь между собой, образуют сплетения.
Пищевод имеет анатомические сужения:
– фарингеальное, или глоточное, находящееся в месте перехода глотки в пищевод;
– бронхиальное, расположенное в месте его соприкосновения с левым главным бронхом;
– аортальное, расположено в области прикосновения пищевода к дуге аорты;
– диафрагмальное — в области пищеводного отверстия диафрагмы;
– кардиальное — находящееся в месте перехода пищевода в желудок.
Пищевод имеет три оболочки: слизистую, мышечную и адвентициальную. Многослойный плоский неороговевающий эпителий выстилает изнутри слизистую оболочку, которая имеет многочисленные продольные складки. Поэтому на поперечном разрезе полость органа обладает звездчатой формой. Эти складки дают возможность пищеводу расширяться при продвижении пищевого комка. Мышечная оболочка верхней части пищевода представлена поперечнополосатой мышечной тканью. В средней трети она содержит, кроме того, гладкие мышечные клетки, а в нижней части — полностью построена из гладкой мышечной ткани. В мышечной оболочке выделяют два слоя: наружный — продольный и внутренний — циркулярный. В шейной и грудной частях пищевод покрыт адвентицией, а в брюшной части — серозной оболочкой.
Основная функция пищевода — проведение пищи из глотки в желудок. Пищевой комок продвигается за счет силы тяжести, действующей на него, и перистальтических сокращений мускулатуры органа. Жидкая пища проходит по пищеводу за 1 — 2 секунды, при этом активных сокращений мышечной оболочки не происходит. Более плотная пища продвигается в течение 3 —10 секунд. При этом ее продвижению активно способствуют мышцы пищевода.
Глотание - это сложный рефлекторный акт, при помощи которого пищевой комок переходит из ротовой полости в желудок. Центр глотания находится в продолговатом мозге и функционально связан с нейронами дыхательного и сосудодвигательного центров, также расположенными в этом отделе нервной системы. Поэтому при глотании автоматически прекращается дыхание, изменяется работа сердца и сосудов. Пища после обработки в ротовой полости превращается в пищевой комок.
Жевательные движения обеспечивают его продвижение к корню языка, где находятся многочисленные чувствительные нервные окончания. От них нервные импульсы поступают в продолговатый мозг — в центр глотания. Далее по двигательным нейронам черепных нервов импульсы идут к мышцам, отвечающим за процесс глотания. Язык запрокидывается назад и проталкивает пищевой комок в глотку. Мягкое нёбо (нёбная занавеска) поднимается и полностью отграничивает носовую часть глотки от ротовой. В результате пищевой комок не может попасть в полость носа. Одновременно происходит поднимание глотки и гортани. При этом надгортанник перекрывает вход в гортань, плотно закрывая его, что создает препятствие для попадания пищи в дыхательные пути. Следует отметить, что разговор при приеме пищи может привести к попаданию пищевого комка в дыхательные пути и вызвать смерть от удушья (асфиксии).
Мышцы глотки, сильно сокращаясь, проталкивают комок через ротоглотку, гортаноглотку в пищевод. Перистальтические сокращения пищевода способствуют перемещению пищи в желудок. В том месте, где в данный момент находится пищевой комок и чуть ниже, мускулатура расслабляется.
Вышележащие отделы сокращаются, проталкивая его. Это движение имеет характер волны. Между желудком и пищеводом в области кардиального сужения расположен своеобразный клапан — кардиальный оком, который пропускает пищу в желудок и препятствует обратному ее движению из желудка в пищевод.
ЭТИОЛОГИЯ И ПАТОГЕНЕЗ ДИВЕРТИКУЛОВ ЦЕНКЕРА.
Более двух столетий ученые многих стран изучают проблемы возникновения и развития дивертикула Ценкера. За это время было предложено множество теорий их образования. Основные теории связаны либо с предположением о врожденном характере дивертикула Ценкера, сводящемся к нарушению формирования пищеварительной трубки на различных сроках эмбрионального развития плода, либо с анатомо-физиологическими особенностями пищевода.
F.A. Zenker пришел к мнению, что главную роль в развитии глоточно- пищеводных дивертикулов играет повышенное внутреннее пищеводное давление и наличие «слабых» мест. Анатомически имеются два слабых места в глоточно- пищеводном переходе: между нижним сжимателем глотки (m. constrictor pharyngis inferior) и перстневидно-глоточной мышцей (m. cricopharyngeus), а также между перстневидно- глоточной мышцей (m. cricopharyngeus) и мускулатурой пищевода. Данные анатомические образования носят названия треугольников Ланье— Геккермана и Лаймера—Киллиана (Рис. 1).
Повышение внутрипищеводного давления приводит к выпячиванию и растягиванию стенки, что влечет за собой образование дивертикула. Факторами, способствующими повышению внутрипищеводного давления, являютя: частое надавливание пищи на заднюю стенку глотки, нарушение функции и координации m. сricopharyngeus, длительное сокращение глоточно-пищеводного сфинктера и его преждевременное закрытие. Для оценки работы глоточно- пищеводного сфинктера и акта глотания используются методы манометрии и видеофлюроскопии [1, 3, 6, 18, 19, 22, 26, 31, 33, 46, 51].
Ряд авторов придают большое значение рефлюкс- эзофагиту в образовании дивертикулов глоточно- пищеводного перехода. Это объясняется наличием постоянного сокращения мышц пищевода, что приводит к повышению внутрипищеводного давления и нарушению работы пищеводных сфинктеров, также происходит увеличение паузы сокращения m. сricopharyngeus. Такая длительная пауза ослабляет пространство между констрикторами и ведет к образованию дивертикула [18, 31].
Таким образом, большинство авторов признает следующие механизмы образования шейных дивертикулов:
– наличие «слабого» места в глоточно-пищеводном переходе;
– наличие физиологического сужения с замедленным прохождением пищевых масс через данное анатомическое образование;
– увеличение внутрипищеводного давления;
– нарушение сократительной способности мышечного аппарата пищевода;
– нарушение работы сфинктеров.
Э.Н. Ванцян (1964) указывает на наличие взаимосвязи образования дивертикулов пищевода с кардиоспазмом и грыжами пищеводного отверстия диафрагмы. В своих трудах автор приводит данные, свидетельствующие о нередком сочетании кардиоспазма и шейного дивертикула (6,4%), наличии единой этиологической причины — резко выраженной дистрофии ветвей блуждающего нерва. Сочетание дивертикула пищевода с грыжей пищеводного отверстия диафрагмы наблюдалось в 7,4%. Данное сочетание приводит к воспалительной дегенерации мышечных и нервных волокон стенки пищевода.
Многие исследователи связывают возникновение дивертикулов с нарушением процессов эмбриогенеза и врожденной неполноценностью мышц пищевода.
Таким образом, во время эмбрионального развития возникают облитерированные тяжи между пищеводом, трахеей или бронхами. В свою очередь, А.Г. Земляной (1970) связывает образование дивертикулов пищевода с наличием у эмбриона на сроке 8–9 недель шаровидных интерстициальных дивертикулов, которые на более поздних сроках эмбрионального развития исчезают [12, 18, 35].
В образовании тракционных дивертикулов большую роль играет наличие воспалительных заболеваний органов грудной клетки и шеи, которые, впоследствии, приводят к развитию спаечного процесса и образованию дивертикулов [1, 5, 6, 18, 19, 22, 26, 31].
Клиническая картина дивертикула Ценкера зависит от его размеров и индивидуальных особенностей больного. Длительность существования дивертикула и наличие осложнений также оказывают влияние на развитие клинической картины заболевания.
Клинические проявления глоточно-пищеводных дивертикулов имеют стадийное течение. Выделяют три стадии развития дивертикула:
Первая стадия характеризуется выпячиванием слизистой оболочки через «слабое» место - треугольник Киллиана. Во время развития первой стадии дивертикула клинические проявления, как правило, неспецифичны. Жалобы пациентов заключаются в наличии чувства першения или царапанья в нижних отделах шеи, сухости или обильном слюноотделении, неловкости при глотании, покашливании и поперхивании при приеме пищи. Также у пациентов можно наблюдать незначительное напряжение мышц шеи и вынужденные движения головы при приеме пищи. Часто первая стадия развития дивертикула проходит под маской фарингита или протекает бессимптомно [1, 5, 13].
Вторая стадия дивертикула глоточно-пищеводного перехода заключается в формировании дивертикулярного мешка, который не является прямым продолжением глотки. При этом клинические проявления становятся разнообразней и связаны с застоем пищи, слизи и воздуха в просвете дивертикула. Пациенты предъявляют жалобы на чувство жжения, першения, сухость в глотке, гиперсаливацию, боли царапающего характера, неприятный запах изо рта. При этом давление дивертикула на соседние органы создает компрессионный синдром, который может проявляться дисфагией, регургитацией малоизмененной пищи, симптомами ночного кашля и «мокрой подушки», дисфонией, и одышкой. При осмотре больного можно выявить асимметричное утолщение шеи с мягким на ощупь выпячиванием, которое уменьшается при пальпации и увеличивается при приеме пищи. Чаще данное выпячивание можно наблюдать в левой половине шеи. При перкуссии выпячивания после приема жидкой пищи отмечается шум плеска, а при надавливании шум усиливается.
Аускультативно слышен звук «клокочущего гейзера». Со временем пациенты привыкают к появившимся симптомам, начинают есть медленно, меняя положение головы, чаще нагибая ее вперед. Периодически во время еды наступает полное нарушение прохождения пищи. Нередко можно наблюдать, как пациенты после приема пищи оказывают себе ручное пособие, надавливая на дивертикулярное выпячивание рукой, что способствует опорожнению дивертикула.
В 1958 году Terracol и Sweet описали триаду, характерную для пищеводно- глоточных дивертикулов, которая включает в себя регургитацию пищей, постоянное наличие слизи в глотке и бурлящие шумы при надавливании на глотку.
Третья стадия (декомпенсации), характеризуется увеличением размеров дивертикула, в результате чего дивертикул опускается в средостение, где он становится прямым продолжением глотки.
Клинические проявления становятся более выраженными, постоянное срыгивание приводит к попаданию содержимого дивертикула в дыхательные пути и развитию аспирационных пневмоний и абсцессов легких. При значительных размерах дивертикула отмечается сдавливание трахеи, пищевода, крупных сосудов, паралич возвратного нерва. У ряда пациентов отмечался венозный застой половины лица. Отмечаются потеря массы тела, вплоть до дистрофии, ухудшение самочувствия [1, 3, 4, 6, 8, 12, 16, 29, 47].
Занимаясь лечением данной группы больных нами был разработан опросник, целью которого являлась оценка клинических проявлений дивертикула Ценкера. С помощью опросника нами оценены клинические проявления у 52 больных с дивертикулом Ценкера. Стоит отметить, что у большей части больных имелся дивертикул средних или больших размеров. Данные опросника приведены в сводной (таблице 3).
Таблица 3. Жалобы анкетированных больных с дивертикулом Ценкера.
|
Симптом |
Количество |
% |
|
Затруднения при глотании |
52 |
100 |
|
Затруднение прохождения пищи |
52 |
100 |
|
Необходимость запивания пищи большим |
46 |
88,4 |
|
Отрыжка воздухом |
52 |
100 |
|
Боли в эпигастральной области |
38 |
73,0 |
|
Снижение массы тела |
46 |
88,4 |
|
Першение в горле |
50 |
96,1 |
|
Диарея |
39 |
75,0 |
|
Вынужденные движения головой при глотании |
31 |
59,6 |
|
Поперхивание |
52 |
100 |
|
Наличие изжоги |
44 |
84,6 |
|
Неприятный запах изо рта |
48 |
92,3 |
|
Одышка |
28 |
53,8 |
|
Ночной кашель |
49 |
94,2 |
|
Боли за грудиной |
26 |
50 |
|
Надавливания на 1/2 шеи при проглатывании пищи |
33 |
63,4 |
|
Приступообразный кашель |
25 |
48,0 |
|
Срыгивание съеденной пищей |
18 |
34,6 |
|
Периодическое повышение температуры тела |
19 |
36,5 |
|
Чувство остановки пищевого комка |
27 |
51,9 |
|
Удушье во время еды |
20 |
38,4 |
|
Жжение в горле |
18 |
34,6 |
|
Повышенное слюноотделение |
12 |
23,0 |
|
Рвота после еды |
17 |
32,6 |
|
Царапанье в горле |
8 |
15,3 |
|
Появление припухлости 1/2 шеи |
12 |
23,0 |
|
Срыгивание во время сна |
8 |
15,3 |
|
Отек 1/2 лица |
3 |
5,7 |
|
Снижение слюноотделения |
2 |
3,8 |
Таким образом, большинство больных предъявляло несколько жалоб, характерных для дивертикула Ценкера.
Более трёх жалоб, характерных для дивертикула Ценкера, предъявляет сто процентов больных.
Ведущим симптомом у данной группы больных является дисфагия.
Давность возникновения данных симптомов различна. Чаще всего первыми симптомами дивертикула Ценкера являлись поперхивание, отрыжка воздухом, ночной или приступообразный кашель, изжога, неприятный запах изо рта, боли в эпигастральной области, необходимость запивать твердую пищу большим количеством воды.
Большинство пациентов отмечали эпизодический характер появления данных симптомов на протяжении
10–15 лет. У ряда больных данные жалобы усугублялись в течение года, и к ним присоединялись срыгивание после еды и во время сна, удушье во время приема пищи, затруднение при прохождении твердой пищи, снижение массы тела. Для более поздних симптомов дивертикула Ценкера характерно ручное пособие во время еды (надавливая рукой на шею или поворачивая голову во время глотка).
У всех пациентов имелась дисфагия различной степени выраженности. Больные отмечали затруднение проглатывания твердой пищи и снижение массы тела. Большинству пациентов приходилось менять привычную пищу на мелко измельченную и увеличивать количество ее приемов. Для дивертикула Ценкера характерной является дисфагия, которая постепенно нарастает в процессе приема пищи, а после срыгивания или применения ручного пособия дисфагия временно исчезает. Такой характер дисфагии присущ больным с дивертикулом Ценкера.
Таким образом, клиническая картина дивертикула Ценкера разнообразна и имеет длительный анамнез развития. На ранних стадиях заболевания симптомы малоспецифичны, что, как правило, затрудняет своевременную диагностику.
ОБСЛЕДОВАНИЕ БОЛЬНЫХ С ДИВЕРТИКУЛОМ ЦЕНКЕРА.
Диагностика дивертикула Ценкера складывается из нескольких методов обследования. Большую роль в диагностике играет клиническая картина и сбор анамнеза. Учитывая жалобы, можно заподозрить наличие данной патологии. Для дивертикула Ценкера характерным симптомом является дисфагия, которая постепенно нарастает во время приема пищи. Явления нарушения прохождения пищи по пищеводу носят ремиттирующий характер.
При подозрении у больного на дивертикул Ценкера следует начинать диагностический поиск с рентгенологических методов обследования. Диагноз дивертикула Ценкера является клинико- рентгенологическим. При дифференциальной диагностике дисфагии и подозрении на дивертикул Ценкера имеются обязательные и дополнительные методы исследования.
Таким образом, при подозрении на наличие у больного дивертикула Ценкера следует проводить диагностический поиск по следующему алгоритму:
1. Обязательные методы исследования.
– рентгенологическое исследования шеи и грудной клетки; -
рентгеноконтрастное исследование пищевода и желудка;
– эндоскопическое исследование верхних отделов желудочно – кишечного тракта;
2. Дополнительные методы исследования.
– зумэндоскопия и хромоскопия слизистой оболочки дивертикула и пищевода;
– биопсия слизистой оболочки дивертикула и пищевода при подозрении на злокачественный процесс;
– измерение РН пищевода и внутрипищеводного давления;
– ультразвуковое исследование мягких тканей шеи;
– компьютерная томография шеи и грудной клетки;
– магнитно – резонансная томография шеи и грудной клетки;
– эндоскопическая ультрасонография пищевода и дивертикула для уточнения состояния крикофарингеальной мышцы.
Рентгенологический и эндоскопический методы исследования являются обязательными в диагностике дивертикула Ценкера и дают исчерпывающую информацию о расположении дивертикула, его размерах степени сдавления пищевода дивертикулом и состоянии слизистой и пищевода.
Данных методов обследования, чаще достаточно для определения метода лечения дивертикула Ценкера. Однако, при выявлении изменений со стороны слизистой дивертикула (выходящих за рамки дивертикулита) или пищевода, нестандартного расположения дивертикула или изменение его формы, необходимо использовать дополнительные методы диагностики. Следует отметить, что эндоскопический метод исследования противопоказан больным с перфорацией дивертикула Ценкера. В случае подозрения на перфорацию дивертикула больному показано рентгеновское исследование пищевода с водорастворимым контрастом. Больным с наличием перфорации дивертикула, эндоскопический метод может быть использован интраоперационно с целью уточнения места перфорации и контроля герметичности пищеводных швов после резекции дивертикула.
РЕНТГЕНОЛОГИЧЕСКОЕ ИССЛЕДОВАНИЕ БОЛЬНЫХ ДИВЕРТИКУЛОМ ЦЕНКЕРА.
Рентгенологический метод исследования является надежным и информативным в диагностике дивертикула Ценкера. На современном уровне развития рентгенологии применение контрастных растворов при рентгенографии, рентгеноскопии и томографии пищевода позволяет изучить не только морфологические изменения пищевода, но и его функцию. Рентгенологическое исследование, как правило, дает возможность составить представление о величине, размере, положении дивертикула, проходимости пищевода, а также возможность оценить заполнение и опорожнение полости дивертикула [2,7,11, 14, 15, 16, 17, 27, 28, 40].
При рентгенологическом исследовании грудной клетки редко удается обнаружить дивертикул, с уровнем жидкости и воздухом в последнем. При подозрении на дивертикул Ценкера всем больным необходимо проведение рентгеноконтрастного исследования. Обязательной является полипозиционная эзофагография, которая позволяет выявить дивертикул и оценить его положение. После прохождения перистальтической волны, в фазе расслабления мускулатуры пищевода, стенки дивертикула сглаживаются. Важным является динамическое наблюдение за пациентами с дивертикулом Ценкера для оценки времени опорожнения дивертикула.
По мнению Л.Г. Розенфельда (1966), для обнаружения дивертикулов пищевода имеют значение следующие моменты:
– качество контрастной массы, обеспечивающее ее попадание в полость дивертикула и визуализацию рельефа слизистой оболочки;
– последовательность рентгенологического исследования пищевода на всем протяжении и в разные фазы перистальтики;
– исследование пищевода в различных проекциях и при различных положениях тела больного;
– применение латеропозиции для определения размеров дивертикула;
– применение функциональных приемов для лучшего заполнения дивертикула.
По мнению автора, при составлении заключения рентгенологу необходимо учитывать:
1. уровень поражения;
2. расположение дивертикула на стенке пищевода;
3. размер и конфигурацию дивертикула;
4. длительность задержки контрастной массы в полости дивертикула;
5. наличие осложнений.
При нативной рентгенографии, с которой следует начинать любое рентгенологическое исследование, в ряде случаев можно выявить дивертикул, который представляет собой тень округлой формы с четкими контурами и горизонтальным уровнем. Чаще всего, дивертикул Ценкера заполняется контрастным веществом после первого глотка, при больших размерах дивертикула, контраст туго заполняет его, после чего начинает перетекать в пищевод [20].
Рентгенологически различают четыре стадии развития дивертикула Ценкера:
– в первой стадии дивертикул напоминает «шип розы»;
– вторая стадия дивертикула напоминает «булаву»;
– в третьей стадии дивертикул приобретает форму мешка, но не сдавливает пищевод;
– при четвертой стадии, дивертикул сдавливает пищевод и оттесняет его кпереди [18,20].
Алгоритм рентгенодиагностики при дивертикуле Ценкера:
1. Проведение подготовки больным с дивертикулом Ценкера.
Обследование проводится натощак, при наличии большого дивертикула, накануне, пищевод промывался теплой водой вечером и утром перед исследованием. Положение больного на правом боку с приведенной правой рукой под голову в течении 30 минут. Данный прием обеспечивает адекватную эвакуацию содержимого дивертикула перед исследованием.
2. Исследование начинается с прямой рентгенографии грудной клетки и шеи. Данная манипуляция позволяет оценить состояние костных структур, выявить те или иные заболевания легких и средостения, которые могут быть причиной образования тракционных дивертикулов. В ряде случаев на рентгенограмме можно обнаружить газ или уровень жидкости в дивертикуле.
3. Рентгеноконтрастное исследование следует проводить в режиме рентгеноскопии с выполнением рентгеновских снимков.
Соблюдение данного правила позволяет нам оценить проходимость, перистальтику, состояние слизистой оболочки и смещение пищевода. Для оценки проходимости исследование проводили с жидкой контрастной массой. Удостоверившись в проходимости пищевода, следует применять контрастную массу обычной консистенции. Больному предлагается набрать в рот взвесь сульфата бария и произвести множество мелких глотков. Таким образом, появляется пневморельеф пищевода и в большинстве случаев хорошо визуализируется рельеф слизистой оболочки. При наличии в дивертикуле зубчатого контура и утолщениях слизистой можно говорить о наличии дивертикулита (Рис. 2).
Оценивается наличие перистальтики пищевода. Особенностью является снижение перистальтики в области дивертикула или ее полное отсутствие, при этом перистальтика на противоположной стенке пищевода может прослеживаться. Обязательным является оценка степени сдавления пищевода дивертикулом (рис. 3,4).
4. Проведение исследования в разных плоскостях. При исследовании необходимо поворачивать больного и менять положение его тела. Такой прием позволяет вывести дивертикул в максимальном размере, оценить точное расположение дивертикула относительно стенок пищевода.
5. Применение раствора густого контраста.
Это в ряде случаев позволяет полностью заполнить дивертикул и оценить его эластичность.
6. Рентген - контроль с часовыми промежутками для оценки времени опорожнения дивертикула.
Соблюдение данных правил позволяет получить исчерпывающую информацию о локализации, размере, природе происхождения, состоянии слизистой оболочки дивертикула и времени его опорожнения (рис 5,6,7,8).
Стоит отметить, что компрессию пищевода необходимо оценивать по рентгеноконтрастным снимкам с густой бариевой взвесью в проекции максимального выведения устья дивертикула.
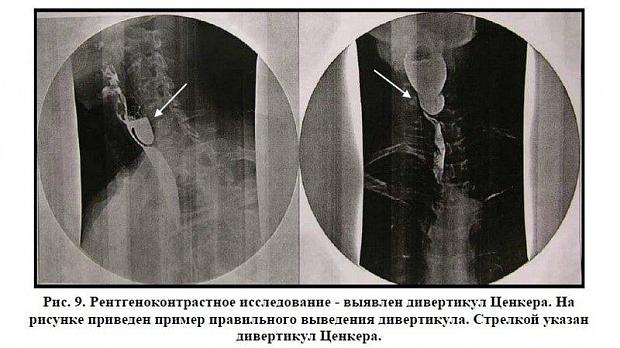
Обязательным является выполнение рентгеноконтрастного исследования в прямой проекции, полубоком с поворотом больного вправо на 30º - 45 º и отведением левого плеча назад. (Рис. 9,10).
В прямой проекции оценивается продольный размер дивертикула Ценкера, в полубоковых проекциях - поперечный размер дивертикула. В обеих проекциях оценивается глубина дивертикула Ценкера. За истинную глубину следует принимать максимальную величину измерения дивертикула в прямой и полубоковых проекциях.
При описании рентгеноконтрастного исследования, следует обращать внимания на различную форму дивертикула Ценкера. При заполнении дивертикула контрастным веществом у 10 (7%) больных выявлен не шаровидный дивертикул, а с перетяжкой в области его дна. При анализе литературы мы обратили внимание на описание клинических случаев с подобной рентгеноконтрастной картиной(рис. 11,12,13).
Размеры дивертикула Ценкера по данным проведенных рентгеноконтрастных исследований, приведены в таблице 4.
Таблица 4. Размеры дивертикула Ценкера по данным рентгеноконтрастных исследований.
|
Размеры дивертикула |
Количество больных |
|
Дивертикулы больших размеров > 6,0 см |
28 (20,6%) |
|
Дивертикулы средних размеров от 2,0 до 6,0 см |
103 (75,8%) |
|
Дивертикулы небольших размеров > 2,0 см. |
5 (3,6%) |
|
Всего |
136 (100%) |
Дивертикулы Ценкера в подавляющем большинстве имеют средние размеры. Почти у четверти больных встречаются дивертикулы больших размеров. С дивертикулами небольших размеров мы сталкиваемся редко, что объясняется неспецифичностью жалоб, предъявляемых больными в начальных стадиях заболевания.
ЭНДОСКОПИЧЕСКОЕ ИССЛЕДОВАНИЕ БОЛЬНЫХ ДИВЕРТИКУЛОМ ЦЕНКЕРА.
Большое значение в диагностике дивертикула Ценкера имеет эндоскопия. С помощью данной методики возможно оценить локализацию дивертикула, размеры и состояние его слизистой, а также место входа в пищевод и слизистую оболочку верхних отделов желудочно-кишечного тракта.
Внедряя эндоскопический метод исследования пищевода при различных заболеваниях, Б.В. Петровский и Э.Н. Ванцян в 40–50-х годах ХХ века имели опыт проведения более 1000 эзофагогастроскопий. С внедрением гибких эндоскопов ФЭГС заняла свое место в диагностике дивертикулов Ценкера.
Появилась возможность осмотреть слизистую оболочку самого дивертикула, и снизилось количество осложнений при исследовании [ 3, 8, 15].
Л.Н. Иншаков (1973) выполнил 1500 эзофагогастроскопий гибким эзофагоскопом «Олимпус», из них 45 по поводу дивертикулов пищевода. Так, у
3 больных был выявлен рак в дивертикуле, а у 22 пациентов признаки дивертикулита. Это подчеркивает необходимость динамического наблюдения за пациентами с дивертикулом пищевода с помощью эндоскопической методики [14].
Помимо визуального осмотра слизистой пищевода, необходимо проводить хромоскопию пищевода водным раствором Люголя и цитогистологическое исследование биопсионного материала. При эндоскопии пищевода необходима тщательная оценка следующих признаков:
– локализация дивертикула, его размеры, состояние устья, шейки и дна;
– степень компрессии пищевода дивертикулом Ценкера;
– характер содержимого мешка дивертикула;
– состояние слизистой оболочки дивертикула: воспаление (гиперемия, отек, пленки фибрина), эрозии и язвы, атрофия, рубцы, деформация, лейкоплакии, опухоли;
– перистальтика пищевода и ее влияние на форму дивертикула;
– эластичность стенок дивертикула.
Осматривая пищевод с дивертикулом, можно определить природу дивертикула. Так, при пульсионных дивертикулах имеется плавный переход неизмененной стенки пищевода на перистальтической волне. Такие дивертикулы нередко меняют форму, а тракционные дивертикулы имеют четкий вход в дивертикул и не изменяют свою форму [23, 24].
При эндоскопическом исследовании возможно выделить следующие виды дивертикулита:
1. Катаральный дивертикулит — слизистая оболочка в дивертикуле ярко гиперемирована и отечна, рыхлая, легко кровоточит при контакте с инструментом.
2. Атрофический дивертикулит — слизистая оболочка в дивертикуле истончена, серовато - розового цвета с выраженным сосудистым рисунком, эластичность слизистой оболочки не нарушена.
3. Эрозивно-язвенный дивертикулит — слизистая оболочка в дивертикуле ярко-красного цвета с наличием поверхностных и глубоких дефектов. Последние могут быть от точечных до 0,5 см, различных форм от округлой до полигональной. На слизистой оболочке может быть фибрин.
4. Рубцово - деформирующий дивертикулит — слизистая оболочка в дивертикуле белесоватая, неровная за счет рубцовой деформации, при инструментальной пальпации отмечается снижение эластичности и отсутствие смещаемости слизистой оболочки.
5. Фибринозно-гнойный дивертикулит — характеризуется наличием фибринозных наложений на стенках дивертикула.
6. Лейкоплакии. В дивертикуле имеются бляшковидные утолщения округлой формы, белесовато-серого цвета, слегка выступающие над поверхностью, размерами от 1 до 8 мм, плотноэластической консистенции.
7. Очаговые гиперплазии — слизистая оболочка в виде отдельных бляшек с гладкой поверхностью и полиповидные выросты, выступающие в просвет дивертикула.
8. Рак в дивертикуле.
Следует отметить некоторые особенности в подготовке больных к эндоскопическому исследованию при выявленном ранее дивертикуле пищевода:
1. Необходимо проведение специальной подготовки больного. При средних или больших дивертикулах Ценкера, особенно с явлениями дивертикулита, в нем остается пища и слизь. При этом осмотр дивертикула затруднен, становится невозможно оценить состояние слизистой оболочки, выявить возможные образования в дивертикуле и правильно определить его размеры. Данное обстоятельство делает эндоскопию не только малоинформативной, но и опасной для пациента из-за большого риска возможных осложнений.
Подготовка больного с дивертикулом Ценкера начинается с диеты. За два дня до исследования больной перестает принимать твердую пищу. При больших дивертикулах Ценкера, вечером накануне исследования больному выполняется промывание дивертикула с помощью зонда. Промывание дивертикула следует проводить, соблюдая следующие принципы:
– зондирование дивертикула является врачебной манипуляцией;
– зонд вводится очень аккуратно до 20–22 сантиметров, сразу за верхний пищеводный сфинктер;
– промывание дивертикула проводится в положении больного на животе с опущенным головным концом;
– промывание дивертикула проводится теплой водой до чистых вод.
В последние годы мы стараемся воздерживаться от промывания дивертикула с помощью зонда в связи с опасностью перфорации дивертикула.
Необходимость в такой подготовке, чаще всего возникает при дивертикулах большого размера и ранее неудачном эндоскопическом исследовании из-за наличия в нем кусочков пищи. В таком случае невозможно выполнить санацию дивертикула с помощью эндоскопа.
2. Больным дивертикулом Ценкера эзофагоскопия, чаще всего, проводится с анестезиологическим пособием. В каждом конкретном случае хирург, анестезиолог и эндоскопист принимают решение о методе анестезиологического пособия. Это снижает риск возможных осложнений при осмотре дивертикула. При осмотре больного с анестезиологическим пособием появляются следующие преимущества:
– удобство при проведении аппарата;
– отсутствие срыгивания воздуха во время манипуляции;
– возможность более длительного осмотра больного;
– выполнение манипуляций по забору биопсионного материала, ZOOM и NBI-эндоскопии;
– возможность выполнить промывание дивертикула и удаление содержимого;
– становится возможным проведение эндоскопической ультросонографии.
3. Эндоскопическое исследование проводится аппаратами с торцевой оптикой. Для лучшей визуализации дивертикула возможно использование дистального колпачка.
4. У пациентов с Ценкеровским дивертикулом при эндоскопическом осмотре обязательно осматриваются желудок и двенадцатиперстная кишка.
5. Диагностическое исследование у больных и интраоперационное пособие должны осуществляться одними специалистами.
При соблюдении вышеперечисленных рекомендаций у больных удается уменьшить риск возникновения осложнений, связанных с эндоскопическим исследованием, оценить состояние слизистой оболочки дивертикула и его размеры.
Перед врачом, выполняющим эндоскопию больным дивертикулом Ценкера, стоят следующие задачи:
– осмотр глоточно-пищеводного перехода и выявление в нем изменений;
– осмотр просвета пищевода и выявление дивертикула;
– измерение расстояния нахождения дивертикула от передних резцов;
– оценка места образования дивертикула по отношению к стенкам пищевода;
– оценка слизистой оболочки пищевода и дивертикула;
– измерение размеров дивертикула;
– оценка подвижности дивертикула;
– выявление других патологических изменений в пищеводе, желудке и двенадцатиперстной кишке.
При эзофагоскопии дивертикул пищевода имеет вид постоянного углубления в стенке пищевода, которое хорошо видно при инсуффляции воздуха в пищевод.
Слизистая оболочка в дивертикуле та же, что и в пищеводе. При наличии дивертикулита слизистая оболочка претерпевает ряд изменений воспалительного характера. При этом вход в пищевод суживается и имеет вид розетки.
При проведении эндоскопического исследования пищевода оценивался размер дивертикула. Для оценки размера дивертикула Ценкера использовался манипулятор типа струны с нанесенной сантиметровой градуировкой. Размер дивертикула оценивался при максимальной инсуффляции в дивертикул воздуха. Размеры дивертикула, полученные при эндоскопическом исследовании пищевода, приведены в таблице 5.
Таблица 5. Размеры дивертикула Ценкера по данным эзофагогастродуоденоскопии.
|
Размеры дивертикула |
Количество больных |
|
Дивертикулы больших размеров > 6,0 см |
25 (20,6%) |
|
Дивертикулы средних размеров от 2,0 до 6,0 см |
105 (74,8%) |
|
Дивертикулы небольших размеров < 2,0 см |
6 (4,6%) |
|
Всего |
136 (100%) |
Во время проведения эндоскопического исследования оценивались явления дивертикулита. (Таблица 6).
Таблица 6. Частота дивертикулита у больных с дивертикулом Ценкера.
|
Характер дивертикулита |
Количество |
|
| |
|
Катаральный дивертикулит |
64 (47,0%) |
|
Эрозивный дивертикулит |
54 (39,8%) |
|
Язвенный дивертикулит |
18 (13,2%) |
|
Отсутствие воспаления в дивертикуле |
— |
|
Всего |
136 (100%) |
Воспалительная реакция в дивертикуле наблюдалась у всех больных. Наибольшее количество больных (47%) имели проявления катарального дивертикулита, на втором месте больные с проявлениями эрозивного дивертикулита. Язвенный дивертикулит наблюдался у 18 больных. Надо отметить, что прослеживается связь между размером дивертикула и выраженностью дивертикулита. У больных с большими дивертикулами явление дивертикулита более выражены (рис.16,17 ).
При проведении эзофагогастродуоденоскопии у больных дивертикулом Ценкера нередко выявлялись различные заболевания верхних отделов желудочно- кишечного тракта. Наиболее частой патологией являются: эзофагит, хронический гастрит, дуоденит, язвенная болезнь желудка и двенадцатиперстной кишки, грыжа пищеводного отдела диафрагмы.
МЕТОДИКА ЭНДОСКОПИЧЕСКОГО ИССЛЕДОВАНИЯ БОЛЬНЫХ ДИВЕРТИКУЛОМ ЦЕНКЕРА.
При выполнении эзофагогастродуоденоскопии больным с жалобами на дисфагию, необходимо помнить, что возможной причиной дисфагии может быть дивертикул Ценкера. Выполнять эндоскопическое исследование данной группе больных следует после рентгеноскопии пищевода и желудка, во избежание возможных осложнений при эзофагогастродуоденоскопии. Одним из самых грозных осложнений является перфорация дивертикула. Рис. 18,19.
Желательно выполнять исследования под седацией. Следует использовать широко-просветный загубник, что обеспечивает дополнительную подвижность эндоскопа. Чаще дивертикул Ценкера находится на расстоянии 20-22 сантиметров от резцов. Проведение аппарата должно осуществляться строго под контролем зрения. При проведении эндоскоп свободно попадает в полость дивертикула. На данном этапе важно не травмировать слизистую оболочку дивертикула, и не перфорировать его эндоскопом. Во избежание возможных осложнений следует продвигать эндоскоп самостоятельно, не прибегая к помощи ассистента.
Осмотр полости дивертикула проводится при постоянной инсуфляции воздуха или СО2. Проводится оценка слизистой оболочки дивертикула, оценивается его размер. Для более точной оценки размера дивертикула, возможно использование струны с нанесённой сантиметровой меткой и гибким концом. Далее эндоскоп медленно выводится из дивертикула Ценкера. В области входа в дивертикул по передней стенке, при инсуффляции, имеется вход в дивертикул, который имеет вид розетки. Аппарат прижимается к передней стенке пищевода, визуализируется вход в пищевод. После визуализации просвета пищевода эндоскоп проводится далее. Данный этап исследования является наиболее сложным и должен выполняться врачом, имеющим достаточный опыт. Далее осмотр производится по общепринятой методике. При необходимости дополнительного осмотра «перегородки» между дивертикулом и пищеводом возможно применение следующего приёма: находясь в просвете желудка через инструментальный канал эндоскопа проводится струна- направитель. Аппарат выводится из пищевода, при этом струна подаётся в инструментальный канал, таким образом, чтобы её конец оставался в желудке. При достижении уровня глотки наличие струны помогает чётко визуализировать вход в пищевод, а при смещении дистального конца эндоскопа на 2-3 градуса струна оттесняет стенку дивертикула и становится возможным полноценная оценка «перегородки» между дивертикулом и пищеводом. При наличии дивертикула Ценкера больших размеров или технических затруднений мы прибегаем к использованию дистального колпачка для лучшей визуализации входа в пищевод.
ЭНДОСОНОГРАФИЧЕСКОЕ ИССЛЕДОВАНИЕ БОЛЬНЫХ С ДИВЕРТИКУЛОМ ПИЩЕВОДА.
Трансэзофагеальная ультрасонография используется для диагностики заболеваний пищевода, сердца и грудной аорты. Обследование пищевода наиболее часто проводится с целью определения степени инвазии опухоли в стенку пищевода, что дает возможность выбора адекватного хирургического пособия.
В нашем исследовании трансэзофагеальная ультрасонография использовалась, как дополнительный способ диагностики дивертикула Ценкера. С помощью данного метода имеется возможность оценить слои стенки пищевода в области дивертикула, состояние крикофарингеальной мышцы и окололежащие ткани. Исследование выполнялось с использованием радиального эндосоно- датчика UM-160.
Проведение трансэзофагеальной ультрасонографии у больных дивертикулом пищевода сопряжено с рядом технических сложностей и возможных осложнений.
Учитывая данные сложности, нами проводился тщательный отбор пациентов для проведения эндоскопической ультрасонографии. Критерии отбора пациентов:
– отсутствие у больного тяжелых соматических заболеваний;
– отсутствие значительных технических сложностей при проведении эндоскопии;
– согласие пациента на проведение данного исследования. Основные цели исследования:
1. выявить дивертикул;
2. оценить состояние стенок пищевода и дивертикула;
3. оценить состояние мышечного слоя пищевода и крикофарингеальной мышцы при дивертикуле Ценкера.
С помощью данной методики нами было обследовано 11 больных дивертикулом пищевода. У 4 пациентов имелся дивертикул Ценкера, у 7 — дивертикул средней трети пищевода.
Осложнений, обусловленных проведением данного исследования, нами отмечено не было.
Данные, полученные при исследовании пищевода с дивертикулом, свидетельствуют о наличии всех слоев пищевода в дивертикуле средней трети и отсутствии мышечного слоя у больных дивертикулом Ценкера.
Нами не было обнаружено связи дивертикула с окружающими тканями. Во всех случаях имелись неравномерное утолщение слизистой оболочки и признаки воспалительных явлений в окружающих дивертикул тканях. У всех больных с дивертикулом Ценкера удалось выявить гипертрофированную крикофарингеальную мышцу, которая имела вид тяжа толщиной до 1,0 сантиметра у входа в дивертикул. Эндосонографическое изображение дивертикула Ценкера представлено на рисунке 20.
УЛЬТРАЗВУКОВОЙ МЕТОД ИССЛЕДОВАНИЯ ШЕИ БОЛЬНЫХ ДИВЕРТИКУЛОМ ЦЕНКЕРА
Ультразвуковой метод исследования применялся нами как дополнительный у больных с подозрением на осложнения при дивертикуле Ценкера. При подозрении на перфорацию, используя ультразвуковое сканирование, возможно выявить жидкость вокруг дивертикула и наличие пузырьков воздуха в мягких тканях шеи. Также возможно выявить изменения тканей шеи при передивертикулите.
Исследование проводилось по стандартной методике. Исследование проводилось поверхностным датчиком на аппарате Siemens Sonoline G60 S. Шея осматривается с учетом анатомических зон.
Анатомические области последовательно изучались ультразвуковым методом. Наибольший интерес при выполнении ультразвукового исследования шеи больным дивертикулом Ценкера представляет передний треугольник шеи. При визуализации данной анатомической области у 31 больного дивертикулом Ценкера удалось визуализировать полость с уровнем жидкости.
Ультразвуковое изображение у больного дивертикулом Ценкера представлено на рисунках 21,22.
КОМПЬЮТЕРНАЯ ТОМОГРАФИЯ БОЛЬНЫХ ДИВЕРТИКУЛОМ ЦЕНКЕРА.
Компьютерная томография использовалась нами как дополнительный способ исследования у больных дивертикулом Ценкера. У трёх больных было выполнено исследование шеи и грудной клетки при подозрении на перфорацию дивертикула и у одного больного при осложненном течении послеоперационного периода. При использовании данного метода диагностики полость дивертикула отчётливо дифференцируется от окружающих тканей рис. 23, 24.
ЛЕЧЕНИЕ БОЛЬНЫХ ДИВЕРТИКУЛОМ ЦЕНКЕРА.
Принципиально возможно разделить лечение дивертикулов Ценкера на хирургическое и консервативное. В настоящее время большая часть врачей отдаёт предпочтение хирургическим методам лечения дивертикула Ценкера.
Показания к оперативному лечению дивертикула Ценкера связаны с их осложнениями. По мнению Э.Н. Ванцяна (1964), оперативное лечение показано:
– при больших дивертикулах (более двух сантиметров) с задержкой контрастной взвеси в дивертикуле;
– при небольших дивертикулах (менее двух сантиметров), но с длительной задержкой контрастного вещества (более двух минут при рентгенологическом исследовании);
– при выраженной клинической картине заболевания (дисфагия, срыгивание, рвота, боли за грудиной, в спине и другие), независимо от величины дивертикула;
– при осложнениях дивертикула пищевода (эзофаготрахеальный или эзофагобронхиальный свищ, изъязвления, кровотечения, полипоз, рак).
Показания для оперативного лечения дивертикула Ценкера описаны Н.А. Смирновой (2001), которая разделяет их на абсолютные и относительные.
К относительным показаниям относятся следующие:
1. Компрессионный синдром, проявляющийся сочетанными симптомами: а) дисфагия первой или второй степени;
б) гиперсаливация;
в) покашливания после приема пищи; г) одышка инспираторного характера; д) дисфония (преходящего характера);
е) венозный застой половины лица и шеи (после приема пищи); ж) синдром Горнера;
2. Выпячивание в области шеи.
3. Симптом Купера (шум в проекции дивертикула во время и после приема пищи).
4. Рвота после приема пищи.
5. Отрыжка воздухом и только что съеденной пищей.
6. Наличие признаков хронического дивертикулита (незначительные боли в проекции дивертикула и субфебрилитет).
7. Дисплазия эпителия, выстилающего полость дивертикула.
8. Дефицит массы тела от 5 до 10 кг.
К абсолютным показаниям для операции относятся:
1. Дисфагия третьей или четвертой степени.
2. Дефицит массы тела от 10 до 20 кг.
3. Наличие аспирационной пневмонии с последующим развитием абсцесса легкого.
4. Острый дивертикулит и перидивертикулит (выраженный болевой синдром в проекции дивертикула, фебрильная температура, резкие боли при глотании).
5. Кровотечение из полости дивертикула.
6. Перфорация дивертикула.
7. Медиастинит.
8. Развитие рака в дивертикуле Ценкера.
9. Безоар в полости фарингоэзофагеального дивертикула.
Необходимо учитывать и противопоказания. Так, по мнению профессора Н.К. Войтенка, к противопоказаниям можно отнести преклонный возраст больных, заболевания сердечно-сосудистой и дыхательной систем в стадии суб- и декомпенсации, хроническую печеночно-почечную недостаточность, а также дивертикулы небольших размеров, протекающие бессимптомно.
По нашему опыту лечения больных с дивертикулом Ценкера показаниями к оперативному лечению являются:
1. наличие клинически значимого дивертикула (дисфагия и явления дивертикулита);
2. перфорация дивертикула;
3. кровотечение из дивертикула;
4. Рак в дивертикуле;
Наличие клинически значимого дивертикула являлось показанием к плановому оперативному лечению, а перфорация дивертикула и кровотечение из его полости являлись показанием к оказанию экстренной хирургической помощи.
Нами не было выявлено ни одного дивертикула Ценкера без наличия дисфагии и явлений дивертикулита. У нескольких больных имелся дивертикул Ценкера средних размеров, диагноз которого был установлен несколько лет назад. Этих больных беспокоила дисфагия и другие симптомы, характерные для дивертикула Ценкера, однако больные воздерживались от предложенной операции или хирургическое лечение им не предлагалось. Все эти больные обращались к нам с симптомами прогрессирования дисфагии. По данным литературы, нами не было выявлено ни одного случая самоизлечения дивертикула Ценкера. Таким образом, показания к хирургическому лечению были у всех больных. Однако трое пациентов не были оперированы по причине отказа от операции (1 больной) или тяжёлой соматической патологии в преклонном возрасте (2 больных).
Пациентам, перед проведением хирургического лечения, проводится тщательная предоперационная подготовка, с учетом возраста, сопутствующих патологических изменений со стороны сердечно- сосудистой системы, органов дыхания, психологическая подготовка.
Особое внимание в подготовке следует уделить лечению дивертикулита. Всем больным дивертикулом Ценкера проводился курс противовоспалительной терапии. Больным в предоперационном периоде проводилась следующая подготовка:
– соблюдение диеты (прием жидкой и полужидкой пищи, химически и физически щадящее питание);
– сон с возвышенным головным концом на 15 градусов (данное положение тела предотвращает заброс содержимого дивертикула в глотку и верхние дыхательные пути);
– за сутки до операции полоскание ротоглотки более 10 раз в течение дня, в положении больного стоя и лежа на животе;
– промывание дивертикула с помощью зонда накануне операции (применялось у больных с большим размером дивертикула при наличии в нем остатков пищи);
– антибактериальная терапия за сутки до операции.
Наиболее распространенными способами хирургического лечения дивертикулов пищевода являются:
1. Открытые операции:
a) резекция дивертикула;
b) резекция дивертикула в сочетании с крикофарингеальной миотомией под контролем эндоскопической техники;
c) инвагинация дивертикула;
d) резекция дивертикула с укреплением линии швов твердой мозговой оболочкой.
6. Эндоскопические операции:
a) диатермическое рассечение мостика тканей между пищеводом и дивертикулом с рассечением нижней порции крикофарингеальной мышцы;
b) лазерные эндоскопические манипуляции;
c) эндоскопические вмешательства с применением сшивающих аппаратов.
ХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕ ДИВЕРТИКУЛОВ ЦЕНКЕРА (ОТКРЫТЫЕ ОПЕРАЦИИ).
При установленном диагнозе и наличии показаний к хирургическому лечению перед врачом появляется сложная задача — выбор оптимального способа лечения. Способ лечения зависит от возраста пациента, размеров дивертикула, технической возможности и опыта хирурга.
В настоящее время предпочтение отдается малоинвазивным способам лечения дивертикула Ценкера, однако в ряде случаев приходится прибегать к открытым операциям. При наличии таких осложнений как перфорация дивертикула, кровотечения из дивертикула, подозрении на рак в дивертикуле и наличии выраженного передивертикулита больным показано традиционное оперативное лечение.
В настоящее время общепринятой открытой операцией является резекция дивертикула Ценкера с крикофарингеальной миотомией. Изолированная резекция дивертикула Ценкера не воздействует на основной этиологический фактор образования дивертикула и не является радикальной. Выполнение рассечения нижней порции крикофарингеальной мышцы делает операцию радикальной. В клиниках, имеющих техническую возможность, данная операция проводится с эндоскопическим ассистированием.
Для выполнения резекции дивертикула с крикофарингеальной миотомией под контролем эндоскопической техники в операционной, необходимо наличие эндоскопической стойки и бригады эндоскопистов. Желательно, чтобы эти же врачи ранее выполняли больному эндоскопическое исследование верхних отделов желудочно – кишечного тракта. Хирургическая бригада состоит из оператора и двух ассистентов. В нашей клинике методика операции резекции дивертикула Ценкера с крикофарингеальной миотомией была модернизирована с учётом анализа послеоперационных осложнений и возможностей современной эндоскопии. Преимущества резекции дивертикула Ценкера с крикофарингеальной миотомией под контролем эндоскопической техники над стандартной резекцией дивертикула:
– отсутствие рецидива заболевания при адекватно выполненной операции;
– визуализация дивертикула при выполнении оперативного доступа;
– облегчение мобилизации дивертикула из окружающих тканей;
– улучшение визуализации волокон крикофарингеальной мышцы;
– сведение к минимуму послеоперационного сужения пищевода;
– возможность проведения пробы на герметичность пищеводных швов.
Перечисленные преимущества позволяют произвести адекватную операцию и уменьшить возможность послеоперационных осложнений и рецидива заболевания.
Оперативный доступ возможно выполнить воротникообразным разрезом по передней поверхности шеи. Однако, чаще оперативным доступом является левосторонний разрез по медиальному краю грудино- ключично-сосцевидной мышцы. В нашей клинике предпочтение отдаётся левостороннему колярному доступу.
Положение больного на операционном столе на спине, с повернутой в правую сторону головой. Под шею подкладывается валик, как при операциях на щитовидной железе.
Больным проводится интубационный наркоз. После обработки и ограничения операционного поля выполняется эзофагоскопия, целью которой является оценка состояния подготовки пищевода, дивертикула и оценка правильности положения больного. Далее осуществляется хирургический доступ. Кожа и подкожная клетчатка рассекается по внутреннему краю грудино- ключично-сосцевидной мышцы. После этого рассекается m. platysma по медиальному краю грудино-ключично-сосцевидной мышцы. Рассекалась поверхностная пластинка шейной фасции (lamina superficialis fasciae cervicalis).
У трех пациентов для лучшей визуализации фарингоэзофагеальной зоны была пересечена m. omohyoideus. Во время осуществления доступа эндоскоп находится в пищеводе. Подсветка помогает хирургу выделить зону глоточно- пищеводного перехода. При осуществлении данного доступа следует соблюдать осторожность и иметь строгий визуальный контроль, так как рядом находятся крупные магистральные сосуды и нервы.
После выделения фарингоэзофагеальной зоны эндоскоп подводится к дивертикулу и производится инсуфляция в просвет дивертикула. При этом эндоскоп должен располагаться, таким образом, чтобы обеспечить подсветку дивертикула. Данный этап операции представлен на рисунках 25,26,27.
Подобный прием в значительной степени облегчает выделение дивертикула из окружающих тканей.
Выделять дивертикул следует преимущественно тупым путем, что в большей степени предохраняет его от повреждения.
После выделения дивертикула эндоскоп вводится в пищевод и далее трансиллюминация производится из его просвета. В условиях подсветки четко визуализируются волокна крикофарингеальной мышцы, что позволяет полноценно выполнить миотомию. Которая заключается в полном рассечении волокон m. cricopharyngeus в поперечном направлении и рассечении в продольном направлении мышечной оболочки пищевода на протяжении 4–5 сантиметров до подслизистого слоя. Рассечение данной мышцы приводит к нормализации пищеводного давления в области глоточно-пищеводного перехода.
Выделение нижней порции крикофарингеальной мышцы представлено на рис. 28.
В момент резекции дивертикула Ценкера эндоскоп должен находиться в просвете пищевода. Таким образом, резекция и наложение швов происходят на эндоскопе, что дает уверенность в проходимости пищевода и делает маловероятным послеоперационный стеноз пищевода.
Дивертикул захватывают окончатым зажимом и выводят в рану. На шейку дивертикула накладывается сшивающий аппарат УО-40. Резекция дивертикула Ценкера представлена на рис. 29.
Проводится наложение механического шва, после чего выполняется резекция дивертикула, с последующей обработкой линии швов раствором антисептика.
Сшивающий аппарат снимается и производится визуальный контроль механического шва. Затем накладывается 2-рядный узловой шов атравматичной иглой.
Основной этап считается законченным после проверки герметичности. Для этого проводится «водная проба». Рана заполняется физиологическим раствором и по указанию хирурга, врач-эндоскопист выводит аппарат в режиме инсуфляции, при этом осматривается линия швов со стороны просвета пищевода. Хирург, в свою очередь, определяет наличие пузырьков воздуха в ране. При отсутствии пузырьков пищевод ушит герметично — «водная проба» отрицательна.
Проведение «водной пробы» представлено на рис. 30,31.
Далее проводится контроль гемостаза, послойное ушивание раны с дренированием по Редону. Рана ушивается узловыми швами. Данный этап операции представлен на рис. 32.
Операция заканчивается наложением асептической повязки и проведением назогастрального зонда.
Препарат представлял собой резецированный дивертикул с измененной слизистой оболочкой. Изменение слизистой соответствовало дивертикулиту (рис. 33, 34).
В ряде случаев выполнялась не резекция, а инвагинация дивертикула в просвет пищевода после рассечения нижней порции крикофарингеальной мышцы. Данная методика была выполнена больным с небольшим дивертикулом Ценкера, размером до 3,0 сантиметров. При данной операции выполняют доступ как при резекции дивертикула Ценкера, с последующим выделением фарингоэзофагеальной зоны. Затем погружают дивертикул в просвет пищевода с помощью 2–3 П-образных швов (метод Жирара). Помимо применения П- образных швов возможно применять узловые швы для погружения дивертикула в просвет пищевода, а также кисетный шов. Данное операционное вмешательство позволяет уменьшить риск возможной несостоятельности швов пищевода.
ПОСЛЕОПЕРАЦИОННЫЙ ПЕРИОД У БОЛЬНЫХ ПОСЛЕ РЕЗЕКЦИИ ДИВЕРТИКУЛА ЦЕНКЕРА С КРИКОФАРИНГЕАЛЬНОЙ МИОТОМИЕЙ ПОД КОНТРОЛЕМ ЭНДОСКОПИЧЕСКОЙ ТЕХНИКИ.
Послеоперационный период у больных с резекцией дивертикула Ценкера с крикофарингеальной миотомией под контролем эндоскопической техники имеет ряд особенностей. В послеоперационном периоде больные получают зондовое питание и инфузионную терапию. На третьи сутки послеоперационного периода выполняется рентгеноскопия с водорастворимым контрастом — при отсутствии затеков разрешается принимать воду и жидкую пищу помимо зонда, затем зонд удаляется, и больной переходит на самостоятельное питание.
Послеоперационная рана осматривается на первые сутки послеоперационного периода. При отсутствии экссудата — удаляется активный дренаж по Редону.
Дренирующая трубка при этом оставляется под повязкой. На вторые сутки после операции проводится перевязка с удалением дренажной трубки. Швы снимались на 7–8 сутки после операции.
У больных, оперированных в нашей клинике, осложнений в послеоперационном периоде не наблюдалось. По литературным данным возможны следующие осложнения при выполнении данной операции:
– инфицирование послеоперационной раны шеи;
– несостоятельность пищеводных швов;
– развитие медиастинита;
– сужения области глоточно-пищеводного перехода.
К наиболее сложным интраоперационным осложнениям относят ранение крупных сосудов, сопровождающихся обильным кровотечением.
ЭНДОСКОПИЧЕСКИЕ МЕТОДЫ ЛЕЧЕНИЯ ДИВЕРТИКУЛА ЦЕНКЕРА.
В современной медицине наблюдается тенденция перехода к малоинвазивным операциям во всех областях хирургии. Малоинвазивная хирургия имеет ряд преимуществ над открытыми операциями:
– уменьшение операционной травмы;
– уменьшение количества возможных осложнений;
– эстетическое превосходство.
Применимые малоинвазивные методики лечения дивертикула Ценкера, сводятся к эндоскопическому рассечению нижней порции крикофарингеальной мышцы. [7,13,28,30,32,36,37,42,43]. При пересечении нижней порции крикофарингеальной мышцы, осуществляется воздействие на основной этиологический фактор дивертикула Ценкера. Полость дивертикула объединяется с просветом пищевода, а избыток слизистой сокращается (Рис. 35).
ЭНДОСКОПИЧЕСКАЯ БАЛЛОННАЯ ДИЛАТАЦИЯ ГЛОТОЧНО- ПИЩЕВОДНОГО ПЕРЕХОДА С ВВЕДЕНИЕМ ПРЕПАРАТА «ДИСПОРТ» В ОБЛАСТЬ КРИКОФАРИНГЕАЛЬНОЙ МЫШЦЫ.
Трем больным с дивертикулом Ценкера была проведена эндоскопическая баллонная дилатация глоточно-пищеводного перехода с введением препарата
«Диспорт» в область крикофарингеальной мышцы. Данная методика была разработана нами в 2008 году, на основе патогенеза дивертикула Ценкера и наличием опыта в лечении больных кардиоспазмом, с успешным применением ботулотоксина у данной группы больных. В патогенезе кардиоспазма и дивертикула Ценкера имеется сходство в этиологии (наличие мышечного спазма). Суть операции заключается в баллонной дилатации, что обеспечивает растяжение m. cricopharyngeus, и введении препарата «Диспорт» в область данной мышцы.
Препарат «Диспорт» относится к группе миорелаксантов. Действующим началом препарата является токсин Clostridium botulinui типа А, который блокирует высвобождение ацетилхолина в нервно- мышечном соединении.
Операция выполнялась неоднократно, для достижения стойкого эффекта манипуляция повторялась через день. В первый сеанс больному проводили баллонную дилатацию, с введением 250 единиц препарата «Диспорт». Второй сеанс проводили на следующей день в том же объеме.
МЕТОДИКА ЭНДОСКОПИЧЕСКОЙ БАЛЛОННОЙ ДИЛАТАЦИИ С ВВЕДЕНИЕМ ПРЕПАРАТА «ДИСПОРТ» В ОБЛАСТЬ КРИКОФАРИНГЕАЛЬНОЙ МЫШЦЫ.
Предоперационная подготовка не отличалась от таковой при проведении открытых операций.
Укладка больного на операционном столе в положении на спине, больному проводится интубационный наркоз, после чего пациента поворачивали на левый бок. Выполнялась эндоскопическое исследование. Оценивалась подготовка больного к операции, размеры дивертикула и состояние верхних отделов желудочно-кишечного тракта. Осмотр и дальнейшие манипуляции следует проводить с надетым на торцевую часть эндоскопа колпачком, который значительно увеличивает поле зрения и облегчает выполнение процедуры (Рис. 36).
Следующим этапом выполняется проведение струны - направителя. Струна проводится через инструментальный канал эндоскопа в желудок. Затем аппарат удаляется таким образом, чтобы струна оставалась в просвете желудка (Рис. 37).
По проведенной струне в пищевод проводится баллонный дилататор и осуществляется его наполнение физиологическим раствором. Заполнение дилататора осуществляется через манометр до 1,5 атмосфер. После достижения данного давления, дилататоры оставляют в просвете пищевода на 30 минут. Уровень нахождения дилататора контролируется визуально (Рис. 38).
Особой проблемой установки дилататора является ненадежность фиксации в данной анатомической области. При заполнении баллона раствором, дилататор может смещаться. Поэтому дилататор необходимо фиксировать на уровне загубника.
Через 30 минут дилататор удаляют. После этого проводят визуальный контроль. После дилатации, дивертикул уменьшается в размерах. Эндоскоп проходит в пищевод свободно. Проводится эндо-УЗИ глоточно-пищеводного перехода, которое позволяет определить гипертрофированную часть крикофарингеальной мышцы. С помощью инъектора в область m. cricopharyngeus вводится 250 единиц препарата «Диспорт». Методика введения представлена на рисунках 39,40.
Операция заканчивается контрольным осмотром зоны глоточно- пищеводного перехода.
В послеоперационном периоде больным разрешается принимать жидкую щадящую пищу с первого дня. На 3–4-е сутки больные употребляли твердую пищу. В течение первых дней больные предъявляли жалобы на боли в горле. Других жалоб отмечено не было.
Через три недели больным проводилась дилатация глоточно-пищеводного перехода по вышеописанной методике. Перед повторной дилатацией больным проводилось рентгеноконтрастное исследование, на котором определялся дивертикул меньших размеров, чем до начала лечения. Опорожнение дивертикула проходило быстро. Наложение рентгенограмм с совмещением костных структур до и после введения препарата «Диспорт» в крикофарингеальную мышцу представлено на рисунке 41.
На рисунке представлены два снимка больного дивертикулом Ценкера. Снимки наложены друг на друга с совмещением костных структур. Первый снимок выполнен до проведения больному эндоскопической баллонной дилатации с введением препарата «Диспорт» в область крикофарингеальной мышцы. Второй сделан спустя три недели после проведения манипуляции. На рисунке видно, что дивертикул значительно уменьшился в размере, явления дисфагии регрессировали.
За двумя больными ведётся наблюдение в течение 6 лет, прогрессирование симптомов характерных для дивертикула Ценкера не наблюдается.
Преимуществом данного метода является максимальная малоинвазивность, так как при применении данной методики не выполняется разрезов, а желаемый эффект достигается путём растягивания мышечных волокон крикофарингеальной мышцы и медикаментозного воздействия.
Недостатками метода является дороговизна препарата «диспорт», и возможность применения данного метода при не больших размерах дивертикула Ценкера.
МЕТОД ЭНДОСКОПИЧЕСКОГО РАССЕЧЕНИЯ СЛИЗИСТОЙ ОБОЛОЧКИ И НИЖНЕЙ ПОРЦИИ КРИКОФАРИНГЕАЛЬНОЙ МЫШЦЫ БОЛЬНЫМ ДИВЕРТИКУЛОМ ЦЕНКЕРА.
Данная методика получила наибольшее распространение в мировой практике малоинвазивного лечения дивертикула Ценкера. Большой вклад в продвижении данной методики принадлежит итальянскому профессору Алессандро Репичи. Методика может проводиться с применением двухлепестковой трубки, или с применением дистального колпачка и СО2 инсуфлятора. В последние годы в мировой практике, чаще используют метод, с применением дистального колпачка и СО2 инсуфлятора. Обладая опытом в хирургии пищевода и оперативной эндоскопии, данный метод был нами модернизирован. В настоящее время в нашей клинике выполняется эндоскопическое рассечение слизистой оболочки и нижней порции крикофарингеальной мышцы больным с дивертикулом Ценкера. Основные отличия нашей методики заключаются в следующем:
– применение модернизированной нами двухлепестковой трубки;
– клипирование дефекта слизистой после рассечения m. Cricopharyngeus;
– проведение назогастрального зонда для питания.
Операционная должна быть оснащена эндоскопической стойкой, СО2 инсуфлятором и набором необходимых инструментов. В нашей клинике для проведения данной операции используются эндоскопическая стойка фирмы
«Olympus» (Рис. 42), СО2 инсуфлятор фирмы «Olympus» (Рис. 43), струна (Рис. 44), игольчатый электронож «Olympus» (Рис. 45), клипатор и различные клипсы
«Olympus» (Рис. 46), двухлепестковая трубка собственного изготовления.
Исследование выполняется торцевым эндоскопом «Олимпус» GIF-Q165.
Операция проводится под эндотрахеальным наркозом. Больному, в положении на левом боку, под шею укладывается валик. Затем выполняется эндоскопическое исследование для оценки состояния глоточно-пищеводного перехода и дивертикула. Для выполнения рассечения слизистой оболочки и нижней порции крикофарингеальной мышцы необходимо проводить процедуру без подачи воздуха через аппарат. В случае проводимой инсуфляции возрастает вероятность послеоперационных осложнений, связанных с попаданием инфицированного воздуха в клетчаточные пространства шеи и груди, допустимо применение инсуфляции углекислым газом. Также нами отмечены значительные технические сложности при работе эндоскопом в области глоточно- пищеводного перехода. Учитывая данные особенности и опыт зарубежных коллег, нами была изготовлена двухлепестковая трубка. Данная трубка должна обеспечивать фиксацию «мостика» между дивертикулом и пищеводом, выполнять каркасную функцию, что позволит проводить манипуляцию без подачи воздуха через эндоскоп. Для выполнения манипуляции двухлепестковая трубка должна свободно гнуться и иметь достаточный просвет для раскрытия клипс. Двухлепестковая трубка представлена на рис. 47 и 48.
Двухлепестковая трубка соответствует следующим характеристикам:
– гофрированная трубка с колпачком;
– двухлепестковое строение колпачка (лепесток, проводимый в пищевод, длиннее на 0,5 см);
– длина трубки — 35 см;
– диаметр трубки на всем протяжении — 1,5 см.
Перед началом операции данную трубку необходимо надеть на эндоскоп. В пищевод по инструментальному каналу эндоскопа проводится струна-направитель. Эндоскоп вводится в просвет пищевода ниже дивертикула, с аппарата в область дивертикула устанавливается двухлепестковая трубка (Рис. 49).
Более длинный лепесток проводится в пищевод, короткий лепесток в дивертикул. После установки двухлепестковой трубки обязательным является отключение подачи воздуха через эндоскоп. В ряде случаев возникают сложности с проведением двухлепестковой трубки. Данные сложности обусловлены узким входом в дивертикул или избытком слизистой оболочки, в таких случаях больным проводилась операция с инсуфляцией углекислым газом и применением дистального колпачка. Затем осуществляется рассечение «мостика» между пищеводом и дивертикулом с пересечением нижней порции крикофарингеальной мышцы с помощью игольчатого электроножа (рис. 50,51).
Закрытие дефекта слизистой оболочки осуществляется клипированием.
Наиболее оптимальным является применение клипс HX 610-135L (Рис. 52).
При удалении двухлепестковой трубки всегда наблюдается сокращение полости дивертикула, вплоть до полного его исчезновения.
Операция заканчивается постановкой назогастрального зонда по струне- направителю.
Ведение больных в послеоперационном периоде имеет некоторые особенности. Учитывая наличие раны в пищеводе и отсутствие возможности проверить наложенные клипсы на герметичность, больному удлиняется срок зондового питания. На этапе освоения метода рентгеноконтрастное исследование пищевода проводилось нами на десятые сутки послеоперационного периода. При отсутствии затеков контрастного вещества разрешалось пить воду. На следующий день назогастральный зонд удаляли и больным разрешалось самостоятельное питание. В последние время срок зондового питания сокращён до 5 суток Рис. 53.
Водорастворимое контрастное вещество свободно проходит по пищеводу.
В области операции визуализируются клипсы. Стрелкой указаны клипсы.
Эффективность данной методики подтверждается полным регрессом клинических симптомов и результатами проведенного рентгеноконтрастного исследования (рисунки 54,55 до операции. Рисунки 56,57 после операции).
ОСОБЕННОСТИ И ИНТРАОПЕРАЦИОННЫЕ СЛОЖНОСТИ ПРИ ПРОВЕДЕНИИ ЭНДОСКОПИЧЕСКОГО РАССЕЧЕНИЯ НИЖНЕЙ ПОРЦИИ КРИКОФАРИНГЕАЛЬНОЙ МЫШЦЫ.
1. У четырех больных наблюдалось полное сокращение полости дивертикула после рассечения нижней порции крикофарингеальной мышцы, что вызывало трудности при клипировании дефекта слизистой оболочки. У двух больных клипирование было выполнено в просвете двухлепестковой трубки, у двух больных пришлось прибегнуть к СО2 инсуфляции с применением дистального колпачка.
2. При устранении дивертикулов Ценкера больших размеров, во время рассечения слизистой оболочки «мостика» с последующим рассечением нижней порции крикофарингеальной мышцы, края раны раскрываются широко, уходя за пределы двухлепестковой трубки, что приводит с существенным техническим трудностям, при дальнейшем клипировании дефекта. В таких случаях нами производится рассечение части мышечных волокон нижней порции крикофарингеальной мышцы до раскрытия раны на расстояние 1-2 мм до краёв двухлепестковой трубки. Затем на края дефекта накладываются 2 клипсы, которые препятствуют выходу краёв раны за пределы трубки во время дальнейшего досечения мышечных волокон крикофарингеальной мышцы.
ОТДАЛЕННЫЕ РЕЗУЛЬТАТЫ И ПОСЛЕОПЕРАЦИОННЫЕ ОСЛОЖНЕНИЯ У БОЛЬНЫХ С ЭНДОСКОПИЧЕСКИМ РАССЕЧЕНИЕМ НИЖНЕЙ ПОРЦИИ КРИКОФАРИНГЕАЛЬНОЙ МЫШЦЫ.
У 9 больных после проведения рассечения нижней порции крикофарингеальной мышцы в течение 6 месяцев отмечено появление клинических симптомов характерных для дивертикула Ценкера. Симптоматика была умеренно выраженной, и уровень дисфагии не превышал первой степени.
По данным рентгенологического контроля выявлена остаточная полость дивертикула Ценкера. Результаты рентгеноконтрастного исследования до операции и через 6 месяцев после операции (рисунки 58,59).
При контрольном эндоскопическом исследовании у данных больных была выявлена остаточная полость дивертикула Ценкера (рисунки 61,62).
Стоит отметить, что на представленных рисунках (58-60), на рентгеновских снимках и на контрольном эндоскопическом исследовании - вход в пищевод свободный. Компрессия пищевода дивертикулом Ценкера отсутствует, что связано с рассечением большинства волокон нижней порции крикофарингеальной мышцы. Однако клинически у данной группы больных отмечаются незначительные затруднения при проглатывании твердой пищи.
Данной группе больных было выполнено повторное рассечение нижней порции крикофарингеальной мышцы (рис 62,63,64,65).
Рецидив заболевания был связан с неполным рассечением мышечных волокон при первичной операции. После досечения нижней порции крикофарингеальной мышцы у всех больных данной группы отмечался регресс клинической симптоматики и отсутствие дивертикула при контрольных рентгеновских исследованиях.
Данным больным мы проводим динамическое наблюдение с периодичностью рентгеноконтрастного исследования 1 раз в 6 месяцев. (Рис. 66,67 – до операции, Рис. 68,69 – через 6 месяцев после операции (эндоскопического рассечения нижней порции крикофарингеальной мышцы).
У одной больной через 2 часа после операции отмечались выраженные боли в грудной клетке, на мультиспиральной компьютерной томографии выявлен правосторонний гидроторакс с высокими цифрами амилазы (7000 ед./л.) в транссудате. На 9 сутки послеоперационного периода при рентгеноскопии подозрение на затек водорастворимого контраста.
Через 42 дня после операции выявлен абсцесс переднего средостения, который был дренирован под контролем ультразвука рисунки 70,71.
Больная выписана в удовлетворительном состоянии, при повторном рентгеноскопическом исследовании дивертикула Ценкера затеков контрастного вещества не выявлено.
Кровотечение из рассеченных волокон крикофарингеальной мышцы наблюдалось нами у 14 больных (Рис. 72).
В 11 случаях был выполнен комбинированный эндоскопический гемостаз методом коагуляции и клипирования. У трех больных мы прибегали к применению СО2 инсуфлятора с удалением двухлепестковой трубки и применением торцевого колпачка с последующим эндоскопическим гемостазом. Во всех случаях кровотечение было остановлено эндоскопически.
ЭНДОСКОПИЧЕСКОЕ ЛЕЧЕНИЕ ДИВЕРТИКУЛА ЦЕНКЕРА С ПРИМЕНЕНИЕМ CO2 ЛАЗЕРА.
Эндоскопическое лечение дивертикула Ценкера с применением CO2 лазера использовалось в Оденсе, Дания, начиная с 1989 г.
Операция начинается с эндоскопического осмотра верхних отделов желудочно-кишечного тракта для уточнения анатомии. Далее дивертикулоскоп (по Benjamin—Hollinger) вводится в пищевод для визуализации тканевой перегородки, разделяющей просвет пищевода с одной стороны и полость дивертикула — с другой. Тканевая перегородка рассекается от вершины до основания с применением CO2 лазера, который встроен в микроманипулятор.
Адекватность рассечения перегородки оценивают под встроенным микроскопом [13, 24, 34, 41, 43, 45, 50].
Электрокоагулятор используется в случаях кровотечения, если кровоостанавливающий эффект лазера был недостаточным. Введение антибиотиков, обычно Cefuroxim (1,5 г i.v.), начинается во время операции и продолжается по 750 мг каждые 8 часов. Курс антибиотиков прекращается на второй послеоперационный день, если послеоперационный период протекает без осложнений. Нами данная методика не применялась в связи с недостаточной оснащённостью и отсутствием опыта работы с CO2 лазером.
ЭНДОСКОПИЧЕСКАЯ ДИВЕРТИКУЛОЭЗОФАГОСТОМИЯ ЦЕНКЕРОВСКОГО ДИВЕРТИКУЛА С ПРИМЕНЕНИЕМ СШИВАЮЩИХ УСТРОЙСТВ.
Для выполнения данного оперативного пособия используется гибкая эндоскопия и жесткий сшивающий аппарат. Хирургическая процедура выполняется под наркозом согласно технике, описанной Collard et al. (1989).
После того как мешок дивертикула санирован и осмотрен, перегородка дивертикула осматривается дивертикулоскопом с двумя концами. Сшивающее устройство Endo GIA 30 вводится измененным концом в основание (дно) дивертикула, а лезвие картриджа со сшивающим устройством (скобы) — в пищевод (Рис. 73).
Надлежащее положение сшивающего устройства проверяется с помощью эндоскопов 0° или 30°.
Сшивающее устройство закрывается, в одну манипуляцию общая стенка (включая m. cricopharyngeus) между полостью дивертикула и шейным отделом пищевода рассекается, а края раны соединяются трехступенчатым рядом скоб (3,5 мм) с каждой стороны.
После извлечения сшивающего устройства производится контроль миотомии. Это в большей степени важно, чтобы избежать оставления остаточной перегородки. Если дивертикулоскоп Weerda не может быть введен в дивертикул по анатомическим причинам, перегородка дивертикула подвергается воздействию более тонкого дивертикулоскопа (Karl Storz), и выполняется миотомия с помощью CO2 лазера [18,54, 57, 65, 90, 106].
В нашей клинике данная методика лечения дивертикула Ценкера не применяется. Недостатком данного метода является отсутствие визуального контроля во время миотомии. По данным литературы, в России имеется небольшой опыт применения данной методики с положительным результатом. Данная методика чаще применяется отоларингологами совместно с эндоскопистами.
В настоящее время малоинвазивные методики занимают ведущие позиции в развитии хирургии. Применение эндоскопических операций при дивертикуле Ценкера дают хороший клинический результат при минимальной операционной травме.
Список литературы:
2. Брусиловский, Е.А. Опыт рентгенологического исследования пищевода с профилактической целью / Е.А. Брусиловский. — 1975. — № 7. — Том XLIII. — С. 42–44
3. Ванцян, Э.Н. Клиника и диагностика дивертикулов пищевода / Э.Н. Ван- цян : автореф. дис. … докт. мед. наук. — 1964. — 25 с
4. Ванцян, Э.Н. Хирургия. Хирургическое лечение осложненных дивертикулов пищевода / Э.Н. Ванцян, А.М. Корчак, М.М. Кебедов. — 1986. — № 4. — С. 103–107.
5. Ванцян, Э.Н. Дивертикулы пищевода и принципы их хирургического лечения / Э.Н. Ванцян, В.И. Чисов // Грудная хирургия. — 1968. — № 4. — С. 84–93.
6. Василенко, В.Х. Хирургия желудочно-кишечного тракта / В.Х. Василенко, А.Л. Гребенев, М.М. Сальман. — М.: Медицина, 1971. — 407 с.
7. Войтёнок, Н.К. Диагностика и лечение дивертикулов пищевода / Н.К. Войтёнок, А.А. Хартоник // Вестник хирургии. — 1988. — № 2. — С. 36– 38.
8. Гаджиев, С.А. Дивертикулы пищевода и их хирургическое лечение / С.А. Гаджиев // Вестник хирургии. — 1964. — № 8. — С. 41–46.
9. Гайворонский И. В. Нормальная анатомия человека. //
10. Голубев, Д.Б. К этиологии дивертикулов пищевода (к 225-летию первого сообщения о дивертикулах пищевода) / Д.Б. Голубев // Вестник рентгено- логии и радиологии. — 1995. — № 1. — С. 31–34.
11. Дориомедова, Л.Н. Рентгендиагностика дивертикулов пищевода / Л.Н. До¬риомедова : дис. … канд. мед. наук. — 1966. — 241 с.
12. Земляной, А.Г. Дивертикулы желудочно-кишечного тракта / А.Г. Земля- ной. — Л., 1970. — С. 19–32.
13. Ивашкин, В.Т. Эндоскопические операции при ценкеровском дивертикуле / В.Т. Ивашкин, А.С. Трухманов // Болезни пищевода. — М., 2000. — С. 162–165.
14. Иншаков, Л.Н. Эндоскопическая диагностика дивертикулов пищевода / Л.Н. Иншаков // Клиническая медицина. — 1973. — № 6. — С. 74–76.
15. Каган, Е.М. Рентгендиагностика заболеваний пищевода / Е.М. Каган. — М.: Медицина, 1968. — 226 с.
16. Королёв, Б.А. Хирургическое лечение больших дивертикулов пищевода / Б.А. Королёв // Учёные труды Горьковского государственного медицинского института им. С.М. Кирова. Вопросы анестезиологии и грудной хирургии. — 1962. — Том IV. — С. 397–407.
17. Лазаревич, Л.Ф. Клинико-рентгенологическое исследование дивертикулов пищеварительного канала : автореф. дис. … канд. мед. наук / Л.Ф. Лаза¬ревич. — Л., 1963. — 13 с.
18. Петровский, Б.В. Дивертикулы пищевода / Б.В. Петровский, Э.Н. Ван- цян. — М., 1968. — 183 с.
19. Петровский, Б.В. О хирургическом лечении дивертикулов пищевода / Б.В. Петровский // Хирургия. — 1961. — № 6. — С. 3–9.
20. Розенфельд, Л.Г. Рентгендиагностика дивертикулов пищевода и их ослож¬нений : автореф. дис. … канд. мед. наук / Л.Г. Розенфельд. — Киев, 1966. — 15 с.
21. Розенфельд, Л.Г. О злокачественном перерождении дивертикулов пище- вода / Л.Г. Розенфельд, Ф.И. Гондя // Врачебное дело. — 1962. — № 6. — С. 23–26.
22. Ротемберг, М.И. К этиологии дивертикулов пищевода / М.И. Ротемберг // Вестник рентгенологии и радиологии. — 1995. — № 1. — С. 31–34.
23. Сайдёнова, М.С. Дивертикулы пищевода, клинико-эндоскопическая диагностика / М.С. Сайдёнова, Л.Н. Иншаков. — СПбМАПО, 2000. — 15 с
24. Смирнова, Н.А. Дивертикул Ценкера : автореф. дис. … канд. мед. наук / Н.А. Смирнова. — СПб., 2001. — 23 с.
25. Стегний К.В. Малоинвазивное лечение пациентов с дивертикулами Ценкера. / Стегний К.В., Крекотень А.А., Агапов М.И. Владивосток / XII Съезд Российского Общества Эндоскопических Хирургов С. 23-25
26. Тамулявичюте, Д.Ю. Болезни пищевода и кардии / Д.Ю. Тамулявичюте, А.М. Витенас. — М.: Медицина, 1986. — 84 с.
27. Adam, S.I. Revision Zenker diverticulum: laser versus stapler outcomes following initial endoscopic failure / S.I. Adam, B. Paskhover, C.T. Sasaki // Ann. Otol. Rhinol. Laryngol. — 2013. — 122 (4): 247–53.
28. Ayav, A. Transcervical video-assisted resection of Zenker’s diverticulum / A. Ayav, L. Bresler, L. Brunaud // Journal of Laparoendoscopic & Advanced Surgical Techniques. — 2005. — 15 (6): 620–623.
29. Brasnu, E. Post-total laryngectomy Zenker’s diverticulum: endoscopic stapled- assisted esophagodiverticulostomy / E. Brasnu, S. Perie, J.L. Guily // Otolaryngo¬logy-Head and Neck Surgery. — 2003. — 128 (6): 902–903.
30. Chiari, C. Significant symptomatic relief after transoral endoscopic staple- assisted treatment of Zenker’s diverticulum / C. Chiari, W. Yeganehfar, M. Scharitzer // Surgical Endoscopy. — 2003. — 17: 596–600.
31. Clarence, T.S. Association between Zenker diverti¬culum and gastroesophageal reflux disease: development of working hypothesis / T.S. Clarence, A.R. Dougias, H. Jagdepp // The American Journal of Medicine. — 2003 Aug. — 115 (3a): 169–171.
32. Conticello, S. Endoscopic diverticulotomy for the threatment of Zenker’s diverticulum / S. Conticello, C. Giordano, G. Succo et al. // International Congress Series. — 2003. — 1240: 901–906.
33. Cook, I.J. Pharyngeal (Zenker’s) diverticulum is a disorder of upper esophageal sphincter opening / I.J. Cook, M. Gabb, V. Panagopoulos // Gastroenterology. — 1992 Oct. — 103 (4): 1229–1235.
34. Costamagna G. Prognostic variables for the clinical success of flexible endoscopic septotomy of Zenker's diverticulum. / Costamagna G, Iacopini F, Bizzotto A, Familiari P, Tringali A, Perri V, Bella A./ Gastrointest Endosc. 2015 Sep 3. pii: S0016-5107(15)02816-3.
35. Dokcu, A.I. Zenker s diverkiculum in childhood: A new case / A.I. Dokcu, M. Fabre, S. Otcu et al. // Eur. J. Pediat. Surg. — 2000. — 3: 191–193.
36. Dwivedi, R.C. A technique of endoscopic stapling of pharyngeal pouch for patients with limited mouth opening / R.C. Dwivedi, P.D. Karkos, M. Porter // Laryngoscope. — 2013. — Jun: 123 (6): 1448–1450.
37. Geisler, F. Endoscopic treatment of a Zenker’s diverticulum using argon plasma coagulation in a patient with massive cachexia and esophageal obstruction: a case report and review of literature / F. Geisler, M. Storr, R. Frisch et al. // Diseases of the Esophagus. — 2002. — 15: 180–185.
38. Jack Bragg. Esophageal Diverticula Jack Bragg, DO; Chief Editor: Julian Katz Updated: Jun 18, 2014
39. Joel A. Zenker Diverticulum. /: Joel A Ernster, MD; Chief Editor: Arlen D Meyers/ MBA Updated: Feb 23, 2015 123-145.
40. Jougon, J. Plea in favour of external approach of Zenker’s diverticulum: 73 cases reported / J. Jougon, L. Le Taillander-de Gabory, F. Delcambre // Annales de Chirurgie. — 2003. — 128: 167–172.
41. Krespi, Y. Endoscopic treatment of Zenker’s diverticulum using CO2 laser /
Y. Krespi, A. Kacker, M. Remacle // Head and Neck Surgery. — 2002. — 127: 309–314.
42. Manni, J.J. The endoscopic stapler diverticulotomy for Zenker’s diverticulum / J.J. Manni, B. Kremer, R.N.P.M. Rinkel // Eur. Arch. Otorhinolaryngology. — 2004. — 261: 68–70.
43. McLean, T.R. Stapled diverticulectomy and myotomy for symptomatic Zenker’s diverticulum / T.R. McLean, C.C. Haller // The American Journal of Surgery. — 2006. — 192: 28–31.
44. Melotti G. Zenker diverticulectomy: first report of robot-assisted transaxillary approach. / Melotti G, Piccoli M, Mullineris B, Varoli M, Colli G, Gozzo D, Smerieri N, Surendra N, Caruso A, Conigliaro R, Frazzoni M/ J Robot Surg. 2015 Mar;9(1):75-8.
45. Nyrop, M. Endoscopic CO2 laser therapy of Zenker’s diverticulum — experience from 61 patients / M. Nyrop, F. Svendstrup, K.E. Jorgensen // Acta Otolaryn¬gol. — 2000. — 543: 232–234.
46. O’Rourke, A.K. Killian-Jamieson diverticulum / A.K. O’Rourke, P.M. Weiberger, G.N. Postma // Ear Nose Throat. — 2012 May. — 91(5): 196.
47. Raut, V.V. Long-term results of endoscopic stepling diverticulotomy for pharyngeal poches / V.V. Raut, W.J. Primrose // Otolaryngology-Head and Neck Surgery. — 2002. — 127 (3): 225–229.
48. Ryan Law. Zenker's Diverticulum / Ryan Law; David A. Katzka; Todd H. Baron/ Clin Gastroenterol Hepatol. 2014;12(11):1773-1782.
49. Spinelli, P. Botulinum toxin type A (Dysport) for the treatment of Zenker’s diverticulum / P. Spinelli, G. Ballardini // Diagnostic and Surgical Endoscopy Unit, Istituto Nazionale Tumori, Via G. Venezian N 1, 2013, Milan, Italy.Received: 22 July 2002; Accepted: 29 July 2002; Online publication: 10 February 2003.
50. Steffen M. Carbon dioxide laser diverticulostomy: a new treatment for Zenker diverticulum / M. Steffen // The American Journal of Medicine. — 2003 Aug.— 115 (3a): 172–174.
51. Tedesco, P. Cause and treatment of epiphrenic diverticula / P. Tedesco, M.F. Piero, W.W. Lawrence, G.P. Marco // The American Journal of Surgery. — 2005. — 190: 902–905.
52. Van Abel Short-term Quality-of-Life Outcomes following Transoral Diverticulotomy for Zenker's Diverticulum: A Prospective Single-Group Study. / Van Abel K.M., Tombers N.M., Krein K.A., Moore E.J., Price D.L., Kasperbauer J.L., Hinni M.L., Lott D.G., Ekbom D.C./ Otolaryngol Head Neck Surg. 2015 Nov 10. С. 1238-1252.
53. Wastrin, K.M. Zenker’s diverticulum — a historical review and trends in therapy / K.M. Wastrin, S. Ergun, B. Carlsoo // Acta Oto Laryngologyca. — 1996 May. — 116 (3): 351–60.
54. Ziaian B. Bicornuate Zenker's Diverticulum. / Ziaian B Md, Moslemi S Md./ Iran J Med Sci. 2015 Nov;40(6):550-1.
Статьи по теме
Рекомендуемые статьи
При эндоскопическом исследовании в случае бронхоэктазов в стадии ремиссии выявляется
частично диффузный бронхит I степени воспаления
Активируйте PUSH уведомления в браузер
Отключите PUSH уведомления в браузер
Содержание
Интернет магазин
Популярное
- О нас
- Правовые вопросы
- Политика
обработки персональных
данных EndoExpert.ru - Связаться с нами
- Стать партнером
© 2016-2022 EndoExpert.ru

Вы находитесь в разделе предназначенном только для специалистов (раздел для пациентов по ссылке). Пожалуйста, внимательно прочитайте полные условия использования и подтвердите, что Вы являетесь медицинским или фармацевтическим работником или студентом медицинского образовательного учреждения и подтверждаете своё понимание и согласие с тем, что применение рецептурных препаратов, обращение за той или иной медицинской услугой, равно как и ее выполнение, использование медицинских изделий, выбор метода профилактики, диагностики, лечения, медицинской реабилитации, равно как и их применение, возможны только после предварительной консультации со специалистом. Мы используем файлы cookie, чтобы предложить Вам лучший опыт взаимодействия. Файлы cookie позволяют адаптировать веб-сайты к вашим интересам и предпочтениям.
Я прочитал и настоящим принимаю вышеизложенное, хочу продолжить ознакомление с размещенной на данном сайте информацией для специалистов.

















.jpg)





.png)

















Комментарии