- Компании
- Takeda. О компании, буклеты, каталоги, контакты
- Olympus. О компании, буклеты, каталоги, контакты
- Boston Scientific. О компании, буклеты, каталоги, контакты
- Pentax. О компании, буклеты, каталоги, контакты
- Fujifilm & R-Farm. О компании, буклеты, каталоги, контакты
- Erbe. О компании, буклеты, каталоги, контакты
- Еще каталоги
- Мероприятия
- Информация
- Обучение
- Классификации
- Атлас
- Quiz
- Разделы
- Пациенту
QR-код этой страницы
Для продолжения изучения на мобильном устройстве ПРОСКАНИРУЙТЕ QR-код с помощью спец. программы или фотокамеры мобильного устройства
Статьи: Диссертация З.В. Галкова БАЛЛОННАЯ ПАПИЛЛОДИЛАТАЦИЯ 2002
Полный текст статьи:
РОССИЙСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ
На правах рукописи
ГАЛКОВА ЗАЛИНА ВИКТОРОВНА
ЭНДОСКОПИЧЕСКАЯ БАЛЛОННАЯ ПАПИЛЛОДИЛАТАЦИЯ В ЛЕЧЕНИИ ХОЛЕДОХОЛИТИАЗА
14.00.27 - Хирургия
Диссертация
на соискание ученой степени кандидата медицинских наук
Научный руководитель: Заслуженный деятель науки РФ, Лауреат Государственной премии, член-корреспондент РАМН, д.м.н., профессор Ю.М.Панцырев
Научный консультант:
к.м.н., ст.науч.сотр. С.Ю.Орлов
Москва – 2002
СОДЕРЖАНИЕ
ВВЕДЕНИЕ.................................................................................................................................. 4
ГЛАВА 1. Эндоскопические методики лечения холедохолитиаза (анализ современного состояния проблемы) 10-32
ГЛАВА 2. Клинический материал и методы обследования........................................ 33-63
2.1. Построение научного исследования...................................................................... 34
2.2. Клиническая характеристика больных.................................................................. 36
2.3. Методы обследования больных.............................................................................. 38
2.4. Техника эндоскопической баллонной папиллодилатации.................................. 52
2.5. Схема ведения больных в послеоперационном периоде..................................... 60
2.6. Методы статистической обработки данных.......................................................... 63
ГЛАВА 3. Результаты эндоскопической диагностики и лечения изолированного холедохолитиаза и их обсуждение.............................................................................................................................................. 64-103
3.1. Результаты отбора больных для выполнения эндоскопической баллонной папиллодилатации в соответствии с диагностическим алгоритмом..................................... 64
3.2. Результаты обследования больных с изолированным холедохолитиазом........ 70
3.3. Результаты эндоскопической баллонной папиллодилатации при холедохолитиазе......................................................................................................................... 75
3.4. Результаты контрольного исследования функции сфинктера Одди после эндоскопической баллонной папиллодилатации.................................................................. 102
ЗАКЛЮЧЕНИЕ....................................................................................................................... 104
ВЫВОДЫ................................................................................................................................. 114
ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ............................................................................. 116
СПИСОК ЛИТЕРАТУРЫ..................................................................................................... 119
СПИСОК СОКРАЩЕНИЙ
АЛТ - аланинаминотрансфераза АСТ - аспартатаминотрансфераза
БДС - большой дуоденальный сосочек ГПП - главный панкреатический проток ДПК - двенадцатиперстная кишка
ЖКБ - желчнокаменная болезнь ЖП - желчный пузырь
ОЖП - общий желчный проток ПЖ - поджелудочная железа
ПХЭС - постхолецистэктомический синдром СО - сфинктер Одди
ТОХ - терминальный отдел холедоха УЗИ - ультразвуковое исследование ЩФ - щелочная фосфатаза
ЭПД - эндоскопическая баллонная папиллодилатация ЭПСМ - эндоскопическая папиллосфинктероманометрия ЭПСТ - эндоскопическая папиллосфинктеротомия
ЭРПХГ - эндоскопическая ретроградная панкреатикохолангиография ЭУС - эндоскопическая ультрасонография
ВВЕДЕНИЕ
Актуальность проблемы
В хирургическом лечении заболеваний панкреатобилиарной зоны в настоящее время предпочтение отдается малоинвазивным вмешательствам, среди которых эндоскопическая папиллосфинктеротомия занимает ведущее место. Более, чем 25 летний опыт применения ЭПСТ в клинической практике позволил считать эту эндоскопическую операцию «золотым стандартом» при лечении многих заболеваний желчевыводящих путей и большого дуоденального сосочка [92,181]. При холедохолитиазе ЭПСТ практически полностью вытеснила хирургические вмешательства [17,21]. Однако, несмотря на накопление опыта данного вмешательства, разработку более безопасного инструментария, число ранних послеоперационных осложнений составляет в среднем 10% [68,77,92,93,107,181,188]. Замыкательная функция сфинктера Одди при папиллосфинктеротомии разрушается, что приводит к дуоденохоледохеальному рефлюксу. С этим пусковым механизмом связывают развитие осложнений в отдаленные сроки после вмешательства [15,69,110,124,176,178].
Большие перспективы в лечении холедохолитиаза и профилактике развития осложнений в отдаленном периоде возлагают на сфинктеросохраняющие методики. Одной из них является эндоскопическая баллонная папиллодилатация, впервые выполненная в 1983 году [192]. По имеющимся данным баллонная папиллодилатация не разрушает сфинктерный аппарат большого дуоденального сосочка [157,218]. Это подтверждается результатами исследований с манометрическим контролем в ранние (до 2 месяцев) сроки после вмешательства [166,183]. Сведений же о функциональном состоянии СО в более отдаленные сроки после вмешательства недостаточно [224]. Вопрос о влиянии дилатации на тканевые структуры БДС, в основном касающийся сохранения функциональной активности сфинктера и возможного его стенозирования, в литературе освещен недостаточно [157,166,183,218,224].
Авторами указывались преимущества данной методики, связанные не только с сохранением автономности билиарной системы за счет сохранения целостности сфинктера Одди, но и с отсутствием таких осложнений вмешательства, как кровотечение, ретродуоденальная перфорация [62,143,179]. Однако, по мнению некоторых авторов, данная методика связана с повышенным риском развития острого панкреатита, что ограничивало ее применение при холедохолитиазе [54,101,147].
К настоящему времени показания и противопоказания для выполнения баллонной папиллодилатации окончательно не определены. Данная методика применяется в основном при холедохолитиазе, однако некоторые авторы использовали ее и при папиллостенозе [3,16,34,54,119,120,147,190]. Причем в последнем случае эффективность дилатации достаточно низкая и кратковременная, а развитие острого панкреатита после вмешательства отмечалось до 50% случаев [34,54,119,120,147]. Показания для дилатации при холедохолитиазе также весьма разноречивы - от возможного и оправданного выполнения методики всем пациентам с камнями желчного протока [63,143,220] до строгих ограничений и показаний только в единичных случаях, в основном при выраженных коагулопатиях [53,82].
Предложены различные модификации данной методики, которые значительно отличаются по техническим параметрам. В последнее время наметилась тенденция к применению более щадящих для тканей сфинктера режимов дилатации [112,160].
Необходимость определения места ЭПД в структуре лечения больных с холедохолитиазом и выяснения влияния данного метода на функциональное состояние сфинктера Одди не только непосредственно после вмешательства, но и в отдаленные сроки явилась отправным моментом данного исследования.
Цель исследования
Оценить возможности эндоскопической баллонной папиллодилатации в лечении холедохолитиаза.
Задачи исследования
1. Определить показания для эндоскопической баллонной папиллодилатации при изолированном холедохолитиазе, учитывая анатомические особенности и сопутствующую патологию желчевыводящих путей.
2. Освоить и усовершенствовать технику эндоскопической баллонной папиллодилатации.
3. Разработать схему ведения больных в послеоперационном периоде.
4. Дать оценку клиническим результатам и функциональному состоянию сфинктера Одди после эндоскопической баллонной папиллодилатации.
Научная новизна
Разработана комплексная диагностическая программа обследования больных с подозрением на патологию желчевыводящих протоков, апробированная на большом клиническом материале, определяющая показания и выбор наиболее оптимального способа эндоскопического лечения холедохолитиаза.
Четко определены и научно обоснованы показания для выполнения эндоскопической баллонной папиллодилатации при холедохолитиазе с учетом данных обследования терминального отдела холедоха и функционального состояния сфинктера Одди.
Усовершенствована методика эндоскопической баллонной папиллодилатации при холедохолитиазе, позволяющая свести к минимуму травматизацию тканей большого дуоденального сосочка во время вмешательства и сохранить его функциональную активность в последующем.
Впервые доказано полное сохранение всех показателей функциональной активности сфинктера Одди на основании данных эндоскопической перфузионной папиллосфинктероманометрии при благоприятном клиническом течении через год после эндоскопической баллонной папиллодилатации.
Практическая значимость
В клиническую практику внедрена комплексная программа обследования при подозрении на холедохолитиаз, включающая эндоскопическую ультрасонографию и манометрическое исследование СО. Данная диагностическая программа влияет на выбор метода эндоскопического лечения холедохолитиаза.
Показано, что ЭУС позволяет точно определить диаметр желчных протоков и характер их содержимого, при выявлении конкрементов - определить их количество и размеры, а также оценить эхографическое состояние терминального отдела холедоха и большого дуоденального сосочка.
Выполнение ЭПСМ перед эндоскопическим вмешательством дает возможность оценить функциональное состояние сфинктера Одди. При выборе метода лечения холедохолитиаза учитывается наличие или отсутствие патологии сфинктера по данным манометрии и необходимость ее коррекции.
Сформулированы рекомендации по техническому выполнению эндоскопической баллонной папиллодилатации с указанием режимов дилатации и выбора оптимальной модификации необходимого инструментария.
Оценена эффективность вмешательства и течение ближайшего послеоперационного периода. Разработана схема ведения больных после ЭПД, направленная на профилактику развития острого панкреатита.
Выявлено благоприятное клиническое течение заболевания и сохранение всех показателей функциональной активности сфинктера Одди через год после эндоскопической баллонной папиллодилатации.
Внедрение в клиническую практику
Разработанная диагностическая программа обследования внепеченочных желчных протоков и БДС для выбора оптимального эндоскопического вмешательства при холедохолитиазе, усовершенствованная техника ЭПД у больных с холедохолитиазом, а также оценка функционального состояния СО после баллонной дилатации, внедрены и используются в клинической практике трех хирургических отделений ГКБ № 31 г. Москвы, кафедры госпитальной хирургии № 2, ПНИЛ хирургической гастроэнтерологии и эндоскопии РГМУ. Диагностические и лечебные методы внедрялись в практику других лечебных учреждений г. Москвы и других городов России путем ознакомления с ними 12 практических врачей – хирургов и эндоскопистов, проходивших специализацию в клинике.
Апробация работы
Материалы диссертации изложены и обсуждены на: 4-м Съезде Российской Ассоциации эндоскопической хирургии (Москва, 2001г.); 32-м заседании Российского общества эндоскопии пищеварительной системы (РОЭПС) (Москва, 2002г.); 63-м Конгрессе Японского общества гастроинтестинальной эндоскопии (Кофу, 2002г.); 6-м Московском Международном Конгрессе по эндоскопической хирургии (Москва, 2002г.), 10-й Европейской гастроэнтерологической неделе (Женева, 2002г.).
Диссертация апробирована на совместной научно-практической конференции кафедры госпитальной хирургии № 2, ПНИЛ хирургической гастроэнтерологии и эндоскопии, хирургических отделений городской клинической больницы № 31 (06.06.2002г.).
Публикации
По теме диссертации опубликованы 5 научных работ в отечественной печати, из них 4 в центральной печати, и 1 работа в зарубежной печати; подготовлено и выполнено 3 доклада на отечественных и 2 доклада на зарубежных форумах.
Структура и объем работы
Диссертация состоит из введения, обзора литературы, трех глав, заключения, выводов, практических рекомендаций и списка литературы. Список литературы включает 225 источников, в том числе 46 отечественных и 179 зарубежных авторов. Диссертация изложена на 141 странице машинописного текста, содержит 23 таблицы, 2 схемы и 26 рисунков.
ГЛ АВ А I
ЭНДОСКОПИЧЕСКИЕ МЕТОДИКИ ЛЕЧЕНИЯ ХОЛЕДОХОЛИТИАЗА
(анализ современного состояния проблемы)
Желчнокаменная болезнь относится к одним из наиболее распространенных заболеваний и, по данным литературы, встречается у 10-15% населения [7,17,21,39]. При этом отмечается неуклонный рост заболеваемости ЖКБ, что связано с увеличением продолжительности жизни населения, расширением сети диагностических учреждений, улучшением качества диагностики заболевания, благодаря применению новых методов исследования [17,39]. Холедохолитиаз, как проявление желчнокаменной болезни, встречается в 15-30% случаев и является причиной постхолецистэктомического синдрома у 30% больных [12,17,39]. Кроме того, наличие камней в желчных протоках может привести к развитию таких серьезных осложнений, как механическая желтуха, острый холангит с последующим развитием холангитических абсцессов печени, печеночная недостаточность, острый билиарный панкреатит, а также стеноз сфинктера Одди и хронический рецидивирующий панкреатит.
До середины 70-х годов основным методом лечения калькулезного холецистита являлась хирургическая холецистэктомия, дополненная при необходимости вмешательствами на желчных протоках [41]. Быстрое развитие малоинвазивных технологий привело к заметным переменам в различных областях хирургии. Особое место новые методы лечения заняли при патологии панкреатобилиарной области, в том числе и при холедохолитиазе. И в настоящее время лапаротомные операции при холедохолитиазе уходят в прошлое, оставаясь лишь операциями резерва [17,21].
Эндоскопическая папиллосфинктеротомия при лечении холедохолитиаза
Рождение и развитие малоинвазивной хирургии заболеваний панкреатобилиарной зоны большинство хирургов относят к моменту внедрения в практику эндоскопической папиллосфинктеротомии [2,6,88,139]. Первая папиллосфинктеротомия была выполнена Classen и Demling 6 июня 1973 года в Германии [85,86] и независимо от них 10 августа 1973 года Kawai с соавт. в Японии [137]. В течение последующих 2 лет данная операция была успешно выполнена более, чем 2000 пациентам 10 Европейских центров с прекрасными результатами [174]. В 70-х годах ЭПСТ активно внедряется и в различных клиниках России [1,2,5,28,36]. На основании полученных данных эндоскопическая папиллосфинктеротомия стала считаться «золотым стандартом» в лечении холедохолитиаза.
Явившись в свое время альтернативой хирургической коррекции протоковой патологии, ЭПСТ позволила добиться существенного улучшения результатов лечения данной категории больных. Новая эндоскопическая методика более легко выполнима, дешевле и безопаснее, по крайней мере, для пожилых больных и больных высокого риска
[6,37,41,87,92]. Таким образом, начиная с 80-х годов, эндоскопическая папиллосфинктеротомия, стала широко применяться в клинической практике и почти полностью вытеснила открытую хирургию при холедохолитиазе [7,17,21]. Даже, несмотря на внедрение лапароскопических вмешательств в билиарной хирургии и попыток извлечения конкрементов этим способом, эндоскопическая папиллосфинктеротомия остается более предпочтительной методикой [67,153].
В начале 90-х годов, наряду с восхищением новой эндоскопической методикой постепенно стала нарастать настороженность, обусловленная осложнениями ближайшего послеоперационного периода и неблагоприятными последствиями ЭПСТ в отдаленные
сроки после ее выполнения [93,97,103,106,124]. Опыт выполнения папиллотомии у отдельных авторов стал насчитывать сотни и даже тысячи наблюдений
[15,35,43,106,176,181,204,223], стремительно увеличивалось число учреждений и специалистов, выполняющих ЭПСТ, благодаря этому расширялись показания к данному вмешательству. Между тем, внедрение в клиническую практику лапароскопической холецистэктомии привело к необходимости углубленного обследования большой группы больных, в том числе молодого возраста, с холедохолитиазом при отсутствии значительного расширения желчных протоков. Проведенные исследования выявили, что при выполнении эндоскопической папиллосфинктеротомии у пациентов молодого возраста, при отсутствии или незначительном расширении желчных протоков наиболее часто возникают такие опасные осложнения ЭПСТ, как ретродуоденальная перфорация, острый панкреатит [68,93,188].
Таким образом, накопленный мировой опыт применения эндоскопической папиллосфинктеротомии, привел к появлению значительного количества ретроспективных исследований по оценке ранних и отдаленных результатов ЭПСТ
[59,60,93,108,110,124,176,178]. Полученные данные только добавили сомнений по поводу безопасности и необходимости "поголовного" выполнения сфинктеротомии [97].
Ранние осложнения эндоскопической папиллосфинктеротомии. Большинство опубликованных данных мультицентровых исследований указывали на общее число ранних осложнений после ЭПСТ в среднем в 10% случаев при летальности до 1,5% [68,77,92,93,107,181,188] (табл.1.1).
Таблица 1.1
Ранние осложнения ЭПСТ
|
Осложнения |
Средняя частота %, (min-max) |
|
Острый панкреатит |
5,5 (0-40) |
|
Кровотечения |
2,5 (1-5) |
|
Ретродуоденальная перфорация |
1,3 (0,3-2,1) |
|
Холангит |
1,0 (0,9-1,5) |
|
Острый холецистит |
0,5 |
|
Другие осложнения |
1,1 |
На основании опыта многоцентровых исследований были выделены различные факторы риска развития осложнений после ЭПСТ [68,81,93,107,164,211]. К ним относятся: тяжелое общее состояние больного, молодой возраст, женский пол, наличие цирроза печени, нарушения свертывающей системы крови, стенозирующие заболевания БДС, дисфункции СО, сложные анатомические условия (нерасширенные желчные протоки, перенесенные операции), «трудная» канюляция, атипичные методы папиллотомии, многократное введение контрастного вещества в главный панкреатический проток, комбинированные чрескожно-эндоскопические методы, а также недостаточный опыт эндоскописта.
Также отмечено, что наибольшее число осложнений возникает у больных с дисфункцией СО (острый послеоперационный панкреатит развивается в 12,5–37,5% случаев) [55,77,93,106,109,150,188,207,211]. Осложнения у больных с циррозом печени после ЭПСТ развиваются в 14,3-16,6%, причем больший процент из них составляют кровотечения, которые могут приводить к печеночно-клеточной недостаточности
[136,143]. По тем же причинам весьма небезопасно выполнение ЭПСТ и при наличии тяжелых коагулопатий.
У больных, перенесших резекцию желудка по Бильрот-2, канюляция Фатерова сосочка значительно затруднена, и риск развития осложнений и летального исхода после ретроградных вмешательств у них выше, чем у больных с нормальной анатомией
[9,93,101]. С аналогичными проблемами эндоскописты сталкиваются при наличии у больных крупных дивертикулов в зоне БДС [9,68]. Длительная канюляция общего желчного протока, выполнение атипичной папиллотомии, большое число введений контрастного вещества в главный панкреатический проток также повышают риск развития осложнений в послеоперационном периоде [106,109,181,211]. Таким образом, при выборе метода эндоскопического вмешательства многими авторами рекомендуется учитывать наличие факторов риска у пациентов.
Осложнения в отдаленном периоде после ЭПСТ. В настоящее время и ближайшие, и отдаленные результаты ЭПСТ достаточно хорошо изучены. Сроки наблюдения за больными, перенесшими эндоскопическую папиллосфинктеротомию, приближаются к 20 годам [60,204]. Поздние осложнения ЭПСТ, такие как холангит, повторное камнеобразование, рестеноз сфинктера, острый холецистит, панкреатит, печеночная колика развиваются у 5,2-24% пациентов [59,92,103,110,124,176,178,204]. При этом процент осложнений выше в работах с более длительным периодом наблюдения за больными, перенесшими папиллосфинктеротомию [74] (табл.1.2).
Таблица 1.2
Осложнения в отдаленном периоде наблюдения после ЭПСТ
|
Авторы, гг. |
Число больных |
Период наблюдения, гг. |
Поздние осложнения, % |
|
Escourrou, 1984 [103] |
96 |
0,5-5 |
5,2 |
|
Cotton, 1984 [92] |
148 |
2-7 |
7,5 |
|
Hawes, 1990 [124] |
115 |
6-11 |
13 |
|
Prat, 1996 [178] |
156 |
8-13 |
10,3 |
|
Bergman, 1996 [59] |
94 |
15 |
24 |
|
Tanaka, 1998 [204] |
410 |
до 20 |
12,3 |
|
Pereira-Lima, 1998 [176] |
203 |
7-10 |
15,4 |
Некоторые авторы считают, что риск осложнений в отдаленном периоде после ЭПСТ несколько преувеличен [42]. К тому же большинство этих осложнений могут быть благополучно корригированы эндоскопически [92,106,110,151]. Тем не менее, проведенные в этой области исследования подтверждают, что папиллосфинктеротомия приводит к новым анатомо-физиологическим взаимоотношениям органов панкреатобилиарной зоны с определенными клиническими последствиями. На основании этих данных в литературе дискутируются возможные механизмы развития осложнений в отдаленном периоде после данного вмешательства.
ЭПСТ разрушает сфинктер Одди, что приводит к частичной, либо полной утрате его функции, что подтверждается данными манометрических исследований
[26,60,115,194]. Манометрический контроль после папиллосфинктеротомии выявляет некомпетентность сфинктера различной степени, вплоть до полной потери его функции - отсутствие или значительное снижение базального давления СО, а также отсутствие или снижение холедохо-дуоденального градиента давления, хотя сократительная активность сфинктера может частично восстанавливаться [26,194,203]. Именно с данным пусковым механизмом - разрушение СО - большинство авторов связывают развитие осложнений в отдаленном периоде после ЭПСТ. Утрата физиологического барьера между двенадцатиперстной кишкой и желчным трактом приводит к дуоденохоледохеальному рефлюксу и бактериальной обсемененности билиарной системы, при этом в желчи выявляется большое количество цитотоксических компонентов [60,69]. Микробной контаминации желчных путей после ЭПСТ подвергаются 60-100% пациентов
[60,110,124,191,205]. В большинстве случаев у этих больных в желчи высевается та же флора, что и в двенадцатиперстной кишке [191]. Hawes с соавт. выявили, что у больных с отсутствием билиарных симптомов в 60% выявляется выраженная степень бактериальной обсемененности желчных протоков [124]. Таким образом, связь между бактериальной
обсемененностью и наличием симптомов холангита прослеживается не всегда. Следовательно, отсутствие клинических проявлений холангита не говорит о полном благополучии билиарной системы.
Кроме того, некоторые авторы по данным своих исследований предположили, что наличие бактерий в желчном тракте приводит к развитию следующих осложнений в отдаленном периоде после ЭПСТ: рецидивный холедохолитиаз, воспалительные изменения желчного тракта, рецидивный восходящий холангит, острый холецистит и даже злокачественные новообразования [59,103,124,141,149,154,176,178,204].
При гистологическом исследовании слизистой оболочки желчного протока в отдаленные сроки после ЭПСТ выявлено наличие хронического воспаления с фиброзом
[13-15,60], что также является возможным фактором риска развития неопластических изменений [60]. В работе A.Ljungh, 2002г. было выявлено, что некоторые штаммы Helicobacter способны развиваться в желчи и вызывать хроническое воспаление с возможной последующей малигнизацией [154]. Тем не менее, достоверно до настоящего времени нельзя говорить о наличии связи между ранее перенесенной ЭПСТ и развитием злокачественных новообразований в отдаленном периоде. Некоторые авторы высказали предположение, что еще не прошло достаточно времени для развития таких серьезных осложнений, в то время как для злокачественной трансформации эпителия в данной ситуации необходимо не менее 10 лет [149].
Обратимся к более ранним примерам в желчной хирургии. Изменения морфофункционального состояния органов панкреатобилиарной системы, развивающиеся после ЭПСТ, аналогичны таковым после наложения билиодигестивных анастомозов при неопухолевых заболеваниях внепеченочных желчных протоков. С момента первых операций на желчных путях в конце 19 - начале 20 века было предложено значительное число модификаций билиодигестивных анастомозов с детальной оценкой непосредственных и отдаленных результатов данных вмешательств [10,32,149]. Основным спорным моментом остается вопрос о влиянии дуоденобилиарного рефлюкса на функциональное состояние печени, поджелудочной железы и на отдаленные результаты наложения билиодигестивных анастомозов [18,33,40]. В 1979 г. М.И.Филимонов с соавт. оценили функциональное состояние печени у больных с супрадуоденальным холедоходуоденоанастомозом и пришли к выводу, что при нормальной функции холедоходуоденоанастомоза и своевременной эвакуации кишечного содержимого из желчных ходов печени появление дуоденобилиарного рефлюкса не оказывает выраженного вредного влияния на функциональное состояние печени [40]. Однако авторы не исключали возможности влияния рефлюкса содержимого ДПК у больных с билиодигестивными анастомозами на развитие у них выраженных дистрофических изменений в печени с исходом в цирроз и печеночную недостаточность, что, по их мнению, могло иметь место при нарушениях оттока из желчных протоков. А А.Т.Лидский полагал, что опасность восходящей инфекции и развития холангита после наложения билиодигестивных анастомозов явно преувеличена, т.к. на своем довольно большом числе наблюдений данное осложнение авторы не встречали [18]. Однако, отсутствие симптомов холангита не отрицает наличия хронических воспалительных изменений слизистой оболочки желчного протока. А.Е.Котовский с соавт. при выполнении ретроградной транспапиллярной холедохоскопии больным в отдаленные сроки (от 1 года до 10 лет) после ЭПСТ обнаружили, что явления холангита имелись не только у больных с рестенозом БДС, но и при полном рассечении сфинктера Одди вследствие развития дуодено-билиарного рефлюкса [14,15]. В целом, отдаленные результаты билиодигестивных анастомозов достаточно хорошие, и в литературе достоверных указаний на наличие связи между дуоденобилиарным рефлюксом и образованием опухолей панкреатобилиарной зоны нет. Вопрос же о возможности малигнизации желчных путей после ЭПСТ в настоящее время остается неизученным.
Проведенные к настоящему времени исследования показали, что бактерии играют важную роль в образовании коричневых пигментных камней, приводя к рецидивному холедохолитиазу [59,124,142,176,178,184,204]. Причем, независимо от вида конкрементов при первичном вмешательстве, все рецидивные камни оказываются по своему строению билирубинатами [204]. Это подтверждает роль восходящей инфекции в образовании вторичных камней, в частности фермента бактерий В-глюкоронидазы и кальция (основных компонентов коричневых пигментных камней) [204]. К тому же, последние исследования указали на роль бактериальной инфекции в образовании не только пигментных, но и холестериновых камней [142].
На основании приведенных данных можно утверждать, что активное внедрение эндоскопической папиллосфинктеротомии в повседневную клиническую практику привело к широкому признанию данной методики в качестве "золотого стандарта" при различной патологии желчных протоков и БДС, особенно при холедохолитиазе. Между тем, набор опыта и анализ выявленных осложнений данного вмешательства заставил многих исследователей пересмотреть свой поход к чрезмерно широкому применению ЭПСТ [91,97]. Попытки избежать ранних осложнений папиллосфинктеротомии и ее нежелательных последствий в отдаленном периоде, а также тенденция сохранения сфинктерного аппарата Фатерова сосочка у больных с холедохолитиазом привели к разработке новых, более безопасных и в то же время эффективных методик удаления камней из желчных протоков [117,132,192,193,200,216].
Медикаментозная релаксация сфинктера Одди
при холедохолитиазе
За последние 20 лет появилось несколько сообщений (в основном из Японии) об использовании медикаментозной релаксации СО при холедохолитиазе с применением нитропрепаратов (глицерил тринитрат, нитроглицерин сублингвально; изосорбид динитрат внутривенно) [132,193,200,216]. Данная методика в отличие от папиллосфинктеротомии сохраняет функциональную активность сфинктерного аппарата. Однако, широкого распространения этот метод не получил из-за низкой эффективности и часто возникающей необходимости дополнять вмешательство папиллотомией [158,167]. В целом нитраты ингибируют моторику СО [116,155,196], обеспечивая расслабление мышечных волокон сфинктера, что значительно облегчает канюляцию холедоха. Вследствие этого некоторые авторы предпочитают применять медикаментозную релаксацию СО как дополнение к другим эндоскопическим вмешательствам на терминальном отделе холедоха [162,209].
Эндоскопическая баллонная дилатация сфинктера Одди при холедохолитиазе
В 1983 году M.Staritz с соавт. впервые предложили методику извлечения камней из желчных протоков без сфинктеротомии, используя эндоскопическую папиллодилатацию
[192]. Позднее появились различные синонимы этого вмешательства: “эндоскопическая баллонная сфинктеропластика” [172], “эндоскопическая баллонная сфинктероклазия”
[177], “эндоскопическая баллонная папиллодилатация” [143]. В начале 80-х годов данная методика, предложенная как менее опасная альтернатива ЭПСТ, вызвала некоторые сомнения по двум основным причинам: во-первых, папиллосфинктеротомия казалась достаточно безопасной методикой, при этом работы по ее осложнениям по мере накопления опыта появились чуть позже, а во-вторых, существовало беспокойство по поводу повышенного риска развития острого панкреатита после баллонной папиллодилатации. Это опасение основывалось на представленном обзоре применения баллонной дилатации в Соединенных Штатах [147] и на данных, касающихся небольшой группы пациентов, опубликованных только в форме тезисов [54]. R.A.Kozarek проанализировал опыт применения гидростатической дилатации БДС 200 больным с дисфункцией сфинктера Одди [147]. Эффективность метода составила 98% непосредственно после вмешательства и 64% через 3 месяца. При этом осложнения развились в 35% случаев. Острый панкреатит в приведенных в данном обзоре работах отмечен в 17-62% случаев. На основании этих данных автор заключил, что баллонная дилатация имеет ограниченное место в эндоскопической практике из-за значительного процента развития осложнений, наличия альтернативных способов лечения (ЭПСТ, хирургические вмешательства и т.д.), а также недостаточной эффективности при контрольном обследовании пациентов в ближайшие сроки после вмешательства. Во втором указанном исследовании M.Bader с соавторами также высказали предположение, что баллонная дилатация связана с высоким риском развития панкреатита [54]. Однако в обеих приведенных работах вмешательство проводилось по поводу дисфункции СО, а не холедохолитиаза. Как известно, дисфункция СО относится к факторам риска развития острого панкреатита после любых ретроградных вмешательств [77,93,106,188,207,212]. И все же этот факт заставил воздержаться многих исследователей от применения нового вмешательства.
Таким образом, в 80-х годах практически единственной работой по баллонной дилатации СО при холедохолитиазе было исследование M.Staritz с соавт. [192]. Они описали небольшую группу, состоящую из 11 больных с холедохолитиазом, которые были успешно оперированы без осложнений, используя баллоны диаметром 15 мм. В дальнейшем методика широкого распространения не получила. Несмотря на желание многих исследователей сохранить сфинктерный аппарат большого дуоденального сосочка, утвердившееся мнение о значительном риске развития панкреатита после вмешательства препятствовало внедрению этой новой эндоскопической методики в клиническую практику.
Тем не менее, в начале 90-х годов неудовлетворенность результатами отдаленных последствий ЭПСТ, вновь возрождает интерес к папиллодилатации. Авторами из разных стран публикуется успешный опыт применения данной методики при холедохолитиазе
[143,156,163]. В форме тезисов докладов было опубликовано несколько исследований, не отличающихся значительно по своим результатам [78,79,101]. К тому же были представлены рандомизированные исследования по сравнению ЭПД и ЭПСТ у больных с холедохолитиазом [53,62,166,187].
Техника эндоскопической баллонной папиллодилатации. Стандартная методика баллонной папиллодилатации состоит в проведении струны-проводника в желчные протоки после выполнения ретроградной холангиографии, последующего проведения по струне на уровень большого дуоденального сосочка катетера с баллоном для дилатации и непосредственно самого сеанса дилатации. Далее выполняется ревизия желчных путей и извлечение конкрементов при помощи корзинки Дормиа и/или ревизионного баллончикового катетера [61,62,143,156,192]. Вмешательство заканчивают - в зависимости от оснащенности клиники современным оборудованием - контрольной холангиографией [143,156], внутрипротоковой ультрасонографией [80,143,173,219] или холедохоскопией для оценки полноты санации желчных путей [166].
Как показал анализ данных литературы технические аспекты вмешательства значительно различаются: а) используются баллоны различных фирм-производителей; б) диаметр баллонов варьирует от 5 до 15 мм; в) длина баллонов составляет 2 и более см; г) максимальное давление, безопасно нагнетаемое в баллонах, находится в пределах от 4 до 12 атмосфер и указывается фирмой производителем; д) время дилатации также колеблется в широких пределах - от 30 секунд до 3 минут; е) одни авторы предпочитали одномоментную дилатацию, другие выполняли до 2-4 повторных сеансов при помощи баллона того же или большего диаметра. При этом во всех работах имеется лишь описание техники без объяснения мотивов использования тех или иных параметров во время вмешательства.
Эффективность эндоскопической баллонной папиллодилатации. Первый опыт выполнения папиллодилатации, которая оказалась эффективной у 85-100% больных, позволил сделать единодушный вывод - баллонная дилатация СО является обоснованной альтернативой ЭПСТ [62,143,163,166,172,187,224]. Впрочем, проводить сравнение результатов опубликованных исследований достаточно сложно ввиду различий в отборе пациентов и определении критериев эффективности [53,63,165]. Одни авторы считали вмешательство эффективным, если камни удавалось извлечь непосредственно после баллонной дилатации, в то время как необходимость выполнения дополнительной сфинктеротомии относили к неудачным результатам. Другие полагали, что понятия "успех" и "неудача" вмешательства определяются только отсутствием или наличием камней в протоках в конце операции, относя дилатацию, дополненную папиллосфинктеротомией, а также необходимость повторных вмешательств к числу успешно выполненных операций [143]. Некоторые авторы для объективной оценки результатов считают целесообразным указывать общий процент эффективности санации желчных путей, а также процент эффективного лечения холедохолитиаза непосредственно после папиллодилатации, уточняя в скольких случаях пришлось дополнить вмешательство папиллотомией [53,62]. Отбор пациентов был также неравнозначен. В некоторые работы включались больные с единичными конкрементами небольших размеров [163,166,177], и, напротив, в других не проводилось отбора, и ЭПД выполнялась
без ограничений всем больным с холедохолитиазом [62,143,172,220]. Существенно отличались больные и по возрасту, выраженности имеющейся сопутствующей патологии. К этому можно добавить и упомянутые выше нюансы техники, применяемые авторами, особенности оснащения лечебных учреждений и квалификации специалистов, что также влияло на эффективность и результаты вмешательства.
Показания к эндоскопической баллонной папиллодилатации. В настоящее время единой точки зрения по поводу применения эндоскопических методов лечения холедохолитиаза нет. Впрочем "лечебные вмешательства никогда не могут быть полностью безопасными" [97], и на любом этапе достижений в области медицины исследователи всегда стремились перейти к менее инвазивным вмешательствам. Вначале эндоскопическая папиллосфинктеротомия успешно заменила многие хирургические вмешательства на желчных протоках и терминальном отделе холедоха. И, казалось, найден оптимальный метод лечения большинства заболеваний панкреатобилиарной зоны. И, тем не менее, благодаря малоинвазивным направлениям стали внедряться новые методики, в том числе в лечении холедохолитиаза: медикаментозная релаксация СО
[132,193,216], баллонная папиллодилатация [62,143,156,163,166,177,192], одномоментные лапароскопические способы извлечения камней желчных протоков [67,104,117,153]. Однако при этом разнообразии, критерии выбора того или иного метода лечения конкретного больного с холедохолитиазом не выработаны. Отношение к различным методикам лечения холедохолитиаза и показания к ним в литературе значительно разнятся [105,158]. Зачастую авторы отстаивают методики, которыми они хорошо владеют и которые материально оснащены [104].
Так, отдельные авторы считают, что эндоскопическая баллонная папиллодилатация при холедохолитиазе может быть успешно выполнена практически у всех пациентов, другие указывают на строго ограниченные показания к ЭПД
[53,63,82,83,101,131,143,160,189]. При этом мелкие конкременты в небольшом количестве удавалось полностью извлечь почти во всех случаях, и, что важно - при первом же вмешательстве, без выполнения литотрипсии [63]. У больных же с крупными и/или множественными камнями в 35-50% случаев возникала необходимость применения различных видов литотрипсии [62,143,172,187,219,220], и в 15-30% требовалось дополнение вмешательства папиллотомией или выполнение повторных вмешательств
[63]. К тому же, применение литотрипсии повышает риск резидуального холедохолитиаза и, как следствие, неполной санации желчных путей от фрагментов разрушенных камней
[73,159,173,219]. Подобный подход требовал наличия высококвалифицированных специалистов, дорогостоящей аппаратуры, а также большей продолжительности госпитализации больного. До сих пор в литературе дискутируется вопрос - стоит ли добиваться санации желчных путей в подобной ситуации, сохраняя при этом сфинктерный аппарат? И если да, то, насколько сохраняется функция СО после длительных и множественных инструментальных вмешательств, естественно приводящих к механической травме этой области? Кроме того, при выраженном расширении желчных путей, при наличии в них крупных конкрементов, функция СО, вероятнее всего, уже нарушена и без вмешательств в этой зоне. Манометрического контроля функционального состояния сфинктера Одди в приведенных работах не проводилось. Все сказанное позволяет сделать вывод, что показания к выполнению баллонной дилатации остаются открытым вопросом и по настоящий момент.
Наиболее часто в литературе встречаются следующие показания к выполнению ЭПД при холедохолитиазе [53,62,65,82,100,136,143,167,168,172,179,189,209,210]: 1)
выраженные нарушения в коагулограмме крови у больных с тяжелыми некоррегируемыми коагулопатиями, циррозом печени, а также у больных, постоянно принимающих антикоагулянты; 2) сложные анатомические условия, при которых выполнение ЭПСТ невозможно или опасно - пациенты, перенесшие резекцию желудка по Бильрот-2, крупные перипапиллярные дивертикулы; 3) небольшой диаметр желчного протока с мелкими конкрементами, особенно у молодых пациентов.
Первые два показания у большинства авторов разногласий не вызывают. Небольшой диаметр желчных протоков также является предпочтительным показанием для выбора дилатации, ибо в данной ситуации общее число осложнений после ЭПСТ выше [44,77,188], а ЭПД позволяет их избежать. К тому же, сохранение функционального состояния сфинктерного аппарата весьма важно для молодых пациентов, поскольку уменьшается опасность развития осложнений в отдаленном периоде [145,209]. С другой стороны, некоторые авторы указали в своих исследованиях на повышенный риск развития панкреатита у пациентов молодого возраста, особенно при трудностях канюляции (что чаще наблюдается при нерасширенных протоках) [64,211,130]. В связи с этим отдельные исследователи рекомендовали при тяжелой и длительной канюляции отказываться от баллонной дилатации в пользу сфинктеротомии [64,131].
Следует отметить, что в некоторых работах баллонная папиллодилатация выполнялась при холедохолитиазе в сочетании с папиллостенозом. Наличие дисфункции СО является фактором повышенного риска развития панкреатита после эндоскопической операции: в исследованиях по выполнению ЭПД при папиллостенозе отмечен высокий (до 25-62) процент развития панкреатита в ближайшие сроки после вмешательства при низкой эффективности вмешательства в целом [34,119,120,147,190]. В патогенезе развития рестеноза БДС после ранее перенесенной папиллосфинктеротомии авторы указывали на роль первоначально выраженного рубцово-воспалительного процесса [9]. При дилатации рубцовых тканей папиллы в отличие от ЭПСТ, рубцово-воспалительный процесс не ликвидируется, также не происходит и адекватного раскрытия устья холедоха. Таким образом, как показал анализ литературных данных выполнение папиллодилатации при папиллостенозе не оправдано и имеет ограниченное применение, как и медикаментозное лечение, а методом выбора является ЭПСТ [52,90,98,147,148,212,215].
Вопрос о выборе операции возникает и при оценке происхождения камней [123,140,169]. M.H.Kim с соавт., 1998г. [140] и S.J.Myung с соавт., 1999г. [169] считают, что при вторичном холедохолитиазе, когда камни попадают в протоки из желчного пузыря (который и является местом камнеобразования), можно выполнять и папиллосфинктеротомию, и баллонную дилатацию, а при первичном холедохолитиазе предпочтительнее выполнять ЭПСТ, так как он часто ассоциирован с папиллостенозом, дисфункцией СО вследствие наличия околососочковых дивертикулов и т.д. (т.е. причина болезни в поврежденном сфинктере). Авторы достаточно логично объясняли выбранную ими тактику. При вторичном холедохолитиазе основная патология находится в желчном пузыре, и размеры камней, проходящих через пузырный проток из пузыря, могут быть относительно небольшими, так как диаметр пузырного протока составляет 0,2-0,6 см [19]. В данной ситуации сохранение сфинктера представляется целесообразным. К тому же диаметр протока значительно не изменяется при миграции мелких камней из пузыря. Так как большинство авторов считают, что риск развития осложнений после ЭПСТ (кровотечений, панкреатита, перфораций) выше у больных с нерасширенными желчными протоками, этот факт также обосновывает и оправдывает применение ЭПД при вторичном холедохолитиазе. Причиной же первичного холедохолитиаза считают наличие патологии большого дуоденального сосочка, которая не устраняется после ЭПД. Поэтому данное вмешательство не является патогенетически обоснованным при первичном холедохолитиазе и не исключает возможность рецидива камнеобразования. Но существует и другая точка зрения. На основании 226 наблюдений применения ЭПД Y.Komatsu с соавт., 1998г. выполняли вмешательство и при первичных, и при вторичных конкрементах с одинаковой эффективностью и заключили, что ЭПД показана и эффективна в обеих ситуациях [143,145]. Вопрос этот спорный и нуждается в более конкретных подтверждениях как одной, так и другой точки зрения. Однако, чтобы делать какие либо выводы при выборе той или иной методики разрешения холедохолитиаза, желательно было иметь представление о функциональном состоянии БДС до операции.
Аналогичные проблемы касаются и размеров конкрементов. Многие авторы высказывались, что при наличии крупных конкрементов сфинктер Одди уже поврежден. Это обстоятельство также можно подтвердить или отвергнуть при проведении манометрического исследования функционального состояния СО перед операцией. Это позволило бы правильно обосновать и выбрать предпочтительное в этих ситуациях вмешательство, учитывая также и повышенный риск развития у них осложнений. Однако подобные исследования с оптимальным выбором эндоскопического вмешательства при холедохолитиазе, основываясь на функциональном исследовании сфинктера Одди до операции, не проводились.
При выраженной билиарной гипертензии, крупных и/или множественных конкрементах общего желчного протока довольно часто при баллонной дилатации возникала необходимость выполнения различных видов литотрипсии, дополнительной сфинктеротомии, неоднократных вмешательств [62,63,143,172,187,220]. Большинство авторов в таких случаях отдавали предпочтение папиллосфинктеротомии.
Осложнения эндоскопической баллонной папиллодилатации. Результаты в ближайшем и отдаленном периоде после ЭПСТ достаточно хорошо изучены по сравнению с результатами баллонной папиллодилатации. Однако до сих пор продолжаются исследования по оценке ранних осложнений папиллосфинктеротомии и путях их профилактики, ведутся работы по анализу последствий ЭПСТ в отдаленном периоде и наличию связи этих последствий с разрушением функции СО.
Осложнения в ранние сроки после ЭПД аналогичны таковым после любых ретроградных манипуляций на БДС. Соответственно факторы риска развития данных осложнений такие же, как и при ЭРПХГ, и ЭПСТ: молодой возраст, женский пол, нерасширенные желчные протоки, контрастирование панкреатического протока,
трудности канюляции и т.д. [93,107,109,164,181,188]. Помимо стандартных для ретроградных вмешательств факторов риска развития осложнений, существуют специфические для баллонной дилатации факторы риска, связанные с травматичностью и техникой вмешательства: диаметр баллона, длительность дилатации, количество повторных сеансов дилатации, отек области вмешательства и т.д. [159].
Одним из основных преимуществ ЭПД является отсутствие интра- и послеоперационных кровотечений, что подтверждено в работах Y.Komatsu с соавт., 1998г. [143] и T.Kawabe с соавт., 1996г. [136], которые выполнили дилатацию 24 и 9 больным с холедохолитиазом и циррозом печени соответственно, при этом у половины из них была выявлена тяжелая коагулопатия. Конкременты удалось извлечь у всех больных, а кровотечений и других серьезных осложнений не было ни у одного пациента.
"Теоретическое преимущество сохранения сфинктерного аппарата … противостоит предположительно высокому риску развития панкреатита" [63]. Частота развития острого панкреатита после ЭПД в среднем составляет 6,3% (3,3-11%) [62,101,143,156,163,166,172,177,220,224]. Опубликованные к настоящему моменту данные не продемонстрировали статистически значимого повышения частоты развития панкреатита по сравнению с ЭПСТ. Лишь в одном рандомизированном исследовании J.A.DiSario с соавт., 1997г., процент развития панкреатита после ЭПД оказался значительно выше, чем при ЭПСТ (11% и 1% соответственно) [101]. Однако эти данные еще не опубликованы в форме полной статьи, что не дает возможности полноценно проанализировать результаты этой работы. Стоит также отметить, что ранние работы указывали на более высокий процент развития панкреатита. Причем некоторые авторы в своих статьях приводили два показателя: на начальных этапах освоения методики и после накопления опыта [160]. Большинство авторов не указывают определенных схем ведения больных после папиллодилатации, отличающихся от стандартных после ретроградных вмешательств. Хорошие результаты показал метод профилактики панкреатита после ЭПД, предложенный T.Aizawa с соавт., 1999г.: временная (на 3 дня) установка дренажа в главный панкреатический проток [49]. Авторы указывают, что данная методика является эффективной мерой профилактики развития панкреатита, однако выполнение ее всем больным после ЭПД достаточно трудоемко и является несколько теоретизированной рекомендацией. Подведя итог своей работе, авторы рекомендуют выполнять стентирование Вирсунгова протока после дилатации СО по крайней мере больным с высоким риском развития послеоперационного панкреатита.
Другие возможные осложнения ЭПД: холангит (4%), острый холецистит (1%), вклинение корзинки Дормиа (0.4%), пневморетроперитонеум (1%) из-за подслизистого введения воздуха через точечный дефект в баллоне при создании давления в нем, после чего баллон стали заполнять физиологическим раствором или физиологическим раствором с контрастным веществом [143].
Уверенность в полной санации желчных путей является важным моментом при выполнении ЭПД. Во-первых, после баллонной дилатации не удается достичь такого раскрытия ампулы БДС, как при сфинктеротомии; во-вторых, при дилатации чаще возникает необходимость применения различных видов литотрипсии [62,63,143,160,172]. Мелкие фрагменты камней после ЭПСТ спонтанно проходят через широко раскрытое устье в просвет кишки с током желчи, в то время, как после ЭПД имеется риск возникновения блокады ТОХ мелкими фрагментами конкремента. Это происходит, так как, во-первых, устье холедоха раскрывается не столь широко, как после ЭПСТ; во- вторых, после дилатации возникает отек тканей БДС, что также может препятствовать спонтанной миграции фрагментов камней в послеоперационном периоде [80,144,206]. Таким образом, после папиллодилатации все мелкие фрагменты должны быть полностью извлечены во время вмешательства, в том числе с использованием специального инструментария [146]. Для диагностики резидуального холедохолитиаза после дилатации различные авторы использовали холедохоскопию, эндоскопическую ультрасонографию,
внутрипротоковую ультрасонографию или ретроградное контрастирование желчных путей [80,143,156,166,173,219].
Сведений в литературе об отдаленных результатах ЭПД нет.
Влияние баллонной папиллодилатации на сфинктерный аппарат большого дуоденального сосочка. Многих исследователей до настоящего времени интересует вопрос - действительно ли баллонная дилатация атравматична для сфинктера, или она все же может приводить к снижению функции СО, образованию рубцовых изменений и нежелательным последствиям, связанными с ними [73,224]? Ни одно из опубликованных исследований не выявило повреждающего воздействия эндоскопической баллонной папиллодилатации на функцию СО в ближайшие сроки, в отличие от папиллосфинктеротомии [134,166,183,218]. При данной методике сфинктер не разрезается, а лишь растягивается, таким образом, его функция может быть сохранена. H.Sato с соавт., 1997г. выявили снижение функциональной активности СО через неделю после ЭПД и полное восстановление всех манометрических показателей через один месяц. [183]. В рандомизированном исследовании A.Minami с соавт., 1995г. небольшой группы больных до и после (через 25-35 дней) ЭПСТ (10 больных) и ЭПД (13 больных) с манометрическим контролем также не было выявлено значимых отличий показателей до и после ЭПД, в то время как после ЭПСТ функция сфинктерного аппарата Одди была практически полностью утрачена [166]. H.Isayama с соавт., 1998г. 10 больным, перенесшим ЭПД с последующей холецистэктомией, с целью оценки функции СО выполнили количественную холесцинтиграфию с технецием-99м-РМТ и сравнили эти данные с контрольной группой [134]. Результаты были аналогичны контрольной группе, и авторы сделали вывод, что данных за наличие папиллостеноза после ЭПД нет. S.Takahata с соавт., 2000г. при обследовании функции СО после ЭПД на собаках отметили снижение практически всех манометрических показателей в течение 3 месяцев после вмешательства [202]. I.Yasuda с соавт., 2001г. выявили значительное снижение всех параметров манометрии СО через неделю после ЭПД, а через год - восстановление базального давления СО, которое, однако, наряду с остальными показателями было ниже исходных данных до вмешательства [224]. Большая часть работ содержит данные, полученные на небольших группах пациентов, в ближайшие сроки после вмешательства. Сведения о влиянии расширения сфинктера на его функциональную активность в более отдаленные сроки скудны и противоречивы. В настоящее время наиболее точным методом, позволяющим оценить функциональное состояние сфинктера, является эндоскопическая манометрия сфинктера Одди [45,114,116,118,119,128,129]. Исследований применения папиллосфинктероманометрии до баллонной дилатации сфинктера и в отдаленные сроки после вмешательства недостаточно для полной характеристики данной методики.
При исследовании на свиньях влияния баллонной сфинктеропластики на морфологическое состояние СО по сравнению с ЭПСТ и контрольной группой было выявлено, что папиллодилатация вызывает острые трансмуральные воспалительные изменения, хроническую фолликулярную гиперплазию (через 12 месяцев) и не связана с развитием фиброза данной области или нарушением строения сфинктера [157]. При этом авторы в своей работе указывали на необходимость проведения манометрического контроля для подтверждения полученных данных.
Хотя сведений об отдаленных результатах ЭПД пока недостаточно, тем не менее, отдельные авторы полагают, что у пациентов молодого возраста после эндоскопического лечения холедохолитиаза без разрушения сфинктера (баллонная папиллодилатация) рецидив заболевания и другие поздние осложнения развиваются реже, чем после ЭПСТ [62,224].
Обобщая литературные данные по проблеме эндоскопического лечения холедохолитиаза, следует отметить, что «золотым стандартом» и наиболее широко применяемым вмешательством остается эндоскопическая папиллосфинктеротомия.
Однако частота осложнений после ЭПСТ не уменьшается, несмотря на накопление большого опыта специалистами, применение современного и более безопасного эндоскопического инструментария, а также анализа факторов риска развития осложнений и разработки профилактических мероприятий. Одним из спорных вопросов является необходимость разрушения сфинктерного аппарата большого дуоденального сосочка при данном вмешательстве у больных с холедохолитиазом. Благодаря современным малоинвазивным подходам к лечению холедохолитиаза многие исследователи стали внедрять и анализировать новые сфинктеросохраняющие методики, одной из которых является эндоскопическая баллонная папиллодилатация. Была разработана техника выполнения вмешательства, которая оказалась более легко выполнимой, нежели ЭПСТ
[192]. Однако особенности техники выполнения папиллодилатации значительно варьируют до настоящего времени, что свидетельствует об отсутствии единого мнения у разных авторов и о недостаточном подтверждении эффективности одного из способов. Весьма актуальными остаются и вопросы выбора показаний к баллонной папиллодилатации, а, следовательно, и решение вопроса о необходимости определения критериев отбора и соответствующего обследования больных. В литературе обсуждается и вопрос осложнений ЭПД, особенно остро - развития панкреатита. Однако, не определена четкая схема ведения пациентов в послеоперационном периоде, направленная на профилактику развития данного осложнения. Также не решен вопрос о влиянии эндоскопической баллонной папиллодилатации на функциональное состоянии сфинктера Одди в отдаленные сроки после вмешательства.
Данная работа проведена с целью определения показаний к выполнению эндоскопической баллонной папиллодилатации при холедохолитиазе, усовершенствования техники выполнения данного вмешательства, определения особенностей ведения больных в послеоперационном периоде и оценки функционального состояния сфинктерного аппарата БДС после папиллодилатации.
ГЛАВА II
КЛИНИЧЕСКИЙ МАТЕРИАЛ И МЕТОДЫ ОБСЛЕДОВАНИЯ
Для решения поставленных задач настоящей работы было проведено проспективное исследование, основанное на анализе результатов обследования и лечения больных с холедохолитиазом при калькулезном холецистите, постхолецистэктомическом синдроме и билиарном панкреатите.
В период с февраля 2000 года по февраль 2002 года в клинике госпитальной хирургии № 2 РГМУ выполнено 935 эндоскопических оперативных вмешательств на БДС при различной патологии панкреатобилиарной области. Из них 357 вмешательств выполнено по неотложным показаниям и 578 - в плановом порядке. Послеоперационные осложнения развились у 46 больных (4,9%), в 8 случаях (0,9%) отмечены летальные исходы.
Из общего числа больных конкременты во внепеченочных желчных протоках были выявлены у 469 пациентов (50,2%; 469/935). Из них у 327 (69,7%; 327/469) при первичном обследовании обнаружен изолированный холедохолитиаз, а в остальных случаях отмечалось сочетание его с другой патологией: холедохолитиаз в сочетании с папиллостенозом (92 больных), в сочетании с доброкачественными новообразованиями БДС (47 больных), в сочетании с послеоперационными стриктурами желчных протоков (3 больных).
Средний возраст больных с холедохолитиазом составил 61,7±16,7 (15-93 года) лет.
2.1. Построение научного исследования.
В плановом порядке за указанный двухлетний период (02.2000 – 02.2002 г.г.) эндоскопические вмешательства по поводу изолированного холедохолитиаза выполнены 151 пациенту (46%; 151/327): из них ЭПСТ с экстракцией конкрементов выполнена 115 больным, ЭПД с экстракцией конкрементов - 33 пациентам, ЭПД, дополненная папиллосфинктеротомией - 3 больным.
Набор в группу больных с холедохолитиазом для выполнения ЭПД проводился проспективно на основании разработанных критериев отбора. Формируя данные критерии, учитывался опыт применения папиллодилатации различными авторами. Ввиду того, что в исследования включались либо все больные, либо больные с ограничениями по возрасту, анатомическим характеристикам билиарного тракта и другим критериям, результаты их значительно отличались, что учтено при определении критериев отбора в данной работе [63,143,156]. Особенное внимание уделено осложнениям данного вмешательства и факторам риска их развития. В основном, это касалось развития острого панкреатита в послеоперационном периоде. К тому же, учитывали необходимость контроля функционального состояния сфинктера Одди после ЭПД в будущем. Ограничение применения нового вмешательства на БДС, особенно на начальных этапах освоения методики, мы считаем целесообразным. Данная тактика внедрения метода в ежедневную практику позволяет избежать отрицательных результатов, не связанных непосредственно с самим эндоскопическим вмешательством.
Таким образом, баллонную папиллодилатацию при холедохолитиазе выполняли в плановом или отсроченном порядке после разрешения клинико-лабораторных проявлений механической желтухи, острого панкреатита или острого калькулезного холецистита, а также после полноценного комплексного обследования. Вмешательство выполняли больным в удовлетворительном общем состоянии, без выраженной сопутствующей патологии, с анатомическими условиями панкреатобилиарной зоны, не предполагающими технических сложностей, а также не требующими применения различных видов литотрипсии. Из исследования исключались больные с папиллостенозом, выявленном при дооперационном обследовании или во время эндоскопической операции.
Учитывая все вышеизложенное, были сформулированы следующие критерии отбора больных:
|
Таким образом, в результате обследования больных и определения показаний к выполнению эндоскопической баллонной папиллодилатации в соответствии с указанными критериями отбора, в исследование были включены 33 пациента с изолированным холедохолитиазом.
2.2. Клиническая характеристика больных.
В период с февраля 2000 года по февраль 2002 года эндоскопическая баллонная папиллодилатация выполнена 33 больным с холедохолитиазом. Среди них было 9 мужчин (27,3%) и 24 женщины (72,7%). Средний возраст больных составил 54,2±11,1 года (32 - 74 года) (рис.2.1).
Рис.2.1. Распределение больных по возрасту.
При первичном обследовании пациентов (учитывая 2-х суточную динамику клинического течения заболевания, лабораторные показатели и данные УЗИ) установлены следующие диагнозы (табл.2.1): калькулезный холецистит - у 26, из них острый холецистит выявлен у 8 и хронический у 18. У остальных 7 больных имелся постхолецистэктомический синдром, проявляющийся симптомами желчной гипертензии разной степени выраженности (от субклинической формы билиарной гипертензии (3) до механической желтухи (4)), а также симптомами острого панкреатита у одного больного и хронического панкреатита у двоих.
Таблица 2.1
Клиническое течение холедохолитиаза
|
Клинические диагнозы |
Механическая желтуха |
Субклиническая форма билиарной гипертензии |
Всего |
|
Калькулезный холецистит - ОКХ - ХКХ |
4 10 |
4 8 |
26 |
|
ПХЭС -хронический панкреатит -острый панкреатит |
1 2 1 |
3 - - |
7 |
|
Итого: |
18 (55 %) |
15 (45 %) |
33 |
Желчнокаменный анамнез прослеживался у 25 больных: до 1 года включительно – у 6, от 2 до 5 лет включительно – у 9, более 6 лет – у 10 пациентов. У остальных 8 пациентов приступ желчной колики отмечен впервые.
Механическая желтуха осложнила течение холедохолитиаза у 18 пациентов (55%), в остальных 15 случаях выявлена субклиническая форма билиарной гипертензии. У троих больных механическая желтуха развилась в стационаре, у остальных 15 больных – в среднем за 1,8 ± 1,3 (1-6) суток до поступления в клинику.
Сопутствующая патология имелась у 25 больных и была представлена в основном ишемической болезнью сердца, гипертонической болезнью (табл.2.2). У всех больных сопутствующая патология на момент настоящей госпитализации была компенсирована.
Следует отметить, что у 3 больных имелся риск возникновения желудочно- кишечного кровотечения вследствие высокой возможности развития нарушений свертывающей системы крови в случае оперативного вмешательства:
1) выраженная тромбоцитопения у больной с лимфосаркомой (в стадии стойкой ремиссии на момент настоящей госпитализации), состояния после нескольких курсов полихимиотерапии;
2) длительный прием непрямых антикоагулянтов (фенилина) наряду с другими кардиальными препаратами по поводу комбинированного порока сердца, состояния после комиссуротомии от 1989 года, мерцательной аритмии;
3) постоянный прием аспирина после перенесенного инфаркта миокарда (1993г.) и аорто-коронарного шунтирования в 1995 году.
Таблица 2.2
Сопутствующая патология у больных с холедохолитиазом
|
Сопутствующая патология |
Число пациентов |
|
Гипертоническая болезнь 2 стадии |
11 |
|
Симптоматическая артериальная гипертензия |
3 |
|
Ишемическая болезнь сердца |
23 |
|
Комбинированный порок сердца, состояние после комиссуротомии |
1 |
|
Состояние после аорто-коронарного шунтирования |
1 |
|
Нарушения ритма - Желудочковая экстрасистолия - Предсердная экстрасистолия - Мерцательная аритмия |
5 - 2 - 1 - 2 |
|
Перенесенный инсульт |
2 |
|
Лимфосаркома в стадии ремиссии, тромбоцитопения |
1 |
|
Наследственная сфероцитарная гемолитическая анемия |
1 |
|
Хронический бронхит |
2 |
|
Хронический пиелонефрит |
1 |
|
Варикозная болезнь нижних конечностей |
1 |
|
Узловой зоб |
2 |
|
Язвенная болезнь ДПК |
2 |
|
Маниакально-депрессивный психоз в стадии ремиссии |
1 |
Примечание: Цветом отмечена сопутствующая патология, повышающая в случае операции риск возникновения кровотечения.
2.3. Методы обследования больных.
Отбор больных для выполнения ЭПД осуществлялся в два этапа с анализом клинической картины заболевания, результатов лабораторной диагностики и инструментальных методов обследования [47,58,175,180].
Первый этап отбора – клинико-лабораторная характеристика заболевания и скрининговое ультразвуковое исследование позволяли предположить у больного наличие холедохолитиаза. Прежде всего, всем больным при наличии подозрений на заболевание внепеченочных желчных протоков или явной механической желтухи в первые двое суток от поступления выполнялось ультразвуковое исследование органов брюшной полости. Выявление при УЗИ камней желчных протоков, дилатации желчевыводящих протоков и/или повышения маркеров холестаза (билирубин, ЩФ, АЛТ, АСТ) по данным биохимического исследования крови требовало расширения диагностической программы (схема 2.1) с целью подтверждения диагноза и выбора оптимального метода лечения
[47,58,180].
Схема 2.1
Лечебно-диагностический алгоритм при подозрении на холедохолитиаза
Второй этап отбора включал выполнение эндоскопической ультрасонографии панкреатобилиарной зоны и эндоскопической папиллосфинктероманометрии для верификации изолированного характера холедохолитиаза [30,31,45,52,71,84,198,221]. ЭУС выполнялась с целью уточнения состояния внепеченочных желчных протоков, определения точного диаметра общего желчного протока и оценки его содержимого; при подтверждении холедохолитиаза - определение количества конкрементов и их размеров; выявления изменений терминального отдела холедоха, включающие различные доброкачественные новообразования данной области; а также определения состояния поджелудочной железы, печени, желчного пузыря. При верификации холедохолитиаза без сопутствующих изменений терминального отдела холедоха, больным, соответствующим критериям отбора, выполнялась эндоскопическая папиллосфинктероманометрия. Целью выполнения ЭПСМ являлась оценка функционального состояния сфинктера Одди с последующим решением вопроса о выборе оптимального способа эндоскопического вмешательства. При выявлении папиллостеноза, определении его локализации и протяженности, больным выполнялась ЭПСТ; при отсутствии функциональных изменений СО – эндоскопическая баллонная папиллодилатация.
Лабораторная диагностика включала проведение клинического анализа крови и мочи по общепринятым методикам; биохимического исследования сыворотки крови с обязательным определением билирубина и его фракций (по методу Ендрашика- Гроффа на приборе КФК-3), аспартатаминотрансферазы (АСТ) и аланинаминотрансферазы (АЛТ) (по унифицированному методу DGKC/IFCC), щелочной фосфатазы (методом DGKC c DEA-буфером (диэтаноламин) прибором Cobas Mira plus, фирмы Hoffman La Roche, Швейцария). Наличие воспалительных изменений в паренхиме поджелудочной железы в до- и послеоперационном периоде определяли по уровню амилазы мочи (по Вольгемуту) в до- и послеоперационном периоде, а также определением
уровня амилазы и липазы сыворотки крови в послеоперационном периоде. Все реагенты сертифицированы МЗ РФ для лабораторной диагностики.
Ультразвуковое исследование гепатопанкреатобилиарной зоны проводилось всем больным в 1-2 сутки от поступления. Исследование выполняли на аппаратах фирм “Siemens” SONOLINE Versa plus, “General Electric Medical Systems” Logiq-700 MR и “Synergy” Diasonics Ultrasound Multisync M-500 при помощи мультичастотных конвексного и линейного датчиков, работающих в диапазоне реального масштаба времени с использованием серой шкалы, с частотой 2 - 10 МГц. Обследование выполняли натощак, проводя полипозиционное сканирование панкреатобилиарной зоны и органов брюшной полости. Задачей ультразвукового исследования была визуализация и определение состояния желчного пузыря (его размеры, толщина стенки, содержимое, при наличии конкрементов в просвете - определение их числа и размеров); внепеченочных желчных протоков (диаметр холедоха, гомогенность просвета, наличие дополнительных структур в его просвете, их количество и размеры, наличие и характер акустической тени); оценка состояния внутрипеченочных и долевых печеночных протоков (их диаметр, гомогенность просвета). Изменения поджелудочной железы оценивали по размерам, контурам, состоянию паренхимы органа и панкреатического протока. Признаками билиарной гипертензии считали расширение диаметра общего желчного протока более 8 мм, что являлось косвенным показателем наличия холедохолитиаза [24]. К прямым признакам камней общего желчного протока относили: выявление в просвете одиночных или множественных гиперэхогенных включений чаще округлой формы с эхонегативной акустической тенью. Иногда при осмотре дистальной части протока определяли неоднородность просвета, без четкой акустической тени, что также позволяло высказаться о наличии холедохолитиаза. Помимо этого, обращали пристальное внимание на присутствие в желчном пузыре мелких (до 5 мм) конкрементов и гиперэхогенной взвеси, что считали прогностически неблагоприятным фактором наличия холедохолитиаза.
Данные находки при отсутствии прямых или косвенных ультразвуковых признаков холедохолитиаза у больных с клиническими и/или лабораторными признаками холестаза являлись показанием для выполнения ЭУС.
Эндоскопическую ультрасонографию выполняли с помощью эхогастрофиброскопа GF-UM20 (Olympus) с радиальным (360°) направлением ультразвукового сканирования. На дистальном конце эхоэндоскопа имеется ультразвуковой датчик, соединенный с ультразвуковым эндоскопическим центром UM- M30 (Olympus), (НГР 97/401). Ультразвуковой центр включает в себя монитор высокого разрешения, панель управления, электронный процессор, совмещенный с генератором ультразвуковых волн. Частота волн генератора составляет 7,5, 12 и 20 МГц [125]. Глубина пенетрации ультразвуковых волн от датчика зависит от их частоты и составляет от 1 до 12 см. Ультразвуковой датчик эхоэндоскопа покрыт сменным латексным баллоном, который в процессе исследования заполняется водой для обеспечения проводящей среды и создания оптимального фокусного расстояния, равного 2 см.
Исследование выполнялось натощак, после стандартной премедикации, включающей антисекреторные препараты (атропин, метацин, платифиллин), спазмолитики (но-шпа, папаверин, бускопан), наркотические анальгетики (промедол) и/или седативные средства (диазепам, седуксен, реланиум). Местная анестезия глотки осуществлялась орошением 10% раствора лидокаина.
Эндосонографическое обследование панкреатобилиарной зоны проводилось из нескольких стандартных положений аппарата [31,138]. Вначале эхоэндоскоп проводили в луковицу ДПК, при этом визуализировали желчный проток и частично желчный пузырь, головку поджелудочной железы и панкреатический проток, воротную вену и Фатеров сосочек в продольном сечении. Во время исследования большое внимание уделяли осмотру области большого дуоденального сосочка на предмет выявления его стенозирующих и обтурирующих изменений. С этой целью эндоскоп продвигали в
вертикальный отдел ДПК и устанавливали его напротив Фатерова сосочка перпендикулярно, добиваясь при этом поперечного сканирования области сосочка. Затем аппарат проводили в нижнегоризонтальную часть кишки на уровень аорты и, постепенно извлекая эндоскоп, выводили его вновь в луковицу ДПК. При этом осматривали головку железы, панкреатический и желчный протоки, сосочек. После выведения аппарата в луковицу осматривали желчный пузырь, проксимальные отделы желчного протока, включая магистральные долевые протоки и частично паренхиму правой доли печени, перешеек железы и воротно-брыжеечное венозное соединение. Далее выполняли сканирование из средней и верхней трети тела желудка, оценивая тело и хвост поджелудочной железы, сосудистые ориентиры, а также зоны регионального лимфооттока (парапанкреатическая клетчатка, гепатодуоденальная связка, зона чревного ствола, области по ходу брыжеечных и селезеночных сосудов).
Проводящая среда создавалась за счет наполнения полости органа (желудка, двенадцатиперстной кишки) водой через биопсийный канал, либо при помощи заполнения баллона водой на дистальном конце аппарата. Из описанных стандартных положений эхоэндоскопа осматриваются желчный пузырь, все отделы поджелудочной железы, желчный и панкреатический протоки на всем их протяжении, а также область Фатерова сосочка.
Желчный проток в норме при ЭУС (рис.2.2) представляет собой анэхогенную трубчатую структуру, шириной не более 7 мм [58, 198,180], с равномерной трехслойной стенкой, как у больных с наличием ЖП, так и после холецистэктомии. По данным A.W.Majeed с соавт., 1999г. нормальный диаметр желчного протока после холецистэктомии статистически достоверно не изменяется [161]. Внутренний гиперэхогенный слой соответствует слизистому и подслизистому слою, гипоэхогенный слой – фибромускулярному слою протока, внешний гиперэхогенный слой –соединительнотканной оболочке, покрывающей фибромускулярный слой. Толщина стенки протока в норме не превышает 1,5 мм.
Рис.2.2. Эндосонографическая картина желчного протока в норме.
![]()
![]()
![]() Камни желчных протоков (рис.2.3а) эндосонографически интерпретировались как единичные или множественные интенсивные гиперэхогенные образования округлой формы, размерами более 2 мм, с эхонегативной акустического тенью, локализованные в различных отделах магистральных желчных протоков. Единичные или множественные внутрипротоковые гиперэхогенные включения (рис.2.3б) неправильной формы со слабой акустической эхонегативной тенью, либо без неѐ, чаще всего локализованные в дистальных отделах холедоха трактовались как желчная замазка (или же мягкие камни). Наличие в просвете дистальной части холедоха, практически в надпапиллярном отделе, единичных гиперэхогенных сигналов размерами менее 2 мм без акустических теней расценивали как крошкообразные массы или микрохоледохолитиаз (2.3в).
Камни желчных протоков (рис.2.3а) эндосонографически интерпретировались как единичные или множественные интенсивные гиперэхогенные образования округлой формы, размерами более 2 мм, с эхонегативной акустического тенью, локализованные в различных отделах магистральных желчных протоков. Единичные или множественные внутрипротоковые гиперэхогенные включения (рис.2.3б) неправильной формы со слабой акустической эхонегативной тенью, либо без неѐ, чаще всего локализованные в дистальных отделах холедоха трактовались как желчная замазка (или же мягкие камни). Наличие в просвете дистальной части холедоха, практически в надпапиллярном отделе, единичных гиперэхогенных сигналов размерами менее 2 мм без акустических теней расценивали как крошкообразные массы или микрохоледохолитиаз (2.3в).
Рис. 2.3. Эндосонографическая картина холедохолитиаза:
а) камни желчного протока,
б) замазкообразные массы желчного протока,
в) крошкообразные массы (микрохоледохолитиаз)
![]()
![]()
![]() Фатеров сосочек (рис.2.4а) в норме (в поперечном сечении) визуализируется как дополнительное округлое (овальное) многослойное образование стенки вертикального отдела ДПК. При идентификации структуры сосочка в подслизистом слое ДПК, начиная от прилежащей к стенке кишки паренхимы железы, определяются поочередно мышечный слой ДПК (гипоэхогенный), подслизистый слой ДПК (гиперэхогенный), сфинктер Одди (тонкий гипоэхогенный) и внутренний гиперэхогенный слой, соответствующий слизистому и подслизистому слоям ампулы сосочка. При смещении ультразвукового датчика в проксимальном направлении подобная эхографическая картина изменяется индивидуально, соответственно изменению структурных соотношений терминальных отделов желчного и панкреатического протоков относительно стенки ДПК. Увеличение Фатерова сосочка в размерах более 1 см в продольном сечении, выявление в просвете ампулы сосочка дополнительных образований исходящих из его стенок или же изменение эхографических характеристик многослойной структуры данного анатомического образования интерпретируется как патологическое изменение области сосочка, а именно интрамуральное образование БДС (рис.2.4 бв).
Фатеров сосочек (рис.2.4а) в норме (в поперечном сечении) визуализируется как дополнительное округлое (овальное) многослойное образование стенки вертикального отдела ДПК. При идентификации структуры сосочка в подслизистом слое ДПК, начиная от прилежащей к стенке кишки паренхимы железы, определяются поочередно мышечный слой ДПК (гипоэхогенный), подслизистый слой ДПК (гиперэхогенный), сфинктер Одди (тонкий гипоэхогенный) и внутренний гиперэхогенный слой, соответствующий слизистому и подслизистому слоям ампулы сосочка. При смещении ультразвукового датчика в проксимальном направлении подобная эхографическая картина изменяется индивидуально, соответственно изменению структурных соотношений терминальных отделов желчного и панкреатического протоков относительно стенки ДПК. Увеличение Фатерова сосочка в размерах более 1 см в продольном сечении, выявление в просвете ампулы сосочка дополнительных образований исходящих из его стенок или же изменение эхографических характеристик многослойной структуры данного анатомического образования интерпретируется как патологическое изменение области сосочка, а именно интрамуральное образование БДС (рис.2.4 бв).
Рис.2.4. Эндосонографическая картина Фатерова сосочка: а) в норме,
б) склеротические изменения (папиллостеноз),
в) новообразование
Эндоскопическая папиллосфинктероманометрия проводилась по принятой в клинике методике [27,45]. Исследование выполняли при помощи дуоденоскопов JF-1T, JF-1T10, JF-1T30; маркированного однопросветного катетера (внешний диаметр 1,7 мм, внутренний диаметр 0,8 мм), соединенного системой микрокапилляров с перфузионным манометрическим комплексом. На дистальном конце катетера имеется металлический закругленный наконечник для облегчения канюляции протоковых систем, в 6 мм от которого на боковой поверхности открывается канал катетера, диаметром 0,5 мм. Проксимальнее отверстия на катетер циркулярно наносятся черные метки на расстоянии 5, 10, 15 и 20 мм.
Манометрический комплекс состоит из емкостных мембранных датчиков, преобразователя сигналов Polygraph HR-93-7110 (рис.2.5), пневмогидравлической помпы, регистрирующего устройства PC IBM. Полученные данные регистрировались и обрабатывались с помощью компьютерной программы Polygraph HR, Synectics.
Рис.2.5. Схема выполнения эндоскопической перфузионной папиллосфинктероманометрии.
Принцип регистрации давления состоит в следующем [45,116,128]. Канал катетера соединен с емкостным датчиком, последний соединяется с пневмогидравлической помпой при помощи системы микрокапилляров, канал перфузируется помпой с постоянной скоростью (0,3 мл/мин; давление помпы на поток жидкости составляет 300 мм рт.ст.) потока жидкости (физиологический раствор). Изменение давления в органе, в котором установлен катетер, приводит к изменению скорости потока жидкости в канале катетера. Возникающие при этом колебания давления в датчиках манометра, преобразуются в электрические сигналы, усиливаются, измеряются и передаются на регистрирующее устройство. Графическая регистрация изменения давления отображается на экране компьютера (рис.2.6). С помощью специальной компьютерной программы Polygraph HR, Synectics происходит обработка полученных данных.
Рис.2.6. Графическое изображение параметров эндоскопической папиллосфинктероманометрии.
Исследование проводилось натощак после премедикации, включающей внутримышечное введение 2,0 мл реланиума за 30 минут до исследования и орошение глотки 10% раствором лидокаина непосредственно перед введением эндоскопа
[51,116,129,195]. ЭПСМ выполняли отдельно от ЭРХПГ.
Перед исследованием проводилась подготовка аппаратуры к работе и внесение информации о больном в локальный архив данных. При помощи пневмогидравлической помпы вся система заполняется физиологическим раствором таким образом, чтобы в ней отсутствовали пузырьки воздуха. Калибровка датчиков осуществлялась автоматически с помощью компьютерной программы путем создания определенного давления на дистальном конце катетера, который вначале располагали на уровне датчиков, а затем выше их уровня на 37 см. Перед началом исследования датчики устанавливали на уровень предполагаемой проекции БДС больного.
При проведении дуоденоскопа к области БДС и осмотре верхних отделов пищеварительного тракта, избегали гиперинсуффляции [195]. После осмотра области БДС по биопсийному каналу эндоскопа катетер проводили в вертикальный отдел ДПК и вначале регистрировали давление кишки. Далее селективно канюлировали холедох и проводили измерение давления в протоке. Положение катетера в желчном протоке контролировали по эндоскопическим признакам (направление катетера на 11 часов циферблата), а также по аспирации желчи по каналу катетера. При канюляции панкреатического протока катетер извлекали в двенадцатиперстную кишку и снова старались селективно катетеризировать холедох. Попытки катетеризации желчного протока выполняли не более 10 минут и в случае неудачи от дальнейшего выполнения ЭПСМ воздерживались. После регистрации давления в желчном протоке катетер постепенно извлекали в двенадцатиперстную кишку через область сфинктера, останавливаясь на каждой метке в течение 2 мин. При необходимости выполняли фармакологическую пробу с папиллорелаксантами [116,118,152,196]. С этой целью использовали сублингвальный прием 0,5 мг нитроглицерина, после чего повторно записывали давление в СО в той же последовательности. После определения давления в сфинктере катетер вновь извлекали в просвет кишки и повторно регистрировали дуоденальное давление.
При оценке полученных результатов определяли следующие показатели функциональной активности сфинктера Одди (рис.2.7) - его тонус и двигательную активность. Тонус СО отражает базальное давление сфинктера; двигательную активность СО - амплитуда и частота сокращений СО; также определяли протяженность СО, градиенты давлений между ДПК, СО и желчным протоком
[25,26,72,114,122,128,129,197,213].
Рис.2.7. Манометрическая запись функционального состояния сфинктера Одди в норме.
Оценивая все перечисленные параметры, мы ориентировались на нормальные показатели функционального состояния СО (табл.2.3), полученные в нашей клинике в предыдущих исследованиях [25,27,30,45].
Таблица 2.3 Нормальные значения параметров функционального состояния сфинктера Одди
|
Показатели моторики СО (показатели давления в mm Hg) |
Нижняя граница нормы |
Среднее значение (min-max) |
Верхняя граница нормы |
|
Давление в ДПК |
2 |
6,6 (4-9) |
12 |
|
Давление холедоха |
5 |
11,8 (10-14) |
18 |
|
Базальное давление СО |
12 |
22,5 (8-50) |
35 |
|
Градиент ДПК-холедох |
3 |
5,8 (5-6,5) |
9 |
|
Градиент холедох-СО |
6 |
8,5 (8-9,5) |
12 |
|
Градиент СО-ДПК |
9 |
15,9 (14-18) |
22 |
|
Амплитуда сокращений |
1 |
21,6 (5-58) |
42 |
|
Частота сокращений в мин |
2 |
3,5 (2,5-4) |
6 |
Определяющим манометрическим признаком папиллостеноза (рис.2.8) являлось повышение среднего значения уровня базального давления выше 35 мм рт.ст., не снижающееся до нормальных значений после приема папиллорелаксантов; а также повышение градиентов давлений между двенадцатиперстной кишкой, сфинктером Одди и желчным протоком [118,119,171,213]. Папиллоспазм (гипертонус СО) характеризовался
снижением повышенного базального давления до нормальных значений после приема папиллорелаксантов [45,116,118,128].
Рис.2.8. Манометрическая картина папиллостеноза.
После исследования всем больным проводилась профилактика развития острого панкреатита, который встречается в 6% случаях [182,221]. Причем, по данным P.Rolny с соавт., 1990г., после канюляции ГПП во время исследования острый панкреатит развивается у 11% больных, при канюляции же только желчных протоков – у 1% больных
[182]. Профилактические мероприятия в нашем исследовании включали голод в течение суток, холод на эпигастральную область, инфузию кристаллоидных растворов с ингибиторами протеаз, назначение спазмолитических и холинолитических средств. Лабораторный контроль включал определение уровня амилазы мочи (диастазурии) через 6 и 12 часов после исследования.
2.4. Техника эндоскопической баллонной папиллодилатации.
Больным с клинико-инструментальной картиной холедохолитиаза, соответствующим критериям отбора, выполняли эндоскопическую ретроградную холангиографию (ЭРХГ) как начальный этап баллонной папиллодилатацией с последующей экстракцией конкрементов.
Рис.2.9. Эндоскопическая картина селективной канюляции общего желчного протока (на фоне сублингвального приема папиллорелаксанта); в направлении 11 часов по циферблату.
Эндоскопическую ретроградную холангиографию выполняли натощак, в положении больного на левом боку и на животе, через 30-40 минут после стандартной премедикации [121]. Премедикация включала следующие препараты: внутримышечное введение наркотических анальгетиков (промедол), спазмолитиков (но-шпа, папаверин, бускопан), холинолитиков (атропин, метацин, платифиллин) за 30 минут до вмешательства; местная анестезия глотки 10% раствором лидокаина непосредственно перед введением эндоскопа; при необходимости - внутривенное или внутримышечное введение седативных препаратов (седуксен, реланиум) [50]. Во время вмешательства в качестве папиллорелаксанта использовали сублингвальный прием 0,5-1 мг нитроглицерина (1-2 таб. или 3 капли 1% спиртового раствора) непосредственно перед канюляцией желчного протока с целью релаксации сфинктера Одди, предупреждения его спазма при инструментальных манипуляциях [19,116,118,152,155] (рис.2.9).
Это в свою очередь облегчало селективное проведение катетера в желчные протоки и являлось мерой предупреждения острого панкреатита в послеоперационном периоде
[162]. По манометрическим данным H.-D.Allescher с соавт., 1990г. применение бускопана также облегчает канюляцию протоков за счет снижения перистальтики антрального отдела желудка и 12-перстной кишки и угнетения моторной активности СО (снижение базального давления, частоты и амплитуды сфинктера) [50].
Эндоскопические вмешательства выполнялись при помощи оборудования фирмы Olympus: EVIS-EXERA, EVIS-140, EVIS-100, СLE-10, видеоэндоскопов с боковой оптикой TJF-160R, JF-140R и фиброскопов с боковой оптикой TJF-10, JF-1T10. При гастродуоденоскопии оценивали состояние желудка и двенадцатиперстной кишки, особое внимание уделяя осмотру малого и большого дуоденального сосочка и околососочковой области. Катетеризацию желчных протоков выполняли при помощи катетеров фирмы Olympus: PR-4Q, PR-104Q-1, PR-126Q1; фирмы Wilson-Cook Medical Inc.: GT-2-T, GT-1.
При канюляции БДС всегда стремились провести катетер селективно в желчный проток. При этом придерживались определенных правил и анатомических ориентиров
[89,94-96]. Непосредственно перед канюляцией БДС четко определяли направление оси ТОХ, необходимой для достижения протока. Кончик катетера устанавливали в устье сосочка без чрезмерных усилий, избегая грубого проведения катетера, вызывающего спазм сфинктера Одди, и приводящего к развитию отека тканей сосочка. Для проведения любого эндоскопического инструмента в желчный проток «подходили» к устью сосочка снизу и немного справа, ориентируя ось катетера в направлении 11 часов по циферблату (см. рис.2.9). Канюляцию желчного протока облегчало введение катетера непосредственно под так называемую "крышу" ампулы БДС, т.е. по верхнему краю устья, приподнимая катетер большим винтом или подъемником вверх. При этом также избегали чрезмерных усилий, давлений катетером на слизистую ампулы БДС. При неудачной канюляции путем стандартных приемов изменяли положение дуоденоскопа в просвете ДПК с отведением эндоскопа от БДС; использовали нежное продвижение катетера вперед с целью облегчения достижения верхнего края папиллы при естественно изогнутом дистальном конце катетера; или наоборот, применяли максимально приближенную технику - "технику поцелуя". При этом, устанавливая кончик катетера в устье в максимально изогнутом кверху положении, несколько извлекая дуоденоскоп, проводили аспирацию воздуха из просвета ДПК. В случаях неудачных попыток селективной канюляции использовали рентгеноконтрастные пластиковые и металлические струны диаметром 0.035 дюйма с атравматичным кончиком: G35-1LB (Olympus), Tracer Metro Met-35-480 (Wilson-Cook Medical Inc.) (рис.2.10), облегчающие канюляцию.
Рис.2.10. Эндоскопическая картина селективной катетеризации общего желчного протока с использованием катетера и рентгеноконтрастной пластиковой и металлической струны.
Канюляцию и контрастирование панкреатического протока старались избегать, так как состояние поджелудочной железы и ее протоковой системы было оценено при эндосонографии до операции, а катетеризация и введения контрастных веществ в панкреатические пути является одним из факторов риска развития острого панкреатита в послеоперационном периоде [109,211].
После глубокой селективной канюляции желчного протока производили аспирацию 2-3 мл желчи для подтверждения локализации катетера, удаления из него пузырьков воздуха и предупреждения создания искусственной гипертензии в желчных
путях (что выражается в появлении болевого синдрома, особенно у больных с постхолецистэктомическим синдромом).
Холангиографию выполняли введением 5-10 мл 60% водорастворимого рентгеноконтрастного вещества (триомбраст, урографин, верографин) с добавлением 1 мл 1% раствора диоксидина. Для достижения полноценной холангиограммы (в том числе и печеночных протоков) введение контрастного вещества начинали от бифуркации протока, постепенно извлекая катетер и заполняя, таким образом, желчные протоки на всем протяжении. Рентгенологическое исследование проводили на мобильных рентгенологических аппаратах с помощью электронно-оптического преобразователя Arcovis HF (Италия) и Siremobil Compact фирмы Siemens (Германия). При этом оценивали состояние желчевыводящих протоков (рис.2.11): диаметр протоков, контуры, просвет, наличие негомогенности и/или теней конкрементов, а также состояние ЖП при его наличии и контрастировании [118]. Нормальным диаметром желчного протока считали до 7 мм включительно [24,58,198].
Рис.2.11. Эндоскопическая ретроградная холангиография.
Эндоскопическую баллонную папиллодилатацию выполняли при подтверждении холедохолитиаза и соответствии данных критериям отбора. Вначале по катетеру в желчный проток проводили рентгеноконтрастную пластиковую или металлическую струну-проводник диаметром 0.035 дюйма с атравматичным кончиком:
G35-1LB (Olympus), Tracer Metro Met-35-480 (Wilson-Cook Medical Inc.). Катетер извлекали и по струне-проводнику на уровень БДС устанавливали катетер с баллоном для дилатации (рис.2.12).
Рис.2.12. Начальный этап эндоскопической баллонной папиллодилатации: а) проведение струны-проводника по катетеру в желчный проток, б) струна-проводник установлена в желчном протоке,
в) проведение баллона в желчный проток по струне-проводнику
В работе использовали баллоны диаметрами 4, 6, 7, 8 и 10 мм (6х3, 7х3, ОЭП МПИ, г. Нижний Новгород, Россия; QBD-4х3, QBD-6х3, QBD-8х3, QBD-10х3, Wilson-Cook Medical Inc., США; Max Force 4х4, Microvasive, США), длиной 3, 4 и 8 см (рис.2.13).
Рис.2.1. Эндоскопическая папиллодилатация различными по диаметру баллонами.
Адекватное положение баллона контролировалось при помощи рентгеноконтрастных меток, имеющихся на обоих концах баллона. Баллон заполняли 50% контрастным веществом (триомбраст, урографин, верографин) под давление при помощи
механического компрессора QBID (Wilson-Cook Medical Inc., США). Давление в баллоне нагнетали постепенно, тем самым, избегая "взрывной" дилатации. Вначале создавали давление 2 атм, а затем при необходимости 4 атм. При заполнении баллона контрастным веществом отчетливо определялось формирование "папиллярной талии" баллона (баллон приобретал форму "песочных часов") (рис.2.14). Постепенно "талия" расправлялась, после чего давление в баллоне выдерживали в течение 20-30 секунд (непосредственно этап дилатации). Визуализация "талии" баллона и ее последующее исчезновение свидетельствовало об успешной дилатации.
Рис. 2.14. Рентгенологическая картина эндоскопической папиллодилатации:
а) формирование «папиллярной талии» баллона б) полное расправление баллона
Необходимость выполнения повторных сеансов дилатации тем же баллоном или баллоном большего диаметра определяли индивидуально у каждого пациента. После выполнения сеанса дилатации контраст из баллонного катетера аспирировали при помощи компрессора и извлекали катетер со струной-проводником из желчного протока (рис.2.15). Критерием адекватности желчеоттока служило поступление желчи из устья холедоха с пузырьками воздуха тотчас после извлечения баллона [27].
Рис.2.15. Завершение сеанса папиллодилатации:
а) аспирация контрастного вещества из баллона; б) адекватное дренирование желчных протоков - поступление из устья холедоха желчи и пузырьков воздуха; в) устье БДС после дилатации.
Ревизию желчных путей и извлечение конкрементов выполняли при помощи различных корзинчатых захватов Дормиа (FG-18Q-1, FG-22Q-1, FG-23Q-1, Olympus), в том числе и корзинки Дормиа с каналом для струны MH-544 фирмы Olympus и/или ревизионного баллончикового катетера типа Фогарти (диаметр в расправленном состоянии 12 мм) (Escort II Double Lumen Extraction Balloon, Wilson-Cook Medical Inc., США) (рис.2.16).
Рис.2.16. Ревизия желчных протоков и экстракция конкрементов:
· верхний ряд – при помощи корзинки Дормиа
· нижний ряд – при помощи баллончикового катетера
С целью минимизации травмы тканей большого дуоденального сосочка проведение инструментов для ревизии желчных путей выполняли в соответствии с рекомендациями, аналогичными для проведения ЭРПХГ.
При наличии нескольких конкрементов извлечение их производили поэтапно, начиная с дистально расположенного камня.
Вмешательство заканчивали контрольной холангиографией для оценки полноты санации желчных путей. Об эффективности папиллодилатации судили на основании поступление желчи из устья холедоха с пузырьками воздуха тотчас после извлечения баллона, отсутствия при контрольной холангиографии конкрементов в просвете ОЖП, своевременной эвакуации контраста из желчных протоков.
2.5. Схема ведения больных в послеоперационном периоде.
Осложнения после эндоскопической баллонной папиллодилатации и степень их тяжести мы оценивали по классификации, предложенной P.B.Cotton с соавт. в 1991 году для эндоскопической ретроградной панкреатикохолангиографии и папиллосфинктеротомии (табл.2.4) [93].
Таблица 2.4
Классификация осложнений после эндоскопических вмешательств на БДС (P.B.Cotton с соавт., 1991)
|
Осложнение |
Легкой степени |
Средней степени |
Тяжелой степени |
|
Кровотечение |
-клинически наличие кровотечения -снижение Нв <3g -нет необходимости в переливании крови |
-необходимо переливание крови (4 порции и меньше) -ангиографические и хирургические вмешательства не показаны |
-переливание 5 и более порций крови -или - необходимость вмешательства (ангиографического или хирургического) |
|
Перфорация |
-возможное, или незначительное просачивание жидкости или контрастного вещества -консервативное лечение (инфузия и аспирация 3 дня и менее) |
Любая перфорация, требующая консервативного лечения от 4 до 10 дней |
-необходимость консервативного лечения более 10 дней -или - необходимость вмешательства (чрескожного или хирургического) |
|
Панкреатит |
-клиника панкреатита -повышение амилазы минимум в 3 раза более чем через 24 часа от операции, требующее назначения или продолжения плановых назначений в течение 2-3 дней |
Панкреатит, требующий госпитализации от 4 до 10 дней |
-госпитализация более 10 дней -или - геморрагический панкреатит, флегмона -или - образование псевдокист -или - необходимость вмешательства (чрескожное дренирование или хирургическая операция) |
|
Холангит |
>38°С 24-48 ч. |
-лихорадочное или септическое состояние, требующее более 3-х дней госпитализации -или - необходимость эндоскопического или чрескожного вмешательства |
Септический шок или операция |
|
Вклинение корзинки |
Спонтанное освобождение корзинки или при повторной эндоскопии |
Чрескожное вмешательство |
Операция |
В послеоперационном периоде проводилась комплексная профилактика развития острого панкреатита (табл.2.5). С этой целью назначалась инфузионная терапия,
включающая введение кристаллоидных препаратов, цитостатиков (5-фторурацил), ингибиторов протеаз (контрикал, гордокс, ингитрил); в качестве папиллорелаксантов назначали дицетел, одестон или нитросорбид в течение суток после вмешательства; проводилась антибактериальная терапия (антибиотики широкого спектра действия); также назначались спазмолитические средства, холинолитики, антисекреторные препараты (блокаторы Н2-гистаминовых рецепторов) и другие препараты, необходимые для индивидуальной коррекции имеющейся сопутствующей патологии [19,22,70,133,185]. При прогрессировании острого панкреатита на фоне проведения указанной консервативной терапии, выполняли ЭПСТ с декомпрессией Вирсунгова протока (панкреатико- дуоденальное стентирование) [49,186,217,220].
Таблица 2.5 Консервативная терапия после эндоскопической баллонной папиллодилатации
|
Группы препаратов |
Препараты |
Дозировки и способы введения |
|
Цитостатики |
5-фторурацил |
500 мг, в/в |
|
Ингибиторы протеаз |
Контрикал |
20 тыс.ед. в/в |
|
|
Гордокс |
200 тыс.ед. в/в |
|
|
Ингитрил |
60 мг в/в |
|
Папиллорелаксанты |
Нитросорбид |
10 мг х 4 р/д per os |
|
|
Одестон |
200 мг х 3 р/д per os |
|
|
Дицетел |
50-100 мг х3 р/д per os |
|
Антибиотики |
Ампиокс |
1 г х 4 р/д в/м |
|
|
Гентамицин |
80 мг х 2 р/д в/м |
|
Спазмолитики |
Но-шпа |
40 мг х 3 р/д в/м |
|
|
Папаверин |
40 мг х 3 р/д в/м |
|
М-холиноблокаторы |
Платифиллин |
2 мг х 3 р/д в/м |
|
|
Метацин |
1 мг х 3 р/д в/м |
|
Анальгетики |
Анальгин |
1 г х 3 р/д в/м |
|
Блокаторы Н2-гистаминовых рецепторов |
Ранитидин |
150 мг х 2 р/д per os |
|
|
Фамотидин |
20 мг х 2 р/д per os 20 мг х 2 р/д в/м |
|
Коррекция сопутствующей патологии (индивидуально) | ||
A.Minami с соавт., 1995г. при манометрическом исследовании до и после дилатации в ближайшие сроки выявили у части больных повышение базального давления и частоты сокращения сфинктера [166]. Вследствие этого, в нашем исследовании всем больным после ЭПД назначали спазмолитики с избирательным расслабляющим действием на СО. К тому же, одестон, обладая высокоселективным спазмолитическим действием на СО, не влияет на двигательную активность желчного пузыря, что позволяет применять его и при сохраненном пузыре, не опасаясь миграции конкрементов в протоки
[22,23,46].
Лабораторный контроль включал: контроль диастазурии через 5, 10 и 24 ч; определение уровня гемоглобина, эритроцитов и лейкоцитов крови через 6 и 24 ч; определение уровня амилазы сыворотки крови через 24 ч после вмешательства. Транзиторной амилаземией считали повышение уровня амилазы в сыворотки крови более чем в 3 раза выше нормальных значений, при отсутствии клинических признаков острого панкреатита [66].
При необходимости на следующие сутки выполняли стандартное ультразвуковое исследование органов брюшной полости и/или эндоскопическую ультрасонографию для оценки состояния поджелудочной железы, желчевыводящих протоков.
Больным с сохраненным желчным пузырем в последующем производили холецистэктомию. Операцию выполняли в максимально короткие сроки после эндоскопического вмешательства при удовлетворительном состоянии больного, в том числе и на следующий день после эндоскопической операции. Предпочтение отдавали лапароскопической холецистэктомии.
Контрольная эндоскопическая перфузионная папиллосфинктероманометрия. J.E.Geenen с соавт.,1984г. при манометрическом контроле не выявили статистически достоверной разницы между длиной разреза через 12 и 24 месяца после ЭПСТ: длина разреза уменьшается в течение первых 12 месяцев, через
24 месяца имеется незначительное уменьшение данного показателя (исходная длина разреза 11,0±1,5 мм; через 12 мес. - 7,5±0,7 мм; через 24 мес. - 6,5±0,7 мм) [115]. Ориентируясь на эти данные, контрольное обследование пациентов проводили в среднем через 1 год после эндоскопической папиллодилатации. После физикального осмотра и опроса больного, направленного на выявление панкреатобилиарных жалоб, выполняли контрольную ЭПСМ в амбулаторных условиях по описанной выше методике. При этом также проводились мероприятия, направленные на профилактику развития острого панкреатита - голод в течение суток, холод на область эпигастрия, назначение в стандартных дозировках спазмолитиков (но-шпа), селективных спазмолитиков для СО (нитроглицерин, дицетел или одестон), блокаторов Н2-гистаминовых рецепторов (ранитидин, фамотидин). Указанная терапия проводилась амбулаторно в течение суток после исследования.
2.6. Методы статистической обработки данных.
В работе количественные показатели представлены как среднее статистическое значение (М) ± стандартное отклонение (σ) [4,8,20]. Статистический анализ данных при определении достоверности различий количественных показателей результатов исследований проводили при помощи t-критерия Стьюдента и однофакторного дисперсионного анализа. При сравнении показателей манометрического исследования функциональной активности сфинктера Одди до и в среднем через 1 год после эндоскопического вмешательства использовали парный критерий Стьюдента. Различия считали статистически достоверными, если вероятность возможной ошибки – P (уровень значимости) была < 0,05. Статистическая обработка данных выполнялась с помощью программы "Биостатистика" для Windows - Primer of Biostatistics Version 4.03 (Stanton Glantz) [8].
ГЛАВА II I
РЕЗУЛЬТАТЫ ЭНДОСКОПИЧЕСКОЙ ДИАГНОСТИКИ И ЛЕЧЕНИЯ ИЗОЛИРОВАННОГО ХОЛЕДОХОЛИТИАЗА И ИХ ОБСУЖДЕНИЕ
3.1. Результаты отбора больных для выполнения эндоскопической баллонной папиллодилатации в соответствии с диагностическим алгоритмом.
Стандартная схема обследования больных с подозрением на холедохолитиаз в большинстве клиник включает проведение лабораторных анализов и стандартного ультразвукового исследования. В настоящее время в связи с расширением как диагностических, так и лечебных возможностей в эндоскопии панкреатобилиарной зоны, все большее значение приобретают дополнительные методики обследования данной категории больных. Для постановки точного диагноза и выбора метода лечения в качестве дополнительных методик применяли эндоскопическую ультрасонографию панкреатобилиарной области и эндоскопическую папиллосфинктероманометрию.
Согласно диагностическому алгоритму проспективно в клинике в плановом порядке было обследовано 290 больных с подозрением на протоковую патологию. Вначале работы были проанализированы результаты отбора пациентов для выполнения ЭПД в соответствии с указанным диагностическим алгоритмом. На данном этапе были проанализированы результаты выполнения больным с предполагаемой протоковой патологией ЭУС и ЭПСМ. Далее были изучены результаты обследования больных с уже верифицированным холедохолитиазом, подходящих для выполнения папиллодилатации, а затем и непосредственные результаты ЭПД. В заключение работы проведен анализ влияния ЭПД на функциональное состояние сфинктера Одди по данным контрольной ЭПСМ.
Результаты эндоскопической ультрасонографии панкреатобилиарной области
С 1997 года в клинике госпитальной хирургии № 2 применяется новый метод диагностики заболеваний пищевода, желудка, толстой кишки, а также поджелудочной железы и желчевыводящих путей - эндоскопическая ультрасонография. ЭУС панкреатобилиарной зоны в сроки проведения работы выполнена 280 больным, соответствующим критериям отбора. По техническим причинам не удалось выполнить ЭУС 10 больным. Из обследованных больных только у 62 (22,1%) при ЭУС выявлен изолированный холедохолитиаз. В остальных случаях выявлены другие заболевания панкреатобилиарной области, отсутствие протоковой патологии, или же холедохолитиаз сочетался с новообразованиями большого дуоденального сосочка (табл. 3.1).
Таблица 3.1
Результаты обследования больных по данным ЭУС
|
Заключение |
Число больных |
% |
|
Изолированный холедохолитиаз |
62 |
22,1 |
|
Холедохолитиаз + новообразования |
10 |
3,6 |
|
Новообразования БДС |
52 |
18,6 |
|
Билиарная или билиарная и панкреатическая гипертензия |
41 |
14,6 |
|
Острый панкреатит |
12 |
4,3 |
|
Опухоль головки ПЖ |
1 |
0,4 |
|
Отсутствие патологии ЖВП |
102 |
36,4 |
|
Всего |
280 |
100 |
Оценивая приведенные в таблице данные очевидно, что в 36,4% случаев (102 пациента) эндосонография позволила отвергнуть патологию желчных протоков у больных с клинико-лабораторными и/или ультразвуковыми признаками заболевания. Таким образом, применение ЭУС уменьшило количество выполнения инвазивных эндоскопических рентгеноконтрастных исследований, которые имеют риск развития осложнений [57,58]. Кроме того, данный метод позволил определить патологию большого
дуоденального сосочка, что сыграло важную роль в выборе оптимального эндоскопического вмешательства и его объема [71]. В нашем исследовании патологические образования БДС выявлены у 103 пациентов (см. табл.3.1): новообразования БДС – у 52 больных (18,6%); новообразования БДС в сочетании с холедохолитиазом – у 10 (3,6%); и подозрения на данную патологию при наличии расширения желчных и панкреатических протоков – у 41 больного (14,6%). Указанным 103 больным с патологическими образованиями Фатерова сосочка, а также при наличии билиарной и панкреатической гипертензии выполнена эндоскопическая папиллосфинктеротомия, при необходимости – вирсунготомия, ревизия желчных протоков с биопсией и гистологической верификацией выявленных при эндосонографии изменений БДС.
Из 62 больных с изолированным холедохолитиазом 18 были исключены из исследования по анатомическим критериям отбора: у 14 выявлены множественные конкременты желчного протока (более 3-х конкрементов), у 4 - выраженное расширение холедоха (более 12 мм). Остальным 44 пациентам в плане дальнейшего обследования предполагалось выполнение манометрического исследования СО, троим из них исследование не выполнено по технически причинам (схема 3.1).
Схема 3.1
Отбор больных с изолированным холедохолитиазом для выполнения ЭПД в соответствии с диагностическим алгоритмом (n = 290)
Результаты оценки функционального состояния СО у больных с холедохолитиазом
Эндоскопическая перфузионная папиллосфинктероманометрия (схема 3.1) за указанный период выполнена 51 больному с верифицированным холедохолитиазом: в 41 случае после выявления конкрементов желчных протоков при эндосонографии и 10 больным без предварительного выполнения ЭУС (по данным стандартного УЗИ) (табл. 3.2). Не удалось селективно катетеризировать желчные протоки в 6 случаях (11,8%). У двоих больных при дуоденоскопии выявлены полиповидные образования, исходящие из устья БДС в одном случае и пролабирующие из ампулы БДС во втором случае; образования были округлой формы, ярко-розового цвета, размерами до 4-5 мм. В двух случаях неудачной канюляции выявлены эндоскопические признаки рубцово-измененного большого дуоденального сосочка, интерпретированные как папиллостеноз: эндоскопически определено уменьшение размеров и уплощение сосочка, бледно-розовый цвет его слизистой, при этом устье отчетливо не дифференцировалось, продольная складка сглажена, пальпаторно ткани сосочка уплотнены.
Таблица 3.2
Результаты эндоскопической папиллосфинктероманометрии
|
Заключение ЭПСМ |
Число больных |
Эндоскопическая операция |
|
Папиллостеноз |
11 |
ЭПСТ |
|
Папиллоспазм |
3 |
ЭПД |
|
Тахиоддия |
1 |
ЭПД + ЭПСТ |
|
Неудачная канюляция: |
|
|
|
- образование БДС |
2 |
ЭПСТ |
|
- папиллостеноз |
2 |
ЭПСТ |
|
- неизмененный БДС |
2 |
ЭПД |
|
Отсутствие патологических изменений моторики СО |
30 |
ЭПД 25 ЭПД + ЭПСТ 2 ЭПСТ 3 |
|
Всего |
51 |
|
Таким образом, эндоскопическая папиллодилатация с экстракцией конкрементов после анализа данных ЭПСМ была выполнена 33 больным:
- 25 больным с нормальными показателями моторики СО;
- троим больным с папиллоспазмом,
- двоим больным, у которых выполнить манометрическое исследование не удалось из-за безуспешной канюляции желчных протоков, однако эндоскопических признаков патологических изменений Фатерова сосочка не выявлено;
- одной больной, страдающей лимфосаркомой, тромбоцитопенией, от выполнения ЭПСМ перед папиллодилатацией решено отказаться из-за выраженных нарушений свертывающей системы крови, вследствие чего любое эндоскопическое исследование сопровождалось контактной кровоточивостью тканей и снижением числа тромбоцитов в общем анализе крови;
- двоим пациенткам, которым манометрическое исследование не проводилось по техническим причинам.
Эндоскопическая баллонная папиллодилатация дополнена папиллосфинктеротомией троим пациенткам со следующими результатами ЭПСМ:
- двоим пациенткам с нормальными значениями моторики СО;
- одной больной с диагнозом тахиоддии.
Эндоскопическая папиллосфинктеротомия с экстракцией конкрементов выполнена 18 больным после ЭПСМ:
- 13 больным с диагностированным по манометрическим данным папиллостенозом;
- двоим больным с образованиями БДС;
- троим больным с нормальными показателями моторики СО по следующим причинам:
1) экстренная ЭПСТ у одного больного из-за развития в стационаре клинической картины острой блокады терминального отдела холедоха; 2) вторая больная была
оперирована в срочном порядке в связи с рецидивом и нарастанием механической желтухи; 3) при выявлении признаков гнойного холангита при ЭРХГ.
Данные дооперационного обследования БДС полностью подтвердились во время эндоскопических вмешательств и по результатам гистологического исследования биоптатов, взятых после выполнения ЭПСТ из области измененных тканей.
3.2. Результаты обследования больных с изолированным холедохолитиазом.
На основании полученных данных обследования эндоскопическая баллонная папиллодилатация в качестве разрешения холедохолитиаза планировалась 37 больным. В одном случае от ее выполнения отказались в пользу ЭПСТ после этапа диагностической холангиографии, у троих больных ЭПД дополнена папиллосфинктеротомией. Более подробно эти четыре случая мы рассмотрим в следующем разделе.
Остальным 33 пациентам эндоскопическая баллонная папиллодилатация выполнена как самостоятельное вмешательство с целью разрешения холедохолитиаза. В данном разделе проанализированы результаты обследования этих пациентов перед эндоскопическим вмешательством на большом дуоденальном сосочке.
Показатели лабораторных методов исследования
После оценки клинической картины заболевания в 1-2 сутки от поступления выполнялись клинические лабораторные исследования крови и мочи, а также определение биохимических маркеров холестаза. При поступлении лейкоцитоз выявлен у 15 пациентов (14,8±4,1; 9,3-24,2 тыс./мкл); повышение уровня диастазы мочи определено у 5 пациентов (от 128 до 1024 Ед). При биохимическом анализе крови только у троих больных не выявлено патологических изменений. В остальных случаях определено повышение различных показателей: повышение билирубина отмечено у 28 больных, трансаминаз - у 25, щелочной фосфатазы - у 21 больного (табл. 3.3).
Таблица 3.3
Результаты биохимического анализа крови больных (n=33)
|
Показатели |
Единицы измерения |
Результаты |
Нормальные показатели |
|
Билирубин общий |
мкмоль/л |
69,3±64,3 (7-323) |
5,1-17,1 |
|
Билирубин связанный |
мкмоль/л |
53,2±49,8 (6,3-210) |
0-5,1 |
|
АЛТ |
U/l |
223,2±193,8 (13-907) |
м 11-41 ж 11-36 |
|
АСТ |
U/l |
206,5±226,2 (17-847) |
м 10-41 ж 10-37 |
|
ЩФ |
U/l |
440,3±375,9 (106-1919) |
80-290 |
Данные лабораторных методов исследования не позволили точно судить о наличии камней желчного протока, как причине механической желтухи. Тем не менее, указанные выше лабораторные показатели дали возможность предположить наличие протоковой патологии, что в свою очередь продиктовало необходимость проведения дополнительных специальных методов исследования.
Сообразно с этим, далее пациентам выполнялась строго аргументированная диагностическая программа, описанная во 2-й главе - стандартное ультразвуковое исследование, эндоскопическая ультрасонография, эндоскопическая папиллосфинктероманометрия (табл.3.4).
Таблица 3.4 Методы обследования больных с холедохолитиазом (n=33)
|
Метод исследования |
Количество больных |
% |
|
Клинические данные |
33 |
100 % |
|
Лабораторные исследования |
33 |
100 % |
|
УЗИ |
33 |
100 % |
|
ЭУС |
23 |
70 % |
|
ЭПСМ |
30 |
91 % |
Данные ультразвукового метода исследования
При выполнении стандартного ультразвукового исследования общий желчный проток визуализирован у 31 больного (31/33; 93,9%); при этом диаметр холедоха составил в среднем 8,2±1,5 мм. Диагноз холедохолитиаза - наличие негомогенности просвета желчного протока и/или конкрементов в нем - выявлено у 20 больных (20/33; 60,6%). Размер обнаруженных в 13 случаях конкрементов желчного протока по данным УЗИ в среднем составил 4,4±1,7 мм (3-8 мм). Помимо этого расширение желчных путей (диаметр желчного протока более 8 мм включительно) без признаков холедохолитиаза обнаружены в 3 случаях; отсутствие патологии желчевыводящих путей констатировано в 8 случаях (табл. 3.5).
Таблица 3.5
Результаты ультразвукового исследования больных (n=33)
|
УЗ-признаки |
Число больных |
|
Визуализация холедоха |
31 |
|
Расширение желчного протока (≥8мм): - признаки холедохолитиаза - ОЖП гомогенный |
20 17 3 |
|
Нерасширенный желчный проток (≤7мм): - признаки холедохолитиаза - отсутствие патологии ЖВП |
11 3 8 |
|
Признаки холедохолитиаза: - негомогенность холедоха - наличие конкрементов |
20 7 13 |
По данным литературы УЗИ позволяет выявить камни желчных протоков только в 15-50% случаев [12,16]. При этом отсутствие выраженного расширения желчных протоков значительно затрудняет диагностику холедохолитиаза при УЗИ. В наше исследование включены именно такие больные и, тем не менее, по результатам УЗИ диагноз холедохолитиаза был поставлен в 60,6% случаев (20/33).
Все вышесказанное позволяет сделать вывод, что УЗИ является важным скрининговым методом диагностики холедохолитиаза. Впрочем, данный метод не
позволяет точно определить диаметр ОЖП, размеры конкрементов, а также высказаться о морфологическом и функциональном состоянии БДС. В данной ситуации необходимо выполнение специальных методов диагностики.
Данные эндоскопической ультрасонографии
При эндоскопической ультрасонографии желчный проток визуализирован у всех 23 больных (10 больным ЭУС не выполнена по техническим причинам). Средний диаметр общего желчного протока составил 8,9±2,0 мм (5-12 мм). При этом расширение диаметра ОЖП выявлено у 17 больных (от 8 до 12 мм), у остальных 6 больных диаметр холедоха находился в пределах нормальных значений (от 5 до 7 мм). Средний размер конкрементов
- 6,2±2,7 мм (1-10 мм).
При сравнении диаметра ОЖП, количества и размеров конкрементов в нем по данным ЭУС и ЭРХГ статистически достоверной разницы не выявлено (табл.3.6). Отсюда следует, что при определении этих показателей результаты ЭУС идентичны контрастному исследованию желчных протоков - ЭРХГ. Это позволяет ориентироваться на результаты ЭУС при отборе пациентов в соответствии с разработанными критериями для выполнения той или иной эндоскопической операции.
Таблица 3.6
Сравнение результатов ЭУС и ЭРХГ (n = 23)
|
Показатели * |
ЭУС |
ЭРХГ |
Р ** |
|
Средний диаметр холедоха, мм мин.-макс. |
8,9±2,0 5-12 |
9,8±2,2 6-12 |
0,144 |
|
Среднее количество конкрементов мин.-макс. |
1,7±0,9 1-4 |
1,5±1,02 1-4 |
0,504 |
|
Средний размер конкрементов, мм мин.-макс. |
6,2±2,7 1-10 |
6,1±1,7 4-9 |
0,876 |
Примечание: * Показатели представлены как среднее ± стандартное квадратичное отклонение (минимальное значение – максимальное значение) ** анализ данных проводился при помощи критерия Стьюдента; вероятность возможной ошибки Р > 0,05, следовательно, различия статистически недостоверны.
На основании полученных данных можно заключить, что ЭУС является важным методом диагностики холедохолитиаза, позволяющим точно определить степень расширения желчных протоков, наличие в нем конкрементов, определить их количество и размеры. Причем эти показатели сравнимы с результатами, полученными при ЭРХГ. Кроме того, ЭУС позволяет оценить эхографические характеристики зоны Одди, ЖП, паренхимы поджелудочной железы и ее протоков, что в свою очередь существенно влияет на выбор метода эндоскопического лечения.
Функциональное состояние СО оценивали по результатам ЭПСМ. Данные эндоскопической перфузионной папиллосфинктероманометрии
ЭПСМ выполнена 30 пациентам, из них полноценная манометрическая «кривая» записи функционального состояния сфинктера Одди получена у 28 (табл.3.7), в остальных
2 случаях (2/28; 7,1%) не удалось выполнить селективную катетеризацию желчного протока. Протяженность СО по манометрическим данным составила в среднем 15,6±3,2 мм (10-20 мм), что соответствует литературным данным [208].
Таблица 3.7
Показатели манометрического исследования СО у больных с изолированным холедохолитиазом (n=28)
|
Показатели моторики СО (показатели давления в mm Hg) |
Нижняя граница нормы |
Верхняя граница нормы |
Результаты (среднее±стандартное отклонение) |
|
Давление в ДПК |
2 |
12 |
5,4±2,0 |
|
Давление холедоха |
5 |
18 |
13,0±5,1 |
|
Базальное давление СО |
12 |
35 |
21,8±6,4 |
|
Градиент ДПК-холедох |
3 |
9 |
7,9±5,3 |
|
Градиент холедох-СО |
6 |
12 |
8,5±4,2 |
|
Градиент СО-ДПК |
9 |
22 |
16,2±6,5 |
|
Амплитуда сокращений |
1 |
42 |
38,7±13,2 |
|
Частота сокращений в мин |
2 |
6 |
5,9±1,1 |
Осложнений после ЭПСМ (развитие острого панкреатита) не было отмечено ни в одном случае. По данным литературы острый панкреатит после манометрии СО развивается в среднем в 6 % случаев. P.Rolny выявил, что осложнения после манометрии только желчных путей развились у 1% пациентов, в то время как после манометрии панкреатических путей острый панкреатит развился в 11% случаев [182].
Селективно канюлировать холедох в нашей работе удалось у 28 больных, что на наш взгляд повлияло на отсутствие осложнений после исследования. В 2 случаях неудачной канюляции желчного протока попытки катетеризации не превышали 10 минут. Кроме того, в обязательном порядке всем больным после ЭПСМ проводилась комплексная профилактическая терапия, направленная на снижение риска развития острого панкреатита.
Выполнение ЭПСМ перед папиллодилатацией позволило исключить больных со стенозом БДС, дало возможность выявить влияние ЭПД на неизмененный сфинктерный аппарат сосочка, сравнивая в последующем результаты контрольных манометрических исследований с первоначальными данными.
3.3. Результаты эндоскопической баллонной папиллодилатации при холедохолитиазе.
Как окончательный метод лечения холедохолитиаза ЭПД с целью ревизии желчных путей и экстракции конкрементов произведена 33 больным. В остальных 4 случаях от выполнения ЭПД отказались в пользу ЭПСТ на различных этапах вмешательства – у одного больного на диагностическом этапе, у троих – в процессе выполнения ЭПД. Остановимся на этих случаях более подробно.
Случай 1. Больной Б., 75 лет, находился на лечении с диагнозом острый калькулезный холецистит, холедохолитиаз, острая неполная разрешающаяся механическая желтуха. При ЭУС выявлена дилатация желчных протоков до 12 мм и единичный конкремент в просвете ОЖП размерами до 10 мм. При ЭПСМ –
патологических изменений функции СО не выявлено. На этапе диагностической ЭРХГ отказались от выполнения папиллодилатации после выявления признаков холангита – поступление гнойной желчи и фибрина при катетеризации желчного протока и введении в него контрастного вещества. Для полноценной декомпрессии и санации желчных путей произведена папиллосфинктеротомия с экстракцией конкремента (рис.3.1).
Рис.3.1. Эндоскопическое вмешательство у больного Б. с холедохолитиазом, осложненном холангитом: а – поступление гнойной желчи при канюляции холедоха; б – холангиография – камень ОЖП; в – ЭПСТ; г – экстракция конкремента.
Следует отметить, что эндоскопическое вмешательство у больного было отсрочено по времени по техническим причинам и выполнено через 11 суток после верификации диагноза холедохолитиаза и обследования в соответствии с диагностической программой. При этом отчетливая клиническая картина холангита не прослеживалась – на 2-3 сутки после поступления, на фоне проведения консервативной терапии отмечено купирование болевого синдрома, разрешение механической желтухи, нормализация температуры тела. Такое несоответствие клинической картины и эндоскопических «находок» (фибринозно-гнойного холангита) не позволило полностью исключить наличие эмпиемы желчного пузыря у больного с острым калькулезным холециститом.
Все вышесказанное подчеркивает возможность развития различных осложнений ЖКБ при наличии холедохолитиаза, а также необходимость выбора оптимального срока эндоскопической санации желчных путей.
Случай 2. Больная Ц., 16 лет, с диагнозом ПХЭС, холедохолитиаз, острая неполная механическая желтуха, за 5 месяцев до настоящего поступления перенесла лапароскопическую холецистэктомию. При обследовании в клинике: данные ЭУС – расширение диаметра ОЖП до 12 мм, единичный конкремент в нем до 6 мм; при ЭПСМ
патологических изменений моторики СО нет. При эндоскопической операции: изначальная селективная катетеризация ОЖП без сложностей, дилатация выполнена баллоном диаметром 4 мм, однако при ревизии желчных путей отмечались трудности в проведении корзинчатых захватов и не удавалось захватить конкремент (размером 5 мм по данным холангиографии) при помощи различных видов корзинок Дормиа. В связи с чем выполнена частичная папиллотомия длиной до 6 мм и извлечение фрагментов трипсированного при манипуляциях конкремента.
Эта операция выполнялась одной из первых в нашей клинике. Недостаточный опыт проведения подобных вмешательств, а также расцененный высокий риск развития острого панкреатита после длительных манипуляций на большом дуоденальном сосочке послужили причиной изменения хода вмешательства у данной пациентки.
Случай 3. Больная К., 50 лет, с диагнозом острый калькулезный холецистит, холедохолитиаз, неполная механическая желтуха. В процессе предоперационного обследования были высказаны предположения о наличии папиллостеноза на основании результатов манометрического исследования функционального состояния сфинктера Одди. ЭПСМ - на 5 и 15 мм от устья БДС отмечалось повышенное базальное давление СО от 41 до 45 мм рт.ст. в среднем, диагностирована тахиоддия (рис.3.2). При ЭУС определено расширение ОЖП до 10 мм, в просвете его несколько гиперэхогенных включений до 3-4 мм, патологических изменений области БДС выявлено не было.
Рис.3.2. Манометрическая картина функции СО больной К.
Вмешательство решено было начать с ЭПД и при неэффективности его перейти на выполнение папиллосфинктеротомии. При селективной канюляции отмечались сложности в проведении катетера со струной (ощущение препятствия в области
ампулы БДС). Дилатацию сфинктера Одди выполнили с помощью баллона диаметром
10 мм (QBD 10х3) под давлением 4 атм. Во время дилатации "папиллярная талия" расправлялась не более 3 мм, в течение 2 минут добиться полного ее расправления не удалось (рис.3.3а).
Рис.3.3. Эндоскопическое вмешательство больной К. с недиагностированным до операции папиллостенозом:
а) ЭРХГ, ЭПД - неполное расправление папиллярной «талии» баллона (указано стрелкой) б) эндо-фото – ревизия желчных протоков при помощи корзинки Дормиа, визуализировано устье холедоха после ЭПСТ, в левом крае разреза имеется новообразование БДС (указано стрелкой)
в) микрофотография – железисто-фиброзный полип с диффузным воспалением (окраска Ван Гизон; х 10).
От дальнейших попыток папиллодилатации (увеличение давления в баллоне, выполнение повторных сеансов дилатации) отказались в пользу папиллосфинктеротомии. После рассечения БДС были извлечены два конкремента по 5 мм и большое количество замазкообразных масс. Ткани БДС были стенотически изменены - белесоватого цвета, пальпаторно уплотненны, растягивались на папиллотоме не более 3 мм (рис.3.3б). Выполнена биопсия рубцово-измененных тканей и при гистологическом исследовании было определено наличие железистого полипа с хроническим воспалением и участками фиброзной ткани (рис.3.3в).
Причиной неудачного выполнения дилатации и перехода на ЭПСТ у данной больной считаем не диагностированный до операции папиллостеноз - отсутствие указаний на наличие новообразования БДС при ЭУС, неправильная интерпретация данных манометрического исследования СО, которые следовало расценить как локальный стеноз интрамурального отдела холедоха.
Случай 4. Больная Р., 43 лет, находилась на обследовании и лечении по поводу постхолецистэктомического синдрома, острого билиарного панкреатита легкой степени тяжести, купировавшегося на фоне проведения консервативной терапии, холедохолитиаза и механической желтухой. При ЭУС выявлена эхографическая картина острого отечного панкреатита, расширение холедоха до 9 мм, единичный конкремент в нем размерами до 8 мм, область ампулы БДС пониженной эхогенности. При ЭПСМ – показатели функционального состояния СО соответствовали нормальным значениям. При ретроградной холангиографии ОЖП расширен до 12-14 мм, в его просвете обнаружены три конкремента размерами 10, 12 и 12 мм. При этом отмечались сложности в селективной канюляции желчного протока. Папиллодилатация выполнена баллоном диаметром 8 мм (QBD 8х3) под давлением 4 атм. На этапе ревизии возникли значительные трудности в проведении различных видов корзинки Дормиа в желчные протоки, манипуляции сопровождались выраженным отеком и травматизацией тканей БДС. При этом удалось захватить только один дистально расположенный конкремент размерами до 10 мм, произошла внутрипротоковая литотрипсия его, после чего были извлечены несколько фрагментов конкремента. Учитывая вышеизложенные технические сложности вмешательства, наличие у больной острого панкреатита при поступлении, а также размеры двух вышележащих конкрементов в ОЖП размерами по 12 мм, решено выполнить папиллосфинктеротомию. После ЭПСТ все конкременты извлечены. После рассечения визуализированы стенотически измененные ткани БДС - значительно отечны, утолщены и уплотнены, белесоватого цвета.
Причиной изменения тактики в пользу ЭПСТ в данном случае считаем недиагностированный до операции папиллостеноз, крупные размеры конкрементов и, как результат, технические трудности вмешательства и травматизация тканей БДС, а также наличие острого панкреатита при поступлении, что в сочетании с трудным эндоскопическим вмешательством на БДС повышает риск развития послеоперационного панкреатита.
Как показал анализ приведенных примеров, во всех случаях имели место тактические ошибки. В основном, это касалось отклонений от сформулированных критериев отбора больных перед выполнением ЭПД. Что позволяет сделать вывод о необходимости строгого соблюдения разработанной диагностической программы и
критического отношения к пограничным показателям исследований (показатели базального давления СО при ЭПСМ, размеры конкрементов и диаметр ОЖП при ЭУС, эндосонографическая картина области БДС).
Данные эндоскопической ретроградной холангиографии
ЭРХГ как этап баллонной дилатации сфинктера Одди выполняли непосредственно перед вмешательством на БДС с целью подтверждения данных предварительного обследования (табл. 3.8). У всех 33 больных удалось селективно катетеризировать желчный проток и выполнить его контрастирование.
Таблица 3.8 Показатели эндоскопической ретроградной холангиографии (n=33)
|
Параметры ЭРХГ |
Число больных |
|
§ Диаметр желчного протока: - ≥8 мм - ≤7 мм |
27 6 |
|
§ Признаки холедохолитиаза: - тени конкрементов - негомогенность желчного протока § Отсутствие конкрементов и негомогенности желчного протока |
· 28 - 19 - 9
· 5 |
По данным холангиографии дилатация внепеченочных желчных протоков выявлена у 27 пациентов, у остальных 6 диаметр желчного протока соответствовал нормальным значениям (табл. 3.9).
Таблица 3.9
Диаметр общего желчного протока по данным ЭРХГ (n=33)
|
Диаметр желчного протока, мм |
Число больных |
|
5 |
1 |
|
6 |
2 |
|
7 |
3 |
|
8 |
7 |
|
9 |
5 |
|
10 |
3 |
|
12 |
12 |
При этом отчетливые признаки наличия конкрементов в желчном протоке выявлены у 28 пациентов, в остальных 5 случаях просвет протоков был гомогенным на всем протяжении (табл. 3.10). Учитывая данные предоперационного обследования, всем пациентам с целью ревизии желчевыводящих протоков выполнена ЭПД.
Таблица 3.10
Количество конкрементов по данным ЭРХГ (n=33)
|
Количество конкрементов |
Число больных |
|
Отсутствие конкрементов |
5 |
|
Негомогенность просвета желчного протока |
9 |
|
1 конкремент |
15 |
|
2 конкремента |
1 |
|
3 конкремента |
1 |
|
4 конкремента |
2 |
Диаметр общего желчного протока по данным ЭРХГ в среднем составил - 9,5±2,2 мм (5-12 мм); количество конкрементов - 1,5±1,0 (1-4), средний диаметр конкрементов - 6,1±1,7 мм (4-9 мм).
ЭРХГ обладает высокой диагностической значимостью в выявлении холедохолитиаза, в том числе и в нерасширенных желчных протоках (чувствительность 96%, общая точность 91%) [11].
Непосредственные результаты выполнения ЭПД у больных с изолированным холедохолитиазом
При анализе непосредственных результатов ЭПД учитывались: 1) технические аспекты выполнения канюляции ОЖП на этапе диагностической ЭРХГ и самого вмешательства; 2) диаметр и длина используемых баллонов; 3) величина давления в баллонах; 4) длительность сеанса дилатации; 5) особенности ревизии желчных протоков и экстракции конкрементов; 6) течение послеоперационного периода (табл.3.11).
Таблица 3.11
Результаты эндоскопической баллонной папиллодилатации при изолированном холедохолитиазе
|
Диагноз |
Возра ст, гг. / пол |
Дуоденоскопия |
ЭРХГ |
Диаметр баллона мм |
Кол- во сеанс ов ЭПД |
После ЭПД |
ЭР ПГ / О П | ||||
|
ОЖП, мм |
Кол-во камней |
Размер камней мм |
Устье холед оха, мм |
Кол- во камне й |
Размер камней мм | ||||||
|
ОБП, ПХЭС, хл, сбг |
66/ж |
|
12 |
1 |
9 |
10 |
1 |
5 |
1* |
9 |
¨ |
|
ОКХ, хл, мж |
69/ж |
Дивертикул |
10 |
- |
- |
6 |
1 |
5 |
- |
- |
|
|
ХКХ, хл, мж |
45/ж |
|
8 |
- |
- |
6 |
1 |
4 |
- |
- |
|
|
ХКХ, хл, мж |
42/ж |
Труд.канюл. |
12 |
Негомогенность |
10 |
1 |
5 |
1 |
6 |
+ ОП | |
|
ХКХ, хл, сбг |
68/м |
Папиллит |
12 |
Негомогенность |
10 |
1 |
5 |
1* |
7 |
| |
|
ОКХ, хл, мж |
50/ж |
|
12 |
1 |
7 |
4;8 |
2 |
5 |
1 |
6 |
|
|
ОКХ, хл, мж |
58/м |
|
7 |
3 |
5 |
4;8 |
2 |
4 |
3 |
5 |
|
|
ХКХ, хл, сбг |
42/ж |
Папиллит |
8 |
Негомогенность |
4;8 |
2 |
5 |
3 |
3 |
| |
|
ХКХ, хл, мж |
61/м |
|
12 |
1 |
6 |
4;8 |
2 |
5 |
3* |
6,4,4 |
¨ |
|
ПХЭС, хл, сбг |
62/ж |
|
10 |
1 |
7 |
4;8 |
2 |
5 |
1 |
7 |
|
|
ПХЭС, хл, мж |
64/ж |
|
12 |
1 |
7 |
8 |
2 |
5 |
1 |
7 |
¨ |
|
ХКХ, хл, мж |
48/ж |
|
6 |
- |
- |
8 |
2 |
3.5 |
- |
- |
+ |
|
ХКХ, хл, сбг |
71/ж |
Труд.канюл. |
9 |
2 |
5;7 |
8 |
2 |
5 |
2 |
5;7 |
¨ |
|
ПХЭС, хл, мж |
70/ж |
|
12 |
1 |
8 |
8 |
1 |
5 |
1 |
8 |
|
|
ХКХ, хл, сбг |
44/ж |
|
12 |
1 |
8 |
8 |
1 |
5 |
1 |
8 |
|
|
ОКХ, хл, сбг |
64/ж |
|
8 |
1 |
4 |
10 |
1 |
5 |
2 |
2 |
¨ |
|
ХКХ, хл, мж |
45/ж |
Папиллит |
8 |
1 |
5 |
8 |
2 |
4 |
1 |
5 |
|
|
ХКХ, хл, сбг |
54/ж |
|
12 |
Негомогенность |
8 |
2 |
4 |
3 |
2 |
¨ | |
|
ХКХ, хл, мж |
63/ж |
Труд.ЭК |
10 |
Негомогенность |
8 |
2 |
5 |
3 |
2 |
| |
|
ОКХ, хл, мж |
49/ж |
|
8 |
1 |
5 |
6 |
2 |
5 |
2* |
5;3 |
|
|
ХКХ, микрохл |
51/м |
дивертикул |
7 |
Негомогенность |
10 |
1 |
5 |
- |
- |
| |
|
ХКХ, хл, мж |
59/м |
Папиллит |
9 |
- |
- |
6 |
1 |
4 |
- |
- |
|
|
ОКХ, хл, сбг |
48/м |
Труд.ЭК |
8 |
1 |
6 |
6 |
3 |
4 |
1* |
6 |
+ ¨ |
|
ХКХ, хл, мж |
74/м |
|
8 |
1 |
6 |
4 |
1 |
5 |
1 |
6 |
+ |
|
ХКХ, хл, сбг |
63/ж |
Труд.канюл. |
7 |
- |
- |
4 |
2 |
3 |
2 |
1.5 |
+ ОП |
|
ОБП, ОКХ, хл, сбг |
38/ж |
|
9 |
Негомогенность |
7 |
1 |
3.5 |
3 |
5,5,2 |
| |
|
ОКХ, хл |
51/м |
Папиллит |
6 |
1 |
4 |
4 |
2 |
4 |
1 |
4.5 |
|
|
ХКХ, хл, мж |
38/ж |
|
9 |
4 |
4;5 |
7 |
1 |
3.5 |
4 |
4,5,6 |
|
|
ОБП, ОКХ, хл, сбг |
39/ж |
|
9 |
Негомогенность |
7 |
1 |
3 |
1* |
5 |
¨ | |
|
ПХЭС, хл, мж |
55/м |
Папиллит |
12 |
4 |
5-9 |
7 |
2 |
5 |
4* |
5,7,8,9 |
¨ |
|
ПХЭС, хл, мж |
57/ж |
|
12 |
1 |
9 |
7 |
1 |
4 |
1* |
9 |
|
|
ХКХ, хл, мж |
32/ж |
Папиллит |
5 |
1 |
4 |
4 |
1 |
3 |
- |
- |
|
|
ПХЭС, ОП, хл, мж |
48/ж |
|
12 |
Негомогенность |
7 |
1 |
5 |
1* |
7 |
ОП | |
Примечания: Пациенты указаны последовательно по времени выполнения ЭПД.
* - трипсия конкрементов при их извлечении; ¨ - транзиторная диастазурия в послеоперационном периоде; (+) – во время вмешательства выполнена ЭРПГ; (-) - отсутствие конкрементов; хл – холедохолитиаз; мж - механическая желтуха; сбг - субклиническая форма билиарной гипертензии.
После успешного выполнения ЭПД полная санация желчных путей при холедохолитиазе достигнута у всех 33 больных. Вмешательство продолжалось в среднем 46,7±16,3 мин (20-90 мин) (рис.3.4). Осложнения в виде острого панкреатита в послеоперационном периоде развились у 3 больных (9,1%).
100
90
80
![]() 70
70
60
50
40
30
20
10
0
1 3 5 7 9 11 13 15 17 19 21 23 25 27 29 31 33
больные, n
Рис.3.4. Длительность эндоскопической баллонной папиллодилатации и экстракции конкрементов.
1) Селективная катетеризация желчного протока удалась у всех пациентов. Однако, несмотря на отсутствие папиллостеноза и применение папиллорелаксантов в составе премедикации (нитроглицерин) трудности селективной канюляции желчных протоков возникли у 3 больных (9,1%; 3/33), что неблагоприятно отразилось на течении послеоперационного периода. При этом у всех этих пациентов в процессе поиска устья холедоха происходила нежелательная канюляция главного панкреатического протока, а у двоих из них выполнена панкреатикография. В послеоперационном периоде у двоих пациентов отмечено развитие острого панкреатита, у одного - транзиторной диастазурии. У остальных 30 пациентов удалось свободно без технических трудностей селективно катетеризировать холедох и выполнить холангиографию (табл. 3.12).
Таблица 3.12
Технические особенности канюляции желчного протока и течение послеоперационного периода у больных с изолированным холедохолитиазом
|
Технические особенности |
Число больных |
Послеоперационный период | |
|
Повышение амилазы сыворотки |
Острый панкреатит | ||
|
Свободная канюляция холедоха: - нежелательная панкреатикография |
30 - 2 |
5 - |
1 - |
|
Трудности канюляции холедоха: - канюляция ГПП без контрастирования - нежелательная панкреатикография |
3 - 1 - 2 |
1 - |
- 2 |
|
Всего: |
33 |
6 (18,2%) |
3 (9,1%) |
Представленные данные подчеркивают значение свободной селективной канюляции желчного протока для последующего технически успешного выполнения папиллодилатации и для благополучного течения послеоперационного периода. Травматизация БДС при многократных попытках его канюляции приводит к развитию отека тканей и спазмированию сосочка, а также может временно нарушить отток панкреатического секрета, повышая, таким образом, риск развития послеоперационного панкреатита [130,159,220]. Большинство авторов считают метод дилатации СО более простым в техническом исполнении, чем папиллосфинктеротомия. И даже рекомендуют выполнение ЭПД молодым специалистам, не имеющим достаточного опыта применения ЭПСТ. Действительно, при выполнении дилатации нет необходимости определять характеристики используемого тока, направление и длину разреза для предотвращения кровотечения и ретродуоденальной перфорации, как при папиллосфинктеротомии. В то же время необходимо еще раз подчеркнуть, что врач-эндоскопист, выполняющий баллонную дилатацию должен обладать достаточно большим опытом выполнения диагностической ретроградной панкреатикохолангиографии и свободно выполнять катетеризацию желаемой протоковой системы (желчной или панкреатической), в том
числе с использованием струн-проводников [56,57,121,125,159,170,222]. Это предотвращает травматизацию тканей ампулы БДС, что облегчает выполнение непосредственно дилатации и снижает риск развития острого панкреатита в послеоперационном периоде.
Таким образом, при изначально трудной и длительной канюляции желчного протока, особенно сопровождающейся нежелательной катетеризацией и контрастированием панкреатических путей, предпочтительно на наш взгляд выполнение папиллосфинктеротомии [131].
2) Диаметр и длина используемых для дилатации баллонов. Баллоны диаметром 10 мм применялись на начальных этапах исследования. В первых сообщениях по ЭПД авторы проводили дилатацию баллонами диаметрами 10 и 15 мм. В последующем стали использовать баллоны меньших диаметров, что обосновывалось стремлением выполнять истинно сфинктеросохраняющую операцию. По опыту нашей клиники дилатация баллоном с максимальным диаметром 10 мм достаточно травматична для тканей сфинктера Одди. У всех пациентов (n=5) при расправлении 10 мм баллона отмечалась болевая реакция во время дилатации, диффузное кратковременное подтекание крови из устья БДС после извлечения баллона и развитие отека тканей сосочка и околососочковой области. Появление новых работ по применению баллонов меньшего диаметра и собственный первоначальный опыт побудил нас к использованию в последующем менее травматичных баллонов (табл.3.13).
Таблица 3.13 Технические особенности выполнения эндоскопической папиллодилатации
|
Диаметр баллона, мм |
Число больных |
Размеры камней, мм* |
Диаметр желчного протока, мм* |
|
10 мм |
5 |
7,3 ± 1,3 (6-9) |
11 ± 2 (8-12) |
|
8 мм |
13 |
5,5 ± 2,2 (2-8) |
10,3 ± 1,9 (7-12) |
|
7 мм |
6 |
6,8 ± 1,8 (5-9) |
10,5 ± 1,6 (9-12) |
|
6 мм |
5 |
5,5 ± 0,7 (5-6) |
8 (8) |
|
4 мм |
4 |
4 ± 1,3 (1,5-6) |
7 ± 1 (6-8) |
Примечание. * среднее ± стандартное отклонение (минимальное значение – максимальное значение).
Выбор диаметра баллона для ЭПД основывался и на размере конкрементов, обнаруженных при ЭРХГ. При небольших камнях холедоха и отсутствии расширения протока успешно использовали баллоны диаметрами 4 и 6 мм.
Оптимальная длина используемых баллонов на наш взгляд является 3 см, также удобны и 4 см баллоны. По опыту других авторов, баллоны меньшей длины часто смещаются или в желчный проток, или в просвет ДПК и удержать их в среднем положении на уровне сфинктера Одди достаточно сложно. В своей работе подобные баллоны мы не использовали. Применение баллонов большей длины чревато нагромождением самого вмешательства, что отражается на течении послеоперационного периода. Мы применили баллоны длиной 8 см у 6 пациентов. При этом во время дилатации в 5 случаях произошла трипсия конкрементов рыхлой консистенции между расправленным баллоном и стенкой нерасширенного холедоха, что потребовало тщательной санации желчных протоков после экстракции конкрементов и их фрагментов. После вмешательства в одном случае развился острый панкреатит, в двух отмечена транзиторная амилазурия. Возможной причиной неблагополучного течения послеоперационного периода явилась неадекватная экстракция мелких фрагментов трипсированных конкрементов и их последующая миграция.
Таким образом, как показал анализ литературных данных и результатов собственного опыта, баллоны диаметрами 4-8 мм длиной 3 и 4 см являются наиболее оптимальными для использования дилатации СО при холедохолитиазе у больных определенной в нашем исследовании группы.
3) Давление в баллонах при дилатации. Максимально возможное нагнетаемое давление, которое в состоянии выдержать баллон, указывается фирмой производителем и отличается в зависимости от диаметра баллона. В начале своих исследований авторы ориентировались именно на эти цифры.
Во время дилатации баллоном любых структур возникают и действуют две силы - циркулярные и радиально направленные [48]. Воздействие циркулярных сил зависит от диаметра баллона и величины давления в нем. На радиально направленные силы влияют длина и изгиб "талии" баллона (что зависит от соответствующих параметров дилатируемой структуры), причем данное воздействие уменьшается при исчезновении указанной "талии". Таким образом, сила дилатации, а, соответственно, и ее воздействие на окружающие ткани больше, чем длиннее и плотнее дилатируемая структура. Учитывая данные физические законы, действующие во время дилатации, фирмы производители баллонов указывают максимальное давление, которое можно создать в баллоне, не опасаясь нарушения его целостности (так называемое "взрывное" давление) даже при дилатации рубцово-измененных тканей. Напротив, для дилатации неизмененного и достаточно податливого сфинктера БДС требуется давление значительно меньшее "взрывного", указанного производителем [61].
Учитывая изложенные аспекты механизма дилатации, в своем исследовании при выполнении ЭПД использовали давление 2-4 атм - постепенно нагнетая давление в баллоне сначала до 2 атм, а затем, оценивая формирование «талии баллона», до 4 атм.
Этого было вполне достаточно для последующего исчезновения папиллярной талии баллона, что являлось критерием успешного выполнения папиллодилатации. Нерасправление "талии" баллона при давлении 4 атм считали косвенным признаком наличия рубцово-измененных тканей БДС.
Использование указанных цифр давления при ЭПД (2-4 атм) позволяет эффективно расширить устье холедоха и удалить конкременты при минимальной травме тканей БДС. Аналогичный подход позволили H.Maguchi, 2000г. снизить частоту развития острого панкреатита по сравнению с дилатацией под давлением 8 атм [160].
4) Длительность дилатации в среднем составила 27,2±5,6 с (15-45 с).
Данное время выдерживалось после исчезновения "талии" баллона, т.е. после его полного расправления. Среднее число сеансов дилатаций составило 1,52±0,57: один сеанс дилатации – у 17 больных (51,5%), два – у 15 (45,5%) и три сеанса – у 1 больного (3,03%). У пациентов, которым выполнили более 1 сеанса общая продолжительность дилатации не превышала 60 с.
Отдельные авторы рекомендуют 2 минутную длительность дилатации с применением повторных сеансов через 1-2 минутные интервалы [143,166]. Другие, по мере накопления опыта рекомендуют сохранять давление на сфинктер в течение 15-60 с и желательно без повторных сеансов [61,112,160,217]. В нашей работе использовалось минимальное время для дилатации (не более 30 с при однократной дилатации и не более 60 с в сумме при повторных сеансах) и предпочтение отдавалось однократной дилатации, что удалось выполнить у 51,5% больных. Необходимость выполнения повторной дилатации определяли по длительности растяжения и податливости тканей сфинктера. При неполном исчезновении "талии" баллона при первой дилатации, при чрезмерном сопротивлении тканей сфинктера растяжению (что особенно явно отмечено у троих больных с установленным по данным ЭПСМ диагнозом папиллоспазма), при трудностях проведения корзинки Дормиа после первичной дилатации (у двоих больных) выполняли повторную дилатацию. Эти нюансы техники, направленные на уменьшение травматизации тканей в области вмешательства, эмпирически определены как меры профилактики развития осложнений в послеоперационном периоде, в частности острого панкреатита.
5) Ревизия желчных протоков и экстракция конкрементов. После дилатации БДС устье холедоха раскрылось в среднем до 4,4 ± 0,7 мм (3-5 мм). С целью ревизии желчных протоков корзинка Дормиа свободно проведена через дилатированное устье холедоха у 31 больного (93,9%). В двух случаях (6,1%) отмечались сложности в проведении инструментов для ревизии по следующим причинам: 1) низкое впадение пузырного протока, в который смещался катетер, 2) конкремент в терминальном отделе холедоха.
У 25 пациентов после баллонной папиллодилатации и ревизии желчных путей извлечены от одного до трех конкрементов, еще у двоих извлекли по 4 конкремента. Всего извлечено 38 конкрементов: среднее количество конкрементов 1,8±1,0 (1-4), средний диаметр конкрементов составил 5,4±2,1 мм (1,5-9 мм) (табл. 3.14).
Таблица 3.14
Сравнение данных ЭУС с результатами ЭПД
|
Показатели |
ЭУС (n=23) |
ЭРХГ (n=33) |
ЭПД (n=33) |
Р* |
|
Средний диаметр холедоха, мм мин.-макс. |
8,9±2,0 5-12 |
9,5±2,2 5-12 |
0,518 | |
|
Среднее количество конкрементов мин.-макс. |
1,7±0,9 1-4 |
1,5±1,0 1-4 |
1,8±1,0 1-4 |
0,451 |
|
Средний размер конкрементов, мм мин.-макс. |
6,2±2,7 1-10 |
6,1±1,7 4-9 |
5,4±2,1 1,5-9 |
0,289 |
Примечание: * Анализ данных при помощи однофакторного дисперсионного анализа; при вероятности возможной ошибки Р > 0,05, различия статистически недостоверны.
Как видно из таблицы, результаты диагностики холедохолитиаза и билиарной гипертензии при ЭУС совпадают с интраоперационными данными. Это позволяет
ориентироваться на результаты ЭУС при отборе пациентов для выполнения эндоскопической операции на ТОХ в соответствии с указанными критериями.
В одном случае для литоэкстракции потребовалось применение корзинки Дормиа со струной, так как обычные способы удаления камней оказались неэффективны. Остановимся подробнее на этом примере.
У больного с ПХЭС при ЭРХГ выявлены следующие данные: расширение ОЖП до 10-12 мм, в средней трети холедоха камень размерами 9 мм, в области бифуркации два конкремента 5 и 7 мм, в левом печеночном протоке - 8 мм камень. ЭПД выполнена баллоном диаметром 7 мм, длиной 8 см. При ревизии желчных путей три конкремента удалены без технических сложностей. Селективно провести стандартную корзинку в левый печеночный проток не удавалось. В данной ситуации мы использовали корзинку со струной. Струна изначально была установлена в левом печеночном протоке без технических сложностей с помощью катетера. После извлечения катетера по струне в левый долевой проток проведена корзинка, конкремент успешно был захвачен и извлечен в просвет кишки.
Отдельные авторы рекомендуют изначальное использование только таких корзинок Дормиа со струной для облегчения вмешательства и меньшей травматизации тканей. После дилатации баллон извлекается без струны-проводника, последняя остается в просвете протока. Проведение корзинки по этой струне в устье холедоха и далее в необходимый проток значительно облегчается. Это позволяет избежать повторных канюляций холедоха инструментом для ревизии (корзинки Дормиа или ревизионного баллончикового катетера) и предотвращает развитие постманипуляционного отека тканей БДС [159].
В 9 случаях при извлечении конкрементов в ДПК произошла их фрагментация. В такой ситуации добивались полной санации желчного протока от мельчайших фрагментов конкремента, так как устье холедоха после ЭПД не раскрывается столь широко, как после папиллосфинктеротомии [80,144,214]. При этом проводили тщательное промывание желчных протоков 150 мл физиологического раствора с добавлением диоксидина до полного извлечения всех крошко- и замазкообразных масс [225].
Применение литотрипсии не потребовалось ни в одном случае. Отбор пациентов для выполнения дилатации в соответствии с установленными критериями, в частности касающихся размера и количества конкрементов, позволил избежать использования этой технически громоздкой и травматичной для сфинктера методики. К тому же, методика требует применения дополнительного дорогостоящего инструментария и должна выполняться высококвалифицированными специалистами. На наш взгляд использование литотрипсии может значительно удлинить продолжительность вмешательства, усилить травматизацию тканей БДС, что в конечном итоге увеличит риск развития осложнений после операции.
После выполнения ЭПД у 6 больных с сохраненным желчным пузырем при ревизии желчных протоков конкременты не были обнаружены. В этой группе больных троим диагноз холедохолитиаза был установлен на основании данных ЭУС (во всех трех случаях в просвете желчного протока на сонограммах выявлены 1-2 мм гиперэхогенные включения). Остальным троим на основании данных стандартного УЗИ: у одного пациента при УЗИ выявлена негомогенность просвета желчного протока, у второго включение до 3 мм, и в 3-ем случае обнаружен конкремент размером 4 мм.
Таким образом, размеры конкрементов не превышали 4 мм у всех 6 больных. Вмешательство выполняли в среднем на 8 ± 2,6 сутки (4-11 сутки) после установки диагноза холедохолитиаза, что наряду с небольшими размерами конкрементов холедоха повышает возможность их самостоятельной миграции [111,200].
При дуоденоскопии в этих 6 случаев признаки стихающего папиллита выявлены у 2 больных, что можно считать косвенным признаком самопроизвольной миграции камня, у 2-х больных обнаружены парапапиллярные дивертикулы с диаметрами шейки 7 и 15 мм. На этапе диагностической ретроградной холангиографии у 2 больных тень желчных протоков была неотчетливо негомогенна, у 4-х просвет протоков был гомогенным. Учитывая клиническую картину заболевания и данные предоперационного обследования, всем 6 больным была выполнена ЭПД с целью ревизии желчных путей и констатации факта отсутствия холедохолитиаза к моменту проведения операции. Учитывая возможность самостоятельной миграции конкрементов, с целью ревизии протоков ЭПД была выполнена баллонами небольшого диаметра - 4 и 6 мм. Послеоперационный период у всех 6 больных протекал без осложнений.
В литературе имеются сообщения о выполнении ЭПД с целью проведения в желчный проток биопсийных щипцов и получения материала для гистологического исследования, а также для проведения билиодуоденального протезирования
[38,127,135,214,218]. В настоящей работе этим 6 больным с невыявленным при ЭРХГ холедохолитиазом дилатация выполнена с целью проведения инструментов (корзинки Дормиа и/или ревизионного баллончикового катетера типа Фогарти) для ревизии желчных путей в неясной ситуации без разрушения сфинктерного аппарата БДС.
Таким образом, у пациентов с мелкими конкрементами холедоха, особенно при сохраненном желчном пузыре, эндоскопическое вмешательство на протоках и санирующую операцию холецистэктомию следует выполнять как можно раньше после верификации диагноза, так как вследствие спонтанной миграции конкрементов повышается и риск возникновения острого панкреатита.
6) Течение послеоперационного периода.
Несмотря на проведение комплексной профилактической терапии в послеоперационном периоде, острый панкреатит развился в 3 случаях. Других осложнений в соответствии с классификацией P.B.Cotton с соавт. отмечено не было (табл.3.15).
Таблица 3.15
Осложнения после эндоскопической баллонной папиллодилатации при изолированном холедохолитиазе
|
Осложнение |
Число больных, % |
|
Острый панкреатит: - легкой степени - средней степени |
3 (9,1%) 2 1 |
|
Кровотечение |
- |
|
Ретродуоденальная перфорация |
- |
|
Летальность |
- |
|
Общее число больных |
33 |
Острый панкреатит развился у троих пациенток женского пола в возрасте 42, 48 и 63 лет: легкой степени в двух случаях, средней степени выраженности – в одном. Особенности техники выполнения вмешательства имелись у всех троих.
1. Больная К., 42 лет, диагноз: ЖКБ, хронический калькулезный холецистит, острая неполная механическая желтуха. При обследовании: УЗИ – в ЖП 3 мм включения и замазкообразные массы, диаметр холедоха 10-11 мм, в просвете его конкременты до 3 мм; ЭУС – в ЖП камни до 3-4 мм, холедох расширен до 11 мм, в просвете его 7 мм конкремент; ЭПСМ – нормальное функциональное состояние СО; ЭРХПГ – аберрантная поджелудочная железа парапапиллярной области, дивертикул нисходящего отдела ДПК, ОЖП до 11-12 мм, конкремент до 6 мм, S-образная деформация средней и нижней трети холедоха. Во время вмешательства отмечались сложности селективной канюляции желчного протока, при этом неоднократно канюлирован ГПП, выполнена панкреатикография. ЭПД произведена 10 мм баллоном, под максимальным давлением 4 атм, в течение 20 с после полного расправления «талии» баллона, устье холедоха раскрылось до 5 мм, при ревизии извлечен конкремент светло-желтого цвета, плотной консистенции, размерами до 6 мм. В послеоперационном периоде развился острый панкреатит легкой степени, который удалось купировать на фоне 3-х дневной консервативной терапии.
Таким образом, в данном случае в развитии панкреатита можно предположить роль травматизации тканей БДС во время сложной канюляции и дилатации баллоном диаметром 10 мм, а также выполнение панкреатикографии.
2. Больная Г., 48 лет, диагноз: ПХЭС, холедохолитиаз, острая неполная механическая желтуха. При обследовании: УЗИ – диаметр ОЖП 9 мм; ЭУС – расширение желчного протока до 9-12 мм, конкремент в нем до 9,5 мм, хронические воспалительные изменения ПЖ средней степени; ЭРХГ – свободная селективная канюляция желчного протока, последний расширен до 10-12 мм, в средней трети описанный конкремент. Папиллодилатация выполнена баллоном диаметром 7 мм, длиной 8 см, в течение 30 с после его расправления, устье холедоха раскрылось до 5 мм. При этом во время расправления баллона под давлением произошла внутрипротоковая фрагментация конкремента (рис.3.5). При ревизии протоков корзинкой Дормиа извлечены крошко- и замазкообразные фрагменты конкремента светло-желтого цвета, размерами до 3-4 мм. В послеоперационном периоде развился острый панкреатит легкой степени, который удалось купировать консервативными мероприятиями в течение 2 суток.
Рис.3.5. Эндоскопическое вмешательство у больной Г.: а – внутрипротоковая фрагментация конкрементов во время папиллодилатации баллоном длиной 8 см, стрелкой указан конкремент между баллоном и стенкой протока; б – устье БДС после дилатации.
В данном случае на наш взгляд, возможными факторами развития панкреатита явились следующие: травматичность вмешательства при дилатации большим по длине баллоном, возможная миграция мелких фрагментов камня после вмешательства.
3. Больная А., 63 лет, диагноз: ЖКБ, хронический калькулезный холецистит, холедохолитиаз, субклиническая форма билиарной гипертензии. При обследовании: ЭУС – диаметр желчного протока 8 мм, в надпапиллярном отделе свободно расположенные гиперэхогенные включения до 1, 2 мм (микрохоледохолитиаз); ЭПСМ – папиллоспазм: повышение базального давления на 15 мм от устья БДС в среднем до 46 мм рт.ст., снижающееся до нормальных значений при фармакологической пробе с нитроглицерином;
ЭРХПГ – технически сложная селективная канюляция желчного протока, при этом неоднократно канюлирован панкреатический проток и выполнена панкреатикография, диаметр ГПП 2,5-1,5 мм, ширина желчного протока 5-7 мм (рис.3.6).
Рис.3.6. Эндоскопическое вмешательство у больной А.
а – канюляция желчного протока, проведение струны-проводника;
б - холангиограмма: конкремент в средней трети холедоха;
в – панкреатикограмма; г – папиллодилатация баллоном диаметром 4 мм.
ЭПД выполнена баллоном диаметром 4 мм, длиной 4 см, под давлением 4 атм, в течение 20 с, через 2 мин выполнен повторный сеанс дилатации в течение 15 с, при ревизии удалены крошкообразные массы, светло-коричневого цвета, размерами до 1-1,5 мм. В послеоперационном периоде развивается клиника острого панкреатита средней степени выраженности, на следующие сутки после вмешательства больная была переведена в отделение интенсивной терапии, после кратковременной подготовки выполнено экстренное повторное эндоскопическое вмешательство (рис.3.7). При ЭРХПГ выявлены признаки острого посттравматического папиллита, расширение желчного протока до 8-9 мм, а также расширение ГПП до 4-6 мм, замедление эвакуации контрастного вещества. Выполнена ЭПСТ, вирсунготомия, установка панкреатикодуоденального протеза длиной 5 см, диаметром 3 мм [102].
Рис.3.7. Повторное экстренной эндоскопическое вмешательство у больной А.: а – эндоскопическая картина острого папиллита; б – расширение панкреатического протока на панкреатикограмме; в – эндоскопическая папиллосфинктеротомия; г – панкреатикодуоденальное стентирование.
После повторной операции отмечен выраженный положительный эффект – стабилизация состояния больной и лабораторных показателей. Далее проводилось комплексное лечение. На 22-е сутки после первичного эндоскопического вмешательства больной выполнена лапароскопическая холецистэктомия.
В этом случае развитие панкреатита вероятнее всего связано с травматизацией тканей БДС во время технически трудной селективной канюляции, что повлекло за собой выполнение контрастирования панкреатического протока – дополнительного фактора риска развития панкреатита после ретроградных вмешательств. Не исключено, что сложности канюляции были обусловлены имеющимся у больной папиллоспазмом. Причем, дисфункция СО является самостоятельным фактором развития панкреатита вследствие частичной или полной обструкции панкреатического протока [75,76,90].
Приобретая опыт выполнения данного вмешательства, мы разделяем мнение авторов, которые считают баллоны диаметрами более 8 мм травматичными для тканей БДС, что может повышать риск развития острого панкреатита после операции. Выполнение канюляции главного панкреатического протока и панкреатикографии является признанным фактором риска возникновения послеоперационного панкреатита после ретроградных вмешательств [93,106,108,109,164]. В данной работе панкреатикография выполнена 5 пациентам, из них в 2 случаях развился острый панкреатит, в одном случае отмечена транзиторная диастазурия.
Частота развития острого панкреатита после баллонной папиллодилатации в среднем составляет 6,3 (3,3-11%) [62,101,143,163,166,156,172,177,220,224].
Опубликованные к настоящему моменту данные не продемонстрировали статистически значимого повышения частоты развития панкреатита по сравнению с ЭПСТ. На наш взгляд методика все-таки связана с бо́льшим воздействием на сфинктер главного панкреатического протока, чем папиллосфинктеротомия, при технически правильном
выполнении которой разрез и воздействие тока не распространяется на устье панкреатического протока. При папиллодилатации во время вмешательства циркулярно направленное воздействие во всех случаях затрагивает устье ГПП, тем самым обеспечивая больший риск травматизации тканей и возникновения отека в данной области.
Тем не менее, нет доказательств того, что предположительная травматизация тканей в области устья вирсунгова протока обязательно приведет к развитию острого панкреатита после операции. Нередко это проявляется повышением уровня панкреатических ферментов в сыворотке крови и/или моче, что не стоит рассматривать как последствие только папиллодилатации. N.Ueno и Y.Ozawa,1999г. выявили повышение уровня амилазы сыворотки крови у 89,6% больных после ЭПД, при этом острый панкреатит легкой степени развился только у 6 больных (5,5%) [220]. В рандомизированном исследовании J.Bergman с соавт., 2001г. транзиторная амилаземия после ЭПД отмечена у 23% больных, при этом панкреатит развился только в 8% случаях
[66]. В нашем исследовании транзиторная диастазурия возникла у 9 пациентов. Из них транзиторное повышение уровня амилазы и сыворотки крови отмечено в 6 случаях (6/33; 18,2%).
Кровотечение, требующее проведения эндоскопического гемостаза, не развилось ни в одном случае. В том числе и у троих больных с наличием нарушений в свертывающей системе крови: лимфосаркома с тромбоцитопенией; постоянный прием непрямых антикоагулянтов (фенилин) после комиссуротомии у больной с комбинированным митрально-аортальным пороком сердца и еще у одного больного после аорто-коронарного шунтирования.
У 5 больных после аспирации контрастного вещества из баллона и извлечения его из желчного протока отмечалось незначительное и кратковременное диффузное подтекание крови из устья БДС (рис.3.8). Это не потребовало проведения каких-либо дополнительных гемостатических мероприятий и не помешало дальнейшему проведению вмешательства. Кратковременное кровоистечение во всех 5 случаях остановилось самостоятельно до ревизии протоков или во время ее выполнения.
Рис.3.8. Кратковременное диффузное подтекание крови из области БДС, остановившееся самостоятельно в процессе литоэкстракции.
Ретродуоденальная перфорация также не возникла ни в одном случае. Следует подчеркнуть, что в данном исследовании вмешательство выполняли больным с незначительным расширением желчных протоков (до 12 мм включительно), а средняя длина ТОХ по данным ЭРХГ составила 11,1±1,4 мм (7-14 мм). Данные показатели являются факторами риска развития перфорации при выполнении разреза ТОХ во время
ЭПСТ. Использование папиллодилатации у данного контингента больных позволяет избежать подобного грозного осложнения.
В двух случаях в послеоперационном периоде мы наблюдали возникновение
кратковременной желтухи.
Случай 1. У больной Б., 66 лет, с диагнозом ПХЭС, холедохолитиаз и сопутствующими нарушениями свертывающей системы крови (лимфосаркома с тромбоцитопенией) во время эндоскопического вмешательства отмечалась повышенная контактная кровоточивость и отек тканей БДС. При этом конкремент имел крошащуюся консистенцию и при извлечении был фрагментирован. Желчные протоки были дополнительно санированы промыванием 200 мл физиологического раствора с диоксидином. На 2-е сутки после ЭПД отмечено появление желтухи. Терапия была усилена назначением папиллорелаксантов (нитросорбид 10 мг х 4 раза в сутки). На 2-е сутки желтуха полностью разрешилась. Контрольное исследование больной не проводили, учитывая особенности сопутствующей патологии.
Анализируя этот случай, можно предположить, что причиной кратковременной желтухи явилось сочетание факторов - склонность тканей к отеку и возможное самостоятельное прохождение мелких фрагментов трипсированного при извлечении конкремента [206]. Эта была первая папиллодилатация в нашей клинике. На примере данного опыта у всех последующих пациентов в послеоперационном периоде профилактически назначались папиллорелаксанты.
Случай 2. У больной Д., 49 лет, с ОКХ, холедохолитиазом, острой неполной механической желтухой при обследовании в желчном пузыре выявлены конкременты размерами до 3 мм, при ЭРХГ - расширение желчного протока до 8,5 мм, в средней трети его камень размерами 5 мм, папиллоспазм по данным ЭПСМ. Папиллодилатация выполнена баллоном диаметром 6 мм в два сеанса по 30 с, так как «папиллярная талия» баллона при первом сеансе расправилась не полностью. Устье холедоха раскрылось до 5 мм. В процессе ревизии протоков конкремент коричневого цвета, рыхлой консистенции был фрагментирован и извлечен по частям. В первые сутки после вмешательства состояние больной было удовлетворительным. А на 2 сутки после операции отмечено появление иктеричности склер. В срочном порядке выполнена повторная ретроградная холангиография. При дуоденоскопии признаков воспаления области вмешательства выявлено не было - слизистая БДС розовая, без признаков отека и воспаления, устье раскрывалось до 2 мм, с активным поступлением светло-желтой желчи, продольная складка без патологических изменений (рис.3.9). Желчный проток был свободно канюлирован. При холангиографии выявлено уменьшение диаметра холедоха до 6-7 мм по сравнению с 8,5 мм при первичном вмешательстве; имелись признаки аэрохолии; конкременты в холедохе не были обнаружены. Учитывая клиническую картину (развитие механической желтухи) выполнена ревизия желчных путей при помощи корзинки Дормиа и ревизионного баллончикового катетера (диаметр баллона в расправленном состоянии 12 мм) - инструменты свободно проходили через ранее дилатированное устье холедоха (при инструментальной ревизии устье раскрывалось до 4 мм), конкрементов получено не было. На следующие сутки отмечено полное разрешение клинических признаков желтухи.
Рис.3.9. Эндоскопическое вмешательство у больной Д.:
а – состояние БДС до папиллодилатации; б, в – устье БДС тотчас после дилатации; г – устье БДС через 2 суток после папиллодилатации.
Резюмируя сказанное, в данном случае причиной развития кратковременной желтухи, возможно, послужила миграция одного из мелких 3 мм конкрементов из желчного пузыря, или миграция фрагмента конкремента. Данный пример подтверждает мнение авторов, рекомендующих выполнение холецистэктомии в ранние сроки после эндоскопического вмешательства, особенно при наличии мелких конкрементов в просвете желчного пузыря [111].
Холецистэктомия как второй этап санации желчных путей выполнена 23 больным: 17 – лапароскопические, 5 – хирургические, 1- из минилапаротомного доступа. 3 больных отказались от предложенной операции. В среднем холецистэктомия выполнена на 5±4,7 сутки (1-22 сутки, медиана=4) после ЭПД (рис.3.10). При этом учитывалось состояние больных после эндоскопической операции, жалобы, данные осмотра, результаты лабораторных анализов.
Рис.3.10 Сроки выполнения холецистэктомии после ЭПД
По данным M.Sugiyama и Y.Atomi, 1999, 2001гг. максимальное сокращение ЖП при ультразвуковом исследовании увеличивалось через 7 дней после ЭПД и возвращалось к исходным значениям через 1 месяц [199,201]. В нашей работе удаление ЖП стремились выполнять в максимально короткие сроки после эндоскопической операции, учитывая возможную миграцию камней из желчного пузыря. У одной больной холецистэктомия выполнена на 22 сутки после папиллодилатации по причине развития и лечения послеоперационного острого панкреатита.
3.4. Результаты контрольного исследования функции сфинктера Одди после эндоскопической баллонной папиллодилатации.
В среднем через 12,3±1,9 месяцев (10-17 мес.) после ЭПД больные повторно обследованы. Хорошее самочувствие и удовлетворительное состояние отметил 31 больной. Жалобы на периодически возникающие приступы желчной колики предъявляли двое больных. У одной из этих больных до операции по данным ЭПСМ поставлен диагноз папиллоспазма. После выполнения контрольного исследования функции СО признаков его стенозирования не выявлено, после чего обеим больным дополнительно назначен курс приема селективного для СО спазмолитика – одестона - с положительным эффектом. У остальных больных в указанные сроки наблюдения после ЭПД приступов желчных колик, рецидивов механической желтухи, острого панкреатита, проявлений холангита не было.
Контрольная манометрия сфинктера Одди выполнена 17 пациентам. Оценивались те же параметры, что и до эндоскопической операции: эндоскопическая картина области БДС, давление двенадцатиперстной кишки и холедоха, базальное давление СО, частота и амплитуда сокращений сфинктера.
Эндоскопических изменений слизистой большого дуоденального сосочка после ЭПД по сравнению с первоначальным осмотром (во время операции) выявлено не было. Селективная канюляция желчного протока и непосредственно исследование выполнено у всех пациентов без технических сложностей. Осложнений после выполнения ЭПСМ в амбулаторных условиях не было.
Длина СО до и после папиллодилатации статистически не отличалась: 14,2±2,4 мм по сравнению с исходными 15,5±3,5 мм (парный критерий Стьюдента; Р=0,089). Результаты значений параметров моторики СО до и после ЭПД представлены в Табл.3.16. Базальное давление СО через год после ЭПД соответствовало нормальным значениям (22,4±7,0 мм рт.ст.) и статистически не отличалось от дооперационных данных (20,9±6,0
мм рт.ст.). Двигательная активность СО после ЭПД полностью сохранилась – показатели амплитуды и частоты сокращений сфинктера также соответствовали данным до ЭПД.
Таблица 3.16 Показатели моторики СО до и после эндоскопической папиллодилатации (n=17)
|
Показатели моторики (показатели давления в mm Hg) |
Нижняя граница нормы |
Верхняя граница нормы |
Результаты (среднее±стандартное отклонение) |
Р* | |
|
до ЭПД |
после ЭПД | ||||
|
Давление в ДПК |
2 |
12 |
5,1±1,8 |
6,9±3,7 |
0,202 |
|
Давление холедоха |
5 |
18 |
11,8±5,0 |
14,2±6,2 |
0,302 |
|
Базальное давление СО |
12 |
35 |
20,9±6,0 |
22,4±7,0 |
0,530 |
|
Градиент ДПК-холедох |
3 |
9 |
5,5±3,1 |
7,6±3,4 |
0,082 |
|
Градиент холедох-СО |
6 |
12 |
8,7±2,9 |
7,5±5,4 |
0,434 |
|
Градиент СО-ДПК |
9 |
22 |
13,8±4,3 |
15,0±6,6 |
0,560 |
|
Амплитуда сокращений |
1 |
42 |
36,6±11,7 |
45,6±13,9 |
0,159 |
|
Частота сокращений в мин |
2 |
6 |
5,7±1,3 |
5,9±0,9 |
0,599 |
Примечание: * Анализ данных при помощи парного критерия Стьюдента; при вероятности безошибочного прогноза > 0,05 различия статистически недостоверны.
Таким образом, при анализе манометрических записей функционального состояния СО до и после ЭПД статистически значимой разницы между показателями тонуса сфинктера и его двигательной активности (базального давления, амплитуды и частоты сокращений СО) выявлено не было. Резюмируя приведенные данные можно с уверенностью сказать, что через год после эндоскопической папиллодилатации функция СО полностью сохраняется. При этом как эндоскопических, так и манометрических признаков папиллостеноза в приведенном исследовании не выявлено.
Исследования в этой области будут продолжены в нашей клинике, и оценка отдаленных результатов с применением контрольной эндоскопической папиллосфинктероманометрии позволит уточнить место эндоскопической баллонной папиллодилатации в лечении холедохолитиаза.
ЗАКЛЮЧЕНИЕ
В настоящее время двухэтапная тактика лечения желчнокаменной болезни при холедохолитиазе является наиболее распространенной: санация желчных протоков при помощи эндоскопической папиллосфинктеротомии с экстракцией конкрементов и последующей операцией холецистэктомией.
С повышением диагностических возможностей лечебных учреждений и увеличением числа больных пожилого возраста, распространенность холедохолитиаза, как одного из проявлений желчнокаменной болезни и постхолецистэктомического синдрома неуклонно растет. При этом холедохолитиаз может приводить к развитию таких серьезных осложнений, как механическая желтуха, холангит, печеночная недостаточность, острый билиарный и хронический панкреатит, стеноз Фатерова сосочка. Таким образом, эндоскопическая санация желчных протоков нисколько не утрачивает своей значимости.
Среди вмешательств по поводу холедохолитиаза наиболее широкое признание приобрела эндоскопическая папиллосфинктеротомия, практически полностью вытеснив хирургические операции при данной патологии. В то же время число осложнений в ранние сроки после ЭПСТ и опасения, касающиеся последствий данного вмешательства в отдаленные сроки, привело к внедрению новых сфинктеросохраняющих методик лечения холедохолитиаза. Эндоскопическая баллонная дилатация сфинктера Одди с целью его сохранения была выполнена в начале 80-х годов и постепенно стала внедряться в клиническую практику только в 90-х годах. Связано это было с опасениями многих авторов в связи с возможным развитием острого панкреатита после дилатации. Теория сохранения функционального состояния сфинктерного аппарата БДС, а также отсутствие при правильном выполнении методики таких серьезных осложнений ЭПСТ, как кровотечение и ретродуоденальная перфорация противостояла предположительно высокому риску развития острого панкреатита после папиллодилатации. Данные опасения основывались на опыте применения дилатации сфинктера Одди при папиллостенозе, что объясняет высокий риск развития панкреатита. Так папиллостеноз является фактором риска развития многих осложнений после ретроградных вмешательств на БДС. При этом для расширения рубцово-измененных тканей необходимо создание большего давления в баллонах, что приводит к значительной травматизации тканей, в том числе и тканей в области устья главного панкреатического протока, отеку области БДС и последующего отрицательного воздействия на паренхиму поджелудочной железы. Все вышеперечисленное в меньшей степени относится к нормально функционирующему сосочку.
Целью настоящего исследования явилась оценка возможности эндоскопической баллонной папиллодилатации в лечении холедохолитиаза.
За 2 летний период в клинике выполнено 935 эндоскопических оперативных вмешательств на БДС при различных заболеваниях панкреатобилиарной области. Холедохолитиаз без сочетания с другой патологией желчных протоков и Фатерова сосочка был выявлен у 327 пациентов. Набор в проспективную группу больных с холедохолитиазом для выполнения ЭПД проводился на основании выработанных в ходе исследования критериев отбора, касающихся в основном анатомических особенностей, а также объективного статуса пациентов. Критерии отбора были сформулированы следующим образом: выполнение вмешательства в плановом или отсроченном порядке; возраст больных до 75 лет; отсутствие тяжелой сопутствующей патологии; диаметр холедоха до 12 мм включительно; количество конкрементов общего желчного протока не более 3-х; размеры конкрементов до 10 мм включительно; отсутствие стеноза СО; отсутствие крупных перипапиллярных дивертикулов, перенесенных операций на большом дуоденальном сосочке (как хирургических, так и эндоскопических), а также послеоперационных деформаций данной области (состояния после резекции желудка по Бильрот-2, или после билиодигестивных анастомозов).
На начальных этапах выполнения работы мы определили необходимый объем дополнительного обследования пациентов перед выполнением баллонной папиллодилатации. В данную диагностическую программу помимо определения стандартных клинико-лабораторных показателей и ультразвукового исследования органов брюшной полости входила эндоскопическая ультрасонография панкреатобилиарной зоны с целью уточнения состояния внепеченочных желчных протоков и терминального отдела холедоха, а также поджелудочной железы и желчного пузыря; и манометрическое исследование сфинктера Одди с целью оценки его функционального состояния, при выявлении папиллостеноза - определение его локализации и протяженности.
С учетов выработанных критериев отбора пациентов в данной работе были обследованы 290 пациентов с подозрением на наличие холедохолитиаза. Эндосонография выполнена 280 пациентам. Из обследованных больных только у 62 (22,1%) выявлен изолированный холедохолитиаз. В остальных случаях обнаружены новообразования большого дуоденального сосочка или терминального отдела холедоха (22,2%), иная патология панкреатобилиарной области (19,3%) или ее отсутствие (36,4%). Эти результаты указывают на необходимость выполнения эндосонографии перед папиллодилатацией, так как данное исследование позволяет уменьшить число применения больным с подозрением на протоковую патологию более инвазивной диагностической методики - эндоскопической ретроградной холангиографии. Кроме того, эндосонография позволяет выявить новообразования большого дуоденального сосочка. Мы считаем, что в случаях сочетания холедохолитиаза с новообразованиями БДС эндоскопическая папиллодилатация противопоказана. Всем этим больным выполнена эндоскопическая папиллосфинктеротомия, экстракция конкрементов и взятие морфологического материала из области образований (биопсии) для гистологического исследования.
Из 62 больных с диагностированным по данным ЭУС изолированным холедохолитиазом 18 были исключены из исследования по анатомическим критериям отбора. В плане дальнейшего обследования эндоскопическая манометрия сфинктера Одди выполнена 51 больному с верифицированным холедохолитиазом. При выявлении манометрических признаков папиллостеноза больные исключались из исследования. Им также выполнялась ЭПСТ с экстракцией конкрементов и биопсией рубцово-измененных тканей.
После проведенного обследования эндоскопическая баллонная папиллодилатация в качестве лечения холедохолитиаза планировалась 37 больным. В одном случае на этапе диагностической ЭРХГ отказались от выполнения папиллодилатации после выявления признаков холангита, и с целью полноценной декомпрессии желчных путей произведена папиллосфинктеротомия с экстракцией конкремента. Еще в 3 случаях для полной санации желчных путей в процессе дилатации потребовалось выполнение папиллотомии. При оценке данных этих 3-х вмешательств были высказаны следующие причины перехода на папиллосфинктеротомию: недиагностированный при манометрическом исследовании папиллостеноз, ошибочное измерение размеров конкрементов при эндосонографии, высокий риск развития острого панкреатита после длительных и технически сложных манипуляций на большом дуоденальном сосочке.
33 пациентам, составившим проспективную группу исследования, эндоскопическая баллонная папиллодилатация выполнена как самостоятельное вмешательство с целью удаления конкрементов желчного протока. Из 33 пациентов в исследовании было 9 мужчин (27,3%) и 24 женщины (72,7%). Средний возраст больных составил 54,2±11,1 года (32 – 74 года). Калькулезный холецистит диагностирован у 26 пациентов, из них острый холецистит выявлен у 8 и хронический у 18, холедохолитиаз послужил причиной постхолецистэктомического синдрома у 7 пациентов. У одной больной кроме этого диагностирован острый панкреатит, у двоих - хронический рецидивирующий панкреатит.
Механическая желтуха осложнила течение холедохолитиаза в 18 случаях (55%), в остальных 15 выявлена субклиническая форма билиарной гипертензии (45%).
Вмешательство выполняли на фоне стандартной премедикации с сублингвальным приемом папиллорелаксантов непосредственно перед его началом. После эндоскопической оценки состояния анатомических ориентиров зоны Одди селективно канюлировали желчный проток. Данному этапу уделяли особое внимание, так как быстрая и свободная селективная канюляция холедоха на наш взгляд является залогом успешного проведения папиллодилатации и мерой профилактики развития послеоперационного панкреатита.
После холангиографии по катетеру в холедох устанавливали струну-проводник. Затем катетер извлекали и вместо него по струне в желчные протоки проводили баллонный дилататор. Применяли баллоны диаметрами от 4 до 10 мм, длиной 3, 4 и 8 см. Баллон заполняли под давлением 50% контрастным веществом при помощи механического компрессора, добиваясь полного расправления "талии" баллона. После папиллодилатации контраст аспирировали и баллон извлекали из желчного протока. Раскрытое устье Фатерова сосочка и поступление желчи с пузырьками воздуха указывало на адекватность вмешательства. Далее выполняли ревизию желчных протоков и извлечение конкрементов при помощи корзинчатых захватов Дормиа и ревизионных баллончиковых катетеров типа Фогарти.
На начальных этапах освоения методики мы использовали описанную в литературе технику выполнения баллонной папиллодилатации 10 мм баллонами в 2 сеанса. Затем стали применять усовершенствованную технику - "щадящую для тканей сфинктера Фатерова сосочка" - использование баллонов диаметрами 8 мм и меньше. При небольших камнях холедоха и невыраженном расширении протока мы с успехом использовали баллоны диаметрами 4 и 6 мм. Давление в баллонах нагнетали дозировано, тем самым избегая "взрывной дилатации" - сначала до 2, затем при необходимости до 4 атм, при этом стремились к одномоментному и кратковременному растяжению тканей сфинктера. В расправленном состоянии баллон удерживали до 20-30 секунд после полного расправления "талии" баллона, что значительно меньше предлагаемых в литературе цифр. В среднем длительность дилатации составила 27,2±5,6 с (15-45 с), среднее число сеансов дилатаций 1,52±0,57. Общая продолжительность вмешательства в среднем составила 46,7±16,3 минут (20-90 мин). При холангиографии диаметр холедоха в среднем был равен 9,5±2,2 мм (5-12). У 27 пациентов после баллонной папиллодилатации и ревизии желчных путей извлечено в среднем 1,8±1,0 (1-4) конкрементов размерами в среднем 5,4±2,1 мм (1,5-9 мм). У 6 больных после выполнения ЭПД при ревизии желчных протоков конкременты не обнаружены. В этих 6 случаях ЭПД выполнена в качестве окончательного диагностического метода с целью ревизии желчных путей и констатации отсутствия холедохолитиаза к моменту проведения операции. В данной ситуации учитывали возможность самостоятельной миграции конкрементов, поэтому с целью ревизии протоков была выполнена сфинктеросохраняющая методика.
Отбор пациентов для выполнения дилатации в соответствии с выработанными критериями позволил добиться успешной санации желчных путей у всех пациентов, не применяя технически непростой и травматичной для сфинктера процедуры - литотрипсии. Таким образом, применение эндоскопической баллонной папиллодилатации при невыраженном расширении желчных протоков и небольших по размеру конкрементах позволяет ликвидировать холедохолитиаз, не разрушая при этом сфинктерный аппарат БДС. Как результат данная методика позволяет сохранить автономность билиарной системы и улучшить результаты лечения больных с холедохолитиазом в отдаленные сроки после вмешательства.
Выбор диаметра баллона основывался на данных ретроградного контрастирования желчных протоков: диаметра протока и размера и количества конкрементов. В своей работе мы использовали минимальный по диаметру баллон, который в то же время позволял удалить конкременты из протока, адекватно расширив устье большого дуоденального сосочка. Оптимально выполнение дилатации баллонами диаметрами 4-8 мм.
В своей работе мы выполняли дилатацию при давлении 2-4 атм. Данное давление вполне оправдано для дилатации неизмененных рубцово-воспалительными процессами тканей большого дуоденального сосочка. Необходимость создания большего давления в баллоне можно считать косвенным признаком папиллостеноза. Трудности при проведении корзинки Дормиа при дальнейшей ревизии желчных протоков также можно считать косвенным признаком стенотически измененных тканей или наличия новообразований ампулы БДС или терминального отдела холедоха, препятствующих свободному проведению инструмента в проток. Это касается ситуации, когда вмешательство выполняет специалист, владеющий техникой ЭРХПГ И ЭПСТ, т.е. при наличии достаточного опыта в выполнении селективной катетеризации желчной и панкреатической протоковых систем. При трудностях проведения ревизионных инструментов (корзинки Дормиа, баллончикового катетера) в желчные протоки неопытным специалистам можно рекомендовать использование корзинок Дормиа по струне, изначально установленной в протоке. Это позволяет избежать травматизации тканей БДС при длительных канюляциях холедоха, приводящих к значительному отеку тканей и еще большим трудностям проведения в проток ревизионных инструментов.
В послеоперационном периоде проводился комплекс профилактических мер, направленных на уменьшение влияния дилатации на состояние поджелудочной железы: инфузионная терапия с введением цитостатиков, ингибиторов протеаз, антисекреторные препараты, антибактериальная терапия, спазмолитики и обезболивание. При этом помимо стандартных консервативных мероприятий значительно улучшает течение послеоперационного периода применение папиллорелаксантов: известных по своим релаксирующим на сфинктер Одди действием нитропрепаратов и новых селективных для сфинктера Одди спазмолитиков, таких как дицетел, одестон, мебеварин и др.
Осложнения после эндоскопической баллонной папиллодилатации и степень их тяжести, что касается в основном развития панкреатита, мы оценивали по классификации, предложенной P.B.Cotton с соавт. в 1991 году для ретроградных вмешательств на Фатеровом сосочке. В нашей работе острый панкреатит развился у 3 пациентов (9,1%) (все трое женского пола; возраст 42, 48 и 53 года): 2 - легкой степени, 1 - средней степени выраженности. После проведенного лечения проявления панкреатита купированы во всех трех случаях: в двух случаях после 2-х дневной консервативной терапии, в одном случае после выполнения эндоскопической папиллосфинктеротомии, вирсунготомии, установки панкреатикодуоденального стента. Транзиторная диастазурия отмечена у 9 пациентов, у 6 из них также определялось транзиторное повышение уровня амилазы сыворотки крови без клинических проявлений панкреатита.
На основании первичного опыта выполнения папиллодилатации, анализа объективного статуса данных пациенток и особенностей операций были сформулированы следующие факторы риска развития острого панкреатита в послеоперационном периоде: наличие острого билиарного панкреатита при поступлении, трудности селективной канюляции желчного протока на этапе диагностической холангиографии или ревизии протоков; контрастирование главного панкреатического протока; дилатация баллонами диаметром более 8 мм, длиной более 4 см.
Кровотечения, ретродуоденальной перфорации не было ни в одном случае.
Второй этап санации желчных путей – холецистэктомию – выполняли в максимально короткие сроки после эндоскопической операции, учитывая объективное состояние больных, жалобы, данные осмотра, результаты лабораторных анализов. Холецистэктомия выполнена 23 больным, в среднем на 5±4,7 сутки (1-22 сутки, медиана=4) после дилатации. У одной больной холецистэктомия выполнена на 22 сутки по причине развития и лечения послеоперационного острого панкреатита. 3 больных от предложенной операции отказались.
Контролировать состояние пациентов желательно на протяжении года после вмешательства – в первые 2 месяца, оценивая эффективность вмешательства (оценивается наличие или появление жалоб, предшествующих операции, при необходимости проводится лабораторного контроля маркеров холестаза и ультразвукового исследования органов брюшной полости с оценкой желчевыводящих протоков); через год после вмешательства выполнение контрольного манометрического исследования сфинктера Одди с целью определения его состояния по сравнению с исходными данными и верификации отсутствия стенотических изменений большого дуоденального сосочка.
Проведенное в данной работе контрольное исследование функционального состояния сфинктера Одди при помощи эндоскопической перфузионной папиллосфинктероманометрии выявило не только полное сохранение активности сфинктера (сохранение сокращений и тонуса сфинктера), но и отсутствие стенотических изменений через год после эндоскопической баллонной папиллодилатации.
Таким образом, эндоскопическая баллонная папиллодилатация, выполненная по строгим показаниям, является эффективным и безопасным вмешательством при лечении холедохолитиаза.
Усовершенствованная в нашей клинике методика эндоскопической дилатации сфинктера Одди позволяет добиться сочетания желаемых результатов: успешной экстракции конкрементов общего желчного протока при минимальной травматизации тканей БДС и сохранение, таким образом, его функциональной активности в последующем.
Отбор пациентов в соответствии с выработанными критериями, тщательный анализ данных дооперационных методов исследования, "щадящая" методика выполнения вмешательства и комплекс профилактических мер с использованием папиллорелаксантов после дилатации позволяют предупредить развитие осложнений в послеоперационном периоде.
На основании проведенного исследования с манометрическим контролем можно заключить, что папиллодилатация не разрушает сфинктерный аппарат Фатерова сосочка, сохраняя автономность билиарной системы, и не приводит к его стенозированию в ближайшие сроки (через один год) после вмешательства.
Выводы
1. Стремление хирургов-эндоскопистов к разработке щадящей для сфинктера Одди эндоскопической операции, которая имеет свои патофизиологические обоснования, вполне оправдано. В настоящей работе представлен один из первых опытов эндоскопической баллонной папиллодилатации у 33 больных с изолированным холедохолитиазом, отобранных из 290 пациентов (11,4%; 33/290), где на первом этапе клинического обследования данный диагноз был предположительным. Диагностическая программа, использованная в работе, позволила верифицировать диагноз изолированного холедохолитиаза, что потребовало выполнения таких прецизионных методов исследования, как эндоскопическая ультрасонография (280 больных) и эндоскопическая папиллосфинктероманометрия (51 больной). Разработанный диагностический алгоритм позволил определить показания к ЭПД с учетом четко сформулированных критериев отбора, исключая при этом сопутствующую патологию Фатерова сосочка и околососочковой зоны и оценивая функциональное состояние сфинктера Одди.
2. Изолированный холедохолитиаз является показанием к выполнению эндоскопической баллонной папиллодилатации после освоения методики ее выполнения: 1) при расширении желчных протоков не более 12 мм; при размерах конкрементов до 10 мм включительно в количестве не более трех; 2) при коагулопатиях и циррозе печени; 3) при сложных анатомических условиях выполнения эндоскопической папиллосфинктеротомии (околососочковые дивертикулы, ранее перенесенная резекция желудка по Бильрот-2).
3. Эндоскопическая баллонная папиллодилатация, выполненная по сформулированным в работе показаниям, является эффективной и безопасной альтернативой эндоскопической папиллосфинктеротомии в лечении изолированного холедохолитиаза (эффективность 91,7%). Конверсия в сторону ЭПСТ потребовалась в 8,3% случаев, причиной которой было неполное соблюдение принятых критериев отбора к вмешательству. Выполнять эндоскопическую баллонную папиллодилатацию следует хирургу-эндоскописту, владеющему достаточным опытом ретроградных вмешательств на большом дуоденальном сосочке. Усовершенствованная в нашей клинике методика папиллодилатации дает возможность адекватно ревизовать и санировать желчевыводящие протоки при минимальной травматизации области вмешательства.
4. Из осложнений послеоперационного периода, связанных с операцией, острый панкреатит в нашем исследовании имел место в 9,1% случаев. Факторами риска развития острого панкреатита после эндоскопической папиллодилатации являются: трудная селективная канюляция желчных протоков, нежелательная канюляция главного панкреатического протока, выполнение панкреатикографии, проведение папиллодилатации баллонами диаметром 10 мм и более. В послеоперационном периоде особое внимание должно быть обращено на адекватные лечебные мероприятия по профилактике послеоперационного панкреатита.
5. Клинические результаты эндоскопической баллонной папиллодилатации следует признать вполне удовлетворительными. Контрольная эндоскопическая папиллосфинктероманометрия, выполненная повторно через год после нового, сфинктеросохраняющего вмешательства, выявила сохранение нормальной функции сфинктера Одди при благоприятном клиническом течении. Оценка результатов в более длительные сроки позволит уточнить место эндоскопической баллонной папиллодилатации в лечении изолированного холедохолитиаза.
ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ
1. Диагностическая программа обследования больных с холедохолитиазом состоит из двух этапов. Первый этап позволяет предположить у больного наличие холедохолитиаза и включает клинико-лабораторную характеристику заболевания и скрининговое ультразвуковое исследование. Второй этап верифицирует изолированный характер холедохолитиаза при помощи эндоскопической ультрасонографии и исследовании функционального состояния сфинктера Одди (эндоскопической папиллосфинктероманометрии).
2. Применение эндоскопической ультрасонографии позволяет верифицировать изолированный характер холедохолитиаза у 25% обследованных больных (72/290) и избежать выполнения инвазивной методики эндоскопической ретроградной панкреатикохолангиографии у 36,4 % обследованных, у которых патологии желчевыводящих протоков при ЭУС не выявлено. Данное исследование дает объективную оценку состояния желчных протоков, большого дуоденального сосочка, желчного пузыря и поджелудочной железы, что влияет на выбор оптимального метода эндоскопического лечения.
3. Выполнение эндоскопической папиллосфинктероманометрии при подтверждении по эндосонографическим данным холедохолитиаза позволяет объективно охарактеризовать функциональное состояние сфинктера Одди и диагностировать начальные стадии папиллостеноза, который, по нашему мнению, является противопоказанием для выполнения ЭПД.
4. Применение эндоскопической баллонной папиллодилатации может быть рекомендовано специалистам, владеющим в полном объеме техникой селективной катетеризации желчного и панкреатического протоков и эндоскопической папиллосфинктеротомии. Выполнение эндоскопической баллонной папиллодилатации необходимо с применением щадящих режимов вмешательства: использование баллонов диаметром не более 8 мм, постепенное увеличение давления в баллоне от 2 до 4 атм, в течение 15-20 секунд после исчезновения «папиллярной талии» баллона.
5. При технических сложностях во время вмешательстве, сопровождающимися трудностями селективной канюляции, выраженным отеком тканей БДС, вследствие его инструментальной травматизации, следует отказаться от выполнения папиллодилатации в пользу эндоскопической папиллосфинктеротомии.
6. Учитывая вероятность развития острого панкреатита после папиллодилатации, следует использовать комплекс интра- и послеоперационных лечебно- профилактических мероприятий по предотвращению и лечению осложнения. В дополнение к стандартной премедикации для облегчения канюляции желчных протоков необходимо использовать в качестве папиллорелаксанта нитроглицерин сублингвально. В послеоперационном периоде в обязательном порядке необходимо проведение комплексной профилактики развития острого панкреатита: инфузионная терапия в объеме не менее 1,5 л, включающая введение кристаллоидных препаратов, цитостатиков (5-фторурацил), ингибиторов протеаз (контрикал, гордокс, ингитрил); папиллорелаксанты (дицетел, одестон, нитросорбид); антибактериальная терапия; спазмолитические средства, холинолитики, антисекреторные препараты (блокаторы Н2-гистаминовых рецепторов). При прогрессировании острого панкреатита необходимо выполнять эндоскопическую папиллосфинктеротомию с декомпрессией главного панкреатического протока.
7. Клиническую оценку результатов эндоскопической папиллодилатации следует проводить в течение первого года после вмешательства на основании клинико- лабораторных данных и показателей контрольного манометрического исследования сфинктера Одди с целью определения его состояния по сравнению с исходными данными и верификации отсутствия стенотических изменений большого дуоденального сосочка. Оценку отдаленных результатов эндоскопической баллонной папиллодилатации следует проводить с обязательным исследованием функционального состояния сфинктера Одди.
Список литературы:
- 1979. - № 11. - С.45-47.
2. Благовидов Д.Ф., Данилов М.В., Вишневский В.А. Показания и техника папиллосфинктеротомии // Вест. хир. - 1976. - № 7. - С.17-21.
3. Васильев Р.Х., Халчевский В.М. Дилатация стриктур терминального отдела общего желчного протока // Хирургия. - 1987. - № 2 - С.110-113.
4. Власов В.В. Введение в доказательную медицину. – М.: Медиа Сфера, 2001. – 392 с.
5. Галлингер Ю.И., Будзинский А.А., Саврасов В.М. Лечение больных со стенозом Фатерова соска и холелитиазом методом эндоскопической папиллотомии // В кн.: 5 Всероссийский съезд хирургов. - Свердловск, 1978. - С.217-219.
6. Галлингер Ю.И. Оперативная гастродуоденоскопия: Дис… докт.мед.наук. – М., 1979. – 322 с.
7. Галлингер Ю.И., Хрусталева М.В. Эндоскопическая ретроградная механическая литотрипсия при холедохолитиазе. - Методическое пособие для врачей. - М., 2001. - 24с.
8. Гланц С. Медико-биологическая статистика: Пер. с англ. - М.: Практика, 1999. - 459 с.
9. Громова И.В. Эндоскопическая папиллосфинктеротомия при нестандартных ситуациях: Дис... канд.мед.наук. - М., 1999. - 133 с.
10. Даскалов М., Шанов Г., Минев Сл., Татарова Н. Гепатикоеюноанастомозы // Хирургия.
- 1988. - № 1 - С.45-48.
11. Кармазановский Г.Г. Оценка диагностической значимости метода («чувствительность», «специфичность», «общая точность») // Анналы хирургической гепатологии. – 1997. – Т.2. – С.139-142.
12. Клименко Г.А. Холедохолитиаз (диагностика и оперативное лечение). - М.: Медицина, 2000. – 224 с.
13. Котовский А.Е., Графская Н.Д., Данилов М.В., Буриев И.М. Эндоскопическая ретроградная панкреатикохолангиоскопия // Хирургия. - 1987. - № 2 - С.47-50.
14. Котовский А.Е., Поздеев И.В., Тупикин Л.В. Холангит в отдаленные сроки после ЭПСТ // В кн.: Осложнения эндоскопической хирургии. Сб. тезисов докладов под ред. Галлингера Ю.И. - М. - 1996. - С….
15. Котовский А.Е., Поздеев И.В., Тупикин Л.В. Отдаленные результаты эндоскопической папиллосфинктеротомии // Анналы хирургической гепатологии. - 1997. - № 2 - С.132- 135.
16. Котовский А.Е. Эндоскопическая баллонная дилатация при рубцовых сужениях билиопанкреатической области // Российский симпозиум "Внутрипросветная эндоскопическая хирургия" - М. - 1998. - С.50-51.
17. Лейшнер У. Практическое руководство по заболеваниям желчных путей: Пер. с нем. – М.: Гоэтар-Мед, 2001. – 264 с.
18. Лидский А.Т. Хирургические заболевания печени и желчевыводящей системы. - М.: Медгиз, 1963. - 408с.
19. Линденбратен Л.Д. Рентгенология печени и желчных путей. - М., Медицина, 1980. - 512 с.
20. Лукьянова Е.А. Медицинская статистика: Учеб пособие. – М.: Изд-во РУДН, 2002. – 255 с.
21. Луцевич Э.В., Уханов А.П., Семенов М.В. Эндоскопическая хирургия желчнокаменной болезни. - Москва; Великий Новгород: Типография "Новгород" - 1999. - 130с.
22. Насонова С.В., Цветкова Л.И. Опыт применения одестона в лечении хронических заболеваний желчного пузыря и желчевыводящих путей // Рос. журн. гастроэнтерол., гепатол., колопроктол. - 2000. - Т.10, № 3. - С.87-90.
23. Насонова С.В., Лебедева О.И. Одестон в лечении хронических заболеваний гепатобилиарной системы // Военно-медицинский журнал. - 2001. - № 2. - С.49-53
24. Нечай А.И., Нечай И.А., Фадеев В.Д. Среднестатистические показатели ширины общего желчного протока при отсутствии в нем камней у лиц разного пола, возраста, роста и массы тела // Рос. журн. гастроэнтерол., гепатол., колопроктол. - 1994. - Т.4, № 4. - С.95-98
25. Орлов С.Ю. Функциональное состояние сфинктера Одди по данным эндоскопической манометрии // Рос. журн. гастроэнтерол., гепатол., колопроктол. - 1994. - Т.4, № 4. - С.28-34.
26. Орлов С.Ю., Чернякевич С.А., Федоров Е.Д. Изменения функционального состояния сфинктера Одди после эндоскопической папиллосфинктеротомии // Рос. журн. гастроэнтерол., гепатол., колопроктол. - 1997. - Прил. №4, Т.7, №5. - С.443.
27. Орлов С.Ю. Значение эндоскопической папиллосфинктероманометрии в диагностике изолированного папиллостеноза и оптимизации техники эндоскопических вмешательств на большом дуоденальном сосочке: Дис… канд.мед.наук. - М., 2001. - 159 с.
28. Панцырев Ю.М., Галлингер Ю.И., Рябов В.И., Саврасов В.М., Будзинский А.А. Эндоскопическая папиллосфинктеротомия // Хирургия. - 1980. - № 1. - С.18-20.
29. Панцырев Ю.М., Галлингер Ю.И. Оперативная эндоскопия желудочно-кишечного тракта. – М.: Медицина, 1984. – 192с.
30. Панцырев Ю.М., Чернякевич С.А., Галлингер Ю.И., Будзинский А.А., Агейчева М.В. Значение эндоскопической холедоходуоденоманометрии в диагностике стеноза большого дуоденального сосочка // Хирургия. - 1987. - № 12 - С.98-102.
31. Панцырев Ю.М., Орлов С.Ю., Федоров Е.Д., Душкина В.А. Эндоскопическая ультрасонография в диагностике болезней поджелудочной железы. // Рос. журн. гастроэнтерол., гепатол., колопроктол. - 1999. - Т.8, №3. - С.6-14.
32. Петров Б.А., Гальперин Е.И. Хирургия внепеченочных желчных протоков - М. - 1971.
- 200с.
33. Полянский В.А., Коптельцев В.В., Лищенко А.Н. Дуоденобилиарный рефлюкс в оценке отдаленных результатов холедоходуоденоанастомоза // Хирургия. - 1986. - № 10 - С.11-15.
34. Примасюк О.П., Котовский А.Е., Гращенко С.А. Эндоскопическая ретроградная дилатация при заболеваниях большого сосочка двенадцатиперстной кишки и поджелудочной железы // 5-й Московский международный конгресс по эндоскопической хирургии. Сб. тезисов. - М. - 2001. - С.273-274.
35. Родионов В.В., Ревякин В.И., Фролов С.В., Вершков А.Ф., Волков А.А. Отдаленные результаты эндоскопической папиллосфинктеротомии у больных с неопухолевыми заболеваниями общего желчного протока // Вестник хирургии. - 1989. - № 7 - С.11-13.
36. Савельев В.С., Филимонов М.И., Балалыкин А.С., Ревякин В.И. Ретроградная холангиопанкреатография и эндоскопическая папиллотомия при желтухе механического характера // Вестник хирургии. - 1980. - № 10. - С.8-11.
37. Савельев В.С., Балалыкин А.С. Эндоскопическая папиллотомия в хирургической клинике // Хирургия. - 1987. - № 7 - С.35-40.
38. Таточенко К.В., Кашеваров С.Б., Кондрашин С.А., Казимиров В.Г., Королев В.М., Дадвани С.А. Дилатация пищевода, мочеточников и желчных путей баллонными катетерами – Хирургия. - 1987. - № 12 - С.111-113.
39. Уханов А.П. Лечение осложненных форм желчнокаменной болезни с применением эндохирургических методов и литотрипсии: Автореф. дис.докт.мед.наук. - М., 1998. - 40с.
40. Филимонов М.И., Амбарцумян Р.Г., Мусин И.И., Абрамович А.Б. Оценка функции печени у больных с супрадуоденальным холедоходуоденоанастомозом – Хирургия. - 1979 - № 2 - С.50-56.
41. Чадаев А.П. Факторы риска, прогнозирование осложнений и их профилактика при абдоминальных операциях у гериатрических больных: Дис… докт.мед.наук. – М., 1989. – 361 с.
42. Шаповальянц С.Г. Дискуссионные вопросы в диагностике и лечении билиарной патологии // Сб. статей научно-практической конференции к 95-летию В.С.Маята - С.68-73.
43. Шаповальянц С.Г. Профилактика и лечение осложнений эндоскопической папиллосфинктеротомии // В кн.: Осложнения эндоскопической хирургии. Сб. тезисов под ред. Галлингера Ю.И. - М. - 1996. - С.228-230.
44. Шаповальянц С.Г., Бурова В.А., Тронин Р.Ю., Арсангереева Г.А. Прогноз и профилактика осложнений эндоскопической папиллосфинктеротомии // Российский симпозиум "Внутрипросветная эндоскопическая хирургия" Тез.докладов. - М. - 1998. - С.94-96.
45. Эндоскопическая перфузионная папиллосфинктероманометрия (информационное письмо) / Под ред. Ю.М.Панцырева // Орлов С.Ю., Чернякевич С.А., Будзинский А.А.
- М. - 1994. - 16с.
46. Яковенко Э.П., Григорьев П.Я. Хронические заболевания внепеченочных желчевыводящих путей, диагностика и лечение. - М.: Медпрактика, 2000. - 31 с.
47. Abbound P-A.C., Malet P.F., Berlin J.A., Staroscik R. et al. Predictors of common bile duct stones prior to cholecystectomy: a meta-analysis // Gastrointest. Endosc. – 1996. – Vol.44,
№4. – P.450-457.
48. Abele J.E. The physics of esophageal dilation. // Hepatogastroenterology. - 1992. - Vol.39. - P.486-489.
49. Aizawa T., Ueno N., Ozawa Y. Temporary pancreatic duct stenting to prevent pancreatitis induced by endoscopic sphincter dilation // Dig. Endosc. - 1999. - Vol.11, №1. - P.32-36.
50. Allescher H.D., Neuhaus H., Hagenmuller F., Classen M. Effect of N-butylscopolamine on sphincter of Oddi motility in patients during routine ERCP - a manometric study // Endoscopy. - 1990. - Vol.22. -P.160-163.
51. Allescher H.D. How to sedate for endoscopic sphincter of Oddi manometry? // Endoscopy - 1993. - Vol.25. - P.399-400.
52. Allescher H.D. Clinical impact of sphincter of Oddi dyskinesia // Endoscopy. - 1998. - Vol.30, №9, Suppl.2 - A231-236.
53. Arnold J.C., Benz C., Martin W.R., Adamek H.E., Riemann J.F. Endoscopic papillary balloon dilation vs. sphincterotomy for removal of common bile duct stones: a prospective randomized pilot study // Endoscopy. - 2001. - Vol.33, № 7. - P.563-567.
54. Bader M., Geenen J.E., Hogan W., Dodds W.S., Venu R., Johnson G.K. Endoscopic balloon dilation of the sphincter of Oddi in patients with suspected biliary dyskinesia: results of a prospective randomized trial // Gastrointest. Endosc. - 1986. - Vol.32. - A158.
55. Bailie J. Complication of endoscopy // Endoscopy. - 1994. - Vol.26. - P.185-203.
56. Bailie J. ERCP training: for the few, not for all // Gut. - 1999. - Vol.45. - P.9-10.
57. Baillie J. Predicting and preventing post-ERCP pancreatitis // Current Gastroenterology Reports. - 2002. - Vol.4. - P.112-119.
58. Berdah S.V., Orsoni P., Bege T., Barthet M., Grimaud J.-C., Picaud R. Follow-up of selective endoscopic ultrasonography and/or endoscopic retrograde cholangiography prior to laparoscopic cholecystectomy: a prospective study of 300 patients // Endoscopy. - 2001. - Vol.33, № 3. - P.216-220.
59. Bergman J.J.G.H.M., Mey S., Rauws E.A.J., Tijssen J.G.P., Gouma D.J., Tytgat G.N.J., Huibregtse K. Long-term follow-up after endoscopic sphincterotomy for bile duct stones in
patients younger than 60 years of age // Gastrointest. Endosc. - 1996. - Vol.44, №6. - P.643- 649.
60. Bergman J.J.G.H.M., Anne-Marie van Berkel, Groen A.K., Schoeman M.N., Offerhaus J., Tytgat G.N.J., Huibregste K. Billiary manometry, bacterial characteristics, bile composition, and histologic changes fifteen to seventeen years after endoscopic sphincterotomy // Gastrointest. Endosc. - 1997. - Vol.45, № 5. - P.400-405.
61. Bergman J.J.G.H.M., Huibregtse K. Endoscopic balloon dilation of the sphincter for removal of bile duct stones: description of the endoscopic technique and a review of the literature // Acta Endoscopica. - 1997. - Vol.27, № 5. - P.405-415.
62. Bergman J.J.G.H.M., Rauws E.A.J., Fockens P., Van Berkel A.M., Bossuyt P.M.M., Tijssen
J.G.P. Randomized trial of endoscopic balloon dilation versus endoscopic sphincterotomy for removal of bile duct stones // Lancet. - 1997. - Vol.349. - P.1124-1129.
63. Bergman J.J.G.H.M., Huibregtse K. What is the current status of endoscopic balloon dilation for stone removal? // Endoscopy. - 1998. - Vol.30. - P.43-45.
64. Bergman J.J.G.H.M., Huibregtse K. Current status of endoscopic balloon dilation for stone removal // Endoscopy. - 1999. - Vol.31. - P.407-408.
65. Bergman J.J.G.H.M., Anne-Marie van Berkel, Bruno M.J., Fockens P., Rauws E.A.J., Tijssen J.G.P., Tytgat G.N.J., Huibregtse K. A randomized trial of endoscopic balloon dilation and endoscopic sphincterotomy for removal of bile duct stones in patients with a prior Billroth II gastrectomy // Gastrointest. Endosc. - 2001. - Vol.53, № 1. - P.19-26.
66. Bergman J.J.G.H.M., Anne-Marie van Berkel, Bruno M.J., Fockens P., Rauws E.A.J., Tijssen J.G.P., Tytgat G.N.J., Huibregtse K. Is endoscopic balloon dilation for removal of bile duct stones associated with an increased risk for pancreatitis or a higher rate of hyperamylasemia? // Endoscopy. - 2001. - Vol.33, №5. - P.416-420.
67. Binmoeller K.F., Soehendra N., Liguory C. The common bile duct stone: time to leave it to the laparoscopic surgeon? // Endoscopy. - 1994. - Vol.26. - P.315-319.
68. Boender J., Nix G.A.J.J., Ridder M.A.J., M. van Blankenstein, Schutte H.E., Dees J., Wilson
J.H.P. Endoscopic papillotomy for common bile duct stones: factors influencing the complication rate // Endoscopy. - 1994. - Vol.26. - P.209-216.
69. Bordas J.M., Elizalde I., Llach J., Mondelo F., Bataller R., Teres J. Biliary reflux due to sphincter of Oddi ablation: a new pathogenetic explanation for long-term major biliary symptoms after endoscopic sphincterotomy // Endoscopy. - 1996. - Vol.28. - P.642.
70. Bordas J.M., Toledo-Pimentel V., Llach J., Montserrat E., Mondelo F., Gines A., Teres J. Effects of bolus somatostatin in preventing pancreatitis after endoscopic pancreatography: results of a randomized study // Gastrointest. Endosc. - 1998. - Vol.47, № 3. - P.230-234.
71. Caletti G., Fusaroli P. Endoscopic ultrasonography // Endoscopy. - 2001. - Vol.33, № 2. - P.158-166.
72. Carr-Locke D. L. Sphincter of Oddi manometry: the control population // Gastroenterology. - 1985. - Vol.17. - P.341-343.
73. Carr-Locke D. L. Can endoscopic papillary balloon dilation really preserve sphincter of Oddi function. Commentary. // Gut. - 2001. - Vol.49. - P.608-609.
74. Cass O. Long-term complications of endoscopic biliary sphincterotomy for choledocholithiasis // Gastrointest. Endosc. - 1998. - Vol.48, № 5. - P.540-542.
75. Chen J.W.C., Saccone G.T.P., Toouli J. Sphincter of Oddi dysfunction and acute pancreatitis.
// Gut. - 1998. - Vol.43. - P.305-308.
76. Chen J.W.C., Thomas A., Woods C.M. et al. Sphincter of Oddi dysfunction produces acute pancreatitis in the opposum // Gut. - 2000. - Vol.47. - P.539-545.
77. Chen Y.K., Foliente R.L., Santoro M.J., Walter M.H., Collen M.J. "Endoscopic sphincterotomy-induced pancreatitis: increased risk associated with nondilated bile ducts and sphincter of Oddi dysfunction // Am. J. Gastroenterol. - 1994. - Vol.89, №3. - P.327-333.
78. Chen Y.K., Deguzman L., Godil A., Chang K.J., Erickson R.A., Walter M.H. Prospective randomized trial of endocopic balloon dilation versus sphincterotomy for extraction of bile duct stones // Gastrointest. Endosc. - 1998. - Vol.47. - AB111.
79. Cho Y.D., Hong S.J., Moon J.H., Kim J.O., Cho J.Y., Kim Y.S., Lee J.S. et al. Endoscopic papillary balloon dilation versus endoscopic sphincterotomy for removal of common bile duct stones // Gastrointest. Endosc. - 1998. - Vol.47. - AB111.
80. Cho Y.D., Hong S.J., Moon J.H., Kim J.O., Cho J.Y. et al. Clinical usefulness of intraductal ultrasonography on detection of small remnant stones after endoscopic papillary balloon dilation // Gastrointest. Endosc. - 1998. - Vol.47, № 4. - AB111 .
81. Choudari C.P., Fogel E., Gottlieb K., Sherman S., Lehman G.A. Therapeutic biliary endoscopy // Endoscopy. - 1998. - Vol.30. - P.163-173.
82. Choudari C.P., Fogel E., Kalayci C., Sherman S., Lehman G.A. Current status of endoscopic balloon dilation for stone removal // Endoscopy. - 1999. - Vol.31. - P.406.
83. Choudari C.P., Fogel E., Kalayci C., Sherman S., Lehman G.A., Jamidar P. Therapeutic biliary endoscopy // Endoscopy. - 1999. - Vol.31, № 1. - P.80-87.
84. Cicala M., Habib F.I., Fiocca F., Pallotta N., Corazziari E. Increased sphincter of Oddi basal pressure in patients affected by gall stone disease: a role for biliary stasis and colicky pain? // Gut. - 2001. - Vol.48. - P.414-417.
85. Classen M., Demling L. Streinextraktion aus dem gallengang endoskopisch moglich // Med.
Trib. - 1973. - Vol.27. - P.1-5.
86. Classen M., Demling L. Endoskopische sphinkterotomie der papilla Vateri und streinextraktion aus dem ductus choledochus // Dtsch. Med. Wochenschr. - 1974. - Vol.99. - P.496-497.
87. Classen M. Endoscopic papillotomy new indications, short and long term results // Clinical Gastroenterology. - 1986. - Vol.15. - P.457-469.
88. Classen M. Back to the future: the first papillotomy at Erlangen // Gastrointest. Endosc. - 2000. - Vol.51. - P.637.
89. Classen M., Tytgat G.N.J., Lightdale C.J. Gastroenterological Endoscopy. - Stuttgart; New York: Thieme, 2002. - 777 p.
90. Corazziari E., Shaffer E.A., Hogan W.J., Sherman S., Toouli J. Functional disorders of the biliary tract and pancreas. // Gut. - 1999. - Vol.45, Suppl.II. - P.1148-1154.
91. Costamagna G., Bianco M.A., Rorondano G. Cost-effectiveness of endoscopic sphincterotomy // Endoscopy. - 1998. - Vol.30, Suppl.2. - A212-A215.
92. Cotton P.B. Endoscopic management of bile duct stones (apples and oranges) // Gut. - 1984.
- Vol.25. - P.587-597.
93. Cotton P.B., Lehman G., Vennes J., Geenen J.E., Russeli R.C.G., Meyers W.C., Liguory C., Nickl N. Endoscopic sphincterotomy complications and their management: an attempt at consensus // Gastrointest. Endosc. - 1991. - Vol.37, № 3. - P.383-393.
94. Cotton P.B., Williams. ERCP and therapy // Practical gastrointestinal endoscopy. - Oxford etc.: Blackwell Science, 1996. - Chapter 8. - P.167-186.
95. Cotton P.B., Williams. ERCP-diagnostic technique // Practical gastrointestinal endoscopy. - Oxford etc.: Blackwell Science, 1996. - Chapter 6. - P.105-138.
96. Cotton P.B., Williams. ERCP-therapeutic technique // Practical gastrointestinal endoscopy. - Oxford etc.: Blackwell Science, 1996. - Chapter 7. - P.139-166.
97. Cotton P.B. Is your sphincterotomy really safe - and necessary? // Gastrointest. Endosc. - 1996. - Vol.44, №6. - P.752-755.
98. Craig A., Toouli J. Sphincter of Oddi dysfunction: is there a role for medical therapy? // Current Gastroenterology Reports. - 2002. - Vol.4. - P.172-176.
99. Dancygier H., Lightdale C.J. Endosonography in Gastroenterology. Principles, techniques, findings. – Stuttgart; New York: Thieme, 1999. – 232p.
100. Dickey W., Jacob S., Porter K.G. Balloon dilation of the papilla via a forward-viewing endoscope: an aid to therapeutic endoscopic retrograde cholangiopancreatography in patients with Billrot-II gastrectomy // Endoscopy. - 1996. - Vol.28. - P.531-532.
101. DiSario J.A., Freeman M.L., Bjorkman D.J., MacMathuna P., Petersen B., Sherman S., Lehman G., Hixson L., Jaffe P. and the EDES study group. Endoscopic balloon dilation compared to sphincterotomy (EDES) for extraction of bile duct stones: preliminary results // Gastrointest. Endosc. - 1997. - Vol.45, №4. - AB129.
102. Elton E., Howell D.A., Parsons W.G., Qaseem T., Hanson B.L. Endoscopic pancreatic sphincterotomy: indication, outcome, and a safe stentless technique // Gastrointest. Endosc. - 1998. - Vol.47, № 3. - P.240-249.
103. Escourrou J., Cordova J.A., Lazorthes F., Frexinos J. Early and late complications after endoscopic sphincterotomy for biliary lithiasis with and without the gall bladder "in situ" // Gut. - 1984. - Vol.25. - P.598-602.
104. Flowers J.L. ERCP versus laparoscopic surgery: the contest over common bile duct stones // Endoscopy. - 1996. - Vol.28. - P.438-440.
105. Fogel E.L., Sherman S., Devereaux B.M., Lehman G.A. Therapeutic biliary endoscopy // Endoscopy. - 2001. - Vol.33, № 1. - P.31-38.
106. Freeman M.L., Nelson D.B., Sherman S., Haber G.B., Herman M.E., Dorsher P.J., Moore J.P., Fennerty M.B., Ryan M.E., Shaw M., Lande J.D., Pheley A.M. Complications of endoscopic biliary sphincterotomy // N. Engl. J. Med. - 1996. - Vol.335, №13. - P.909-918.
107. Freeman M.L. Complications of endoscopic biliary sphincterotomy: a review // Endoscopy. - 1997. - Vol. 29. - P.288-297.
108. Freeman M.L. Complications of endoscopic sphincterotomy // Endoscopy. - 1998. - Vol.
30, №9, Suppl.2 - A216-220.
109. Friedland S., Soetikno R.M., Vandervoort J., Montes H., Tham T., Carr-Locke D.L. Bedside scoring system to predict the risk of developing pancreatitis following ERCP // Endoscopy. - 2002. - Vol.34, №6. - P.483-488.
110. Frimberger E. Long-term sequelae of endoscopic papillotomy // Endoscopy. - 1998. - Vol. 30, №9, Suppl.2. - A221-227.
111. Frossard J.L., Hadengue A., Amouyal G., Choury A., Marty O., Giostra E., Sivignon F., Sosa L. Amouyal P. Choledocholithiasis: a prospective study of spontaneous common bile duct stone migration // Gastrointest. Endosc. - 2000. - Vol.51, № 2. - P.175-179.
112. Fujita N. Endoscopic balloon dilation of the duodenal papilla: is it a safe and effective treatment for bile duct stones? // Dig. Endosc. - 2000. - Vol.12, Suppl. - S42-S44.
113. Fullarton G.M., Murray W.R. Evaluation of endoscopic sphincterotomy in sphincter of Oddi dysfunction // Endoscopy. - 1992. - Vol.24. - P.199-202.
114. Funch-Jensen P., Kruse A., Ravnsbaek J. Endoscopic sphincter of Oddi manometry in healthy volunteers // Scand. J. Gastroenterol. - 1984. - Vol.22, № 4. - P.245-249.
115. Geenen J.E., Toouli J., Hogan W.J., Dodds W.J., Stewart E.T., Mavrelis P., Riedel D., Venu R. Endoscopic sphincterotomy: follow-up evaluation of effects on the sphincter of Oddi // Gastroenterology. - 1984. - Vol.87. - P.754-758.
116. Geenen J.E., Hogan W.J., Dodds W.J. Sphincter of Oddi // In: Gastroenterologic endoscopy. Ed. Sivak M.V. - W.B.Sounders company, 1987. - Chapter 33. - P.735-751.
117. Gil S., de la Iglesia P., Verdu J.F., de Espana F., Arenas J., Irurzun J. Effectiveness and safety of balloon dilation of the papilla and the use of an occlusion balloon for clearance of bile duct calculi // Am. J. Roentgenol. - 2000. - Vol.174, № 5. - P.1455-1460.
118. Grace P.A., Poston G.J., Williamson R.N.C. Biliary motility // Gut. – 1990. – Vol.31. – P.571-582.
119. Guelrud M. Papillary stenosis // Endoscopy - 1988. - Vol.20. - P.193-202.
120. Guelrud M., Mendoza S., Viera L., Gelrud D. Somatostatin prevents acute pancreatitis after pancreatic duct sphincter hydrostatic balloon dilation in patients with idiopathic recurrent pancreatitis // Gastrointest. Endosc. - 1991. - Vol.37, № 1. - P.44-47.
121. Haber G.B., Sandha G.S. Endoscopic retrograde cholangiopancreatography // In: Classen M., Tytgat G.N.J., Lightdale C.J. Gastroenterological Endoscopy. - Stuttgart; New York: Thieme, 2002. - Chapter 13. - P.152-161.
122. Hagenmuller F., Classen M. Motility of Oddi's sphincter in parkison's disease, progressive systemic sclerosis and achalasia // Endoscopy. - 1988. - Vol.20. - P.189-192.
123. Hall R.I., Ingolby C.J.H., Denyer M.E. Periampullary diverticula predispose to primary rather than secondary stones in the common bile duct // Endoscopy. - 1990. - Vol.22. - P.127- 128.
124. Hawes R.H., Cotton P.B., Vallon A.G. Follow-up 6 to 11 years after duodenoscopic sphincterotomy for stones in patients with prior cholecystectomy // Gastroenterology. - 1990.
- Vol.98. - P.1008-1012.
125. Hawes R.H. Endoscopic ultrasound // Gastrointest. Endosc. - 2000. - Vol.10, № 1. - P.161-174.
126. Hellier M.D., Morris A.I. ERCP training - time for change // Gut. - 2000. - Vol.47. - P.459-460.
127. Hidaka T., Ueno N. Experience in diagnosing biliary tract stricture using endoscopic transpapillary bile duct biopsy assisted by endoscopic balloon sphincter dilation // Gastrointest. Endosc. - 1997. - Vol.46, № 6. - P.576-577.
128. Hogan W.J., Geenen J.E. Biliary dyskinesia // Endoscopy. - 1988. - Vol.20. - P.179-183.
129. Hogan W.J., Sherman S., Pasricha P., Carr-Locke D. Sphincter of Oddi manometry // Gastrointest. Endosc. - 1997. - Vol.45, № 3. - P.342-348.
130. Huibregtse K. Complications of endoscopic sphincterotomy and their prevention // N. Engl. J. Med. - 1996. - Vol.335, №13. - P.961-963.
131. Huibregtse K. Endoscopic balloon dilation for removal of bile duct stones: special indications only // Endoscopy. - 2001. - Vol.33, № 7. - P.620-622.
132. Ibuki Y., Kudo M., Toto A. Endoscopic retrograde extraction of common bile duct stones with drip infusion of isosorbide dinitrate // Gastrointest. Endosc. - 1992. - Vol.38. - 178-180.
133. Imrie C.W., Mckey C.J. The scientific basis of medical therapy of acute pancreatitis // Gastroenterol. Clin. North Am. - 1999. - Vol.28, № 3. - P.591-599.
134. Isayama H., Komatsu Y., Tateishi K., Yamagata M., Tada M., Yoshida H., et al.
Quantitative cholescintigraphic evaluation on the function of sphincter of Oddi after papillary balloon dilation (EPBD) // Gastrointest. Endosc. - 1998. - Vol.47, № 4. - AB117.
135. Jacob H., Fenster J., Zinberg J., Kadish S. Biliary balloon dilation using a triple-lumen catheter // Gastrointest. Endosc. - 1996. - Vol.44, № 4. - P.465-468.
136. Kawabe T., Komatsu Y., Tada M., Toda N., Ohashi M., Shiratori Y., Omata M. Endoscopic papillary balloon dilation in cirrhotic patients: removal of common bile duct stones without sphincterotomy // Endoscopy. - 1996. - Vol.28. - P.694-698.
137. Kawai K., Akasaka Y., Murakami K., Tada M., Kohli Y. Endoscopic sphincterotomy of the ampulla of Vater // Gastrointest. Endosc. - 1974. - Vol.20. - P.148-151.
138. Kawai K. Endoscopic ultrasonography in gastroenterology. - Tokyo, New York: Igaku- Shoin, 1988. - 235 p.
139. Kawai K. In the beginning // Gastrointest. Endosc. - 2000. - Vol.51. - P.637-638.
140. Kim M.H., Myung S.J., Lee S.K. Should we cut or dilate the sphincter? That may depend on whether it is primary or secondary common bile duct stones // Am. J. Gastroenterol. - 1998. - Vol.93, № 5. - P.846-847.
141. Kinami Y., Ashida Y., Seto K., Takashima S., Kita I. Influence of incomplete bile duct obstruction on the occurrence of cholangiocarcinoma induced by diisopropanolnitrosamine in hamsters // Oncology. - 1990. - Vol.47. - P.170-176.
142. Ko C.W., Lee S.P. Gallstone formation // Gastroenterol. Clin. North Am. - 1999. - Vol.28, № 1. - P.99-115.
143. Komatsu Y., Kawabe T., Toda N., Ohashi M., Isayama M., Tateishi K., Sato S., Koike Y., Yamagata M., Tada M., Shiratori Y., Yamada H., Ihori M., Kawase T., Omata M. Endoscopic papillary balloon dilation for the management of common bile duct stones: experience of 226 cases // Endoscopy. - 1998. - Vol.30. - P.12-17.
144. Komatsu Y., Kawabe T., Shiratori Y., Omata M Replay to the letter by Misra et al. (Endoscopic papillary balloon dilation has sufficient potential to replace endoscopic sphincterotomy for the removal of common bile duct stones) // Endoscopy. - 1999. - Vol.31,
№ 2. - P.212.
145. Komatsu Y., Kawabe T., Shiratori Y., Omata M. Replay to Myung et al. // Endoscopy. - 1999. - Vol.31, № 2. - P.210.
146. Komatsu Y., Toda N., Isayama H., Tsujino T., Tateishi K. et al. Washout of small stones in the bile duct by saline infusion using a side-holed balloon catheter in patients undergoing endoscopic papillary balloon dilation // Gastrointest. Endosc. - 1999. - Vol.49, № 1. - P.101- 104.
147. Kozarek R.A. Balloon dilation of the sphincter of Oddi // Endoscopy. – 1988. – Vol.20. – P.207-210.
148. Krims P.E., Cotton P.B. Papillotomy and functional disordes of the sphincter of Oddi // Endoscopy. - 1988. - Vol.20. - P.203-206.
149. Kurumado K., Nagai T., Kondo Y., Abe H. Long-term observation on morphological cganges of choledochal epithelium after choledochoenterostomy in rats // Dig. Dis. Sci. - 1994. - Vol.39, № 4. - P.809-820.
150. Lachmanan S., Guinane M., Stoner E., Evans D., Yazaki E., Ainley C. Is sphincter of Oddi dysfunction a risk factor for post ERCP pancreatitis? // Gut. - 1999. - Vol.45, Suppl.V.
- A299.
151. Lai K-H., Lin L-F., Lo G-H., Cheng J-S., Huang R-L. et al. Does cholecystectomy after endoscopic sphincterotomy prevent the recurrence of biliary complications // Gastrointest. Endosc. - 1999. - Vol.49, № 4. - P.483-487.
152. Lans J.L., Parikh N.P., Geenen J.E. Application of sphincter of Oddi manometry in routine clinical investigations // Endoscopy. - 1991. - Vol.23. - P.139-143.
153. Lew R.S., Kochman M.L. Endoscopic management of biliary diseases // Curr.Opi.Gastroenterol. - 2000. - Vol.16. - P.454-460.
154. Ljungh A., Wadstrom T. The role of microorganisms in biliary tract disease // Current Gastroenterology Reports. - 2002. - Vol.4. - P.167-171.
155. Luman W., Pride A., Heading R.C., Palmer K.R. Topical glyceryl trinitrate relaxes the sphincter of Oddi. // Gut. - 1997. - Vol.40. - P.541-543.
156. MacMathuna P., White P., Clarke E., Merriman R., Lennon J., Crowe J. Endoscopic balloon sphincteroplasty (papillary dilation) for bile duct stones: efficacy, safety, and follow- up in 100 patients // Gastrointest. Endosc. - 1995. - Vol.42, № 5. - P.468-474.
157. MacMathuna P., Siegenberg D., Gibbons D., Gorin D., O'Brien M. et al. The acute and long-term effect of balloon sphincteroplasty on papillary stricture in pigs // Gastrointest. Endosc. - 1996. - Vol.44, № 6. - P.650-655.
158. MacMathuna P. Endoscopic treatment of bile duct stones: should we cut or dilate the sphincter? // Am. J. Gastroenterol. - 1997. - Vol.92, № 9. - P.1411-1412.
159. Maeshiro K. Preventing acute pancreatitis induced by endoscopic papillary balloon dilation // Dig. Endosc. - 2000. - Vol12, Suppl. - S41.
160. Maguchi H. Modification of the endoscopic papillary balloon dilation method // Dig.
Endosc. - 2000. - Vol.12, Suppl. - S36-S40.
161. Majeed A.W., Ross B., Johnson A.G. The preoperatively normal bile duct does not dilate after cholecystectomy: results of a five year study // Gut. - 1999. - Vol.45. - P.741-743.
162. Masahiko Y., Masafumi I., Yoshihiro I., Masayasu O., Kyo F., Shigeto I. Isosorbide dinitrate drip infusion and slow inflation of balloon for preventing pancreatitis induced by endoscopic papillary dilation // Endoscopy. - 2000. - Vol.32, Suppl.1. - E49.
163. May G.R., Cotton P.B., Edmunds S.E.J., Chong W. Removal of stones from the bile duct at ERCP without sphincterotomy // Gastrointest. Endosc. - 1993. - Vol.39, № 6. - P.749-754.
164. Mehta S.N., Pavone E., Barkun J.S., Bouchard S.,Barkun A.N. Predictors of post-ERCP complications in patients with suspected choledocholithiasis // Endoscopy. - 1998. - Vol.30. - P.457-463.
165. Mergener K., Baillie J. Comment to the article Komatsu Y. et al. Endoscopic papillary balloon dilation for the management of common bile duct stones: experience of 226 cases // Gastrointest. Endosc. - 1998. - Vol.48, № 4. - P.444-446.
166. Minami A., Nakatsu T., Uchida N., Hirabayashi S., Fukuma H., Morshed S.A., Nishioka
M. Papillary dilation vs sphincterotomy in endoscopic removal of bile duct stones: randomized trial with manometric function // Dig. Dis. Sci. - 1995. - Vol.40. - P.2550-2554.
167. Misra S.P., Dwivedi M. Endoscopic management of choledocholithiasis: to cut, stretch or relax? // J. Gastroenterol. Hepatol. - 1998. - Vol.13. - P.1180-1182.
168. Misra S.P., Dwivedi M. Endoscopic papillary balloon dilation for choledocholithiasis: does it have a future? // Endoscopy. - 1999. - Vol.31, № 2. - P.211.
169. Myung S.J., Kim M.H., Kim H.J., Lee S.K. Endoscopic papillary balloon dilation for the management of common bile duct stones: the two faces of sphincter preservation // Endoscopy. - 1999. - Vol.31. - P.209.
170. Neuhaus H. The future of endoscopic retrograde cholangiopancreatography: what is necessary and what should be improved? // Endoscopy. - 1998. - Vol.30, №9, Suppl.2. - P.207-211.
171. Ochi T., Nakazava S., Naito Y., Tsukamoto Y. Endoscopic manometry of the sphincter of Oddi and pancreatic duct in patients with papillary stenosis // Endoscopy. - 1991. - Vol.23.
- P.255-258.
172. Ohashi A., Tamada K., Tomiyama T., Aizava T., Wada S., Miyata T., Nishizono T., Tano S., Sato Y., Ueno N., Kimura K. Influence of bile duct diameter on the therapeutic quality of endoscopic balloon sphincteroplasty // Endoscopy. - 1999. - Vol.31, № 2. - P.137- 141.
173. Ohashi A., Ueno N., Tamada T., Wada S., Miyata T., Nishizono T., Tano S. et al.
Assessment of residual bile duct stones with use of intraductal US during endoscopic balloon sphincteroplasty: comparison with balloon cholangiography // Gastrointest. Endosc. - 1999. - Vol.49, № 3. - P.328-333.
174. Ossenberg F.W., Classen M. Endoscopic-radiological examination and therapy in biliary tract diseases // In: Wright R., Alberti K.G., Karran S, editors. Liver and biliary diseases. - Philadelphia: Saunders, 1979. - P.507-528.
175. Palazzo L. Which test for common bile duct stones? Endoscopic and intraductal ultrasonography // Endoscopy. - 1997. - Vol.29. - P.655-665.
176. Pereira-Lima J.C., Jacobs R., Winter U.H., Benz C., Martin W.R., Adamek H.E., Riemann J.F. Long-term results (7 to 10 years) of endoscopic papillotomy for choledocholithiasis. Multivariate analysis of prognostic factors for the recurrence of biliary symptoms // Gastrointest. Endosc. - 1998. - Vol.48, № 5. - P.457-464.
177. Prat F., Boyer J., Pelletier G., Fritsch J., Choury A.D., Person B., Bretagne J.F., Buffet C. Endoscopic sphincteroclasy for choledocholithiasis // Endoscopy. - 1996. - Vol.28. - S52.
178. Prat F., Malak N.A., Pelletier G., Buffet C., Fritsch J., Choury A.D., Altman C., Liguory C., Etienne J.P. Billiary symptoms and complications more than 8 years after endoscopic sphincterotomy for choledocholithiasis // Gastroenterology. - 1996. - Vol.110. - P.894-899.
179. Prat F., Fritsch J., Choury A.D., Meduri B., Pelletier G., Buffet C. Endoscopic sphincteroclasy: a useful therapeutic tool for biliary endoscopy in Billroth 2 gastrectomy patients // Endoscopy. - 1997. - Vol.29. - P.79-81.
180. Prat F., Meduri B., Ducot B., Chiche R., Salimbeni-Bartolini R., Pelletier G. Prediction of common bile duct stones by noninvasive tests // Annals of Surgery. – 1999. – Vol.229,
№3. – P.362-368.
181. Rabenstein T., Schneider H.T., Hahn E.G., Ell C. 25 years of endoscopic sphincterotomy in Erlangen: assessment of the experience in 3498 patients // Endoscopy. - 1998. - Vol.30, № 9, Suppl.2. - A194-A201.
182. Rolny P., Anderberg B., Lindstrom E., Olaison G., Arvill A. Pancreatitis after sphincter of Oddi manometry // Gut. - 1990. - Vol.31. - P.821-824.
183. Sato H., Kodama T., Takaaki J., Tatsumi Y., Maeda T. et al. Endoscopic papillary balloon dilattaion may preserve sphincter of Oddi function after common bile duct stone management: evaluation from the viewpoint of endoscopic manometry // Gut. - 1997. - Vol. 41. - P.541-544.
184. Saunders K.D., Cates J.A., Roslyn J.J. Pathogenesis of gallstones // Surg. Clin. North Am. – 1990. - Vol.70, № 6. - P.1197-1216.
185. Sauter G., Grabein G., Mannes G.A., Ruckdeschel G., Sauerbruch T. Antibiotic prophilaxis of infectious complications with endoscopic retrograde cholangiopancreatography. A randomized controlled study // Endoscopy. - 1990. - Vol.22. - P.164-167.
186. Schmalz M.J., Geenen J.E. Therapeutic pancreatic endoscopy // Endoscopy. - 1999. - Vol.31, № 1. - P.88-94.
187. Seo D.W. Prospective analysis of endoscopic papillary balloon dilation and endoscopic sphincterotomy for removal of common bile duct stones // Gastrointest. Endosc. - 2000. - Vol.52, № 1. – P.140-142.
188. Sherman S., Ruffolo T.A., Hawes R.H., Lehman G.A. Complications of endoscopic sphincterotomy. A prospective series with emphasis on the increased risk associated with sphincter of Oddi dysfunction and nondilated bile ducts // Gastroenterology. – 1991. - Vol.101, № 4. - P.1068-1075.
189. Sherman S., Gottlieb K., Lehman G.A. Therapeutic biliary endoscopy // Endoscopy. - 1994. - Vol.26. - P.93-112.
190. Siegel J.H., Guelrud M. Endoscopic cholangiopancreatoplasty: hydrostatic balloon dilation in the bile duct and pancreas // Gastrointest. Endosc. - 1983. - Vol.29, № 2. - P.99- 103.
191. Skar V., Skar A.G., Midtvedt T., Osnes M. Bacterial Growth in the duodenum and in the bile of patients with gallstone disease treated with endoscopic papillotomy (EPT) // Endoscopy. - 1986. - Vol.18. - P.10-13.
192. Staritz M., Ewe K., Meyer zum Buschebfelde K.H. Endoscopic papillary dilation (EPD) for the treatment of common bile duct stones and papillary stenosis // Endoscopy. - 1983. - Vol.15. - P.197-198.
193. Staritz M., Poralla T., Dormeyer H.H. et al. Endoscopic removal of common bile duct stones through the intact papilla after medical sphincter dilation // Gastroenterology. - 1985. - Vol.88. - P.1807-1811.
194. Staritz M., Ewe K., Meyer zum Buschenfelde K.H. Investigation of the sphincter of Oddi before, immediately after and six weeks after endoscopic papillotomy // Endoscopy. - 1986. - Vol.18. - P.14-16.
195. Staritz M., Goeke M., Rambow A., Meyer zum Buschenfelde K.H. Investigation of the effect of duodenoscopy on sphincter of Oddi manometry // Endoscopy. - 1991. - Vol.23. - P.130-132.
196. Staritz M. Pharmacology of the sphincter of Oddi // Endoscopy. - 1988. - Vol.20. - P.171- 174.
197. Stendal C. Practical guide to gastrointestinal function testing. - Oxford etc.: Blackwell Sience, 1997. - 280 p.
198. Sugiyama M., Atomi Y. Endoscopic ultrasonography for diagnosing choledocholithiasis: a prospective comparative study with ultrasonography and computed tomography // Gastrointest. Endosc. - 1997. - Vol.45, № 2. - P.143-146.
199. Sugiyama M., Atomi Y. Does endoscopic papillary balloon dilation affect gallbladder motility? // Gastrointest. Endosc. - 1999. - Vol.50, № 1. - P.74-78.
200. Sugiyama M., Izumisato Y., Hatano N., Mori T., Atomi Y. Management of unsuspected common bile duct stones found during laparoscopic cholecystectomy by means of transcystic catheter placement and papillary dilation // Gastrointest. Endosc. - 1999. - Vol.50, № 6. - P.837-840.
201. Sugiyama M., Atomi Y. Medium-term effects of endoscopic papillary balloon dilation on gallbladder motility // Gastrointest. Endosc. - 2001. - Vol.54, № 4. - P.459-463.
202. Takahata S., Yokohata K., Nabae T., Nishiyama K., Yamaguchi K., Chijiiwa K., Tanaka
M. Sphincter of Oddi contractile function after balloon dilation: detailed manometric evaluation in conscious dogs // Gastrointest. Endosc. - 2000. Vol.52, № 5. - P.618-623.
203. Tanaka M., Ikeda S. Sphincter of Oddi manometry: comparison of microtransducer and perfusion methods // Endoscopy. - 1988. - Vol.20. - P.184-188.
204. Tanaka M., Takahata S., Konomi H., Matsunaga H., Yokohata K., Takeda T., Utsunomiya N., Ikeda S. Long-term consequence of endoscopic sphincterotomy for bile duct stones // Gastrointest. Endosc. - 1998. - Vol.48, № 5. - P.465-469.
205. Targarona E.M., Pros I., Trias M. Effects of sphincterotomy on gallbladder physiology: a review // Endoscopy. - 1995. - Vol.27. - P.388-391.
206. Tarnasky P.R., Cunningham J.T., Hawes R.H., Hoffman B.J., Cotton P.B. Pitfalls of bile duct stone removal after balloon sphincter dilation // Am. J. Gastroenterol. - 1996. - Vol.91,
№ 4. - P.822.
207. Tarnasky P., Cunningham J., Cotton P., Hoffman B., Palesch Y., Freeman J., Curry N., Hawes R. Pancreatic sphincter hypertension increases the risk of post-ERCP pancreatitis // Endoscopy. - 1997. - Vol.29. - P.252-257.
208. Teilum D. In vitro measurement of the length of the sphincter of Oddi // Endoscopy. - 1991. - Vol.23. - P.114-116.
209. Tham T.C.K., Carr-Locke D.L., Collins J.S.A. Endoscopic sphincterotomy in the young patient: is there cause for concern? // Gut. - 1997. - Vol.40. - P.697-700.
210. Tibble J.A., Cairns S.R. Endoscopic balloon sphincteroplasty: use in a patient with a Billroth II gastrectomy // Endoscopy. - 1996. - Vol.28. - P.790.
211. Tittobello A. Diagnosis and prevention of post-ERCP pancreatitis // Endoscopy. - 1997. - Vol.29. - P.285-287.
212. Toouli J., Roberts-Thomson I.C., Kellow J., Dowsett J., Saccone G.T.P., Evans P. Et al.
Manometry based randomised trial of endoscopic sphincterotomy for sphincter of Oddi dysfunction. // Gut. - 2000. - Vol.46. - P.98-102.
213. Torsoli A. Physiology of the human sphincter of Oddi // Endoscopy. - 1988. - Vol.20. - P.166-170.
214. Tytgat G.N.J., Meenan J.K.P., Rauws E.A.J., Huibregtse K. Endoscopic biliopancreatic balloon dilation // Endoscopy. - 1996. - Vol.28. - P.367-371.
215. Tytgat G.N.J., Lightdale C.J. Billiary tract diseases // In: Classen M., Tytgat G.N.J., Lightdale C.J. Gastroenterological Endoscopy. - Stuttgart; New York: Thieme, 2002. - Chapter 43. - P.614-633.
216. Uchida N., Ezaki T., Hirabayashi S. et al. Endoscopic lithotomy of common bile duct stones with sublingual nitroglycerin and guidewire // Am. J. Gastroenterol. - 1997. - Vol.92. - P.1440-1443.
217. Ueno N., Hashimoto M., Ozawa Y., Yoshizawa K. Treatment of pancreatic duct stones with the use of endoscopic balloon dilation // Gastrointest. Endosc. - 1998. - Vol.47, № 3. - P.309-310.
218. Ueno N., Kurihara K. Impact of endoscopic sphincter dilation on papillary structure: a case report // Gastrointest. Endosc. - 1999. - Vol.50, № 5. - P.
219. Ueno N., Ozawa Y. Endoscopic sphincter dilation in patients with bile duct stones: immediate and medium-term results // J. Gastroenterol. Hepatol. - 1999. - Vol.14, № 8. - P.822-826.
220. Ueno N., Ozawa Y. Pancreatitis induced by endoscopic balloon sphincter dilation and changes in serum amylase levels after the procedure // Gastrointest. Endosc. - 1999. - Vol.49,
№ 4. - P.472-476.
221. Wehrmann T., Stergiou N., Riphaus A., Lembcke B. Correlation between sphincter of Oddi manometry and intraductal ultrasound morphology in patients with suspected sphincter of Oddi dysfunction // Endoscopy. - 2001. - Vol.33, № 9. - P.773-777.
222. Wicks A.C.B., Robertson G.S.M., Veitch P.S. Structured training and assessment in ERCP has become essential for the Calman era // Gut. - 1999. - Vol.45. - P.154-156.
223. Wojtun S., Gil J., Gietka W., Gil M. Endoscopic sphincterotomy for choledocholithiasis: a prospective single-center study on the short-term and long-term treatment results in 483 patients // Endoscopy. - 1997. - Vol.29. - P.258-265.
224. Yasuda I., Tomita E., Enya M., Kato T., Moriwaki H. Can endoscopic papillary balloon dilation really preserve sphincter of Oddi function? // Gut. - 2001. - Vol.49, № 5. - P.686- 691.
225. Zhang Q. Endoscopic sphincterotomy and balloon sphincteroplasty for common bile duct stones: a Chinese experience // Endoscopy. - 1999. - Vol.31, №5. - P.6.
Статьи по теме
Рекомендуемые статьи
Синдром Бернара-Горнера
птоз, миоз и энофтальм при повреждении симпатического нерва (С7—Тh11) при осложненных дивертикулах, опухолях пищевода или метастазах в позвоночник.
При эндоскопическом исследовании в случае бронхоэктазов в стадии ремиссии выявляется
частично диффузный бронхит I степени воспаления
Активируйте PUSH уведомления в браузер
Отключите PUSH уведомления в браузер
Содержание
Интернет магазин
Популярное
- О нас
- Правовые вопросы
- Политика
обработки персональных
данных EndoExpert.ru - Связаться с нами
- Стать партнером
© 2016-2022 EndoExpert.ru

Вы находитесь в разделе предназначенном только для специалистов (раздел для пациентов по ссылке). Пожалуйста, внимательно прочитайте полные условия использования и подтвердите, что Вы являетесь медицинским или фармацевтическим работником или студентом медицинского образовательного учреждения и подтверждаете своё понимание и согласие с тем, что применение рецептурных препаратов, обращение за той или иной медицинской услугой, равно как и ее выполнение, использование медицинских изделий, выбор метода профилактики, диагностики, лечения, медицинской реабилитации, равно как и их применение, возможны только после предварительной консультации со специалистом. Мы используем файлы cookie, чтобы предложить Вам лучший опыт взаимодействия. Файлы cookie позволяют адаптировать веб-сайты к вашим интересам и предпочтениям.
Я прочитал и настоящим принимаю вышеизложенное, хочу продолжить ознакомление с размещенной на данном сайте информацией для специалистов.











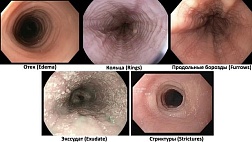




.jpg)




.png)















Комментарии