- Компании
- Takeda. О компании, буклеты, каталоги, контакты
- Olympus. О компании, буклеты, каталоги, контакты
- Boston Scientific. О компании, буклеты, каталоги, контакты
- Pentax. О компании, буклеты, каталоги, контакты
- Fujifilm & R-Farm. О компании, буклеты, каталоги, контакты
- Erbe. О компании, буклеты, каталоги, контакты
- Еще каталоги
- Мероприятия
- Информация
- Обучение
- Классификации
- Атлас
- Quiz
- Разделы
- Пациенту
QR-код этой страницы
Для продолжения изучения на мобильном устройстве ПРОСКАНИРУЙТЕ QR-код с помощью спец. программы или фотокамеры мобильного устройства
Документы и приказы: ОБЕСПЕЧЕНИЕ ЭПИДЕМИОЛОГИЧЕСКОЙ БЕЗОПАСНОСТИ НЕСТЕРИЛЬНЫХ ЭНДОСКОПИЧЕСКИХ ВМЕШАТЕЛЬСТВ НА ЖЕЛУДОЧНО–КИШЕЧНОМ ТРАКТЕ И ДЫХАТЕЛЬНЫХ ПУТЯХ МУ 3.1.3420-17
Полный текст статьи:
____________________________________________________________
Федеральная служба по надзору в сфере защиты прав потребителей и благополучия человека
____________________________________________________________
3.1. Эпидемиология. Профилактика инфекционных заболеваний
ОБЕСПЕЧЕНИЕ ЭПИДЕМИОЛОГИЧЕСКОЙ БЕЗОПАСНОСТИ НЕСТЕРИЛЬНЫХ ЭНДОСКОПИЧЕСКИХ ВМЕШАТЕЛЬСТВ НА ЖЕЛУДОЧНО-КИШЕЧНОМ ТРАКТЕ И ДЫХАТЕЛЬНЫХ ПУТЯХ
Методические указания
МУ 3.1.3420-17
Москва
2017
1. Методические указания разработаны Федеральной службой по надзору в сфере защиты прав потребителей и благополучия человека (Е. Б. Ежлова, А. А. Мельникова, Н. В. Фролова, Е. П. Игонина, С. В. Сенников), ФБУН «Московский научно-исследовательский институт эпидемиологии и микробиологии им. Г. Н. Габричевского» Роспотребнадзора (В. А. Алешкин, Е. П. Селькова, Т. А. Гренкова, А. И. Чижов), ФБУН «Научно-исследовательский институт дезинфектологии» Роспотребнадзора (Н. В. Шестопалов, Л. Г. Пантелеева, Л. С. Федорова, И. А. Храпунова), ФГБОУ ВО «Первый МГМУ им. И. М. Сеченова» Минздрава России (В. Г. Акимкин, И. М. Абрамова), Ассоциацией «Эндоскопическое общество «РЭндО» (М. П. Королев, А. Г. Короткевич, А. М. Субботин, А. В. Сапегин), Общероссийской общественной организацией «Ассоциация медицинских сестер России» (Е. В. Коровина).
2. Рекомендованы к утверждению Комиссией по санитарно-эпидемиологическому нормированию Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (протокол от 22 декабря 2016 г. № 2).
3. Утверждены Руководителем Федеральной службы по надзору в сфере защиты прав потребителей, Главным государственным санитарным врачом Российской Федерации А. Ю. Поповой 20 февраля 2017 года.
4. Введены впервые.
Содержание
|
1. |
Область применения |
|
|
2. |
Общие сведения |
|
|
3. |
Общие требования к обработке эндоскопов для нестерильных вмешательств и инструментов к ним |
|
|
4. |
Стандарт обработки гибких эндоскопов для нестерильных вмешательств |
|
|
5. |
Содержание и условия эффективного проведения процессов обработки гибких эндоскопов для нестерильных вмешательств ручным способом |
|
|
6. |
Требования к механизированному способу обработки гибких эндоскопов для нестерильных вмешательств. Порядок проведения |
|
|
7. |
Требования к условиям транспортирования и хранения эндоскопов для нестерильных вмешательств |
|
|
8. |
Требования к обработке инструментов к эндоскопам |
|
|
9. |
Организация мероприятий по профилактике инфекций, связанных с проведением нестерильных эндоскопических вмешательств |
|
|
10. |
Порядок проведения планового микробиологического контроля качества обработки эндоскопов для нестерильных вмешательств и инструментов к ним |
|
|
11. |
Требования к проведению профилактической дезинфекции в эндоскопическом отделении/кабинете |
|
|
12. |
Разработка и внедрение программы внутреннего контроля качества обработки эндоскопов в эндоскопическом отделении/кабинете |
|
|
|
Приложения: |
|
|
1. |
Перечень основных нестерильных эндоскопических вмешательств |
|
|
2. |
Алгоритм обработки ультразвуковых зондов |
|
|
3. |
Формы и содержание обучения медицинских работников, занимающихся проведением эндоскопических вмешательств и обработкой эндоскопов |
|
|
4. |
Порядок расчета потребности в эндоскопах в зависимости от планируемого (выполняемого) числа вмешательств |
|
|
5. |
Рабочая инструкция по обработке эндоскопов. Алгоритм обработки видеогастроскопа с дополнительным каналом для подачи воды (пример) |
|
|
6. |
Порядок проведения расширенных внеплановых микробиологических исследований на качество обработки эндоскопов |
|
УТВЕРЖДАЮ
Руководитель
Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека – Главный государственный санитарный врач Российской Федерации
А.Ю. Попова
20 февраля 2017г.
3.1. Эпидемиология. Профилактика инфекционных болезней
Обеспечение эпидемиологической безопасности
нестерильных эндоскопических вмешательств
на желудочно-кишечном тракте и дыхательных путях
Методические указания
МУ 3.1.3420—17
I. Область применения
1.1. Настоящие методические указания (далее – МУ) предназначены для медицинских организаций, проводящих эндоскопические вмешательства, органов и организаций Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека, образовательных и научных организаций, реализующих образовательные программы дополнительного профессионального образования медицинских работников, проводящих эндоскопические вмешательства.
1.2. Методические указания следует применять совместно с санитарно-эпидемиологическими правилами СП 3.1.3263—15 «Профилактика инфекционных заболеваний при эндоскопических вмешательствах»[1] (далее – СП 3.1.3263—15).
1.3. В методических указаниях изложены положения к санитарно-противоэпидемическим (профилактическим) мероприятиям, обеспечивающим эпидемиологическую безопасность нестерильных эндоскопических вмешательств на желудочно-кишечном тракте, дыхательных путях и органе слуха.
II. Общие сведения
Эндоскопические вмешательства, при которых эндоскоп вводят через естественные пути в органы, в норме содержащие собственную микрофлору (желудочно-кишечный тракт – ЖКТ, верхние и нижние дыхательные пути – ДП, наружное и среднее ухо), относятся к нестерильным. В ходе их проведения могут реализоваться эндогенный и экзогенный типы инфицирования пациентов.
При эндогенном типе инфицирования собственные микроорганизмы пациента переносятся эндоскопом из одного локуса организма в другой (например, из ротоглотки в бронхи) или проникают в кровоток вследствие бактериальной транслокации при давлении на слизистую оболочку эндоскопа и дистензионной среды (жидкая или газовая среда, создаваемая искусственно в полом органе для его расширения при проведении эндоскопического вмешательства). Риски развития эндогенных инфекций малы и колеблются от значения, близкого к 0 % для эзофагогастродуоденоскопии и сигмоидоскопии до 1—2 % для процедуры эндоскопической ретроградной холангиопанкреатографии (ЭРХПГ).
В реализации экзогенного типа инфицирования участвуют следующие факторы передачи возбудителя инфекции в порядке убывания их значимости: эндоскоп, принадлежности и инструменты к нему; вода и лекарственные препараты, вводимые во время эндоскопического вмешательства через эндоскоп, моюще-дезинфицирующая машина (МДМ).
Эндоскоп может стать фактором передачи возбудителя инфекции при нарушении герметичности, производственных дефектах, неадекватной очистке и/или неэффективной дезинфекции высокого уровня (ДВУ), недостаточном высушивании каналов.
Основными возбудителями инфекций, связанных с нестерильными эндоскопическими вмешательствами, являются патогенные (например, Mycobacterium tuberculosis, Salmonella spp., Hepatitis C virus, Hepatitis B virus) и условно-патогенные (например, Pseudomonas aeruginosa, Acinetobacter spp., Enterobacter spp.) микроорганизмы. В этиологии инфекций, связанных с бронхоскопией и ЭРХПГ, в последние годы значительно увеличилась значимость условно-патогенных микроорганизмов с множественной устойчивостью к антибиотикам.
Размножению и накоплению на/в эндоскопах микроорганизмов с образованием биопленок могут способствовать остаточные органические загрязнения (при некачественной очистке) и хранение во влажном состоянии. Внутри биопленки микроорганизмы защищены от действия дезинфицирующих средств.
Все пациенты рассматриваются как потенциальные источники возбудителей инфекции, в связи с чем все эндоскопы и принадлежности к ним после использования обрабатываются по единому стандарту.
Исключение составляют эндоскопы, использованные для обследования пациентов с установленным диагнозом (или подозрением) болезни Крейтцфельдта-Якоба/нового варианта болезни Крейтцфельдта-Якоба, которые подвергаются предварительной и окончательной очистке в растворах щелочных моющих средств, стерилизации парами пероксида водорода и далее используются для оказания медицинской помощи только данной категории пациентов. При этом использованные в ходе эндоскопического вмешательства инструменты, биопсийный клапан (если через него проводились инструменты), приспособления для очистки эндоскопа (щетки, салфетки, емкости) обезвреживаются как отходы класса В (рекомендуется сжигание).
Медицинские работники, осуществляющие проведение эндоскопических вмешательств и обработку эндоскопов, подвергаются воздействию негативных биологических и химических факторов. Потенциальную опасность для здоровья представляют:
– микробные аэрозоли, которые образуются при кашле пациента и введении в его дыхательные пути трубки бронхоскопа; во время проведения механической очистки щетками каналов и клапанов эндоскопа, продувки очищенных каналов воздухом;
– биологические жидкости (например, рвотные массы, содержимое кишечника), которые могут выделяться во время вмешательства естественным путем или в виде аэрозоля через негерметичные (неисправные) клапаны эндоскопа;
– пары и растворы дезинфицирующих и моющих средств;
– травмы рук колюще-режущими инструментами к эндоскопам, полученные персоналом на этапах их подготовки к стерилизации.
Проведение исследований верхних отделов ЖКТ является фактором риска колонизации врачей и медицинских сестер Helicobacter pylori. Предполагается, что в передаче возбудителя определенную роль играет воздушно-пылевой механизм.
В целях предотвращения негативных воздействий факторов производственной среды должны выполняться требования к охране здоровья медицинского персонала, установленные СП 3.1.3263—15.
III. Общие требования к обработке эндоскопов
для нестерильных вмешательств и инструментов к ним
3.1. Для проведения нестерильных эндоскопических вмешательств (перечень основных вмешательств представлен в прилож. 1) используются эндоскопы, которые являются изделиями многократного применения, инструменты одноразового и/или многоразового использования, дополнительное эндоскопическое оборудование (осветитель, инсуфлятор, эндовидеосистема, монитор, аспиратор-ирригатор и др.).
3.2. Эндоскопы после каждого использования последовательно подвергаются следующим процессам обработки: предварительной очистке (ПО), окончательной очистке самостоятельной (ОО) или при совмещении с дезинфекцией (ОО+Д), ДВУ.
3.2.1. Предварительная очистка внешних поверхностей эндоскопа проводится способом протирания салфетками или губкой одноразового использования, смоченными раствором моющего средства. Каналы промываются раствором моющего средства и/или водой.
3.2.2. Окончательная очистка является важнейшим этапом обработки эндоскопа, от которого зависит эффективность последующей ДВУ. Она проводится в качестве самостоятельного процесса или при совмещении с дезинфекцией, что определяется применяемыми для этих целей средствами (моющими или моюще-дезинфицирующими).
3.2.3. Моющие средства на основе ферментов и/или поверхностно-активных веществ (ПАВ) не содержат антимикробные компоненты, поэтому их растворы для цели окончательной очистки эндоскопов применяются строго однократно.
3.2.4. Дезинфицирующие средства с малым пенообразованием, не обладающие фиксирующими свойствами в используемых концентрациях, могут применяться для очистки при совмещении с дезинфекцией до появления первых визуальных признаков загрязнения, но не более одной рабочей смены, при этом для предотвращения перекрестной контаминации эндоскопы для исследований верхних, нижних отделов ЖКТ и ДП обрабатываются раздельно.
3.2.5. После слива моющего/моюще-дезинфицирующего раствора моечная ванна очищается и дезинфицируется способом протирания дезинфицирующим средством (ДС) по режиму, эффективному в отношении вирусов, микобактерий и грибов рода Candida) и может быть использована повторно для обработки любой модели эндоскопа (гастроскоп, колоноскоп, бронхоскоп и др.).
3.2.6. Дезинфекция высокого уровня выполняется ручным (при полном погружении в раствор ДС) или механизированным способами. Не допускается проведение ДВУ эндоскопов способом протирания.
3.2.7. Для ДВУ эндоскопов для нестерильных вмешательств и стерилизации инструментов к ним применяются химические средства, регламентированные п. 7.5 и 7.6 СП 3.1.3263—15 с учетом рекомендаций производителей эндоскопов по воздействию на материалы изделий. Для разработанных к настоящему времени средств концентрации наиболее распространенных действующих веществ (ДВ) в рабочих растворах (или готовых к применению формах), для которых научно доказано наличие спороцидных свойств при комнатных значениях температуры, составляют, как правило, для глутарового альдегида – не менее 2,0 %, ортофталевого альдегида – 0,55 %, перекиси водорода – не менее 6,0 %, надуксусной кислоты – не менее 0,2 %.
3.3. Допустимым уровнем обеззараживания жестких и гибких бронхоскопов на заключительном этапе обработки является ДВУ, однако при наличии в медицинской организации (МО) необходимых условий и оборудования возможно проведение стерилизации. Жесткие эндоскопы для исследования ЖКТ (ректоскопы), ЛОР-органов (риноскопы, ларингоскопы, отоскопы и др.) на заключительном этапе обработки также могут подвергаться ДВУ или стерилизации (как правило, насыщенным паром под давлением в соответствии с рекомендациями производителей).
3.4. Непосредственно после использования, включая выполнение эндоскопических вмешательств в ночное время и за пределами МО, эндоскопы должны пройти все процессы обработки. Предварительная очистка всегда выполняется в полном объеме на месте проведения вмешательства. При оказании медицинской помощи за пределами базовой МО и отсутствии условий для проведения ОО и ДВУ эндоскопа выполнение этих процессов может быть отсрочено до возвращения эндоскопа в МО.
3.5. Инструменты к эндоскопам независимо от вида эндоскопического вмешательства должны быть стерильными. После использования они последовательно подвергаются предварительной очистке, предстерилизационной очистке при совмещении с дезинфекцией, стерилизации.
3.5.1. Предварительная очистка проводится в эндоскопической манипуляционной способом полного погружения инструментов в раствор моющего/моюще-дезинфицирующего средства, не обладающего фиксирующими свойствами. После завершения этапа замачивания раствор сливается, инструменты промываются водой на перфорированном поддоне (при наличии в эндоскопической манипуляционной моечной ванны для инструментов). При отсутствии условий для слива раствора и ополаскивания инструментов допускается их транспортирование в моечно-дезинфекционное помещение или централизованное стерилизационное отделение (ЦСО) в закрытом контейнере в растворе.
3.5.2. Предстерилизационная очистка при совмещении с дезинфекцией проводится в растворе дезинфицирующего средства, не обладающего фиксирующими свойствами в применяемой концентрации.
3.5.3. Допускается отсрочить проведение стерилизации инструментов к эндоскопам до следующей смены при условии, что изделия подвергнуты дезинфекции, предстерилизационной очистке и хорошо просушены.
3.5.4. Выбор средства, метода и режима стерилизации осуществляется с учетом рекомендаций производителя инструментов. Стерилизация инструментов к эндоскопам механизированным способом является предпочтительнее, стерилизация растворами химических средств допускается, если другие методы недоступны.
IV. Стандарт обработки гибких эндоскопов
для нестерильных вмешательств
|
Место проведения |
Последовательность проведения обработки эндоскопов
| ||
|
Эндоскопическая Манипуляционная |
Предварительная очистка
| ||
|
Моечно-дезинфекционное помещение |
Тест на герметичность | ||
|
Окончательная очистка или окончательная очистка при совмещении с дезинфекцией ручным способом с применением щеток для доступных каналов, клапанов, гнезд клапанов, элеватора и области вокруг него (при наличии) | |||
|
Полный цикл
|
Проведение ДВУ
|
Проведение ДВУ
| |
|
ОО промыванием растворами моющих средств Ополаскивание ДВУ Ополаскивание Сушка Промывание 70%-м этиловым или изопропиловым спиртом* Продувка воздухом |
ДВУ Ополаскивание Сушка Промывание 70%-м этиловым или изопропиловым спиртом* Продувка воздухом |
ДВУ Ополаскивание Сушка Промывание 70%-м этиловым или изопропиловым спиртом* Продувка воздухом | |
Примечание: * Этап дополнительной сушки каналов эндоскопов проводится спиртом, соответствующим микробиологической чистоте категории 2 (табл. 1 раздела 1 «Рекомендаций к установлению норм микробиологической чистоты лекарственных препаратов, субстанций и вспомогательных веществ для введения в нормативные документы» (Изменение 3 к статье «Методы микробиологического контроля лекарственных средств», ГФ XI, вып. 2, 187 с.)
|
Последовательность и содержание этапов для процессов ПО, ОО/ОО + Д, ДВУ |
Материально-техническое обеспечение
|
Условия эффективного выполнения определенного этапа или процесса обработки |
|
1 |
2 |
3 |
|
I. Предварительная очистка Проводится в эндоскопической манипуляционной до отключения эндоскопа от источника света и аспирационного насоса. Предназначена для удаления массивных, в том числе видимых загрязнений, с поверхности и из каналов эндоскопа для предотвращения их высыхания | ||
|
В течение 10 с провести аспирацию воздуха через систему каналов биопсия-аспирация (БА) для предотвращения вытекания биологических жидкостей из биопсийного канала |
- Средства индивидуальной защиты (СИЗ) персонала. - Оборудование (источник света и аспирационный насос). - Промывочные трубки дополнительных каналов при их наличии. - Водонепроницаемый колпачок для видеоэндоскопа некоторых производителей. - Адаптер для очистки канала подачи воздуха/воды эндоскопов некоторых производителей. - Одноразовые или обрабатываемые емкости вместимостью не менее 200 мл для моющего раствора и воды. - Приготовленный раствор моющего средства. - Чистые салфетки или губки одноразового использования. - Контейнер для дезинфекции или мешок желтого цвета для сбора медицинских отходов класса Б |
|
|
Протереть рабочую часть эндоскопа от блока управления к дистальному концу чистой одноразовой салфеткой (губкой), смоченной в растворе моющего средства, изгибающуюся часть – вращательными движениями |
Использованную салфетку сбросить в раствор ДС или контейнер (пакет) желтого цвета для отходов класса Б. Губку можно использовать для проведения ОО/ОО+Д, после чего сбросить в раствор ДС или контейнер (пакет) желтого цвета для отходов класса Б | |
|
Промыть моющим раствором систему каналов БА. Опустить дистальный конец эндоскопа в емкость с 150—200 мл раствора моющего средства. Попеременно аспирировать раствор и воздух. Завершить процедуру аспирацией воздуха |
Не допускать переполнения аспирационной банки | |
|
Промыть водой систему каналов БА, опустив дистальный конец в емкость с водой на 10 с, завершить процедуру аспирацией воздуха |
Этап выполняется в том случае, если в ходе предварительной и окончательной очистки используются различные средства для предотвращения проблем с их совместимостью | |
|
Промыть водой каналы и форсунки подачи воздуха и воды в соответствии с инструкцией производителя |
|
Предварительно заменить клапан воздух-вода (ВВ) на адаптер для очистки канала подачи ВВ (если это определено инструкцией производителя) |
|
Промыть водой или моющим средством дополнительные каналы (при их наличии) в соответствии с инструкцией производителя |
|
Обработке подлежат все каналы, даже если они не были использованы в предшествующем исследовании |
|
Отсоединить эндоскоп от осветителя, видеопроцессора, аспирационного насоса, снять клапаны |
| |
|
Присоединить водонепроницаемый колпачок (заглушку) к коннектору эндоскопа |
Процедура выполняется при обработке видеоэндоскопа | |
|
Перенести эндоскоп в моечное помещение |
Транспортировать по коридорам отделения (организации) в закрытом виде на лотке | |
|
Тест на герметичность1) Позволяет подтвердить водонепроницаемость (герметичность) эндоскопа до его погружения в раствор химического средства, чтобы избежать серьезных повреждений при контакте с ним | ||
|
Использование
|
|
|
|
Подключить течеискатель к устройству подачи воздуха |
Средства индивидуальной защиты (СИЗ) персонала. - устройство подачи воздуха, - течеискатель (разных типов), - моечная ванна, - вода водопроводная питьевого качества. |
Убедиться в поступлении воздуха через течеискатель |
|
1.Присоединить течеискатель к эндоскопу и подать воздух для создания избыточного давления в аппарате. При использовании ручного течеискателя избыточное давление создается при помощи груши до уровня, указанного на манометре («сухой тест»). Наблюдать за показаниями манометра в течение времени, указанного производителем эндоскопа. |
О поступлении воздуха в эндоскоп судят по растяжению наружного покрытия.
| |
|
При использовании тестера с автоматизированным определением утечки воздуха необходимо следовать инструкции производителя тестера |
| |
|
2.Полностью погрузить эндоскоп в воду. С помощью винтов блока управления изменять угол изгиба вводимой трубки во всех направлениях. Наблюдать за поверхностью погруженного эндоскопа в течение времени, указанного производителем (тест на протечки в воде). Проводится самостоятельно или как второй этап после завершения «сухого теста» |
О нарушении герметичности эндоскопа свидетельствует появление единичных или в виде дорожки пузырьков воздуха.
| |
|
3.Извлечь эндоскоп с течеискателем из воды, отключить подачу воздуха на тестер (сбросить давление при использовании ручного течеискателя), через несколько секунд отсоединить тестер от устройства подачи воздуха, а затем от эндоскопа | ||
|
II. Окончательная очистка или окончательная очистка при совмещении с дезинфекцией Проводится с целью максимально возможного удаления всех видов загрязнений, в том числе лекарственных препаратов и микроорганизмов с поверхности и из каналов эндоскопа | ||
|
1этап. ОО/ОО + Д наружных поверхностей и каналов эндоскопа | ||
|
Полностью погрузить эндоскоп и съемные детали в раствор моющего или моюще-дезинфицирующего средства, принудительно заполнив все каналы через вспомогательные приспособления при помощи шприца или помпы. Отсоединить вспомогательные приспособления, оставив их в растворе |
Моечная ванна вместимостью не менее 10 л с крышкой. Рабочий раствор моющего или моюще-дезинфицирующего средства, приготовленный в соответствии с инструкцией по применению в режиме ОО или ОО + Д. |
О полном заполнении каналов свидетельствует прекращение выделения пузырьков воздуха из выходных отверстий эндоскопа |
|
Выдержать в растворе в течение времени, указанного в инструкции по применению используемого средства |
Вода водопроводная питьевого качества. Чистые безворсовые салфетки/губки одноразового использования. Вспомогательные приспособления для обработки каналов эндоскопа3). Шприц емкостью 20—30 см3 (20—30 мл) или помпа. Таймер. Термометр. Стерильные щетки многоразового использования или щетки одноразового использования4). Контейнер с раствором ДС, не обладающего фиксирующими биологические загрязнения свойствами, для предстерилизационной очистки при совмещении с дезинфекцией (ПСО +Д) щеток многоразового использования. Контейнер для дезинфекции или мешок желтого цвета для сбора медицинских отходов класса Б |
Строго соблюдать режим применения средства: концентрацию раствора, время выдержки, температуру раствора |
|
После завершения выдержки в растворе очистить от загрязнений внешнюю поверхность эндоскопа чистыми одноразовыми салфетками или губкой |
Использованные салфетки сбросить в емкость с ДС или в мешок желтого цвета | |
|
Очистить специальными щетками клапан и адаптер подачи воздуха/воды, аспирационный клапан, биопсийный клапан, торцевую часть вводимой трубки, механизм элеватора (для дуоденоскопа), гнезда клапанов, а также все доступные каналы в соответствии с рекомендациями производителя. Продолжать обработку каналов до тех пор, пока на щетке не перестанут обнаруживаться видимые загрязнения (не менее 3 проходов) |
Все процедуры очистки проводить при полном погружении эндоскопа и съемных принадлежностей в раствор, чтобы избежать разбрызгивания контаминированной жидкости.
| |
|
Присоединить вспомогательные приспособления для обработки каналов, через которые промыть все каналы раствором средства с помощью шприца/помпы для удаления остатков загрязнений. Строго следовать инструкции производителя |
Проводить данные процедуры при полном погружении эндоскопа в раствор | |
|
Вытеснить раствор средства из каналов воздухом через вспомогательные приспособления |
Проводить данные процедуры при полном погружении эндоскопа в раствор | |
|
2 этап. Ополаскивание эндоскопа от остатков моющего/моюще-дезинфицирующего средства Проводится с целью удаления остатков средства, использованного для ОО или ОО+Д, с поверхности и из каналов эндоскопа | ||
|
Погрузить эндоскоп в воду питьевого качества. При помощи душевой насадки тщательно ополоснуть внешние поверхности эндоскопа и принадлежности к нему |
Моечная ванна, вместимостью не менее 10 л (при использовании растворов моющих средств однократного применения допускается проведение всех этапов окончательной очистки в одной ванне). Вода водопроводная питьевого качества. Вспомогательные приспособления для обработки каналов эндоскопа. Шприц емкостью 20—30 см3 (20—30 мл) или помпа |
Для ополаскивания каждого эндоскопа использовать новую порцию водопроводной воды питьевого качества |
|
Ополоснуть водой каналы через вспомогательные приспособления при помощи шприца или помпы |
Каждый канал ополоснуть не менее 90 мл воды при помощи шприца или прокачать воду при помощи помпы не менее 1 мин | |
|
3 этап. Сушка эндоскопа после ополаскивания Проводится для предотвращения разбавления водой средства для ДВУ | ||
|
Внешнюю поверхность эндоскопа высушить чистыми салфетками. Воду из каналов удалить продувкой или аспирацией воздуха через вспомогательные приспособления при помощи шприца или помпы |
Стол/рабочая поверхность или моечная ванна, в которой проводилось ополаскивание. Чистая простыня (пеленка). Чистые салфетки. Вспомогательные приспособления. Шприц/помпа |
Выходы каналов при продувке закрыть салфетками для предотвращения образования микробных аэрозолей. Использованные салфетки сбросить в контейнер для дезинфекции или в мешок желтого цвета для сбора отходов класса Б |
|
Контроль качества очистки путем постановки: – азопирамовой или другой регламентированной для этой цели пробы5); – фенолфталеиновой пробы6) |
После использования растворов химических средств (азопирам, фенолфталеин) биопсийный канал ополоснуть 20—30 мл водопроводной воды питьевого качества и продуть воздухом, а наружную поверхность протереть последовательно салфеткой, смоченной водопроводной водой, и сухой салфеткой | |
|
III. Дезинфекция высокого уровня Выполняется в зоне ДВУ моечно-дезинфекционного помещения. Проводится с целью уничтожения вегетативных форм бактерий (в том числе микобактерий), грибов, вирусов и снижения количества споровых форм микроорганизмов на/в эндоскопе | ||
|
1этап. Дезинфекционная выдержка | ||
|
Полностью погрузить эндоскоп в раствор ДС, заполнить каналы через вспомогательные приспособления при помощи шприца или помпы |
Продезинфицированная емкость объемом не менее 10 л с крышкой. Рабочий раствор средства ДВУ многократного применения из перечня регламентированных СП 3.1.3263—15 групп химических веществ в стерилизующей (спороцидной) концентрации. Вспомогательные приспособления для обработки каналов. Шприц или помпа7). Таймер. Водный термометр. Химические индикаторы8) |
О полном заполнении каналов свидетельствует прекращение выделения пузырьков воздуха из выходных отверстий эндоскопа |
|
Вспомогательные приспособления отсоединить, заполнить раствором средства ДВУ через шприц и оставить в растворе вместе с эндоскопом, шприц снять и сбросить в контейнер для отходов класса Б. Удалить пузырьки воздуха с внешних поверхностей эндоскопа и вспомогательных приспособлений салфеткой |
Необходимо обеспечить полный контакт всех элементов эндоскопа и вспомогательных приспособлений с раствором средства ДВУ | |
|
Дезинфекционная выдержка в растворе. При использовании помпы раствор в течение времени дезинфекционной выдержки принудительно циркулирует по каналам |
Контролировать режим применения раствора или готового к применению средства ДВУ: концентрацию ДВ (для средств многократного применения) химическими индикаторами (не реже одного раза в смену), температуру – термометром, время дезинфекционной выдержки – таймером | |
|
После завершения дезинфекционной выдержки выдуть раствор из каналов воздухом вручную при помощи вновь присоединенных вспомогательных приспособлений и стерильного шприца или при помощи помпы |
Вспомогательные приспособления. Стерильный шприц или помпа. Спиртосодержащий кожный антисептик. Стерильные перчатки |
Этап выполняется с соблюдением правил асептики. Персонал снимает в зоне очистки халат или фартук, нарукавники, перчатки, переходит в зону ДВУ, проводит гигиеническую обработку рук и надевает стерильные перчатки перед |
|
|
|
манипуляциями с продезинфицированным эндоскопом |
|
2 этап. Ополаскивание после ДВУ | ||
|
Переложить эндоскоп с присоединенными вспомогательными приспособлениями в моечную ванну/емкость с водой регламентированного микробиологического качества. Ополоснуть каналы эндоскопа через вспомогательные приспособления при помощи стерильного шприца/помпы, вытеснить воду воздухом. Отсоединить вспомогательные приспособления от эндоскопа. Ополоснуть наружные поверхности эндоскопа, используя стерильные салфетки и/или душевую насадку. Тщательно ополоснуть водой вспомогательные приспособления |
Моечная ванна объемом не менее 10 л для ополаскивания гастроинтестинальных эндоскопов или емкость достаточного объема для ополаскивания бронхоскопов при полном погружении. Вода водопроводная питьевого качества для ополаскивания гастроинтестинальных эндоскопов. Вода стерильная, кипяченая или очищенная на антимикробных (обеспечивающих задержку частиц размером более 0,2 мкм) фильтрах для ополаскивания бронхоскопов. Вспомогательные приспособления. Стерильный шприц или помпа |
Этап выполняется с соблюдением правил асептики. Порядок ополаскивания прописан в инструкции на применяемое средство (кратность и длительность ополаскивания). Объем воды, используемой для ополаскивания каждого канала, не может быть менее 90 мл. Вода для ополаскивания используется строго однократно |
|
3 этап. Сушка эндоскопа | ||
|
Извлечь эндоскоп и вспомогательные приспособления из воды и перенести на стерильную простыню (предварительно слить из них воду). Стерильными салфетками просушить наружные поверхности эндоскопа, клапаны. Присоединить вспомогательные приспособления и просушить каналы продувкой воздухом или аспирацией через стерильную силиконовую трубку |
Стерильные салфетки. Стерильная простыня. Вспомогательные приспособления. Стерильная силиконовая трубка и вакуумный аспиратор или стерильный шприц, или помпа |
Этап выполняется с соблюдением правил асептики |
|
Промыть каналы эндоскопа и область элеватора (для дуоденоскопа) спиртом и продуть их воздухом |
Спирт этиловый или изопропиловый 70%-й, соответствующий фармакопейной статье. Вспомогательные приспособления. Стерильный шприц |
Количество используемого спирта должно соответствовать объему промываемых каналов определенной модели эндоскопа |
Примечания:
1) Способ тестирования на герметичность, оборудование для его проведения и порядок тестирования определены производителем эндоскопа.
2) Способ обеззараживания течеискателя указан в инструкции по его эксплуатации.
3) Вспомогательные приспособления для обработки каналов эндоскопа (приспособления для промывки и заполнения каналов моющим раствором, водой, раствором средства для ДВУ, спиртом и воздухом: ирригатор аспирационного канала и каналов ВВ, адаптер для аспирационной очистки биопсийного канала, промывочные трубки дополнительных каналов) при ручном способе проходят с эндоскопом весь цикл обработки, после чего могут сразу повторно использоваться.
4) После использования щетка многократного применения подвергается ПСО+Д и стерилизации как инструменты к эндоскопам. При использовании щеток однократного применения необходимо следовать указаниям производителя на соответствие диаметрам каналов и порядка проведения очистки.
5) На качество очистки тестируют каждый десятый обрабатываемый эндоскоп, но не менее одного за смену. При постановке азопирамовой пробы необходимо руководствоваться требованиями п. 8.1.3 МУ 3.5.1937—04, «Очистка, дезинфекция и стерилизация эндоскопов и инструментов к ним» (далее – МУ 3.5.1937—04), при использовании других тестов – инструкциями их производителей.
6) Фенолфталеиновая проба ставится при использовании для очистки растворов, имеющих рН 8,5 и выше.
7) При проведении процесса ДВУ (дезинфекционная выдержка, ополаскивание, сушка) можно использовать помпу, которая устанавливается в зоне ДВУ.
8) Химические индикаторы для оценки концентрации ДВ в рабочем растворе ДС используются в соответствии с инструкциями производителя ДС и химических индикаторов
6.1. Использование МДМ является основной мерой по снижению рисков инфицирования пациентов при эндоскопических вмешательствах за счет проведения в замкнутом цикле стандартизированных и валидированных процессов обработки, возможности контроля и документирования критических параметров ДВУ, обеспечения этапов ополаскивания и сушки каналов эндоскопа после ДВУ очищенными на антимикробных фильтрах водой и воздухом в автоматическом режиме.
6.2. Требования к выбору МДМ:
– наличие регистрационного удостоверения;
– совместимость машины с моделями и сериями эндоскопов, которые планируется в ней обрабатывать (проверить по перечню производителя МДМ), что гарантирует наличие оригинальных адаптеров для подключения всех каналов эндоскопа. Если МДМ не имеет адаптеров для подключения дополнительных каналов, они обрабатываются вручную (ОО и ДВУ) до начала цикла в МДМ;
– наличие инструкции пользователя на русском языке, в которой указаны: порядок подключения каналов эндоскопа и проведения теста на герметичность; необходимость (отсутствие необходимости) проведения ОО ручным способом до цикла в МДМ; перечень моющих и дезинфицирующих средств, для которых подтверждена микробиологическая эффективность и безопасность (для материалов эндоскопа); сведения о возможности многократного применения готового средства или рабочего раствора средства для ДВУ, в том числе о методах и средствах контроля длительности его применения (максимальное число циклов и/или дней применения, наличие химических индикаторов к готовому средству/рабочему раствору); порядок проведения самодезинфекции машины;
– наличие возможности проведения самодезинфекции МДМ;
– обеспечение подачи в МДМ воды и воздуха, очищенных на антимикробных фильтрах.
6.3. Перед каждым циклом обработки в МДМ эндоскоп подвергается окончательной очистке ручным способом с использованием щеток, если в инструкции по эксплуатации машины нет других указаний.
6.4. Перед первым вводом в эксплуатацию, после ремонта или длительных (свыше 1 месяца) простоев процесс окончательной очистки в МДМ валидируется с использованием тестов, разрешенных для этих целей на территории Российской Федерации.
6.5. Вспомогательные приспособления, которые использовались перед автоматическим циклом в МДМ для проведения окончательной очистки ручным способом, подлежат дезинфекции в растворе ДС по режиму, эффективному в отношении вирусов, бактерий и грибов рода Candida (в МО туберкулезного профиля – по туберкулоцидному режиму ДС, тестированными на Mycobacterium terrae).
6.6. Эндоскопы для исследования ДП и ЖКТ могут обрабатываться последовательно в одной МДМ при соблюдении следующих условий:
– средства ДВУ относятся к группам химических веществ, регламентированных СП 3.1.3263—15, и рекомендованы производителями в инструкции по эксплуатации МДМ (для них доказана эффективность автоматизированного цикла);
– вышеуказанные средства ДВУ применяются однократно или многократно. При этом МДМ, использующие средства ДВУ многократно, должны быть обеспечены средствами химического контроля концентрации ДВ в готовом средстве/рабочем растворе (химическими индикаторами) и функцией индикации максимального количества циклов обработки/дней применения раствора;
– МДМ имеет оригинальные адаптеры для подключения всех каналов обрабатываемых эндоскопов.
Для обработки бронхоскопов выделяется отдельная МДМ при невозможности выполнения даже одного из вышеперечисленных условий.
Запрещается в одном цикле совместно обрабатывать бронхоскопы и гастроинтестинальные эндоскопы.
6.7. Не допускается использовать для обработки бронхоскопов МДМ без антимикробных фильтров для очистки воды, обеспечивающих задержку микроорганизмов размером более 0,2 мкм.
6.8. Если в МДМ отсутствует опция дополнительной сушки 70%-м этиловым или изопропиловый спиртом, соответствующим фармакопейной статье, этот этап проводится вручную после извлечения эндоскопа из машины.
6.9. Самодезинфекция МДМ проводится в сроки, средством и по режиму, которые указаны в инструкции по эксплуатации машины. При отсутствии таких указаний процедура самодезинфекции проводится при замене раствора средства для ДВУ. Не допускается для этой цели применять отработанный раствор для ДВУ эндоскопов.
VII. Требования к условиям транспортирования и хранения эндоскопов для нестерильных вмешательств
7.1. Эндоскопы транспортируются между помещениями эндоскопического отделения, в ЦСО, другие отделения медицинской организации, а также при оказании медицинской помощи вне медицинской организации, в закрытом виде на лотках или в контейнерах. В качестве упаковки используются полиэтиленовые маркированные (стерильные и нестерильные) вкладыши, тканый и нетканый материал (стерильный, для упаковки обработанных эндоскопов).
7.2. Для предотвращения смешивания потоков чистых и грязных эндоскопов при транспортировании предусматриваются различные варианты маркировки: маркируют лотки, используют цветные полиэтиленовые вкладыши или одноразовые бирки и др.
7.3. После использования лотки обрабатывают способом протирания ДС по режиму, эффективному в отношении вирусов, бактерий и грибов рода Candida (в МО туберкулезного профиля – по туберкулоцидному режиму ДС, тестированными на Mycobacterium terrae).
7.4. Хранение обработанных эндоскопов между сменами осуществляется в разобранном виде, упакованными в стерильный материал или неупакованными в асептических условиях в специализированных (для хранения/хранения и сушки) шкафах, имеющих регистрационное удостоверение. Срок хранения эндоскопов в шкафу для сушки и хранения в асептической среде указывается в инструкции/руководстве по эксплуатации шкафа. Срок хранения эндоскопов, упакованных в стерильные тканевые чехлы, не должен превышать 72 часа. После истечения срока хранения эндоскоп подлежит ДВУ повторно.
7.5. В специализированных шкафах для хранения/хранения и сушки эндоскопов должна обеспечиваться рециркуляция воздуха, обеззараженного ультрафиолетовым излучением и/или антимикробными фильтрами. Съемные детали хранятся в шкафу отдельно от эндоскопа, но их принадлежность определенному изделию должна быть обеспечена.
7.6. После завершения цикла обработки эндоскоп может храниться перед очередным использованием в собранном виде в стерильной упаковке на лотке не более 3 часов. Если в течение указанного времени эндоскоп не использован, он подлежит повторной ДВУ и сушке.
VIII. Требования к обработке инструментов к эндоскопам
8.1. Инструменты к эндоскопам характеризуются сложным строением, в том числе могут иметь колюще-режущие поверхности, в связи с чем представляют угрозу травмирования медицинского персонала на этапах обработки.
8.2. Не допускается одновременная с эндоскопом обработка инструментов в одной емкости/мойке.
8.3. Большинство инструментов, в том числе имеющих каналы, относятся к изделиям однократного применения и не подлежат повторной обработке.
8.4. Содержание и условия эффективного проведения процессов обработки инструментов к эндоскопам ручным способом.
|
Последовательность и содержание этапов процессов ПО, ПСО + Д, стерилизации |
Материально-техническое обеспечение процессов обработки |
Условия эффективного выполнения отдельных этапов и/или всего процесса обработки | ||
|
I. Предварительная очистка Проводится в эндоскопической манипуляционной. Предназначена для удаления массивных загрязнений (до их высыхания) с/из инструмента | ||||
|
Удаление салфеткой (тампоном) крупных загрязнений с инструмента |
СИЗ персонала. Одноразовые чистые салфетки (тампоны) сухие или увлажненные моющим средством. Контейнер с перфорированным поддоном достаточной вместимости для полного погружения инструментов. Целевое моющее (предпочтительно ферментное) средство. Шприц или другое приспособление для промывки каналов |
| ||
|
Полное погружение в емкость с раствором моющего средства. Каналы и полости при их наличии заполняются принудительно |
Минимальное время выдержки в растворе указано в инструкции по применению средства, максимальное – в соответствии с рекомендациями производителя | |||
|
Ополаскивание инструментов под струей воды на перфорированном поддоне (при наличии моечной ванны для инструментов). Транспортирование в ЦСО или моечно-дезинфекционное помещение |
Инструменты транспортируются во влажном состоянии (после ополаскивания) или в растворе (без ополаскивания) | |||
|
II. Предстерилизационная очистка при совмещении с дезинфекцией* Проводится в моечно-дезинфекционном помещении или ЦСО с целью обеззараживания и максимально возможной очистки | ||||
|
Полное погружение в раствор средства. Каналы и внутренние полости (при наличии) в инструментах многократного применения заполняются принудительно. Дезинфекционная выдержка |
Контейнеры с перфорированными поддонами. Ерши, щетки, моющий пистолет с насадками, салфетки. ДС с моющими свойствами в режиме применения «ПСО+Д» для инструментов к эндоскопам. |
Соблюдать режим применения рабочего раствора ДС: концентрацию (при приготовлении раствора использовать мерную емкость), температуру (контролировать термометром), время дезинфекционной выдержки (контролировать таймером) | ||
|
Очистка в том же растворе при помощи салфеток, щеток и ершей |
Водопроводная вода питьевого качества. Дистиллированная вода |
| ||
|
Ополаскивание водопроводной водой, в том числе внутренних полостей и каналов принудительно. Ополаскивание дистиллированной водой |
|
Порции воды для ополаскивания используются строго однократно | ||
|
Сушка при помощи чистых салфеток, воздушного пистолета |
Чистый материал. Воздушный пистолет. Кронштейн или другое приспособление для сушки длинных инструментов |
Длинные изделия перед упаковкой досушивают в расправленном виде на кронштейнах | ||
|
Пробы на качество очистки (азопирамовая, фенолфталеиновая или другие регламентированные для этих целей пробы)** | ||||
|
Функциональные тесты. Смазка. Проводятся для контроля и поддержания функций инструментов | ||||
|
Упаковка перед загрузкой в стерилизатор |
Упаковочные материалы, соответствующие выбранному методу стерилизации |
Для обеспечения сохранности инструмента используются стерилизационные контейнеры, рекомендованные производителями | ||
|
III. Стерилизация Проводится в стерилизационном помещении эндоскопического отделения, ЦСО | ||||
|
В растворе химических средств ручным способом: – полное погружение в раствор стерилизующего средства; – ополаскивание стерильной водой; – сушка стерильным материалом |
Контейнеры стерильные. Стерилизующее средство из групп кислородактивных или альдегидсодержащих химических веществ. Химические индикаторы. Таймер. Термометр. Стерильная вода для ополаскивания. Стерильный материал |
Проводится контроль параметров стерилизации (концентрация и температура раствора, время стерилизационной выдержки). Все действия с инструментом после извлечения из стерилизующего средства проводятся в асептических условиях. Стерильный контейнер и стерильная порция воды для ополаскивания используются однократно | ||
|
В стерилизаторах паровых, газовых (с применением этиленоксида, формальдегида), а также в стерилизаторах с приме- |
Стерилизатор, зарегистрированный в РФ в установленном порядке |
Выбор режима стерилизации из числа предусмотренных программами работы стерилизатора осуществляют с учетом | ||
|
нением паров перекиси водорода (включая плазменные) |
|
рекомендаций производителя конкретного медицинского изделия | ||
|
|
|
|
|
|
* При использовании средств, не обладающих одновременно моющими и дезинфицирующими свойствами, процессы предстерилизационной очистки и дезинфекции проводятся самостоятельно (без совмещения).
** На качество очистки тестируется один из 10, но не менее трех одновременно обрабатываемых инструментов. При постановке азопирамовой пробы необходимо руководствоваться требованиями п. 8.1.3—8.1.4 МУ 3.5.1937—04
8.5. Предстерилизационная очистка в виде самостоятельного процесса и при совмещении с дезинфекцией может проводиться механизированным способом в ультразвуковых установках (УЗУ) средствами, для которых разработан и указан в инструкции соответствующий режим применения.
8.6. Процессы очистки и дезинфекции инструментов механизированным способом в полном объеме могут выполняться в специализированных МДМ. Выбор средств очистки и дезинфекции определяется исходя из требований настоящих МУ, рекомендаций производителей инструментов и МДМ.
8.7. Последовательность обработки чрезпищеводных ультразвуковых датчиков представлена в прилож. 2.
9.1. Обработку эндоскопов проводит специально выделенный медицинский персонал, прошедший обучение в соответствии с п. 3.4 СП 3.1.3263—15.
9.2. В медицинской организации должна быть создана система непрерывного обучения медицинского персонала, занимающегося обработкой эндоскопов. Формы обучения представлены в прилож. 3.
9.3. Медицинская организация, в которой выполняются нестерильные эндоскопические вмешательства, должна быть оснащена необходимым количеством эндоскопов и инструментов к ним, оборудованием для очистки и хранения эндоскопов, средствами очистки, дезинфекции и ДВУ из регламентированных СП 3.1.3263—15 групп химических веществ и рекомендованных фирмами-производителями медицинских изделий, другими расходными материалами.
9.3.1. Необходимое количество эндоскопов в условиях конкретной МО определяется исходя из рабочей нагрузки, суммарного времени проведения эндоскопического вмешательства и полного цикла обработки эндоскопа, проводимого в соответствии с требованиями СП 3.1.3263—15 и настоящих МУ. Формула расчета потребности в эндоскопах приведена в прилож. 4.
9.3.2. При большой нагрузке (одновременно обрабатываются три и более эндоскопов одного вида) использование МДМ является обязательным.
9.4. Каждому эндоскопу должен быть присвоен индивидуальный код, который содержит сведения о его модели и серийном номере. Код указывается в графе особые отметки журнала регистрации исследований, выполняемых в отделе, отделении, кабинете эндоскопии, в журнале контроля обработки эндоскопов для нестерильных вмешательств, в протоколе эндоскопического исследования.
9.5. В эндоскопическом отделении ведутся все формы журналов в соответствии с требованиями действующего санитарного законодательства и локальные формы учета, принятые в МО.
9.6. В журнале контроля обработки эндоскопов для нестерильных вмешательств заполняются графы в соответствии с применяемым способом обработки (ручной, механизированный). Объединенные по датам распечатки протоколов, содержащих информацию о параметрах цикла в МДМ, хранятся в отдельной папке. Срок хранения журналов и распечаток 1 год.
9.7. Руководителем (врачом) эндоскопического отделения/кабинета, разрабатывается рабочая инструкция по обработке эндоскопов, имеющихся на оснащении эндоскопического отделения (кабинета), которая утверждается руководителем медицинской организации (прилож. 5).
10.1. Контроль качества обработки эндоскопов проводится микробиологическим методом.
10.2. Плановый отбор проб смывов осуществляется с/из полностью обработанного и просушенного эндоскопа ежеквартально. Пробы отбираются лаборантом или врачом-микробиологом при помощи медицинской сестры отделения. Контролю подлежат: биопсийный канал, вводимая трубка, клапаны и гнезда клапанов.
10.2.1. Отбор смывов с наружной поверхности вводимой трубки эндоскопа осуществляют стерильными тампонами, смоченными в стерильной дистиллированной воде по стандартной методике.
Смывы со всех поверхностей каждого клапана (наружные поверхности, поверхности полых пространств и сквозных отверстий) отбирают одним тампоном. Смывы с поверхностей гнезда клапана отбирают при круговом движении тампона с захватом всей поверхности цилиндра.
10.2.2. Тампоны помещаются в пробирки с мясо-пептонным бульоном (МПБ) и транспортируются в микробиологическую лабораторию с соблюдением требований п. 4 МУ 4.2.2039—05 «Техника сбора и транспортирования биоматериалов в микробиологические лаборатории» (далее – МУ 4.2.2039—05).
Перед высевом пробирки встряхивают вручную или помещают на шейкер. Затем по 0,2 мл МПБ засевают газоном на поверхности плотных питательных сред (желточно-солевая среда, кровяной агар, среда Эндо или аналог, агар с бриллиановым зеленым или аналог, среда Сабуро). Посевы термостатируют при температуре 37 °С в течение 48 часов (для среды Сабуро – при 28 °С 5 суток), после чего учитывают результаты.
10.2.3. Биопсийный канал промывают при помощи стерильного шприца 10 мл стерильной дистиллированной воды, которую собирают в стерильный контейнер. Для выделения микроорганизмов смывную жидкость с биопсийного канала пропускают через мембранный фильтр, который в асептических условиях переносят на поверхность плотной питательной среды (мясо-пептонный агар/кровяной агар/среда Мюллера-Хинтона). При отсутствии фильтрующего устройства смывную жидкость по 0,2 мл засевают на поверхности питательной среды (желточно-солевая среда, кровяной агар, среда Эндо или аналогичная, агар с бриллиантовым зеленым или аналог, среда Сабуро). Посевы термостатируют при температуре 37 °С в течение 48 часов (для среды Сабуро – при 28 °С 5 суток), после чего учитывают результаты. Количественную оценку обсемененности биопсийного канала (общее микробное число) проводят по количеству колониеобразующих единиц (КОЕ) в 1 мл смывной жидкости.
10.3. Выделение и идентификация микроорганизмов, указанных в п. 10.4 проводятся в соответствии с МУК 4.2.2942—11 «Методы санитарно-бактериологических исследований объектов окружающей среды, воздуха и контроля стерильности в лечебных организациях» (далее – МУ 4.2.2942—11).
10.4. Критерием эффективности полного цикла обработки эндоскопа является отсутствие роста бактерий группы кишечной палочки, золотистого стафилококка, синегнойной палочки, плесневых и дрожжевых грибов, а также других условно-патогенных и патогенных микроорганизмов. При этом условии показатель общей микробной обсемененности биопсийного канала эндоскопа должен быть менее 100 КОЕ/мл.
10.5. При выявлении микроорганизмов, указанных в п. 10.4 или обсемененности биопсийного канала микроорганизмами в количестве ³ 100 КОЕ/мл, обработка признается неудовлетворительной. Эндоскоп подвергается полному циклу обработки и контрольному отбору проб. При повторном неудовлетворительном результате микробиологических исследований и отсутствии выявленных нарушений в технологии обработки эндоскопа рекомендуется обратиться в сервисный центр для тестирования его технической исправности.
10.6. Внеплановый микробиологический контроль качества обработки эндоскопа проводится по эпидемическим показаниям. Порядок проведения расширенных внеплановых микробиологических исследований на качество обработки эндоскопов по эпидемиологическим показаниям представлен в прилож. 6.
10.7. Микробиологический контроль качества самодезинфекции МДМ проводится не реже одного раза в полгода. Смывы с различных участков машины (ванна, трубки подачи воды и воздуха, штуцеры) отбираются тампонами, смоченными стерильной дистиллированной водой, непосредственно после завершения цикла самодезинфекции. Транспортирование проб смывов и идентификация микроорганизмов проводятся в соответствии с п. 10.2.2 настоящих МУ. Критерий эффективности – отсутствие роста вегетативных форм микроорганизмов в исследуемых образцах смывов.
10.8. Инструменты к эндоскопам, подлежащие контролю на стерильность, направляют в микробиологическую лабораторию в упаковке, в которой осуществляли их стерилизацию. Отбор проб проводят в соответствии с требованиями МУ 3.5.1937—04. Проведение микробиологических исследований проводится в соответствии с МУК 4.2.2942—11. Критерий эффективности стерилизации – отсутствие роста микроорганизмов.
XI. Требования к проведению профилактической дезинфекции в эндоскопическом отделении/кабинете
11.1. Уборка и профилактическая дезинфекция в манипуляционных для нестерильных эндоскопических вмешательств и в моечно-дезинфекционном помещении должны проводиться по мере загрязнения, но не реже одного раза в смену или 2 раза в день. В медицинской организации общесоматического профиля для этой цели применяют ДС по режиму, обеспечивающему гибель вирусов, бактерий и грибов рода Candida; в МО туберкулезного профиля – по режиму, обеспечивающему гибель микобактерий, в прочих инфекционных стационарах – по режиму, обеспечивающему гибель наиболее устойчивого возбудителя (вирусов, микобактерий туберкулеза или других микроорганизмов в соответствии с профилем стационара).
11.2. В эндоскопической манипуляционной после каждого пациента поверхности кушетки (стола) для исследований и дополнительного эндоскопического оборудования, с которыми он контактировал, должны подвергаться обеззараживанию средствами с короткой дезинфекционной выдержкой. Для каждого пациента кушетка/стол застилается чистой простыней.
11.3. Моечные ванны подвергаются дезинфекции способом протирания, а вспомогательные приспособления для обработки каналов эндоскопов – дезинфекции способом погружения после завершения процесса окончательной очистки (без совмещения с дезинфекцией) каждого эндоскопа.
11.4. Обращение с медицинскими отходами, образующимися при проведении эндоскопических вмешательств, обработке эндоскопов и инструментов к ним осуществляется в соответствии с требованиями СанПиН 2.1.7.2790—10 «Санитарно-эпидемиологические требования к обращению с медицинскими отходами»[2].
11.5. В конце рабочей смены в моечно-дезинфекционном помещении дезинфекции подлежат:
– все емкости и моечные ванны для окончательной и предстерилизационной очистки, ополаскивания эндоскопов после ДВУ, раковины для мытья рук медицинского персонала, все горизонтальные поверхности;
– аспирационная банка и соединительные трубки. Аспирационная банка дезинфицируется при полном погружении в раствор средства, не обладающего фиксирующими биологические загрязнения свойствами, затем очищается при помощи ершей и щеток. Очистку и дезинфекцию трубок рекомендуется проводить в МДМ в ЦСО. При отсутствии МДМ обработка трубок проводится ручным способом в растворе кислородактивных средств с использованием приспособлений для прокачивания растворов (например, помпы, шприца и др.). Обработка завершается проверкой трубок на целостность и сушкой с использованием чистого материала, помпы или воздушного пистолета;
– емкость (контейнер, банка) для воды, предназначенной для очистки линз, крышка и соединительные трубки к ней подлежат очистке, сушке и стерилизации в конце рабочей смены. Крышка и соединительные трубки очищаются с использованием ершей и щеток, после чего тщательно высушиваются, упаковываются и подвергаются стерилизации. Перед началом эндоскопических исследований стерильная банка заполняется стерильной водой;
– водно-воздушный контур помпы, используемой в процессе окончательной очистки, дезинфицируется способом непрерывной прокачки раствора ДС, примененного по режиму, обеспечивающему гибель вирусов, бактерий и грибов рода Candida (в МО туберкулезного профиля – по режиму, обеспечивающему гибель микобактерий), затем промывается водой в течение времени, указанного в инструкции на примененное средство, и продувается воздухом.
В эндоскопическом отделении/кабинете должны быть разработаны процедуры внутреннего контроля качества обработки эндоскопов. Они включают:
– периодические (ежемесячные) визуальные проверки процесса ОО/ОО+Д со стороны лица, ответственного за организацию и проведение противоэпидемических мероприятий, в том числе за качество обработки эндоскопического оборудования (п. 3.2 СП 3.1.3263—15);
– еженедельный контроль со стороны старшей медицинской сестры с занесением в журнал контроля обработки эндоскопов для нестерильных вмешательств результатов контроля:
◦ качества очистки эндоскопов с использованием регламентированных для этих целей тестов;
◦ концентрации ДВ в рабочем растворе средства ДВУ многократного применения с использованием химических индикаторов;
– микробиологический контроль качества полного цикла обработки эндоскопов (ежеквартально) и качества самодезинфекции МДМ
(2 раза в год). Исследования проводятся в бактериологической лаборатории МО или по договору в испытательном лабораторном центре (ИЛЦ), аккредитованном на проведение таких исследований;
– разработку и внедрение графика профилактического и технического обслуживания эндоскопов;
– составление графика обслуживания МДМ (замена фильтров воды, воздуха и валидация качества очистки эндоскопов);
– документирование каждого цикла обработки эндоскопа с указанием его идентификационного кода, проведенных этапов обработки и их параметров (ведение журнала контроля обработки эндоскопов для нестерильных вмешательств);
– контроль соблюдения персоналом эндоскопического отделения/кабинета правил гигиены рук, использования нестерильных/стерильных перчаток, прочих СИЗ старшей медицинской сестрой отделения или лицом, ответственным за данный раздел работы в ЛПО;
– контроль владения персоналом техническими приемами предотвращения образования микробных аэрозолей при очистке эндоскопов, процедурами безопасного обращения с колюще-режущими инструментами, медицинскими отходами старшей медицинской сестрой отделения или лицом, ответственным за данный раздел работы в ЛПО;
– контроль готовности персонала к ликвидации аварийных ситуаций (разлив химических средств или биологических жидкостей, попадание биологических жидкостей на тело, травмы нестерильным инструментом) со стороны лица, ответственного за данный раздел работы в ЛПО;
– контроль со стороны лица, ответственного за данный раздел работы в ЛПО, полноты выявления, учета и регистрации, информирования администрации, органов и организаций Роспотребнадзора о случае инфицирования пациента, предположительно связанного с эндоскопическим вмешательством, контроль ведения журнала учета инфекционных заболеваний.
Приложение 1
Перечень основных нестерильных эндоскопических вмешательств
Бронхоскопия
Интестиноскопия
Капсульная эндоскопия
Колоноскопия
Ларингоскопия
Отоскопия
Ректоскопия
Ретроградная холедохоскопия, вирсунгоскопия
Риноскопия
Сиалоскопия
Сигмоидоскопия
Трахеоскопия
Эзофагогастродуоденоскопия
Эзофагогастроскопия
Эзофагоскопия
Эндоскопическая ультрасонография
ЭРХПГ и другие рентгенэндоскопические манипуляции
Приложение 2
Алгоритм обработки ультразвуковых чрезпищеводных датчиков
|
Процесс/этапы |
Ручной способ |
Механизированный
|
|
ПО |
Очистить салфеткой, смоченной в моющем средстве, вводимую часть датчика, удалить передающий гель. Отключить датчик от системы и снять все принадлежности, подключенные к датчику или надетые на него. Протереть датчик сухой салфеткой | |
|
ОО/ОО+Д |
Погрузить датчик до метки, установленной производителем, в раствор моющего/ДС на время, указанное в инструкции на средство. Использовать салфетку для очистки. Ополоснуть в воде питьевого качества. Высушить чистой салфеткой |
Использовать МДМ, рекомендованные производителем. Обеспечить погружение датчика до отметки производителя. Выполнить полный цикл, включающий ОО и ДВУ |
|
ДВУ |
Погрузить датчик до метки, установленной производителем, в раствор средства для ДВУ на время дезинфекционной выдержки. Ополоснуть в воде не ниже питьевого качества, высушить стерильным материалом |
|
|
Хранение |
В асептической среде | |
Примечание. Непогружаемые части датчика должны оставаться сухими, для чего необходимо держать их выше частей, которые подвергаются погружению в раствор химического средства и ополаскиванию в воде.
Приложение 3
|
Форма
|
Содержание
|
Кто проводит |
Подтверждение компетенции |
Форма документации |
|
Первичное обучение на рабочем месте при поступлении на работу |
Конструктивные особенности и технология обработки имеющихся моделей эндоскопов, ведение документации |
Заведующий отделением, старшая медицинская сестра, эпидемиолог МО |
Тестирование на рабочем месте, визуальный контроль |
Журнал обучения персонала |
|
Обучение процедурам обработки новых моделей эндоскопов |
Особенности строения новой модели эндоскопа, изучение инструкции производителя по ее обработке |
Заведующий отделением, старшая медицинская сестра, представитель фирмы производителя |
Визуальный контроль |
Составление алгоритма обработки модели эндоскопа.
|
|
Обучение процедурам механизированного способа обработки эндоскопа при введении в эксплуатацию новой МДМ |
Изучение инструкции по эксплуатации МДМ, выбор приемлемого цикла, средств очистки и дезинфекции, валидация очистки |
Заведующий отделением, старшая медицинская сестра, технический персонал фирмы производителя |
Тестирование на рабочем месте |
Составление алгоритма обработки эндоскопов механизированным способом. Отметка в журнале обучения персонала |
|
Раз в 5 лет повышение квалификации по программам дополнительного профессионального образования по вопросам эпидемиологической безопасности эндоскопических вмешательств |
Организация и функционирование системы эпидемиологической безопасности эндоскопических вмешательств в МО |
Организации, имеющие лицензию на образовательную деятельность |
Тестирование |
Удостоверение о повышении квалификации установленного образца |
Приложение 4
Ориентировочное количество эндоскопов каждой модели (гастроскопов, колоноскопов, бронхоскопов, дуоденоскопов и др.) для выполнения планируемого числа вмешательств можно рассчитать по формуле:
h = n × (a + b) : c, где
a – среднее значение длительности полного цикла обработки эндоскопа определенной модели, мин;
b – средняя продолжительность вмешательства, выполняемого эндоскопами данной модели, мин;
c – продолжительность рабочей смены, в течение которой выполняются эндоскопические вмешательства данной моделью эндоскопов, мин;
n – планируемое или реально выполняемое число вмешательств данной моделью эндоскопов, абс. ед.
Значения a и b определяются путем хронометража длительности нескольких циклов обработки эндоскопов каждой модели эндоскопа или эндоскопических вмешательств, проводимых с их использованием, соответственно. Полученное значение h округляется до целого значения в большую сторону.
Приложение 5
Рекомендуемое содержание рабочей инструкции
по обработке эндоскопов
1. Свод нормативных правовых, методических и инструктивных документов, на основании которых разработана инструкция и сами документы, в виде приложений, журналов ведения учета.
2. Список сотрудников, допущенных к обработке эндоскопов, с указанием форм и дат проведения обучения.
3. Перечень эндоскопов с указанием их идентификационных кодов, дат ввода в эксплуатацию, технического состояния, дат технических неисправностей.
4. Перечень оборудования для обработки и хранения эндоскопов (МДМ, полуавтоматы или помпы, шкафы) с указанием даты ввода в эксплуатацию, технического состояния, дат технических неисправностей.
5. Перечень и потребность (месячная) в расходных материалах, необходимых для проведения обработки эндоскопов (фильтры для очистки воды, воздуха, 70%-й этиловый или изопропиловый спирт, соответствующий фармакопейной статье, средства очистки, дезинфекции и стерилизации, стерильный и нестерильный материал, перчатки и др).
6. Перечень средств для обработки рук с указанием вида, назначения и количества с расчетом потребности.
7. Описание технологического процесса (алгоритм) обработки разных моделей эндоскопов, имеющих отличия в приемах предварительной, окончательной очистки, порядке тестирования на герметичность, заполнении и промывки каналов.
Алгоритм обработки видеогастроскопа с дополнительным каналом
для подачи воды (пример)
I. Предварительная очистка
1. Выключить видеоинформационный центр и источник света, подготовить обработанные емкости с моющим средством и водой объемом по 500 мл.
2. Аспирировать содержимое вводимой трубки 7—10 с.
3. Протереть вводимую трубку эндоскопа от ограничителя на блоке управления салфеткой, смоченной в растворе средства для предварительной очистки (указать наименование салфетки, импрегнированной ДС, или концентрацию применяемого средства).
4. Включить аспиратор, закрыть колпачок на клапане для биопсии.
5. Промыть систему каналов БА раствором средства для предварительной очистки (указать наименование и концентрацию применяемого средства). Чередовать аспирацию раствора (не менее 150—200 мл) с аспирацией воздуха.
6. Заменить клапан подачи ВВ на адаптер клапана для очистки системы каналов ВВ.
7. Промыть систему ВВ, чередуя аспирацию воды и воздуха.
8. Промыть дополнительный канал для подачи воды через промывочную трубку, которую присоединить ко входу в канал, отсоединив предварительно колпачок. Погрузить дистальный конец вводимой трубки эндоскопа в чистую воду. Шприцем емкостью _____ см3 (указать объем) несколько раз (не менее 3) последовательно ввести моющий раствор и воздух в канал пока из его отверстия на дистальном конце не прекратится выделение пузырьков воздуха.
9. Отсоединить от эндоскопа клапаны, промывочную трубку, отключить эндоскоп от источника света и электроотсоса.
10. Надеть защитный видеоколпачок.
11. Транспортировать эндоскоп в моечное помещение в упакованном виде на лотке.
Тест на герметичность
Заполнить моечную ванну чистой водой до отметки 10 л.
Вставить разъем течеискателя в выходной разъем блока для технического обслуживания, а соединительный колпачок присоединить к вентиляционному адаптеру водозащитного колпачка. Подать воздух. Погрузить эндоскоп в воду и наблюдать в течение не менее 30 с за всей поверхностью эндоскопа. Появление единичных или дорожки пузырьков воздуха говорит о негерметичности эндоскопа. Извлечь эндоскоп из ванны, выключить блок технического обслуживания и через 30 с отсоединить колпачок коннектора течеискателя от выпускного коннектора эндоскопа.
II. Окончательная очистка
1. Погрузить в свежий раствор средства для окончательной очистки (указать наименование, концентрацию применяемого средства) эндоскоп и клапаны (сделать ими в растворе несколько рабочих движений), присоединить вспомогательные приспособления для очистки (всеканальный ирригатор и промывочная трубка) и заполнить через них каналы при помощи шприца. Отсоединить вспомогательные приспособления и выдержать эндоскоп и клапаны в растворе в течение ___ мин (указать время выдержки в растворе).
2. Протереть все внешние поверхности эндоскопа чистой безворсовой салфеткой.
3. Провести очистку салфеткой и малой щеткой поверхностей торцевой части эндоскопа, в том числе оптики.
4. Прочистить соответствующей щеткой систему БА. Выпрямить подвижную часть эндоскопа. Щетку вводить через гнезда биопсийного и аспирационного клапанов (под углом 90° и 45° соответственно). После каждого выхода из дистального конца вводимой трубки щетку очищать. Процедуру проводить до чистой щетки (не менее 3 проходов) при полном погружении эндоскопа.
5. Очистить щеткой аспирационный клапан, клапан и адаптер клапана ВВ, биопсийный клапан при их полном погружении в раствор моющего средства.
6. Очистить щеткой гнезда клапанов при полном погружении эндоскопа в раствор моющего средства.
7. Надеть вспомогательные приспособления для очистки, в том числе промывочную трубку дополнительного канала для подачи воды. Промыть систему каналов БА, ВВ, дополнительный канал подачи воды раствором средства для окончательной очистки (не менее 90 мл для каждого) и продуть воздухом.
8. Слить моющий раствор и налить в моечную ванну воду питьевого качества.
9. Ополоснуть наружные поверхности эндоскопа, клапаны (сделать ими в воде несколько рабочих движений), промыть водой через вспомогательные приспособления все каналы, в том числе для подачи воды (не менее 90 мл воды для каждого).
10. Воду слить, наружные поверхности просушить салфетками, каналы продуть воздухом через вспомогательные приспособления, закрыв чистыми салфетками выходы каналов на дистальном конце и блоке управления.
11. При необходимости (в соответствии с ссылкой 5) раздела V настоящих МУ) провести азопирамовую пробу на качество очистки биопсийного канала и наружной оболочки, после чего протереть ее салфеткой, смоченной водой питьевого качества и промыть биопсийный канал 20—30 мл воды питьевого качества (1 объем шприца).
III. ДВУ
1. Погрузить эндоскоп и все съемные элементы в емкость с раствором средства для ДВУ (указать конкретное применяемое средство, концентрацию – в случае приготовления раствора из концентрата).
2. Заполнить раствором при помощи шприца через вспомогательные приспособления все каналы, отсоединить их и погрузить в раствор вместе с эндоскопом, убрать пузыри воздуха с внешних поверхностей эндоскопа и вспомогательных приспособлений салфеткой. Использованный шприц удалить как медицинские отходы класса Б.
3. Выдержать эндоскоп, клапаны и вспомогательные приспособления в растворе ДВУ в течение __ мин (указать время дезинфекционной выдержки).
4. Надеть стерильные перчатки. Присоединить вспомогательные приспособления к эндоскопу. Стерильным шприцем выдуть раствор из каналов.
5. Вынуть эндоскоп из раствора и переложить в моечную ванну, заполненную свежей порцией воды питьевого качества.
6. Промыть все каналы водой (не менее 90 мл для каждого) через вспомогательные приспособления. Процедуру закончить продувкой воздухом.
7. Отсоединить вспомогательные приспособления, ополоснуть, слить из них воду и выложить на стерильную простыню.
8. Ополоснуть водой наружные поверхности эндоскопа при помощи салфетки, клапаны (сделать в воде несколько рабочих движений). Выложить на стерильную простыню.
9. Просушить поверхность эндоскопа и клапанов стерильными салфетками.
10. Присоединить вспомогательные приспособления и продуть через них каналы.
11. Присоединить стерильный шприц к порту аспирационного канала всеканального ирригатора и промыть систему каналов БА ___ мл (указать необходимое количество) 70%-го ______ (этилового/изопропилового, указать) спирта, затем присоединить шприц к порту ВВ канала ирригатора и промыть систему каналов ВВ ____ мл 70%-го ______ (этилового/изопропилового, указать). Продуть каналы воздухом.
12. Повесить эндоскоп в шкаф для сушки и хранения в асептической среде, съемные детали выложить на сетку шкафа, соответствующую номеру кронштейна для эндоскопа.
Приложение 6
Данная методика применяется при выявлении случая инфицирования пациента предположительно связанного с эндоскопическим вмешательством. Как правило, возбудитель известен и задача микробиологических исследований состоит в подтверждении или отрицании его передачи через эндоскоп.
Отбор проб осуществляют лаборант или врач-микробиолог при участии медицинской сестры эндоскопического отделения/кабинета под контролем лица, ответственного за проведение эпидемиологического расследования.
Пробы отбираются с/из эндоскопа, который рассматривается в качестве предполагаемого фактора передачи возбудителя инфекции. Данный эндоскоп выявляется при анализе и сопоставлении сведений журнала контроля обработки эндоскопов для нестерильных вмешательств, журнала регистрации исследований, выполняемых в отделе (отделении, кабинете) эндоскопии, и протокола эндоскопического исследования пострадавшего пациента.
Исследованию подвергают образцы смывов, отобранных через систему каналов БА, ВВ, с элеваторного канала (у дуоденоскопов), гнезд клапанов, клапанов, механизма элеватора (у дуоденоскопов) или с торцевой части дистальной области вводимой трубки.
Материалы
1. Стерильные шприцы: 20 (30) см3 – 3 шт.
2. Стерильные контейнеры для отбора проб с каналов (по числу исследуемых каналов) и механизма элеватора.
3. Стерильный нейтрализатор, приготовленный на дистиллированной воде и соответствующий применяемому средству ДВУ (1,0%-й тиосульфат натрия для кислородактивных ДС и универсальный нейтрализатор для альдегидсодержащих ДС), в количестве: два объема по 20 мл для каждой системы каналов эндоскопа, 10 мл для элеваторного канала и 50 мл для отбора проб с элеватора дуоденоскопа, 10 мл для смачивания тампонов.
4. Мясо-пептонный бульон в пробирках по 2 мл (по количеству планируемых мест для отбора смывов).
5. Стерильные адаптеры, рекомендованные производителем эндоскопа, для промывки каждой из исследуемых систем каналов и элеваторного канала (стерилизуются паром под давлением в щадящем режиме).
6. Чашки Петри с селективной плотной питательной средой.
7. Стерильные тампоны для отбора проб смывов с гнезд клапанов, клапанов, наружной оболочки эндоскопа и торцевой части дистальной области вводимой трубки.
8. Стерильные щетки для очистки элеватора дуоденоскопа, рекомендованные производителем эндоскопа.
Методика отбора проб с системы каналов БА
1. Набрать в стерильный шприц 10 мл стерильного нейтрализатора.
2. Присоединить шприц с помощью стерильной промывочной трубки к штуцеру системы каналов БА, расположенному на блоке присоединения внешних устройств (коннекторный блок).
3. Нажать клапан аспирации и пропустить по каналу 10 мл стерильного нейтрализатора.
4. Собрать смывную жидкость на дистальном конце эндоскопа в стерильный контейнер.
5. Используемый шприц наполнить воздухом и выдуть в контейнер остатки жидкости из каналов.
6. Закрыть контейнер, промаркировать и транспортировать в лабораторию с соблюдением требований п. 4 МУ 4.2.2039—05.
Отбор проб из каналов ВВ осуществляется аналогичным образом. Промывочная трубка крепится к штуцеру для присоединения внешних устройств на коннекторном блоке. Промывка осуществляется при нажатом клапане ВВ.
При исследовании элеваторного канала объем пропускаемой жидкости должен быть 5,0 мл. Промывочную трубку крепят к штуцеру на блоке управления.
Смывы со всех поверхностей каждого клапана (наружные поверхности, поверхности полых пространств и сквозных отверстий) отбираются одним тампоном. Смывы с поверхностей гнезда клапана отбираются при круговом движении тампона с захватом всей поверхности цилиндра. Тампоны смачивают в растворе нейтрализатора и после использования помещают в пробирку с МПБ.
При расследовании случая инфицирования пациента, предположительно связанного с ЭРХПГ, проводят микробиологическое исследование
образцов смывов с механизма элеватора. Дистальный конец дуоденоскопа помещают в стерильный контейнер с фиксированным количеством стерильного нейтрализатора и при полном погружении маленькой стерильной щеткой, рекомендованной производителем, очищают элеватор при разных его положениях. Щетку выполаскивают в растворе и извлекают из контейнера.
Проведение микробиологического исследования смывов с каналов эндоскопов и механизма элеватора
1. Пробу смывной жидкости пропускают через мембранный фильтр, который помещают в чашку Петри на плотную селективную питательную среду для выделения возбудителя зарегистрированного инфекционного заболевания. При отсутствии мембранных фильтров на плотную селективную среду делают высев 0,2 мл смывной жидкости.
2. Инкубируют чашки при 37 °С 48 часов, после чего учитывают результаты.
3. Проводят видовую идентификацию микроорганизма с определением антибиотикограммы в соответствии с действующими нормативным документами.
Проведение микробиологического исследования смывов с клапанов, гнезд клапанов
Отбор проб с клапанов, гнезд клапанов и торцевой оптики, проведение микробиологического исследования проводят по методике, указанной в п. 10.2.1, 10.2.2 настоящих МУ.
Для доказательства идентичности бактерий одного вида, выделенных из клинического материала и проб с эндоскопа, при наличии возможности, проводят молекулярно-генетические исследования.
[1] Утверждены Постановлением Главного государственного санитарного врача Российской Федерации от 08.06.2015 № 20; зарегистрированы в Минюсте России 21 июля 2015 г., регистрационный номер 38110.
[2] Утверждены Постановлением Главного государственного санитарного врача Российской Федерации от 09.12.2010 № 163, зарегистрированы в Минюсте России 17 февраля 2011 г., регистрационный номер 19871.
Обсуждение этой статьи на форуме для специалистов по ссылке
Рекомендуемые статьи
Гематохезия
наличие неизмененной крови в стуле
При эндоскопическом исследовании в случае бронхоэктазов в стадии ремиссии выявляется
частично диффузный бронхит I степени воспаления
Активируйте PUSH уведомления в браузер
Отключите PUSH уведомления в браузер
Содержание
Интернет магазин
Популярное
- О нас
- Правовые вопросы
- Политика
обработки персональных
данных EndoExpert.ru - Связаться с нами
- Стать партнером
© 2016-2022 EndoExpert.ru

Вы находитесь в разделе предназначенном только для специалистов (раздел для пациентов по ссылке). Пожалуйста, внимательно прочитайте полные условия использования и подтвердите, что Вы являетесь медицинским или фармацевтическим работником или студентом медицинского образовательного учреждения и подтверждаете своё понимание и согласие с тем, что применение рецептурных препаратов, обращение за той или иной медицинской услугой, равно как и ее выполнение, использование медицинских изделий, выбор метода профилактики, диагностики, лечения, медицинской реабилитации, равно как и их применение, возможны только после предварительной консультации со специалистом. Мы используем файлы cookie, чтобы предложить Вам лучший опыт взаимодействия. Файлы cookie позволяют адаптировать веб-сайты к вашим интересам и предпочтениям.
Я прочитал и настоящим принимаю вышеизложенное, хочу продолжить ознакомление с размещенной на данном сайте информацией для специалистов.











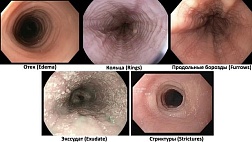




.jpg)




.png)















Комментарии