- Компании
- Takeda. О компании, буклеты, каталоги, контакты
- Olympus. О компании, буклеты, каталоги, контакты
- Boston Scientific. О компании, буклеты, каталоги, контакты
- Pentax. О компании, буклеты, каталоги, контакты
- Fujifilm & R-Farm. О компании, буклеты, каталоги, контакты
- Erbe. О компании, буклеты, каталоги, контакты
- Еще каталоги
- Мероприятия
- Информация
- Обучение
- Классификации
- Атлас
- Quiz
- Разделы
- Пациенту
QR-код этой страницы
Для продолжения изучения на мобильном устройстве ПРОСКАНИРУЙТЕ QR-код с помощью спец. программы или фотокамеры мобильного устройства
Документы и приказы: Цитомегаловирусная инфекция (ЦМВИ) у взрослых. Клинические рекомендации 2025 - 2027
Анонс:

Полный текст статьи:
Министерство
Здравоохранения
Российской Федерации
Клинические рекомендации Цитомегаловирусная инфекция (ЦМВИ) у взрослых
Кодирование по Международной статистической классификации болезней и проблем, связанных со здоровьем: B25
Год утверждения (частота пересмотра): 2025 Пересмотр не позднее: 2027
ID: 1009_1
Возрастная категория: Взрослые
Специальность:
Разработчик клинической рекомендации Российское общество акушеров-гинекологов, Национальная ассоциация специалистов по инфекционным болезням имени академика В. И. Покровского (НАСИБ)
Одобрено Научно-практическим Советом Минздрава России
Оглавление
· Список сокращений
· Термины и определения
· 1. Краткая информация по заболеванию или состоянию (группы заболеваний или состояний)
· 1.1 Определение заболевания или состояния (группы заболеваний или состояний)
· 1.2 Этиология и патогенез заболевания или состояния (группы заболеваний или состояний)
· 1.3 Эпидемиология заболевания или состояния (группы заболеваний или состояний)
· 1.4 Особенности кодирования заболевания или состояния (группы заболеваний или состояний) по Международной статистической классификации болезней и проблем, связанных со здоровьем
· 1.5 Классификация заболевания или состояния (группы заболеваний или состояний)
· 1.6 Клиническая картина заболевания или состояния (группы заболеваний или состояний)
· 2. Диагностика заболевания или состояния (группы заболеваний или состояний) медицинские показания и противопоказания к применению методов диагностики
· 2.1 Жалобы и анамнез
· 2.2 Физикальное обследование
· 2.3 Лабораторные диагностические исследования
· 2.4 Инструментальные диагностические исследования
· 2.5 Иные диагностические исследования
· 3. Лечение, включая медикаментозную и немедикаментозную терапии, диетотерапию, обезболивание, медицинские показания и противопоказания к применению методов лечения
· 4. Медицинская реабилитация и санаторно-курортное лечение, медицинские показания и противопоказания к применению методов медицинской реабилитации, в том числе основанных на использовании природных лечебных факторов
· 5. Профилактика и диспансерное наблюдение, медицинские показания и противопоказания к применению методов профилактики
· 6. Организация оказания медицинской помощи
· 7. Дополнительная информация (в том числе факторы, влияющие на исход заболевания или состояния)
· Критерии оценки качества медицинской помощи
· Список литературы
· Приложение А1. Состав рабочей группы по разработке и пересмотру клинических рекомендаций
· Приложение А2. Методология разработки клинических рекомендаций
· Приложение А3. Справочные материалы, включая соответствие показаний к применению и противопоказаний, способов применения и доз лекарственных препаратов, инструкции по применению лекарственного препарата
· Приложение Б. Алгоритмы действий врача
· Приложение В. Информация для пациента
· Приложение Г1-ГN. Шкалы оценки, вопросники и другие оценочные инструменты состояния пациента, приведенные в клинических рекомендациях
Список сокращений
АлАТ – аланинаминотрансфераза
АсАТ – аспартатаминотрансфераза
ВГН – верхняя граница нормы
ВИЧ – вирус иммунодефицита человека
ВУИ – внутриутробная инфекция
ГГТП – гаммаглютамилтранспептидаза
Д.м.н. – доктор медицинских наук
ДНК – дезоксирибонуклеиновая кислота
ИБ – иммуноблот
ИФА – иммуноферментный анализ
К.м.н. – кандидат медицинских наук
КТ – компьютерная томография
МКБ-10 – международная статистическая классификация болезней и проблем, связанных со здоровьем 10-го пересмотра
МЗ РФ – Министерство здравоохранения Российской Федерации
МРТ – магнитно-резонансная томография
НГН – нижняя граница нормы
ННОИ – Некоммерческое партнерство «Национальное научное общество инфекционистов»
П/к – подкожное введение
ПЦР – полимеразная цепная реакция
РИФ – реакция иммунофлюоресценции
РКИ – рандомизированное контролируемое исследование
РНК – рибонуклеиновая кислота
РФ – Российская Федерация
СОЭ – скорость оседания эритроцитов
ЩФ – щелочная фосфатаза
ЦМВ – цитомегаловирус
ЦМВИ – цитомегаловирусная инфекция
УЗИ – ультразвуковое исследование
IgG – иммуноглобулин G
IgМ – иммуноглобулин М
Термины и определения
Активная ЦМВ инфекция – состояние, при котором цитомегаловирус активно размножается, ускользая от контроля со стороны иммунной системы, приводя к поражению различных органов.
Доказательная медицина – подход к медицинской практике, при котором решения о применении профилактических, диагностических и лечебных мероприятий принимаются исходя из имеющихся доказательств их эффективности и безопасности, а такие доказательства подвергаются поиску, сравнению, обобщению и широкому распространению для использования в интересах пациентов.
Заболевание – возникающее в связи с воздействием патогенных факторов нарушение деятельности организма, работоспособности, способности адаптироваться к изменяющимся условиям внешней и внутренней среды при одновременном изменении защитно-компенсаторных и защитно-приспособительных реакций и механизмов организма.
Инструментальная диагностика – диагностика с использованием для обследования больного различных приборов, аппаратов и инструментов.
Качество медицинской помощи – совокупность характеристик, отражающих своевременность оказания медицинской помощи, правильность выбора методов профилактики, диагностики, лечения и реабилитации при оказании медицинской помощи, степень достижения запланированного результата.
Клинические рекомендации – документ, основанный на доказанном клиническом опыте, описывающий действия врача по диагностике, лечению, реабилитации и профилактике заболеваний, помогающий ему принимать правильные клинические решения.
Лабораторная диагностика – совокупность методов, направленных на анализ исследуемого материала с помощью различного специализированного оборудования.
Латентная инфекция – форма проявления инфекционного процесса, характеризуется длительным сохранением возбудителя в организме без клинических признаков заболевания. Клинические проявления могут появиться при ослаблении иммунитета.
Медицинский работник – физическое лицо, которое имеет медицинское или иное образование, работает в медицинской организации и в трудовые (должностные) обязанности которого входит осуществление медицинской деятельности, либо физическое лицо, которое является индивидуальным предпринимателем, непосредственно осуществляющим медицинскую деятельность.
Пневмонит – интерстициальное воспаление сосудистой стенки альвеол, сопровождающееся их рубцеванием, в патогенезе которого основную роль играют иммунопатологические механизмы преимущественно клеточного типа.
Рабочая группа – двое или более людей одинаковых или различных профессий, работающих совместно и согласованно в целях создания клинических рекомендаций, и несущих общую ответственность за результаты данной работы.
Ретинит – воспаление сетчатки глаза человека, чаще двустороннее, возникает в результате заноса в сосуды сетчатки возбудителей инфекции.
Синдром – совокупность симптомов с общими этиологией и патогенезом.
Уровень достоверности доказательств – отражает степень уверенности в том, что найденный эффект от применения медицинского вмешательства является истинным.
Уровень убедительности рекомендаций – отражает не только степень уверенности в достоверности эффекта вмешательства, но и степень уверенности в том, что следование рекомендациям принесет больше пользы, чем вреда в конкретной ситуации.
Цитомегаловирусная инфекция – широко распространенная вирусная инфекция, характеризующаяся многообразными проявлениями от бессимптомного течения до тяжелых генерализованных форм с поражением внутренних органов и центральной нервной системы, с возможной трансплацентарной передачей вируса и внутриутробным поражением плода.
1. Краткая информация по заболеванию или состоянию (группы заболеваний или состояний)
1.1 Определение заболевания или состояния (группы заболеваний или состояний)
Цитомегаловирусная инфекция (ЦМВИ) – вирусная антропонозная инфекция, характеризующаяся многообразием проявлений от бессимптомного течения до тяжелых генерализованных форм с поражением внутренних органов и центральной нервной системы.
1.2 Этиология и патогенез заболевания или состояния (группы заболеваний или состояний)
Возбудитель ЦМВИ – Cytomegalovirus hominis – отнесен к семейству Herpesviridae, подсемейству Betaherpesvirinae, роду Cytomegalovirus. Особенностями цитомегаловируса (ЦМВ) являются крупный геном, содержащий дезоксирибонуклеиновую кислоту (ДНК), возможность репликации без повреждения клетки, малая цитопатогенность в культуре ткани, медленная репликация, сравнительно низкая вирулентность, существенное подавление клеточного иммунитета [1, 2, 3, 4, 5,113].
Двуцепочечная ДНК ЦМВ содержит около 235000 пар оснований и имеет более 200 открытых рамок считывания, кодирующих не менее 59 белков. ЦМВ способен реплицироваться в полиморфноядерных лейкоцитах, лимфоцитах, моноцитах, макрофагах, эпителиальных и эндотелиальных клетках. Вирус обладает ферментами ДНК-полимеразой, протеинкиназой (кодирующейся геном UL 97). Репликация включает экспрессию трех классов генов: сверхранние, ранние и поздние гены, кодирующие соответственно сверхранние, ранние и поздние антигены. Сверхранние белки pp72 и IE2 являются главными регуляторами экспрессии вирусных генов. Ранние белки, UL97 фосфокиназа и UL54 ДНК-полимераза, способствуют репликации вирусного генома, а поздние протеины, такие как pp65 и гликопротеин B, являются структурными белками и обнаруживаются в капсиде, матриксе и оболочке вируса [1, 2, 3, 4, 5, 6, 7, 8].
В международных каталогах зарегистрировано 3 штамма ЦМВ – AD 169, Davis и Kerr. От одного человека может быть выделено несколько штаммов вируса [6, 7, 8].
Вирус термолабилен, инактивируется при температуре +56⁰С, длительно сохраняется при комнатной температуре. ЦМВ быстро теряет свою инфекционность при замораживании (-20⁰С). ЦМВ обладает относительной нечувствительностью к действию эндогенного интерферона, что способствует его персистенции, не чувствителен к действию антибактериальных препаратов системного действия, значительно менее чувствителен по сравнению с другими герпес-вирусами к ацикловиру и его аналогам (Нуклеозиды и нуклеотиды, кроме ингибиторов обратной транскриптазы, код по АТХ: J05AB) [1, 2, 3, 9,114].
При постнатальной ЦМВИ входными воротами для возбудителя служат слизистые оболочки ротоглотки, дыхательной системы, пищеварительного и генитального трактов. После преодоления вирусом входных ворот и его локального размножения наступает кратковременная виремия, моноциты и лимфоциты переносят вирус к различным органам [1, 2, 3, 6, 7,126].
При острой ЦМВ-инфекции вирус поражает преимущественно эпителиальные клетки легких, печени, кишечника, почек, мочевого пузыря, молочных и слюнных желез, генитального тракта. Поражение эпителиальных клеток облегчает вирусную трансмиссию подлежащим тканям и инфицирование фибробластов. ЦМВ может инфицировать нервные клетки, клетки гладкой мускулатуры, клетки стромы костного мозга [1, 2, 3, 6, 113, 129].
Цитомегаловирус персистирует и размножается в эндотелиоцитах. Инфицированные эндотелиальные клетки крупных сосудов являются резервуарами ЦМВ и вносят свой вклад в виремию, передавая вирус циркулирующим моноцитам. Вирусная инфекция в микрососудах приводит к разрушению зараженных эндотелиальных клеток, их слущиванию, образованию микротромбов, вызывает постепенное продуктивное поражение всех слоев сосудистой стенки, приводящее к склеротическим изменениям, стенозу и облитерации сосудов. [1, 2, 3, 6, 7, 9].
Несмотря на клеточный и гуморальный ответ, ЦМВ индуцирует хроническую латентную инфекцию. Резервуаром вирусных частиц служат моноциты, лимфоциты, эндотелиальные и эпителиальные клетки. Возможны периоды локальной активизации ЦМВ с выделением вируса из носоглотки или урогенитального тракта [1, 2, 7, 10, 11, 12, 13].
В случае иммунологических нарушений происходит возобновление репликации вируса, виремия, диссеминация возбудителя, развитие клинически выраженного заболевания. Активность вирусной репликации, риск манифестации ЦМВ-инфекции, тяжесть ее течения во многом определяет глубина иммуносупрессии, прежде всего, уровень снижения количества СD4-лимфоцитов в крови [10, 11, 12, 13].
С ЦМВ-инфекцией связан широкий спектр органных поражений: легких, пищеварительного тракта, надпочечников, почек, головного и спинного мозга, сетчатки глаза. У больных ЦМВИ при посмертных исследованиях выявляют фиброзирующий альвеолит, фиброз легких; эрозивно-язвенное с выраженным фиброзом подслизистого слоя поражение пищевода, толстой кишки, реже желудка и тонкой кишки; массивное, часто двустороннее некротическое поражение надпочечников; энцефаловентрикулит с преимущественным поражением стенок желудочков и близлежащих структур головного мозга, некротическое поражение спинного мозга, сетчатки глаза. Специфичность морфологической картины определяют крупные цитомегалоклетки (ЦМК), лимфогистиоцитарные инфильтраты, а также продуктивно-инфильтративные панваскулиты с поражением всех оболочек мелких артерий и вен с исходом в склерозирование. Подобное поражение сосудов служит основой для тромбообразования, приводит к хронической ишемии, на фоне которой развиваются деструктивные изменения, сегментарные некрозы и язвы, выраженный фиброз. У большинства больных патологический процесс носит генерализованный характер [1, 2, 3, 6, 7, 9, 13, 14, 113, 124, 125, 126, 130].
Клинически выраженная ЦМВИ – одно из серьезных инфекционных осложнений при трансплантации солидных органов и костного мозга и является одной из частых причин длительной госпитализации больных и их смерти [15, 16, 17, 18, 19, 117].
Манифестная генерализованная ЦМВИ занимает одно из первых мест в структуре оппортунистических заболеваний у ВИЧ-инфицированных. В международных классификациях ВИЧ-инфекции «цитомегаловирусное поражение органов (за исключением или помимо печени, селезенки, лимфатических узлов) у больного старше 1 месяца» включено в перечень 24 точно диагностирующих СПИД заболеваний. Данная патология имеет место у 10-40% больных СПИДом, не получающих антиретровирусную терапию (АРВТ) и в 3-7% случаев в популяции больных ВИЧ-инфекцией при ее назначении [20, 21, 22, 23, 24, 113].
Проблема клинически выраженной ЦМВИ актуальна для лиц, имеющих иммуносупрессию иной природы, в частности, онкогематологических пациентов, больных лучевой болезнью, лиц, длительно принимающих кортикостероидную, туберкулостатическую терапию, перенесших ожоговую травму [1, 2, 7, 9, 115, 116].
ЦМВ может быть причиной посттрансфузионных гепатитов, синдрома и болезни Бадда-Киари, разнообразной гинекологической патологии [25, 26, 27, 28].
Предполагается роль ЦМВ, как одного из ко-факторов, в развитии системных васкулитов, хронических диссеминированных заболеваний легких (в частности, фиброзирующего альвеолита), криоглобулинемии, опухолевых процессов (аденокарциномы предстательной железы, аденокарциномы толстой кишки, рака шейки матки), атеросклероза, кардиомиопатии, детского церебрального паралича, эпилепсии, синдрома Гийена-Барре, синдрома хронической усталости, аутизма [29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 124, 130].
Возможно развитие клинически выраженной ЦМВИ у взрослых лиц, не имеющих выраженных иммунологических нарушений, вследствие стрессовых и иных ситуаций [40, 41, 42, 43, 113, 130].
1.3 Эпидемиология заболевания или состояния (группы заболеваний или состояний)
Источником инфекции при ЦМВИ является человек.
Наличие в крови специфических антител в абсолютном большинстве случаев означает присутствие в организме самого вируса. Доля серопозитивных лиц среди взрослого населения составляет 73-98%. У 20-30% здоровых беременных ЦМВ присутствует в слюне, у 3-10% – в моче, у 5-20% – в цервикальном канале или вагинальном секрете. Вирус обнаруживают в грудном молоке у 20-60% серопозитивных матерей. Установлена значительная частота выявления (до 35%) и длительность присутствия (в среднем, до 22 месяцев) ЦМВ в сперме. Кровь около 1% доноров содержит ЦМВ [1, 2, 3, 7, 44, 45, 46, 47, 48, 49, 50, 51, 127].
Заражение вирусом возможно половым, парентеральным, вертикальным путями, а также контактно-бытовым через слюну при близких контактах [44, 52, 53, 54, 113, 126,127]. Частота врожденной ЦМВИ составляет 0,2-2,5% среди всех родившихся младенцев [57, 58, 126, 128]. Критическим периодом заражения ЦМВ является возраст 16-30 лет. При обследовании доноров установлено, что у молодых людей частота сероконверсии составляет около 2% в год. В данной группе лиц передача вируса осуществляется главным образом через поцелуи и половым путем [44, 45, 48, 49, 52, 53, 54, 127].
Гемотрансфузии и парентеральные манипуляции могут приводить к заражению ЦМВ. Переливание цельной крови и ее компонентов, содержащих лейкоциты, ведет к передаче вируса с частотой 0,14-10,0 на 100 доз. Риск инфицирования ЦМВ с каждой гемотрансфузией возрастает на 5-12%. Крайне опасно заражение новорожденного ЦМВ при переливании крови от серопозитивного донора, не прошедшую соответствующую обработку [44, 45, 55, 56, 122].
Реализация контактно-бытового пути обеспечивает заражение ЦМВ детей младшего возраста друг от друга в домах ребенка, детских садах, передачу вируса от матери к ребенку и от инфицированного ребенка матери. У матерей, имеющих старшего ребенка в возрасте до 3-х лет или ребенка до 6 лет, посещающего детский сад частота сероконверсии составляет 24% в год. Совокупная распространенность ЦМВ-инфекции среди детей, находящихся в детских учреждениях, по данным мета-анализа исследований составила 32%, тогда как распространенность среди детей, не посещавших детские сады, составила 22%. Частота сероконверсии у родителей ребенка в возрасте до 2-х лет, выделяющего ЦМВ, составляет около 50% в год, тогда как у доноров это показатель находится на уровне 2% в год. У взрослых лиц – отрудников детских отделений больниц, домов ребенка, дошкольных учреждений, родителей детей дошкольного возраста значительно чаще выявляют сероконверсию (с частотой до 8% в год) и диагностируют острую ЦМВ-инфекцию [44, 48, 49, 59, 60, 61, 126]. По данным систематического обзора работники по уходу за детьми имеют риск ЦМВ-инфекции в 1,6 раза выше, риск еще больше увеличивается при наличии хотя бы одного ребенка, проживающего дома [135].
1.4 Особенности кодирования заболевания или состояния (группы заболеваний или состояний) по Международной статистической классификации болезней и проблем, связанных со здоровьем
В 25 Цитомегаловирусная болезнь
В25.0 Цитомегаловирусная пневмония (J17.1*).
В25.1 Цитомегаловирусный гепатит (К77.0*).
В25.2 Цитомегаловирусный панкреатит (К87.1*).
В25.8 Другие цитомегаловирусные болезни.
В25.9 Цитомегаловирусная болезнь неуточненная.
1.5 Классификация заболевания или состояния (группы заболеваний или состояний)
Заболевание классифицируют в зависимости от сроков и механизмов заражения: врожденная (в том числе антенатальная, интранатальная и постнатальная) и приобретенная инфекция; степени активности вируса: латентная, субклиническая, персистирующая, активная (низкой, средней, высокой степени); первичного или повторного заражения: острая инфекция, реактивация вируса и реинфекция.
По клинической картине выделяют следующие формы [1,2,4,5,7,8, 113,117]:
I. Врожденная ЦМВИ:
а) субклиническая (бессимптомная) форма;
б) манифестная форма (легкая, среднетяжелая, тяжелая, изолированное снижение слуха).
II. Приобретенная ЦМВИ:
1. Острая ЦМВИ, первичное инфицирование:
а) субклиническая (бессимптомная) форма;
б) мононуклеозоподобный синдром;
в) ЦМВ-болезнь (манифестная ЦМВИ).
2. Латентная ЦМВИ.
3. Активная ЦМВИ (реинфекция или реактивация вируса):
а) субклиническая (бессимптомная) форма;
б) ЦМВ-ассоциированный синдром.
4. ЦМВ-болезнь (манифестная ЦМВИ).
С цитомегаловирусом связаны также следующие коды МКБ-10:
В27.1 Цитомегаловирусный мононуклеоз.
P35.1 Врожденная цитомегаловирусная инфекция.
В20.2 Болезнь, вызванная ВИЧ, с проявлениями цитомегаловирусного заболевания.
Цитомегаловирусный мононуклеоз представляет собой форму течения острой приобретенной ЦМВИ – мононуклеозоподобный синдром.
Врожденная ЦМВИ рассмотрена в отдельных клинических рекомендациях.
Проявления ЦМВИ на фоне ВИЧ-инфекции описаны разделе данных клинических рекомендаций.
1.6 Клиническая картина заболевания или состояния (группы заболеваний или состояний)
Продолжительность инкубационного периода составляет 2-12 нед.
Приобретенная ЦМВИ в случае первичного инфицирования взрослых иммунокомпетентных лиц обычно протекает бессимптомно в субклинической форме или в виде нерезко выраженного мононуклеозоподобного синдрома. Острая ЦМВИ имеет яркую клиническую симптоматику только у 5% впервые инфицированных взрослых. Характерны высокая лихорадка неправильного типа длительностью более 2 недель, слабость, выраженная утомляемость, потеря аппетита, лимфаденопатия. Возможны головная боль, миалгии, артралгии, гепатоспленомегалия, характерно повышение активности аминотрансфераз и щелочной фосфатазы. Ангину и увеличение заднешейных и затылочных лимфатических узлов наблюдают редко. Описано развитие гепатита, холангита, эзофагита и пневмонии как проявлений первичного заражения вирусом. Ряд заболевших отмечают выраженную сухость во рту, нарушение выработки слюны из-за развития сиалоаденита. Прогноз благоприятный.
Острая ЦМВИ у беременных протекает с умеренно выраженным фарингитом, субфебрилитетом, наличием слабости, артралгий или миалгий, повышением активности печеночных ферментов, лимфоцитозом. У трети пациенток инфекция протекает бессимптомно. В редких случаях острая ЦМВИ приводит к развитию интерстициальной пневмонии, сопровождающейся неправильного типа лихорадкой, сильным сухим кашлем, астенией. Необходимо обращать внимание на любые признаки острой инфекционной патологии у беременных, при наличии которых следует провести внеплановые лабораторные исследования для исключения первичной ЦМВИ.
При отсутствии иммунодефицита острая ЦМВИ переходит в латентную ЦМВИ, при которой клинические проявления отсутствуют. В случае иммуносупрессии может произойти возобновление репликации ЦМВ с развитием манифестации заболевания в виде активной ЦМВИ. Повторное попадание вируса в организм человека на фоне иммунодефицитного состояния также может быть причиной манифестной ЦМВ-инфекции. При реинфекции манифестация ЦМВИ происходит чаще и протекает более тяжело, чем при реактивации вируса.
Заражение вирусом при гемотрансфузии или трансплантации органа серонегативному реципиенту может привести к развитию острого заболевания, возникающего через 2-8 нед после переливания инфицированной крови или через 8-12 нед после пересадки зараженного органа и характеризующегося высокой лихорадкой, выраженной астенией, болями в горле, лимфаденопатией, миалгией и артралгией. В крови выявляют нейтропению и тромбоцитопению. Возможны пневмония, плеврит, гепатит, нефрит, миокардит, артрит. Заражение ЦМВ серонегативного реципиента органа в 70-80% случаев вызывает развитие манифестной ЦМВИ, которая при отсутствии лечения может закончиться летальным исходом.
Для ЦМВИ у иммуносупрессивных лиц характерно развитие «ЦМВ-ассоциированного синдрома», который проявляется постепенным, в течение нескольких недель, развитием заболевания, появлением симптомов-предвестников в виде быстрой утомляемости, слабости, потери аппетита, значительного снижения веса, длительной волнообразной лихорадки неправильного типа с подъемами температуры тела выше 38,5°С, реже – потливости по ночам, артралгии, миалгии. Через 1-3 мес при сохранении выраженной иммуносупрессии развивается тяжелая органная патология с тенденцией к генерализации процесса. Частота поражения легких у ВИЧ-инфицированных больных ЦМВИ составляет 70%, сетчатки с развитием ЦМВ-ретинита – 45%, надпочечников – 60%, ЖКТ – 39%, пищевода – 13%, печени – 13%, головного мозга – 16%, спинного мозга – 8%, корешков спинных нервов – 20%. Летальность стационарных больных ВИЧ-инфекцией, страдающих ЦМВИ, составляет 25-27%.
2. Диагностика заболевания или состояния (группы заболеваний или состояний) медицинские показания и противопоказания к применению методов диагностики
Критерии установления диагноза заболевания/состояния:
Ввиду малоспецифичной клинической картины и отсутствии патогномоничных симптомов, клинический диагноз ЦМВИ требует обязательного лабораторного подтверждения.
Диагноз приобретенной ЦМВИ устанавливается на основании определения антител классов M, G (IgM, IgG) к цитомегаловирусу (Cytomegalovirus) в крови, определения ДНК цитомегаловируса (Cytomegalovirus) методом ПЦР в периферической (и пуповинной) крови, качественное исследование, а также определения ДНК цитомегаловируса (Cytomegalovirus) в моче методом ПЦР, качественное исследование, определения ДНК цитомегаловируса (Cytomegalovirus) методом ПЦР в слюне, качественное исследование, определения ДНК цитомегаловируса (Cytomegalovirus) в отделяемом из цервикального канала методом ПЦР, качественное исследование. В зависимости от анамнестических данных и клинической симптоматики определяется форма заболевания.
Диагноз острой ЦМВИ субклинической формы (ранее бессимптомная форма) устанавливается в случае определения антител класса M (IgM) к цитомегаловирусу (Cytomegalovirus) в крови при отсутствии IgG, с последующим снижением уровня IgM и нарастанием уровня IgG и при отсутствии клинической симптоматики. Если в анамнезе присутствует лихорадка, умеренный катаральный синдром и лимфаденопатия на момент осмотра или в течение трех месяцев от определения лабораторных маркеров, то диагностируется мононуклеозоподобный синдром острой ЦМВИ. Манифестная форма ЦМВИ или ЦМВ-болезнь диагностируется при яркой клинической картине заболевания, характеризующейся фебрильной лихорадкой, интоксикационным синдромом, лимфаденопатией, гепатолиенальным синдромом и другой органной патологией.
Для острой ЦМВИ, развившейся при первичном инфицировании, характерно присутствие ДНК ЦМВ в крови (при определении ДНК цитомегаловируса (Cytomegalovirus) методом ПЦР в периферической (и пуповинной) крови, качественное исследование). При субклинической форме ЦМВИ отрицательный результат исследования на ДНК ЦМВ в крови (при определении ДНК цитомегаловируса (Cytomegalovirus) методом ПЦР в периферической (и пуповинной) крови, качественное исследование) не исключает диагноз и требует дополнительного определения ДНК вируса в моче и в слизи цервикального канала (определения ДНК цитомегаловируса (Cytomegalovirus) в моче методом ПЦР, качественное исследование, определения ДНК цитомегаловируса (Cytomegalovirus) в отделяемом из цервикального канала методом ПЦР, качественное исследование) у беременных.
Латентная ЦМВИ диагностируется при определении в крови антител класса IgG к ЦМВ при отсутствии IgM и какой-либо клинической симптоматики (определение антител классов M, G (IgM, IgG) к цитомегаловирусу (Cytomegalovirus) в крови). ДНК цитомегаловируса не определяется в крови и других биологических жидкостях (при определении ДНК цитомегаловируса (Cytomegalovirus) методом ПЦР в периферической (и пуповинной) крови, качественное исследование).
Активная ЦМВИ в следствие реинфекции или реактивации вируса диагностируется при обнаружении ДНК ЦМВИ в крови (при определении ДНК цитомегаловируса (Cytomegalovirus) методом ПЦР в периферической (и пуповинной) крови, качественное исследование) и других биологических жидкостях (в зависимости от формы заболевания) и IgG к ЦМВ в крови при отрицательном IgM (определения антител классов M, G (IgM, IgG) к цитомегаловирусу (Cytomegalovirus) в крови). В отсутствии клинической симптоматики диагностируется субклиническая форма (ранее бессимптомная). Определение ДНК ЦМВ (определение ДНК цитомегаловируса (Cytomegalovirus) методом ПЦР в периферической (и пуповинной) крови, качественное исследование) в различных биологических субстратах при ассоциированной с ним органной патологии (эзофагит, нефрит, миокардит, энцефаломиелит, ЦМВ-ретинит и др.) рассматривается как ЦМВ-ассоциированный синдром, более характерный для иммуно-супрессированных лиц. При развитии клинической картины острого инфекционного заболевания диагностируется манифестная форма – ЦМВ-болезнь.
Скрининговое обследование на ЦМВ (определение антител классов М и G (IgM и IgG) к цитомегаловирусу (Cytomegalovirus) в крови) показано следующим группам населения [8, 9, 20, 21, 22, 23, 26, 120, 130, 133, 134, 155, 156]:
· женщины с отягощенным акушерским анамнезом (перинатальные потери, рождение ребенка с врожденными пороками развития), планирующие беременность;
· беременные женщины при многоплодной беременности, в случае повторных беременностей, постоянного контакта с детьми до 3 лет;
· беременные женщины, имеющие ультразвуковые признаки внутриутробной инфекции, лимфаденопатии, лихорадку, гепатит и гепатоспленомегалию неясного генеза;
· реципиенты крови и ее компонентов, органов и тканей (при подозрении на инфицирование ЦМВ и в течение 6 месяцев после переливания компонентов крови);
· наличие полового контакта с серопозитивным партнером;
· пациенты с гепатитами, панкреатитами, менингоэнцефалитом, пневмонией, поражением глаз (увеит, кератит, ретинит, ретинальный некроз), поражением желудочно-кишечного тракта, при неустановленной этиологии;
· пациенты с иммунодефицитом (пациенты с ВИЧ-инфекцией, онкологическими заболеваниями, пациенты на гемодиализе, пациенты на лечении иммунодепрессантами и др.).
· доноры крови (ее компонентов), органов и тканей, спермы (при каждой донации или каждом взятии донорского материала).
2.1 Жалобы и анамнез
· Для диагностики первичного инфицирования ЦМВ или реинфекции при сборе эпидемиологического анамнеза рекомендовано уточнить связь с возможным источником инфекции [1, 2, 44, 59, 60, 61].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
· Для выявления источника инфекции рекомендовано обратить внимание на наличие в окружении пациента ребенка дошкольного возраста, посещающего детские учреждения [1, 2, 44, 59, 60, 61].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
· Для выявления источника инфекции рекомендовано обратить внимание на близкий бытовой контакт с больным типичными и атипичными формами инфекционного мононуклеоза или вирусовыделителем, а также больным, имеющим лихорадку с неуточненным диагнозом или ОРВИ, фарингит [1, 2, 45, 49, 54].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
· Для выявления источника инфекции рекомендовано обратить внимание на половые контакты с серопозитивным партнером без использования барьерных контрацептивов [44, 52, 53, 127].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
· Для выявления источника инфекции рекомендовано обратить внимание на проведение гемотрансфузии в течение последних 6 месяцев [44, 55, 56, 116, 130].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
· При постановке диагноза рекомендовано обратить внимание на длительную волнообразную лихорадку неправильного типа с подъемами температуры тела выше 38,5ºС или длительный субфебрилитет, астению, боли в горле, выраженную слабость, быструю утомляемость, сонливость, потерю аппетита, существенное снижение веса, реже – потливость по ночам, артралгии, миалгии, характерные для манифестных форм ЦМВБ [1, 2, 4, 8, 9, 13, 62, 113].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
2.2 Физикальное обследование
Ввиду разнообразия клинических форм и частого субклинического (бессимптомного) течения ЦМВИ у взрослых, физикальное исследование имеет небольшое диагностическое значение и помогает распознать только манифестные формы ЦМВИ.
На этапах постановки диагноза:
· Рекомендуется начать с общего осмотра кожных покровов и видимых слизистых оболочек ЛОР-органов (гортань, слизистая носа) (визуальный осмотр терапевтический) [1, 4, 17, 19, 20, 23].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарий: с использованием шпателя (зонда) определяют состояние надгортанника, оценивают текстуру и плотность поверхности, обращают внимание на наличие пятен и характер дефектов слизистой полости рта. При осмотре обращают внимание на локализацию, величину, глубину патологических изменений (везикулы, афты), болезненность или отсутствие чувствительности при исследовании. Обращают внимание на признаки фарингита, сиалоаденита.
· Рекомендуется проведение осмотра и пальпации лимфатических узлов с определением их болезненности и размеров для выявления признаков воспаления [1, 4, 9].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарий: исследование лимфатических узлов проводится бимануально и билатерально, сравнивая правую и левую области исследования. Осмотр лимфатических узлов позволяет предположить наличие воспалительного, инфекционного и онкологического процессов. Увеличение лимфатических узлов наиболее характерно для мононуклеозоподобного синдрома.
· Рекомендовано проведение перкуссии и пальпации с определением размеров и консистенции печени и селезенки (перкуссия при заболеваниях печени и желчевыводящих путей; пальпация при заболеваниях печени и желчевыводящих путей) для установления возможного вовлечения органов в воспалительный процесс [8, 9, 26].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарий: Определение размеров и консистенции края печени и селезенки позволяет выявить патологию со стороны этих органов и начать обследование для дифференциальной диагностики и выяснения этиологии процесса. Гепатит – одно из клинических проявлений ЦМВИ у реципиентов после пересадки печени и инфицированных ЦМВ во время гемотрансфузий. Клинической особенностью ЦМВ-гепатита является частое сочетание с патологией желчевыводящих путей. Холангиопатии ЦМВ-этиологии включают в себя склерозирующий холангит, папиллярный стеноз, стриктуру общего желчного потока и некалькулезный холецистит. ЦМВ-гепатит характеризуется мягким клиническим течением с умеренными гепатомегалией и цитолизом, но при развитии склерозирующего холангита добавляются боли в верхней части живота, тошнота, диарея, болезненность печени, повышение активности ЩФ и ГГТ. Может развиться надпеченочная желтуха. Патология поджелудочной железы у больных генерализованной ЦМВИ обычно протекает бессимптомно или со стертой клинической картиной и проявляется повышением активности панкреатических ферментов в крови и в моче.
· Рекомендовано провести перкуссию и аускультацию легких (Перкуссия при заболеваниях легких и бронхов A01.09.004; Аускультация при заболеваниях легких и бронхов A01.09.005) для выявления патологии дыхательной системы [8, 9, 26, 121].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарий: Для поражения легких при активной ЦМВИ характерны: постепенно усиливающийся сухой или малопродуктивный кашель, умеренная одышка, нарастание симптомов интоксикации, перкуторная и аускультативная картина пневмонии.
· Рекомендовано определить наличие очаговой неврологической симптоматики и менингеального синдрома у пациентов с иммунодефицитом группы ВИЧ-пациентов для выявления возможной патологии центральной и/или периферической нервной системы [1, 2, 5, 8, 24, 158].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
Комментарий: Для ЦМВ-энцефалита у больных ВИЧ-инфекцией характерны повышение температуры тела, скудная неврологическая симптоматика (непостоянные головные боли, головокружение, горизонтальный нистагм, у части пациентов в поздние сроки болезни – парез глазодвигательного нерва и лицевого нерва), развитие в большинстве случаев выраженных изменений психического статуса в виде личностных изменений, грубых нарушений памяти, снижения интеллектуальной деятельности, резкого ослабления психической и двигательной активности, нарушения ориентировки в месте и времени, анозогнозии, снижения контроля за функцией тазовых органов.
ЦМВ принадлежит ведущая роль в развитии миелита у больных ВИЧ-инфекцией. Поражение спинного мозга носит диффузный характер и является поздним проявлением ЦМВИ. В дебюте заболевание имеет клиническую картину полинейропатии или полирадикулопатии, в дальнейшем, в соответствии с уровнем поражения спинного мозга, развиваются тетрапарез или нижний парапарез, появляются пирамидные знаки, значительное снижение всех видов чувствительности, характерны расстройства функции тазовых органов.
2.3 Лабораторные диагностические исследования
2.3.1 На этапе постановки диагноза:
· При манифестных формах ЦМВИ всем пациентам рекомендовано проведение общего (клинического) анализа крови, с дифференцированным подсчетом лейкоцитов (лейкоцитарная формула) и исследованием уровня тромбоцитов в крови для своевременного выявления осложнений и неотложных состояний и в комплексной оценке степени тяжести заболевания [1, 2, 5, 9].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5).
Комментарии: для общего (клинического) анализа крови характерны лейкоцитоз, относительный лимфоцитоз, наличие атипичных мононуклеаров (лимфоцитов с широкой базофильной цитоплазмой), возможна тромбоцитопения. При иммуносупрессии частыми проявлениями ЦМВ-болезни являются тромбоцитопения со снижением способности клеток к агрегации и экзоцитозу, а также умеренные анемия, лейкопения, лимфопения и моноцитоз. Снижение концентрации гемоглобина, количества эритроцитов и тромбоцитов у больных ВИЧ-инфекцией коррелирует с увеличением концентрации ДНК ЦМВ в крови.
· Рекомендовано проведение общего (клинического) анализа мочи пациентам с подозрением на манифестную форму ЦМВИ во время первичного обследования для выявления признаков нарушения функции почек [1, 2, 5, 9].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5).
Комментарии: для общего (клинического) анализа мочи характерны изменения воспалительного характера в случае развития ЦМВ-ассоциированного нефрита: микропротеинурия, микрогематурия, лейкоцитурия.
· Рекомендовано выполнение анализа крови биохимического общетерапевтического, включая такие показатели как исследование уровня общего билирубина, уровня свободного и связанного билирубина, определение активности аланинаминотрансферазы и аспартатаминотрансферазы (АЛТ, АСТ), гамма-глютамилтрансферазы (ГГТ), щелочной фосфатазы (ЩФ) в крови, исследование уровня мочевины, креатинина, альфа-амилазы в крови всем пациентам с подозрением на манифестную форму ЦМВИ для оценки нарушения пигментного обмена, цитолиза, холестаза, почечной недостаточности, нарушения функции поджелудочной железы [1, 2, 6, 9, 63, 64, 65, 66, 113, 130].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: При биохимическом исследовании крови (анализе крови биохимическом общетерапевтическом), в случае развития гепатита, наблюдается повышение АЛТ, АСТ, ЩФ, ГГТП, возможно нарушение обмена билирубина. Цитомегаловирусный интерстициальный нефрит, как правило, протекает без клинических проявлений. В редких случаях, может развиваться нефротический синдром с почечной недостаточностью и повышением уровня креатинина и мочевины. Поражение поджелудочной железы проявляется возрастанием уровня альфа-амилазы крови. В случае присоединения холангита отмечается повышение уровня свободного и связанного билирубина, повышение уровня ЩФ, ГГТП, при нерезком возрастании АЛТ и АСТ.
· Рекомендуется пациентам с подозрением на манифестную форму ЦМВИ для оценки состояния свертывающей системы крови определение протромбинового (тромбопластинового) времени в крови или плазме или коагулограммы (ориентировочного исследования системы гемостаза): исследование времени свертывания нестабилизированной крови или рекальцификации плазмы неактивированное, исследование времени кровотечения, тромбинового времени в крови, и определение международного нормализованного отношения (МНО) для оказания своевременной помощи [159].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
Комментарии: коагулограмма (ориентировочное исследование системы гемостаза) проводится при протромбиновом индексе менее 70%.
· Рекомендовано пациентам с подозрением на манифестную форму ЦМВИ и признаками поражения центральной нервной системы проведение клинического исследования спиномозговой жидкости (Микроскопическое исследование спинномозговой жидкости, подсчет клеток в счетной камере (определение цитоза)) для выявления признаков воспаления и его характера [1, 2, 5, 9].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: Для ЦМВ-энцефалита и ЦМВ-обусловленной полирадикулопатии характерно умеренно повышенное содержание белка при отсутствии плеоцитоза или 2-3-значном лимфоцитарном плеоцитозе, нормальное содержание глюкозы.
· Рекомендовано выявление серологических маркеров ЦМВ – определение антител классов M, G (IgM, IgG) к цитомегаловирусу (Cytomegalovirus) в крови, а также определение индекса авидности антител класса G (IgG avidity) к цитомегаловирусу (Cytomegalovirus) в крови при помощи иммуноферментного анализа (ИФА), твердофазного хемилюминисцентного иммуноферментного метода или иммуноблота (ИБ) [18, 64, 67].
Уровень убедительности рекомендаций для определения антител класса M (IgM) к цитомегаловирусу (Cytomegalovirus) в крови В (уровень достоверности доказательств – 2)
Уровень убедительности рекомендаций для определения антител класса G (IgG) к цитомегаловирусу (Cytomegalovirus) в крови, а также определения индекса авидности антител класса G (IgG avidity) к цитомегаловирусу (Cytomegalovirus) в крови С (уровень достоверности доказательств – 5)
Комментарии: Основными лабораторными маркерами, подтверждающими острую ЦМВ-инфекцию (первичное заражение вирусом) являются IgM антитела в сочетании с сероконверсией IgG и/или низкоавидные IgG антитела. При первичном заражении вирусом на 5-7 день вырабатываются анти-ЦМВ IgM, через 10-14 дней – низкоавидные анти-IgG, затем постепенно авидность антител увеличивается, они становятся высокоавидными. Анти-IgM в большинстве случаев исчезают через 1-2 месяца, низкоавидные анти-IgG – через 1-3 месяца, высокоавидные антитела класса IgG циркулируют в крови носителя пожизненно. При использовании различных тест-систем для выявления анти-ЦМВ IgM антител специфичность и чувствительность тестов методом ИФА составляют от 30% до 88%, соответственно. С учетом этого, выявление в крови анти-ЦМВ IgM (при определении антител класса M (IgM) к цитомегаловирусу (Cytomegalovirus) в крови) недостаточно для установления диагноза острой ЦМВИ, необходимо повторное исследование крови через 2 недели для установления факта появления IgG (сероконверсии) при их отсутствии, а при наличии анти-ЦМВ IgG антител – необходимо определение их авидности. При латентной инфекции в крови присутствуют только высокоавидные IgG антитела. При активной ЦМВ-инфекции вследствие реактивации или реинфекции вируса возможно выявление IgM (определение антител класса M (IgM) к цитомегаловирусу (Cytomegalovirus) в крови) (но в меньшем титре и на протяжении более короткого временного периода по сравнению с острой ЦМВ-инфекцией) и высокоавидных IgG антител. Титр или количество IgG антител не отражает степени репликативной активности ЦМВ и не может служить основанием для постановки диагноза активной ЦМВ-инфекции и назначения специфической противовирусной терапии. Твердофазный хемилюминесцентный иммуноферментный метод обладает существенно более высокими аналитическими чувствительностью и специфичностью по сравнению со стандартным методом ИФА, что снижает вероятность ложноположительных результатов и делает его методом выбора по определению серологических маркеров. Иммуноблот, позволяющий детектировать анти-IgМ и анти-IgG к отдельным структурным и неструктурным белкам ЦМВ, является золотым стандартом для выявления антител класса IgМ (определение антител класса M (IgM) к цитомегаловирусу (Cytomegalovirus) в крови) (аналитические чувствительность и специфичность 100%). Присутствие антител к антигену рр65 (ранний белок), рр72 (предранний белок) расценивается как маркер активной репликации вируса. По мере развития инфекционного процесса появляются антитела к белку рp28.
· Рекомендовано определение ДНК цитомегаловируса (Cytomegalovirus) методом ПЦР в периферической (и пуповинной) крови, качественное исследование и определение ДНК цитомегаловируса (Cytomegalovirus) методом ПЦР в периферической (и пуповинной крови), количественное исследование всем пациентам с подозрением на острую и активную ЦМВИ [64, 65, 67, 68, 69, 70, 80, 81, 82, 83, 113].
Уровень убедительности рекомендаций В (уровень достоверности доказательств –2).
Комментарии: Обнаружение ДНК ЦМВ в крови (определение ДНК цитомегаловируса (Cytomegalovirus) методом ПЦР в периферической и пуповинной крови, качественное исследование) имеет наиболее важное диагностическое значение, свидетельствующее о высоко активной репликации вируса и его роли в имеющейся патологии. При первичном инфицировании в стадии «серологического окна» до начала синтеза антител выявление ДНК ЦМВ в крови является единственным маркером активной репликации вируса. При положительном результате качественного исследования, рекомендуется проведение количественного исследования ПЦР (определение ДНК цитомегаловируса (Cytomegalovirus) методом ПЦР в периферической и пуповинной крови, количественное исследование). Результаты количественной ПЦР предназначены для определения степени репликативной активности ЦМВ и обоснования наличия манифестной инфекции. Диагностическое значение имеет вирусная нагрузка 105 и выше в лейкоцитах и 104 в плазме крови.
У беременных наличие ДНК ЦМВ в лейкоцитах крови является достоверным признаком активной репликации ЦМВ и служит важным маркером высокого риска антенатального заражения вирусом плода.
· Рекомендовано определение ДНК цитомегаловируса (Cytomegalovirus) в мокроте, бронхоальвеолярной лаважной жидкости методом ПЦР иммунокомпрометированным пациентам с клиникой острого поражения дыхательной системы [64, 65, 67, 68, 121].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2).
Комментарии: Поражение органов дыхания более характерно для детей с врожденной ЦМВИ, инфицированных во время родов или в раннем постнатальном периоде. У взрослых, перенесших трансплантацию органа или гемотрансфузию от серопозитивного донора, в период до 12 недель возможно развитие острой инфекции ЦМВИ с клиникой пневмонии.
· Рекомендовано определение ДНК цитомегаловируса (Cytomegalovirus) методом ПЦР в слюне, качественное исследование, определение ДНК цитомегаловируса (Cytomegalovirus) методом ПЦР в слюне, количественное исследование, определение ДНК цитомегаловируса (Cytomegalovirus) в мазках со слизистой оболочки ротоглотки методом ПЦР, качественное исследование, определение ДНК цитомегаловируса (Cytomegalovirus) в мазках со слизистой оболочки ротоглотки методом ПЦР, количественное исследование пациентам с признаками сиалоаденита при подозрении на острую ЦМВИ [1, 2, 5, 9].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: Клиническое и прогностическое значение определения ДНК в различных биологических жидкостях не одинаково. Присутствие возбудителя в слюне является лишь маркером инфицированности и не свидетельствует о существенной вирусной активности. Важно сопоставление результатов исследования с клиническими проявлениями заболевания.
· Рекомендовано определение ДНК цитомегаловируса (Cytomegalovirus) в моче методом ПЦР, качественное исследование, при положительном результате – определение ДНК цитомегаловируса (Cytomegalovirus) в моче методом ПЦР, количественное исследование всем пациентам с манифестной формой ЦМВИ и клинико-лабораторными признаками поражения почек, а также беременным с признаками острой или активной ЦМВИ [1, 2, 5, 9, 107].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: Наличие ДНК ЦМВ в моче доказывает факт заражения и определенную вирусную активность, но вследствие длительного (до нескольких лет после заражения) обнаружения вируса в моче не может быть единственным лабораторным критерием активной ЦМВ-инфекции, и требует дополнительных исследований. Прогностическая ценность изолированного обнаружения вируса в моче беременной для антенатальной ЦМВ-инфекции составляет не более 20-30% и должна рассматриваться в совокупности с результатами других исследований.
· Рекомендовано определение ДНК цитомегаловируса (Cytomegalovirus) в спинномозговой жидкости методом ПЦР, качественное исследование всем пациентам с манифестной формой ЦМВИ и клинико-лабораторными признаками поражения центральной нервной системы [1, 2, 5, 9].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: Обнаружение ДНК ЦМВ (определение ДНК цитомегаловируса (Cytomegalovirus) в спинномозговой жидкости методом ПЦР, качественное исследование) в ликворе подтверждает этиологическую роль вируса в развившейся патологии нервной системы.
· Рекомендовано при наличии показаний в группах риска у женщины с отягощенным акушерским анамнезом и беременным с признаками острой или активной ЦМВИ определение ДНК цитомегаловируса (Cytomegalovirus) в отделяемом из цервикального канала методом ПЦР, качественное исследование, при положительном результате – проведение количественного исследования (определение ДНК цитомегаловируса (Cytomegalovirus) в отделяемом из цервикального канала методом ПЦР, количественное исследование) [1, 2, 5, 64, 65, 67, 68, 69, 70, 80, 81, 82, 83, 84, 113, 121, 130, 140].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: Наличие ЦМВ в генитальном тракте у беременных женщин – причина заражения ребенка во время родов. Частота обнаружения ЦМВ в цервикальном канале, вагинальном секрете здоровых беременных женщин составляет от 2-8% до 18-20%. С увеличением срока беременности вероятность обнаружения ЦМВ в вагинальном содержимом возрастает, у ВИЧ-инфицированных беременных ДНК ЦМВ в соскобах из цервикального канала была выявлена в 33,3% случаев.
· Рекомендовано, в качестве дополнительного метода, определение антигенов ЦМВ в биологическом материале с использованием реакции иммунофлюоресценции (РИФ), иммуноцитохимического метода, mRNA NASBA для подтверждения этиологической принадлежности [64, 65, 68, 69, 73, 74, 75, 76, 80, 82, 113].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 2)
Комментарий: Для обнаружения предраннего и раннего белков вируса с молекулярной массой рр72 и рр65 в слюне и моче используют метод РИФ. По количеству светящихся клеток делают вывод об интенсивности выделения вируса. Время выполнения исследования 24-36 часов. В диагностике активной ЦМВ-инфекции используют определение в лейкоцитах крови вирусного антигена pp65 иммуноцитохимическим методом. Появление в крови вирусного белка pp65 опережает развитие клинических симптомов ЦМВ-инфекции, количественный уровень антигенемии коррелирует с развитием клинических симптомов и вероятностью ЦМВИ. Современная методика детекции активной ЦМВ-инфекции путем определения ЦМВ-антигена pp67 методом mRNA NASBA показывает большую специфичность по сравнению с pp65-антигенемией и позволяет определять антиген ЦМВ в замороженных или лизированных образцах крови. Методы выявления антигенов уступают по чувствительности молекулярным методам, основанным на ПЦР, дающим возможность прямого качественного и количественного обнаружения ДНК ЦМВ в биологическом материале в кратчайшие сроки.
· Рекомендовано проведение цитологического исследования отделяемого полости рта, микропрепарата тканей полости рта, при манифестных формах ЦМВИ с признаками сиалоаденита и биопсийных материалов пораженных органов (цитологическое исследование микропрепарата тканей нижних дыхательных путей, тканей легкого, трахеи и бронхов, тканей печени, органов желудочно-кишечного тракта, почек) при манифестных формах ЦМВИ с признаками органных поражений с целью выявления цитомегалоклеток при окраске гематоксилином и эозином [1, 2, 5].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: Метод не является строго специфическим и требует подтверждения методом ПЦР (определения ДНК цитомегаловируса (Cytomegalovirus) методом ПЦР в слюне, качественное исследование).
2.3.2 На этапе патогенетической и симптоматической терапии
При манифестных формах ЦМВИ всем пациентам, при наличии отклонений от лабораторной нормы во время первичного обследования, проводится динамический контроль измененных показателей.
· Рекомендовано определение ДНК цитомегаловируса (Cytomegalovirus) методом ПЦР в периферической (и пуповинной) крови, качественное исследование и определение ДНК цитомегаловируса (Cytomegalovirus) методом ПЦР в периферической (и пуповинной крови), количественное исследование пациентам с манифестными формами, получающими этиотропную терапию, для динамического контроля ее эффективности [5, 64, 69, 70, 83, 84].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4).
Комментарии: Целью терапии является нормализация клинической картины и достижение авиремии крови.
· Рекомендовано у беременных пациенток при острой ЦМВИ с сиалоаденитом определение ДНК цитомегаловируса (Cytomegalovirus) методом ПЦР в слюне, качественное исследование, определение ДНК цитомегаловируса (Cytomegalovirus) в мазках со слизистой оболочки ротоглотки методом ПЦР, качественное исследование, для динамического контроля эффективности этиотропной терапии [66].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: Целью терапии является нормализация клинической картины и достижение элиминации вируса.
· Рекомендовано определение ДНК цитомегаловируса (Cytomegalovirus) в моче методом ПЦР, качественное исследование, пациентам с манифестной формой ЦМВИ и клинико-лабораторными признаками поражения почек, получающим этиотропную терапию, для динамического контроля ее эффективности, а также беременным с признаками острой или активной ЦМВИ на 32-34 неделях для прогноза вероятности инфицирования новорожденного [1, 2, 5, 9, 63, 64, 65, 66, 113].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: Наличие ДНК ЦМВ в моче доказывает факт заражения и определенную вирусную активность, но вследствие длительного (до нескольких лет после заражения) обнаружения вируса в моче (определения ДНК цитомегаловируса (Cytomegalovirus) в моче методом ПЦР, качественное исследование) не может быть единственным лабораторным критерием активной ЦМВ-инфекции, и требует дополнительных исследований. Прогностическая ценность изолированного обнаружения вируса в моче беременной для антенатальной ЦМВ-инфекции составляет 20-30% и должна рассматриваться в совокупности с результатами других исследований.
2.3.3 На этапе диспансерного наблюдения:
В случаях выявления первичного инфицирования, реинфекции или реактивации ЦМВИ во время беременности, диспансерное наблюдение беременной проводится совместно врачами-инфекционистами и врачами-акушерами-гинекологами до родоразрешения.
· Рекомендовано беременным с признаками острой или активной ЦМВИ определение ДНК цитомегаловируса (Cytomegalovirus) в отделяемом из цервикального канала методом ПЦР, качественное исследование, при положительном результате – проведение количественного исследования (определение ДНК цитомегаловируса (Cytomegalovirus) в отделяемом из цервикального канала методом ПЦР, количественное исследование) на 23-24 неделе и, в случае положительного результата, на 32-34 неделях беременности для прогноза вероятности инфицирования новорожденного [1, 2, 5, 9, 64, 65, 67, 68, 69, 70, 80, 81, 82, 83, 84, 113, 121, 130, 140].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: Риск интранатального инфицирования ребенка при наличии вируса в генитальном тракте матери составляет 50-57%. Наличие ДНК ЦМВ в цервикальном канале у женщин при сроке беременности 32-34 нед имеет значение как фактор риска интранатального заражения ребенка и является показателем для его обследования на 4-6-й неделе жизни.
· Рекомендовано пациентам с ВИЧ-инфекцией, имеющим количество CD4-лимфоцитов менее 200 клеток в 1 мкл проходить прием (осмотр, консультацию) врача-офтальмолога первичный и повторный для исключения ЦМВ-ретинита [1, 2, 5, 9].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: Одним из основных профилактических мероприятий у ВИЧ-инфицированных пациентов с уровнем CD4 менее 200 клеток/мкл остается выполнение офтальмоскопии каждые 3 месяца. При хорошем восстановлении иммунитета интервал между офтальмологическими обследованиями может быть увеличен.
2.4 Инструментальные диагностические исследования
· Рекомендовано выполнение ультразвукового исследования органов брюшной полости (комплексного), при манифестных формах ЦМВИ и проводится при наличии клинических (гепатомегалия) и лабораторных признаков поражения печени (повышении АЛТ, АСТ), поджелудочной железы (повышении уровня альфа-амилазы в крови), что помогает выявить патологию и уточнить ее природу [25].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4).
Комментарий: УЗИ органов брюшной полости (ультразвуковое исследование органов брюшной полости (комплексное)) и забрюшинного пространства проводится для диагностики увеличения и изменения структуры печени, увеличения селезенки, увеличения диаметра сосудов, исключения сопутствующей патологии желудочно-кишечного тракта, что в некоторых случаях может иметь решающее значение в определении тактики лечения [25]. Поражение печени при ЦМВБ носит характер гранулематозного гепатита, в редких случаях наблюдают выраженный фиброз и исход в цирроз печени.
· Рекомендовано выполнение ультразвукового исследования почек реципиентам почечного трансплантата при манифестных формах ЦМВИ при наличии лабораторных признаков нарушения функции почек (повышении уровня креатинина и мочевины, патологии в общем (клиническом) анализе мочи), что помогает выявить патологию и уточнить ее природу [164].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4).
· Рекомендовано выполнение рентгенографии легких (рентгенография легких цифровая) при наличии признаков поражения органов дыхательной системы при манифестных формах ЦМВИ [9, 32, 33, 81, 113, 121].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: Рентгенологические признаки могут отсутствовать или ограничиваться незначительным усилением легочного рисунка, снижением прозрачности легочных полей, характерны выраженная сетчатость, ячеистость легочного рисунка, наличие на фоне деформированного легочного рисунка двусторонних мелкоочаговых инфильтративных теней, преимущественно в средних и нижних отделах легких.
· Рекомендовано проведение спиральной компьютерной томографии легких (при наличии симптоматики поражения легких) при манифестных формах ЦМВИ у пациентов с иммуносупрессией [5].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: спиральная КТ легких у больных ЦМВ-пневмонией выявляет изменения легочной ткани по типу «матового стекла», уплотнение легочной ткани, утолщение стенок бронхиол или бронхоэктазы, интерстициальную сетчатость без эмфиземы, наличие очаговых и мелкофокусных изменений. При несвоевременной диагностике возможно развитие ДН, РДС, наступление летального исхода. Степень поражения легких у больных ЦМВИ может варьировать от минимально выраженного интерстициального пневмонита до распространенного фиброзирующего бронхиолита и альвеолита с формированием двустороннего полисегментарного фиброза легких.
· Рекомендовано выполнение трахеобронхоскопии, получение бронхо-альвеолярного лаважа при наличии признаков поражения органов дыхательной системы для определения этиологической принадлежности заболевания при манифестных формах ЦМВИ у пациентов с иммуносупрессией [21, 32].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: Диагностическая фибробронхоскопия (трахеобронхоскопия) с анализом клеточного состава бронхоальвеолярной жидкости и исследованием на наличие ДНК ЦМВ (определения антител классов М и G (IgM и IgG) к цитомегаловирусу (Cytomegalovirus) в крови) легочной патологии выполняется у пациентов с поражением легких.
· Рекомендовано проведение компьютерной томографии головного мозга (КТ) или магнитно-резонансной томографии (МРТ) головного мозга (при наличии общемозговой или очаговой неврологической симптоматики) при манифестных формах ЦМВИ у пациентов с иммуносупрессией [2, 21].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: В остром периоде, когда имеются симптомы интоксикации, лихорадка, выполнение КТ головного мозга или МРТ головного мозга позволяет провести дифференциальную диагностику с менингоэнцефалитом, опухолями мозга, сосудистыми изменениями и т.д. Определяют сливающиеся мелкие очаги в перивентрикулярной области, стволе головного мозга, расширение боковых желудочков.
· Рекомендовано проведение регистрации электрокардиограммы и электрокардиографических исследований при наличии признаков поражения сердечно-сосудистой системы [5, 160, 161]
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4).
Комментарии: ЦМВ может быть причиной «идиопатических» миокардитов и миоперикардитов у пациентов без иммуносупрессии. При иммунодефицитных состояниях у больных манифестной ЦМВИ нередко наблюдают развитие дилатационной кардиопатии.
· Рекомендовано пациентам с подозрением на манифестную форму ЦМВИ и признаками поражения центральной нервной системы проведение спинномозговой пункции (спинномозговая пункция, микроскопическое исследование спинномозговой жидкости, подсчет клеток в счетной камере (определение цитоза), исследование уровня белка в спинномозговой жидкости, исследование уровня глюкозы в спинномозговой жидкости) для оценки характера и выраженности воспалительного процесса и проведения дифференциальной диагностики [1, 2, 5].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарии: Поражение центральной нервной системы характерно для пациентов с ВИЧ-инфекцией.
· Рекомендовано выполнение эзофагогастродуоденоскопии и колоноскопии при наличии признаков поражения органов желудочно-кишечного тракта при манифестных формах ЦМВИ у пациентов с иммуносупрессией [21, 29, 30, 31].
Для эзофагогастродуоденоскопии уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Для колоноскопии уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
Комментарии: Эндоскопический осмотр (эзофагогастродуоденоскопия, колоноскопия) при не тяжелом общем состоянии пациента, рекомендуется проводить амбулаторно с использованием местной аппликационной анестезии.
ЦМВ – основной этиологический фактор язвенных дефектов пищеварительного тракта у больных ВИЧ-инфекцией. Патологический процесс локализуется в пищеводе, толстой кишке, реже – в терминальном отделе тонкой кишки и желудке, описаны случаи поражения глотки, слизистой ротовой полости, языка. Типичными признаками ЦМВ-эзофагита служат лихорадка, затруднение при глотании, загрудинная боль при прохождении пищевого комка, отсутствие эффекта противогрибковой терапии, наличие неглубоких округлых язв и/или эрозий в дистальном отделе пищевода. Поражение желудка ЦМВ-этиологии характеризуется сочетанием симптомов интоксикации и наличием острых или подострых язв в центре полиповидных образований в различных отделах желудка. Клиническая картина ЦМВ-колита или энтероколита характеризуется значительным снижением массы тела, лихорадкой, диареей, постоянными болями в животе, болезненностью толстой кишки при пальпации. Колоноскопия выявляет эрозии и изъязвления слизистой оболочки толстой кишки.
2.5 Иные диагностические исследования
На этапе постановки диагноза:
· Рекомендуется определение ДНК цитомегаловируса (Cytomegalovirus) в биоптатах и пунктатах из очагов поражения органов и тканей методом ПЦР, качественное исследование и морфологическое (гистологическое) исследование тканей почки (патолого-анатомическое исследование биопсийного (операционного) материала почек) у пациентов с эзофагитом, колитом, поражением легких, поражением почек [1, 2, 5, 9, 21, 85, 86, 87].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: При гистологическом исследовании биопсийных материалов (патолого-анатомическое исследование биопсийного (операционного) материала почек) выявляют характерные воспалительные изменения в органах и наличие специфических цитомегалоклеток (окраска гематоксилином и эозином). Обнаружение цитомегалоклеток – гигантских клеток с крупным ядром, узкой каймой цитоплазмы и внутриядерными вирусными включениями – при гистологическом исследовании биопсийных и аутопсийных материалов является безусловным подтверждением цитомегаловирусной природы органной патологии. Чувствительность стандартного гистологического метода диагностики ЦМВ-инфекции не превышает 50%. Для повышения чувствительности и специфичности метода дополнительно исследуют гистологические препараты на наличие в тканях вирусного антигена или ДНК ЦМВ методом ПЦР (определение ДНК цитомегаловируса (Cytomegalovirus) в биоптатах и пунктатах из очагов поражения органов и тканей методом ПЦР, качественное исследование)
· При наличии признаков нарушения зрения, неврологической симптоматики, изменений при инструментальных методах исследования рекомендуются консультации смежных специалистов – офтальмолога (прием (осмотр, консультация) врача-офтальмолога первичный), невролога (прием (осмотр, консультация) врача-невролога первичный), акушера-гинеколога (прием (осмотр, консультация) врача-акушера-гинеколога беременной первичный, повторный или диспансерный прием (осмотр, консультация) врача-акушера-гинеколога) [1, 2, 5, 65].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
· Рекомендуется выполнение спинномозговой пункции при наличии общемозговой или очаговой неврологической симптоматики, определение ДНК цитомегаловируса (Cytomegalovirus) в спинномозговой жидкости методом ПЦР, качественное исследование, исследование уровня белка в спинномозговой жидкости, микроскопическое исследование спинномозговой жидкости, подсчет клеток в счетной камере (определение цитоза) [1, 2, 3, 5, 21, 67, 113].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: Диагностическая спинномозговая (люмбальная) пункция выполняется при наличии менингеальных или очаговых симптомов, подозрении на поражение головного мозга (спинномозговая пункция, микроскопическое исследование спинномозговой жидкости, подсчет клеток в счетной камере (определение цитоза), исследование уровня белка в спинномозговой жидкости, исследование уровня глюкозы в спинномозговой жидкости), исследованием ликвора на наличие ДНК ЦМВ (определение ДНК цитомегаловируса (Cytomegalovirus) в спинномозговой жидкости методом ПЦР, качественное исследование).
· Рекомендуется выполнение пункции плевральной полости под контролем ультразвукового исследования при наличии признаков экссудативного плеврита [1, 2, 5, 9, 63, 64, 65, 66, 113]
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
2.6 Дифференциальная диагностика
При мононуклеозоподобном заболевании у взрослых постановка диагноза острой ЦМВИ требует исключения инфекций, вызываемых другими герпесвирусами (вирус Эпштейна-Барр (ВЭБ), вирусами герпеса 6 и 7 типов), острой ВИЧ-инфекции, а также стрептококкового тонзиллита и дебюта онкогематологического заболевания [1, 2, 5, 9].
В случае наличия патологии органов дыхания дифференциальный диагноз ЦМВ-пневмонии проводят с бактериальным бронхитом, респираторно-синцитиальной вирусной инфекцией (РС-инфекция), коклюшом, трахеобронхитом, вызванным микоплазменной или хламидийной пневмонией.
У взрослых, имеющих иммуносупрессию, манифестную ЦМВИ следует дифференцировать с пневмоцистной пневмонией, туберкулезом, грибковыми и герпетическими инфекциями, бактериальным сепсисом.
При развитии у пациента выраженных нейрокогнитивных расстройств диагноз следует дифференцировать между ЦМВ-энцефаловентрикулитом, ВИЧ-энцефалитом, многоочаговой лейкоэнцефалопатией, нейросифилисом.
Полинейропатия и полирадикулопатия ЦМВ-этиологии требует дифференцировки с полирадикулопатией, вызванной герпесвирусами 2 и 6 типов, синдромом Гийена-Барре, токсической полинейропатией, связанной с приемом лекарственных средств, алкоголя, наркотических психотропных веществ.
При наличии ретинита, хориоретинита проводят дифференциальный диагноз между ЦМВИ, токсоплазмозом, вирусными заболеваниями, вызываемыми вирусом простого герпеса (ВПГ), и вирусом Varicella Zoster (VZV).
3. Лечение, включая медикаментозную и немедикаментозную терапии, диетотерапию, обезболивание, медицинские показания и противопоказания к применению методов лечения
На выбор тактики лечения оказывают влияние следующие факторы [1, 2, 4, 9, 62, 63, 65, 66, 70, 113, 130]:
· период болезни;
· клиническая форма болезни;
· тяжесть заболевания;
· возраст больного;
· наличие и характер осложнений;
· доступность и возможность выполнения лечения в соответствии с необходимым видом оказания медицинской помощи;
· период беременности и лактации.
3.1 Консервативное лечение
3.1.1 Этиотропная (противовирусная) терапия
Цели лечения:
· подавление репликации вируса;
· снижение тяжести и продолжительности болезни;
· предотвращение развития осложнений.
· Рекомендовано пациентам с ослабленной иммунной системой/с иммунодефицитом (в т.ч. при СПИД, иммунодефиците, связанном с трансплантацией органов или химиотерапией) при первичном эпизоде болезни или рецидиве назначение противовирусного лечения для минимизации осложнений и сокращения сроков заболевания/рецидива, а также рецидивов в дальнейшем [1, 2, 4, 5, 9, 62, 63, 65, 66, 70].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
· Противовирусная терапия с использованием ганцикловира** для подавления репликации вируса рекомендуется в качестве метода выбора для лечения цитомегаловирусной инфекции (ЦМВ) пациентов с иммунодефицитом, с манифестными формами (ЦМВ-болезнь) при первичном эпизоде заболевания или рецидиве ЦМВИ [1, 2, 4, 5, 9, 62, 89, 90, 92, 113].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4).
Комментарии:
Ганцикловир** является одним из наиболее эффективных, но при этом и сложных в применении препаратов. Противовирусный эффект обусловлен образованием в пораженных вирусом клетках ганцикловиртрифосфата, тормозящего синтез вирусной ДНК в результате двух механизмов: конкурентного ингибирования ДНК-полимеразы и прямого включения в вирусную ДНК (последнее прекращает ее элонгацию). Фосфорилированный ганцикловир** сохраняется в цитоплазме в течение нескольких дней. Его назначают при цитомегаловирусной инфекции, осложнённой тяжёлыми органными патологиями у пациентов с иммунодефицитом, а также для профилактики ЦМВ заболеваний у пациентов с медикаментозной иммуносупрессией (например, после трансплантации органов или химиотерапии по поводу злокачественного новообразования). При активной ЦМВ-инфекции ганцикловир** назначают внутривенно из расчета 5 мг/кг, растворив в 100 мл натрия хлорида** или 5% раствора декстрозы**, в течение одного часа 2 раза в сутки. Продолжительность лечения определяют индивидуально, ориентируясь на исчезновение симптомов заболевания и ДНК ЦМВ из крови (определения ДНК цитомегаловируса (Cytomegalovirus) методом ПЦР в периферической и пуповинной крови, качественное исследование).
· Рекомендуется длительность индукционного курса #ганцикловира** от 2 до 6 недель: при поражении легких или пищеварительного тракта – 4 нед, при патологии ЦНС – 6 нед и более [5].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарии:
Пациентам c ВИЧ-инфекцией и медикаментозной иммуносупрессией (например, после трансплантации органов или химиотерапии по поводу злокачественного новообразования) после прохождения курса лечения манифестной ЦМВИ для профилактики рецидива назначают поддерживающую терапию – #ганцикловир** 5 мг/кг 1 раз в сутки в/в капельно в течение часа ежедневно длительностью не менее одного месяца [5].
· Противовирусная терапия с использованием валганцикловира** для подавления репликации вируса рекомендуется в качестве метода выбора пациентам с ЦМВ-ретинитом у пациентов со СПИДом [5].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарии:
Валганцикловир** – противовирусный препарат прямого действия (пролекарство) – L-валиловый эфир ганцикловира**, после приема внутрь быстро превращающийся в ганцикловир** под действием кишечных и печеночных эстераз.
При ЦМВ-ретините назначают валганцикловир** по 900 мг (2 таблетки) 2 раза в сутки в течение 21 дня; поддерживающая терапия – по 900 мг 1 раз в сутки. Поддерживающее лечение у больных ВИЧ-инфекцией, перенесших ЦМВ-ретинит, проводится на фоне АРВТ до момента повышения количества СD4-лифоцитов более 100 кл/мкл, сохраняющегося не менее 3 мес. При рецидиве заболевания проводится повторный курс индукционной терапии.
· С целью профилактики развития ЦМВИ у пациентов из группы риска после трансплантации солидных органов в качестве превентивной терапии активной ЦМВИ рекомендован валганцикловир** по 900 мг в сутки длительностью до 100-200 дней (в зависимости от типа органа) посттрансплантационного периода для подавления репликации вируса [1, 2, 4, 9, 62, 63].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарий: Критерии прекращения терапии – отсутствие ДНК ЦМВ в крови (определения ДНК цитомегаловируса (Cytomegalovirus) методом ПЦР в периферической и пуповинной крови, качественное исследование).
· Беременным с ослабленным иммунитетом или иммунодефицитом при наличии клинической симптоматики ЦМВИ с признаками острой или активной ЦМВИ рекомендовано введение иммуноглобулина человека антицитомегаловирусного [1, 2, 5, 66, 69, 96].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарий: Иммуноглобулин человека антицитомегаловирусный оказывает иммуномодулирующее действие, повышает содержание в организме антител против ЦМВ человека. Он сочетает высокую эффективность и почти полное отсутствие токсичности и противопоказаний. При наличии клинической симптоматики ЦМВИ иммуноглобулин человека антицитомегаловирусный вводят в разовой дозе 1 мл/кг массы тела каждые 48 часов до исчезновения клинических симптомов. Превентивная терапия при острой или активной ЦМВИ во время беременности (наличие ДНК ЦМВ в крови или наличие ДНК ЦМВ в моче в сочетании с анти-ЦМВ IgM) проводится введением #иммуноглобулина человека антицитомегаловирусного по 1 мл/кг в сутки внутривенно трехкратно с интервалом в 2 недели [5]. Иммуноглобулин человека антицитомегаловирусный вводят внутривенно (перед введением раствор нагревают до комнатной температуры или температуры тела), с начальной скоростью 0,08 мл/кг массы тела/час в течение 10 минут. В случае возникновения нежелательных реакций должна быть снижена скорость введения препарата или инфузия должна быть прекращена. При хорошей переносимости препарата скорость введения можно постепенно увеличить максимум до 0,8 мл/кг массы тела/час и сохранять ее до конца введения. Критерии прекращения терапии – отсутствие ДНК ЦМВ в крови (определения ДНК цитомегаловируса (Cytomegalovirus) методом ПЦР в периферической и пуповинной крови, качественное исследование).
3.1.2 Патогенетическая и симптоматическая терапия
· Рекомендовано проведение дезинтоксикационной, метаболической, антиоксидантной терапии при манифестных формах ЦМВ-болезни при интоксикационном синдроме, клинике органной дисфункции [1, 2, 5, 9].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарии: Дезинтоксикационная терапия направлена на купирование синдрома интоксикации, ее объем зависит от степени тяжести пациента. Метаболическая терапия влияет на обмен веществ в организме. Схема назначения адеметионина**, начальная терапия: рекомендуемая доза составляет 5-12 мг/кг/сут внутривенно или внутримышечно в течение 2 недель, с последующим переходом на таблетированную форму по 800-1600 мг/сут в день на протяжении 2-4 недель.
Основными задачами симптоматических средств является купирование воспалительных и токсических проявлений заболевания, предупреждение развития осложнений.
4. Медицинская реабилитация и санаторно-курортное лечение, медицинские показания и противопоказания к применению методов медицинской реабилитации, в том числе основанных на использовании природных лечебных факторов
4.1 Реабилитация
Реабилитационные мероприятия должны начинаться уже в периоде разгара или в периоде ранней реконвалесценции и носить комплексный характер с участием различных специалистов и с применением разнообразных методов воздействия, в зависимости от формы заболевания и вовлеченных органов и систем. При этом учитываются скорость и степень восстановления функционального состояния и профессионально-значимых функций переболевших (косвенными и прямыми методами). Важны постепенность возрастания дозированных физических и умственных нагрузок, а также дифференцированное применение различных методов воздействия.
5. Профилактика и диспансерное наблюдение, медицинские показания и противопоказания к применению методов профилактики
5.1 Диспансерное наблюдение
· Пациентам с активной и манифестной ЦМВИ на фоне беременности рекомендовано диспансерный прием (осмотр, консультация) врача-инфекциониста в медицинской организации по месту жительства или в территориальном специализированном центре с проведением комплексного клинико-лабораторного обследования до родоразрешения с обязательным определением ДНК цитомегаловируса (Cytomegalovirus) методом ПЦР в периферической и пуповинной крови, качественное исследование, определением ДНК цитомегаловируса (Cytomegalovirus) в моче методом ПЦР, качественное исследование 1 раз в 3 месяца [1, 2, 5, 113, 130].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
· Пациентам после пересадки костного мозга, других органов в первый год после трансплантации не реже одного раза в месяц рекомендуется определение ДНК цитомегаловируса (Cytomegalovirus) методом ПЦР в периферической и пуповинной крови, качественное исследование [1, 2, 5, 113, 130].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
· Больным ВИЧ-инфекцией, имеющим количество СD4-лимфоцитов <100 кл./мкл, рекомендован прием (осмотр, консультация) врача-офтальмолога первичный и повторный и определение ДНК цитомегаловируса (Cytomegalovirus) методом ПЦР в периферической и пуповинной крови, качественное исследование не реже одного раза в 3 мес. [1, 2, 5, 113, 130].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
5.2 Профилактика
Специфическая профилактика ЦМВ-инфекции в настоящее время не разработана [1, 2, 4, 9, 13, 16, 113].
· Рекомендовано информирование серонегативных по ЦМВ женщин, планирующих беременность или уже беременных, об источниках и путях инфицирования (половые контакты с серопозитивным партнером, физический контакт при ежедневном уходе за ребенком дома или профессиональный контакт с детьми младшего возраста в стационарах, домах ребенка, детских дошкольных учреждениях). [65, 66, 69, 103, 104, 105, 106, 126].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4).
· Для снижения риска первичного заражения или реинфекции ЦМВ беременным, не имеющим специфических антител IgG, рекомендовано использование барьерных контрацептивов при половых контактах, соблюдение правил личной гигиены после смены пеленок или после прикосновения к игрушкам, испачканным слюной или мочой детей, избегание пользования одной посудой с ребенком, поцелуев в губы детей грудного возраста, которые могут выделять вирус со слюной [65, 66, 69, 103, 104, 105, 106, 126].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4).
· Рекомендован временный перевод серонегативных беременных на работу, не связанную с опасностью их заражения вирусом [135].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
· Рекомендуется проведение вторичной профилактики ЦМВИ противовирусными препаратами системного действия пациентам с ВИЧ-инфекцией, пациентам с медикаментозной иммуносупрессией (например, после трансплантации органов или химиотерапии по поводу злокачественного новообразования) с целью предотвращения возникновения повторного эпизода инфекции после перенесенной[5].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарии: Проведение вторичной профилактики противовирусными препаратами системного действия начинается сразу после завершения курса лечения инфекции. Отмена поддерживающей терапии рекомендуется не ранее чем через 6 месяцев, после восстановления иммунитета и достижения уровня CD4 более 200-250 клеток/мкл.
6. Организация оказания медицинской помощи
Форма помощи
Медицинская помощь оказывается в форме:
· экстренной медицинской помощи;
· неотложной медицинской помощи;
· плановой медицинской помощи.
Условия оказания медицинских услуг
Медицинская помощь оказывается в виде:
· первичной медико-санитарной помощи;
· скорой, в том числе скорой специализированной, медицинской помощи;
· специализированной, в том числе высокотехнологичной, медицинской помощи.
Медицинская помощь взрослым больным с ЦМВИ может оказываться в следующих условиях:
· амбулаторно (в условиях, не предусматривающих круглосуточное медицинское наблюдение и лечение);
· в дневном стационаре (в условиях, предусматривающих медицинское наблюдение и лечение в дневное время, не требующих круглосуточного медицинского наблюдения и лечения);
· стационарно (в условиях, обеспечивающих круглосуточное медицинское наблюдение и лечение).
Первичная медико-санитарная помощь пациентам оказывается в амбулаторных условиях и в условиях дневного стационара.
Первичная доврачебная медико-санитарная помощь в амбулаторных условиях осуществляется в фельдшерско-акушерских пунктах.
Первичная врачебная медико-санитарная помощь осуществляется врачом-терапевтом участковым, врачом общей практики (семейным врачом) в амбулаторных условиях.
Первичная специализированная медико-санитарная помощь осуществляется врачом-инфекционистом медицинской организации, оказывающим медицинскую помощь пациентам в амбулаторных условиях.
Специализированная, в том числе высокотехнологичная, медицинская помощь оказывается в условиях стационара врачами-инфекционистами и другими врачами-специалистами и включает в себя профилактику, диагностику, лечение заболеваний и состояний, требующих использования специальных методов и сложных медицинских технологий, а также медицинскую реабилитацию.
Лечение пациентов осуществляется в условиях стационара по направлению врача-терапевта участкового, врача общей практики (семейного врача), врача-инфекциониста, медицинских работников, выявивших ЦМВИ.
7. Дополнительная информация (в том числе факторы, влияющие на исход заболевания или состояния)
7.1 Ко-инфекция ЦМВ/ВИЧ
Особую значимость приобретает ЦМВ-инфекция связи с распространением ВИЧ-инфекции среди взрослого населения. Как оппортунистическая инфекция из группы герпетических, она лидирует (в том числе и в России) по частоте и значимости, развиваясь более чем у 40% больных на поздних стадиях ВИЧ. При обследовании ВИЧ-инфицированных лиц, употребляющих наркотические вещества внутривенно при общей ЦМВ-инфицированности в 80% в большинстве случаев выявлены низкоавидные антитела, указывающие на сравнительно недавние сроки инфицирования данным вирусом.
При ослаблении клеточного иммунитета в результате ВИЧ-инфекции цитомегаловирус реактивируется и вызывает клинически выраженную инфекцию. У взрослых с ВИЧ-инфекцией ЦМВ проявляется в виде генерализованной формы с разнообразными поражениями органов и систем. Данное заболевание встречается преимущественно у пациентов, не получавших лечения, чаще всего они узнают о ВИЧ-инфекции на момент установления диагноза ЦМВ-инфекции. В процесс могут быть вовлечены центральная нервная система, лёгкие, печень, почки, желудочно-кишечный тракт, мочеполовая система [1, 2, 3, 5, 20, 21, 22, 23, 24, 51, 59, 73, 74, 83, 93, 113, 130].
Наиболее часто диагностируют ретинит, интерстициальную пневмонию, энтероколиты, воспалительные процессы различных отделов половых органов (чаще у женщин), энцефалиты, гепатит. При полиорганных поражениях заболевание отличает тяжёлое течение, оно может принимать черты сепсиса. Исход часто неблагоприятный.
Ретинит выявляют у 30-40% больных СПИДом, у которых содержание лимфоцитов CD4 в крови составляет менее 50 в мкл. Задержки в диагностике и лечении ЦМВ-ретинита всегда угрожают потерей зрения. При нарушениях зрения практически во всех случаях имеются поражения такой степени, которые не могут подвергаться полному обратному развитию даже на фоне адекватной терапии. Таким образом, ЦМВ-ретинит даже сегодня остается опасным заболеванием, независимо от того, что внедрение АРВТ привело к улучшению общего прогноза. Исход ЦМВ-ретинита в 40% случаев – слепота, несмотря на интенсивное лечение, т.к. терапия ЦМВ-инфекции может остановить прогрессирование процесса, но не вызвать его обратное развитие.
При уровне CD4+ менее 100 клеток/мкл основным дифференциальным диагнозом является хориоретинит, вызванный Toxoplasma gondii. При уровне CD4+ более 100 клеток/мкл ЦМВ-ретинит можно практически исключить, при этом более вероятны другие вирусные инфекции, а также нейросифилис.
ЦМВ-энцефалит развивается у ВИЧ-инфицированных при снижении числа лимфоцитов CD4 менее 50 в мкл, проявляется клиникой СПИД-деменции. Энцефалит часто и быстро прогрессирует, сопровождается нарушением функций черепных нервов, нистагмом, головными болями с лихорадкой. Кроме того, возможно развитие вялотекущей энцефалопатии, которая заканчивается слабоумием и полирадикуломиелопатией.
Форма с поражением надпочечников встречается у 60% ВИЧ-инфицированных пациентов с манифестной ЦМВ-инфекцией.
Дифференциальная диагностика ЦМВ-инфекции довольно затруднительна из-за отсутствия или разнообразия клинических проявлений. У больных с иммунодефицитом манифестную цитомегаловирусную инфекцию следует дифференцировать с пневмоцистной пневмонией, туберкулёзом, токсоплазмозом, микоплазменной пневмонией, бактериальным сепсисом, нейросифилисом, прогрессирующей многоочаговой лейкоэнцефалопатией, лимфопролиферативными заболеваниями, грибковыми и герпетическими инфекциями, ВИЧ-энцефалитом. Полинейропатия и полирадикулопатия цитомегаловирусной этиологии требует дифференцировки с полирадикулопатией, вызванной герпесвирусами, синдромом Гийена-Барре, токсической полинейропатией, связанной с приёмом лекарств, алкоголя и наркотических, психотропных веществ. При наличии ретинита, хориоретинита проводят дифференциальный диагноз между ЦМВ-инфекцией, токсоплазмозом, ВПГ-инфекцией, ВВЗ-инфекцией.
Таблица 1. Дифференциальный диагноз болезни, вызванной ВИЧ с проявлениями ЦМВ заболевания с другими инфекциями ВИЧ-инфицированных
|
Перечень критериев диагностики |
Болезнь, вызванная ВИЧ, с проявлениями ЦМВИ |
Болезнь, вызванная ВИЧ, с проявлениями токсоплазмоза |
Болезнь, вызванная ВИЧ, с проявлениями пневмоцистной пневмонии |
Болезнь, вызванная ВИЧ, с проявлениями туберкулеза |
|
Инкубационный период |
15-90 дней |
14-15 дней |
10 недель |
2-5 дней |
|
Температура |
фебрильная |
длительный субфебрилитет |
субфебрилитет, сменяющийся лихорадкой |
постоянная или интермиттирующая лихорадка |
|
Синдром интоксикации |
выражен |
вариабелен |
выражен |
выражен |
|
Поражение лимфоузлов |
генерализованная лимфаденопатия |
генерализованная лимфаденопатия |
не характерно |
увеличение лимфатических узлов (преимущественно шейных и подмышечных, реже паховых |
|
Поражения других органов и систем |
гепатолиенальный синдром |
поражение сердечно-сосудистой системы (миокардит) |
поражение сердечно-сосудистой системы |
перикардит |
|
Поражение ЦНС |
деменция, вентрикулоэнцефалит, вялотекущая энцефалопатия, восходящая полирадикуломиелопатия (миелорадикулит) |
энцефалит, очаговая симптоматика: гемипарезы, поражение черепно-мозговых нервов, афазия, очаговые эпилептические припадки, поражение сенсорной системы |
менингит |
менингизм, очаговые неврологические нарушения |
|
Поражения глаз |
ретинит, при осмотре глазного дна: периваскулярные желтовато-белые инфильтраты + кровоизлияния в сетчатку |
хориоретинит, без геморрагического компонента, на сетчатке множественные очаги белого или кремового цвета на сетчатке |
не характерно |
не характерно |
|
Поражение ЖКТ |
эзофагит, колит, язвенные поражения, склонны к прободению и кровотечению |
не характерно |
не характерно |
энтероколит |
|
Поражение легких |
пневмонит, интерстициальные инфильтраты, затенения на рентгенограмме легких |
не характерно |
одышка в покое и непродуктивный кашель; диффузные билатеральные прикорневые инфильтраты, распространяющиеся от корней легких к периферии |
прикорневая лимфоаденопатия, милиарные высыпания, наличие преимущественно интерстициальных изменений и образованием плеврального выпота |
|
Поражение почек |
белок в моче, увеличение количества эпителиальных клеток |
не характерно |
не изменены |
не характерно |
|
Поражение надпочечников |
снижение функциональной активности надпочечников |
не характерно |
не характерно |
не характерно |
|
Уровень CD4, клеток/мкл |
менее 50 |
менее 200-100 |
менее 200 |
не зависит |
7.2 ЦМВ-инфекция у реципиентов солидных органов и костного мозга
В отсутствие профилактики ЦМВ-инфекция может развиваться у 25% пациентов после трансплантации почки, 35% – после трансплантации печени, тонкой кишки и сердца, 50% – после трансплантации поджелудочной железы, 80% – после трансплантации легких. При несвоевременной диагностике и неадекватном лечении ЦМВИ представляет реальную угрозу жизни реципиентам органов.
У пациентов с трансплантированными органами выделяют:
· цитомегаловирусную инфекцию (подтвержденная репликация вируса без клинических симптомов);
· цитомегаловирусную болезнь (подтвержденная репликация ЦМВ в сочетании с соответствующими симптомами), которая подразделяется на:
o «цитомегаловирусный синдром» (лихорадка, недомогание, лейкопения и/или тромбоцитопения);
o «тканево-инвазивную болезнь» (тяжелая форма заболевания с вирусным поражением различных органов и тканей).
Существует 3 основных эпидемиологических варианта ЦМВ-инфекции у больных с трансплантированными органами:
· первичная инфекция, развивающаяся у ЦМВ-серонегативных больных, получивших трансплантат от серопозитивных доноров – D+R- (частота ЦМВИ составляет до 60%);
· реактивация латентного эндогенного вируса, когда донор серонегативен по ЦМВ, а реципиент серопозитивен – D-R+ (частота ЦМВИ – 10-15%);
· суперинфекция, когда и донор, и реципиент серопозитивны, а активный ЦМВ имеет донорское происхождение – D+R+ (у 25-30% больных развивается ЦМВИ).
ЦМВ не только вызывает тяжелые органные поражения (прямое действие вируса) у иммунокомпрометированных больных, но и обладает рядом «непрямых» эффектов – общих и трансплантат-специфических. Следует учитывать, что непрямые эффекты ЦМВ могут реализовываться при длительно сохраняющемся невысоком уровне вирусной нагрузки, который обычно не сопровождается возникновением прямых эффектов.
Возможные непрямые эффекты ЦМВ у реципиентов солидных органов:
1. Трансплантат-специфические эффекты:
o Острое отторжение трансплантата;
o Хроническая нефропатия аллотрансплантата и/или потеря ренального трансплантата;
o Ускоренный возврат вирусного гепатита C после трансплантации печени;
o Тромбоз печеночной артерии после трансплантации печени;
o Васкулопатия трансплантата после трансплантации печени;
o Облитерирующий бронхиолит после трансплантации легких.
2. Общие непрямые эффекты ЦМВ (повышение риска):
o Бактериальные инфекции;
o Грибковые инфекции;
o Другие вирусные инфекции;
o Посттрансплантационные лимфопролиферативные заболевания;
o Сердечно-сосудистые осложнения;
o Посттрансплантационный сахарный диабет;
o Преждевременное иммунологическое старение;
o Летальность.
Факторы риска развития ЦМВ-инфекции после трансплантации почки:
1. Особенности претрансплантационного цитомегаловирусного серологического статуса донора и реципиента. Наиболее высок риск развития активной ЦМВИ при сочетании донора, имеющего специфические антитела к ЦМВ (инфицированного вирусом), и реципиента без антител к ЦМВ в сыворотке крови (D+/R–). Однако и варианты D+/R+ (и у донора, и у реципиента есть антитела к ЦМВ), D–/R+ (антитела только у реципиента) не исключают развития ЦМВИ.
2. Любое повышение интенсивности иммуносупрессии, например, очень высокие концентрации в крови циклоспорина** или такролимуса**, применение больших доз иммунодепрессантов (микофенолатов – код по АТХ: L04AA, селективные иммунодепрессанты, других иммунодепрессантов – код по АТХ: L04AX) в качестве индукционной иммуносупрессии или лечения криза отторжения.
3. Тяжелые сопутствующие заболевания.
4. Выраженное снижение количества лейкоцитов периферической крови.
5. Гипогаммаглобулинемия – только для реципиентов сердца и легких, но не для реципиентов почки или печени.
Наиболее высок риск развития ЦМВ-инфекции и ЦМВИ в первые 6 месяцев после трансплантации, однако возможны эпизоды поздней ЦМВ-инфекции – через 6 – 12 месяцев и даже через несколько лет после операции, особенно после окончания плановой анти-ЦМВ профилактики, на фоне других тяжелых инфекционных осложнений, при лечении отторжения трансплантата.
· Рекомендуется перед проведением трансплантации с целью оценки риска заболевания реципиента в посттрансплантационном периоде ЦМВИ определение антител классов M, G (IgM, IgG) к цитомегаловирусу (Cytomegalovirus) в крови у донора и реципиента [162].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
Комментарий: Если претрансплантационное обследование реципиента дало отрицательный результат, необходимо его повторить во время трансплантации. У взрослых пациентов с сомнительными результатами серологического обследования результат донора должен считаться положительным, а результат потенциального реципиента должен тщательно интерпретироваться для выделения группы больных с наиболее высоким риском ЦМВИ. Интерпретация претрансплантационного серологического обследования может быть сложной у доноров и потенциальных реципиентов с недавними гемотрансфузиями в анамнезе.
Поскольку у реципиентов органов начало лечения ЦМВ-инфекции в стадии развернутых клинических проявлений недостаточно эффективно, основную роль играет предупреждение заболевания, которое снижает частоту ЦМВИ и нивелирует «непрямые» эффекты вируса. Существуют две стратегии предупреждения ЦМВ-инфекции:
· превентивная (упреждающая) терапия и профилактика, причем существуют значительные различия применения этих стратегий в разных центрах трансплантации;
· комбинированная (гибридная) стратегия – сочетание профилактики с последующей превентивной терапией.
· Рекомендуется определение ДНК цитомегаловируса (Cytomegalovirus) методом ПЦР в периферической и пуповинной крови, количественное исследование с целью диагностики ЦМВ-инфекции после трансплантации органов [1, 2, 5].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарий: определение ДНК цитомегаловируса (Cytomegalovirus) методом ПЦР в периферической и пуповинной крови, является предпочтительным методом диагностики ЦМВ-инфекции после трансплантации органов, принятия решения о проведении превентивной терапии и мониторинга ответа на лечение в связи с возможностью стандартизировать этот метод исследования. Стратегия превентивной терапии предусматривает регулярный мониторинг (1 раз в неделю) определения ДНК цитомегаловируса (Cytomegalovirus) методом ПЦР в периферической и пуповинной крови, количественного исследования и немедленное назначение лечения при обнаружении большого числа копий ДНК вируса.
· Рекомендуется проведение иммуногистохимического выявления возбудителей инфекций с целью диагностики тканево-инвазивной ЦМВИ (патолого-анатомическое исследование биопсийного (операционного) материала печени с применением иммуногистохимических методов) [1, 2, 5].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарий: Патолого-анатомическое исследование биопсийного (операционного) материала печени с применением иммуногистохимических методов не имеет большого значения в диагностике тканево-инвазивной болезни, но может быть полезным при поражении желудочно-кишечного тракта с отрицательным результатом ПЦР исследования крови.
Профилактика подразумевает назначение противовирусного препарата прямого действия в течение первых месяцев после трансплантации всем реципиентам группы высокого риска ЦМВ-инфекции. Профилактический прием эффективных в отношении ЦМВ противовирусных препаратов прямого действия не только предотвращает развитие цитомегаловирусного синдрома и ЦМВИ, но и снижает риск развития других герпетических инфекций (в том числе вызванных вирусами простого и опоясывающего герпеса), бактериальных и протозойных инфекций, а также риск смерти от любой причины. Достоинствами противовирусной профилактики является высокая эффективность, влияние на непрямые эффекты ЦМВ и простота применения, недостатком – относительно высокая стоимость.
В различных центрах для профилактики ЦМВ-инфекции у пациентов с медикаментозной иммуносупрессией используют ганцикловир** внутривенно, валганцикловир** – внутрь для профилактики ЦМВ-инфекции после трансплантации солидных органов; значительно реже, у пациентов с подавленной медикаментами иммунной системой, в частности после трансплантации органов, – иммуноглобулин человека антицитомегаловирусный.
Дозы ганцикловира** и валганцикловира** требуют обязательной коррекции в соответствии с функцией нефронов пациента по клиренсу креатинина по формуле, которая указана в инструкции. Эта коррекция крайне важна, особенности для пациентов с трансплантированной почкой, поскольку нередко наблюдается отсроченная или не оптимальная функция почечного аллотрансплантата. Реципиенты не почечных трансплантатов также могут иметь сниженную почечную функцию. Применение полных доз противовирусных препаратов прямого действия у таких пациентов может сопровождаться развитием серьезных нежелательных явлений.
Продолжительность медикаментозной профилактики ЦМВ-инфекции является важным аспектом. Трехмесячная профилактика валганцикловиром** ЦМВ-инфекции после трансплантации почки является недостаточной. Оптимальная продолжительность профилактического приема валганцикловира** у больных с пересаженной почкой продолжается до 200-го дня посттрансплантационного периода (повышает бессобытийную выживаемость реципиентов и существенно снижает частоту ЦМВИ и цитомегаловирусной виремии).
Вторичная профилактика ЦМВ-инфекции валганцикловиром** необходима также после трансплантации солидных органов, ганцикловиром** – в случае использования иммунодепрессантов (микофенолатов – код по АТХ: L04AA, селективные иммунодепрессанты, других иммунодепрессантов – код по АТХ: L04AX). Стандартом является пероральный прием валганцикловира** в дозе 900 мг в сутки при функции нефронов по клиренсу креатинина ≥60 мл/мин, у пациентов с медикаментозной иммуносупрессией может быть использован ганцикловир** внутривенно в дозе 5 мг/кг в сутки.
7.3 ЦМВ-инфекция у беременных
Вертикальная передача ЦМВ приводит к врожденной ЦМВИ, являющейся наиболее частой среди ВУИ, поражая 0,5-2% всех новорожденных. В Соединенных Штатах ЦМВ вызывает врожденные дефекты примерно у 1 из 200 новорожденных. Врожденная ЦМВИ служит основной негенетической причиной врожденной сенсоневральной тугоухости, различных серьезных неврологических нарушений, может приводить к смерти плода или новорожденного [137, 146]. Однако вопрос систематического скрининга беременных женщин и новорожденных на ЦМВ все еще обсуждается во многих странах [133, 134]. В последнее время достигнуты успехи в терапии и профилактике врожденной ЦМВИ, связанные с противовирусным лечением беременных женщин и детей грудного возраста, внедрением программ скрининга беременных и новорожденных на ЦМВ, диагностикой осложнений среди инфицированных детей [137, 139, 141, 153, 154].
Врожденная ЦМВИ развивается как в результате острой первичной инфекции у матери, так и вследствие реактивации материнской инфекции из латентного течения в активное, или в результате повторного заражения матери. В высокосеропозитивных популяциях значительный риск вертикальной передачи связан именно с реактивацией ЦМВ и/или реинфекцией во время беременности. При этом, из-за большого числа серопозитивных людей, увеличивается и риск первичной ЦМВ-инфекции у серонегативных женщин [151, 152]. У 35% серопозитивных по специфическому IgG женщин, обследовавшихся в каждом триместре в течение беременности, цитомегаловирус хотя бы один раз обнаруживался методом ПЦР в биологических жидкостях (моча, слюна, вагинальные мазки, кровь) (определение ДНК цитомегаловируса (Cytomegalovirus) методом ПЦР в периферической и пуповинной крови, качественное исследование, определение ДНК цитомегаловируса (Cytomegalovirus) в моче методом ПЦР, качественное исследование, определение ДНК цитомегаловируса (Cytomegalovirus) в отделяемом из цервикального канала методом ПЦР, качественное исследование, определение ДНК цитомегаловируса (Cytomegalovirus) методом ПЦР в слюне, качественное исследование), и у 75% беременных в какой-то момент – в моче [149, 150]. Риск врожденной инфекции составляет 30-40% при острой первичной инфекции у матери и 1-2% при непервичных инфекциях. Вероятность передачи вируса увеличивается с гестационным возрастом. Однако тяжелые последствия для плода чаще встречаются, когда инфекция возникает до 20 недели беременности. Внутриутробная ЦМВИ может проявляться церебральными или экстрацеребральными аномалиями при ультразвуковом исследовании плода, задержкой роста плода и потерей плода. За последние десять лет риск первичной ЦМВ во время беременности возрос в отдельных странах Европы с 5,4 до 8,2% [151].
Только 5-10% новорожденных с врожденной ЦМВИ имеют характерные симптомы при рождении. Бессимптомные новорожденные, в том числе рожденные от матерей с непервичными инфекциями, также подвержены риску отдаленных последствий, которые чаще развиваются в первые 1-2 года жизни и могут продолжаться до 5-7 лет. В 40-60% случаев у них развивается нейросенсорная тугоухость, когнитивный дефицит, нарушение зрения [147]. Наибольший риск развития неврологических осложнений наблюдается после первичной инфекции в первом триместре. В этой связи, серологическое тестирование (определение антител классов M, G (IgM, IgG) к цитомегаловирусу (Cytomegalovirus) в крови) женщины до 14 недель беременности имеет решающее значение для выявления первичной инфекции [137].
Диагностический поиск врожденной ЦМВ-инфекции проводят в случаях выявления на пренатальном ультразвуковом исследовании плода отставания развития плода для срока гестации, повышенной эхогенности кишечника, выпотов или любых церебральных аномалий. Чувствительность рутинного ультразвукового исследования плода для прогнозирования симптомов у новорожденных низкая и составляет около 25%, но повторные ультразвуковые исследования плода и магнитно-резонансная томография плода (A05.30.015) заведомо инфицированных плодов демонстрируют чувствительность более 95% для выявления аномалий головного мозга [137].
Пренатальное выявление врожденной ЦМВ-инфекции помогает предотвратить отдаленные неврологические осложнения. Анализ ПЦР на ДНК ЦМВ в амниотической жидкости (определение ДНК цитомегаловируса (Cytomegalovirus) в амниотической жидкости методом ПЦР, количественное исследование) является золотым стандартом диагностики внутриутробной ЦМВ-инфекции. Присутствие ДНК ЦМВ в секрете шейки матки матери служит прогностическим признаком возникновения врожденной ЦМВ-инфекции у беременных с положительным IgM ЦМВ. Отрицательный результат амниоцентеза у беременных с ЦМВ-инфекцией гарантирует отсутствие инсульта у плода и отдаленных последствий для ребенка, даже если передача инфекции имела место [140, 145, 154].
Профилактика материнской ЦМВ-инфекции в настоящее время основывается на гигиенических мерах, санитарно-просветительской работе, информировании родителей о необходимости избегать контакта с биологическими жидкостями инфицированных людей, особенно детей, систематическом проведении гигиены рук. В Европе и США первичное инфицирование в первом триместре в основном наблюдается у молодых рожавших женщин, у которых уже есть ребенок младше 3 лет.
Активно разрабатываются медицинские методы профилактики снижения риска вертикальной передачи, такие как гипериммунные глобулины против цитомегаловируса (иммуноглобулин человека антицитомегаловирусный – J06BB09) и применение противовирусных препаратов (противовирусные препараты прямого действия – J05A) [128, 137, 138]. В ряде систематических обзоров с метаанализом показано, что пренатальное введение #валацикловира беременным с материнской ЦМВ-инфекцией может снизить риск врожденной ЦМВИ, даже при инфицировании в первом триместре. Беременные, получавшие #валацикловир, имели значительно более низкий риск врожденной ЦМВ-инфекции у плода по сравнению с беременными, не получавшими #валацикловир [141]. #Валацикловир, вводимый с момента постановки диагноза первичной инфекции, снижал частоту вертикальной передачи с 29,8% до 11,1%. В открытом исследовании фазы II пероральный прием #валацикловира (8 г/сут), назначаемый беременным женщинам с легкими симптомами врожденной ЦМВИ плода, увеличивал вероятность рождения бессимптомного новорожденного до 82%, по сравнению с нелеченой исторической когортой – 43 % [137]. Однако, безопасность применения #валацикловира в период беременности продолжает оцениваться, препарат не может быть рекомендован для рутинного назначения.
· Рекомендуется у беременных для выявления риска врожденной ЦМВИ плода обратить внимание на анамнез (сбор акушерско-гинекологического анамнеза и жалоб) и уточнить следующие вопросы: отягощенный акушерский анамнез (выкидыши, антенатальная гибель плода, мертворожденность и др.); отягощенный гинекологический анамнез (цервицит, эктопия шейки матки, хронический эндометрит и т.д.); перенесенные в период беременности мононуклеозоподобные заболевания [163].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
· Рекомендуется при обследовании беременных для выявления активной ЦМВИ и степени риска вертикальной передачи вируса плоду:
- определение антител классов M, G (IgM, IgG) к цитомегаловирусу (Cytomegalovirus) в крови;
- при отсутствии IgG, но наличии IgМ к цитомегаловирусу (Cytomegalovirus) - повторное определение антител классов M, G (IgM, IgG) к цитомегаловирусу (Cytomegalovirus) в крови через 14 дней;
- определение индекса авидности антител класса G (IgG avidity) к цитомегаловирусу (Cytomegalovirus) в крови при их одновременном обнаружении с анти-ЦМВ IgM в первом исследовании крови (определении антител класса M (IgM) к цитомегаловирусу (Cytomegalovirus) в крови) или при наличии признаков острой инфекционной патологии;
- определение ДНК цитомегаловируса (Cytomegalovirus) методом ПЦР в периферической (и пуповинной крови), количественное исследование при подозрении на острую или активную ЦМВИ;
- определение ДНК цитомегаловируса (Cytomegalovirus) в моче методом ПЦР, количественное исследование при подозрении на активную ЦМВИ;
определение ДНК цитомегаловируса (Cytomegalovirus) в отделяемом из цервикального канала методом ПЦР, качественное исследование [1, 2, 5].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Цель терапии у беременных – предупреждение генерализации инфекции и внутриутробного заражения плода.
Диагноз первичного материнского ЦМВ при беременности должен основываться на сероконверсии во время беременности (появление de novo вирусоспецифического иммуноглобулина G (IgG) в сыворотке беременных, которые ранее были серонегативными при определении антител класса G (IgG) к цитомегаловирусу (Cytomegalovirus) в крови) или на обнаружении специфических иммуноглобулинов M (IgM) и IgG (определение антител классов M, G (IgM, IgG) к цитомегаловирусу (Cytomegalovirus) в крови) в сочетании с низкой авидностью IgG (определение индекса авидности антител класса G (IgG avidity) к цитомегаловирусу (Cytomegalovirus) в крови).
Критерии оценки качества медицинской помощи
|
№ п/п |
Критерии качества |
Оценка выполнения Да/нет |
|
1 |
Пациентам с манифестными формами ЦМВИ выполнен общий (клинический) анализ крови, с дифференцированным подсчетом лейкоцитов (лейкоцитарная формула) и исследованием уровня тромбоцитов в крови |
Да/нет |
|
2 |
При подозрении на манифестную форму ЦМВИ выполнен общий (клинический) анализ мочи |
Да/нет |
|
3 |
При подозрении на манифестную форму ЦМВИ выполнен анализ крови биохимический общетерапевтический (исследование уровня общего билирубина, уровня свободного и связанного билирубина, определение активности аланинаминотрансферазы и аспартатаминотрансферазы (АЛТ, АСТ), гамма-глютамилтрансферазы (ГГТ), щелочной фосфатазы (ЩФ) в крови, исследование уровня мочевины, креатинина, альфа-амилазы в крови) |
Да/нет |
|
4 |
При подозрении на манифестную форму ЦМВИ определение протромбинового (тромбопластинового) времени в крови или плазме или коагулограммы (ориентировочного исследования системы гемостаза) |
Да/нет |
|
5 |
При подозрении на манифестную форму ЦМВИ выполнено определение антител классов M, G (IgM, IgG) к цитомегаловирусу (Cytomegalovirus) в крови, а также определение индекса авидности антител класса G (IgG avidity) к цитомегаловирусу (Cytomegalovirus) в крови при помощи иммуноферментного анализа (ИФА), твердофазного хемилюминисцентного иммуноферментного метода или иммуноблота (ИБ) |
Да/нет |
|
6 |
Всем пациентам с подозрением на острую и активную ЦМВИ выполнено определение ДНК цитомегаловируса (Cytomegalovirus) методом ПЦР в периферической (и пуповинной) крови, качественное исследование |
Да/нет |
|
7 |
Иммунокомпрометированным пациентам с клиникой острого поражения дыхательной системы с подозрением на острую и активную ЦМВИ выполнено определение ДНК цитомегаловируса (Cytomegalovirus) в мокроте, бронхоальвеолярной лаважной жидкости методом ПЦР, качественное исследование |
Да/нет |
|
8 |
Всем пациентам с манифестной формой ЦМВИ с клиникой острого поражения центральной нервной системы выполнено определение ДНК цитомегаловируса (Cytomegalovirus) в спиномозговой жидкости методом ПЦР, качественное исследование |
Да/нет |
|
9 |
Всем пациентам с манифестной формой ЦМВИ и клинико-лабораторными признаками поражения почек, а также беременным с признаками острой или активной ЦМВИ с клиникой острого поражения мочевыделительной системы выполнено определение ДНК цитомегаловируса (Cytomegalovirus) в моче методом ПЦР, качественное исследование |
Да/нет |
|
10 |
Всем пациентам с подозрением на острую и активную ЦМВИ с клиникой острого сиалоаденита: выполнено определение ДНК цитомегаловируса (Cytomegalovirus) методом ПЦР в слюне, качественное исследование |
Да/нет |
|
11 |
Всем беременным с подозрением на острую и активную ЦМВИ выполнено определение ДНК цитомегаловируса (Cytomegalovirus) в отделяемом из цервикального канала методом ПЦР, качественное исследование |
Да/нет |
|
12 |
Всем пациентам с манифестными формами ЦМВИ с признаками поражения печени (повышение уровня общего билирубина, АЛТ, АСТ) выполнено ультразвуковое исследование органов брюшной полости (комплексное) |
Да/нет |
|
13 |
Всем пациентам при манифестных формах ЦМВИ и при наличии признаков поражения органов дыхательной системы выполнена рентгенография легких цифровая |
Да/нет |
|
14 |
Всем пациентам с иммуносупрессией при манифестных формах ЦМВИ и при наличии признаков поражения легких выполнена спиральная компьютерная томография легких |
Да/нет |
|
15 |
Всем пациентам с подозрением на острую и активную ЦМВИ выполнена регистрация электрокардиограммы и электрокардиографические исследования при наличии признаков поражения сердечно-сосудистой системы |
Да/нет |
|
16 |
Проведена противовирусная терапия с использованием ганцикловира** для лечения цитомегаловирусной инфекции (ЦМВ) пациентов с иммунодефицитом |
Да/нет |
|
17 |
Проведена противовирусная терапия с использованием валганцикловира** для лечения ЦМВ-ретинита у взрослых пациентов со СПИДом |
Да/нет |
Список литературы
1. Шахгильдян В.И. Цитомегаловирусная инфекция в кн. «Лекции по инфекционным болезням: в 2 т./Н.Д. Ющук, Ю.Я. Венгеров. 4-е изд., перераб. и доп. М.: ГЭОТАР-Медиа. 2016: Т.2, 592 с.
2. Шахгильдян В.И. Цитомегаловирусная инфекция в «Вирусные болезни: учебное пособие / под ред. Н.Д. Ющука. М.: ГЭОТАР-Медиа, 2016: 540 с.
3. Львов Д.К. Руководство по вирусологии: Вирусные инфекции человека и животных. М.: Издательство «МИА», 2013: 1200 с.
4. Исаков В.А., Архипова Е.И., Исаков Д.В. Герпесвирусные инфекции человека. Руководство для врачей. СПб.: Спецлит, 2006: 302 с.
5. Инфекционные болезни: национальное руководство / под ред. Н.Д Ющука, Ю.Я. Венгерова. – 3-е изд., перераб. и доп. – М.: ГЭОТАР-Медиа, 2021. – 1104с.
6. Кистенева Л.Б. Цитомегаловирусная инфекция как проблема перинатальной патологии: этиология, патогенез, диагностика. Российский вестник перинатологии и педиатрии 2003; 4: С.55 – 60.
7. Kosugi I. Cytomegalovirus (CMV). Virus 2010; 60(2): Р. 209 – 220.
8. Гусева Л.Н., Рогова Л.А., Егорова Н.Ю. и др. Цитомегаловирусная инфекция (ЦМВИ): классификация и варианты течения. Детские инфекции. 2003; 1: С. 57 – 61.
9. Скворцов В.В., Мязин Р.Г., Емельянов Д.Н. Цитомегаловирусная инфекция в клинике внутренних болезней. Лечащий врач 2004; 9: С. 8 –11.
10. Sylwester A.W., Mitchell B.L., Edgar J.B. et al. Broadly targeted human cytomegalovirus-specific CD4+ and CD8+ T cells dominate the memory compartments of exposed subjects. J Exp Med. 2005; 202: Р.673.
11. Gillespie G.M., Wills M.R., Appay V. et al. Functional heterogeneity and high frequencies of cytomegalovirus-specific CD 8(+) T lymphocytes in healthy seropositive donors. J Virol. 2000; 74: Р.8140.
12. Корсакова И.И., Пашанина Т.П., Елизарова В.В. Основные параметры иммунного статуса у лиц с цитомегаловирусной инфекцией. Эпидемиология и инфекционные болезни. 2004; 3: С. 32 – 34.
13. Gandhi M.K., Khanna R. Human cytomegalovirus: clinical aspects, immune regulation, and emerging treatments. Lancet Infect Dis. 2004; 4: Р.725.
14. Gervasi M.T., Romero R., Bracalente G. et al. Viral invasion of the amniotic cavity (VIAC) in the midtrimester of pregnancy. Matern Fetal Neonatal Med. 2012; 25(10): Р.2002 – 2013.
15. Van den Berg A. P., van der Bij W., van Son W. J. Cytomegalovirus antigenemia as a useful marker of symptomatic cytomegalovirus infection after renal transplantation – report of 130 consequtive patients. Transplantation 1989; 48: Р. 991 – 996.
16. Ликарь Ю.Н., Пашанов Е.Д., Масчан А.А. Цитомегаловирусная инфекция после трансплантации гемопоэтических стволовых клеток (обзор литературы). Вопросы гематологии, онкологии и иммунопатологии в педиатрии. 2005; 4(2): С. 49 – 55.
17. Halfon Ph., Berger P., Khiri H. et al. Algorithm based on CMV kinetics DNA viral load for preemptive therapy initiation after hematopoietic cell transplantation. J. Med. Virol. 2011; 83(3): Р. 490 – 495.
18. Zhang X., Fan J., Yang M.F. et al. Monitoring of human cytomegalovirus infection in bone marrow and liver transplant recipients by antigenaemia assay and enzyme-linked immunosorbent assay. J. Int. Med. Res. 2009; 37(1): Р. 31 – 36.
19. Козлова А.В., Сюткин В.Е., Чжао А.В. Цитомегаловирусная инфекция и трансплантация печени. Инфекционные болезни. 2010; 3: С.46 – 52.
20. Долгих Т.И., Черешнев В.А., Назарова О.Г. Распространенность и диагностика оппортунистических инфекций, вызванных цитомегаловирусом и парвовирусом В19 у больных с вторичными иммунодефицитами. Эпидемиология и инфекционные болезни. 2004;4: С. 24 – 27.
21. Степанова Е.В. Герпесвирусные заболевания и ВИЧ-инфекция. Часть II. ВИЧ-инфекция и иммуносупрессии. 2010; 2 (1): С. 23 – 36.
22. Jabs D.A., Van Natta M.L., Kempen J.H. et al. Characteristics of patients with cytomegalovirus retinitis in the era of highly active antiretroviral therapy. Am. J. Ophthalmol.2000; 133: Р 48 – 61.
23. Teoh S.C., Wang P.X., Wong E.P. The epidemiology and incidence of cytomegalovirus retinitis in the HIV population in Singapore over 6 years. Invest. Ophthalmol. Vis. Sci. 2012; 53 (12): P. 7546 – 7552.
24. Amedia S.C., Penalva de Oliveira A.C., Vilas-Boas L. et al. Neurologic cytomegalovirus complications in patients with AIDS: Retrospective review of 13 cases and review of the literature. Rev. Inst. Med. Trop. S. Paulo. 2010; 52(6): Р. 303 – 310.
25. Squizzato A., Ageno W., Cattaneo A. et al. A case report and literature review of portal vein thrombosis associated with cytomegalovirus infection in immunocompetent patients. Clin Infect Dis. 2007; 44:e13.
26. Spahr L., Cerny A., Morard I. et al. Acute partial Budd-Chiari syndrome and portal vein thrombosis in cytomegalovirus primary infection: a case report. BMC Gastroenterol. 2006; 6: Р.10.
27. Clarke J., Craig R.M., Saffro R. et al. Cytomegalovirus granulomatous hepatitis. Am J Med. 1979; 66:Р.264.
28. Bonkowsky H.L., Lee R.V., Klatskin G.. Acute granulomatous hepatitis. Occurrence in cytomegalovirus mononucleosis. JAMA. 1975; 233: Р.1284.
29. Bobak D.A. Gastrointestinal Infection Caused by Cytomegalovirus. Current Infectious Disease Reports. 2003; 5: P. 101 – 107.
30. Kaniel A., Lashner B. Cytomegalovirus colitis complicating inflammatory bowel disease. Am. Journal Gastroenterology. 2006;101:P. 2857 – 2865.
31. Барышников Е.Н., Дроздов В.Н., Шулятьев И.С., Парфенов А.И. Цитомегаловирусная инфекция у больных язвенным колитом. Экспериментальная и клиническая гастроэнтерология. 2010; 10: С.25 – 28.
32. Cunha B.A. Cytomegalovirus pneumonia: community-acquired pneumonia in immunocompetent hosts. Infect. Dis. Clin. North Am. 2010; 24 (1): Р.147 – 158.
33. Шахгильдян В.И. Цитомегаловирусная инфекция. В кн. «Пневмония». Под ред. Чучалина А.Г., Синопальникова А.И., Страчунского Л.С. М.: ООО «Медицинское информационное агентство», 2006: 444 с.
34. Chee S.P., Jap A. Cytomegalovirus anterior uveitis: Outcome of treatment. Br. J. Ophthalmol. 2010; 94(12): Р. 1648 – 1652.
35. Orlikowski D., Porcher R., Sivadon-Tardy V. et al. Guillain-Barré syndrome following primary cytomegalovirus infection: a prospective cohort study. Clin Infect Dis. 2011; 52:Р.837.
36. Steininger C., Popow-Kraupp T., Seiser A. et al. Presence of cytomegalovirus in cerebrospinal fluid of patients with Guillain-Barre syndrome. J Infect Dis. 2004; 189: Р.984.
37. Lurain N.S., Hanson B.A., Martinson J. et al. Virological and immunological characteristics of human cytomegalovirus infection associated with Alzheimer disease. J Infect Dis. 2013; 208:Р.564.
38. Kytö V., Vuorinen T., Saukko P. et al. Cytomegalovirus infection of the heart is common in patients with fatal myocarditis. Clin Infect Dis. 2005; 40: Р.683.
39. Blum A., Giladi M., Weinberg M. et al. High anti-cytomegalovirus (CMV) IgG antibody titer is associated with coronary artery disease and may predict post-coronary balloon angioplasty restenosis. Am J Cardiol. 1998; 81: Р.866.
40. Colomba C., Lalicata F., Siracusa L. et al. Cytomegalovirus infection in immunocompetent patients. Clinical and immunological considerations. Infez. Med. 2012; 20 (1): P. 12 – 15.
41. Eddleston M., Peacock S., Juniper M. et al. Severe cytomegalovirus infection in immunocompetent patients. Clin Infect Dis. 1997; 24: Р.52.
42. Heininger A, Jahn G., Engel C. et al. Human cytomegalovirus infections in nonimmunosuppressed critically ill patients. Crit Care Med. 2001; 29:Р.541.
43. De Vlieger G., Meersseman W., Lagrou K. et al. Cytomegalovirus serostatus and outcome in nonimmunocompromised critically ill patients. Crit Care Med. 2012; 40: Р.36.
44. Ho M. Epidemiology of cytomegalovirus infections. Rev Infect Dis. 1990; 12 Suppl 7:S701.
45. Выдумкина С.П., Зазимко Л.А., Кузенкова А.В. Частота острой цитомегаловирусной инфекции среди лиц разных возрастных групп. Вопр. вирусол. 1999;1: С.19 – 20.
46. Down J.B. Family poverty is associated with cytomegalovirus antibody titeris in U.S. children. Health Psychol. 2012; 31(1): Р. 5 – 10.
47. Staras S.A., Dollard S.C., Radford K.W. et al. Seroprevalence of cytomegalovirus infection in the United States, 1988 – 1994. Clin Infect Dis 2006; 43: Р.1143.
48. Bate S.L., Dollard S.C., Cannon M.J. Cytomegalovirus seroprevalence in the United States: the national health and nutrition examination surveys, 1988 – 2004. Clin Infect Dis 2010; 50: Р.1439.
49. Luvira V., Chamnanchanunt S., Bussaratid V. et al. Seroprevalence of latent cytomegalovirus infection among elderly Thais. Southeast Asian J. Trop. Med. Publ. Hlth. 2012; 43(6): Р.1419 – 1425.
50. Lopo S. Seroprevalence to cytomegalovirus in the Portuguese population, 2002 – 2003. Euro Surveill. 2011; 23(16): Р. 25 – 28.
51. De França T.R., de Albuquerque Tavares Carvalho A., Gomes V.B. Salivary shedding of Epstein-Barr virus and cytomegalovirus in people infected or not by human immunodeficiency virus 1.Clin. Oral Investig. 2012; 16 (2): P. 659 – 664.
52. Handsfield H.H., Chandler S.H., Caine V.A. et al. Cytomegalovirus infection in sex partners: evidence for sexual transmission. J Infect Dis. 1985; 151: Р.344.
53. Jordan M.C., Rousseau W.E., Noble G.R. et al. Association of cervical cytomegaloviruses with venereal disease. N Engl J Med. 1973; 288: Р.932.
54. Викулов Г.Х. Герпесвирусные инфекции человека в новом тысячелетии: классификация, эпидемиология и медико-социальное значение. Эпидемиология и инфекционные болезни. Актуальные вопросы. 2014; 3: 35 – 40.
55. Tolpin M.D., Stewart J.A., Warren D. et al. Transfusion transmission of cytomegalovirus confirmed by restriction endonuclease analysis. J Pediatr. 1985; 107: Р.953.
56. Prince A.M., Szmuness W., Millian S.J. et al. A serologic study of cytomegalovirus infections associated with blood transfusions. N Engl J Med. 1971; 284: Р.1125.
57. Colugnati F.A., Staras S.A., Dollard S.C., Cannon M.J. Incidence of cytomegalovirus infection among the general population and pregnant women in the United States. BMC Infect Dis 2007; 7: Р.71.
58. Kenneson A., Cannon M.J. Review and meta-analysis of the epidemiology of congenital cytomegalovirus (CMV) infection. Rev. Med. Virol. 2007;17 (4): Р.253 – 276.
59. Stadler L.P., Bernstein D.I., Callahan S.T. et al. Seroprevalence of cytomegalovirus (CMV) and risk factors for infection in adolescent males. Clin Infect Dis 2010; 51:e76.
60. Adler S.P. Molecular epidemiology of cytomegalovirus: viral transmission among children attending a day care center, their parents, and caretakers. J Pediatr. 1988; 112: Р.366.
61. Blackman J.A., Murph J.R., Bale J.F. Jr. Risk of cytomegalovirus infection among educators and health care personnel serving disabled children. Pediatr Infect Dis J. 1987; 6:Р.725.
62. Sissons J. G. P., Carmishael A. J. Clinical aspects and management of cytomegalovirus infection. J. Infection.2002; 44: P. 78 – 83.
63. Шульженко А.Е. Герпетические инфекции человека: перспективы диагностики и противовирусной терапии. Цитокины и воспаление. 2005; 3: C. 76 – 81.
64. Ross S.A., Novak Z., Pati S. et al. Diagnosis of Cytomegalovirus Infections. Infect Disord Drug Targets. 2011;11(5): Р.466 – 474.
65. Кистенева Л.Б., Мартынов К.А., Хижнякова Т.М. и др. Цитомегаловирусная инфекция у беременных. Диагностика, трактовка результатов обследования. Вопросы вирусологии. 2003; 48 (6): С. 4 – 8.
66. Кузьмин В.Н. Диагностика, лечение и профилактика цитомегаловирусной инфекции у беременных. Лечащий врач. 2002;11: С. 22 – 25.
67. Griffits P.D. Diagnosis of cytomegalovirus infection. The Journal of Antimicrobal Chemotheraphy. 1989; 23 (Suppl. E): Р.11 – 16.
68. Каражас Н.В., Рыбалкина Т.Н., Евсеева Л.Ф. Лабораторная диагностика цитомегаловирусной инфекции. Журнал микробиологии, эпидемиологии и иммунологии. 2000; 8: С. 15 – 16.
69. Bonalumi S., Trapanese A., Santamaria A. et al. Cytomegalovirus infection in pregnancy: review of the literature. Journal of Prenatal Medicine 2011;5(1): Р.1 – 8.
70. Revello M.G., Gerna G. Diagnosis and management of human cytomegalovirus infection in the mother, fetus and newborn infant. Clin. Microbiol. Rev.2002; 15(4): P.680 – 715.
71. Szenborn L. Significance of diagnostics and treatment in preventing congenital infections with Toxoplasma gondii (Tg), cytomegalovirus (CMV) and parvowirus B19 (PVB19). Przegl. Lek. 2010; 67 (1): Р.54 – 57.
72. Эбрамидзе Л.Н., Ведунова С.Л., Мальцева Н.Н. Иммуноферментная тест-система для выявления низкоавидных иммуноглобулинов G -антител к цитомегаловирусу человека («Цитомегаловирус-диагностикум») – перспективный подход к диагностике первичной герпетической инфекции. Вопросы вирусологии. 2004; 2: С. 46 – 49.
73. Шахгильдян В. И., Шипулина О. Ю., Каpажас Н. В. и др. Лабоpатоpная диагностика цитомегаловиpусной инфекции у ВИЧ-инфицированных пациентов. Эпидемиология и инфекционные болезни. 2001;1: С. 36 – 40.
74. Шахгильдян В.И., Шипулина О.Ю., Сильц В.В., и др. Значение лабораторных маркеров активной репликации цитомегаловируса у ВИЧ-инфицированных беременных женщин при оценке риска врожденной и внутриутробной цитомегаловирусной инфекции. Эпидемиология и инфекционные болезни 2004;4: С.30 – 34.
75. Leung J., Cannon M.J., Grosse S.D., Bialek S.R. Laboratory testing for cytomegalovirus among pregnant women in the United States: a retrospective study using administrative claims data BMC Infectious Diseases. 2012; 12: Р.334.
76. Leung J., Cannon M.J., Grosse S.D., Bialek S.R. Laboratory testing and diagnostic coding for cytomegalovirus among privately insured infants in the United States: a retrospective study using administrative claims data. BMC Pediatrics 2013;13: Р. 90.
77. Eisen H.N., Siskin G. M. Variation in affinities of antibodyes during the immune respons. Biochemisry. 1964; 3: P. 966 – 1008.
78. Jiang H., Wen L., Ling X. Diagnostic value of human cytomegalovirus late m RMA dertection inactive intrauterine infection. Clin. Med. J. 2002;115 (1): Р. 1507 – 1509.
79. Lassaroto T., Gall C. Envaluation of the Abbott Ax SYM cytomegalovirus IgG assay in conjunction with other CMV JgM tests and CMV JgG-avidity assay. Clin. Diagn. Lab. Immunol. 2001;1: P. 196 – 199.
80. Alves Bonon S. H., Rossi C. L., De Souza C. A. Comparison of serology, antigenemia assay for the polymerase chain reaction for monitoring active cytomegalovirus infections in hematopoietic stem cell transplantation patients. Rev. Inst. Med. Trop. S. Paulo. 2006; 48(5): Р. 275 – 278.
81. Aspin M.M., Gallez-Hawkins G.M., Guigni T.D., et al. Comparison of plasma PCR and bronchoalveolar lavage fluid culture for detection of cytomegalovirus infection in adult bone marrow transplant recipients. J Clin Microbiol 1994; 32: Р. 2266 – 2269.
82. Fregmuth F., Gennetay E., Petitjean J. et al. Comparison of nested PCR for detection of DNA in plasma with PP65 leucocytic antigenemia procedure for diagnosis human cytomegalovirus infection. J Clin Microbiol 1994; 32: Р. 1614 – 1618.
83. Hansen K.K., Ricksten A., m Hoffmann B. et al. Detection of cytomegalovirus DNA in serum correlstes with clinical cytomegalovirus retinitis in AIDS. J. Infect. Dis., 1994; 170: Р. 1271 – 1274.
84. Drew W.L. Cytomegalovirus resistance testing: pitfalls and problems for the clinician. Clin. Infect. Dis. 2010;50 (5): Р.733 – 736.
85. Макарова Н. Е. Получение моноклональных антител к сверхранним белкам цитомегаловируса человека и их применение для выявления инфицированных клеток. Вопр. вирусологии. 1996; 41(1): С. 28 – 32.
86. Paradowska E., Prezikevich M., Nowakowska D. Detection of cytomegalovirus in human placental cells by polymerase chain reaction.APMIS. 2006; 114 (11): P. 764 – 771.
87. Меджидова А. А. Сравнение различных методов лабораторной диагностики при выявлении цитомегаловируса в аутопсийном материале умерших новорожденных и детей, умерших на первом году жизни. ЖМЭИ. 2000; 3 (2):С. 63 – 69.
88. Reed Е.С., Bowden R.A., Dandliker P.S. et al. Treatment of cytomegalovirus pneumonia with ganciclovir and intravenous cytomegalovirus immunoglobulin in patients with bone marrow transplants. Ann Intern Med 1988; 15: Р. 783 – 788.
89. Laing R.B., Dykhuizen R.S., Smith C.C. et al. Parenteral ganciclovir treatment of acute CMV infection in the immunocompetent host. Infection 1997; 25: Р.44.
90. Serna-Higuera C., González-García M., Milicua J.M. et al. Acute cholestatic hepatitis by cytomegalovirus in an immunocompetent patient resolved with ganciclovir. J Clin Gastroenterol. 1999; 29:Р.276.
91. Buonuomo P.S., Maurizi P., Valentini P. et al. Successful treatment with oral valganciclovir in immunocompetent infant with gastrointestinal manifestations of cytomegalovirus infection. J Perinatol. 2006; 26:Р.648.
92. Fernández-Ruiz M., Muñoz-Codoceo C., López-Medrano F. et al. Cytomegalovirus myopericarditis and hepatitis in an immunocompetent adult: successful treatment with oral valganciclovir. Intern Med. 2008; 47:Р.1963.
93. Шахгильдян В.И., Галина М.В., Шамшурина М.К., Сильц В.В. Первый случай применения валганцикловира для лечения цитомегаловирусной инфекции у ВИЧ-инфицированной беременной женщины. Эпидемиология и инфекционные болезни 2008;3: С.60-65.
94. Jonjic S., Pavic J., Polic В. et al. Antibodies are not essential for the resolution of primary cytomegalovirus infection but limit dissemination of recurrent virus. J Exp Med 1994; 179(5): Р. 1713 – 1717.
95. Andereoni K.J., Nang X., Huang S.-M., Huang E.S. Human cytomegalovirus hyperimmune globuli not only neutralizes HCMV infectivity but also inhibits HCMV-induced intracellular NF-KB. J Med Virol. 2002; 67(1): Р. 33 – 40.
96. Чешик С.Г., Кистенева Л.Б., Стаханова В.М. и др. Диагностика и лечение цитомегаловирусной инфекции у беременных женщин. Инфекционные болезни. 2005; 3 (2): С. 31 – 36.
97. Баринский И.Ф., Алимбарова Л.М. Препараты для лечения герпетической инфекции. Российские аптеки. 2005; 71 (1): С. 30 – 33.
98. Исаков В.А., Исаков Д.В. Иммуномодуляторы в терапии и профилактике герпесвирусных инфекций. Клиническая медицина. 2015; 93(4): С. 16 – 24.
99. Змушко Е.И., Шувалова Е.Е., Кацалуха В.В., Старенченко В.В. Сравнительная оценка эффективности индукторов интерферона при экспериментальной генерализованной герпетической инфекции. Инфекционные болезни. 2014; 12(2): С. 59 – 63.
100. Зуйкова И.Н., Шульженко А.Е., Щубелко Р.В. Коррекция цитокиновых нарушений у пациентов с хронической рецидивирующей герпесвирусной инфекцией. Фарматека. 2014;10 (283): С. 48 – 54.
101. Bonaros N., Mayer B., Schachner N. et al. CMV-hyperimmune globulin for preventing cytomegalovirus infection and disease in solid organ transplant recipients: a metaanalysis. Clin. Transplant. 2008; 22(1): Р. 89 – 87.
102. Sia I., Patel R. New strategies for prevention and therapy of cytomegalovirus infection and disease in solid-organ transplant recipients. Clin Microbiol Rev 2000; (1): Р. 83 – 121.
103. Walker S.P., Palma-Dias R., Wood E. et al. Cytomegalovirus in pregnancy: to screen or not to screen. BMC Pregnancy and Childbirth 2013,13: Р. 96.
104. Carlson A., Norwitz E.R., Stiller R.J. Cytomegalovirus Infection in Pregnancy: Should All Women Be Screened? Rev Obstet Gynecol. 2010;3(4):Р.172 – 179.
105. Ornoy A. Fetal Effects of Primary and Non-primary Cytomegalovirus Infection in Pregnancy: Are we Close to Prevention? IMAJ 2007, May, 9: Р.398 – 401.
106. Johnson J., Anderson B., Pass RF. Prevention of Maternal and Congenital Cytomegalovirus Infection. Clin Obstet Gynecol. 2012 June; 55(2):Р.521 – 530.
107. Прокопенко Е.И., Щербакова Е.О., Ватазин А.В. и др. Результаты профилактики цитомегаловирусной инфекции валганцикловиром у пациентов с трансплантированной почкой. Клиническая нефрология. 2013;5: С. 37 – 41.
108. Hirsch H.H., Lautenschlager I., Pinsky B.A. et al. An international multicenter perfomance analysis of cytomegalovirus load tests // Clin Infect Dis. 2013. Vol. 56. P. 367.
109. Humar A., Limaye A.P., Blumberg E.A. et al. Extended valganciclovir prophylaxis in D+/R- kidney transplant recipients is associated with long-term reduction in cytomegalovirus disease: two-year results of the IMPACT study. Transplantation. 2010; 90: P. 1427.
110. Kidney Disease: Improving Global Outcomes (KDIGO) Transplant Work Group. KDIGO clinical practice guideline for the care of kidney transplant recipients. Am J Transplant. 2009; 9(Suppl 3): S1 – S157.
111. Kotton C.N., Kumar D., Caliendo A.M. et al. Updated international consensus guidelines on the managament of cytomegalovirus in solid-organ transplantation // Transplantation. 2013; 96: P. 333 – 360.
112. Rostaing L., Wéclawiak H., Mengelle C., Kamar N. Viral infections after kidney transplantation. Minerva Urol Nefrol. - 2011; 63(1): P. 59 – 71.
113. Городин В.Н. Жукова Л.И. Ковалевская О.И. Шахвердян Ю.Г. Цитомегаловирусная инфекция (учебно – методич. пособие). - Краснодар. - 2016.-112 с.
114. Limaye A.P., Stapleton R.D., Peng L. et al. Effect of ganciclovir on IL-6 levels among cytomegalovirus-seropositive adults with critical illness: a randomized clinical trial. JAMA. 2017; 318: 731-740
115. Tay M.R., Lim S.T., Tao M. et al. Cytomegalovirus infection and end-organ disease in Asian patients with lymphoma receiving chemotherapy. Leuk Lymphoma. 2014; 55: 182-187
116. Green M.L., Leisenring W., Xie H. et al. Cytomegalovirus viral load and mortality after haemopoietic stem cell transplantation in the era of pre-emptive therapy: a retrospective cohort study. Lancet Haematol. 2016; 3: e119-e127
117. Ljungman P., Boeckh M., Hirsch H.H. et al. Definitions of cytomegalovirus infection and disease in transplant patients for use in clinical trials. Clin Infect Dis. 2017; 64: 87-91
118. Kotton CN, Kumar D, Caliendo AM, et al. The Third International Consensus Guidelines on the Management of Cytomegalovirus in Solid-organ Transplantation. Transplantation 2018; 102:900.
119. Caliendo AM. The long road toward standardization of viral load testing for cytomegalovirus. Clin Infect Dis 2013; 56:374.
120. Hayden RT, Sun Y, Tang L, et al. Progress in Quantitative Viral Load Testing: Variability and Impact of the WHO Quantitative International Standards. J Clin Microbiol 2017; 55:423.
121. Lodding IP, Schultz HH, Jensen JU, et al. Cytomegalovirus Viral Load in Bronchoalveolar Lavage to Diagnose Lung Transplant Associated CMV Pneumonia. Transplantation 2018; 102:326.
122. Westall GP, Cristiano Y, Levvey BJ, et al. A Randomized Study of Quantiferon CMV-directed Versus Fixed-duration Valganciclovir Prophylaxis to Reduce Late CMV After Lung Transplantation. Transplantation 2019; 103:1005.
123. Fisher CE, Knudsen JL, Lease ED, et al. Risk Factors and Outcomes of Ganciclovir-Resistant Cytomegalovirus Infection in Solid Organ Transplant Recipients. Clin Infect Dis 2017; 65:57.
124. Khurana MP, Lodding IP, Mocroft A, et al. Risk Factors for Failure of Primary (Val)ganciclovir Prophylaxis Against Cytomegalovirus Infection and Disease in Solid Organ Transplant Recipients. Open Forum Infect Dis 2019; 6:ofz215.
125. Braccio S., Irwin A., Riordan A. et al. Acute infectious hepatitis in hospitalised children: a British Paediatric Surveillance Unit study. Arch Dis Child. 2017; 102: 624-628
126. Zheng QY, Huynh KT, van Zuylen WJ, Craig ME, Rawlinson WD. Cytomegalovirus infection in day care centres: A systematic review and meta-analysis of prevalence of infection in children. Rev Med Virol. 2019 Jan;29(1):e2011. doi:10.1002/rmv.2011.
127. Public Health England. Sexually transmitted infections (STIs): annual data tables. https://www.gov.uk/government/statistics/sexually-transmitted-infections-stis-annual-data-tables. Date accessed: October 9, 2018
128. Bartlett A.W., Hall B.M., Palasanthiran P., McMullan B., Shand A.W., Rawlinson W.D. Recognition, treatment, and sequelae of congenital cytomegalovirus in Australia: an observational study. J Clin Virol. 2018; 108: 121-125
129. Rawlinson W.D., Boppana S.B., Fowler K.B. et al. Congenital cytomegalovirus infection in pregnancy and the neonate: consensus recommendations for prevention, diagnosis, and therapy. Lancet Infect Dis. 2017; 17: e177-e188
130. Muldoon K.M., Armstrong-Heimsoth A., Thomas J. Knowledge of congenital cytomegalovirus (cCMV) among physical and occupational therapists in the United States. PLoS One. 2017; 12e0185635
131. Utah Department of Health. Cytomegalovirus (CMV) public health initiative. http://health.utah.gov/cshcn/programs/cmv.html (accessed Feb 10, 2017).
132. Akhter K., Wills T.S., Talavera F., King J.W. Cytomegalovirus (CMV)/ MedScape. Infectious Diseases Society of America. https://emedicine.medscape.com/article/215702-overview/ Updated: May 05, 2018.
133. Bolyard E, Tablan O, Williams W, Pearson M, Shapiro C, Deitchmann S. Guideline for infection control in health care personnel. Centers for Disease Control and Prevention. Infection Control and. Hosp Epidemiol. 1998;19:408–63;
134. Stagno S, Whitley R. Herpesvirus infections of pregnancy. Part 1: Cytomegalovirus and Epstein-Barr virus infections. N Engl J Med. 1985;313:1270–4).
135. Balegamire SJ, McClymont E, Croteau A, Dodin P, Gantt S, Besharati AA, Renaud C, Mâsse B, Boucoiran I. Prevalence, incidence, and risk factors associated with cytomegalovirus infection in healthcare and childcare worker: a systematic review and meta-analysis. Syst Rev. 2022 Jun 27;11(1):131. doi:10.1186/s13643-022-02004-4.
136. Trombetta CM, Viviani S, Montomoli E, Marchi S. Seroprevalence of antibodies to cytomegalovirus in pregnant women in the Apulia region (Italy). J Prev Med Hyg. 2021 Jul 30;62(2):E372-E376. doi: 10.15167/2421-4248/jpmh2021.62.2.1800.
137. Leruez-Ville M(1), Foulon I(2), Pass R(3), Ville Y(4). Leruez-Ville M, Foulon I, Pass R, Ville Y. Cytomegalovirus infection during pregnancy: state of the science. Am J Obstet Gynecol. 2020 Sep;223(3):330-349. doi: 10.1016/j.ajog.2020.02.018.
138. Lazzarotto T, Blázquez-Gamero D, Delforge ML, Foulon I, Luck S, Modrow S, Leruez-Ville M. Congenital Cytomegalovirus Infection: A Narrative Review of the Issues in Screening and Management From a Panel of European Experts. Front Pediatr. 2020 Jan 31;8:13. doi: 10.3389/fped.2020.00013.
139. Carmona AS, Kakkar F, Gantt S. Perinatal Cytomegalovirus Infection. Curr Treat Options Pediatr. 2022;8(4):395-411. doi: 10.1007/s40746-022-00261-y.
140. Tanimura K, Yamada H. Potential Biomarkers for Predicting Congenital Cytomegalovirus Infection. Int J Mol Sci. 2018 Nov 27;19(12):3760. doi:10.3390/ijms19123760
141. D'Antonio F, Marinceu D, Prasad S, Khalil A. Effectiveness and safety of prenatal valacyclovir for congenital cytomegalovirus infection: systematic review and meta-analysis. Ultrasound Obstet Gynecol. 2022 Dec 9. doi:10.1002/uog.26136
142. Sapuan S, Theodosiou AA, Strang BL, Heath PT, Jones CE. A systematic review and meta-analysis of the prevalence of human cytomegalovirus shedding in seropositive pregnant women. Rev Med Virol. 2022 Nov;32(6):e2399. doi:10.1002/rmv.2399
143. Iijima S. Pitfalls in the Serological Evaluation of Maternal Cytomegalovirus Infection as a Potential Cause of Fetal and Neonatal Involvements: A Narrative Literature Review. J Clin Med. 2022 Aug 26;11(17):5006. doi:10.3390/jcm11175006
144. El-Qushayri AE, Ghozy S, Abbas AS, Dibas M, Dahy A, Mahmoud AR, Afifi AM, El-Khazragy N. Hyperimmunoglobulin therapy for the prevention and treatment of congenital cytomegalovirus: a systematic review and meta-analysis. Expert Rev Anti Infect Ther. 2021 May;19(5):661-669. doi: 10.1080/14787210.2021.1846521
145. Chatzakis C, Sotiriadis A, Dinas K, Ville Y. Neonatal and long-term outcomes of infants with congenital cytomegalovirus infection and negative amniocentesis: systematic review and meta-analysis. Ultrasound Obstet Gynecol. 2023 Feb;61(2):158-167. doi: 10.1002/uog.26128
146. Yassine BB, Hulkower R, Dollard S, Cahill E, Lanzieri T. A Legal Mapping Assessment of Cytomegalovirus-Related Laws in the United States. J Public Health Manag Pract. 2022 Mar-Apr 01;28(2):E624-E629. doi: 10.1097/PHH.0000000000001401.
147. Şahiner F. Konjenital Sitomegalovirüs Enfeksiyonlarının Tanı ve Yönetiminde Güncel Yaklaşımlar ve Türkiye’deki Durum [Current Approaches in the Diagnosis and Management of Congenital Cytomegalovirus Infections and the Situation in Turkey]. Mikrobiyol Bul. 2020 Jan;54(1):171-190. Turkish. doi: 10.5578/mb.68978.
148. Gatta LA, Rochat E, Weber JM, Valencia S, Erkanli A, Dotters-Katz SK, Permar S, Hughes BL. Clinical factors associated with cytomegalovirus shedding among seropositive pregnant women. Am J Obstet Gynecol MFM. 2022 Mar;4(2):100560. doi:10.1016/j.ajogmf.2021.100560
149. Barbosa NG, Yamamoto AY, Duarte G, Aragon DC, Fowler KB, Boppana S, Britt WJ, Mussi-Pinhata MM. Cytomegalovirus Shedding in Seropositive Pregnant Women From a High-Seroprevalence Population: The Brazilian Cytomegalovirus Hearing and Maternal Secondary Infection Study. Clin Infect Dis. 2018 Aug 16;67(5):743-750. doi: 10.1093/cid/ciy166.
150. Gatta LA, Rochat E, Weber JM, Valencia S, Erkanli A, Dotters-Katz SK, Permar S, Hughes BL. Clinical factors associated with cytomegalovirus shedding among seropositive pregnant women. Am J Obstet Gynecol MFM. 2022 Mar;4(2):100560. doi:10.1016/j.ajogmf.2021.100560.
151. Gorun F, Motoi S, Malita D, Navolan DB, Nemescu D, Olariu TR, Craina M, Vilibic-Cavlek T, Ciohat I, Boda D, Dobrescu A. Cytomegalovirus seroprevalence in pregnant women in the western region of Romania: A large-scale study. Exp Ther Med. 2020 Sep;20(3):2439-2443. doi: 10.3892/etm.2020.8945. Epub 2020 Jun 25.
152. Zhou Q, Wang Q, Shen H, Zhang Y, Zhang S, Li X, Acharya G. Seroprevalence of Cytomegalovirus and Associated Factors Among Preconception Women: A Cross- Sectional Nationwide Study in China. Front Public Health. 2021 Aug 25;9:631411. doi: 10.3389/fpubh.2021.631411.
153. Fowler KB, Boppana SB. Congenital cytomegalovirus infection. Semin Perinatol. 2018 Apr;42(3):149-154. doi: 10.1053/j.semperi.2018.02.002. Epub 2018 Mar 2. PMID: 29503048.
154. Périllaud-Dubois C, Belhadi D, Laouénan C, Mandelbrot L, Picone O, Vauloup-Fellous C. Current practices of management of maternal and congenital Cytomegalovirus infection during pregnancy after a maternal primary infection occurring in first trimester of pregnancy: Systematic review. PLoS One. 2021 Dec 3;16(12):e0261011. doi: 10.1371/journal.pone.0261011
155. Deka S, Kalita D, Paul M, Badoni G, Mathuria YP. Seroprevalence and Determinants of ToRCH Pathogens in Pregnant Women in the Sub-Himalayan Region. Cureus. 2022 Feb 5;14(2):e21946. doi: 10.7759/cureus.21946. PMID: 35273887.
156. Huang Y, Li T, Yu H, Tang J, Song Q, Guo X, Wang H, Li C, Wang J, Liang C, Yao X, Qiu L, Zhuang C, Bi Z, Su Y, Wu T, Ge S, Zhang J. Maternal CMV seroprevalence rate in early gestation and congenital cytomegalovirus infection in a Chinese population. Emerg Microbes Infect. 2021 Dec;10(1):1824-1831. doi:10.1080/22221751.2021.1969290.
157. Саматова Л. Д., Раимова Д. А., Сабурова Ю. Т. Клиническое значение, подходы к диагностике и лечению активной цитомегаловирусной инфекции //Academic research in educational sciences. – 2021. – Т. 2. – №. 5. – С. 738-746
158. Шахгильдян В.И. Лекция 23. Цитомегаловирусная инфекция //Лекции по ВИЧ-инфекции. – С. 293.
159. Kamatani K, Kenzaka T, Sugimoto R, Kumabe A, Kitao A, Akita H. Multiple thrombosis associated with Cytomegalovirus enterocolitis in an immunocompetent patient: a case report. BMC Infect Dis. 2021 Jun 5;21(1):530. doi: 10.1186/s12879-021-06230-4. PMID: 34090366; PMCID: PMC8180152.
160. Padala SK, Kumar A, Padala S. Fulminant cytomegalovirus myocarditis in an immunocompetent host: resolution with oral valganciclovir. Tex Heart Inst J. 2014 Oct 1;41(5):523-9. doi: 10.14503/THIJ-13-3504. PMID: 25425988; PMCID: PMC4189357.
161. Wasey W, Badesha N, Rossi M, Carter C, Bibee S. Cytomegalovirus-Induced Pericarditis, Pulmonary Embolism, and Transaminitis in an Immunocompetent Patient. Cureus. 2021 Nov 5;13(11):e19285. doi: 10.7759/cureus.19285. PMID: 34900468; PMCID: PMC8648299.
162. Elfors MA, Helmy MGE, Mahmoud HEA, Hussein MM, Naguib AM, Ahmed MBED, Elbaz HSI, Aly Aly MO. Risk factors affecting the incidence of CMV infection in recipients after living donor liver transplantation. BMC Gastroenterol. 2025 Jun 25;25(1):440. doi: 10.1186/s12876-025-03911-1. PMID: 40563087; PMCID: PMC12188661.
163. Кочкина С. С., Ситникова Е. П. Особенности цитомегаловирусной инфекции: обзор литературы //Доктор. ру. – 2016. – №. 6 (123). – С. 62-67.
164. Salgado OJ, Henríquez C, Rosales B, Martín MG, García R, Rodríguez-Iturbe B. Renal Doppler sonographic and histologic findings in post-transplant primary cytomegalovirus disease. J Clin Ultrasound. 2000 Oct;28(8):430-4. doi: 10.1002/1097-0096(200010)28:8<430::aid-jcu9>3.0.co;2-y. PMID: 10993972.
Приложение А1. Состав рабочей группы по разработке и пересмотру клинических рекомендаций
1. Авдеева М.Г., д.м.н., профессор, заведующая кафедрой инфекционных болезней и фтизиопульмонологии ФГБОУ ВО «Кубанский государственный медицинский университет» Минздрава России
2. Баранов И.И., д.м.н., профессор, заведующий отделом научно-образовательных программ ФГБУ «НМИЦ АГП им. В.И. Кулакова»» Минздрава России
3. Городин В.Н., Заслуженный врач РФ, д.м.н., профессор, заведующий кафедрой инфекционных болезней и эпидемиологии ФПК и ППС ФГБОУ ВО «Кубанский государственный медицинский университет» Минздрава России
4. Горелов А.В., академик РАН, профессор, заместитель директора по научной работе ФБУН Центральный НИИ эпидемиологии Роспотребнадзора
5. Долгушина Н.В., д.м.н., профессор, заместитель директора-руководитель департамента организации научной деятельности ФГБУ «НМИЦ АГП им. В.И. Кулакова» Минздрава России, главный внештатный специалист по репродуктивному здоровью женщин Минздрава России
6. Кан Н.Е., д.м.н., профессор, заместитель директора по науке ФГБУ «НМИЦ АГП им. В.И. Кулакова» Минздрава России
7. Новак К.Е. к.м.н., доцент, доцент кафедры инфекционных болезней взрослых и эпидемиологии ФГБОУ ВО «Санкт-Петербургский государственный педиатрический медицинский университет» Минздрава России
8. Прокопенко Е.И., д.м.н., профессор кафедры трансплантологии, нефрологии и искусственных органов ФУВ ГБУЗ «МО МОНИКИ им. М.Ф. Владимирского»
9. Чуланов В.П., д.м.н., профессор, заместитель директора по научной работе и инновационному развитию ФГБУ НМИЦ ФИБ МЗ РФ
10. Шмаков Р.Г., д.м.н., профессор, директор института акушерства ФГБУ «НМИЦ АГП им. В.И. Кулакова» Минздрава России, главный внештатный специалист по акушерству Минздрава России
11. Эсауленко Е.В., д.м.н., профессор, заведующая кафедрой инфекционных болезней взрослых и эпидемиологии ФГБОУ ВО «Санкт-Петербургский государственный педиатрический медицинский университет» Минздрава России.
Все члены рабочей группы являются членами Национальной ассоциации специалистов по инфекционным болезням имени академика В.И. Покровского (НАСИБ) или ООО «Российское общество акушеров-гинекологов» (РОАГ).
Конфликт интересов отсутствует.
Приложение А2. Методология разработки клинических рекомендаций
Целевая аудитория клинических рекомендаций:
1. врач-инфекционист;
2. врач-эпидемиолог;
3. врач-терапевт;
4. врач-гастроэнтеролог;
5. врач-хирург;
6. врач-гематолог;
7. врач общей практики (семейный врач);
8. врач-акушер-гинеколог;
9. студенты медицинских вузов, ординаторы, врачи-стажеры.
В данных клинических рекомендациях все сведения ранжированы по уровню достоверности (доказательности) в зависимости от количества и качества исследований по данной проблеме.
Таблица 1. Шкала оценки уровней достоверности доказательств (УДД) для методов диагностики (диагностических вмешательств)
|
УДД |
Расшифровка |
|
1 |
Систематические обзоры исследований с контролем референсным методом1 или систематический обзор рандомизированных клинических исследований с применением мета-анализа |
|
2 |
Отдельные исследования с контролем референсным методом или отдельные рандомизированные клинические исследования и систематические обзоры исследований любого дизайна, за исключением рандомизированных клинических исследований, с применением мета-анализа |
|
3 |
Исследования без последовательного контроля референсным методом или исследования с референсным методом, не являющимся независимым от исследуемого метода или нерандомизированные сравнительные исследования, в том числе когортные исследования |
|
4 |
Несравнительные исследования, описание клинического случая |
|
5 |
Имеется лишь обоснование механизма действия или мнение экспертов |
1 Общепринятым стандартом КИ диагностических вмешательств является одномоментный дизайн исследования, в котором к каждому включённому пациенту параллельно и в одинаковых условиях применяются исследуемый диагностический метод и референсный метод, являющийся «золотым стандартом» диагностики изучаемого заболевания или состояния, при этом исследуемый и референсный методы должны применяться независимо друг от друга (т.е. исследуемый метод не может быть частью референсного) и должны интерпретироваться исследователем без знания результатов применения другого метода (рекомендуется использовать ослепление)
Таблица 1. Шкала оценки уровней достоверности доказательств (УДД) для методов профилактики, лечения, медицинской реабилитации, в том числе основанных на использовании природных лечебных факторов (профилактических, лечебных, реабилитационных вмешательств)
|
УУР |
Расшифровка |
|
1 |
Систематический обзор РКИ с применением мета-анализа |
|
2 |
Отдельные РКИ и систематические обзоры исследований любого дизайна, за исключением РКИ, с применением мета-анализа |
|
3 |
Нерандомизированные сравнительные исследования, в т.ч. когортные исследования |
|
4 |
Несравнительные исследования, описание клинического случая или серии случаев, исследования «случай-контроль» |
|
5 |
Имеется лишь обоснование механизма действия вмешательства (доклинические исследования) или мнение экспертов |
Таблица 3. Шкала оценки уровней убедительности рекомендаций (УУР) для методов профилактики, диагностики, лечения, медицинской реабилитации, в том числе основанных на использовании природных лечебных факторов (профилактических, диагностических, лечебных, реабилитационных вмешательств)
|
УУР |
Расшифровка |
|
A |
Сильная рекомендация (все рассматриваемые критерии эффективности (исходы) являются важными, все исследования имеют высокое или удовлетворительное методологическое качество, их выводы по интересующим исходам являются согласованными) |
|
B |
Условная рекомендация (не все рассматриваемые критерии эффективности (исходы) являются важными, не все исследования имеют высокое или удовлетворительное методологическое качество и/или их выводы по интересующим исходам не являются согласованными) |
|
C |
Слабая рекомендация (отсутствие доказательств надлежащего качества (все рассматриваемые критерии эффективности (исходы) являются неважными, все исследования имеют низкое методологическое качество и их выводы по интересующим исходам не являются согласованными) |
Порядок обновления клинических рекомендаций
Механизм обновления клинических рекомендаций предусматривает их систематическую актуализацию – не реже чем один раз в три года, а также при появлении новых данных с позиции доказательной медицины по вопросам диагностики, лечения, профилактики и реабилитации конкретных заболеваний, наличии обоснованных дополнений/замечаний к ранее утверждённым КР, но не чаще 1 раза в 6 месяцев.
Приложение А3. Справочные материалы, включая соответствие показаний к применению и противопоказаний, способов применения и доз лекарственных препаратов, инструкции по применению лекарственного препарата
Данные клинические рекомендации разработаны с учётом следующих нормативно-правовых документов:
1. Федеральный закон от 29.11.2010 № 326-ФЗ «Об обязательном медицинском страховании в Российской Федерации».
2. Федеральный закон от 21.11.2011 № 323-ФЗ «Об основах охраны здоровья граждан в Российской Федерации».
3. Приказ Минздравсоцразвития РФ от 09.08.2005 № 494 «О порядке применения лекарственных средств у больных по жизненным показаниям».
4. Приказ Минздрава России от 13.10.2017 № 804н «Об утверждении номенклатуры медицинских услуг».
5. Приказ Минздравсоцразвития России от 31.01.2012 № 69н «Об утверждении Порядка оказания медицинской помощи взрослым больным при инфекционных заболеваниях».
6. Приказ Минздрава России от 20.10.2020 № 1130н «Об утверждении Порядка оказания медицинской помощи по профилю "акушерство и гинекология».
7. Приказ Минздрава России от 02.05.2023 № 205н «Об утверждении Номенклатуры должностей медицинских работников и фармацевтических работников».
8. Приказ Минздрава России от 07.10.2015 № 700н «О номенклатуре специальностей специалистов, имеющих высшее медицинское и фармацевтическое образование».
9. Приказ Минтруда России от 26.07.2024 № 374н «Об утверждении классификаций и критериев, используемых при осуществлении медико-социальной экспертизы граждан федеральными учреждениями медико-социальной экспертизы».
10. Постановление Главного государственного санитарного врача РФ от 28.01.2021 № 4 «Об утверждении санитарных правил и норм СанПиН 3.3686-21 «Санитарно-эпидемиологические требования по профилактике инфекционных болезней» (вместе с «СанПиН 3.3686-21. Санитарные правила и нормы... »).
Приложение Б. Алгоритмы действий врача
Приложение В. Информация для пациента
Цитомегаловирус (ЦМВ) относится к семейству герпесвирусов. Этот повсеместно распространенный вирус с большой вероятностью передается человеку в течение первых пяти лет жизни. По крайней мере 80% взрослого населения земли имеет антитела к нему. Заражение ЦМВ в большинстве случаев проходит незаметно для человека и не ведет к клинически выраженному заболеванию. Тем не менее, иногда возможно повышение температуры, пневмония, энтерит, увеличение лимфатических узлов и гепатит.
Источник инфекции – всегда человек. Вирус содержится в слюне, крови, молоке, моче, кале, семенной жидкости и секрете шейки матки. По разным данным на планете этот вирус носят от 50 до 80% взрослых людей. Инфицирование ЦМВ может быть врожденным, может произойти во время родов или позднее при переливании крови, через продукты переработки крови, слюну и другие жидкости организма.
Попав в организм человека, вирус, как правило, останется в нем навсегда. А попасть он может воздушно-капельным, фекально-оральным, половым и антенатальным (от матери к ребенку) путями, при переливании крови и трансплантации органов. ЦМВ может передаваться при половых контактах.
Опасен цитомегаловирус при беременности, особенно если вирус впервые попал в организм матери именно в период вынашивания ребенка. В этом случае очень велика вероятность инфицирования плода. Ведь если вирус попал в организм впервые, в организме еще нет к нему антител, и тогда неослабленный вирус легко поражает плод. Чаще всего в организм ребенка вирус попадает через плодные оболочки, но возможно инфицирование при рождении и после рождения.
Опасен цитомегаловирус и для ВИЧ-инфицированных. В этом случае вирус не только поражает многие органы и системы, но и, по некоторым данным, способствует развитию онкологических заболеваний.
Если вирус себя никак не проявляет, то и лечить его не надо. Другое дело, если он активен. Тогда показана комплексная терапия, назначать лекарства должен врач, самостоятельная терапия недопустима, так как многие противовирусные средства (противовирусные препараты прямого действия, код по АТХ: J05A) в отношении цитомегаловируса не эффективны, или имеют серьезные побочные действия.
Чтобы не вызвать реактивацию вируса, нужно следить за своим иммунитетом, не переохлаждаться, предохраняться от различных инфекций, в том числе и передающихся половым путем, принимать витамины, заниматься физкультурой и не забывать про закаливание.
Для профилактики важно соблюдение гигиены, в том числе интимной. Не стоит пользоваться общими умывальными принадлежностями и посудой с малознакомыми людьми и вступать в новые интимные отношения без презерватива. После контакта с деньгами и другими предметами, которые трогали незнакомые люди, необходимо тщательно мыть руки.
Приложение Г1-ГN. Шкалы оценки, вопросники и другие оценочные инструменты состояния пациента, приведенные в клинических рекомендациях
Не применяются.
.
- При подозрении на ЦМВ-инфекцию у взрослых учитывайте клинический контекст и иммунный статус пациента.
- При поражении ЖКТ, печени или системных проявлениях требуется дифференциальная диагностика с другими вирусными и воспалительными заболеваниями.
- Эндоскопическое исследование с биопсией рассматривается при поражении пищевода, желудка или кишечника по показаниям.
- Тактика ведения и противовирусная терапия определяются клиническими рекомендациями с учётом тяжести и сопутствующих факторов.
Когда следует подозревать ЦМВ-инфекцию у взрослых?
Какова роль эндоскопии при ЦМВИ?
Когда требуется изменение тактики ведения?
Дополнительно
Цитомегаловирусная инфекция у взрослых представляет клиническую значимость в связи с разнообразием форм течения и риском поражения внутренних органов. В практической работе важна своевременная диагностика, особенно при иммунодефицитных состояниях и системных проявлениях.
Клинические рекомендации 2025–2027 систематизируют подходы к диагностике, лечению и мониторингу пациентов, включая алгоритмы обследования и критерии оценки эффективности терапии.
Рекомендуемые статьи
При эндоскопическом исследовании в случае бронхоэктазов в стадии ремиссии выявляется
частично диффузный бронхит I степени воспаления
Активируйте PUSH уведомления в браузер
Отключите PUSH уведомления в браузер
Содержание
Интернет магазин
Популярное
- О нас
- Правовые вопросы
- Политика
обработки персональных
данных EndoExpert.ru - Связаться с нами
- Стать партнером
© 2016-2022 EndoExpert.ru

Вы находитесь в разделе предназначенном только для специалистов (раздел для пациентов по ссылке). Пожалуйста, внимательно прочитайте полные условия использования и подтвердите, что Вы являетесь медицинским или фармацевтическим работником или студентом медицинского образовательного учреждения и подтверждаете своё понимание и согласие с тем, что применение рецептурных препаратов, обращение за той или иной медицинской услугой, равно как и ее выполнение, использование медицинских изделий, выбор метода профилактики, диагностики, лечения, медицинской реабилитации, равно как и их применение, возможны только после предварительной консультации со специалистом. Мы используем файлы cookie, чтобы предложить Вам лучший опыт взаимодействия. Файлы cookie позволяют адаптировать веб-сайты к вашим интересам и предпочтениям.
Я прочитал и настоящим принимаю вышеизложенное, хочу продолжить ознакомление с размещенной на данном сайте информацией для специалистов.











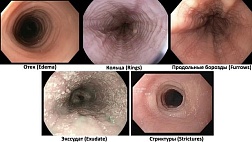


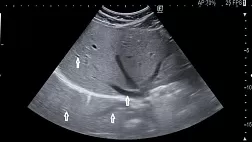


.jpg)




.png)















Комментарии