- Компании
- Takeda. О компании, буклеты, каталоги, контакты
- Olympus. О компании, буклеты, каталоги, контакты
- Boston Scientific. О компании, буклеты, каталоги, контакты
- Pentax. О компании, буклеты, каталоги, контакты
- Fujifilm & R-Farm. О компании, буклеты, каталоги, контакты
- Erbe. О компании, буклеты, каталоги, контакты
- Еще каталоги
- Мероприятия
- Информация
- Обучение
- Классификации
- Атлас
- Quiz
- Разделы
- Пациенту
QR-код этой страницы
Для продолжения изучения на мобильном устройстве ПРОСКАНИРУЙТЕ QR-код с помощью спец. программы или фотокамеры мобильного устройства
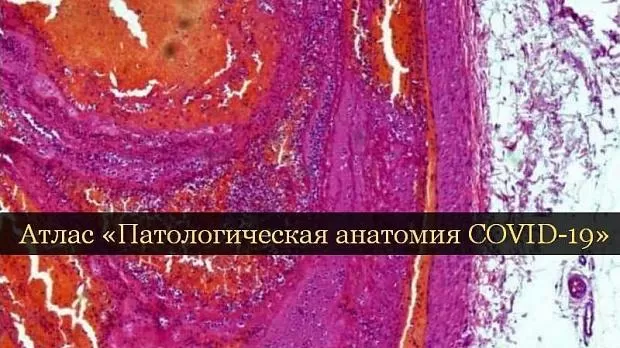
Статьи: Атлас «Патологическая анатомия COVID-19»
Анонс:
Клинический комитет по COVID-19 Департамента здравоохранения города Москвы информирует о выходе Атласа «Патологическая анатомия COVID-19» и рекомендует его всем врачам для использования в практической деятельности.
Департамент здравоохранения города Москвы
ГБУ «НИИ ОЗММ ДЗМ»,
ФГБОУ ВО «МГМСУ им. А.И.Евдокимова» Минздрава России ФГБУ «НИИ пульмонологии» ФМБА России
ФГ АОУ ВО «РНИМУ им. И.И.Пирогова» Мннздрава России ФГБНУ «НИИ морфологии человека»
ГБУЗ «ГКБ№ 31 ДЗМ»
ГБУ РО «Бюро судебно-медицинской экспертизы нм. Д.И.Мастбаума» ФГБУ «НМИЦ хирургии им. А.В.Вишневского» Мннздрава России ГБУЗ «ГКБ нм. И.В.Давыдовского ДЗМ»
ПАТОЛОГИЧЕСКАЯ АНАТОМИЯ COVID-19 АТЛАС
Под общей редакцией О.В.Зайратьянца
Москва 2020
Авторы:
Зайратьянц О.В., главный внештатный специалист патологоанатом Департамента здравоохранения города Москвы, главный внештатный специалист-эксперт патологоанатом Росздравнадзора по ЦФО, заведующий кафедрой патологической анатомии ФГБОУ ВО «МГМСУ им. А.И.Евдокимова» Минздрава России, Заслуженный врач РФ, доктор медицинских наук, профессор, вице-президент Российского общества патологоанатомов, председатель Московского общества патологоанатомов; Самсонова М.В., заведующая лабораторией патологической анатомии ФГБУ «НИИ пульмонологии» ФМБА России, доктор медицинских наук;
Черняев А.Л., заведующий отделом фундаментальной пульмонологии ФГБУ «НИИ пульмонологии» ФМБА России, Заслуженный врач РФ, доктор медицинских наук, профессор; член Президиума Российского общества патологоанатомов.
Мишнев О.Д., главный внештатный патологоанатом Минздрава России по ЦФО, заведующий кафедрой патологической анатомии лечебного факультета ФГАОУ ВО РНИМУ им. И.И. Пирогова Минздрава России, Заслуженный врач РФ, доктор медицинских наук, профессор, вице-президент Российского общества патологоанатомов;
Михалева Л.М., директор ФГБНУ «НИИ морфологии человека», заведующая патологоанатомическим отделением ГБУЗ «ГКБ № 31 ДЗМ», доктор медицинских наук, профессор, вице-президент Российского общества патологоанатомов;
Крупнов Н.М., главный внештатный патологоанатом Минздрава Рязанской области, начальник ГБУ РО «Бюро судебно-медицинской экспертизы им. Д.И. Мастбаума», Заслуженный работник здравоохранения РФ, кандидат медицинских наук, члеи Президиума Российского общества патологоанатомов.
Калинин Д.В., заведующий патологоанатомическими отделениями ФГБУ НМИЦ хирургии им. А.В.Вишневского Минздрава России и ГБУЗ «ГКБ им. И.В. Давыдовского ДЗМ», кандидат медицинских наук.
Рецензенты:
Какrурскнй Л.В. - научный руководитель НИИ морфологии человека, главный специалист-эксперт по патологической анатомии Росздравнадзора, президент Российского общества патологоанатомов, член-корреспондент РАН, докгор медицинских наук, профессор.
Забозлаев Ф.Г. профессор кафедры клинической лабораторной диагностики и патологической анатомии Академии постдипломного образования ФНКЦ ФМБА России, главный внештатный специалист по патологической анатомии, вице-президент Российского общества патологоанатомов, докгор медицинских наук, Заслуженный врач РФ
Аннотация. Атлас явился итогом аутопсийной работы патологоанатомической службы Москвы по посмертной диагностике проявлений и осложнений COVID-19 в более, чем 2000 наблюдениях - самого большого в мире объема патологоанатомический вскрытий умерших от COVID-19. Эго стало возможным благодаря тому, что в Москве в 100% случаев летальных исходов с подозрением на COVID-19 производятся патологоанатомические вскрытия с детальным клинико-морфологическим анализом. Результаты патологоанатомических исследований легли в основу новых методики и классификации, которые детализируют методические рекомендации ВОЗ по выбору причин смерти у умерших при COVID-19. Применение на практике этой методики позволило усовершенствовать не только учет случаев смерти от COVID-19, но и оказало существенное влияние на подходы к лечению таких пациентов. Вкладом в теорию патологии является введение понятия клинических и морфологических
«масок» COVID-19. В атласе представлен широкий спектр проявлений и осложнений COVID-19, что позволит наметить пути изучения их патогенеза и морфогенеза, совершенствовать методы диагностики и лечения больных, детальную классификацию причин смерти, прямо или косвенно связанных с COVID-19.
Предназначение. Данный атлас предназначен для врачей патологоанатомов, судебно-медицинских экспертов, а также врачей всех клинических специальностей и учащихся медицинских образовательных организаций, в том числе при повышении квалификации в ходе непрерывного медицинского образования
Данный аrплас является собственностью коллектива авторов и не подлежит тиражированию и распространению без соответствующего разрешения. Опубликован на портале ДЗМ в файле для скачивания
ISBN _
© Коллектив авторов, 2020
Авторы выражают благодарность за предоставление материалов исследований и помощь в подготовке атласа врачам-патологоанатомам:
Авдалян А.М., заведующий патологоанатомическим отделением ГБУЗ
«ГКБ № 40 ДЗМ», д.м.н.
Астахова О.И., заведующая патологоанатомическим отделением ГБУЗ
«ГКБ им. С.И. Спасокукоцкого ДЗМ»;
Березовский Ю.С. заведующий отделением патоморфологии ФГБНУ
ЦНИИТ МЗ РФ, к.м.н.;
Варясии В.В., заведующий патологоанатомическим отделением ГБУЗ «ГКБ
№ 52 ДЗМ», к.м.н.
Виноградов С.А., заведующий патологоанатомическим отделением клинической больницы МЕДСИ (АО «Группа компаний «МЕДСИ»);
Волков А.В., заведующий патологоанатомическим отделением ГБУЗ «ГКБ им. Е.О. Мухина ДЗМ» д.м.н., доцент кафедры патологической анатомии ФГАО МУ РУДН, с.и.с. лаборатории соединительной ткани ФГБУ «НМИЦ травматологии и ортопедии имени Н.Н.Приорова» Минздрава России; Даабуль А.С., заведующий патологоанатомическим отделением ГБУЗ «ГКБ им. М.Е. Жадкевича ДЗМ»;
Добряков А.В., заведующий патологоанатомическим отделением ГБУЗ
«ГКБ им. братьев Бахрущиных ДЗМ», к.м.н.;
Золотенкова И.В., заведующая патологоанатомическим отделением ГБУЗ
«ГКБ № 17 ДЗМ»;
Келли Е.И., заведующая патологоанатомическим отделением ГБУЗ «ИКБ № 1 ДЗМ», к.м.н.;
Медников Г.Н., заведующий патологоанатомическим отделением ГБУЗ
«ГКБ № 15 им. O.М. Филатова ДЗМ»;
Мельченко Д.С., заведующий патологоанатомическим отделением ЦКБ
РАН, к.м.н., доцент;
Орехов О.О., заведующий патологоанатомическим отделением ГБУЗ «ГКБ
№ 67 им. Л.А. Ворохобова ДЗМ», к.м.н.;
Петрова С.Ю., заведующая патологоанатомическим отделением ГБУЗ
«ГВВ № 3 ДЗМ»;
Тишкевич О.А., и.о. заведующий патологоанатомическим отделением ГБУЗ «ИКБ № 2 ДЗМ»;
Цыганов С.Е., заведующий патологоанатомическим отделением ГБУЗ «ГКБ
№4ДЗМ».
Авторы выражают искреннюю признательность начальнику Бюро судебно-медицинской экспертизы ДЗМ, главному судебно-медицинскому эксперту ДЗМ, доктору медицинских наук С.В.Шигееву и всем сотрудникам Бюро СМЭ ДЗМ за постоянную поддержку, взаимопомощь и тесное сотрудничество.
Предисловие
Атлас явился итогом уникальной аутопсийной работы патологоанатомической службы Москвы по посмертной диагностике многообразных патологических проявлений и осложнений COVID-19 в более, чем 2000 наблюдениях. Не будет преувеличением подчеркнуть, что это самый большой в мире объем патологоанатомический вскрытий умерших от COVID-19.
Московские патологоанатомы в тесном содружестве с клиницистами выступили инициаторами и приняли активное участие в подготовке новой методики и классификации, которые детализируют методические рекомендации Всемирной организации здравоохранения по выбору причин смерти у умерших при COVID-19. Применение на практике этой методики позволило усовершенствовать не только учет случаев смерти от COVID-19 в качестве основной причины смерти либо в составе прочих причин, где он выступил своего рода «катализатором» обострения другого основного заболевания, но и оказал существенное влияние на подходы к лечению таких пациентов.
Важно отметить, что созданная классификация нужна не только для целей статистики и учета причин смерти, но и позволила раскрыть основные особенности течения COVID-19 для корректировки протоколов лечения и тактики ведения больных.
Существенным вкладом в теорию патологии является введение понятия клинических и морфологических «масок» COVID-19, например, инфаркта миокарда или декомпенсации сахарного диабета.
Уже в результате первых патологоанатомических вскрытий были обнаружены тяжелые проявления и осложнения COVID-19 в виде тромбозов и эмболий, микроангиопатии, риска развития почечной недостаточности, декомпенсации сахарного диабета и разнообразных поражений других органов, что позволило оперативно внедрять в клинической практике соответствующие новые протоколы лечения.
Это стало возможным благодаря тому, что в Москве в 100% случаев летальных исходов с подозрением на COVID-19 производятся патологоанатомические вскрытия с детальным клинико-морфологическим анализом их результатов. Так, используются методы полимеразной цепной реакции для идентификации коронавируса, других возбудителей, включая бактериальных, гистологический и иммуногистохимический методы для выявления тончайших изменений в тканях и органах. При этом развитость патологоанатомической службы позволяла формулировать окончательные патологоанатомические диагнозы в течение 2-х недель, при нормативно установленном по стране сроке в 45 дней.
На основе результатов более 2000 аутопсий умерших от COVID-19 московские патологоанатомы составили атлас патологических изменений, выявленных на разных стадиях этого заболевания. Атлас позволяет увидеть спектр возможных проявлений и осложнений COVID-19, наметить пути изучения патогенеза и морфогенеза выявленных структурных изменений, совершенствовать методы диагностики и лечения больных, составить детальную классификацию причин смерти, прямо или косвенно связанных с COVID-19.
Министр правительства Москвы, Руководитель Департамента здравоохранения города Москвы
А.И.Хрипун
Оглавление
Введение
11 марта 2020 r. Всемирная организация здравоохранения (ВОЗ) объявила о начале пандемии новой коронавирусной инфекции, вызванной вирусом SARS-CoV-2, которая стала 11-й в XX-XXI веках.
Первые случаи заболевания бьли официально зарегистрированы на юго востоке КНР в r. Ухань (провинция Хубэй) в декабре 2019 r. Несмотря на принятые КНР и ВОЗ беспрецедентные меры по нераспространению новой коронавирусной инфекции, в феврале эпидемия охватила, по меньшей мере, Южную Корею, Иран и Италию, а к марту - и другие страны мира, превратившись в пандемию. В настояшее время эксперты ВОЗ не исключают, что и в Европе (в частности, во Франции) первые заболевшие после поездок в Китай, появились уже в декабре 2019 r. (подтверждено вирусологическими исследованиями).
11 февраля 2020 г. ВОЗ присвоила новой коронавирусной инфекции официальное название - COVID-19 («COronaVIn1s Disease 2019»), а международный комитет по таксономии вирусов - официальное название возбудителю этой инфекции - SARS-CoV-2.
В России Постановлением Правительства РФ от 31 января 2020 г. № 66 новый коронавирус SARS-CoV-2, из линии вирусов Beta-CoV В, как и SARS CoV, и МERS-CoV, включен в перечень заболеваний, представляюших опасность для окружаюших, наряду с особо опасными инфекциями II группы патогенности (чума, холера, оспа), утвержденный Постановлением Правительства РФ от 01.12.2004 г. №715.
SARS-CoV-2 - это одноцепочечный РНК-содержаший вирус, принадлежаший к семейству Coronaviridae. Согласно секвенированию генома было показано генетическое сходство нового вируса с ранее известными коронавирусами SARS-CoV (сходство ~ 79%) и МERS-CoV (сходство~ 50%). S-белок вируса SARS-CoV-2 имеет сродство к рецептору ангиотензинпреврашаюшего фермента 2 (АПФ2), причем его аффинность в отношении этого рецептора в 10-20 раз выше, чем у SARS-CoV, что и обеспечивает высокую коитагиозиость. Обсуждается, ио ие доказана роль рецептора CD\47.
Рецептор к АПФ2 экспрессируется в эпителии респираторных путей, альвеолоцитах, альвеолярных моноцитах, эндотелии сосудов, эпителии желудочно-кишечного тракта, мочевых путей, макрофагах и других клетках многих органов и тканей, включая миокард и некоторые отделы ЦНС. SARS-CoV-2 способен к наиболее активной репликации в верхних дыхательных путях. Тропность вируса к эпителию верхних дыхательных путей, вероятно, объясняет непрерывное выделение вируса из глотки и более эффективную передачу SARS-CoV-2, чем SARS-CoV. Течение и прогрессирование болезни COVID-19 в определенной мере напоминает тяжелый острый респираторный синдром (ТОРС, SARS) по репликации вируса в нижних дыхательных путях с развитием вторичной виремии, иммунных нарушений и гипоксии, приводящих к поражению мноmх органов-мишеней: сердца, почек, желудочно-кишечного тракта и других, клетки которых экспрессируют рецептор к АПФ2, приводя к клиническим ухудшениям на второй неделе от начала заболевания. Однако кардинальным отличием являются развитие микроангиопатии в виде деструктивно продуктивного тромбоваскулита и гиперкоагуляционного синдрома, а также повреждение органов иммунной системы.
Персистируюший воспалительный статус у пациентов с тяжелой и критической степенью тяжести COVID-19 действует как важный триггер ДJJЯ каскада коагуляции, в частности IL-6, может активировать систему свертывания и подавлять фибринолитическую систему. Вследствие прямого воздействия вируса происходит повреждение эндотелия сосудов легких и периферических сосудов, что также является важным индуктором гиперкоагуляции, как и агрессивный иммунный ответ. Появление антифосфолипидных антител может усиливать коагулопатию.
Такое явление у пациентов с тяжелыми и критическими состояниями редко встречалось при других коронавирусных инфекциях или гриппе типа А. Клиническое течение COVID-19 характеризуется гиперкоагуляцией с удлинением протромбинового времени, повышением уровня D-димера и фибриногена в сыворотке крови, при почти нормальном активированном частичном тромбоплатиновом времени (АЧТВ), что приводит к развитию диссеминированной внутрисосудистой коагуляции (ДВС-синдрома).
Прогрессирование COVID-19 также связывают с постоянным снижением доли лимфоцитов и значительным повышением доли нейтрофилов в крови. Помимо этого в сыворотке крови происходит повышение уровня маркеров воспаления: С-реактивного белка, ферритина, интерлейкина (IL-6, IP-10, MCPI, MIPIA и TNFa). Было показано, что снижение числа лимфоцитов, повышение уровня ферритина, IL-6 и D димера являются неблагоприятными прогностическими факторами COVID- 19. Однако механизмы, лежашие в основе прогрессируюшей лимфопении у тяжелых и критических пациентов с COVID-19, остаются неясными. Очевидно, что это функциональным истошением может быть связано не только с лимфоцитов и/или гибелью части лимфоцитов посредством алоптоза или пироптоза, а также патологического митоза собственными макрофагами.
Несомненна роль гиперэргической иммунной реакции на SARS-CoV-2 у части больных, что обусловливают бурное развитие иммунной воспалительной реакции, выраженного синдрома системной воспалительной реакции, с тяжелой альтерацией ткани легких в виде диффузного альвеолярного повреждения, а также и других органов, с развитием картины септического шока. Полагают, что ведущую роль в этом играют CD4+ Т- лимфоциты и различные провоспалительные цитокины ("цитокиновый шторм"). Не исключается также роль вирус-индуцированных аутоиммунных реакций.
Обсуждается возможность развития генерализованных форм течения SARS-CoV-2, вирусного сепсиса, и поражением различных органов, включая цнс.
Гипотеза о роли вирусного повреждения гемоглобина с развитием химического пневмонита, вызванного продуктами распада гемма, не нашла своего морфологического подтверждения.
Пока не ясны патогенез и морфогенез многих проявлений и осложнений COVID-19, в частности характерной временной потери обоняния (аносмии)- одного из частых симптомов COVID-19, что может быть вызвано как поражением слизистой оболочки носоглотки, так и определенных отделов ЦНС.
При аутопсии умерших от COVID-19 основные патологические изменения выявляют в легких, но нередко отмечают одновременное с легкими поражение других органов, которое по своей тяжести может превалировать над легочной патологией, а также, сепсис и септический шок при присоединении бактериальной инфекции. Следует подчеркнуть, что шок, клинически сходный с септическим, наблюдался и без бактериальной коинфекции.
Патологическая анатомия, патогенез и морфогенез пизменений при COVID-19 остаются недостаточно изученными, и раскрытие их особенностей позволит разработать эффективные методы профилактики и лечения этого инфекционного заболевания.
Краткая статистическая информация (2000 патологоанатомических вскрытий умерших от COVID-19 в г. Москве с 20 марта по 22 мая)
Результаты анализа 2000 летальных исходов от COVID-19 в г. Москве с 20 марта по 22 мая, выявили, что соотношение мужчин и женщин составило 1,54 : 1 (1212 мужчин и 788 женщин). Средний возраст умерших был 68,5 ± 15,63 лет (от 20 до 99 лет, что, в среднем, составило 72,1 ± 13,71 - у женщин и 66,3 ± 14,58 лет - у мужчин)
Рис. 1. Частота смертельных осложнений (непосредственных причин смерти, в
%) у умерших от COVID-19 в г. Москве с 20 марта по 22 мая 2020 г.(n = 2000).
Рис. 2. Частота (абс. цифры) тромботических и тромбоэмболических осложнений (смертельных и прочих вместе) у умерших от COVID-19 с 20 марта по 22 мая (n = 2000).
Примечания: l) тромбозы коронарных артерий сердца, головного мозга и др. - без нестабильных атеросклеротических бляшек; 2) ТЭЛА и тромбоз легочных артерий (крупных ветвей и ствола) представлены вместе, в связи с возможной ошибкой дифференциальной морфологической диагностики на вскрытии; 3) ДВС-синдром подразумевает морфологическую картину распространенного геморрагического синдрома с фибриновыми тромбами в микроциркуляции
Рис. 3. Коморбидные заболевание (абс. число) у умерших от COVID-19 в г. Москве с 20 марта по 22 мая 2020 г. (n = 2000).
Прuмечания: 1) частота ожирения и сахарного диабета (СД) выше, чем у умерших без COVID-19; ожирение - 19,3%, из них 4 случая - синдром Пиквика; сахарный диабет 1го и 2-го типов - 21,9%, из них 5 случаев - ед 1-го типа; 2) частота ГБ, ИБС, ХИГМ, ХОБЛ, БА, хронического пиелонефрита, различных злокачественных опухолей - сопоставима с умершими без COVID-19, частота хронической алкогольной интоксикации (ХАИ) - ниже, чем у умерших без COVID-19
ПАТОЛОГИЧЕСКАЯАНАТОМИЯСОVID-19
При аутопсии патологические изменения разной степени тяжести и распространенности были выявлены у всех умерших от COVID-19 в легких, однако отмечалось одновременное поражение других органов, которое в отдельных наблюдениях по своей тяжести могло преобладать над легочными изменениями и быть причиной смерти.
Присоединение бактериальной (или, редко, микотической) инфекции в виде вирусно-бактериальной и микотической (клебсиела, стафилококки, кандида и др.) пневмонии, а также сепсиса и септического (инфекционно токсического) шока бьшо характерно, преймушественно, у больных, длительно (более недели) находившихся на ИВЛ. Их частота, доказанная морфологически и/или бактериологически, составила, в целом, 37% (746 из 2000 аутопсий), что несколько выше значений, характерных, например, для гриппа A/HINI (около 30%).
Исследование показало, что основным морфологическим субстратом поражения легких является достаточно специфическое диффузное альвеолярное повреждение в сочетании с вовлечением в патологический процесс сосудистого русла легких и альвеолярно-геморрагическим синдромом. Термин вирусной (интерстициальной) пневмонии, широко используемый в клинике, по сути своей отражает именно развитие диффузного альвеолярного повреждения, а при COVID-19 должен подразумевать еше и патологию сосудов легких, прежде всего микроциркуляторного русла - микроангиопатии в виде деструктивно продуктивного тромбоваскулита. В свою очередь, тяжелое диффузное альвеолярное повреждение является синонимом клинического понятия «острый респираторный дистресс-синдром» (ОРДС). В патологоанатомической практике для макроскопического обозначения этих изменений легких, которые также наблюдаются при различных тяжелых травмах, шоке любой этиологии, применяется термин «шоковые легкие», что не совсем корректно для COVID-19, так как не подразумевает поражения сосудистого русла.
На аутопсии легкие увеличены в объеме и массе, причем у части больных поражены, преимущественно, задне-базальные отделы (встречается примерно в трети летальных исходов), а на вскрытии в их передних отделах наблюдается острое вздутие (ткань легких повышенной воздушности, розового цвета, режется с хрустом).
Изменения легких макроскопически соответствовали понятию
«шоковое легкое». Ткань легких диффузно уплотнена и, практически, безвоздушна, с поверхности и на разрезе темно-вишневого или красно бурого цвета (характерного «лакового» вида), с участками ателектазов (дистелектазов), часто обширными сливными кровоизлияниями и, нередко, различной величины геморрагическими инфарктами. Также характерны множественные пристеночные и обтурирующие тромбы ветвей легочных артерий и вен разного калибра, причем в отдельных случаях тромбоз легочных артерий распространялся на правые отделы сердца - желудочек и даже предсердие.
Тромбы ветвей легочной артерии следует дифференцировать с тромбоэмболами, которые также были выявлены в части наблюдений, а их источником явились глубокие вены нижних конечностей, вены малого таза, реже - правые отделы сердца. На плевре характерны наложения фибрина (очаговый и распространенный фибринозный плеврит обычно без значительного выпота в плевральных полостях), причем не только при геморрагических инфарктах. При присоединении бактериальной суперинфекции развивается фибринозно-гнойный плеврит.
Гистологически изменения легких относительно близки к двум классическим фазам диффузного альвеолярного повреждения.
Для экссудативной (первой, ранней) фазы (первые 7-8 суток, реже - до 14-х суток от начала заболевания) были характерны следующие изменения:
• интраальвеолярный отек с примесью в отечной жидкости эритроцитов, моноцитов и макрофагов, слущенных альвеолоцитов, нейтрофилов, лимфоцитов и плазмоцитов;
• гиалиновые мембраны (разной толщины и распространенности, продолжающиеся вплоть до внутренней поверхности бронхиол);
• десквамация альвеолярного (в виде отдельных клеток и их пластов) и бронхиолярного эпителия; появление крупных, неправильной формы альвеолоцитов II типа, с увеличенными ядрами с грубозернистым хроматином и отчетливыми ядрышками (в некоторых из них вокруг ядра видно гало, а в цитоплазме - округлые базофильные или эозинофильные включения, харакгерные дЛЯ вирусного повреждения клеток); пролиферация альвеолоцитов II типа, образование их симпластов;
• деструктивно-продуктивный тромбоваскулит, периваскулярная и перибронхиальная лимфо-плазмоклеточная и макрофагальная инфильтрация, а также инфильтрация межальвеолярных перегородок; выраженное полнокровие капилляров межальвеолярных перегородок, а также ветвей легочных артерий и вен, со сладжами эритроцитов, свежими фибриновыми и организующимися тромбами;
• периваскулярные, внутрибронхиальные, внутрибронхиолярные и интраальвеолярные кровоизлияния (являющиеся субстратом дЛЯ кровохарканья); выраженный альвеолярно-геморрагический синдром харакгерен дЛЯ большинства наблюдений, вплоть до формирования, фактически, геморрагических инфарктов (хотя и истинные геморрагические инфаркты не редки);. вторичный интраальвеолярный и периваскулярный гемосидероз выражен минимально;
• мегакариоциты типичного строения в капиллярах межальвеолярных перегородок так называемая «мегакарноцитарная эмболия», что харакгерно для «шоковых легких» любой этиологии, в том числе и для септического шока.
В экссудативную фазу диффузного альвеолярного повреждения обнаружен ранее не описанный при поражении другими коронавирусами феномен аутоцитофагии: в просветах альвеол в части наблюдений выявлялись макрофаги, содержашие в своей цитоплазме фрагменты различных клеток, более вероятно - лимфоцитов (апоптотические тельца), а также эритроцитов. Эгот феномен имеет сходство с изменеиями при вторичном гемофагоцитарном лимфогистиоцитозе, обусловленном вирусной инфекцией. Аналогичные изменения обнаруживаются в лимфоидной ткани.
Пролиферативная (вторая, поздняя) фаза альвеолярного повреждения (после 7- 8 суток и более от начала болезни) характеризовалась следующими изменениями:
• в просветах альвеол накапливался фибрин разной степени зрелости; в части альвеол определялись полиповидные разрастания фибробластической (грануляционной) ткани;
• сливные поля облитерирущего бронхиолита и организующейся пневмонии или участки рыхлого фиброза с щелевидными структурами, выстланными металлазированным плоским эпителием;
• в части наблюдений обнаружено выраженное интерстициальное воспаление с утолщением и отеком межальвеолярных перегородок, отеком и миксоматозом периваскулярной стромы;
• нередко имело место прогрессирование микроангиопатии и тромбоза микроциркуляторного русла, ветвей легочных артерий и вен разного калибра.
В 37% наблюдений выявлена, наряду с признаками вирусной пневмонии (причем как на экссудативной, так и пролиферативной стадиях альвеолярного повреждения), бактериальная очаговая, сливная или долевая пневмония. В одном наблюдении с вирусной пневмонией была обнаружена аспирапионная бронхопневмония (инородные пищевые фрагменты в просветах бронхов, бронхиол и альвеол).
В более позднюю стадию заболевания в легких (чаще в нижних долях) обнаруживаются участки организующейся пневмонии и умеренно выраженные разрастания фиброзной ткани, а также изменения, характерные для фиброзирующего альвеолита (макроскопически - «сотовое легкое»). Описанные выше изменения в ткани легких в дальнейшем могут приводить к развитию хронической дыхательной недостаточности, вторичной легочной гипертензии и легочного сердца.
В изученных наблюдениях обращала на себя внимание не только выраженность сосудистой патологии легких и альвеоляорно- геморрагического синдрома, но и несоответствие классических стадий диффузного альвеолярного повреждения длительности заболевания. Так, в части наблюдений изменения легких, характерные для ранней экссудативной стадии бьши обнаружены после 14 суток от начала заболевания при отсутствии изменений, характерных для поздней пролиферативной стадии.
Помимо изменений легких, разной степени выраженности, на аутопсиях были выявлены достаточно разнообразные поражения других органов и систем, патогенез которых пока не ясен, но вероятно носит сложный многофакторный характер. Среди таких основных факторов - специфическое повреждающее действие SARS-CoV-2, гипоксия, микроангиопатия и гиперкоагуляция и гиперэргическая иммунная реакция (возможно, и аутоиммунная), а также ятрогенное лекарственное повреждение. Кроме того различные патологические изменения связаны с коморбидными заболеваниями и их осложнениями, что очень характерно для COVID-19, летальные исходы от которого в подавляющем большинстве наблюдаются у больных старших возрастных группа.
В отличие от, например, гриппа, для eOVID-19 не характерен трахеобронхит с яркой воспалительной гиперемией. В большинстве наблюдений слизистая оболочка бледная, без явных повреждений, с точечными кровоизлияниями при две-синдроме. Исключением являются умершие, находившиеся на ИВЛ с развитием бактериальных трахеитов и бронхитов.
Типично выраженное острое общее венозное полнокровие, у большой части умерших - микроанпюпатия и две-синдром с распространенным геморрагическим синдромом (включая кожу, слизистые и серозные оболочки), свежие или организующиеся тромбы в просветах артерий и вен разной локализации (помимо легких). У отдельных умерших бьш диагностирован сепсис (этиология - различная бактериальная смешанная флора), протекавший как с полиорганными гнойными очагами (септикопиемия), так как септический шок, что наблюдалось более часто.
В головном мозге обнаружены диффузные гипоксические и очаговые, разной величины ишемические повреждения, вплоть до развития ишемических инфарктов (при тромбозах крупных артерий), микроангиопатия, васкулиты, диапедезные и сливные кровоизлияния, иногда прогрессирующие до геморрагических инфарктов и, реже гематом. В ряде случаев дифференциальная диагностика таких проявлений и осложиений eOVID-19 с различными нозологическими единицами из группы цереброваскулярных болезней представляет серьезную проблему, особенно у коморбидных больных.
Лимфоидная периваскулярная и оболочечная инфильтрация, в отдельных наблюдениях (в том числе и в случаях без сепсиса), не позволяет исключить возможиость развития специфического энцефалита и менингита.
В миокарде также характерны диффузные гипоксические, метаболические и разной величины ишемические повреждения, реже - микроангиопатия, петехиальные и сливные кровоизлияния. При тромбозах коронарных артерий (в отсутствии нестабильных атеросклеротических бляшек или вообше атеросклероза) у части умерших развивались мелкоочаговые, реже - трансмуральные инфаркты миокарда, что при выявлении микроскопической картины вирусного повреждения стенки венечной артерии, отсутствии нередко атеросклреоза, следует расценивать как проявление или осложнение COVID-19. Такие инфаркты миокарда следует дифференцировать с инфарктами миокарда 1 типа, при осложненных нестабильных атеросклеротических бляшках коронарных артерий сердца - самостоятельными нозологическими единицами из группы ИБС.
Межклеточная и периваскулярная мононуклеарная инфильтрация указывает на возможность развития в редких случаях миокардита различной этиологии, возможно, специфического.
В почках наблюдали гипоксические, метаболические и ишемические повреждения - субстрат нередко наблюдаюшегося синдрома острой почечной недостаточности с некрозом и дистрофическими/некротическими изменениями эпителия извитых канальцев. Встречались ишемические инфаркты, вследствие тромбозов артерий почек разного калибра. Однако нельзя исключить специфический характер поражения почек в виде микроангиопатии и вариантов повреждения клубочков по типу формируюшегося фокального сегментарного гломерулосклероза (коллабируюшей гломерулопатии), а также гломерулонефрита (пролиферация мезангиальных клеток и инфильтрация лимфоцитами, фибриноидный некроз капилляров клубочков) с тубуло-интерстициальным компонентом (лимфоидная инфильтрация, отек стромы). Как и при анализе патологических изменений других органов, большие трудности представляет собой дифференциальная диагностика этих проявлений и осложнений COVID-19 с различными коморбидными заболеваниями, в частности, с хроническим пиелонефритом.
В печени во всех наблюдениях выявлялась жировая дистрофия, разной степени выраженности, вероятно, mпоксического и метаболического, возможно и ятрогенного патогенеза. Характерны петехиальные кровоизлияния и, в отдельных случаях, лимфоидиая инфильтрация портальных трактов, сходная с реактивным межуточным гепатитом (помимо наблюдений с сепсисом, для которого такие изменения типичны). В отдельных наблюдениях обнаружены обширные некрозы ткани печени, вплоть до субтотальных.
В органах иммунной системы выявлен широкий диапазон изменений, зависяший, как и поражения других органов, по-видимому, от инфекционных агентов, длительности болезни, коморбидных заболеваний, особенностей терапии и др. - от выраженного опустошения, напоминающего изменения при ВИЧ-инфекции на стадии СПИД, до разной степени гиперплазии, преимущественно, Т-зависимых, так и, реже - В-зависимых зон лимфоидной ткани. Также, как и в легких, в краевых синусах лимфатических узлов были обнаружены феномены аутоцитофагии, от гемоцитофагии до фагоцитоза макрофагами фрагментов и целых лимфоцитов.
Селезенка была в разной степени гиперплазирована, полнокровна, давала умеренный соскоб на срезе, встречались ее инфаркты и тромбы в сосудах.
Патология желудочно-кишечного тракта представляет большой интерес в связи с сообщениями о кишечных клинических проявлениях COVID-19 и развитии катарального гастроэнтероколита. Однако изучение изменений слизистой оболочки затруднено посмертным аутолизом и характер патологических изменений желудочно-кишечного тракта остается пока недостаточно изученным.
Изменения кожи отличались чрезвычайным полиморфизмом и, вероятно, разнообразной этиологией, от геморрагического синдрома до различных высыпаний, гистологически выявлялась микроангиопатия в виде деструктивно-продуктивного тромбоваскулита.
КЛИНИКО-МОРФОЛОГИЧЕСКАЯ КЛАССИФИКАЦИЯ ПРИЧИН СМЕРТИ ПРИ COVID-19
На основании результатов патологоанатомических вскрытий более 2000 умерших с COVID-19 и накопленного клинического опыта при лечении таких больных, для повышения качества аналитической информации о причинах смерти при COVID-19 и их кодирования по МКБ-10 в рамках рекомендаций ВОЗ от апреля 2020 г. (с их детализацией) целесообразно выделять следуюшие группы учета по причинам смерти. Такая клинико морфологическая классификация служит не только целям статистики, но является важной основой для разработки новых протоколов и методов лечения COVID-19.
Первая группа - случаи смерти, в которых COVID-19 являлся основной причиной смерти (U07. l, U07.2).
Вторая группа - случаи смерти, когда COVID-19 не стал основной их причиной и, являясь коморбидным или сопутствуюшим заболеванием, не оказал существенного влияния на течение основного заболевания и развитие его смертельных осложнений.
Например:
S00-S99; ТОО-Т65 Травмы, отравления 161.0-163.5 Инсульты
120.0-121.3 -Острые инфаркты миокарда 1 типа
125.5 -Ишемическая кардиомиопатия - 197
!05.2, 135.8 Пороки сердца, декомпенсированные
СОО-С97 Онкологические заболевания (включая лейкозы и лимфомы) 4-й стадии
К25-К38, К40-К46, К70.3, К74.6, К85, KS0-87 Болезни органов пищеварения (язва желудка с кровотечением и прободением, острая кишечная непроходимость, ущемленная грыжа, острый аппендицит, острый холецистит, цирроз печени алкогольный и неуточненный
Полный текст статьи:
Рекомендуемые статьи
При эндоскопическом исследовании в случае бронхоэктазов в стадии ремиссии выявляется
частично диффузный бронхит I степени воспаления
Активируйте PUSH уведомления в браузер
Отключите PUSH уведомления в браузер
Содержание
Интернет магазин
Популярное
- О нас
- Правовые вопросы
- Политика
обработки персональных
данных EndoExpert.ru - Связаться с нами
- Стать партнером
© 2016-2022 EndoExpert.ru

Вы находитесь в разделе предназначенном только для специалистов (раздел для пациентов по ссылке). Пожалуйста, внимательно прочитайте полные условия использования и подтвердите, что Вы являетесь медицинским или фармацевтическим работником или студентом медицинского образовательного учреждения и подтверждаете своё понимание и согласие с тем, что применение рецептурных препаратов, обращение за той или иной медицинской услугой, равно как и ее выполнение, использование медицинских изделий, выбор метода профилактики, диагностики, лечения, медицинской реабилитации, равно как и их применение, возможны только после предварительной консультации со специалистом. Мы используем файлы cookie, чтобы предложить Вам лучший опыт взаимодействия. Файлы cookie позволяют адаптировать веб-сайты к вашим интересам и предпочтениям.
Я прочитал и настоящим принимаю вышеизложенное, хочу продолжить ознакомление с размещенной на данном сайте информацией для специалистов.














.jpg)





.png)



.jpg)














Комментарии