- Компании
- Takeda. О компании, буклеты, каталоги, контакты
- Olympus. О компании, буклеты, каталоги, контакты
- Boston Scientific. О компании, буклеты, каталоги, контакты
- Pentax. О компании, буклеты, каталоги, контакты
- Fujifilm & R-Farm. О компании, буклеты, каталоги, контакты
- Erbe. О компании, буклеты, каталоги, контакты
- Еще каталоги
- Мероприятия
- Информация
- Обучение
- Классификации
- Атлас
- Quiz
- Разделы
- Пациенту
QR-код этой страницы

Для продолжения изучения на мобильном устройстве ПРОСКАНИРУЙТЕ QR-код с помощью спец. программы или фотокамеры мобильного устройства
Статьи: ЭНДОСКОПИЧЕСКАЯ ДИАГНОСТИКА БАКТЕРИАЛЬНЫХ КОЛИТОВ
| Авторы: | Аникина М.С. 1 2018г. |
| Об авторах: |
1. Врач-эндоскопист ГБУЗ НСО «ГНОКБ». Новосибирск |
Аннотация:
Острые кишечные инфекции (ОКИ, острые диарейные болезни) — по терминологии ВОЗ это большая группа заболеваний, объединённых развитием диарейного синдрома. Число клинических форм превышает 30 нозологических единиц, возбудителями которых могут быть бактерии, вирусы и простейшие.

Полный текст статьи:
В соответствии с Международной статистической классификацией болезней и проблем, связанных со здоровьем (МКБ–10 пересмотра; 1995), в группе кишечных инфекций (А.00–А.09) регистрируются следующие заболевания:
А.00 — холера;
А.01 — брюшной тиф и паратифы А, В, С;
А.04 — другие бактериальные инфекции и в том числе эшерихиоз, кампилобактериоз, кишечный иерсиниоз, клостридиоз, вызванный Сl.difficile;
А.05 — другие бактериальные пищевые отравления и в том числе стафилококковое, ботулизм, клостридиоз, вызванный Cl.perfringens, Vibrio parahaemolyticus, Bac. cereus, бактериальное пищевое отравление неуточненной этиологии;
А.06 — амебиаз;
А.07 — другие протозойные кишечные болезни и в том числе балантидиаз, лямблиоз, криптоспоридиоз, изоспороз;
А.08 — вирусные кишечные инфекции и в том числе ротавирусный энтерит, вызванный агентом Норфолк, аденовирусный гастроэнтерит;
А.09 — диарея и гастроэнтерит предположительно инфекционного происхождения. [9]
Основными особенностями инфекционных колитов являются специфичность, контагиозность, цикличность течения, формирование постинфецкционного специфического
иммунитета. Течение заболевания зависит как от биологических свойств возбудителя, так и от реактивности макроорганизма. Инфекционный колит часто имеет внезапное начало и быструю инволюцию клинических проявлений, однако может встречаться затяжное и интермиттирующее течение. [3;7]
При явной картине инфекционного процесса колоноскопия не показана. Однако в определенных случаях имеет важное диагностическое значение. Колоноскопия показана всем пациентам с кишечными расстройствами невыясненной этиологии. Несмотря на ограниченную диагностическую ценность, применение эндоскопических методов при подозрении на инфекционный колит позволяет объективно оценить характер, степень выраженности, локализацию и протяженность поражения слизистой толстой кишки, провести забор материала для гистологического исследования, а так-же контролировать эффективность проводимой терапии. [2; 3; 4; 23; 26] Некоторые авторы отмечают более высокую информативность материала (биоптаты для ПЦР, кал, смывы), забранного адресно из зоны поражения при эндоскопическом исследовании перед материалами, полученными традиционными способами. Биоптат для микробиологического исследования или ПЦР следует помещать в физиологический раствор. [21]
Эндоскопическая картина инфекционного колита в большинстве случаев неспецифична и должна основываться на стандартном алгоритме описания воспалительных изменений толстой кишки (эндоскопические проявления, оценка активности процесса, локализация и протяженность поражения).
По преимущественной локализации колит может быть:
1. Тотальный (воспалительный процесс поражает все отделы толстой кишки. В этом случае макроскопические изменения на всем протяжении могут носить однородный или неоднородный характер).
2. Сегментарный (толстая кишка поражается в пределах одного анатомического отдела (проктит, сигмоидит, трансверзит, тифлит и т.д.).
3. Полисегментарный (в патологический процесс вовлекается несколько анатомических отделов толстой кишки (проктосигмоидит, левостороннний колит, правосторонний колит). В этом случае макроскопические изменения могут носить непрерывный или прерывистый (скачкообразный) характер).
4. Локальный (поражаются участки толстой кишки в пределах одного из её анатомических отделов (локальный сигмоидит, локальный проктит, локальный трансверзит и т.д. [3; 7]
При колитах выявляются признаки воспаления слизистой оболочки толстой кишки различной степени выраженности:
а) катаральные,
б) катарально-геморрагические,
г) язвенные,
д) фибринозные (крупозные и дифтеритические).
При морфологическом исследовании определяется отек, расширение капилляров, воспалительная клеточная инфильтрация, которая в основном ограничивается собственной пластинкой слизистой.
При резко выраженном катаральном воспалении слизистая оболочка толстой кишки резко отечна, гиперемирована, за счет выраженной воспалительной инфильтрации складки утолщены, сосудистый рисунок отсутствует. На этом фоне обнаруживаются поверхностные повреждения слизистой оболочки с кровоточащим или темно-красным дном до 0,2 см, то есть развивается эрозивный процесс. На поверхности слизистой оболочки обнаруживается слизистый или слизисто-геморрагический экссудат. При морфологическом исследовании выявляется отек и воспалительная клеточная инфильтрация, которые распространяются на всю толщу слизистой оболочки и, в некоторых случаях, частично — на под слизистую основу, некроз покровного эпителия и деструкция кишечных желез. На фоне тугого воспалительного инфильтрата также определяются резко расширенные капилляры и субэпителиальные кровоизлияния.
Обычно, диффузное катаральное воспаление сопровождает большинство инфекционных бактериальных колитов, а также наблюдается при неспецифических колитах. В некоторых случаях на фоне катарального воспаления отчетливо выявляется увеличение фолликулов в виде своеобразной зернистости слизистой оболочки (фолликулярно-катаральное воспаление). При значительной выраженности воспалительного процесса наряду с катаральными изменениями в слизистой оболочке выявляются мелкие точечные кровоизлияния или более крупные геморрагии диаметром до 2–3 мм (катарально-геморрагические изменения). В части случаев на фоне катарально-геморрагического процесса обнаруживаются поверхностные повреждения слизистой оболочки с кровоточащим или темно-красным дном, то есть развивается эрозивный процесс. На поверхности слизистой оболочки обнаруживается слизистый или слизисто-геморрагический экссудат. При морфологическом исследовании определяются дефекты слизистой оболочки, ограниченные ее мышечной пластинкой. В краях эрозий имеется воспалительная инфильтрация, клеточный состав которой зависит от вида заболевания. В слизистой оболочке вокруг изъязвлений микроскопически также обнаруживаются признаки воспаления: выраженная круглоклеточная инфильтрация, отек, капилляростаз и субэпителиальные кровоизлияния.
При фибринозно-некротическом воспалении появляются плотные грязно-серые налеты. Некроз может достигать подслизистой основы и даже мышечного cлоя толстой кишки. При этом гнойное расплавление и отторжение некротических масс приводят к образованию язв. Язвенный колит, также как и эрозивный, характеризуется двумя типами воспалительных изменений: диффузное катаральное воспаление (различной степени выраженности) сопровождает очаговый некротический процесс. Глубокие дефекты слизистой оболочки, одиночные или множественные, могут иметь различную форму, размеры, характер краев и дна.
При морфологическом исследовании выявляются дефекты, пенетрирующие в подслизистую основу или в мышечный слой кишечной стенки. В краях язв — отёк и выраженная воспалительная инфильтрация, клеточный состав которой определяется видом заболевания. Эрозивно-язвенные процессы наблюдаются при тяжелых формах инфекционных колитов, болезни Крона, неспецифическом язвенном колите, НПВС-ассоциированном колите, болезни Бехчета, ишемическом и лучевом колите, при некоторых видах дисбиозов.
|
Наименование инфекции |
Неспецифический язвенный колит |
Болезнь Крона |
|
Шигеллез |
+++ |
- |
|
Сальмонеллез |
+++ |
+ |
|
Цитомегаловирусная инфекция |
+++ |
+ |
|
Иерсиниоз |
++ |
+++ |
|
Туберкулез |
-/+ |
+++ |
|
Амебиаз |
++ |
++ |
|
Герпес |
- |
+ |
Таблица 1. Степени сходства эндоскопической картины инфекционных колитов с неспецифическими воспалительными заболеваниями толстой кишки (по Silverstein et Tygat, 1987) [3;7]
Следует отметить, что вариабельность патоморфологических изменений кишечной стенки в ответ на различные повреждающие факторы достаточно ограничена, в результате чего эндоскопическая картина и данные гистологического исследования при хронический воспалительных заболеваниях кишечника и инфекционных колитах в ряде случаев неразличимы или плохо дифференцируемы. Степень сходства эндоскопической картины инфекционных колитов с хроническими воспалительными заболеваниями толстой кишки приведены в таблице 1. Судить об этиологическом факторе инфекционного поражения по эндоскопической картине можно только с большей или меньшей степенью вероятности (заключение носит предполагаемый характер). При этом наличие хронического воспалительного заболевания в анамнезе не исключает инфекционную природу болезни. Для проведения дифференциальной диагностики требуется весь комплекс копрологического, микробиологического и серологического обследования. Наибольшие трудности дифференциальной диагностики инфекционных колитов и хронических воспалительных заболеваний кишечника возникают в дебюте острой тяжелой формы НЯК, а также хронического рецидивирующего течения НЯК с дизентерией. [2; 3; 7;10; 18; 22]
Патофизиологические механизмы бактериальной диареи могут включать в себя выработку энтеротоксина, повышающего активность аденилатциюлазы (и соответственно увеличивающего внутриклеточное содержание цАМФ) и стимулирующего таким образом секрецию воды и электролитов энтероцитами, или же прямую инвазию бактерий в эпителиальные клетки слизистой оболочки кишечника с их последующим повреждением и развитием воспалительной реакции. Таким образом возбудителей бактериальных инфекционных поражений кишечника разделить на две группы: инвазивные (шигеллезный тип): заболевания, вызываемые этими возбудителями, благодаря их способности к клеточной инвазии и последующей токсинемией (эндотоксин), характеризуются выраженной общеинтоксикационной симптоматикой (лихорадка, миалгии, головная боль и т.д.) и явлениями кишечного цитолиза, проявляющимися наличием в испражнениях эритроцитов и лейкоцитов. К данной группе относятся возбудители дизентерии, сальмонеллеза, йерсиниоза, кампилобактерной инфекции и др.; неинвазивные (холерный тип): патогенетическое влияние реализуется через нарушение мембранного транспорта (энтеротоксин — токсин, выработанный бактерией вне организма человека, экзотоксины — токсины, выделяющиеся бактерией в кишечнике) и характеризуется сравнительно слабо выраженной общей симптоматикой (за исключением выраженной степени обезвоживания) и цитолитическим синдромом. К данной группе относятся холерный вибрион, некоторые шигеллы, клостридии и др.
При этом все бактериальные кишечные инфекции имеют сравнительно схожую клиническую картину, в которой выделяют: интоксикационный синдром (лихорадка, тахикардия, миалгии, артралгии, кожная сыпь); гастоэнтеритический синдром (диспепсические явления, диарея, боли в животе); синдром гастроэнтерита или гастроэнтероколита, энтероколита или колита.
При различных кишечных инфекциях локализация поражения того или иного отдела желудочно–кишечного тракта различна. Примерами могут служить пищевые токсикоинфекции с преимущественным поражением желудка и тонкой кишки и шигеллез с преимущественным поражением толстой кишки. Эндоскопические проявления в каждом конкретном случае будут зависеть в первую очередь от глубины воспалительно-некротического поражения кишечной стенки (вирулентности микроорганизма и величины бактериальной обсемененности). [2; 3; 6; 9; 10]
Шигеллез (дизентерия) — острое инфекционное заболевание, вызываемое большой группой микробов рода шигелл, характеризующиеся симптомами общей интоксикации и поражением преимущественно дистального отдела толстого кишечника (прямая и сигмовидная), в 1-2 % случаев возможно полисегментарное непрерывное поражение толстой кишки (левосторонний колит, тотальный колит).
Согласно Международной классификации (1968) различают 4 подгруппы рода шигелл: А – Sh. dysenteriae включает 12 сероваров (Григорьева-Шига,Штуцера-Шмитца, Ларджа-Сакса); В – Sh. flexneri включает 6 сероваров, 10 подтипов и варианты X, У и вид Ньюкасл; С – Sh. boydii включает 18 cеротипов; D – включает шигеллы Зонне. Они различаются по ферментативной и колициногенной характеристике, хотя и имеют совпадающую антигенную структуру. Ключевым фактором вирулентности шигелл является их инвазивность.
По степени выраженности симптомов интоксикации и диспепсии бактериальная дизентерия может быть легкой, среднетяжелой и тяжелой формы. Степень выраженности изменений кишечной стенки коррелирует с клинической формой течения инфекционного заболевания.При остром шигеллезе воспалительные изменения слизистой толстой кишки могут быть любой степени выраженности, от диффузного катарального до фибринозно-гнойного. В пределах пораженного сегмента изменения чаще носят непрерывный и однотипный характер.
Геморрагический синдром обусловлен токсической капилляропатией, по этому опережает воспалительно-деструктивные изменения слизистой оболочки толстой кишки: катаральное воспаление сопровождается образованием контактных субэпителиальных геморрагии, в то время как эрозивный и язвенный колит сопровождается умеренной контактной кровоточивостью.
При хроническом шигеллезе морфологические изменения многообразны,что обусловлено постоянным сочетанием процессов регенерации и свежих воспалительных изменений. Воспалительный процесс обычно течет вяло, выявляются участки с деформированными криптами и выраженной атрофией слизистой оболочки. В тонкой кишке развивается острое капиллярное полнокровие с выраженным отёком ворсин и крипт слизистой оболочки. Вследствие токсинемии, наряду с патогномоничными изменениями желудочно-кишечного тракта развиваются неспецифические изменения и в других органах и тканях организма.
Результаты морфологического исследования биоптата неспецифичны: острая воспалительная инфильтрация, ограниченная собственной пластинкой слизистой оболочки. Заживление дефектов слизистой оболочки происходит путем эпителизации, без видимых структурных изменений стенки кишки.
Результаты копрологического исследования характерны для острого воспаления слизистой оболочки толстой кишки.
Khuroo MS, Mahajan R отмечают стадийность поражения слизистой толстой кишки при шигеллезах: отек слизистой оболочки наиболее часто определялся в первую неделю заболевания. Ломкость сосудов и эрозивно-язвенные поражения выявляются на 2-й и 3-й неделе заболевания. Неоднородность поражения в виде точечных геморрагий с промежутками нормальной слизистой оболочки являются признаком этого заболевания от 4-й недели. Таким образом, однородные поражения в первые недели заболевания сменяются неоднородными на более поздней стадии. Изменения слизистой сохранялись на протяжении 38,8 +/- 12,1 (10-65) дней. [15]
Картина и характер макроскопических изменений слизистой оболочки толстой кишки при шигеллезах в ряде случаев сходны с сальмонеллезом, иерсиниозом, амебиазом, а также с неспецифическим язвенным колитом и болезнью Крона.
Специфическая диагностика: результаты бактериологического исследования специфичны, методика наиболее чувствительна при заборе материала в первые 3 дня от начала заболевания. Ускоренная диагностика может осуществляться без выделения чистых культур по обнаружению антигенов возбудителей и их токсинов в биосубстратах: слюне, моче, копрофильтрате, крови. Используются ИФА (иммуноферментный анализ), РАЛ (реакция агглютинации латекса), РКоА (реакция коагглютинации), РИФ (реакция иммунофлюоресценции), ПЦР (полимеразная цепная реакция). Для выявления антител применяют реакции непрямой (пассивной) гемагглютинации (РНГА, РПГА). Диагностически достоверным считается увеличение титра антител в парных сыворотках с интервалом 8-10 дней не менее, чем в 4 раза. [4; 9; 14; 154 26 ]
Иерсиниоз — острое инфекционное заболевание с преимущественным поражением органов желудочно-кишечного тракта. Возбудитель Y. enterocolitica, относящаяся к роду Yersinia (к этому роду относится и
Y. pseudotuberculosis, возбудитель псевдотуберкулеза, антигенная структура и факторы агрессии схожи). По О-антигену выделяют 50 сероваров Y. enterocolitica и 8 сероваров
Y. pseudotuberculosis. В большинстве случаев источником заболевания являются селькохозяйственные животные или грызуны. При разрушении возбудителя выделяется большое количество эндотоксина, но некоторые штаммы могут выделять экзотоксин.
По ведущему синдрому выделяют несколько клинических форм: а) локализованные (гастроинтестинальную (гастроэнтеритическую, энтероколитическую, гастроэнтероколитическую) и абдоминальную (аппендикулярную, мезентериальную)); б) генерализованные (желтушную, экзантемную, артралгическую, септическую); в) вторично-очаговую формы. Болеют, как правило, дети; часто поражаются кожа и суставы. Заболевание может протекать в лёгкой, средне-тяжёлой и тяжёлой форме. При иерсиниозном колите изменения слизистой имеют сегментарный характер, поражается преимущественно правая половина толстой кишки, всегда отмечается поражение слизистой подвздошной кишки, причем изменения стенки терминального отдела подвздошной кишки выражены сильнее. Отмечается несоответствие между выраженностью изменений слизистой и контактной кровоточивостью. Всегда поражается лимфатический аппарат слизистой, что проявляется наличием шероховатости или зернистости слизитой, что связано с патогенезом иерсиниоза. Макроскопические изменения стенки кишки коррелируют с тяжестью течения заболевания. При лёгкой форме изменения слизистой минимальны. Отмечается слабая гиперемия и отёк слизистой, сосудистый рисунок сохранён, но обеднён, слизистая мелкозернистая, складки слизистой сохранены, несколько утолщены, снижены. Кровоточивость слизистых отсутствует. Морфологически выявляется полиморфноклеточная инфильтрация подслизистой основы и частично глубоких слоев слизистой оболочки, гиперплазия лимфоидной ткани, входящей в состав слизистой оболочки.
При среднетяжёлой форме слизистая оболочка очагово гиперемирована, имеет сетчатый или мозаичный рисунок, блестящая, с выраженной зернистостью, сосудистый рисунок смазан, складки низкие, широкие. На этом фоне обнаруживаются множественные афты: эрозии размерами 0,3-0,5 см округлой формы, окруженные венчиком гиперемии. Контактная кровоточивость отсутствует или выражена слабо (рис. 2 (E)).
Морфологически отмечаются: выраженная воспалительная инфильтрация подслизистой основы и слизистой оболочки, представленная нейтрофилами, эозинофилами и плазматическими клетками; деструкция кишечных желез с формированием «крипт-абсцессов»; гиперплазия лимфоидной ткани слизистой оболочки.
При тяжёлой форме слизистая оболочка диффузно гиперемирована, отёчная, с выраженной зернистостью, сосудистый рисунок отсутствует, определяются мелкоточечные внутрислизистые кровоизлияния. За счёт отёка кишечной стенки складки сглажены. На этом фоне имеются глубокие язвенные дефекты до 1 см в диаметре овальной или округлой формы, в дне язв — фибринозно-гнойный экссудат. Язвы не склонны к слиянию. Контактная кровоточивость минимальная или умеренно выражена.
При морфологическом исследовании выявляется полиморфноклеточная инфильтрация всех слоёв кишечной стенки, наиболее выраженная в подслизистой основе, микротромбозы, некроз покровного эпителия, деструкция желез. Редко обнаруживаются иерсиниозные гранулемы, состоящие из макрофагов, эпителиоидных клеток и единичных гигантских клеток типа Пирогова-Лангханса. Для иерсиниозных гранулем характерны кариорексис и гнойное расплавление. В материале, полученном из дна язв при помощи «браш-биопсии» (фи- бринозно-гнойный экссудат), определяются возбудители. Заживление язв происходит путем эпителизации, но может протекать и через рубцевание без стенозирования просвета.
Дифференциальный диагноз проводят с острыми желудочно-кишечными инфекционными заболеваниями (острой дизентерией, эшерихиозом, сальмонеллезом, псевдотуберкулезом, вирусным гепатитом, скарлатиной, краснухой, токсико-аллергической эритемой).
В установлении окончательного диагноза решающую роль имеют лабораторные методы — бактериологический и серологический. В остром периоде болезни выделить возбудителя возможно из фекалий, мочи, мазков слизи из ротоглотки, удалённых аппендиксов и мезентериальных лимфатических узлов. Для диагностики псевдотуберкулеза используют методику Паттерсона и Кука, основанную на способности Y. pseudotuberculosis расти при пониженной температуре в среде подращивания (стерильный фосфатно-солевой буфер рН 7,4, среда Серова и др.).
В серологической диагностике используют реакции агглютинации (РА) и непрямой гемагглютинации (РНГА). Диагностическим титром может считаться для РА 1:200, для РНГА 1:100. Достоверным диагностическим критерием является четырёхкратное нарастание титра специфических антител в динамике заболевания при исследовании парных сывороток. Использование серологических методов, основанных на обнаружении специфических антител к антигенам иерсиний, имеет ряд серьезных недостатков, основными из которых являются невысокая специфичность и поздние сроки подтверждения диагноза.
РНГА, РНИФ (реакция непрямой иммунофлюоресценции), РКА (реакция коагглютинации), латексагглютинация, ИФА (иммуноферментный анализ) используют для ранней экспрессдиагностики. Для выделения возбудителя из различных сред организма может использоваться ПЦР (полимеразная цепная реакция). [3; 7; 10; 7; 6; 21]
Сальмонеллез — это полиэтиологическая инфекционная болезнь, вызываемая различными серотипами бактерий рода Salmonella, характеризуется разнообразными клиническими проявлениями от бессимптомного носительства до тяжелых септических форм. В большинстве случаев протекает с преимущественным поражением органов пищеварительного тракта (гастроэнтериты, колиты). Возбудитель — большая группа сальмонелл (семейство Enterobacteriaceae, род Salmonella), насчитывающая в настоящее время более 2200 серотипов. Основными факторами патогенности сальмонелл являются холероподобный энтеротоксин и эндотоксин липополисахаридной природы. Некоторые штаммы обладают способностью инвазии в эпителий толстой кишки (S. enteritidis et S. typhimurium). Клинические формы сальмонеллеза: гастроинтестинальная (локализованная), протекающая в гастритическом, гастроэнтеритическом, гастроэнтероколитическом и энтероколитическом вариантах; генерализованная форма в виде тифоподобного и септического вариантов; бактерионосительство: острое, хроническое и транзиторное; субклиническая форма. Манифестные формы сальмонеллеза различаются по тяжести течения. Наиболее частый клинический вариант гастроэнтеритический. Гастроэнтероколитические и колитические варианты заболевания должны диагностироваться только, если в клинической картине заболевания преобладают проявления колита и имеется бактериологическое или серологическое подтверждение диагноза, так как эти варианты сальмонеллеза весьма сходны по течению с острой дизентерией. Эндоскопическая картина при сальмонеллезе также зависит от тяжести течения. Изменения слизистой желудка и тонкой кишки носят преимущественно катаральный характер, катарально-геморрагические проявления регистрируются лишь в небольшом проценте случаев. Учитывая, что внедрение возбудителя происходит в тонкой кишке, всегда регистрируются изменения в терминальном отделе подвздошной кишки, при этом они обычно менее выражены, чем в толстой кишке. Чаще поражаются правые отделы толстой кишки. Изменения слизистой в пределах одного поражённого сегмента кишки однотипные и непрервные. Отмечаются признаки поражения лимфоидного аппарата в виде зернистости и шероховатости слизистой. При лёгкой форме слизистая оболочка поражённых отделов толстой кишки отёчна, гиперемирована, сосудистый рисунок смазан, поверхность её шероховатая, мелкозернистая, блеск сохранён. Складки чётко контурируются, однако высота их снижена. Контактная кровоточивость выражена, даже при лёгком дотрагивании аппаратом образуются внутрислизистые кровоизлияния. При среднетяжёлой форме на фоне резко выраженного катарального колита имеются множественные сливные внутрислизистые кровоизлияния, складки вследствие воспалительной инфильтрации подслизистой основы несколько сглажены. Сохраняется зернистость слизистой оболочки (величина
«зёрен» до 0,2 см). Контактно образуются неправильной формы подслизистые кровоизлияния, крайне редко кровь появляется на поверхности слизистой оболочки. Редко обнаруживаются небольшие поверхностные дефекты до 0,5 см неправильной формы с нежным налетом фибрина. В просвете много мутноватой жидкости. При тяжёлой форме на фоне вышеописанных изменений определяются множественные неправильной формы поверхностные дефекты слизистой оболочки размерами до 1 см. Края их умеренно инфильтрированы. И только в 1-1,5 % случаев при выраженном катаральном воспалении обнаруживаются единичные язвенные дефекты вытянутой формы с инфильтрированными краями, дно их покрыто фибрином. Язвы не склонны к слиянию. Увеличение их размеров происходит в продольном направлении. Отмечается значительная контактная кровоточивость (Шувалова Е.П., 1976). Морфологически при исследовании тканей обнаруживается различной степени выраженности воспалительная инфильтрация, захватывающая слизистую оболочку и подслизистую основу, деструкция отдельных желёз, множественные очаги кровоизлияний. Лимфоидные фолликулы слизистой оболочки гиперплазированы, капилляры расширены, в некоторых из них выявляются микротромбозы. Дефекты слизистой оболочки пенетрируют в подслизистую основу, края их также инфильтрированы. При заживлении язвы при сальмонеллезном колите эпителизируются. Окончательный диагноз устанавливается на основании бактериологического исследования (фекалии, рвотные массы, промывные воды желудка, а при генерализованных формах — кровь и гнойное отделяемое). Из серологических проб проводится РПГА и РИГА. Более информативна последняя реакция. Антитела выявляются с 4-6-го дня, достигая максимума на 2-3-й неделе. Диагностический титр 1:160 и выше. Более доказательно на- растание титра антител при повторном исследовании с сальмонелезным антигеном. [6; 7; 10]
Кампилобактериоз — острое инфекционное заболевание, характеризующееся острым началом, лихорадкой, интоксикацией, преимущественным поражением желудочно-кишечного тракта.
Возбудителем кампилобактериоза являются микроорганизмы рода Campylobacter, объединяющие 10 видов. Из них следует вы- делить С.jejuni, являющийся возбудитлем наибольшего числа заболеваний и С. fetus, ответственный за большее число генерализованных форм кампилобактериоза. В последнее время большое внимание уделяют болезням, обусловленным С. pylori, который в настоящее время получил название Helicobacter pylori, а болезни, им обусловленные — хеликобактериоз. Хронический гастрит и язва желудка, которые этиологически связывают с кампилобактериозом, изучаются терапевтами гастроэнтерологамии. Нет необходимости рассматривать их как инфекционные болезни. С.jejuni С. fetus имеют термостабильные О-антигены и термолабильные Н-антигены. Отмечена антигенная связь с бруцеллами. Подразделяются на серотипы (их более 50), однако 10 наиболее распространённых серотипов обусловливают около 70 % всех заболеваний. По клиническому течению выделяют следующие формы кампилобактериоза:
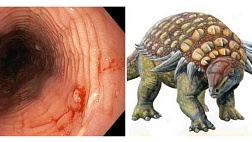
Кампилобактерный колит отличается тотальным непрерывным поражением слизистой толстой кишки, изменения носят преимущественно катаральный или катарально-геморрагический характер. Обнаруживается диффузная гиперемия слизистой. При этом патогномоничным признаком является поражение илеоцекального клапана в виде небольших округлых язв с кровоизлияниями в краях (рис. 2 (D)). [10; 11; 21; 26]
Диагноз подтверждают выделением возбудителя из испражнений, крови, цереброспинальной жидкости, ткани абортированного плода. Посевы делают на специальные селективные твёрдые питательные среды с бриллиантовым зелёным, с тиогликолятом или триптиказосоевый бульон с 5 % бараньей или лошадиной кровью и антибиотиками. Для ретроспективной диагностики используют серологические методы. Исследуют парные сыворотки, взятые с интервалом 10-14 дней. Для выявления антител используют различные реакции (РСК, РПГА, микроагглютинации, иммунофлюоресцентный метод). [6; 10]
Антибиотик-ассоциированный геморрагический колит — инфекционное заболевание, характеризующееся поражением слизистой оболочки толстой кишки, которое в большинстве случаев наблюдается при использовании полусинтетических пенициллинов. У большинства пациентов оно развивается в ближайшие трое суток от момента начала лечения, клинически протекает относительно легко, характеризуется умеренными болями в животе и расстройством стула, редко в испражнениях отмечается примесь крови. Как правило, симптомы общей интоксикации отсутствуют или выражены слабо. После отмены антибиотика (замены) и проведения симптоматической терапии клинические проявления заболевания купируются в течение нескольких суток. Точные причины данного состояния не до конца изучены. Учитывая, что при бактериологическом исследовании стула практически у всех пациентов выделяется Klebsiella oxytoca, предполагается её роль в этиопатогенезе этого вида колита. Вторым механизмом развития антибиотик-ассоциированного геморрагического колита считаются аллегрические реакции по типу ГЗТ на полусинтетические пенициллины. Klebsiella oxytoca — капсульная грамотрицательная палочка, которая, как условно-патогенная флора, может вегетировать в желудочно-кишечном тракте здорового человека. При антибиотикотерапии, в условиях нарушения биоценоза естественной микрофлоры, устойчивые к воздействию препарата штаммы Klebsiella oxytoca начинают активно размножаться, оказывая местное патологическое воздействие на макроорганизм: очаговое или диффузное воспаление слизистой оболочки толстой кишки, нарушение проницаемости сосудистой стенки, что проявляется выраженным геморрагическим синдромом.
При антибиотик-ассоциированном геморрагическом колите поражение толстой кишки носит сегментарный характер, поражается правая или левая половина толстой кишки, прямая кишка обычно интактна. Тонкая кишка (терминальный отдел подвздошной кишки) также неизменена. Изменения в пределах поражённого сегмента однородные. Макроскопически слизистая оболочка поражённого сегмента толстой кишки очагово или диффузно гиперемирована, отёчна, с множественными мелкоточечными субэпителиальными кровоизлияниями, сосудистый рисунок отсутствует или смазан, складки сохранены, обычной конфигурации (рис.3). Кровоточивость контактная, выраженная. Спонтанная кровоточивость может выявляться при средне-тяжёлом течении. Геморрагический синдром сохраняется в течение нескольких недель после купирования катарального воспаления.
При морфологическом исследовании выявляется лимфогистиоцитарная инфильтрация слизистой оболочки толстой кишки, ограниченная её собственной пластинкой, полнокровие капилляров, выраженное нарушение проницаемости капиллярной стенки (рис.4). [7;25]
Псевдомембранозный колит — острое инфекционное заболевание, развивающееся на фоне антибиотикотерапии, характеризуется поражением желудочно-кишечного тракта, вызванным CI. difficile, споро-образующей, грамположительной анаэробной палочкой. Основными препаратами, способствующими развитию этого вида колита, являются аминогликозиды и цефалоспорины. Возбудители (Clostridium difficile) обладают свойствами, общими и для других видов клостридий. Паразитируют в кишечнике человека. На искусственных питательных средах образуют большое количество газа и споры. Токсигенные штаммы возбудителя образуют токсин А (летальный энтеротоксин) и токсин В (цитотоксин). Около 5 % здоровых людей являются носителями токсигенных клостридий. Токсин А — летальный энтеротоксин, обусловливающий кровоизлияния и секрецию жидкости в кишечнике, и токсин В — цитотоксин, обладающий цитопатическим эффектом в культуре ткани. В патогенезе болезни играют роль оба токсина, однако в начальный период заболевания большая роль принадлежит токсину А. Оба токсина разрушают клеточные мембраны, микрофилярии и синтез протеина. Бурное размножение клостридий и продукция ими токсинов являются результатом дисбактериоза, когда антибиотики подавляют конкурентов клостридий в нормальной микрофлоре кишечника. В большинстве случаев псевдомембранозный колит протекает в тяжелой или среднетяжелой форме. Как правило, тяжесть клинической картины болезни соответствует характеру и протяженности макроскопических изменений кишечника. При псевдомембранозном колите поражение толстой кишки носит полисегментарный или тотальный характер, дистальные отделы также вовлекаются в патологический процесс. При полисегментарном поражении толстой кишки изменения слизистой оболочки, как правило, носят неоднородный характер, они наиболее выражены в её дистальных отделах (прямая и сигмовидная кишка). Тонкая кишка также может вовлекаться в патологический процесс, независимо от протяжённости поражения толстой кишки. Макроскопически слизистая оболочка поражённого сегмента толстой кишки, как правило, с явлениями диффузного поверхностного воспаления: отёчна, гиперемирована, разрыхлена, сосудистый рисунок отсутствует. Контактная кровоточивость не выражена. На этом фоне имеются множественные, небольших размеров (до 0,3-0,5 см в диаметре) желтовато-белые бляшки, плотно фиксированные к подлежащим тканям, которые при взятии биопсии с трудом от них «отрываются» (участки фибриноидного некроза). При поражении проксимальных отделов толстой кишки может быть выявлено нодулярное поражение слизистой. Морфологическое исследование биоптатов, полученных из белесовато-желтых бляшек, выявляет очаговый некроз покровного эпителия, пронизанный нитями фибрина, слизью и колониями бактерий. Эндоскопический диагноз псевдомембранозного колита почти всегда (в 95 %) удаётся подтвердить выделением Сl. difficile (рис. 5). Если данные эндоскопии не дают достаточных оснований для диагностики псевдомембранозного колита, то используется метод обнаружения в испражнениях токсина А (энтеротоксин) или токсина В (цитотоксин), продуцируемых Сl. difficile. Диагностическое значение имеет изменение течения болезни (улучшение) после от- мены антибиотиков. [6; 7; 10; 17; 24]
- несовершенство специфической профилактики (вакцинации БЦЖ) и химиотерапии первичного периода инфекции;
- наличие послепервичных очагов туберкулёзной инфекции в органах брюшной полости (в лимфоузлах, печени, селезёнке);
- наличие деструктивного внелёгочного туберкулёза (почек, гениталий, костей, суставов);
- деструктивные формы туберкулёза лёгких;
- иммунодефицитные состояния взрослых, в первую очередь ВИЧ-инфицирование со снижением параметров клеточного иммунитета — Т-хелперов (CD4) ниже 300-250 в 1 мл/крови;
- несовершенство иммунитета у детей;
- алкоголизм;
- неспецифические заболевания органов брюшной полости (хронический гастрит, гастродуоденит, язвенная болезнь, хронический холецистит, болезни кишечника) у больных туберкулёзом лёгких;
- ятрогении (терапия инфликсимабом, глюкокортикоидами, цитостатиками).
Абдоминальный туберкулёз может быть первичным или вторичным. Специфическое воспаление при абдоминальном туберкулёзе может протекать с преимущественно альтеративными, пролиферативными и альтеративно-пролиферативными воспалительными тканевыми реакциями.
При альтеративном типе воспаления туберкулёзные гранулемы характеризуются обширной зоной казеозного некроза и «бедным» клеточным составом. Макроскопически визуализируются эрозии и/или язвы на слизистых оболочках гастроинтестинального тракта, очаги казеозного некроза в лимфатических узлах, печени и селезёнке. Пролиферативный (продуктивный) тип тканевых реакций характеризуется типичными гранулемами с преобладанием эпителиоидноклеточных элементов и лимфоцитов, с гигантскими клетками Пирогова-Лангханса, но со скудным казеозным некрозом. Скопления таких гранулем визуально определяются в виде беловато-жёлтых бугорков размером 2-4 мм (иногда более крупных) на слизистых оболочках полых органов, брюшине, капсуле печени и селезёнки, в лимфатических узлах, а также в стенках полых органов, паренхиме печени и селезёнки. Гастроинтестинальный туберкулёз встречается в 43,7 % случаев абдоминального туберкулёза. В структуре гастроинтестинального туберкулёза преобладает туберкулёз кишечника.
В предлагаемых определениях туберкулёза органов пищеварения различных локализаций в связи с разными классификационными подходами его формы именуются различно. Туберкулёз кишечника и других органов гастроинтестинального тракта различными авторами подразделяется на язвенную, стенозирующую, милиарную, гипертрофическую (опухолевидную), гиперпластическую, фиброзно-скеротическую, рубцово-склеротическую, смешанную, узелково-язвенную, инфильтративно-склеротическую, инфильтративную, инфильтративно-язвенную формы (Мирзоян Э.З., 1960; Терехова Т.Г. и др., 1969; Бибер О.И. и др., 1974; Кривохиж В.М., 1987; Комаров Ф.И. и др., 1995, 1996; Юдицкий М.В. и др., 1996; Маев И.В., Самсонов А.А., 2005; Фтизиатрия: национальное руководство, 2007). На сегодняшний день наиболее распространённым является разделение гастроинтестинального туберкулёза на инфильтративную, язвенную и язвенно-инфильтративную формы. [1]
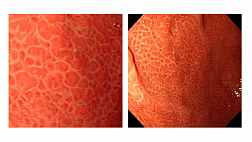
Макроскопические проявления туберкулёза толстой кишки крайне разнообразны. В процесс может быть вовлечён любой отдел толстой кишки, но несколько чаще изменения регистрируются в правых отделах с поражением илеоцекального клапана и подвздошной кишки.
В местах инфильтратов наблюдается утрата сосудистого рисунка, выпрямление складок слизистой, реже визуализируются «просовидные» высыпания на слизистой оболочке кишечника. В зависимости от глубины повреждения кишечной стенки полиповидные образования имеют милиарный, узелковый или крупноочаговый вид (Hiatt G.A., 1978; Pettengell К.Е. et al., 1991). При колоноскопии тонус поражённого сегмента толстой кишки повышен, на фоне бледно-розовой, гладкой блестящей слизистой оболочки с обеднённым сосудистым рисунком имеются единичные, чаще сгруппированные мелкие, с просовидное зерно (0,1 см в диаметре) субэпителиально расположенные образования белесоватого цвета, округлой формы, плотной консистенции. Как правило, они имеют тенденцию к слиянию, в процессе которого образуются более крупные очаги — бугорки (узелки). Их размеры составляют от 2-3 до 5 мм в диаметре. Бугорки белесоватого цвета, плотной консистенции, покрыты неизмененной или слегка гиперемированной слизистой оболочкой. Контактная кровоточивость окружающих тканей отсутствует. При вовлечении в патологический процесс лимфоидной ткани подслизистой основы формируются одиночные, иногда близко расположенные подслизистые образования размерами 0,7-1 см в диаметре, округлой формы, плотные. Слизистая оболочка над ними в большинстве случаев имеет более бледный белесоватый цвет. Окружающая слизистая оболочка, как правило, визуально не изменена, сосудистый рисунок несколько обеднён, контактная кровоточивость отсутствует. Туберкулёз кишечника иногда встречается в виде изолированного гиперпластического псевдоопухолевого процесса с локализацией, с резким утолщением стенки, с воспалительным процессом специфических бугорков, казеозным распадом, с последующим рубцеванием, сужением просвета кишки.
Макроскопическая характеристика изъязвлений, формирующихся при развитии казеозного некроза в туберкулёзных гранулемах, в большинстве случаев зависит от сроков их возникновения. На ранних этапах образования одиночные дефекты, как правило, располагаются на фоне визуально неизмененной слизистой оболочки, имеют округлую форму, ровные закруглённые края, гладкое дно, покрытое налетом фибрина. Размеры язв в большинстве случаев не превышают 1 см, глубина их зависит от уровня повреждения кишечной стенки (на всю толщу слизистой оболочки или до подслизистой основы). В связи с реактив- ной гиперплазией лимфоидной ткани в зоне образования язвенного дефекта, он всегда возвышается над уровнем окружающей слизистой оболочки. Контактная кровоточивость отсутствует (Nagasako К., 1984; ReedersJ. et al., 1994).
При прогрессировании и хронизации процесса язвы увеличиваются в размерах по периметру кишки, дно их углубляется (они часто пенетрируют в мышечный слой кишечной стенки), приобретает шероховатый мелкозернистый вид, что обусловлено образованием туберкулёзных гранулем. Развитие грануляционной ткани в краях дефектов придает им бугристый вид. Распространение язв идёт в поперечном направлении. Большие язвы, как правило, циркулярно охватывают просвет кишки (Nagasako К., 1984).
В результате многократной гематогенной диссеминации в стенке органа формируются очаги специфического воспаления,
которые, как правило, имеют разную величину, форму и морфологическую структуру. Макроскопически на протяжении пораженного сегмента кишки изменения носят неоднородный характер. В большинстве случаев при колоноскопии выявляются элементы туберкулёзного поражения кишечной стенки, находящиеся на разных стадиях развития: милиарные образования, бугорки и крупноочаговые подслизистые образования, на фоне которых имеются единичные, глубокие язвенные дефекты (как правило, не более 1-2 язв) с бугристыми, полиповидно изменёнными краями и мелкозернистым дном. Визуально окружающая слизистая оболочка может быть интактна или с явлениями очагового или диффузного поверхностного воспаления.
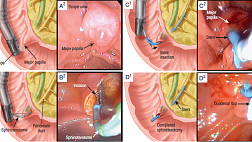
Язвы при туберкулёзе заживают через рубцевание, возможно формирование кольцевидных стриктур толстой кишки (рис. 2 (А)). После назначения противотуберкулёзной химиотерапии всегда происходит регресс изменений слизистой, это может служить дифференциально-диагностическим при- знаком (рис. 6).
Для окончательной диагностики туберкулёза кишечника требуется бактериологическое и гистологическое исследование содержимого кишечника, язв, инфильтратов и высыпаний методами бактериоскопии, мазков-отпечатков с окраской по Цилю-Нильсену, посева, ПЦР. Возбудитель туберкулёза в фекалиях обнаруживается при обследовании редко, чувствительность метода можно увеличить при заборе материала адресно из зоны поражения при эндоскопии. [16; 19; 8; 5; 1; 12; 20 21]
Вывод:
1. Пациенты с бактериальным колитом могут встретиться в практике любого врача-эндоскописта.
2. Эндоскопическая семиотика бактериальных колитов крайне разнообразна, но не специфична. Во многом зависит от патогенетических механизмов развития того или иного инфекционного процесса и тяжести течения заболевания.
3. Этиологический фактор бактериального колита в большинстве случаев можно назвать только предположительно, исключение составляет псевдомембранозный колит, имеющий яркую эндоскопическую картину.
4. Описание изменений слизистой толстой кишки при инфекционных колитах основано на стандартном алгоритме описания воспалительных изменений толстой кишки (эндоскопические проявления, оценка активности процесса, локализация и протяженность поражения).
5. Патоморфологические изменения при бактериальных колитах в большинстве случаев также неспецифичны. Возможно проведение биопсии и взятие смывов для микробиологического исследования и ПЦР-диагностики во время эндоскопии.
Список литературы:
2. Ивашкин В Т., Шептулин А. А., Склянская О.А. ИИ Синдром диареи. — 2-е изд., расшир. и перераб. — М.. ГЭОТАРМЕД, 2002. — 168 с. ил. [Текст]
3. Кондратенко П.Г., Стукало А.А., Раденко Е.Е. Гастроинтестинальная эндоскопия. Практическое руководство. //Донецк, 2007. – 374 с. [Текст]
4. Малый В.П. , Волобуева О.В, Лядова Т.И. Шигеллез// Вiсн. Харк. нац. ун-ту.№797, 2008г.- с. 150-167 [https://cyberleninka.ru/article/v/shigellez]
5. Решетников М.Н., Матросов М.В., Антипов А.Г., Мальцев Р.В., Богородская Е.М., Зубань О.Н. Колоноскопия в диагностике туберкулеза органов брюшной полости. Московский городской научно-практический центр борьбы с туберкулезом (МнпЦ Бт) Департамента здравоохранения Москвы Эндоскопическая хирургия, 3, 2014 [https://www.mediasphera.ru/issues/endoskopicheskaya-khirurgiya/2014/3/downloads/ru/091025-72092015036]
6. Руководство по инфекционным болезням (в 3 частях) Под ред. Ю.В. Лобзина Издательство: СПб.: Феникс: 2001г. – 932с. [https://studfiles.net/preview/1904427/page:18/]
7. Сотников В.Н., Разживина А.А., Веселов В.В., Кузьмин А.И. и др. Колоноскопия в диагностике заболеваний толстой кишки// М: Экстрапринт, 2006г.-280 с. [Текст]
8. Т.В. Зырянова, Л.В. Поддубная, М.В. Федорова, К.А. Липский Туберкулез органов брюшной полости у больных туберкулезом легких.ГОУ ВПО «Новосибирский государственный медицинский университет Росздрава» (г. Новосибирск).[МЕДИЦИНА И ОБРАЗОВАНИЕ В СИБИРИ Текущее название: Journal of Siberian Medical Sciences Издательство: Новосибирский государственный медицинский университет (Новосибирск) ISSN: 2542-1174https://elibrary.ru/pic/1pix.gif]
9. Ющук Н.Д., Бродов Л.Е. Инфекционные диареи // РМЖ. – 2001. – Т. 9. – № 16-17 [https://www.rmj.ru/articles/infektsiya/infekcionnye_diarei/]
10. Ющук Н.Д., Мартынов Ю.В., Кулагина М.Г., Бродов Л.Е.Острые кишечные инфекции 2-е издание переработанное и дополненное//М: ГЭОТАР-медиа.-2012г. – 396 с. [Текст]
11. Allos BM1.Campylobacter jejuni Infections: update on emerging issues and trends. Clin Infect Dis. 2001 Apr 15;32(8):1201-6. Epub 2001 Mar 28 [PMID: 11283810 DOI: 10.1086/319760]
12. Das HS1, Rathi P, Sawant P, Chodankar CM, Vyas K, Patrawala V, Dhadphale S. Colonic tuberculosis: colonoscopic appearance and clinico-pathologic analysis. J Assoc Physicians India. 2000 Jul;48(7):708-10. [PMID: 11273506]
13. El Salvador Atlas of Gastrointestinal Video Endoscopy
14. Katakura S1, Reinholt FP, Kärnell A, Huan PT, Trach DD, Lindberg AA. The pathology of Shigella flexneri infection in rhesus monkeys: an endoscopic and histopathological study of colonic lesions. APMIS. 1990 Apr;98(4):313-9. [PMID: 2191692]
15. Khuroo MS1, Mahajan R, Zargar SA, Panhotra BR, Bhat RL, Javid G, Mahajan B. The colon in shigellosis: serial colonoscopic appearances in Shigella dysenteriae I. Endoscopy. 1990 Jan;22(1):35-8. [PMID: 2407526 DOI:10.1055/s-2007-1012784]
16. Lakhe P, Khalife A, Pandya J. Ileocaecal and transverse colonic tuberculosis mimicking colonic malignancy - A case report. Int J Surg Case Rep. 2017;36:4-7. [doi: 10.1016/j.ijscr.2017.04.016. Epub 2017 Apr 19. PMID: 28486175]
17. Loza Vargas LA1, Núñez Rodríguez H2, Benito Sanz M2, Zamora Martínez T3, Díez Redondo P2, Pérez Miranda M2. Nodular colitis: endoscopic image an unusual findin//. Rev EspEnferm Dig. 2016 Oct;108(10):659-600. [PMID: 27701886]
18. Matsumoto T1, Nakamura S, Okawa K, Kitano A. [Differential diagnosis of ulcerative colitis].[Article in Japanese] Nihon Rinsho. 1999 Nov;57(11):2461-5. [PMID: 10572412]
19. Misra SP1, Misra V, Dwivedi M, Arora JS, Kunwar BK.Tuberculous colonic strictures: impact of dilation on diagnosis. Endoscopy. 2004 Dec;36(12):1099-103. [PMID: 15578302 DOI: 10.1055/s-2004-826046]
20. Mukewar S, Ravi R, Prasad A, S Dua K. Colon tuberculosis: endoscopic features and prospective endoscopic follow-up after anti-tuberculosis treatment. Clin Transl Gastroenterol 2012; 3:e24. [doi: 10.1038/ctg.2012.19.]
21. Naoyoshi Nagata, Takuro Shimbo, Katsunori Sekine, Shouhei Tanaka, Ryota Niikura, Kazuhisa Mezaki, Eriko Morino, Hirohisa Yazaki, Toru Igari, Norio Ohmagari, Junichi Akiyama, Shinichi Oka, Naomi Uemura Combined endoscopy, aspiration, and biopsy analysis for identifying infectious colitis in patients with ileocecal ulcers. Clin Gastroenterol Hepatol. 2013 Jun;11(6):673-80.e2. [doi: 10.1016/j.cgh.2012.12.034. Epub 2013 Jan 26. doi: 10.1016/Дж.сгг.2012.12.034]
22. Simadibrata M1, Tytgat GN, Yuwono V, Daldiyono, Lesmana LA, Syam AF, Ariawan I, Rani A. Microorganisms and parasites in chronic infective diarrhea. Acta Med Indones. 2004 Oct-Dec;36(4):211-4. [PMID: 15931720]
23. Stampfer L1, Deutschmann A, Dür E, et al. . Causes of hematochezia and hemorrhagic antibiotic-associated colitis in children and adolescents. Medicine (Baltimore). 2017 Aug;96(33):e7793. [doi: 10.1097/MD.0000000000007793. PMID: 28816966 PMCID:PMC5571703 DOI: 10.1097/MD.0000000000007793]
24. Surawicz C, Brandt L, Binion D, et al. Guidelines for diagnosis, treatment, and prevention of Clostridium difficile infections. Am J Gastroenterol 2013;108:478-98. [DOI: 10.1038/ajg.2013.4]
25. Tanaka K1, Fujiya M2, Sakatani A1, Fujibayashi S1, Nomura Y1, Ueno N1, Kashima S1, Goto T1, Sasajima J1, Moriichi K1, Okumura T1 Second-line therapy for Helicobacter pylori eradication causing antibiotic-associated hemorrhagic colitis. Ann Clin Microbiol Antimicrob. 2017 Aug 14;16(1):54. doi: 10.1186/s12941-017-0230-0. [PMID: 28806959 PMCID: PMC5557549 DOI: 10.1186/s12941-017-0230-0]
26. Thapa BR1, Ventkateswarlu K, Malik AK, Panigrahi D. Shigellosis in children from north India: a clinicopathological study. J Trop Pediatr. 1995 Oct;41(5):303-7. [PMID:8531265]
27. C.M., Munoz-Navas M., Sung J. Atlas of Clinical Gastrointestinal Endoscopy, 2nd etdition пер. с англ. под ред. Федорова Е.Д. РидЭлсивер, 2009г. – 483 с. [текст]
Рекомендуемые статьи
Ахалазия кардии
Ахалазия кардии (синонимы: мегаэзофагус или долихоэзофагус, идиопатическое расширение пищевода, кардиоспазм и др.)— идиопатическое нервно-мышечное заболевание, проявляющееся функциональным нарушением проходимости кар-дии вследствие дискоординации между глотком, рефлекторным раскрытием нижнего пищеводного сфинктера (НПС) идвигательной итонической активностью гладкой мускулатуры пищевода. Код по МКБ-10К.22.0. Ахалазия кардиальной части.
При эндоскопическом исследовании в случае бронхоэктазов в стадии ремиссии выявляется
частично диффузный бронхит I степени воспаления
Активируйте PUSH уведомления в браузер
Отключите PUSH уведомления в браузер
Содержание
Интернет магазин
Популярное
- О нас
- Правовые вопросы
- Политика
обработки персональных
данных EndoExpert.ru - Связаться с нами
- Стать партнером
© 2016-2022 EndoExpert.ru

Вы находитесь в разделе предназначенном только для специалистов (раздел для пациентов по ссылке). Пожалуйста, внимательно прочитайте полные условия использования и подтвердите, что Вы являетесь медицинским или фармацевтическим работником или студентом медицинского образовательного учреждения и подтверждаете своё понимание и согласие с тем, что применение рецептурных препаратов, обращение за той или иной медицинской услугой, равно как и ее выполнение, использование медицинских изделий, выбор метода профилактики, диагностики, лечения, медицинской реабилитации, равно как и их применение, возможны только после предварительной консультации со специалистом. Мы используем файлы cookie, чтобы предложить Вам лучший опыт взаимодействия. Файлы cookie позволяют адаптировать веб-сайты к вашим интересам и предпочтениям.
Я прочитал и настоящим принимаю вышеизложенное, хочу продолжить ознакомление с размещенной на данном сайте информацией для специалистов.











.jpg)





.png)



















Комментарии