- Компании
- Takeda. О компании, буклеты, каталоги, контакты
- Olympus. О компании, буклеты, каталоги, контакты
- Boston Scientific. О компании, буклеты, каталоги, контакты
- Pentax. О компании, буклеты, каталоги, контакты
- Fujifilm & R-Farm. О компании, буклеты, каталоги, контакты
- Erbe. О компании, буклеты, каталоги, контакты
- Еще каталоги
- Мероприятия
- Информация
- Обучение
- Классификации
- Атлас
- Quiz
- Разделы
- Пациенту
QR-код этой страницы
Для продолжения изучения на мобильном устройстве ПРОСКАНИРУЙТЕ QR-код с помощью спец. программы или фотокамеры мобильного устройства
Статьи: Гранулематозные заболевания кишечника: болезнь Крона и туберкулез. Сложности дифференциальной диагностики (клиническое наблюдение и обзор литературы)
| Авторы: | Варданян А.В., Меркулова Е.С., Белинская В.А.1, Майновская О.А. 1 Фролова К.С. 2 2025г. |
| Об авторах: |
1. ФГБУ «НМИЦ колопроктологии имени А.Н. Рыжих» Минздрава России 2. ГУБЗ «Московский научно-практический центр борьбы с туберкулезом ДЗМ» |
Аннотация:
Своевременная диагностика внелегочных форм туберкулеза до сих пор представляет значительные трудности. Абдоминальный туберкулез не имеет патогномоничных признаков, поэтому большинство пациентов наблюдается с различными диагнозами. В данном клиническом наблюдении сложность установления диагноза была обусловлена отсутствием отягощенного по туберкулезу анамнеза, и манифестацией туберкулезного процесса изолированно с поражения кишечника. Это заставило нас провести широкий дифференциально-диагностический поиск, прежде всего, с целью исключения воспалительных заболеваний кишечника (ВЗК) и новообразований, а также потребовало привлечения врачей различных специальностей. Мультидисциплинарный подход, осведомленность и настороженность специалистов позволили достичь успеха в курации данной пациентки.
Полный текст статьи:
ВВЕДЕНИЕ
В настоящий момент, несмотря на позитивные тенденции в эпидемической ситуации по туберкулезу в целом, динамика заболеваемости внелегочным туберкулезом (ВЛТ) нестабильна [1]. Диагностика туберкулеза внелегочных локализаций трудна, заболевание может протекать протекать скрыто, под
«маской» других патологических процессов (инфекционных, гастроэнтерологических, хирургических, онкологических) [2].
Абдоминальный туберкулез — инфекционное заболевание, вызываемое микобактериями туберкулеза, относящееся к внелегочным формам туберкулеза и характеризующееся наличием специфического воспалительного процесса в органах брюшной полости [3]. Согласно эпидемиологическим данным, из внелегочных форм туберкулеза на долю абдоминального туберкулеза приходится от 4,4–8,3% до 17–21% случаев, что не позволяет считать его редким заболеванием [4]. Официальная клиническая классификация абдоминального туберкулеза включает в себя туберкулез кишечника, брюшины, мезентериальных лимфатических узлов и прочие формы [5]. Наиболее часто в патологический процесс вовлекается кишечник, а именно илеоцекальная зона (70–89,5% случаев), дистальные формы являются редкостью [6]. Известно, что для выявления абдоминального туберкулеза не существует скрининговых методов [7], а все проводимые лабораторные и инструментальные обследования не всегда позволяют верифицировать диагноз.
Клиническое наблюдение
Пациентка К., 89 лет, обратилась в консультативную поликлинику ФГБУ «НМИЦ колопроктологии имени А.Н. Рыжих» Минздрава России в январе 2022 года с жалобами на периодические схваткообразные боли в нижних отделах живота, снижение веса, повышение температуры тела в вечернее время до 37,3 °С, рвоту 1 раз в три дня, полуоформленный стул 1–2 раза в сутки без патологических примесей.
Из анамнеза заболевания известно, что летом 2021 года на фоне полного благополучия пациентка
стала отмечать эпизоды повышения температуры до 40 °С. Обращалась к терапевту по месту жительства, заподозрена острая респираторная вирусная инфекция, анализ на новую коронавирусную вирусную инфекцию был отрицательный, назначалась системная антибактериальная терапия (препараты уточнить не могла) с положительным эффектом в виде нормализации температуры тела, параллельно принимала пробиотики. В ноябре 2021 года появились боли в животе без определенной локализации и эпизоды неоформленного стула. Обратилась в поликлинику по месту жительства и была направлена в одну из городских больниц для обследования. При колоноскопии в декабре 2021 года выявлено циркулярное сужение просвета восходящей ободочной кишки — заподозрена опухоль. При морфологическом исследовании биоптатов данных за опухолевый рост не выявлено. Направлена в ФГБУ «НМИЦ колопроктологии имени А.Н. Рыжих» Минздрава России для дообследования и верификации диагноза.
На первичной консультации пациентка осмотрена врачом-онкологом. Объективно: общее состояние удовлетворительное, несколько астенизирована. Рост 158 см, вес 50 кг. Индекс массы тела (ИМТ) —
20 кг/м2. Кожные покровы и видимые слизистые бледные, отмечается пастозность нижних конечностей. Гемодинамических нарушений не выявлено. Язык влажный, обложен белым налетом у корня. На передней брюшной стенке послеоперационный рубец после холецистэктомии без признаков воспаления. Живот не вздут, при пальпации мягкий, безболезненный во всех отделах. Пальцевое исследование прямой кишки и ректороманоскопия без особенностей. Лабораторные показатели от 17.01.2022 г.: общий белок — 59,5 г/л, гемоглобин — 91 г/л, тромбоциты — 454 × 109/л.
По данным компьютерной томографии (КТ) от 21.01.2022 г.: легочный рисунок с признаками очагового пневмосклероза, явных очаговых и инфильтративных изменений не обнаружено. Восходящая кишка до области правого изгиба и терминальный отдел подвздошной кишки на протяжении 5 см изменены, стенка утолщена до 1,0–1,5 см за счет всех слоев. Окружающая клетчатка выраженно уплотнена.
Рисунок 1. Компьютерная томография. Стрелками указано утолщение стенки подвздошной и восходящей кишки, воспалительно инфильтрированная клетчатка
Figure 1. CT scan. The arrows indicate the thickening of the wall of the ileum and ascending colon, inflammatory infiltrated tissue
Инфильтрация распространяется на брюшину правого латерального канала. По ходу сосудов брыжейки лимфатические узлы до 0,6 см. (Рис. 1). Заключение: КТ-картина инфильтративных изменений восходящей ободочной и подвздошной кишки может соответствовать опухолевому процессу.
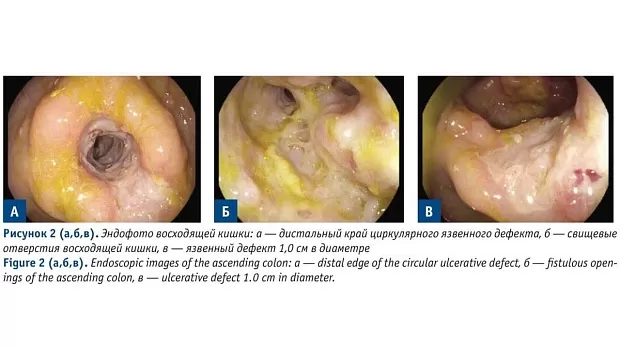
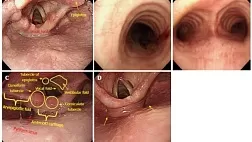
По данным колоноскопии от 01.02.2022 г.: аппарат проведен в среднюю треть восходящей кишки, где определяется дистальный край циркулярного язвенного дефекта, эластичной консистенции, просвет сужен до 1,3 см. Аппарат проведен проксимальнее на 5–6 см, просвет конусовидно сужается до 0,6 см и визуализируются внутренние отверстия, не позволяющие исключить систему свищевых ходов. Слизистая оболочка на данном промежутке бледнорозового цвета, представлена циркулярным язвенным дефектом, местами с налетом фибрина, кровоточива при контакте. Дистальнее на гаустру — язвенный дефект, занимающий ½ окружности, ярко-красного цвета, с налетом фибрина. В области правого изгиба ободочной кишки — язвенный дефект размером 1,0 см, ярко-красного цвета, с налетом фибрина. В дистальной трети восходящей кишки — афты
до 0,2 см в диаметре с венчиком гиперемии и налетом фибрина, выполнена биопсия. Расположенные дистальнее отделы толстой кишки не изменены (Рис. 2). Заключение: эндоскопическая картина трудна для интерпретации, следует дифференцировать между инфильтративным опухолевым процессом, болезнью Крона в стадии язв, лимфосаркомой и туберкулезом. Результат гистологического исследования от 03.02.2022 г.: в участках собственной пластинки слизистой и подслизистого слоя определяются группы гистиоцитарных гранулем, частью сливающихся, с единичными гигантскими многоядерными клетками типа Пирогова-Лангханса (Рис. 3). Заключение: признаков опухолевого роста (включая лимфопролиферативные процессы) не обнаружено, морфологическая картина может соответствовать болезни Крона (дифференциальный диагноз с туберкулезом).
Консультирована гастроэнтерологом, с учетом возраста пациентки, данных анамнеза, результатов обследования, было высказано предположение о высокой вероятности инфекционной природы заболевания. Установлен диагноз: болезнь Крона в форме илеоколита (?), туберкулез кишечника (?).
Рисунок 2 (а,б,в). Эндофото восходящей кишки: а — дистальный край циркулярного язвенного дефекта, б — свищевые отверстия восходящей кишки, в — язвенный дефект 1,0 см в диаметре
Figure 2 (а,б,в). Endoscopic images of the ascending colon: а — distal edge of the circular ulcerative defect, б — fistulous openings of the ascending colon, в — ulcerative defect 1.0 cm in diameter.
Рекомендована консультация фтизиатра, назначено изучение уровня фекального кальпротектина, анализ кала на токсины А и В Clostridium difficile, клинические инфекции. Назначено лечение: месалазин 3 г в сутки, метронидазол 1 г в сутки, ципрофлоксацин 1 г в сутки, спазмолитики при болях в животе, сбалансированная смесь для энтерального питания.
На фоне проводимой терапии состояние оставалось стабильным, однако первоначальные жалобы пациентки сохранялись. Анализы на кишечные инфекции (иерсиниоз, сальмонеллез, шигеллез, лямблиоз, амебиаз) и токсины А и В Clostridium difficile отрицательные. Фекальный кальпротектин от 25.02.2022 г: 538 мкг/гр (N = 0–150 мкг/гр). По месту жительства больная осмотрена фтизиатром, пересмотрены результаты КТ грудной клетки от 21.01.2022 г., выполнены проба Манту и исследование мокроты на наличие кислотоустойчивых микобактерий (КУМ), данных за активный туберкулез не получено. Лабораторные показатели от 01.03.2022 г.: гемоглобин — 84 г/л, тромбоциты — 574 × 109/л, общий белок — 62 г/л, альбумин — 30 г/л.
С учетом отсутствия клинического улучшения, отрицательной лабораторной динамики в виде прогрессирования анемии, тромбоцитоза, гипоальбуминемии, рекомендовано выполнение магнито-резонансной томографии (МРТ) кишечника с контрастированием. По данным МРТ от 24.03.2022 г.: в терминальном отделе подвздошной кишки на протяжении 4,8 см, в слепой кишке и восходящей ободочной кишке на протяжении 6,2 см отмечается циркулярное утолщение стенки до 1,0 см, просвет циркулярно сужен до 0,5 см (Рис. 4). В дистальной трети подвздошной кишки — участок циркулярного утолщения кишечной стенки до 0,9 см на протяжении 4,9 см, просвет сужен до 0,3 см. Подвздошная кишка проксимальнее сужения на всем протяжении расширена до 4,5 см. В средней трети подвздошной кишки — участок циркулярного утолщения кишечной стенки до 0,9 см на протяжении 2,5 см, просвет сужен до 0,3 см. Изменения накапливают контраст. Заключение: МРкартина сегментарного поражения подвздошной кишки и восходящей ободочной кишки (следует дифференцировать между воспалительным и неопластическим процессом). Расширение просвета тонкой кишки.
Пациентка консультирована хирургом-колопроктологом: учитывая данные анамнеза, возраст пациентки, результаты инструментального обследования, отрицательную лабораторную динамику (снижение уровня гемоглобина, альбумина), неэффективность проводимой консервативной терапии, сохранение воспалительных сужений тонкой и толстой кишки, наличие престенотического расширения, были выставлены показания для проведения хирургического лечения. Получено согласие больной на операцию. Пациентка была госпитализирована с диагнозом:
Болезнь Крона (?) в форме илеоколита, осложненная формированием воспалительных стриктур подвздошной кишки и правых отделов ободочной кишки, с признаками частичного нарушения кишечного пассажа по тонкой кишке. Опухолевый процесс (?) в правых отделах толстой кишки, Туберкулез кишечника (?), Хроническая железодефицитная анемия средней степени тяжести.
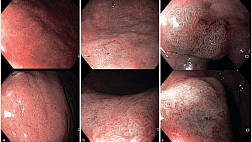
06.04.2022 г. выполнена лапароскопически-ассистированная операция. Интраоперационно (Рис. 5) определялся деформированный рубцово-измененный илеоцекальный отдел кишечника с выраженными воспалительными изменениями и плотным эндофитным компонентом. В подвздошной кишке выявлены 7 воспалительных участков с сужением просвета, при этом отсутствовало воспаление в брыжейке кишки. После 3-го участка сужения имелось престенотическое расширение подвздошной кишки. Картина сложна для интерпретации. Визуально изменения со стороны кишечной стенки не характерны для болезни Крона. В дифференциальный ряд необходимо поставить болезнь Крона и туберкулез. Учитывая протяженность поражения тонкой кишки, с учетом возраста пациентки, от обширной резекции и стриктуропластики было решено воздержаться. Принято решение о резекции илеоцекального отдела кишечника (Рис. 6) с формированием илео-асцендоанастомоза и обходного илео-илеоанастомоза по типу «бок-в-бок» между неизмененными участками подвздошной кишки в 40 см от проксимальной границы резекции и участком тощей кишки, таким образом «отключив» 3 участка сужения в подвздошной кишке с необратимыми изменениями со стороны кишечной стенки.
Результат гистологического исследования от 12.04.2022 г.: во всех слоях кишечной стенки, в прилежащей клетчатке и лимфатических узлах определяются множественные сливающиеся гистиоцитарные гранулемы с большим количеством гигантских многоядерных клеток типа Пирогова-Лангханса. Часть гранулем с фиброзными изменениями в центре, единичные с центральными мелкими некрозами. Заключение: морфологическая картина более всего соответствует туберкулезу в области резецированного илеоцекального отдела.
Таким образом, по результатам гистологического исследования операционного матери ала пациентке был верифицирован заключительный клинический диагноз: Туберкулез кишечника с поражением тонкой и толстой кишки. Туберкулезный мезаденит.
Послеоперационный период протекал без осложнений, больная выписана под наблюдение врача-фтизиатра по месту жительства.
При попытке приема комбинированной противотуберкулезной терапии отмечала появление тошноты, рвоты, диареи, в связи с чем лечение прекращено. Через 4 месяца после операции состояние пациентки удовлетворительное, жалоб не
Рисунок 3. А. Морфологическая картина в биоптате из края язвы: признаки хронического воспаления и грануляционная ткань с очагами некроза, большим количеством гистиоцитов, формирующих гранулемы с наличием гигантских многоядерных клеток типа Пирогова-Ланхганса (ув. ×10). Б. Грануляционная ткань (деталь, ув. ×100). В. Гранулема из эпителиоидных и лимфоидных клеток, клетками Пирогова-Ланхганса и очагом некроза в центре (деталь, ув. ×100). Стрелками указаны клетки Пирогова-Ланхганса. А, Б, В — окраска гематоксилином и эозином.
Figure 3. А. The morphological picture in the biopsy from the edge of the ulcer: signs of chronic inflammation and granulation tissue with foci of necrosis, a large number of histiocytes that form granulomas with the presence of giant multinucleated cells of the Pirogov-Lankhgans type (magn. ×10). Б. Granulation tissue (detail, magn. ×100). В. Granuloma of epithelioid and lymphoid cells, Pirogov-Lankhgans cells and a necrosis focus in the center (detail, magn. ×100). Arrows indicate Pirogov-Langhans cells. А, Б, В — staining with hematoxylin and eosin.
Рисунок 4. Магнито-резонансная томограмма. Стрелками указано циркулярное сужение просвета восходящей ободочной кишки до 5 мм, циркулярное утолщение стенки до 10 мм, уплотнение окружающей клетчатки.
Figure 4. MRI. The arrows indicate the circular narrowing of the ascending colon up to 5 mm, the circular thickening of the wall up to 10 mm, and the compaction of the surrounding tissue
Рисунок 5 (а,б). Интраоперационная фотография: а — деформированный илеоцекальный отдел кишечника с воспалительными изменениями, б — один из участков сужения в подвздошной кишке.
Figure 5(а,б). Intraoperative photo: a — deformed ileocecal zone with inflammatory, б — one of the ileumstrictures.
Рисунок 6. Илеоцекальный отдел. Утолщение кишечной стенки и сужение просвета в области илеоцекального перехода.
Figure 6. Ileocecal region. Thickening of the intestinal wall and narrowing of the lumen at the ileocecal junction
предъявляла, у фтизиатра продолжено динамическое наблюдение.
ОБСУЖДЕНИЕ
В настоящий момент, несмотря на наличие различных лабораторных диагностических тестов, доступность выполнения эндоскопической и лучевой диагностики, большие сложности возникают при дифференциальной диагностике двух гранулематозных заболеваний кишечника, имеющих разную этиологию, но схожесть проявлений. Это туберкулез кишечника и болезнь Крона, что и демонстрирует данный клинический случай.
Клинические признаки обоих заболеваний включают боль в животе, лихорадку, потерю массы тела, хроническую диарею, гематохезию, рецидивирующую частичную кишечную непроходимость, внекишечные проявления в виде артралгий, афтозного стоматита, поражения кожи и глаз [8]. Из-за своей неспецифичности, ни один из этих признаков отдельно или в совокупности, не позволяет достоверно предположить то или иное заболевание.
Среди иммунологических тестов для выявления специфического клеточного иммунного ответа на антигены микобактерий тестов широкую распространенность имеют традиционная проба Манту с 2 ТЕ ППД-Л, кожная проба с аллергеном туберкулезным рекомбинантным (препарат ДИАСКИНТЕСТ®), а также тесты на высвобождение Т-лимфоцитами интерферона-γ (QuantiFERON®-TB Gold/Gold Plus, T-SPOT®.TB). Положительный результат пробы Манту регистрируется у 50–100% пациентов с туберкулезом кишечника. Однако, согласно данным литературы по изучению роли иммунодиагностики в верификации патологии, проведено несколько метаанализов, которые сообщают о чувствительности и специфичности примерно 80% пробы Манту [12], это обусловлено высоким процентом ложноположительных результатов пробы Манту у вакцинированных и инфицированных в детстве [9–11], что делает данный метод малоэффективным для выявления туберкулезной инфекции.
Анализ кала на наличие микобактерий не проводят ввиду практически полного отсутствия положительных результатов [5].
Как и при любом другом инфекционном заболевании, обнаружение M. tuberculosis с помощью микробиологических методов в образцах может быть диагностическим признаком туберкулеза, но, поскольку кишечный туберкулез является малобациллярным (малая концентрация микобактерий) заболеванием, их выявление затруднено, что объясняет низкую чувствительность этих тестов [13]. В последние годы
для ускорения роста микобактерий предложены питательные среды на агаровой основе с различными ростовыми добавками и применением газовой смеси. Для получения роста микроорганизмов на этих средах создают атмосферу с повышенным содержанием углекислого газа (4–7%), для этого используются специальные CO2-инкубаторы. Наибольшее развитие получили автоматизированные системы: MGITBACTEC-960 и MB/Bact [5]. Чувствительность данного метода варьирует от 19% до 70% [14].
Применение полимеразной цепной реакции (ПЦР) в диагностике абдоминального туберкулеза связано с большими сложностями. Для проведения ПЦР молекулы дезоксирибонуклеиной кислоты (ДНК) возбудителя должны быть выделены из биоптатов. Для лизиса биоптата используют фермент (протеиназа К) в конечной концентрации 200–500 мг/л при температуре 56 °С в течение ночи. Избыток неспецифической ДНК при ПЦР-анализе нередко служит причиной ингибирования реакции, что требует повторно экстрагирования ДНК [5]. В недавнем метаанализе девяти исследований совокупная чувствительность и специфичность ПЦР с выделением КУМ составила 44% и 95%, соответственно [15].
Эндоскопическая диагностика занимает одно из ключевых мест в верификации диагноза, но также достаточно сложна и неоднозначна. Критериями диагностики болезни Крона при проведении колоноскопии являются регионарное (прерывистое) поражение слизистой оболочки, симптом «булыжной мостовой» (сочетание глубоких продольно ориентированных язв и поперечно-направленных язв c островками отёчной гиперемированной слизистой оболочкой), линейные язвы (язвы-трещины), афты, а в некоторых случаях — стриктуры и устья свищей [16]. Макроскопические проявления туберкулёза толстой кишки крайне разнообразны. В процесс может быть вовлечён любой отдел толстой кишки, но несколько чаще изменения регистрируются в правых отделах с поражением илеоцекального клапана и подвздошной кишки. Как правило, наблюдается утрата сосудистого рисунка, выпрямление складок слизистой, реже визуализируются
«просовидные» высыпания на слизистой оболочке кишечника. Характеристика изъязвлений, формирующихся при развитии казеозного некроза в туберкулёзных гранулемах, в большинстве случаев зависит от сроков их возникновения. На ранних этапах образования одиночные дефекты, как правило, располагаются на фоне визуально неизмененной слизистой оболочки, имеют округлую форму, ровные закруглённые края, гладкое дно, покрытое налетом фибрина. Размеры язв в большинстве случаев не превышают 1 см, глубина их зависит от уровня повреждения кишечной стенки (на всю толщу слизистой оболочки или до подслизистой основы). В связи с реактивной гиперплазией лимфоидной ткани в зоне образования язвенного дефекта он всегда возвышается над уровнем окружающей слизистой оболочки. Контактная кровоточивость отсутствует. При прогрессировании и хронизации процесса язвы увеличиваются в размерах по периметру кишки, дно их углубляется (они часто пенетрируют в мышечный слой кишечной стенки), приобретает шероховатый мелкозернистый вид, что обусловлено образованием туберкулёзных гранулем. Развитие грануляционной ткани в краях дефектов придает им бугристый вид. Распространение язв идёт в поперечном направлении. Большие язвы, как правило, циркулярно охватывают просвет кишки [17]. При поражении толстой кишки воспалительный процесс может проявляться развитием стриктур, гипертрофическими поражениями, напоминающими полипы или опухоли, сегментарными язвами [18].
КТ или МРТ являются предпочтительными методами дифференциальной диагностики поражений тонкой и толстой кишки [19]. В метаанализе Kedia S., и соавт. проанализирован ряд признаков (симптом гребня, поражение лимфатических узлов, асимметричное утолщение стенки кишечника, пролиферация жировой клетчатки, расслоение стенки, вовлечение илеоцекальной области), и их роль в верификации патологии. Поражение лимфатических узлов имело самую высокую точность (чувствительность — 23%; специфичность — 100%) для диагностики туберкулеза кишечника, а признак гребня (чувствительность — 82%, специфичность — 81%) — для болезни Крона. При анализе чувствительности других признаков их диагностическая точность, за исключением асимметричного утолщения стенки кишечника, оставалась одинаковой [20].
Решающая роль в диагностике абдоминального туберкулеза принадлежит обнаружению при гистологическом исследовании в пораженных органах и тканях специфических гранулём, представляющих в классическом варианте участок клеточного детрита — казеозного некроза, окруженного так называемыми эпителиоидными клетками, гигантскими клетками Пирогова-Лангханса и лимфоцитами по периферии [3]. Туберкулезные гранулемы обычно большие, склонные к слиянию, плотные, располагаются в подслизистой оболочке и характеризуются центральным казеозом, а гранулемы при болезни Крона — мелкие (микрогранулемы), дискретные, редкие и плохо очерченные, без участков некроза. Обнаружение КУМ в образцах биопсии при окраске по Цилю-Нильсену, хотя и очень специфично, но встречается нечасто [21].
Если все-таки не удается дифференцировать болезнь Крона и туберкулез кишечника, а лечение начинать необходимо, то применение глюкокортикостероидов (ГКС) в такой ситуации может способствовать генерализации туберкулезного процесса и быть фатальным. Данную проблему можно обойти с помощью эмпирического назначения противотуберкулезной терапии (ПТТ). В консенсусе 2016 года Азиатско-Тихоокеанского региона по ведению пациентов с болезнью Крона упоминается, что у больных с дилеммой «ВЗК/абдоминальный туберкулез» диагноз болезни Крона следует рассматривать только в случае отсутствия ответа на ПТТ [22]. Однако до сих пор остаются неопределенными сроки, через которые необходимо проводить оценку эффективности терапии. В исследовании Kedia S., и соавт. из 358 пациентов с болезнью Крона, 135 (38,0%) получали ПТТ в течение не менее 3 месяцев, прежде чем им был окончательно установлен диагноз болезни Крона. Их ответ на терапию сравнивали с 157 пациентами с туберкулезом кишечника. Через 3–6 месяцев более чем у 90% пациентов с туберкулёзом отмечен положительный эффект от лечения в сравнении с 38% у пациентов с болезнью Крона. В течение года при абдоминальном туберкулезе сохранялся ответ на терапию, а при болезни Крона в 80% случаев состояние пациентов ухудшалось. Более того, повторная колоноскопия через 6 месяцев лечения показала заживление слизистой оболочки у 100% пациентов с туберкулезом кишечника, тогда как эндоскопический ответ наблюдался у < 5% пациентов с болезнью Крона. Поэтому, основываясь на данных результатах, авторами предложен алгоритм наблюдения за пациентами, прошедшими эмпирическую ПТТ [12] (Рис. 7).
Рисунок 7. Алгоритм ведения пациентов, получающих эмпирическую противотуберкулезную терапию [13]
Figure 7. Algorithm for the patients receiving empirical antituberculosis therapy [13]
Показания к хирургическому лечению абдоминального туберкулеза определяются как абсолютные: осложнения туберкулеза внутрибрюшных лимфатических узлов и других органов брюшной полости (абсцессы, перитонит, межкишечные свищи, кишечная непроходимость, перфорация, кровотечение), так и индивидуальные: вопрос о проведении операции зависит от особенностей клинических проявлений заболевания у конкретного пациента [5]. Около 20–40% пациентов с абдоминальным туберкулезом имеют клиническую картину «острого живота» и нуждаются в оперативном лечении [23]. В проспективном исследовании Barot M. и соавт. показано, что наиболее частым показанием к хирургическому лечению было поражение тонкой кишки и илеоцекальной зоны с развитием кишечной непроходимости [24]. Операции, выполняемые при туберкулезе кишечника, в основном бывают трех типов [25]. Первый тип — это операции, которые проводятся для обхода вовлеченных сегментов кишечника, например, энтероэнтеростомия или илеотрансверзостомия. Второй тип — сегментарные резекции, например, ограниченная илеоцекальная резекция. При этом астенизация пациентов и распространенность поражения часто являются ограничивающими факторами. Третий тип — стриктуропластика. Для случаев с множественными стриктурами предложена как метод, имеющий преимущества по сравнению с множественными резекциями и энтероанастомозами, поскольку позволяет избежать риска синдрома короткой кишки или слепых петель. Протяженные стриктуры с активным воспалением или множественные стриктуры могут потребовать резекции [26].
ЗАКЛЮЧЕНИЕ
В данном клиническом наблюдении продемонстрирован весь сложный дифференциально-диагностический путь от момента появления первых симптомов до верификации диагноза, который у пациентки занял более полугода. Неспецифичность симптомов вынуждала больную обращаться к терапевту, врачу общей практики, хирургу, онкологу, гастроэнтерологу, фтизиатру. Были выполнены различные лабораторные и инструментальные обследования. Лучевые методы визуализации описывали различные патологические изменения, но не позволяли их идентифицировать по принадлежности к какой-то определенной нозологической форме. Эндоскопическое исследование с последующим морфологическим описанием биопсийного материала дало значительно больше информации и помогло клиницистам определиться с дальнейшим поиском. Но, как и указано в литературных источниках, окончательно подтвердить диагноз туберкулеза кишечника смогло только гистологическое исследование. Таким образом, осведомленность специалистов в отношении ВЛТ, настойчивость в диагностическом поиске, привлечение врачей различных специальностей способствовали благоприятному исходу.
.
Список литературы:
2. ЖуковаИ.И., Кульчавеня Е.В., ХолтобинД.П., и соавт. Туберкулез мочеполовой системы сегодня. Урология. 2013;1:13-16.
3. Арямкина О.Л., Савоненкова Л.Н. Абдоминальный туберкулез: патоморфология, патогенез, классификация, клиника, диагностика: учебно-методическое пособие. Ульяновск: УлГУ, 2010. с. 83.
4. Скопин М.С., Батыров Ф.А., Корнилова З.Х. Распространенность туберкулеза органов брюшной полости и особенности его выявления. Проблемы туберкулеза и болезней легких. 2007;84;1:22-26.
5. Фтизиатрия. Национальное руководство / под ред. М.И. Перельмана. М. ГЭОТАР-Медиа, 2007. 512 с. (Серия «Национальные руководства»).
6. Васильев А.В. (ред.). Внелегочный туберкулез. Руководство для врачей. Санкт-Петербург, 2000;560 с.
7. Савоненкова Л.Н., Рузов В.И., Колчин Д.В., и соавт. Трудности и ошибки диагностики абдоминального туберкулеза в практике терапевта. Терапевтический архив. 2019;91(11):16-19. https://doi.org/10.26442/00403660.2019.11.000374
8. Huang X, Liao WD, Yu C, et al. Differences in clinical features of Crohn’s disease and intestinal tuberculosis. World J Gastroenterol. 2015;21:3650-3656. https://doi.org/10.3748/wjg.v21.i12.3650
9. Kapoor VK. Abdominal tuberculosis: the Indian contribution. Indian J Gastroenterol. 1998;17:141-147. PMID: 9795502.
10. Hallur V, Sharma M, Sethi S, et al. Development and evaluation of multiplex PCR in rapid diagnosis of abdominal tuberculosis. Diagn Microbiol Infect Dis. 2013;76:51-55. https://doi.org/10.1016/j.diagmicrobio.2013.02.022
11. Pollock N, McAdam A, Pai M, et al. Interferon γ-release assays for diagnosis of latent tuberculosis in healthcare workers in lowincidence of settings: pro and cons. Clin Chem. 2014;60(5):714-718.
12. Chen W, Fan JH, Luo W, et al. Effectiveness of interferon-gamma release assays for differentiating intestinal tuberculosis from Crohn’s disease: a meta-analysis. World J Gastroenterol. 2013;19:8133-8140. https://doi.org/10.3748/wjg.v19.i44.8133
13. Kedia S, Das P, Madhusudhan KS, et al. Differentiating Crohn’s disease from intestinal tuberculosis. World J Gastroenterol. 2019 Jan 28;25(4):418-432. https://doi.org/10.3748/wjg.v25.i4.418
14. Bae JH, Park SH, Ye BD, et al. Development and Validation of a Novel Prediction Model for Differential Diagnosis Between Crohn’s Disease and Intestinal Tuberculosis. Inflamm Bowel Dis. 2017;23:1614-1623. https://doi.org/10.1097/MIB.0000000000001162
15. Jin T, Fei B, Zhang Y, et al. The diagnostic value of polymerase chain reaction for Mycobacterium tuberculosis to distinguish intestinal tuberculosis from Crohn’s disease: A meta-analysis. Saudi J Gastroenterol. 2017;23:3-10. https://doi.org/10.4103/1319-3767.199135
16. Ивашкин В.Т., Шелыгин Ю.А., Абдулганиева Д.И., и соавт. Клинические рекомендации по диагностике и лечению болезни Крона у взрослых (проект). Колопроктология. 2020;19(2):8-38. https://doi.org/10.33878/2073-7556-2020-19-2-8-38
17. Решетников М.Н., Матросов М.В., Антипов А.Г., Мальцев Р.В. Колоноскопия в диагностике туберкулёза органов брюшной полости. Туберкулез и социально значимые заболевания. 2014;3:39-42.
18. Chatzicostas C, Koutroubakis IE, Tzardi M., et al. Colonic tuberculosis mimicking Crohn’s disease: case report. BMC Gastroenterol. 2002. 2, 10. https://doi.org/10.1186/1471-230X-2-10
19. Елигулашвили Р.Р., Зароднюк И.В., Варданян А.В., и соавт. Возможности магнитно-резонансной энтероколонографии в количественной оценке активности воспалительного процесса в тонкой и толстой кишке при болезни Крона. REJR. 2020;10(1):99-109. https://doi.org/10.21569/2222-7415-2020-10-1-99-109
20. Kedia S, Sharma R, Sreenivas V, et al. Accuracy of computed tomographic features in differentiating intestinal tuberculosis from Crohn’s disease: a systematic review with metaanalysis. Intest Res. 2017 Apr;15(2):149-159. https://doi.org/10.5217/ir.2017.15.2.149
21. Makharia GK, Srivastava S, Das P, et al. Clinical, endoscopic, and histological differentiations between Crohn’s disease and intestinal tuberculosis. Am J Gastroenterol. 2010;105:642-651. https://doi.org/10.1038/ajg.2009.585
22. Ooi CJ, Makharia GK, Hilmi I et al. Asia Pacific Association of Gastroenterology (APAGE) Working Group on Inflammatory Bowel Disease. Asia Pacific Consensus Statements on Crohn’s disease. Part 1: Definition, diagnosis, and epidemiology: (Asia Pacific Crohn’s Disease Consensus-Part 1). J Gastroenterol Hepatol. 2016;31:45-55. https://doi.org/10.1111/jgh.12956
23. Saxena P, Saxena S. The role of laparoscopy in diagnosis of abdominal tuberculosis. Int Surg J. 2016;3:1557-1563. https://doi.org/10.18203/2349-2902.isj20162747
24. Barot M, Yagnik VD, Patel K, et al. Surgical management of abdominal tuberculosis: A prospective single-center study. Tzu Chi Med J. 2021 Jul-Sep;33(3):282-287. https://doi.org/10.4103/tcmj.tcmj_206_20
25. Wariyapperuma UM, Jayasundera CI. Peritoneal tuberculosis presenting with portal vein thrombosis and transudative Ascites - a diagnostic dilemma: case report. BMC Infect Dis. 2015;15:394. https://doi.org/10.1186/s12879-015-1122-6
26. Weledji EP, Pokam BT. Abdominal tuberculosis: Is there a role for surgery? World J Gastrointest Surg. 2017;9(8):174181. https://doi.org/10.4240/wjgs.v9.i8.174
Статьи по теме
Рекомендуемые статьи
При эндоскопическом исследовании в случае бронхоэктазов в стадии ремиссии выявляется
частично диффузный бронхит I степени воспаления
Активируйте PUSH уведомления в браузер
Отключите PUSH уведомления в браузер
Содержание
Интернет магазин
Популярное
- О нас
- Правовые вопросы
- Политика
обработки персональных
данных EndoExpert.ru - Связаться с нами
- Стать партнером
© 2016-2022 EndoExpert.ru

Вы находитесь в разделе предназначенном только для специалистов (раздел для пациентов по ссылке). Пожалуйста, внимательно прочитайте полные условия использования и подтвердите, что Вы являетесь медицинским или фармацевтическим работником или студентом медицинского образовательного учреждения и подтверждаете своё понимание и согласие с тем, что применение рецептурных препаратов, обращение за той или иной медицинской услугой, равно как и ее выполнение, использование медицинских изделий, выбор метода профилактики, диагностики, лечения, медицинской реабилитации, равно как и их применение, возможны только после предварительной консультации со специалистом. Мы используем файлы cookie, чтобы предложить Вам лучший опыт взаимодействия. Файлы cookie позволяют адаптировать веб-сайты к вашим интересам и предпочтениям.
Я прочитал и настоящим принимаю вышеизложенное, хочу продолжить ознакомление с размещенной на данном сайте информацией для специалистов.


.jpg)




.png)















Комментарии