- Компании
- Takeda. О компании, буклеты, каталоги, контакты
- Olympus. О компании, буклеты, каталоги, контакты
- Boston Scientific. О компании, буклеты, каталоги, контакты
- Pentax. О компании, буклеты, каталоги, контакты
- Fujifilm & R-Farm. О компании, буклеты, каталоги, контакты
- Erbe. О компании, буклеты, каталоги, контакты
- Еще каталоги
- Мероприятия
- Информация
- Обучение
- Классификации
- Атлас
- Quiz
- Разделы
- Пациенту
QR-код этой страницы
Для продолжения изучения на мобильном устройстве ПРОСКАНИРУЙТЕ QR-код с помощью спец. программы или фотокамеры мобильного устройства
Статьи: ПРОЕКТ КЛИНИЧЕСКИХ РЕКОМЕНДАЦИЙ ПО ДИАГНОСТИКЕ И ЛЕЧЕНИЮ ЯЗВЕННОГО КОЛИТА 2019

Полный текст статьи:
https://doi.org/10.33878/2073-7556-2019-18-4-7-36
ПРОЕКТ КЛИНИЧЕСКИХ РЕКОМЕНДАЦИЙ
ПО ДИАГНОСТИКЕ И ЛЕЧЕНИЮ ЯЗВЕННОГО КОЛИТА
Ивашкин В.Т., Шелыгин Ю.А., Белоусова Е.А., Абдулганиева Д.И., Алексеева О.А., Ачкасов С.И., Валуйских Е.Ю., Варданян А.В., Веселов А.В., Веселов В.В., Головенко О.В., Губонина И.В., Жигалова Т.Н., Кашников В.Н., Князев О.В., Макарчук П.А., Москалев А.И., Нанаева Б.А., Низов А.А., Никитина Н.В., Николаева Н.Н., Павленко В.В., Полуэктова Е.А.,
Светлова И.О., Тарасова Л.В., Ткачев А.В., Фролов С.А., Хлынова О.В., Чашкова Е.Ю., Шапина М.В., Шептулин А.А., Шифрин О.С., Щукина О.Б.
PROJECT: CLINICAL GUIDELINES FOR THE DIAGNOSTICS AND TREATMENT OF ULCERATIVE COLITIS
Ivashkin V.T., Shelygin Yu.A., Belousova E.A., Abdulganieva D.I., Alekseeva O.A., Achkasov S.I.,
Valuiskikh E.Yu., Vardanyan A.V., Veselov A.V., Veselov V.V., Golovenko O.V., Gubonina I.V., Zhigalova T.N., Kashnikov V.N., Knyazev O.V., Makarchuk P.A., Moskaliev A.I., Nanaeva B.A., Nizov A.A., Nikitina N.V., Nikolaeva N.N., Pavlenko V.V., Poluektova E.A., Svetlova I.O., Tarasova L.V., Tkachev A.V., Frolov S.A., Khlynova O.V., Chashkova E.Yu., Shapina M.V., Sheptulin A.A., Shifrin O.S., Shchukina O.B.
Ключевые слова
o Биологическая терапия
o Воспалительные заболевания кишечника
o Взрослые
o Глюкокортикостероиды
o Диарея
o Иммуносупрессоры
o Месалазин
o Язвенный колит
Список сокращений:
5- АСК – 5-аминосалициловая кислота
АЗА – азатиоприн
БК – болезнь Крона
БОС – биологическая обратная связь
ГИБП – генно-инженерный биологический препарат
ГКС – глюкокортикостероиды
ДИ – доверительный интервал
ИАРА – илеоанальный резервуарный анастомоз
ИМГ – индекс массы тела
КТ – компьютерная томография ММХ – мультиматриксная оболочка МП – меркаптопурин
МРТ – магнитно-резонансная томография
НПВС – нестероидные противовоспалительные средства
РКИ – рандомизированное контролируемое испытание
СРБ – С-реактивный белок
ЯК – язвенный колит
ТЕРМИНЫ И ОПРЕДЕЛЕНИЯ
Язвенный колит (ЯК) – хроническое заболевание толстой кишки, характеризующееся иммунным воспалением ее слизистой оболочки.
Обострение (рецидив, атака) ЯК – появление типичных симптомов заболевания у больных ЯК в стадии клинической ремиссии, спонтанной или медикаментозно поддерживаемой. На практике признаками клинического обострения являются увеличение частоты дефекаций с выделением крови и/или характерные изменения, обнаруживаемые при эндоскопическом исследовании толстой кишки.
Ремиссия ЯК – исчезновение основных клинических симптомов заболевания [1] и заживление слизистой оболочки толстой кишки («глубокая ремиссия») [2]. Ремиссия ЯК, клиническая – отсутствие примеси крови в стуле, отсутствие императивных/ложных позывов при частоте дефекаций не более 3 раз в сутки. Ремиссия ЯК, эндоскопическая – отсутствие видимых макроскопических признаков воспаления при эндоскопическом исследовании толстой кишки.
Ремиссия ЯК, гистологическая – отсутствие микроскопических признаков воспаления.
1. КРАТКАЯ ИНФОРМАЦИЯ
1.1 Определение
Язвенный колит – хроническое заболевание толстой кишки, характеризующееся иммунным воспалением ее слизистой оболочки.
1.2 Этиология и патогенез
Этиология воспалительных заболеваний кишечника (ВЗК), в том числе ЯК, не установлена: заболевание развивается в результате сочетания нескольких факторов, включающих генетическую предрасположенность, дефекты врожденного и приобретенного иммунитета, кишечную микрофлору и различные факторы окружающей среды. Описано около 100 однононуклеотидных полиморфизмов, ассоциированных с ЯК. Данный генетический фон предрасполагает к изменениям врожденного иммунного ответа, аутофагии, механизмов распознавания микроорганизмов, эндоплазматического ретикулоцитарного стресса, функций эпителиального барьера и адаптивного иммунного ответа. Ключевым дефектом иммунитета, предрасполагающим к развитию ВЗК являются нарушения распознавания бактериальных молекулярных маркеров (паттернов) дендритными клетками, что приводит к гиперактивации сигнальных провоспалительных путей. Также при ВЗК отмечается снижение разнообразия кишечной микрофлоры за счет снижения доли анаэробных бактерий, преимущественно Bacteroidetes и Firmicutes. При наличии указанных микробиологических и иммунологических изменений ВЗК развивается под действием пусковых факторов, к которым относят курение, нервный стресс, дефицит витамина D, питание с пониженным содержанием пищевых волокон и повышенным содержанием животного белка, кишечные инфекции, особенно инфекцию C.difficile.
Результатом взаимного влияния данных факторов риска является активация Т-хелперов второго типа, гиперэкспрессия провоспалительных цитокинов, в первую очередь, фактора некроза опухоли-альфа (ФНО-альфа) и молекул клеточной адгезии. Результатом этих реакций становится лимфоплазмоцитарная инфильтрация слизистой оболочки толстой кишки с развитием характерных макроскопических изменений и симптомов ЯК.
При ЯК поражается только толстая кишка (за исключением ретроградного илеита), в процесс обязательно вовлекается прямая кишка, воспаление чаще всего ограничивается слизистой оболочкой (за исключением острого тяжелого колита) и носит диффузный характер.
1.3 Эпидемиология
Согласно зарубежным данным, заболеваемость ЯК составляет от 0,6 до 24,3 на 100 000 человек, распространенность достигает 505 на 100 000 человек [3]. Данные о распространенности ЯК в Российской Федерации ограничены [4]. Распространенность ЯК выше в северных широтах и на Западе. Заболеваемость и распространенность ЯК в Азии ниже, однако, увеличивается. Европеоиды страдают заболеванием чаще, чем представители негроидной и монголоидной рас. Пик заболеваемости отмечается между 20 и 30 годами жизни, а второй пик заболеваемости описан в возрасте 60-70 лет. Заболеваемость приблизительно одинакова у мужчин и женщин.
1.4 Кодирование по МКБ 10
K51.0 – Язвенный (хронический) энтероколит K51.0 – Язвенный (хронический) илеоколит K51.0 – Язвенный (хронический) проктит
K51.0 – Язвенный (хронический) ректосигмоидит
K51.4– Псевдополипоз ободочной кишки
K51.5– Мукозный проктоколит
K51.8– Другие язвенные колиты
K51.9– Язвенный колит неуточненный
1.5 Классификация
Надлежащая классификация ЯК по протяженности поражения, характеру течения, тяжести атаки и наличию осложнений определяет вид и форму введения лекарственных препаратов, а также периодичность скрининга на колоректальный рак [5].
Для описания протяженности поражения применяется Монреальская классификация (Табл. 1), оценивающая протяженность макроскопических изменений при эндоскопическом исследовании толстой кишки.
Таблица 1. Монреальская классификация ЯК по протяженности поражения [6].
|
Проктит |
Поражение ограничено прямой кишкой |
|
Левосторонний колит |
Поражение распространяется до левого изгиба толстой кишки (включая проктосигмоидит) |
|
Тотальный колит |
Поражение распространяется проксимальнее левого изгиба толстой кишки (включая субтотальный колит, а также тотальный ЯК с ретроградным илеитом) |
По характеру течения выделяют:
• Острое течение (менее 6 месяцев от дебюта заболевания):
• Хроническое непрерывное течение (отсутствие более чем 6-месячных периодов ремиссии на фоне адекватной терапии).
• Хроническое рецидивирующее течение (наличие более чем 6-месячных периодов ремиссии).
Тяжесть заболевания, в целом, определяется: тяжестью текущей атаки, наличием внекишечных проявлений и осложнений, рефрактерностью к лечению, в частности, развитием гормональной зависимости и резистентности. Однако для формулирования диаг-
Таблица 2. Тяжесть атаки ЯК согласно критериям Truelove-Witts [7].
|
|
Легкая |
Среднетяжелая |
Тяжелая |
|
Частота дефекаций с кровью |
<4 |
≥4, если: |
≥6, если: |
|
Пульс |
Нормальные значения |
≤90 уд/мин |
>90 уд/мин или |
|
Температура |
≤37,5°С |
>37,5°С или | |
|
Гемоглобин |
≥105 г/л |
<105 г/л или | |
|
СОЭ |
≤30 мм/ч |
>30 мм/ч | |
|
Контактная ранимость слизистой оболочки толстой кишки |
Нет |
Есть |
Есть |
Таблица 3. Тяжесть атаки согласно индексу активности ЯК (индекс Мейо)
|
Значение индекса |
0 |
1 |
2 |
3 |
|
Частота стула |
Обычная |
на 1-2/день больше обычной |
На 3-4/день больше обычной |
на 5/день больше обычной |
|
Примесь крови в стуле |
Нет |
Прожилки |
Видимая кровь |
Преимущественно кровь |
|
Состояние слизистой оболочки |
Норма |
Минимальная активность (1 балл по шкале Schroeder) |
Умеренная активность (2 балла по шкале Schroeder) |
Выраженная активность (3 балла по шкале Schroeder) |
|
Общая оценка состояние врачом |
Норма |
Удовлетворительное состояние |
Состояние средней тяжести |
Тяжелое состояние |
Среднетяжелая и тяжелая атака констатируются при значении индекса (сумма оценок по 4 параметрам) от 6 и выше.
Таблица 4. Классификация ЯК в зависимости от эндоскопической активности (по Schroeder) [11]
|
0 |
1 (минимальная активность) |
2 (умеренная активность) |
3 (выраженная активность) |
|
Норма или неактивное заболевание |
Легкая гиперемия, смазанный сосудистый рисунок. Легкая контактная ранимость |
Выраженная гиперемия, отсутствие сосудистого рисунка, умеренная контактная ранимость, эрозии |
Спонтанная ранимость, изъязвления |
ноза и определения тактики лечения следует определять тяжесть текущего обострения (атаки), для чего используются простые критерии Truelove-Witts, как правило, применяемые в повседневной клинической практике, и индекс активности ЯК (индекс Мейо), как правило, применяемый в клинических испытаниях. Выделяют легкую, среднетяжелую и тяжелую атаки ЯК (Табл. 2 и 3).
В клинической практике нередко встречается так называемая «сверхтяжелая» или «крайне тяжелая» атака ЯК, характеризующаяся диареей более 10-15 раз в сутки, нарастающим падением гемоглобина, лихорадкой выше 38°С, тяжелой гипопротеинемией и электролитными сдвигами, высоким уровнем СРБ [8,9]. Подходы к лечению такого колита отличаются от обычных. В англоязычной литературе такое состояние называется «острый тяжелый ЯК» (acute severe UC) [10]. Используемая в индексе Мейо шкала оценки состояния слизистой оболочки по Schroeder приведена в таблице 4 и применяется для оценки эндоскопической активности ЯК.
Классификация ЯК, в зависимости от ответа на гормональную терапию, облегчает выбор рациональной лечебной тактики, поскольку целью консервативного лечения является достижение стойкой ремиссии с прекращением терапии глюкокортикостероидами (ГКС). Для этих целей выделяются:
1. Гормональная резистентность:
a. В случае тяжелой атаки – отсутствие положительной динамики со стороны клинических и лабораторных показателей, несмотря на применение системных ГКС в дозе, эквивалентной 2 мг/кг массы тела преднизолона в сутки, в течение более чем 7 дней;
б. В случае среднетяжелой атаки – сохранение активности заболевания при пероральном приеме ГКС в дозе, эквивалентной 1 мг/кг массы тела преднизолона, в течение 2 недель.
2. Гормональная зависимость:
a. Увеличение активности болезни, возникшее при уменьшении дозы ГКС после достижения исходного улучшения в течение 3 месяцев от начала лечения;
б. Возникновение рецидива болезни в течение 3 месяцев после окончания лечения ГКС.
При формулировании диагноза следует отразить характер течения заболевания, протяженность поражения, тяжесть текущей атаки или наличие ремиссии, наличие гормональной зависимости или резистентности, а также наличие внекишечных или кишечных осложнений ЯК. Ниже приведены примеры формулировок диагноза:
1. «Язвенный колит, хроническое рецидивирующее течение, проктит, среднетяжелая атака».
2. «Язвенный колит, хроническое непрерывное течение, левостороннее поражение, среднетяжелая атака. Гормональная зависимость. Внекишечные проявления (периферическая артропатия)».
3. «Язвенный колит, хроническое рецидивирующее течение, тотальное поражение, тяжелая атака. Гормональная резистентность. Токсический мегаколон».
Таблица 5. Основные симптомы язвенного колита
|
Возможные симптомы болезни в анамнезе |
Типичные клинические симптомы в момент осмотра | |
|
aЭпизоды диареи aВнекишечные симптомы aПримесь крови в кале (поражение кожи, сли- aТенезмы зистых оболочек, суставов, глаз и др.) |
aДиарея aКровь в кале aНочная дефекация (чаще при выраженной активности процесса) |
aТенезмы (чаще при проктитах и проктосигмоидитах) aПотеря массы тела aЛихорадка aАнемия aВнекишечные симптомы |
Таблица 6. Внекишечные (системные) проявления язвенного колита
|
Аутоиммунные, связанные с активностью заболевания: |
Аутоиммунные, не связанные с активностью заболевания: |
Обусловленные длительным воспалением и метаболическими нарушениями: |
|
Артропатии (артралгии, артриты) |
Анкилозирующий спондилит |
Холелитиаз |
|
Поражение кожи (узловатая эритема, |
(сакроилеит) |
Стеатоз печени, стеатогепатит |
|
гангренозная пиодермия) |
Первичный склерозирующий холангит |
Тромбоз периферических вен, тромбоэмболия |
|
Поражение слизистых (афтозный стоматит) |
Остеопороз, остеомаляция |
легочной артерии |
|
Поражение глаз (увеит, ирит, иридоциклит, |
Псориаз |
Амилоидоз |
|
эписклерит) |
|
|
1.6 Клиническая картина
К основным клиническим симптомам язвенного колита относятся диарея и/или ложные позывы с кровью, тенезмы и императивные позывы на дефекацию, а также ночная дефекация. При тяжелой атаке ЯК возможно появление общих симптомов, таких как снижение массы тела, общая слабость, анорексия и лихорадка. Основные симптомы перечислены в таблице 5.
Для ЯК, в отличие от болезни Крона (БК), боль в животе менее характерна и носит умеренный (спастический) характер, чаще перед стулом; при проктитах и проктосигмоидитах диарея может отсутствовать, а частые ложные позывы могут сочетаться с запорами или оформленным стулом.
У значительной доли больных могут обнаруживаться внекишечные проявления заболевания (Табл. 6) [12]. Аутоиммунные проявления, связанные с активностью воспалительного процесса, появляются вместе с основными кишечными симптомами обострения и исчезают вместе с ними на фоне лечения. Аутоиммунные проявления, не связанные с активностью процесса (в англоязычной литературе их часто называют «сопутствующими аутоиммунными заболеваниями»), имеют тенденцию к прогрессированию независимо от фазы основного заболевания (обострение или ремиссия) и часто определяют негативный прогноз болезни. Кишечные осложнения ЯК включают кишечное кровотечение, токсическую дилатацию и перфорацию толстой кишки, а также колоректальный рак. Поскольку эти осложнения в большей степени требуют хирургического лечения, подробно они рассматриваются в Разделе 3.2 «Хирургическое лечение»
2. ДИАГНОСТИКА
Однозначных диагностических критериев ЯК не существует. Диагноз выставляется на основании сочетания данных анамнеза, клинической картины и типичных эндоскопических и гистологических изменений.
2.1 Жалобы и анамнез
У всех пациентов при подозрении на ЯК рекомендовано при сборе анамнеза обратить внимание на частоту и характер стула, длительность данных симптомов, наличие примеси крови, характер болей в животе [13,14].
Уровень убедительности рекомендаций – B (уровень достоверности доказательств – 3)
• У всех пациентов при подозрении на ЯК при сборе анамнеза следует провести подробный опрос, включающий, в частности, сбор информации о:
o поездках в южные страны [15].
Уровень убедительности рекомендаций – В (уровень достоверности доказательств – 3)
o принимаемых лекарствах (в частности, антибио-
тиках и нестероидных противовоспалительных средствах (НПВС)) [16].
Уровень убедительности рекомендаций – В (уровень достоверности доказательств – 3)
o курении [17].
Уровень убедительности рекомендаций – A (уровень достоверности доказательств – 1)
o наличии воспалительных и злокачественных заболеваний кишечника у родственников [18].
Уровень убедительности рекомендаций – В (уровень достоверности доказательств – 3)
2.2 Физикальное обследование
• У всех пациентов с подозрением на ЯК рекомендовано в обязательном порядке проводить физикальное обследование [19,20,21]:
– осмотр перианальной области;
– пальцевое исследование прямой кишки; Комментарий. При физикальном осмотре могут быть обнаружены различные проявления ЯК, вклю-
чая лихорадку, периферические отеки, дефицит питания, наличие признаков перфорации или токсической дилатации толстой кишки, а также внекишечных проявлений.
2.3 Лабораторная диагностика
• Для всех пациентов обязательным минимумом лабораторной диагностики является:
– Клинический анализ крови (гемоглобин, гематокрит [22,23] лейкоциты, нейтрофилы, лимфоциты, моноциты [23,24,25], тромбоциты [23], скорость оседания эритроцитов (СОЭ) [26]);
– Биохимия крови (общий белок, альбумины [23], печеночные ферменты [27], электролиты [28]);
– С-реактивный белок [26,29];
– Гемокоагулограмма (фибриноген) [30].
Уровень убедительности рекомендаций – C (уровень достоверности доказательств – 5) Комментарий. При клиническом анализе крови могут быть диагностированы анемия (железодефицитная, анемии хронического заболевания), лейкоцитоз (на фоне хронического воспаления или на фоне стероидной терапии), тромбоцитоз. Биохимическое исследование позволяет выявить электролитные нарушения, гипопротеинемию (в частности, гипоальбуминемию), а также повышение щелочной фосфатазы, что является возможным проявлением ассоциированного с ЯК первичного склерозирующего холангита.
• У всех пациентов с острым течением ЯК (первой атаке заболевания) рекомендовано выполнить бактериологическое и микроскопическое исследование кала для исключения острой кишечной инфекции [17].
Уровень убедительности рекомендаций – В (уровень достоверности доказательств – 3) Комментарий. Как при дебюте заболевания, так и при обострениях, рекомендуется исследование токсинов А и В C.difficile (особенно, при недавно проведенном курсе антибиотикотерапии или пребывании в стационаре). Данное исследование также рекомендуется выполнять при тяжелом развитии резистентности к проводимой терапии [31,32]. Для выявления инфекции в 90% случаев требуется минимум 4 образца кала [33,34]. При тяжелом и сверхтяжелом ЯК необходимо исключение цитомегаловирусной (ЦМВ) инфекции.
• У всех пациентов с подозрением на ЯК рекомендовано исследование уровня фекального кальпротектина при первичной дифференциальной диагностике с функциональными заболеваниями кишечника, а также для неивазивной оценки активности воспалительного процесса в кишечнике на фоне лечения [35,36].
Уровень убедительности рекомендаций – В (уровень достоверности доказательств – 2b)
• Пациентам при среднетяжелой и тяжелой атаках язвенного колита, а также в случае гормональной резистентности или гормональной зависимости, резистентности к терапии иммуносупрессорами или препаратами биологической терапии, потере эффекта на терапии иммуносупрессорами или препаратами биологической терапии показано проведение исследования ДНК цитомегаловируса в биоптате из пораженных участков толстой кишки методом полимеразной цепной реакции [20,37].
Уровень убедительности рекомендаций – В (уровень достоверности доказательств – 3) Комментарий: Диагностически значимым титром считается более 5000 копий/105 клеток.
2.4 Инструментальная диагностика
Диагностика ЯК, преимущественно, основана на инструментальных методах исследования. Для подтверждения диагноза необходимы следующие мероприятия:
• Всем пациентам с ЯК рекомендована ректороманоскопия [19,38].
Уровень убедительности рекомендаций – C (уровень достоверности доказательств – 5);
• Пациентам с тяжелой атакой ЯК рекомендована обзорная рентгенография брюшной полости для исключения токсической дилятации и перфорации толстой кишки [39,40].
Уровень убедительности рекомендаций – C (уровень достоверности доказательств – 5);
• Всем пациентам с подозрением на ЯК рекомендовано проведение колоноскопии с илеоскопией для определения локализации, протяженности, степени активности воспалительного процесса [41].
Уровень убедительности рекомендаций – А (уровень достоверности доказательств – 1); Комментарий. Колоноскопия обязательная для установления диагноза ЯК, а также для решения вопроса о колэктомии;
Эндоскопическое исследование толстой кишки является основным методом диагностики ЯК, однако, специфичные эндоскопические признаки отсутствуют. Наиболее характерными являются непрерывное воспаление, ограниченное слизистой оболочкой, начинающееся в прямой кишке и распространяющееся проксимальнее, с четкой границей воспаления. Эндоскопическую активность ЯК наилучшим образом отражают контактная ранимость (выделение крови при контакте с эндоскопом), отсутствие сосудистого рисунка и наличие или отсутствие эрозий и изъязвлений. Обнаружение стойкого сужения кишки на фоне ЯК требует обязательного исключения колоректального рака.
• Всем пациентам с подозрением на ЯК при первичной постановке диагноза, при сомнениях в правильности ранее выставленного диагноза, рекомендовано выполнение биопсии слизистой оболочки толстой кишки [41,42].
Уровень убедительности рекомендаций – А (уровень достоверности доказательств – 1); Комментарий. При длительном анамнезе ЯК (более 7-10 лет) – хромоэндоскопия с прицельной биопсией или ступенчатая биопсия (из каждого отдела толстой кишки) для исключения дисплазии эпителия; Рекомендуемым стандартом биопсии при постановке диагноза является взятие биоптатов слизистой оболочки прямой кишки и не менее чем из 4 других участков толстой кишки, а также слизистой оболочки подвздошной кишки.
К микроскопическим признакам ЯК относятся деформация крипт (разветвленность, разнонаправленность, появление крипт разного диаметра, уменьшение плотности крипт, «укорочение крипт», крипты не достигают подлежащего слоя мышечной пластинки слизистой оболочки), «неровная» поверхность слизистой в биоптате слизистой оболочки, уменьшение числа бокаловидных клеток, базальный плазмоцитоз, инфильтрация собственной пластинки слизистой оболочки, наличие крипт-абсцессов и базальных лимфоидных скоплений. Степень воспалительной инфильтрации обычно уменьшается по мере удаления от прямой кишки.
• Всем пациентам с подозрением на ЯК при первичной постановке диагноза, при сомнениях в правильности ранее выставленного диагноза, при длительном анамнезе ЯК, при подозрении на осложнения ЯК, а также для исключения патологии других органов брюшной полости рекомендовано ультразвуковое исследование органов брюшной полости, забрюшинного пространства, малого таза [43,44].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 4);
• Всем пациентам с подозрением на ЯК при необходимости дифференциальной диагностики или при невозможности проведения полноценной илеоколоноскопии рекомендуются рентгенологические исследования:
– Магнитно-резонансная томография (МРТ) с контрастированием кишечника [45,46];
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 5);
В случае недоступности экспертной оценки или невозможности выполнения МРТ с контрастированием кишечника рекомендована – Компьютерная томография (КТ) с контрастированием кишечника [47,48]; Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 5);
• Всем пациентам с подозрением на ЯК при необходимости дифференциальной диагностики или при невозможности проведения полноценной илеоколоноскопии, МРТ и КТ рекомендуется проведение ирригоскопии с двойным контрастированием для оценки протяженности поражения в толстой кишке, уточнения наличия образований, стриктур и др. [20,49].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 5); Дополнительными исследованиями при наличии показаний могут быть:
– трансабдоминальное ультразвуковое сканирование тонкой и ободочной кишки;
– трансректальное ультразвуковое исследование прямой кишки и анального канала;
– фиброгастродуоденоскопия;
– видеокапсульная эндоскопия;
– одноили двухбаллонная энтероскопия.
2.5 Иная диагностика
Дополнительные инструментальные и лабораторные исследования выполняются, преимущественно, с целью проведения дифференциальной диагностики срядомзаболеваний. Этоинфекционные, сосудистые, медикаментозные, токсические и радиационные поражения, а также дивертикулит и др. На следующем этапе дифференциальной диагностики проводится верификация клинических диагнозов ЯК и БК, относящихся к группе ВЗК. Таким образом, дифференциальный диагноз ЯК проводится с болезнью Крона толстой кишки, острыми кишечными инфекциями (дизентерия, сальмонеллез, кампилобактериоз, иерсиниоз, амебиаз), паразитозами, антибиотико-ассоциированными поражениями кишечника (псевдомембранозный колит, вызываемый C.Difficile) [50], туберкулезом кишечника, системными васкулитами, раком толстой кишки, дивертикулитом, микроскопическими колитами (коллагеновым и лимфоцитарным) [51], радиационным проктитом.
С целью дифференциальной диагностики и подбора терапии при внекишечных проявлениях ЯК и сопутствующих состояниях может потребоваться консультация:
• Психотерапевта, психолога (невроз, планируемая операция с наличием стомы и т.п.);
• Эндокринолога (стероидный сахарный диабет, надпочечниковая недостаточность у больных на длительной гормональной терапии);
• Дерматолога (дифференциальный диагноз узловатой эритемы, пиодермии и т.п.);
• Ревматолога (артропатии, сакроилеит и т.п.);
• Акушера-гинеколога (беременность).
3. ЛЕЧЕНИЕ
3.1 Консервативное лечение
3.1.1 Принципы терапии
Лечебные мероприятия при ЯК включают в себя назначение лекарственных препаратов, хирургическое лечение, психосоциальную поддержку и диетические рекомендации.
Выбор вида консервативного или хирургического лечения определяется тяжестью атаки, протяженностью поражения толстой кишки, наличием внекишечных проявлений, длительностью анамнеза, эффективностью и безопасностью ранее проводившейся терапии, а также риском развития осложнений ЯК [52,53].
Целью терапии является достижение и поддержание беcстероидной ремиссии (прекращение приема ГКС в течение 12 недель после начала терапии) [54], профилактика осложнений ЯК, предупреждение операции, а при прогрессировании процесса и/или развитии опасных для жизни осложнений – своевременное назначение хирургического лечения. Поскольку полное излечение больных ЯК достигается только путем удаления толстой кишки (колпроктэктомии), при достижении ремиссии неоперированный больной должен оставаться на постоянной поддерживающей (противорецидивной) терапии.
Следует особо отметить, что ГКС не могут применяться в качестве поддерживающей терапии.
Ниже представлены рекомендации по выбору препаратов для индукции и поддержания ремиссии в зависимости от протяженности поражения и тяжести атаки [20].
3.1.2 Проктит. Легкая и среднетяжелая атака.
• Данной группе пациентов рекомендовано назначение суппозиториев с месалазином** (1-2 г/сут.) или ректальной пены месалазина (1-2 г/сут.) [55]. Уровень убедительности рекомендации A (уровень достоверности доказательств – 1). Комментарий. Оценка терапевтического ответа производится через 2 недели [55]. При положительном ответе лечение в указанных дозах пролонгируется до 6-8 недель.
• Данной группе пациентов при неэффективности лечения ректальными формами месалазина рекомендованы ректальные формы ГКС (ректальная пена будесонид 2 мг в сутки, суппозитории с преднизолоном 10 мг ´ 1-2 раза в сутки) с оценкой ответа через 2 недели [56].
Уровень убедительности рекомендации A (уровень достоверности доказательств – 1).
• Данной группе пациентов при достижении ремиссии рекомендована поддерживающая терапия – ректальное введение месалазина (свечи или ректальная пена) 1-2 г´ 3 раза в неделю в виде монотерапии (терапия «выходного дня») не менее 2 лет [57]. Уровень убедительности рекомендации A (уровень достоверности доказательств – 1).
• Данной группе пациентов при неэффективности местного лечения рекомендовано подключить пероральные формы месалазина (гранулы, таблетки, таблетки в мультиматриксной оболочке (ММХ)) в дозе 2,4-4,8 г/сут. [58].
Уровень убедительности рекомендации В (уровень достоверности доказательств – 1).
• Данной группе пациентов при отсутствии эффекта от пероральных форм месалазина рекомендовано назначение ГКС в дозе, эквивалентной 0,5-0,75 мг/кг массы тела преднизолона в таблетках в сутки. Возможно также назначение топических стероидов (будесонид ММХ в дозе 9 мг в сутки) [59].
Уровень убедительности рекомендации В (уровень достоверности доказательств – 3).
• Данной группе пациентов в случае рецидива, требующего повторного назначения ГКС, рекомендована комбинация ГКС с азатиоприном (АЗА) или меркаптопурином (МП) [59].
Уровень убедительности рекомендации В (уровень достоверности доказательств – 3).
Комментарий. АЗА назначается по 2-2,5 мг/кг, а 6-МП по 1,5 мг/кг. Местная терапия (ректальная пена будесонид 2 мг в сутки, свечи с преднизолоном 10 мг ´ 1-2 раза в сутки) может быть продолжена.
• Данной группе пациентов при достижении ремиссии, индуцированной ГКС, рекомендована поддерживающая терапия АЗА 2-2,5 мг/кг (или МП 1,5 мг/кг) не менее 2 лет [59].
Уровень убедительности рекомендации В (уровень достоверности доказательств – 3).
• В случае выявления у пациента в биоптате из пораженного участка слизистой толстой кишки ДНК цитомегаловируса методом полимеразной цепной реакции пациенту показана терапия ганцикловиром в дозе 5 мг/кг 2 раза в сутки в течение 14-21 дня [20,60].
Уровень убедительности рекомендации C (уровень достоверности доказательств – 4).
3.1.3 Проктит. Тяжёлое течение (развивается крайне редко).
• Данной группе пациентов при тяжелом язвенном проктите рекомендовано внутривенное ГКС в дозе, эквивалентной преднизолону 1-2 мг/кг массы тела в сутки в комбинации с местной терапией месалазином (суппозитории, ректальная пена) или ГКС (ректальная пена будесонид 2 мг в сутки, свечи с преднизолоном 10 мг ´ 1-2 раза в сутки) [56,59].
Уровень убедительности рекомендации C (уровень достоверности доказательств – 5).
Комментарий. Возможно назначение топических стероидов – будесонид ММХ в дозе 9 мг в сутки, в комбинации с местной терапией месалазином или ГКС.
• Данной группе пациентов в случае первой атаки поддерживающая терапия при достижении ремиссии проводится местными формами препаратов месалазина (суппозитории, ректальная пена) 1-2 г´ 3 раза в неделю в виде монотерапии (регулярное применение, терапия по требованию или терапия «выходного дня») или в комбинации с пероральным месалазином (гранулы, таблетки, таблетки ММХ) в дозе 2-2,4 г – не менее 2 лет [57].
Уровень убедительности рекомендации А (уровень достоверности доказательств – 1).
• Данной группе пациентов при рецидиве, требующем повторного назначения ГКС (системных или топических), одновременно рекомендовано назначение АЗА 2-2,5 мг/кг (или МП 1,5 мг/кг) и продолжение поддерживающей терапии иммуносупрессорами (АЗА или МП) не менее 2 лет [59].
Уровень убедительности рекомендации C (уровень достоверности доказательств – 5).
• В случае выявления у пациента в биоптате из пораженного участка слизистой толстой кишки ДНК цитомегаловируса методом полимеразной цепной реакции пациенту показана терапия ганцикловиром в дозе 5 мг/кг 2 раза в сутки в течение 14-21 дня [20,60].
Уровень убедительности рекомендации C (уровень достоверности доказательств – 4).
3.1.4 Левосторонний и тотальный язвенный колит. Легкая атака.
• Данной группе пациентов при первой атаке или рецидиве рекомендовано назначение месалазина внутрь (гранулы, таблетки, таблетки ММХ) 2,4-3 г/сут. (или сульфасалазин 3 г/сут.) в комбинации с месалазином в клизмах 2-4 г/сут. (в зависимости от эндоскопической активности) [61-66].
Уровень убедительности рекомендации А (уровень достоверности доказательств – 1).
Комментарий. Терапевтический ответ оценивается через 2 недели. При положительном ответе терапия продолжается до 6-8 недель.
• Данной группе пациентов при отсутствии эффекта от комбинированной терапии препаратами 5-аминосалициловой кислоты (5-АСК) рекомендовано назначение ректальных форм ГКС: ректальной пены будесонид 2 мг в сутки или суспензии гидрокортизонаацетата с лидокаином 125-250 мг 1 раз в сутки в виде клизм или ректального капельного введения [67]. Уровень убедительности рекомендации C (уровень достоверности доказательств – 4).
• Данной группе пациентов при достижении ремис-
сии рекомендовано проводить поддерживающую терапию пероральным месалазином (гранулы, таблетки, таблетки ММХ) 2-2,4 г/сут. [68].
Уровень убедительности рекомендации А (уровень достоверности доказательств – 1).
Комментарий. Дополнительное введение месалазина в клизмах по 2 г ´ 2 раза в неделю («терапия выходного дня») увеличивает вероятность долгосрочной ремиссии. Допустимо назначение сульфасалазина (2 г) вместо месалазина.
• Данной группе пациентов при отсутствии ответа на терапию пероральными препаратами 5-АСК в сочетании с любым местным вариантом лечения, как правило, рекомендовано назначение топических ГКС (будесонид MMX) или системных ГКС (см. раздел 3.1.4) [69].
Уровень убедительности рекомендации В (уровень достоверности доказательств – 2).
• В случае выявления у пациента в биоптате из пораженного участка слизистой толстой кишки ДНК цитомегаловируса методом полимеразной цепной реакции пациенту показана терапия ганцикловиром в дозе 5 мг/кг 2 раза в сутки в течение 14-21 дня [20,60].
Уровень убедительности рекомендации C (уровень достоверности доказательств – 4).
3.1.5 Левосторонний и тотальный язвенный колит. Среднетяжелая атака.
• Данной группе пациентов при первой атаке или рецидиве рекомендовано назначение перорального месалазина (гранулы, таблетки, таблетки ММХ) 3,0-4,8 г/сут. в комбинации с месалазином в клизмах 2-4 г/сут. (в зависимости от эндоскопической активности) [63,70].
Уровень убедительности рекомендации А (уровень достоверности доказательств – 1).
Комментарий. Терапевтический ответ оценивается через 2 недели. При улучшении клинической симптоматики и положительной лабораторной динамике терапия продолжается до 6-8 недель.
• Данной группе пациентов при достижении ремиссии рекомендована поддерживающая терапия препаратами месалазина (гранулы, таблетки, таблетки ММХ) 2-2,4 г/сут. внутрь + месалазин в клизмах по 2 г´ 2 раза в неделю (терапия «выходного дня») [66,71].
Уровень убедительности рекомендации А (уровень достоверности доказательств – 1).
Комментарий. Допустимо назначение сульфасалазина 2 г/сут. вместо месалазина [70].
• Данной группе пациентов при отсутствии эффекта от 5-АСК и отсутствии системных признаков воспаления показано назначение топических ГКС (будесонид ММХ) [69,72-74].
Уровень убедительности рекомендации В (уровень достоверности доказательств – 2).
Данной группе пациентов при отсутствии эффекта от 5-АСК и наличии системного воспаления показано назначение системных ГКС [69,72-74].
Комментарий. Системные ГКС назначают в дозе, эквивалентной преднизолону 0,75-1 мг/кг массы тела, топические (будесонид ММХ) в дозе 9 мг/сут. Снижение дозы системных ГКС производится по 5 мг в 5-7 дней до полной отмены. После 10-недельного приема будесонида ММХ, снижение дозы проводится через день в течение 1-2 недель до полной отмены.
• Данной группе пациентов при повторном назначении ГКС в течение года и менее или в случае непереносимости препаратов 5-АСК рекомендована комбинация ГКС с АЗА 2-2,5 мг/кг или МП 1,5 мг/кг [75,76]. Уровень убедительности рекомендации A (уровень достоверности доказательств – 1).
• Данной группе пациентов при достижении ремиссии рекомендовано продолжение поддерживающей терапии АЗА 2-2,5 мг/кг/сут. или МП 1,5 мг/кг не менее 2 лет [75,76].
Уровень убедительности рекомендации А (уровень достоверности доказательств – 1).
• Данной группе пациентов при отсутствии эффекта от ГКС в течение 2 недель показано проведение биологической терапии (инфликсимаб, адалимумаб, голимумаб, ведолизумаб или тофацитиниб), начиная с индукционного курса, в дозах, соответствующих инструкции по применению [77-81].
Уровень убедительности рекомендации А (уровень достоверности доказательств – 1).
• Пациентам, получающим инфликсимаб, для повышения его эффективности рекомендуется комбинировать с иммуносупрессорами (АЗА 2-2,5 мг/кг или МП 1,5 мг/кг [82,83].
Уровень убедительности рекомендации А (уровень достоверности доказательств – 1).
Комментарий. Для других биологических препаратов такая комбинация может не проводиться [84,85].
• Данной группе пациентов при эффективности индукционного курса биологических препаратов поддерживающая терапия проводится ими же в соответствии с инструкцией по применению в течение, как минимум, 2 лет [86-90].
Уровень убедительности рекомендации А (уровень достоверности доказательств – 1).
• Данной группе пациентов при отсутствии первичного ответа на анти-ФНО препараты рекомендована смена терапии на тофацитиниб [91].
Уровень убедительности рекомендации А (уровень достоверности доказательств – 1).
Комментарий. Тофацитиниб может быть назначен в качестве 1-ой и 2-ой линии терапии в комбинации с ГКС. Смена анти-ФНО на ведолизумаб возможна, но ее эффективность ниже.
• Данной группе пациентов при рецидиве ЯК на фоне ранее достигнутой ремиссии (потере ответа) на терапии анти-ФНО препаратами рекомендована оптимизация терапии в виде увеличения дозы препарата (10 мг/кг инфликсимаба каждые 8 недель, 100 мг
голимумаба каждые 4 недели) или сокращения интервалов между введениями (инфликсимаб каждые 4 недели, адалимумаб каждую неделю) или смена терапии на ведолизумаб или тофацитиниб [86-90].
Уровень убедительности рекомендации В (уровень достоверности доказательств – 2).
Комментарий. Смена на другой анти-ФНО препарат возможна, но ее эффективность ниже, чем при переходе на тофацитиниб.
• Данной группе пациентов при потере ответа на ведолизумаб в стандартной дозе 300 мг каждые 8 недель рекомендована оптимизация терапии в виде сокращения интервалов между введениями до 4 недель или смена на биологический препарат другого класса [92].
Уровень убедительности рекомендации C (уровень достоверности доказательств – 4).
• Данной группе пациентов при потере ответа на тофацитиниб в стандартной дозе 10 мг в день рекомендована оптимизация терапии до 20 мг в день или смена на биологический препарат другого класса [93]. Уровень убедительности рекомендации А (уровень достоверности доказательств – 1). Комментарий. Длительность биологической терапии определяется лечащим врачом. В большинстве стран лечение проводят в течение многих лет. Ранняя отмена препаратов, как правило, приводит к рецидиву ЯК в короткие сроки. При невозможности пролонгированного использования биологических препаратов, поддерживающая терапия проводится только тиопуринами. В случае непереносимости тиопуринов – монотерапия биологическими препаратами. В настоящее время зарегистрированы биосимиляры (биоаналоги) анти-ФНО препаратов, схожие с оригинальными биологическими лекарственными средствами по эффективности и безопасности, однако их взаимозаменяемость с оригинальными препаратами в настоящее время не доказана. С учетом отсутствия клинических испытаний у пациентов с ВЗК, доказавших безопасность и эффективность чередования или полного переключения с оригинального препарата на биоаналоги и наоборот, подобный терапевтический подход не рекомендован.
• Данной группе пациентов при снижении дозы ГКС,
эквивалентной 35-45 мг преднизолона, если пациент не получает иммуносупрессоров и биологической терапии, дополнительно рекомендовано подключить месалазин (гранулы, таблетки, таблетки ММХ) в дозе 4-4,8 г. [66].
Уровень убедительности рекомендации А (уровень достоверности доказательств – 1b).
Комментарий. Дальнейшее снижение ГКС следует проводить на фоне месалазина с последующим переходом на поддерживающую терапию месалазином (гранулы, таблетки, таблетки ММХ) 2-2,4 г в сутки.
Допустимо назначение сульфасалазина 2 г вместо месалазина.
• Данной группе пациентов с рецидивом тяжелого ЯК, возникшим на фоне поддерживающей терапии месалазином, сразу рекомендовано назначение ГКС в сочетании с АЗА/МП [94].
Уровень убедительности рекомендации C (уровень достоверности доказательств – 4).
Комментарий. Дальнейшая тактика аналогична лечению при первой атаке.
• Данной группе пациентов при рецидиве, возникшем на фоне поддерживающей терапии тиопуринами, рекомендовано назначение биологических препаратов (инфликсимаб, адалимумаб, голимумаб, ведолизумаб или тофацитиниб) [86-90].
Уровень убедительности рекомендации А (уровень достоверности доказательств – 1).
• В случае выявления у пациента в биоптате из пораженного участка слизистой толстой кишки ДНК цитомегаловируса методом полимеразной цепной реакции пациенту показана терапия ганцикловиром в дозе 5 мг/кг 2 раза в сутки в течение 14-21 дня [20,60]. Уровень убедительности рекомендации C (уровень достоверности доказательств – 5)
3.1.6 Левосторонний и тотальный язвенный колит. Тяжелая атака.
• Данной группе пациентов рекомендована внутривенная терапия ГКС в дозе, эквивалентной преднизолону 1-2 мг/кг массы тела в течение 7 дней или в/в введение гидрокортизона в дозе 300 мг в сутки [95]. Уровень убедительности рекомендации А (уровень достоверности доказательств – 1). Комментарий. Эквивалентность доз и длительности действия ГКС приведена в таблице 7.
• Данной группе пациентов дополнительно рекомендовано назначить местную терапию клизмами с месалазином 2-4 г в сутки или суспензией гидрокортизона-ацетата с лидокаином 125-250 мг´ 1 раз в сутки в виде клизм или ректального капельного введения [67].
Уровень убедительности рекомендации C (уровень достоверности доказательств – 3).
• Данной группе пациентов при наличии метаболических нарушений рекомендована инфузионная терапия с целью регидратации, коррекции белковоэлектролитных нарушений [54].
Уровень убедительности рекомендации C (уровень достоверности доказательств – 4).
Комментарий. Гипокалиемия и гипомагниемия повышают риск токсической дилатации ободочной кишки.
• Данной группе пациентов при уровне гемоглобина ниже 80 г/л рекомендована коррекция анемии в виде гемотрансфузии (эритромасса), от 80 до 100 г/л – терапия препаратами железа парентерально (железа
(III) гидрооксид сахарозный комплекс, железа (III) гидроксид декстрана, железо карбоксимальтозат) [96].
Уровень убедительности рекомендации А (уровень достоверности доказательств – 1).
• У пациентов с дефицитом массы тела (ИМТ менее
18) рекомендовано подключение дополнительного энтерального (зондового) питания [97];
Уровень убедительности рекомендации C (уровень достоверности доказательств – 5).
Комментарий. Полностью парентеральное питание и/или временное ограничение приема пищи внутрь нецелесообразно
• При наличии симптомов интоксикации рекомендовано назначение антибиотиков:
o 1 линия – метронидазол 1 г/сутки в/в + фторхинолоны (ципрофлоксацин, офлоксацин) в/в 10-14 дней; [95,98].
o 2 линия – цефалоспорины 1-2 г в сутки в/в 7-10
дней [99,100].
Уровень убедительности рекомендации C (уровень достоверности доказательств – 4).
Таблица 7. Сравнительная характеристика ГКС
|
Препарат |
Длительность действия (t1/2) |
Эквивалентная доза (мг) |
|
Кортизол (гидрокортизон) |
8-12 ч |
20 |
|
Преднизон |
12-36 ч |
5 |
|
Преднизолон |
12-36 ч |
5 |
|
Метилпреднизолон |
12-36 ч |
4 |
• Данной группе пациентов при клиническом ответе на ГКС через 7 дней показан перевод на пероральный прием преднизолона с последующим снижением до полной отмены по 5-10 мг преднизолона в 5-7 дней [54].
Уровень убедительности рекомендации В (уровень достоверности доказательств – 3).
Лечебная тактика при отсутствии эффекта от терапии ГКС при тяжелой атаке описана в п. 3.1.7.
3.1.7 Сверхтяжелый язвенный колит любой протяженности.
В такой форме может протекать как первая атака ЯК, так и любое из последующих обострений (характеристику см. в разделе «классификация ЯК»). Больной должен быть госпитализирован в многопрофильный (специализированный) стационар с последующим обязательным наблюдением специалистомгастроэнтерологом и специалистом-колопроктологом (хирургом).
• Пациентам при сверхтяжелой атаке ЯК рекомендовано назначение в/в ГКС в дозе, эквивалентной преднизолону 2 мг/кг массы тела.
Комментарий. Эффект оценивается не позднее 7 суток после начала терапии с обязательным осмотром специалистом-гастроэнтерологом и специалистом-колопроктологом и оценкой лабораторных параметров на 3 и 5 сутки. Переход с в/в на пероральный прием ГКС осуществляется так же, как при тяжелой атаке, при необходимости в/в гормональная терапия может быть пролонгирована до достижения стабильной положительной динамики, но не более 14 дней. Можно добавить местное введение гормональных препаратов (гидрокортизонаацетата с лидокаином, преднизолон в микроклизмах).
• Данной группе пациентов при наличии гормональной резистентности продолжение гормональной монотерапии или увеличение дозы ГКС не рекомендовано [69].
Уровень убедительности рекомендации В (уровень достоверности доказательств – 2).
• Если нет непосредственной угрозы жизни больного или развития тяжелых осложнений, требующих немедленного оперативного вмешательства, данной группе пациентов рекомендовано назначение терапии «второй линии» (в англоязычной литературе
«терапии спасения»), которая включает следующие варианты лечения:
• Инфликсимаб 5 мг/кг (введения в рамках индукционного курса на 0, 2 и 6 неделе) [101,102].
Уровень убедительности рекомендации А (уровень достоверности доказательств – 1).
• Циклоспорин А (лучше в/в) 2-4 мг/кг в течение 7 дней с мониторированием показателей функции почек [103,104].
Уровень убедительности рекомендации А (уровень достоверности доказательств – 1).
Комментарий. Другие анти-ФНО-препараты и ведолизумаб в качестве «терапии спасения» не используются. Применение тофацитиниба возможно, однако в настоящий момент данные ограничены.
• Данной группе пациентов при отсутствии ответа на 2-ю инфузию инфликсимаба или 7-дневной терапии циклоспорином А рекомендовано рассмотреть варианты хирургического лечения [105].
Уровень убедительности рекомендации C (уровень достоверности доказательств – 4).
• Данной группе пациентов при ответе на индукционный курс инфликсимаба дальнейшая поддерживающая терапия проводится каждые 8 недель в течение не менее чем 2 лет в комбинации с АЗА 2 мг/кг (или МП 1,5 мг/кг) или без него [83,106,107].
Уровень убедительности рекомендации А (уровень достоверности доказательств – 1).
• Данной группе пациентов при невозможности длительного назначения инфликсимаба поддерживающую терапию рекомендовано проводить АЗА в дозе
2 мг/кг не менее 2 лет. Системные ГКС отменяются по схеме снижения [75,76].
Уровень убедительности рекомендации C (уровень достоверности доказательств – 4).
• Данной группе пациентов при положительном ответе на в/в циклоспорин А через 7 дней рекомендовано перейти на пероральный прием препарата в дозе 2 мг/кг веса с дополнительным назначением АЗА 2 мг/кг (на фоне терапевтической дозы стероидов) с постепенной отменой стероидов в течение 12 недель до момента достижения терапевтической концентрации и начала действия АЗА. При достижении ремиссии можно отменять пероральный циклоспорин, оставив больного на поддерживающей терапии АЗА не менее 2 лет [75,76,108,109].
Уровень убедительности рекомендации В (уровень достоверности доказательств – 2).
• В случае выявления у пациента в биоптате из пораженного участка слизистой толстой кишки ДНК цитомегаловируса методом полимеразной цепной реакции пациенту показана терапия ганцикловиром в дозе 5 мг/кг 2 раза в сутки в течение 14-21 дня [20,60].
Уровень убедительности рекомендации C (уровень достоверности доказательств – 4).
3.1.8 Прогнозирование эффективности консервативной терапии при сверхтяжелой атаке ЯК. Совместное наблюдение пациента гастроэнтерологом и колопроктологом необходимо для оптимального контроля за течением заболевания. Хотя медикаментозная терапия во многих случаях оказывается эффективной, имеются данные, указывающие, что задержка в проведении необходимого оперативного лечения пагубно сказывается на исходе лечения больного, в частности, увеличивая риск операционных осложнений [110]. Большинство исследований предикторов колэктомии проведены до широкого применения биологической терапии и циклоспорина и позволяют прогнозировать неэффективность ГКС, а не инфликсимаба и иммуносупрессоров:
– Частота стула >12 раз/сутки на 2 сутки в/в гормональной терапии повышает риск колэктомии до 55% [111];
– Если на 3 день гормональной терапии частота стула превышает 8 раз/сутки или составляет от 3 до 8 раз/сутки и при этом уровень СРБ превышает 45 мг/л, вероятность колэктомии составляет 85% (т.н. «Оксфордский индекс») [112];
– На 3 день также можно определить «Шведский индекс» по формуле: частота стула ´ 0,14 ´ уровень СРБ. Его значение 8 и более повышает вероятность колэктомии до 75% [113];
– Риск колэктомии также повышается в 5-9 раз при наличии гипоальбуминемии и лихорадки при поступлении, а также при отсутствии более чем 40% уменьшения частоты стула за 5 дней в/в гормональной терапии [114];
– Наличие глубоких изъязвлений толстой кишки (на фоне которых остаточная слизистая оболочка определяется только в виде «островков») повышает риск колэктомии до 86-93% [115,116].
Эффективность инфликсимаба при гормональной резистентности по разным данным колеблется от 25% до 80%, что может объясняться различиями в эффективности препарата у отдельных пациентов. Исследования, посвященные прогнозированию эффективности биологической терапии, остаются ограниченными, однако, установлено:
– эффективность инфликсимаба при гормонорезистентной тяжелой атаке ЯК уменьшается с возрастом [117], при наличии тотального поражения толстой кишки [118], а также при выраженной гипоальбуминемии [119], уровне гемоглобина менее 95 г/л и уровне С-реактивный белок более 10 мг/л на момент первого введения инфликсимаба [120];
– эффективность инфликсимаба существенно ниже у пациентов, у которых показания к антицитокиновой терапии возникли уже при первой атаке ЯК;
– наличие обширных язвенных дефектов слизистой оболочки («островков слизистой оболочки») толстой кишки при колоноскопии до начала терапии инфликсимабом с 80% точностью прогнозирует ее дальнейшую неэффективность [105], повышая риск колэктомии в 2,38-5,13 раз [121,122].
У пациентов с высоким риском колэктомии следует принимать индивидуальное решение о проведении терапии «второй линии» при помощи циклоспорина или инфликсимаба или о хирургическом лечении непосредственно после неэффективного курса в/в ГКС.
3.2 Хирургическое лечение
3.2.1 Показания к хирургическому лечению ЯК: Неэффективность или невозможность продолжения консервативной терапии.
Показаниями к хирургическому лечению ЯК служат неэффективность консервативной терапии (гормональная резистентность, неэффективность биологической терапии) или невозможность ее продолжения (гормональная зависимость, непереносимость или противопоказания для проведения консервативной терапии), кишечные осложнения ЯК (токсическая дилатация, перфорация кишки, кишечное кровотечение), а также рак толстой кишки или высокий риск его возникновения.
О неэффективности консервативной терапии свидетельствуют (см. раздел 1.5):
• гормональная резистентность;
• гормональная зависимость.
Гормональную зависимость удается эффективно преодолеть при помощи биологических препаратов и/или иммуносупрессоров (АЗА, МП) в 40-55% случаев [65,109], а при гормональной резистентности назначение циклоспорина А или биологической терапии позволяет индуцировать ремиссию в 43-80% случаев [123]. Однако, у части больных с высоким риском осложнений и неэффективностью консервативной терапии при развитии гормональной резистентности или зависимости возможно проведение хирургического лечения без попытки применения биологических препаратов или иммуносупрессоров.
3.2.2 Показания к хирургическому лечению ЯК: Кишечные осложнения ЯК.
• У всех пациентов с осложнением ЯК в виде кишечного кровотечения показана экстренная операция в объеме субтотальной колэктомии или тотальной колэктомии (колпроктэктомии – при выраженной активности в прямой кишке) [112].
Уровень убедительности рекомендации C (уровень достоверности доказательств – 4).
• У всех пациентов с осложнением ЯК в виде токсической дилатации на фоне адекватной интенсивной терапии показана экстренная операция в объеме субтотальной колэктомии или тотальной колэктомии (колпроктэктомии – при выраженной активности в прямой кишке) [111,124].
Уровень убедительности рекомендации C (уровень достоверности доказательств – 4).
Комментарий. Токсическая дилатация ободочной кишки (токсический мегаколон), представляет собой не связанное с обструкцией расширение ободочной кишки до 6 см и более с явлениями интоксикации. К факторам риска токсической дилатации относятся гипокалиемия, гипомагниемия, подготовка кишки к колоноскопии при помощи осмотических слабительных и прием антидиарейных препаратов. Косвенно о развитии токсической дилатации свидетельствует внезапное сокращение частоты стула на фоне имевшейся диареи, вздутие живота, а также внезапное уменьшение или исчезновение болевого синдрома и нарастание симптомов интоксикации (нарастание тахикардии, снижение АД).
• У всех пациентов с осложнением ЯК в виде перфорации толстой кишки при выявлении угрожающих симптомов (перитонеальные симптомы, свободный газ в брюшной полости по данным обзорной R-графии) показана субтотальная колэктомия или тотальная колэктомия (колпроктэктомия – при выраженной активности в прямой кишке) [111].
Уровень убедительности рекомендации C (уровень достоверности доказательств – 4).
Комментарий. Перфорация толстой кишки является наиболее опасным осложнением ЯК с почти 50% смертностью.
3.2.3 Показания к хирургическому лечению ЯК: Колоректальный рак. Рекомендации по скринингу. У больных с длительным анамнезом ЯК существенно повышен риск колоректального рака, что обусловливает необходимость регулярного обследования для выявления дисплазии эпителия толстой кишки. На вероятность развития рака влияют следующие факторы:
а) длительность анамнеза ЯК: риск колоректального рака составляет 2% при 10-летнем, 8% – при 20-летнем и 18% – при 30-летнем анамнезе [125]; б) начало заболевания в детском и подростковом возрасте, хотя этот фактор может лишь отражать длительность анамнеза и не являться независимым предиктором колоректального рака [126]; в) протяженность поражения: риск наиболее повышен у пациентов с тотальным ЯК, в то время как у пациентов с проктитом риск не отличается от среднего в популяции;
г) наличие первичного склерозирующего холангита [127];
д) семейный анамнез колоректального рака;
е) тяжелые обострения ЯК в анамнезе или непрерывное течение ЯК. Последствием высокой активности ЯК может являться воспалительный полипоз, также являющийся фактором риска развития колоректального рака [128].
Контрольная колоноскопия должна проводиться в условиях хорошей подготовки кишки и, желательно, в период ремиссии, поскольку активное воспаление затрудняет выявление дисплазии.
Для скрининга неопластических изменений слизистой оболочки используются два подхода:
1. Хромоэндоскопия с прицельной биопсией участков, подозрительных на неоплазию.
2. Биопсия слизистой оболочки по 4 фрагмента из каждых 10 см ободочной и прямой кишки (при эндоскопии в белом свете). Такой подход не исключает обязательной биопсии всех подозрительных образований. Результаты скриниговой биопсии влияют на тактику дальнейшего лечения и наблюдения.
• Всем пациентам с ЯК при обнаружение дисплазии высокой степени при биопсии в неизмененной слизистой оболочке (т.е. не в приподнятых образованиях), рекомендовано хирургическое лечение в объеме тотальной колэктомии (колпроктэктомия с формированием постоянной концевой илеостомы) или тотальной колэктомии с формированием резервуара (колпроктэктомия с одномоментным формированием тонкокишечного резервуара под прикрытием петлевой илеостомы) [125].
Уровень убедительности рекомендации В (уровень достоверности доказательств – 2).
Комментарий. Наличие дисплазии должно быть подтверждено вторым независимым патоморфологом. Объем хирургического лечения обсуждается совместно с пациентом, тем самым учитывается желание пациента в отношении сохранения анальной дефекации или формирования постоянной илеостомы.
• У всех пациентов с ЯК обнаружение дисплазии легкой степени в неизмененной слизистой оболочке (не в приподнятых образованиях) решение следует принимать индивидуально совместно с больным: необходимо обсудить два варианта – тотальная колэктомия (колпроктэктомия) с формированием постоянной концевой илеостомы и формированием резервуара (колпроктэктомия с одномоментным формированием тонкокишечного резервуара под прикрытием петлевой илеостомы), но приемлемым может быть продолжение регулярного эндоскопического скрининга с сокращением интервала между исследованиями до 3 месяцев [125].
Уровень убедительности рекомендации В (уровень достоверности доказательств – 2).
Комментарий. Объем хирургического лечения обсуждается совместно с пациентом, тем самым учитывается желание пациента в отношении сохранения анальной дефекации или формирования постоянной илеостомы. Пациент вправе воздержаться от оперативного лечения, в таком случае предлагается эндоскопический скрининг.
• Всем пациентам с ремиссией ЯК, при подтверждении наличия аденоматозного полипа (эндоскопически и по результатам патоморфологического исследования), рекомендовано выполнение стандартной полипэктомии [127].
Уровень убедительности рекомендации В (уровень достоверности доказательств – 2).
• Всем пациентам с ЯК при наличии полипа с дисплазией в участке толстой кишки, пораженной ЯК, не рекомендована колэктомия, если гистологическое строение полипа соответствует аденоме и признаки дисплазии отсутствуют в окружающей неизменной слизистой оболочке или где-либо в кишке, а также в краях удаленного полипа [127].
Уровень убедительности рекомендации В (уровень достоверности рекомендации – 2).
3.2.4 Виды хирургических вмешательств.
У большинства больных ЯК современная консервативная терапия позволяет контролировать течение воспалительного процесса, однако у 10-30% больных, в связи с неэффективностью медикаментозного лечения, приходится прибегать к хирургическому вмешательству, направленному на удаление толстой кишки [112]. До начала 1980-х годов стан-
Таблица 8. Методы хирургического лечения ЯК
|
С формированием постоянной илеостомы |
С восстановлением дефекации через задний проход | ||
|
1. Колэктомия с резекцией прямой кишки и формированием постоянной концевой илеостомы |
С формированием ИАРА, в 2 этапа: |
С формированием ИАРА, в 3 этапа: |
* Субтотальная резекция ободочной кишки с формированием илеоректального анастомоза (в исключительных случаях) |
|
• Колэктомия с резекцией прямой кишки, формирование ИАРА, петлевая илеостомия • Закрытие петлевой илеостомы |
1. Субтотальная резекция ободочной кишки (субтотальная колэктомия), концевая илеостомия; 2. Проктэктомия, формирование ИАРА, петлевая илеостомия; 3. Закрытие петлевой илеостомы | ||
дартом хирургического лечения являлась колпроктэктомия с концевой илеостомией, несмотря на эпизодическое формирование илеоректального анастомоза. За последние 20 лет новым золотым стандартом стала восстановительно-пластическая операция – тотальная колэктомия с формированием резервуара (колпроктэктомия с илеоанальным резервуарным анастомозом (ИАРА)) [129,130] (Табл. 8). При успешном выполнении данная операция обеспечивает возможность контролируемой дефекации через задний проход с удовлетворительным качеством жизни [131]: средняя частота дефекации после формирования ИАРА составляет от 4 до 8 раз в сутки [132-134], а суточный объем полуоформленного/ жидкого стула составляет около 700 мл в сутки (в сравнении с 200 мл/сутки у здорового человека).
3.2.5 Выбор вида хирургического лечения. Проведение реконструктивно-пластической операции с формированием ИАРА, несмотря на очевидную привлекательность для пациента, возможно не во всех случаях, поскольку ряд факторов ухудшают функциональный исход операции и увеличивают риск осложнений, приводя к необходимости удаления резервуара у 3,5-10% больных [135-137].
У больных ЯК, несмотря на более высокую частоту сопутствующих заболеваний после 65 лет, само хирургическое вмешательство с формированием тонкокишечного резервуара у лиц старших возрастных групп безопасно и эффективно [138].
Функция анального держания, играющая ключевую роль для нормального функционирования ИАРА, очевидно, ухудшается в старших возрастных группах [139]. Кроме того, у пожилых пациентов чаще развиваются осложнения, в частности резервуарит и стриктуры анастомоза [140,141]. В то же время, какой-либо определенный возрастной порог для отказа от формирования ИАРА не определен.
Формирование тонкокишечного резервуара (ИАРА) на 30-70% [142-146] повышает риск бесплодия у женщин детородного возраста с ЯК.
Риск бесплодия связан со спаечным процессом, вовлекающим маточные трубы. Планируемая беременность и молодой возраст женщины не являются противопоказаниями к формированию ИАРА, однако,
пациентка должна быть предупреждена о потенциальном риске бесплодия. В отдельных случаях возможно рассмотреть вопрос о формировании илеоректального анастомоза в качестве промежуточного этапа хирургического лечения (см.ниже).
У всех пациенток с ЯК, при возникновении показаний к операции, использование лапароскопических технологий снижает риск развития бесплодия на 90% [142-146].
У приблизительно 10% пациентов с колитом даже при изучении операционного материала, полученного при колэктомии, не удается провести дифференциальный диагноз между БК и ЯК, в связи с чем им выставляется диагноз неуточненного язвенного колита. Решение о формировании ИАРА в таких случаях принимается индивидуально, при этом пациент должен быть предупрежден о рисках неэффективности реконструктивно-пластической операции и иных осложнениях, связанных с БК.
• Всем пациентам с ЯК при наличии таких сопутствующих заболеваний, как рак прямой кишки и выраженное анальное недержание (2 или 3 степень) не рекомендовано формирование тонкокишечного резервуара (ИАРА) [147].
Уровень убедительности рекомендации В (уровень достоверности доказательств – 3).
• У пациентов с тяжелой атакой ЯК, не ответивших на консервативное лечение, рекомендовано трехэтапное хирургическое лечение (с колэктомией на первом этапе, формированием тонкокишечного резервуара и петлевой илеостомы – на втором и закрытие петлевой илеостомы – на третьем этапе) [148-150].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 4).
• У пациентов с ЯК, у которых к моменту выставления показаний к операции, была проведена гормональная терапия преднизолоном в дозе не менее 20 мг в сутки в течение более чем 6 недель, рекомендовано трехэтапное хирургическое лечение (с колэктомией на первом этапе, формированием тонкокишечного резервуара и петлевой илеостомы – на втором и закрытие петлевой илеостомы – на третьем этапе) [148-150]. Уровень убедительности рекомендации С (уровень достоверности доказательств – 4).
Комментарий. Колэктомия с концевой илеостомией купирует интоксикацию, обусловленную колитом, что позволяет улучшить общее состояние больного, восстановить метаболизм, а изучение операционного препарата также позволяет уточнить диагноз и исключить БК. Колэктомия является относительно безопасным вмешательством даже у пациентов в критическом состоянии [148-150], при этом, при достаточной квалификации хирурга безопасным является также выполнение минимально инвазивных или лапароскопических операций [151,152].
Илеоректальный анастомоз [153-155]. Формирование илеоректального анастомоза не приводит к излечению пациента и не исключает возможность рецидива воспаления в прямой кишке и развития рака. Данная операция при ЯК может выполняться только в исключительных случаях у женщин, планирующих беременность. Обязательным условием является наличие ремиссии в прямой кишке и согласие пациентки на регулярное обследование прямой кишки с биопсией слизистой оболочки [156,147].
3.2.6 Особенности хирургического вмешательства при формировании тонкокишечного резервуара (ИАРА).
• Пациентам с ЯК, которым выполнена колэктомия, реконструктивно-пластические операции с формированием тонкокишечного резервуара (ИАРА) рекомендовано выполнять в специализированных стационарах, поскольку частота осложнений и функциональный исход таких операций существенно зависит от квалификации хирурга (в частности, от числа проведенных аналогичных вмешательств) [147].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 4).
Длина сохраняемой прямой и/или сигмовидной кишки.
• Всем пациентам с ЯК, перенесшим колэктомию по срочным показаниям при язвенном колите, которым планируется формирование тонкокишечного резервуара (ИАРА) в дальнейшем, рекомендовано сохранить всю прямую кишку и нижние брыжеечные сосуды [147].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 4).
Комментарий. Прямую кишку целесообразно пересечь на уровне мыса крестца (т.е. на уровне «ректосигмоидного перехода») или дополнительно сохранить дистальный отдел сигмовидной кишки (решение принимается оперирующим хирургом). При сохранении дистального отдела сигмовидной кишки, она выводится на переднюю брюшную стенку в виде концевой сигмостомы. Последний вариант является наиболее безопасным, поскольку при этом в брюшной полости не остается культи кишки. При пересечении прямой кишки на уровне мыса в течение нескольких дней рекомендуется дренирование культи через задний проход для профилактики несостоятельности швов в связи с накоплением в культе слизи.
В случае сохранения отключённой прямой или прямой и сигмовидной кишки, возможно развитие вторичных воспалительных изменений слизистой оболочки по типу колита отключенной кишки. Контролируемые испытания лекарственных средств у больных после колэктомии не проводились. Эмпирическое лечение заключается в применении местного месалазина [157], преднизолона, промывании отключенной прямой кишки растворами антисептиков.
Наложение анастомоза при формировании ИАРА
• Всем пациентам с ЯК, которым планируется хирургическое лечение с формированием тонкокишечного резервуара (ИАРА), рекомендовано сохранять слизистую оболочку между зубчатой линией и анастомозом не более 2 см длиной [158].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 4).
Комментарий. Сохранение протяженного участка прямой кишки (более 2 см над зубчатой линией) при использовании сшивающего аппарата для формирования ИАРА может быть причиной хронического воспаления в ней с дисфункцией резервуара, а также способствует сохранению риска дисплазии и (очень редко) рака [158]. При невозможности сформировать анастомоз при помощи сшивающего аппарата следует выполнить брюшно-анальную резекцию прямой кишки и наложить ручной илеоанальный анастомоз.
У пациентов ЯК, перенесших хирургическое лечение с формированием тонкокишечного резервуара (ИАРА), несмотря на то, что при использовании сшивающего аппарата сохраняется небольшой фрагмент слизистой оболочки, риск рака невысок и соответствует таковому при формировании ручного анастомоза [158].
• Всем пациентам с ЯК формирование тонкокишечного резервуара (ИАРА) проводить под прикрытием петлевой илеостомы [158].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 4).
Наблюдение пациентов с ИАРА.
Морфологические изменения эпителиальной выстилки резервуара обычно развиваются через 1218 месяцев после закрытия илеостомы и характеризуются уплощением и сокращением числа ворсинок, приводящими к их атрофии («толстокишечная метаплазия») [159,160], что потенциально связано с риском развития злокачественной трансформации слизистой оболочки резервуара. Кроме того, при наложении аппаратного ИАРА сохраняется небольшой
участок слизистой оболочки прямой кишки («манжетка»). Риск развития рака резервуара повышен у пациентов, оперированных по поводу рака или дисплазии на фоне ЯК (и при обнаружении дисплазии в операционном материале), а также у больных первичным склерозирующим холангитом (ПСХ). Научное обоснование частоты контрольных обследований больных с ИАРА не выполнялось, однако, у пациентов с наличием вышеуказанных факторов риска целесообразно проведение контрольных эндоскопических исследований (резервуароскопии) с биопсией слизистой оболочки не реже одного раза в 2 года.
3.2.7 Медикаментозная терапия в период хирургического лечения.
Влияние лекарственной терапии на риск хирургических вмешательств.
Прием преднизолона в дозе более 20 мг в течение более чем 6 недель увеличивает частоту хирургических осложнений [161,162]. Предоперационный прием АЗА и МП не ухудшает исход хирургического лечения [163], в то время как введение инфликсимаба и циклоспорина незадолго до операции может увеличивать частоту послеоперационных осложнений [164,165], хотя данные по инфликсимабу остаются противоречивыми [166].
Гормональная терапия перед операцией и в раннем послеоперационном периоде.
Резкое прекращение терапии ГКС может вызвать синдром отмены (острую недостаточность коры надпочечников, т.н. Аддисонический криз), что обусловливает необходимость временного продолжения гормональной терапии после операции до полной отмены.
На настоящий момент отсутствует надежная научная база для обоснования какой-либо схемы прекращения гормональной терапии после колэктомии по поводу ЯК. Доза ГКС для дальнейшего перорального приема в период отмены гормональной терапии определяется длительностью предшествовавшей терапии и величиной использованных доз. Согласно рекомендациям Европейского общества по изучения ЯК и БК (ECCO) [20], в случае, если гормональная терапия перед операцией проводилась не более месяца, сразу после операции возможно прекращение приема ГКС.
Если перед операцией пациент более месяца получал ГКС, после хирургического вмешательства целесообразно перейти с вышеописанной высокой парентеральной дозы ГКС на пероральный прием ГКС внутрь в дозе не ниже верхней границы суточной стрессовой продукции кортизола, то есть не ниже
20 мг преднизолона. Дальнейшее снижение дозы и отмена ГКС проводится под наблюдением врачаэндокринолога.
3.2.8 Резервуарит и другие осложнения хирургического лечения при формировании тонкокишечного резервуара.
Резервуарит представляет собой неспецифическое воспаление тонкокишечного резервуара и наиболее частое осложнение ИАРА. Частота его возникновения колеблется в широком диапазоне от 15 до 50% в течение 10 лет после формирования ИАРА в крупных специализированных центрах [167-169]. Такие различия могут быть обусловлены существенно большим риском резервуарита при ЯК, превышающим частоту этого осложнения при формировании ИАРА по поводу других заболеваний (в частности, семейного аденоматоза толстой кишки) [170,171].
Осложнения резервуарита включают абсцессы, свищи, стеноз резервуаро-анального анастомоза и аденокарциному резервуара. Последнее осложнение встречается исключительно редко и почти всегда – при выявленной дисплазии или раке в операционном препарате, полученном при выполнении колэктомии. Дифференциальный диагноз при подозрении на резервуарит проводится с синдромом раздраженного резервуара (СРР), ишемическими поражениями, БК и другими редкими причинами дисфункции резервуара, такими как коллагенозный, цитомегаловирусный и Clostridium difficile-ассоциированный резервуарит. Следует учитывать возможность развития неспецифического илеита, вызываемого приемом НПВС и синдрома избыточного бактериального роста.
Лечение резервуарита и поддержание ремиссии. Основными препаратами, применяемыми для лечения резервуарита, остаются антибиотики, что позволяет классифицировать резервуарит как антибиотикочувствительный, антибиотикозависимый и антибиотикорезистентный.
• У всех пациентов с резервуаритом первая линия терапии включает 14-дневный курс перорального метронидазола (15-20 мг/кг/сутки) или ципрофлоксацина (1000 мг/сут.) [172].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 3).
Комментарий. Нежелательные явления значительно чаще отмечаются при приеме метронидазола. В случаях антибиотико-резистентного резервуарита возможно назначение перорального будесонида (9 мг) в течение 8 недель.
• У пациентов с резервуаритом при отсутствии эффекта или при развитии зависимости от приема указанных препаратов рекомендовано назначение резервных препаратов – рифаксимина (2000 мг/сут.), тинидазола, ректальных ГКС, ректальных препаратов месалазина, азатиоприна [172].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 3).
Воспаление слизистой оболочки сохраненного участка прямой кишки и синдром раздраженного резервуара.
Другим потенциальным осложнением ИАРА является воспаление слизистой оболочки прямой кишки, сохраняемой при наложении аппаратного анастомоза.
• У пациентов с проктитом после формирования тонкокишечного резервуара, лечение проводится свечами месалазина 500 мг 2 раза в сутки и/или ректальными ГКС [172].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 3).
Синдром раздраженного резервуара [173] представляет собой функциональное расстройство, симптомы которого совпадают с проявлениями резервуарита. Синдром раздраженного резервуара чаще встречается у пациентов, принимавших анксиолитики или антидепрессанты до колэктомии, что косвенно свидетельствует о проявлениях у таких пациентов синдрома раздраженного кишечника до операции. Методы лечения этих двух функциональных расстройств совпадают и включают психотерапевтическую помощь и назначение антидепрессантов, назначение пищевых волокон, противодиарейных препаратов, спазмолитиков, а также неабсорбируемых антибиотиков для коррекции синдрома избыточного бактериального роста.
3.2.9. Дисфункция илеостомы после хирургического лечения ЯК.
Под дисфункцией илеостомы понимается увеличение объема кишечного отделяемого по илеостоме более 1000 мл в сутки. Данное состояние также сопровождается быстро прогрессирующими метаболическими и водно-электролитными нарушениями [174]. Необходимо проводить общий физикальный осмотр больного с оценкой общего состояния, контроль общего анализа крови, биохимического анализа крови, гемокоагулограммы, общего анализа мочи, оценка местного статуса. Определяется характер нарушения функции пищеварения.
• Пациентам с дисфункцией илеостомы первоначально на амбулаторном этапе рекомендовано исключить энтерит, вызванный Clostridium difficile [174]. Уровень убедительности рекомендации B (уровень достоверности доказательств – 3). Комментарий. Помимо обильного жидкого отделяемого по стоме, в клинической картине также отмечается повышение температуры тела до 39 °С, метеоризм, редко жалобы на тошноту, рвоту, боли в животе спастического характера. При лабораторных исследованиях: анемия, гипопротеинемия, гипоальбуминемия, гипокалиемия, повышение уровня СРБ, редко увеличение концентрации креатинина.
• Пациентам с дисфункцией илеостомы для проведения экспресс-диагностики энтерита вызванного Clostridium difficile в микробиологической лаборатории рекомендовано [174,175]:
1. Определения глутаматдегидрогеназы (ГДГ) и токсинов А и В в просветных фекалиях: метод иммунохроматографического анализа (ИХА);
2. Диагностические тест-наборы для определения антигенов С.difficile: ГДГ, токсинов А и В – метод ИФА;
3. Диагностические тест-наборы для определения антигенов С.difficile: ГДГ, токсинов А и В – иммунохемилюминесцентный анализ;
4. Тесты для выявления ГДГ, токсинов А и В, бинарного токсина – ПЦР, в том числе, мультиплексная. Уровень убедительности рекомендации А (уровень достоверности доказательств – 1b).
• Пациентам с лёгкой формой заболевания рекомендована диетотерапия, спазмолитики и препараты замедляющие пассаж по ЖКТ [175].
Уровень убедительности рекомендации B (уровень достоверности доказательств – 2).
• Пациентам со среднетяжёлой формой заболевания назначается метронидазол в дозе 500 мг внутрь три раза в день в течение 10 дней [176].
Уровень убедительности рекомендации В (уровень достоверности доказательств – 2).
• Пациентам со среднетяжелой формой заболевания при отсутствии клинического эффекта от метронидазола через 5-7 дней производят смену препарата на ванкомицин в дозе 125 мг 4 раза в день per os в течение 10 дней [177].
Уровень убедительности рекомендации A (уровень достоверности доказательств – 1).
Комментарий. Если в лабораторных показателях отмечается увеличение уровня лейкоцитов в крови более 15 ´ 109 кл/л, креатинина в сыворотке крови выше 115 мкмоль/л, подъём температуры тела выше 38,8 °C и снижении уровня альбумина менее 25 г/л, пациенты должны получать лечение в условиях круглосуточного стационара. Этим пациентам изначально показано назначение ванкомицина в дозе 125 мг внутрь 4 раза в день в течение 10 дней.
• Пациентам с ухудшением состояния и возникновением гипотонии, задержки стула, выраженного вздутия живота, изменения сознания, повышения уровня лактата в сыворотке крови выше 2,2 ммоль/л, развития синдрома полиорганной недостаточности рекомендован перевод в отделение интенсивной терапии для дальнейшего лечения [178].
Уровень убедительности рекомендации В (уровень достоверности доказательств – 2).
Комментарий: Наряду с инфузионной терапией назначается ванкомицин внутрь в дозе 500 мг 4 раза в день в сочетании с метронидазолом в дозе 500 мг 3 раза в день внутривенно. При невозможности введения препарата через рот ванкомицин назначается ректально. При этом препарат в дозе 500 мг разводится в 500 мл 0,9% раствора хлорида натрия и вводится в виде клизм четыре раза в день.
4. РЕАБИЛИТАЦИЯ
Специфические меры реабилитации пациентов с ЯК отсутствуют. Меры медицинской реабилитации направлены на профилактику колоректального рака. Поскольку в ряде случаев терапия ЯК сопряжена с применением иммуносупрессоров, основным способом реабилитации пациентов является профилактика оппортунистических инфекций, описанная в разделе 5.
У больных, которым потребовалось хирургическое лечение язвенного колита, возможна реабилитация в три этапа.
1- й этап – ранняя реабилитация, осуществляется непосредственно после хирургического лечения со 2-х по 14-е сутки. Основной задачей 1 этапа реабилитации является восстановление нормального функционирования желудочно-кишечного тракта после хирургического вмешательства. Именно на этом этапе чаще всего выявляются и должны быть корригированы нарушения мочеиспускания. Важная роль отводится также контролю гомеостаза, мероприятиям, направленным на заживление послеоперационных ран, купированию послеоперационного болевого синдрома, активизации пациента. В данный период проводится контроль общего анализа крови, биохимического анализа крови, коагулограммы крови, общего анализа мочи.
2- й этап реабилитации начинается после 15 суток и продолжается по мере необходимости в последующем. Направлен на окончательное заживление послеоперационных ран с контролем за деятельностью желудочно-кишечного тракта и других систем организма. Данный этап возможно осуществлять как амбулаторно, так и в условиях стационара дневного или круглосуточного пребывания.
3- й этап реабилитации осуществляется в поздний реабилитационный период у пациентов как с постоянной илеостомой, так и перед реконструктивновосстановительной операцией. Основной задачей на данном этапе является компенсация функции желудочно-кишечного тракта, мероприятия направленные на выявление и коррекцию функции запирательного аппарата прямой кишки.
Недостаточность анального сфинктера – реабилитация возможна на 2 и 3 этапах.
У ряда пациентов, у которых оперативное вмешательство по поводу ЯК завершилось формированием тонкокишечного резервуара, отмечается снижение функции держания.
• Пациентам с ЯК с недостаточностью анального сфинктера перед реконструктивно-восстановительным лечением рекомендовано выполнение патофизиологического исследования (сфинктерометрия, профилометрия, исследование проводимости по срамному нерву) с последующей консультаций физиотерапевта [179].
Уровень убедительности рекомендации В (уровень достоверности доказательств – 2).
• Пациентам с ЯК при выявлении недостаточности анального сфинктера 2-3 степени необходимо провести реабилитационное лечение, включающее 10-дневный цикл БОС-терапии и тибиальной нейромодуляции в условиях дневного или круглосуточного стационара [179,180].
Уровень убедительности рекомендации В (уровень достоверности доказательств – 2).
Комментарий. В реабилитации больных с недостаточностью анального сфинктера, по данным литературы, широкое применение имеет метод лечения биологической обратной связью (БОС), направленный на улучшение сократительной способности мышц наружного сфинктера и тазового дна за счет увеличения как силы, так и длительности произвольного сжатия [179,180]. Данный неинвазивный метод вовлекает в процесс реабилитации собственные ресурсы организма с выработкой правильных навыков на уровне создания новых условно-рефлекторных связей. Так же эффективным является метод тибиальной нейромодуляции. Нейромодуляция – это процесс, при котором электрический ток по одним нервным путям модулирует существовавшую ранее активность в других нервных путях или центрах. Чрескожная электростимуляция заднего большеберцового нерва применяется при функциональных заболеваниях органов малого таза, так как в составе заднего большеберцового нерва проходят волокна из II и III крестцовых сегментов спинного мозга, играющие значительную роль в иннервации прямой кишки, мочевого пузыря и их сфинктеров. Доказано, что мышечные структуры отключенного запирательного аппарата могут реагировать на терапию биологической обратной связью и проведение тибиальной нейромодуляции, увеличивая как тонус, так и силу волевых сокращений [179,180]. Стимуляцию тибиального нерва проводят с помощью накожного стимулирующего электрода, что позволяет пациенту после курса предварительного обучения продолжить курс лечения самостоятельно в домашних условиях. В таком случае курс лечения с ежедневными сеансами стимуляции может продлеваться до 1-3 месяцев. Контроль эффективности БОС-терапии производится перед началом и по окончании каждого курса процедур путем комплексного физиологического исследования функции запирательного аппарата пря-
мой кишки (сфинктерометрия + физиологическое исследование резервуарной функции низведенной кишки). При улучшении показателей тонуса и сократительной способности анальных сфинктеров, можно ставить вопрос о выполнении реконструктивно-восстановительной операции, направленной на возобновление естественного пассажа по желудочно-кишечному тракту.
5. ПРОФИЛАКТИКА
И ДИСПАНСЕРНОЕ НАБЛЮДЕНИЕ
Язвенный колит характеризуется хроническим рецидивирующим течением. Диспансерное наблюдение при ЯК проводится пожизненно и может быть прервано только при удалении толстой кишки. Целью диспансерного наблюдения является, в первую очередь, профилактика колоректального рака. У большинства пациентов в стадии клинической ремиссии колоноскопия должна выполняться не реже, чем каждые 3 года. У части пациентов периодичность диспансерного наблюдения с проведением колоноскопии может быть иной. К особенностям наблюдения за пациентами, получающими иммуносупрессоры и/или биологические препараты, относится профилактика оппортунистических инфекции. К факторам риска развития оппортунистических инфекций относят: прием преднизолона 20 мг в сутки и более в течение 2 недель, прием иммуносупрессоров (азатиоприна, 6-меркаптопурина, метотрексата) и биологических препаратов, возраст старше 50 лет, сопутствующие заболевания (хронические заболевания легких, алкоголизм, органические заболевания головного мозга, сахарный диабет). В соответствие с Европейским консенсусом по профилактике, диагностике и лечению оппортунистических инфекций при ВЗК, такие пациенты подлежат обязательной вакцинопрофилактике. Необходимым минимумом вакцинопрофилактики является:
• Рекомбинантная вакцина против HBV;
• Поливалентная инактивированная пневмококковая вакцина;
• Трехвалентная инактивированная вакцина против вируса гриппа.
Для женщин до 26 лет, при отсутствии вируса на момент скрининга рекомендуется вакцинация от вируса папилломы человека.
• В период терапии ГКС рекомендован мониторинг уровня гликемии.
Уровень убедительности рекомендации B (уровень достоверности доказательств – 3).
• В период терапии иммуносупрессорами рекомендуется ежемесячный контроль уровня лейкоцитов и печёночных ферментов (в начале лечения раз в две недели, далее раз в месяц в течение первых 6 месяцев терапии, далее раз в три месяца).
• Уровень убедительности рекомендации C (уровень достоверности доказательств – 3).
• Пациентам перед проведением биологической терапии и далее каждые 6 месяцев, согласно приказу Минздрава России, обязательно рекомендуется консультация врача-фтизиатра и скрининг на туберкулез (квантифероновый тест, а при невозможности проведения – проба Манту, диаскин-тест) [181].
Уровень убедительности рекомендации A (уровень достоверности доказательств – 1b).
• Пациентам до назначения иммуносупрессивной терапии, включая ГИБП и на фоне лечения рекомендуется проводить скрининг на наличие маркеров вирусных гепатитов В (HBsAg, анти-HBc, ДНК качественным методом), С (анти-HCV) и иммунодефицита человек (анти-ВИЧ), а также сифилиса.
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5).
• Рекомендовано строгое соблюдение доз и графика введения биологических препаратов. Нерегулярное введение биологических препаратов повышает риск аллергических реакций и неэффективности лечения [20].
Уровень убедительности рекомендации B (уровень достоверности доказательств – 1b).
Комментарий: Недопустимы перерывы в лечении без медицинских показаний
• Всем пациентам, получающим биологическую терапию, не рекомендована смена оригинального препарата на биоаналог или наоборот более одного раза. Уровень убедительности рекомендации C (уровень достоверности доказательств – 5). Комментарий. В настоящее время зарегистрированы биосимиляры (биоаналоги) анти-ФНО препаратов, схожие с оригинальными биологическими лекарственными средствами по эффективности и безопасности, однако их взаимозаменяемость с оригинальными препаратами в настоящее время не доказана. С учетом отсутствия клинических испытаний у пациентов с ВЗК, доказавших безопасность и эффективность чередования или полного переключения с оригинального препарата на биоаналоги и наоборот, подобный терапевтический подход не рекомендован [57]. Больному следует разъяснить необходимость постоянного приема лекарственных препаратов, поскольку соблюдение предписаний по терапии существенно (в 2-2,5 раза) снижает частоту обострений, а сама терапия является методом химиопрофилактики колоректального рака.
С точки зрения долгосрочного прогноза течения ЯК целесообразно регулярно оценивать наличие эндоскопической ремиссии (заживления слизистой оболочки). Для этих целей рекомендуется каждые 6 месяцев выполнять исследование кала на уровень фекального кальпротектина и/или ректороманоскопию.
6. ДОПОЛНИТЕЛЬНАЯ ИНФОРМАЦИЯ, ВЛИЯЮЩАЯ НА ТЕЧЕНИЕ И ИСХОД ЗАБОЛЕВАНИЯ
Риск тяжелого обострения ЯК в течение жизни составляет 15%, при этом вероятность тяжелой атаки выше у больных с тотальным поражением толстой кишки. При проведении адекватной противорецидивной терапии в течение 5 лет обострений удается избежать у половины пациентов, а в течение 10 лет – у 20% больных. В течение первого года после постановки диагноза вероятность колэктомии составляет 4-9% (при тяжелой атаке – около 50%), в дальнейшем с каждым годом заболевания риск колэктомии увеличивается на 1%. Факторами риска агрессивного течения ЯК являются прогрессирование поражения от дистального (проктита) к тотальному, первичный склерозирующий холангит, а также детский и подростковый возраст на момент начала заболевания.
Планирование беременности необходимо осуществлять в период ремиссии ВЗК, что позволяет улучшать исходы беременности. Применение беременными большинства препаратов для лечения ВЗК сопряжено с низким риском неблагоприятного воздействия на плод, за исключением метотрексата и препаратов 5-АСК, содержащих дибутилфталат. Отмена анти-ФНО или переход на монотерапию возможны лишь у ограниченного числа пациенток с низким риском реактивации ВЗК. Лечение генно-инженерными биологическими препаратами, не противопоказанными при беременности (см. инструкцию по применению), может быть продолжено, если польза для матери превышает потенциальные риски для плода.
Уменьшение рисков, связанных с назначением ГКС, достигается строгим соблюдением принципов гормональной терапии. ГКС не могут применяться в качестве поддерживающей терапии.
При назначении гормональной терапии необходимо учитывать следующее:
• Постепенное снижение дозы стероидов до полной отмены – строго обязательно;
• Суммарная продолжительность гормональной терапии не должна превышать 12 недель;
• Обязательным является сопутствующий прием препаратов кальция, витамина D;
• В период лечение необходим регулярный контроль уровня глюкозы в крови.
Пациентам, которым в результате хирургического лечения была сформирована кишечная стома, может потребоваться консультация и наблюдение специалистом по реабилитации стомированных пациентов.
6.1. Область применения рекомендаций Клинические рекомендации предназначены врачамтерапевтам, врачам общей практики (семейным врачам), гастроэнтерологам, колопроктологам, хирургам,
эндоскопистам, организаторам здравоохранения, медицинским работникам со средним медицинским образованием, врачам-экспертам медицинских страховых организаций, в том числе при проведении медико-экономической экспертизы. Консервативное лечение может проводиться в амбулаторных условиях при участии гастроэнтеролога и/или колопроктолога. Наблюдение и лечение диагностически сложных случаев должно проводиться в специализированных центрах по диагностике и лечению воспалительных заболеваний кишечника. Стационарное лечение проводится в специализированных гастроэнтерологических и колопроктологических отделениях (в исключительных случаях – в терапевтических отделениях при наличии специализированных гастроэнтерологических коек и специалиста, имеющего профессиональную переподготовку по специальности «гастроэнтерология», и, соответственно, в хирургических отделениях при наличии специализированных колопроктологических коек и специалиста, имеющего профессиональную переподготовку по специальности «колопроктология»).
Инициация генно-инженерной терапии, а также поддерживающая генно-инженерная терапия, может быть проведена в условиях дневного стационара, в таких случаях применяется КСГ ds 36.004 «Лечение с применением генно-инженерных биологических препаратов», или круглосуточного стационара в рамках оказания высокотехнологичной медицинской помощи по профилю «гастроэнтерология», включенной в перечень видов высокотехнологичной медицинской помощи базовой программы обязательного медицинского страхования, финансовое обеспечение которых осуществляется за счет субвенции из бюджета Федерального фонда обязательного медицинского страхования бюджетам территориальных фондов обязательного медицинского страхования. В стационарных условиях при оказании специализированной медицинской помощи необходимо применение КСГ st 36.003 «Лечение с применением генно-инженерных биологических препаратов в случае отсутствия эффективности базисной терапии». Учитывая особенности кратности введения биологических препаратов, при проведении медико-экономической экспертизы и экспертизы качества медицинской помощи неприменим критерий отклонения от стандарта лечения (случай для проведения 100% экспертизы)
«Повторная госпитализация по одному заболеванию в течение 90 дней после завершения первого случая лечения (по реестрам одной медицинской организации)». Частота госпитализации определяется схемой введения конкретного биологического препарата и варьирует от 1 раза в 2 недели до 1 раза в 8 недель. Количество госпитализаций более чем 1 в течение 90 дней после завершения первого случая лечения (по реестрам одной медицинской организации) при проведении генно-инженерной терапии не может быть причиной для установления дефекта оказания медицинской помощи и подвергаться штрафным санкциям.
При хирургическом лечении в условиях круглосуточного стационара применяется КСГ st 14.003 – операции на кишечнике и анальной области (уровень 3), или, в зависимости от метода лечения и характера течения заболевания, оказывается высокотехнологичная медицинская помощь по профилю «Абдоминальная хирургия», включенной в перечень видов высокотехнологичной медицинской помощи базовой программы обязательного медицинского страхования, финансовое обеспечение которых осуществляется за счет субвенции из бюджета Федерального фонда обязательного медицинского страхования бюджетам территориальных фондов обязательного медицинского страхования.
6.2. Ограничение применения рекомендаций. Клинические рекомендации отражают мнение экспертов по основным вопросам. В клинической практике могут возникать ситуации, выходящие за рамки представленных рекомендаций, поэтому окончательное решение о тактике ведения каждого пациента должен принимать лечащий врач, на котором лежит ответственность за его лечение.
 Вам может быть интересно:
Вам может быть интересно:
- Образовательный модуль "Воспалительные заболевания кишечника" с Веселовым В.В.
- Дифференциальная диагностика НЯК и болезни Крона
- Монреальская классификация язвенного колита по протяженности поражения
- Классификация язвенного колита в зависимости от эндоскопической активности
- Гистологическая шкала активности язвенного колита (по Гебсу, 2010)
- Франкфуртская классификация ВЗК-ассоциированных новообразований (FACILE)
- Статьи: СВЯЗЬ МЕЖДУ АЦЕТАМИНОФЕНОМ И НЕСТЕРОИДНЫМИ ПРОТИВОВОСПАЛИТЕЛЬНЫМИ ПРЕПАРАТАМИ (НПВП) И РИСКОМ ОБОСТРЕНИЯ БОЛЕЗНИ КРОНА И ЯЗВЕННОГО КОЛИТА
Список литературы:
1. Travis SP, Dinesen L. Remission in trials of ulcerative colitis: what does it mean? Pract Gastroenterol. 2010;30:17-20.
2. D'Haens G, et al. A review of activity indices and efficacy end points for clinical trials of medical therapy in adults with ulcerative colitis. Gastroenterology. 2007;132:763-86.
3. Cosnes J, Gower-Rousseau C, Seksik P, Cortot A. Epidemiology and natural history of inflammatory bowel diseases. Gastroenterology. 2011;140:1785-94.
4. Белоусова Е.А., Абдулганиева Д.И., Алексеева О.П., Алексеенко С.А. и соавт. Социально-демографическая характеристика, особенности течения и варианты лечения воспалительных заболеваний кишечника в России. Результаты двух многоцентровых исследований. Альманах клинической медицины. 2018;46(5):445-463. https://doi.org/10.18786/2072-05052018-46-5-445-463.
5. Katsanos KH, Vermeire S, Christodoulou DK, Riis L et al. Dysplasia and cancer in inflammatory bowel disease 10 years after diagnosis: results of a population-based European collaborative follow-up study. Digestion. 2007;75: 113-21.
6. Silverberg MS, et al. Toward an integrated clinical, molecular and serological classification of inflammatory bowel disease: report of a working party of the 2005 Montreal World Congress of Gastroenterology. Can J Gastroenterol. 2005;19(Suppl A):5-36.
7. Truelove SC et al. Cortisone in ulcerative colitis; final report on a therapeutic trial. Br Med J. 1955;2:1041-8.
8. Seah D, De Cruz P. Review article: the practical management of acute severe ulcerative colitis. Aliment Pharmacol Ther. 2016 Feb;43(4):482-513.
9. Hindryckx P, Jairath V, D'Haens G. Acute severe ulcerative colitis: from pathophysiology to clinical management. Nat Rev Gastroenterol Hepatol. 2016 Sep 1.
10. Chen JH, Andrews JM, Kariyawasam V, Moran N. IBD Sydney Organisation and the Australian Inflammatory Bowel Diseases Consensus Working Group. Review article: acute severe ulcerative colitis – evidence-based consensus statements. Aliment Pharmacol Ther. 2016 Jul;44(2):127-44.
11. Schroeder KW, Tremaine WJ, Ilstrup DM. Coated oral 5-aminosalicylic acid therapy for mildly to moderately active ulcerative colitis. A randomized study. N Engl J Med. 1987;317:1625-9.
12. Григорьева Г.А., Мешалкина Н.Ю. О проблеме системных проявлений воспалительных заболеваний кишечника. Фарматека. 2011; № 15, с. 44-49.
13. Sands BE. From symptom to diagnosis: clinical distinctions among various forms of intestinal inflammation. Gastroenterology. 2004;126:1518-32.
14. Perler B, Ungaro R, Baird G, Malette M. et al. Presenting symptoms in inflammatory bowel disease: descriptive analysis of a community-based inceptive cohort. BMC Gastroenterol. 2019; 19:47.
15. Fine KD, Schiller LR. AGA technical review on the evaluation and management of chronic diarrhea. Gastroenterology. 1999;116:1464-86.
16. Forrest K, Symmons D, Foster P. Systematic review: is ingestion of paracetamol or non-steroidal anti-inflammatory drugs associated with exacerbations of inflammatory bowel disease? Aliment Pharmacol Ther. 2004;20:1035-43.
17. Mahid SS, Minor KS, Soto RE, et al. Smoking and inflammatory bowel disease: a meta-analysis. Mayo Clin Proc. 2006;81:1462-71.
18. Vermeire S. Review article: genetic susceptibility and application of genetic testing in clinical management of inflammatory bowel disease. Aliment Pharmacol Ther. 2006;24:2-10.
19. Carter MJ, Lobo AJ, Travis SP; IBD Section, British Society of Gastroenterology. Guidelines for the management of inflammatory bowel disease in adults. Gut. 2004;53:V1-16.
20. Dignass A, et al. Second EUROPEAN evidence-based Consensus on the diagnosis and management of ulcerative colitis: Current management, Journal of Crohn's and Colitis. 2012.
21. Travis SP, Jewell DP. Ulcerative colitis: clinical presentation and diagnosis. In: Satsangi J, Sutherland LR, editors. Inflammatory Bowel Diseases. London: Churchill Livingstone. 2003: 169-81.
22. Lucendo AJ, Arias Á, Roncero Ó, Hervías D, et al. Anemia at the time of diagnosis of inflammatory bowel disease: Prevalence and associated factors in adolescent and adult patients. Sao Paulo Med J. 2014;132(3):140-6.
23. Irwin JR, Ferguson E, Simms LA, Hanigan K, et al. Detectable Laboratory Abnormality Is Present up to 12 Months Prior to Diagnosis in Patients with Crohn's Disease. Dig Dis Sci. 2019 Feb;64(2):503-517.
24. Cherfane CE, Gessel L, Cirillo D, Zimmerman MB, Polyak S. Monocytosis and a Low Lymphocyte to Monocyte Ratio Are Effective Biomarkers of Ulcerative Colitis Disease Activity. Inflamm Bowel Dis. 2015 Aug;21(8):1769-75.
25. Feng JR, Qiu X, Wang F, Chen PF, et al. Diagnostic Value of Neutrophil-to-Lymphocyte Ratio and Platelet-to-Lymphocyte Ratio in Crohn's Disease. Gastroenterol Res Pract. 2017;2017:3526460. doi: 10.1155/2017/3526460.
26. Yoon JY, Park SJ, Hong SP, Kim TI, et al. Correlations of C-reactive protein levels and erythrocyte sedimentation rates with endoscopic activity indices in patients with ulcerative colitis. Dig Dis Sci. 2014 Apr;59(4):829-37.
27. Yamamoto-Furusho JK, Sánchez-Osorio M, Uribe M. Prevalence and factors associated with the presence of abnormal function liver tests in patients with ulcerative colitis. Ann Hepatol. 2010 Oct-Dec;9(4):397-401
28. Archampong EQ, Harris J, Clark CG. The absorption and secretion of water and electrolytes across the healthy and the diseased human colonic mucosa measured in vitro. Gut. 1972 Nov;13(11):880-6.
29. Maharshak N, Arbel Y, Gal-Oz A, Rogowski O, et al. Comparative analysis of Bayer wide-range C-reactive protein (wr-CRP) and the Dade-Behring high sensitivity C-reactive protein (hs-CRP) in patients with inflammatory bowel disease. J Dig Dis. 2008 Aug;9(3):140-3.
30. Weber P, Husemann S, Vielhaber H, Zimmer KP, Nowak-Göttl U. Coagulation and fibrinolysis in children, adolescents, and young adults with inflammatory bowel disease. J Pediatr Gastroenterol Nutr. 1999 Apr;28(4):418-22.
31. Issa M, Vikayapal A, Gracham MB et al. Impact of Clostridium difficile in inflammatory bowel disease patients. Clin Gastroenterol Hepatol. 2007; 5: 345-351.
32. Rodeman JF, Dubberke ER, Reske KA et al. Incidence of Clostridium difficile in inflammatory bowel disease. Clin Gastroenterol Hepatol. 2007; 5: 339-344.
33. Issa M, Ananthakrishnan AN, Binion DG. Clostridium difficile and inflammatory bowel disease. Inflamm Bowel Dis. 2008; 14:1432-42.
34. Nguyen GC, Kaplan GG, Harris ML et al. A national survey of the prevalence and impact of Clostridium difficile infection among hospitalized inflammatory bowel disease patients. Am J Gastroenterol. 2008; 103: 1443-50.
35. Mindenmark M, Larsson A. Rulling out IBD estimation of the possible economic effects of pre-endoscopic screening with F-calprotectin. Clin Biochem. 2012; 45: 552-5.
36. Costa F, Mumolo MG, Bellini M, Romano MR et al. Role of faecal calprotectin as non-invasive marker of intestinal inflammation. Dig Liver Dis. 2003;35:642-7.
37. Kim JJ, Simpson N, Klipfel N, Debose R, et al. Cytomegalovirus infection in patients with active inflammatory bowel disease. Dig Dis Sci. 2010 Apr;55(4):1059-65. doi: 10.1007/s10620-010-1126-4.
38. Lin WC, Chang CW, Chen MJ, Hsu TC, Wang HY. Effectiveness of sigmoidoscopy for assessing ulcerative colitis disease activity and therapeutic response. Medicine (Baltimore). 2019 May;98(21):e15748. doi: 10.1097/MD.0000000000015748.
39. Bansal J, Jenaw RK, Rao J, et al. Effectiveness of plain radiography in diagnosing hollow viscus perforation: study of 1,723 patients of perforation peritonitis. Emerg Radiol. 2012 Apr;19(2):115-9. doi: 10.1007/s10140-011-1007-y.
40. Colombel JF, Ordás I, Ullman T, Rutgeerts Petal. Agreement Between Rectosigmoidoscopy and Colonoscopy Analyses of Disease Activity and Healing in Patients With Ulcerative Colitis. Agreement Between Rectosigmoidoscopy and Colonoscopy Analyses of Disease Activity and Healing in Patients With Ulcerative Colitis. Gastroenterology. 2016 Feb; 150(2):389-95.e3. doi: 10.1053/j.gastro.2015.10.016.
41. Annese V, Daperno M, Rutter M.D., et al. European evidence based consensus for endoscopy in inflammatory bowel disease. Journal of Crohn’s and Colitis. 2013; 7(12): 982-1018.
42. Tanaka M, Saito H, Fukuda S, Sasaki Y, et al. Simple mucosal biopsy criteria differentiating among Crohn disease, ulcerative colitis, and other forms of colitis: measurement of validity. Scand J Gastroenterol. 2000 Mar;35(3):281-6.
43. Parente F, Greco S, Molteni M, et al. Role of early ultrasound in detecting inflammatory intestinal disorders and identifying their anatomical location within the bowel. Alimentary Pharmacology and Therapeutics. 2003;18:1009-1016.
44. Socaciu M, Ciobanu L, Diaconu B, Hagiu C, et al. Non-Invasive Assessment of Inflammation and Treatment Response in Patients
with Crohn's Disease and Ulcerative Colitis using ContrastEnhanced Ultrasonography Quantification. J Gastrointestin Liver Dis. 2015 Dec;24(4):457-65. doi: 10.15403/jgld.2014.1121.244.chr.
45. Pouillon L, Laurent V, Pouillon M, Bossuyt P et al. Diffusion-weighted MRI in inflammatory bowel disease. Lancet Gastroenterol Hepatol. 2018 Jun;3(6):433-443. doi: 10.1016/S24681253(18)30054-2.
46. Kılıçkesmez O, Soylu A, Yaşar N, Demirbaş T, Dolapçıoğlu C, et al. Is quantitative diffusion-weighted MRI a reliable method in the assessment of the inflammatory activity in ulcerative colitis? Diagn Interv Radiol. 2010 Dec;16(4):293-8. doi: 10.4261/1305-3825. DIR.2989-09.1.
47. Jia Y, Li C, Yang X, Dong Z, et al. CT Enterography score: a potential predictor for severity assessment of active ulcerative colitis. BMC Gastroenterol. 2018 Nov 9;18(1):173. doi: 10.1186/ s12876-018-0890-z.
48. Gashin L, Villafuerte-Galvez J, Leffler DA, et al. Utility of CT in the emergency department in patients with ulcerative colitis. Inflamm Bowel Dis. 2015 Apr;21(4):793-800. doi: 10.1097/ MIB.0000000000000321.
49. Милько В.И., Минцер О.П., Топчий Т.В., Корсуновский А.А. Клиническая оценка данных ирригоскопии при неспецифическом язвенном колите. Вест., рентгенологии и радиологии. 1983;
№ 5, с. 46-50.
50. Корнеева О.И., Ивашкин В.Т. Антибиотикоассоциированный колит: патоморфология, клиника, лечение. Российский журнал гастроэнтерологии, гепатологии, колопроктологии. 2007; т. 17.
№ 3, с. 65-71
51. Ивашкин В.Т., Шептулин А.А., Шифрин О. С., Галимова С.Ф., и соавт. Микроскопический колит: клинические формы, диагностика, лечение. Российский журнал гастроэнтерологии, гепатологии, колопроктологии. 2006; т. 16, № 6, с. 56-60.
52. Белоусова Е.А., Никитина Н.В., Цодикова О.М. Лечение язвенного колита легкого и среднетяжелого течения. Фарматека. 2013; № 2, с. 42-46.
53. Халиф И.Л. Принципы лечения язвенного колита (Рекомендации российской группы по изучению воспалительных заболеваний кишечника). Колопроктология, 2006; №2; с. 31-33.
54. Халиф И.Л. Лечебная тактика при язвенном колите. Российский журнал гастроэнтерологии, гепатологии, колопроктологии. 2006; т. 16, № 3, с. 58-62.
55. Marshall JK, Thabane M, Steinhart AH, Newman JR et al. Rectal 5-aminosalicylic acid for induction of remission in ulcerative colitis. Cochrane Database Syst Rev. 2010 [CD004115-CD004115].
56. Marshall JK, Irvine EJ. Rectal corticosteroids versus alternative treatments in ulcerative colitis: a meta-analysis. Gut. 1997;40: 775-81.
57. Lamet M. A multicenter, randomized study to evaluate the efficacy and safety of mesalamine suppositories 1 g at bedtime and 500 mg twice daily in patients with active mild-to-moderate ulcerative proctitis. Dig Dis Sci. 2011;56:513-22.
58. Safdi M, DeMicco M, Sninsky C, Banks P, et al. A double-blind comparison of oral versus rectal mesalamine versus combination therapy in the treatment of distal ulcerative colitis. Am J Gastroenterol. 1997;92:1867-71.
59. Gecse KB1, Lakatos PL. Ulcerative proctitis: an update on the pharmacotherapy and management. Expert Opin Pharmacother. 2014;15(11):1565-73.
60. Ahmed I, Kassem W, Salam Y, Furnari M, Mehta T. Outcome of Cytomegalovirus Colitis in Inflammatory Bowel Disease with Different Regimes of Ganciclovir. Middle East J DigDis. 2018 Oct;10(4):220-229. doi: 10.15171/mejdd.2018.114.
61. Sutherland L, Macdonald JK. Oral 5-aminosalicylic acid for induction of remission in ulcerative colitis. Cochrane Database Syst Rev. 2006:CD000543.
62. Regueiro M, Loftus Jr EV, Steinhart AH, Cohen RD. Medical management of left-sided ulcerative colitis and ulcerative proc-
titis: critical evaluation of therapeutic trials. Inflamm Bowel Dis. 2006;12:979-94.
63. Ford AC, Achkar J-P, Khan KJ, Kane SV, Talley NJ et al. Efficacy of 5-aminosalicylates in ulcerative colitis: systematic review and meta-analysis. Am J Gastroenterol. 2011;106:601-16.
64. Ford AC, Khan KJ, Achkar JP, et al. Efficacy of oral vs. topical, or combined oral and topical 5-aminosalicylates, in Ulcerative Colitis: systematic review and meta-analysis. The American journal of gastroenterology. 2012;107:167-76;
65. Kane SV, Bjorkman DJ. The efficacy of oral 5-ASAs in the treatment of active ulcerative colitis: a systematic review. Rev Gastroenterol Disord. 2003;3:210-8.
66. Kane SV, Bjorkman DJ. The efficacy of oral 5-ASAs in the reatment of active ulcerative colitis: a systematic review. Rev Gastroenterol Disord. 2003;3:210-8.
67. Danielsson A, Löfberg R, Persson T, Salde L, et al. A steroid enema, budesonide, lacking systemic effects for the treatment of distal ulcerative colitis or proctitis. Scand J Gastroenterol. 1992;27(1):9-12.
68. Nguyen NH, Fumery M, Dulai PS, Prokop LJ,et al. Comparative efficacy and tolerability of pharmacological agents for management of mild to moderate ulcerative colitis: a systematic review and network meta-analyses. Lancet Gastroenterol Hepatol. 2018 Nov;3(11):742-753. doi: 10.1016/S2468-1253(18)30231-0.
69. D'Haens G. Systematic review: second-generation vs. conventional corticosteroids for induction of remission in ulcerative colitis. Aliment Pharmacol Ther. 2016;44:1018-1029.
70. Sutherland L, Macdonald JK. Oral 5-aminosalicylic acid for induction of remission in ulcerative colitis. Cochrane Database Syst Rev. 2006:CD000543.
71. Feagan BG, MacDonald JK. Once daily oral mesalamine compared to conventional dosing for induction and maintenance of remission in ulcerative colitis: a systematic review and metaanalysis. Inflammatory bowel diseases. 2012;18:1785-94.
72. Lichtenstein GR. Budesonide Multi-matrix for the Treatment of Patients with Ulcerative Colitis. Dig Dis Sci. 2016 Feb;61(2):358-70.
73. Sherlock ME, MacDonald JK, Griffiths AM, Steinhart AH, Seow CH. Oral budesonide for induction of remission in ulcerative colitis. Cochrane Database Syst Rev. 2015 Oct 26;(10):CD007698.
74. Danese S, Siegel CA, Peyrin-Biroulet L. Review article: integrating budesonide-MMX into treatment algorithms for mildto-moderate ulcerative colitis. Aliment Pharmacol Ther. 2014 May;39(10):1095-103.
75. Timmer A, Patton PH, Chande N, et al. Azathioprine and 6-mercaptopurine for maintenance of remission in ulcerative colitis. Cochrane Database Syst Rev. 2016:Cd000478.
76. Gisbert JP, Linares PM, McNicholl AG, Mate J, Gomollon F. Metaanalysis: the efficacy of azathioprine and mercaptopurine in ulcerative colitis. Aliment Pharmacol Ther. 2009;30:126-37.
77. Rutgeerts P, Sandborn WJ, Feagan BG, et al. Infliximab for induction and maintenance therapy for ulcerative colitis. New England Journal of Medicine. 2005;353:2462-2476.
78. Sandborn WJ, van Assche G, Reinisch W, et al. Adalimumab induces and maintains clinical remission in patients with moderateto-severe ulcerative colitis. Gastroenterology. 2012;142:257-65 e1-3.
79. Sandborn WJ, Feagan BG, Marano C, et al. Subcutaneous golimumab induces clinical response and remission in patients with moderate-to-severe ulcerative colitis. Gastroenterology. 2014;146:8595; quiz e14-5.
80. Feagan BG, Rutgeerts P, Sands BE, et al. Vedolizumab as induction and maintenance therapy for ulcerative colitis. The New England journal of medicine. 2013;369:699-710.
81. Sandborn W SB, D'Haens GR, et al. Efficacy and safety of oral tofacitinib as induction therapy in patients with moderate to severe ulcerative colitis: results from two phase 3 randomized controlled trials. Gastroenterology. 2016:S157.
82. Panaccione R, Ghosh S, Middleton S, et al. Combination therapy with infliximab and azathioprine is superior to monotherapy with either agent in ulcerative colitis. Gastroenterology. 2014;146:392400.e3.
83. Panaccione R, Ghosh S, Middleton S, et al. Infliximab, azathioprine or infliximab + azathioprine for treatment of moderate to severe ulcerative colitis. The UC SUCCESS trial. J Crohns Colitis. 2011;5:13.
84. Yarur AJ, Rubin DT. Therapeutic Drug Monitoring of Anti-tumor Necrosis Factor Agents in Patients with Inflammatory Bowel Diseases. Inflamm Bowel Dis. 2015 Jul;21(7):1709-18.
85. Steenholdt C, Bendtzen K, Brynskov J, Ainsworth MA. Optimizing Treatment with TNF Inhibitors in Inflammatory Bowel Disease by Monitoring Drug Levels and Antidrug Antibodies. Inflamm Bowel Dis. 2016 Aug;22(8):1999-2015.
86. Sandborn WJ, C Su, Sands BE, et al. OCTAVE Induction 1, OCTAVE Induction 2, and OCTAVE Sustain Investigators. Tofacitinib as induction and maintenance therapy for ulcerative colitis. N Engl J Med. 2017;376:1723-36.
87. Reinisch W, Sandborn WJ, Rutgeerts P, et al. Long-term infliximab maintenance therapy for ulcerative colitis: the ACT-1 and -2 extension studies. Inflamm Bowel Dis. 2012;18:201-11.
88. Sandborn WJ, van Assche G, Reinisch W, et al. Adalimumab induces and maintains clinical remission in patients with moderateto-severe ulcerative colitis. Gastroenterology. 2012;142:257-65 e1-3.
89. Sandborn WJ, Feagan BG, Marano C, et al. Subcutaneous golimumab maintains clinical response in patients with moderate-tosevere ulcerative colitis. Gastroenterology. 2014;146:96-109.e1.
90. Feagan BG, Rutgeerts P, Sands BE, et al. Vedolizumab as induction and maintenance therapy for ulcerative colitis. The New England journal of medicine. 2013;369:699-710.
91. Danese S, D'Amico F, Bonovas S, Peyrin-Biroulet L. Positioning Tofacitinib in the Treatment Algorithm of Moderate to Severe Ulcerative Colitis. Inflamm Bowel Dis. 2018 Apr 25.
92. Shmidt E, Kochhar G, Hartke J, et al. Predictors and Management of Loss of Response to Vedolizumab in Inflammatory. Bowel Disease Inflamm Bowel Dis. 2018;18 [Epub ahead of print].
93. Sands BE et al. DOP026 Efficacy and safety of dose escalation to tofacitinib 10 mg BID for patients with ulcerative colitis following loss of response on tofacitinib 5 mg BID maintenance therapy: results from OCTAVE open. Journal of Crohn's and Colitis. vol. 12, Issue supplement_1, 16 January 2018, Pages S049, https://doi. org/10.1093/ecco-jcc/jjx180.063
94. Халиф И.Л., Нанаева Б.А., Головенко А.О., Головенко О.В. Отдаленные результаты консервативного лечения больных с тяжелым обострением язвенного колита. Терапевтический архив. 2015;87(2):34-38. https://doi.org/10.17116/terarkh201587234-38
95. Turner D, Walsh CM, Steinhart AH, et al. Response to corticosteroids in severe ulcerative colitis: a systematic review of the literature and a meta-regression. Clin Gastroenterol Hepatol. 2007;5:103-110.
96. Dignass AU, Gasche C, Bettenworth D, et al. European consensus on the diagnosis and management of iron deficiency and anaemia in inflammatory bowel diseases. J Crohns Colitis. 2015;9:211-22.
97. Gonzalez-Huix F, Fernandez-Banares F, Esteve-Comas M, et al. Enteral versus parenteral nutrition as adjunct therapy in acute ulcerative colitis. Am J Gastroenterol. 1993;88:227-32.
98. Parlak E, Dağli U, Ulker A, et al. Comparison of 5-amino salicylic acid plus glucocorticosteroid with metronidazole and ciprofloxacin in patients with active ulcerative colitis. J Clin Gastroenterol. 200;33(1):85-6xxxiv.
99. Khan KJ, Ullman TA, Ford AC, Abreu MT, et al. Antibiotic therapy in inflammatory bowel disease: a systematic review and metaanalysis. Am J Gastroenterol. 2011;106:661-73.
100. Ohkusa T, Kato K, Terao S, Chiba T, et al. Newly developed antibiotic combination therapy for ulcerativecolitis: a double-
blind placebo-controlled multicenter trial. Am J Gastroenterol.
2010;105:1820-9.
101. Järnerot G, Hertervig E, Friis-Liby I, et al. Infliximab as rescue therapy in severe to moderately severe ulcerative colitis: a randomized, placebo-controlled study. Gastroenterology. 2005;128:180511.
102. Lees CW, Heys D, Ho GT, Noble CL et al. A retrospective analysis of the efficacy and safety of infliximab as rescue therapy in acute severe ulcerative colitis. Aliment Pharmacol Ther. 2007;26:411-9.
103. Van Assche G, D'Haens G, Noman M, Vermeire S, et al. Randomized, double-blind comparison of 4 mg/kg versus 2 mg/kg intravenous cyclosporine in severe ulcerative colitis. Gastroenterology. 2003;125:1025-31.
104. Sjoberg M, Walch A, Meshkat M, Gustavsson A, et al. Infliximab or cyclosporine as rescue therapy in hospitalized patients with steroid-refractory ulcerative colitis: a retrospective observational study. Inflamm Bowel Dis. 2012; 18(2), p. 212-8.
105. Головенко А.О., Халиф И.Л., Головенко О.В., Веселов В.В. Предикторы эффективности инфликсимаба у больных с тяжелой атакой язвенного колита. Российский журнал гастроэнтерологии, гепатологии, колопроктологии. 2013;5(23):65-73.
106. Sokol H, Seksik P, Carrat F, Nion-Larmurier I, et al. Usefulness of co-treatment with immunomodulators in patients with inflammatory bowel disease treated with scheduled infliximab maintenance therapy. Gut. 2010;59:1363-8.
107. Reinisch W, Sandborn WJ, Rutgeerts P, Feagan BG, et al. Longterm infliximab maintenance therapy for ulcerative colitis: the ACT-1 and -2 extension studies. Inflamm Bowel Dis. 2012;18:201-11.
108. Chebli LA, LDdM Chaves, Pimentel FF, Guerra DM, et al. Azathioprine maintains long-term steroid-free remission through
3 years in patients with steroid-dependent ulcerative colitis.
Inflamm Bowel Dis. 2010;16:613-9.
109. Ardizzone S, Maconi G, Russo A, Imbesi V, et al. Randomised controlled trial of azathioprine and 5-aminosalicylic acid for treatment of steroid dependent ulcerative colitis. Gut. 2006;55:47-53.
110. Randall JSB, Warren BF, Travis SP, Mortensen NJ, et al. Delayed surgery for acute severe colitis is associated with increased risk of postoperative complications. Br J Surg. 2010;97: 404-9.
111. Lennard-Jones JE, Ritchie JK, Hilder W, Spicer CC. Assessment of severity in colitis: a preliminary study. Gut. 1975;16:579-84.
112. Travis SP, Farrant JM, Ricketts C, Nolan DJ, et al. Predicting outcome in severe ulcerative colitis. Gut. 1996;38:905-10.
113. Lindgren SC, Flood LM, Kilander AF, Lofberg R et al. Early predictors of glucocorticosteroid treatment failure in severe and moderately severe attacks of ulcerative colitis. Eur J Gastroenterol Hepatol. 1998;10:831-5.
114. Benazzato L, D'Inca R, Grigoletto F, Perissinotto E, et al. Prognosis of severe attacks in ulcerative colitis: effect of intensive medical treatment. Dig Liver Dis. 2004;36:461-6.
115. Almer S, Bodemar G, Franzen L, Lindstrom E, et al. Use of air enema radiography to assess depth of ulceration during acute attacks of ulcerative colitis. Lancet. 1996;347: 1731-5.
116. Carbonnel F, Lavergne A, Lemann M, Bitoun A, et al. Colonoscopy of acute colitis. A safe and reliable tool for assessment of severity. Dig Dis Sci. 1994;39: 1550-7.
117. Ferrante M, Vermeire S, Katsanos KH. Predictors of early response to infliximab in patients with ulcerative colitis. Inflamm Bowel Dis. 2007 Feb;13(2):123-8.
118. Gonzalez-Lama Y, Fernandez-Blanco I, Lopez-SanRoman A. Open-label infliximab therapy in ulcerative colitis: a multicenter survey of results and predictors of response. Hepatogastroenterology. 2008 Sep-Oct;55(86-87):1609-14.
119. Fasanmade AA, Adedokun OJ, Olson A, Strauss R, et al. Serum albumin concentration: a predictive factor of infliximab pharmacokinetics and clinical response in patients with ulcerative colitis. Int J Clin Pharmacol Ther. 2010 May;48(5):297-308.
120. Oussalah A, Evesque L, Laharie D, Roblin X. A multicenter experience with infliximab for ulcerative colitis: outcomes and predictors of response, optimization, colectomy, and hospitalization. Am J Gastroenterol. 2010 Dec;105(12):2617-25.
121. Cacheux W, Seksik P, Lemann M, Marteau P, et al. Predictive factors of response to cyclosporine in steroid-refractory ulcerative colitis. Am J Gastroenterol. 2008; 103: 637-42.
122. Monterubbianesi R, Aratari A, Armuzzi A, Daperno M, et al. Infliximab three-dose induction regimen in severe corticosteroidrefractory ulcerative colitis: early and late outcome and predictors of colectomy. J CrohnsColitis. 2014; 8: 852-8.
123. Van Assche G, D'Haens G, Noman M, Vermeire S, et al. Randomized, double-blind comparison of 4 mg/kg versus 2 mg/kg intravenous cyclosporine in severe ulcerative colitis. Gastroenterology. 2003;125:1025-31.
124. Gan SI, Beck PL. A new look at toxic megacolon: an update and review of incidence, etiology, pathogenesis, and management. Am J Gastroenterol. 2003;98:2363-2371.
125. Eaden JA, Abrams KR, Mayberry JF. The risk of colorectal cancer in ulcerative colitis: a meta-analysis. Gut. 2001;48:526-35.
126. Jess T, Loftus Jr EV, Velayos FS, Harmsen WS, et al. Risk of intestinal cancer in inflammatory bowel disease: a populationbased study from olmsted county, Minnesota. Gastroenterology. 2006;130:1039-46.
127. Bergeron V, Vienne A, Sokol H, Seksik P, et al. Risk factors for neoplasia in inflammatory bowel disease patients with pancolitis. Am J Gastroenterol. 2010, [advance online publication, 15 June 2010].
128. Rutter M, Saunders B, Wilkinson K, Rumbles S, et al. Severity of inflammation is a risk factor for colorectal neoplasia in ulcerative colitis. Gastroenterology. 2004;126:451-9.
129. Richards DM, Hughes SA, Irving MH, Scott NA. Patient quality of life after successful restorative proctocolectomy is normal. Colorectal Dis. 2001;3:223-6.
130. McLaughlin SD, Clark SK, Thomas-Gibson S, Tekkis P, et al. Guide to endoscopy of the ileo-anal pouch following restorative proctocolectomy with ileal pouch-anal anastomosis; indications, technique, and management of common findings. Inflamm Bowel Dis. 2009;15:1256-63.
131. Berndtsson I, Oresland T. Quality of life before and after proctocolectomy and IPAA in patients with ulcerative proctocolitis—a prospective study. Colorectal Dis. 2003;5:173-9.
132. Marcello PW, Roberts PL, Schoetz Jr DJ, Coller JA, et al. Long-term results of the ileoanal pouch procedure. Arch Surg. 1993;128:500-3 [discussion 503-4].
133. Sagar PM, Pemberton JH. Ileo-anal pouch function and dysfunction. Dig Dis. 1997;15:172-88.
134. Meagher AP, Farouk R, Dozois RR, Kelly KA, et al. J ileal pouchanal anastomosis for chronic ulcerative colitis: complications and long-term outcome in 1310 patients. Br J Surg. 1998;85:800-3.
135. Setti-Carraro P, Ritchie JK, Wilkinson KH, et al. The first 10 years’ experience of restorative proctocolectomy for ulcerative colitis. Gut. 1994;35:1070-1075.
136. Fazio VW, Ziv Y, Church JM, et al. Ileal pouch-anal anastomoses complications and function in 1005 patients. Ann Surg. 1995;222:120-127.
137. Belliveau P, Trudel J, Vasilevsky CA, et al. Ileoanal anastomosis with reservoirs: complications and long-term results. Can J Surg. 1999;42: 345-352.
138. Pinto RA, Canedo J, Murad-Regadas S, Regadas SF, et al. Ileal pouch-anal anastomosis in elderly patients: is there a difference in morbidity compared with younger patients? Colorectal Dis. 2011;13:177-83.
139. Church JM. Functional outcome and quality of life in an elderly patient with an ileal pouch-anal anastomosis: a 10-year follow up. Aust N Z J Surg. 2000;70:906-7.
140. Chapman JR, Larson DW, Wolff BG, Dozois EJ, et al. Ileal pouch-anal anastomosis: does age at the timeof surgery affect outcome? Arch Surg. 2005;140:534-40.
141. Delaney CP, Dadvand B, Remzi FH, et al. Functional outcome, quality of life, and complications after ileal pouch-anal anastomosis in selected septuagenarians. Dis Colon Rectum. 2002;45:890-4.
142. Olsen KO, Joelsson M, Laurberg S, Oresland T. Fertility after ileal pouch-anal anastomosis in women with ulcerative colitis. Br J Surg. 1999;86:493-5.
143. Ording OK, Juul S, Berndtsson I, Oresland T et al. Ulcerative colitis: female fecundity before diagnosis, during disease, and after surgery compared with a population sample. Gastroenterology. 2002;122:15-9.
144. Gorgun E, Remzi FH, Goldberg JM, Thornton J, et al. Fertility is reduced after restorative proctocolectomy with ileal pouch anal anastomosis: a study of 300 patients. Surgery. 2004;136:795-803.
145. Johnson P, Richard C, Ravid A, Spencer L, et al. Female infertility after ileal pouch-anal anastomosis for ulcerative colitis. Dis Colon Rectum. 2004;47:1119-26.
146. Oresland T, Palmblad S, Ellstrom M, Berndtsson I, et al. Gynaecological and sexual function related to anatomical changes in the female pelvis after restorative proctocolectomy. Int J Colorectal Dis. 1994;9:77-81.
147. Burns EM, Bottle A, Aylin P, Clark SK, et al. Volume analysis of outcome following restorative proctocolectomy. Br J Surg. 2011;98:408-17.
148. Alves A, Panis Y, Bouhnik Y, Maylin V, et al. Subtotal colectomy for severe acute colitis: a 20-year experience of a tertiary care center with an aggressive and early surgical policy. J Am Coll Surg. 2003;197:379-85
149. Berg DF, Bahadursingh AM, Kaminski DL, Longo WE. Acute surgical emergencies in inflammatory bowel disease. Am J Surg. 2002;184:45-51.
150. Hyman NH, Cataldo P, Osler T. Urgent subtotal colectomy for severe inflammatory bowel disease. Dis Colon Rectum. 2005;48: 70-3.
151. Holubar SD, Larson DW, Dozois EJ, Pattana-Arun J, et al. Minimally invasive subtotal colectomy and ileal pouch-anal anastomosis for fulminant ulcerative colitis: a reasonable approach? Dis Colon Rectum. 2009;52:187-92.
152. Marceau C, Alves A, Ouaissi M, Bouhnik Y, et al. Laparoscopic subtotal colectomy for acute or severe colitis complicating inflammatory bowel disease: a case-matched study in 88 patients. Surgery. 2007;141:640.
153. Annibali R, Oresland T, Hulten L. Does the level of stapled ileoanal anastomosis influence physiologic and functional outcome? Dis Colon Rectum. 1994;37:321-9.
154. Burns EM, Bottle A, Aylin P, Clark SK, et al. Volume analysis of outcome following restorative proctocolectomy. Br J Surg. 2011;98:408-17.
155. Tekkis PP, Fazio VW, Lavery IC, Remzi FH, et al. Evaluation of the learning curve in ileal pouch-anal anastomosis surgery. Ann Surg. 2005;241:262-8.
156. Lepisto A, J. JH. Fate of the rectum after colectomy with ileorectal anastomosis in ulcerative colitis. Scand J Surg. 2005;94:40-2.
157. Edwards, C.M., B. George, and B.F. Warren, Diversion colitis: new light through old windows. Histopathology. 1999. 35(1): p. 86-7.
158. Annibali R, Oresland T, Hulten L. Does the level of stapled ileoanal anastomosis influence physiologic and functional outcome? Dis Colon Rectum. 1994;37:321-9.
159. Shepherd NA, Jass JR, Duval I, Moskowitz RL, et al. Restorative proctocolectomy with ileal reservoir: pathological and histochemical study of mucosal biopsy specimens. J Clin Pathol. 1987;40:601-7.
160. Setti Carraro PG, Talbot IC, Nicholls JR. Patterns of distribution of endoscopic and histological changes in the ileal reservoir
after restorative proctocolectomy for ulcerative colitis. A longterm follow-up study. Int J Colorectal Dis. 1998;13:103-7.
161. Ferrante M, D'Hoore A, Vermeire S, et al. Corticosteroids but not infliximab increase short-term postoperative infectious complications in patients with ulcerative colitis. Inflamm Bowel Dis. 2009;15:1062-70.
162. Lake JP, Firoozmand E, Kang JC, Vassiliu P, et al. Effect of high-dose steroids on anastomotic complications after proctocolectomy with ileal pouch-anal anastomosis. J Gastrointest Surg. 2004;8:547-51.
163. Mahadevan U, Loftus Jr EV, Tremaine WJ, Pemberton JH, Harmsen WS, Schleck CD, et al. Azathioprine or 6-mercaptopurine before colectomy for ulcerative colitis is not associated with increased postoperative complications. Inflamm Bowel Dis. 2002;8:311-6.
164. Pugliese D, Armuzzi A, Rizzo G, et al. Effect of anti-TNF-alpha treatment on short-term post-operative complications in patients with inflammatory bowel disease. Gut. 2010;59(Suppl III):A13.
165. Subramanian V, Pollok RC, Kang JY, Kumar D. Systematic review of postoperative complications in patients with inflammatory bowel disease treated with immunomodulators. Br J Surg. 2006;93:793-9.
166. Yang Z, Wu Q, Wang F, Wu K, Fan D. Meta-analysis: effect of preoperative infliximab use on early postoperative complications in patients with ulcerative colitis undergoing abdominal surgery. Aliment Pharmacol Ther. 2012 Nov;36(10):922-8. doi: 10.1111/ apt.12060. Epub 2012 Sep 24.
167. Meagher AP, Farouk R, Dozois RR, Kelly KA, et al. J ileal pouchanal anastomosis for chronic ulcerative colitis: complications and long-term outcome in 1310 patients. Br J Surg. 1998;85:800-3.
168. Simchuk EJ, Thirlby RC. Risk factors and true incidence of pouchitis in patients after ileal pouch-anal anastomoses. World J Surg. 2000;24:851-6.
169. Stahlberg D, Gullberg K, Liljeqvist L, Hellers G, et al. Pouchitis following pelvic pouch operation for ulcerative colitis. Incidence, cumulative risk, and risk factors. Dis Colon Rectum. 1996;39:1012-8.
170. Penna C, Tiret E, Kartheuser A, Hannoun L, et al. Function of ileal J pouch-anal anastomosis in patients with familial adenomatous polyposis. Br J Surg. 1993;80:765-7.
171. Tjandra JJ, Fazio VW, Church JM, Oakley JR, et al. Similar functional results after restorative proctocolectomy in patients with familial adenomatous polyposis and mucosal ulcerative colitis. Am J Surg. 1993;165:322-5.
172. Shen B, Lashner BA. Diagnosis and Treatment of Pouchitis.
Gastroenterology & Hepatology. 2008;4(5):355-361.
173. Shen B, Achkar JP, Lashner BA. Irritable pouch syndrome: a new category of diagnosis for symptomatic patients with ileal pouch-anal anastomosis. Am J Gastroenterol. 2002 Apr;97(4):972-7.
174. Корнеева О. Н., Ивашкин В. Т. Антибиотикоассоциированный колит: патоморфология, клиника, лечение. Российский журнал гастроэнтерологии гепатологии и колопроктологии. 2007;
№17(3), c. 65-70.
175. Aguado JM, Anttila VJ, Galperine T, Goldenberg SD et al. Highlighting clinical needs in Clostridium difficile infection: the views of European healthcare professionals at the front line. J Hosp Infect. 2015; 2(50): 117-125.
176. Metan G, Türe Z, Kaynar L. Tigecycline for the treatment
of Clostridium difficile infection refractory to metronidazole in haematopoietic stem cell transplant recipients. Journal of Chemotherapy. 2015;6(27): 354-357.
177. Chiu CY, Sarwal A, Feinstein A, Hennessey K. Effective Dosage of Oral Vancomycin in Treatment for Initial Episode of Clostridioides difficile Infection: A Systematic Review and MetaAnalysis. Antibiotics (Basel). 2019 Oct 1;8(4). pii: E173. doi: 10.3390/antibiotics8040173.
178. Tschudin-Sutter S, Braissant O, Erb S, et al. Growth Patterns of Clostridium difficile – Correlations with Strains, Binary Toxin and Disease Severity: A Prospective Cohort Study. PLoS One. 2016; 9(11): e0161711.
179. Фоменко О.Ю., Ачкасов С.И., Титов А.Ю., Алешин Д.В., и соавт. Современные возможности улучшения функционального состояния запирательного аппарата у пациентов с наличием превентивных кишечных стом. Российский журнал гастроэнтерологии, гепатологии, колопроктологии. 2015; № 5, с. 77-83.
REFERENCES
1. Travis SP, Dinesen L. Remission in trials of ulcerative colitis: what does it mean? Pract Gastroenterol. 2010;30:17-20.
2. D'Haens G, et al. A review of activity indices and efficacy end points for clinical trials of medical therapy in adults with ulcerative colitis. Gastroenterology. 2007;132:763-86.
3. Cosnes J, Gower-Rousseau C, Seksik P, Cortot A. Epidemiology and natural history of inflammatory bowel diseases. Gastroenterology. 2011;140:1785-94.
4. Belousova E.A., Abdulganieva D.I., Alexeeva O.P., Alexeenko S.A. et al. Social and demographic characteristics, features of disease course and treatment options of inflammatory bowel disease in Russia: results of two multicenter studies. Almanac of Clinical Medicine. 2018;46(5):445-463. https://doi.org/10.18786/20720505-2018-46-5-445-463 (In Russ.)
5. Katsanos KH, Vermeire S, Christodoulou DK, Riis L, et al. Dysplasia and cancer in inflammatory bowel disease 10 years after diagnosis: results of a population-based European collaborative follow-up study. Digestion. 2007;75: 113-21.
6. Silverberg MS, et al. Toward an integrated clinical, molecular and serological classification of inflammatory bowel disease: report of a working party of the 2005 Montreal World Congress of Gastroenterology. Can J Gastroenterol. 2005;19(Suppl A):5-36.
7. Truelove SC et al. Cortisone in ulcerative colitis; final report on a therapeutic trial. Br Med J. 1955;2:1041-8.
8. Seah D, De Cruz P. Review article: the practical management of acute severe ulcerative colitis. Aliment Pharmacol Ther. 2016 Feb;43(4):482-513.
9. Hindryckx P, Jairath V, D'Haens G. Acute severe ulcerative colitis: from pathophysiology to clinical management. Nat Rev Gastroenterol Hepatol. 2016 Sep 1.
10. Chen JH, Andrews JM, Kariyawasam V, Moran N. IBD Sydney Organisation and the Australian Inflammatory Bowel Diseases Consensus Working Group. Review article: acute severe ulcerative colitis – evidence-based consensus statements. Aliment Pharmacol Ther. 2016 Jul;44(2):127-44.
11. Schroeder KW, Tremaine WJ, Ilstrup DM. Coated oral 5-aminosalicylic acid therapy for mildly to moderately active ulcerative colitis. A randomized study. N Engl J Med. 1987;317:1625-9.
12. Grigor’eva GA, Meshalkina NYu. On The Problem Of Systemic Manifestations Of Inflammatory Bowel Diseases. Farmateka. 2011; 5: 44-49. (In Russ.)
13. Sands BE. From symptom to diagnosis: clinical distinctions among various forms of intestinal inflammation. Gastroenterology. 2004;126:1518-32.
14. Perler B, Ungaro R, Baird G, Malette M. et al. Presenting symptoms in inflammatory bowel disease: descriptive analysis of a community-based inceptive cohort. BMC Gastroenterol. 2019; 19:47.
15. Fine KD, Schiller LR. AGA technical review on the evaluation and management of chronic diarrhea. Gastroenterology. 1999;116:1464-86.
16. Forrest K, Symmons D, Foster P. Systematic review: is ingestion of paracetamol or non-steroidal anti-inflammatory drugs associated with exacerbations of inflammatory bowel disease? Aliment Pharmacol Ther. 2004;20:1035-43.
180. Фоменко О.Ю., Ачкасов С.И., Титов А.Ю., Джанаев Ю.А., и соавт. Роль аноректальной манометрии, БОС-терапии и тибиальной нейромодуляции в диагностике и консервативном лечении анальной инконтиненции у пожилых. Клиническая геронтология. 2015; № 5-6, с. 16-20.
181. American Thoracic Society/Centers for Disease Control and Prevention/Infectious Diseases Society of America: controlling tuberculosis in the United States. Am J Respir Crit Care Med. 2005. 172(9): 1169-227.
17. Mahid SS, Minor KS, Soto RE, et al. Smoking and inflammatory bowel disease: a meta-analysis. Mayo Clin Proc. 2006;81:1462-71.
18. Vermeire S. Review article: genetic susceptibility and application of genetic testing in clinical management of inflammatory bowel disease. Aliment Pharmacol Ther. 2006;24:2-10.
19. Carter MJ, Lobo AJ, Travis SP; IBD Section, British Society of Gastroenterology. Guidelines for the management of inflammatory bowel disease in adults. Gut. 2004;53:V1-16.
20. Dignass A, et al. Second EUROPEAN evidence-based Consensus on the diagnosis and management of ulcerative colitis: Current management, Journal of Crohn's and Colitis. 2012.
21. Travis SP, Jewell DP. Ulcerative colitis: clinical presentation and diagnosis. In: Satsangi J, Sutherland LR, editors. Inflammatory Bowel Diseases. London: Churchill Livingstone. 2003: 169-81.
22. Lucendo AJ, Arias Á, Roncero Ó, Hervías D, et al. Anemia at the time of diagnosis of inflammatory bowel disease: Prevalence and associated factors in adolescent and adult patients. Sao Paulo Med J. 2014;132(3):140-6.
23. Irwin JR, Ferguson E, Simms LA, Hanigan K, et al. Detectable Laboratory Abnormality Is Present up to 12 Months Prior to Diagnosis in Patients with Crohn's Disease. Dig Dis Sci. 2019 Feb;64(2):503-517.
24. Cherfane CE, Gessel L, Cirillo D, Zimmerman MB, Polyak S. Monocytosis and a Low Lymphocyte to Monocyte Ratio Are Effective Biomarkers of Ulcerative Colitis Disease Activity. Inflamm Bowel Dis. 2015 Aug;21(8):1769-75.
25. Feng JR, Qiu X, Wang F, Chen PF, et al. Diagnostic Value of Neutrophil-to-Lymphocyte Ratio and Platelet-to-Lymphocyte Ratio in Crohn's Disease. Gastroenterol Res Pract. 2017;2017:3526460. doi: 10.1155/2017/3526460.
26. Yoon JY, Park SJ, Hong SP, Kim TI, et al. Correlations of C-reactive protein levels and erythrocyte sedimentation rates with endoscopic activity indices in patients with ulcerative colitis. Dig Dis Sci. 2014 Apr;59(4):829-37.
27. Yamamoto-Furusho JK, Sánchez-Osorio M, Uribe M. Prevalence and factors associated with the presence of abnormal function liver tests in patients with ulcerative colitis. Ann Hepatol. 2010 Oct-Dec;9(4):397-401
28. Archampong EQ, Harris J, Clark CG. The absorption and secretion of water and electrolytes across the healthy and the diseased human colonic mucosa measured in vitro. Gut. 1972 Nov;13(11):880-6.
29. Maharshak N, Arbel Y, Gal-Oz A, Rogowski O, et al. Comparative analysis of Bayer wide-range C-reactive protein (wr-CRP) and the Dade-Behring high sensitivity C-reactive protein (hs-CRP) in patients with inflammatory bowel disease. J Dig Dis. 2008 Aug;9(3):140-3.
30. Weber P, Husemann S, Vielhaber H, Zimmer KP, Nowak-Göttl U. Coagulation and fibrinolysis in children, adolescents, and young adults with inflammatory bowel disease. J Pediatr Gastroenterol Nutr. 1999 Apr;28(4):418-22.
31. Issa M, Vikayapal A, Gracham MB et al. Impact of Clostridium difficile in inflammatory bowel disease patients. Clin Gastroenterol
Hepatol. 2007; 5: 345-351.
32. Rodeman JF, Dubberke ER, Reske KA et al. Incidence of Clostridium difficile in inflammatory bowel disease. Clin Gastroenterol Hepatol. 2007; 5: 339-344.
33. Issa M, Ananthakrishnan AN, Binion DG. Clostridium difficile and inflammatory bowel disease. Inflamm Bowel Dis. 2008; 14:1432-42.
34. Nguyen GC, Kaplan GG, Harris ML et al. A national survey of the prevalence and impact of Clostridium difficile infection among hospitalized inflammatory bowel disease patients. Am J Gastroenterol. 2008; 103: 1443-50.
35. Mindenmark M, Larsson A. Rulling out IBD estimation of the possible economic effects of pre-endoscopic screening with F-calprotectin. Clin Biochem. 2012; 45: 552-5.
36. Costa F, Mumolo MG, Bellini M, Romano MR, et al. Role of faecal calprotectin as non-invasive marker of intestinal inflammation. Dig Liver Dis. 2003;35:642-7.
37. Kim JJ, Simpson N, Klipfel N, Debose R, et al. Cytomegalovirus infection in patients with active inflammatory bowel disease. Dig Dis Sci. 2010 Apr;55(4):1059-65. doi: 10.1007/s10620-010-1126-4.
38. Lin WC, Chang CW, Chen MJ, Hsu TC, Wang HY. Effectiveness of sigmoidoscopy for assessing ulcerative colitis disease activity and therapeutic response. Medicine (Baltimore). 2019 May;98(21):e15748. doi: 10.1097/MD.0000000000015748.
39. Bansal J, Jenaw RK, Rao J, et al. Effectiveness of plain radiography in diagnosing hollow viscus perforation: study of 1,723 patients of perforation peritonitis. Emerg Radiol. 2012 Apr;19(2):115-9. doi: 10.1007/s10140-011-1007-y.
40. Colombel JF, Ordás I, Ullman T, Rutgeerts Pet al. Agreement Between Rectosigmoidoscopy and Colonoscopy Analyses of Disease Activity and Healing in Patients With Ulcerative Colitis. Agreement Between Rectosigmoidoscopy and Colonoscopy Analyses of Disease Activity and Healing in Patients With Ulcerative Colitis. Gastroenterology. 2016 Feb; 150(2):389-95.e3. doi: 10.1053/j.gastro.2015.10.016.
41. Annese V, Daperno M, Rutter M.D., et al. European evidence based consensus for endoscopy in inflammatory bowel disease. Journal of Crohn’s and Colitis. 2013; 7(12): 982-1018.
42. Tanaka M, Saito H, Fukuda S, Sasaki Y, et al. Simple mucosal biopsy criteria differentiating among Crohn disease, ulcerative colitis, and other forms of colitis: measurement of validity. Scand J Gastroenterol. 2000 Mar;35(3):281-6.
43. Parente F, Greco S, Molteni M, et al. Role of early ultrasound in detecting inflammatory intestinal disorders and identifying their anatomical location within the bowel. Alimentary Pharmacology and Therapeutics. 2003;18:1009-1016.
44. Socaciu M, Ciobanu L, Diaconu B, Hagiu C, et al. Non-Invasive Assessment of Inflammation and Treatment Response in Patients with Crohn's Disease and Ulcerative Colitis using ContrastEnhanced Ultrasonography Quantification. J Gastrointestin Liver Dis. 2015 Dec;24(4):457-65. doi: 10.15403/jgld.2014.1121.244.chr.
45. Pouillon L, Laurent V, Pouillon M, Bossuyt P et al. Diffusion-weighted MRI in inflammatory bowel disease. Lancet Gastroenterol Hepatol. 2018 Jun;3(6):433-443. doi: 10.1016/S24681253(18)30054-2.
46. Kılıçkesmez O, Soylu A, Yaşar N, Demirbaş T, Dolapçıoğlu C, et al. Is quantitative diffusion-weighted MRI a reliable method in the assessment of the inflammatory activity in ulcerative colitis? Diagn Interv Radiol. 2010 Dec;16(4):293-8. doi: 10.4261/1305-3825. DIR.2989-09.1.
47. Jia Y, Li C, Yang X, Dong Z, et al. CT Enterography score: a potential predictor for severity assessment of active ulcerative colitis. BMC Gastroenterol. 2018 Nov 9;18(1):173. doi: 10.1186/ s12876-018-0890-z.
48. Gashin L, Villafuerte-Galvez J, Leffler DA, et al. Utility of CT in the emergency department in patients with ulcerative coli-
tis. Inflamm Bowel Dis. 2015 Apr;21(4):793-800. doi: 10.1097/ MIB.0000000000000321.
49. Mil'ko V.I., Mincher O.P., Topchiy T.V., Korsunovskiy A.A. Clinical assessment of irrigoscopy data in ulcerative colitis. Vestnik rentgenologii i radiologii. 1983; 5:46-50. (In Russ.)
50. Korneeva O.I., Ivashkin V.T. Cl.Difficile colitis: pathomorfology, symptoms and treatment. Russian Journal of Gastroenterology, Hepatology, Coloproctology. 2007; 17(3):65-71 (In Russ.).
51. Ivashkin V.T., Sheptulin A.A., Shifrin O.S., Galimova S.F. et al. Microscopic colitis: clinical forms, diagnosis and treatment. Russian Journal of Gastroenterology, Hepatology, Coloproctology. 2006; 16(6):56-60. (In Russ.).
52. Belousova E.A., Nikitina N.V., Tsodikova O.M. Treatment Of Mild To Moderate Ulcerative Colitis. Farmateka. 2013; 2: 42-46. (In Russ.).
53. Khalif I.L. Treatment strategies in ulcerative colitis (Russian inflammatory bowel disease group guidelines). Koloproktologia. 2006;2:31-33 (In Russ.)
54. Khalif I.L. Treatment strategies in ulcerative colitis. Russian Journal of Gastroenterology, Hepatology, Coloproctology. 2006; 16(3):58-62. (In Russ.).
55. Marshall JK, Thabane M, Steinhart AH, Newman JR, et al. Rectal 5-aminosalicylic acid for induction of remission in ulcerative colitis. Cochrane Database Syst Rev. 2010 [CD004115-CD004115].
56. Marshall JK, Irvine EJ. Rectal corticosteroids versus alternative treatments in ulcerative colitis: a meta-analysis. Gut. 1997;40: 775-81.
57. Lamet M. A multicenter, randomized study to evaluate the efficacy and safety of mesalamine suppositories 1 g at bedtime and 500 mg twice daily in patients with active mild-to-moderate ulcerative proctitis. Dig Dis Sci. 2011;56:513-22
58. Safdi M, DeMicco M, Sninsky C, Banks P, et al. A double-blind comparison of oral versus rectal mesalamine versus combination therapy in the treatment of distal ulcerative colitis. Am J Gastroenterol. 1997;92:1867-71.
59. Gecse KB1, Lakatos PL. Ulcerative proctitis: an update on the pharmacotherapy and management. Expert Opin Pharmacother. 2014;15(11):1565-73.
60. Ahmed I, Kassem W, Salam Y, Furnari M, Mehta T. Outcome of Cytomegalovirus Colitis in Inflammatory Bowel Disease with Different Regimes of Ganciclovir. Middle East J DigDis. 2018 Oct;10(4):220-229. doi: 10.15171/mejdd.2018.114.
61. Sutherland L, Macdonald JK. Oral 5-aminosalicylic acid for induction of remission in ulcerative colitis. Cochrane Database Syst Rev. 2006:CD000543.
62. Regueiro M, Loftus Jr EV, Steinhart AH, Cohen RD. Medical management of left-sided ulcerative colitis and ulcerative proctitis: critical evaluation of therapeutic trials. Inflamm Bowel Dis. 2006;12:979-94.
63. Ford AC, Achkar J-P, Khan KJ, Kane SV, Talley NJ, et al. Efficacy of 5-aminosalicylates in ulcerative colitis: systematic review and meta-analysis. Am J Gastroenterol. 2011;106:601-16.
64. Ford AC, Khan KJ, Achkar JP, et al. Efficacy of oral vs. topical, or combined oral and topical 5-aminosalicylates, in Ulcerative Colitis: systematic review and meta-analysis. The American journal of gastroenterology. 2012;107:167-76;
65. Kane SV, Bjorkman DJ. The efficacy of oral 5-ASAs in the treatment of active ulcerative colitis: a systematic review. Rev Gastroenterol Disord. 2003;3:210-8.
66. Kane SV, Bjorkman DJ. The efficacy of oral 5-ASAs in the reatment of active ulcerative colitis: a systematic review. Rev Gastroenterol Disord. 2003;3:210-8.
67. Danielsson A, Löfberg R, Persson T, Salde L, et al. A steroid enema, budesonide, lacking systemic effects for the treatment of distal ulcerative colitis or proctitis. Scand J Gastroenterol. 1992;27(1):9-12.
68. Nguyen NH, Fumery M, Dulai PS, Prokop LJ,et al. Comparative efficacy and tolerability of pharmacological agents for management of mild to moderate ulcerative colitis: a systematic review and network meta-analyses. Lancet Gastroenterol Hepatol. 2018 Nov;3(11):742-753. doi: 10.1016/S2468-1253(18)30231-0.
69. D'Haens G. Systematic review: second-generation vs. conventional corticosteroids for induction of remission in ulcerative colitis. Aliment Pharmacol Ther. 2016;44:1018-1029.
70. Sutherland L, Macdonald JK. Oral 5-aminosalicylic acid for induction of remission in ulcerative colitis. Cochrane Database Syst Rev. 2006:CD000543.
71. Feagan BG, MacDonald JK. Once daily oral mesalamine compared to conventional dosing for induction and maintenance of remission in ulcerative colitis: a systematic review and metaanalysis. Inflammatory bowel diseases. 2012;18:1785-94.
72. Lichtenstein GR. Budesonide Multi-matrix for the Treatment of Patients with Ulcerative Colitis. Dig Dis Sci. 2016 Feb;61(2):358-70.
73. Sherlock ME, MacDonald JK, Griffiths AM, Steinhart AH, Seow CH. Oral budesonide for induction of remission in ulcerative colitis. Cochrane Database Syst Rev. 2015 Oct 26;(10):CD007698.
74. Danese S, Siegel CA, Peyrin-Biroulet L. Review article: integrating budesonide-MMX into treatment algorithms for mildto-moderate ulcerative colitis. Aliment Pharmacol Ther. 2014 May;39(10):1095-103.
75. Timmer A, Patton PH, Chande N, et al. Azathioprine and 6-mercaptopurine for maintenance of remission in ulcerative colitis. Cochrane Database Syst Rev. 2016:Cd000478.
76. Gisbert JP, Linares PM, McNicholl AG, Mate J, Gomollon F. Metaanalysis:
Рекомендуемые статьи
При эндоскопическом исследовании в случае бронхоэктазов в стадии ремиссии выявляется
частично диффузный бронхит I степени воспаления
Активируйте PUSH уведомления в браузер
Отключите PUSH уведомления в браузер
Содержание
Интернет магазин
Популярное
- О нас
- Правовые вопросы
- Политика
обработки персональных
данных EndoExpert.ru - Связаться с нами
- Стать партнером
© 2016-2022 EndoExpert.ru

Вы находитесь в разделе предназначенном только для специалистов (раздел для пациентов по ссылке). Пожалуйста, внимательно прочитайте полные условия использования и подтвердите, что Вы являетесь медицинским или фармацевтическим работником или студентом медицинского образовательного учреждения и подтверждаете своё понимание и согласие с тем, что применение рецептурных препаратов, обращение за той или иной медицинской услугой, равно как и ее выполнение, использование медицинских изделий, выбор метода профилактики, диагностики, лечения, медицинской реабилитации, равно как и их применение, возможны только после предварительной консультации со специалистом. Мы используем файлы cookie, чтобы предложить Вам лучший опыт взаимодействия. Файлы cookie позволяют адаптировать веб-сайты к вашим интересам и предпочтениям.
Я прочитал и настоящим принимаю вышеизложенное, хочу продолжить ознакомление с размещенной на данном сайте информацией для специалистов.


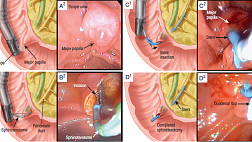











.jpg)





.png)


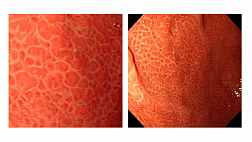
.jpg)

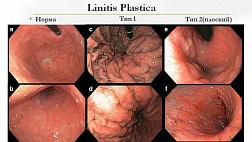
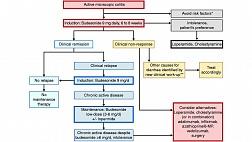













Комментарии