- Компании
- Takeda. О компании, буклеты, каталоги, контакты
- Olympus. О компании, буклеты, каталоги, контакты
- Boston Scientific. О компании, буклеты, каталоги, контакты
- Pentax. О компании, буклеты, каталоги, контакты
- Fujifilm & R-Farm. О компании, буклеты, каталоги, контакты
- Erbe. О компании, буклеты, каталоги, контакты
- Еще каталоги
- Мероприятия
- Информация
- Обучение
- Классификации
- Атлас
- Quiz
- Разделы
- Пациенту
QR-код этой страницы

Для продолжения изучения на мобильном устройстве ПРОСКАНИРУЙТЕ QR-код с помощью спец. программы или фотокамеры мобильного устройства
Статьи: РОЛЬ ЛИГИРОВАНИЯ ВАРИКОЗНО-РАСШИРЕННЫХ ВЕН ПИЩЕВОДА В ПРОФИЛАКТИКЕ КРОВОТЕЧЕНИЙ ПОРТАЛЬНОГО ГЕНЕЗА
| Авторы: | Шишин К.В., д.м.н., заведующий отделением оперативной эндоскопии 1 Бакулин И.Г., д.м.н., проф., руководитель отдела заболеваний печени Недолужко И.Ю., к.м.н., с.н.с. отделения оперативной эндоскопии» Курушкина Н.А., к.м.н., н.с. отделения оперативной эндоскопии Бабаян А.Ф., врач-ординатор 2016г. |
| Об авторах: |
1. ГБУЗ «Московский клинический научно-практический центр Департамента здравоохранения г. Москвы» |



Полный текст статьи:
Актуальность
Хронические заболевания печени различной этиологии зачастую приводят к портальной гипертензии, которая является причиной формирования порто-системных венозных коллатералей, включая варикозное расширение вен (ВРВ) пищевода и желудка. Варикозное кровотечение является самым серьезным жизнеугрожающим осложнением портальной гипертензии. Летальность при первом эпизоде кровотечения составляет 30–50 %. У 60 % пациентов, перенесших кровотечение из ВРВ пищевода и желудка в прошлом, в течение первого года возникает рецидив, от которого погибают еще от 30 до 70 % больных. Таким образом, именно гастроэзофагеальные кровотечения делают портальную гипертензию у больных с циррозом печени хирургической проблемой.
Материал и методы
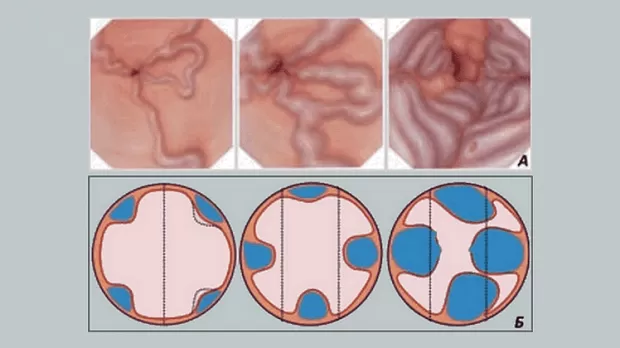
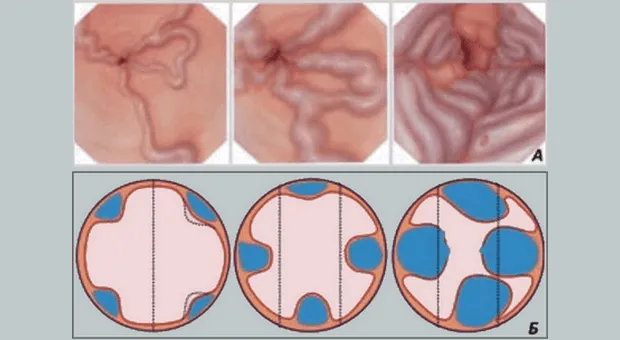
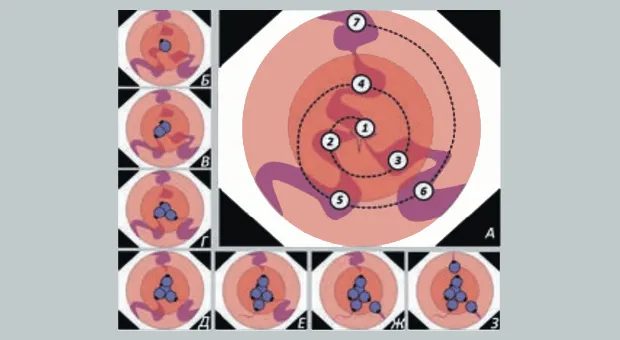
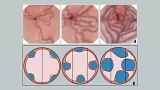
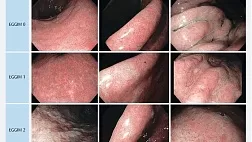
В период с ноября 2013 года по декабрь 2015 года включительно в отделении оперативной эндоскопии ГБУЗ Московского клинического научного центра ДЗ Москвы (МКНЦ) выполнено 237 эндоскопических лигирований вен пищевода 211 пациентам. Все пациенты первично находились на обследовании и лечении в отделении заболеваний печени МКНЦ. В протокол обязательного обследования пациентов включено выполнение эзофагогастродуоденоскопии с оценкой степени варикозного расширения вен по классификации N. Soehendra или ее модификации (Рис.1). Эндоскопическое лигирование выполнялось пациентам с ВРВ пищевода 3 степени согласно указанной выше классификации.
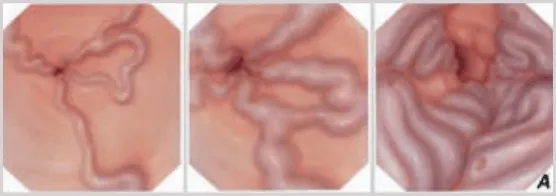
Рис 1А. Классификация варикозного расширения вен пищевода N.Soehendra, K.Binmoeller (1997):
1 степень: диаметр вен не превышает 5 мм, вытянутые, располагаются только в нижней трети пищевода;
2 степень: диаметр вен от 5 до 10 мм, извитые, расположены в средней трети пищевода;
3 степень: диаметр более 10 мм, напряженные, с тонкой стенкой, расположены вплотную друг к другу, на поверхности вен «красные маркеры».
(Из N. Soehendra, K.F. Binmoeller, H. Seifert, H. W. Schreiber. Therapeutic Endoscopy. Color Atlas of Operative Techniques for the Gastrointestinal Tract. 2005.)
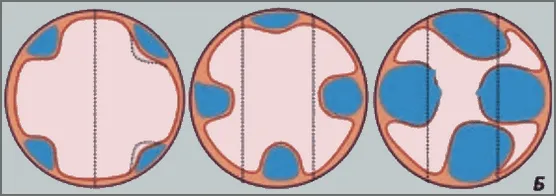
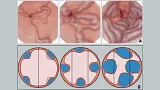
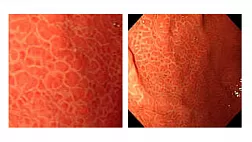
Рис 1Б. Усовершенствованная классификация (рекомендована ESGE):
1 степень (G1, малый варикоз): Варикозное расширение вен в виде прямых венозных стволов небольшого диаметра, которые частично или полностью спадаются при инсуфляции воздуха;
2 степень (G2, средний варикоз): Варикозное расширение вен в виде извилистых стволов, которые занимают менее 1/3 просвета пищевода и не спадаются при инсуфляции воздуха;
3 степень (G3, большой варикоз): Варикозное расширение вен в виде извитых петлистых стволов, которые занимают более 1/3 просвета пищевода, наличие предикторов кровотечения в виде супервариксов и «вишневых» пятен.
Средний возраст пациентов составил 55,3 года (min 25 — max 82), из них мужчин было 111 (52,6 %), женщин — 100 (47,4%). Распределение по этиологии развития цирроза печени было представлено следующим образом: алиментарный гепатит — 87 (41,2%), вирусные гепатиты — 48 (22,7 %), цирроз смешанной этиологии — 29 (13,8 %), первичный билиарный цирроз печени — 21 (10%), токсический — 7 (3,3%) и аутоимунный цирроз — 4 (1,9 %), неалкогольная жировая болезнь печени — 2 (0,9 %), криптогенный цирроз — 1 (0,5 %), гепатолентикулярная дегенерация — 1 (0,5 %), цирроз неясной этологии — 10 (4,7%).
Лигирование ВРВ пищевода в подавляющим большинстве было выполнено в плановом порядке. При этом у 41 (19,4 %) пациента в анамнезе уже было кровотечение из ВРВ пищевода. В 5 (2,4 %) наблюдениях лигирование выполнено после эндоскопической констатации продолжающегося кровотечения из варикозно расширенных вен пищевода. Выполнение лигирования вен на высоте кровотечения считали нецелесообразным. Всем пациентам первым этапом лечения проводился временный гемостаз с использованием зонда Сенгстакена-Блэкмора, инфузионная терапия с восстановлением объема циркулирующей крови, вазопрессорная терапия, направленная на снижение давления в системе воротной вены с последующим лигированием ВРВ пищевода в качестве окончательного метода гемостаза.
Техника оперативного вмешательства
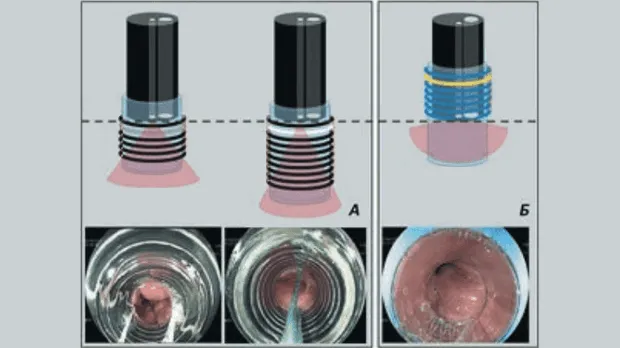
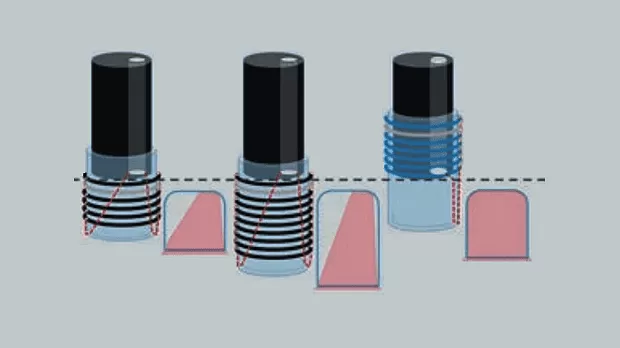
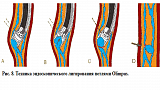
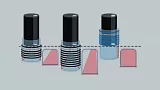
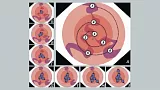
Операцию проводили под внутривенной анестезией. Для лигирования ВРВ использовали специальные устройства — лигаторы. В своей практике использовали многозарядные лигаторы фирм Cook Medical и Boston Scientific с числом предзаряженных лигатур от 6 до 10. Аппарат проводился до области пищеводно-желудочного перехода при минимальной инсуфляции воздуха с целью избежать срыгивания и разрыва вариксов. Лигирующие устройства разных фирм-производителей принципиально отличаются особенностями расположения колец на колпачке. У большинства производителей они попадают в поле зрения эндоскопа и существенно снижают угол зрения. Это, безусловно, является недостатком устройства, ограничивающим возможности уверенных манипуляций, особенно в условиях имеющегося кровотечения или при его возникновении по ходу процедуры (Рис. 2). Техническое решение в виде размещения лигирующих колец на колпачке вне поля зрения эндоскопа значительно облегчает условия визуализации за счет расширения бокового поля зрения через прозрачную стенку колпачка. Также следует отметить, что в зависимости от числа предзаряженных лигатур и методов их освобождения, имеющих разные конструктивные решения у разных производителей, внутренняя полость колпачка может иметь различный объем. Эти особенности необходимо принимать во внимание в процессе лигирования, т.к. обе ситуации, как аспирации недостаточного объема варикозного узла, так и избыточного его объема с большим участком подслизистого слоя, могут явиться причиной возникновения интра- и послеоперационных осложнений в виде соскакивания лигатуры, разрыва варикса с последующими кровотечением или формирования стриктуры в отдаленном послеоперационном периоде (Рис. 3).
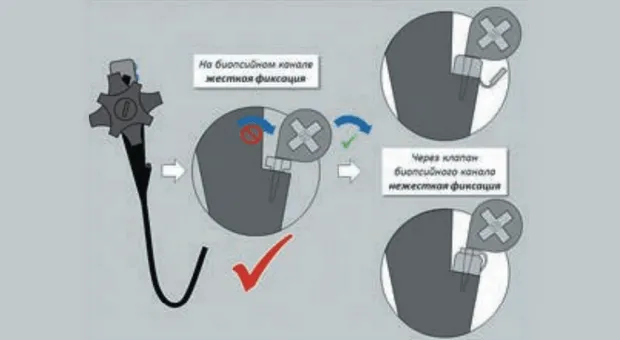
Особое внимание заслуживают некоторые особенности монтажа рукоятки лигирующего устройства на биопсийном канале эндоскопа (Рис. 4). Принципиальное значение имеет герметичное расположение конструкции, которое позволяет беспрепятственно добиться оптимального разрежения в колпачке при аспирации варикса. С учетом возможных несоответствий диаметра стыкуемых частей, обусловленных различиями в строении эндоскопов и лигирующих устройств различных компаний производителей, фиксация рукоятки лигатора на биопсийном канале может быть осуществлена как непосредственно на наружном отверстии канала, так и через герметизирующий резиновый колпачок. Другим важным практическим аспектом является надежная жесткая фиксация рукоятки лигатора, которая обеспечивает стабильность конструкции на всех этапах операции.
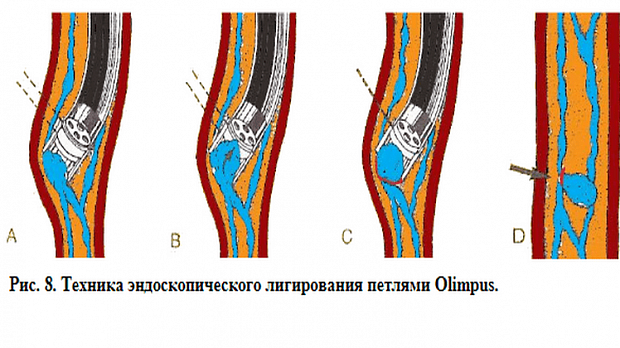
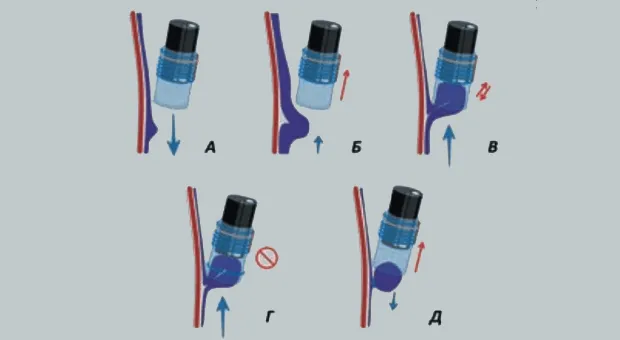
При минимальной инсуфляции воздуха определяли варикозный узел наибольшего размера или с наличием наиболее выраженных предикторов кровотечения с наличием супервариксов или «вишневых пятен» (Рис. 5). Выбранный варикозный узел на аспирации максимально втягивали в просвет колпачка до полного касания его объектива эндоскопа и появления «красного пятна» в поле зрения. Низкоамплитудные движения дистальным концом аппарата облегчали подвижность слизистой и полноценное заполнение полости колпачка. Излишняя аспирация варикса нецелесообразна, т.к. может приводить к попаданию тканей в биопсийный канал аппарата и перфорации вены на фоне разреженного давления. В последующем на высоте аспирации, избегая активных движений эндоскопом, сбрасывали игатуру на основание варикса. Освобождение лигированных тканей из колпачка осуществлялось путем аккуратного извлечения аппарата на 2–3 см на фоне возобновления подачи воздуха, способствующего выталкиванию лигированных тканей. В последующем кольца накладывали по спирали, избегая наложения лигатурных колец в одной плоскости по окружности пищевода с целью профилактики дисфагии в ближайшем послеоперационном периоде и формирования стриктуры на более поздних сроках (Рис. 6). В зависимости от степени выраженности ВРВ за сеанс накладывали до 10 лигатур. При проведении лигирования после предварительного временного гемостаза первую лигатуру накладывали на тромбированный варикс, а затем лигировали остальные ВРВ пищевода.
Результаты
Среднее время оперативного вмешательства составило 10 минут (5–15 минут). В двух наблюдениях отмечались интраоперационные кровотечения, обусловленные соскакиванием наложенной лигатуры (1) и травмой вены краем лигирующего колпачка (1). Оба осложнения устранены повторным лигированием с вовлечением источника кровотечения и не потребовали изменения лечебной тактики. В день вмешательства пациентам был разрешен прием только прохладной негазированной воды. Со второго дня разрешали питание прохладной, жидкой или протертой пищей. У пациентов с наличием загрудинной боли назначали препараты группы НПВС. Болевой синдром обычно купировался к вторым — третьим суткам. Средний койко-день составил 2 дня. Повторный эндоскопический осмотр в ранние сроки после операции (до 10 дней) считали нецелесообразным. Более того, считаем, что оно провоцирует риск развития кровотечения, т.к. приходится на пик эрозивно-язвенного поражения, обусловленного отхождением лигатур.
Контрольная ЭГДС назначалась с интервалом 1 раз в 3 месяца и при наличии новых стволов варикозных вен проводились повторные лигирования. Всего 10 (4,7%) пациентам из группы наблюдения потребовались повторные лигирования (от 1 до 3 раз за период наблюдения). У 3 (1,4%) пациентов, которым было выполнено лигирование в экстренном порядке, развились послеоперационные кровотечения (от 3 до 7 дней послеоперационного периода). После выполнения ЭГДС и констатации состоявшегося кровотечения, устанавливался зонд Сенгстакена-Блэкмора с последующим проведением склеротерапии. 2 (0,6%) пациента с кровотечениями умерли в отделении реанимации на фоне нарастания полиорганной недостаточности. Оба имели терминальную стадию цирроза печени класса С по классификации Чайлд-Пью.
В настоящее время все пациенты, которым выполнено эндоскопическое лигирование ВРВ пищевода, находятся под динамическим наблюдением специалистов-гепатологов отделения заболеваний печени МКНЦ с проведением мониторинга выраженности портальной гипертензии. Повторные лигирования ВРВ потребовалось 26 (12,3%) пациентам наблюдаемой группы.
Вывод:
Статьи по теме
Рекомендуемые статьи
При эндоскопическом исследовании в случае бронхоэктазов в стадии ремиссии выявляется
частично диффузный бронхит I степени воспаления
Активируйте PUSH уведомления в браузер
Отключите PUSH уведомления в браузер
Содержание
Интернет магазин
Популярное
- О нас
- Правовые вопросы
- Политика
обработки персональных
данных EndoExpert.ru - Связаться с нами
- Стать партнером
© 2016-2022 EndoExpert.ru

Вы находитесь в разделе предназначенном только для специалистов (раздел для пациентов по ссылке). Пожалуйста, внимательно прочитайте полные условия использования и подтвердите, что Вы являетесь медицинским или фармацевтическим работником или студентом медицинского образовательного учреждения и подтверждаете своё понимание и согласие с тем, что применение рецептурных препаратов, обращение за той или иной медицинской услугой, равно как и ее выполнение, использование медицинских изделий, выбор метода профилактики, диагностики, лечения, медицинской реабилитации, равно как и их применение, возможны только после предварительной консультации со специалистом. Мы используем файлы cookie, чтобы предложить Вам лучший опыт взаимодействия. Файлы cookie позволяют адаптировать веб-сайты к вашим интересам и предпочтениям.
Я прочитал и настоящим принимаю вышеизложенное, хочу продолжить ознакомление с размещенной на данном сайте информацией для специалистов.













.jpg)




.png)

















Комментарии