Полный текст статьи:
Принципы скрининга
Определение термина "скрининг" (применимо к неопластической патологии толстой кишки) - выявление пациентов с наиболее вероятным наличием колоректального рака (КРР) или аденоматозных полипов среди лиц без симптомов данной патологии.
Основные принципы скрининга КРР:
- Пациенты с клиническими симптомами КРР не подлежат скринингу, а должны быть обследованы в соответствии с подозреваемым заболеванием.
- Семейные и индивидуальные факторы риска должны быть оценены при решении вопроса о методе и времени начала скрининга.
- Врач должен рекомендовать дальнейшее обследование толстой кишки после положительного результата скринингового теста.
- Пациент должен быть проинформирован о положительных и отрицательных сторонах каждого из применяемых тестов и схем, что позволит ему сделать информированный выбор.
Скрининговые тесты
Существует 4 основных скрининговых теста для выявления КРР:
- анализ кала на скрытую кровь,
- гибкая сигмоидоскопия,
- фиброколоноскопия (ФКС)
- ирригоскопия методом двойного контрастирования толстой кишки.
В последнее время к ним добавилась виртуальная колоноскопия. Ряд авторов настаивают на сочетании двух методов, как например: анализ кала на скрытую кровь с последующей сигмоидоскопией.
Самым дешевым и широко используемым методом скрининга является анализ кала на скрытую кровь, основанный на выявлении обладающего пероксидазной активностью гемоглобина с помощью гуаякового теста, бензидиновой или пирамидоновой пробы. Большинство тестов используемых в амбулаторной практике основаны на клее "гуаяк" который может окисляться в присутствии пероксидазы и перекиси водорода. Порядок проведения теста на скрытую кровь незначительно варьирует в зависимости от типа теста и описан во многих руководствах. Основными его недостатками являются большое количество ложноотрицательных, когда полипы или опухоль толстой кишки остаются не выявленными, и ложноположительных результатов, когда для исключения патологии пациенту приходиться проходить неприятную, дорогую и таящую в себе определенный риск процедуру - фиброколоноскопию. Обычно опухоли толстой кишки кровоточат незначительно и их трудно выявить с помощью теста на скрытую кровь. Чаще кровоточат образования более 2 см в диаметре [6]. Эффективность теста зависит от размера и локализации опухоли, большое влияние на него так же оказывает диета и ряд медикаментозных средств. Для уменьшения числа ложноположительных и ложноотрицательных результатов за несколько дней до исследования рекомендуется исключить употребление мяса, нестероидные противовоспалительные препараты, препараты железа и антиоксиданты типа витамина С. Тест желательно проводить с пробами, взятыми из нескольких порций кала (3 последовательных дефекации). С помощью данного теста невозможно определить количество крови в стуле, он так же неспецифичен, так как при доброкачественных заболеваниях: геморрое, язве желудка и двенадцатиперстной кишки, воспалительных заболеваниях кишечника он также может быть положительным. Разработаны несколько вариантов данного теста (Hemoc-cult, Hemoccult II), однако их чувствительность не превышает по самым оптимистичным данным 50%, а при ранних формах КРР составляет только около 5-10% [9]. Lieberman D et al. сообщает о низкой чувствительности этого теста (23,9%) даже в диагностики опухоли более 10 мм в диаметре. В этом же исследовании ложно положительные результаты встречались в 6,2 % случаев [14]. По данным Letsou G et al. у 59% пациентов с полипами и у 36% с раком толстой кишки тест на скрытую кровь был отрицательным [12]. Проведенное в Германии скрининговое обследование более 60 тысяч пациентов 47-75 лет с использованием теста на скрытую кровь показало снижение смертности от рака толстой кишки в течении 10 лет в группе скрининга на 18% [10]. Рекомендуется проводить тест на скрытую кровь по крайней мере один раз в год. При сравнении двух скрининговых методик, использующих тест на скрытую кровь - ежегодное прохождение теста или раз в два года, выживаемость в группе ежегодного скрининга была достоверно большей [15].
Следующим шагом в обследовании пациента с положительным результатом теста на скрытую кровь должна являться фиброколоноскопия, либо ирригография с двойным контрастированием (желательно в сочетании с сигмоидоскопией).
Использование комбинации теста на скрытую кровь и сигмоидоскопии повышает эффективность скрининга по сравнению с любым из этих методов, взятых отдельно. Однако даже сочетание однократного теста на скрытую кровь с сигмоидоскопией позволяет выявить злокачественную опухоль толстой кишки только у 75,8% пациентов [14].
Сигмоидоскопия позволяет успешно диагностировать КРР левой половины толстой кишки [19]. На основе обследования 2885 пациентов Lieberman D et al. сообщал, что гибкая сигмоидоскопия позволяет выявить неоплазму кишки в 70,3% случаев [14], по данным других авторов эта методика позволяет выявить до 95 % аденом и 80% случаев инвазивного КРР [18]. Однако проксимальные отделы ободочной кишки для обследования этим способом недоступны. Недостатком является и необходимость повторного исследования - ФКС, при выявлении патологии левой половины толстой кишки. На основе обследования 4411 пациентов Muller et al. сообщает о 60 % снижении риска смерти от колоректального рака при использовании скрининговой сигмоидоскопии [16]. Сигмоидоскопия проводится либо гибким сигмоидоскопом - аппаратом длиной около 35-60 см, либо ригидным ректороманоскопом длинной 25-30 см, хотя может выполняться и стандартным фиброколоноскопом. Необходимо подчеркнуть, что подготовка к сигмоидоскопии должна быть такой же, как и к ФКС. К сожалению 2-3 клизмы утром перед исследованием, иногда рекомендуемые для подготовки, часто не позволяют провести адекватную очистку исследуемого участка толстой кишки, приводя к сложностям при выполнении исследования и определенным сомнениям в его результатах. Участок толстой кишки, который может быть осмотрен при выполнении сигмоидоскопии, варьирует от места перехода сигмовидной в нисходящую ободочную кишки до селезеночного изгиба, а иногда и левой половины поперечно-ободочной кишки. Принципы выполнения сигмоидоскопии полностью соответствуют таковым при ФКС и приведены ниже. Рекомендуется проводить сигмоидоскопию по крайней мере 1 раз в 3-5 лет. Выбор такого промежутка времени между осмотрами обусловлено рядом факторов: существуют доказательства, что скрининговая эффективность сигмоидоскопии одинаковы при ежегодном осмотре и при осмотре раз в три года; развитие злокачественной опухоли из полипа редко происходит быстрее чем за 3 года [8, 21]. По данным ряда авторов "защитный эффект" сигмоидоскопии может длиться до 10 лет [20].
Пациенты с полипами или опухолями толстой кишки, выявленными при сигмоидоскопии должны в обязательном порядке пройти фиброколоноскопию или ирригографию.
Ирригография с двойным контрастированием является достаточно чувствительным методом выявления КРР и аденом больших размеров (более 90%). Ряд авторов сообщают о более высокой его эффективности при инфильтративном росте опухоли [4]. Недостатками ирригографии являются низкий процент диагностики раннего КРР, в особенности его поверхностно распространяющихся форм, значительное количество ложно положительных результатов и невозможность морфологической верификации диагноза. Данная методика позволяет выявить 50-80% полипов менее 1,0 см, 70-90% полипов более 1,0 см и 55-85% рака стадии A, B по Duke [5, 7]. В любом случае при обнаружении патологии проведение ФКС необходимо для подтверждения и морфологической верификации диагноза. Winawer S et al. на основе обследования 973 пациентов сравнил эффективность диагностики полипов толстой кишки у больных, ранее перенесших полипэктомию путём сравнения исследования кишечника с двойным контрастированием с барием и ФКС [23]. Ирригография выявила только 39% полипов, обнаруженных при ФКС, причем эта цифра варьировала от 32 до 52 % при образованиях менее 0,5 и более 0,6 см соответственно. Т.е. степень выявления полипов при ирригографии в значительной степени зависела от их размеров. Необходимо отметить, что не было выявлено 48% аденом размером больше 1,0 см - наиболее опасных в плане озлокачествления. При проведении ФКС не были выявлены 20% аденом (26% и 6% при образования менее 0,5 см и 0,6 - 1,0 см соответственно), диагностированных с помощью ирригографии, однако не одного образования более 1,0 см в диаметре пропущено не было. Подготовка и техника выполнения ирригографии прекрасно изложена Л.М. Портным в методическом пособии [4]. Он отмечает, что только хорошая подготовка кишечника к исследованию делает его высокоинформативным. Пероральная подготовка препаратом Фортранс является, по его мнению, методом выбора. Частота выполнения ирригографии с двойным контрастированием с целью скрининга КРР - 1 раз в 5 лет.
Фиброколоноскопия в настоящее время играет ведущую роль в установлении или исключении колоректальной патологии [2,13]. Однако не следует считать ФКС методом абсолютно и 100% исключающим патологию толстой кишки. Так, по данным П.А. Никифорова у 28 из 377 пациентов через год после выполнения колоноскопии был выявлен рак II или III стадии, а у 34 - рак I стадии, что косвенно свидетельствует о пропуске этой патологии при первичном осмотре [2]. Rex et al сообщает о пропуске 25% аденом размером менее 10 мм и 6% размером более 10 мм при стандартной ФКС [17]. В одном из исследований скрининговая ФКС позволила уменьшить встречаемость колоректального рака на 3570 случаев на 100000 населения в течении 10 лет [16]. Об успешно выполненной ФКС можно говорить только при условии достижении аппаратом купола слепой кишки. ФКС проводится пациентам после адекватной подготовки кишечника. Необходимо подчеркнуть, что под термином "адекватная подготовка" подразумевается полное удаление содержимого толстой кишки на всем ее протяжении (допускается только наличие небольшого количества прозрачной жидкости). Пероральная подготовка является способом выбора, так как приводит к адекватной очистке толстой кишки более чем в 95% случаев, легче переносится пациентом, связана с меньшим риском осложнений и побочных эффектов, чем очистительная клизма.
Важность полноценной очистки толстой кишки можно проиллюстрировать на следующем клиническом примере: Больная Р. 28 лет, была направлена на ФКС с подозрением на опухоль правой половины толстой кишки. Поскольку за 15 суток до обследования женщине было выполнено кесарево сечение, было принято решение о проведении исследования под общим обезболиванием. Подготовка к процедуре проводилась по принятой на тот момент методике - две клизмы по 1,5 литра вечером в день, предшествующий исследованию и две утром в день исследования. Клизмы выполнялись опытной медицинской сестрой. При осмотре уже на уровне сигмовидной кишки было обнаружено большое количество содержимого, которое с уровня селезеночного изгиба ободочной кишки полностью закрывала все стенки кишки, позволяя, однако, провести аппарат по просвету до купола слепой кишки. В связи со сложностями с повторным применением наркоза решено было продолжить процедуру. Патологии найдено не было. Однако клинические проявления, характерные для токсикоанемической формы опухоли толстой кишки позволили усомниться в результатах ФКС. При диагностической лапароскопии выявлена опухоль восходящего отдела ободочной кишки с преимущественно эндофитным ростом без стенозирования просвета кишки. Была произведена правосторонняя гемиколэктомия с анастомозом. Осмотр макропрепарата позволил сделать вывод о том, что при условии адекватной подготовки опухоль несомненно была бы выявлена во время эндоскопического осмотра (ФКС).
Наш опыт позволяет утверждать, что препарат для перорального очищения кишечника Фортранс является оптимальным средством подготовки к проведению ФКС, сигмоидоскопии и ирригографиии. Макроголь 4000, лежащий в основе препарата Фортранс не метаболизируется и не всасывается в кишечнике, обеспечивает эффективный лаваж без развития электролитных нарушений и побочных явлений. Для подготовки к исследованию принимают 3-4 пакетика препарата, растворив каждый в литре воды. Пациентам с запорами рекомендуется приём 4 пакетиков, при жидком стуле - трёх. Несмотря на необходимость выпить достаточно большое количество жидкости (3-4 литра), средний темп приёма препарата - 1 стакан каждые 15 минут, в подавляющем большинстве случаев делает это необременительным для пациента и легко им выполняется. Выделение промывных вод начинается в большинстве случаев через 60-80 минут после начала приёма препарата и продолжается до 45-60 минут после окончания его приема. При подготовке к амбулаторному обследованию мы не видим альтернативы пероральному методу подготовки, т.к. только очень небольшой процент населения может эффективно очистить кишечник с помощью клизм.
В данной работе не будем подробно останавливаться на технических аспектах выполнения ФКС, ограничившись лишь общими принципами:
- Кишку раздувать воздухом настолько мало, насколько это возможно для поддержания обзора, проводить аспирацию излишков воздуха при каждой возможности.
- Избегать формирования лишних петель.
- Отступать обратно и "присборивать" кишку при каждой возможности.
- Оценивать расстояние, на которое введён колоноскоп, ориентируясь на анатомические особенности кишки (селезёночный угол на 50 см от края ануса).
- Обращать внимание на ощущения дискомфорта пациентом, что говорит о чрезмерном образовании петель или чрезмерном раздувании кишки.
Применение кишечного спазмолитика - Дицитела в дозировке 50 мг 3 раза в день в течение 3 дней до исследования и 50 мг непосредственно пе-ред выполнением ФКС позволяет уменьшить неприятные ощущения во время и после процедуры. Частота проведения колоноскопии как скринингового метода в группе пациентов средней степени риска - 1 раз в 5-10 лет.
Новым методом диагностики патологии толстой кишки является виртуальная колоноскопия, впервые предложенная в 1994 году. Она позволяет на основе множества срезов, полученных с помощью компьютерного томографа и обработанных специальной программой получить изображение толстой кишки изнутри. Этот метод позволяет выявлять образования более 10 мм в 90% случаев, а менее 10 мм в 70-80% случаев [11]. Однако возможны и ложноположительные результаты, чаще всего обусловленные неадекватной подготовкой. Большим недостатком виртуальной колоноскопии является невозможность морфологической верификации диагноза. Данных о необходимой частоте выполнения виртуальной колоноскопии с целью скрининга в доступной литературе нами найдено не было.
Табл.1 Чувствительность основных скрининговых тестов
| Скрининговые тесты | Чувствительность (%) |
|
| Образование менее 10 мм | Образование более 10 мм |
| 1. Тест на скрытую кровь | Около 17 | 23,9 |
| 2. Сигмоидоскопия | Около 65* | 70,3* |
| 3. Бариевая клизма | 32-52 | 48-90 |
| 4. Фиброколоноскопия | 75-85 | 94 |
| 5. Виртуальная колоноскопия | 70-80 | 90 |
*Чувствительность сигмоидоскопии в выявлении образований прямой и сигмовидной кишки аналогична таковой при ФКС.
У пациентов повышенной группы риска по колоректальному раку скрининговые методы и частота их проведения не отличаются от группы лиц со средней степенью риска, но начинаться скрининг должен с 40 лет, или на 10 лет раньше, чем самый ранний возраст возникновения рака толстой кишки у родственника.
Скрининг КРР и предраковых заболеваний
В литературе приводятся различные схем скрининга КРР как для общей популяции так и для групп риска по данному заболеванию [1]. Большинство этих схем сходны и отличаются друг от друга в деталях. Предлагаемая нами программа скрининга в целом основана на тех же принципах и представлена в виде единого алгоритма.
Алгоритм скрининга













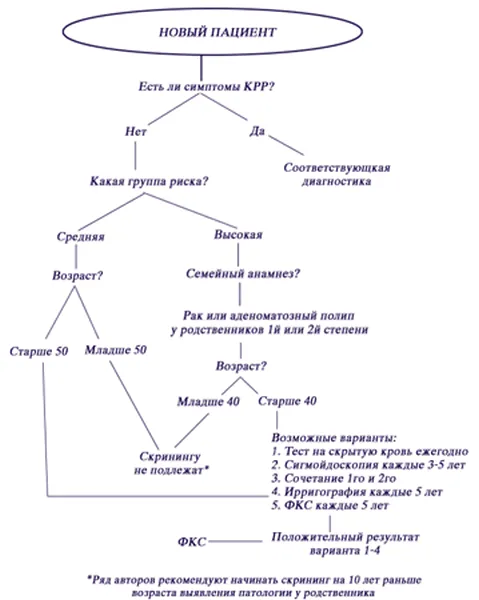
.jpg)





.png)


















Комментарии