- Компании
- Takeda. О компании, буклеты, каталоги, контакты
- Olympus. О компании, буклеты, каталоги, контакты
- Boston Scientific. О компании, буклеты, каталоги, контакты
- Pentax. О компании, буклеты, каталоги, контакты
- Fujifilm & R-Farm. О компании, буклеты, каталоги, контакты
- Erbe. О компании, буклеты, каталоги, контакты
- Еще каталоги
- Мероприятия
- Информация
- Обучение
- Классификации
- Атлас
- Quiz
- Разделы
- Пациенту
QR-код этой страницы
Для продолжения изучения на мобильном устройстве ПРОСКАНИРУЙТЕ QR-код с помощью спец. программы или фотокамеры мобильного устройства
Статьи: Современные аспекты фотодинамической терапии
| Авторы: | Kenneth K. Wang, MD 2000г. |
Введение:
Фотодинамическая терапия (ФДТ) была одобрена для использования в США с декабря 1998 года. Показания к ее применению вышли за пределы патологии пищеварительного тракта и включают рак легких и кожи. В дополнение к этому появились сообщения о новых показаниях для применения ФДТ в лечения заболеваний желудочно-кишечного тракта (ЖКТ) включая патологию пищевода (в основном пищевод Барретта) и заболевания желудка, ДПК, билиарного и панкреатического трактов [1-4]. Основой для столь широкого применения ФДТ является ее способность к оказанию лечебного воздействия на большие области слизистой без необходимости их полной визуализации. Терапевтическое воздействие может осуществляться через фиброволокно, которое проводит свет перпендикулярно оси эндоскопа, что делает эту технологию идеальной для ЖКТ. Также наблюдается прогресс в способах доставки светового излучения и лазерных технологиях, что сделало эту процедуру гораздо более легкой для применения, чем в прошлом.
Полный текст статьи:
Технология
ФДТ заболеваний ЖКТ может проводиться путем инъекции Фотофрина II. Он обычно вводится внутривенно в дозе 2 мг/кг за 48 часов до проведения эндоскопии с фотооблучением. Хотя формула препарата не претерпела изменений Администрация по пищевым продуктам и лекарствам США обновила данные по длительности кожной фоточувствительности связанной с приемом препарата, которая составляет 30-90 дней после введения. Эти цифры более соответствуют клиническому опыту. Однако пациент может снизить этот период фоточувствительности путем дозированного действия солнечного света на кожу, что приводит к разрушению препарата в ней в результате процесса называемого "photobleaching."[5]. Этот препарат недавно был продан его первым владельцем QLT (Ванкувер, Британская Колумбия) Канадской компании Axcan Pharma (Монреаль, Квебек). Это привело к изменению дистрибьютора препарата в США от Sanofi к Axcan.5-аминолевулиновая кислота (5-ALA) так же применяется в США, но в настоящее время только в сфере дерматологии. Фотосенсибилизаторы второго поколения, дающие возможность более глубокого разрушающего эффекта на патологические ткани и с кожной фоточувствительностью только в течение 1-3 дней в настоящее время проходят клинические испытания. Фотооблучение осуществляется светом лазера с помощью фиброволоконного рассеивателя проведенного через биопсийный канал стандартного эндоскопа. В прошлом, длинна рассеивателя была ограничена 1,0-2,5 см, что приводило к повышению длительности процедуры при необходимости облучать большие участки тканей т.к. приходилось перемещать фиброволокно через каждые 2,5 см патологического участка ЖКТ. Недавно разработанный рассеиватель длинной 5,0 см облегчил выполнение процедуры. Появления рассеивателей такой длинны делает необходимым использование измерителей мощности излучения для его адекватной установки. Т.к. работа лазера оценивается на основе мощности излучения на верхушке рассеивателя, все фиброволокно должно быть помещено в измеритель мощности для получения правильного результата. В дополнении к этому был разработан баллонный рассеиватель, предназначенный для лечения длинных сегментов пищевода Барретта, который позволяет поместить 9 см фиброволокно в специальный 7 см баллон [6]. Этот баллон устанавливается в необходимое положение по проводнику под контролем детского гастроскопа. В коммерческой продаже этот баллон в настоящее время отсутствует. Красный свет лазера, проходящий через фиброволокно рассеивателя и активирующий фотосенсибилизатор ранее генерировался путем использования аргонового или содового-титаново-фосфатного/ неодим: иптрий-алюминий-гранатового (KTR-YAG) лазеров с целью заставить цветные лазеры дать необходимую длину волны. Этот тип лазеров был относительно громоздким и иногда требовал использования специальных источников питания и охлаждения. Размер и сложность этих устройств был обусловлен необходимостью совместного использования двух разных типов лазеров. Значительно более маленькие, простые и меньше весящие устройства для фотооблучения были созданы с помощью диодной лазерной технологии (630 PDT Laser, Model T2USA, Diomed, Кембридж, Великобритания). Эти лазеры могут быть помещены в стандартную эндоскопическую стойку и используют нормальную силу тока. Этот прогресс в сфере технологии уменьшил сложность ФДТ и должен значительно уменьшить уровень ее осложнений.
Применение при патологии пищевода
ФДТ была изначально одобрена для паллиативного лечения рака пищевода, для которого другое лечение не возможно. Было показано, что оно эффективнее абляции высокоэнергетическим неодим: иптрий-алюминий-гранатовым лазером (Nd:YAG) [7]. Это лечение применяется как для аденокарциномы так и плоскоклеточного рака пищевода как с паллиативной целью так и для радикального лечения [8]. Лечебное воздействие осуществляется легко т.к. пищевод просто достижим при выполнении эндоскопии. Терапия наиболее эффективна при раке с обструкцией и резким сужением просвета пищевода, что делает термальное паллиативное воздействие, например Nd:YAG лазером более сложным. ФДТ также высоко эффективна в областях пищевода сложных для установки стента, что наиболее часто встречается в проксимальных его отделах. Sodium porfimer вводится пациенту в дозе примерно 2,0 мг/кг за примерно 48 часов до облучения. Затем выполняется эндоскопия с подведением к опухоли цилиндрического фиброволоконного рассеивателя диаметром около 1 мм. Длинна фиброволокна выбирается в зависимости от протяженности опухоли, с тем расчетом, что бы некоторое количество нормальных тканей захватывалось в область облучения (для гарантии адекватного воздействия на опухоль). Сила светового воздействия обычно соответствует 400 милливаттам на сантиметр фиброволокна облучающего опухоль и общей дозе 300 джоулей на сантиметр фиброволокна. Т.к. некроз тканей не виден сразу после облучения, некоторые эндоскописты предпочитают осмотреть область лечения через 1-2 дня, что бы быть уверенными в адекватном его объеме. Если ответа на терапию не получено, то проводится повторное облучение в дозе 80 джоулей на сантиметр фиброволокна. Исследования показывают, что паллиативный эффект лечения рака пищевода через месяц после лечения имеет место в 32 % случаев при использовании ФДТ и 20 % в случае Nd:YAG лазера [7].ФДТ так же используется для радикального лечения поверхностных случаев рака пищевода у пациентов имеющих противопоказания к хирургическому лечению. Первые сообщения указывали, что ФДТ может быть эффективна в лечении поверхностных опухолей менее 2 см в диаметре у 74 % пациентов в сроках наблюдения 5 лет, хотя сроки наблюдения в этой группе были ограничены в связи с сопутствующей патологией [8]. Недавние исследования показали, что опухоли меньшего размера лучше отвечают на ФДТ и опухоль должна проникать вглубь не более чем на 2 мм для достижения успешной абляции при использовании в качестве фотосенсибилизатора ALA [9]. Использование эндоскопической резекции слизистой имеет основное преимущество в точной установки глубины пенетрации опухоли, что должно помочь эндоскопистам в выборе оптимальных кандидатов для ФДТ. Одной из наиболее интересных сфер применения ФДТ является пищевод Барретта (ПБ) [1,10]. Надежды связаны с циркулярным повреждающим воздействием на патологические ткани, что возможно при ФДТ, при диффузном поражении слизистой, что имеет место при ПБ. Начальные исследования показали способность ФДТ устранять дисплазию высокой степени у почти 90 % пролеченных пациентов [1]. В дополнение к этому все сегменты ПБ были полностью устранены у 1/3 пациентов. Это было достигнуто при применении существующей в настоящее время - технологии введения sodium porfimer в дозе 2 мг/кг и дозы облучения около 200 джоулей на сантиметр фиброволокна рассеивателя. ФДТ проводилась с использованием такого же цилиндрического рассеивателя, как и при паллиативном лечении рака пищевода. Контрольная эндоскопия, проводившаяся через 48 часов после первой процедуры, являлась стандартной процедурой. При обнаружении "пропущенных" областей или оценке лечебного воздействия как "неполного" проводилась добавочная терапия в дозе 50 джоулей на сантиметр фиброволокна. Основной проблемой связанной с этим видом терапии являются осложнения, наиболее серьезное из которых - формирование стриктур и кожная фотосенсибилизация [11]. Стриктуры формируются у примерно 28 % - 35 % всех пролеченных пациентов. Требующими решения техническими задачами остается разработка лучших облучающих устройств как, например, баллонный рассеиватель и улучшенных фотосенсибилизаторов дающих кожную фоточувствительность только в течение 1- 14 дней. Некоторые, интенсивно изучаемые в Европе фотосенсибилизаторы, такие, как ALA, могут назначаться перорально в день облучения [12]. Важным вопросом, ответ на который еще предстоит получить является отдаленный результат лечения т.к. преимущество абляции слизистой над наблюдением при ПБ с дисплазией высокой степени не доказано. Предварительные результаты продолжающегося проспективного рандомизированного исследования включающего 208 пациентов с дисплазией высокой степени и сравнивающие результаты применения ФДТ в сочетании с ингибиторами протонной помпы и только ингибиторов протонной помпы обнаружило, что ФДТ имеет значительное преимущество в сфере ингибиции развития рака. Однако это заключение базируется на предварительном анализе проведенном спустя 6 месяцев после включения последнего пациента в исследование. Хотя долговременная эффективность этой терапии не изучена, имеются указания, что для успеха может требоваться полная эрадикация слизистой ПБ [13]. Генетический дефект слизистой может сохраняться после ФДТ несмотря на гистологическое улучшение. Другой потенциальной проблемой абляции является наличие слизистой ПБ лежащей под нормальным плоским эпителием. Имеется сообщение о, по крайней мере, одном таком случае, что показывает, что карцинома может развиваться и при этом типе слизистой [14]. В настоящее время ФДТ по поводу ПБ, как и другие вмешательства основанные на абляции, должны применяться только у избранных пациентов. Необходимость наблюдения за пациентами сохраняется и после выполнения процедуры.Применение при патологии желудка
ФДТ в основном применяется для радикального лечения у пациентов с поверхностными желудочными неоплазмами и противопоказанным хирургическим лечением. ФДТ с sodium porfimer в дозе 2 мг/кг и дозой облучения 30 - 50 джоулей на сантиметр квадратный, как было выявлено, ведет к излечению поверхностного рака желудка у 82 % пациентов [15]. Наилучший эффект достигается в случае приподнятых опухолей менее 20 мм в диаметре и незначительно углубленных опухолей менее 10 мм в диаметре [16]. Недавние исследования так же подтвердили эти результаты - примерно 80 % поверхностного рака "кишечного типа" были успешно пролечены ФДТ с использованием в качестве фотосенсибилизатора мезо-тетрагидрофенил-хлорина (mTHPC) [17]. Этот препарат в настоящее время не доступен в США, но известно, что он увеличивает глубину некроза и дает меньшую кожную фоточувствительность, чем sodium porfimer. Сообщается о минимальных побочных эффектах ФДТ в желудке с менее выраженными болевыми ощущениями и меньшим риском формирования стриктур, чем при применении ее в пищеводе [18].Неопластические заболевания поджелудочной железы
Клиническое использование ФДТ в лечении неопластических поражений поджелудочной железы все еще находится в состоянии развития. На основании исследований на животных с использованием mTHPC и феофорбида A выявлено, что эти фотосенсибилизаторы накапливаются в очагах рака поджелудочной железы [19-22]. Исследования с использованием одного из вариантов коммерчески доступного sodium porfimer под названием дериват гематопорфирина, показали, что этот фотосенсибилизатор так же может распределяться в поджелудочной железе [23]. Существуют неопубликованные сообщения о небольшой группе пациентов пролеченных по поводу злокачественных заболеваний поджелудочной железы с помощью mTHPC и использовании техники "кишечной имплантации". Трудностью лечения в случае поджелудочной железы является необходимости обеспечения адекватной дозиметрии светового воздействия на опухоль. Это обычно достижимо только путем использования светочувствительных зондов установленных непосредственно рядом с опухолью, что трудно осуществить клинически. В дополнение к этому mTHPC не доступен в США.Неопластические заболевания билиарного тракта
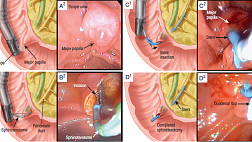
Начальные преклинические работы показали, что холангиокарцинома должна быть чувствительна к ФДТ с использованием sodium porfimer [24]. Лечение хирургически некурабельных холангиокарцином (Bismuth III-IV) этим методом вызвало большой интерес т.к. первые сообщения показали, что у пролеченных с помощью ФДТ 9 человек наблюдалось значительное улучшение качества жизни и выживаемости по сравнению с контрольной группой [25]. Это лечение может проводиться путем введения sodium porfimer в дозе 2,0 мг/кг за 48 часов до облучения. Фотооблучение может быть сложно осуществить в билиарном тракте из-за ригидности коммерчески доступных цилиндрических фиброволоконных рассеивателей. Эта проблема может быть преодолена путем предварительного введения 1,0-2,5 см цилиндрического рассеивателя в билиарный катетер диаметром 8F [26]. Этот катетер имеет отверстие, размером 0,038-inch, на дистальном конце, которое может быть использовано для введения проводника диаметром 0.035-inch. Локализация холангиокарциномы выявляется при РХПГ, устанавливается ее проксимальный и дистальный края. Проводник диаметром 0.035-inch проводится через холангиокарциному. Катетер затем может быть аккуратно продвинут по проводнику к дистальной части области обструкции и затем аккуратно извлечен. Позиция цилиндрического рассеивателя проверяется путем использования флюроскопии. Затем осуществляется лечебное воздействие на холангиокарциному с мощностью 400 милливатт на сантиметр длинны фиброволокна и в общей дозе 180 джоулей на сантиметр квадратный. Наиболее сложным моментом фотооблучения является осторожная установка фиброволокна без нарушения его целостности. После фотооблучения производится установка билиарных катетеров размером 10F или 11.5F для обеспечения дренажа желчи непосредственно после лечения. Возможные осложнения этого лечения включают холангит и длительную кожную фоточувствительность. Хотя этот факт и не доказан, кажется разумным инструктировать пациентов получавших лечение по поводу билиарной обструкции соблюдать осторожность в отношении воздействия солнечного света более длительный период т.к. соединения порфирина экскретируются через билиарную систему.Неопластические заболевания ДПК
Существует сообщение о небольших исследованиях включавших 10 пациентов как с карциномой ампулы БДС так и дуоденальным полипозом [27]. Эти исследователи также использовали производные гематопорфирина в дозе 4 мг/кг, которые должны быть эквивалентны коммерчески доступному sodium porfimer в дозе 2,0 мг/кг. Через 48 часов проводилось лечебное фотооблучение в дозе варьирующей от 50 до 70 джоулей на сантиметр фиброволокна. Об осложнениях (исключая кожную фоточувствительность у 3-х пациентов) не сообщалось. Если зона поражение была ограничена ампулой, могла быть достигнута ее полная абляция, хотя через год часто возникал рецидив. Если опухоль выходила за пределы ампулы, наблюдалось только некоторое уменьшение ее размеров, а большие опухоли переходящие на ДПК на лечение вообще не отвечали. Полипы ДПК у 6 пациентов с семейным аденоматозным полипозом также были пролечены с использованием sodium porfimer [3]. Полный ответ наблюдался у одного пациента с поверхностным очагом рака в полипе. Другое исследование с использованием sodium porfimer у 3-х пациентов с большими полипами ДПК обнаружило уменьшение их размеров на 50 % после лечения [28]. Эти исследования показывают, что ФДТ заболеваний ДПК должно выполняться в случае небольших поражений ампулы БДС или поверхностных полипов ДПК.Неопластические заболевания толстой кишки
Интенсивные доклинические исследования на клеточных и животных моделях показали, что большой спектр фотосенсибилизирующих агентов могут быть эффективными в лечение рака толстой кишки [2,29-31]. В особенности важно то, что ФДТ оставляет коллагеновый слой стенки толстой кишки интактным, в отличие от термального воздействия, что должно уменьшит риск перфорации кишки после лечения [32]. Множество агентов исследовались in vitro, включая фталоцианины, аминолевулиновую, mTHPC, и алюминий сульфацированный фталоцианин. Однако доступно ограниченное количество клинической информации по использованию ФДТ в случае полипов и рака толстой кишки. Восемь пациентов с неполным удалением ворсинчатых опухолей с помощью Nd:YAG лазера получили лечение ФДТ с сочетанием sodium porfimer и производных гематопорфирина [2]. Световое воздействие осуществлялось в дозе 50 джоулей. Положительный ответ, заключающийся в полной элиминации полипа, наблюдался во всех, кроме 2 случаев. ФДТ с использованием mTHPC также применялась и при раке толстой кишки, но результаты его противоречивы [28]. Один из пациентов в этом исследовании был полностью излечен от поверхностного рака 8 мм в диаметре при использовании ФДТ основанной на sodium porphimer.Вывод:
Было установлено, что ФДТ превосходит термальное воздействие в паллиативном лечении рака пищевода. Ее основная роль базируется на возможности воздействия на большие участки слизистой желудочно-кишечного тракта без необходимости их непосредственной визуализации. Большие поверхностные полипы или небольшие очаги рака в областях пищевода, желудка, ДПК и билиарного дерева неудобных для хирургической резекции являются перспективными областями для проведения дальнейших исследований. ПБ с дисплазией высокой степени может стать показанием для данного вида терапии при положительном заключении проводящегося в настоящее время рандомизированного исследования.
Список литературы:
- Wang KK. Photodynamic therapy of Barrett's esophagus. Gastrointest Endosc Clin N Am 2000;10:409-19.
- Loh CS, Bliss P, Bown SG, et al. Photodynamic therapy for villous adenomas of the colon and rectum. Endoscopy 1994; 26:243-6.
- Mlkvy P, Messmann H, Debinski H, et al. Photodynamic therapy for polyps in familial adenomatous polyposisNa pilot study. Eur J Cancer 1995;31A:1160-5.
- Bown SG, Lovat LB. The biology of photodynamic therapy in the gastrointestinal tract. Gastrointest Endosc Clin N Am 2000;10:533-50.
- Georgakoudi I, Nichols MG, Foster TH. The mechanism of Photofrin photobleaching and its consequences for photodynamic dosimetry. Photochem Photobiol 1997;65:135-44.
- Overholt BF, DeNovo RC, Panjehpour M, et al. A centering balloon for photodynamic therapy of esophageal cancer tested in a canine model. Gastrointest Endosc 1993;39:782-7.
- Lightdale CJ, Heier SK, Marcon NE, et al. Photodynamic therapy with porfimer sodium versus thermal ablation therapy with Nd:YAG laser for palliation of esophageal cancer: a multicenter randomized trial. Gastrointest Endosc 1995;42:507-12.
- Sibille A, Lambert R, Souquet JC, et al. Long-term survival after photodynamic therapy for esophageal cancer. Gastroenterology 1995;108:337-44.
- Gossner L, May A, Sroka R, et al. Photodynamic destruction of high grade dysplasia and early carcinoma of the esophagus after the oral administration of 5-aminolevulinic acid. Cancer 1999;86:1921-8.
- Overholt BF. Results of photodynamic therapy in Barrett's esophagus: a review. Can J Gastroenterol 1999;13:393-6.
- Wang KK, Nijhawan PK. Complications of photodynamic therapy in gastrointestinal disease. Gastrointest Endosc Clin N Am 2000;10:487-95.
- Tan WC, Fulljames C, Stone N, et al. Photodynamic therapy using 5-aminolevulinic acid for oesophageal adenocarcinoma associated with Barrett's metaplasia. J Photochem Photobiol B 1999;53:75-80.
- Krishnadath K, Wang KK, Taniguchi K, et al. Persistent genetic abnormalities in Barrett's esophagus after photodynamic therapy. Gastroenterology 2000;119:624-30.
- Overholt BF, Panjehpour M, Haydek JM. Photodynamic therapy for Barrett's esophagus: follow-up in 100 patients. Gastrointest Endosc 1999;49:1-7.
- Kato H, Horai T, Furuse K, et al. Photodynamic therapy for cancers: a clinical trial of porfimer sodium in Japan. Jpn J Cancer Res 1993;84:1209-14.
- Ito Y, Kameya A, Kano T, et al. [Indications and limitations of laser treatment for early gastric cancer and palliative treatments for malignant obstruction of the esophagus and stomach] [in Japanese]. Gan to Kagaku Ryoho 1988;15:1435-9.
- Ell C, Gossner L, May A, et al. Photodynamic ablation of early cancers of the stomach by means of mTHPC and laser irradiation: preliminary clinical experience. Gut 1998;43:345-9.
- Gossner L, Ell C. Photodynamic therapy of gastric cancer. Gastrointest Endosc Clin N Am 2000;10:461-80.
- Keller P, Sowinska M, Tassetti V, et al. Photodynamic imaging of a rat pancreatic cancer with pheophorbide a. Photochem Photobiol 1996;63:860-7.
- Evrard S, Keller P, Hajri A, et al. Experimental pancreatic cancer in the rat treated by photodynamic therapy. Br J Surg 1994;81:1185-9.
- Mlkvy P, Messmann H, Pauer M, et al. Distribution and photodynamic effects of meso-tetrahydroxyphenylchlorin (mTHPC] in the pancreas and adjacent tissues in the Syrian golden hamster. Br J Cancer 1996;73:1473-9.
- Mikvy P, Messman H, MacRobert AJ, et al. Photodynamic therapy of a transplanted pancreatic cancer model using meta-tetrahydroxyphenylchlorin (mTHPC]. Br J Cancer 1997;76:713-8.
- Schroder T, Chen IW, Sperling M, et al. Hematoporphyrin derivative uptake and photodynamic therapy in pancreatic carcinoma. J Surg Oncol 1988;38:4-9.
- Wong Kee Song LM, Wang KK, Zinsmeister AR. Mono-L-aspartyl chlorin e6 (NPe6] and hematoporphyrin derivative (HpD] in photodynamic therapy administered to a human cholangiocarcinoma model. Cancer 1998;82:421-7.
- Ortner MA, Liebetruth J, Schreiber S, et al. Photodynamic therapy of nonresectable cholangiocarcinoma. Gastroenterology 1998;114:536-42.
- Rumalla A, Baron TH, Wang RR, et al. Endoscopic application of photodynamic therapy for cholangiocarcinoma. Gastrointest Endosc. In press 2001.
- Abulafi AM, Allardice JT, Williams NS, et al. Photodynamic therapy for malignant tumours of the ampulla of Vater. Gut 1995;36:853-6.
- Mlkvy P, Messmann H, Regula J, et al. Photodynamic therapy for gastrointestinal tumors using three photosensitizersNALA induced PPIX, Photofrin and MTHPC. A pilot study. Neoplasma 1998;45:157-61.
- Gederaas OA, Rasch MH, Berg K, et al. Photodynamically induced effects in colon carcinoma cells (WiDr] by endogenous photosensitizers generated by incubation with 5-aminolevulinic acid. J Photochem Photobiol B 1999;49:162-70.
- Baumler W, Abels C, Karrer S, et al. Photo-oxidative killing of human colonic cancer cells using indocyanine green and infrared light. Br J Cancer 1999;80:360-3.
- Whitacre CM, Feyes DK, Satoh T, et al. Photodynamic therapy with the phthalocyanine photosensitizer Pc 4 of SW480 human colon cancer xenografts in athymic mice. Clin Cancer Res 2000;6:2021-7.
- Barr H, Tralau CJ, MacRobert AJ, et al. Photodynamic therapy in the normal rat colon with phthalocyanine sensitisation. Br J Cancer 1987;56:111-8.
Статьи по теме
Рекомендуемые статьи
Эндоскопическая ретроградная холангиопанкреатография
- рентген-эндоскопический метод диагностики патологии желчных и панкреатических протоков.
При эндоскопическом исследовании в случае бронхоэктазов в стадии ремиссии выявляется
частично диффузный бронхит I степени воспаления
Активируйте PUSH уведомления в браузер
Отключите PUSH уведомления в браузер
Содержание
Интернет магазин
Популярное
- О нас
- Правовые вопросы
- Политика
обработки персональных
данных EndoExpert.ru - Связаться с нами
- Стать партнером
© 2016-2022 EndoExpert.ru

Вы находитесь в разделе предназначенном только для специалистов (раздел для пациентов по ссылке). Пожалуйста, внимательно прочитайте полные условия использования и подтвердите, что Вы являетесь медицинским или фармацевтическим работником или студентом медицинского образовательного учреждения и подтверждаете своё понимание и согласие с тем, что применение рецептурных препаратов, обращение за той или иной медицинской услугой, равно как и ее выполнение, использование медицинских изделий, выбор метода профилактики, диагностики, лечения, медицинской реабилитации, равно как и их применение, возможны только после предварительной консультации со специалистом. Мы используем файлы cookie, чтобы предложить Вам лучший опыт взаимодействия. Файлы cookie позволяют адаптировать веб-сайты к вашим интересам и предпочтениям.
Я прочитал и настоящим принимаю вышеизложенное, хочу продолжить ознакомление с размещенной на данном сайте информацией для специалистов.













.jpg)





.png)

.jpg)















Комментарии