- Компании
- Takeda. О компании, буклеты, каталоги, контакты
- Olympus. О компании, буклеты, каталоги, контакты
- Boston Scientific. О компании, буклеты, каталоги, контакты
- Pentax. О компании, буклеты, каталоги, контакты
- Fujifilm & R-Farm. О компании, буклеты, каталоги, контакты
- Erbe. О компании, буклеты, каталоги, контакты
- Еще каталоги
- Мероприятия
- Информация
- Обучение
- Классификации
- Атлас
- Quiz
- Разделы
- Пациенту
QR-код этой страницы
Для продолжения изучения на мобильном устройстве ПРОСКАНИРУЙТЕ QR-код с помощью спец. программы или фотокамеры мобильного устройства
Статьи: Классификация опухолей желудочно-кишечного тракта ВОЗ 2019, пятое издание.
Анонс:
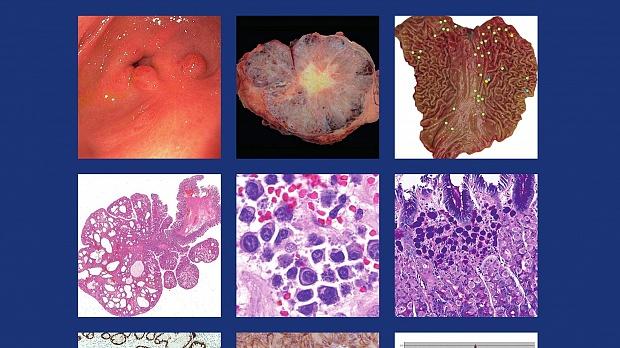
Полный текст статьи:
Коротко
Пятое издание классификации опухолей пищеварительной системы WHO 2019 отражает переход к более интегрированному морфолого-молекулярному подходу. При этом гистопатологическая классификация сохраняет статус основного диагностического стандарта, а молекулярные маркеры используются там, где они действительно влияют на верификацию диагноза, прогноз или выбор лечения.
Что изменилось принципиально
Главное изменение — часть нозологий теперь определяется не только по морфологии, но и по молекулярному профилю. Для ряда опухолей молекулярные тесты из категории желательных перешли в категорию практически значимых или обязательных.
В классификации усилен акцент на клинически значимые маркеры: те, которые помогают уточнить диагноз, оценить биологическое поведение опухоли и выбрать терапевтическую тактику.
Нейроэндокринные неоплазии
Новая логика классификации
Одно из самых важных обновлений касается нейроэндокринных неоплазий. Во всех органах пищеварительной системы предложен единый подход: разделение на хорошо дифференцированные нейроэндокринные опухоли (NET) и плохо дифференцированные нейроэндокринные карциномы (NEC).
Что важно для практики
NET и NEC теперь рассматриваются как разные сущности не только морфологически, но и молекулярно. Для хорошо дифференцированных NET характерны мутации MEN1, DAXX и ATRX, тогда как для NEC типичны изменения TP53 и RB1.
Дополнительно признано, что хорошо дифференцированные NET могут быть высокозлокачественными по пролиферативным критериям — G3 NET. Это принципиально отличает их от NEC, которые по определению являются высокозлокачественными и больше не градуируются как отдельные уровни злокачественности.
MiNEN вместо MANEC
Смешанные опухоли этого спектра теперь объединены в категорию MiNEN — mixed neuroendocrine–non-neuroendocrine neoplasms. Это более точный термин, чем прежний MANEC, и он лучше отражает биологическую неоднородность таких новообразований.
Предраковые поражения
Стандартизация терминологии
Введена более последовательная терминология предшественников инвазивного рака. Для тубулярного отдела ЖКТ предпочтителен термин дисплазия, а для поджелудочной железы, желчного пузыря и билиарного тракта — интраэпителиальная неоплазия.
Двухступенчатая градация
Стандартом стала двухуровневая оценка: low-grade и high-grade. Эта схема заменила прежнюю трехступенчатую систему, в частности в панкреатобилиарной патологии.
Термин, который не рекомендован
Использование термина carcinoma in situ для практической работы по сути не рекомендуется. Его предлагают рассматривать внутри категории high-grade dysplasia / intraepithelial neoplasia.
Опухоли пищевода и желудка
Для аденокарцином пищевода и желудка подчеркивается клиническая значимость тестирования ERBB2 (HER2), поскольку этот маркер влияет на лечебную тактику.
В патогенезе рака желудка усилен акцент на воспалительном механизме, ассоциированном прежде всего с Helicobacter pylori. Также описаны молекулярные подтипы, хотя их внедрение в повседневную практику пока ограничено.
Тонкая и толстая кишка, аппендикс, анальный канал
Лучше описаны молекулярные пути колоректального канцерогенеза, включая традиционные аденомы и зубчатые предшественники. Термин sessile serrated lesion закреплен как предпочтительный.
Для колоректального рака, когда это влияет на лечение, подчеркивается необходимость молекулярного тестирования: MSI, а также расширенного анализа KRAS, NRAS и BRAF.
Опухоль аппендикса, ранее известная как goblet cell carcinoid/carcinoma, переименована в goblet cell adenocarcinoma, что лучше отражает ее биологический потенциал.
Для плоскоклеточных поражений анального канала рекомендованы p16 и HPV-тестирование.
Печень и внутрипеченочные желчные протоки
Классификация опухолей печени стала заметно более молекулярно ориентированной. В качестве одного из ярких примеров выделена фиброламеллярная карцинома с характерной транслокацией DNAJB1-PRKACA.
Для внутрипеченочной холангиокарциномы подчеркнуто разделение на large duct type и small duct type, поскольку эти варианты отличаются по происхождению, молекулярным особенностям и клиническому поведению.
Поджелудочная железа
Для PanIN, IPMN и MCN закреплена двухуровневая система дисплазии по наивысшей выявленной степени. Отдельно выделены intraductal oncocytic papillary neoplasm и intraductal tubulopapillary neoplasm как образования с самостоятельными морфологическими и геномными признаками.
Сущность acinar cell cystadenoma пересмотрена: теперь используется термин acinar cystic transformation of the pancreas, поскольку накоплены данные в пользу ее неневоопластической природы.
Наследственные опухолевые синдромы
Отдельная глава посвящена наследственным синдромам опухолевой предрасположенности. Помимо Lynch syndrome и FAP, расширено описание других полипозов и включен GAPPS как клинически значимый вариант.
Практический вывод
WHO 2019 не отменяет морфологию, а делает диагностику точнее за счет клинически оправданной молекулярной стратификации. Для патоморфолога и клинициста это означает три ключевых последствия: более строгую терминологию, более точную нозологическую верификацию и более тесную связь классификации с прогнозом и выбором терапии.
Список литературы:
Рекомендуемые статьи
При эндоскопическом исследовании в случае бронхоэктазов в стадии ремиссии выявляется
частично диффузный бронхит I степени воспаления
Активируйте PUSH уведомления в браузер
Отключите PUSH уведомления в браузер
Содержание
Интернет магазин
Популярное
- О нас
- Правовые вопросы
- Политика
обработки персональных
данных EndoExpert.ru - Связаться с нами
- Стать партнером
© 2016-2022 EndoExpert.ru

Вы находитесь в разделе предназначенном только для специалистов (раздел для пациентов по ссылке). Пожалуйста, внимательно прочитайте полные условия использования и подтвердите, что Вы являетесь медицинским или фармацевтическим работником или студентом медицинского образовательного учреждения и подтверждаете своё понимание и согласие с тем, что применение рецептурных препаратов, обращение за той или иной медицинской услугой, равно как и ее выполнение, использование медицинских изделий, выбор метода профилактики, диагностики, лечения, медицинской реабилитации, равно как и их применение, возможны только после предварительной консультации со специалистом. Мы используем файлы cookie, чтобы предложить Вам лучший опыт взаимодействия. Файлы cookie позволяют адаптировать веб-сайты к вашим интересам и предпочтениям.
Я прочитал и настоящим принимаю вышеизложенное, хочу продолжить ознакомление с размещенной на данном сайте информацией для специалистов.


.jpg)


















Комментарии