- Компании
- Takeda. О компании, буклеты, каталоги, контакты
- Olympus. О компании, буклеты, каталоги, контакты
- Boston Scientific. О компании, буклеты, каталоги, контакты
- Pentax. О компании, буклеты, каталоги, контакты
- Fujifilm & R-Farm. О компании, буклеты, каталоги, контакты
- Erbe. О компании, буклеты, каталоги, контакты
- Еще каталоги
- Мероприятия
- Информация
- Обучение
- Классификации
- Атлас
- Quiz
- Разделы
- Пациенту
QR-код этой страницы
Для продолжения изучения на мобильном устройстве ПРОСКАНИРУЙТЕ QR-код с помощью спец. программы или фотокамеры мобильного устройства
Обзоры: Cap poliposis (Кеп полипозиз) или полипоз с фибриновой "шапочкой"
Анонс:
Синдром множественных полипов с фибриновой шапочкой

Полный текст статьи:
Cap polyposis
Аникина М.С., ГБУЗ НСО «Государственная Новосибирская областная клиническая больница», 2019 год
Аннотация. Cap polyposis (CP) — редкое заболевание, характеризующееся наличием в толстой кишке гиперемированных воспалительных полипов, покрытых фибринозно-гнойными налетами в виде шапочки на фоне визуально неизмененной слизистой. Впервые СР был описан Г. Уильямсом с соавторами в 1985 году [1]. По данным портала Orphanet (www.orpha.net), посвященного редким болезням, на сегодняшний день в мировой литературе описано 67 случаев данного заболевания. В отечественной литературе сообщений о данной патологии не найдено. Однако в клинической практике пациенты с СР встречаются, и тогда возникает вопрос, не связано ли отсутствие публикаций с низкой осведомленностью врачей и недостаточной клинической настороженностью. Цель обзора — диагностика и лечение СР.
Эпидемиология. По данным Orphanet, распространенность СР < 1:1000 000. Наибольшее количество случаев отмечается на пятом десятилетии жизни, однако описаны случаи заболевания у пациентов любого возраста, включая период новорожденности [2–4]. Выраженных гендерных различий нет [3]. Некоторые авторы отмечают преобладание среди заболевших лиц мужского пола [4].
Этиология и патогенез СР недостаточно изучены. Возможна связь с нарушениями моторики толстой кишки, ишемией, Т-клеточным воспалением и инфекцией [2, 3]. В качестве инфекционного агента рассматривается Helicobacter pylori. Однако H. pylori не был выделен внутри воспалительных полипов толстой кишки. Предполагаемые механизмы, посредством которых H. pylori вызывает внежелудочный СР, включают молекулярную мимикрию и высвобождение медиаторов воспаления [5, 6].
На основании сходных гистологических особенностей была предложена возможная ассоциация с синдромом пролапса слизистой оболочки [7, 8]. Существует гипотеза, что у пациентов с СР аномальная моторика толстой кишки может приводить к выпадению слизистой оболочки при избыточном напряжении во время дефекации, что приводит к локальной ишемии, рецидивирующей травме слизистой оболочки и развитию полипов [9].
Клиническая картина. Основные симптомы СР — ректальное кровотечение (82%) и примесь слизи в кале (46%), которые могут присутствовать в течение недель или месяцев до постановки диагноза [11]. Другие клинические проявления включают боль в животе, тенезмы, потерю веса и запор. В редких случаях у пациентов наблюдается умеренный периферический отек из-за белковой энтеропатии [9]. Также СР может протекать бессимптомно [10].
Лабораторная диагностика. Данные лабораторных тестов, включающие маркеры воспаления, например С-реактивный белок, как правило, в пределах нормы [5]. Однако в редких случаях у пациентов может наблюдаться гипопротеинемия вследствие белковой энтеропатии и железодефицитная анемия вследствие ректального кровотечения [12].
Эндоскопическая диагностика. Основной метод диагностики СР — колоноскопия. СР характеризуется наличием множественных воспалительных полипов, покрытых фибринозно-гнойным налетом в виде шапочки на фоне неизмененной слизистой (рис. 1, 2). Чаще полипы при СР локализуются в прямой или сигмовидной кишке, однако могут быть расположены в любом отделе толстой кишки [2, 12].
Для подготовки к колоноскопии у пациентов с СР используются стандартные подходы. Однако следует уделить особое внимание качеству подготовки толстой кишки к эндоскопическому исследованию: в противном случае характерный симптом — «шапочка» из фибринозно-гнойного налета — может быть принят за последствие плохой подготовки и недооценен.
В 2014 году был проведен метаанализ, включивший 11 исследований, целью которого было сравнение малообъемного полиэтиленгликоля (ПЭГ) в комбинации с аскорбатным комплексом (АК) — МОВИПРЕП®— и ПЭГ стандартного объема (4 л) в качестве препаратов для подготовки кишечника к колоноскопии. Метаанализ выявил, что частота нежелательных явлений — рвоты и тошноты — на фоне подготовки малообъемным ПЭГ в комбинации с АК по сравнению с ПЭГ стандартного объема была ниже. Согласно воронкообразному графику, значимых систематических ошибок не выявлено. Таким образом, малообъемный ПЭГ в комбинации с АК не менее эффективен для очистки кишечника в качестве средства подготовки к колоноскопии, более приемлем для пациентов и характеризуется меньшей частотой нежелательных явлений по сравнению с ПЭГ стандартного объема [13]. Таким образом, для подготовки пациентов с СР к колоноскопии следует рассматривать использование малообъемного препарата ПЭГ с раствором электролитов и АК (МОВИПРЕП®) в сплит-дозе или одноэтапно в день исследования. Схемы подготовки в режиме приема всего объема для очистки кишечника накануне вечером использоваться не должны в связи с неудовлетворительными результатами подготовки правых отделов толстой кишки, что отражено в рекомендациях Европейского общества гастроинтестинальной эндоскопии (European Society of Gastrointestinal Endoscopy) [14].
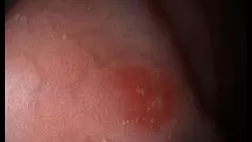
Рисунок 1. СР с поражением прямой кишки у новорожденного ребенка [2].
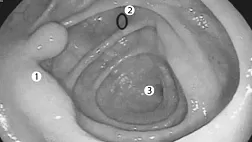
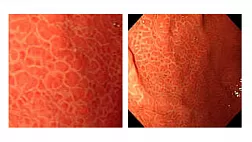
Рисунок 2. СР с поражением ректосигмоидного отдела толстой кишки у пациента 20 лет [12].
А, В. Полиповидные образования, покрытые «шапочками» фибринозно-гнойного экссудата на фоне визуально неизмененной слизистой.
C, D. Осмотр с увеличением: участок аморфного фибринозно-гнойного экссудата, покрывающий длинные извилистые крипты.
Е. На эндосонограмме отмечается значительное утолщение слоев слизистой оболочки толстой кишки.
Гистологическое исследование. При гистологическом исследовании СР представлены ненеопластическими поражениями, состоящими из удлиненных гиперпластических желез со смешанным воспалительным инфильтратом и фибромышечной облитерацией собственной пластинки слизистой (рис. 3, 4 — С). Эти изменения также характерны для синдрома пролапса слизистой, но фибромышечная облитерация более выражена при СР. Синдром пролапса слизистой обычно ограничивается прямой кишкой, в то время как СР обычно включает сигмовидную и/или нисходящую ободочную кишку, а также прямую кишку. Результаты эндосонографии при СР также свидетельствуют о значительном утолщении слизистой оболочки, в то время как синдром пролапса слизистой характеризуется плавным диффузным утолщением подслизистой оболочки и минимальным утолщением собственной пластинки слизистой [12].
Рисунок 3. Гистологическое строение СР [2].
Дифференциальный диагноз проводится с воспалительными полипами при ВЗК, дивертикулярной болезнью, синдромом солитарной язвы прямой кишки, полипозными синдромами — наследственными аденоматозными (семейный аденоматозный и MUTYH-ассоциированный полипозы) и гамартомными (например, семейный ювенильный полипоз). Однако, несмотря на сходство эндоскопической картины, СР может быть дифференцирован гистологически [15, 16].
Лечение и прогноз. Прогноз при СР благоприятный: возможно самоисцеление — описаны случаи спонтанной ремиссии в сроки от 18 месяцев [6, 12, 23]; образования не имеют злокачественного потенциала [2].
Лечение показано только при симптомном течении СР. Из-за редкости заболевания оптимальные схемы лечения не разработаны. При консервативной терапии применяются 5-АСК, глюкокортикоиды и инфликсимаб. Существует определенное сходство между СР и псевдополипами при язвенном колите. Т-клеточное воспаление — возможный механизм эффективности стероидов или инфликсимаба при СР [17]. В то же время есть сообщения о неэффективности инфликсимаба и глюкокортикостероидов. Поэтому их не следует назначать во всех случаях СР [18, 19].
Ограниченные данные, основанные на докладах о единичных случаях или небольших сериях случаев, свидетельствуют об эффективности эрадикационной терапии H. pylori у пациентов с СР на фоне хеликобактерной инфекции. Клиническое улучшение наступало в течение 3 месяцев, деградация полипов, по данным колоноскопии, — в сроки от 6 месяцев. Это позволило предположить, что иммунный ответ на персистенцию H. pylori может быть причиной СР [6, 11, 20]. В то же время применение эрадикационных схем не дает эффекта у пациентов, не инфицированных H. pylori [12].
Синдром пролапса слизистой оболочки включает пролапс прямой кишки, синдром солитарной язвы прямой кишки и глубокий кистозно-полипозный проктит [21]. Эти заболевания вызваны повышением анального давления во время дефекации и хроническим чрезмерным напряжением вследствие запоров. Из-за гистологического сходства между синдромом пролапса слизистой оболочки и СР хроническое механическое повреждение слизистой оболочки из-за аномальной моторики было предложено в качестве решающего патогенетического фактора СР. Борьба с чрезмерным напряжением во время дефекации была успешной стратегией лечения СР в некоторых случаях [8, 9, 22]. С другой стороны, хроническое напряжение во время дефекации отмечается только у 64% пациентов с СР [18].
Хирургические методы применяются при неэффективности консервативного лечения. Считается, что хирургическая тактика должна быть выбрана при сохранении стойких симптомов заболевания через 3 месяца с начала терапии [24]. Чаще всего применяются эндоскопическая петлевая электроэксцизия или петлевая электроэксцизия, дополненная аргоноплазменной коагуляцией. Отмечено, что у пациентов с небольшим количеством полипов — до 10 штук — после эндоскопической полипэктомии клиническая ремиссия сохраняется на протяжении нескольких лет [18]. При невозможности эндоскопического лечения у симптомных пациентов следует рассматривать открытые хирургические вмешательства вплоть до колэктомии. В то же время СР имеет тенденцию к рецидивированию — рецидивные полипы могут возникать как после эндоскопической полипэктомии, так и в зоне анастомозов после резекции кишки [2, 7]. В последнее время в качестве альтернативы резекции толстой кишки рассматривается диссекция в подслизистом слое — ESD (рис. 4). Однако эффективность данного метода лечения СР требует дальнейшего изучения [12].
Рисунок 4. ESD при СР с локализацией в ректосигмоидном отделе толстой кишки у пациента 20 лет [12].
A. Послеоперационные язвы после ESD на сигмовидной кишке и прямой кишке. B. Резецированная слизистая. C. Резецированная слизистая после фиксации, видны признаки кровотечения в полипах. D. Микропрепарат.
Выводы
Cap polyposis — редкое заболевание, характеризующееся наличием множественных воспалительных полипов, покрытых фибринозно-гнойным налетом на фоне визуально неизмененной слизистой, с преимущественной локализацией в прямой и сигмовидной кишке, причем воспалительные полипы могут встречаться в любом отделе толстой кишки. СР может возникнуть у пациентов любой возрастной группы. Основные клинические проявления — ректальные кровотечения и примесь слизи в кале. Также к симптомам СР относятся боли в животе, тенезмы, диарея или констипация. В некоторых случаях СР сопровождается энтеропатией с потерей белка. У большинства пациентов лабораторные показатели находятся в пределах нормы. Основной метод диагностики заболевания — колоноскопия. Для подготовки к колоноскопии следует рассматривать применение препарата МОВИПРЕП® в сплит-режиме. Дифференциальный диагноз проводится в первую очередь с псевдополипами при хронических воспалительных заболеваниях кишечника и наследственными полипозными синдромами. При гистологическом исследовании СР представлен ненеопластическими поражениями, состоящими из удлиненных гиперпластических желез со смешанным воспалительным инфильтратом и фибромышечной облитерацией собственной пластинки слизистой. Прогноз благоприятный, СР не склонен к малигнизации, отмечаются случаи самоисцеления, в лечении нуждаются только пациенты с выраженными симптомами. Терапевтические подходы точно не определены — применяются препараты 5-АСК, глюкокортикоиды, инфликсимаб, проводится эрадикационная терапия Н. рylori, лечение запоров. При неэффективности консервативной терапии следует рассмотреть возможность эндоскопического удаления полипов, а при невозможности эндоскопического лечения проводится резекция пораженного сегмента толстой кишки.
Список литературы
1. Williams G.T., Bussey H.J., Morson B.C. Inflammatory “cap” polyps of the large intestine. Br J Surg. 1985. 72: S133.
2. Kim S.C., Kang M.J., Jeong Y.J., Hwang P.H. A case of cap polyposis with epidermal nevus in an infant. J Korean Med Sci. 2017. May; 32 (5): 880–884. DOI: 10.3346/jkms.2017.32.5.880.
3. Spiethoff A., Hoch J., Jakobs R., Bohrer M.H. Cap polyposis: a rare colorectal disease. Diagnostic Pathology. Volume 2. Article number: S12 (2007).
4. Brunner M., Agaimy A., Atreya R., Grützmann R., Matzel K.E. Cap polyposis in children: case report and literature review. Int J Colorectal Dis. 2019. 34 (2): 363–368. Epub 2018 Nov 13.
5. Akamatsu T., Nakamura N., Kawamura Y., Shinji A., Tateiwa N., Ochi Y., Katsuyama T., Kiyosawa K. Possible relationship between Helicobacter pylori infection and cap polyposis of the colon. Helicobacter. 2004. 9: 651–656.
6. Suzuki H., Sato M., Akutsu D., Sugiyama H., Sato T., Mizokami Y. A case of cap polyposis remission by betamethasone enema after antibiotics therapy including Helicobacter pylori eradication. J Gastrointestin Liver Dis. 2014. 23: 203–206.
7. Konishi T., Watanabe T., Takei Y., Kojima T., Nagawa H. Confined progression of cap polyposis along the anastomotic line, implicating the role of inflammatory responses in the pathogenesis. Gastrointest Endosc. 2005. 62 (3): 446.
8. Konishi T., Watanabe T., Takei Y., Kojima T., Nagawa H. Cap polyposis: an inflammatory disorder or a spectrum of mucosal prolapse syndrome? Gut. 2005. 54 (9): 1342.
9. Oriuchi T., Kinouchi Y., Kimura M., Hiwatashi N., Hayakawa T., Watanabe H., Yamada S., Nishihira T., Ohtsuki S., Toyota T. Successful treatment of cap polyposis by avoidance of intraluminal trauma: clues to pathogenesis. Am J Gastroenterol. 2000. 95 (8): 2095.
10. Shimizu K., Koga H., Iida M., Yao T., Hirakawa K., Hoshika K., Mikami Y., Haruma K. Does metronidazole cure cap polyposis by its antiinflammatory actions instead of by its antibiotic action? A case study. Dig Dis Sci. 2002. 47 (7): 1465.
11. Nakagawa Y., Nagai T., Okawara H., Nakashima H., Tasaki T., Soma W., Hisamatsu A., Watada M., Murakami K., Fujioka T. Cap polyposis (CP) which relapsed after remission by avoiding straining at defecation, and was cured by Helicobacter pylori eradication therapy. Intern Med. 2009. 48 (23): 2009–2013. Epub 2009 Dec 1.
12. Murata M., Sugimoto M., Ban H., Otsuka T., Nakata T., Fukuda M., Inatomi O., Bamba S., Kushima R., Andoh A. Cap polyposis refractory to Helicobacter pylori eradication treated with endoscopic submucosal dissection. World J Gastrointest Endosc. 2017. Oct 16; 9 (10): 529–534. DOI: 10.4253/wjge.v9.i10.529.
13. Xie Q., Chen L., Zhao F., Zhou X., Huang P., et al. (2014) A meta-analysis of randomized controlled trials of low-volume polyethylene glycol plus ascorbic acid versus standard-volume polyethylene glycol solution as bowel preparations for colonoscopy. PLoS One.9 (6): e99092. DOI: 10.1371/ journal.pone.0099092.
14. Hassan C., Bretthauer V., Kaminski M.F., Polkowski M., Rembacken B., Saunders B., Benamouzig R., Holme O., Green G., Kuiper T., Marmo R., Omar M., Petruzziello L., Spada C., Zullo A., Dumonceau J.M. Bowel preparation for colonoscopy: European Society of Gastrointestinal Endoscopy (ESGE) guideline. Endoscopy. 2013; 45: 142–150. DOI: 10.1055/s-0032-1326186.
15. Ehsanullah M., Filipe M.I., Gazzard B. Mucin secretion in inflammatory bowel disease: correlation with disease activity and dysplasia. Gut. 1982. 23 (6): 485.
16. Aggarwal R., Gupta P., Chopra P., Nundy S. Rectal polyposis masquerading as ulcerative colitis with pseudopolyposis and presenting as chronic anemia: a case study with review of literature. Saudi J Gastroenterol. 2013. Jul-Aug; 19 (4): 187–189. DOI: 10.4103/1319-3767.114507.
17. Bookman I.D., Redston M.S., Greenberg G.R. Successful treatment of cap polyposis with infliximab. Gastroenterology. 2004. 126: 1868–1871.
18. Ng K.H., Mathur P., Kumarasinghe M.P., Eu K.W., Seow-Choen F. Cap polyposis: further experience and review. Dis Colon Rectum. 2004. 47: 1208–1215.
19. Maunoury V., Breisse M., Desreumaux P., Gambiez L., Colombel J.F. Infliximab failure in cap polyposis. Gut. 2005. 54: 313–314.
20. Oiya H., Okawa K., Aoki T., Nebiki H., Inoue T. Cap polyposis cured by Helicobacter pylori eradication therapy. J Gastroenterol. 2002. 37: 463–466.
21. Abid S., Khawaja A., Bhimani S.A., Ahmad Z., Hamid S., Jafri W. The clinical, endoscopic and histological spectrum of the solitary rectal ulcer syndrome: a single-center experience of 116 cases. BMC Gastroenterol. 2012. 12: 72.
22. Singh B., Mortensen N.J., Warren B.F. Histopathological mimicry in mucosal prolapse. Histopathology. 2007. 50: 97–102.
23. Kim E.S., Jeen Y.T., Keum B., Seo Y.S., Chun H.J., Um S.H., Kim C.D., Ryu H.S. Remission of cap polyposis maintained for more than three years after infliximab treatment. Gut Liver. 2009. Dec; 3 (4): 325–328. Epub 2009 Dec 31.
24. Isomoto H., Urata M., Nakagoe T., Sawai T., Nomoto T., Oda H., Nomura N., Takeshima F., Mizuta Y., Murase K., et al. Proximal extension of cap polyposis confirmed by colonoscopy. Gastrointest Endosc. 2001. 54: 388–391.
Рекомендуемые статьи
Эозинофильный эзофагит
— хроническое, медленно прогрессирующее иммуноопосредованное заболевание пищевода, характеризующееся выраженным эозинофильным воспалением слизистой оболочки пищевода, развитием подслизистого фиброза, клинически проявляющееся нарушением глотания (дисфагия, обтурация пищевода пищевым комком, рвота проглоченной пищей и др.)
При эндоскопическом исследовании в случае бронхоэктазов в стадии ремиссии выявляется
частично диффузный бронхит I степени воспаления
Активируйте PUSH уведомления в браузер
Отключите PUSH уведомления в браузер
Содержание
Интернет магазин
Популярное
- О нас
- Правовые вопросы
- Политика
обработки персональных
данных EndoExpert.ru - Связаться с нами
- Стать партнером
© 2016-2022 EndoExpert.ru

Вы находитесь в разделе предназначенном только для специалистов (раздел для пациентов по ссылке). Пожалуйста, внимательно прочитайте полные условия использования и подтвердите, что Вы являетесь медицинским или фармацевтическим работником или студентом медицинского образовательного учреждения и подтверждаете своё понимание и согласие с тем, что применение рецептурных препаратов, обращение за той или иной медицинской услугой, равно как и ее выполнение, использование медицинских изделий, выбор метода профилактики, диагностики, лечения, медицинской реабилитации, равно как и их применение, возможны только после предварительной консультации со специалистом. Мы используем файлы cookie, чтобы предложить Вам лучший опыт взаимодействия. Файлы cookie позволяют адаптировать веб-сайты к вашим интересам и предпочтениям.
Я прочитал и настоящим принимаю вышеизложенное, хочу продолжить ознакомление с размещенной на данном сайте информацией для специалистов.











.jpg)




.png)

















Комментарии 1