- Компании
- Takeda. О компании, буклеты, каталоги, контакты
- Olympus. О компании, буклеты, каталоги, контакты
- Boston Scientific. О компании, буклеты, каталоги, контакты
- Pentax. О компании, буклеты, каталоги, контакты
- Fujifilm & R-Farm. О компании, буклеты, каталоги, контакты
- Erbe. О компании, буклеты, каталоги, контакты
- Еще каталоги
- Мероприятия
- Информация
- Обучение
- Классификации
- Атлас
- Quiz
- Разделы
- Пациенту
QR-код этой страницы
Для продолжения изучения на мобильном устройстве ПРОСКАНИРУЙТЕ QR-код с помощью спец. программы или фотокамеры мобильного устройства
Статьи: Профилактика осложнений трахестомии у больных с временным и постоянным канюленосителем Методические рекомендации 2020
Полный текст статьи:
ПРАВИТЕЛЬСТВО МОСКВЫ ДЕПАРТАМЕНТ ЗДРАВООХРАНЕНИЯ ГОРОДА МОСКВЫ
ПРОФИЛАКТИКА ОСЛОЖНЕНИЙ ТРАХЕСТОМИИ У БОЛЬНЬIХ С
ВРЕМЕННЫМ И ПОСТОЯННЫМ КАНЮЛЕНОСИТЕЛЬСТВОМ
Методические рекомендации № 57
Москва - 2020
Учреждение-разработчик:
Государственное бюджетное учреждение здравоохранения города Москвы «Научно-исследовательский клинический институт оториноларингологии им. Л.И. Свержевского» Департамента здравоохранения города Москвы.
Составители:
Член-корр. РАН, Заслуженный деятель науки РФ, д.м.н., проф. А.И. Крюков, д.м.н., проф. Н.Л. Кунельская, д.м.н. Е.А. Кирасирова, д.м.н. Е.И. Зелекович, к.м.н. Р.Ф. Мамедов, к.м.н. Н.В. Лафуткина, к.м.н. Р.А. Резаков, М.А. Усова, Кулабухов Е.В.
Рецензенты:
доктор медицинских наук, профессор кафедры оториноларингологии ГБОУ ВПО МГМСУ
им. А.И.Евдокимова МЗ РФ Н.А.Мирошниченко
кандидат медицинских наук,
заведующий оториноларингологическим отделением
ГБУЗ ГКБ №1 им Н.И. Пирогова ДЗМ А.А.Лапченко
Предназначение:
В методических рекомендациях представлены алгоритм послеоперационного ведения пациентов, перенесших трахеостомию, хронических канюленосителей. Методические рекомендации рассчитаны на врачей оториноларингологов, реаниматологов, врачей общей практики.
Профилактика осложнений трахестомии у больных с временным и постоянным канюленосительством / Методические рекомендации. – Под редакцией А.И. Крюкова. – Москва. – 2020. – 23с.
Данный документ является собственностью Департамента здравоохранения города Москвы и не подлежит тиражированию без соответствующего разрешения.
Введение
Актуальность работы обусловлена ростом числа больных– канюленосителей. Это обусловлено рядом причин: необходимостью пролонгированной вентиляции легких и трахеостомии у исходно тяжелой категории больных, а, следовательно, ростом числа пациентов с постинтубационным и посттрахеостомическим повреждением гортани и трахеи (Горбунов В.А., 1999; Фоломеев В.Н., 2001; Паршин В.Д., 2002; Кирасирова Е.А., 2006; Лафуткина Н.В., 2007;, Maheer M. M. et al.,2018).
Отмечается неуклонный рост больных стенозом гортани и трахеи после различных медицинских вмешательств на органах шеи – пищеводе, щитовидной железе, лимфатичеких узлах, магистральных сосудах, позвоночнике (Е.А.Кирасирова, 1998; В.Г.Зенгер, 2004; Younis R.T., Lasar R.M., 1997;, V. Pandian et al., 2014). Рубцовые стенозы гортани и трахеи развиваются после реконструктивных и органосохраняющих операций, произведенных по поводу злокачественных новообразований гортани (Н.В. Чернов, А.Л. Клочихин, 2004, Н.С. Grillo 2004;). Кроме того, стабильно высоко число пациентов с тяжелой соматической патологией, для жизнеобеспечения которых необходима трахеостомия (V. Pandian et al.,2014, John D. Cramer et al.,2018).
Ввиду того, что разные группы пациентов наблюдаются разными специалистами и отсутствуют необходимые сведения о мерах профилактики осложнений канюленосительства и правилах ухода за трахеостомой, разработан алгоритм ведения данной группы пациентов, направленный на снижение тяжести осложнений канюленосительства, повышения качества жизни пациентов с трахеостомой.
Виды и причины осложнения канюленосительсьтва у трахеостомированных пациентов.
Снижение качества жизни у больных с трахеостомой носит многофакторный характер: потребность в длительном наблюдении в специализированном лечебном учреждении, временное или постоянное канюленосительство с длительной или постоянной дисфонией, дисфагией, болевым синдромом. Трахеостомированные больные зачастую выписываются из стационаров без необходимых рекомендаций и не получают должного наблюдения на амбулаторном этапе.
Учитывая, что пациент с трахеостомой наблюдается разными специалистами, мы выделили наиболее частые осложнения трахеостомии и разработали план лечения в зависимости от превалирующих симптомов.
1) Осложнения, вызванные недостаточным уходом за трахеостомой:
· гнойно-воспалительные осложнения с воспалением прилежащих тканей вплоть до формирования абсцессов передней поверхности шеи;
· расхождение послеоперационных швов;
· формирование грануляций в области трахеостомы;
· гнойный трахеобронхит.
2) Осложнения, вызванные травмой трахеи трахеостомической трубкой:
· эрозивный трахеит;
· пролежни трахеи, трахео-пищеводные и трахео-медиастинальные свищи;
· формирование грануляций в области дистального конца трахеостомической трубки, приводящие в последующем к формированию рубцового стеноза трахеи;
· образование грануляционого козырька над трахеостомической трубкой, приводящего к формированию гортанно-трахеальной атрезии;
· кровотечение, в т.ч. из грануляций.
3) Осложнение вследствие неправильного подбора трахеостомической трубки:
· сложность замены трахеостомической трубки;
· неадекватный просвет для нормального дыхания пациента;
· травма трахеальной стенки.
Нередко, наличие грануляционной ткани в области трахеостомы является причиной кровотечения при смене трахеостомической трубки, развитию паники у пациента и его родственников, что может привести к неправильным их действиям с серьезными последствиями, вплоть до асфиксии.
Бактериальная инфекция у трахеостомированных больных.
Слизистые оболочки верхних дыхательных путей обладают очищающими, увлажняющими и защитными свойствами. Эти механизмы реализуются за счет продукции слизи, содержащей в своем составе IgA; мукоцилиарного транспорта, направление которого идет к верхним дыхательным путям. При наличии трахеостомы эти механизмы нарушены, в результате чего слизистая оболочка дыхательных путей подвергается охлаждению и высыханию, перестают работать механизмы мукоцилиарного клиренса, возникает застой секрета, что способствует повышенному обсеменению микрофлорой, в том числе - условно-патогенной и патогенной. В итоге возрастает число осложнений как со стороны тканей вокруг трахеостомы, так и со стороны нижних дыхательных путей и легких. Присутствие трахеостомической трубки усугубляет течение воспалительного процесса и при неправильном ее положении может вызвать некроз слизистой оболочки. Это способствует развитию воспаления хрящей трахеи с развитием перихондрита, что в дальнейшем может привести к трахеомаляции, развитию рубцовых деформаций трахеи и возникновению рубцового стеноза.
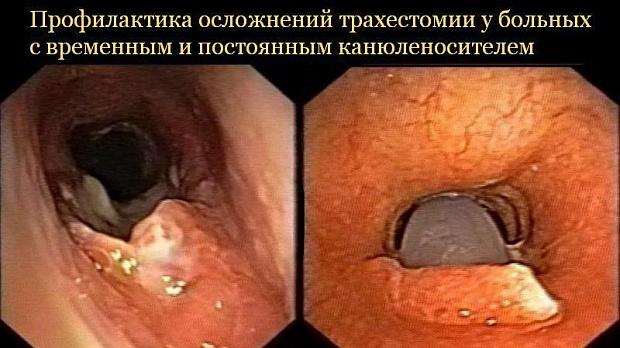
Присоединение госпитальной или внебольничной флоры в послеоперационном периоде способствует развитию ранних и поздних послеоперационных осложнений. В реконструктивной хирургии гортани и трахеи доказано, что количество осложнений у пациентов с выделенными госпитальными штаммами микроорганизмов (P.aeruginosa, S.aureus, A.baumanii, K.pneumoniae,) (рис.1,2), было в 2-2,5 раза больше, чем при выделении негоспитальных штаммов микроорганизмов. Наиболее неблагоприятным является присоединение нозокомиальных штаммов P. aeruginosa и A.baumanii, которое сопровождается не только воспалительными гнойными послеоперационными осложнениями, но и провоцирует избыточный рост грануляционной ткани (рис.1), формирование рубцов, и, как следствие, рестенозирование сформированного просвета гортани и трахеи.
Учитывая большое количество повторных госпитализаций, длительное пребывание в стационаре, многократные хирургические вмешательства в анамнезе, у данной группы пациентов происходит контаминация слизистой оболочки трахеи внутрибольничными возбудителями, резистентными к большинству антибактериальных препаратов. К тому же, воздействие инфекционных агентов и их токсинов ведет к подавлению иммунной защиты организма.
Таким образом, присоединение госпитальной микрофлоры у пациентов, перенесших трахеостомию, ведет к развитию ранних и поздних осложнений.
Рис 1. Разрастание грануляционной ткани в области трахеостомы у пациентов с госпитальным штаммом s.aureus.
Рис. 2. Эрозивный трахеит у пациента с госпитальным штаммом
K.pneumoniae.
Осложнения, связанные с присоединением госпитальной микрофлоры:
- Ранние:
Ø воспаление тканей в области оперативного вмешательства;
Ø расхождение послеоперационных швов;
Ø воспалительные явления со стороны слизистой оболочки трахеи;
Ø эрозивной трахеит.
- Поздние:
Ø формирование грануляций и стенозирование трахеи в области дистального конца трахеостомической трубки;
Ø увеличение сроков канюленосительства в послеоперационном периоде;
Ø формирование грануляций в области трахеостомы, приводущее к сложности смены и установки трахеостомической трубки.
Антибактериальная терапия у трахеостомированных больных
§ Препаратами выбора у пациентов, перенесших трахеостомию, являются цефалоспорины III поколения (цефтриаксон, цефотаксим) в/в капельно.
§ Присоединение гнойно-воспалительных осложнений требует смены антибактериальных препаратов на респираторные фторхинолоны (Левофлоксацин 400 мг в\в кап в течение 7-10 дней).
§ Амбулаторным больным при наличии гнойно-воспалительных осложнений назначаются респираторные фторхинолоны в таблетированном виде на 10 дней, либо таблетированные препараты фузидиевой кислоты на 7-10 дней.
§ При наличии гнойно-воспалительных осложнений у стационарных больных обязателен микробиологический контроль раневого отделяемого в 1, 3, 7 и 14 сутки после операции, т.к. присоединение госпитальной флоры может потребовать коррекции антибактериальной терапии. У амбулаторных пациентов с гнойно- воспалительными осложнениями производится взятие посева в день обращения, на 7 и 14 сутки.
§ В случае резистентности выделенных микроорганизмов к назначенным препаратам производится своевременная коррекция антибактериальной терапии по результатам антибиотикограммы.
§ Антибиотики карбапенемового ряда или ванкомицин назначаются только при выраженном активном воспалении в зоне операции и при подтвержденной устойчивости выделенных возбудителей к другим группам антибактериальных препаратов.
Во время перевязок необходимо применение местных антибактериальных препаратов (мази с хлорамфениколом, фузидиевой кислотой, неомицином, полимиксином в сочетании с глюкокортикостероидами).
Своевременная смена антибактериальной терапии способствует снижению случаев инфицирования госпитальными штаммами микроорганизмов в 1,5-2 раза и тем самым снижению количества послеоперационных осложнений на 30-40%.
Ингаляционная терапия у пациентов в послеоперационном периоде
При наличии у пациента трахеита или трахеобронхита в послеоперационном периоде ежедневно рекомендуется выполнение ингаляций с антисептиками в сочетании с глюкокортикостеройдами для уменьшения отека в области оперативного вмешательства и предотвращения бактериальной контаминации. Для ингаляций используют 0,25% раствор диоксидина или 0,01% раствор мирамистина в количестве 3 мл, в который добавляется 0,5 мл 0,04% раствора дексаметазона. Ингаляции проводят с помощью компрессорного или MESH-небулайзера.
Продолжительность ингаляции должна составлять 5 минут, ее проводят либо через нос или рот, при этом герметично закрывается трахеостома, либо проводится через саму трахеостому. Кратность ингаляций в сутки в раннем послеоперационном периоде должна составлять 2-3 раза. При наличии густой мокроты добавляют ингаляционные формы муколитиков (лазолван, флуимуцил-антибиотик)
Обработка трахеостомических трубок
Наряду с применением системных антибактериальных препаратов необходимо соблюдение алгоритма смены и обработки трахеостомических трубок.
Трахеостомическая трубка, установленная через трахеостому, является инородным телом для организма и вызывает физиологический ответ - воспалительную реакцию контактирующей ткани. Также трахеостомическая трубка может служить источником инфекции. Под действием инородного тела в трахее стимулируется продукция слизи, ухудшается мукоцилиарный клиренс, возникает постепенная метаплазия слизистой оболочки. Процесс метаплазии занимает длительное время, в результате нее теряются реснитчатые клетки, изменяется нормальная физиология трахеи и возникают предпосылки к развитию грануляционной ткани.
Слизь и выделения трахеобронхиального дерева являются агрессивной средой для трахеостомической трубки, в результате чего ее материал начинает разрушаться, появляются поверхностные микротрещины на поверхности трахеостомической трубки, что способствует лучшей адгезии на ее поверхности бактерий.
В повседневной практике больные-канюленосители после выписки из стационаров не наблюдаются у врачей, не получают рекомендаций по обработке трахеостомической трубки и частоте ее замены.
В последние десятилетия были усовершенствованы методы исследования микроорганизмов, появилась возможность понять сложность организации микробных сообществ в естественных условиях обитания. Бактерии в окружающей среде и организме людей существуют в форме сообществ (биопленок) и свободных планктонных форм. Биоплёнка - структурированное сообщество бактерий, окруженное продуцируемым ими самими полимерным матриксом и адгезированное к инертным или живым поверхностям.
Бактерии, находящиеся в колонии бактериальной пленки, отмечают повышенную резистентность к антибактерильным и антисептическим препаратам, которая реализуется несколькими механизмами:
§ Во-первых, компоненты полисахаридного матрикса, продуцируемые бактериями, замедляют проникновение антибактериальных препаратов внутрь биопленки.
§ Во-вторых, бактерии, находясь в составе биопленок, имеют разную метаболическую активность. Так, метаболически активные клетки находятся на периферии биопленок, а метаболически неактивные – внутри. Как известно, мишенями действия антибиотиков являются активно растущие клетки. Таким образом, находящиеся внутри биопленок клетки оказываются защищенными от воздействия антибиотиков;
§ В-третьих, уменьшается свободная поверхность бактерий за счет прилегания друг к другу, что также повышает устойчивость бактерий к стандартным концентрациям антибиотиков;
§ В-четвертых, различные виды бактерий, входящих в состав биопленки, способны передавать друг другу гены резистентности к антибиотикам в условиях тесного контакта внутри биопленки.
Трахеостомическая трубка также является хорошим субстратом для прикрепления биопленки, как и различного вида медицинские импланты (мочевые, внутривенные катетеры, назогастральные зонды, искусственные клапаны сердца и т.д.).
Perkins et al (2004) при изучении микробиооценозов на поверхности трахеостомических трубок у стационарных больных, выявили наличие биопленок в просвете трахеостомических трубок у 91% исследуемых пациентов, и увеличение плотности биопленок к дистальному концу трубки. Авторы показали, что ежедневный туалет трахеостомических трубок, частично разрушает биопленку за счет механического воздействия.
При исследовании различных трахеостомических трубок Solomon et al. (2009) определяли наличие биопленок у пациентов уже через неделю после установки на 90% трахеостомических трубок. Биопленки состояли из 12 разных видов бактерий (S. aureus, P. aeruginosa, E.coli, E.fecalis, S.mitis, S. marcescens, S.maltophila, P.vulgaris, и т.д.). При этом отмечалась обратная корреляция между количеством КОЕ бактерий и частотой смены внутренней канюли трахеостомической трубки. 10% пациентов, у которых биопленки не были обнаружены вообще, осуществляли туалет трахеостомической трубки со сменой внутренней канюли несколько раз в день. (табл.1)
У пациентов хронических канюленосителей часто возникает рост грануляционной ткани по периметру трахеостомы и в просвете трахеи из-за неправильного ухода за трахеостомой. Неадекватный подбор трахеостомической трубки, нефизиологичность ее формы и материала, ведут к сложностям при установке и гнойно-воспалительным осложнениям (рис. 5,6).
Табл.1. Соотношение частоты смены трахеостомической трубки и наличия осложнений у пациентов-хронических канюленосителей.
|
Осложнения |
Частота смены трахеостомической трубки | |||||
|
1-3 дня |
3-7 дн |
7-21 дн |
3-6 мес |
6-12 мес |
>12 мес | |
|
Воспаление кожи вокруг трахеостомы. |
- |
- |
- |
++ |
++ |
+++ |
|
Рост грануляционной ткани в области трахеостомы |
+ |
+ |
+ |
++ |
++ |
++++ |
|
Наличие грануляционной ткани в области дистального конца трахеостомической трубки |
- |
- |
+ |
++ |
+++ |
++++ |
|
Формирование рубцовой ткани в области дистального конца трахеостомической трубки |
- |
- |
- |
+ |
++ |
+++ |
|
Наличие эрозивного трахеита или бронхита |
- |
+ |
+ |
+ |
++ |
+++ |
|
++++ - > 75% случаев, +++ - от 50 до 75%, ++ - от 25 до 50, + - от 5 до 25% - - < 5% | ||||||
Результаты собственных исследований способности к биопленкообразованию бактерий на трахеостомических трубках и эффективности антибактериальных и антисептических средств в отношении биопленок и планктонных форм бактерий.
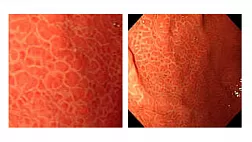
Нами было проведено исследование способности различных видов микроорганизмов формировать структуру биопленки на поверхности трахеостомических трубок, изготовленных из различных материалов (рис.3). По результатам исследования было установлено, что P.aeruginosa характеризуется наиболее выраженной способностью к адгезии и образованию биопленок на силиконовых трахеостомических трубках, как Т- образных, так и bivona®. Прочие исследуемые бактерии (A.baumanii, S.aureus, K.pneumoniae) хуже всего образуют биопленки на силиконовых трубках bivona®. Пластиковые двухпросветные трубки явились самым благоприятным субстратом для образования бактериальных биопленок.
Стандартные концентрации исследуемых антисептиков (хлоргексидин 0,02%, мирамистин 0,01% и диоксидин 0,5%) показали недостаточную эффективность в отношении бактерий, существующих в виде биопленок. Добавление к раствору антисептика химотрипсина, существенно увеличило эффективность антисептика. В отношении P.aeruginosa наиболее эффективна оказалась комбинация 0,01% р-ра мирамистина в сочетании с 10 мг химотрипсина, в отношении S.aureus, A.baumanii и K.pneumoniae - 0,5% р-ра диоксидина и 10 мг химотрипсина.
Таким образом, при обработке трахеостомических трубок необходимо учитывать выделенную микрофлору и при выявлении P.aeruginosa, используемый по умолчанию антисептик, должен быть заменен на 0,01% раствор мирамистина.
Рис. 3. Виды трахеостомических трубок: ПВХ, пластиковая, силиконовая Т-образная, силиконовая bivonaTM
Смена трахеостомических трубок:
Для создания алгоритма послеоперационного наблюдения все пациенты поделены на 3 группы в зависимости от наличия рисков при смене трахеостомических трубок:
1 группа - Трахеостомическая трубка свободно удаляется, трахеостома сформирована, дыхательные пути можно легко осмотреть с помощью эндоскопа
2 группа - Трахеостомическая трубка может быть удалена на короткое время, однако для установки трубки требуются специальные устройства или маневры (проводник, гибкий эндоскоп и тд.)
3 группа - Трахеостомическая трубка амбулаторно не удаляется из-за высокого риска асфиксии
Пациентов первых двух групп необходимо обучить самостоятельной смене трубки, и они могут наблюдаться амбулаторно по месту жительства. Пациенты 3 группы должны наблюдаться в отделении до купирования послеоперационного воспаления, возможности амбулаторной смены трубки.
Амбулаторным пациентам – хроническим канюленосителям, которым трахеостомия произведена ранее, при наличии выраженного воспаления требуется наблюдение врачом и смена трубки медицинским персоналом до купирования воспаления. Если сложность замены обусловлена разрастанием грануляционной ткани (рис.4), или тем, что неправильно сформирован и не оформлен канал трахеостомы, рекомендовано хирургическое переоформление трахеостомы стационарно, либо, при наличии возможности, удаление грануляций амбулаторно. В последующем пациенты третьей группы также обучаются самостоятельной смене трахеостомической трубки, и наблюдаются амбулаторно.
Рис.4. Разрастание грануляционной ткани, вызывающее трудности при смене и установки трахеостомических трубок у амбулаторных пациентов.
Алгоритм смены и обработки трахеостомических трубок.
Ø Рекомендовано отказаться от использования двухпросветных пластиковых и металлических трубок не только у пациентов после реконструктивных операций на гортани и трахее, но и у любых канюленосителей.
Ø В первые дни после операции внутренние трахеостомические канюли (вкладыши) 2-3 раза в сутки промывать проточной водой с механическим удалением находящегося в их просвете отделяемого специальной щеткой. Затем внутреннюю и наружную поверхность обрабатывать стерильным марлевым тампоном, смоченным раствором химотрипсина, и на 5 минут замочить в растворе диоксидина, после этого канюля устанавливается в просвет трахеостомической трубки (рис.7).
Ø Вся трахеостомическая трубка обрабатывается по аналогичной методике, её замена производится 1 раз в сутки.
Ø В случае отсутствия внутренней канюли в трахеостомической трубке, производится смена всей трубки и ее обработка по вышеуказанной схеме.
Ø Трахеостомические трубки из современных материалов, желательно менять ежемесячно, силиконовые - раз в 2 месяца, при невозможности это делать (из-за каких-либо причин), хотя бы 1 раз в 3 месяца.
Ø После смены трахеостомической трубки медицинскими работниками в условиях медицинских учреждений необходим контроль правильной установки трахеостомической трубки с помощью гибкой эндоскопической техники для адекватного подбора трахеостомической трубки.
Ø При замене трахеостомической трубки кожа вокруг трахеостомической трубки должна быть тщательно очищена
стерильной салфеткой, смоченной антисептиками (не спиртовыми) от трахеального и раневого отделяемого.
Ø Между кожей и фланцем трахеостомической трубки прокладывают стерильную салфетку с антибактериальными мазями или антисептиками, она требует своевременной замены при пропитывании ее трахеальным или раневым отделяемым.
Ø Швы после трахеостомии должны быть сняты на 7-10 сутки после операции, т.к. длительное их нахождение в раневом канале является дополнительным источником инфекции.
Ø Перед выпиской из стационара пациент или его родственники должны быть обучены уходу за трахеостомой и смене трахеостомической трубки.
Рис. 5. Использование устаревших видов трахеостомических трубок в сочетании с неправильной их установкой.
Рис.6. Наличие грануляций по периметру трахеостомы у пациентки с ненадлежащим уходом за трахеостомой.
Рис. 7. Трахеостомическая трубка с принадлежностями: щетка, фиксирующая лента, 2 внутренние канюли (вкладыша).
Заключение
Присоединение в послеоперационном периоде госпитальных штаммов микроорганизмов
в значительной степени ухудшает результат операции, вызывая у больных ранние и поздние послеоперационные осложнения. Ненадлежащие ведение трахеостомированных пациентов может привести к хроническому канюленосительству и возникновению осложнений при замене трахеостомической трубки, вплоть до летального исхода.
У пациентов со сложностями установки трахеостомической трубки ввиду неправильного формирования трахеостомы, рекомендовано ее переоформление.
Применение разработанного алгоритма смены и обработки трахеостомических трубок, ухода за трахеостомированными пациентами позволяет значительно уменьшить количество послеоперационных осложнений, уменьшить количество дней госпитализации и улучшает послеоперационный прогноз, уменьшает длительность канюленосительства (при временной трахеостомии), улучшает качество жизни данной категории больных.
Список литературы:
Рекомендуемые статьи
При эндоскопическом исследовании в случае бронхоэктазов в стадии ремиссии выявляется
частично диффузный бронхит I степени воспаления
Активируйте PUSH уведомления в браузер
Отключите PUSH уведомления в браузер
Содержание
Интернет магазин
Популярное
- О нас
- Правовые вопросы
- Политика
обработки персональных
данных EndoExpert.ru - Связаться с нами
- Стать партнером
© 2016-2022 EndoExpert.ru

Вы находитесь в разделе предназначенном только для специалистов (раздел для пациентов по ссылке). Пожалуйста, внимательно прочитайте полные условия использования и подтвердите, что Вы являетесь медицинским или фармацевтическим работником или студентом медицинского образовательного учреждения и подтверждаете своё понимание и согласие с тем, что применение рецептурных препаратов, обращение за той или иной медицинской услугой, равно как и ее выполнение, использование медицинских изделий, выбор метода профилактики, диагностики, лечения, медицинской реабилитации, равно как и их применение, возможны только после предварительной консультации со специалистом. Мы используем файлы cookie, чтобы предложить Вам лучший опыт взаимодействия. Файлы cookie позволяют адаптировать веб-сайты к вашим интересам и предпочтениям.
Я прочитал и настоящим принимаю вышеизложенное, хочу продолжить ознакомление с размещенной на данном сайте информацией для специалистов.














.jpg)





.png)


.jpg)
















Комментарии