- Компании
- Takeda. О компании, буклеты, каталоги, контакты
- Olympus. О компании, буклеты, каталоги, контакты
- Boston Scientific. О компании, буклеты, каталоги, контакты
- Pentax. О компании, буклеты, каталоги, контакты
- Fujifilm & R-Farm. О компании, буклеты, каталоги, контакты
- Erbe. О компании, буклеты, каталоги, контакты
- Еще каталоги
- Мероприятия
- Информация
- Обучение
- Классификации
- Атлас
- Quiz
- Разделы
- Пациенту
QR-код этой страницы
Для продолжения изучения на мобильном устройстве ПРОСКАНИРУЙТЕ QR-код с помощью спец. программы или фотокамеры мобильного устройства
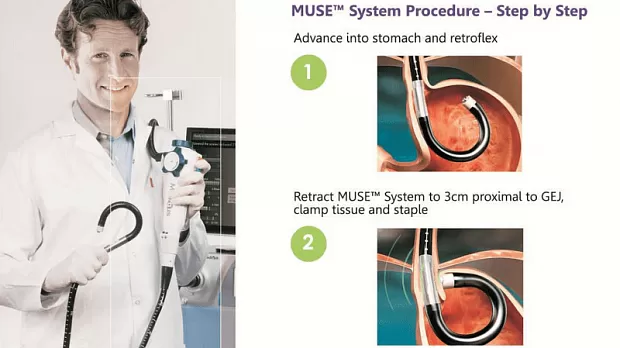
Статьи: Transoral incisionless fundoplication for gastro-esophageal reflux disease: Techniques and outcomes
Полный текст статьи:
Гастроэзофагеальная рефлюксная болезнь (ГЭРБ) является очень распространенным заболеванием, которое возникает в основном из-за потери эффективного антирефлюксного барьера, который является механическим препятствием для ретроградного движения содержимого желудка. В настоящее время ГЭРБ можно лечить с помощью медикаментозной терапии, хирургического или эндоскопического трансорального вмешательства. Медикаментозная терапия является наиболее распространенным подходом, хотя в последние годы все больше высказывалось беспокойство по поводу потенциальных побочных эффектов непрерывного длительного приема лекарств, непереносимости лекарств или безответственности, а также необходимости высоких дозировок в течение длительных периодов для лечения симптомов или предотвращения рецидивов. Операция также может в некоторых случаях иметь такие последствия, как длительная дисфагия, метеоризм, неспособность отрыгнуть или вызвать рвоту, диарея или функциональная диспепсия, связанные с задержкой опорожнения желудка. В последние несколько лет, трансоральная безоперационная фундопликация (TIF) доказала свою эффективность и перспективность в качестве альтернативы медицинской и хирургической терапии. В этом обзоре описаны этапы техники TIFс использованием EsophyX® устройство и система MUSE TM . Осложнения и методы их лечения подробно описаны, а последние литературные данные о результатах рассмотрены. TIF реконфигурирует ткань для получения желудочно-пищеводного клапана полной толщины изнутри желудка, путем серозно-серозных сращений, которые включают мышечные слои. До настоящего времени процедура достигла длительного улучшения симптомов ГЭРБ (до шести лет), прекращения или уменьшения приема ингибиторов протонной помпы примерно у 75% пациентов, а также улучшения функциональных показателей, измеряемых с помощью мониторинга рН или импеданса.
Ключевые слова: гастроэзофагеальная рефлюксная болезнь, трансоральная безоперационная фундопликация, передняя фундопликация с помощью ультразвукового хирургического эндостеплера, EsophyX, MUSE, хирургическая фундопликация
Основной совет: в последнее время трансоральная безоперационная фундопликация (TIF) стала эффективным и многообещающим терапевтическим вариантом в качестве альтернативы медицинской и хирургической терапии гастроэзофагеальной рефлюксной болезни (ГЭРБ). Был опубликован ряд проспективных наблюдательных исследований для TIF с использованием устройства EsophyX ®, но все еще имеются только ограниченные данные для TIF с системой MUSE TM . В этом обзоре описаны методы для TIF с обоими этими устройствами, и он призван объединить текущую литературу, чтобы лучше прояснить результаты TIF у пациентов с ГЭРБ.
ВСТУПЛЕНИЕ
Гастроэзофагеальная рефлюксная болезнь (ГЭРБ) является очень распространенным заболеванием, которое в настоящее время можно лечить с помощью медикаментозной терапии, хирургического или эндоскопического трансорального вмешательства. Медикаментозная терапия ингибиторами протонной помпы (ИПП) является наиболее распространенным подходом: однако в последние годы все чаще высказывались опасения относительно потенциальных побочных эффектов, связанных с ИПП, непереносимости или невосприимчивости, а в некоторых случаях необходимости долгосрочной терапии. с высокими дозировками для облегчения симптомов или предотвращения рецидивов. Хирургическая терапия также может в некоторых случаях иметь такие последствия, как длительная дисфагия, метеоризм, невозможность отрыжки или рвоты, диарея или функциональная диспепсия, связанные с задержкой опорожнения желудка [ 1 - 4]. Даже для вмешательств, проводимых в центрах передового опыта, после 3-х случаев были отмечены грыжи в месте надреза в месте введения троакара [ 5 ].
По этим причинам несколько трансоральных эндоскопических методов были предложены за последние 15 лет в качестве альтернативы медицинской и хирургической терапии; однако большинство из них имели неутешительные результаты и были заброшены.
В последние несколько лет трансоральная безоперационная фундопликация (TIF) оказалась эффективной и многообещающей терапевтической альтернативой медицинской и хирургической терапии; Процедура обеспечивает длительное улучшение симптомов ГЭРБ (до шести лет) и функциональных результатов, а также прекращение или снижение приема ИПП у примерно 75% пациентов. TIF реконфигурирует ткань для получения желудочно-пищеводного клапана полной толщины изнутри желудка, путем серозно-серозных сращений, которые включают мышечные слои; новый клапан повышает барьерную функцию LES с потенциально меньшим количеством побочных эффектов, связанных с процедурой, чем хирургическое вмешательство.
TIF можно выполнить с помощью устройства EsophyX ® (EndoGastric Solutions, Редмонд, Вашингтон, США) или ультразвуковой хирургический эндостеплер Medigus (MUSE ™, Medigus Ltd., Omer; Израиль). EsophyX ®Устройство создает омега-образный клапан длиной 3-5 см с круговым рисунком 250-300 ° вокруг желудочно-пищеводного соединения путем развертывания неабсорбируемых полипропиленовых крепежных элементов через два слоя (пищевода и желудка) под эндоскопическим зрением оператор. Система MUSE ™ скрепляет глазное дно желудка с пищеводом под диафрагмой, используя несколько комплектов металлических швов, помещенных под ультразвуковым контролем, и создает переднюю фундопликацию, функционально аналогичную стандартной хирургической операции Dor-Thal. У пациента со скользящей хиатальной грыжей процедура может быть выполнена только в том случае, если грыжу можно уменьшить ниже диафрагмы.
Публикации по TIF с устройством EsophyX ® сообщают о сохранении вновь созданного клапана в течение шести месяцев во всех исследованиях и до шести лет в одном исследовании с удовлетворительными результатами, оцененными с помощью 24-часового мониторинга pH и / или импеданса [ 6 - 27 ]. Информации о TIF с помощью системы MUSE ™ пока мало: одно исследование на животных показало, что метод безопасен и выполним, а в двух исследованиях на людях были получены хорошие клинические и функциональные результаты при шестимесячном и пятилетнем наблюдении [ 28 - 30 ].
В этом обзоре описываются методы TIF, использование устройства EsophyX ® и системы MUSE TM , ведение пациентов до и после процедуры, а также осложнения. Результаты сообщаются подробно, и был проведен пересмотр литературы для оценки эффективности TIF у пациентов с ГЭРБ. Рукописи были идентифицированы путем поиска в базах данных PubMed, Embase и The Cochrane Library, используя следующие ключевые слова: «гастроэзофагеальная рефлюксная болезнь», «трансоральная безоперационная фундопликация», «передняя фундопликация», «ультразвуковой хирургический эндостеплер medigus», «EsophyX», « MUSE »и« хирургическая фундопликация ».
Перейти к:
ТЕХНИКА
Оценка перед процедурой
Предоперационная эндоскопия верхних отделов желудочно-кишечного тракта должна проводиться для оценки расстояния между зубами резца и пищеводно-желудочным соединением (EGJ), а также поперечного размера диафрагмального перерыва. С помощью современной техники TIF ниже диафрагмы может быть уменьшена только грыжевая грыжа длиной не более 3,0 см, в то время как хиатус более 3,0 см может способствовать смещению черепа в складку вверх в грудной клетке, делая неэффективным вновь созданный клапан.
Перед вмешательством все пациенты должны быть обследованы с помощью манометрии пищевода, чтобы исключить первичные нарушения моторики, и с помощью мониторинга импеданса pH в течение 24 часов, чтобы исключить функциональную изжогу. Если используется система MUSE ™, необходимо выполнить проглатывание бария, чтобы оценить степень уменьшения грыжи, поскольку несводимость является противопоказанием к процедуре.
Трансоральная фундопликация с EsophyX ® устройства
EsophyX ®устройство состоит из: (1) ручки, на которой размещены органы управления; (2) шасси диаметром 18 мм, содержащее рабочие каналы, через которые можно вставить эндоскоп диаметром 9 мм спереди; (3) тканевой инвагинатор, снабженный боковыми отверстиями на дистальной части шасси, к которым может применяться внешнее всасывание; (4) тканевая форма, которая может быть введена в ретрофлексию и прижимает ткань к стержню устройства; (5) винтовой винт, который продвигается в ткань, так что ткань между тканевой формой и стержнем может быть втянута; (6) два стилета, которые проходят через складчатую ткань и тканевую форму, и Н-образные полипропиленовые застежки могут быть размещены над ними; и (7) картридж, содержащий 20 крепежных элементов. Устройство было недавно обновлено и улучшено в приборе нового поколения: EsophyX® Z устройство. Развертывание застежки аналогично механизму срабатывания хирургического сшивателя с уменьшением сложности управления и развертыванием двойной застежки и улучшено за счет управления задней лапой. Профиль скрещивания был уменьшен с устранением локтя тканевой плесени и увеличением боковой жесткости плесени ткани; кончик тканевой формы покрывает стилеты во время развертывания
Детали первого и второго устройств поколения проиллюстрированы на рисунке Figure11 .
Внешний файл, содержащий изображение, иллюстрацию и т. Д. Имя объекта: WJGPT-7-179-g001.jpg.
Открыть в отдельном окне
фигура 1
Устройство EsophyX ® : устройства первого и второго поколения (любезно предоставлено EndoGastric Solutions, Inc. Редмонд, Вашингтон, США). A1-A2: устройство, используемое в настоящее время (© 2014 EndoGastric Solutions, Inc); B1-B2: устройство нового поколения (© EndoGastric Solutions, Inc, 2014).
Процедура требует двух операторов: один обрабатывает устройство, а другой - эндоскоп.
Устройство вводится трансорально пациенту в левом боковом или лежачем положении под общим наркозом. В случаях со сложным введением устройство можно осторожно поворачивать во время введения: этот маневр позволяет легко проходить через верхний пищеводный сфинктер. На этом этапе существует риск перфорации гипофарингеальной области, если инструмент вставлен без осторожности.
Во время процедуры воздух или СО 2 вдуваются, чтобы растянуть желудочную полость и обеспечить адекватное зрение глазного дна и EGJ; CO 2 является предпочтительным, поскольку он уменьшает дискомфорт пациента и безопаснее в случае перфорации.
Когда пациент находится в левом положении лежа, а эндоскоп - в ретрофлексном виде, меньшая кривая находится в положении 12 часов, а большая кривая - в 6 часов. Плесень ткани ретрофлексируется и закрывается против устройства Esophyx; затем его поворачивают на 11 или 1 час (меньший изгиб) и отводят назад, чтобы его наконечник находился прямо внутри просвета пищевода. В этот момент: (1) спиральный ретрактор выдвигается для зацепления ткани под прямым зрением чуть ниже линии Z; (2) пресс-форма ткани открыта, и спиральный винтовой кабель вытянут назад, чтобы убрать ткань; (3) на этом этапе процедуры желудок десуффулируется, чтобы задействовать достаточное количество ткани для фундопликации; (4) после того, как такой маневр завершен, когда спиральный ретрактор и тканевая форма зафиксированы на месте, отсасывание применяется к тканевому инвагинатору, а затем устройство продвигается в желудок, который был повторно инсуффлирован. Это позволяет создать пищеводно-желудочную пликацию во внутрибрюшном положении и уменьшить любую грыжу пищевода.
Пликация выполняется путем развертывания нескольких Н-образных полипропиленовых крепежных элементов, продвинутых над двумя стилетами, начиная с дальней задней и передней сторон пищеводно-желудочного соединения; затем дополнительные крепежные элементы развертывают вдоль большей части кривизны клапана, вращая тканевую форму в осевом направлении, чтобы скользить желудком по пищеводу. Этот маневр приводит к круговой затяжке и новой окружности клапана> 240 °. Как правило, 14 крепежных элементов необходимы для создания адекватного окружного клапана; тем не менее, чем больше крепежных элементов задействовано, тем больше материка - это клапан.
Подробная информация о EsophyX ® техники показаны на рисунке Figure2.2 . Эндоскопические до и после процедурного результаты представлены на рисунке Рисунок3 3 .
Внешний файл, содержащий изображение, иллюстрацию и т. Д. Имя объекта: WJGPT-7-179-g002.jpg.
фигура 2
Схематическое изображение процедуры с устройством EsophyX ® (предоставлено EndoGastric Solutions Inc. Редмонд, Вашингтон, США). A: Устройство EsophyX ® поступает в пищевод через рот и располагается в желудочно-пищеводном соединении; B: устройство оборачивает глазное дно вокруг дистального отдела пищевода и закрепляет складку ткани; C: Затем этот шаг повторяется несколько раз, чтобы восстановить надежный, герметичный клапан (© 2014 EndoGastric Solutions, Inc).
Внешний файл, содержащий изображение, иллюстрацию и т. Д. Имя объекта: WJGPT-7-179-g003.jpg
Рисунок 3
Эндоскопические исследования желудочно-пищеводного клапана до и сразу после трансоральной безрезультатной процедуры фундопликации с помощью прибора EsophyX ® (случай авторов). A: Гастроэзофагеальный клапан: перед процедурой с устройством EsophyX ® ; B: маневр «Bell Roll» для создания нового желудочно-пищеводного клапана; C: Желудочно-пищеводный клапан: сразу после процедуры с устройством EsophyX ® ; D: Желудочно-пищеводный клапан: через шесть месяцев после процедуры.
Помимо стандартной процедуры, с течением времени были описаны две модифицированные методики для создания фундопликации.
Тот, который мы используем, зацепляет ткань ниже Z-линии в положениях 11 и 1 час; затем крутящий момент прикладывается вращением запертой формы для ткани по часовой стрелке и против часовой стрелки перед тем, как вставить стилет. В результате этого маневра часть глазного дна вращается вокруг стенки пищевода, и стилет задействует больше тканей. Четыре крепежа для каждого участка развернуты в 1 и 11 часов, и два для каждого участка в средней части клапана, в 4, 6 и 8 часов, чтобы усилить складку. Этот метод увеличил на 30% показатель успешности процедуры, достигнув полной элиминации применения ИПП через 12 месяцев у 14/22 пациентов (63,6%), в то время как со стандартной техникой только 11/27 пациентов (40,7%) полностью прекратили ИПП. ,
Белл и др. [ 19 ] разработали так называемую ротационную фундопликацию. Спиральный ретрактор включается в 12 часов, а тканевая форма помещается в 6 часов. Затем запертая тканевая форма вращается в направлении меньшей кривой радиальным движением рукоятки устройства в положение 12 часов. Этот маневр переворачивает глазное дно и вокруг дистального отдела пищевода в положение «1 час».
В конце пликации проводится эндоскопия для исследования глотки, просвета пищевода и дна желудка, а также фундопликации.
Трансоральная фундопликация с помощью системы MUSE ™
Система MUSE ™ включает в себя эндостеплер и связанную с ним консоль, содержащую контроллер для камеры, ультразвуковой дальномер и различные датчики, насос для инсуффляции и орошения, систему всасывания, питание и органы управления для светодиода.
Эндостеплер имеет: (1) ручку, в которой размещены органы управления; (2) вставная трубка диаметром 15,5 мм, длиной 66 см, содержащая всасывающий, инсуффляционный / ирригационный каналы и электрические и механические кабели для управления устройством; (3) жесткая секция длиной 66 мм, содержащая картридж. Каждый картридж содержит пять стандартных 4,8-мм титановых скоб, ультразвуковое зеркало, одну воронку с центрирующим штифтом и две воронки с наковальней; и (4) дистальный наконечник, аналогичный эндоскопу, для всасывания, ирригации, освещения (с помощью светодиода) и визуализации (с помощью миниатюрной камеры). Наковальня, установочный штифт, винт наковальни и ультразвук предназначены для обеспечения правильного выравнивания и позиционирования устройства во время сшивания. Дистальный наконечник может быть шарнирно соединен в одном направлении с жестким участком и патроном с радиусом изгиба 26 и 40 мм.Figure44 .
Внешний файл, содержащий изображение, иллюстрацию и т. Д. Имя объекта: WJGPT-7-179-g004.jpg.
Рисунок 4
Ультразвуковая эндостеплерная система Medigus Surgical, MUSE ™ (предоставлено Medigus Ltd., Омер, Израиль). A: Система MUSE ™ (© Все права защищены Medigus Ltd 2008-2015); B: Консоль, соединенная с эндостеплером, содержащая контроллер для камеры, ультразвуковой дальномер и различные датчики (угол изгиба, сила изгиба, установочный штифт, винты с наковальней, зазор) (© Все права защищены Medigus Ltd 2008-2015).
Вся процедура может быть выполнена одним оператором в опытных руках. Пациент находится в положении лежа на спине, под общим наркозом с интубацией трахеи. Положительное давление в конце выдоха , по меньшей мере , на 5 мм рт.ст. (7,5 CMH 2О) предоставляется. После предварительной эндоскопической оценки пищевода и желудка и до тех пор, пока противопоказания не обнаружены, ставится пробирка. Эндостеплер затем вводится трансорально через наружную трубку и осторожно продвигается в желудок под прямым контролем; проходя жесткий участок через глоточно-пищеводный переход, он может столкнуться с некоторым сопротивлением. Чтобы избежать применения чрезмерной силы и риска травмировать пищевод, наружную трубку можно вынуть примерно на 5 см, а затем продвинуть с помощью эндостеплера как единого целого. Этот маневр может повторяться до тех пор, пока система не достигнет середины пищевода. Сгибание шеи может облегчить проход.
Попав в желудок, раздутый за счет инсуффляции воздуха или CO 2 , степлер продвигается до тех пор, пока наконечник не окажется на расстоянии примерно 5 см от EGJ, а затем ретрофлексируется на 180 ° для получения адекватного обзора дна желудка и EGJ, чтобы выбрать место сшивания , Самое важное местоположение - самое левое, и обычно делается первым. Это точка крепления для глазного дна, и она должна быть как можно дальше от пищевода. Иногда, в зависимости от анатомии, может быть легче сделать первое сшивание в более центральном положении.
Последующие сшивания должны быть в пределах 60-180 ° до тех пор, пока самый правый сшиватель не будет находиться на меньшей кривой, где он может прикрепить антральный отдел к пищеводу и открыть пищеводно-желудочное соединение, а не закрыть его. Дальнейшие сшивания могут быть размещены между крайним левым и самым правым.
После определения правильных мест для сшивания остальная часть процедуры выполняется под ультразвуковым контролем. Последующие этапы включают зажим ткани, развертывание установочного штифта, продвижение винта наковальни, сшивание и извлечение винтов наковальни.
Подробная информация о музе ™ техники показаны на рис Figure5.5 . Эндоскопические пред- и пост-процедурные выводы после TIF с этим устройством представлены на рисунке Figure66 .
Внешний файл, содержащий изображение, иллюстрацию и т. Д. Имя объекта: WJGPT-7-179-g005.jpg
Рисунок 5
Схематическое изображение процедуры ультразвукового хирургического эндостеплера Medigus (MUSE ™) (предоставлено Medigus Ltd., Омер, Израиль). A: Эндостеплер вводится трансорально через наружную трубку и плавно продвигается в желудок под прямым контролем; B: Попав в желудок, раздутый за счет инсуффляции воздуха или CO 2 , сшиватель продвигается до тех пор, пока кончик не окажется на расстоянии примерно 5 см от EGJ, а затем ретрофлексируется на 180 °, чтобы дать адекватное видение глазного дна и EGJ для выбора места сшивания , Ткань зажата и сшита под ультразвуковым руководством; C: Затем этот шаг повторяется, по крайней мере, дважды, чтобы восстановить надежный, герметичный клапан. Дополнительные места сшивания должны быть в пределах 60-180 ° от окружности клапана (© Все права принадлежат Medigus Ltd 2008-2015). EGJ: пищеводно-желудочный узел.
Внешний файл, содержащий изображение, иллюстрацию и т. Д. Имя объекта: WJGPT-7-179-g006.jpg.
Рисунок 6
Эндоскопический обзор желудочно-пищеводного клапана до и после трансоральной безрезультатной процедуры фундопликации с помощью ультразвукового хирургического эндостеплера Medigus (MUSE ™) (случай авторов). A: Гастроэзофагеальный клапан: перед трансоральной процедурой безоперационной фундопликации (TIF) с системой MUSE ™; B: Гастроэзофагеальный клапан: сразу после процедуры TIF системой MUSE ™; C: Желудочно-пищеводный клапан: через шесть месяцев после процедуры TIF системой MUSE ™.
Послеоперационный уход
Противорвотная профилактика, по крайней мере, двумя препаратами (согласно рекомендациям ASA для вмешательств с высоким риском постпроцедурной тошноты и рвоты) и полное расслабление мышц на протяжении всей процедуры являются обязательными для TIF. Противорвотная профилактика поддерживается внутривенно в течение 24 часов, а антибиотикотерапия широкого спектра действия продолжается внутривенно в течение 48 часов, затем перорально в течение пяти дней.
Временное раздражение глотки возникает у большинства пациентов в результате введения и манипуляции с устройством; некоторые пациенты страдают от болей в эпигастрии от легкой до умеренной степени через шесть часов после вмешательства. Если боль сохраняется дольше, следует рассмотреть утечку из пищевода или желудка; в этих случаях следует провести компьютерную томографию и рентгеноконтрастное исследование с растворимостью в воде. Временное незначительное повышение количества лейкоцитов может произойти через 24 ч после вмешательства.
Пациенты должны соблюдать жидкую диету в течение первых двух недель и мягкую диету в течение следующих четырех недель. Их также просят воздерживаться от энергичных упражнений в течение четырех недель. ИЦП могут быть прекращены через семь дней после процедуры.
Перейти к:
ОСЛОЖНЕНИЯ
Общая частота осложнений, о которых сообщалось до сих пор для TIF с устройством EsophyX ®, составляет от 3% до 10%. Основные осложнения возникали редко и были кровотечением, разрывом слизистой оболочки или перфорацией, требующей эндоскопического вмешательства или хирургического вмешательства, пневмоторакса и абсцессов средостения. Кровотечение, требующее переливания крови, отмечалось примерно в 3-5% случаев. Абсцессы средостения были зарегистрированы менее чем в 2% случаев. Случаев смерти не было.
Среди двух исследований, опубликованных на TIF с системой MUSE ™, только одно сообщило об осложнениях [ 28 ]. Незначительные побочные эффекты, такие как боль в груди, боль в горле, преходящая ателектазия, боль в плече и отрыжка, отмечались у 5,5–22% пациентов. Основные осложнения возникли в 6,2% случаев (4 из 64 пациентов): пневмоторакс, пневмоторакс и утечка пищевода, пневмомедиастинум и сильное кровотечение. Пациентам с пневмотораксом и утечкой из пищевода и с кровотечением требуется вмешательство. Все основные осложнения произошли у первых 24 пациентов.
Никаких поздних осложнений или длительных побочных эффектов при использовании техники TIF не наблюдалось.
Перейти к:
ИСХОДЫ
На сегодняшний день 21 проспективное исследование (3 рандомизированных, контролируемых) и одно ретроспективное исследование были опубликованы для TIF с использованием устройства Esophyx ® . Большинство исследований были обсервационными и проводились ограниченными сериями, с последующим наблюдением от одного до трех лет. Одно исследование сообщило о результатах до шести лет после процедуры. Шестнадцать исследований оценивали симптомы с использованием вопросов качества жизни, связанных со здоровьем (GQL); 11 оцененных записей pH-импеданса до и после процедуры. Многоцентровое проспективное исследование по сравнению эффективности TIF против омепразола в рандомизированном контролируемом исследовании.
В целом, 16 исследований показали, что TIF позволяет пациентам прекратить прием антирефлюксных препаратов или заметно снизить их дозы; четыре высказали озабоченность по поводу эффективности процедуры. В успешных исследованиях результаты через 6 и 12 месяцев после TIF показали, что 75-93% и 72-85% пациентов либо прекратили ИПП, либо снизили дозу вдвое. Нормализация воздействия на пищеводную кислоту с точки зрения общего кислотного рефлюкса, количества рефлюксов и показателя Де Мейстера была отмечена у 37-89% пациентов. Через 24 месяца после TIF ежедневная зависимость от высоких доз PPI была устранена в 75-93% [ 8 , 21 , 22 ].
Эндоскопические данные , сравнивающие фундопликации сразу после процедуры и через два года , как сообщается на рисунке Figure7.7 . В двух сериях отчетов о трехлетних исходах длительное прекращение ежедневного ИЦП варьировалось от 74% до 84% случаев [ 22 , 24 ].
Внешний файл, содержащий изображение, иллюстрацию и т. Д. Имя объекта: WJGPT-7-179-g007.jpg.
Рисунок 7
Эндоскопический обзор желудочно-пищеводного клапана сразу после и через 24 мес после трансоральной безоперационной процедуры фундопликации с помощью прибора EsophyX ® (случай авторов). A: Гастроэзофагеальный клапан: сразу после трансоральной процедуры безоперационной фундопликации (TIF) с помощью устройства EsophyX ® ; Б: Желудочно-пищеводный клапан: 24 мес после процедуры TIF с EsophyX ® устройства.
В единственном исследовании, которое наблюдалось у пациентов в течение шести лет после TIF (14 из 50), зависимость от высоких доз PPI была устранена у 86%, и примерно половина полностью остановила PPI. Неудачные результаты в основном происходили между 6 и 12 месяцами после вмешательства; результаты существенно не изменились между 12 и 36 мес. Результаты шестилетних были похожи на те , на 36 мес [ 24 ], что свидетельствует о длящейся efficay из TIF (рис (Figure88 ).
Внешний файл, содержащий изображение, иллюстрацию и т. Д. Имя объекта: WJGPT-7-179-g008.jpg.
Рисунок 8
Симптоматические реакции через шесть месяцев и через 1-6 лет после трансоральной безоперационной фундопликации с помощью устройства Esophyx ® , классифицированные в соответствии с использованием ингибитора протонной помпы. Пациенты были сгруппированы как полные респонденты [которые полностью прекратили использовать ингибитор протонного насоса (PPI)] или частичные респонденты (которые вдвое сократили предыдущую дозу PPI) и нереспонденты (которые все еще использовали дозу PPI до TIF): 12 месяцев против 6 месяцев после TIF P = 0,8; 24 месяца против 12 месяцев, P = 0,4; 36 месяцев против 24 месяцев, P = 0,7; 4 года против 36 месяцев, P = 1,0; 5 лет против 4 лет, P = 1,0; 6 лет против5 лет, Р = 1,0.
Эти результаты показывают, что отбор пациентов является определяющим фактором для достижения клинического успеха, и подтверждают, что у большинства пациентов неудачи возникают в течение первых 6-12 месяцев после процедуры.
Опыт оператора также важен в результатах. Все сбои TIF в нашей серии были у пациентов, которые прошли процедуру на ранней стадии обучения оператора. Ретроспективное исследование на 124 невыбранных пациентах в двух больницах сообщества показало, что у 75% и 80% пациентов отсутствуют симптомы GER в течение среднего периода наблюдения в течение семи месяцев, подтверждая, что опыт оператора заметно влияет на результаты [ 20 ].
На данный момент опубликовано только три проспективных рандомизированных контролируемых исследования. Двое из них сравнивали эффективность TIF или омепразола в течение шести месяцев: один обнаружил, что TIF более эффективен, чем PPI, при лечении регургитации и внепищеводных симптомов (97% и 50% пациентов, соответственно, P = 0,006) [ 26 ]; во втором анализе «намерение лечить» было показано, что TIF был более эффективным, чем PPI, для устранения симптомов ГЭРБ (67% против 45%, P = 0,023) [ 27]. Эти расхождения требуют дополнительных рандомизированных исследований для выяснения эффективности TIF при лечении ГЭРБ. В третьем исследовании сравнивались результаты TIF и фундопликации Ниссена за 3 и 12 месяцев, показав, что TIF столь же эффективен и безопасен, как и метод Ниссена, но со значительно более коротким пребыванием в стационаре (2,9 ± 0,8 д против 6,4 ± 0,7 д, р <0,0001) [ 31 ]. Симптомом ответы до шести лет после TIF с EsophyX ® устройства, с точки зрения PPI отмены или сокращения 50%, в опубликованных серии (20 исследований), приведены в таблице Table1.1 . Результаты до пяти лет после TIF от MUSE TMСистема, в отношении воздействие на использовании PPI, опубликованной в серии (два исследования) представлены в таблице Table22 .
Таблица 1
Симптоматические реакции после трансоральной безрезультатной фундопликации с помощью аппарата EsophyX®
Ссылка 6 мес 12 мес 24 мес 36 мес 6 лет
Cadière et al. [ 6 ], 2008 - 85% - - -
Cadière et al. [ 8 ], 2009 - - 93% - -
Тестони и др. [ 9 ], 2010 82% 76% - - -
Веланович и др. [ 11 ], 2010 79% - - - -
Репичи и др. [ 12 ], 2010 55% 47% - - -
Demyttenaere и др. [ 10 ], 2010 - 53% - - -
Хоппо и др. [ 13 ], 2010 - 42% - - -
Барнс и др. [ 20 ], 2011 93% - - - -
Bell et al [ 14 ], 2011 75% - - - -
Ihde et al [ 15 ], 2011 76% - - - -
Trad et al [ 18 ], 2012 - 82% - - -
Тестони и др. [ 21 ], 2012 - - 75% 75% -
Петерсен и др. [ 17 ], 2012 58% - - - -
Bell et al [ 23 ], 2012 86% - - - -
Мулс и др. [ 22 ] 2013 - 77% - 65% -
Bell et al. [ 34 ], 2013 - 82% - - -
Bell et al [ 25 ], 2014 - - 77% -80% - -
Trad et al. [ 26 ], 2015 93% - - - -
Хантер и др. [ 27 ], 2015 - 72% - - -
Тестони и др. [ 24 ], 2015 84% 80% 88% 84% 86%
Таблица 2
Симптоматические ответы после трансорального incisionless фундопликации музы ТМ системы
Ссылка 6 мес 12 мес 24 мес 36 мес 6 лет
Зачери и др. [ 28 ], 2015 83% - - - -
Рой-Шапира и др. [ 29 ], 2015 - 82% 73% 73% -
Неудачные результаты после TIF были зарегистрированы в трех исследованиях. Две серии обнаружили ухудшение воздействия на дистальную пищеводную кислоту в 66,7% случаев и стойкие симптомы GER в 68% случаев, в небольших сериях с коротким периодом наблюдения (12 месяцев) [ 12 , 13 ]. В исследовании, сравнивающем TIF с фундопликацией по Ниссену у пациентов с резистентной к PPI ГЭРБ, отмечалась ремиссия симптомов и нормализация рефлюкса желудочно-пищеводной кислоты у 30% и 100% пациентов после TIF и у 50% и 100% после хирургической фундопликации [ 16 ]. Эти данные свидетельствуют о том, что у пациентов, не реагирующих на ИПП, фундопликация Ниссена кажется более эффективной, чем TIF по EsophyX ® .
Когда TIF терпит неудачу, хирургическая фундопликация все еще возможна, без технических трудностей или увеличенной заболеваемости. Хирургическая ревизия после неудачи TIF отмечалась в 8,1% -18,0% случаев [ 21 , 22 , 32 , 33 ]. В двух исследованиях (9 и 11 пациентов) фундопликация Ниссена достигла полного исчезновения симптомов во всех случаях недостаточности TIF [ 32 , 33 ]. В нашей серии, однако, только один из четырех пациентов, которым требовалась фундопликация по Ниссену для сохранения симптомов ГЭРБ после ТИФ, прекратил применение кислотоподавляющей терапии [ 21].]. Это может зависеть от того факта, что у пациентов, перенесших TIF в нашей серии, было только незначительное нарушение желудочно-пищеводного соединения и симптомы ГЭРБ, связанные с несколькими механизмами, включая повышенную чувствительность пищевода к рефлюксату.
С другой стороны, повторное вмешательство после лапароскопической фундопликации было зарегистрировано в 14% случаев [ 1 ], а TIF был признан эффективным после неудачной операции [ 34 ].
Только в двух исследованиях до настоящего времени сообщалось о результатах после TIF с использованием техники MUSE TM (передняя фундопликация): пилотное исследование с пятилетним наблюдением и многоцентровое проспективное исследование. Пилотное исследование изучало симптомы, связанные с ГЭРБ, и использование ИПП в течение пяти лет после процедуры у 13 пациентов: оценка симптомов, связанных с ГЭРБ, нормализовалась в 92% случаев, применение ИПП было прекращено или уменьшено вдвое в 77% (54% прекратили PPI полностью) [ 29 ].
В другом исследовании сообщалось о результатах после TIF с использованием метода MUSE в многоцентровом проспективном международном исследовании, в котором приняли участие 66 пациентов с шестимесячным наблюдением [ 28 ]. Показатели симптомов, связанных с ГЭРБ, улучшились более чем на 50% у 73% пациентов, и 64,6% больше не принимали ежедневные ИПП. Среди пациентов, которые продолжали принимать ИПП, 56,5% сократили дозу более чем наполовину. При 24-часовой регистрации pH общее время при pH пищевода <4,0 значительно снизилось по сравнению с исходным уровнем. После лапароскопической фундопликации, таких как вздутие живота, отрыжка или рвота, дисфагия или диарея, не наблюдалось никаких побочных эффектов после процедуры.
Факторы, влияющие на результаты TIF
Важным вопросом, касающимся всех новых интервенционных процедур, внедряемых в клиническую практику, является признание факторов, связанных с техникой или пациентом, которые могут повлиять на результаты. Факторы, влияющие на результаты TIF, были зарегистрированы только в исследованиях EsophyX.
В нашей серии с технической точки зрения количество развернутых крепежных элементов и техника вращения были связаны с лучшим результатом; большее количество крепежей увеличило в четыре раза вероятность успеха [ 21 ]. Другое исследование также сообщило, что количество крепежных элементов играет ключевую роль для успеха процедуры [ 19 ]. Согласно другим сообщениям, ротационная техника увеличилась вдвое с вероятностью ответчика [ 19 , 23 ].
Связанными с пациентом факторами, влияющими на послеоперационные результаты в нашей серии, были предоперационные степени Хилла III и IV, грыжа пищеводной грыжи размером более 2 см и неэффективная моторика пищевода, которые были связаны с более высокой частотой неудачных результатов. Нарушение клиренса пищевода может вызывать сенсибилизацию эпителия и симптомы, связанные с рефлюксом, даже при наличии рефлюкса с низким объемом [ 35 ].
Однофакторный и многофакторный анализ предоперационных факторов, влияющих на симптоматические исходы TIF с помощью прибора EsophyX ®, был проведен на основе данных от 158 выявленных пациентов [ 25 ]. Предикторами успешных исходов для пациентов с типичными симптомами были возраст 50 лет и более, показатель качества жизни, связанный со здоровьем GERD (GERD-HRQL) на ИПП 15 или более, индекс симптомов рефлюкса> 13 на ИПП и показатель симптомов гастроэзофагеального рефлюкса 18 или больше на ИЦП. Возраст и GERD-HRLQ оставались значимыми предикторами и в многомерном анализе. Для пациентов с атипичными симптомами GER только успешные результаты были связаны только с оценкой GERD-HRQL 15 и более по ИПП.
Статьи по теме
Рекомендуемые статьи
Эластография при эндосонографии (ЭУС или эндоУЗИ)
Эластография (эластосонография) – метод виртуальной пальпации (технология улучшенной визуализации при ЭУС диагностике), позволяющий дифференцировать злокачественные и доброкачественные поражения лимфоузлов. Основана на принципе, что более мягкие ткани при сжатии легче деформируются, это позволяет объективно оценить консистенцию ткани, показать различия в плотности между нормальными и патологически измененными тканями.
При эндоскопическом исследовании в случае бронхоэктазов в стадии ремиссии выявляется
частично диффузный бронхит I степени воспаления
Активируйте PUSH уведомления в браузер
Отключите PUSH уведомления в браузер
Содержание
Интернет магазин
Популярное
- О нас
- Правовые вопросы
- Политика
обработки персональных
данных EndoExpert.ru - Связаться с нами
- Стать партнером
© 2016-2022 EndoExpert.ru

Вы находитесь в разделе предназначенном только для специалистов (раздел для пациентов по ссылке). Пожалуйста, внимательно прочитайте полные условия использования и подтвердите, что Вы являетесь медицинским или фармацевтическим работником или студентом медицинского образовательного учреждения и подтверждаете своё понимание и согласие с тем, что применение рецептурных препаратов, обращение за той или иной медицинской услугой, равно как и ее выполнение, использование медицинских изделий, выбор метода профилактики, диагностики, лечения, медицинской реабилитации, равно как и их применение, возможны только после предварительной консультации со специалистом. Мы используем файлы cookie, чтобы предложить Вам лучший опыт взаимодействия. Файлы cookie позволяют адаптировать веб-сайты к вашим интересам и предпочтениям.
Я прочитал и настоящим принимаю вышеизложенное, хочу продолжить ознакомление с размещенной на данном сайте информацией для специалистов.














.jpg)





.png)



.jpg)














Комментарии