- Компании
- Takeda. О компании, буклеты, каталоги, контакты
- Olympus. О компании, буклеты, каталоги, контакты
- Boston Scientific. О компании, буклеты, каталоги, контакты
- Pentax. О компании, буклеты, каталоги, контакты
- Fujifilm & R-Farm. О компании, буклеты, каталоги, контакты
- Erbe. О компании, буклеты, каталоги, контакты
- Еще каталоги
- Мероприятия
- Информация
- Обучение
- Классификации
- Атлас
- Quiz
- Разделы
- Пациенту
QR-код этой страницы
Для продолжения изучения на мобильном устройстве ПРОСКАНИРУЙТЕ QR-код с помощью спец. программы или фотокамеры мобильного устройства
Статьи: ПАРИЖСКАЯ КЛАССИФИКАЦИЯ ОПУХОЛЕВЫХ ПОРАЖЕНИЙ ЖКТ
- ВКонтакте
- РћРТвЂВВВВВВВВнокласснРСвЂВВВВВВВВРєРСвЂВВВВВВВВ
- Viber
- Skype
- Telegram
Из статьи Вы узнаете:
- Парижская классификация
- Термины
- Обучающее видео о Парижской классификации (Англ.)
Полный текст статьи:
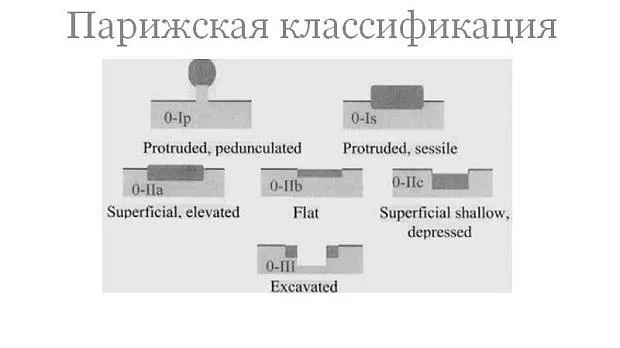
Парижская классификация опухолевых поражений
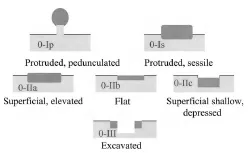
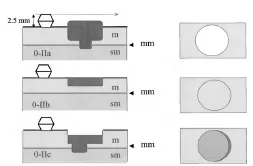
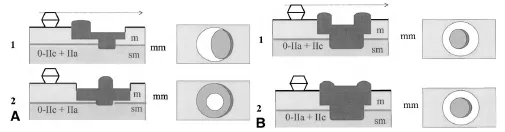
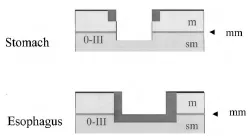
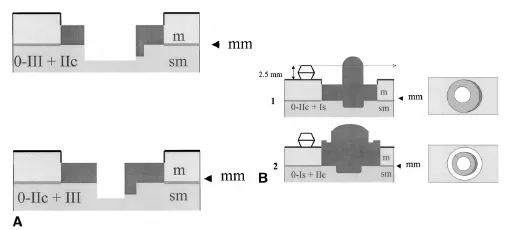
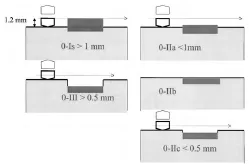
- с небольшими изменениями поверхности (слегка приподнятые (0-IIa), плоские (0-IIb), слегка вдавленные – углубленные (0-IIc)) и
- подрытые (язвенные) поражения (0-III).
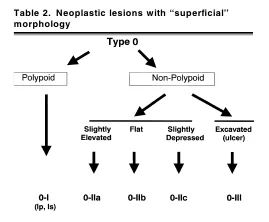
- тип 0 – поверхностные полиповидные, плоские/углубленные или подрытые опухоли;
- тип 1 – полиповидный рак, как правило, на широком основании;
- тип 2 – язвенная форма рака с четкими границами и приподнятыми краями;
- тип 3 – язвенно-инфильтративная форма рака без определенных границ;
- тип 4 – неязвенная, диффузная инфильтративная форма рака;
- тип 5 – неклассифицируемый прогрессирующий рак.
- неинвазивная низкой степени,
- неинвазивная высокой степени и
- рак с инвазией в собственную пластинку.
- Кишечная метаплазия I типа в основном состоит из поглощающих клеток с четко определенными ворсинчатыми границами, некоторого количества бокаловидных клеток, а иногда клеток Панета.
- Для кишечной метаплазии II и III типа характерны цилиндрические промежуточные клетки и бокаловидные клетки, которые выделяют сиаломуцин (тип II) или сульфомуцин (тип III).
- Отрицательная ИЭН;
- Неопределенная ИЭН;
- ИЭН низкой степени
- Аденома/дисплазия
- ИЭН высокой степени (внутриэпителиальная или внутрислизистая)
- Аденома/дисплазия
- Неинвазивный рак
- Подозрение на инвазивный рак
- Внутрислизистая карцинома (инвазия в собственную пластинку)
- Подслизистый рак
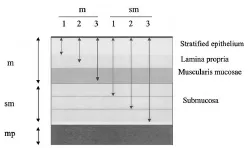
- До начала лечения с помощью диагностических тестов и процедур опухоль стадируется в соответствии с классификацией TNM; глубина инвазии опухоли в стенке кишечника соответствует Т классификации.
- В пищеводе, желудке, и толстой кишке эндоскопист классифицирует изменения «поверхностных» опухолевых поражений (интраэпителиальной неоплазии и рака) как варианты типа 0.
- Патологоанатом классифицирует гистологию опухоли по группам Венской классификации неоплазии.
- Когда доступен оперативный материал, глубина инвазии классифицируется морфологом в соответствии с T- по р-TNM классификации («р» - послеоперационный).
- В пищеводе и желудке интраэпителиальная опухоль без инвазии в собственную пластинку (р-Tis) называется «рак in situ» и не включается в реестры опухоли.
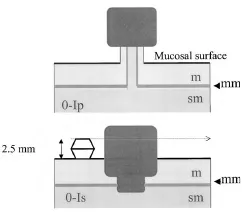
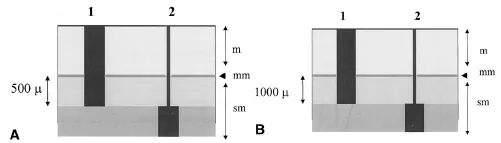
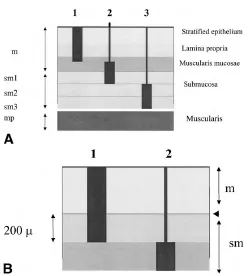
- Интраэпителиальная карцинома с инвазией в собственную пластинку СО называется р-T1m;
- Карцинома с инвазией в подслизистую оболочку – р-T1sm.
- Когда есть инвазия в подслизистую оболочку, опухоль определяется как р-T1sm.
- р-Tis, р-Tm (пищевод, желудок) или
- р-Tsm (пищевод, желудок, толстая кишка).





- классификации в эндоскопии
- Азбука Эндоскописта. Эндоскопические классификации для описания и оценки патологических изменений толстой кишки при колоноскопии
- Классификация WASP: дифференциальная диагностика гиперпластических полипов, зубчатых аденом и обычных аденом толстой кишки
- Классификация и диагностика гастритов и гастропатий
- Номенклатурная классификация медицинских изделий 3.15 Эндоскопы гастроэнтерологические
- Z-линия пищевода. Классификация ZAP
- Парижская классификация
- Классификации ЭУС критериев хронического панкреатита
- Статьи: Классификация раннего рака толстой кишки в зависимости от глубины инвазии в подслизистую основу по Кудо (S.Kudo 1993)
Статьи по теме
Рекомендуемые статьи
При эндоскопическом исследовании в случае бронхоэктазов в стадии ремиссии выявляется
частично диффузный бронхит I степени воспаления
Активируйте PUSH уведомления в браузер
Отключите PUSH уведомления в браузер
Содержание
Интернет магазин
Популярное
- О нас
- Правовые вопросы
- Политика
обработки персональных
данных EndoExpert.ru - Связаться с нами
- Стать партнером
© 2016-2022 EndoExpert.ru

Вы находитесь в разделе предназначенном только для специалистов (раздел для пациентов по ссылке). Пожалуйста, внимательно прочитайте полные условия использования и подтвердите, что Вы являетесь медицинским или фармацевтическим работником или студентом медицинского образовательного учреждения и подтверждаете своё понимание и согласие с тем, что применение рецептурных препаратов, обращение за той или иной медицинской услугой, равно как и ее выполнение, использование медицинских изделий, выбор метода профилактики, диагностики, лечения, медицинской реабилитации, равно как и их применение, возможны только после предварительной консультации со специалистом. Мы используем файлы cookie, чтобы предложить Вам лучший опыт взаимодействия. Файлы cookie позволяют адаптировать веб-сайты к вашим интересам и предпочтениям.
Я прочитал и настоящим принимаю вышеизложенное, хочу продолжить ознакомление с размещенной на данном сайте информацией для специалистов.



.jpg)




.png)



 (1).jpg)














Комментарии 3