- Компании
- Takeda. О компании, буклеты, каталоги, контакты
- Olympus. О компании, буклеты, каталоги, контакты
- Boston Scientific. О компании, буклеты, каталоги, контакты
- Pentax. О компании, буклеты, каталоги, контакты
- Fujifilm & R-Farm. О компании, буклеты, каталоги, контакты
- Erbe. О компании, буклеты, каталоги, контакты
- Еще каталоги
- Мероприятия
- Информация
- Обучение
- Классификации
- Атлас
- Quiz
- Разделы
- Пациенту
QR-код этой страницы
Для продолжения изучения на мобильном устройстве ПРОСКАНИРУЙТЕ QR-код с помощью спец. программы или фотокамеры мобильного устройства
Статьи: Манометрия пищевода высокого разрешения. Методические рекомендации. 2018
| Авторы: | В.О. КАЙБЫШЕВА Е.Л. НИКОНОВ Д.С. БОРДИН С.В. МОРОЗОВ Э.Р. ВАЛИТОВА, В.А. ИСАКОВ, А.А. СМИРНОВ, Е.Д. ФЕДОРОВ, С.Г. ШАПОВАЛЬЯНЦ 2018г. |
Анонс:
Полный текст статьи:
Предисловие авторов
Исследование двигательной функции пищевода началось в 50-х годах прошлого века. В 90-х годах возникли предпосылки для создания манометрии высокого разрешения. В настоящее время метод получил повсеместное признание и широко используется в клинической практике. С каждым годом спектр нозологий, в диагностике которых применимо использование манометрии высокого разрешения, расширяется. Число центров в Российской Федерации, в которых используется данная методика, прогрессивно увеличивается. В связи с этим возникла необходимость создания настоящих методических рекомендаций.
В руководстве кратко отражены основные пункты проведения исследования моторной функции пищевода и ключевые этапы анализа. Описаны трудности, нередко возникающие в ходе исследования, пути их преодоления, возможные ошибки.
Ключевая глава посвящена описанию фундаментальных основ моторики пищевода, нозологиям, патогенетически связанным с нарушениями двигательной функции пищевода, последним международным классификациям нарушений моторной функции пищевода, знание которых необходимо для правильной формулировки диагноза.
Каждая глава методических рекомендаций написана как независимый раздел, к которому при необходимости можно обратиться, не перечитывая предыдущих глав.
Понятие о манометрии высокого разрешения
В основе патогенеза многих заболеваний пищевода, таких как гастроэзофагеальная рефлюксная болезнь (ГЭРБ), ахалазия кардии, эзофагоспазм, лежат нарушения двигательной функции грудного отдела пищевода и/или нижнего пищеводного сфинктера (НПС). При других заболеваниях (системная склеродермия, эозинофильный эзофагит, стриктуры пищевода) моторные нарушения являются последствиями органических изменений стенки пищевода и НПС.
Наиболее точно оценить двигательную функцию пищевода и его сфинктеров позволяет манометрия пищевода высокого разрешения. Возможности этого современного и высокотехнологичного метода включают в себя измерение давления покоя и давления расслабления верхнего пищеводного сфинктера (ВПС) и НПС, частоты и длительности преходящих расслаблений НПС, интенсивности сокращений грудного отдела пищевода, определение расположения ВПС и НПС (расстояние от крыльев носа), длины пищевода. С помощью манометрии пищевода можно идентифицировать наличие грыжи пищеводного отверстия диафрагмы (ПОД), точно определить ее размеры, выявить преждевременные (спастические) или неэффективные сокращения гладкомышечного сегмента пищевода, обнаружить наличие препятствия для прохождения болюса на уровне сфинктеров [1].
Проведение манометрии пищевода показано пациентам с клиническими симптомами, свидетельствующими о возможном нарушении двигательной функции пищевода (дисфагия, загрудинная боль, регургитация, отрыжка). Особую важность оценка моторики пищевода имеет для принятия решения о возможности и необходимости хирургического лечения ГЭРБ, ахалазии кардии, для выбора метода оперативного лечения. В последние годы интерес к манометрии существенно вырос, во многом этому способствовало развитие лапароскопической и эндоскопической хирургии.
История метода
Первые исследования двигательной функции пищевода (так называемая «традиционная» (conventional) манометрия) проводились еще в 40—50-х годах XХ века с помощью внутрипищеводного баллона, заполненного водой или газом, который вводили в просвет органа. Однако данная методика имела значительные ограничения в связи с крайне медленным ответом и низкой чувствительностью регистрирующей системы на изменения внутрипищеводного давления, а также из-за влияния баллона на двигательную активность пищевода. В 70-х годах Вайл Доддс (W. Dodds) и Рой Арндорфер (R. Arndorfer) разработали принципиально новую систему измерения давления в пищеводе: манометрию с использованием водно-перфузионного катетера, состоящего из системы капиллярных трубочек, в которые наружной помпой нагнеталась вода [2, 3]. Преимуществом водно-перфузионной манометрии являлась значительно большая чувствительность (по сравнению с баллоном) и возможность регистрировать перистальтическую активность в нескольких точках по ходу пищевода. Из недостатков метода можно выделить малое количество каналов на катетере, расположенных на большом расстоянии друг от друга (не менее 5 см), а также трудоемкость и невысокую точность данных, получаемых при измерении давления в области НПС в связи со смещением сфинктера в проксимальном направлении при прохождении перистальтической волны, инициированной актом глотания.
В 1977 г. Д. Дентом (J. Dent) была предложена модификация манометрической системы с использованием принципа sleeve-катетера, который включал в себя так называемый «рукав»: шестисантиметровую область на дистальном конце катетера, содержащую большое количество каналов на близком расстоянии друг от друга, работающих как единый чувствительный элемент [4]. Наличие рукава (sleeve) позволило нивелировать подвижность НПС и проводить более точные измерения, результаты которых выдавались на экран в виде нескольких двухмерных кривых (по оси ординат — давление, по оси абсцисс — время). Анализ кривых позволял оценить давление покоя и остаточное давление в НПС, амплитуду сокращений грудного отдела пищевода, диагностировать спастические сокращения, отсутствие сокращений в грудном отделе пищевода в ответ на глоток [1, 4].
Работы по оптимизации методов исследования нарушений моторной функции пищевода проводились также и в России. В 1970—1980 гг. В.Х. Василенко и А.Л. Гребенев использовали зонд, имеющий несколько баллонов небольшого диаметра, что позволяло избежать излишней стимуляции пищевода и возникновения вторичных сокращений его стенки [5].
Неоценимый вклад в развитие методов функциональной диагностики пищевода в нашей стране внесла С.А. Чернякевич, разработав принципиально новый метод исследования — иономанометрию с применением специального комбинированного зонда («Исток-система», Фрязино), несущего кроме датчиков рН также два открытых манометрических катетера, расстояние между которыми составляло 5 см. Принцип метода состоял в протягивании зонда из желудка в пищевод с интервалом 1—0,5 см с фиксацией изменений давления в различных отделах пищевода. Совмещение возможностей рН-метрии и манометрии в одном исследовании позволяло одновременно обнаружить нарушения двигательной функции пищевода, структурные аномалии НПС (скользящую хиатальную грыжу) и гастроэзофагеальный рефлюкс [5, 6].
В 1990-х годах Рэй Клаус (Ray Clouse) с коллегами разработали новую систему измерения давления, характеризовавшуюся тем, что расстояние между чувствительными элементами уменьшилось с 3—5 до 1 см, а число датчиков, расположенных на катетере от глотки до пищевода, увеличилось до 36. Такой подход дал возможность оценивать моторную функцию ВПС, пищевода и НПС одновременно и в совокупности [7].
Существенным преимуществом метода (перед использовавшейся ранее традиционной манометрией пищевода) стало добавление цветного отображения данных, позволившее оценивать перистальтическую активность пищевода с использованием 3 параметров: расстояние (см) — по оси Y, время © — по оси Х, давление (мм рт.ст.) отражено цветом (по аналогии с географическими картами). При этом более высоким значениям давления соответствуют цвета красно-коричневого спектра, а более низким — сине-голубого, что дает возможность получить наглядную и удобную для анализа и интерпретации картину моторно-эвакуаторной функции пищевода (рис. 1)
Основными преимуществами манометрии высокого разрешения являются точность вычислений, простота выполнения процедуры и наглядность метода. Непосредственно в процессе исследования программное обеспечение синтезирует целостную картину двигательной активности пищевода таким образом, что на экране выдается изображение функциональной анатомии пищевода в режиме реального времени.
Для стандартизации методики проведения исследования, анализа результатов, систематизации нозологий в 2008 г. в Сан-Диего (США) был проведен консенсус специалистов в области манометрии пищевода, итогом которого явилось создание Чикагской классификации нарушений моторной функции пищевода (The Chicago Classification of esophageal motility disorders). В последующем подобные консенсусы проводились в 2011 г. в Асконе (Швейцария) и в 2014 г. в Чикаго (США). Результаты последнего консенсуса Чикагской классификации нарушений моторной функции пищевода 3-го пересмотра (The Chicago Classification of esophageal motility disorders, v 3.0) опубликованы в журнале Neurogastroenterology and Motility в 2015 г. [9].
В Российской Федерации первое заседание рабочей группы и Экспертного совета, посвященное методологии и терминологии манометрии высокого разрешения, было проведено 11 ноября 2017 г. в рамках научно-практической конференции «Современные аспекты диагностики и лечения доброкачественных заболеваний пищевода 2017» (Санкт-Петербург). Результатами работы Экспертного совета, опубликованными в виде «Первого российского соглашения по манометрии пищевода высокого разрешения» в журнале «Доказательная гастроэнтерология» (№ 1, 2018 г.) стало принятие единой методики проведения манометрии пищевода и общепринятой русскоязычной терминологии [37].
Преимущества манометрии высокого разрешения
Несмотря на очевидно более высокую точность, заложенную в метод манометрии пищевода высокого разрешения в сравнении с традиционной, прямые сравнения обоих методов достаточно сложны. Одной из основных характеристик любого диагностического метода являются воспроизводимость результатов, которую оценивают, используя коэффициенты внутриисследовательской (однородность значений, получаемых одним и тем же исследователем) и межисследовательской (однородность значений, получаемых разными исследователями) согласованности. Для манометрии пищевода высокого разрешения как внутри-, так и межисследовательская согласованность получаемых данных достаточно высока. Преимущества манометрии пищевода высокого разрешения по сравнению с традиционной манометрией приведены в табл. 1.
Таблица 1. Преимущества и недостатки манометрии пищевода высокого разрешения по сравнению с традиционной манометрией
Показания к проведению манометрии пищевода высокого разрешения
— Дисфагия (после исключения органических причин): диагностика эзофагоспазма, ахалазии, неэффективной моторики пищевода.
— Некардиальная боль в грудной клетке: диагностика дистального эзофагоспазма, гиперконтрактильного пищевода, ахалазии, грыжи ПОД.
— Предоперационное обследование больных с ахалазией кардии (для подтверждения диагноза, уточнения типа ахалазии).
— Предоперационное обследование больных с ГЭРБ, которым планируется проведение антирефлюксных операций (для исключения неэффективной моторики пищевода, ахлазии, уточнения размера грыжи ПОД).
— Предоперационное обследование больных с ожирением, которым планируется проведение бариатрических операций.
— Контроль эффективности оперативного лечения ахалазии кардии и ГЭРБ.
— Определение положения НПС перед проведением рН-метрии или рН-импедансометрии пищевода.
— Дисфагия после антирефлюксных операций.
Противопоказания к проведению манометрии пищевода высокого разрешения
— Злокачественные новообразования пищевода и желудка.
— Язвы пищевода и желудка.
— Варикозное расширение вен пищевода 2—4-й степени.
— Недавние (до 3 мес) хирургические вмешательства или кровотечения из верхних отделов желудочно-кишечного тракта.
— Ожоги, дивертикулы, декомпенсированные стриктуры пищевода.
— Упорный кашель или рвота.
— Аневризма аорты.
— Тяжелые формы гипертонической болезни и ишемической болезни сердца.
— Обструкция носоглотки.
— Челюстно-лицевые травмы.
— Тяжелые формы коагулопатий.
— Психические заболевания.
Подготовка пациента к исследованию
Манометрия пищевода высокого разрешения проводится натощак. Исследование не должно проводиться в один день с эндоскопическими процедурами и с рентгеноскопией пищевода. Не рекомендуется употреблять твердую пищу в течение минимум 4 ч, а жидкость — как минимум в течение 2 ч до начала исследования. У больных, у которых эвакуация содержимого из просвета пищевода или желудка замедлена (ахалазия кардии, гастропарез), требуется более длительный период отказа от приема пищи. Следует предупредить пациентов о необходимости воздержаться от жевательной резинки и курения за 3—4 ч до начала процедуры.
Препараты, способные повлиять на моторную функцию пищевода, по возможности должны быть отменены за 24 ч до начала исследования. К таким лекарственным средствам относятся: препараты, воздействующие на бета-адренорецепторы (бета-адреноблокаторы, бета-агонисты), нитраты, антагонисты кальция, холинолитики, прокинетики, седативные средства, никотин, кофеин, опиаты, алкоголь. В случае если пациент использовал лекарственные средства перед проведением процедуры, перечень этих препаратов должен быть отражен в протоколе исследования.
В соответствии с законодательством Российской Федерации пациент или его законный представитель должен быть надлежащим образом и в доступной форме проинформирован «о целях, методах оказания медицинской помощи, связанном с ними риске, возможных вариантах медицинского вмешательства, о его последствиях, а также о предполагаемых результатах», при этом добровольное информированное согласие пациента должно быть получено в письменном виде до начала исследования.
При получении согласия пациент должен иметь возможность задать вопросы и получить на них ответы. Пациент должен быть проинформирован о возможности отзыва информированного согласия на проведение исследование в любое время по своему усмотрению.
Пациенту необходимо предоставить информацию о правилах поведения в период проведения исследования для уменьшения риска осложнений (не сопротивляться введению зонда, не морщить нос, не отклонять голову, не пытаться самостоятельно удалять зонд).
До начала исследования специалист, проводящий манометрию пищевода, должен ознакомиться с жалобами обследуемого пациента и его анамнезом для выявления возможных противопоказаний и ограничений к проведению процедуры, состояний, которые способны повлиять на технику проведения и интерпретацию результатов (большие грыжи ПОД, предшествующие оперативные вмешательства). Должен быть проведен сбор аллергологического анамнеза и переносимости лекарственных средств, в том числе использующихся для анестезии.
Психологическое состояние пациента и прием лекарств могут значительно повлиять на результаты исследования двигательной функции пищевода, в связи с чем в кабинете по проведению исследования рекомендовано создать спокойную и дружественную атмосферу, детально рассказать пациенту об этапах исследования. Желательно заранее разъяснить пациенту, что в процессе выполнения процедуры потребуется его активное участие в виде совершения глотков (питьевая вода комнатной температуры, дополнительные тесты с использованием твердой пищи).
В случае ахалазии пищевода 2—3-й степени (при скоплении пищевых масс в расширенном пищеводе) перед исследованием рекомендуется провести промывание пищевода через желудочный зонд.
Методика проведения манометрии высокого разрешения
В настоящем пособии кратко описаны ключевые этапы проведения манометрии пищевода высокого разрешения на системе для клинических исследований Solar GI HRM
производимой компанией «MMS» (Нидерланды). Более подробно ознакомиться с работой на данном аппарате можно в руководстве пользователя Solar GI HRM, прилагаемом к аппарату. Для измерений на данном аппарате можно выбрать электронные (твердотельные) или водно-перфузионные катетеры в комбинации с перфузионной системой MMS.
Компания «MMS» впервые представила манометрию высокого разрешения в 1995 г. под названием «Контурные графики Клозе» (в честь французского ученого Ray Clouse, являвшегося одним из основоположников метода).
Процедура манометрии пищевода высокого разрешения включает в себя несколько этапов:
1. Подготовка к исследованию и калибровка катетера.
2. Введение катетера в пищевод и установка его на нужную глубину.
3. Проведение исследования по протоколу, соответствующему Чикагской классификации.
4. Анализ результатов.
5. Формирование заключения.
Этап 1. Подготовка к исследованию, калибровка катетера
Подготовка оборудования
До начала исследования оборудование должно быть проверено и откалибровано в соответствии с рекомендациями производителя, описанными в руководстве пользователя Solar GI (код документа MMS: 0075-MAN-009).
Многоразовые катетеры должны быть подвергнуты надлежащей дезинфекции до проведения процедуры в соответствии с действующими нормативными актами и инструкцией производителя. Следует соблюдать правила асептики во избежание контаминации оборудования перед исследованием. Исследованию предшествует создание паспорта пациента в базе данных (БД) программного обеспечения компьютера и калибровка системы.
Для начала нового исследования в базу данных «MMS Database» необходимо ввести сведения о пациенте, выбрав на верхней панели инструментов кнопку «Новый пациент» и введя требуемую информацию в появившемся окошечке (рис. 3).
После сохранения информации по пациенту его имя будет отображаться в БД программы. Найти ранее зарегистрированного в БД пациента можно путем поиска через поисковую строку. Для начала нового обследования нужно выбрать зарегистрированного ранее пациента из БД и нажать кнопку «Новое обследование» на верхней панели экрана (рис. 4).
Сразу после активации нового исследования программа предложит список возможных протоколов, по которым возможно осуществление исследования (манометрия пищевода, аноректальная манометрия и др.). На данном этапе необходимо выбрать пункт «Манометрия пищевода» и решить (в зависимости от используемого катетера), будет проводиться манометрия с оценкой изменений импеданса или без нее (рис. 5).
После выбора протокола программа предложит подтвердить соответствие подготовленного для исследования катетера данному протоколу (рис. 6)
После подтверждения соответствия катетера активизируется нагнетание давления в помпу и поступление воды по капиллярам водно-перфузионного катетера. В этот период внизу экрана (на так называемой панели информации) выводятся данные о величине давления в помпе, которое должно достигнуть 1000 mBar. Более низкие цифры давления говорят о неисправности или о негерметичности помпы (рис. 7).
На этом этапе необходимо подождать несколько минут, пока все капилляры заполнятся водой, и затем приступить к калибровке катетера.
Калибровка водно-перфузионного катетера
Калибровка катетера представляет собой создание так называемого «нулевого уровня». Для этого водно-перфузионный катетер располагают на уровне предполагаемого нахождения тела пациента в период исследования. Как правило, обнуление проводят путем расположения катетера чуть выше кушетки, на которой будет лежать пациент во время исследования, после нажатия кнопок на верхней панели экрана «Обнулить все» (процесс обнуления начнется сразу после активации кнопки) или «Обнулить после 10 секунд» (процесс обнуления начнется через 10 с) (рис. 8).
После обнуления катетера все датчики давления, расположенные на экране сбоку от анатомической панели, будут демонстрировать нулевой уровень (давление 0 мм рт.ст.) с небольшими колебаниями (±1 мм рт.ст.) (рис. 9).
Для того чтобы убедиться в бесперебойной работе всех капилляров, рекомендовано приподнять катетер (удерживая его горизонтально) на 40—50 см выше кушетки, что в норме приведет к повышению цифр давления на каждом датчике до 40—50 мм рт.ст. Опускание катетера ниже нулевого уровня будет сопровождаться появлением одинаково отрицательных цифр давления.
В случае если все датчики давления демонстрируют одинаковые результаты, можно приступать к введению катетера в пищевод.
Калибровка твердотельного катетера
Для калибровки твердотельного катетера необходимо погрузить участок катетера, содержащего датчики давления, в дистиллированную воду не менее чем на 2 мин (максимальная глубина 1 см=1 мбар=0,75 мм рт.ст.=0,1 кПа). При этом обнуление результатов происходит сразу после нажатия кнопки «Обнулить все» («Zero all»). Далее рекомендуется провести оценку работоспособности и чувствительности всех каналов катетера. Это возможно путем создания последовательного легкого сдавливания рабочей поверхности катетера (например, стерильной салфеткой), в ответ на которое датчики зафиксируют повышение давления, что отобразится на экране монитора компьютера. При этом следует избегать растяжения рабочей поверхности зонда для сохранения его долговечности.
Проверка чувствительности проводится путем погружения зонда в воду на глубину 20 см. При этом давление должно увеличиться на 15 мм рт.ст. с допустимым отклонением ±0,75 мм рт.ст.
Этап 2. Введение катетера в пищевод и установка его на нужную глубину
Введение катетера
Катетер для проведения манометрии вводится в пищевод трансназально, что значительно улучшает переносимость исследования. В качестве местной анестезии перед интубацией рекомендуется орошение полости носа спреем с лидокаином либо нанесение на катетер лубриканта с лидокаином. Важно до проведения анестезии провести опрос в отношении наличия аллергических реакций на используемый анестетик.
Перед проведением анестезии спреем с лидокаином пациента просят вдохнуть и задержать дыхание на вдохе. После того как орошение слизистой оболочки носа проведено, пациента просят осуществить спокойный выдох через рот.
Введение катетера должно проводиться без значительных усилий, через нижний носовой ход той ноздри, дыхание через которую осуществляется легче. Прохождение катетера через полость носа в глотку обычно сопровождается ощущением «провала» катетера (приблизительно на расстоянии 15 см от крыла носа).
Далее пациента следует попросить слегка наклонить голову вперед к грудной клетке. Пациенту дается чистая питьевая вода комнатной температуры для совершения глотательных движений, облегчающих введение зонда в просвет пищевода. Момент дальнейшего продвижения катетера следует координировать с глотательным движением пациента (глоток по команде). После прохождения катетером уровня надгортанника необходимо попросить пациента сказать несколько слов громким голосом, чтобы исключить попадание катетера в дыхательные пути (в данном случае пациент не сможет говорить из-за раздражения голосовых связок, а будет кашлять). Дальнейшее введение катетера должно проводиться без усилий, постепенно, предпочтительно под визуальным контролем изображения на экране монитора, на глубину 40—60 см (в зависимости от роста пациента и длины пищевода).
Адекватной глубиной введения зонда считается та, при которой на экране монитора отображаются ВПС, и не менее 3 см ниже дистальной границы НПС. После установки катетер должен быть зафиксирован гипоаллергенным пластырем у носа пациента.
При правильном введении катетера 3—5 см его дистального отдела должны находиться в желудке. Учитывая, что в среднем НПС расположен на расстоянии 40—45 см от ноздрей, катетер вводят до метки 50—60 см (метки, указывающие глубину введения, обозначены на катетере). Если после введения катетера на контурном графике удается четко распознать две зоны высокого давления, соответствующие ВПС И НПС, как указано на рис. 10, то
процедуру введения катетера заканчивают, устанавливая (с помощью левой кнопкой мыши) индикаторы ВПС и НПС на анатомической панели в соответствии с их положением на графике. Область катетера с большим количеством датчиков давления (sleeve) при правильной установке должна находиться в области пищеводно-желудочного соединения (см. рис. 10).
Если же катетер был введен слишком глубоко, то на контурном графике будет видна только одна зона высокого давления, соответствующая НПС. В таких случаях следует чуть вытянуть катетер наружу до тех пор, пока на графике не станут видны оба сфинктера.
Введение катетера при ахалазии или стенозе кардии
В некоторых ситуациях (при стенозе или ахалазии кардии) могут возникнуть сложности в проведении катетера через НПС в желудок: кончик катетера сворачивается в пищеводе, на контурном графике не удается идентифицировать НПС, желудочное давление и дальнейшее исследование становится невозможным. В подобных случаях введение манометрического катетера необходимо проводить в условиях эндоскопического отделения, контролируя процесс прохождения через ригидный НПС в желудок трансназальным эндоскопом.
Проверка правильности установки катетера
В покое давление в полости желудка в норме ниже, чем в области НПС: под областью давления 20—40 мм рт.ст. (зеленый цвет, соответствующий НПС) располагается область более низкого давления, окрашенная в сине-зеленый цвет. Судить о попадании катетера в желудок можно, попросив пациента сделать глубокий вдох и выдох и наблюдая на экране монитора за изменениями цвета на контурном графике. При правильной установке катетера во время вдоха давление в желудке увеличивается (появляется слабо-зеленая окраска), а в грудной полости уменьшается и становится отрицательным (глубокий синий цвет) (рис. 11).
Адаптация к катетеру
После успешного введения катетера пациенту предлагают лечь на спину с чуть приподнятым головным концом кровати (15°) и 3—5 мин спокойно полежать (стабилизация моторики). За это время прекращаются позывы на рвоту (если таковые были), температура катетера выравнивается с температурой тела, пациент успокаивается. При использовании твердотельного катетера принимать горизонтальное положение не обязательно, достаточно находиться в состоянии покоя в течение 3—5 мин. В этот период для уменьшения вызванных введением зонда неприятных ощущений пациенту следует по возможности не фиксировать свое внимание на них и стараться совершать меньше глотательных движений.
На данном этапе, ориентируясь на манометрическое изображение, можно изменить положение катетера (подтягивая его наружу или вводя глубже) таким образом, чтобы на контурных графиках были обязательно видны НПС, ВПС, желудочное давление.
Убедившись в правильной установке (на манометрическом плоте четко визуализируются все анатомические ориентиры: ВПС, НПС, желудочное давление) и надежной фиксации катетера (во избежание его смещения в период процедуры регистрации) можно начинать исследование.
Перед началом регистрации моторной функции пищевода пациенту нужно объяснить, что во время исследования ему по возможности следует воздержаться от глотков слюны («сухих» глотков), разговоров, покашливания. Приступать к исследованию следует тогда, когда пациент будет способен не совершать глотательных движений, не кашлять и находиться в спокойном состоянии.
Процесс записи моторной функции пищевода начинается с момента активации кнопки на верхней панели экрана «Старт записи» («Start investigation») (рис. 12).
Сразу после начала исследования на экране монитора появится окошко, требующее указать глубину, на которую был введен катетер (Catheter depth) (рис. 13).
Глубина введения определяется исследователем по меткам, нанесенным на катетер.
После указания глубины введения катетера следует приступить непосредственно к выполнению протокола исследования.
Если во время процедуры произойдет смещение катетера, следует своевременно внести возникшие изменения в программу, путем активации на верхней панели экрана кнопки с изображением зонда (рис. 14).
Изменить данные о глубине введения катетера возможно только в процессе проведения исследования, на этапе анализа функция смены глубины отсутствует.
Этап 3. Проведение исследования
Исследование двигательной функции пищевода с использованием водно-перфузионной системы проводится в положении лежа на спине (чтобы исключить влияние силы тяжести на давление жидкости в капиллярах водно-перфузионного катетера и на двигательную функцию пищевода). При использовании твердотельных катетеров исследование можно проводить как в вертикальном положении пациента, так и в положении лежа, однако необходимо помнить о том, что действующие нормативы моторики пищевода разработаны для горизонтального положения пациента.
В ходе исследования проводят оценку давления покоя НПС и перистальтическую активность грудного отдела пищевода в ответ на 10 глотков по 5 мл жидкости. Интервал между совершением глотков должен составлять не менее 30 с [9].
Кроме выполнения стандартного протокола, многие исследователи признают важность проведения дополнительных диагностических тестов (выходящих за рамки Чикагской классификации), таких как глотки твердой пищи (вареный рис, сухой крекер) и «множественные быстрые глотки» жидкости (5 глотков жидкости объемом по 2 мл, следующих с интервалом в 2—3 с), что позволяет более полно оценить латентные нарушения и резервные возможности моторной функции пищевода [10—15].
Чикагская классификация рассматривает только первичные нарушения моторной функции пищевода (у лиц, не подвергавшихся хирургическому лечению). В период исследования проводят оценку расположения НПС и ВПС (расстояние от крыльев носа), давления покоя сфинктеров, остаточного давления в НПС и ВПС при их расслаблении в ответ на глоток, определение сократительной и эвакуаторной функции пищевода.
Исследование давления покоя ВПС и НПС
Для проведения анализа считается репрезентативным 30-секундный интервал без глотательных движений, срыгивания, разговора, кашля, задержек пациентом дыхания (свободное ритмичное дыхание без усилий) и пр.
Регистрация давления покоя НПС инициируется нажатием кнопки «Давление покоя» (Resting pressure), которая находится в левом верхнем углу экрана (рис. 15).
В период записи давления покоя пациент не должен глотать и разговаривать по меньшей мере 30 с.
Для окончания записи давления покоя требуется нажать на эту же кнопку, которая будет теперь называться «Остановить давление покоя» («Stop resting pressure»).
Обычно измерение давления покоя проводится в начале исследования, однако оно может быть проведено и после проведения стандартных тестов. Российская группа экспертов по проведению манометрии пищевода высокого разрешения пришла к соглашению, что исследование давления покоя должно проводиться как до проведения тестов, так и после него, с расчетом средних значений (во избежание ошибок интерпретации).
Исследование перистальтической активности пищевода
Для записи перистальтической активности пищевода в ответ на глотки жидкости («влажные глотки»), пациента, лежащего на спине, просят по команде исследователя делать глотки чистой негазированной воды комнатной температуры объемом 5 мл. Вода подается в рот пациента с помощью одноразового шприца. По команде доктора «Глоток!» пациент должен проглотить весь объем жидкости, в этот же момент исследователь нажимает на верхней панели экрана кнопку «Глоток жидкости 5 мл» или «Влажный глоток» («Wet swallow») (в зависимости от настроек программы и типа программного обеспечения названия кнопок могут отличаться) (см. рис. 15).
После осуществления каждого влажного глотка пациента просят не глотать слюну, не разговаривать и не кашлять в течение 30 с. Это связано с необходимостью реполяризации мышечных волокон тела пищевода для следующего полноценного сокращения. В случае если пациент не смог выполнить вышеперечисленные условия, необходимо нажать кнопку на верхней панели экрана «Удалить последнее событие» («Remove last marker») и повторить глоток заново после 30-секундного покоя.
Согласно Чикагской классификации, для получения достоверных результатов необходимы данные по меньшей мере 10 полноценно выполненных глотков. Если исследователь сомневается в правильности выполнения глотка, то лучше продублировать его, провести большее количество глотков. В дальнейшем в процессе анализа можно будет выбрать глотки, наиболее соответствующие указанным требованиям, удалив остальные.
По совершении 10 влажных глотков возможно проведение дополнительных провокационных тестов, после чего необходимо завершить исследование нажатием кнопки «Остановка записи» («Stop investigation») (рис. 16),
что приведет к прекращению работы помпы и выходу программы в основное меню (БД).
После проведения всех необходимых тестов и завершения исследования пациента просят сделать глубокий вдох и задержать дыхание, затем быстрым, но не резким движением вынимают катетер.
Катетер отсоединяется от аппарата и подвергается стерилизации в соответствии с действующими нормативными актами и рекомендациями производителя. В случае использования одноразовых катетеров они могут быть утилизированы без дополнительной обработки.
Этап 4. Анализ исследования
Анализ проведенного исследования осуществляется на приборе Solar GI специальной программой QuickView, которая запускается автоматически из БД путем выбора нужного исследования из списка.
Программа QuickView имеет несколько режимов, позволяющих быстро и удобно провести необходимые шаги по анализу исследований (рис. 17):
Режимы работы программы анализа.
— Overview (быстрый просмотр и удаление ненужных событий);
— Edit (редактирование событий);
— Timeline (просмотр целого исследования, не разделенного на события);
— Shuffle (просмотр событий в режиме 3D).
Важно знать, что справа от контурных графиков в любом из режимов программы анализа расположена панель, содержащая краткий перечень рекомендуемых шагов анализа (analysis guide), которая поможет вспомнить начинающему исследователю порядок действий (рис. 18).
Алгоритм анализа данных
В программе QuickView для выполнения анализа полученных данных рекомендуется следующая последовательность шагов:
1. Обзор всех выполненных (влажные глотки, давление покоя) событий (в режиме Overview).
2. Удаление глотков, выполнение которых не соответствует рекомендованному протоколу (в режиме Overview).
3. Редактирование и утверждение положения маркеров анатомических ориентиров в окне Landmark («Ориентиры») в режиме Edit.
4. Анализ и утверждение каждого события (глотков и давления покоя) в отдельности в режиме Edit.
5. Утверждение диагноза по Чикагской классификации (в режиме Edit).
6. Формирование отчета (в режиме Overview).
При выборе любого проведенного исследования в БД программа анализа автоматически открывается в режиме Overview (быстрый просмотр). Режим Overview дает возможность увидеть одномоментно все события, которые были отмечены исследователем во время процедуры: влажные глотки, давление покоя, множественные глотки и т. д. На данном этапе необходимо бегло просмотреть события и удалить ненужные (рис. 19).
Далее рекомендуется провести детальный анализ событий в режиме Edit, который открывается щелчком левой кнопки мыши на любом событии в режиме Overview. Работу в режиме Edit следует начинать с окошка «Landmark» (рис. 20).
Окно «Landmark» предназначено для проверки правильности расположения маркеров анатомических ориентиров на контурном графике.
К ключевым анатомическим ориентирам, необходимым для корректного анализа моторной функции пищевода, относятся:
— ВПС (UES) и НПС (LES);
— переходная зона (TZ);
— точка инверсии давления (PIP);
— желудочное давление (gastric).
Определить границы ВПС и НПС, как правило, не представляет сложности. В норме это зоны высокого давления, отражаемые на графике теплыми цветами (от зеленого до интенсивно красного). Желудочное давление — зона низкого давления, располагающаяся непосредственно под пищеводно-желудочным соединением.
Идентификация точки инверсии давления PIP является более сложной задачей, которая решается путем передвижения маркера PIP снизу вверх — от зоны желудочного давления в сторону грудной полости (рис. 21).
В момент движения маркера PIP в верхней части экрана (над контурным графиком) отображаются два линейных графика (красный и синий). Один из них отображает давление на 1 см выше индикатора PIP, другой — на 1 см ниже. Пересечение красной и синей линий свидетельствует о нахождении маркера PIP на уровне диафрагмы.
После проверки и коррекции расположения маркеров анатомических ориентиров ВПС, НПС, TZ, PIP, желудочного давления необходимо утвердить выбранное положение маркеров нажатием кнопки «Аpprove» (рис. 22).
Рис. 22. Работа в режиме Edit: редактирование и подтверждение положения анатомических ориентиров ВПС, НПС, TZ, PIP, желудочного давления в окошке «Landmark».
Это приведет к автоматической установке маркеров на том же уровне на всех последующих событиях и позволит программе анализа провести расчеты.
Как только подтверждение положения маркеров будет произведено, в нижней части контурного графика появится надпись «Select next» (рис. 23),
Рис. 23. Работа в режиме Edit: маркеры ВПС, НПС, TZ, PIP, желудочного давления установлены правильно, подтверждены.
нажатие на которую позволит перейти дальше, к анализу глотков и давления покоя.
Последующий анализ в режиме Edit проходит по единой схеме для каждого отдельного события (глотка или давления покоя), которую кратко можно описать как «проверь и подтверди».
Этапы анализа каждого события включают:
— проверку правильности расположения анатомических маркеров в данном событии (verify swallow);
— проверку правильности заключения, выдаваемого программой анализа (verify scoring);
— утверждение события (approve);
— переход к анализу следующего события.
Анализ события «давление покоя» в режиме Edit
Анализ давления покоя включает коррекцию (при необходимости) расположения анатомических ориентиров (ВПС, НПС, желудочное давление, PIP) и оценку правильности результатов, которые выдала программа.
Для события «давление покоя» программа вычисляет следующие показатели, которые выводятся в виде таблицы под контурным графиком (рис. 24):
Верхний пищеводный сфинктер
— Верхняя и нижняя граница ВПС (расстояние от ноздрей).
— Давление покоя среднее (resting mean).
— Давление покоя минимальное (resting min).
Нижний пищеводный сфинктер
— Верхняя граница НПС (расстояние от ноздрей).
— Давление покоя среднее (resting mean).
— Давление покоя минимальное (resting min).
— Длина грыжи пищеводного отверстия диафрагмы (выдается только в случае, если точка инверсии давления PIP расположена ниже НПС).
Полученные результаты можно сравнить с установленными референсными значениями, которые выводятся на экран справа от контурного графика при нажатии кнопки F9 (рис. 25).
Кроме расчета анатомических и функциональных показателей ВПС и НПС программа анализа выдает в таблице с результатами заключение «Scoring». Для давления покоя заключение включает в себя суждение о наличии или отсутствии грыжи ПОД (hiatal hernia), о величине давления в НПС и ВПС (нормальное, пониженное, повышенное давление) (рис. 26, 27).
В случае если исследователь не согласен с заключением программы, то он может изменить его, кликнув мышкой на соответствующий результат и выбрав в открывшемся окошке другой вариант (рис. 28).
Если при визуальном анализе давления покоя исследователь делает вывод, что у пациента имеется грыжа ПОД, а программа выдает результат об отсутствии грыжи, то также можно внести изменения в графу «Scoring» (рис. 29).
Однако в данном случае нужно проверить — правильно ли на графике расположен ориентир точки инверсии давления PIP, поскольку диафрагма (а следовательно и PIP) при наличии грыжи должна быть расположена ниже НПС. Таким образом, чтобы получить в заключении результат «грыжа ПОД», имеет смысл пересмотреть расположение маркера PIP, расположив его ниже нижней границы НПС (рис. 30),
после чего программа идентифицирует грыжу и заключение изменится автоматически.
После внесения правок и изменений, требуется утвердить проделанную работу нажатием кнопки «Одобрить» и перейти к анализу следующего изображения. Только события, получившие подтверждение «Одобрить», будут в дальнейшем включены в расчет средних показателей результата исследования.
Анализ события «влажный глоток» в режиме Edit
Анализ глотков включает правку расположения анатомических ориентиров глотка и при необходимости — коррекцию заключений программы.
При анализе перистальтики пищевода в ответ на глоток жидкости в режиме Edit на контурном графике появляются дополнительные ориентиры (кроме тех, что были на графиках давления покоя), которые расставляются программой автоматически. К таким ориентирам относятся: точка начала расслабления ВПС (UES relaxation start), точка замедления сокращения дистального отдела пищевода (contractile deceleration point, CDP), маркер переходной зоны TZ (рис. 31).
Если исследователь не согласен с автоматической расстановкой маркеров, можно изменить ее, перетаскивая маркеры левой кнопкой мыши.
Важно помнить, что пренебрежение данным этапом анализа может привести к получению недостоверных и даже абсурдных заключений (рис. 32—34).
Рис. 33. Ручная корректировка расположения маркеров глотка, изображенного на рис. 32, и получение правильных результатов измерений суммарного давления расслабления ВПС.
Рис. 34. Неправильно выполненный и проанализированный глоток.
Рис. 32. Пример получения ошибочных результатов измерения при неправильном расположении маркеров глотка: в заключении программы указано крайне высокое суммарное давление расслабления ВПС.
На следующем рисунке (рис. 34) показан пример сразу нескольких ошибок, совершенных в пределах одного исследования в процессе записи глотков и при их анализе: исследователь слишком поздно отметил глоток в процессе записи исследования, в связи с чем программа ошибочно идентифицировала момент открытия ВПС, сокращение грудного отдела пищевода. При анализе исследования положение маркеров также не было скорректировано. Заключение, рассчитанное при таком расположении маркеров, будет абсолютно неинформативно.
Опираясь на расположение ориентиров глотка, программа анализа вычисляет следующие показатели (рис. 35):
Рис. 35. Работа в режиме Edit: таблица с результатами измерений «влажного глотка».
Верхний пищеводный сфинктер
— Верхняя и нижняя граница ВПС (расстояние от ноздрей).
— Суммарное давление расслабления ВПС, вычисляемое за период 0,2 с (суммарное давление расслабления, IRP 0,2 с).
— Суммарное давление расслабления ВПС, вычисляемое за период 0,8 с (суммарное давление расслабления, IRP 0,8 с).
Нижний пищеводный сфинктер
— Верхняя граница НПС (расстояние от ноздрей).
— Суммарное давление расслабления НПС, вычисляемое за период 4 с (суммарное давление расслабления, IRP).
Грудной отдел пищевода
— Дистальный сократительный интеграл (DCI).
— Наибольший разрыв перистальтки (Largest break).
— Дистальная латентность (Distal latency).
— Интраболюсное давление (IBP).
Детально проанализировав изображение, выделив имеющиеся отклонения от нормы, сравнив цифровые результаты измерений двигательной функции пищевода с нормами (анализу глотков и давления покоя посвящена отдельная глава методического пособия), нужно перейти к оценке глотка, которое выдала программа анализа в таблице результатов в графе «Scoring».
Оценка «Scoring» глотка жидкости дает характеристику:
— интенсивности (силе) перистальтических сокращений грудного отдела пищевода (нормальное, слабое, неудавшееся, гиперсокращение);
— структурному типу сокращения грудного отдела пищевода (нормальное перистальтическое сокращение, преждевременное, фрагментированное);
— интраболюсному давлению (норма, тотальное повышение интраболюсного давления, сегментарное повышение интраболюсного давления, повышение интраболюсного давления в зоне пищеводно-желудочного соединения).
Просмотрев заключение программы и согласившись с ним, необходимо закончить анализ глотка нажатием кнопки «Approve» (одобрить). Если же по каким то пунктам исследователь не согласен с автоматическим результатом, то он может изменить его, кликнув мышкой на соответствующую строку, выбрать верный вариант в открывшемся окне и затем одобрить глоток.
Как только все глотки будут проанализированы, система выдаст конечный результат в виде контурного графика, который является математически сгенерированным изображением абстрактного среднего глотка (рис. 36).
Рис. 36. Работа в режиме Edit: средний результат по 10 глоткам жидкости по 5 мл.
Под контурным графиком в таблице результатов также будут отражены усредненные показатели глотков, получивших в процессе анализа статус «Approved» (одобрены).
Таблица результатов среднего глотка вместо графы «Scoring» содержит графу «Classification», состоящую из двух пунктов:
— наличие обструкции пищеводно-желудочного соединения;
— заключение по Чикагской классификации.
В случае если исследователь не согласен с заключением программы в отношении диагноза, можно изменить его, выбрав из списка Чикагской классификации нарушений моторики пищевода нужный диагноз (рис. 37).
Заканчивают анализ «среднего глотка» обязательным нажатием кнопки «Approve» (одобрить), в противном случае данные расчета средних показателей не отразятся в заключении.
Этап 5. Формирование заключения
После проверки и одобрения всех усредненных событий приступают к формированию заключения, перейдя с этой целью в режим Overview (рис. 38).
Режим Overview дает возможность еще раз наглядно оценить, какие события были проанализированы и одобрены (они отмечены зеленой галочкой в правом верхнем углу каждого события), какие события были проанализированы, но не были одобрены (отмечены восклицательным знаком), какие события вовсе не были проанализированы (отмечены красным кружком). Только события, отмеченные зеленой галочкой, будут включены в расчет средних показателей и в заключение.
При необходимости режим Overview позволяет исследователю исключить те или иные события из процесса математического анализа или же, напротив, — включить в анализ те события, которые ранее показались исследователю непригодными: для этого необходимо сменить зеленую галочку «Approved» (одобрен) в правом верхнем углу события на желтый восклицательный знак «Not approved» (не одобрен) и наоборот.
По умолчанию в заключение в виде рисунка включаются только «средние» глотки и их параметры. В связи с этим изначально на всех событиях стоит значок, изображающий перечеркнутый лист бумаги и означающий, что данное событие не будет отображаться в заключении в виде отдельного рисунка. Если же какой-то из глотков обладает особенно-важной диагностической ценностью, то его изображение и цифровые параметры можно дополнительно включить в отчет, путем нажатия на иконку «Включить в отчет» (рис. 39).
Выбрав события для расчета средних показателей и для включения в отчет, переходят непосредственно к созданию отчета. С этой целью необходимо нажать кнопку «Reporter» на верхней панели экрана режима Overview (рис. 40).
Если исследователь хочет дополнить отчет своим заключением или комментарием, то их вписывают в окне для комментариев, открывающемся при нажатии соответствующей кнопки (см. рис. 40).
Таким образом, в заключении будут отражены диагноз в соответствии с Чикагской классификацией, комментарии и диагноз врача-исследователя, включены таблицы с цифровыми результатами по всем глоткам отдельно и их средние значения, цветное изображение усредненного глотка, дополнительные события, выбранные исследователем (рис. 41).
Этапы анализа моторной функции пищевода, согласно Чикагской классификации нарушений моторной функции пищевода
Для проведения анализа контурных графиков, полученных в результате исследования, введены ключевые понятия и ориентиры.
В состоянии покоя (отсутствие глотков, разговора и кашля) в зоне расположения ВПС и НПС на контурных графиках выделяют 2 зоны повышенного давления, обозначаемые в Чикагской классификации термином «давление покоя» (resting pressure). Кроме того, можно наблюдать изменения давления в функционально различных отделах пищевода, связанные с изменением давления в грудной и брюшной полостях в зависимости от фазы дыхания (рис. 42):
— на вдохе давление в грудной полости снижается (отрицательное давление), пищеводно-желудочное соединение (esophago-gastric junction, EGJ) сдвигается по направлению к желудку в связи с сокращением ножек диафрагмы, давление в пищеводно-желудочном соединении при этом повышается [10];
— на выдохе давление в грудной полости повышается, а зона пищеводно-желудочного соединения сдвигается в проксимальном направлении.
Анализ контурных графиков в покое включает оценку:
— давления покоя НПС;
— cтруктуры пищеводно-желудочного соединения.
Чикагская классификация нарушений моторной функции пищевода не рассматривает патологические состояния, касающиеся давления покоя НПС. Более того, для данного показателя отсутствуют общепринятые манометрические нормативы. Значения давления покоя НПС, полученные в исследованиях на здоровых добровольцах, различаются в зависимости от аппаратуры, числа участников и колеблются в среднем от 19 до 31 мм рт.ст. (табл. 2).
Таблица 2. Давление покоя НПС в исследованиях среди здоровых добровольцев [16]
Имеет ли клиническое значение оценка давления покоя НПС — по сей день не вполне понятно. Исследований, однозначно доказывающих корреляцию давления покоя с заболеваниями пищевода, нет [16]. Считается, что снижение цифр давления покоя НПС наиболее характерно для больных с ГЭРБ [10] и системной склеродермией (рис. 43),
тогда как повышение давления покоя НПС чаще всего наблюдается при ахалазии (рис. 44).
Рис. 44. Давления покоя НПС 45 мм рт.ст. у больного с ахалазией кардии 3-го типа.
Разработан новый показатель оценки функционального состояния пищеводно-желудочного соединения: сократительный интеграл пищеводно-желудочного соединения (esophagogastric junction contractile integral, EGJ-CI), который оценивает одновременно тонус и продольную длину НПС совместно с ножками диафрагмы. В норме значения EGJ-CI не должны быть ниже 39—47 мм рт.ст./см [38, 39]. По всей видимости, данный показатель войдет в новую классификацию нарушений моторной функции пищевода, что позволит более точно изучать состояние пищеводно-желудочного соединения.
Согласно Чикагской классификации выделяют следующие структурные типы пищеводно-желудочного соединения [9]:
— 1-й тип (норма): полное совпадение НПС и ножек диафрагмы — на контурном графике пищеводно-желудочное соединение представлено единым пиком давления покоя (рис. 45);
Рис. 45. Морфология пищеводно-желудочного соединения: 1-й тип.
— 2-й тип (вариант нормы): небольшое (1—2 см) разделение НПС и ножек диафрагмы, создающее 2 пика давления, но снижение давления между пиками не достигает уровня внутрижелудочного давления (рис. 46);
Рис. 46. Морфология пищеводно-желудочного соединения: 2-й тип.
— 3-й тип (аксиальная диафрагмальная грыжа): НПС и ножки диафрагмы разделены более чем на 2 см и давление между ними ниже внутрижелудочного (рис. 47).
Рис. 47. Морфология пищеводно-желудочного соединения: 3-й тип.
Анализ контурных графиков в ответ на глотки жидкости
После оценки функции пищевода в покое переходят к исследованию моторики пищевода в ответ на глотки жидкости. В период осуществления пациентом глотков манометрия пищевода оценивает способность ВПС и НПС к релаксации, интенсивность сокращения грудного отдела пищевода, наличие всех обязательных сегментов перистальтической волны.
В норме наблюдаются синхронная релаксация ВПС и НПС, возрастающая продолжительность и сила перистальтических сокращений грудного отдела пищевода при продвижении волны в дистальном направлении. Хорошо визуализируется переходная зона между проксимальным (с поперечнополосатой мускулатурой) и средним (гладкомышечным) отделом пищевода.
Согласно Чикагской классификации [9] рекомендовано проводить анализ двигательной функции пищевода по определенной иерархической схеме, сначала оценивая каждый глоток в отдельности, а затем рассматривая совокупность выявленных изменений.
Анализ каждого нового глотка начинают с вычисления эффективности расслабления НПС с помощью специального интегрального показателя — суммарное давление расслабления (integrated relaxation pressure, IRP).
IRP является математической величиной, которая рассчитывается программой анализа в 10-секундном интервале (начинающемся с момента открытия ВПС) как сумма участков с наименьшим остаточным давлением за период 4 с. В норме IRP не превышает 15 мм рт.ст. [9]. Цифровое значение IRP вычисляется как относительная величина (на сколько мм рт.ст. давление выше, чем в желудке) и зависит от внутрижелудочного давления (в случае, если датчик желудочного давления «gastric» будет расположен неправильно, то цифры IRP могут оказаться отрицательными). В связи с этим рекомендовано дистальный кончик катетера проводить в желудок достаточно глубоко (как минимум на 2 см ниже пищеводно-желудочного соединения).
Повышение суммарного давления расслабления в НПС свидетельствует о функциональной (ахалазия) или органической (стриктура, опухоль) обструкции пищеводно-желудочного соединения (см. рис. 61—66).
Рис. 62. Повышение интраболюсного давления в зоне пищеводно-желудочного соединения (EGJ pressurization).
Рис. 63. Ахалазия 1-го типа (type I achalasia): повышение IRP, отсутствие перистальтических сокращений грудного отдела пищевода.
Рис. 64. Ахалазия 2-го типа (type II achalasia): повышение IRP, отсутствие перистальтических сокращений грудного отдела пищевода, тотальное повышение интраболюсного давления.
Рис. 65. Ахалазия 3-го типа (type III achalasia): повышение IRP, преждевременные (спастические) сокращения грудного отдела пищевода.
Рис. 66. Обструкция пищеводно-желудочного соединения (EGJ outflow obstruction).
Рис. 61. Сегментарное повышение интраболюсного давления (сompartmentalized pressurization).
После анализа IRP приступают к оценке силы (интенсивности, мощности) сокращений гладкомышечного отдела пищевода, возникающих в ответ на глоток 5 мл жидкости. С этой целью используется интегральный показатель — дистальный сократительный интеграл (distal contractile integral, DCI), который отражает одновременно силу и скорость сокращения гладкомышечного отдела пищевода [9].
В зависимости от силы (интенсивности) сокращения (contraction vigor) Чикагская классификация 3-го пересмотра подразделяет сокращения на следующие типы [9, 16, 17]:
— сокращение нормальной силы (normal): 450<DCI<8000 мм рт.ст. · см · с (рис. 48);
Рис. 48. Сокращение нормальной силы (normal): 450<DCI<8000 мм рт.ст. · см · с.
— гиперсокращение (hypercontractile): DCI>8000 мм рт.ст. · см · с. Сокращение становится чрезмерно интенсивным, сопровождается выраженной загрудинной болью (рис. 49);
Рис. 49. Гиперсокращение (hypercontractile): DCI>8000 мм рт.ст. · см · с.
— неэффективное сокращение (ineffective): DCI<450 мм рт.ст. · см · с.
Неэффективные сокращения в зависимости от степени снижения DCI в свою очередь подразделяются на неудавшиеся сокращения (failed, DCI<100 мм рт.ст. · см · с, рис. 50)
Рис. 50. Неудавшееся сокращение (failed): DCI<100 мм рт.ст. · см · с.
и ослабленные сокращения (weak, 100<DCI<450 мм рт.ст. · см · с, рис. 51).
Рис. 51. Ослабленное сокращение (weak): 100<DCI<450 мм рт.ст. · см · с.
Если после анализа силы перистальтического сокращения патологии выявлено не было, то приступают к следующему этапу иерархического анализа: оценке структуры перистальтического сокращения (contraction pattern).
В норме перистальтическое сокращение распространяется от ВПС в дистальном направлении постепенно (рис. 52).
Рис. 52. Сегменты перистальтического сокращения пищевода.
Начавшись c поперечнополосатых мышц проксимального отдела пищевода (сегмент S1), преодолевая так называемую переходную зону (transition zone, TZ), где перистальтические сокращения отсутствуют в связи с переходом поперечнополосатой мускулатуры в гладкую, сокращение достигает гладкомышечного отдела пищевода (сегменты S2 и S3). При переходе на область пищеводно-желудочного соединения сокращения замедляются и сменяются так называемым «ампулярным очищением» (сегмент S4) [9].
Однако не всегда сокращения в пищеводе следуют описанному алгоритму, иногда сокращения гладкомышечного отдела пищевода начинаются преждевременно, что приводит к практически одновременному сокращению проксимального и дистального отделов пищевода, сопровождающихся сильнейшей болью за грудиной, нарушением перистальтической функции пищевода, дисфагией. Другим нарушением структуры перистальтического сокращения является появление в пределах перистальтической волны больших разрывов перистальтики, что может приводить к нарушению осуществления пищеводного клиренса.
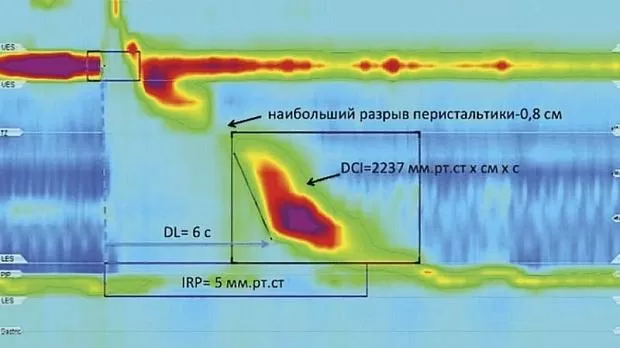
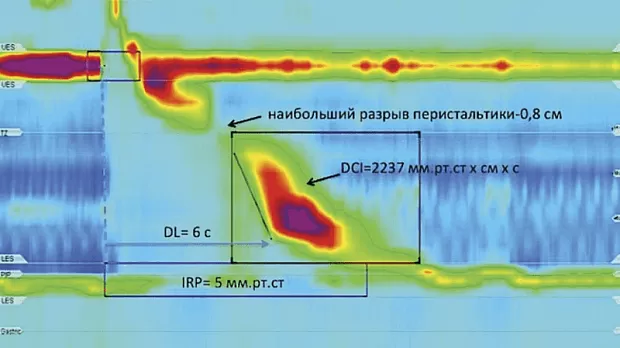
Для анализа структуры сокращений пищевода используются следующие показатели (рис. 53):
Рис. 53. Ключевые показатели манометрии пищевода высокого разрешения.
точка замедления сокращения (contractile deceleration point, CDP), наибольший разрыв перистальтики (largest break), дистальная латентность (distal latency, DL) [9].
CDP — точка на изобаре 30 мм рт.cт., в которой перистальтические сокращения дистального отдела пищевода замедляются и сменяются «ампулярным очищением» (рис. 54).
Рис. 54. Точка замедления сокращения на изобаре 30 мм рт.ст.
В случае если установить расположение CDP затруднительно (при атипичной форме перистальтической волны), следует придерживаться правила: CDP находится в пределах 3 см от проксимального края НПС [9].
При неэффективной моторике пищевода, когда сокращения дистального отдела пищевода протекают со сниженной интенсивностью, CDP измеряют на изобаре 20 мм рт.ст. (рис. 55).
Рис. 55. Определение CDP на изобаре 20 мм рт.ст. при неэффективной моторике пищевода.
При чрезмерно сильных сокращениях CDP определяют на 50 мм рт.ст. В случае если в просвете пищевода находится болюс (например, при обструкции зоны пищеводно-желудочного соединения), то CDP также находят на изобаре 50 мм рт.ст., чтобы исключить влияние интраболюсного давления (рис. 56)
Рис. 56. Определение CDP на изобаре 50 мм рт.ст. при повышенном давлении в просвете пищевода, связанном с наличием болюса.
[9].
Правильное определение точки CDP имеет решающее значение, поскольку позволяет вычислить продолжи тельность дистальной латентности (DL, distal latency).
DL — временной отрезок, продолжающийся от начала раскрытия ВПС до CDP. В норме длительность интервала DL составляет не менее 4,5 с (см. рис. 53, 55, 56). Данный показатель был введен в анализ с целью выявления так называемых преждевременных сокращений, возникающих при дистальном эзофагоспазме или ахалазии 3-го типа. С патофизиологической точки зрения появление преждевременных сокращений свидетельствует о дисфункции (или гибели) ингибиторных нейронов межмышечного сплетения [11].
Наибольший разрыв перистальтики (largest break) — область на перистальтической волне, где сокращения мышечной стенки пищевода отсутствуют или протекают с амплитудой менее 20 мм рт.ст. В норме длина наибольшего перистальтического разрыва не превышает 5 см (рис. 57 и 59).
Рис. 59. Фрагментированное сокращение (fragmented): длина наибольшего разрыва перистальтики более 5 см, 450<DCI<8000 мм рт.ст. · см · с.
Рис. 57. Нормальное сокращение (intact): DL>4,5 с, разрыв перистальтики отсутствует, 450<DCI<8000 мм рт.ст. · см · с.
В зависимости от длительности интервала DL и длины наибольшего разрыва перистальтики Чикагская классификация 3-го пересмотра подразделяет сокращения с нормальным DCI (450<DCI<8000 мм рт.ст. · см · с) на следующие структурные типы (contraction pattern) [9, 16]:
— нормальное сокращение (intact): DL>4,5 с, длина наибольшего разрыва перистальтики менее 5 см (см. рис. 57);
— преждевременное (спастическое) сокращение (premature): DL<4,5 с (рис. 58);
Рис. 58. Преждевременное сокращение (premature): DL<4,5 c, 450<DCI<8000 мм рт.ст. · см · с.
— фрагментированное сокращение (fragmented): длина наибольшего разрыва перистальтики более 5 см (см. рис. 59).
Необходимо отметить, что сокращения с DCI<450 мм рт.ст. · см · с не подлежат анализу по структуре, так как признаются неэффективными.
Следующим этапом анализа является оценка давления болюса в полости пищевода в период осуществления глотка. При нормальной перистальтической активности пищевода интраболюсное давление (intrabolus pressure, IBP) должно превышать внутрижелудочное, но быть не выше 30 мм рт.ст.
При наличии препятствия для продвижения болюса и сохраненной перистальтической активности грудного отдела пищевода IBP повышается.
Согласно Чикагской классификации 3-го пересмотра выделяют несколько типов повышения интраболюсного давления (intrabolus pressure pattern) [9, 11]:
— тотальное повышение интраболюсного давления (panesophageal pressurization): повышение интраболюсного давления (более 30 мм рт.ст.) в пищеводе на всем протяжении от НПС до ВПС. Наиболее часто тотальное повышение интраболюсного давления наблюдается при ахалазии 2-го типа (рис. 60);
Рис. 60. Тотальное повышение интраболюсного давления (panesophageal pressurization).
— сегментарное повышение интраболюсного давления (сompartmentalized pressurization): повышение интраболюсного давления, распространяющееся от фронта волны сокращения до зоны пищеводно-желудочного соединения. Данная манометрическая картина наблюдается при механической обструкции кардии (стриктура, грыжа) или при дебюте ахалазии на фоне сохраненной сократительной активности дистального отдела пищевода (рис. 61);
— повышение интраболюсного давления в зоне пищеводно-желудочного соединения (EGJ pressurization): повышение давления болюса в зоне, ограниченной ножками диафрагмы и НПС при грыже ПОД (рис. 62).
После анализа каждого из глотков в отдельности выявленные нарушения моторики пищевода оцениваются в совокупности с применением иерархического алгоритма, рекомендованного Чикагской классификацией.
Типы нарушений двигательной функции пищевода
Чикагская классификация подразделяет все возможные состояния двигательной функции пищевода на четыре большие группы [9]:
— нарушения, обусловленные обструкцией пищеводно-желудочного соединения (disorders with EGJ outflow obstruction);
— значительные нарушения перистальтики (major disorders of peristalsis);
— малые нарушения перистальтики (minor disorders of peristalsis);
— нормальная моторика пищевода (normal esophageal motility).
Нарушения, обусловленные обструкцией пищеводно-желудочного соединения
Согласно алгоритму анализа исследования, рекомендованному Чикагской классификацией, первым оцениваемым показателем является суммарное давление расслабления (IRP). Отсутствие адекватного расслабления НПС, сопровождаемое повышением IRP>15 мм рт.ст., наблюдается при нескольких формах нарушений двигательной функции пищевода (схема 1), объединенных под общим названием «Нарушения, обусловленные обструкцией пищеводно-желудочного соединения» (Disorders with EGJ outflow obstruction) [9, 18]:
Схема 1 Чикагская классификация нарушений моторной функции пищевода: нарушения, обусловленные обструкцией пищеводно-желудочного соединения
— ахалазия (achalasia): IRP>15 мм рт.ст., перистальтические сокращения в грудном отделе пищевода отсутствуют (DCI<100 мм рт.ст. · см · с) или наблюдаются преждевременные (спастические) сокращения (DL<4,5 с, DCI>450 мм рт.ст. · см · с);
— обструкция пищеводно-желудочного соединения (EGJ outflow obstruction): IRP>15 мм рт.ст., перистальтические сокращения в грудном отделе пищевода сохранены.
Ахалазия (Achalasia)
Среди первичных расстройств моторики пищевода наибольшее значение имеет ахалазия* (от греч. — отсутствие расслабления). В основе патогенеза ахалазии лежит дегенеративный процесс, избирательно поражающий возбуждающие и ингибиторные нейроны, обеспечивающие сокращение и расслабление гладкой мускулатуры пищевода.
В зависимости от обнаруженных при проведении манометрии пищевода изменений перистальтики грудного отдела пищевода, Чикагская классификация 3-го пересмотра выделяет три основных типа нарушений двигательной функции пищевода, характерных для заболевания «ахалазия кардии» [9]:
— ахалазия 1-го типа (type I achalasia): повышение суммарного давления расслабления НПС (IRP>15 мм рт.ст.) сопровождается полным отсутствием сокращений в грудном отделе пищевода (в 100% глотков DCI<100 мм рт.ст. · см · с), интраболюсное давление не повышено (рис. 63);
— ахалазия 2-го типа (type II achalasia): повышение суммарного давления расслабления НПС (IRP>15 мм рт.ст.) сопровождается отсутствием перистальтических сокращений, однако сохраненный тонус стенок пищевода обуславливает тотальное повышение интраболюсного давления как минимум в 20% глотков (рис. 64);
— ахалазия 3-го типа (type III achalasia): повышение суммарного давления расслабления НПС (IRP>15 мм рт.ст.) сопровождается преждевременными (спастическими) неперистальтическими сокращениями (DCI>450 мм рт.ст. · см · с, DL<4,5 с) гладкомышечного отдела пищевода как минимум в 20% глотков (рис. 65).
Существует гипотеза, что описываемые на манометрии пищевода типы нарушений моторики пищевода, наблюдаемые у больных с ахалазией кардии, являются не тремя разными формами заболевания, а последовательными этапами развития ахалазии [19]. Считается, что на начальной стадии заболевания (возникающей при постепенной гибели ингибирующих мотонейронов) наблюдаются изменения моторики по типу спастической ахалазии (3-й тип), затем, по мере гибели возбуждающих нейронов и угнетения сократительной функции пищевода наблюдается картина ахалазии 2-го типа. При тотальной гибели двигатель-ных нейронов межмышечного сплетения возникают изменения моторики, описываемые, как ахалазия 1-го типа, сопровождающиеся значительным расширением пищевода, его S-образной деформацией [19].
Обструкция пищеводно-желудочного соединения (EGJ outflow obstruction)
Заключение «Обструкция пищеводно-желудочного соединения» делается в том случае, если полученные показатели не полностью удовлетворяют манометрическим критериям ахалазии: перистальтика грудного отдела пищевода сохранена, несмотря на значительное повышение суммарного давления расслабления НПС (IRP>15 мм рт.ст.) (рис. 66). Таким пациентам необходимо проведение дополнительных уточняющих исследований: компьютерная томография органов грудной клетки и брюшной полости, эндосонография и др.
В дальнейшем, манометрическое заключение «Обструкция пищеводно-желудочного соединения», вероятнее всего, трансформируется в диагноз «ахалазия кардии» или будет выявлена механическая обструкция зоны пищеводно-желудочного соединения (стриктура или опухоль пищевода или кардиального отдела желудка, параэзофагеальная грыжа ПОД и др.) [18].
В случае если патология со стороны пищеводно-желудочного соединения исключена, переходят к следующему этапу иерархического анализа: оценке интенсивности и структуры перистальтических сокращений грудного отдела пищевода. Согласно Чикагской классификации нарушения перистальтики делятся на две большие подгруппы [9]:
— значительные нарушения перистальтики;
— малые нарушения перистальтики.
Значительные нарушения перистальтики (major disorders of peristalsis)
Значительные нарушения перистальтики никогда не встречаются у здоровых лиц, они связаны с выраженными изменениями показателей дистальной латентности (DL) и дистального сократительного интеграла (DCI) при нормальных средних значениях суммарного давления расслабления (IRP), протекают с явной клинической симптоматикой и включают в себя следующие типы (схема 2):
Схема 2 Чикагская классификация нарушений моторной функции пищевода: значительные нарушения перистальтики.
— дистальный эзофагоспазм (distal esophageal spasm): в 20% глотков и более наблюдаются преждевременные сокращения (DL<4,5 с) при нормальных средних значениях IRP и DCI (см. рис. 58);
— гиперконтрактильный пищевод (hypercontractile esophagus): в 20% глотков и более наблюдается повышение DCI>8000 мм рт.ст. · см · с при нормальных средних значениях IRP (рис. 67);
Рис. 67. Гиперконтрактильный пищевод (hypercontractile esophagus): более чем в 20% глотков наблюдается повышение DCI>8000 мм рт.ст. · см · с.
— отсутствие сократимости (absent contractility): в 100% глотков сокращения пищевода отсутствуют (failed, DCI<100 мм рт.ст. · см · с), средние значения IRP находятся в пределах нормы, что не позволяет установить диагноз «ахалазия» (рис. 68).
Рис. 68. Отсутствие сократимости (absent contractility) в грудном отделе пищевода у больной с системной склеродермией.
При гиперконтрактильном пищеводе сокращения неперистальтические, зачастую имеют спастический характер: мультипиковые, повторяющиеся, преждевременные (DL<4,5 c), сопровождаются выраженной загрудинной болью и дисфагией. Наиболее эффективными методами лечения гиперконтрактильного пищевода являются хирургические операции, применяемые для лечения ахалазии (прежде всего, пероральная эндоскопическая миотомия).
Отсутствие сократимости чаще всего наблюдается у больных с системными заболеваниями соединительной ткани (системная склеродермия) и лежит в основе патогенеза развития тяжелой эрозивной ГЭРБ, зачастую рефрактерной к антисекреторной терапии.
Малые нарушения перистальтики (minor disorders of peristalsis)
Малые нарушения перистальтики могут обнаруживаться при проведении манометрии у бессимптомных пациентов как случайная находка. Характеризуются они снижением интенсивности (DCI<450 мм рт.ст. · см · с) или нарушением структуры перистальтических сокращений (наибольшие разрывы перистальтики менее 5 см).
Малые нарушения перистальтики имеют клиническое значение для пациентов с ГЭРБ, так как в большинстве случаев приводят к нарушению пищеводного клиренса. Считается также, что малые нарушения перистальтики могут служить предикторами послеоперационной дисфагии в случае проведения антирефлюксных операций [10, 16].
Малые нарушения перистальтики включают в себя следующие типы (схема 3) [9]:
Схема 3 Чикагская классификация нарушений моторной функции пищевода: малые нарушения перистальтики.
— неэффективная моторика пищевода (ineffective esophageal motility): более 50% сокращений неэффективны (DCI<450 мм рт.ст. · см · с) при нормальных средних значениях IRP<15 мм рт.ст. (рис. 69);
Рис. 69. Неэффективная моторика пищевода (ineffective esophageal motility) у больного ГЭРБ.
— фрагментированная перистальтика (fragmented peristalsis): более 50% сокращений протекают с большими разрывами перистальтики (largest break более 5 см) при нормальных значениях DCI>450 мм рт.ст. · см · с и IRP<15 мм рт.ст. (см. рис. 59).
Манометрия пищевода в рамках предоперационного обследования больных с ахалазией кардии
Основываясь на данных, полученных при проведении манометрии пищевода у больных с ахалазией, возможно проводить выбор метода оперативного лечения (в зависимости от выявленного типа нарушений моторики) и прогнозировать успех лечения. Так, по имеющимся на сегодняшний день данным, наилучшие результаты хирургического лечения наблюдаются при ахалазии 2-го типа, сложнее всего поддается лечению ахалазия 3-го типа, поскольку при данном типе высока вероятность рецидивов (табл. 3).
Таблица 3. Вероятность успешного лечения в зависимости от типа ахалазии [11]
Сравнительная эффективность и безопасность трех наиболее распространенных инвазивных методов лечения ахалазии — баллонной пневмокардиодилатации (БПКД), пероральной эндоскопической миотомии (ПОЭМ) и лапароскопической миотомии по Геллеру (ЛМГ) интенсивно изучается в проспективных рандомизированных исследованиях и окончательное заключение еще не сделано. Однако ни у кого из специалистов нет сомнений в том, что выбор метода эндоскопического и хирургического лечения ахалазии зависит не только от стадии заболевания, но и от данных, полученных при проведении манометрии.
При проведении манометрии пищевода у больных с дисфагией, загрудинной болью могут выявляться и другие (кроме ахалазии) нарушения перистальтики пищевода, сопровождающиеся преждевременными сокращениями или гиперсокращениями, такие как гиперконтрактильный пищевод и дистальный эзофагоспазм. Наиболее эффективным методом лечения гиперконтрактильных нарушений моторики пищевода (так же, как и при спастической ахалазии) является проведение ПОЭМ. Однако результаты ПОЭМ при данных патологиях не столь обнадеживающие, как при ахалазии (табл. 4).
Таблица 4. Эффективность ПОЭМ при заболеваниях, сопровождающихся гиперконтрактильными нарушениями моторики пищевода [44]
Проведение манометрии пищевода при подозрении на ахалазию кардии дает возможность верифицировать диагноз, установить тип ахалазии, провести дифференциальный диагноз с органической обструкцией кардии, гиперконтрактильным пищеводом, эзофагоспазмом, выбрать оптимальный метод эндоскопического или хирургического лечения.
Манометрия пищевода в рамках предоперационного обследования больных с гастроэзофагеальной рефлюксной болезнью
При проведении манометрии пищевода у больных с ГЭРБ нередко удается выявить снижение интенсивности сокращений гладкомышечного отдела пищевода, объединенные понятием «неэффективная моторика пищевода», большие разрывы перистальтической волны. Неэффективная моторика зачастую не сопровождается клиническими симптомами, но может приводить к нарушениям пищеводного клиренса, а следовательно, к длительной экспозиции рефлюктата в пищеводе [45]. В то же время, согласно современным представлениям, проведение фундопликации больным с неэффективной моторикой пищевода может привести к развитию дисфагии.
Кроме неэффективной моторики пищевода, у больных с ГЭРБ в некоторых случаях удается выявить полное отсутствие сократимости пищевода (см. рис. 68). Отсутствие сократимости чаще всего наблюдается у больных с системными заболеваниями соединительной ткани (системная склеродермия) и лежит в основе патогенеза развития тяжелой эрозивной ГЭРБ, зачастую рефрактерной к антисекреторной терапии. Проведение фундопликации таким больным сопряжено с высоким риском развития послеоперационной дисфагии. Имеющиеся на сегодняшний день данные исследований по лечению больных с ГЭРБ с отсутствием сократимости пищевода свидетельствуют о более благоприятных результатах частичной фундопликации (по Toupe) по сравнению с классической операцией по Ниссену [16].
Согласно современным рекомендациям, лечение больных с ГЭРБ на фоне неэффективной перистальтики пищевода включает назначение высокоэффективных ингибиторов протонной помпы (эзомепразол 40 мг) и соблюдение определенных условий при приеме пищи: тщательно пережевывать и запивать пищу водой, отдавать предпочтение полужидкой пище, есть в вертикальном положении, не ложиться после еды, не принимать пищу перед сном [10, 16, 46].
Существуют исследования, показывающие некоторое улучшение моторики пищевода на фоне применения прокинетиков: пиридостигмина, буспирона [47], метоклопрамида [48], эритромицина [49, 50], цизаприда и тагасерода [51, 52], однако выраженные и очень серьезные побочные эффекты не позволяют использовать данные препараты для лечения больных с ГЭРБ с неэффективной моторикой пищевода. Прокинетические препараты, разрешенные для длительного применения (итоприд и прукалоприд), не оказывают значимого влияния на силу и продолжительность сокращений гладкомышечного отдела пищевода, в связи с чем их применение при неэффективной моторике пищевода нерационально [53—55].
Кроме оценки перистальтической активности грудного отдела пищевода манометрия позволяет проводить диагностику скользящей грыжи ПОД, с высокой точностью определяя ее размеры. В академическом варианте при грыже ПОД на манометрическом графике область пищеводно-желудочного перехода оказывается представлена двумя зонами повышенного давления: дистальное повышение давления соответствует уровню ножек диафрагмы, проксимальное — собственно тонусу НПС (см. рис. 47).
Важно помнить также о том, что ахалазия кардии в ряде случаев сопровождается клиническими симптомами ГЭРБ. При проведении фундопликации у таких пациентов клиническая картина лишь усугубится, а больной будет обречен на повторное оперативное вмешательство. Согласно современным рекомендациям по хирургическому лечению ГЭРБ [56], манометрия пищевода является обязательным исследованием перед проведением фундопликации.
Таким образом, обследование больного с ГЭРБ с использованием современных методов функциональной диагностики дает возможность врачу понять, что лежит в основе развития симптомов и осложнений рефлюксной болезни, и более дифференцированно и грамотно подойти к лечению каждого конкретного пациента. Так, например, выявление большой грыжи пищеводного отверстия диафрагмы позволит объяснить ГЭРБ анатомическими дефектами кардии и прибегнуть к обоснованному в данном случае хирургическому лечению. В то же время обнаружение неэффективной моторики пищевода у больного с изжогой и эрозивными изменениями слизистой оболочки, напротив, будет являться возможным противопоказанием к хирургическому лечению из-за опасности развития тяжелой послеоперационной дисфагии.
Нормальная моторика пищевода
Нормальная двигательная функция пищевода (рис. 70),
Рис. 70. Нормальная моторика пищевода (normal esophageal motility).
согласно Чикагской классификации, определяется следующими манометрическими критериями [9]:
— обструкция пищеводно-желудочного соединения отсутствует (IRP<15 мм рт.ст.);
— более 50% глотков эффективны (DCI>450 мм рт.ст. · см · с, largest break менее 5 см);
— число патологических (преждевременных, неудавшихся или гиперсокращений) сокращений не превышает 20%.
Дополнительные провокационные тесты
Дополнительные провокационные тесты могут проводиться для выявления изменений моторики в условиях, более приближенным к физиологическим. К таким провокационным тестам относят питье больших объемов воды: больной выпивает быстрыми глотками 200 мл воды (rapid drink chalange, RDC) и/или выполнение пяти быстрых глотков по 2 мл воды (multiple rapid swallows, MRS), использование единичных глотков с большим (15 мл) объемом жидкости. С этой же целью могут быть использованы дополнительные тесты с проглатыванием твердого болюса (хлеб или аналоги) или приемов пищи (стандартный прием пищи или использование тех продуктов, которые провоцируют возникновение симптомов у обследуемого). Эти тесты обычно проводятся в вертикальном положении тела обследуемого (сидя) [12—15].
Значение теста с множественными быстрыми глотками (MRS) заключается в том, что в норме в период совершения нескольких глотков подряд происходит расслабление ВПС и НПС с одновременным угнетением перистальтики грудного отдела пищевода, но с последующим мощным суммарным сокращением по окончании акта глотания (рис. 71).
Рис. 71. Тест с множественными быстрыми глотками, норма.
Эффективное результирующее сокращение тела пищевода в данном случае свидетельствует о перистальтическом «резерве».
Отсутствие перистальтического сокращения после серии глотков говорит о выраженном снижении перистальтического резерва, неэффективной моторике пищевода, нарушении пищеводного клиренса и является своеобразным предиктором развития дисфагии в случае проведения фундопликации по Ниссену (рис. 72)
Рис. 72. Тест с множественными быстрыми глотками при неэффективной моторике пищевода: отсутствие перистальтического сокращения тела пищевода после серии множественных глотков.
[12—16].
Тест с множественными быстрыми глотками позволяет выявить также нарушение угнетения перистальтики в момент совершения глотательных движений, что приводит к возникновению преждевременных спастических сокращений, сопровождающихся загрудинной болью (рис. 73)
Рис. 73. Тест с множественными быстрыми глотками: появление преждевременного сокращения.
[12—16].
Интерпретация результатов в зависимости от типа аппаратуры, катетера и положения пациента в момент исследования
Указанные в методических рекомендациях нормативы манометрических показателей (согласно Чикагской классификации) являются достаточно условными, поскольку базируются на исследованиях, проведенных на аппарате Sierra Scientific Instruments с использованием твердотельных катетеров диаметром 4,2 мм с 36 датчиками, расстояние между которыми не превышает 1 см. За норму принимались значения в диапазоне 5—95 процентилей [9, 20—22].
В Чикагской классификации подчеркивается, что результаты манометрии пищевода высокого разрешения в значительной мере зависят от используемого аппарата, типа катетера (водно-перфузионный, твердотельный), его диаметра, расстояния между датчиками давления на катетере, массы тела, возраста, расовой принадлежности пациента, положения пациента в момент исследования и многих других условий. Тем не менее нормативы Чикагской классификации разработаны без учета типа катетера и не отражают данные различия, а во многих работах [23—25], посвященных определению нормальных показателей манометрии пищевода, показатели DCI, IRP среди группы здоровых добровольцев оказываются значительно ниже, чем в действующей Чикагской классификации.
Кроме того, в исследованиях по сравнению манометрических показателей, полученных при исследовании твердотельным и водно-перфузионным катетером, было показано, что если значения DL, DCI практически не зависят от типа катетера, то результаты давления покоя НПС и ВПС значительно разнятся при использовании водно-перфузионного и твердотельного катетеров [26—29]. Это связано с разным диаметров катетеров, более высокой скоростью записи и циркулярным расположением датчиков давления у твердотельного катетера.
Несколько исследований с применением водно-перфузионных катетеров у больных с верифицированной ахалазией кардии показали, что значения IRP>15 мм рт.ст., принятые в Чикагской классификации за верхнюю границу нормы, не всегда адекватны для водно-перфузионных катетеров: у 50% больных с ахалазией IRP оказалось ниже 15 мм рт.ст. [28]. Исследования M. Zavala-Solares и соавт. [27], G. Capovilla и соавт. [24] также подтвердили, что результаты IRP, DCI, давления покоя ВПС, полученные при использовании водно-перфузионного катетера, как правило, значительно ниже аналогичных показателей, полученных при измерении твердотельным катетером.
Таким образом, при использовании нормативов, указанных в Чикагской классификации, необходимо с осторожностью (учитывая клинические данные и данные других методов исследования) интерпретировать результаты, полученные с помощью водно-перфузионных систем [17].
При анализе результатов манометрии пищевода важное значение имеет также положение пациента во время исследования. Имеющиеся на сегодняшний день нормативы манометрии пищевода разработаны для горизонтального положения. Это связано с тем, что в горизонтальном положении пациента нивелируется влияние силы тяжести на транзит болюса по пищеводу. Кроме того, применение водно-перфузионных катетров не позволяет использовать вертикальное положение пациента в связи с влиянием силы тяжести на давление жидкости в капиллярах катетера.
В то же время вертикальное положение в момент исследования является более физиологичным, а также позволяет минимализировать влияние передаточной пульсации аорты на результаты манометрии пищевода (особенно это важно при диагностике обструкции пищеводно-желудочного соединения) [30]. В нескольких работах было показано, что перевод пациента в вертикальное положение зачастую приводит к исключению полученного в горизонтальном положении диагноза «неэффективная моторика пищевода» [31, 32]. В ходе целого ряда исследований удалось выявить снижение показателей DCI, DL, IRP в вертикальном положении пациентов [32—34]. На сегодняшний день во многих центрах Европы и США, где для диагностики используются твердотельные катетеры, наиболее распространено «полусидячее» положение пациента (с приподнятой на 30° верхней частью туловища) в момент исследования [35].
В РФ согласно принятому 11 ноября 2017 г. соглашению «Первое российское соглашение по манометрии пищевода высокого разрешения» рекомендовано проводить исследование моторной функции пищевода в горизонтальном положении с приподнятым на 15° головным концом (для исключения поперхивания и аспирации при глотании) [37].
В сообществе ученых, занимающихся манометрией пищевода, также активно обсуждается вопрос использования различных типов болюса (твердого, вязкого) для повышения диагностической ценности исследования. В имеющихся на сегодняшний день работах [30, 33, 36] показано, что применение твердого болюса приводит к значимому повышению показателей DCI, IRP, что является своего рода провоцирующим фактором, позволяющим с большей вероятностью выявить нарушения моторики пищевода. Однако при применении твердого и вязкого болюса существуют сложности в стандартизации количества, объема болюса, применяемого продукта (хлеб, крекер, маршмеллоу). В связи с чем для внедрения данных методик в клиническую практику требуются дальнейшие исследования.
Первое российское соглашение по манометрии пищевода высокого разрешения
В Российской Федерации первое заседание рабочей группы и Экспертного совета, посвященное методологии и терминологии манометрии высокого разрешения, было проведено 11 ноября 2017 г. в рамках научно-практической конференции «Современные аспекты диагностики и лечения доброкачественных заболеваний пищевода 2017» (Санкт-Петербург). Результатами работы Экспертного совета стало принятие единой общепринятой русскоязычной терминологии, представленной в табл. 5—9
Таблица 5. Ключевые показатели манометрии пищевода высокого разрешения
Таблица 6. Классификация типов сокращений грудного отдела пищевода по интенсивности сокращения (contraction vigor) Гиперсокращение DCI≥8000 Hypercontractile 77,7
Таблица 7. Классификация типов сокращений грудного отдела пищевода по структуре сокращения (contraction pattern)
Таблица 8. Классификация типов интраболюсного давления в просвете пищевода (intrabolus pressure pattern)
Таблица 9. Классификация типов нарушений двигательной функции пищевода Примечание. В данной классификации термин «ахалазия» отражает тип нарушений двигательной функции пищевода, характеризующийся отсутствием расслабления НПС (от греч. — отсутствие расслабления), а не нозологическую форму «Ахалазия кардиальной части пищевода» (код K22.0 по МКБ).
[37].
При анализе интраболюсного давления в просвете пищевода [3] рекомендовано использовать термины, представленные в табл. 8.
Протокол заключения
По результатам работы второго заседания рабочей группы и Экспертного совета, посвященного разработке шаблона единого протокола заключения манометрии пищевода высокого разрешения (в рамках 44-й Научной сессии ЦНИИГ «Персонализированная медицина в эпоху стандартов» от 1 марта 2018 г.), был создан и утвержден проект протокола, рекомендованный к использованию в центрах Российской Федерации (табл. 10).
Таблица 10. Протокол заключения по исследованию.
Заключение
Манометрия высокого разрешения — современный метод функциональной диагностики, позволяющий объективизировать патогенетические механизмы дисфагии, загрудинной боли, изжоги, отрыжки, регургитации и многих других клинических симптомов при таких заболеваниях, как ГЭРБ, ахалазия кардии, функциональная отрыжка, системные заболевания соединительной ткани, грыжа ПОД и др. Используя данные об особенностях моторики пищевода и НПС у каждого конкретного больного, врачи (клиницист, гастроэнтеролог, эндоскопист, хирург) имеют сегодня возможность обоснованно назначить грамотное медикаментозное лечение, сформулировать показания и определить характер и объем оперативного лечения.
Кроме больших возможностей, которые дает нам данный метод, существуют и нерешенные вопросы: отсутствие четкого понимания и классификации нарушений двигательной функции ВПС, послеоперационных расстройств перистальтики, изменений моторики на фоне приема лекарственных препаратов. Не вполне ясна диагностическая ценность повышения или снижения давления покоя НПС, малых нарушений перистальтики, выявляемых у пациентов c ГЭРБ. Требуют стандартизации новые диагностические подходы с использованием провокационных тестов с глотками жидкости и твердой пищи.
Все вышесказанное обусловливает большие перспективы будущих научных и клинических исследований, открытий и свершений.
*Примечание. В данном случае термин «ахалазия» отражает форму нарушений двигательной функции пищевода, характеризующуюся отсутствием расслабления НПС, а не нозологическую форму «Ахалазия кардиальной части пищевода» (код K22.0 по МКБ).
Список литературы:
Список литературы:
Бордин Д.С., Валитова Э.Р. Методика проведения и клиническое значение манометрии пищевода. М.: Медпрактика-М; 2009.
Stef JJ, Dodds WJ, Hogan WJ, Linehan JH, Stewart ET. Intraluminal esophageal manometry: an analysis of variables affecting recording fidelity of peristaltic pressures. Gastroenterology. 1974;67(2):221-230.
Arndorfer RC, Stef JJ, Dodds WJ, Linehan JH, Hogan WJ. Improved infusion system for intraluminal esophageal manometry. Gastroenterology. 1977;73(1):23-27.
Dent J. A new technique for continuous sphincter pressure measurement. Gastroenterology. 1976;71(2):263-267.
Сторонова О.А., Трухманов А.С. Методика изучения двигательной функции пищевода. М.: Медпрактика-М; 2011.
Чернякевич С.А., Бабкова И.В., Орлов С.Ю. Функциональные методы исследования в хирургической гастроэнтерологии. М.: Медпрактика-М; 2002.
Clouse RE, Staiano A. Topography of the esophageal peristaltic pressure wave. Am J Physiol. 1991;4:677-684.
Clouse RE, Staiano A, Alrakawi A, Haroian L. Application of topographical methods to clinical esophageal manometry. Am J Gastroenterol. 2000;95(10):2720-2730.
Kahrilas PJ, Bredenoord AJ, Fox M, Gyawali CP, Roman S, Smout AJ, Pandolfino JE. International High Resolution Manometry Working Group. The Chicago Classification of esophageal motility disorders, v3.0. Neurogastroenterol Motil. 2015;27(2):160-174. https://doi.org/10.1111/nmo.12477
Savarino E, Bredenoord AJ, Fox M, Pandolfino JE, Roman S, Gyawali CP. International Working Group for Disorders of Gastrointestinal Motility and Function. Expert consensus document: Advances in the physiological assessment and diagnosis of GERD. Nat Rev Gastroenterol Hepatol. 2017;14(11):665-676. https://doi.org/10.1038/nrgastro.2017.130
Kahrilas PJ, Bredenoord AJ, Fox M, Gyawali CP, Roman S, Smout AJPM, Pandolfino JE. International Working Group for Disorders of Gastrointestinal Motility and Function. Expert consensus document: Advances in the management of oesophageal motility disorders in the era of high-resolution manometry: a focus on achalasia syndromes. Nat Rev Gastroenterol Hepatol. 2017;14(11):677-688. https://doi.org/10.1038/nrgastro.2017.132
Sweis R, Anggiansah A, Wong T, Brady G, Fox M. Assessment of esophageal dysfunction and symptoms during and after a standardized test meal: development and clinical validation of a new methodology utilizing high-resolution manometry. Neurogastroenterol Motil. 2014;26(2):215-228. https://doi.org/10.1111/nmo.12252
Ang D, Hollenstein M, Misselwitz B, Knowles K, Wright J, Tucker E, Sweis R, Fox M. Rapid Drink Challenge in high-resolution manometry: an adjunctive test for detection of esophageal motility disorders. Neurogastroenterol Motil. 2017;29(1). https://doi.org/10.1111/nmo.12902
Marin I, Serra J. Patterns of esophageal pressure responses to a rapid drink challenge test in patients with esophageal motility disorders. Neurogastroenterol Motil. 2016;28(4):543-553. https://doi.org/10.1111/nmo.12749
Elvevi A, Mauro A, Pugliese D, Bravi I, Tenca A, Consonni D, Conte D, Penagini R. Usefulness of low- and high-volume multiple rapid swallowing during high-resolution manometry. Dig Liver Dis. 2015;47(2):103-107. https://doi.org/10.1016/j.dld.2014.10.007
Gyawali CP, Roman S, Bredenoord AJ, Fox M, Keller J, Pandolfino JE, Sifrim D, Tatum R, Yadlapati R, Savarino E. International GERD Consensus Working Group. Classification of esophageal motor findings in gastro-esophageal reflux disease: Conclusions from an international consensus group. Neurogastroenterol Motil. 2017;29(12). https://doi.org/10.1111/nmo.13104
Herregods TV, Roman S, Kahrilas PJ, Smout AJ, Bredenoord AJ. Normative values in esophageal high-resolution manometry. Neurogastroenterol Motil. 2015;27(2):175-187. https://doi.org/10.1111/nmo.12500
Ponds FA, van Raath MI, Mohamed SMM, Smout AJPM, Bredenoord AJ. Diagnostic features of malignancy-associated pseudoachalasia. Aliment Pharmacol Ther. 2017;45(11):1449-1458. https://doi.org/10.1111/apt.14057
Salvador R, Voltarel G, Savarino E, Capovilla G, Pesenti E, Perazzolo A, Nicoletti L, Costantini A, Merigliano S, Costantini M. The natural history of achalasia: Evidence of a continuum — «The evolutive pattern theory». Dig Liver Dis. 2017. https://doi.org/10.1016/j.dld.2017.11.012
Ghosh SK, Pandolfino JE, Zhang Q, Jarosz A, Shah N, Kahrilas PJ. Quantifying esophageal peristalsis with high-resolution manometry: a study of 75 asymptomatic volunteers. Am J Physiol Gastrointest Liver Physiol. 2006;290(5):988-997.
Ghosh SK, Pandolfino JE, Rice J, Clarke JO, Kwiatek M, Kahrilas PJ. Impaired deglutitive EGJ relaxation in clinical esophageal manometry: a quantitative analysis of 400 patients and 75 controls. Am J Physiol Gastrointest Liver Physiol. 2007;293(4):878-885.
Pandolfino JE, Ghosh SK, Rice J, Clarke JO, Kwiatek MA, Kahrilas PJ. Classifying esophageal motility by pressure topography characteristics: a study of 400 patients and 75 controls. Am J Gastroenterol. 2008;103(1):27-37.
Weijenborg PW, Kessing BF, Smout AJ, Bredenoord AJ. Normal values for solid-state esophageal high-resolution manometry in a European population; an overview of all current metrics. Neurogastroenterol Motil. 2014;26(5):654-659. https://doi.org/10.1111/nmo.12314
Capovilla G, Savarino E, Costantini M, Nicoletti L, Zaninotto G, Salvador R. Inter-Rater and Inter-Device Agreement For The Diagnosis of Primary Esophageal Motility Disorders based on Chicago Classification Between Solid-State and Water-Perfused HRM System A Prospective, Randomized, Double Blind, Cross-over Study. Digestive Disease Week; 03/05/2014; Chicago. 2014.
Kuribayashi S, Iwakiri K, Kawada A, Kawami N, Hoshino S, Takenouchi N, Hosaka H, Shimoyama Y, Kawamura O, Yamada M, Kusano M. Variant parameter values-as defined by the Chicago Criteria-produced by ManoScan and a new system with Unisensor catheter. Neurogastroenterol Motil. 2015;27(2):188-194. https://doi.org/10.1111/nmo.12446
Kessing BF, Weijenborg PW, Smout AJ, Hillenius S, Bredenoord AJ. Water-perfused esophageal high-resolution manometry: normal values and validation. Am J Physiol Gastrointest Liver Physiol. 2014;306(6):491-495. https://doi.org/10.1152/ajpgi.00447.2013
Zavala-Solares MR, Saleme E, Vargas-Vorackova F, Valdovinos MA. Sa1191 high resolution esophageal pressure topography (HREPT) in asymptomatic volunteers. A comparative study between solid-state and water-perfused systems. Gastroenterology. 2012;142:239. https://doi.org/10.1016/s0016-5085(12)60898-1
Ortiz V, Poppele G, Alonso N, Castellano C, Garrigues V. Evaluation of esophagogastric junction relaxation by 4-second Integrated Relaxation Pressure in achalasia using High Resolution Manometry with water-perfused catheters. Neurogastroenterol Motil. 2014;26(11):1551-1556. https://doi.org/10.1111/nmo.12415
Bredenoord AJ, Hebbard GS. Technical aspects of clinical high-resolution manometry studies. Neurogastroenterol Motil. 2012;24:5-10. https://doi.org/10.1111/j.1365-2982.2011.01830.x
Bernhard A, Pohl D, Fried M, Castell DO, Tutuian R. Influence of bolus consistency and position on esophageal high-resolution manometry findings. Dig Dis Sci. 2008;53(5):1198-1205. https://doi.org/10.1007/s10620-007-0014-z
Xiao Y, Nicodème F, Kahrilas PJ, Roman S, Lin Z, Pandolfino JE. Optimizing the swallow protocol of clinical high-resolution esophageal manometry studies. Neurogastroenterol Motil. 2012;24(10):489-496. https://doi.org/10.1111/j.1365-2982.2012.01989.x
Roman S, Damon H, Pellissier PE, Mion F. Does body position modify the results of oesophageal high resolution manometry? Neurogastroenterol Motil. 2010;22(3):271-275. https://doi.org/10.1111/j.1365-2982.2009.01416.x
Sweis R, Anggiansah A, Wong T, Kaufman E, Obrecht S, Fox M. Normative values and inter-observer agreement for liquid and solid bolus swallows in upright and supine positions as assessed by esophageal high-resolution manometry. Neurogastroenterol Motil. 2011;23(6):509-198. https://doi.org/10.1111/j.1365-2982.2011.01682.x
Xiao Y, Read A, Nicodème F, Roman S, Kahrilas PJ, Pandolfino JE. The effect of a sitting vs supine posture on normative esophageal pressure topography metrics and Chicago Classification diagnosis of esophageal motility disorders. Neurogastroenterol Motil. 2012;24(10):509-516. https://doi.org/10.1111/j.1365-2982.2012.02001.x
Niebisch S, Wilshire CL, Peters JH. Systematic analysis of esophageal pressure topography in high-resolution manometry of 68 normal volunteers. Dis Esophagus. 2013;26(7):651-660. https://doi.org/10.1111/dote.12027
Shi Y, Xiao Y, Peng S, Lin J, Xiong L, Chen M. Normative data of high-resolution impedance manometry in the Chinese population. J Gastroenterol Hepatol. 2013;28(10):1611-1615. https://doi.org/10.1111/jgh.12285
Абдулхаков С.Р., Багненко С.Ф., Баркалова Е.В., Бордин Д.С., Bredenoord AJ, Бурганова Г.Р., Валитова Э.Р., Василевский Д.И., Гасанов А.М., Исаков В.А., Кайбышева В.О., Кляритская И.Л., Кривой В.В., Кучерявый Ю.А., Любченко М.Е., Морозов С.В., Никонов Е.Л., Овсепян М.А., Пасечников В.Д., Петриков С.С., Сажин А.В., Смирнов А.А., Федоров Е.Д., Хатьков И.Е., Шаповальянц С.Г. Резолюция Экспертного совета «Первое Российское соглашение по манометрии пищевода высокого разрешения». Доказательная гастроэнтерология. 2018;7(1):50-54. https://doi.org/10.17116/dokgastro20187150-54
Gor P, Li Y, Munigala S, et al. Interrogation of esophagogastric junction barrier function using the esophagogastric junction contractile integral: an observational cohort study. Dis Esophagus. 2016;29:820-828.
Jasper D, Freitas-Queiroz N, Hollenstein M, et al. Prolonged measurement improves the assessment of the barrier function of the esophago- gastric junction by high-resolution manometry. Neurogastroenterol Motil. 2017;29. https://doi.org/10.1111/nmo.12925
Pandolfino JE, et al. Achalasia: a new clinically relevant classification by high-resolution manometry. Gastroenterology. 2008;135:152601533.
Salvador R, et al. The preoperative manometric pattern predicts the outcome of surgical treatment for esophageal achalasia. J Gastrointest Surg. 2010;14:1635-1645.
Pratap N, et al. Achalasia cardia subtyping by high-resolution manometry predicts the therapeutic outcome of pneumatic balloon dilatation. J Neurogastroenterol Motil. 2011;17:48-53.
Rohof WO, et al. Outcomes of treatment for achalasia depend on manometric subtype. Gastroenterology. 2013;144:718-725.
Khan AK, et al. Is POEM the answer for management of spastic esophageal disorders? A systematic review and meta-analysis. Dig Dis Sci. 2017;62:35-44.
Porter RF, Kumar N, Drapekin JE, et al. Fragmented esophageal smooth muscle contraction segments on high resolution manometry: a marker of esophageal hypomotility. Neurogastroenterol Motil. 2012;24:763-768, e353.
Maradey-Romero C, Gabbard S, Fass R. Treatment of esophageal motility disorders based on the chicago classification. Curr Treat Options Gastroenterol. 2014;12(4):441-455. https://doi.org/10.1007/s11938-014-0032-9
Blonski W, Vela MF, Freeman J, Sharma N, Castell DO. The effect of oral buspirone, pyridostigmine, and bethanechol on esophageal function evaluated with combined multichannel esophageal impedance- manometry in healthy volunteers. J Clin Gastroenterol. 2009;43(3):253-2560.
Johnson DA, Drane WE, Curran J, et al. Metoclopramide response in patients with progres- sive systemic sclerosis. Effect on esophageal and gastric motility abnormalities. Arch Intern Med. 1987;147(9):1597-1601.
Chrysos E, Tzovaras G, Epanomeritakis E, et al. Erythromycin enhances oesophageal motility in pa- tients with gastro-oesophageal reflux. ANZ J Surg. 2001;71(2):98-102.
Chang CT, Shiau YC, Lin CC, Li TC, Lee CC, Kao CH. Improvement of esophageal and gastric motility after 2-week treatment of oral erythromycin in patients with non-insulin-dependent diabetes mellitus. J Diabetes Complicat. 2003;17(3):141-144.
Staiano A, Clouse RE. The effects of cisapride on the topography of oesophageal peristalsis. Aliment Pharmacol Ther. 1996;10(6):875-882.
Fox M, Menne D, Stutz B, Fried M, Schwizer W. The effects of tegaserod on oesophageal function and bolus transport in healthy volunteers: studies using concurrent high-resolution manometry and videofluoroscopy. Aliment Pharmacol Ther. 2006;24(7):1017-1027.
Scarpellini E, Vos R, Blondeau K, et al. The effects of itopride on oesophageal motility and lower oesophageal sphincter function in man. Aliment Pharmacol Ther. 2011;33:99-105.
Kessing BF, Smout AJ, Bennink RJ, et al. Prucalopride decreases esophageal acid exposure and accelerates gastric emptying in healthy subjects. Neurogastroenterol Motil. 2014;26:1079-1086.
Zerbib F, Roman S. Current Therapeutic Options for Esophageal Motor Disorders as Defined by the Chicago Classification. J Clin Gastroenterol. 2015;49(6):451-460. Review. https://doi.org/10.1097/MCG.0000000000000317
Статьи по теме
Рекомендуемые статьи
При эндоскопическом исследовании в случае бронхоэктазов в стадии ремиссии выявляется
частично диффузный бронхит I степени воспаления
Активируйте PUSH уведомления в браузер
Отключите PUSH уведомления в браузер
Содержание
Интернет магазин
Популярное
- О нас
- Правовые вопросы
- Политика
обработки персональных
данных EndoExpert.ru - Связаться с нами
- Стать партнером
© 2016-2022 EndoExpert.ru

Вы находитесь в разделе предназначенном только для специалистов (раздел для пациентов по ссылке). Пожалуйста, внимательно прочитайте полные условия использования и подтвердите, что Вы являетесь медицинским или фармацевтическим работником или студентом медицинского образовательного учреждения и подтверждаете своё понимание и согласие с тем, что применение рецептурных препаратов, обращение за той или иной медицинской услугой, равно как и ее выполнение, использование медицинских изделий, выбор метода профилактики, диагностики, лечения, медицинской реабилитации, равно как и их применение, возможны только после предварительной консультации со специалистом. Мы используем файлы cookie, чтобы предложить Вам лучший опыт взаимодействия. Файлы cookie позволяют адаптировать веб-сайты к вашим интересам и предпочтениям.
Я прочитал и настоящим принимаю вышеизложенное, хочу продолжить ознакомление с размещенной на данном сайте информацией для специалистов.














.jpg)





.png)



.jpg)

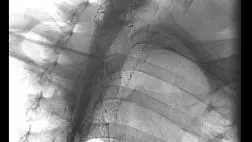
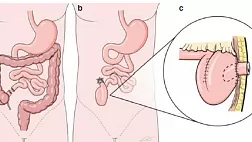













Комментарии