- Компании
- Takeda. О компании, буклеты, каталоги, контакты
- Olympus. О компании, буклеты, каталоги, контакты
- Boston Scientific. О компании, буклеты, каталоги, контакты
- Pentax. О компании, буклеты, каталоги, контакты
- Fujifilm & R-Farm. О компании, буклеты, каталоги, контакты
- Erbe. О компании, буклеты, каталоги, контакты
- Еще каталоги
- Мероприятия
- Информация
- Обучение
- Классификации
- Атлас
- Quiz
- Разделы
- Пациенту
QR-код этой страницы
Для продолжения изучения на мобильном устройстве ПРОСКАНИРУЙТЕ QR-код с помощью спец. программы или фотокамеры мобильного устройства
Статьи: Колопроктология. Клинические рекомендации 2015 под ред. Ю. А. Шелыгина
Анонс:
Настоящее издание - клинические рекомендации по колопроктологии - посвящен оклинической картине, диагностике и лечению наиболее распространенных заболеваний толстой кишки, анального канала и промежности. Книга подготовлена ведущими спе-циалистами Общероссийской общественной организации "Ассоциация колопроктоло-гов России", Российской гастроэнтерологической ассоциации, Российского обществахирургов и Ассоциации онкологов России. Рассмотрены алгоритмы действий врачапри диагностике, лечении, профилактике заболеваний и реабилитации пациентов,которые позволяют врачу быстро принимать обоснованные клинические решения.
Клинические рекомендации предназначены для практикующих врачей (колопроктологов, гастроэнтерологов, хирургов, онкологов, терапевтов, врачей смежных специальностей), а также ординаторов и студентов старших курсов медицинских вузов.

Полный текст статьи:
УДК 616.34/.35-07-08 03-КЛР-1484
ББК 54.13я73-1 К49
К49 Клинические рекомендации. Колопроктология / под ред. Ю. А. Шелыгина. — М.: ГЭОТАР-Медиа, 2015. — 528 с.: ил.
ISBN 978-5-9704-3423-9
Настоящее издание — клинические рекомендации по колопроктологии — посвящено клинической картине, диагностике и лечению наиболее распространенных заболеваний толстой кишки, анального канала и промежности. Книга подготовлена ведущими специалистами ООО «Ассоциация колопроктологов России», Российской гастроэнтерологической ассоциации, Российского общества хирургов и Ассоциации онкологов России. Рассмотрены алгоритмы действий врача при диагностике, лечении, профилактике заболеваний и реабилитации пациентов, которые позволяют врачу быстро принимать обоснованные клинические решения.
Клинические рекомендации предназначены для практикующих врачей (колопроктологов, гастроэнтерологов, хирургов, онкологов, терапевтов, врачей смежных специальностей), а также ординаторов и студентов старших курсов медицинских вузов.
УДК 616.34/.35-07-08 ББК 54.13я73-1
Права на данное издание принадлежат ООО Издательская группа «ГЭОТАР-Медиа». Воспроизведение и распространение в каком бы то ни было виде части или целого издания не могут быть осуществлены без письменного разрешения ООО Издательская группа
«ГЭОТАР-Медиа».
© Коллектив авторов, 2015
© ООО Издательская группа «ГЭОТАР-Медиа, 2015
© ООО Издательская группа «ГЭОТАР-Медиа,
ISBN 978-5-9704-3423-9 оформление, 2015
Оглавление
Предисловие................................................................................................................... 4
Участники издания...................................................................................................... 5
Список сокращений................................................................................................ 11
Анальная трещина..................................................................................................... 12
Острый и хронический геморрой......................................................................... 30
Эпителиальный копчиковый ход......................................................................... 53
Острый парапроктит................................................................................................. 67
Хронический парапроктит (свищ заднего прохода,
свищ прямой кишки)............................................................................................... 82
Ректовагинальные свищи..................................................................................... 108
Пресакральные кисты............................................................................................ 126
Ректоцеле.................................................................................................................... 147
Выпадение прямой кишки, внутренняя ректальная инвагинация
и солитарная язва прямой кишки.................................................................... 168
Недостаточность анального сфинктера........................................................... 190
Остроконечные кондиломы перианальной области и анального
канала........................................................................................................................... 216
Анальные полипы.................................................................................................... 236
Дивертикулярная болезнь ободочной кишки................................................ 248
Болезнь Гиршпрунга.............................................................................................. 277
Долихоколон............................................................................................................. 294
Идиопатический мегаколон................................................................................. 311
Ангиодисплазия кишечника................................................................................ 330
Семейный аденоматоз толстой кишки............................................................. 346
Болезнь Крона......................................................................................................... 363
Язвенный колит........................................................................................................ 395
Синдром раздраженного кишечника................................................................ 430
Ведение взрослых пациентов с кишечной стомой...................................... 449
Острая кишечная непроходимость опухолевой этиологии...................... 491
Критерии оценки качества оказания медицинской помощи по профилю гастроэнтерология и колопроктология
в стационарных и амбулаторных условиях .................................................. 519
Предметный указатель........................................................................................... 523
Предисловие
Уважаемые коллеги!
Представляем вам национальные клинические рекомендации по колопроктологии, разработанные ведущими специалистами ООО «Ассоциация колопроктологов России», Российского общества гастроэнтерологов, Российского общества хирургов и Ассоциации онкологов России. Рекомендации охватывают наиболее распространенные заболевания толстой кишки, анального канала и промежности и предназначены врачам-колопроктологам, гастроэнтерологам, хирургам и онкологам, работающим как в поликлиниках, так и в стационарах.
Клинические рекомендации по колопроктологии — это систематически разрабатываемые и обновляемые документы, описывающие действия врача по диагностике, лечению и профилактике заболеваний толстой кишки и помогающие ему принимать правильные клинические решения. Цель создания клинических рекомендаций по колопроктологии — необходимость внедрения во врачебную практику наиболее эффективных и безопасных медицинских технологий (в том числе лекарственных средств), отказ от необоснованных вмешательств, повышение качества медицинской помощи. Данные рекомендации могут служить методологической основой для создания других документов и применяться для контроля качества медицинской помощи, а также в системе непрерывного медицинского образования. В предлагаемых рекомендациях отражены не только рутинные методы диагностики и лечения, используемые врачами в повседневной работе, но и новые, перспективные и динамически развивающиеся направления, способные улучшить качество оказания медицинской помощи больным с колопроктологическими заболеваниями.
В основу предлагаемого издания положен многолетний обобщенный опыт ведущих специалистов в области колопроктологии, хирургии, гастроэнтерологии и онкологии, которые приняли участие в его подготовке в качестве авторов-составителей, научных редакторов, рецензентов. К написанию рекомендаций привлекались наиболее авторитетные эксперты, занимающиеся как врачебной, так и научно-исследовательской работой. Перед составлением клинических рекомендаций авторы проводили поиск и анализ компьютеризированных источников информации: национальных клинических рекомендаций, подготовленных профессиональными сообществами многих стран Европы и Америки, систематических обзоров литературы, клинических испытаний и др.
Надеемся, что разработанные клинические рекомендации окажутся полезными в повседневной работе и помогут в оказании высококвалифицированной помощи пациентам с заболеваниями толстой кишки.
Приглашаем всех заинтересованных читателей к сотрудничеству.
Будем благодарны за все критические замечания и пожелания.
Главный редактор профессор Ю.А. Шелыгин
Участники издания
Главный редактор
Шелыгин Юрий Анатольевич — д-р мед. наук, проф., директор ФГБУ
«Государственный научный центр колопроктологии им. А.Н. Рыжих» Минздрава России (Москва)
Ответственный редактор
Фролов Сергей Алексеевич — д-р мед. наук, заместитель директора по научной работе ФГБУ «Государственный научный центр колопроктологии им. А.Н. Рыжих» Минздрава России (Москва)
Авторы
В разработке клинических рекомендаций приняли участие члены Ассоциации колопроктологов России, Российской гастроэнтерологической ассоциации, Ассоциации онкологов России, Российского общества хирургов.
Абдулганиева Диана Ильдаровна — д-р мед. наук, проф., зав. кафедрой госпитальной терапии с курсом эндокринологии ГБОУ ВПО «Казанский государственный медицинский университет» Минздрава России (Казань)
Алексеенко Сергей Алексеевич — д-р мед. наук, проф., зав. кафедрой госпитальной терапии ГБОУ ВПО «Дальневосточный государственный медицинский университет» Минздрава России (Хабаровск)
Ачкасов Евгений Евгеньевич — д-р мед. наук, проф., зав. кафедрой лечебной физкультуры и спортивной медицины, профессор кафедры госпитальной хирургии № 1 лечебного факультета ГБОУ ВПО «Первый Московский государственный медицинский университет им. И.М. Сеченова» Минздрава России (Москва)
Ачкасов Сергей Иванович — д-р мед. наук, профессор, руководитель отдела онкологии и хирургии ободочной кишки ФГБУ «Государственный научный центр колопроктологии им. А.Н. Рыжих» Минздрава России (Москва)
Багненко Сергей Федорович — д-р мед. наук, проф., акад. РАН, ректор ГБОУ ВПО «Первый Санкт-Петербургский государственный медицинский университет им. акад. И.П. Павлова» Минздрава России (Санкт-Петербург)
Барановский Андрей Юрьевич — д-р мед. наук, проф., зав. кафедрой гастроэнтерологии и диетологии ГБОУ ВПО «Северо-Западный государственный медицинский университет им. И.И. Мечникова» Минздрава России (Санкт-Петербург)
Беляев Алексей Михайлович — д-р мед. наук, проф., зав. кафедрой онкологии ГБОУ ВПО «Северо-Западный государственный медицинский университет им. И.И. Мечникова» Минздрава России, директор ФГБУ
«Санкт-Петербургский научно-исследовательский институт онкологии им. проф. Н.Н. Петрова» Минздрава России, (Санкт-Петербург)
Белоусова Елена Александровна — д-р мед. наук, проф., руководитель отделения гастроэнтерологии и гепатологии ГБУЗ МО «Московский областной научно-исследовательский клинический институт им. М.Ф. Владимирского» (Москва)
Бердов Борис Александрович — д-р мед. наук, проф., заместитель директора ФГБУ «Медицинский радиологический научный центр им. А.Ф. Цыба» РАМН (Обнинск)
Благодарный Леонид Абрамович — д-р мед. наук, проф. кафедры колопроктологии ГБОУ ДПО «Российская медицинская академия последипломного образования» Минздрава России (Москва)
Болихов Кирилл Валерьевич — канд. мед. наук, старший научный сотрудник отдела онкологии и хирургии ободочной кишки ФГБУ «Государственный научный центр колопроктологии им. А.Н. Рыжих» Минздрава России (Москва)
Васильев Сергей Васильевич — д-р мед. наук, проф., зав. кафедрой хирургических болезней с курсом колопроктологии ГБОУ ВПО «Первый Санкт-Петербургский государственный медицинский университет им. акад. И.П. Павлова» Минздрава России, главный колопроктолог Санкт-Петербурга (Санкт-Петербург)
Веселов Алексей Викторович — канд. мед. наук, руководитель отдела по организационной, образовательной работе и развитию колопроктологической службы ФГБУ «Государственный научный центр колопроктологии им. А.Н. Рыжих» Минздрава России (Москва)
Веселов Виктор Владимирович — д-р мед. наук, проф., руководитель отдела эндоскопической диагностики и хирургии ФГБУ «Государственный научный центр колопроктологии им. А.Н. Рыжих» Минздрава России (Москва)
Вышегородцев Дмитрий Вячеславович — канд. мед. наук, старший научный сотрудник отдела общей колопроктологии с группой изучения семейного аденоматоза ФГБУ «Государственный научный центр колопроктологии им. А.Н. Рыжих» Минздрава России (Москва)
Головенко Олег Владимирович — д-р мед. наук, проф., зав. гастроэнтерологическим отделением ФГБУ «Государственный научный центр колопроктологии им. А.Н. Рыжих» Минздрава России (Москва)
Григорьев Евгений Георгиевич — д-р мед. наук, проф., чл.-кор. РАМН, зав. кафедрой госпитальной хирургии ГБОУ ВПО «Иркутский государственный медицинский университет» Минздрава России, директор Института хирургии и Научного центра реконструктивной и восстановительной хирургии ФГБУ «Восточно-Сибирский научный центр экологии человека» Сибирского отделения РАМН (Иркутск)
Давыдов Михаил Иванович — д-р мед. наук, проф., акад. РАН, директор ФГБУ «Российский онкологический научный центр им. Н.Н. Блохи-
на» РАМН, лауреат Государственной премии РФ, заслуженный деятель науки РФ (Москва)
Зароднюк Ирина Владимировна – д-р мед. наук, ведущий научный сотрудник отдела рентгенодиагностики, компьютерной и магнитно-резонансной томографии ФГБУ «Государственный научный центр колопроктологии им. А.Н. Рыжих» Минздрава России (Москва)
Затевахин Игорь Иванович — д-р мед. наук, проф., акад. РАН, зав. кафедрой хирургических болезней педиатрического факультета ГБОУ ВПО
«Российский национальный исследовательский медицинский университет им. Н.И. Пирогова» Минздрава России (Москва)
Захаренко Александр Анатольевич — д-р мед. наук, зав. онкологическим отделением Клиники факультетской хирургии ГБОУ ВПО «Первый Санкт-Петербургский государственный медицинский университет им. акад. И.П. Павлова» Минздрава России (Санкт-Петербург)
Ивашкин Владимир Трофимович – д-р мед. наук, проф., акад. РАН, зав. кафедрой пропедевтики внутренних болезней лечебного факультета ГБОУ ВПО «Первый Московский государственный медицинский университет им. И.М. Сеченова» Минздрава России, директор Клиники им. В.Х. Василенко (Москва)
Калашникова Ирина Анатольевна – зав. отделением реабилитации ФГБУ «Государственный научный центр колопроктологии им. А.Н. Рыжих» Минздрава России (Москва)
Карпухин Олег Юрьевич — д-р мед. наук, проф. кафедры хирургии № 1 ГБОУ ВПО «Казанский государственный медицинский университет» Минздрава России (Казань)
Кашников Владимир Николаевич – канд. мед. наук, заместитель директора по лечебной работе ФГБУ «Государственный научный центр колопроктологии им. А.Н. Рыжих» Минздрава России (Москва)
Костарев Иван Васильевич — канд. мед. наук, старший научный сотрудник отдела общей и реконструктивной колопроктологии ФГБУ
«Государственный научный центр колопроктологии им. А.Н. Рыжих» Минздрава России (Москва)
Костенко Николай Владимирович — д-р мед. наук, проф., проректор по лечебной работе и последипломному образованию, доцент кафедры общей хирургии ГБОУ ВПО «Астраханский государственный медицинский университет» Минздрава России (Астрахань)
Кубышкин Валерий Алексеевич — д-р мед. наук, проф., акад. РАН, директор ФГБУ «Институт хирургии им. А.В. Вишневского» Минздрава России, главный внештатный хирург Минздрава России (Москва)
Кузьминов Александр Михайлович — д-р мед. наук, проф., руководитель отдела общей колопроктологии с группой изучения семейного аденоматоза ФГБУ «Государственный научный центр колопроктологии им. А.Н. Рыжих» Минздрава России (Москва)
Куликовский Владимир Федорович — д-р мед. наук, проф., зав. кафедрой хирургических болезней Института последипломного медицинского образования, зав. кафедрой хирургии медицинского факультета ФГАОУ ВПО «Белгородский государственный национальный исследовательский университет» Минобрнауки России (Белгород)
Мансуров Юрий Владимирович — канд. мед. наук, доцент кафедры хирургических болезней факультета повышения квалификации и профессиональной переподготовки специалистов ГБОУ ВПО «Уральский государственный медицинский университет» Минздрава России, зав. хирургическим отделением № 2 ГБУЗ СО «Свердловская областная клиническая больница № 1» (Екатеринбург)
Москалёв Алексей Игоревич — канд. мед. наук, научный сотрудник отделения онкологии и хирургии ободочной кишки ФГБУ «Государственный научный центр колопроктологии им. А.Н. Рыжих» Минздрава России (Москва)
Муравьёв Александр Васильевич — д-р мед. наук, проф. кафедры общей хирургии ГБОУ ВПО «Ставропольский государственный медицинский университет» Минздрава России, зав. отделением колопроктологии ГБУЗ СК «Городская клиническая больница № 2» (Ставрополь)
Невольских Алексей Алексеевич – д-р мед.наук, заместитель главного врача ФГБУ «Медицинский радиологический научный центр им. А.Ф. Цыба» РАМН (Обнинск)
Низов Алексей Александрович — д-р мед. наук, проф., зав. кафедрой внутренних болезней и поликлинической терапии ГБОУ ВПО «Рязанский государственный медицинский университет им. акад. И.П. Павлова» Минздрава России (Рязань)
Олейник Наталья Витальевна — д-р мед. наук, доцент, проф. кафедры госпитальной хирургии ФГАОУ ВПО «Белгородский государственный национальный исследовательский университет» Минобрнауки России, врач-колопроктолог ОГБУЗ «Белгородская областная клиническая больница Святителя Иоасафа» (Белгород)
Орлова Лариса Петровна — д-р мед. наук, проф., руководитель отдела ультразвуковой диагностики ФГБУ «Государственный научный центр колопроктологии им. А.Н. Рыжих» Минздрава России (Москва)
Осипенко Марина Федоровна — д-р мед. наук, проф., зав. кафедрой пропедевтики внутренних болезней ГБОУ ВПО «Новосибирский государственный медицинский университет» Минздрава России (Новосибирск)
Павленко Владимир Васильевич — д-р мед. наук, проф., зав. кафедрой пропедевтики внутренних болезней ГБОУ ВПО «Ставропольский государственный медицинский университет» Минздрава России (Ставрополь)
Полуэктова Елена Александровна — канд. мед. наук, ведущий научный сотрудник НОКЦ инновационной терапии ГБОУ ВПО «Первый Московский государственный медицинский университет им. И.М. Сеченова» Минздрава России (Москва)
Прудков Михаил Иосифович — д-р мед. наук, проф., зав. кафедрой хирургических болезней факультета повышения квалификации и профессиональной переподготовки специалистов ГБОУВПО «Уральский государственный медицинский университет» Минздрава России (Екатеринбург)
Пугаев Андрей Владимирович – д-р мед. наук, проф., профессор кафедры госпитальной хирургии № 1 лечебного факультета ГБОУ ВПО
«Первый Московский государственный медицинский университет им. И.М. Сеченова» Минздрава России (Москва)
Расулов Арсен Османович — д-р мед. наук, зав. отделением онкопроктологии ФГБУ «Российский онкологический научный центр им. Н.Н. Блохина» РАМН (Москва)
Родоман Григорий Владимирович — д-р мед. наук, проф., главный врач ГБУЗ «Городская клиническая больница № 24» ДЗМ (Москва)
Румянцев Виталий Григорьевич — д-р мед. наук, проф., главный врач ООО «Он-клиник-Элит (БИО)» (Москва)
Рыбаков Евгений Геннадиевич — д-р мед. наук, руководитель отдела онкопроктологии ФГБУ «Государственный научный центр колопроктологии им. А.Н. Рыжих» Минздрава России (Москва)
Стойко Юрий Михайлович — д-р мед. наук, проф., главный хирург, руководитель Клиники хирургии ФГБУ «Национальный медико-хирургический центр им. Н.И. Пирогова» Минздрава России, главный хирург Минздрава России в Центральном федеральном округе (Москва)
Сушков Олег Иванович — канд. мед. наук, старший научный сотрудник отдела онкологии и хирургии ободочной кишки ФГБУ «Государственный научный центр колопроктологии им. А.Н. Рыжих» Минздрава России (Москва)
Тимербулатов Виль Мамилович — д-р мед. наук, проф., акад. АН РБ, чл.-кор. РАМН, руководитель Республиканского эндоскопического центра (Уфа)
Титов Александр Юрьевич – д-р мед. наук, проф., ученый секретарь ФГБУ «Государственный научный центр колопроктологии им. А.Н. Рыжих» Минздрава России (Москва)
Тихонов Андрей Александрович — д-р мед. наук, руководитель отдела рентгенодиагностики, компьютерной и магнитно-резонансной томографии ФГБУ «Государственный научный центр колопроктологии им. А.Н. Рыжих» Минздрава России (Москва)
Ткачёв Александр Васильевич — д-р мед. наук, проф., зав. кафедрой пропедевтики внутренних болезней ГБОУ ВПО «Ростовский государственный медицинский университет» Минздрава России (Ростов-на-Дону)
Ткаченко Евгений Иванович — д-р мед. наук, проф., зав. кафедрой пропедевтики внутренних болезней ГБОУ ВПО «Северо-Западный государственный медицинский университет им. И.И. Мечникова» Минздрава России (Санкт-Петербург)
Тотиков Валерий Зелимханович — д-р мед. наук, проф., зав. кафедрой хирургических болезней № 2 ГБОУ ВПО «Северо-Осетинская государственная медицинская академия» Минздрава России (Владикавказ)
Фоменко Оксана Юрьевна — канд. мед. наук, руководитель лаборатории клинической патофизиологии ФГБУ «Государственный научный центр колопроктологии им. А.Н. Рыжих» Минздрава России (Москва)
Фролов Сергей Алексеевич — д-р мед. наук, заместитель директора по научной работе ФГБУ «Государственный научный центр колопроктологии им. А.Н. Рыжих» Минздрава России (Москва)
Халиф Игорь Львович — д-р мед. наук, проф., руководитель отдела по изучению воспалительных и функциональных заболеваний кишечника ФГБУ «Государственный научный центр колопроктологии им. А.Н. Рыжих» Минздрава России (Москва)
Хубезов Дмитрий Анатольевич — д-р мед. наук, проф., зав. отделением колопроктологии ГБУЗ РО «Областная клиническая больница» (Рязань) Черкасов Михаил Федорович — д-р мед. наук, проф., зав. кафедрой хирургических болезней № 4 ГБОУ ВПО «Ростовский государственный медицинский университет» Минздрава России (Ростов-на-Дону)
Шелыгин Юрий Анатольевич — д-р мед. наук, проф., директор ФГБУ
«Государственный научный центр колопроктологии им. А.Н. Рыжих» Минздрава России (Москва)
Шифрин Олег Самойлович — д-р мед. наук, проф., зав. отделением хронических заболеваний кишечника и поджелудочной железы ГБОУ ВПО «Первый Московский государственный медицинский университет им. И.М. Сеченова» Минздрава России (Москва)
Эктов Владимир Николаевич — д-р мед. наук, проф., зав. кафедрой хирургии № 2 факультета усовершенствования врачей ГБОУ ВПО «Воронежская государственная медицинская академия им. Н.Н. Бурденко» Минздрава России (Воронеж)
Эфрон Александр Григорьевич — врач-хирург хирургического отделения № 1 (колопроктология) ОГБУЗ «Клиническая больница скорой медицинской помощи» (Смоленск)
Яновой Валерий Владимирович — д-р мед. наук, проф., зав. кафедрой госпитальной хирургии с курсом детской хирургии ГБОУ ВПО
«Амурская государственная медицинская академия» Минздрава России (Благовещенск)
Список сокращений
5- АСК — 5-аминосалициловая кислота 6-МП — 6-меркаптопурин
БОС — биологическая обратная связь
ВЗК — воспалительные заболевания кишечника ВПЧ — вирус папилломы человека
ГКС — глюкокортикостероиды ДИ — доверительный интервал
ЖКТ — желудочно-кишечный тракт
ЗАПК — запирательный аппарат прямой кишки ИАРА — илеоанальный резервуарный анастомоз КТ — компьютерная томография
МКБ-10 — Международная классификация болезней 10-го пересмотра МПО — максимально переносимый объем
МРТ — магнитно-резонансная томография
РКИ — рандомизированное клиническое исследование САТК — семейный аденоматоз толстой кишки
СР — степени рекомендации
СРК — синдром раздраженного кишечника УЗИ — ультразвуковое исследование
УД — уровень доказательности
ЭКХ — эпителиальный копчиковый ход
АНАЛЬНАЯ ТРЕЩИНА
Введение
Анальная трещина — одно из самых распространенных колопроктологических заболеваний. Удельный вес трещины заднего прохода среди болезней толстой кишки составляет 11–15%, а заболеваемость колеблется от 20 до 23 на 1000 человек взрослого населения (уровень доказательности (УД) 5, степень рекомендации (СР) D [1]).
Настоящие рекомендации по диагностике и лечению анальной трещины являются руководством для практических врачей, осуществляющих ведение и лечение данных пациентов. Рекомендации подлежат регулярному пересмотру в соответствии с новыми данными научных исследований в этой области.
Эти рекомендации составлены на основании анализа литературы из базы данных РubМеd, MEDLINE, Cochraine Collaboration, the Standards Practice Task Force of the American Society of Colon and Rectal Surgeon.
Для отдельных положений рекомендаций приведены уровни доказательности согласно общепринятой классификации Оксфордского центра доказательной медицины (табл. 1.1) [2, 3].
Таблица 1.1. Уровни доказательности и степени рекомендаций на основании руководства Оксфордского центра доказательной медицины
|
Уровень |
Исследования методов диагностики |
Исследования методов лечения |
|
1а |
Систематический обзор гомогенных диагностических исследований 1-го уровня |
Систематический обзор гомогенных РКИ |
|
1b |
Валидизирующее когортное исследование с качественным «золотым стандартом» |
Отдельное РКИ (с узким доверительным интервалом) |
|
1с |
Специфичность или чувствительность столь высокие, что положительный или отрицательный результат позволяет исключить/установить диагноз |
Исследование «Всё или ничего» |
|
2а |
Систематический обзор гомогенных диагностических исследований >2-го уровня |
Систематический обзор (гомогенных) когортных исследований |
Табл. 1.1. Окончание
|
Уровень |
Исследования методов диагностики |
Исследования методов лечения |
|
2b |
Разведочное когортное исследование с качественным «золотым стандартом» |
Отдельное когортное исследование (включая РКИ низкого качества; т.е. с <80% пациентов, прошедших контрольное наблюдение) |
|
2с |
Нет |
Исследование «исходов»; экологические исследования |
|
3а |
Систематический обзор гомогенных исследований уровня 3b и выше |
Систематический обзор гомогенных исследований «случай–контроль» |
|
3b |
Исследование с непоследовательным набором или без проведения исследования ««золотого стандарта»» у всех испытуемых |
Отдельное исследование «случай– контроль» |
|
4 |
Исследование «случай–контроль» или исследование с некачественным или зависимым «золотым стандартом» |
Серия случаев (и когортные исследования или исследования «случай–контроль» низкого качества) |
|
5 |
Мнение экспертов без тщательной критической оценки или основанное на физиологии, лабораторные исследования на животных или разработка «первых принципов» |
Мнение экспертов без тщательной критической оценки, лабораторные исследования на животных или разработка «первых принципов» |
|
Степень рекомендации | ||
|
A |
Согласующиеся между собой исследования 1-го уровня | |
|
B |
Согласующиеся между собой исследования 2-го или 3-го уровня или экстраполяция на основе исследований 1-го уровня | |
|
C |
Исследования 4-го уровня или экстраполяция на основе уровня 2 или 3 | |
|
D |
Доказательства 4-го уровня или затруднительные для обобщения или некачественные исследования любого уровня | |
ВАЛИДИЗАЦИЯ РЕКОМЕНДАЦИЙ
Настоящие рекомендации составлены общероссийской общественной организацией «Ассоциация колопроктологов России» и в предварительной версии были рецензированы независимыми экспертами, которых попросили прокомментировать прежде всего, насколько интерпретация доказательств, лежащих в основе рекомендаций, доступна для понимания. Получены комментарии со стороны врачей амбулаторного звена. Полученные комментарии тщательно систематизировались и обсуждались на совещаниях экспертной группы.
Последние изменения в настоящих рекомендациях были представлены для дискуссии на заседании профильной комиссии «Колопроктология» Экспертного совета Минздрава России 12 сентября 2013 г. Проект рекомендаций был повторно рецензирован независимыми экспертами и врачами амбулаторного звена. Для окончательной редакции и контроля качества рекомендации были повторно проанализированы членами экспертной группы, которые пришли к заключению, что все замечания и комментарии приняты во внимание, риск систематических ошибок при разработке рекомендаций сведен к минимуму.
ОБЛАСТЬ ПРИМЕНЕНИЯ РЕКОМЕНДАЦИЙ
Данные клинические рекомендации применимы при осуществлении медицинской деятельности в рамках Порядка оказания медицинской помощи взрослому населению с заболеваниями толстой кишки, анального канала и промежности колопроктологического профиля.
Определение
Анальная трещина — спонтанно возникающий линейный или элипсовидный дефект (язва) слизистой оболочки анального канала (УД 5, СР D [4]). Ведущий патогенетический механизм в развитии анальной трещины — спазм внутреннего сфинктера, который приводит к нарушению кровоснабжения анодермы и появлению длительно незаживающего язвенного дефекта анодермы (УД 5, СР D [5–7]).
Код по Международной классификации болезней 10-го пересмотра [8]
K60.0 Острая трещина заднего прохода K60.1 Хроническая трещина заднего прохода
K60.2 Трещина заднего прохода неуточненная
Классификация (уровень доказательности 5, степень рекомендации D [4])
По характеру течения выделяют:
n острую анальную трещину;
n хроническую анальную трещину.
По локализации дефекта выделяют:
n заднюю анальную трещину;
n переднюю анальную трещину;
n боковую анальную трещину.
По наличию спазма сфинктера выделяют:
n со спазмом;
n без спазма.
Формулировка диагноза
При формулировании диагноза следует отразить характер течения заболевания с указанием локализации поражения и наличия спазма сфинктера.
n Хроническая передняя анальная трещина со спазмом сфинктера.
n Хроническая задняя анальная трещина без спазма сфинктера.
n Острая задняя анальная трещина.
Профилактика
Ряд исследований свидетельствует, что средствами профилактики анальной трещины могут служить диета (ограничение острой и жирной пищи) и употребление пищевых волокон (УД 1a, СР A [9, 10]).
Диагностика
КЛИНИЧЕСКИЕ ДИАГНОСТИЧЕСКИЕ КРИТЕРИИ
К основным клиническим симптомам анальной трещины относятся характерные жалобы, данные анамнеза и клинико-инструментального обследования.
Жалобы. Для анальной трещины характерны жалобы на боли в области заднего прохода во время и после дефекации, выделения крови во время дефекации в виде помарок на стуле и туалетной бумаге (УД 4, СР С [11]). Сбор анамнеза. Выявляются этиологические факторы возникновения заболевания: недостаточное употребление пищевых волокон, жирная, богатая углеводами пища, острая пища, запор или диарея, роды, занятия определенными видами спорта (велосипедный спорт) (УД 1b, СР А [9]). Осмотр врачом-колопроктологом. Пациента осматривают на гинекологическом кресле в положении на спине с максимально приведенными к животу ногами или в коленно-локтевом положении. У соматически тяжелых больных осмотр производят в положении на боку. При наружном осмотре области промежности и заднего прохода обращают внимание на форму ануса, его зияние, наличие рубцовых изменений и деформаций, состояние кожных покровов.
Определяют наличие сторожевого бугорка. Чтобы визуализировать дистальный край дефекта анодермы, оценить его расположение, размеры и форму, разводят края заднего прохода.
Характерно наличие линейного или эллипсовидного дефекта (эрозии или язвы) с ровными краями, не распространяющегося за анатомические границы анодермы (УД 4, СР С [10]).
Пальцевое исследование. Определяют наличие дефектов анодермы, а также тоническое состояние анального сфинктера и силу волевых сокращений. Выявляют характерное для анальной трещины повышение тонуса сфинктера (УД 1b, СР A [12]).
Аноскопия, ректороманоскопия, колоноскопия проводятся после купирования болевого синдрома.
Функциональные исследования запирательного аппарата прямой кишки. Профилометрия — метод оценки давления в просвете полого органа при протягивании измерительного катетера. Аноректальная профилометрия обеспечивает регистрацию давления в разных плоскостях по всей длине анального канала. С помощью компьютерной программы строится график распределения величин давления и проводится подсчет максимальных, средних величин давления, а также коэффициента асимметрии. Программа обработки предусматривает анализ данных давления на любом уровне поперечного сечения анального канала.
Методика. Исследование проводится в положении больного на боку. После предварительной калибровки катетер вводится в прямую кишку больного на глубину 6 см. Устанавливается скорость перфузии жидкости по катетеру, равная 1 мл/мин. С помощью специального устройства — пулера — катетер вытягивается из прямой кишки со скоростью 1 мм/с, при этом регистрируется давление на всем протяжении его перемещения (табл. 1.2).
Анализ данных проводится с помощью компьютерной программы с построением графика, на котором отражается распределение давления в анальном канале (УД1b, СР A [11]).
Таблица 1.2. Показатели профилометрии в норме (мм рт.ст.)
|
Показатель профилометрии |
Покой |
Волевое сокращение |
|
Анальный канал в целом | ||
|
Максимальное давление |
100,8±11,4 |
137,1±12,6 |
|
Среднее давление |
52,2±8,2 |
76,6±8,9 |
|
Коэффициент асимметрии, ЕД |
19,8±2,3 |
19,2±2,6 |
|
Зона высокого давления* | ||
|
Длина зоны, см |
2,2±0,5 |
2,7±0,65 |
|
Среднее давление |
72,1±9,7 |
100,1±12,5 |
|
Коэффициент асимметрии |
15,5±2,1 |
13,9±2,2 |
* Зона высокого давления соответствует проекции внутреннего и глубокой порции наружного сфинктера.
У всех пациентов с анальной трещиной имеется хотя бы один из манометрических признаков спазма внутреннего сфинктера.
1. Повышение среднего давления в анальном канале в покое.
2. Повышение максимального давления в анальном канале в покое.
3. Наличие ультрамедленных волн.
При сопутствующих заболеваниях необходима консультация смежных специалистов.
УСТАНОВЛЕНИЕ ДИАГНОЗА
n Острая анальная трещина (УД 1b, СР A [12])
1. Заболевание длится менее 2 мес.
2. Отсутствуют рубцовые изменения в области краев и дна анальной трещины.
n Хроническая анальная трещина (УД 1b, СР A [12])
Анальная трещина считается хронической, если имеется один из следующих критериев.
1. Длительность заболевания с момента первого эпизода болевого синдрома более 2 мес.
2. Сторожевой бугорок.
3. Рубцовые края.
4. Наличие волокон внутреннего сфинктера в дне дефекта.
5. Фиброзный полип анального канала.
ДИФФЕРЕНЦИАЛЬНАЯ ДИАГНОСТИКА
Типичная клиническая картина анальной трещины складывается из периодически возникающих обострений, заключающихся в появлении болевого синдрома во время и после дефекации и незначительных (в виде помарок на кале и туалетной бумаге) выделений алой крови. Однако это может быть симптомами и других заболеваний толстой кишки (УД 4, СР С [13]) (табл. 1.3).
Таблица 1.3. Дифференциальная диагностика
|
Жалобы |
Возможные заболевания |
|
Выраженный болевой синдром в анальном канале |
Острый парапроктит |
|
Злокачественные опухоли анального канала и прямой кишки с распространением на анальный канал | |
|
Осложненные каудальные тератомы | |
|
Болезнь Крона с перианальными поражениями | |
|
Идиопатический анокопчиковый болевой синдром | |
|
Эндометриоз | |
|
Прокталгия | |
|
Тромбоз наружных геморроидальных узлов | |
|
Аноректальное кровотечение |
Злокачественные и доброкачественные опухоли прямой кишки и анального канала |
|
Воспалительные заболевания кишечника (ВЗК) | |
|
Ангиодисплазии толстой кишки |
Табл. 1.3. Окончание
|
Жалобы |
Возможные заболевания |
|
|
Эндометриоз |
|
Травма прямой кишки | |
|
Солитарная язва прямой кишки | |
|
Геморрой | |
|
Наличие дефекта анодермы |
Злокачественные и доброкачественные опухоли прямой кишки и анального канала |
|
Гемобластозы | |
|
Сифилис | |
|
ВИЧ-инфекция | |
|
Герпетическая инфекция перианальной кожи | |
|
Нейродермит | |
|
Псориаз | |
|
ВЗК |
КОНСЕРВАТИВНАЯ ТЕРАПИЯ
Лечение
Показания. Острая анальная трещина.
Стандартная схема консервативного лечения, включающая теплые сидячие ванночки и послабляющие средства препараты, содержащие пищевые волокна в виде оболочек семян подорожника, позволяет купировать болевой синдром, добиться остановки кровотечений и заживления у 50% больных острой анальной трещиной с минимальным риском развития побочных эффектов. Добавление в схему лечения местных анестетиков и противовоспалительных средств не влияет на его результаты (УД 1b, СР А [14–16]).
Противопоказания
1. Эрозивно-язвенные поражения верхних отделов желудочно-кишечного тракта (ЖКТ), что требует ограничения приема клетчатки.
2. Нарушения проходимости кишечника.
3. Онкологические заболевания с локализацией поражения в области малого таза.
КОНСЕРВАТИВНАЯ ТЕРАПИЯ В СОЧЕТАНИИ С МЕДИКАМЕНТОЗНОЙ РЕЛАКСАЦИЕЙ ВНУТРЕННЕГО СФИНКТЕРА ПРЯМОЙ КИШКИ
Показания. Острая и хроническая анальная трещина.
При хронической анальной трещине в схему консервативной терапии следует включать препараты для медикаментозной релаксации внутреннего сфинктера прямой кишки (УД 1b, СР A [12]). В качестве препаратов первой линии применяют органические нитраты.
n Нитроглицериновая мазь 0,4%. Препарат готовится путем смешивания концентрированного масляного раствора нитроглицерина и вазелина.
Методика применения. Мазь в количестве 0,5 мл наносят 2 раза в день на перианальную кожу и вводят пальцем в анальный канал на глубину 1 см. Необходимо защищать кожу рук от контакта с препаратом напальчником или перчаткой. Для точного дозирования препарата используют линейку, на которую наносят столбик мази (в том случае, если она расфасована в тубы), либо используют шприц.
Применение 0,4% нитроглицериновой мази позволяет добиться выздоровления у 50% больных с хронической анальной трещиной (УД 1b, СР А [17–27]). Однако, согласно обновленным данным Cochrane Database, ее применение лишь незначительно повышает частоту заживления анальной трещины, существенно сокращается только время купирования болевого синдрома (УД 1a, СР А [28]). Частота развития рецидивов анальной трещины после лечения 0,4% нитроглицериновой мазью существенно превышает таковую после хирургического лечения, хотя частота осложнений значительно меньше (УД 1b, СР А [18, 21, 25]). Повышение дозы не увеличивает эффективность лечения (УД 1b, СР А [17, 23, 24]).
Осложнения. Основной побочный эффект 0,4% нитроглицериновой мази — головная боль, которая наблюдается у 20–30% больных (УД 1b, СР А [17, 23, 28]). Частота развития головных болей дозозависимая и приводит к прекращению терапии у 20% больных (УД 1b [24]).
При возникновении побочных эффектов, препятствующих проведению лечения органическими нитратами, возможно применение препаратов-блокаторов кальциевых каналов (крем дилтиазема, нифедипина).
n Крем дилтиазема 2%, нифедипина 0,3%.
Методика применения. Такая же, как и органических нитратов.
Применение указанных препаратов сопровождается заживлением анальной трещины у 65–95% больных (УД 4, СР C [29–37]). Частота побочных эффектов по сравнению с нитроглицериновой мазью существенно ниже, но недостаточно доказательств их большей эффективности по сравнению с плацебо.
Осложнения. К побочным эффектам лечения относится головная боль, которая наблюдается реже, чем при терапии органическими нитратами (УД 1b, СР A [32–35]), но может достигать 25% (УД 1b [35]). Однако до сих пор количество контролируемых исследований эффективности и безопасности этих препаратов при лечении анальной трещины существенно меньше, чем эффективности и безопасности нитроглицериновой мази.
Поскольку приготовление препаратов по магистральным прописям затруднено, а официнальные препараты не зарегистрированы в России, возможно пероральное применение нифедипина в дозе 20 мг 2 раза
в день, дилтиазема в дозе 60 мг 2 раза в день (УД 4, СР C [36–39]). Пероральное применение этих препаратов сопровождается снижением эффективности лечения и возрастанием частоты побочных эффектов по сравнению с их местным применением (УД 1b [39]).
В случае неэффективности препаратов первой линии в качестве второй линии терапии назначают ботулотоксин (УД 1b, СР А [17, 18]).
n Ботулинический токсин типа A — ботокс.
Методика применения. Препарат вводится во внутренний сфинктер по обе стороны от анальной трещины в дозе 10–100 ЕД. Однако в настоящее время не существует единой точки зрения о его эффективности, точной локализации места введения, необходимой дозировке и количестве инъекций препарата.
Введение препарата приводит к эпителизации анальной трещины у 60–80% больных (УД 4, СР С [40, 41, 44, 46, 48, 50, 51]), что превышает эффективность плацебо. Частота рецидивов может достигать 42% (УД 1b, СР А [43, 44, 50, 51]), однако возможно повторное введение с хорошими результатами (УД 2b, СР В [42,49]). Увеличение дозы препарата улучшает результаты лечения и не сопровождается возрастанием частоты побочных эффектов (УД 2b, СР В [44, 49]). Добавление в схему лечения 0,4% нитроглицериновой мази повышает эффективность ботокса у больных с устойчивой к терапии анальной трещиной (УД 4, СР C [39, 52]).
Осложнения. Недержание газов у 18% (УД 1b, СР А [46, 47, 50, 53]), кишечного содержимого у 5% больных (УД 1b [53]).
В случае если терапия ботоксом неэффективна, больным рекомендуется хирургическое лечение (УД 2b [45]).
Противопоказания для проведения консервативной терапии хронической анальной трещины
1. Выпадение фиброзного полипа из анального канала или наличие фиброзного полипа диаметром более 1 см.
2. Пектеноз — ригидное сужение заднего прохода за счет фиброзных изменений внутреннего сфинктера прямой кишки вследствие его длительного спазма и нарушения кровообращения (УД 1b, СР А [54]).
При наличии указанных симптомов консервативное лечение не проводится, сразу переходят к хирургическому лечению.
ХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕ ХРОНИЧЕСКОЙ АНАЛЬНОЙ ТРЕЩИНЫ
Под хирургическим лечением хронической анальной трещины понимают различные методы хирургической релаксации внутреннего сфинктера прямой кишки. При наличии выраженных рубцово-воспалительных изменений, таких как сторожевой бугорок, гипертрофированный анальный сосочек, выраженные рубцовые изменения края трещины, хирургическую релаксацию внутреннего сфинктера необходимо дополнять иссечением анальной трещины (УД 1b, СР А [54]).
Показания: неэффективность консервативной терапии.
Боковая подкожная сфинктеротомия
Закрытая методика. В анальный канал вводят указательный палец левой кисти. Под контролем пальца, расположенного в анальном канале, вводят узкий глазной скальпель между внутренним и наружным сфинктером через межсфинктерное пространство. Глубина введения скальпеля — до зубчатой линии. Рассечение сфинктера производят одним движением, извлекая скальпель наружу. Пальцем, находящимся в анальном канале, определяют наличие диастаза рассеченного сфинктера, что свидетельствует о правильно выполненной манипуляции.
Открытая методика. В 0,5–1,0 см от края ануса на 3 ч по циферблату производят полуовальный разрез кожи длиной около 1,0 см. В подслизистый слой стенки анального канала для отслоения ее от внутреннего сфинктера вводят 3,0–5,0 мл 0,5% раствора прокаина (новокаина). Зажимом или ножницами производят отделение внутреннего сфинктера от слизистой оболочки анального канала, а также отделение внутреннего сфинктера от наружного. Высоту рассечения ограничивают зубчатой линией. После проведения сфинктеротомии на кожу накладывают два шва рассасывающейся нитью.
Боковая подкожная сфинктеротомия — метод выбора в случае неэффективности консервативной терапии (УД 1a, СР А [28, 55]). Большое количество исследований (УД 1b, СР A [56–59]) и данные Cochrane Database (УД 1a, СР A [60]) подтверждают ее большую эффективность и меньшее число осложнений по сравнению с неконтролируемой пальцевой дивульсией анального сфинктера. Применение боковой подкожной сфинктеротомии сопровождается большей частотой заживления анальной трещины и меньшим риском развития анального недержания по сравнению с задней открытой сфинктеротомией и/или иссечением трещины (УД 4, СР C [61]). Хорошо организованные исследования подтверждают одинаковую эффективность и безопасность как открытой, так и закрытой боковой подкожной сфинктеротомии (УД 1a, СР A [62–65]). Однако наличие передней и задней анальной трещины, а также наружного и внутреннего геморроя затрудняет выполнение открытой сфинктеротомии.
Противопоказания
n Наличие скрытых нарушений функции ЗАПК.
Осложнения
n Гематомы в области сфинктеротомии.
n Абсцессы в области сфинктеротомии.
n Формирование свищей в области сфинктеротомии.
n Недостаточность анального сфинктера.
Контролируемая пневмодивульсия анального сфинктера
Причиной развития большинства осложнений после боковой подкожной сфинктеротомии является отсутствие непосредственного визуального контроля за проведением манипуляции. В таких условиях возможны избыточное или недостаточное рассечение внутреннего сфинктера прямой кишки, повреждение дистальных ветвей нижней прямокишечной артерии и геморроидальных венозных сплетений (УД 4, СР С [73]) (Эктов). Поэтому хирургическая релаксация внутреннего сфинктера прямой кишки путем его растяжения, т.е. без рассечения, может служить альтернативой сфинктеротомии.
Методика. Перед проведением манипуляции определяют необходимый диаметр пневмобаллона. Для этого в анальный канал вводят специальный градуированный конус с надетым на него латексным чехлом и смазанный вазелиновым маслом с целью определения исходного диаметра анального канала. Вращательным движением измерительное устройство для определения диаметра анального канала вводят в прямую кишку под контролем динамометра с усилием, не превышающим 2 кг, до его максимального соприкосновения со стенками анального канала. На измерительном устройстве имеются деления: 1, 2, 3, 4. Каждое деление соответствует определенному диаметру, так, цифра «1» соответствует диаметру 41 мм, цифра «2» — диаметру 45 мм, цифра «3» — 48 мм, цифра
«4» — 51 мм. После определения исходного диаметра анального канала
на уровне наружного его края конус удаляют, и в анальный канал вводитят пневмобаллон соответствующего диаметра с надетым на него латексным чехлом, предварительно смазанным вазелиновым маслом. Путем постепенного нагнетания воздуха (в течение 1 мин) до 0,7 атм. баллон полностью расширяется до своего предельного диаметра, и в течение 7 мин производят пневмодивульсию анального сфинктера. Затем баллон сдувают и извлекают из анального канала.
Пневмодивульсия позволяет достичь устойчивой релаксации внутреннего сфинктера прямой кишки и по данным эндоректальной ультрасонографии не сопровождается повреждением ЗАПК. Транзиторная анальная инконтиненция наблюдалась только у пациенток с многократными родами в анамнезе (УД 1b, СР А [66]).
Противопоказания
n Наружный и внутренний геморрой 3–4-й стадии.
n Ранее перенесенные вмешательства на анальном канале.
n Свищи прямой кишки.
n Ригидное сужение заднего прохода — пектеноз (УД 4, СР С [67]).
Иссечение трещины в сочетании с медикаментозной релаксацией внутреннего сфинктера
Показания
n Наличие высокого риска развития анального недержания после сфинктеротомии:
v разрывы промежности во время родов у женщин;
v клинические признаки опущения тазового дна;
v возраст старше 60 лет (УД 4, СР С [68]).
Методика. С помощью электрокоагулятора производят разрез слизистой оболочки и кожи вокруг трещины. Затем плоско вдоль проекции мышечных волокон сфинктера иссекают в пределах здоровых тканей трещину с криптой, сторожевым бугорком и гипертрофированным анальным сосочком. Иссечение производят в виде треугольника, обращенного вершиной в кишку, основанием на перианальную кожу или в виде эллипса. При удалении трещины недопустимо оставлять нависающие края слизистой оболочки из-за возможного сращения их с последующим образованием свища прямой кишки. Операцию заканчивают аппликацией на перианальную кожу 0,4% нитроглицериновой мази, или 2% крема дилтиазема, или 0,3% крема нифедипина либо производят инъекцию ботокса. Данные нерандомизированных исследований свидетельствуют, что результаты иссечения анальной трещины статистически достоверно улучшаются не только в случае применения в послеоперационном периоде 0,4% нитроглицериновой мази, но и 2% крема дилтиазема, 0,3% крема нифедипина либо ботокса. Однако из-за наличия побочных эффектов этих препаратов применять этот метод следует пациентам с высоким
риском развития анального недержания (УД 4, СР C [68–73]).
Противопоказания
n Наличие толерантности к органическим нитратам.
Чего нельзя делать
n Проводить консервативную терапию в течение длительного, более 6 нед, периода времени (УД 1b, СР A [12]).
n Проводить хирургическое лечение анальной трещины без релаксации внутреннего сфинктера прямой кишки (УД 5, СР D [74]).
Дальнейшее ведение
В послеоперационном периоде до момента заживления ран пациентам требуется производить регулярную санацию анальной области с использованием сидячих ванночек со слабым раствором перманганата калия или ромашки, а также выполнять ежедневные перевязки с использованием мазевых основ, обладающих противовоспалительным и ранозаживляющим действием (УД 5, СР D [4]).
Необходим еженедельный врачебный контроль за течением раневого процесса до полного заживления ран (УД 5, СР D [4]).
На период заживления ран требуется соблюдение диеты, богатой растительной клетчаткой, прием пищевых волокон для смягчения стула (УД 5, СР D [4]).
Прогноз
Консервативная терапия приводит к выздоровлению приблизительно 50–60% больных, что, вероятно, связано с низкой комплаентностью пациентов (УД 1a, СР A [34, 63]), в то же время хирургическое лечение более эффективно и позволяет добиться устойчивого выздоровления у 94–100% пациентов (УД 1b, СР A [75–79]).
Критерии оценки качества помощи в стационаре представлены в таблице 1.4. Для оценки качества медицинской помощи используют временные, процессуальные и профилактирующие критерии. Временные характеризуют своевременность оказания определенных этапов медицинской помощи. Выполнение пациенту ряда медицинских манипуляций, инструментальных и лабораторных исследований, необходимых для качественного оказания медицинской помощи, оценивают в процессуальных критериях. Для анализа мероприятий, направленных на предотвращение развития осложнений, используют профилактирующие критерии.
Таблица 1.4. Критерии оценки качества медицинской помощи в стационаре больным с доброкачественными заболеваниями анального канала (анальная трещина) (0 — нет, 1 — да)
|
Клинические рекомендации |
Временные |
Процессуальные |
Профилактирующие |
|
Клинические рекомендации по диагностике и лечению взрослых паци- ентов с анальной трещиной (код МКБ — К60: K60.0; K60.1; K60.2) |
Установка клинического диагноза в течение 72 ч: 0/1 |
Оценка анального рефлекса: 0/1. Пальцевое исследование прямой кишки: 0/1. Аноскопия: 0/1. Ректороманоскопия: 0/1. Определение группы крови: 0/1. Исследование крови на сифилис, вирусный гепатит В, вирусный гепатит С: 0/1. Клинический анализ крови; биохимический анализ крови; клинический анализ мочи; коагулограмма: 0/1. Метод оперативного лечения в соответствии с клиническими рекомендациями: 0/1. Метод анестезии в соответствии с объемом оперативного лечения: 0/1 |
Отсутствие осложнений: • кровотечение: 0/1; • абсцесс: 0/1; • флегмона: 0/1; • пневмония: 0/1; • тромбоэмболия: 0/1; • летальный исход: 0/1 |
ЛИТЕРАТУРА
1. Врублевский В.А., Милитарев Ю.М. Распространенность болезней прямой и ободочной кишок у взрослого населения Москвы // Проблемы проктологии. — М., 1983. — Вып. 4. — С. 6–10.
2. Phillips B., Ball C., Sackett D. et al. Oxford Center for Evidence-Based Medicine — Levels of Evidence. — 2009. — Available from: http://www.cebm.net/ oxford-centre-evidence-based-medicine-levels-evidence-march-2009.
3. Hoffmann J.C., Fischer I., Höhne W. et al. Methodische Grundlagen für die Ableitung von Konsensusempfehlungen [Methodological basis for the development of consensus recommendations] // Z. Gastroenterol. — 2004. — Vol. 42, N 9. — P. 984–986.
4. Воробьев Г.И. Основы колопроктологии. — Ростов-н/Д, 2001. — 413 с.
5. Braun J., Raguse T. Pathophysiologic role of the internal anal sphincter in chronic anal fissure // Z. Gastroenterol. — 1985 — Vol. 1, N 23. — P. 565–572.
6. Klosterhalfen B., Vogel P., Rixen H., Mittermayer C. Topography of the inferior rectal artery: a possible cause of chronic, primary anal fissure // Dis. Colon Rectum. — 1989. — Vol. 1, N 32. — P. 43–52.
7. Международная классификация болезней 10-го пересмотра. МКБ-10. Доступен с сайта: www.10mkb.ru.
8. Jensen S.L. Diet and other risk factors for fissure-in-ano. Prospective case control study // Dis. Colon Rectum. — 1988. — Vol. 31, N 10. — P. 770–773.
9. Gupta P.J. Consumption of red-hot chili pepper increases symptoms in patients with acute anal fissures // Ann. Ital. Chir. — 2008. — Vol. 79, N 5. — P. 347–351.
10. Kuehn H.G., Gebbensleben O., Hilger Y., Rohde H. Relationship between anal
symptoms and anal findings // Int. J. Med. Sci. — 2009. — Vol. 6. — P. 77–84.
11. Opazo A., Aguirre E., Saldana E. et al. Patterns of impaired internal anal sphincter activity in patients with anal fissure // Colorectal Dis. — 2013. — Vol. 15, N 4. — P. 492–499.
12. Gagliardi G., Pascariello A., Bove A. Optimal treatment duration of glyceryl trinitrate for chronic anal fissure: results of a prospective randomized multicenter trial // Tech. Coloproctol. — 2010. — Vol. 14. — P. 241–248.
13. Титов А.Ю., Жарков Е.Е., Варданян А.В., Рыбаков Е.Г. Дифференциально-
диагностические критерии эрозивно-язвенных поражений анального канала и перианальной кожи // Колопроктология. — 2012. — Т. 3, № 41. — С. 3–10.
14. Gough M.J., Lewis A. The conservative treatment of fissure-in ano // Br. J. Surg. — 1983. — Vol. 70. — P. 175–176.
15. Gupta P. Randomized, controlled study comparing sitz-bath and no-sitz-bath treatments in patients with acute anal fissures // Aust. N.Z. J. Surg. — 2006. — Vol. 76. — P. 718–721.
16. Jensen S.L. Treatment of first episodes of acute anal fissure: prospective randomised study of lignocaine ointment versus hydrocortisone ointment or warm sitz baths plus bran // BMJ. — 1986. — Vol. 292. — P. 1167–1169.
17. Evans J., Luck A., Hewett P. Glyceryl trinitrate vs. lateral sphincterotomy for chronic anal fissure: prospective, randomized trial // Dis. Colon Rectum. — 2001. — Vol. 44. — P. 93–97.
18. Kennedy M.L., Sowter S., Nguyen H., Lubowski D.Z. Glyceryl trinitrate
ointment for the treatment of chronic anal fissure: results of a placebo-controlled trial and long-term follow-up // Dis. Colon Rectum. — 1999. — Vol. 42. — P. 1000–1006.
19. Libertiny G., Knight J.S., Farouk R. Randomised trial of topical 0,2% glyceryl trinitrate and lateral internal sphincterotomy for the treatment of patients with
chronic anal fissure: long-term follow-up // Eur. J. Surg. — 2002. — Vol. 168. — P. 418–421.
20. Oettle G.J. Glyceryl trinitrate vs. sphincterotomy for treatment of chronic fissure-in-ano: a randomized, controlled trial // Dis. Colon Rectum. — 1997. — Vol. 40. — P. 1318–1320.
21. Werre A.J., Palamba H.W., Bilgen E.J., Eggink W.F. Isosorbide dinitrate in
the treatment of anal fissure: a randomised, prospective, double blind, placebocontrolled trial // Eur. J. Surg. — 2001. — Vol. 167. — P. 382–385.
22. Scholefield J.H., Bock J.U., Marla B. et al. A dose finding study with 0,1%, 0,2%, and 0,4% glyceryl trinitrate ointment in patients with chronic anal fissures // Gut. — 2003. — Vol. 52. — P. 264–269.
23. Zuberi B.F., Rajput M.R., Abro H., Shaikh S.A. A rando.mized trial of glyceryl
trinitrate ointment and nitroglycerin patch in healing of anal fissures // Int. J. Colorectal Dis. — 2000. — Vol. 15. —P. 243–245.
24. Bailey H.R., Beck D.E., Billingham R.P. et al. Fissure Study GrouP. A study to determine the nitroglycerin ointment dose and dosing interval that best promote the healing of chronic anal fissures // Dis. Colon Rectum. — 2002. — Vol. 45. — P. 1192–1199.
25. Lund J.N., Scholefield J.H. A randomised, prospective, double-blind, placebo-
controlled trial of glyceryl trinitrate ointment in treatment of anal fissure [published correction appears in Lancet // Lancet. — 1997. — Vol. 349. — P. 11–14.
26. Chaudhuri S., Pal A.K., Acharya A. et al. Treatment of chronic anal fissure with topical glyceryl trinitrate: a double-blind, placebocontrolled trial // Indian J. Gastroenterol. — 2001. — Vol. 20. — P. 101–102.
27. Bacher H., Mischinger H.J., Werkgartner G. et al. Local nitroglycerin for
treatment of anal fissures: an alternative to lateral sphincterotomy? // Dis. Colon Rectum. — 1997. — Vol. 40. — P. 840–845.
28. Nelson R. Non surgical therapy for anal fissure // Cochrane Database Syst. Rev. — 2006. — CD003431.
29. Carapeti E.A., Kamm M.A., Phillips R.K. Topical diltiazem and bethanechol decrease anal sphincter pressure and heal anal fissures without side effects // Dis. Colon Rectum. — 2000. — Vol. 43. — P. 1359–1362.
30. Knight J.S., Birks M., Farouk R. Topical diltiazem ointment in the treatment of chronic anal fissure // Br. J. Surg. — 2001. — Vol. 88. — P. 553–556.
31. Ezri T., Susmallian S. Topical nifedipine vs. topical glyceryl trinitrate for treatment of chronic anal fissure // Dis. Colon Rectum. — 2003. — Vol. 46. — P. 805–808.
32. Bielecki K., Kolodziejczak M. A prospective randomized trial of diltiazem and glyceryl trinitrate ointment in the treatment of chronic anal fissure // Colorectal Dis. — 2003. — Vol. 5. — P. 256–257.
33. Kocher H.M., Steward M., Leather A.J., Cullen P.T. Randomized clinical trial
assessing the side-effects of glyceryl trinitrate and diltiazem hydrochloride in the treatment of chronic anal fissure // Br. J. Surg. — 2002. — Vol. 89. — P. 413–417.
34. Perrotti P., Bove A., Antropoli C. et al. Topical nifedipine with lidocaine ointment vs. active control for treatment of chronic anal fissure: results of a prospective, randomized, double-blind study // Dis. Colon Rectum. — 2002. — Vol. 45. — P. 1468–1475.
35. Antropoli C., Perrotti P., Rubino M. et al. Nifedipine for local use in
conservative treatment of anal fissures: preliminary results of a multicenter study // Dis. Colon Rectum. — 1999. — Vol. 42. — P. 1011–1015.
36. Jonas M., Neal K.R., Abercrombie J.F., Scholefield J.H. A randomized trial of oral vs. topical diltiazem for chronic anal fissures // Dis. Colon Rectum. — 2001. — Vol. 44. — P. 1074–1078.
37. Ansaloni L., Bernabe A., Ghetti R. et al. Oral lacidipine in the treatment of anal fissure // Tech. Coloproctol. — 2002. — Vol. 6. — P. 79–82.
38. Ağaoğlu N., Cengiz S., Arslan M.K., Türkyilmaz S. Oral nifedipine in the treatment of chronic anal fissure // Dig. Surg. — 2003. — Vol. 20. — P. 452–456.
39. Cook T.A., Humphreys M.M., Mortensen N.J. Oral nifedipine reduces resting anal pressure and heals chronic anal fissure // Br. J. Surg. — 1999. — Vol. 86. — P. 1269–1273.
40. Brisinda G., Cadeddu F., Brandara F. et al. Randomized clinical trial comparing botulinum toxin injections with 0,2 per cent nitroglycerin ointment for chronic anal fissure // Br. J. Surg. — 2007. — Vol. 94. — P. 162–167.
41. Jones O.M., Ramalingam T., Merrie A. et al. Randomized clinical trial of botulinum toxin plus glyceryl trinitrate vs. botulinum toxin alone for medically resistant chronic anal fissure: overall poor healing rates // Dis. Colon Rectum. — 2006. — Vol. 49. — P. 1574–1580.
42. Arroyo A., Perez F., Serrano P. et al. Long-term results of botulinum toxin for the treatment of chronic anal fissure: prospective clinical and manometric study // Int. J. Colorectal Dis. — 2005. — Vol. 20. — P. 267–271.
43. Brisinda G., Maria G., Sganga G. et al. Effectiveness of higher doses of botulinum toxin to induce healing in patients with chronic anal fissures // Surgery. — 2002. — Vol. 131. — P. 179–184.
44. Maria G., Brisinda G., Bentivoglio A.R. et al. Influence of botulinum toxin site of injections on healing rate in patients with chronic anal fissure // Am. J. Surg. — 2000. — Vol. 179. — P. 46–50.
45. Brisinda G., Maria G., Bentivoglio A.R. et al. A comparison of injections of botulinum toxin and topical nitroglycerin ointment for the treatment of chronic anal fissure // N. Engl. J. Med. — 1999. — Vol. 341. — P. 65–69.
46. Maria G., Cassetta E., Gui D. et al. A comparison of botulinum toxin and saline for the treatment of chronic anal fissure // N. Engl. J. Med. — 1998. — Vol. 338. — P. 217–220.
47. Colak T., Ipek T., Kanik A., Aydin S. A randomized trial of botulinum toxin vs. lidocaine pomade for chronic anal fissure // Acta Gastroenterol. Belg. — 2002. — Vol. 65. — P. 187–190.
48. Madalinski M.H., Slawek J., Zbytek B. et al. Topical nitrates and the higher doses of botulinum toxin for chronic anal fissure // Hepatogastroenterology. — 2001. — Vol. 48. — P. 977–979.
49. Lindsey I., Jones O.M., Cunningham C. et al. Botulinum toxin as secondline therapy for chronic anal fissure failing 0.2 percent glyceryl trinitrate // Dis. Colon Rectum. — 2003. — Vol. 46. — P. 361–366.
50. Mentes B.B. et al. Comparison of botulinum toxin injection and lateral internal sphincterotomy for the treatment of chronic anal fissure // Dis. Colon Rectum. — 2003. — Vol. 46. — P. 232–237.
51. Minguez M., Herreros B., Espi A. et al. Long-term follow-up (42 months) of chronic anal fissure after healing with botulinum toxin // Gastroenterology. — 2002. — Vol. 123. — P. 112–117.
52. Lysy J., Israelit-Yatzkan Y., Sestiery-Ittah M. et al. Topical nitrates potentiate the effect of botulinum toxin in the treatment of patients with refractory anal fissure // Gut. — 2001. — Vol. 48. — P. 221–224.
53. Jost W.H. One hundred cases of anal fissure treated with botulinum toxin: early and long-term results // Dis. Colon Rectum. — 1997. — Vol. 40. — P. 1029–1032.
54. Gupta P.J. Hypertrophied anal papillae and fibrous anal polyps, should they be removed during anal fissure surgery? // World J. Gastroenterol. — 2004. — Vol. 10, N 16. — P. 2412–2414.
55. Richard C.S., Greggoire R., Plewes E.A. et al. Internal sphincterotomy is superior to topical nitroglycerine in the treatment of chronic anal fissure: results of a randomized, controlled trial by the Canadian Colorectal Surgical Trials Group //
Dis. Colon Rectum. — 2000. — Vol. 43. — P. 1048–1047.
56. Jensen S.L., Lund F., Nielsen O.V., Tange G. Lateral subcutaneous sphincterotomy versus anal dilatation in the treatment of fissure in ano in outpatients: a prospective randomized study // BMJ. — 1984. — Vol. 289. — P. 528–530.
57. Saad A.M., Omer A. Surgical treatment of chronic fissure-in-ano: a prospective randomized study // East Afr. Med. J. — 1992. — Vol. 69. — P. 613–615.
58. Olsen J., Mortensen P.E., Krogh Petersen I. et al. Anal sphincter function after treatment of fissure-in-ano by lateral subcutaneous sphincterotomy versus anal dilation // Int. J. Colorectal Dis. — 1987. — Vol. 2. — P. 155–157.
59. Weaver R.M., Ambrose N.S., Alexander-Williams J. et al. Manual dilation of the anus vs. lateral internal sphincterotomy in the treatment of chronic fissure-in-
ano: results of a prospective, randomized clinical trial // Dis. Colon Rectum. — 1987. — Vol. 30. — P. 420–423.
60. Nelson R. Operative procedures for fissure in ano // Cochrane Database Syst. Rev. — 2005. — CD002199.
61. Abcarian H. Surgical correction of chronic anal fissure: results of lateral internal sphincterotomy vs. fissurectomy-midline sphincterotomy // Dis. Colon Rectum. — 1980. — Vol. 23. — P. 31–36.
62. Boulous P.B., Araujo J.G. Adequate internal sphincterotomy for chronic anal fissure: subcutaneous or open technique? // Br. J. Surg. — 1984. — Vol. 71. — P. 360–362.
63. Kortbeek J.B., Langevin J.M., Khoo R.E. et al. Chronic fissure-in-ano: a randomized study comparing open and subcutaneous lateral internal sphincterotomy // Dis. Colon Rectum. — 1992. — Vol. 35. — P. 835–837.
64. Arroyo A., Perez F., Serrano P. et al. Open versus closed lateral internal sphincterotomy performed as an outpatient procedure under local anesthesia for chronic anal fissure: prospective randomized study of clinical and manometric long-
term results // J. Am. Coll. Surg. — 2004. — Vol. 199. — P. 361–367.
65. Wiley M., Day P., Rieger N. et al. Open vs. closed lateral internal sphincterotomy for idiopathic fissure-in-ano: a prospective, randomized, controlled trial // Dis. Colon Rectum. — 2004. — Vol. 47. — P. 847–852.
66. Renzi A., Izzo D., Di Sarno G. et al. Clinical, manometric, and ultrasonographic results of pneumatic balloon dilatation vs. lateral internal sphincterotomy for chronic anal fissure: a prospective, randomized, controlled trial // Dis. Colon
Rectum. — 2008. — Vol. 51. — P. 121–127.
67. Багдасарян С.Л. Хирургическое лечение анальной трещины с пневмодивульсией анального сфинктера. — М., 2010. — 89 с.
68. Жарков Е.Е. Комплексное лечение хронической анальной трещины. — M., 2009. — 113 с.
69. Baraza W., Boereboom C., Shorthouse A. et al. The long-term efficacy of fissurectomy and botulinum toxin injection for chronic anal fissure in females // Dis. Colon Rectum. — 2008. — Vol. 51. — P. 236–243.
70. Scholz T., Hetzer F.H., Dindo D. et al. Long-term follow-up after combined fissurectomy and Botox injection for chronic anal fissures // Int. J. Colorectal Dis. — 2007. — Vol. 22. — P. 1077–1081.
71. Lindsey I., Cunningham C., Jones O.M. et al. Fissurectomy-botulinum toxin: a novel sphincter-sparing procedure for medically resistant chronic anal fissure // Dis. Colon Rectum. — 2004. — Vol. 47. — P. 1947–1952.
72. Arthur J.D., Makin C.A., El-Sayed T.Y., Walsh C.J. A pilot comparative study of fissurectomy/diltiazem and fissurectomy/botulinum toxin in the treatment of chronic anal fissure // Tech. Coloproctol. — 2008. — Vol. 12, N 4. — P. 331–336.
73. Engel A.F., Eijsbouts Q.A., Balk A.G. Fissurectomy and isosorbide dinitrate for chronic fissure-in-ano not responding to conservative treatment // Br. J. Surg. 2002. — Vol. 89, N 1. — P. 79–83.
74. Bhardwaj R., Parker M.C. Modern perspectives in the treatment of chronic anal fissures // Ann. R. Coll. Surg. Engl. — 2007. — Vol. 89. — P. 472–478.
75. Arroyo A., Perez F., Serrano P. et al. Surgical versus chemical (botulinum toxin) sphincterotomy for chronic anal fissure: long-term results of a prospective randomized clinical and manometric study // Am. J. Surg. — 2005. — Vol. 189. — P. 429–434.
76. Iswariah H., Stephens J., Rieger N. et al. Randomized prospective controlled trial of lateral internal sphincterotomy versus injection of botulinum toxin for the treatment of idiopathic fissure-in-ano // Aust. N.Z. J. Surg. — 2005. — Vol. 75. — P. 553–555.
77. Katsinelos P., Papaziogas B., Koutelidakis I. et al. Topical 0.5% nifedipine vs. lateral internal sphincterotomy for the treatment of chronic anal fissure: long term follow-up // Int. J. Colorectal Dis. — 2006. — Vol. 21. — P. 179–183.
78. Brown C.J., Dubreuil D., Santoro L. et al. Lateral internal sphincterotomy is superior to topical nitroglycerine for healing chronic anal fissure and does not compromise long-term fecal incontinence: six year follow-up of a multicenter, randomized, controlled trial // Dis. Colon Rectum. — 2007. — Vol. 50. — P. 442– 448.
79. Sileri P., Mele A., Stolfi V.M. et al. Medical and surgical treatment of chronic anal fissure: a prospective study // J. Gastrointest. Surg. — 2007. — Vol. 11. — P. 1541–1548.
ОСТРЫЙ И ХРОНИЧЕСКИЙ ГЕМОРРОЙ
Введение
Геморрой — одно из самых распространенных заболеваний человека и наиболее частая причина обращения к врачу-колопроктологу. Распространенность заболевания составляет 130–145 человек на 1000 взрослого населения, а его удельный вес в структуре заболеваний толстой кишки колеблется от 34 до 41% (УД 5, СР D [1]). Эта патология одинаково часто встречается у мужчин и у женщин.
Современный темп жизни сопровождается усилением гиподинамии. Вынужденное длительное сидение за компьютером, на работе и дома, за рулем автомобиля и т.п. сопровождается постоянным застоем кровообращения в органах малого таза, в основном в прямой кишке. Это, в свою очередь, приводит к росту заболеваемости геморроем, которым все чаще страдают люди молодого трудоспособного возраста (УД 5, СР D [1]).
Настоящие рекомендации по диагностике и лечению геморроидальной болезни являются руководством для практических врачей, осуществляющих ведение и лечение данных пациентов.
Рекомендации подлежат регулярному пересмотру в соответствии с новыми данными научных исследований в этой области. Настоящие рекомендации составлены на основании анализа литературы из базы данных PubMed, MEDLINE, Cochrane Collaboration, the Standards Practice Task Force of the American Society of Colon and Rectal Surgeon, Oxford Center for Evidence-based Medicine — Levels of Evidence.
Для отдельных положений рекомендаций приведены уровни доказательности согласно общепринятой классификации Оксфордского центра доказательной медицины (табл. 2.1) [2, 3].
Таблица 2.1. Уровни доказательности и степени рекомендаций на основании классификации Оксфордского центра доказательной медицины
|
Уровень |
Исследования методов диагностики |
Исследования методов лечения |
|
1а |
Систематический обзор гомогенных диагностических исследований 1-го уровня |
Систематический обзор гомогенных РКИ |
Табл. 2.1. Окончание
|
Уровень |
Исследования методов диагностики |
Исследования методов лечения |
|
1b |
Валидизирующее когортное исследование с качественным «золотым стандартом» |
Отдельное РКИ (с узким доверительным интервалом) |
|
1с |
Специфичность или чувствительность столь высокие, что положительный или отрицательный результат позволяет исключить/установить диагноз |
Исследование «Всё или ничего» |
|
2а |
Систематический обзор гомогенных диагностических исследований >2-го уровня |
Систематический обзор (гомогенных) когортных исследований |
|
2b |
Разведочное когортное исследование с качественным «золотым стандартом» |
Отдельное когортное исследование (включая РКИ низкого качества; т.е. с <80% пациентов, прошедших контрольное наблюдение) |
|
2с |
Нет |
Исследование «исходов»; экологические исследования |
|
3а |
Систематический обзор гомогенных исследований уровня 3b и выше |
Систематический обзор гомогенных исследований «случай–контроль» |
|
3b |
Исследование с непоследовательным набором или без проведения исследования «золотого стандарта» у всех испытуемых |
Отдельное исследование «случай– контроль» |
|
4 |
Исследование «случай–контроль» или исследование с некачественным или зависимым «золотым стандартом» |
Серия случаев (и когортные исследования или исследования «случай–контроль» низкого качества) |
|
5 |
Мнение экспертов без тщательной критической оценки или основанное на физиологии, лабораторные исследования на животных или разработка «первых принципов» |
Мнение экспертов без тщательной критической оценки, лабораторные исследования на животных или разработка «первых принципов» |
|
Степень рекомендации | ||
|
A |
Согласующиеся между собой исследования 1-го уровня | |
|
B |
Согласующиеся между собой исследования 2-го или 3-го уровня или экстраполяция на основе исследований 1-го уровня | |
|
C |
Исследования 4-го уровня или экстраполяция на основе уровня 2 или 3 | |
|
D |
Доказательства 4-го уровня или затруднительные для обобщения или некачественные исследования любого уровня | |
ВАЛИДИЗАЦИЯ РЕКОМЕНДАЦИЙ
Настоящие рекомендации составлены Общероссийской общественной организацией «Ассоциация колопроктологов России» и в предварительной версии были рецензированы независимыми экспертами, которых попросили прокомментировать прежде всего, насколько интерпретация доказательств, лежащих в основе рекомендаций, доступна для понимания. Получены комментарии со стороны врачей амбулаторного звена. Полученные комментарии тщательно систематизировались и обсуждались на совещаниях экспертной группы.
Последние изменения в настоящих рекомендациях были представлены для дискуссии на заседании профильной комиссии «Колопроктология» Экспертного совета Минздрава России 17 декабря 2012 г. Проект рекомендаций был повторно рецензирован независимыми экспертами и врачами амбулаторного звена. Для окончательной редакции и контроля качества рекомендации были повторно проанализированы членами экспертной группы, которые пришли к заключению, что все замечания и комментарии приняты во внимание, риск систематических ошибок при разработке рекомендаций сведен к минимуму.
ОБЛАСТЬ ПРИМЕНЕНИЯ РЕКОМЕНДАЦИЙ
Данные клинические рекомендации применимы при осуществлении медицинской деятельности в рамках Порядка оказания медицинской помощи взрослому населению с заболеваниями толстой кишки, анального канала и промежности колопроктологического профиля.
Определение
Геморрой — патологическое увеличение геморроидальных узлов (внутренних узлов — внутренний геморрой, наружных узлов — наружный геморрой). Комбинированный геморрой — увеличение одновременно наружных и внутренних геморроидальных узлов [1, 4].
Причиной патологического увеличения геморроидальных узлов является острое или хроническое нарушение кровообращения в кавернозных образованиях. Наряду с нарушением кровообращения в развитии геморроя значительную роль играют дистрофические изменения в связочном аппарате геморроидальных узлов (УД 5, СР D [4, 5]).
Под действием перечисленных факторов геморроидальные узлы увеличиваются в размерах, смещаются в дистальном направлении, при этом нарастают процессы дистрофии в удерживающем аппарате, и геморроидальные узлы начинают выпадать из анального канала. Развитие дистрофических процессов в общей продольной мышце подслизистого слоя прямой кишки и в связке Паркса, удерживающих кавернозные тельца в анальном канале, приводит к постепенному, но необратимому смещению геморроидальных узлов в дистальном направлении.
Код по Международной классификации болезней 10-го пересмотра [6]
К64.0 Геморрой 1 ст. К64.1 Геморрой 2 ст. К64.2 Геморрой 3 ст. К64.3 Геморрой 4 ст.
К64.4 Остаточные геморроидальные кожные бахромки К64.5 Перианальный венозный тромбоз
К64.8 Другой уточненный геморрой К64.9 Геморрой неуточненный
Классификация [4, 5, 7]
По форме:
n внутренний;
n наружный;
n комбинированный.
По течению:
n хронический (табл. 2.2);
n острый (табл. 2.3).
Таблица 2.2. Классификация хронического геморроя
|
Хроническое течение |
Стадии |
Симптоматика |
|
1 |
Кровотечение, без выпадения узлов | |
|
2 |
Выпадение внутренних геморроидальных узлов с самостоятельным вправлением в анальный канал, с/без кровотечения | |
|
3 |
Выпадение внутренних геморроидальных узлов с необходимостью их ручного вправления в анальный канал, с/без кровотечения | |
|
4 |
Постоянное выпадение внутренних геморроидальных узлов и невозможность их вправления в анальный канал, с/без кровотечения |
Таблица 2.3. Классификация острого геморроя
|
Острое течение* |
Степень |
Симптоматика |
|
1 |
Тромбоз узлов без воспалительной реакции | |
|
2 |
Тромбоз узлов с их воспалением | |
|
3 |
Тромбоз узлов с их воспалением и переходом воспаления на подкожную клетчатку, с отеком перианальной кожи, некрозом слизистой оболочки узлов |
* Под острым течением заболевания также понимается профузное, обильное кровотечение из внутренних геморроидальных узлов, требующее срочной госпитализации пациента в стационар для остановки кровотечения и проведения корригирующей терапии.
Формулировка диагноза
При формулировании диагноза следует отразить наличие наружного и/или внутреннего компонента, указать стадию заболевания при хроническом течении, желательно отразить локализацию узлов по условному циферблату, соответствующих данной стадии заболевания. Острый геморрой является осложнением хронического течения.
Примеры формулировок диагноза
n Внутренний геморрой 2-й стадии.
n Наружный и внутренний геморрой 3–4-й стадии.
n Наружный геморрой, осложненный острым тромбозом.
n Внутренний геморрой 2-й (3, 11 ч) — 4-й стадии (7 ч).
Диагностика
Диагностика геморроя основана на оценке жалоб, длительности заболевания, результатов пальцевого исследования и инструментальных методов обследования (УД 2b, СР В [8]).
К основным клиническим симптомам хронического геморроя относятся выпадение внутренних геморроидальных узлов из заднего прохода при дефекации, выделение крови из заднего прохода при дефекации (примесь алой крови к стулу, выделение крови в виде капель или струйки), наличие увеличенных наружных геморроидальных узлов. К более редким симптомам относятся ощущение дискомфорта, влажности в области заднего прохода, зуд, жжение в области заднего прохода, слизистые выделения из прямой кишки. Болевые ощущения при хроническом геморрое встречаются редко и, как правило, связаны с осложнениями заболевания (тромбоз наружных и/или внутренних геморроидальных узлов) или появлением анальной трещины, свища прямой кишки (табл. 2.4).
К основным клиническим симптомам острого геморроя относятся боли в области заднего прохода и прямой кишки, появление плотного болезненного образования (ий) в области расположения наружных и/или внутренних геморроидальных узлов, профузное обильное выделение крови из прямой кишки, не останавливающееся с помощью консервативных мероприятий (свечи, мази, местное применение холода, флеботропные препараты и т.п.). При развитии воспалительных осложнений острого тромбоза геморроидальных узлов с переходом воспалительного процесса на окружающие ткани, параректальную клетчатку, возможно появление общих воспалительных симптомов, таких как повышение температуры тела, лихорадка.
Сбор анамнеза. Выявлены этиологические факторы возникновения заболевания: желудочно-кишечные расстройства, погрешности в диете, злоупотребление алкоголем, малоподвижный и сидячий образ жизни, беременность и роды (УД 5, СР D [1, 4, 9]).
Таблица 2.4. Клиническая картина геморроидальной болезни
|
Возможные клинические проявления болезни в анамнезе |
Типичные клинические симптомы в момент осмотра |
|
• Периодическое выделение крови из заднего прохода при дефекации. • Ощущение дискомфорта, влажности в области заднего прохода. • Увеличение геморроидальных узлов, как правило, связанное с нарушением стула, диеты, у женщин с беременностью и родами |
• Наличие увеличенных наружных геморроидальных узлов. • Выделение крови из заднего прохода с источником, локализующимся в области внутренних геморроидальных узлов. • Наличие выпавших или выпадающих при натуживании внутренних геморроидальных узлов мягкоэластической консистенции. • Наличие плотного геморроидального узла(ов) синюшного цвета с наличием или без воспалительных изменений окружающих мягких тканей, эрозий слизистой оболочки в области узла |
Осмотр врачом-колопроктологом. Пациента осматривают на гинекологическом кресле в положении на спине с максимально приведенными к животу ногами или в коленно-локтевом положении. У соматически тяжелых больных осмотр производят в положении на боку. При наружном осмотре области промежности и заднего прохода обращают внимание на форму ануса, его зияние, наличие рубцовых изменений и деформации, состояние кожных покровов. Определяют выраженность наружных геморроидальных узлов, степень выпадения внутренних узлов и возможность их самостоятельного вправления в анальный канал (УД 5, СР D [1, 4, 9]).
Оценка анального рефлекса. Выполняют штриховое раздражение кожи перианальной области для определения рефлекторных сокращений анального сфинктера.
Пальцевое обследование прямой кишки. Определяют тоническое состояние анального сфинктера и силу волевых сокращений, болезненность при исследовании, наличие дефектов слизистой оболочки анального канала, объемных образований анального канала и прямой кишки (УД 5, СР D [1, 4, 9]).
Аноскопия. Осматривают анальный канал и дистальную часть прямой кишки, оценивают расположение и степень выраженности внутренних геморроидальных узлов, состояние слизистой оболочки, покрывающей внутренние геморроидальные узлы, зубчатую линию с анальными криптами, состояние слизистой оболочки нижнеампулярного отдела прямой кишки.
Ректороманоскопия (до 25 см). Диагностика сопутствующих заболеваний прямой и сигмовидной кишки.
Колоноскопия и ирригоскопия. Диагностика сопутствующих изменений толстой кишки, исключение воспалительных изменений, характерных для язвенного колита и болезни Крона. Колоноскопия или ирригоскопия показаны с целью исключения новообразований толстой кишки всем пациентам старше 50 лет (УД 1с, СР А [10, 11]).
Исследование функционального состояния ЗАПК (профилометрия, сфинктерометрия, электромиография). Показано перед операцией у больных с изначальными клиническими признаками нарушения функции анального сфинктера.
При наличии сопутствующих заболеваний других органов и систем необходима консультация смежных специалистов.
ДИФФЕРЕНЦИАЛЬНАЯ ДИАГНОСТИКА
Дифференциальная диагностика геморроидальной болезни проводится с другими заболеваниями толстой кишки (табл. 2.5) (УД 5, СР D [4, 12, 13]).
Таблица 2.5. Дифференциальная диагностика геморроя
|
Жалобы |
Возможные заболевания |
|
Аноректальное кровотечение |
Анальная трещина |
|
Злокачественные и доброкачественные опухоли прямой кишки и анального канала | |
|
Выпадение слизистой оболочки прямой кишки | |
|
Выпадение прямой кишки | |
|
Язвенный колит | |
|
Болезнь Крона | |
|
Гемангиома | |
|
Эндометриоз | |
|
Травма прямой кишки | |
|
Солитарная язва прямой кишки | |
|
Выпадение геморроидальных узлов |
Выпадение слизистой оболочки прямой кишки |
|
Выпадение прямой кишки | |
|
Фиброзные анальные полипы | |
|
Ворсинчатые аденомы прямой кишки | |
|
Выраженный болевой синдром в анальном канале |
Трещина анального канала |
|
Острый и хронический парапроктит | |
|
Опухоли анального канала | |
|
Осложненные каудальные тератомы | |
|
Болезнь Крона, осложненная перианальными поражениями |
Табл. 2.5. Окончание
|
Жалобы |
Возможные заболевания |
|
|
Идиопатический анокопчиковый болевой синдром |
|
Эндометриоз | |
|
Прокталгия | |
|
Анальный зуд |
Выпадение прямой кишки |
|
Недостаточность анального сфинктера | |
|
Сахарный диабет | |
|
Ворсинчатая опухоль прямой кишки | |
|
Хронический парапроктит | |
|
Идиопатический анальный зуд | |
|
Злокачественная опухоль прямой кишки | |
|
Болезнь Крона | |
|
Грибковые заболевания анального канала и промежности | |
|
Гельминтоз | |
|
Аллергический дерматит | |
|
Контактный дерматит (на местные препараты) | |
|
Псориаз | |
|
Недостаточная гигиена области промежности | |
|
Слизистые или гнойные выделения из анального канала |
Выпадение прямой кишки |
|
Солитарная язва прямой кишки | |
|
Остроконечные перианальные кондиломы | |
|
Анальная трещина | |
|
Злокачественная опухоль анального канала и прямой кишки | |
|
Ворсинчатая опухоль прямой кишки | |
|
Синдром раздраженной толстой кишки | |
|
Воспалительные заболевания толстой кишки (болезнь Крона, язвенный колит) | |
|
Отек перианальной кожи |
Острый парапроктит |
|
Остроконечные кондиломы | |
|
Опухоли анального канала и прямой кишки с перифокальным воспалением | |
|
Диарея | |
|
Пиодермия промежности |
КОНСЕРВАТИВНОЕ ЛЕЧЕНИЕ
Лечение
Основной метод консервативной коррекции геморроидальных симптомов — нормализация деятельности ЖКТ и устранение запора с помощью потребления адекватного количества жидкости и пищевых волокон (УД 2b, СР В [14–17]).
В качестве источника пищевых волокон в нашей стране традиционно применяют пшеничные отруби, морскую капусту и льняное семя в их природном виде или в форме фармакологических препаратов. Также применяют семена и шелуху подорожника, обладающих высокой водоудерживающей способностью, что позволяет избегать натуживания при дефекации (УД 2b, СР В [15–18]). Однако только консервативная терапия, направленная на нормализацию деятельности желудочно-кишечного тракта, не является самостоятельным эффективным методом лечения геморроя, особенно при 3–4-й стадии (УД 2b, СР В [15–18]).
Фармакотерапия острого и хронического геморроя преследует следующие цели (УД 5, СР D [4, 9, 18–20]):
n купирование симптомов острого геморроя;
n предотвращение осложнений;
n профилактику обострений при хроническом течении;
n подготовку больного к операции;
n послеоперационную реабилитацию.
При болевом синдроме показано применение ненаркотических анальгетиков и местных комбинированных обезболивающих препаратов в виде гелей, кремов, мазей и суппозиториев (проктозан, ауробин, ультрапрокт, лидокаин/трибенозид (прокто-гливенол♠), постеризан, бензокаин (релиф адванс♠). При тромбозе геморроидальных узлов показано применение антикоагулянтов местного действия (мазевые основы, содержащие гепарин натрия, мазь с троксерутином).
При тромбозе геморроидальных узлов, осложненном воспалением окружающих мягких тканей (в случае если исключен гнойно-воспалительный процесс), показано использование комбинированных препаратов, содержащих обезболивающие, тромболитические и противовоспалительные компоненты, а также комбинированных флеботонических препаратов [очищенная микронизированная флавоноидная фракция (детралекс♠1)]. Для купирования воспаления и обезболивания применяют топические препараты и нестероидные противовоспалительные средства с комбинированным действием.
1 Торговое наименование Детралекс, компания-производитель Les Laboratoires Servier (Франция). Очищенная микронизированная флавоноидная фракция 500 мг, в том числе диосмин (90%) 450 мг, флавоноиды в пересчете на гесперидин (10%) 50 мг № 30, № 60.
Рекомендуемая доза при остром геморрое – 6 таблеток /сутки (по 3 таблетки утром и 3 таблетки вечером) в течение 4 дней, затем по 4 таблетки в сутки (по 2 таблетки утром и 2 таблетки вечером) в течение последующих 3 дней, далее по 2 таблетки в день до 2 месяцев для предотвращения рецидивов.
При геморроидальных кровотечениях возможно использование местных гемостатических препаратов в виде суппозиториев (натрия альгинат, фенилэфрин1, свечи, содержащие эпинефрин, а также системных гемостатических препаратов и комбинированных флеботонических препаратов [очищенная микронизированная флавоноидная фракция (детралекс♠)].
МАЛОИНВАЗИВНЫЕ ХИРУРГИЧЕСКИЕ МЕТОДЫ
Большинству пациентов с внутренним геморроем 1–3-й стадии при неэффективности или недостаточной эффективности консервативной терапии показано выполнение малоинвазивных хирургических методов лечения: склеротерапия, инфракрасная фотокоагуляция, лигирование геморроидальных узлов латексными кольцами, дезартеризация геморроидальных узлов под контролем ультразвуковой допплерометрии, дезартеризация геморроидальных узлов с мукопексией (УД 1a, СР В [5, 13, 21–36]).
Малоинвазивные хирургические методы лечения направлены на уменьшение кровотока в геморроидальных узлах, уменьшение объема узлов и фиксации их к стенке кишки. Метод лечения подбирается индивидуально для каждого пациента исходя из ведущих симптомов геморроя.
Склерозирование внутренних геморроидальных узлов
Показания: метод может применяться при 1–3-й стадии кровоточащего геморроя; наибольшая эффективность метода отмечается при кровоточащем геморрое 1–2-й стадии. Также возможно использование метода для остановки кровотечений у пациентов с любой стадией геморроя в случае осложнения заболевания развитием постгеморрагической анемии средней и тяжелой степени (УД 1b, СР В [27, 29–31, 37–39]).
Противопоказания для склерозирования внутренних узлов — острый геморрой, острый парапроктит, анальная трещина.
Методика. После визуализации внутренних геморроидальных узлов
с помощью аноскопа производят инъекцию склерозирующего раствора в ткань внутренних геморроидальных узлов с помощью иглы, согнутой под углом 45°. Иглу вводят на глубину 1,0–1,5 см до ощущения «проваливания». В зависимости от размеров геморроидального узла объем вводимого препарата составляет от 0,5 до 3,0 мл.
Наиболее часто в качестве склерозирующих препаратов используют склерозанты из группы детергентов: натрия тетрадецилсульфат (фибровейн♠ 0,5–3%), лауромакрогол 400 (этоксисклерол♠ 1–3%).
Эффективность данного метода составляет 75–89%. Послеоперационный период характеризуется низкой интенсивностью или полным отсутствием болевого синдрома (УД 1b, СР В [27, 29, 30, 38, 39]).
 |
1 Торговое наименование РЕЛИФ (RELIEF) МНН Фенилэфрин, ФОРМА ВЫПУСКА: суппозитории ректальные, 5 мг. Мазь для ректального и наружного применения, 0,25%, 28,4 г. Компания-производитель Байер.
Инфракрасная фотокоагуляция геморроидальных узлов
Показания. Методика показана при кровоточащем геморрое 1–2-й стадии (УД 1b, СР В [40, 41]).
Противопоказания. Воспалительные заболевания аноректальной области и промежности.
Методика. С помощью световода производят коагуляцияю ножки геморроидального узла под действием теплового потока, создаваемого инфракрасным сфокусированным лучом, направляемым к геморроидальному узлу. Перемещая световод на 45° вправо и влево, производят коагуляцию в 3–4 точках в области ножки узла, оставляя между ними промежутки свободной слизистой оболочки до 0,5 см. Продолжительность коагуляции в каждой точке зависит от размера узла и составляет от 1 до 3 с.
Эффективность метода — 60–70%. При поздних стадиях заболевания с пролапсом слизистой оболочки нижнеампулярного отдела прямой кишки инфракрасная фотокоагуляция малоэффективна (УД 1b, СР В [32]).
Лигирование геморроидальных узлов латексными кольцами
Показания. Метод наиболее эффективен при 2–3-й стадии геморроя с наличием отдельно расположенных внутренних геморроидальных узлов с четкими границами (УД 1b, СР В [5, 16–28]).
Противопоказанием для данной методики являются циркулярный геморрой, отсутствие четких границ между наружным и внутренним компонентом, анальная трещина, свищи прямой кишки.
Методика. Через аноскоп к внутреннему геморроидальному узлу
подводят вакуумный лигатор, присоединенный к отсосу для создания отрицательного давления. Часть узла, расположенная проксимальнее зубчатой линии, всасывается в трубчатую полость лигатора. После достижения отрицательного давления 0,7–0,8 атм. с помощью спускового механизма на захваченную часть геморроидального узла сбрасываются два латексных кольца с последующим выравниванием давления и удалением лигатора из просвета кишки.
Лигирование латексными кольцами считается эффективным методом малоинвазивного лечения геморроя, имеет низкий процент рецидивов. Однако болевой синдром после лигирования более выражен, чем при склерозировании и инфракрасной коагуляции внутренних геморроидальных узлов (УД 1b, СР В [21, 22]). Кроме того, после данной методики имеется риск возникновения тромбоза наружных геморроидальных узлов, и в редких случаях могут встречаться воспалительные осложнения (УД 5, СР D [42]). При одноэтапном лигировании более 2 геморроидальных узлов увеличивается вероятность возникновения вагусных симптомов (брадикардия, гипотония, коллапс), выраженного болевого синдрома в послеоперационном периоде, а также возрастает риск рецидива симптомов геморроя по сравнению с разделением процедуры на несколько этапов с интервалом 3–4 нед (УД 1b, СР В [23–25]).
Хорошие результаты лечения отмечаются в 65–85% случаев при наблюдении в отдаленном послеоперационном периоде (УД 1b, СР В [26–28]).
ДЕЗАРТЕРИЗАЦИЯ ГЕМОРРОИДАЛЬНЫХ УЗЛОВ ПОД КОНТРОЛЕМ УЛЬТРАЗВУКОВОЙ ДОППЛЕРОМЕТРИИ
Показания. Методика показана при геморрое 2–4-й стадии. Наиболее эффективен метод у больных с 2–3-й стадией заболевания (УД 1b, СР В [40, 41]).
Противопоказания. Воспалительные заболевания аноректальной области и промежности.
Методика. С помощью специального аноскопа с ультразвуковым допплеровским датчиком определяют расположение терминальных ветвей верхней прямокишечной артерии по условному циферблату. Через окно аноскопа производят прошивание и перевязку выявленных ветвей верхней прямокишечной артерии в нижнеампулярном отделе прямой кишки, на уровне 2–4 см выше аноректальной линии. Как правило, во время операции выполняют перевязку от 3 до 6 артерий (УД 1а, СР В [33, 43]). Эффективность методики составляет 81% у пациентов со 2–3-й стадией геморроя. После операции не требуется проведение антибактериальной терапии и использование наркотических анальгетиков. Низкая интенсивность послеоперационного болевого синдрома позволяет сократить сроки реабилитации пациентов (УД 1а, СР В [34, 35]).
ДЕЗАРТЕРИЗАЦИЯ ГЕМОРРОИДАЛЬНЫХ УЗЛОВ С МУКОПЕКСИЕЙ
Показания. Методика показана при геморрое 2–4-й стадии. Наиболее эффективен метод у больных со 2–3-й стадией заболевания (УД 3а, СР В [33, 36]).
Противопоказания. Воспалительные заболевания аноректальной области и промежности.
Методика. Данное вмешательство производят с использованием специального оборудования для выполнения фиксации слизистой оболочки нижнеампулярного отдела прямой кишки. После прошивания и перевязки ветвей верхней прямокишечной артерии восьмиобразными швами под контролем допплерометрии в области наиболее выраженного пролапса слизистой оболочки прямой кишки накладывают непрерывный шов от зоны дезартеризации (3–4 см выше зубчатой линии) до уровня, расположенного на 0,5–1,0 см проксимальнее зубчатой линии. Путем завязывания концов нитей производят подтягивание прошитой слизистой оболочки в проксимальном направлении со сдавливанием проксимальной пролабирующей части внутреннего геморроидального узла.
Хорошие результаты отмечаются в 91,8% наблюдений (УД 3а, СР В [4, 44]). После применения данной методики пациенты могут быть выписаны из стационара под динамическое наблюдение в течение 24 ч.
Из возможных осложнений в послеоперационном периоде отмечены боли при дефекации (10%), задержка мочеиспускания (5%), тромбоз наружных геморроидальных узлов (2%). При рецидиве заболевания, сопровождающемся выпадением внутренних геморроидальных узлов, дезартеризация узлов с мукопексией может быть применена повторно.
В настоящее время дезартеризация геморроидальных узлов с мукопексией является наиболее эффективным и безопасным методом лечения больных со 2–3-й стадией геморроя (УД 1b, СР А [33, 36, 44]).
ХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕ
Геморроидэктомия показана пациентам при 3–4-й стадии заболевания с выраженными наружными геморроидальными узлами, при неэффективности или невозможности применения малоинвазивных хирургических методов (УД 1a, СР В [1, 4, 7, 16, 21, 45–59]).
Геморроидэктомия остается одним из самых эффективных методов лечения геморроя (УД 1а, СР А [21]). В то же время после операции необходим длительный период реабилитации, и отмечается достаточно высокая частота осложнений, практически не встречающихся после других методик. Наиболее часто используют открытую и закрытую геморроидэктомию, которая может выполняться с помощью хирургического скальпеля, диатермокоагуляции, лазера или ультразвуковых ножниц. Ни один из видов геморроидэктомии не имеет существенного преимущества над другими (УД 1a, СР В [45–49]).
Закрытая геморроидэктомия (с восстановлением слизистой оболочки анального канала)
Закрытая геморроидэктомия применяется при отсутствии четких границ между наружным и внутренним геморроидальными узлами (УД 1b, СР В [13, 60, 61]).
Из осложнений наиболее часто встречаются признаки анальной инконтиненции (8,5%), стриктуры анального канала (2%), кровотечения в послеоперационном периоде (2,7%), запор (4%).
Методика. На основание внутреннего геморроидального узла, выше зубчатой линии, накладывают зажим Бильрота. Отсекают геморроидальный узел до сосудистой ножки с последующим ее прошиванием и перевязыванием. Узел отсекают дистальнее места перевязки сосудистой ножки. Рану ушивают с захватом краев и дна отдельными узловыми швами или непрерывным швом рассасывающейся нитью (викрил рапид 3-0, софил 3-0, кетгут 3-0). Наружный геморроидальный узел иссекают единым блоком с внутренним узлом или отдельно. Рану также ушивают отдельными швами рассасывающейся нитью.
Открытая геморроидэктомия
Открытая геморроидэктомия применяется у пациентов с 3–4-й стадией заболевания как отдельный метод, а также в случаях сочетания геморроя с наличием воспалительных заболеваний анального канала (анальная трещина, свищ прямой кишки) (УД 1b, СР В [13, 49, 60–61]).
Из осложнений наиболее часто встречаются анальная инконтиненция (8%), острая задержка мочеиспускания (1%), кровотечения в раннем послеоперационном периоде (2%).
Методика. Внутренний геморроидальный узел отсекают до сосудистой ножки с последующим ее прошиванием и перевязыванием. Узел отсекают дистальнее места перевязки сосудистой ножки. Достигается тщательный гемостаз. Рану не ушивают. Наружный геморроидальный узел иссекают единым блоком с внутренним узлом или отдельно.
Подслизистая геморроидэктомия
Методика позволяет без деформации и натяжения полностью восстановить слизистую оболочку анального канала и прямой кишки с подслизистым расположением культи узла (УД 5, СР D [1, 4, 62]).
В связи с повышенной кровоточивостью тканей при подслизистом выделении кавернозной ткани операция сопровождается техническими сложностями (УД 5, СР D [1]).
Наиболее частыми осложнениями данного варианта геморроидэктомии являются рефлекторная задержка мочеиспускания (6%), кровотечение из ран анального канала в раннем послеоперационном периоде (1,5%) (УД 5, СР Д [1, 4]).
Методика. В подслизистый слой, в области внутреннего геморроидального узла, вводят 2–3 мл 0,25% раствора прокаина, создавая гидравлическую подушку. Двумя дугообразными разрезами рассекают слизистую оболочку над узлом с последующим выделением его из окружающих тканей до сосудистой ножки. Затем ножку прошивают и узел отсекают. Слизистую оболочку анального канала восстанавливают отдельными узловыми швами (викрил рапид 3-0, софил 3-0, кетгут 3-0), погрузив культю геморроидального узла в подслизистый слой (УД 5, СР D [18]).
Степлерная геморроидопексия (операция Лонго)
Показанием к применению метода являются геморрой 3–4-й стадии, а также сочетание геморроя с выпадением слизистой оболочки нижнеампулярного отдела прямой кишки.
Цель операции — фиксация и лифтинг внутреннего геморроидального сплетения путем циркулярной резекции слизисто-подслизистого слоя нижнеампулярного отдела прямой кишки сшивающим аппаратом с формированием механического шва, что в дальнейшем препятствует выпадению внутренних геморроидальных узлов (УД 1а, СР А [7, 20, 51– 58, 63–68]). Внутреннее и наружное сплетения в результате степлерной геморроидопексии не удаляются.
В числе осложнений после данной операции в литературе описаны случаи развития ректовагинального свища, свища прямой кишки, стриктуры прямой кишки, кровотечения, флегмоны забрюшинной клетчатки, перфорации прямой кишки (УД 1а, СР А [7, 20, 63–68]).
При степлерной геморроидопексии отмечаются снижение послеоперационного болевого синдрома и более короткий срок реабилитации пациента по сравнению с традиционной геморроидэктомией.
Однако процент послеоперационных осложнений как при степлерной геморроидопексии, так и при традиционной геморроидэктомии (открытая и закрытая) примерно одинаков (УД 1а, СР А [7, 51–57, 69]).
При сравнении результатов степлерной геморроидопексии и лигирования геморроидальных узлов латексными кольцами отмечено, что болевой синдром в послеоперационном периоде выражен сильнее после геморроидопексии (УД 5, СР Д [70]).
Методика. Данное вмешательство производят с использованием специального комплекта.
Операцию начинают с введения в анальный канал прозрачного аноскопа, с помощью которого возможен контроль расположения зубчатой линии. Зубчатая линия служит ориентиром при выборе высоты формирования кисетного шва. Через аноскоп, на расстоянии 4–5 см от зубчатой линии, накладывают кисетный шов. Шов начинают с проекции 3 ч и накладывают с захватом слизистой оболочки и подслизистого слоя кишечной стенки. Вращая аноскоп, производят наложение непрерывного кисетного шва по всей окружности нижнеампулярного отдела прямой кишки с расстоянием между стежками от 0,5 до 1,0 см. После извлечения аноскопа вводят головку циркулярного степлера выше наложенного кисетного шва с последующим затягиванием кисета на стержне аппарата. При этом слизистая оболочка должна плотно сомкнуться вокруг штока аппарата.
Концы нитей протягивают через латеральные отверстия, расположенные в основании циркулярного аппарата, и фиксируют снаружи. Головку сближают с основанием аппарата и производят резекцию циркулярного участка слизисто-подслизистого слоя нижнеампулярного отдела прямой кишки с формированием двухрядного скобочного шва.
Геморроидэктомия аппаратами LigaSure, UltraCision (уровень доказательности 1а, степень рекомендации А [4, 47, 59, 71–73])
Применение этих методик при геморрое 3–4-й стадии позволяет значительно уменьшить интенсивность и продолжительность болевого синдрома, сократить сроки реабилитации пациентов, существенно уменьшить частоту дизурических расстройств (УД 1а, СР А [71, 72]). Хороших результатов удается добиться у 96,4% оперированных пациентов.
n После геморроидэктомии аппаратом LigaSure отмечается значительное снижение болевого синдрома, особенно в первые сутки после операции, уменьшение объема интраоперационной кровопотери. Длительность операции сокращается до 9–15 мин. После данного метода геморроидэктомии отмечается сокращение сроков реабилитации пациентов.
n В случае преждевременного расхождения краев ран (на 3–6-й день после операции) после геморроидэктомии аппаратом LigaSure отмечается более длительное заживление раневых поверхностей.
n По сравнению с другими методами хирургического лечения геморроидэктомия аппаратом LigaSure не имеет существенных преимуществ при оценке частоты осложнений (кровотечение в раннем послеоперационном периоде, анальная инконтиненция, стриктура анального канала) (УД 1a, СР A [59, 73]).
Методика геморроидэктомии аппаратом LigaSure. Внутренний геморроидальный узел захватывают зажимом Люэра с последующим прошиванием сосудистой ножки. На основание узла по направлению снаружи внутрь накладывают бранши коагуляционного зажима LigaSure с дальнейшей коагуляцией. По наружному краю коагуляционного слоя узел отсекают ножницами до сосудистой ножки. Коагуляцию сосудистой ножки аппаратом выполняют дважды с перемещением бранш прибора без оставления промежутка между коагулированными участками. Затем по наружному краю коагуляционного слоя ножницами производят пересечение сосудистой ножки, узел удаляется.
Методика геморроидэктомии аппаратом UltraСision. Производят рас-
сечение тканей в области основания наружного геморроидального узла ультразвуковыми ножницами в режиме резания. Затем поэтапно удаляют наружный и внутренний компонент единым блоком до полного пересечения. Обработку сосудистой ножки производят в режиме коагуляции (УД 1а, СР А [34]).
ЛЕЧЕНИЕ ОСТРОГО ГЕМОРРОЯ
Лечение острого тромбоза наружных геморроидальных узлов включает как динамическое наблюдение c проведением комплексной консервативной терапии (см. раздел «Консервативное лечение»), так и хирургическую коррекцию (УД 4, СР В [1, 4, 70]).
Показанием к хирургическому лечению служит острый тромбоз геморроидального узла (ов) в случае, если сроки с момента начала заболевания составляют 48–72 ч. Во время операции производят либо удаление тромботических масс из геморроидального узла (тромбэктомия), либо иссечение тромбированного геморроидального узла. Операция может быть выполнена как в амбулаторных условиях, так и в стационаре.
n Выполнение тромбэктомии или иссечения тромбированного узла(ов) в течение 48–72 ч от начала заболевания приводит к сокращению сроков реабилитации пациентов (УД 4, СР В [70]).
n Хирургическое лечение в условиях стационара показано при больших размерах тромбированного геморроидального узла, распространении воспалительного процесса на дистальную часть анального канала и ткани перианальной области.
n При тромбозе геморроидальных узлов, в случае, когда сроки от начала заболевания превышают 72 ч, показана консервативная терапия, направленная на купирование болевого синдрома и воспалительного процесса с последующим плановым хирургическим лечением.
Чего нельзя делать (УД 5, СР D [4])
n Не следует выполнять хирургическое лечение геморроя без обследования толстой кишки.
n Не следует применять малоинвазивные методы лечения при циркулярном геморрое и сливном характере наружных и внутренних узлов.
n Не следует выполнять малоинвазивные методы хирургического лечения при наличии гнойно-воспалительного процесса в параректальных тканях.
n Не следует выполнять радикальные операции у больных со 2–3-й степенью анемии.
Дальнейшее ведение
n В послеоперационном периоде до момента заживления ран пациентам требуется производить регулярную санацию анальной области с использованием сидячих ванночек со слабым раствором перманганата калия или ромашки, а также выполнять ежедневные перевязки с использованием мазевых основ, обладающих противовоспалительным и ранозаживляющим действием (УД 5, СР D [4, 9]).
n Необходим еженедельный врачебный контроль за течением раневого процесса до полного заживления ран (УД 5, СР D [4, 9]).
n На период заживления ран требуются соблюдение диеты, богатой растительной клетчаткой, прием пищевых волокон для смягчения стула (УД 5, СР D [4, 9, 18]).
Профилактика
Основополагающим в профилактике развития геморроя являются нормализация деятельности желудочно-кишечного тракта, устранение запора, соблюдение гигиенического режима. При появлении симптомов, характерных для геморроя, необходима консультация колопроктолога. Своевременная диагностика и лечение заболевания на ранних стадиях могут значительно улучшить прогноз и уменьшить вероятность развития осложнений (УД 5, СР Д [4, 9, 13]).
Прогноз
Дифференцированный подход к выбору метода лечения геморроя в зависимости от стадии заболевания, применение малоинвазивных способов лечения позволяют достичь хороших результатов у 98–100% пациентов.
Критерии оценки качества помощи в стационаре представлены в таблице 2.6 Для оценки качества медицинской помощи используют временные, процессуальные и профилактирующие критерии. Временные характеризуют своевременность оказания определенных этапов медицинской помощи. Выполнение пациенту ряда медицинских манипуляций, инструментальных и лабораторных исследований, необходимых для качественного оказания медицинской помощи, оценивают в процессуальных критериях. Для анализа мероприятий, направленных на предотвращение развития осложнений, используют профилактирующие критерии.
Таблица 2.6. Критерии оценки качества медицинской помощи в стационаре больным с доброкачественными заболеваниями прямой кишки и анального канала (геморрой) (0 — нет, 1 — да)
|
Клинические рекомендации |
Временные |
Процессуальные |
Профилактирующие |
|
Клинические рекомендации по диагностике и лечению взрослых пациентов с острым и хроническим геморроем (код МКБ — I84: I84.0; I84.1; I84.2; I84.3; I84.4; I84.5; I84.6; I84.7; I84.8; I84.9) |
Установка клинического диагноза в течение 72 ч: 0/1 |
Оценка анального рефлекса: 0/1. Пальцевое обследование прямой кишки: 0/1. Аноскопия: 0/1. Ректороманоскопия: 0/1. Определение группы крови: 0/1. Исследование крови на сифилис, вирусный гепатит В, вирусный гепатит С: 0/1. Клинический анализ крови; биохимический анализ крови; клинический анализ мочи; коагулограмма: 0/1. Метод оперативного лечения в соответствии с клиническими рекомендациями: 0/1. Метод анестезии в соответствии с объемом оперативного лечения: 0/1 |
Отсутствие осложнений: • кровотечение: 0/1; • абсцесс: 0/1; • флегмона: 0/1; • пневмония: 0/1; • тромбоэмболия: 0/1; • летальный исход: 0/1 |
Литература
1. Шелыгин Ю.А., Благодарный Л.А. Справочник колопроктолога. — М.: Литтерра, 2012. — С. 64–89.
2. Phillips B., Ball C., Sackett D. et al. Oxford Center for Evidence-Based Medicine — Levels of Evidence. — 2009. — Available from: http://www.cebm.net/ oxford-centre-evidence-based-medicine-levels-evidence-march-2009.
3. Hoffmann J.C., Fischer I., Höhne W. et al. Methodische Grundlagen für die
Ableitung von Konsensusempfehlungen [Methodological basis for the development of consensus recommendations] // Z. Gastroenterol. — 2004. — Vol. 42, N 9. — P. 984–986.
4. Воробьев Г.И., Шелыгин Ю.А., Благодарный Л.А. Геморрой. — М.: Литтерра, 2010. — С. 38–40, 114–116, 137–138, 154–183.
5. Генри М., Свош М. Колопроктология и тазовое дно. — М.: Медицина, 1988. — С. 232–255.
6. Международная классификация болезней 10-го пересмотра. МКБ-10. Доступен с сайта: www.10mkb.ru.
7. Sutherland L.M., Burchard A.K., Matsuda K. et al. A systematic review of stapled hemorrhoidectomy // Arch. Surg. — 2002. — Vol. 137. — P. 1395–406.
8. Fazio F.W., Tjandra J.J. The management of perianal diseases // Adv. Surg. — 1996. — Vol. 29. — P. 59–78.
9. Воробьев Г.И. Основы колопроктологии. — М.: МИА, 2006. — С. 79–82, 94.
10. Church J.M. Analysis of the colonoscopic findings in patients with rectal bleeding according to the pattern of their presenting symptoms // Dis. Colon Rectum. — 1991. — Vol. 34. — P. 391–395.
11. Rex D.K., Bond J.H., Winawer S. et al. Quality in the technical performance
of colonoscopy and the continuous quality improvement process for colonoscopy: recommendations of the U.S. Multi-Society Task Force on colorectal cancer // Am. J. Gastroenterol. — 2002. — Vol. 97. — P. 1296–308.
12. Laurence R., Dana R. Ambulatory Colorectal Surgery. — N.Y.: Informa, 2009. — P. 79–85.
13. Marvin L., Corman M.D. Colon and Rectal Surgery. — Philadelphia: Lippincott, 2005. — P. 177–255.
14. The American Society of Colon and Rectal Surgeons. Practice Parameters for the Management of Hemorrhoids // Dis. Colon Rectum. — 2005. — Vol. 48. — P. 189–194.
15. Webster D.J., Gough D.C., Craven J.L. The use of bulky evacuants in patients with haemorrhoids // Br. J. Surg. — 1978. — Vol. 65. — P. 291.
16. Moesgaard F., Nielsen M.C., Hansen J.B., Knudsen J.T. High fiber diet reduces bleeding and pain in patients with hemorrhoids // Dis. Colon Rectum. — 1982. — Vol. 25. — P. 454–456.
17. Keighley M.R., Buchmann P., Minervium S. et al. Prospective trials of minor
surgical procedures and high fibre diet for haemorrhoids // BMJ. — 1997. — Vol. 2. — P. 967–96.
18. Salvati E.P. Nonoperative management of hemorrhoids // Dis. Colon Rectum. — 1999. — Vol. 42. — P. 989–993.
19. Perera N., Liolitsa D., Iype S. et al. Phlebotonics for haemorrhoids // The Cochrane Collaboration. — 2012.
20. Cheetham M.J., Mortensen N.J., Nystrom P.O. et al. Persistent pain and faecal urgency after stapled haemorrhoidectomy // Lancet. — 2000. — Vol. 356. — P. 730–733.
21. MacRae H.M., McLeod R.S. Comparison of hemorrhoidal treatment modalities: a meta-analysis // Dis. Colon Rectum. — 1995. — Vol. 38. — P. 687– 694.
22. MacRae H.M., McLeod R.S. Comparison of hemorrhoidal treatments: a
meta-analysis // Can. J. Surg. — 1997. — Vol. 40. — P. 14–17.
23. Lee H.H., Spencer R.J., Beart R.W. Multiple hemorrhoidal banding in a single session // Dis. Colon Rectum. — 1994. — Vol. 37. — P. 37–41.
24. Chaleoykitti B. Comparative study between multiple and single rubber band ligation in one session for bleeding internal hemorrhoids: a prospective study // J. Med. Assoc. Thai. — 2002. — Vol. 85. — P. 345–350.
25. Armstrong D.N. Multiple hemorrhoidal ligation: a prospective, randomized
trial evaluating a new technique // Dis. Colon Rectum. — 2003. — Vol. 46. — P. 179–186.
26. Bat L., Melzer E., Koler M. et al. Complications of rubber band ligation of symptomatic internal hemorrhoids // Dis. Colon Rectum. — 1993. — Vol. 36. — P. 287–290.
27. Johanson J.F., Rimm A. Optimal nonsurgical treatment of hemorrhoids: a
comparative analysis of infrared coagulation, rubber band ligation, and injection sclerotherapy // Am. J. Gastroenterol. — 1992. — Vol. 87. — P. 1601–1605.
28. Savoiz D., Roche B., Glauser T. et al. Rubber band ligation of hemorrhoids: relapse as a function of time // Int. J. Colorectal Dis. — 1998. — Vol. 13. — P. 154–156.
29. Sim A.J., Murie J.A., Mackenzie I. Three-year follow-up study on the
treatment of firstand second-degree hemorrhoids by sclerosant injection or rubber band ligation // Surg. Gynecol. Obstet. — 1983. — Vol. 157. — P. 534–536.
30. Chew S.S., Marshall L., Kalish L. et al. Short-term and long-term results of combined sclerotherapy and rubber band ligation of hemorrhoids and mucosal prolapse // Dis. Colon Rectum. — 2003. — Vol. 46. — P. 1232–1237.
31. Kanellos I., Goulimaris I., Christoforidis E. et al. A comparison of
the simultaneous application of sclerotherapy and rubber band ligation, with sclerotherapy and rubber band ligation applied separately, for the treatment of haemorrhoids: a prospective randomized trial // Colorectal Dis. — 2003. — Vol. 5. — P. 133–138.
32. Templeton J.L., Spence R.A., Kennedy T.L. et al. Comparison of infrared coagulation and rubber band ligation for first and second degree haemorrhoids: a randomised prospective clinical trial // BMJ (Clin. Res. Ed.). — 1983. — Vol. 286. — P. 1387–1389.
33. Ratto C., Donisi L., Parello A. et al. Distal Doppler-guided dearterialization’
is highly effective in treating haemorrhoids by transanal haemorrhoidal dearterialization // Colorectal Dis. — 2012. — Vol. 14. — P. 786–789.
34. Ratto C., Donisi L., Parello A. et al. Evaluation of transanal hemorrhoidal dearterialization as aminimally invasive therapeutic approach to hemorrhoids // Dis. Colon Rectum. — 2010. — Vol. 53. — P. 803–811.
35. Zampieri N., Castellani R., Andreoli R., Geccherle A. Long-term results
and quality of life in patients treated with hemorrhoidectomy using two different techniques: Ligasure versus transanal hemorrhoidal dearterialization // Am. J. Surg. — 2012. — Vol. 204. — P. 684–688.
36. Lienert M., Ulrich B. Doppler-guided ligation of the hemorrhoidal arteries. Report of experiences with 248 patients // Dtsch. Med. Wochenschr. — 2004. — Vol. 129. — P. 947–950.
37. Andrews E. The treatment of hemorrhoids by injection // Med. Rec. —
1879. — Vol. 15. — P. 451.
38. Terrell E.H. The treatment of hemorrhoids by a new method // Trans. Am. Proctol. Soc. — 1916. — 65 p.
39. Фролов С.А., Благодарный Л.А., Костарев И.В. Склеротерапия детергентами — метод выбора лечения больных кровоточащим геморроем, осложненным анемией // Колопроктология. — 2011. — Т. 36, № 2. — С. 23–27.
40. Leicester R.J., Nicholls R.J., Mann C.V. Comparison of infrared coagulation
with conventional methods and the treatment of hemorrhoids // Coloproctology. — 1981. — Vol. 5. — P. 313.
41. Leicester R.J., Nicholls R.J., Mann C.V. Infrared coagulation: a new treatment for hemorrhoids // Dis. Colon Rectum. — 1981. — Vol. 24. — P. 602.
42. Quevado-Bonilla G., Farkas A.M., Abcarian H. et al. Septic complications of hemorrhoidal banding // Arch. Surg. — 1988. — Vol. 123. — P. 650.
43. Sohn N., Aronoff J.S., Cohen F.S. et al. Transanal hemorrhoidal dearterialization is an alternative to operative hemorrhoidectomy // Am. J. Surg. — 2001. — Vol. 182. — P. 515–519.
44. Загрядский Е.А., Горелов С.И. Трансанальная допплер-контролируемая
дезартеризация в сочетании с мукопексией в лечении геморроя 3–4 стадии // Колопроктология. — 2010. — Т. 32, № 2. — С. 8–14.
45. Thorbeck C.V., Montes M.F. Haemorrhoidectomy: randomised controlled clinical trial of ligasure compared with Milligan-Morgan operation // Eur. J. Surg. — 2002. — Vol. 168. — P. 48–54.
46. Chung C.C., Ha J.P., Tai Y.P. et al. Double-blind, randomized trial comparing
harmonic scalpel hemorrhoidectomy, bipolar scissors hemorrhoidectomy, and scissors excision: ligation technique // Dis. Colon Rectum. — 2002. — Vol. 45. — P. 789–94.
47. Armstrong D.N., Frankum C., Schertzer M.E. et al. Harmonic scalpel hemorrhoidectomy: five hundred consecutive cases // Dis. Colon Rectum. — 2002. — Vol. 45. — P. 354–359.
48. Khan S., Pawlak S.E., Eggenberger J.C. et al. Surgical treatment of hemorrhoids:
prospective, randomized trial comparing closed excisional hemorrhoidectomy and the harmonic scalpel technique of excisional hemorrhoidectomy // Dis. Colon Rectum. — 2001. — Vol. 44. — P. 845–849.
49. Arbman G., Krook H., Haapaniemi S. Closed vs open hemorrhoidectomy — is there any difference? // Dis. Colon Rectum. — 2000. — Vol. 43. — P. 31–34.
50. Tan J.J., Seow-Choen F. Prospective, randomized trial comparing diathermy and harmonic scalpel hemorrhoidectomy // Dis. Colon Rectum. — 2001. — Vol. 44. — P. 677–679.
51. Ho Y.H., Cheong W.K., Tsangg C. et al. Stapled hemorrhoidectomy — cost
and effectiveness. Randomized, controlled trial including incontinence scoring, anorectal manometry, and endoanal ultrasound assessments at up to three months // Dis. Colon Rectum. — 2000. — Vol. 43. — P. 1666–1675.
52. Hetzer F.H., Demartines N., Handschin A.E., Clavien P.A. Stapled vs excision hemorrhoidectomy: long-term results of a prospective randomized trial // Arch. Surg. — 2002. — Vol. 137. — P. 337–340.
53. Mehigan B.J., Monson J.R., Hartley J.E. Stapling procedure for haemorrhoids versus Milligan-Morgan haemorrhoidectomy: randomised controlled trial // Lancet. — 2001. — Vol. 355. — P. 782–785.
54. Pope V., Doran H., Fearn S. et al. Randomized, controlled trial comparing
quality of life after open hemorrhoidectomy plus stapled anopexy [meeting abstract] // Dis. Colon Rectum. — 2001. — Vol. 44. — P. A8.
55. Shalaby R., Desoky A. Randomized clinical trial of stapled versus MilliganMorgan haemorrhoidectomy // Br. J. Surg. — 2001. — Vol. 88. — P. 1049–1053.
56. Ganio E., Altomare D.F., Gabrielli F. et al. Prospective randomized multicentre trial comparing stapled with open haemorrhoidectomy // Br. J. Surg. — 2001. — Vol. 88. — P. 669–674.
57. Senagore A.J., Singer M., Abcarian H. et al. A prospective, randomized,
controlled trial comparing stapled hemorrhoidopexy and Ferguson hemorrhoidectomy: perioperative and one-year results // Dis. Colon Rectum. — 2004. — Vol. 47. — P. 1824–1836.
58. Peng B.C., Jayne D.G., Ho Y.H. Randomized trial of rubber band ligation vs. stapled hemorrhoidectomy for prolapsed piles // Dis. Colon Rectum. — 2003. — Vol. 46. — P. 291–297.
59. Simon W. Nienhuijs, Ignace H.J.T de Hingh. Conventional versus Ligasure
hemorrhoidectomy for patients with symptomatic hemorrhoids // The Cochrane Collaboration. — 2011.
60. Хмылов Л.М., Титов А.Ю., Капуллер Л.Л. и др. Сравнительная характеристика течения раневого процесса и послеоперационного периода у больных, перенесших геморроидэктомию ультразвуковым скальпелем и традиционными способами // Колопроктология. — 2004. — Т. 8, № 2. — С. 14–20.
61. Andrews B.T., Layer G.T., Jackson B.T., Nicholls R.J. Randomized trial
comparing diathermy hemorrhoidectomy with the scissor dissection MilliganMorgan operation // Dis. Colon Rectum. — 1993. — Vol. 36. — P. 580–583.
62. Parks A.G. Surgical treatment of haemorrhoids // Br. J. Surg. — 1956. — Vol. 43. — P. 337.
63. Pessaux P., Tuech J.J., Laurent B. et al. Morbidity after stapled haemorrhoidectomy: long-term results about 140 patients and review of the literature // Ann. Chir. — 2004. — Vol. 129. — P. 571–577.
64. Oughriss M., Yver R., Faucheron J.L. Complications of stapled
hemorrhoidectomy: a French multicentric study // Gastroenterol. Clin. Biol. — 2005. — Vol. 29. — P. 429–433.
65. Molloy Rg., Kingsmore D. Life-threatening pelvis sepsis after stapled haemorrhoidectomy // Lancet. — 2000. — Vol. 355. — P. 782–578.
66. Pescatori M., Gagliardi G. Postoperative complications after procedure for prolapsed hemorrhoids and stapled transanal rectal resection procedures // Tech. Coloproctol. — 2008. — Vol. 12. — P. 7–19.
67. Wong L.-Y., Jiang J.-K., Chang S.-C. et al. Rectal perforation: a life-
threatening complication of stapled hemorrhoidectomy: report of a case // Dis. Colon Rectum. — 2003. — Vol. 46. — P. 116–117.
68. Pescatori M. Management of post-anopexy rectal stricture // Tech. Coloproctol. — 2002. — Vol. 6. — P. 125–126.
69. Cheetham M.J., Mortensen N.J.M., Nystrom P.-O. et al. Persistent pain and fecal urgency after stapled haemorrhoidectomy // Lancet. — 2000. — Vol. 356. — P. 730–733.
70. Jongen J., Bach S., Stubinger S.H., Bock J.U. Excision of thrombosed external hemorrhoid under local anesthesia: a retrospective evaluation of 340 patients // Dis. Colon Rectum. — 2003. — Vol. 46. — P. 1226–1231.
71. Chung Y.-C., Wu H.-J. Clinical experience of sutureless closed hemorrhoidectomy with Ligasure // Dis. Colon Rectum. — 2003. — Vol. 46. — P. 87–92.
72. Franklin E.J., Seetharam S., Lowney J. et al. Randomized, clinical trial of Ligasure vs conventional diathermy in hemorrhoidectomy // Dis. Colon Rectum. — 2003. — Vol. 46. — 1380 p.
73. Благодарный Л.А., Шелыгин Ю.А., Хмылов Л.А., Соттаева В.Х. Бесшовная геморроидэктомия // Колопроктология. — 2006. — Т. 17, № 3. — С. 8–12.
ЭПИТЕЛИАЛЬНЫЙ КОПЧИКОВЫЙ ХОД
Введение
На протяжении многих лет в центре внимания отечественных и зарубежных колопроктологов остается проблема лечения больных эпителиальным копчиковым ходом (ЭКХ). ЭКХ является довольно частым заболеванием и составляет 1–2% всех хирургических больных. В общей популяции заболевание встречается у 26 на 100 тыс. человек. Актуальность изучения данной патологии объясняется тем, что заболевание проявляется в наиболее активном трудоспособном возрасте, пик заболеваемости приходится на возраст от 15 до 30 лет с преобладанием мужского пола в соотношении 3:1. Несмотря на длительность изучения данной проблемы и множество вариантов оперативных вмешательств, их результаты нельзя назвать полностью удовлетворительными в связи с длительным сроком заживления ран крестцово-копчиковой области, составляющим, по данным литературы, от 14 до 80 сут, высокой частотой рецидивов заболевания от 2 до 40% и послеоперационных осложнений от 2,5 до 53%. Все это приводит к удлинению сроков лечения и нетрудоспособности пациентов и значительному ухудшению качества их жизни [22, 24, 41]. Таким образом, вопросы реабилитации данного контингента пациентов, а также выбора оперативного вмешательства остаются нерешенными до настоящего времени [22, 24, 59].
Рекомендации по диагностике и лечению пациентов с ЭКХ служат ру-
ководством для практических врачей, осуществляющих ведение и лечение таких больных, и подлежат регулярному пересмотру в соответствии с новыми данными научных исследований в этой области.
Рекомендации включают следующие разделы: определение заболевания, классификация, профилактика, диагностика, консервативное и оперативное лечение, правила ведения периоперационного периода, а также прогноз у больных с ЭКХ.
Для отдельных положений рекомендаций приведены уровни доказательности согласно общепринятой классификации Оксфордского центра доказательной медицины [56] (табл. 3.1).
Таблица 3.1. Уровни доказательности и степени рекомендаций на основании руководства Оксфордского центра доказательной медицины
|
Уровень |
Исследования методов диагностики |
Исследования методов лечения |
|
1а |
Систематический обзор гомогенных диагностических исследований 1-го уровня |
Систематический обзор гомогенных РКИ |
|
1b |
Валидизирующее когортное исследование с качественным «золотым стандартом» |
Отдельное РКИ (с узким доверительным интервалом) |
|
1с |
Специфичность или чувствительность столь высокие, что положительный или отрицательный результат позволяет исключить/установить диагноз |
Исследование «Всё или ничего» |
|
2а |
Систематический обзор гомогенных диагностических исследований >2-го уровня |
Систематический обзор (гомогенных) когортных исследований |
|
2b |
Разведочное когортное исследование с качественным «золотым стандартом» |
Отдельное когортное исследование (включая РКИ низкого качества; т.е. с <80% пациентов, прошедших контрольное наблюдение) |
|
2с |
Нет |
Исследование «исходов»; экологические исследования |
|
3а |
Систематический обзор гомогенных исследований уровня 3b и выше |
Систематический обзор гомогенных исследований «случай– контроль» |
|
3b |
Исследование с непоследовательным набором или без проведения исследования «золотого стандарта» у всех испытуемых |
Отдельное исследование «случай–контроль» |
|
4 |
Исследование «случай–контроль» или исследование с некачественным или независимым «золотым стандартом» |
Серия случаев (и когортные исследования или исследования «случай–контроль» низкого качества) |
|
5 |
Мнение экспертов без тщательной критической оценки или основанное на физиологии, лабораторных исследованиях на животных или разработка «первых принципов» |
Мнение экспертов без тщательной критической оценки, лабораторные исследования на животных или разработка «первых принципов» |
|
Степень рекомендаций | ||
|
А |
Согласующиеся между собой исследования 1-го уровня | |
|
В |
Согласующиеся между собой исследования 2-го или 3-го уровня или экстраполяция на основе исследований 1-го уровня | |
|
С |
Исследования 4-го уровня или экстраполяция на основе уровня 2 или 3 | |
|
D |
Доказательства 5-го уровня или затруднительные для обобщения или некачественные исследования любого уровня | |
ВАЛИДИЗАЦИЯ РЕКОМЕНДАЦИЙ
Настоящие рекомендации составлены Общероссийской общественной организацией «Ассоциация колопроктологов России», и в предварительной версии были рецензированы независимыми экспертами, которых попросили прокомментировать прежде всего, насколько интерпретация доказательств, лежащих в основе рекомендаций, доступна для понимания. Получены комментарии со стороны врачей амбулаторного звена, комментарии тщательно систематизировались и обсуждались на совещаниях экспертной группы.
Последние изменения в настоящих рекомендациях были представлены для дискуссии на заседании профильной комиссии «Колопроктология» Экспертного совета Минздрава России 12 сентября 2013 г. Проект рекомендаций был повторно рецензирован независимыми экспертами и врачами амбулаторного звена. Для окончательной редакции и контроля качества рекомендации были повторно проанализированы членами экспертной группы, которые пришли к заключению, что все замечания и комментарии приняты во внимание, риск систематических ошибок при разработке рекомендаций сведен к минимуму.
ОБЛАСТЬ ПРИМЕНЕНИЯ РЕКОМЕНДАЦИЙ
Данные клинические рекомендации применимы при осуществлении медицинской деятельности в рамках Порядка оказания медицинской помощи взрослому населению с заболеваниями толстой кишки, анального канала и промежности колопроктологического профиля.
Определение
Эпителиальный копчиковый ход представляет собой узкий канал, выстланный эпителием, содержащий волосяные луковицы, сальные железы и открывающийся на коже межъягодичной складки одним или несколькими точечными (первичными) отверстиями [4, 43].
Код по Международной классификации болезней 10-го пересмотра
n Класс: Болезни кожи и подкожной клетчатки (XII).
n Блок: Инфекции кожи и подкожной клетчатки (L00–L08).
n Код:
v L05.0 Пилонидальная киста с абсцессом
v L05.9 Пилонидальная киста без абсцессов
Классификация
Разнобой в результатах лечения и применяемых методов во многом объясняется отсутствием общепринятой классификации. При одном
и том же процессе, называемом по-разному, выполняются различные оперативные вмешательства. Это вносит путаницу в оценку результатов лечения и определение наиболее адекватного оперативного пособия на разных этапах одного и того же заболевания. Кроме того, это влечет за собой не всегда обоснованные действия хирурга при тех или иных проявлениях данной болезни.
Классификация ЭКХ должна отражать развитие заболевания, своеобразие его клинических форм, что позволит четко сформулировать клинический диагноз и избрать наиболее оптимальный способ лечения [4, 8, 43]. Наиболее полной в настоящее время является классификация, предложенная ГНЦ колопроктологии в 1988 г.
n Неосложненный ЭКХ (без клинических проявлений).
n Острое воспаление ЭКХ:
v инфильтративная стадия;
v абсцедирование.
n Хроническое воспаление ЭКХ:
v инфильтративная стадия;
v рецидивирующий абсцесс;
v гнойный свищ.
n Ремиссия воспаления ЭКХ.
Формулировка диагноза
При формулировании диагноза следует отразить стадию заболевания, (см. раздел «Диагностика»). Ниже приведены примеры формулировок диагноза.
n Острое воспаление ЭКХ в стадии абсцедирования.
n Хроническое воспаление ЭКХ в стадии гнойного свища.
Диагностика
Диагностика ЭКХ основана на жалобах больного, степени их выраженности, длительности болезни, анализе результатов клинического и объективного обследования пациента. В преобладающем большинстве случаев для достоверной постановки диагноза достаточно лишь анамнестических данных и осмотра пациента (УД 3b, СР C [1, 2, 4, 17, 67]).
Сбор анамнеза. Выявляются этиологические факторы возникновения заболевания, длительность и характер жалоб, травмы крестцово-копчиковой области в анамнезе, а также наличие нарушения функций тазовых органов (для дифференциальной диагностики с менингоцеле) (УД 3b, СР C [1, 4, 17, 67]).
Осмотр больного проводят в положении больного лежа на животе или в коленно-локтевом положении. При этом оценивают наличие, количество и расположение первичных и вторичных отверстий ЭКХ, состояние кожных покровов перианальной, крестцово-копчиковой об-
ласти и ягодиц. При осмотре промежности и заднего прохода выявляют сопутствующие заболевания в этой области — анальную трещину, геморрой, свищи или выпадение прямой кишки. При пальпации определяют наличие рубцового и воспалительного процесса крестцово-копчиковой области (УД 3b, СР C [2, 4, 42, 43]).
Пальцевое обследование прямой кишки. Проводят всем пациентам независимо от наличия верифицированного диагноза ЭКХ. При этом оценивают область морганиевых крипт, а также состояние крестцовых и копчиковых позвонков (УД 4, СР C [1, 3, 4]).
Ректороманоскопия. Осматривают слизистую оболочку прямой и дистального отдела сигмовидной кишки. Оценивают характер сосудистого рисунка, наличие воспалительных изменений в дистальном отделе толстой кишки (УД 5, СР D [1, 4]).
Фистулография. Применяют только в сложных случаях для проведения дифференциальной диагностики (УД 4, СР D [1, 4]).
Ультразвуковое исследование (УЗИ) крестцово-копчиковой области позволяет оценить локализацию, размеры, структуру патологического очага, наличие дополнительных ходов, степень вовлечения в воспалительный процесс окружающих тканей, подкожной жировой клетчатки, глубину расположения патологического очага от кожных покровов (УД 4, СР C [1, 4]).
Методика. Исследование выполняется на ультразвуковых диагности-
ческих приборах с использованием линейного датчика частотой 10 мгц. Датчиком проводят линейное УЗ-сканирование путем проведения продольных сечений крестцово-копчиковой области (УД 4, СР C [2]).
Лечение
Лечебные мероприятия при ЭКХ зависят от стадии процесса. Радикальное лечение ЭКХ только хирургическое. Острое воспаление требует незамедлительной операции. Хроническое воспаление ЭКХ целесообразно оперировать в плановом порядке (УД 2b, СР A [25, 27, 36, 69]).
Цель — радикальное удаление ЭКХ.
Показания к госпитализации — острое воспаление ЭКХ или госпитализация на плановое оперативное лечение любой стадии процесса.
КОНСЕРВАТИВНОЕ ЛЕЧЕНИЕ
Консервативное лечение используется в основном при хроническом процессе ЭКХ или как подготовка к хирургическому вмешательству. Терапия состоит (УД 3b, СР B [46, 53]):
n из гигиены (частое педантичное мытье и высушивание межъягодичной области);
n бритья (1 раз в неделю, захватывая межъягодичную складку шириной 2 см — от поясничной области до анального канала (УД 4, СР C [6, 57]);
n озонотерапии (гипербарическая оксигенация — насыщение тканей под давлением кислородом, что способствует регенерации пораженных участков);
n криотерапии или диатермии (уничтожение эпителия, выстилающего свищевой ход, с помощью низких или высоких температур).
ХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕ
Вид оперативного вмешательства при ЭКХ зависит от клинической классификации, стадии и распространенности процесса. Тактика хирургического лечения направлена на ликвидацию основного источника воспаления, а именно эпителиального канала со всеми первичными отверстиями, а также воспалительно измененных окружающих тканей и вторичных свищей. При всех способах лечения пациента укладывают в положение на живот со слегка разведенными ногами, что обеспечивает адекватный доступ к межъягодичной складке. В настоящее время применяются следующие операции: иссечение ЭКХ без ушивания раны, иссечение ЭКХ с ушиванием раны наглухо различными методами, операция марсупиализации, пластические операции с выкраиванием кожных лоскутов и подкожное иссечение ЭКХ (синусэктомия) (УД 2b, СР B [30, 37, 39, 69]).
Требования к хирургическим методам лечения эпителиального копчикового хода
Идеальная хирургическая техника должна:
n обеспечить полное излечение ЭКХ с минимальным риском рецидивов;
n быть простой;
n требовать небольших сроков госпитализации;
n давать наименьший риск осложнений;
n гарантировать быстрое восстановление пациента (УД 1b, СР A [8, 27, 39, 48]).
Иссечение эпителиального копчикового хода с ушиванием раны наглухо
Показания. Выполняется пациентам с неосложненным ЭКХ (УД 1b, СР A [7, 50, 68]).
Методика. Пациента укладывают в положение на живот со слегка разведенными ногами, что обеспечивает адекватный доступ к межъягодичной складке. В первичные отверстия вводят краситель (метиленовый синий) для обнаружения всех ответвлений и затеков. Далее с помощью скальпеля или электроножа двумя окаймляющими разрезами ходы иссекаются единым блоком с кожей межъягодичной складки со всеми открывающимися там отверстиями, подкожной клетчаткой, содержащей ходы, до крестцово-копчиковой фасции. Существуют различные способы ушивания полученной при этом раны наглухо (УД 2a, СР A [60]):
n отдельными швами;
n по Донати;
n параллельными п-образными швами.
Противопоказания. Ранее оперированные пациенты с рубцовой деформацией межъягодичной области, инфильтраты в межъягодичной области (УД 4, СР D [26]). Хорошие результаты лечения после операции отмечаются в 58–88% случаев (УД 2a, СР A [63]). Послеоперационные осложнения по различным данным достигают 9–31% (УД 2a, СР A [31, 49]).
Иссечение эпителиального копчикового хода с подшиванием краев раны ко дну. Марсупиализация
Показания. Выполняется в стадии инфильтрата при остром воспалении ЭКХ (УД 1b, СР A [66, 69]).
Методика. С помощью скальпеля или электроножа двумя окаймляющими разрезами ходы иссекаются единым блоком с кожей межъягодичной складки со всеми открывающимися там отверстиями, подкожной клетчаткой, содержащей ходы, до фасции копчика. Далее иссекают заднюю стенку хода и частично верхние участки боковых стенок, после чего кожные края разреза подшивают к поверхности крестца и копчика в шахматном порядке. Швы снимают на 10–12 сут (УД 1b, СР A [54, 55]).
Хорошие отдаленные результаты сохраняются у 93,1% пациентов (УД 1b, СР A [20, 55]).
Двухэтапное хирургическое лечение эпителиального копчикового хода, открытые операции
Показания. Выполняется в стадии абсцесса при остром воспалении ЭКХ (УД 1b, СР A [40, 50, 66, 69, 70]).
Методика. На первом этапе полость абсцесса пунктируют в точке наибольшей флюктуации и шприцем откачивают жидкое содержимое. Затем продольным разрезом вскрывают полость абсцесса. На втором этапе, после стихания острого воспаления (обычно 5–7 дней), в пределах неизмененных тканей осуществляется экономное иссечение копчикового хода и его разветвлений, а также окружающей клетчатки, рана при этих операциях ведется открытым способом (УД 1b, СР B [52, 70]).
Хорошие и удовлетворительные результаты отмечаются у 79–87, 1% пациентов (УД 1b, СР A [32]).
Иссечение эпителиального копчикового хода с пластикой раны перемещенными лоскутами (по Лимбергу, Каридакису c L-, Z-, Y-, W-пластикой; УД 3b, СР B [18, 28], УД 3b, СР C [14, 28, 29, 44], УД 4,
СР C [51])
Показания. Рецидивный ЭКХ или запущенные формы с множественными свищевыми затеками на правую и левую ягодичные области.
Методика. Иссекают ЭКХ со всеми его разветвлениями, наружными свищевыми отверстиями и окружающей их кожей, тканями, прилежащими к свищевым ходам, инфильтратами и полостями единым блоком до крестцовой фасции. Планирование и выкраивание кожно-жировых лоскутов производят дополнительными разрезами кожи и подкожной
клетчатки на всю ее толщу под углом к краям основного раневого дефекта, близким к 60°. Известно, что этот угол обеспечивает адекватное кровоснабжение лоскутов при хорошей степени их подвижности. Одну из сторон выкраиваемого треугольного лоскута образует край дефекта, возникшего после удаления копчикового хода, другую сторону составляет край дополнительного разреза. Мобилизацию лоскутов производят отслаиванием их от подлежащих тканей над крестцовой и ягодичной фасцией. Толщина их при этом должна быть максимальной, содержать всю подкожную жировую клетчатку. Закрытие раневого дефекта начинают с каудально расположенного угла раны. Лоскут перемещают на раневой дефект, фиксируют за нижний край жировой клетчатки к крестцовой фасции отдельными швами, после чего одну сторону его сшивают с каудальным краем раны. Перемещение, фиксацию и сшивание последующих лоскутов проводят аналогично (УД 3b, СР C [9, 18, 23, 28, 33, 34, 44, 47]). Хорошие и удовлетворительные результаты отмечаются у 84,2% паци-
ентов (УД 3b, СР C [31, 33, 71]).
Подкожное иссечение эпителиального копчикового хода (синусэктомия)
Показания. Неосложненный ЭКХ, хроническое воспаление ЭКХ в стадии гнойного свища, ремиссия воспаления ЭКХ (УД 4, СР C [13, 54, 64]). Противопоказания. Абсолютными противопоказаниями для этой процедуры являются наличие разветвлений, гнойных затеков и полостей,
большая удаленность первичных и вторичных отверстий друг от друга.
Методика. ЭКХ иссекают под кожей от первичного отверстия ко вторичным. ЭКХ через первичное или через вторичное свищевое отверстие прокрашивают метиленовой синью. Далее через отверстия ЭКХ проводят пуговчатый зонд и с помощью электрокоагуляции иссекают ход на зонде. Образованные при этом раны не ушиваются (УД 4, СР C [12, 55]).
В отдаленные сроки наблюдения положительный результат наблюдается в 93% случаев (УД 4, СР C [55, 65]).
Чего нельзя делать
n При остром воспалении ЭКХ недопустима необоснованная задержка хирургического лечения.
n Недопустимо проведение операции в условиях недостаточного обезболивания и миорелаксации.
n При длительно сохраняющейся после вскрытия абсцесса температуре тела недопустимо назначение антибактериальной терапии без проведения диагностических мероприятий и ревизии раны.
n Недопустимо проведение закрытых операций и сложных пластических операций (пластика кожными лоскутами) в условиях выраженного воспаления и отека окружающих тканей.
n Нежелательна длительная отсрочка в проведении радикальной операции после вскрытия и дренирования абсцесса (УД 4, СР C [35, 62]).
Дальнейшее ведение
В послеоперационном периоде как после радикального, так и после первого этапа многоэтапного лечения пациентам проводят:
n ежедневные перевязки послеоперационной раны с использованием перекиси водорода и антисептиков (повидон-йод, повидон-йод + калия йодид, хлоргексидин, гидроксиметилхиноксалиндиоксид) (УД 3b, СР B [10, 16, 61, 72]);
n местное применение мазей, ускоряющих репарацию тканей (метилурацил♠) и обладающих антимикробным и противовоспалительным эффектом (левомеколь♠, левосин♠, фузимет♠) (УД 3b, СР C [15, 58, 72]);
n комплексное физиотерапевтическое лечение — ежедневные десятиминутные сеансы УФ-облучения, использование воздействия УВЧ в диапазоне 40–70 Вт и микроволновую терапию в пределах 20–60 Вт.
Объем физических воздействий выбирают на основании целого ряда факторов, отражающих общее состояние пациента, но определяющие из них — распространенность и выраженность воспалительных проявлений (УД 4, СР D [38, 61, 62]).
Прогноз
При радикальном лечении ЭКХ прогноз в любой стадии процесса благоприятный. Наступает полное выздоровление (УД 3a, СР B [1, 4]).
Профилактика
Специфической профилактики воспаления ЭКХ не существует (УД 4, СР C [21]). Профилактика острого воспаления заключается в основном в общеукрепляющих организм мероприятиях, направленных на устранение этиологических факторов возникновения заболевания.
n Соблюдение правил личной гигиены, в основном межъягодичной складки.
n Поддержка и укрепление местного и гуморального иммунитета.
n Лечение и санация очагов острой и хронической инфекции.
n Коррекция хронических заболеваний — сахарного диабета, атеросклероза.
n Коррекция функциональных нарушений (запор, понос).
n Своевременное лечение сопутствующих проктологических заболеваний (геморрой, трещины заднего прохода, криптит и т.д.) (УД 4, СР C [2, 3, 24]). Критерии оценки качества помощи в стационаре представлены в таблице 3.2 Для оценки качества медицинской помощи используют временные, процессуальные и профилактирующие критерии. Временные характеризуют своевременность оказания определенных этапов медицинской помощи. Выполнение пациенту ряда медицинских манипуляций, инструментальных и лабораторных исследований, необходимых для качественного оказания медицинской помощи, оценивают
в процессуальных критериях. Для анализа мероприятий, направленных на предотвращение развития осложнений, используют профилактирующие критерии.
Таблица 3.2. Критерии оценки качества медицинской помощи в стационаре больным с доброкачественными заболеваниями промежности (эпителиальный копчиковый ход) (0 — нет, 1 — да)
|
Клинические рекомендации |
Временные |
Процессуальные |
Профилактирующие |
|
1. Клинические рекомендации по диагностике и лечению взрослых пациентов с эпителиальным копчиковым ходом (код МКБ — L05: L05.0; L05.9). |
Установка клинического диагноза в течение 72 ч: 0/1 |
Оценка анального рефлекса: 0/1. Пальцевое обследование прямой кишки: 0/1. Аноскопия: 0/1. Ректороманоскопия: 0/1. Определение группы крови: 0/1. Исследование крови на сифилис, вирусный гепатит В, вирусный гепатит С: 0/1. Клинический анализ крови; биохимический анализ крови; клинический анализ мочи; коагулограмма: 0/1. Метод оперативного лечения в соответствии с клиническими рекомендациями: 0/1. Метод анестезии в соответствии с объемом оперативного лечения: 0/1 |
Отсутствие осложнений: • кровотечение: 0/1; • абсцесс: 0/1; • флегмона: 0/1; • пневмония: 0/1; • тромбоэмболия: 0/1; • летальный исход: 0/1 |
Литература
1. Воробьев Г.И. Основы колопроктологии. — М.: МИА, 2006. — 430 с.
2. Кайзер А.М. Колоректальная хирургия. — М.: БИНОМ, 2011. — 737 с.
3. Федоров В.Д., Дульцев Ю.В. Проктология. — М.: Медицина, 1984. — 384 с.
4. Шелыгин Ю.А., Благодарный Л.А. Справочник по колопроктологии. — М.: Литтерра, 2012. — 596 с.
5. Akinci O., Coskun A., Uzunkoy A. Simple and Effective Surgical Treatment of pilonidal sinus, asymmetric excision and primary closure using suction drain and subcuticular skin closure // Dis. Colon Rectum. — 2000. — Vol. 43. — P. 701–707.
6. Akinci O.F., Bozer M., Uzunköy A. et al. Incidence and aetiological factors in pilonidal sinus among Turkish soldiers // Eur. J. Surg. — 1999. — Vol. 165. — P. 339–342.
7. Aldean I., Shankar P., Mathew J. et al. Simple excision and primary closure of pilonidal sinus: a simple modification of conventional technique with excellent results // Colorectal Dis. — 2005. — Vol. 7. — P. 81–85.
8. Allen-Mersh T.G. Pilonidal sinus: finding the right track for treatment // Br. J. Surg. —1990. — Vol. 77. — P. 123–132.
9. Arumugam P., Chandrasekaran T., Morgan A. et al. The rhomboid flap for pilonidal disease // Colorectal Dis. — 2003. — Vol. 5. — P. 218–221.
10. Bannerjee D. Pilonidal sinus wounds: the clinical approach // J. Community Nurs. — 1999. — Vol. 13. — P. 22–26.
11. Bascom J. Pilonidal sinus // Current Therapy in Colon and Rectal Surgery. — 1990. — P. 1–8.
12. Bascom J. Pilonidal disease: long term results of follicle removal // Dis. Colon Rectum. — 1983. — Vol. 26. — P. 800–807.
13. Bascom J. Pilonidal sinus // Current Therapy in Colon and Rectal Surgery / Eds V.W. Fazio, J.M. Church, C.P. Delaney. — Toronto: BC Decker, 1990.
14. Berkem H., Topaloglu S., Ozel H. et al. V–Y advancement flap closures for complicated pilonidal sinus disease // Int. J. Colorectal Dis. — 2005. — Vol. 20. — P. 343–348.
15. Berry D.P. Pilonidal sinus disease // J. Wound Care. — 1992. — Vol. 1. — P. 29–32.
16. Berry D.P., Bale S., Harding K.G. Dressings for treating cavity wounds // J. Wound Care. — 1996. — Vol. 5. — P. 1–13.
17. Bissett I.P., Isbister W.H. The management of patients with pilonidal disease a comparative study // Aust. N.Z. J. Surg. — 1987. — Vol. 57. — P. 939–942.
18. Bozkurt M.K., Tezel E. Management of pilonidal sinus with the Limberg flap // Dis. Colon Rectum. — 1998. — Vol. 41. — P. 775–777.
19. Branagan G., Thompson M., Senapati A. Cleft closure for the treatment of unhealed perineal sinus // Colorectal Dis. — 2006. — Vol. 8. — P. 314–317.
20. Buie L.A., Curtiss R.K. Pilonidal Disease // Surg. Clin. North Am. — 1952. — Vol. 32. — P. 1247–1259.
21. Chamberlain J.W., Vawter G.F. The congenital origin of pilonidal sinus // J. Pediatr. Surg. — 1974. — Vol. 9. — P. 441–444.
22. Chintapatla S., Safarani N., Kumar S. Sacrococcygeal pilonidal sinus: historical review, pathological insight and surgical options // Tech. Coloproctol. — 2003. — Vol. 7. — P. 3–8.
23. Cihan A., Ucan B., Comert M. et al. Superiority of asymmetric modified Limberg flap for surgical treatment of pilonidal disease // Dis. Colon Rectum. — 2006. — Vol. 49. — P. 244–249.
24. Clothier P.R., Haywood I.R. The natural history of the post anal (pilonidal) sinus // Ann. R. Coll. Surg. Engl. — 1984. — Vol. 66. — P. 201–203.
25. Cripps N., Evans J., Nordon I. et al. Sacrococcygeal pilonidal sinus disease // Colorectal Dis. — 2009. — Vol. 11. — P. 105–106.
26. Cubukçu A., Carkman S., Gönüllü N.N. et al. Lack of evidence that obesity is a cause of pilonidal sinus disease // Eur. J. Surg. — 2001. — Vol. 167. — P. 297–298.
27. Da Silva J. Pilonidal cyst: cause and treatment // Dis. Colon Rectum. — 2000. — Vol. 43. — P. 1146–1156.
28. Daphan C., Tekelioglu H., Sayilgan C. Limberg flap repair for pilonidal sinus disease // Dis. Colon Rectum. — 2004. — Vol. 47. — P. 233–237.
29. Dylek O.N., Bekereciodlu M. Role of simple V–Y advancement flap in the treatment of complicated pilonidal sinus // Eur. J. Surg. — 1998. — Vol. 164. — P. 961–964.
30. Edwards M. Pilonidal sinus. A 5 year appraisal of the Millar-Lord treatment // Br. J. Surg. — 1977. — Vol. 64. — P. 867–868.
31. Ersoy O.F., Karaca S., Kayaoglu H.A. Comparison of different surgical options in the treatment of pilonidal disease: retrospective analysis of 175 patients // Kaohsiung J. Med. Sci. — 2007. — Vol. 23, N 2. — P. 67–70.
32. Fabricius R., Wiuff L., Bertelsen C.A. Treatment of pilonidal sinuses in Denmark is not optimal // Dan. Med. Bull. — 2010. — Vol. 57, N 12. — P. 4200.
33. Fazeli M., Adel M., Lebaschi A. Comparison of 39 outcomes in Z-plasty and delayed healing by secondary intention of the wound after excision of the sacral pilonidal sinus: results of a randomized, clinical trial // Dis. Colon Rectum. — 2006. — Vol. 49. — P. 1831–1836.
34. Galala K., Salam I., Sim A. et al. Treatment of pilonidal sinus by primary closure with a transposed rhomboid flap compared with deep suturing: a prospective randomized clinical trial // Eur. J. Surg. — 1999. — Vol. 165. — P. 468–472.
35. Gilchrist B. Wound infection. Sampling bacterial flora: a review of the literature // J. Wound Care. — 1996. — Vol. 5. — P. 386–388.
36. Goligher J.C. Pilonidal sinus // Surgery of the Anus, Rectum and Colon. — 4th ed. / Eds M.R.B. Keighley, N.S. Williams. — Saunders, 1980.
37. Golladay E. Outpatient adolescent surgical problems // Adolesc. Med. Clin. — 2004. — Vol. 15. — P. 503–520.
38. Gupta P. Radiofrequency incision and lay open technique of pilonidal sinus clinical practice paper on modified technique // Kobe J. Med. Sci. — 2003. — Vol. 49. — P. 75–82.
39. Guyuron B., Dinner M., Dowden R. Excision and grafting in treatment of recurrent pilonidal sinus disease // Surg. Gynecol. Obstet. — 1983. — Vol. 156. — P. 201–204.
40. Hart J. Inflammation 2: its role in the healing of chronic wounds // J. Wound Care. — 2002. — Vol. 11. — P. 245–249.
41. Hodges R.M. Pilo-nidal sinus // Boston Med. Surg. J. — 1980. — Vol. 103. — P. 485–486.
42. Jeffery M., Billingham N., Billingham R. Pilonidal disease and hidradenitis suppurativa // The ASCRS Textbook of Colon and Rectal Surgery. — 1st ed. / Eds
B. Wolff, J. Fleshman, D. Beck et al. — N.Y.: Springer, 2007. — P. 228–239.
43. Jones D.J. Pilonidal sinus. ABC of colorectal diseases // BMJ. — 1992. — Vol. 305. — P. 410–412.
44. Kapan M., Kapan S., Pekmezci S. et al. Sacrococcygeal pilonidal sinus disease with Limberg flap repair // Tech. Coloproctol. — 2002. — Vol. 6. — P. 27–32.
45. Karydakis G.E. Easy and successful treatment of pilonidal sinus after explanation of its causative process // Aust. N.Z. J. Surg. — 1992. — Vol. 62. — P. 385–389.
46. Kaymakcioglu N., Yagci G., Simsek A. et al. Treatment of pilonidal sinus by phenol application and factors affecting the recurrence // Tech. Coloproctol. — 2005. — Vol. 9. — P. 21–24.
47. Khatri V., Espinosa M., Amin A. Management of recurrent pilonidal sinus by simple V–Y fasciocutaneous flap // Dis. Colon Rectum. — 1994. — Vol. 37. — P. 1232–1235.
48. Kronborg G., Christensen K., Zimmermann-Nielsen C. Chronic pilonidal disease: a randomized trial with a complete 3-year follow-up // Br. J. Surg. — 1985. — Vol. 72. — P. 303–304.
49. Lundhus E., Gottrup F. Outcome at three to five years of primary closure of perianal and pilonidal abscess // Eur. J. Surg. — 1993. — Vol. 159. — P. 555–558.
50. Mahdy T. Surgical treatment of the pilonidal disease: primary closure or flap reconstruction after excision // Dis. Colon Rectum. — 2008. — Vol. 51. — P. 1816–1822.
51. Manterola C., Barroso M., Araya J. et al. Pilonidal disease: 25 cases treated by the Dufourmentel technique // Dis. Colon Rectum. — 1991. — Vol. 34. — P. 649–652.
52. Marks J., Harding K.G., Hughes L.E., Ribeiro C.D. Pilonidal sinus excision — healing by open granulation // Br. J. Surg. — 1985. — Vol. 72. — P. 637–640.
53. Maurice B.A., Greenwood R.K. A conservative treatment of pilonidal sinus // Br. J. Surg. — 1964. — Vol. 51. — P. 510–512.
54. Notaras M.J. A review of three popular methods of treatment of postanal (pilonidal) sinus disease // Br. J. Surg. — 1970. — Vol. 57, N 12. — P. 886–890.
55. Oncel M., Kurt N., Kement M. Excision and marsupialization versus sinus excision for the treatment of limited chronic pilonidal disease: a prospective, randomized trial // Tech. Coloproctol. — 2002. — Vol. 6. — P. 165–169.
56. OCEBM Levels of Evidence Working Group. The Oxford 2011 Levels of Evidence. — Oxford Centre for Evidence-Based Medicine, 2011.
57. Page B.H. The entry of hair into a pilonidal sinus // Br. J. Surg. — 1969. — Vol. 56. — P. 32.
58. Patel H., Lee M., Bloom I. et al. Prolonged delay in healing after surgical treatment of pilonidal sinus is avoidable // Colorectal Dis. — 1999. — Vol. 1. — P. 107–110.
59. Patey D.H., Scarff R.W. Pathology of postanal pilonidal sinus disease: its bearing on treatment // Lancet. — 1946. — Vol. 251. — P. 484–486.
60. Petersen S., Koch R., Stelzner S. et al. Primary closure techniques in chronic pilonidal sinus. A survey of the results of different surgical approaches // Dis. Colon Rectum. — 2002. — Vol. 45. — P. 1458–1467.
61. Price P.E., Butterworth R.J., Bale S. Harding K.G. Measuring quality of life in patients with granulating wounds // J. Wound Care. — 1994. — Vol. 3. — P. 49–50.
62. Price P.E., Harding K.G. Acute and chronic wounds: differences in selfreported health-related quality of life // J. Wound Care. — 2000. — Vol. 9. — P. 93–95.
63. Sakr M., Elserafy M., Hamed H. Management of 634 consecutive patients with chronic pilonidal sinus: a nine-year experience of a single institute // Surg. Sci. — 2012. — Vol. 3. — P. 145–154.
64. Senapati A., Cripps N.P.J., Thompson M.R. Bascom’s operation in the daysurgical management of symptomatic pilonidal sinus // Br. J. Surg. — 2000. — Vol. 87. — P. 1067–1070.
65. Soll C., Dindo D., Steinmann D. Sinusectomy for primary pilonidal sinus: less no more // Surgery. — 2011. — Vol. 150, N 5. — P. 996–1001.
66. Solla J.A., Rothenberger D.A. Chronic pilonidal disease: An assessment of 150 cases // Dis. Colon Rectum. — 1990. — Vol. 33. — P. 758–761.
67. Sondenaa K., Anderson E., Nesvik I., Soreide J.A. Patient characteristics and symptoms in chronic pilonidal sinus disease // Int. J. Colorectal Dis. — 1995. — Vol. 10. — P. 39–42.
68. Spivak H., Brooks V.L., Nussbaum M., Friedman I. Treatment of chronic pilonidal disease // Dis. Colon Rectum. — 1996. — Vol. 39. — P. 1136–1139.
69. Surrell J.A. Pilonidal disease // Surg. Clin. North Am. — 1994. — Vol. 74. — P. 1309–1315.
70. Testini M., Piccinni G., Miniello S. et al. Treatment of chronic pilonidal sinus with local anaesthesia: a randomized trial of closed compared with open technique // Colorectal Dis. — 2001. — Vol. 3. — P. 427–430.
71. Topgul K., Özdemir E., Kilic K. et al. Long-term results of Limberg flap procedure for treatment of pilonidal sinus. A Report of 200 Cases // Dis. Colon Rectum. — 2003. — Vol. 46. — P. 1545–1548.
72. Viciano V., Castera J.E., Medrano J. et al. Effect of hydrocolloid dressings on healing by second intention after excision of pilonidal sinus // Eur. J. Surg. — 2000. — Vol. 166. — P. 229–232.
ОСТРЫЙ ПАРАПРОКТИТ
Введение
Острый парапроктит является самым распространенным заболеванием в практике неотложной хирургической проктологии. Пациенты этой группы составляют около 1% всех госпитализированных в различные стационары хирургического профиля и 5% среди страдающих заболеваниями ободочной и прямой кишки [5]. В числе острых гнойных поражений аноректальной зоны частота острого парапроктита приближается к 45% [1].
Острый парапроктит распространен повсеместно и на протяжении многих десятилетий является предметом оживленных дискуссий на страницах отечественной и зарубежной литературы. Наиболее часто обсуждаются ишеоанальные, пельвиоректальные, ретроректальные и подковообразные гнойники, встречающиеся, по разным данным, с впечатляющим размахом — от 5 до 58% [10, 45].
Развитие острого парапроктита обусловлено рядом предрасполагающих факторов: ослаблением иммунитета вследствие сопутствующей острой или хронической инфекции, сосудистыми изменениями вследствие сахарного диабета, желудочно-кишечные расстройствами, наличием геморроя, трещин, криптита [2, 4, 11].
Рекомендации по диагностике и лечению пациентов с острым парапроктитом служат руководством для практических врачей, осуществляющих ведение и лечение таких больных, и подлежат регулярному пересмотру в соответствии с новыми данными научных исследований в этой области.
Рекомендации включают следующие разделы: определение заболевания, классификация, профилактика, диагностика, консервативное и оперативное лечение, правила ведения периоперационного периода, а также прогноз у больных острым парапроктитом.
Для отдельных положений рекомендаций приведены уровни доказательности согласно общепринятой классификации Оксфордского центра доказательной медицины [31] (табл. 4.1).
ВАЛИДИЗАЦИЯ РЕКОМЕНДАЦИЙ
Настоящие рекомендации составлены Общероссийской общественной организации «Ассоциация колопроктологов России» и в предварительной
Таблица 4.1. Уровни доказательности и степени рекомендаций на основании руководства Оксфордского центра доказательной медицины
|
Уровень |
Исследования методов диагностики |
Исследования методов лечения |
|
1а |
Систематический обзор гомогенных диагностических исследований 1-го уровня |
Систематический обзор гомогенных РКИ |
|
1b |
Валидизирующее когортное исследование с качественным «золотым стандартом» |
Отдельное РКИ (с узким доверительным интервалом) |
|
1с |
Специфичность или чувствительность столь высокие, что положительный или отрицательный результат позволяет исключить/установить диагноз |
Исследование «Всё или ничего» |
|
2а |
Систематический обзор гомогенных диагностических исследований >2-го уровня |
Систематический обзор (гомогенных) когортных исследований |
|
2b |
Разведочное когортное исследование с качественным «золотым стандартом» |
Отдельное когортное исследование (включая РКИ низкого качества; т.е. с <80% пациентов, прошедших контрольное наблюдение) |
|
2с |
Нет |
Исследование «исходов»; экологические исследования |
|
3а |
Систематический обзор гомогенных исследований уровня 3b и выше |
Систематический обзор гомогенных исследований «случай–контроль» |
|
3b |
Исследование с непоследовательным набором или без проведения исследования «золотого стандарта» у всех испытуемых |
Отдельное исследование «случай– контроль» |
|
4 |
Исследование «случай–контроль» или исследование с некачественным или зависимым «золотым стандартом» |
Серия случаев (и когортные исследования или исследования «случай– контроль» низкого качества) |
|
5 |
Мнение экспертов без тщательной критической оценки или основанное на физиологии, лабораторных исследованиях на животных или разработка «первых принципов» |
Мнение экспертов без тщательной критической оценки, лабораторные исследования на животных или разработка «первых принципов» |
|
Степени рекомендаций | ||
|
А |
Согласующиеся между собой исследования 1-го уровня | |
|
В |
Согласующиеся между собой исследования 2-го или 3-го уровня или экстраполяция на основе исследований 1-го уровня | |
|
С |
Исследования 4-го уровня или экстраполяция на основе уровня 2 или 3 | |
|
D |
Доказательства 5-го уровня или затруднительные для обобщения или некачественные исследования любого уровня | |
версии были рецензированы независимыми экспертами, которых попросили прокомментировать прежде всего, насколько интерпретация доказательств, лежащих в основе рекомендаций, доступна для понимания. Получены комментарии со стороны врачей амбулаторного звена, комментарии тщательно систематизировались и обсуждались на совещаниях экспертной группы.
Последние изменения в настоящих рекомендациях были представлены для дискуссии на заседании профильной комиссии «Колопроктология» Экспертного совета Минздрава России 12 сентября 2013 г. Проект рекомендаций был повторно рецензирован независимыми экспертами и врачами амбулаторного звена. Для окончательной редакции и контроля качества рекомендации были повторно проанализированы членами экспертной группы, которые пришли к заключению, что все замечания и комментарии приняты во внимание, риск систематических ошибок при разработке рекомендаций сведен к минимуму.
ОБЛАСТЬ ПРИМЕНЕНИЯ РЕКОМЕНДАЦИЙ
Данные клинические рекомендации применимы при осуществлении медицинской деятельности в рамках Порядка оказания медицинской помощи взрослому населению с заболеваниями толстой кишки, анального канала и промежности колопроктологического профиля.
Определение
Острый парапроктит — острое воспаление околопрямокишечной клетчатки, обусловленное распространением воспалительного процесса из анальных крипт и анальных желез [4, 6, 11].
Код по Международной классификации болезней 10-го пересмотра
n Класс: Болезни органов пищеварения (XI).
n Блок: Абсцесс заднего прохода и прямой кишки (К61).
n Код:
v K61.0 Анальный [заднепроходный] абсцесс
v K61.1 Ректальный абсцесс
v K61.2 Аноректальный абсцесс
v K61.3 Ишеоанальный абсцесс
v K61.4 Интрасфинктерный абсцесс
Классификация
В настоящее время в клинической практике используется классификация, подразделяющая острый парапроктит по характеру возбудителя, локализации поражения, по локализации крипты, вовлеченной в процесс
воспаления, по характеру гнойного хода. Классификация применяется для определения тяжести поражения и выбора метода лечения [3, 11]. В клинической практике данная классификация чаще всего используется в следующем виде.
По характеру возбудителя:
n аэробный;
n анаэробный:
v клостридиальный;
v неклостридиальный.
По локализации поражения:
n подкожный;
n подслизистый;
n межмышечный;
n седалищно-прямокишечный (ишеоанальный);
n тазово-прямокишечный:
v пельвиоректальный;
v ретроректальный;
v подковообразный.
По локализации крипты, вовлеченной в процесс воспаления:
n задний;
n передний;
n боковой.
По характеру гнойного хода:
n интрасфинктерный;
n транссфинктерный;
n экстрасфинктерный.
Формулировка диагноза
При формулировании диагноза следует отразить характер возбудителя, локализацию гнойного очага, а также локализацию пораженной крипты (см. раздел «Диагностика»). Ниже приведены примеры формулировок диагноза.
n Острый аэробный боковой подкожный интрасфинктерный парапроктит.
n Острый анаэробный пельвиоректальный экстрасфинктерный парапроктит.
n Острый аэробный задний межмышечный транссфинктерный парапроктит.
Диагностика
Диагностика острого парапроктита основана на жалобах больного, степени их выраженности, длительности болезни, анализе результатов клинического и объективного обследования пациента. К основным клиническим проявлениям ОП относятся острое начало заболевания, нарастающая боль в прямой кишке, промежности или в тазу, повышение температуры тела (УД 3b, СР C [2–4, 6, 11, 16, 30, 38]).
Сбор анамнеза. Выявляются жалобы больного, длительность заболевания, характер и интенсивность болей, а также этиологические факторы возникновения заболевания: ослабление иммунитета вследствие сопутствующей острой или хронической инфекции, сосудистые изменения вследствие сахарного диабета, желудочно-кишечные расстройства, наличие геморроя, трещин, криптита, история предыдущих аноректальных или промежностных оперативных вмешательств (УД 3b, СР C [2–4, 6, 11]). Осмотр больного. Проводят на гинекологическом кресле в положении как для литотомии или в коленно-локтевом положении. При этом оценивают гиперемию, припухлость кожных покровов перианальной, крестцово-копчиковой области и ягодиц, наличие резко болезненного инфильтрата или флюктуации в этой области. При осмотре промежности и заднего прохода выявляют патологические выделения гноя или слизи, сопутствующие заболевания — анальную трещину, геморрой, свищи
или выпадение прямой кишки (УД 3b, СР C [2–4, 6, 11]).
Пальцевое исследование прямой кишки. Этот диагностический прием является основным при остром парапроктите и несет определяющую информацию при сложных разновидностях заболевания.
n При тазово-прямокишечном парапроктите отмечают болезненность одной из стенок среднеампулярного или верхнеампулярного отдела прямой кишки, тестоватой консистенции инфильтрацию кишечной стенки или плотный инфильтрат за ее пределами. В более поздних стадиях определяют утолщение стенки кишки, оттеснение ее извне, затем выбухание в просвет эластичной, иногда флюктуирующей опухоли, над которой слизистая оболочка кишки может оставаться подвижной.
n При позадипрямокишечной форме определяют выбухание в области задней стенки прямой кишки, а также усиление болей при давлении на копчик.
n При подковообразной форме острого парапроктита выявляют уплощение и уплотнение стенки кишки выше анального канала, сглаженность складок на стороне поражения, повышение температуры в кишке. К концу первой недели заболевания воспалительный инфильтрат оттесняет стенку кишки и выбухает в ее просвет. Если воспалительная инфильтрация ткани захватывает предстательную железу и мочеиспускательный канал, пальпация их вызывает болезненный позыв на мочеиспускание.
n При внутристеночно-инфильтративном парапроктите выше зубчатой линии, непосредственно над ней или высоко в ампулярном отделе прямой кишки, через стенку кишки пальпируют плотный, неподвижный, безболезненный инфильтрат, часто без четких границ (УД 3b, СР C [2–4, 6, 11, 17, 18]).
Фистулография. Не считается обязательным методом обследования, используют для уточнения диагноза. Определяются расположение и размеры гнойной полости, ход свища по отношению к наружному сфинктеру (УД 4, СР D [11, 27, 46]).
Бактериологическое исследование. Не считается обязательным методом обследования. Заключается в видовом исследовании микрофлоры гной-
ного очага для уточнения диагноза и проведения адекватной антибиотикотерапии. Взятие материала (гной) производится в условиях операционной во время пункции гнойника. Материал берется двумя тампонами, один из которых для микроскопии, а другой для посева. Не более чем через 1 ч после взятия весь материал доставляется в бактериологическую лабораторию для немедленного посева (УД 4, СР С [2, 13]).
В послеоперационном периоде в динамике определяют количество микробных тел на раневой поверхности или в 1 г пораженной ткани.
«Сигнальным» показателем служит число 105, уменьшение степени которого свидетельствует о благополучном течении воспалительного процесса, а увеличение вызывает необходимость различных корригирующих действий. Исследование необходимо для решения вопроса о возможности выполнения отсроченной радикальной операции (УД 4, СР С [2, 13]).
ЭНДОРЕКТАЛЬНОЕ УЛЬТРАЗВУКОВОЕ ИССЛЕДОВАНИЕ
Не считается обязательным методом обследования, используют для уточнения диагноза.
УЗИ со стороны промежности и трансректальная сонография позволяют оценить локализацию, размеры, структуру патологического очага, наличие дополнительных ходов, степень вовлечения в воспалительный процесс стенки прямой кишки и волокон наружного сфинктера, глубину расположения патологического очага от кожных покровов (УД 2b, СР B [9, 15, 39, 43, 44]). Эффективность УЗИ в определении ОП составляет
80–89% (УД 2b, СР B [9, 15, 39, 43, 44]).
Методика. Исследование проводится на эхотомографах, работающих в режиме реального времени и серой шкалы, снабженных секторальными конвексными и линейными датчиками от 2 до 5 мГц, а также на ультразвуковых сканерах, работающих в режиме серой шкалы и цветном допплеровском режиме (CDI) с датчиками PVV-375 AT (3–6 мГц), PlM-805 AT (6–12 мГц). Результаты исследования документируются на фотоприставке с осуществлением необходимых измерений на экране монитора и Video Printer P-91-E. Больному, находящемуся в коленнолоктевом положении или на боку, в анальный канал вводят ректальный датчик на расстояние 8 см с предварительно надетым на него резиновым баллончиком и откачанным из него воздухом. Через переходник баллончик заполняют дистиллированной водой 30–50 мл, что обеспечивает хорошую проводимость УЗ-луча. Датчиком проводят вращательные движения по часовой стрелке и делают линейное УЗ-сканирование путем проведения продольных сечений анального канала, вращая датчик. Точность УЗИ достигает 90% (УД 3b, СР C [14, 22, 47, 48]).
ДИФФЕРЕНЦИАЛЬНАЯ ДИАГНОСТИКА
Учитывая особенности клинических проявлений острого парапроктита, в основном проводят дифференциальную диагностику с нагно-
ившейся тератомой параректальной клетчатки, абсцессом дугласова пространства, вскрывшимся в параректальную клетчатку. Парапроктит также может быть осложнением распадающейся опухоли прямой кишки.
Лечение
Лечение острого парапроктита только хирургическое. Операция должна быть выполнена в ближайшие часы после верификации диагноза. Промедление с операцией не только ухудшает состояние больного, но и отягощает прогноз, так как чревато опасностью распространения гнойного процесса по клетчаточным пространствам таза, разрушения мышечных структур сфинктера и тазового дна, стенки прямой кишки. Хирургическое лечение может быть как радикальным одномоментным, так и многоэтапным. Наиболее целесообразно разделение хирургического лечения острого парапроктита на несколько этапов. На первом из них производится неотложное вскрытие гнойника, на втором — ранние отсроченные радикальные операции, осуществляемые 5–7 дней спустя, после полного стихания воспалительных явлений (УД 2b, СР B [2, 4, 8, 19, 40]).
Цель — вскрытие и дренирование гнойника, поиск и ликвидация пораженной крипты и гнойного хода [23, 25].
Показания к госпитализации — верифицированный диагноз острого парапроктита любой этиологии [2, 11].
ХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕ
Сам по себе вопрос о радикальном лечении гнойного очага при остром парапроктите не вызывает сомнений, поэтому первостепенные хирургические действия заключаются в неотложном широком вскрытии гнойного промежностного очага, ревизии и санации послеоперационной раны. Вид оперативного вмешательства зависит от величины и локализации гнойника, распространенности воспалительного инфильтрата в окружающих тканях. Эффективность лечения при остром парапроктите составляет 98% (УД 2b, СР B [2, 4, 8]), однако, по данным иностранных авторов, количество осложнений может достигать 43%.
РАДИКАЛЬНЫЕ ОПЕРАЦИИ
Показания к радикальному оперативному лечению пациентов с остром парапроктитом: четкое представление о локализации гнойника, гнойного хода и пораженной крипты, относительная интактность окружающих гнойный очаг тканей (УД 4, СР С [3, 11, 23, 25]).
Противопоказание к проведению радикальных операций: невозможность определения пораженной крипты, тяжелое соматическое состояние пациента, выраженные воспалительные изменения тканей в зоне предполагаемого оперативного вмешательства (УД 5, СР D [2, 3, 11]).
ВСКРЫТИЕ И ДРЕНИРОВАНИЕ АБСЦЕССА, ИССЕЧЕНИЕ ПОРАЖЕННОЙ КРИПТЫ И ГНОЙНОГО ХОДА В ПРОСВЕТ КИШКИ
Показания. Расположение гнойного хода кнутри от наружного сфинктера или захват только подкожной его порции (УД 2с, СР С [3, 11, 12, 45]).
Методика. Под обезболиванием проводят ревизию анального канала с целью поиска пораженной крипты внутреннего свищевого отверстия. Для четкой визуализации свищевого хода и гнойной полости используют пробу с красителем. Для уточнения расположения хода относительно волокон сфинктера проводят исследование пуговчатым зондом. После этого производят широкий полулунный разрез кожи на стороне поражения, а затем полностью иссекают пораженные ткани (УД 2с, СР С [3, 11, 12, 45]).
Хорошие результаты лечения в раннем периоде после операции отмечаются в 65–88% случаев (УД 2a, СР A [20, 32, 33, 36]).
ВСКРЫТИЕ И ДРЕНИРОВАНИЕ АБСЦЕССА, ИССЕЧЕНИЕ ПОРАЖЕННОЙ КРИПТЫ И СФИНКТЕРОТОМИЯ
Показания. Межсфинктерный парапроктит (УД 2с, СР С [3, 11, 32]).
Методика. Производят полулунный разрез кожи на стороне поражения, затем отделяют волокна внутреннего сфинктера от окружающих тканей и под визуальным контролем рассекают только внутренний сфинктер (УД 2с, СР С [3, 11, 32, 35]).
Цель. Вскрытие и дренирование межсфинктерного пространства
в просвет кишки. (УД 2с, СР С [3, 11, 35]).
ВСКРЫТИЕ И ДРЕНИРОВАНИЕ АБСЦЕССА, ИССЕЧЕНИЕ ПОРАЖЕННОЙ КРИПТЫ, ПРОВЕДЕНИЕ ЭЛАСТИЧЕСКОЙ ДРЕНИРУЮЩЕЙ ЛИГАТУРЫ
Показания. Транссфинктерное (захватывает более 20% сфинктера) или экстрасфинктерное расположение гнойного хода (УД 3b, СР С [7, 19, 32, 42, 45]).
Методика. Производят широкий полулунный разрез кожи на стороне поражения, затем после эвакуации гноя и обнаружения гнойного хода разрез продлевается до средней линии. Из просвета кишки производят окаймляющий разрез вокруг пораженной крипты с его продолжением по всей длине анального канала до соединения с углом промежностной раны. Узкой полоской иссекают выстилку анального канала и перианальную кожу. Через отверстие в месте удаленной крипты проводят эластический дренаж Сетона, один конец которого выводят из раны промежности по средней линии, а второй — через внутреннее отверстие в просвете кишки. Лигатуру затягивают (УД 3b, СР С [19, 32, 42. 45]).
Цель. Создание адекватного оттока для подготовки к проведению по-
следующей радикальной операции (УД 3b, СР С [7, 19, 32, 42, 45]).
МНОГОЭТАПНЫЙ ПОДХОД К ЛЕЧЕНИЮ
Это наиболее целесообразный и оправданный метод лечения острого парапроктита.
Квалифицированные действия на первом этапе хирургического лечения играют определяющую роль в дальнейшем течении воспалительного процесса. Основные хирургические принципы первого этапа.
n Выполнение оперативного вмешательства в возможно ранние сроки.
n Широкое вскрытие подкожного гнойника для обеспечения достаточного оттока гнойного содержимого и адекватное дренирование гнойной полости.
n Обеспечение интактности волокон анального сфинктера при ликвидации абсцесса.
n Исключение применения скальпеля при манипуляциях в глубине раны.
n Выполнение различных действий в просвете гнойной полости только под контролем введенного в прямую кишку пальца другой руки.
n Обязательное вскрытие и адекватное дренирование основного гнойного очага, а не только воспалительного фокуса в подкожной клетчатке (УД 3b, СР С [40, 49]).
ОПЕРАЦИИ ПРИ ТАЗОВО-ПРЯМОКИШЕЧНОМ ПАРАПРОКТИТЕ
Вскрытие и дренирование пельвиоректального парапроктита
Показания. Гнойники, локализующиеся в пельвиоректальном пространстве.
Методика. Полулунным разрезом на стороне поражения, отступив от края ануса не менее чем на 3 см, рассекают кожу, подкожную и ишиоректальную клетчатку. Продольным разрезом рассекают мышечную ткань диафрагмы таза. Эта манипуляция должна выполняться под визуальным контролем. Если ее не удается произвести на глаз, расслаивание мышцы может быть осуществлено тупым путем — пальцем, браншами большого зажима Бильрота или корнцангом. Дренирование гнойника выполняется с таким расчетом, чтобы в глубине раны не оставалось кармана, и отток был достаточным. С этой целью кожную рану расширяют и заполняют тампоном с дренажной трубкой (УД 2b, СР C [2, 4, 26, 35]). Хорошие результаты лечения в послеоперационном периоде отмечаются в 77,5% случаев (УД 2b, СР C [2, 4, 26]). Количество ранних после-
операционных осложнений составляет 8,1% (УД 2b, СР C [26]).
Вскрытие и дренирование ретроректального парапроктита
Показания. Гнойники, локализующиеся в ретроректальном пространстве.
Методика. Производят разрез кожи посередине между проекцией верхушки копчика и задним краем анального отверстия длиной до 5 см. Заднепроходно-копчиковая связка пересекается на расстоянии 1 см от верхушки копчика. Далее манипуляции выполняют тупым путем. Полость гнойника обследуют пальцем, при этом разъединяют соединительноткан-
ные перемычки. После эвакуации гноя рану осушивают и обрабатывают перекисью водорода. Край раны, прилегающий к стенке кишки, с помощью крючка отводят и хорошо экспонируют заднюю стенку анального канала, окруженного мышцами сфинктера. Операция заканчивается тампонированием ретроректального пространства (УД 3b, СР C [2, 4, 41, 26]). Хорошие отдаленные результаты сохраняются у 92,2% пациентов,
в то время как осложнения наблюдаются лишь у 3% больных (УД 3b, СР C [2, 4, 26]).
Вскрытие и дренирование подковообразного парапроктита
Показания. Подковообразное или двустороннее расположение гнойников при остром парапроктите (УД 3b, СР C [24, 33, 37]).
Методика. Объем вмешательства зависит от отношения гнойного хода к мышцам сфинктера, направления и локализации дуги подковы. Опорожнив гнойник и сориентировавшись в направлении гнойного хода и его ответвлений, рану тампонируют и выполняют аналогичное вмешательство на противоположной стороне. Раскрыв гнойные полости, находят дугу подковы и гнойный ход, ведущий в кишку. Определяют его отношение и дуги подковы к мышцам сфинктера. Если дуга расположена в подкожной клетчатке, ее рассекают по зонду. Точно так же поступают, если она располагается в пельвиоректальном пространстве. При этом пересекают заднепроходно-копчиковую связку. Рану дренируют и тампонируют (УД 3b, СР C [24, 33, 37]).
Хорошие и удовлетворительные отдаленные результаты отмечаются у 94,8% пациентов [24, 33, 37]).
Чего нельзя делать
n Операция при остром парапроктите должна выполняться незамедлительно — недопустима необоснованная задержка оперативного лечения.
n Недопустимо проведение операции в условиях недостаточного обезболивания и миорелаксации.
n При длительно сохраняющейся после вскрытия абсцесса температуре тела недопустимо назначение антибактериальной терапии без проведения диагностических мероприятий и ревизии раны.
n Недопустимо проведение сложных пластических операций (низведение лоскута) в условиях выраженного воспаления и отека окружающих тканей.
n Нежелательна длительная отсрочка в проведении радикальной операции после вскрытия и дренирования абсцесса (УД 4, СР C [2, 4, 11]).
Дальнейшее ведение
В послеоперационном периоде как после радикального, так и после первого этапа многоэтапного лечения пациентам проводят:
n ежедневные перевязки послеоперационной раны с использованием перекиси водорода и антисептиков (повидон-йод, повидон-йод + калия йодид хлоргексидин, гидроксиметилхиноксалиндиоксид) (УД 3b, СР C [2, 4, 28]);
n местное применение мазей, ускоряющих репарацию тканей и обладающих антимикробным и противовоспалительным эффектом до заживления раны;
n комплексное физиотерапевтическое лечение — ежедневные 10-минутные сеансы УФО-облучения, использование воздействия УВЧ в диапазоне 40–70 Вт и микроволновая терапия в пределах 20–60 Вт.
Объем физических воздействий выбирают на основании целого ряда факторов, отражающих общее состояние пациента, но определяющие из них — распространенность и выраженность воспалительных проявлений. Продолжительность самого лечения зависит от клинической, лабораторной и бактериологической картины полного купирования признаков острого процесса.
По длительности этот период в большинстве случаев составляет от 5 до 10 дней после поступления больного в стационар, а при инфильтративном процессе в кишке — до 2 нед или несколько дольше (УД 3b, СР C [2, 11, 28]).
СРОКИ ВЫПОЛНЕНИЯ РАДИКАЛЬНОГО ЭТАПА ОПЕРАЦИИ
При решении вопроса о проведении радикального этапа операции необходимо руководствоваться Клиническими рекомендациями по лечению свищей прямой кишки.
Прогноз
Прогноз в целом благоприятный при своевременно и правильно выполненной радикально операции. При операции простого вскрытия абсцесса без ликвидации связи его с просветом кишки выздоровление маловероятно — сформируется свищ прямой кишки или возникнет рецидив острого парапроктита (УД 2a, СР A [11, 29]). Прогностически неблагоприятными факторами хирургического лечения ОП являются длительный период заболевания, выраженная интоксикация и сопутствующие тяжелые полиорганные нарушения (УД 4, СР C [2]).
Профилактика
Специфической профилактики ОП не существует. Профилактика острого парапроктита заключается в основном в общеукрепляющих организм мероприятиях, направленных на устранение этиологических факторов возникновения заболевания.
n Поддержка и укрепление местного и гуморального иммунитета.
n Лечение и санация очагов острой и хронической инфекции.
n Коррекция хронических заболеваний — сахарного диабета, атеросклероза.
n Коррекция функциональных нарушений (запора, поноса).
n Своевременное лечение сопутствующих проктологических заболеваний (геморроя, трещин заднего прохода, криптита и т.д.) (УД 4, СР C [28]).
Критерии оценки качества помощи в стационаре представлены в таблице 4.2. Для оценки качества медицинской помощи используют временные, процессуальные и профилактирующие критерии. Временные характеризуют своевременность оказания определенных этапов медицинской помощи. Выполнение пациенту ряда медицинских манипуляций, инструментальных и лабораторных исследований, необходимых для качественного оказания медицинской помощи, оценивают в процессуальных критериях. Для анализа мероприятий, направленных на предотвращение развития осложнений, используют профилактирующие критерии.
Таблица 4.2. Критерии оценки качества медицинской помощи в стационаре больным острыми воспалительными заболеваниями параректальной клетчатки (0 — нет, 1 — да)
|
Клинические рекомендации |
Временные |
Процессуальные |
Профилактирующие |
|
1. Клинические рекомендации по диагностике и лечению взрослых пациентов с острым парапроктитом (код МКБ — K61) |
Установка диагноза в течение 2 ч: 0/1. Выполнение операции не позднее 8 ч с момента госпитализации |
Оценка анального рефлекса: 0/1. Пальцевое исследование прямой кишки: 0/1. Определение группы крови: 0/1. Исследование крови на сифилис, вирусный гепатит В, вирусный гепатит С: 0/1. Клинический анализ крови; биохимический анализ крови; клинический анализ мочи; коагулограмма: 0/1. Метод оперативного лечения в соответствии с клиническими рекомендациями: 0/1. Метод анестезии в соответствии с объемом оперативного лечения: 0/1 |
Отсутствие осложнений: • кровотечение: 0/1; • пневмония: 0/1; • тромбоэмболия: 0/1; • летальный исход: 0/1 |
Литература
1. Акопян А.С. и др. Улучшение результатов лечения больных острым парапроктитом // Проблемы колопроктологии: Сборник. — М., 2002. — Вып. 7. — С. 24–28.
2. Болквадзе Э.Э. Cложные формы острого парапроктита. Обзор литературы // Колопроктология. — 2009. — Т. 27, № 1. — С. 38–46.
3. Воробьев Г.И. Основы колопроктологии. — М.: МИА, 2006. — 430 с.
4. Дульцев Ю.В., Саламов К.Н. Парапроктит. — М.: Медицина, 1981. — 208 с.
5. Жуков Б.Н., Исаев В.Р., Чернов А.А. Основы колопроктологии для врача общей практики: монография. — Самара: Офорт, 2009. — 218 с.
6. Кайзер А.М. Колоректальная хирургия. — М.: БИНОМ, 2011. — С. 473–477.
7. Коплатадзе А.М., Бондарев Ю.А. Способ лечения экстрасфинктерного парапроктита // Проблемы колопроктологии: Сборник. — М., 1994. — Вып. 14. — С. 21–23.
8. Лаврешин П.М. Комплексный подход к лечению острого парапроктита.
Актуальные проблемы колопроктологии // V Всероссийская конференция с международным участием. — Ростов-н/Д, 2001. — 44 с.
9. Орлова Л.П., Коплатадзе А.М., Филиппов Д.Ю. Cпособ ультразвуковой диагностики острого парапроктита (патент РФ № 2134544).
10. Слесаренко С.С., Федоров В.Э. Результаты хирургического лечения острого парапроктита // Актуальные проблемы колопроктологии: Сборник. — М., 2005. — Вып. 8. — С. 125–126.
11. Шелыгин Ю.А., Благодарный Л.А. Справочник по колопроктологии. —
М.: Литтерра, 2012. — 596 с.
12. Beck D.E., Fazio V.W., Jagelman D.G. et al. Catheter drainage of ischiorectal abscesses // South. Med. J. — 1988. — Vol. 81. — P. 444–446.
13. Brook I. Microbiology and management of soft tissue and muscle infections // Int. J. Surg. — 2008. — Vol. 6. — Р. 328–338.
14. Buchanan G.N., Bartram C.I., Williams A.B. et al. Value of hydrogen peroxide enhancement of three-dimensional endoanal ultrasound in fistula-in-ano // Dis. Colon Rectum. — 2005. — Vol. 48. — P. 141–147.
15. Buchanan G.N., Halligan S., Bartram C.I. et al. Clinical examination,
endosonography, and MR imaging in preoperative assessment of fistula-in-ano: comparison with outcome-based reference standard // Radiology. — 2004. — Vol. 233. — P. 674–681.
16. Buchmann P., Keighley M.R., Allan R.N. et al. Natural history of perianal Crohn’s disease. Ten year follow-up: a plea for conservatism // Am. J. Surg. — 1980. — Vol. 140. — P. 642–644.
17. Chinn B.T. Outpatient management of pilonidal disease // Semin. Colon
Rectal Surg. — 2003. — Vol. 14. — P. 166–172.
18. Cirocco W.C., Reilly J.C. Challenging the predictive accuracy of Goodsall’s rule for anal fistulas // Dis. Colon Rectum. — 1992. — Vol. 35. — P. 537–542.
19. Corman M.L. Colon and Rectal Surgery. — 4th ed. — Philadelphia, 1998. — P. 224–237.
20. Cox S.W., Senagore A.J., Luchtefeld M.A., Mazier W.P. Outcome after incision and drainage with fistulotomy for ischiorectal abscess // Am. Surg. — 1997. — Vol. 63. — P. 686–689.
21. Gingold B.C. Reducing the recurrence risk of fistula-in-ano // Surg. Gynecol.
Obstet. — 1983. — Vol. 156, N 5. — P. 661–662.
22. Gustafsson U.M., Kahvecioglu B., Aström G. et al. Endoanal ultrasound or magnetic for preoperative assessment of anal fistula: a comparative study // Colorectal Dis. — 2001. — Vol. 3. — P. 189–197.
23. Gordon P.H. Principles and Practice of Surgery for the Colon, Rectum, and Anus. — 3rd ed. — N.Y., 2007. — 1354 p.
24. Held D., Khubchandani I., Sheets J. et al. Management of anorectal horseshoe abscess and fistula // Dis. Colon Rectum. — 1986. — Vol. 29. — P. 793–797.
25. Abcarian H. Anorectal infection: abscess-fistula // Clin. Colon Rectal Surg. — 2011. — Vol. 24, N 1. — P. 14–21.
26. Holzheimer R.G., Siebeck M. Treatment procedures for anal fistulous cryptoglandular abscess — how to get the best results // Eur. J. Med. Res. — 2006. — Vol. 11, N 12. — P. 501–515.
27. Kuijpers H.C., Schulpen T. Fistulography for fistula-in-ano: is it useful? //
Dis. Colon Rectum. — 1985. — Vol. 28. — P. 103–104.
28. Luchteveld M. Anorectal abscess // Prim. Care. — 1999. — Р. 69–80.
29. Lunniss P.J., Phillips R.K. Surgical assessment of acute anorectal sepsis is a better predictor of fistula than microbiological analysis // Br. J. Surg. — 1994. — Р. 368–369.
30. Nelson J., Billingham R. Pilonidal disease and hidradenitis suppurativa // The ASCRS Textbook of Colon and Rectal Surgery / Eds B.G. Wolff, J.W. Fleshman,
D.E. Beck et al. — N.Y.: Springer, 2007. — P. 228–235.
31. OCEBM Levels of Evidence Working Group. The Oxford 2011 Levels of Evidence. — Oxford Centre for Evidence-Based Medicine, 2011.
32. Oliver I., Lacueva F.J., Pérez Vicente F. et al. Randomized clinical trial comparing simple drainage of anorectal abscess with and without fistula track treatment // Int. J. Colorectal Dis. — 2003. — Vol. 18, N 2. — P. 107–110.
33. Onaca N., Hirshberg A., Adar R. Early reoperation for perirectal abscess: a
preventable complication // Dis. Colon Rectum. — 2001. — Vol. 44. — P. 1469–1473.
34. Orsoni P., Barthet M., Portier F. et al. Prospective comparison of endosonography, magnetic resonance imaging and surgical findings in anorectal fistula and abscess complicating Crohn’s disease // Br. J. Surg. — 1999. — Vol. 86. — P. 360–364.
35. Quah H.M., Tang C.L., Eu K.W. et al. Meta-analysis of randomized clinical trials comparing drainage alone vs primary sphincter-cutting procedures for anorectal abscess-fistula // Int. J. Colorectal Dis. — 2006. — Vol. 21, N 6. — P. 602–609.
36. Ramanujam P.S., Prasad M.L., Abcarian H., Tan A.B. Perianal abscesses
and fistulas: a study of 1023 patients // Dis. Colon Rectum. — 1984. — Vol. 27. — P. 593–597.
37. Rosen S.A., Colquhoun P., Efron J. et al. Horseshoe abscesses and fistulas: how are we doing? // Surg. Innov. — 2006. — Vol. 13. — P. 17–21.
38. Sahni V.A., Ahmad R., Burling D. Which method is best for imaging of perianal fistula? // Abdom. Imaging. — 2008. — Vol. 33. — P. 26–30.
39. Santoro G.A., Fortling B. The advantages of volume rendering in threedimensional endosonography of the anorectum // Dis. Colon Rectum. — 2007. — Vol. 50. — P. 359–368.
40. Schouten W.R., van Vroonhoven T.J. Treatment of anorectal abscess with
or without primary fistulectomy. Results of a prospective randomized trial // Dis, Colon Rectum. — 1991. — Vol. 34, N 1. — P. 60–63.
41. Scoma J.A., Salvati E.P., Rubin R.J. Current concepts of rectum and sphincter preservation in inflammatory bowel disease // Dis. Colon Rectum. — 1981. — Vol. 24, N 5. — P. 370–372.
42. Steele S.R, Kumar R., Feingold D.L. et al. Practice parameters for the management of perianal abscess and fistula-in-ano // Dis. Colon Rectum. — 2011. — Vol. 54. — P. 1465–1474.
43. Toyonaga T., Matsushima M., Tanaka Y. et al. Microbiological analysis and endoanal ultrasonography for diagnosis of anal fistula in acute anorectal sepsis // Int. J. Colorectal Dis. — 2007. — Vol. 22. — P. 209–213.
44. Toyonaga T., Tanaka Y., Song J.F. et al. Comparison of accuracy of physical examination and endoanal ultrasonography for preoperative assessment in patients with acute and chronic anal fistula // Tech. Coloproctol. —2008. — Vol. 12. — P. 217–223.
45. Vasilveski C.A. Anorectal abscesses and fistulas // The ASCRS Textbook of Colorectal Surgery / Eds B.G. Wolff, J.W. Fleshman, D.E. Beck et al. — N.Y.: Springer, 2007. — P. 192–214.
46. Weisman R.I., Orsay C.P., Pearl R.K., Abcarian H. The role of fistulography in fistula-in-ano: report of five cases // Dis. Colon Rectum. — 1991. — Vol. 34. — P. 181–184.
47. West R.L., Dwarkasing S., Felt-Bersma R.J. et al. Hydrogen peroxideenhanced three-dimensional endoanal ultrasonography and endoanal magnetic resonance imaging in evaluating perianal fistulas: agreement and patient preference // Eur. J. Gastroenterol. Hepatol. — 2004. — Vol. 16. — P. 1319–1324.
48. West R.L., Zimmerman D.D., Dwarkasing S. et al. Prospective comparison of hydrogen peroxide-enhanced three-dimensional endoanal ultrasonography and endoanal magnetic resonance imaging of perianal fistulas // Dis. Colon Rectum. — 2003. — Vol. 46. — P. 1407–1415.
49. Wang C., Lu G., Cao Y.Q. et al. Traditional Chinese surgical treatment for anal fistulae with secondary tracks and abscess // World J. Gastroenterol. — 2012. — Vol. 18, N 40. — P. 5702–5708.
ХРОНИЧЕСКИЙ ПАРАПРОКТИТ (СВИЩ ЗАДНЕГО ПРОХОДА, СВИЩ ПРЯМОЙ КИШКИ)
Введение
По статистическим данным, примерно 95% больных со свищами прямой кишки связывают начало заболевания с перенесенным острым парапроктитом. В 30–50% случаев после острого парапроктита у больных формируется свищ прямой кишки (УД 5, СР D [1–3]). К формированию свища прямой кишки предрасполагают простое вскрытие и дренирование абсцесса без ликвидации входных ворот инфекции. Через область пораженной анальной крипты или через входные ворота другой этиологии (травма) происходит постоянное инфицирование параректальных тканей из просвета кишки. Гнойный ход окружается стенкой из соединительной ткани, происходит постепенное формирование свища. По ходу свища в клетчатке при недостаточно хорошем дренировании могут формироваться инфильтраты и гнойные полости.
Заболеваемость свищом прямой кишки составляет 2 случая на 10 тыс. населения в год (УД 5, СР D [4]). Распространенность заболевания составляет 9 случаев на 100 тыс. населения (УД 5, СР D [5]). Наиболее часто заболевание развивается в возрасте от 30 до 50 лет, что обусловливает социальную значимость данного заболевания. Мужчины страдают несколько чаще, чем женщины (УД 5, СР D [4, 6, 7]).
Настоящие рекомендации по диагностике и лечению больных со свищом прямой кишки являются руководством для практических врачей, осуществляющих ведение и лечение пациентов с данной нозологией.
Рекомендации подлежат регулярному пересмотру в соответствии с новыми данными научных исследований в этой области. Данные рекомендации составлены на основании анализа литературы из базы данных PubMed, MEDLINE, Cochrane Collaboration, the Standards Practice Task Force of the American Society of Colon and Rectal Surgeon, Oxford Center for Evidence-based Medicine — Levels of Evidence.
Рекомендации включают следующие разделы: определение и классификация свищей прямой кишки, диагностика, хирургическое лечение. Для отдельных положений рекомендаций приведены уровни дока-
зательности согласно общепринятой классификации Оксфордского центра доказательной медицины (табл. 5.1). В зависимости от достоверности приводимых данных рекомендации разделены на степени A, B, C, D.
Таблица 5.1. Уровни доказательности и степени рекомендаций на основании классификации Оксфордского центра доказательной медицины
|
Уровень |
Исследования методов диагностики |
Исследования методов лечения |
|
1a |
Систематический обзор гомогенных диагностических исследований 1-го уровня |
Систематический обзор гомогенных РКИ |
|
1b |
Валидизирующее когортное исследование с качественным «золотым стандартом» |
Отдельное РКИ (с узким доверительным интервалом) |
|
1c |
Специфичность или чувствительность столь высокие, что положительный или отрицательный результат позволяет исключить/установить диагноз |
Исследование «Всё или ничего» |
|
2a |
Систематический обзор гомогенных диагностических исследований >2-го уровня |
Систематический обзор (гомогенных) когортных исследований |
|
2b |
Разведочное когортное исследование с качественным «золотым стандартом» |
Отдельное когортное исследование (включая РКИ низкого качества; т.е. с <80% пациентов, прошедших контрольное наблюдение) |
|
2c |
Нет |
Исследование «исходов»; экологические исследования |
|
3a |
Систематический обзор гомогенных исследований уровня 3b и выше |
Систематический обзор гомогенных исследований «случай–контроль» |
|
3b |
Исследование с непоследовательным набором или без проведения исследования «золотого стандарта» у всех испытуемых |
Отдельное исследование «случай– контроль» |
|
4 |
Исследование «случай–контроль» или исследование с некачественным или зависимым «золотым стандартом» |
Серия случаев (и когортные исследования или исследования «случай– контроль» низкого качества) |
|
5 |
Мнение экспертов без тщательной критической оценки или основанное на физиологии, лабораторные исследования на животных или разработка «первых принципов» |
Мнение экспертов без тщательной критической оценки, лабораторные исследования на животных или разработка «первых принципов» |
Табл. 5.1. Окончание
|
Уровень |
Исследования методов диагностики |
Исследования методов лечения |
|
Степень рекомендации | ||
|
A |
Согласующиеся между собой исследования 1-го уровня | |
|
B |
Согласующиеся между собой исследования 2-го или 3-го уровня или экстраполяция на основе исследований 1-го уровня | |
|
C |
Исследования 4-го уровня или экстраполяция на основе уровня 2 или 3 | |
|
D |
Доказательства 4-го уровня или затруднительные для обобщения или некачественные исследования любого уровня | |
ВАЛИДИЗАЦИЯ РЕКОМЕНДАЦИЙ
Настоящие рекомендации составлены общероссийской общественной организацией «Ассоциация колопроктологов России» и в предварительной версии были рецензированы независимыми экспертами, которых попросили прокомментировать прежде всего, насколько интерпретация доказательств, лежащих в основе рекомендаций, доступна для понимания. Получены комментарии со стороны врачей амбулаторного звена. Полученные комментарии тщательно систематизировались и обсуждались на совещаниях экспертной группы.
Последние изменения в настоящих рекомендациях были представлены для дискуссии на заседании профильной комиссии «Колопроктология» Экспертного совета Минздрава России 12 сентября 2013 г. Проект рекомендаций был повторно рецензирован независимыми экспертами и врачами амбулаторного звена. Для окончательной редакции и контроля качества рекомендации были повторно проанализированы членами экспертной группы, которые пришли к заключению, что все замечания и комментарии приняты во внимание, риск систематических ошибок при разработке рекомендаций сведен к минимуму.
ОБЛАСТЬ ПРИМЕНЕНИЯ РЕКОМЕНДАЦИЙ
Данные клинические рекомендации применимы при осуществлении медицинской деятельности в рамках Порядка оказания медицинской помощи взрослому населению с заболеваниями толстой кишки, анального канала и промежности колопроктологического профиля.
Определение
Хронический парапроктит (свищ заднего прохода, свищ прямой кишки) — хронический воспалительный процесс в анальной крипте, межсфинктерном пространстве и параректальной клетчатке, сопровождающийся формированием свищевого хода. При этом пораженная крипта
является внутренним отверстием свища. Наружное свищевое отверстие наиболее часто располагается на коже перианальной области, промежности, ягодичной области, во влагалище, или свищ может быть неполным внутренним, т.е. заканчивается слепо в мягких тканях (УД 5, СР D [8, 9]).
Свищи прямой кишки могут быть и другой этиологии:
n посттравматические, в том числе послеоперационные;
n свищи, дренирующие параректальные кисты;
n свищи при болезни Крона и т.д.
Код по Международной классификации болезней 10-го пересмотра
n Класс: Болезни органов пищеварения (XI).
n Код:
v К 60.3 Свищ заднего прохода
v К 60.4 Прямокишечный свищ
Профилактика
В настоящее время не существует каких-либо профилактических мер, которые могли бы препятствовать формированию свища заднего прохода или прямой кишки после вскрытия острого парапроктита. Возможным средством профилактики является своевременное хирургическое лечение острого парапроктита с адекватным дренированием гнойной полости и последующим контролем заживления раны (УД 5, СР D [9]).
Прежде всего следует убедиться, что пациенты после вскрытия острого парапроктита имеют ясное представление о возможности неполного заживления раны с последующим формированием свища или возможности рецидивирования гнойно-воспалительного процесса в параректальных тканях (УД 5, СР D [9]).
Необходимо убедиться, что пациенты после вскрытия острого парапроктита представляют всю важность своевременного извещения врача о возникновении любых клинических проявлений (УД 5, СР D [9]).
Возможная мера профилактики развития заболевания — своевременное лечение сопутствующих заболеваний аноректальной зоны (геморрой, анальная трещина, криптит) (УД 5, СР D [9]).
Скрининг
Формально специализированный скрининг на наличие свища заднего прохода и прямой кишки не показан. В то же время при проведении рутинного клинического обследования у больных с перечисленными ниже состояниями следует исключать возможность наличия свища заднего прохода и прямой кишки с помощью осмотра промежности, перианальной области, заднего прохода и пальцевого исследования прямой кишки (УД 5, СР D [9]).
n Наличие анамнестических указаний на перенесенный или периодически повторяющийся гнойно-воспалительный процесс мягких тканей в области промежности, заднего прохода, ягодичной области.
n Наличие жалоб на длительно не заживающую ранку, раздражение, зуд в области заднего прохода, промежности, ягодичной области, постоянные или периодически появляющиеся гнойные, серозные или сукровичные выделения из свищевого отверстия в перианальной области, области промежности, ягодичной области или из заднего прохода.
n Наличие жалоб на дискомфорт, боли в области заднего прохода, прямой кишки.
Классификация [8, 9]
Свищ заднего прохода и прямой кишки бывает:
n полным (есть внутреннее и наружное свищевое отверстие);
n неполным внутренним (наружного отверстия нет, есть только внутреннее).
По локализации внутреннего отверстия в анальном канале или прямой кишке:
n задний;
n передний;
n боковой.
В зависимости от расположения свищевого хода по отношению к наружному сфинктеру заднего прохода выделяют:
n интрасфинктерный;
n транссфинктерный;
n экстрасфинктерный.
Экстрасфинктерные свищи по сложности делятся на 4 степени [2]:
n первая степень экстрасфинктерного свища: внутреннее отверстие узкое, без рубцов вокруг него, нет гнойников и инфильтратов в клетчатке, ход достаточно прямой;
n вторая степень: в области внутреннего отверстия имеются рубцы, но нет воспалительных изменений в клетчатке;
n третья степень: внутреннее отверстие узкое без рубцового процесса вокруг, но в клетчатке имеется гнойно-воспалительный процесс;
n четвертая степень: внутреннее отверстие широкое, окружено рубцами, в параректальной клетчатке воспалительные инфильтраты или гнойные полости.
Отдельно выделяются свищи прямой кишки высокого уровня, при которых внутреннее свищевое отверстие расположено выше зубчатой линии, в нижнеампулярном отделе прямой кишки.
Формулировка диагноза
При формулировании диагноза следует отразить локализацию внутреннего свищевого отверстия, расположение свищевого хода по отношению к наружному анальному сфинктеру, наличие или отсутствие
наружного свищевого отверстия (полный или неполный свищ), а также наличие или отсутствие полостей, затеков по ходу свища и их локализацию. При экстрасфинктерных свищах дополнительно устанавливается степень сложности свища (см. раздел «Классификация»). Ниже приведены примеры формулировок диагноза.
n Передний интрасфинктерный свищ прямой кишки.
n Задний транссфинктерный свищ прямой кишки с ишеоанальным затеком.
n Боковой неполный внутренний транссфинктерный свищ прямой кишки.
n Задний экстрасфинктерный свищ прямой кишки 3-й степени сложности.
Диагностика
КЛИНИЧЕСКИЕ ДИАГНОСТИЧЕСКИЕ КРИТЕРИИ
К основным клиническим симптомам свища заднего прохода и прямой кишки относятся наличие наружного свищевого отверстия на коже перианальной области, промежности или ягодичной области, серозные, гнойные или сукровичные выделения из наружного свищевого отверстия, периодически возникающий болезненный инфильтрат в перианальной области, промежности, чаще всего расположенный в области наружного свищевого отверстия, дискомфорт, боли в области заднего прохода. При наличии обострения гнойно-воспалительного процесса в параректальной клетчатке возможно появление общих воспалительных симптомов, таких как повышение температуры тела, лихорадка (табл. 5.2).
Таблица 5.2. Клиническая картина свища зхаднего прохода и прямой кишки
|
Возможные клинические проявления болезни в анамнезе |
Типичные клинические симптомы в момент осмотра |
|
• Однократное или многократное вскрытие острого парапроктита. • Самопроизвольное вскрытие гнойника в области заднего прохода. • Боли неясного генеза в области заднего прохода и прямой кишки. • Гноевидные выделения из заднего прохода |
• Наличие наружного свищевого отверстия на коже. • Дискомфорт, боли в области заднего прохода. • Серозные, гнойные или сукровичные выделения из наружного свищевого отверстия и/или заднего прохода. • Воспалительный инфильтрат в мягких тканях перианальной области, промежности или ягодичной области |
Интрасфинктерные свищи — самые простые свищи, составляющие примерно 25–30% всех свищей прямой кишки. Также данные свищи называются подкожно-подслизистыми, краевыми.
Свищевой ход, как правило, бывает прямым, рубцовый процесс не выражен, давность заболевания обычно небольшая. Наружное свищевое
отверстие чаще всего локализуется вблизи от ануса, внутреннее может быть в любой из анальных крипт.
Диагностика этого вида свищей достаточно проста: пальпация перианальной области позволяет определить свищевой ход в подслизистом и подкожном слое, зонд, введенный в наружное свищевое отверстие, обычно свободно проходит в просвет кишки через внутреннее отверстие или подходит к нему в подслизистом слое. Проба с красителем (метиленовым синим) у больных с таким свищом обычно бывает положительной. Функция сфинктера сохранена. Фистулография и другие дополнительные методы исследования обычно не требуются.
Транссфинктерные свищи встречаются наиболее часто, составляют 40–45%. Причем отношение свищевого хода к наружному жому может быть разным: ход может идти через подкожную, поверхностную или еще выше — через глубокую порцию.
При низких транссфинктерных свищах ход определяется в мягких тканях в виде плотного тяжа, идущего от наружного свищевого отверстия к передней, задней или боковой стенке анального канала. Чем выше по отношению к сфинктеру расположен ход, тем чаще встречаются не прямые, а разветвленные ходы, чаще в клетчатке обнаруживаются полости затеков, сильнее выражен рубцовый процесс в тканях, окружающих ход, в том числе и в сфинктере.
Экстрасфинктерные свищи встречаются в 15–20% наблюдений. Свищевой ход располагается высоко, как бы огибает наружный сфинктер, но внутреннее отверстие находится в области крипт, т.е. ниже. Такие свищи, как правило, образуются вследствие острого пельвиоректального и ретроректального парапроктита. Для них характерно наличие длинного извитого хода, часто по ходу свища обнаруживаются гнойные затеки, рубцы. Нередко очередное обострение воспалительного процесса приводит к образованию новых свищевых отверстий. Иногда воспалительный процесс переходит из клетчаточного пространства одной стороны на другую и возникает подковообразный свищ. Подковообразный свищ может быть и задним, и передним. Проба с красителем у данной категории больных не всегда положительная, при зондировании определяется глубокий свищевой ход, чаще всего идущий параллельно прямой кишке. В область внутреннего свищевого отверстия, как правило, конец зонда не проникает.
При транссфинктерных и экстрасфинктерных свищах прямой кишки обследование больного необходимо дополнять фистулографией, эндоректальной ультрасонографией, магнитно-резонансной томографией (MPТ) для определения порции сфинктера, через которую проходит свищ, локализации внутреннего свищевого отверстия, оценки расположения гнойных полостей, а также для дифференциальной диагностики с другими заболевания, при которых могут появляться свищевой ход и свищевое отверстие (УД 1с, СР С [13–20, 23, 24]).
УСТАНОВЛЕНИЕ ДИАГНОЗА
Диагноз выставляется на основании сочетания данных анамнеза, клинической картины и типичных изменений выявляемых при ультразвуковом и/или рентгенологическом исследованиях. Для этого врачу необходимо провести следующее.
n Обязательные методы исследования при наличии свища заднего прохода или прямой кишки
v Сбор жалоб, анамнеза заболевания и анамнеза жизни.
v Наружный осмотр перианальной и крестцово-копчиковой области (определение локализации патологического процесса).
v Исследование анального рефлекса.
v Пальпация (определение наличия или отсутствия инфильтративных изменений мягких тканей в области свищевых отверстий, по ходу свища).
v Пальцевое исследование анального канала и прямой кишки [оценка функционального состояния запирательного аппарата прямой кишки (ЗАПК), локализации внутреннего свищевого отверстия, наличия сопутствующих заболеваний анального канала и прямой кишки, оценка наличия параректальных инфильтратов] (УД 5, СР D [10]).
v Зондирование хода (оценка расположения свищевого хода по отношению к анальному каналу, прямой кишке, оценка степени вовлеченности мышечных структур сфинктера, наличия полостей затеков по ходу свища) (УД 5, СР D [11, 12]).
v Проба с красителем (выявление сообщения наружного свищевого отверстия с просветом прямой кишки, прокрашивание дополнительных свищевых ходов и полостей) (УД 5, СР D [11, 12]).
v Аноскопия (визуализация внутреннего свищевого отверстия).
v Ректороманоскопия (диагностика сопутствующих заболеваний прямой и сигмовидной кишки).
n Дополнительные исследования при наличии свища заднего прохода или прямой кишки
v Колоноскопия (оценка наличия или отсутствия сопутствующих изменений толстой кишки, воспалительных изменений, характерных для болезни Крона и язвенного колита).
v Фистулография (метод выбора при свищах прямой кишки с наличием полостей затеков в параректальных клетчаточных пространствах, при высоко расположенном внутреннем свищевом отверстии, при подковообразных, рецидивных экстрасфинктерных свищах, при дифференциальной диагностике между свищом прямой кишки и параректальной кистой) (УД 1с, СР С [13]).
v Ультрасонография ректальным датчиком, в том числе трехмерная (метод выбора для оценки расположения свищевого хода по отношению к анальному сфинктеру, для уточнения расположения внутреннего свищевого отверстия, диагностики параректальных и межсфинктерных затеков, выявления дополнительных свищевых ходов, оценки расположения свищевого хода при неполных внутренних свищах прямой кишки) (УД 1с, СР С [14–20]).
v Компьютерная томография (КТ) малого таза и промежности (метод выбора при диагностике пельвиоректальных затеков, для оценки расположения свищевых ходов и полостей у пациентов с перианальными осложнениями при болезни Крона) (УД 1, СР С [21, 22]).
v Магнитно-резонансная томография малого таза (наряду с УЗИ-ректальным датчиком является методом выбора для оценки расположения свищевого хода по отношению к анальному сфинктеру, уточнения локализации внутреннего свищевого отверстия, диагностики параректальных и межсфинктерных затеков, выявления дополнительных свищевых ходов) (УД 1а, СР А [20, 23, 24]).
v Исследование функционального состояния замыкательного аппарата прямой кишки (показано перед операцией у больных с изначальными нарушениями функции анального сфинктера, у больных, ранее оперированных по поводу свища заднего прохода или прямой кишки, у больных, которым предстоит операция по поводу транссфинктерного свища, захватывающего более 30% сфинктера, экстрасфинктерного свища или свища высокого уровня) (УД 4, СР В [10]).
ДИФФЕРЕНЦИАЛЬНАЯ ДИАГНОСТИКА
При подозрении на свищ прямой кишки дифференциальная диагностика начинается с исключения воспалительных заболеваний кожи и мягких тканей, которые не имеют связи с анальным каналом и прямой кишкой (УД 5, СР D [25]). Кроме того, дифференциальную диагностику проводят:
n со специфическими инфекциями (туберкулез, актиномикоз);
n воспалительными заболеваниями кишечника с перианальными осложнениями (болезнь Крона, язвенный колит);
n параректальными кистами, тератомами;
n хроническим воспалением ЭКХ;
n хроническим остеомиелитом костей таза.
При туберкулезе легких, кишечника нельзя исключать и банальные свищи прямой кишки. Подозрение на специфический процесс вызывают случаи, когда из свищей обильно выделяется жидкий гной, при гистологическом исследовании обнаруживаются многочисленные сливающиеся гранулемы с казеозным некрозом. В редких случаях бывает озлокачествление свища прямой кишки, при этом выделения из него становятся кровянистыми с примесью слизи. Надежным методом диагностики является цитологическое исследование соскоба из свищевого хода, причем соскоб лучше делать из глубокой части хода, а не из области наружного отверстия (УД 5, СР D [26]).
Хирургическое лечение
ПОКАЗАНИЯ ДЛЯ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ
Показания. Единственный радикальный метод лечения свищей прямой кишки — хирургический (УД 5, СР D [9]).
Противопоказания. Тяжелые заболевания различных органов и систем в стадии декомпенсации. Если удается добиться улучшения состояния после проведенного лечения, то операция становится возможной.
Сроки выполнения радикальной операции определяются в основном клиническим течением болезни. Большинство больных оперируются в плановом порядке. При обострении хронического парапроктита с формированием абсцесса операция проводится, как и при остром парапроктите в неотложном порядке. Нецелесообразно откладывать радикальное лечение надолго, потому что обострение может повториться, воспалительный процесс с последующим рубцеванием стенки анального канала, сфинктера и параректальной клетчатки может привести к деформации анального канала и промежности и к развитию недостаточности анального сфинктера.
Наиболее распространенные виды операций при свищах прямой кишки
(УД 5, СР D [8, 9]):
n иссечение свища в просвет прямой кишки;
n иссечение свища в просвет прямой кишки со вскрытием и дренированием затеков;
n иссечение свища в просвет прямой кишки с ушиванием сфинктера;
n иссечение свища с проведением эластичной лигатуры;
n иссечение свища с перемещением слизисто-подслизистого, слизистомышечного или полнослойного лоскута прямой кишки в анальный канал.
Выбор метода операции в основном определяется с учетом следующих характеристик:
n локализация свищевого хода по отношению к наружному сфинктеру заднего прохода;
n степень развития рубцового процесса в стенке кишки, области внутреннего отверстия и по ходу свища;
n наличие гнойных полостей и инфильтратов в параректальной клетчатке.
ВИДЫ ХИРУРГИЧЕСКИХ ВМЕШАТЕЛЬСТВ
Хирургическое лечение интрасфинктерных и транссфинктерных свищей, захватывающих дистальную треть наружного сфинктера
Рассечение или иссечение свища в просвет кишки
Методика. Свищевой ход рассекается в просвет кишки на зонде или иссекается из окружающих тканей на зонде. Рана не ушивается или производится подшивание краев раны ко дну.
В настоящее время нет однозначного ответа на вопрос, какой объем мышечных структур может быть рассечен при операции по поводу свища заднего прохода или прямой кишки. Эффективность операции рассечения или иссечения свища в просвет кишки достаточно высока и колеблется от 92 до 97% (УД b, СР В [27, 28]). Вероятность возникновения нарушения функции держания после иссечения свища в просвет кишки, по данным литературы, колеблется от 0 до 45% (УД 2b, СР В [27, 29–37]). Широкий разброс процентного соотношения пациентов, у которых после операции развивается нарушение функционального состояния ЗАПК,
возможно, связан с различными подходами к его оценке, различными сроками наблюдения за пациентами в послеоперационном периоде.
Факторы риска развития анальной инконтиненции после рассечения или иссечения свища в просвет кишки: наличие признаков недостаточности анального сфинктера в предоперационном периоде, рецидивный характер свища, женский пол, свищи, захватывающие более 30% наружного сфинктера, а также пациенты, ранее перенесшие операции по поводу заболевания заднего прохода и промежности (УД 1b, СР В [27, 38–40]). Подшивание краев раны ко дну после ликвидации свища уменьшает риск развития кровотечения в послеоперационном периоде, улучшает процесс
заживления раны (средний срок заживления 4 нед) (УД 1c, СР В [41, 42]). По данным отдельных авторов, сравнивающих два метода — иссече-
ние свища в просвет кишки и рассечение свища в просвет кишки, было установлено, что после иссечения свища отмечается более длительное заживление раны, послеоперационные раны имеют большие размеры, выше риск развития недостаточности анального сфинктера. Частота рецидивов заболевания при сравнении двух данных подходов статистически значимо не различается (УД 1c, СР В [43, 44]).
Лечение свищей путем введения в свищевой ход фибринового клея
Методика. После обработки свищевого хода с помощью щеточки или ложечки Фолькмана с целью максимального удаления некротических тканей и грануляций, с помощью шприца производят заполнение свища фибриновым клеем.
Данный метод имеет несколько преимуществ: простая техника вмешательства, возможность повторного выполнения процедуры, отсутствие повреждающего влияния на мышечные структуры промежности.
Методика обладает преимуществом у пациентов с высоким риском развития недостаточности анального сфинктера или с уже имеющейся анальной инконтиненцией.
Проведенные исследования показали, что данный метод эффективен у 40–78% пациентов со свищами, захватывающими менее 30% анального сфинктера (УД 1b, СР B [45–53]). Однако при выборе метода лечения интраи транссфинктерных свищей, захватывающих небольшую порцию анального сфинктера, способ значительно уступает операции рассечения или иссечения свища в просвет кишки, при которой риск развития нарушения функции ЗАПК также является низким.
Хирургическое лечение транссфинктерных свищей, захватывающих более трети наружного сфинктера, и экстрасфинктерных свищей прямой кишки
Лечение свищей путем введения в свищевой ход фибринового клея
Методика. (См. выше.)
В рандомизированном исследовании, проведенном I. Lindsey и соавт. (УД 2, СР C [51]), было показано, что использование фибринового клея
привело к заживлению свища у 69% больных. В других исследованиях, где не использовалась рандомизация, приводятся данные об эффективности метода у 10–67% пациентов с высокими чрессфинктерными и экстрасфинктерными свищами прямой кишки (УД 2a, СР C [46–48, 54, 55]). Хотя частота заживления свищей при использовании фибринового клея недостаточно высока, учитывая малотравматичный характер процедуры, отсутствие влияния на сфинктерный аппарат прямой кишки, способ может быть рекомендован в качестве первичной процедуры при хирургическом лечении у больных со свищами, захватывающими
более трети сфинктера, и с экстрасфинктерными свищами.
Лечение свищей с помощью герметизирующих тампонов
Герметизирующие тампоны из биологического материала (подслизистая основа кишки свиньи, межклеточный матрикс дермы, биологически совместимые искусственные материалы — полигликоевая кислота) используются для лечения свищей прямой кишки с целью закрытия внутреннего свищевого отверстия с последующим заживлением свищевого хода. Биологический материал, из которого изготовлен тампон, служит основой для облитерации свищевого хода (УД 2a, СР C [57, 58]).
Методика. После обработки свищевого хода с помощью щеточки
или ложечки Фолькмана с целью максимального удаления некротических тканей и грануляций в свищевой ход вводится герметизирующий тампон, полностью заполняющий свищ. Дистальный конец тампона выводится через наружное свищевое отверстие. Расширенная часть герметизирующего тампона, расположенная в области внутреннего свищевого отверстия, для более надежной фиксации подшивается несколькими швами к краям слизистой оболочки со стороны просвета прямой кишки.
По литературным данным, методика эффективна в 70–100% случаев у пациентов со свищами, захватывающими менее трети наружного сфинктера. У пациентов с более высокими свищами данный метод имеет меньшую эффективность (УД 2a, СР C [56–59]).
Приводятся данные о применении герметизирующих тампонов у больных со свищами прямой кишки, захватывающими более трети наружного сфинктера на фоне болезни Крона. Хорошие результаты в исследовании получены в 80–83% случаев (УД 2, СР C [56, 59]). Однако, по данным большинства других исследований, эффективность метода значительно меньше и составляет менее 50% (УД 2c, СР C [56, 57, 60–62]). Возможно, это обусловлено более длительным периодом наблюдения за пациентами.
Малотравматичный характер операции, отсутствие влияния на сфинктерный аппарат прямой кишки, возможность повторения процедуры считаются аргументом в пользу применения метода в качестве первоначального у больных со свищами, захватывающими более трети сфинктера, и экстрасфинктерными свищами.
Иссечение свища с низведением лоскута стенки прямой кишки
Методика. Низведение лоскута прямой кишки — сфинктеросохраняющая операция, при которой производят иссечение свищевого хода, мобилизацию лоскута стенки прямой кишки (лоскут может состоять из слизистой оболочки, слизисто-подслизистого слоя или может быть полностенным) протяженностью, достаточной для закрытия внутреннего свищевого отверстия. Путем низведения лоскута и подшивания его края к коже перианальной области происходит закрытие внутреннего свищевого отверстия.
По литературным данным, метод эффективен в 44–87% случаев (УД 1c, СР C [63–65]). Факторами, увеличивающими риск развития рецидива свища после данной операции, служат ранее проведенная лучевая терапия, болезнь Крона в стадии обострения, проктит в фазе обострения, развитие свища на фоне злокачественного процесса, ранее перенесенные операции в аноректальной области (УД 1c, СР C [27, 64, 66–69]).
Хотя при низведении лоскута отсутствует прямое повреждающее воздействие на анальный сфинктер, в 7–38% случаев отмечается явление незначительной или умеренно выраженной анальной инконтиненции, что подтверждается данными аноректальной манометрии в послеоперационном периоде (снижение давления в анальном канале в покое и при волевом сокращении) (УД 1, СР C [66, 70–72]).
Иссечение свища с проведением лигатуры
Методика. Метод использования лигатуры при хирургическом лечении свищей заднего прохода и прямой кишки имеет 2 основных варианта. При наличии острого или хронического гнойно-воспалительного процесса в области свища лигатура может выполнять функцию дренирования с последующим формированием прямого свищевого хода с четко отграниченными стенками (дренирующая лигатура, как правило, накладывается на срок 6–8 нед). Данный вариант проведения лигатуры является первым этапом перед радикальным хирургическим лечением свища.
Второй вариант — проведение лигатуры (шелковой или латексной) с целью постепенного рассечения свищевого хода и волокон сфинктера путем периодического затягивания лигатуры. Медленное рассечение мышечных волокон сфинктера лигатурой препятствует их расхождению, что направлено на профилактику развития недостаточности анального сфинктера в послеоперационном периоде.
Частота ухудшения функции анального держания при использовании лигатурного метода, по литературным данным, колеблется от 0 до 54%; данное осложнение чаще встречается при использовании пересекающей лигатуры. При этом наиболее часто у пациентов отмечается недержание газов, чем жидкий и оформленный стул (УД 1c, СР В [73–78]).
Несмотря на большое количество литературных данных, имеется лишь 4 рандомизированных контролируемых исследования, в которых
получены различные результаты использования лигатурного метода (УД 1c, СР В [51, 79–81]). В тех случаях, когда лигатуру проводят с дренирующей целью, с последующим выполнением второго радикального этапа для ликвидации свища (низведение лоскута стенки прямой кишки, фибриновый клей, герметизирующий тампон), частота хороших результатов колеблется от 62 до 100% в зависимости от варианта радикальной операции (УД 1c, СР В [73–76, 82]).
Использование лигатуры является эффективным методом и может применяться для лечения чрессфинктерных свищей, захватывающих более 50% наружного сфинктера и экстрасфинктерных свищей прямой кишки, в особенности в тех случаях, когда с помощью других методов не удается добиться хорошего результата.
Иссечение свища с ушиванием сфинктера
Методика. Метод заключается в иссечении свищевого хода с пересечением порции сфинктера, через которую идет свищ, и последующим ушиванием концов пересеченной части жома.
По данным исследований, в которых методика применялась для лечения высоких чрессфинктерных и экстрасфинктерных свищей прямой кишки, эффективность метода составила 54–97% (УД 1b, СР A [83–86]). Нарушение функции анального сфинктера встречается в 4–32% наблюдений. Расхождение краев ушитого сфинктера или нагноение раны значительно увеличивает риск развития анальной инконтиненции, в особенности у пациентов с экстрасфинктерными свищами (УД 1b,
СР A [85]).
Частота хороших результатов после иссечения свища с ушиванием сфинктера в среднем составляет 60–80% и сопоставима с результатами других методик (УД 1b, СР A [83–86]).
В связи с достаточно высоким риском развития анальной инконтиненции после данной операции пациенты должны быть заранее предупреждены о характере хирургического вмешательства, возможных последствиях и осложнениях.
Метод лечения свищей с помощью перевязки и пересечения свищевого хода в межсфинктерном пространстве (LIFT)
Методика. Заключается в перевязке и пересечении части свищевого
хода, проходящей в межсфинктерном пространстве (УД 5, СР D [87–89]). С целью обеспечения адекватного дренирования дистальную часть свищевого хода в области наружного свищевого отверстия иссекают или производят расширение наружного свищевого отверстия.
Как правило, операцию выполняют после установки в свищевой ход на 6–8 нед дренирующей латексной лигатуры, что способствует формированию прямого свища с фиброзными стенками и значительно уменьшает риск сохранения полостей затеков по ходу свища.
Положительной характеристикой данной операции является отсутствие повреждающего воздействия на мышечные структуры аналь-
ного сфинктера, что служит профилактикой развития анальной инконтиненции.
По данным исследований, оценивающих эффективность данной операции, заживление свища происходит в 57–94% случаев при среднем периоде наблюдения за пациентами от 3 до 8 мес. Частота рецидива заболевания составляет 6–18% (УД 5, СР D [87–89]).
В связи с небольшим количеством исследований относительно данного варианта хирургического лечения свищей заднего прохода и прямой кишки в настоящее время уровень доказательности приведенных данных оценить невозможно.
Лечение свищей заднего прохода и прямой кишки, связанных с болезнью Крона
Перианальные поражения при болезни Крона встречаются в 40–80% случаев (УД 4, СР С [90]). Выбор метода лечения свища прямой кишки при болезни Крона — сложная задача и требует индивидуального подхода.
Как правило, лечение свищей на фоне болезни Крона начинается с консервативных мероприятий на фоне терапии основного заболевания. В 90% случаев применение антибактериальных препаратов, метронидазола способствует уменьшению выраженности перианальных поражений (УД 4, СР С [91]).
По отдельным данным литературы, использование в терапии 6-меркаптопурина (6-МП), циклоспорина также способствует уменьшению выраженности воспалительного процесса при наличии свищей прямой кишки на фоне болезни Крона (УД 1b, СР B [92–94]).
Применение инфлексимаба и других препаратов моноклональных антител к фактору некроза опухоли способствует заживлению свищей заднего прохода и прямой кишки в среднем в 46% случаев (УД 4, СР С [95]).
Несмотря на хорошие результаты консервативной терапии болезни Крона с перианальными поражениями, выбор метода лечения у каждого пациента индивидуальный, зависит от тяжести основного заболевания, выраженности симптоматики. Методом выбора лечения у больных с выраженной активностью воспалительного процесса в перианальной области с формированием свищей на фоне обострения болезни Крона является формирование постоянной стомы или операция, сопровождающаяся удалением пораженной прямой кишки (УД 4, СР С [96–99]).
Наличие свища заднего прохода или прямой кишки без каких-либо клинических проявлений у пациентов с болезнью Крона не требует хирургической коррекции.
Свищи заднего прохода и прямой кишки на фоне болезни Крона могут
быть вторичными, т.е. связанными с основным заболеванием, но также могут быть связаны с воспалительным процессом в криптогландулярной
зоне. Независимо от этиологии развития свища при отсутствии какихлибо его проявлений, т.е. при бессимптомном течении, отсутствии воспалительного процесса, хирургическое лечение не требуется (УД 1c, СР C [100, 101]). В таких случаях свищ на протяжении длительного срока может не давать каких-либо симптомов, однако пациенты должны быть предупреждены о возможности выполнения операции по поводу свища в дальнейшем.
Хирургическое лечение интрасфинктерных и транссфинктерных свищей, захватывающих дистальную треть наружного сфинктера на фоне болезни Крона
Метод выбора хирургического лечения — рассечение или иссечение свища в просвет кишки.
Рассечение или иссечение свища в просвет кишки является достаточно безопасным и эффективным оперативным вмешательством при интрасфинктерных свищах и свищах, захватывающих дистальную треть наружного сфинктера (УД 1c, СР C [91, 102]). Учитывая хроническое течение заболевания и высокую вероятность рецидива, во время операции требуется максимальное сохранение мышечных структур ЗАПК. В связи с этим перед выполнением операции должен быть учтен ряд факторов: активность воспалительного процесса в прямой кишке, функциональное состояние ЗАПК, наличие ранее перенесенных операций на прямой кишке и промежности, частота и консистенция стула.
При тщательном отборе пациентов хорошие результаты при данной операции отмечаются в 56–100% случаев. Частота развития умеренно выраженного нарушения функции держания кишечного содержимого составляет 6–12% (УД 1c, СР C [28, 73, 102–104]).
Хирургическое лечение транссфинктерных свищей, захватывающих более трети наружного сфинктера, и экстрасфинктерных свищей прямой кишки
Использование дренирующей лигатуры на протяжении длительного срока может значительно улучшить результаты хирургической коррекции высоких чрессфинктерных и экстрасфинктерных свищей.
При транссфинктерных свищах, захватывающих более трети наружного сфинктера и экстрасфинктерных свищах прямой кишки, ассоциированных с болезнью Крона, требуется установка дренирующей лигатуры на срок 6 нед и более с целью адекватного дренирования гнойной полости и предотвращения закрытия наружного свищевого отверстия (УД 1c, СР C [90, 91, 102]). Однако, несмотря на проведение данного вмешательства, в среднем у 20–40% пациентов периодически происходит обострение воспалительного процесса в параректальной клетчатке (УД 1c, СР C [76, 105, 106]). По последним литературным данным, сочетанное использование дренирующей лигатуры с биологической терапией препаратом инфликсимаб позволяет добиться заживления свищевого хода у 24–78% пациентов. Для 25–100% данных больных в последующем требуется продолжение терапии инфлексимабом (УД 1c, СР C [107–109]).
Иссечение свища с низведением лоскута стенки прямой кишки у пациентов с болезнью Крона (при отсутствии воспалительных изменений слизистой оболочки прямой кишки)
Операция с низведением лоскута стенки прямой кишки может использоваться у пациентов с высокими чрессфинктерными и экстрасфинктерными свищами на фоне болезни Крона при условии отсутствия обострения воспалительного процесса в прямой кишке. Анализ непосредственных результатов показал эффективность данной операции у 64–75% больных (УД 2c, СР C [64, 69, 110, 111]). Частота рецидивов свища несколько возрастает при увеличении периода наблюдения за оперированными больными (УД 2c, СР C [98, 112]). При наличии обострения воспалительного процесса в прямой кишке использование биологических препаратов может в последующем дать возможность выполнения операции с низведением лоскута.
Лечение свищей прямой кишки высокого уровня
При расположении внутреннего свищевого отверстия выше зубчатой линии: в области аноректального перехода или нижнеампулярном отделе прямой кишки (свищ высокого уровня), при выраженных гнойно-воспалительных, инфильтративных изменениях в параректальной клетчатке и стенке прямой кишки, у некоторых пациентов требуется проведение многоэтапного хирургического лечения. В качестве первого этапа с целью отключения пассажа кишечного содержимого по прямой кишке больным выполняют формирование двуствольной колостомы. На втором этапе после ликвидации воспалительных, инфильтративных изменений выполняют оперативное вмешательство по поводу свища прямой кишки (иссечение свища с низведением лоскута стенки прямой кишки). При хорошем исходе операции, заживлении раны в качестве третьего этапа выполняют внутрибрюшное закрытие колостомы (через 2–6 мес) (УД 5, СР D [9]).
Чего нельзя делать (УД 5, СР D [8, 9])
n Не следует выполнять пластические операции (низведение лоскута стенки прямой кишки, ушивание сфинктера) при интрасфинктерных свищах и свищах, захватывающих незначительную порцию наружного сфинктера.
n Не следует начинать лечение высоких чрессфинктерных и экстрасфинктерных свищей прямой кишки при отсутствии выраженного рубцового и гнойно-воспалительного процесса, нормальном функциональном состоянии ЗАПК, с операции рассечения или иссечения свища с ушиванием сфинктера в связи с высоким риском нарушения функции держания анального сфинктера.
n Не следует применять методы лечения свищей с использованием фибринового клея или биологических тампонирующих материалов при наличии полостей, затеков по ходу свища в связи с высоким риском рецидива заболевания.
n Не следует стремиться к выполнению одномоментного радикального вмешательства при наличии выраженного гнойно-воспалительного процесса в параректальных тканях у пациентов с высокими чрессфинктерными, экстрасфинктерными свищами и свищами высокого уровня. Некоторым больным в данном случае требуется временное проведение дренирующей латексной лигатуры, а в отдельных случаях формирование двуствольной колостомы.
n Не следует выполнять пластические операции у больных со свищами прямой кишки на фоне болезни Крона при обострении воспалительного процесса в прямой кишке.
Дальнейшее ведение (УД 5, СР D [9])
n В послеоперационном периоде пациентам, перенесшим операцию по поводу свища заднего прохода или прямой кишки, требуется регулярное выполнение перевязок, заключающихся в очищении ран растворами антисептиков и нанесении на раневую поверхность мазевых основ на водорастворимой основе.
n До настоящего времени нет определенных данных о необходимости применения антибактериальных препаратов в послеоперационном периоде (УД 1b, СР B [113, 114]). Возможно, проведение антибактериальной терапии целесообразно после пластических операций по поводу свища прямой кишки (низведение лоскута стенки прямой кишки, иссечение свища с ушиванием сфинктера), а также при наличии выраженного воспалительного процесса в параректальных тканях и стенке прямой кишки с целью ускорения его купирования.
n Необходимость смягчения стула с помощью диеты и приема слабительных препаратов целесообразно после пластических операций по поводу свища прямой кишки.
Прогноз
Операции по поводу свищей прямой кишки требуют знания анатомии, физиологии и клинического опыта. Поэтому плановое лечение больных со свищами прямой кишки следует проводить только в специализированных стационарах.
Основные осложнения после операции — это рецидив свища и недостаточность анального сфинктера. Причинами рецидива могут быть как ошибки в выборе метода операции, так и технические погрешности, а также дефекты в послеоперационном ведении больного.
Критерии оценки качества помощи в стационаре представлены в таблице 5.3. Для оценки качества медицинской помощи используют временные, процессуальные и профилактирующие критерии. Временные характеризуют своевременность оказания определенных этапов медицинской помощи. Выполнение пациенту ряда медицинских манипуляций, инструментальных и лабораторных исследований, необходимых для качественного оказания медицинской помощи, оценивают
в процессуальных критериях. Для анализа мероприятий, направленных на предотвращение развития осложнений, используют профилактирующие критерии.
Таблица 5.3. Критерии оценки качества медицинской помощи в стационаре больным с доброкачественными заболеваниями промежности, прямой кишки и анального канала (свищ прямой кишки) (0 — нет, 1 — да)
|
Клинические рекомендации |
Временные |
Процессуальные |
Профилактирующие |
|
Клинические рекомендации по диагностике и лечению взрослых пациентов с хроническим парапроктитом (свищ заднего прохода, прямокишечный свищ, аноректальный свищ) (код МКБ — К60: K60.3; К60.4; K60.5) |
Установка клинического диагноза в течение 72 ч: 0/1 |
Оценка анального рефлекса: 0/1. Пальцевое исследование прямой кишки: 0/1. Аноскопия: 0/1. Ректороманоскопия: 0/1. Определение группы крови: 0/1. Исследование крови на сифилис, вирусный гепатит В, вирусный гепатит С: 0/1. Клинический анализ крови; биохимический анализ крови; клинический анализ мочи; коагулограмма: 0/1. Метод оперативного лечения в соответствии с клиническими рекомендациями: 0/1. Метод анестезии в соответствии с объемом оперативного лечения: 0/1 |
Отсутствие осложнений: • кровотечение: 0/1; • абсцесс: 0/1; • флегмона: 0/1; • пневмония: 0/1; • тромбоэмболия: 0/1; • летальный исход: 0/1 |
Литература
1. Аминев A.M. Руководство по проктологии. — М., 1973. — Т. 3. — С. 63–345.
2. Дульцев Ю.В., Саламов К.Н. Парапроктит. — М., 1981.
3. Федоров В.Д., Дульцев Ю.В. Проктология. — М, 1984. — С. 136–154, 299–307.
4. Ommer A., Herold A., Berg E. et al. Cryptoglandular anal fistulas // Dtsch. Arztebl. Int. — 2011. — Vol. 108, N 42. — P. 707–713.
5. Bleier J., Moloo H. Current management of cryptoglandular fistula-in-ano // World J. Gastroenterol. — 2011. — Vol. 17, N 28. — P. 3286–3291.
6. Zanotti C., Martinez-Puente C., Pascual I. et al. An assessment of the incidence of fistula-in-ano in four countries of the European Union // Int. J. Colorectal Dis. — 2007. — Vol. 22. — P. 1459–1462.
7. Sainio P. Fistula-in-ano in a defined population. Incidence and epidemiological aspects // Ann. Chir. Gynaecol. — 1984. — Vol. 73. — P. 219–224.
8. Воробьев Г.И. Основы колопроктологии. — М., 2006. — С. 135–152.
9. Шелыгин Ю.А., Благодарный Л.А. Справочник колопроктолога. — М.: Литтерра, 2012.
10. Becker A., Koltun L., Sayfan J. Simple clinical examination predicts complexity of perianal fistula // Colorectal Dis. — 2006. — Vol. 8. — P. 601–604.
11. Schwartz D.A., Wiersema M.J., Dudiak K.M. et al. A comparison of endoscopic ultrasound, magnetic resonance imaging, and exam under anesthesia for evaluation of Crohn’s perianal fistulas // Gastroenterology. — 2001. — Vol. 121. — P. 1064–1072.
12. Gonzalez-Ruiz C., Kaiser A.M., Vukasin P. et al. Intraoperative physical
diagnosis in the management of anal fistula // Am. Surg. — 2006. — Vol. 72. — P. 11–15.
13. Weisman R.I., Orsay C.P., Pearl R.K., Abcarian H. The role of fistulography in fistula-in-ano: report of five cases // Dis. Colon Rectum. — 1991. — Vol. 34. — P. 181–184.
14. Bussen D., Sailer M., Wening S. et al. Wertigkeit der analen Endosonographie
in der Diagnostik anorektaler Fisteln // Zentralbl. Chir. — 2004. — Vol. 129. — P. 404–407.
15. Lengyel A.J., Hurst N.G., Williams J.G. Pre-operative assessment of anal fistulas using endoanal ultrasound // Colorectal Dis. — 2002. — Vol. 4. — P. 436–440.
16. Maor Y., Chowers Y., Koller M. et al. Endosonographic evaluation of perianal fistulas and abscesses: comparison of two instruments and assessment of the role of hydrogen peroxide injection // J. Clin. Ultrasound. — 2005. — Vol. 33. — P. 226–232.
17. Ratto C., Grillo E., Parello A. et al. Endoanal ultrasound-guided surgery for
anal fistula // Endoscopy. — 2005. — Vol. 37. — P. 722–728.
18. Toyonaga T., Matsushima M., Tanaka Y. et al. Microbiological analysis and endoanal ultrasonography for diagnosis of anal fistula in acute anorectal sepsis // Int. J. Colorectal Dis. — 2007. — Vol. 22. — P. 209–213.
19. Toyonaga T., Tanaka Y., Song J.F. et al. Comparison of accuracy of physical examination and endoanal ultrasonography for preoperative assessment in patients with acute and chronic anal fistula // Tech. Coloproctol. — 2008. — Vol. 12. — P. 217–223.
20. Buchanan G.N., Halligan S., Bartram C.I. et al. Clinical examination,
endosonography, and MR imaging in preoperative assessment of fistula-in-ano: comparison with outcome-based reference standard // Radiology. — 2004. — Vol. 233. — P. 674–681.
21. Guillaumin E., Jeffrey R.B.Jr., Shea W.J. et al. Perirectal inflammatory disease: CT findings // Radiology. — 1986. — Vol. 161. — P. 153–157.
22. Yousem D.M., Fishman E.K., Jones B. Crohn disease: perianal and perirectal findings at CT // Radiology. — 1988. — Vol. 167. — P. 331–334.
23. Sahni V.A., Ahmad R., Burling D. Which method is best for imaging of perianal fistula? // Abdom. Imaging. — 2008. — Vol. 33. — P. 26–30.
24. Schaefer O., Lohrmann C., Langer M. Assessment of anal fistulas with highresolution subtraction MR-fistulography: comparison with surgical findings //
J. Magn. Reson. Imaging. — 2004. — Vol. 19. — P. 91–98.
25. Nelson J., Billingham R. Pilonidal disease and hidradenitis suppurativa // The ASCRS Textbook of Colon and Rectal Surgery / Eds B.G. Wolff, J.W. Fleshman,
D.E. Beck et al. — N.Y.: Springer, 2007. — P. 228–235.
26. Gaertner W.B., Hagerman G.F., Finne C.O. et al. Fistula-associated anal adenocarcinoma: good results with aggressive therapy // Dis. Colon Rectum. — 2008. — Vol. 51. — P. 1061–1067.
27. Garcia-Aguilar J., Belmonte C., Wong W.D. et al. Anal fistula surgery: factors associated with recurrence and incontinence // Dis. Colon Rectum. — 1996. — Vol. 39. — P. 723–729.
28. Davies M., Harris D., Lohana P. et al. The surgical management of fistula-
in-ano in a specialist colorectal unit // Int. J. Colorectal Dis. — 2008. — Vol. 23. — P. 833–838.
29. Stelzner F., Dietl H., Hahne H. Ergebnisse bei Radikaloperationen von 143 Analfisteln (Kritik der einzeitigen Sphinktertrennung bei ein — oder mehrzeitigen Fisteloperationen) // Chirurg. — 1956. — Vol. 27. — P. 158–162.
30. Van der Hagen S.J., Baeten C.G., Soeters P.B., van Gemert W.G. Long-
term outcome following mucosal advancement flap for high perianal fistulas and fistulotomy for low perianal fistulas: recurrent perianal fistulas: failure of treatment or recurrent patient disease? // Int. J. Colorectal Dis. — 2006. — Vol. 21. — P. 784–790.
31. Bokhari S., Lindsey I. Incontinence following sphincter division for treatment of anal fistula // Colorectal Dis. — 2010. — Vol. 12. — P. 135–139.
32. Parks A.G., Stitz R.W. The treatment of high fistula-in-ano // Dis. Colon Rectum. — 1976. — Vol. 19. — P. 487–499.
33. Van Tets W.F., Kuijpers H.C. Continence disorders after anal fistulotomy // Dis. Colon Rectum. — 1994. — Vol. 37. — P. 1194– 1197.
34. Mylonakis E., Katsios C., Godevenos D. et al. Quality of life of patients after surgical treatment of anal fistula; the role of anal manometry // Colorectal Dis. — 2001. — Vol. 3. — P. 417–421.
35. Westerterp M., Volkers N.A., Poolman R.W., van Tets W.F. Anal fistulotomy
between Skylla and Charybdis // Colorectal Dis. — 2003. — Vol. 5. — P. 549–551.
36. Van Koperen P.J., Wind J., Bemelman W.A. et al. Long-term functional outcome and risk factors for recurrence after surgical treatment for low and high perianal fistulas of cryptoglandular origin // Dis. Colon Rectum. — 2008. — Vol. 51. — P. 1475–1481.
37. Toyonaga T., Matsushima M., Tanaka Y. et al. Non-sphincter splitting fistulectomyvs conventional fistulotomy for high trans-sphincteric fistula-in-ano: a prospective functional and manometric study // Int. J. Colorectal Dis. — 2007. — Vol. 22. — P. 1097–1102.
38. Jordán J., Roig J.V., García-Armengol J. et al. Risk factors for recurrence
and incontinence after anal fistula surgery // Colorectal Dis. — 2010. — Vol. 12, N 3. — P. 254–260.
39. Van Koperen P.J., Wind J., Bemelman W.A. et al. Long-term functional outcome and risk factors for recurrence after surgical treatment for low and high perianal fistulas of cryptoglandular origin // Dis. Colon Rectum. — 2008. — Vol. 51. — P. 1475–1481.
40. Van Tets W.F., Kuijpers H.C. Continence disorders after anal fistulotomy //
Dis. Colon Rectum. — 1994. — Vol. 37. — P. 1194–1197.
41. Pescatori M., Ayabaca S.M., Cafaro D. et al. Marsupialization of fistulotomy and fistulectomy wounds improves healing and decreases bleeding: a randomized controlled trial // Colorectal Dis. — 2006. — Vol. 8. — P. 11–14.
42. Ho Y.H., Tan M., Leong A.F., Seow-Choen F. Marsupialization of fistulotomy wounds improves healing: a randomized controlled trial // Br. J. Surg. — 1998. — Vol. 85. — P. 105–107.
43. Kronborg O. To lay open or excise a fistula-in-ano: a randomized trial //
Br. J. Surg. — 1985. — Vol. 72. — P. 970.
44. Belmonte Montes C., Ruiz Galindo G.H., Montes Villalobos J.L., Decanini Terán C. Fistulotomy vs fistulectomy: ultrasonographic evaluation of lesion of the anal sphincter function // Rev. Gastroenterol. Mex. — 1999. — Vol. 64. — P. 167–170.
45. Adams T., Yang J., Kondylis L.A., Kondylis P.D. Long-term outlook after successful fibrin glue ablation of cryptoglandular transsphincteric fistula-in-ano // Dis. Colon Rectum. — 2008. — Vol. 51. — P. 1488–1490.
46. Sentovich S.M. Fibrin glue for anal fistulas: long-term results // Dis. Colon
Rectum. — 2003. — Vol. 46. — P. 498–450.
47. Swinscoe M.T., Ventakasubramaniam A.K., Jayne D.G. Fibrin glue for fistulain-ano: the evidence reviewed // Tech. Coloproctol. — 2005. — Vol. 9. — P. 89–94.
48. Yeung J.M., Simpson J.A., Tang S.W. et al. Fibrin glue for the treatment of fistulae-in-ano: a method worth sticking to? // Colorectal Dis. — 2010. — Vol. 12, N 4. — P. 363–366.
49. Cintron J.R., Park J.J., Orsay C.P. et al. Repair of fistulas-in-ano using
fibrin adhesive: long-term follow-up // Dis. Colon Rectum. — 2000. — Vol. 43. — P. 944–949.
50. Park J.J., Cintron J.R., Orsay C.P. et al. Repair of chronic anorectal fistulae using commercial fibrin sealant // Arch. Surg. — 2000. — Vol. 135. — P. 166–169.
51. Lindsey I., Smilgin-Humphreys M.M., Cunningham C. et al. A randomized, controlled trial of fibrin glue vs. conventional treatment for anal fistula // Dis. Colon Rectum. — 2002. — Vol. 45. — P. 1608–1615.
52. Ellis C.N., Clark S. Fibrin glue as an adjunct to flap repair of anal fistulas:
a randomized, controlled study // Dis. Colon Rectum. — 2006. — Vol. 49. — P. 1736–1740.
53. Hammond T.M., Grahn M.F., Lunniss P.J. Fibrin glue in the management of anal fistulae // Colorectal Dis. — 2004. — Vol. 6. — P. 308–319.
54. Loungnarath R., Dietz D.W., Mutch M.G. et al. Fibrin glue treatment of complex anal fistulas has low success rate // Dis. Colon Rectum. — 2004. — Vol. 47. — P. 432–436.
55. de Parades V., Far H.S., Etienney I. et al. Seton drainage and fibrin glue
injection for complex anal fistulas // Colorectal Dis. — 2010. — Vol. 12, N 5. — P. 459–463.
56. Song W.L., Wang Z.J., Zheng Y. et al. An anorectal fistula treatment with acellular extracellular matrix: a new technique // World J. Gastroenterol. — 2008. — Vol. 14. — P. 4791–4794.
57. Ky A.J., Sylla P., Steinhagen R. et al. Collagen fistula plug for the treatment of
anal fistulas // Dis. Colon Rectum. — 2008. — Vol. 51. — P. 838–843.
58. Ellis C.N., Rostas J.W., Greiner F.G. Long-term outcomes with the use of bioprosthetic plugs for the management of complex anal fistulas // Dis. Colon Rectum. — 2010. — Vol. 53. — P. 798–802.
59. Zubaidi A., AL-Obeed O. Anal fistula plug in high fistula-in ano: an early Saudi experience // Dis. Colon Rectum. — 2009. — Vol. 52. — P. 1584–1588.
60. Schwandner O., Stadler F., Dietl O. et al. Initial experience on efficacy in closure of cryptoglandular and Crohn’s transsphincteric fistulas by the use of the anal fistula plug // Int. J. Colorectal Dis. — 2008. — Vol. 23. — P. 319–324.
61. Safar B., Jobanputra S., Sands D. et al. Anal fistula plug: initial experience and
outcomes // Dis. Colon Rectum. — 2009. — Vol. 52. — P. 248–252.
62. Christoforidis D., Etzioni D.A., Goldberg S.M. et al. Treatment of complex anal fistulas with the collagen fistula plug // Dis. Colon Rectum. — 2008. — Vol. 51. — P. 1482–1487.
63. Van Koperen P.J., Wind J., Bemelman W.A., Slors J.F. Fibrin glue and transanal rectal advancement flap for high transsphincteric perianal fistulas: is there any advantage? // Int. J. Colorectal Dis. — 2008. — Vol. 23. — P. 697–701.
64. Mizrahi N., Wexner S.D., Zmora O. et al. Endorectal advancement flap: are there
predictors of failure? // Dis. Colon Rectum. — 2002. — Vol. 45. — P. 1616–1621.
65. Mitalas L.E., Gosselink M.P., Zimmerman D.D., Schouten W.R. Repeat transanal advancement flap repair: impact on the overall healing rate of high transsphincteric fistulas and on fecal continence // Dis. Colon Rectum. — 2007. — Vol. 50. — P. 1508–1511.
66. Schouten W.R., Zimmerman D.D., Briel J.W. Transanal advancement flap repair of transsphincteric fistulas // Dis. Colon Rectum. — 1999. — Vol. 42. — P. 1419–1422.
67. Zimmerman D.D., Briel J.W., Gosselink M.P., Schouten W.R. Anocutaneous
advancement flap repair of transsphincteric fistulas // Dis. Colon Rectum. — 2001. — Vol. 44. — P. 1474–1480.
68. Jones I.T., Fazio V.W., Jagelman D.G. The use of transanal rectal advancement flaps in the management of fistulas involving the anorectum // Dis. Colon Rectum. — 1987. — Vol. 30. — P. 919–923.
69. Sonoda T., Hull T., Piedmonte M.R., Fazio V.W. Outcomes of primary repair
of anorectal and rectovaginal fistulas using the endorectal advancement flap // Dis. Colon Rectum. — 2002. — Vol. 45. — P. 1622–1628.
70. Athanasiadis S., Helmes C., Yazigi R., Köhler A. The direct closure of the internal fistula opening without advancement flap for transsphincteric fistulas-inano // Dis. Colon Rectum. — 2004. — Vol. 47. — P. 1174–1180.
71. Perez F., Arroyo A., Serrano P. et al. Randomized clinical and manometric
study of advancement flap versus fistulotomy with sphincter reconstruction in the management of complex fistula-in-ano // Am. J. Surg. — 2006. — Vol. 192. — P. 34–40.
72. Uribe N., Millán M., Minguez M. et al. Clinical and manometric results of endorectal advancement flaps for complex anal fistula // Int. J. Colorectal Dis. — 2007. — Vol. 22. — P. 259–264.
73. Williams J.G., MacLeod C.A., Rothenberger D.A., Goldberg S.M. Seton
treatment of high anal fistulae // Br. J. Surg. — 1991. — Vol. 78. — P. 1159–1161.
74. Isbister W.H., Al Sanea N. The cutting seton: an experience at King Faisal Specialist Hospital // Dis. Colon Rectum. — 2001. — Vol. 44. — P. 722–727.
75. Mentes B.B., Oktemer S., Tezcaner T. et al. Elastic one-stage cutting seton for the treatment of high anal fistulas: preliminary results // Tech. Coloproctol. — 2004. — Vol. 8. — P. 159–162.
76. Eitan A., Koliada M., Bickel A. The use of the loose seton technique as a definitive treatment for recurrent and persistent high trans-sphincteric anal fistulas: a long-term outcome // J. Gastrointest. Surg. — 2009. — Vol. 13, N 6. — P. 1116– 1119.
77. Theerapol A., So B.Y., Ngoi S.S. Routine use of setons for the treatment of anal fistulae // Singapore Med. J. — 2002. — Vol. 43. — P. 305–307.
78. Chuang-Wei C., Chang-Chieh W., Cheng-Wen H. et al. Cutting seton for complex anal fistulas // Surgeon. — 2008. — Vol. 6. — P. 185–188.
79. Zbar A.P., Ramesh J., Beer-Gabel M. et al. Conventional cutting vs. internal anal sphincter-preserving seton for high trans-sphincteric fistula: a prospective randomized manometric and clinical trial // Tech. Coloproctol. — 2003. — Vol. 7. — P. 89–94.
80. Shukla N. Multicentric randomized controlled clinical trial of Kshaarasootra
(Ayurvedic medicated thread) in the management of fistula-in-ano. Indian Council of Medical Research // Indian J. Med. Res. — 1991. — Vol. 94. — P. 177–185.
81. Ho K.S., Tsang C., Seow-Choen F. et al. Prospective randomized trial comparing ayurvedic cutting seton and fistulotomy for low fistula-in-ano // Tech. Coloproctol. — 2001. — Vol. 5. — P. 137–141.
82. Tyler K.M., Aarons C.B., Sentovich S.M. Successful sphincter-sparing surgery
for all anal fistulas // Dis. Colon Rectum. — 2007. — Vol. 50. — P. 1535–1539.
83. Gemsenjager E. Results with a new therapy concept in anal fistula: suture of the anal sphincter // Schweiz. Med. Wochenschr. — 1996. — Vol. 126. — P. 2021–2025.
84. Perez F., Arroyo A., Serrano P. et al. Fistulotomy with primary sphincter reconstruction in the management of complex fistula-in-ano: prospective study of clinical and manometric results // J. Am. Coll. Surg. — 2005. — Vol. 200. — P. 897–903.
85. Jordan J., Roig J.V., Garcia-Armengol J. et al. Risk factors for recurrence
and incontinence after anal fistula surgery // Colorectal Dis. — 2010. — Vol. 12. — P. 254–260.
86. Kraemer M., Picke D. Fistelspaltung und primäre Sphinkterrekonstruktion zur Behandlung von Analfisteln // Coloproctology. — 2011. — Vol. 33. — P. 104–108.
87. Bleier J.L., Moloo H., Goldberg S.M. Ligation of the intersphincteric fistula
tract: an effective new technique for complex fistulas // Dis. Colon Rectum. — 2010. — Vol. 53. — P. 43–46.
88. Shanwani A., Nor A.M., Amri N. Ligation of the intersphincteric fistula tract: a sphincter-saving technique for fistula-inano // Dis. Colon Rectum. — 2010. — Vol. 53. — P. 39–42.
89. Rojanasakul A., Pattanaarun J., Sahakitrungruang C., Tantiphlachiva K. Total
anal sphincter saving technique for fistula-in-ano: the ligation of the intersphincteric fistula tract // J. Med. Assoc. Thai. — 2007. — Vol. 90. — P. 581–586.
90. Makowiec F., Jehle E.C., Becker H.D., Starlinger M. Perianal abscess in Crohn’s disease // Dis. Colon Rectum. — 1997. — Vol. 40. — P. 443–450.
91. McKee R.F., Keenan R.A. Perianal Crohn’s disease: is it all bad news? // Dis. Colon Rectum. — 1996. — Vol. 39. — P. 136 –142.
92. Korelitz B.I., Present D.H. Favorable effect of 6-mercaptopurine on fistulae of Crohn’s disease // Dig. Dis. Sci. — 1985. — Vol. 30. — P. 58–64.
93. Sandborn W.J., Present D.H., Isaacs K.L. et al. Tacrolimus for the treatment of fistulas in patients with Crohn’s disease: a randomized, placebo-controlled trial // Gastroenterology. — 2003. — Vol. 125. — P. 380–388.
94. Present D.H., Lichtiger S. Efficacy of cyclosporine in treatment of fistula of Crohn’s disease // Dig. Dis. Sci. — 1994. — Vol. 39. — P. 374–380.
95. Present D.H., Rutgeerts P., Targan S. et al. Infliximab for the treatment of fistulas in patients with Crohn’s disease // N. Engl. J. Med. — 1999. — Vol. 340. — P. 1398–1405.
96. Yamamoto T., Allan R.N., Keighley M.R. Effect of fecal diversion alone on perianal Crohn’s disease // World J. Surg. — 2000. — Vol. 24. — P. 1258–1262.
97. Galandiuk S., Kimberling J., Al-Mishlab T.G., Stromberg A.J. Perianal Crohn disease: predictors of need for permanent diversion // Ann. Surg. — 2005. — Vol. 241. — P. 796–801.
98. Löffler T., Welsch T., Mühl S. et al. Long-term success rate after surgical treatment of anorectal and rectovaginal fistulas in Crohn’s disease // Int. J. Colorectal Dis. — 2009. — Vol. 24, N 5. — P. 521–526.
99. Gaertner W.B., Decanini A., Mellgren A. et al. Does infliximab infusion
impact results of operative treatment for Crohn’s perianal fistulas? // Dis. Colon Rectum. — 2007. — Vol. 50. — P. 1754–1760.
100. Solomon M.J. Fistulae and abscesses in symptomatic perineal Crohn’s disease // Int. J. Colorectal Dis. — 1996. — Vol. 11. — P. 222–226.
101. Mardini H.E., Schwartz D.A. Treatment of perianal fistula and abscess: Crohn’s and non-Crohn’s // Curr. Treat. Options Gastroenterol. — 2007. — Vol. 10. — P. 211–220.
102. Sangwan Y.P., Schoetz D.J.Jr., Murray J.J. et al. Perianal Crohn’s disease: results of local surgical treatment // Dis. Colon Rectum. — 1996. — Vol. 39. — P. 529–535.
103. Williamson P.R., Hellinger M.D., Larach S.W., Ferrara A. Twenty-year
review of the surgical management of perianal Crohn’s disease // Dis. Colon Rectum. — 1995. — Vol. 38. — P. 389–392.
104. Pescatori M., Interisano A., Basso L. et al. Management of perianal Crohn’s disease: results of a multicenter study in Italy // Dis. Colon Rectum. — 1995. — Vol. 38. — P. 121–124.
105. Galis-Rozen E., Tulchinsky H., Rosen A. et al. Long-term outcome of loose-
seton for complex anal fistula: a two-centre study of patients with and without Crohn’s disease // Colorectal Dis. — 2010. — Vol. 12, N 4. — P. 358–362.
106. Takesue Y., Ohge H., Yokoyama T. et al. Long-term results of seton drainage on complex anal fistulae in patients with Crohn’s disease // J. Gastroenterol. — 2002. — Vol. 37. — P. 912–915.
107. Topstad D.R., Panaccione R., Heine J.A. et al. Combined seton placement,
infliximab infusion, and maintenance immunosuppressives improve healing rate in fistulizing anorectal Crohn’s disease: a single center experience // Dis. Colon Rectum. — 2003. — Vol. 46. — P. 577–583.
108. Guidi L., Ratto C., Semeraro S. et al. Combined therapy with infliximab and seton drainage for perianal fistulizing Crohn’s disease with anal endosonographic monitoring: a single-centre experience // Tech. Coloproctol. — 2008. — Vol. 12. — P. 1111–1117.
109. Hyder S.A., Travis S.P., Jewell D.P. et al. Fistulating anal Crohn’s disease:
results of combined surgical and infliximab treatment // Dis. Colon Rectum. — 2006. — Vol. 49. — P. 1837–1841.
110. Hull T.L., Fazio V.W. Surgical approaches to low anovaginal fistula in Crohn’s disease // Am. J. Surg. — 1997. — Vol. 173. — P. 95–98.
111. Joo J.S., Weiss E.G., Nogueras J.J., Wexner S.D. Endorectal advancement flap in perianal Crohn’s disease // Am. Surg. — 1998. — Vol. 64. — P. 147–150.
112. Ozuner G., Hull T.L., Cartmill J., Fazio V.W. Long-term analysis of the use of transanal rectal advancement flaps for complicated anorectal/vaginal fistulas // Dis. Colon Rectum. — 1996. — Vol. 39. — P. 10–14.
113. Joos A.K., Palma P., Jonescheit J.O. et al. Enteral vs parenteral nutrition in reconstructive anal surgery — a prospective-randomized trial // Colorectal Dis. — 2008. — Vol. 10. — P. 605–609.
114. Nessim A., Wexner S.D., Agachan F. et al. Is bowel confinement necessary after anorectal reconstructive surgery? A prospective, randomized, surgeon-blinded trial // Dis. Colon Rectum. — 1999. — Vol. 42. — P. 16–23.
РЕКТОВАГИНАЛЬНЫЕ СВИЩИ
Введение
По данным литературы, число ректовагинальных свищей не превышает 5% всех свищей прямой кишки (УД 5, СР D [1, 8, 10, 11]). Однако, учитывая полиэтиологичность заболевания, количество больных с ректовагинальными свищами значительно выше. Истинные показатели частоты заболевания неизвестны, так как эти пациентки по-прежнему остаются
«многопрофильными» и получают помощь в гинекологических, проктологических, общехирургических стационарах либо не лечатся вообще.
По имеющимся в настоящее время данным, известно, что 88% ректовагинальных свищей возникают после акушерской травмы, при этом травма промежности с последующим формированием свища отмечается в 0,1% родов через естественные родовые пути (УД 5, СР D [8, 16]). Кроме того, ректовагинальные свищи являются перианальным осложнением у пациентов с ВЗК в 0,2–2,1% наблюдений (УД 5, СР D [11, 19, 66, 67]). Частота формирования ректовагинального свища после различных низких резекций прямой кишки превышает 10% (УД 5, СР D [2, 8, 16–19, 29, 30–35]). В последние годы количество послеоперационных ректовагинальных свищей значительно возросло за счет использования различных степлеров при хирургическом лечении геморроя и применения синтетических имплантатов при хирургической коррекции тазового пролапса (УД 5, СР D [21–26, 36–40, 41–46, 49, 51–55]). Частота формирования ректовагинальных свищей после такого хирургического лечения отмечается в 0,15% случаев [55]. Если вопрос о частоте заболевания может считаться открытым и дискутабельным, то трудности его хирургического лечения общепризнаны. Красноречивым доказательством сказанного служит то, что для ликвидации находящегося в видимой легкой доступности свища и при кажущейся технической простоте самого вмешательства предложено более 100 методов различных операций. Несмотря на это, результаты лечения остаются неудовлетворительными, рецидив заболевания отмечается в 20–70% случаев.
Рекомендации по диагностике и лечению пациенток с ректовагинальны-
ми свищами служат руководством для практических врачей, осуществляющих ведение и лечение таких больных, и подлежат регулярному пересмотру в соответствии с новыми данными научных исследований в этой области.
Рекомендации включают следующие разделы: определение заболевания, классификация по МКБ-10, профилактика, диагностика, консервативное и оперативное лечение, правила ведения периоперационного периода, а также прогноз у оперированных больных.
Рекомендации подлежат регулярному пересмотру в соответствии с новыми данными научных исследований в этой области. Настоящие рекомендации составлены на основании анализа литературы из базы данных PubMed, MEDLINE, Cochrane Collaboration, the Standards Practice Task Force of the American Society of Colon and Rectal Surgeon, Oxford Center for Evidence-based Medicine — Levels of Evidence. Рекомендации сопровождаются пояснениями об уровне доказательности отдельных положений согласно рекомендациям Оксфордского центра доказательной медицины (табл. 6.1) [13, 14]. В зависимости от достоверности приводимых данных рекомендации разделены на степени: A, B, C, D.
Таблица 6.1. Уровни доказательности и степени рекомендаций на основании классификации Оксфордского центра доказательной медицины
|
Уровень |
Исследования методов диагностики |
Исследования методов лечения |
|
1а |
Систематический обзор гомогенных диагностических исследований 1-го уровня |
Систематический обзор гомогенных РКИ |
|
1b |
Валидизирующее когортное исследование с качественным «золотым стандартом» |
Отдельное РКИ (с узким доверительным интервалом) |
|
1с |
Специфичность или чувствительность столь высокие, что положительный или отрицательный результат позволяет исключить/установить диагноз |
Исследование «Всё или ничего» |
|
2а |
Систематический обзор гомогенных диагностических исследований >2-го уровня |
Систематический обзор (гомогенных) когортных исследований |
|
2b |
Разведочное когортное исследование с качественным «золотым стандартом» |
Отдельное когортное исследование (включая РКИ низкого качества; т.е. с <80% пациентов, прошедших контрольное наблюдение) |
|
2с |
Нет |
Исследование «исходов»; экологические исследования |
|
3а |
Систематический обзор гомогенных исследований |
Систематический обзор гомогенных исследований уровня 3b и выше исследований «случай–контроль» |
|
3b |
Исследование с непоследовательным набором или без проведения исследования «золотого стандарта» у всех испытуемых |
Отдельное исследование «случай– контроль» |
Табл. 6.1. Окончание
|
Уровень |
Исследования методов диагностики |
Исследования методов лечения |
|
4 |
Исследование «случай–контроль» или исследование с некачественным или зависимым «золотым стандартом» |
Серия случаев (и когортные исследования или исследования «случай– контроль» низкого качества) |
|
5 |
Мнение экспертов без тщательной критической оценки или основанное на физиологии, лабораторные исследования на животных или разработка «первых принципов» |
Мнение экспертов без тщательной критической оценки, лабораторные исследования на животных или разработка «первых принципов» |
|
Степень рекомендации | ||
|
A |
Согласующиеся между собой исследования 1-го уровня | |
|
B |
Согласующиеся между собой исследования 2-го или 3-го уровня или экстраполяция на основе исследований 1-го уровня | |
|
C |
Исследования 4-го уровня или экстраполяция на основе уровня 2 или 3 | |
|
D |
Доказательства 4-го уровня или затруднительные для обобщения или некачественные исследования любого уровня | |
ВАЛИДИЗАЦИЯ РЕКОМЕНДАЦИЙ
Настоящие рекомендации составлены общероссийской общественной организацией «Ассоциация колопроктологов России», в предварительной версии были рецензированы независимыми экспертами, которых попросили прокомментировать прежде всего, насколько интерпретация доказательств, лежащих в основе рекомендаций, доступна для понимания. Получены комментарии со стороны врачей амбулаторного звена. Полученные комментарии тщательно систематизировались и обсуждались на совещаниях экспертной группы.
Последние изменения в настоящих рекомендациях были представлены для дискуссии на заседании профильной комиссии «Колопроктология» Экспертного совета Минздрава России 12 сентября 2013 г. Проект рекомендаций был повторно рецензирован независимыми экспертами и врачами амбулаторного звена. Для окончательной редакции и контроля качества рекомендации были повторно проанализированы членами экспертной группы, которые пришли к заключению, что все замечания и комментарии приняты во внимание, риск систематических ошибок при разработке рекомендаций сведен к минимуму.
Определение
Ректовагинальный свищ — патологическое соустье между прямой кишкой и влагалищем.
Код по Международной классификации болезней 10-го пересмотра
n Класс: Болезни мочеполовой системы (XIV).
n Блок: Невоспалительные болезни женских половых органов (N82).
n Код: N82.3.
n Название: Свищ влагалищно-толстокишечный.
Профилактика
Профилактика формирования ректовагинальных свищей заключается в следующем (УД 5, СР D [1, 2, 8, 10]).
n Улучшение качества акушерских пособий, сокращение послеродовых осложнений. При возникающих акушерских осложнениях показано правильное и своевременное их лечение (ушивание разрывов) и адекватное послеродовое и послеоперационное ведение.
n Улучшение качества хирургической помощи больным с заболеваниями анального канала и дистальной части прямой кишки:
v правильный выбор оперативного лечения;
v правильная техника выполнения данных вмешательств.
n Улучшение качества периоперационного ведения пациентов.
n Своевременное выявление и правильное ведение пациентов с ВЗК.
n Правильный подбор дозы лучевой терапии.
Скрининг
Специализированный скрининг на наличие ректовагинального свища не показан.
Классификация
По этиологическому фактору [1, 8, 10]
n Посттравматические:
v послеродовые [8, 17, 20–26];
v послеоперационные:
- низкие резекции прямой кишки (с аппаратными анастомозами и без межкишечных соустий) [2, 7, 8, 10, 29–35];
- операции по поводу геморроя (степлерные резекции и др.) [36–40];
- операции по поводу тазового пролапса (степлерная трансанальная резекция прямой кишки — STARR и др.) [41–46, 49, 51–55];
- дренирование абсцессов малого таза [8, 27, 10];
v ранения инородными предметами и половые девиации [8].
n Перианальные проявления ВЗК (болезнь Крона, язвенный колит) [8, 10, 11, 65–69]:
v воспалительные (парапроктиты, бартолиниты) [8, 10, 27, 28];
v опухолевая инвазия [2, 8, 10].
n Постлучевые [56–59].
n Ишемические (локальная ишемия, вызванная применением ректальных суппозиториев с сосудосуживающими препаратами, нестероидные противовоспалительные средства и др.) [8].
По уровню расположения свищевого отверстия в кишке [2, 8, 10]
n Интрасфинктерные ректовагинальные свищи.
n Транссфинктерные ректовагинальные свищи.
n Экстрасфинктерные ректовагинальные свищи.
n Ректовагинальные свищи высокого уровня.
Формулировка диагноза
При формулировании диагноза следует отразить этиологию заболевания, уровень расположения свищевого отверстия в кишке (указывается только при высоком расположении свищевого отверстия, при низком свище указывается отношение свищевого хода к анальному сфинктеру), а также наличие или отсутствие полостей, затеков по ходу свища и их локализацию. Если свищ — проявление осложнений ВЗК, то вначале полностью формулируется диагноз основного заболевания. Ниже приведены примеры формулировок диагноза.
n Послеродовый ректовагинальный свищ высокого уровня.
n Транссфинктерный ректовагинальный свищ с подкожным затеком.
n Болезнь Крона в форме колита с поражением восходящей, сигмовидной и прямой кишки, хроническое непрерывное течение, тяжелая форма. Перианальные проявления в виде ректовагинального свища высокого уровня. Гормональная зависимость.
Диагностика
КЛИНИЧЕСКИЕ ДИАГНОСТИЧЕСКИЕ КРИТЕРИИ
К основным клиническим симптомам ректовагинального свища относятся выделение кишечных компонентов через влагалище, при низких свищах возможно наличие наружного свищевого отверстия на коже промежности либо в преддверии влагалища, дискомфорт, боли в области заднего прохода. При наличии обострения гнойно-воспалительного процесса в параректальной клетчатке (учитывая анатомическое строение ректовагинальной перегородки, отмечается крайне редко (УД 5, СР D [1, 8, 10,])) возможно появление общих воспалительных симптомов, таких как повышение температуры тела, лихорадка.
При любых ректовагинальных свищах обследование больного необходимо дополнять проктографией, эндоректальной ультрасонографией для определения уровня локализации свищевого отверстия в прямой кишке, оценки расположения гнойных полостей.
УСТАНОВЛЕНИЕ ДИАГНОЗА
Диагноз утанавливают на основании сочетания данных анамнеза, клинической картины и типичных изменений, выявляемых при ультра-
звуковом и/или рентгенологическом исследовании (УД 5, СР D [1, 8, 10, 18, 19]). Для этого врачу необходимо провести следующее.
ОБЯЗАТЕЛЬНЫЕ МЕТОДЫ ИССЛЕДОВАНИЯ ПРИ НАЛИЧИИ РЕКТОВАГИНАЛЬНОГО СВИЩА
Клинические методы
Сбор анамнеза. Выявляют этиологические факторы возникновения заболевания: роды и особенности их течения; наличие в анамнезе оперативных вмешательств на органах малого таза; проведение лучевой терапии; оценивается кишечная симптоматика (УД 5, СР D [1, 2, 8–10]). Осмотр больного проводят на гинекологическом кресле в положении, как для литотомии. При этом оценивают расположение и сомкнутость заднепроходного отверстия, наличие рубцовой деформации промежности и заднего прохода, состояние кожных покровов перианальной, крестцовокопчиковой области и ягодиц. Оценивают состояние наружных женских половых органов. При пальпации определяют наличие рубцового и воспалительного процесса области промежности, наличие гнойных затеков, состояние подкожной порции наружного сфинктера (УД 5, СР D [1, 2, 8–10]). Вагинальное исследование. Определяют наличие, уровень расположения свищевого отверстия во влагалище, наличие и выраженность рубцового процесса во влагалище, наличие гнойных затеков в полости таза
(УД 5, СР D [1, 2, 8, 10]).
Оценка анального рефлекса используется для изучения сократительной способности мышц сфинктера. Нормальный рефлекс — при штриховом раздражении перианальной кожи происходит полноценное сокращение наружного сфинктера; повышенный — когда одновременно со сфинктером происходит сокращение мышц промежности; ослабленный — реакция наружного сфинктера малозаметна (УД 5, СР D [1, 10]).
Пальцевое исследование прямой кишки. Определяют наличие, уровень расположения свищевого отверстия в кишке, а также наличие и протяженность рубцового процесса в области свищевого отверстия и в ректовагинальной перегородке. Выявляются гнойные затеки в полости таза. Оценивают состояние анального сфинктера, сохранность и состояние мышц тазового дна. Определяются также анатомические соотношения мышечных и костных структур тазового кольца. Во время исследования оцениваются тонус и волевые усилия сфинктера заднего прохода, характер его сокращений, наличие зияния заднего прохода после извлечения пальца (УД 5, СР D [1, 2, 8, 10]).
Бимануальное исследование. Оценивают состояние ректовагинальной перегородки, подвижность передней стенки прямой кишки и задней стенки влагалища относительно друг друга. Определяются наличие и выраженность гнойных затеков и рубцового процесса в ректовагинальной перегородке и полости таза. Определяют характер свищевого хода: трубчатый либо губчатый (УД 5, СР D [1, 2, 8, 10]).
Зондирование свищевого хода. Определяют характер свищевого хода, его протяженность, отношение свищевого хода к анальному сфинктеру (УД 5, СР D [1, 2, 8, 10]).
Проба с красителем (выполняется только при наличии наружного свищевого отверстия). Выявляют сообщение наружного свищевого отверстия с просветом прямой кишки, прокрашивают дополнительные свищевые ходы и полости (УД 5, СР D [1, 2, 8, 10]).
Инструментальные методы
Аноскопия. Осматривают зону аноректальной линии, нижнеампулярный отдел прямой кишки, оценивают состояние стенок анального канала, визуализируют свищевое отверстие (УД 5, СР D [1, 2, 8, 10]).
Ректороманоскопия. Осматривают слизистую оболочку прямой кишки и дистального отдела сигмовидной кишки. Оценивают характер сосудистого рисунка, наличие воспалительных изменений в дистальном отделе толстой кишки. Визуализируют зону свищевого отверстия (УД 5, СР D [1, 2, 8, 10]).
Кольпоскопия. Оценивают состояние стенок влагалища, шейки матки.
Визуализируют зону свищевого отверстия (УД 5, СР D [1, 2, 8, 10]).
Колоноскопия. Оценивают состояние слизистой оболочки толстой кишки, наличие ВЗК, новообразований и т.п. (УД 5, СР D [1, 2, 8, 10]).
Рентгенологические методы
Проктография; ирригоскопия. Выявляют уровень выхода контраста из прямой кишки во влагалище, протяженность свищевого хода при его трубчатом характере, наличие и распространенность гнойных затеков. Также определяют рельеф слизистой оболочки прямой кишки, величину ректоанального угла, состояние тазового дна, наличие суженных и расширенных участков, каловых камней, аномальное расположение отделов толстой кишки и т.д. (УД 5, СР D [1, 2, 8, 10]).
Микробиологические исследования
Исследование кишечной и влагалищной микрофлоры. У пациенток с ректовагинальным свищом производится исследование степени чистоты влагалища (УД 5, СР D [1, 8, 10]).
Функциональные исследования состояния запирательного аппарата прямой кишки
Профилометрия — метод оценки давления в просвете полого органа при протягивании измерительного катетера. Аноректальная профилометрия обеспечивает регистрацию давления в разных плоскостях по всей длине анального канала. С помощью компьютерной программы строят график распределения величин давления и проводят подсчет максимальных, средних величин давления, а также коэффициента асимметрии. Программа обработки предусматривает анализ данных давления на любом уровне поперечного сечения анального канала (УД 5, СР D [1, 10]).
Аноректальная манометрия является простым, неинвазивным способом измерения тонуса внутреннего и наружного анального сфинктера и длины зоны высокого давления в анальном канале, что доказано несколькими крупными исследованиями (УД 3а, СР В [9, 76, 91–93]).
Электромиография наружного сфинктера и мышц тазового дна — метод, позволяющий оценить жизнеспособность и функциональную активность мышечных волокон и определить состояние периферических нервных путей иннервирующих мышцы ЗАПК. Результат исследования играет важную роль в прогнозировании эффекта от пластических операций (УД 5, СР D [1, 10]).
Эндоректальное ультразвуковое исследование
УЗИ позволяет определить характер свищевого хода, его протяженность, отношение к анальному сфинктеру, наличие и характер гнойных затеков. Также выявляются локальные изменения в мышечных структурах ЗАПК, наличие и протяженность его дефектов, состояние мышц тазового дна. Доказана несомненная эффективность трансанального УЗИ в определении дефектов внутреннего и наружного сфинктера (УД 2а, СР В [62, 63]). Следует отметить, что при свищах прямой кишки информативность ультразвуковой диагностики не уступает МРТ (УД 2а, СР В [5, 28, 61]).
Магнитно-резонансная томография малого таза
Наряду с эндоректальным УЗИ магнитно-резонансная томография малого таза — метод выбора для оценки расположения свищевого хода по отношению к анальному сфинктеру, уточнения локализации свищевого отверстия во влагалище и кишке, диагностики гнойных затеков, выявления дополнительных свищевых ходов (УД 1a, СР A [90, 91]).
ДИФФЕРЕНЦИАЛЬНАЯ ДИАГНОСТИКА1
Учитывая характерную клиническую картину, дифференциальную диагностику следует проводить лишь со свищами между другими отделами ЖКТ и женскими половыми органами (коловагинальные свищи, энтеровагинальные свищи). Наиболее важно выявить этиологические причины формирования ректовагинального свища.
Лечение2
КОНСЕРВАТИВНОЕ ЛЕЧЕНИЕ
В единичных исследованиях описаны случаи закрытия ректовагинального свища на фоне:
1 В рекомендациях не рассмотрены принципы диагностики и лечения коловагинальных свищей, наиболее частой причиной которых является осложненное течение дивертикулярной болезни [18].
2 В рекомендациях не рассмотрены вопросы лечения ректовагинальных свищей, являющихся следствием опухолевой инвазии, специфических инфекций (туберкулез, актиномикоз и т.п.).
n ограничения пассажа кала в зоне свищевого отверстия (высокие клизмы, диета);
n санации прямой кишки и влагалища, воздействия на выстилку свищевого хода физическими (выскабливание), химическими (щелочные растворы), биологическими (ферментативные препараты) методами;
n применения аутогемотерапии в зоне свища и т.п. Исследования проведены на крайне малых группах пациенток, отдаленные результаты не описаны (УД 5, СР D [2–4, 8]).
При свищах, являющихся следствием ВЗК, пациенткам показано специфическое противовоспалительное лечение (УД 2а, СР В [65–69, 80]).
ХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕ
Показания. Наличие ректовагинального свища служит показанием к хирургическому лечению.
Выбор метода хирургического лечения ректовагинального свища зависит от уровня расположения свищевого хода в кишке, сложности свища (характер свищевого хода, наличие гнойных затеков), взаимоотношения свищевого хода и анального сфинктера, состояния ЗАПК (наличие дефектов сфинктера по передней окружности). Условно можно выделить методы, применяющиеся при лечении низких ректовагинальных свищей, и способы для ликвидации высоких ректовагинальных соустий (УД 3b, СР С [2, 8, 10, 64, 73]).
Хирургическое лечение низких ректовагинальных свищей
1. Иссечение свища в просвет кишки (УД 3b, СР С [8, 10, 64, 70]).
Показания. Выполняют больным при интрасфинктерных и транссфинктерных свищах (подкожная порция анального сфинктера).
Методика. Выполняют иссечение свища в просвет кишки. Излечения больных удается добиться в 70–96,6% наблюдений.
2. Иссечение свища. Сфинктеропластика (УД 2b, СР В [8, 10, 23–26, 64, 70, 71, 75, 87]).
Показания. Выполняют больным при высоких транссфинктерных и экстрасфинктерных свищах при расположении свищевого отверстия в кишке ниже или на уровне зубчатой линии, при наличии дефекта сфинктера по передней полуокружности.
Методика. Выполняют иссечение свища в просвет кишки. Выделяются и мобилизуются концы сфинктера и без натяжения, ушиваются конец в конец. Хорошие результаты лечения возможны только при адекватной мобилизации обоих концов сфинктера. Излечения больных удается добиться в 41–100% наблюдений.
3. Сегментарная проктопластика (низведение слизисто-мышечного лоскута) (УД 3b, СР С [8, 10, 28, 19, 24, 50, 68, 70, 71]).
Показания. Выполняют больным при экстрасфинктерных свищах с расположением свищевого отверстия в кишке на уровне зубчатой линии или несколько выше (в пределах границ хирургического анального канала).
Методика. Выполняют иссечение свища до свищевого отверстия в кишке. Мобилизуют и низводится слизисто-мышечный лоскут с его фиксацией в анальном канале. Излечения больных удается добиться в 50–70% наблюдений.
Хирургическое лечение высоких ректовагинальных свищей
1. Операция Мартиуса (транспозиция луковично-пещеристой мышцы в ректовагинальную перегородку между ушитыми дефектами прямой кишки и влагалища. Варианты операции: перемещение фрагмента жировой ткани на сосудистой ножке из области большой половой губы либо паховой складки) (УД 3b, СР С [8, 76, 77]).
Показания. Высокие ректовагинальные свищи, рецидивные ректовагинальные свищи, ректовагинальные свищи при болезни Крона.
Методика. Расщепляют ректовагинальную перегородку, иссекаются свищевые отверстия в кишке и влагалище. Дефекты стенок влагалища и прямой кишки ушиваются. Выделяют луковично-пещеристую мышцу на сосудистой ножке (фрагмент жировой ткани на сосудистой ножке из области большой половой губы либо паховой складки), осуществляют ее транспозицию в ректовагинальную перегородку. Излечения больных удается добиться в 50–94% наблюдений.
2. Транспозиция нежной мышцы бедра в ректовагинальную перегородку между ушитыми дефектами прямой кишки и влагалища (УД 3b, СР С [8, 78, 79, 88)]).
Показания. Высокие ректовагинальные свищи, рецидивные ректовагинальные свищи, ректовагинальные свищи при болезни Крона.
Методика. Расщепляют ректовагинальную перегородку, иссекают свищевые отверстия в кишке и влагалище. Дефекты стенок влагалища и прямой кишки ушивают. Выделяют нежную мышцу бедра на сосудистой ножке, осуществляют ее транспозицию в ректовагинальную перегородку. Излечения больных удается добиться в 50–92% наблюдений.
3. Ушивание дефекта либо резекция сегмента кишки, несущего свищевое отверстие абдоминальным (лапароскопическим) либо комбинированным доступом (УД 3b, СР С [1, 2, 8, 10, 72, 73, 82–84]).
Показания. Высокие (среднеи верхнеампулярный отдел прямой кишки) ректовагинальные свищи, часто рецидивирующие высокие ректовагинальные свищи, ректовагинальные свищи при болезни Крона с высоким уровнем поражения и распространенным гнойным процессом.
Методика. Абдоминальным (лапароскопическим) либо комбинирован-
ным доступом мобилизуют прямую кишку (объем мобилизации проксимальных отделов толстой кишки определяется после интраоперационной ревизии) и заднюю стенку влагалища дистальнее свища. Выполняют иссечение свища и патологически измененных тканей в области свищевых отверстий. Выполняют раздельное ушивание дефектов стенки влагалища и прямой кишки. При выраженных проявлениях гнойно-воспалитель-
ного процесса, больших размерах дефекта стенки кишки, выраженных рубцовых изменениях с деформацией стенки кишки выполняют резекцию сегмента прямой кишки, несущего свищевое отверстие. Формируют ректоректальный (колоректальный) либо ректоанальный (колоанальный) анастомоз. Излечение больных описано в 75–100% наблюдений.
4. Ликвидация свища расщепленным влагалищно-прямокишечным лоскутом (УД 5, СР D)1.
Показания. Высокие ректовагинальные свищи любой этиологии.
Методика. Свищ иссекают в пределах здоровых тканей. Затем производят расщепление ректовагинальной перегородки и мобилизацию задней стенки влагалища и передней стенки прямой кишки в проксимальном направлении от раны. Затем формируют ложе для фиксации низведенного расщепленного лоскута во влагалище и в прямой кишке. Расщепленную ректовагинальную перегородку низводят в виде рукава и фиксируют к анальному сфинктеру, в прямой кишке и во влагалище.
Предварительные результаты. Излечение больных отмечено в 92% наблюдений.
Роль кишечной стомы в лечении ректовагинальных свищей
Вопрос о формировании стомы должен решаться строго индивидуально в каждом конкретном случае. При высоких и сложных ректовагинальных свищах, независимо от этиологии, формирование превентивной кишечной стомы позволяет существенно снизить риск развития послеоперационных осложнений, улучшить результаты лечения (УД 3b, СР С [1, 2, 8, 10, 89]).
Чего нельзя делать
n Недопустимо выполнение оперативных вмешательств без тщательного объективного обследования пациентки (УД 4, СР D [1, 8, 10]).
n Недопустимо выполнение операций у пациенток с ВЗК без назначения специфической терапии (УД 4, СР D [1, 8, 10]).
n Недопустимо выполнение пластических операций на фоне выраженного гнойно-воспалительного процесса (УД 4, СР D [1, 8, 10]).
n Недопустимо выполнение операций по поводу высоких и сложных свищей без отключения пассажа кишечного содержимого в зоне операции (УД 4, СР D [1, 8, 10]).
n Недопустимо проведение пластических операций вне специализированных центров хирургами с недостаточным опытом (УД 4, СР D [1, 8, 10]).
Послеоперационное ведение
 |
В послеоперационном периоде пациентам, перенесшим операцию по поводу ректовагинального свища, требуется регулярное выполнение
1 Метод внедрен в ФГБУ «Государственный научный центр колопроктологии» Минздрава России в 2012 г.
перевязок, заключающихся в санации влагалища и зоны послеоперационной раны растворами антисептиков 2–3 раза в день (водные растворы хлоргексидина, повидон-йода, мирамистин). Швы с послеоперационной раны снимаются на 12–14-й день после операции (УД 4, СР D [1, 8, 10]). До настоящего времени нет определенных данных о необходимости применения антибактериальных препаратов в послеоперационном периоде (УД 4, СР D [1, 8, 10]). Проведение антибактериальной терапии целесообразно после пластических операций, а также при наличии выраженного воспалительного процесса в окружающих тканях с целью
ускорения его купирования.
Ограничение физических нагрузок, сопровождающихся повышением внутрибрюшного давления, в течение 2–4 нед целесообразно после пластических операций по поводу ректовагинального свища (УД 4, СР D [1, 8, 10]).
Необходимость смягчения с помощью диеты и приема слабительных препаратов показана после пластических операций по поводу свища прямой кишки.
Прогноз
Операции по поводу ректовагинальных свищей требуют знания анатомии, физиологии и клинического опыта. Поэтому плановое лечение пациенток с ректовагинальными свищами следует проводить только в специализированных стационарах.
Основные осложнения после операции — это рецидив свища и недостаточность анального сфинктера. Причинами рецидива могут быть как ошибки в выборе метода операции, так и технические погрешности, а также дефекты в послеоперационном ведении больного. Хирургическое лечение больных с ректовагинальными свищами в специализированных клиниках позволяет добиться излечения уже после первой операции в 70–100% случаев. Исключение составляют пациенты, страдающие болезнью Крона, а также с постлучевыми свищами. Рецидив заболевания у этой категории пациенток после первого оперативного вмешательства отмечается в 50% наблюдений (УД 3b, СР С [8, 10, 11, 65–69]).
Критерии оценки качества помощи в стационаре представлены в таблице 6.2. Для оценки качества медицинской помощи используют временные, процессуальные и профилактирующие критерии. Временные характеризуют своевременность оказания определенных этапов медицинской помощи. Выполнение пациенту ряда медицинских манипуляций, инструментальных и лабораторных исследований, необходимых для качественного оказания медицинской помощи, оценивают в процессуальных критериях. Для анализа мероприятий, направленных на предотвращение развития осложнений, используют профилактирующие критерии.
Таблица 6.2. Критерии оценки качества медицинской помощи в стационаре больным с доброкачественными заболеваниями прямой кишки (ректовагинальный свищ) (0 — нет, 1 — да)
|
Клинические рекомендации |
Временные |
Процессуальные |
Профилактирующие |
|
Клинические рекомендации по диагностике и лечению взрослых пациентов с ректовагинальными свищами (код МКБ — N82.3) |
Установка клинического диагноза в течение 72 ч: 0/1 |
Оценка анального рефлекса: 0/1. Пальцевое исследование прямой кишки: 0/1. Аноскопия: 0/1. Ректороманоскопия: 0/1. Определение группы крови: 0/1. Исследование крови на сифилис, вирусный гепатит В, вирусный гепатит С: 0/1. Клинический анализ крови; биохимический анализ крови; клинический анализ мочи; коагулограмма: 0/1. Метод оперативного лечения в соответствии с клиническими рекомендациями: 0/1. Метод анестезии в соответствии с объемом оперативного лечения: 0/1 |
Отсутствие осложнений: • кровотечение: 0/1; • абсцесс: 0/1; • флегмона: 0/1; • пневмония: 0/1; • тромбоэмболия: 0/1; • летальный исход: 0/1 |
Литература
1. Воробьев Г.И. Основы колопроктологии. — М., 2006. — 432 с.
2. Додица А.Н. Лечение больных с неполными внутренними, коловагинальными и колопромежностными свищами, после сфинктеросохраняющих операций на прямой кишке: Дис. … канд. мед. наук. — М., 1998. — 122 с.
3. Кабулова Р.Х. Ближайшие и отдаленные результаты оперативного лечения ректовагинальных свищей // Вопросы акушерства, гинекологии и педиатрии: Сборник. — Ташкент, 1975. — С. 104–105.
4. Краснопольский В.И., Буянова С.Н., Ищенко А.И. Этиология, диагностика
и основные хирургические принципы лечения кишечно-генитальных свищей // Акуш. и гин. — 1986. — № 9. — С. 21–23.
5. Орлова Л.П. УЗ-диагностика заболеваний толстой кишки // Практическое руководство по УЗИ диагностике / Под ред. В.В. Митькова. — М.: Видар-М, 2011. — С. 331–342.
6. Подмаренкова Л.Ф., Алиева Э.И., Полетов Н.Н. и др. Роль функцио-
нальных методов исследования запирательного аппарата прямой кишки в выявлении патогенетических механизмов анальной инконтиненции // Колопроктология. — 2006. — Т. 16, № 2. — С. 24–30.
7. Приказ Минздравсоцразвития России от 28.07.2011 № 823н «Об утверждении классификации технических средств реабилитации (изделия)
в рамках федерального перечня реабилитационных мероприятий, технических средств реабилитации и услуг, предоставляемых инвалиду, в целях определения размера компенсации за технические средства реабилитации (изделия), приобретенные инвалидами (ветеранами) за собственный счет, и (или) оплаченные за счет собственных средств услуги по их ремонту».
8. Проценко В.М. Хирургическое лечение толстокишечно-влагалищных свищей: Дис. … д-ра мед. наук. — М., 1990. — 267 с.
9. Федоров В.Д., Дульцев Ю.В. Проктология. — М.: Медицина. 1984. — 384 с.
10. Шелыгин Ю.А., Благодарный Л.А. Справочник по колопроктологии. — М.: Литтерра, 2012. — 608 с.
11. Tsang C.B., Rothenberger D.A. Rectovaginal fistulas. Therapeutic options // Surg. Clin. North Am. —1997. — Vol. 77, N 1. — P. 95–114.
12. Schmiegel W., Reinacher-Schick A., Arnold D. et al. S3-Leitlinie «Kolorektales Karzinom» — Aktualisierung 2008 [UpdateS3-guideline «colorectal cancer» 2008] // Z. Gastroenterol. —2008. — Vol. 46, N 8. — P. 799–840.
13. Phillips B., Ball C., Sackett D. et al. Oxford Centre for Evidence-Based
Medicine — Levels of Evidence. — 2009. — Available from: http://www.cebm.net/ oxford-centre-evidence-based-medicine-levels-evidence-march-2009.
14. Hoffmann J.C., Fischer I., Höhne W. et al. Methodische Grundlagen für die Ableitung von Konsensusempfehlungen [Methodological basis for the development of consensus recommendations] // Z. Gastroenterol. —2004. — Vol. 42, N 9. — P. 984–986.
15. Ommer A., Herold A., Berg E. S3-Leitlinie: Rektovaginale Fisteln (ohne
M. Crohn) // Coloproctology. — 2012. — Vol. 34. — P. 211–246.
16. Homsi R., Daikoku N.H., Littlejohn J., Wheeless C.R.Jr. Episiotomy: risks of dehiscence and rectovaginal fistula // Obstet. Gynecol. Surv. — 1994 — Vol. 49, N 12. — P. 803–808.
17. Senatore P.J.Jr. Anovaginal fistulae // Surg. Clin. North Am. — 1994. — Vol. 74, N 6. — P. 1361–1375.
18. Bahadursingh A.M., Longo W.E. Colovaginal fistulas. Etiology and management // J. Reprod. Med. — 2003. — Vol. 48, N 7. — P. 489–495.
19. Saclarides T.J. Rectovaginal fistula // Surg. Clin. North Am. — 2002. — Vol. 82, N 6. — P. 1261–1272.
20. Genadry R.R., Creanga A.A., Roenneburg M.L., Wheeless C.R. Complex obstetric fistulas // Int. J. Gynaecol. Obstet. — 2007. — Vol. 99. — Suppl. 1. — P. 51–56.
21. Goldaber K.G., Wendel P.J., McIntire D.D., Wendel G.D.Jr. Postpartum
perineal morbidity after fourth-degree perineal repair // Am. J. Obstet. Gynecol. — 1993. — Vol. 168, N 2. — P. 489–493.
22. Brown H.W., Wang L., Bunker C.H., Lowder J.L. Lower reproductive tract fistula repairs in inpatient US women, 1979–2006 // Int. Urogynecol. J. — 2012. — Vol. 23, N 4. — P. 403–410.
23. Delancey J.O., Miller N.F., Berger M.B. Surgical approaches to postobstetrical
perineal body defects (rectovaginal fistula and chronic third and fourth-degree lacerations) // Clin. Obstet. Gynecol. — 2010. — Vol. 53, N 1. — P. 134–144.
24. Khanduja K.S., Padmanabhan A., Kerner B.A. et al. Reconstruction of rectovaginal fistula with sphincter disruption by combining rectal mucosal advancement flap and anal sphincteroplasty // Dis. Colon Rectum. — 1999. — Vol. 42, N 11. — P. 1432–1437.
25. Khanduja K.S., Yamashita H.J., Wise W.E.Jr. et al. Delayed repair of obstetric injuries of the anorectum and vagina. A stratified surgical approach // Dis. Colon Rectum. — 1994. — Vol. 37, N 4. — P. 344–349.
26. McCall M.L. Gynecological aspects of obstetrical delivery // Can. Med. Assoc. J. — 1963. — Vol. 88. — P. 177–181.
27. Zoulek E., Karp D.R., Davila G.W. Rectovaginal fistula as a complication to a Bartholin gland excision // Obstet. Gynecol. — 2011. — Vol. 118, N 2. — Pt 2. — P. 489–491.
28. Ommer A., Herold A., Berg E. et al. Cryptoglandular anal fistulas // Dtsch.
Arztebl. Int. — 2011. — Vol. 108, N 42. —P. 707–713.
29. Kosugi C., Saito N., Kimata Y. et al. Rectovaginal fistulas after rectal cancer surgery: Incidence and operative repair by gluteal-fold flap repair // Surgery. — 2005. — Vol. 137, N 3. — P. 329–336.
30. Matthiessen P., Hansson L., Sjödahl R., Rutegard J. Anastomoticvaginal fistula after anterior resection of the rectum for cancer — occurrence and risk factors // Colorectal Dis. — 2010. — Vol. 12, N 4. — P. 351–357.
31. Yodonawa S., Ogawa I., Yoshida S. et al. Rectovaginal fistula after low
anterior resection for rectal cancer using a double stapling technique // Case Rep. Gastroenterol. — 2010. — Vol. 4, N 2. — P. 224–228.
32. Shin U.S., Kim C.W., Yu C.S., Kim J.C. Delayed anastomotic leakage following sphincter-preserving surgery for rectal cancer // Int. J. Colorectal Dis. — 2010. — Vol. 25, N 7. — P. 843–849.
33. Kim C.W., Kim J.H., Yu C.S. et al. Complications after sphincter-saving
resection in rectal cancer patients according to whether chemoradiotherapy is performed before or after surgery // Int. J. Radiat. Oncol. Biol. Phys. — 2010. — Vol. 78, N 1. — P. 156–163.
34. Gecim I.E., Wolff B.G., Pemberton J.H. et al. Does technique of anastomosis play any role in developing late perianal abscess or fistula? // Dis. Colon Rectum. — 2000. — Vol. 43, N 9. — P. 1241–1245.
35. Lolohea S., Lynch A.C., Robertson G.B., Frizelle F.A. Ileal pouch-anal
anastomosis-vaginal fistula: a review // Dis. Colon Rectum. — 2005. — Vol. 48, N 9. — P. 1802–1810.
36. Angelone G., Giardiello C., Prota C. Stapled hemorrhoidopexy. Complications and 2-year follow-up // Chir. Ital. — 2006. — Vol. 58, N 6. — P. 753–760.
37. Giordano P., Gravante G., Sorge R. et al. Long-term outcomes of stapled hemorrhoidopexy vs conventional hemorrhoidectomy: a meta-analysis of randomized controlled trials // Arch. Surg. — 2009. — Vol. 144, N 3. — P. 266–272.
38. Giordano P., Nastro P., Davies A., Gravante G. Prospective evaluation of
stapled haemorrhoidopexy versus transanal haemorrhoidal dearterialisation for stage II and III haemorrhoids: three-year outcomes // Tech. Coloproctol. — 2011. — Vol. 15, N 1. — P. 67–73.
39. Beattie G.C., Loudon M.A. Haemorrhoid surgery revised // Lancet. — 2000. — Vol. 355, N 9215. — P. 1648.
40. Giordano A., della Corte M. Non-operative management of a rectovaginal fistula complicating stapled haemorrhoidectomy // Int. J. Colorectal Dis. — 2008. — Vol. 23, N 7. — P. 727–728.
41. Bassi R., Rademacher J., Savoia A. Rectovaginal fistula after STARR
procedure complicated by haematoma of the posterior vaginal wall: report of a case // Tech. Coloproctol. — 2006. — Vol. 10, N 4. — P. 361–363.
42. Naldini G. Serious unconventional complications of surgery with stapler for haemorrhoidal prolapse and obstructed defaecation because of rectocoele and rectal intussusceptions // Colorectal Dis. — 2011. — Vol. 13, N 3. — P. 323–327.
43. Gagliardi G., Pescatori M., Altomare D.F. et al. Outcome predictors and complications after stapled transanal rectal resection for obstructed defecation // Dis. Colon Rectum. — 2008. — Vol. 51, N 2. — P. 186–195.
44. Martellucci J., Talento P., Carriero A. Early complications after stapled
transanal rectal resection performed using the Contour® Transtar™ device // Colorectal Dis. — 2011. — Vol. 13, N 12. — P. 1428–1431.
45. Pescatori M., Dodi G., Salafia C, Zbar A.P. Rectovaginal fistula after double-stapled transanal rectotomy (STARR) for obstructed defaecation // Int. J. Colorectal Dis. — 2005. — Vol. 20, N 1. — P. 83–85.
46. Pescatori M., Zbar A.P. Reinterventions after complicated or failed STARR
procedure // Int. J. Colorectal Dis. — 2009. — Vol. 24, N 1. — P. 87–95.
47. Mortensen C., Mackey P., Pullyblank A. Rectovaginal fistula: an unusual presentation // Colorectal Dis. — 2010. — Vol. 12, N 7. — P. 703–704.
48. Krissi H., Levy T., Ben-Rafael Z., Levavi H. Fistula formation after large loop excision of the transformation zone in patients with cervical intraepithelial neoplasia // Acta Obstet. Gynecol. Scand. — 2001. — Vol. 80, N 12. — P. 1137–1138.
49. Boccasanta P., Venturi M., Calabrò G. et al. Which surgical approach
for rectocele? A multicentric report from Italian coloproctologists // Tech. Coloproctol. — 2001. — Vol. 5, N 3. — P. 149–156.
50. Zimmerman D.D., Gosselink M.P., Briel J.W., Schouten W.R. The outcome of transanal advancement flap repair of rectovaginal fistulas is not improved by an additional labial fat flap transposition // Tech. Coloproctol. — 2002. — Vol. 6, N 1. — P. 37–42.
51. Devaseelan P., Fogarty P. The role of synthetic mesh in the treatment of
pelvic organ prolapsed: Review // Obstetrician Gynaecologist. — 2009. — Vol. 11, N 3. — P. 169–176.
52. Huffaker R.K., Shull B.L., Thomas J.S. A serious complication following placement of posterior Prolift // Int. Urogynecol. J. Pelvic Floor Dysfunct. — 2009. — Vol. 20, N 11. — P. 1383–1385.
53. Chen H.W., Guess M.K., Connell K.A., Bercik R.S. Ischiorectal abscess
and ischiorectal-vaginal fistula as delayed complications of posterior intravaginal slingplasty: a case report // J. Reprod. Med. — 2009. — Vol. 54, N 10. — P. 645– 648.
54. Hilger W.S., Cornella J.L. Rectovaginal fistula after posterior intravaginal slingplasty and polypropylene mesh augmented rectocele repair // Int. Urogynecol.
J. Pelvic Floor Dysfunct. — 2006. — Vol. 17, N 1. — P. 89–92.
55. Caquant F., Collinet P., Debodinance P. et al. Safety of Trans Vaginal Mesh procedure: retrospective study of 684 patients // J. Obstet. Gynaecol Res. — 2008. — Vol. 34, N 4. — P. 449–456.
56. Anderson J.R., Spence R.A., Parks T.G. et al. Rectovaginal fistulae following radiation treatment for cervical carcinoma // Ulster Med. J. — 1984. — Vol. 53, N 1. — P. 84–87.
57. Cooke S.A., Wellsted M.D. The radiation-damaged rectum: resection with
coloanal anastomosis using the endoanal technique // World J. Surg. — 1986. — Vol. 10, N 2. — P. 220–227.
58. Narayanan P., Nobbenhuis M., Reynolds K.M. et al. Fistulas in malignant gynecologic disease: etiology, imaging, and management // Radiographics. — 2009. — Vol. 29, N 4. — P. 1073–1083.
59. Bricker E.M., Johnston W.D., Patwardhan R.V. Repair of postirradiation damage to colorectum: a progress report // Ann. Surg. — 1981. — Vol. 193, N 5. — P. 555–564.
60. Kröpil F., Raffel A., Renter M.A. et al. Individualisierte und differenzierte
Therapie von rektovaginalen Fisteln [Individualised and differentiated treatment of rectovaginal fistula] // Zentralbl. Chir. — 2010. — Vol. 135, N 4. — P. 307–311.
61. Ommer A., Herold A., Berg E. et al. S3-Leitlinie Kryptoglanduläre Analfistel // Coloproctology. — 2011. — Vol. 33. — P. 295–324.
62. Stoker J., Rociu E., Wiersma T.G., Laméris J.S. Imaging of anorectal disease // Br. J. Surg. — 2000. — Vol. 87, N 1. — P. 10–27.
63. Sudol-Szopinska I., Jakubowski W., Szczepkowski M. Contrast-enhanced endosonography for the diagnosis of anal and anovaginal fistulas // J. Clin. Ultrasound. — 2002. — Vol. 30, N 3. — P. 145–150.
64. Russell T.R., Gallagher D.M. Low rectovaginal fistulas. Approach and
treatment // Am. J. Surg. — 1977. — Vol. 134, N 1. — P. 13–18.
65. Penninckx F., Moneghini D., D’Hoore A. et al. Success and failure after repair of rectovaginal fistula in Crohn’s disease: analysis of prognostic factors // Colorectal Dis. — 2001. — Vol. 3, N 6. — P. 406–411.
66. Andreani S.M., Dang H.H., Grondona P. et al. Rectovaginal fistula in Crohn’s disease // Dis. Colon Rectum. — 2007. —Vol. 50, N 12. — P. 2215–2222.
67. Hannaway C.D., Hull T.L. Current considerations in the management of rectovaginal fistula from Crohn’s disease // Colorectal Dis. — 2008. — Vol. 10, N 8. — P. 747–755.
68. Ruffolo C., Scarpa M., Bassi N., Angriman I. A systematic review on
advancement flaps for rectovaginal fistula in Crohn’s disease: transrectal vs transvaginal approach // Colorectal Dis. — 2010. — Vol. 12, N 12. — P. 1183–1191.
69. Zhu Y.F., Tao G.Q., Zhou N., Xiang C. Current treatment of rectovaginal fistula in Crohn’s disease // World J. Gastroenterol. — 2011. — Vol. 17, N 8. — P. 963–967.
70. Baig M.K., Zhao R.H., Yuen C.H. et al. Simple rectovaginal fistulas // Int. J.
Colorectal Dis. — 2000. — Vol. 15, N 5–6. — P. 323–327.
71. Lowry A.C., Thorson A.G., Rothenberger D.A., Goldberg S.M. Repair of simple rectovaginal fistulas. Influence of previous repairs // Dis. Colon Rectum. — 1988. — Vol. 31, N 9. — P. 676–678.
72. Pelosi M.A. 3rd, Pelosi M.A. Transvaginal repair of recurrent rectovaginal fistula with laparoscopic-assisted rectovaginal mobilization // J. Laparoendosc. Adv. Surg. Tech. A. — 1997. — Vol. 7, N 6. — P. 379–383.
73. Herbst F., Jakesz R. Method for treatment of large high rectovaginal fistula //
Br. J. Surg. — 1994. — Vol. 81, N 10. — P. 1534–1535.
74. Mengert W.F., Fish S.A. Anterior rectal wall advancement; technic for repair of complete perineal laceration and recto-vaginal fistula // Obstet. Gynecol. — 1955. — Vol. 5, N 3. — P. 262–267.
75. Tsang C.B., Madoff R.D., Wong W.D. et al. Anal sphincter integrity and function influences outcome in rectovaginal fistula repair // Dis. Colon Rectum. — 1998. — Vol. 41, N 9. — P. 1141–1146.
76. Gosselink M.P., Oom D.M., Zimmerman D.D., Schouten R.W. Martius flap: an adjunct for repair of complex, low rectovaginal fistula // Am. J. Surg. — 2009. — Vol. 197, N 6. — P. 833–834.
77. Cui L., Chen D., Chen W., Jiang H. Interposition of vital bulbocavernosus graft in the treatment of both simple and recurrent rectovaginal fistulas // Int. J. Colorectal Dis. — 2009. — Vol. 24, N 11. — P. 1255–1259.
78. Ruiz D., Bashankaev B., Speranza J., Wexner S.D. Graciloplasty for
rectourethral, rectovaginal and rectovesical fistulas: technique overview, pitfalls and complications // Tech. Coloproctol. — 2008. — Vol. 12, N 3. — P. 277–281.
79. Fürst A., Schmidbauer C., Swol-Ben J. et al. Gracilis transposition for repair of recurrent anovaginal and rectovaginal fistulas in Crohn’s disease // Int. J. Colorectal Dis. — 2008. — Vol. 23, N 4. — P. 349–353.
80. García-Olmo D., García-Arranz M., García L.G. et al. Autologous stem cell
transplantation for treatment of rectovaginal fistula in perianal Crohn’s disease: a new cell-based therapy // Int. J. Colorectal Dis. — 2003. — Vol. 18, N 5. — P. 451–454.
81. Li Destri G., Scilletta B., Tomaselli T.G., Zarbo G. Rectovaginal fistula: a new approach by stapled transanal rectal resection // J. Gastrointest. Surg. — 2008. — Vol. 12, N 3. — P. 601–603.
82. Kux M., Fuchsjäger N., Hirbawi A. Einzeitige anteriore Resektion in der
Therapie hoher recto-vaginaler Fisteln [One-stage anterior resection in the therapy of high rectovaginal fistulas] // Chirurg. — 1986. — Vol. 57, N 3. — P. 150–154.
83. Van der Hagen S.J., Soeters P.B., Baeten C.G., van Gemert W.G. Laparoscopic fistula excision and omentoplasty for high rectovaginal fistulas: a prospective study of 40 patients // Int. J. Colorectal Dis. — 2011. — Vol. 26, N 11. — P. 1463–1467.
84. Schwenk W., Böhm B., Gründel K., Müller J. Laparoscopic resection of high
rectovaginal fistula with intracorporeal colorectal anastomosis and omentoplasty // Surg. Endosc. — 1997. — Vol. 11, N 2. — P. 147–149.
85. iPostoperative urinary retention after surgery for benign anorectal disease: potential risk factors and strategy for prevention // Int. J. Colorectal Dis. — 2006. — Vol. 21, N 7. — P. 676–682.
86. Tunuguntla H.S., Gousse A.E. Female sexual dysfunction following vaginal surgery: a review // J. Urol. — 2006. — Vol. 175, N 2. — P. 439–446.
87. El-Gazzaz G., Hull T.L., Mignanelli E. et al. Obstetric and cryptoglandular rectovaginal fistulas: long-term surgical outcome; quality of life; and sexual function // J. Gastrointest. Surg. — 2010. — Vol. 14, N 11. — P. 1758–1763.
88. Zmora O., Tulchinsky H., Gur E. et al. Gracilis muscle transposition for
fistulas between the rectum and urethra or vagina // Dis. Colon Rectum. — 2006. — Vol. 49, N 9. — P. 1316–1321.
89. Ommer A., Athanasiadis S., Köhler A., Psarakis E. Die Bedeutung der Stomaanlage im Rahmen der Behandlung der komplizierten Analfisteln und der rektovaginalen Fisteln // Coloproctology. — 2000. — Vol. 22. — P. 14–22.
90. Buchanan G.N., Halligan S., Bartram C.I. et al. Clinical examination,
endosonography, and MR imaging in preoperative assessment of fistula-in-ano: comparison with outcome-based reference standard // Radiology. — 2004. — Vol. 233. — P. 674–681.
91. Guillaumin E., Jeffrey R.B.Jr., Shea W.J. et al. Perirectal inflammatory disease: CT findings // Radiology. — 1986. — Vol. 161. — P. 153–157.
92. Yousem D.M., Fishman E.K., Jones B. Crohn disease: perianal and perirectal findings at CT // Radiology. — 1988. — Vol. 167. — P. 331–334.
ПРЕСАКРАЛЬНЫЕ КИСТЫ
Введение
На протяжении многих лет в центре внимания отечественных и зарубежных колопроктологов остается проблема лечения больных с пресакральными кистами. Актуальность этой проблемы связана с совершенствованием диагностических мероприятий и, следовательно, увеличением количества верифицированных диагнозов пресакральных кист как в нашей стране, так и за рубежом [62, 75]. Существующие методики лечения этой группы пациентов предполагают длительные сроки стационарного и амбулаторного лечения, что не удовлетворяет ни врача, ни пациента. Среди колоректальных хирургов не существует единого мнения в отношении тактики лечения больных с каудальными кистами [74, 78].
Каудальные кисты — одни из врожденных пороков развития аноректальной области. Все врожденные патологические процессы в крестцово-копчиковой области являются результатом неправильного развития на разных стадиях эмбриогенеза зародышевых зачатков, и сложные, порой химероподобные образования могут сформироваться из менее дифференцированных частей, подвергнувшихся аномалиям. Особую опасность для пациента и врача представляют тератомы больших размеров, а также их осложнения (малигнизация, нагноение, образование тазовых абсцессов, свищевых ходов) [11, 25, 71, 79].
Рекомендации по диагностике и лечению пациентов с пресакральными кистами служат руководством для практических врачей, осуществляющих ведение и лечение таких больных, и подлежат регулярному пересмотру в соответствии с новыми данными научных исследований в этой области.
Рекомендации включают следующие разделы: определение заболевания, классификация, профилактика, диагностика, консервативное и хирургическое лечение, правила ведения периоперационного периода, а также прогноз у больных с пресакральными кистами после предпринятого лечения.
Для отдельных положений рекомендаций приведены уровни доказательности согласно общепринятой классификации Оксфордского центра доказательной медицины [61] (табл. 7.1).
Таблица 7.1. Уровни доказательности и степени рекомендаций на основании руководства Оксфордского центра доказательной медицины
|
Уровень |
Исследования методов диагностики «случай–контроль» |
Исследования методов лечения «случай–контроль» |
|
1а |
Систематический обзор гомогенных диагностических исследований 1-го уровня |
Систематический обзор гомогенных РКИ |
|
1b |
Валидизирующее когортное исследование с качественным «золотым стандартом» |
Отдельное РКИ (с узким доверительным интервалом) |
|
1с |
Специфичность или чувствительность столь высокие, что положительный или отрицательный результат позволяет исключить/установить диагноз |
Исследование «Всё или ничего» |
|
2а |
Систематический обзор гомогенных диагностических исследований >2-го уровня |
Систематический обзор (гомогенных) когортных исследований |
|
2b |
Разведочное когортное исследование с качественным «золотым стандартом» |
Отдельное когортное исследование (включая РКИ низкого качества; т.е. с <80% пациентов, прошедших контрольное наблюдение) |
|
2с |
Нет |
Исследование «исходов»; экологические исследования |
|
3а |
Систематический обзор гомогенных исследований уровня 3b и выше |
Систематический обзор гомогенных исследований «случай–контроль» |
|
3b |
Исследование с непоследовательным набором или без проведения исследования «золотого стандарта» у всех испытуемых |
Отдельное исследование «случай– контроль» |
|
4 |
Исследование «случай–контроль» или исследование с некачественным или с зависимым «золотым стандартом» |
Серия случаев (и когортные исследования или исследования «случай– контроль» низкого качества) |
|
5 |
Мнение экспертов без тщательной критической оценки или основанное на физиологии, лабораторных исследованиях на животных или разработка «первых принципов» |
Мнение экспертов без тщательной критической оценки, лабораторные исследования на животных или разработка «первых принципов» |
|
Степени рекомендаций | ||
|
A |
Согласующиеся между собой исследования 1-го уровня | |
|
B |
Согласующиеся между собой исследования 2-го или 3-го уровня или экстраполяция на основе исследований 1-го уровня | |
|
C |
Исследования 4-го уровня или экстраполяция на основе уровня 2 или 3 | |
|
D |
Доказательства 5-го уровня или затруднительные для обобщения или некачественные исследования любого уровня | |
ВАЛИДИЗАЦИЯ РЕКОМЕНДАЦИЙ
Настоящие методические рекомендации составлены Общероссийской общественной организацией «Ассоциация колопроктологов России».
Настоящие рекомендации в предварительной версии были рецензированы независимыми экспертами, которых попросили прокомментировать прежде всего, насколько интерпретация доказательств, лежащих в основе рекомендаций, доступна для понимания. Получены комментарии со стороны врачей амбулаторного звена, комментарии тщательно систематизировались и обсуждались на совещаниях экспертной группы.
Последние изменения в настоящих рекомендациях были представлены для дискуссии на заседании профильной комиссии «Колопроктология» Экспертного совета Минздрава России 12 сентября 2013 г. Проект рекомендаций был повторно рецензирован независимыми экспертами и врачами амбулаторного звена. Для окончательной редакции и контроля качества рекомендации были повторно проанализированы членами экспертной группы, которые пришли к заключению, что все замечания и комментарии приняты во внимание, риск систематических ошибок при разработке рекомендаций сведен к минимуму.
ОБЛАСТЬ ПРИМЕНЕНИЯ РЕКОМЕНДАЦИЙ
Данные методические рекомендации применимы при осуществлении медицинской деятельности в рамках Порядка оказания медицинской помощи взрослому населению с заболеваниями толстой кишки, анального канала и промежности колопроктологического профиля.
Определение
Пресакральные (параректальные) кисты — врожденные аномальные структуры, локализующиеся в параректальной клетчатке, от простых дермоидных кист до сложных опухолей, содержащих целые органы или их зачатки, так называемое гистологическое попурри, и даже неполные паразитарные плоды [1, 8, 9, 18, 71, 86].
Код по Международной классификации болезней 10-го пересмотра
n Класс: Болезни кожи и подкожной клетчатки (XII).
n Блок: Инфекции кожи и подкожной клетчатки (L00–L08).
n Код:
v L05.0 Пилоинидальная киста с абсцессом
v L05.9 Пилоинидальная киста без абсцесса
Классификация
Существуют различные классификации пресакральных кист, с помощью которых можно оценить сферу поражения параректальной области, объем и характер оперативного вмешательства.
В настоящее время в клинической практике используется классификация, подразделяющая пресакральные (параректальные) кисты [49, 63] по размеру, этиологии (характеру зародышевых листков, из которых они образованы) и локализации. Классификация применяется в основном для определения тактики оперативного лечения [1, 8, 9, 65, 86].
По гистогенетическому признаку:
n однолистковые (эктодермальные) образования:
v эпидермальные кисты;
v дермоидные кисты;
n собственно тератомы:
v двухлистковые тератоидные образования;
v трехлистковые тератоидные образования.
По макроструктуре:
n тератоидные образования кистозного строения:
v однокамерная;
v многокамерная;
v лентовидная;
n тератоидные образования солидного строения.
По локализации:
n внутритазовые:
v в пресакральном пространстве;
v у боковых стенок прямой кишки;
v в ректовагинальной перегородке;
n внетазовые (подкожная клетчатка промежности, ягодиц).
По клиническому течению:
n неосложненное;
n осложненное.
Формулировка диагноза
При формулировании диагноза следует отразить гистогенетическую характеристику (о характере которой можно судить лишь при проведении пункционной биопсии или микроскопическом исследовании удаленного препарата), макроструктуру, локализацию и клиническое течение заболевания (см. раздел «Диагностика»). Ниже приведены примеры формулировок диагноза.
n Неосложненная однокамерная пресакральная дермоидная киста.
n Неосложненная лентовидная эпидермальная киста ректовагинальной перегородки.
n Пресакральная многокамерная тератома, осложненная формированием инфралеваторного (или иного) свища.
Диагностика
Диагностика пресакральных кист основана на жалобах больного, степени их выраженности, длительности заболевания, анализе результатов клинического и инструментального обследования пациента (УД 3b, СР C [1, 3, 8, 9, 16, 41, 64, 82, 83]).
Сбор анамнеза. Выявляют жалобы больного, время их появления и интенсивность, акушерский анамнез, историю предыдущих аноректальных или промежностных оперативных вмешательств, а также травм области промежности и прямой кишки (УД 3b, СР C [26, 37, 64, 78]). Тератоидные образования длительное время могут не иметь клинических проявлений и не вызывать жалоб. Первые симптомы проявляются по мере роста этих образований — боли в области крестца и копчика, внизу живота, иногда появление опухолевидных образований в области промежности; выделение слизи, гноя из прямой кишки; частые позывы на дефекацию, мочеиспускание; лентовидный кал. Однако наиболее частые жалобы пациентов при обращении к специалистам — это нагноение тератом, их злокачественное перерождение, образование наружных и внутренних свищей, нарушение кишечной проходимости.
Осмотр больного проводят на гинекологическом кресле в положении, как для литотомии, и в коленно-локтевом положении. При осмотре промежности особое внимание обращают на внешний вид кожных покровов, наличие и расположение наружных свищевых отверстий, следов мацерации, расчесов, каловых масс и рубцов, сформировавшихся в результате перенесенных ранее оперативных вмешательств; выявляют возможные сопутствующие заболевания этой области — анальную трещину, геморрой, свищи или выпадение прямой кишки. При пальпации промежности обращают внимание на наличие пальпируемых опухолевидных образований, что особенно ценно при локализации кисты ниже уровня леваторов в параректальной клетчатке (УД 3b, СР C [26, 35, 64, 78]).
Оценка анального рефлекса. Используется для оценки сохранности нервно-рефлекторных связей наружного сфинктера. Нормальный рефлекс сохранен тогда, когда при штриховом раздражении перианальной кожи происходит полноценное сокращение наружного сфинктера; повышенный — когда одновременно со сфинктером происходит сокращение мышц промежности; ослабленный — реакция наружного сфинктера малозаметна (УД 5, СР D [26, 35]).
Пальцевое исследование прямой кишки. Определяют тонус и волевые усилия анального сфинктера, наличие и выраженность рубцовых изменений в анальном канале, отмечают участки, подозрительные в отношении наличия внутреннего свищевого отверстия. Затем проводят пальпацию стенок прямой кишки. При этом обращают внимание на наличие выбухания стенки прямой кишки, консистенцию образования, локализацию нижнего и достижимость верхнего полюсов, распростра-
ненность образования, подвижность или фиксацию слизистой оболочки прямой кишки в проекции выявляемого образования. Особое внимание обращают на целостность слизистой оболочки прямой кишки в проекции тератоидного образования, наличие рубцов и рубцово-воспалительных изменений в тканях параректальной клетчатки, о которых косвенно может свидетельствовать консистенция образования. При обнаружении внутреннего отверстия свища пациента просят напрячь мышцы анального жома для точного определения отношения расположения внутреннего дренирующего отверстия к волокнам анального сфинктера и пуборектальной мышцы [1, 8, 9, 26, 35].
Таким образом, при пальцевом исследовании прямой кишки у пациентов с подозрением на наличие пресакральной кисты выявляют:
1) локализацию образования;
2) его размеры и консистенцию;
3) наличие и локализацию внутреннего свищевого отверстия и его отношение к волокнам анального сфинктера и пуборектальной мышцы;
4) диаметр внутреннего отверстия и наличие рубцовых изменений в его краях;
5) наличие рубцовых изменений в анальном канале;
6) функциональное состояние ЗАПК и лонно-прямокишечной мышцы (УД 3a, СР C [1, 8, 9, 26, 35]).
Ректороманоскопия. Осматривают слизистую оболочку прямой кишки и дистального отдела сигмовидной кишки. При наличии свища исследование позволяет оценить внешний вид внутреннего отверстия, его диаметр, характер отделяемого, наличие признаков хронического воспаления (грануляционная ткань). Обнаруживают признаки, характерные для наличия объемных образований в полости малого таза — нависание задней стенки прямой кишки на различных уровнях, смещение прямой кишки кпереди и сужение ее просвета. Оценивают состояние слизистой оболочки прямой кишки. Так, у 55,4% пациентов при осложненном течении заболевания с развитием прямокишечных свищей, дренирующих пресакральные кисты, имеются воспалительные изменения — гиперемия, отечность слизистой оболочки, контактная ранимость, сглаженность сосудистого рисунка. Воспалительный процесс слизистой оболочки прямой кишки у этих пациентов обусловлен воздействием на слизистую оболочку отделяемым через свищевой ход содержимым кисты с вирулентной флорой (УД 3b, СР C [1, 8, 9, 26, 35]).
Рентгенологические методы: проктография, фистулография. Выявляют размеры образования, форму и разветвленность свищевых ходов на всем их протяжении, наличие гнойных затеков и полостей, взаимоотношения свищевого хода и внутреннего отверстия свища с волокнами анального сфинктера и лонно-прямокишечной мышцы. Непосредственно перед выполнением фистулографии пациентам выполняют рентгенографию
крестцово-копчикового отдела позвоночника для исключения таких патологических изменений, как незаращение дужек крестцовых позвонков, остеомиелит костей крестца (УД 3a, СР C [26, 35, 38, 39]).
Методика выполнения проктофистулографии:
n при наличии наружных отверстий свища: в прямую кишку вводят и заполняют бариевой взвесью аноконтрастор. В наружное отверстие шприцем вводят водорастворимое контрастное вещество (кардиотраст, верографин, урографин). Количество контрастного вещества зависит от величины и размеров контрастируемых полостей и затеков, протяженности свищевых ходов. Методика позволяет точно определить длину анального канала и верхнюю его границу, проходящую по верхнему краю лонно-прямокишечной мышцы; точно дифференцировать свищи ампулярного отдела прямой кишки от свищей, дренирующихся в анальный канал (УД 3b, СР C [1, 8, 9, 46, 47]);
n при отсутствии наружных свищевых отверстий, т.е. при неполном внутреннем свище: с помощью резинового катетера с множеством боковых отверстий диаметром 0,2 см, расположенных по всей окружности резиновой трубки, вводят бариевую взвесь в прямую кишку под контролем зрения с помощью экрана. Небольшими вращательными движениями сопоставляют одно из отверстий на боковой поверхности катетера с внутренним отверстием в стенке анального канала или прямой кишки. В момент совпадения просветов отверстий на экране можно видеть поступление контраста во внутреннее отверстие свища и заполнение полости. Далее выполняют проктографию по методике двойного контрастирования. При высоком расположении внутреннего отверстия (выше уровня лонно-прямокишечной мышцы) выполняют проктофистулографию по методике двойного контрастирования. Для изучения пресакрального пространства рентгенограммы выполняют в прямой и боковой проекциях (УД 3b, СР C [1, 8, 9, 46, 47]).
На рентгенограммах кистозные образования проявляются расширением ретроректального пространства и смещением прямой кишки в противоположную от образования сторону, с дугообразным вдавлением ее задней и заднебоковой стенки (симптом «кулис»). Стенка прямой кишки, покрывающая кисту, и стенки контрастированных кистозных полостей имеют четкий и ровный контур (УД 3b, СР C [43, 46, 47]).
Компьютерная рентгеновская и магнитно-резонансная томография
Методика. Исследования выполняют в положении больного на спине. Делают серию снимков срезов малого таза. Толщина среза 0,4–0,6 см, ход (расстояние между срезами) составляет 10–20% толщины среза. Выполняют снимки в сагиттальной, аксиальной и фронтальной проекции (УД 2b, СР B [28, 44, 82, 84, 85]).
При этих исследованиях получают максимально полную и точную информацию о размерах, структуре образования, взаимоотношении массы опухоли с органами малого таза и стенкой кишки, рубцовых и воспалительных изменениях в полости малого таза (УД 2b, СР B [28, 44, 82, 84, 85]).
Эндоректальное и трансвагинальное ультрасонографическое исследование
Методика. Исследование выполняют в коленно-локтевом положении
или положении больного на боку. Ректальный датчик диаметром 10 мм, частотой 7,5 МГГц, на который предварительно герметично надет резиновый резервуар, вводят ректально на глубину 8–10 см. Затем производят заполнение резинового резервуара по окружности датчика раствором натрия хлорида до плотного соприкосновения стенок резервуара со стенками прямой кишки [44, 48, 77].
При исследовании оценивают органическое состояние внутреннего и наружного сфинктеров прямой кишки, толщину мышечного слоя, наличие рубцовых и воспалительных изменений в его массе, длину анального сфинктера. Затем оценивают стенку прямой кишки, толщину слизистого и мышечного слоев прямой кишки, наличие рубцов, воспалительных изменений. На последнем этапе производят оценку структуры кистозного образования, его размеров, наличия или отсутствия дополнительных камер, гнойных ходов и полостей (УД 3a, СР C [35, 44, 48, 76]).
ДИФФЕРЕНЦИАЛЬНАЯ ДИАГНОСТИКА
Пресакральные кисты дифференцируют от острых или хронических парапроктитов, ЭКХ, крестцово-копчиковых хорд, мезенхимом, остеомиелита крестца и копчика, менингоцеле, рака прямой кишки, однако при проведении всего комплекса указанных выше диагностических мероприятий удается достаточно точно установить верный диагноз.
Лечение
Все выявленные опухолевые образования параректальной клетчатки, независимо от их размеров, локализации, наличия или отсутствия осложнений, подлежат обязательному хирургическому удалению (УД 2b, СР B [3, 21, 27, 38, 63, 75, 78]).
Цель — радикальное удаление пресакральной (параректальной) кисты. Показания к госпитализации — планируемое оперативное вмеша-
тельство.
ХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕ
Оперативные вмешательства по удалению тератом технически сложны и должны выполняться в специализированных колопроктологических стационарах хирургами, имеющими опыт подобных операций. Вид хирургического вмешательства, а также выбор оперативного доступа зависит от величины и локализации пресакральной (параректальной) кисты. Выбор способа завершения оперативного лечения зависит от наличия свищевых ходов и супралеваторного или инфралеваторного расположе-
ния внутреннего свищевого отверстия. Современная тактика хирургического лечения направлена на радикальное иссечение пресакральной кисты вместе со всеми свищевыми ходами, затеками и на ликвидацию внутреннего свищевого отверстия. В настоящее время применяются следующие оперативные доступы: парасакральный, промежностный, трансвагинальный, абдоминальный и комбинированный (УД 2b, СР B [2, 4, 12, 13, 21, 49, 50, 66, 72, 81]).
Абсолютное противопоказание к оперативному лечению — наличие у пациентов тяжелых соматических и эндокринных заболеваний в стадии декомпенсации.
Удаление кисты парасакральным доступом
Показания. Выполняется пациентам с локализацией неосложненной кисты в пресакральном пространстве, начиная от уровня зубчатой линии и распространяющейся до V–IV крестцового позвонка (УД 3a, СР B [1, 8, 9, 19, 29, 37, 40, 53, 74, 80]).
Методика. Операция выполняется под перидуральной анестезией или эндотрахеальным наркозом (вид анестезии определяется врачоманестезиологом) в положении больного на правом боку с согнутыми и приведенными к животу ногами. Разрез начинают от II–III крестцового позвонка, отступив 1,5–2 см от средней линии (вправо или влево в зависимости от расположения кисты), и далее по межъягодичной складке во избежание повреждения сфинктера, не доходя 2–3 см до заднего прохода. Анокопчиковую связку пересекают у верхушки копчика, выделяют из окружающих тканей и удаляют копчик. Частично и бережно отсекают волокна большой ягодичной мышцы в местах их прикрепления к боковым стенкам крестца. В прямую кишку вводят указательный палец левой руки и им выпячивают заднюю стенку прямой кишки в образовавшуюся рану. Затем при непрерывном контроле указательным пальцем левой руки производят мобилизацию задней и боковых стенок нижнего полюса кисты, потом мобилизуют ее переднюю поверхность, отделяя ее острым путем от задней стенки прямой кишки, стараясь не повредить последнюю, после этого — заднюю стенку верхнего полюса. При значительных размерах пресакральной кисты производят пункцию кисты и эвакуацию содержимого, что может облегчить в дальнейшем выделение кисты из окружающих тканей. Образовавшуюся на месте удаленной кисты операционную рану многократно промывают антисептическими растворами, например хлоргексидином, повидон-йодом, дренируют трубками, проведенными через контрапертуры справа и слева от нижнего края разреза, и ушивают наглухо отдельными швами [1, 7–9, 40, 53, 68, 74].
Хорошие отдаленные результаты, подразумевающие отсутствие ре-
цидива кисты, наблюдаются у 96% пациентов (УД 2a, СР B [2, 24, 29, 40,
53, 71]).
Удаление кисты промежностным доступом
Показания. Выполняется пациентам с локализацией кисты у боковых стенок прямой кишки в параректальной клетчатке (УД 3a, СР B [6, 67, 72, 80]).
Методика. Операция выполняется под перидуральной анестезией в положении больного на спине, как для литотомии или геморроидэктомии. Выполняют полуовальный разрез кожи в проекции прощупываемой опухоли. Под контролем зрения и пальца, введенного в прямую кишку, киста иссекается без повреждения ее стенки и стенки прямой кишки в пределах здоровых тканей [7, 67, 68].
Если киста дренируется в прямую кишку, целесообразно использование трансанального доступа.
Хорошие отдаленные результаты сохраняются у 96% пациентов (УД 2a, СР B [1, 8, 9, 67]).
Удаление кисты ректовагинальной перегородки перинеальным (промежностным) доступом
Показания. Выполняется пациенткам с локализацией кисты в ректовагинальной перегородке в области преддверия влагалища размером не более 3–4 см (УД 2a, СР B [36, 48, 52, 73, 77, 80]).
Методика. В положении больной, как для литотомии, под перидуральной анестезией производят полулунный разрез перианальной кожи по передней полуокружности, отступив от анального канала 1,5–2 см. Под контролем пальца, введенного во влагалище или в просвет прямой кишки, определяют нижний полюс кисты ректовагинальной перегородки, который фиксируют зажимом Алиса и в дальнейшем выделяют острым путем из окружающей клетчатки, стараясь избежать как повреждения передней стенки прямой кишки, так и влагалища. Образовавшуюся рану дренируют выпускником и ушивают отдельными швами.
Удаление кисты ректовагинальной перегородки трансвагинальным доступом
Показания. Выполняется пациенткам с локализацией кисты в области средней трети влагалища, размеры которой превышают 5–7 см.
Методика. В положении больной, как для литотомии, под перидуральной анестезией производят продольный разрез задней стенки влагалища в проекции локализации кисты. После гидравлической препаровки ректовагинальной перегородки острым путем выделяют кистозное образование из окружающих тканей. При необходимости в случае пересечения передних порций леваторов последние ушиваются, а над ними ушивается отдельными швами задняя стенка влагалища.
Удаление кисты ректовагинальной перегородки абдоминальным или комбинированным доступом
Показания. При удалении тератом больших размеров, находящихся в области заднего свода влагалища и с локализацией верхнего полюса
под тазовой брюшиной, используют комбинированный чрезбрюшинный или комбинированный абдоминальный и трансвагинальный доступы (УД 2a, СР B [14, 51, 52, 54, 60, 73, 76]).
Методика. Техника операции заключается в том, что под эндотрахеальным наркозом выполняется нижнесрединная лапаротомия, производят лирообразный разрез тазовой брюшины, при котором становится доступным для визуализции верхний полюс кисты ректовагинальной перегородки. Последовательно острым путем под контролем зрения производят выделение кисты из окружающих тканей, стараясь не повредить как заднюю стенку влагалища, так и переднюю стенку прямой кишки. В случае невозможности выделить нижний полюс кисты со стороны брюшной полости, не меняя положения больной, со стороны влагалища производят его продольный разрез и выделяют нижний полюс кисты трансвагинально. Операция завершается ушиванием раны влагалища и раны передней брюшной стенки с подведением дренажа к ложу удаленного образования.
Хорошие отдаленные результаты сохраняются у 80–93% пациентов (УД 2a, СР B [20, 23, 52, 56, 87]).
Удаление пресакральной кисты комбинированным доступом
Показания. При удалении тератом больших размеров с локализацией верхнего полюса под тазовой брюшиной на уровне мыса крестца, а нижнего полюса на уровне III крестцового позвонка используют комбинированный абдоминальный и парасакральный доступы (УД 2a, СР B [14, 51, 52, 54, 60, 73, 76]).
Методика. Техника операции заключается в том, что под эндотрахеальным наркозом выполняется нижнесрединная лапаротомия, производят лирообразный разрез тазовой брюшины, при котором становится доступным для визуализции верхний полюс пресакральной кисты. Последовательно острым путем под контролем зрения производят выделение кисты из окружающих тканей, стараясь не повредить как заднюю стенку прямой кишки, так и собственную фасцию крестца. В случае невозможности выделения нижнего полюса кисты со стороны брюшной полости больного после наложения поддерживающих швов на лапаротомную рану переводят в положение на правом боку с приведенными к животу ногами, выполняют парасакральный разрез, через который мобилизуют нижний полюс кисты. Операцию завершают восстановлением целостности тазовой брюшины, ушиванием лапаратомной раны и раны промежности с дренированием последней через контрапертуры.
Удаление пресакральной кисты абдоминальным доступом
Показания. При удалении тератом больших размеров с локализацией верхнего полюса под тазовой брюшиной на уровне мыса крестца, а ниж-
него полюса на уровне IV крестцового позвонка используют комбинированный абдоминальный доступ.
Методика. Техника операции заключается в том, что под эндотрахеальным наркозом выполняется нижнесрединная лапаротомия, производят лирообразный разрез тазовой брюшины, при котором становится доступным для визуализции верхний полюс пресакральной кисты. Последовательно острым путем под контролем зрения производят выделение кисты из окружающих тканей. После удаления кисты восстанавливают целостность тазовой брюшины, ушивают лапаротомную рану.
МЕТОДЫ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ПАЦИЕНТОВ С КАУДАЛЬНЫМИ ТЕРАТОМАМИ, ДРЕНИРУЮЩИМИСЯ В ПРОСВЕТ КИШКИ ИНФРАЛЕВАТОРНЫМИ СВИЩАМИ
Хирургическая тактика у пациентов с каудальными тератомами, осложненными инфралеваторными свищами с интрасфинктерным свищевым ходом
Промежностный доступ
Показания. Параректальная (внетазовая) локализация кистозного образования, расположенного ниже уровня леваторов в ишиоректальной клетчатке, осложненная интрасфинктерным свищом (УД 3b, СР C [5, 18, 39, 50, 59, 63]).
Методика. В положении больного для геморроидэктомии выполняют полуовальный разрез кожи в области промежности. Выделение образования из окружающих тканей выполняют острым путем под контролем зрения. Ликвидацию внутреннего свищевого отверстия выполняют методом трансанального иссечения свища в просвет кишки с тщательным удалением всех рубцов по ходу свища. Вмешательство завершают подшиванием краев раны ко дну либо тщательным послойным ушиванием раны. Ушивание раны выполняют в случае наличия минимальных воспалительных изменений в тканях параректальной клетчатки и удалении образования без вскрытия его просвета, при этом осуществляют дренирование латексным выпускником либо микроирригатором (УД 3b, СР C [5, 7]).
Парасакральный доступ
Показания. Интрасфинктерный ход свища и пресакральная (внутритазовая) локализация тератоидного образования (УД 3b, СР C [18, 39, 59, 63]).
Методика. Выполняют иссечение кистозного образования парасакральным доступом с удалением копчика, трансанально — иссечение свища в просвет кишки с последующим выделением и иссечением свищевого хода на протяжении. При интимном спаянии свищевого хода с волокнами сфинктера выполняют ушивание образовавшегося дефекта анального жома (УД 3b, СР C [1, 7–9]). Хорошие результаты отмечаются у 77,8% пациентов (УД 3b, СР C [5, 18, 39, 55]).
Хирургическая тактика у пациентов с каудальными тератомами, дренирующимися в просвет кишки транссфинктерным свищевым ходом
Промежностный доступ
Показания. Транссфинктерное расположение свищевого хода и локализация кистозного образования в параректальной клетчатке ниже уровня леваторов (УД 3b, СР C [5, 45, 59]).
Методика. Выполняют иссечение кисты промежностным доступом с последующим иссечением свища в просвет кишки и сфинктеропластикой. Тщательно иссекают все рубцово-измененные ткани в области анального сфинктера, что позволяет произвести сшивание здоровых краев анального жома (УД 3b, СР C [6, 7]).
Парасакральный доступ
Показания. Транссфинктерное расположение свищевого хода и пресакральная локализация тератоидного образования (УД 3b, СР C [5, 45, 50, 58]).
Методика. Выполняют иссечение кисты парасакральным доступом (см. раздел «Удаление кисты парасакральным доступом»), с удалением копчика, иссечение свищевого хода в просвет кишки с ушиванием сфинктера (УД 3b, СР C [6, 7]).
Трансректальный доступ
Показания. Транссфинктерное расположение свищевого хода и подслизистая локализация тератоидного образования (УД 3b, СР C [5, 45, 50, 58]).
Методика. Выполняют иссечение кисты трансректальным доступом с последующей ликвидацией внутреннего свищевого отверстия путем низведения лоскута слизистой оболочки прямой кишки в анальный канал (УД 3b, СР C [6, 7]).
Трансперинеальный доступ в сочетании со сфинктеролеваторопластикой Показания. Транссфинктерное расположение свищевого хода и локализация кистозного образования в ректовагинальной перегородке
(УД 3b, СР C [45]).
Методика. Выполняют иссечение кисты трансперинеальным доступом с иссечением свища и выполнением передней сфинктеролеваторопластики (УД 3b, СР C [6, 7]).
Хорошие результаты отмечаются в 91,3% случаев (УД 3b, СР C [5–7]). Однако в 8,7% случаев возможно развитие недостаточности анального сфинктера [55, 70].
Хирургическая тактика при кистах, дренирующихся в просвет кишки экстрасфинктерным свищевым ходом
Показания. Параректальная или пресакральная локализация тератоидного образования и экстрасфинктерное расположение свищевого хода с локализацией внутреннего отверстия ниже уровня леваторов, в стенке
анального канала на уровне зубчатой линии (инфралеваторный свищ) (УД 4, СР D [5, 8, 9, 70]).
Методика. Выполняют иссечение тератоидного образования промежностным или парасакральным доступом с последующей ликвидацией внутреннего отверстия методом низведения полнослойного лоскута стенки прямой кишки. Метод заключается в том, что в зоне локализации внутреннего свищевого отверстия на расстоянии 2 см от переходной складки производят полулунный разрез кожи и подкожной клетчатки. Острым путем отсепаровывают слизисто-мышечный лоскут, несущий свищевое отверстие, от перианальной кожи до нижнеампулярного отдела прямой кишки (на 1–2 см выше зубчатой линии) так, чтобы низводимый сегмент мог быть свободно перемещен до уровня перианальной кожи, а свищевое отверстие оказалось бы вне анального канала.
Таким образом формируется рана, сверху представленная дистальным отделом стенки прямой кишки, в то время как мобилизованный лоскут стенки прямой кишки с внутренним свищевым отверстием после отсечения его выше уровня внутреннего сфинктера находится за пределами перианальной кожи. После тщательного гемостаза на мобилизованный сегмент кишки накладывают узловые кетгутовые швы-держалки, после чего его низводят до края перианальной кожи поверх скелетизированной порции внутреннего сфинктера, где и фиксируют узловыми кетгутовыми швами. Хорошие результаты отмечаются в 95% наблюдений (УД 4, СР D [5, 70]).
МЕТОДЫ ЛЕЧЕНИЯ ПРЕСАКРАЛЬНЫХ КИСТ, ОСЛОЖНЕННЫХ СУПРАЛЕВАТОРНЫМИ СВИЩАМИ ПРЯМОЙ КИШКИ
Хирургическое лечение больных с супралеваторными свищами включает 2 основных этапа (УД 3b, СР C [21, 31]).
1. Удаление тератоидного образования.
2. Ликвидацию внутреннего свищевого отверстия с последующим ушиванием дефекта стенки прямой кишки и дренированием раны.
МЕТОДИКИ УШИВАНИЯ ВНУТРЕННЕГО СВИЩЕВОГО ОТВЕРСТИЯ
Показания. Каудальные тератомы, осложненные супралеваторными свищами прямой кишки (УД 4, СР D [5, 15, 59]).
Методика. Иссечение пресакральной тератомы выполняют в положении пациента на правом боку парасакральным доступом с удалением копчика. После удаления образования производят максимально возможную мобилизацию задней и боковых стенок прямой кишки таким образом, чтобы ушивание можно было выполнить без натяжения стенок кишки. Затем производят иссечение рубцов в краях отверстия. По боковым углам внутреннего отверстия накладывают швы-держалки. Производят ушивание дефекта кишечной стенки в поперечном направлении по типу формирования кишечного анастомоза в 3/4. Первый ряд — узловые швы
через все слои с погружением краев внутреннего отверстия в просвет кишки, второй ряд — узловые мышечно-мышечные швы. Послеоперационную рану дренируют одним или двумя дренажами (в зависимости от объема), после чего производят тщательное послойное ее ушивание при сохраненных леваторах, выполняют сшивание их задних порций с укрытием анастомоза (УД 4, СР C [7, 15]). При наличии выраженного рубцового или воспалительного процесса в области ушитого свищевого отверстия операцию дополняют формированием разгрузочной сигмостомы, которая в случае состоятельности швов на стенке прямой кишки может быть закрыта через 1–2 мес.
Данный метод способствует полному излечению и заживлению свища примерно у 93,7% пациентов, в то время как рецидив наблюдается лишь у 6,3% пациентов (УД 4, СР C [5, 7, 15, 55, 70]).
Чего нельзя делать
n Выполнять оперативное вмешательство без тщательного объективного обследования больного.
n Выполнять операцию без достаточных знаний анатомических и функциональных особенностей параректальной области, ЗАПК.
n Выполнять операции вне специализированных центров, хирургами с недостаточным опытом по удалению пресакральных кист (УД 5, СР D [8, 9]).
n Выполнять операции без консультации нейрохирурга или травматолога с целью исключения опухолей нервной системы (шваннома, невринома, менингоцеле и т.д.) или патологии со стороны костей таза, например остеомиелита.
Дальнейшее лечение
Послеоперационный период направлен на профилактику воспалительных явлений в операционной ране, лечение воспалительных осложнений (УД 4, СР C [32]).
Дренажи промываются дважды в день капельно по 200–400 мл 0,2% раствором гидроксиметилхиноксалиндиоксида в растворе натрия хлорида либо хлоргексидином до чистой воды. Промывание осуществляют в течение 5–7 сут, когда промывные воды становятся прозрачными, без примесей, после чего дренажи удаляют (УД 5, СР D [32]).
Прогноз
При радикальном хирургическом лечении неосложненных пресакральных кист прогноз в целом благоприятный, наступает полное выздоровление (УД 2b, СР B [30, 34, 43, 57, 58]). Прогностически неблагоприятными факторами хирургического лечения пресакральных кист
являются выраженные воспалительные изменения, наличие высоких супралеваторных свищей (УД 3b, СР C [8, 9, 57]).
Профилактика
Параректальные тератоидные кисты являются врожденными аномальными структурами, поэтому профилактики их возникновения и роста в течение жизни человека не существует (УД 3b, СР C [10, 30, 33]).
Критерии оценки качества помощи в стационаре представлены в таблице 7.2. Для оценки качества медицинской помощи используют временные, процессуальные и профилактирующие критерии. Временные характеризуют своевременность оказания определенных этапов медицинской помощи. Выполнение пациенту ряда медицинских манипуляций, инструментальных и лабораторных исследований, необходимых для качественного оказания медицинской помощи, оценивают в процессуальных критериях. Для анализа мероприятий, направленных на предотвращение развития осложнений, используют профилактирующие критерии.
Таблица 7.2. Критерии оценки качества медицинской помощи в стационаре больным с тазовыми образованиями (0 — нет, 1 — да)
|
Клинические рекомендации |
Временные |
Процессуальные |
Профилактирующие |
|
1. Клинические рекомендации по диагностике и лечению взрослых пациентов с пресакральной кистой (код МКБ — L05.9) |
Установка диагноза в течение 72 ч: 0/1 |
Оценка анального рефлекса: 0/1. Пальцевое исследование прямой кишки: 0/1. Аноскопия: 0/1. Ректороманоскопия: 0/1. Проктография 0/1. Компьютерная томография или магнитно-резонансная томография: 0/1. Определение группы крови: 0/1. Исследование крови на сифилис, вирусный гепатит В, вирусный гепатит С: 0/1. Клинический анализ крови; биохимический анализ крови; клинический анализ мочи; коагулограмма: 0/1. Метод оперативного лечения в соответствии с клиническими рекомендациями: 0/1. Метод анестезии в соответствии с объемом оперативного лечения: 0/1 |
Отсутствие осложнений: • кровотечение: 0/1; • абсцесс: 0/1; • флегмона: 0/1; • пневмония: 0/1; • тромбоэмболия: 0/1; • летальный исход: 0/1 |
Литература
1. Воробьев Г.И. Основы колопроктологии. — М.: МИА, 2006. — 430 с.
2. Живилов А.П., Клейн К.В., Лахин А.В. и др. Лечение тератом параректального пространства и крестцово-копчиковой области // Проблемы колопроктологии. — М.: МНПИ, 2002. — Вып. 18. — С. 72–74.
3. Кайзер А.М. Колоректальная хирургия. — М.: БИНОМ, 2011. — 737 с.
4. Кузьминов А.М., Волков М.В., Чубаров Ю.Ю. и др. Хирургическая тактика у больных с пресакральными кистами // Проблемы колопроктологии. — М.: МНПИ, 2000. — Вып. 17. — С. 105–108.
5. Кузьминов А.М., Волков М.В., Чубаров Ю.Ю., Обухов В.К. Сравнительный анализ различных методов хирургического лечения ректальных свищей высокого уровня, дренирующих каудальные тератомы // Третий конгресс ассоциации хирургов им Н.И. Пирогова: Сборник. — М., 2001. — 138 с.
6. Кузьминов А.М. Параректальные тератоидные кисты // Основы коло-
проктологии / Под ред. Г.И. Воробьева. — Ростов-н/Д, 2001. — С. 405–412.
7. Никитин А.М., Волков М.В., Якушин А.В. и др. Хирургическое лечение ректальных свищей высокого уровня, дренирующих каудальные тератомы // Анналы хирургии. — 1998. — № 3. — С. 32–36.
8. Федоров В.Д., Коплатадзе А.М. Каудальные тератомы у взрослых больных. — Тбилиси, 1984. — 201 с.
9. Шелыгин Ю.А., Благодарный Л.А. Справочник по колопроктологии. — М.: Литтерра, 2012. — 596 с.
10. Abubakar A.M., Nggada H.A., Chinda J.Y. Sacrococcygeal teratoma in Northeastern Nigeria: 18-years experience // Pediatr. Surg. Int. — 2005. — Vol. 21, N 8. — P. 645–648.
11. Ackerman L., van Drunen M., Reyes C.V. Case report 836: Malignant large cell
lymphoma of sacrum // Skeletal Radiol. — 1994. — Vol. 23, N 3. — P. 232–235.
12. Altman R.P., Randolph J.G., Lilly J.R. Sacrococcygeal teratoma: American Academy of Pediatrics Surgical Section Survey-1973 // J. Pediatr. Surg. — 1974. — Vol. 9, N 3. — P. 389–398.
13. Bakshi N.A., Ross C.W., Finn W.G. et al. ALK-positive anaplastic large cell lymphoma with primary bone involvement in children // Am. J. Clin. Pathol. — 2006. — Vol. 125, N 1. — P. 57–63.
14. Bax N.M., van der Zee D.C. The laparoscopic approach to sacrococcygeal
teratomas // Surg. Endosc. — 2004. — Vol. 18, N 1. — P. 128–130.
15. Bittmann S., Bittmann V. Surgical experience and cosmetic outcomes in children with sacrococcygeal teratoma // Curr. Surg. — 2006. — Vol. 63, N 1. — P. 51–54.
16. Bohm B., Milsom J.W., Fazio V.W. et al. Our approach to the management of congenital presacral tumors in adults // Int. J. Colorectal Dis. — 1993. — Vol. 8, N 3. — P. 134–138.
17. Brindley G.V. Sacral and presacral tumors // Ann Surg. — 1945. — Vol. 121,
N 5. — P. 721–734.
18. Buchs N., Taylor S., Roche B. The posterior approach for low retrorectal tumors in adults // Int. J. Colorectal Dis. — 2007. — Vol. 22, N 4. — P. 381–385.
19. Bullard Dunn K. Retrorectal tumors // Surg. Clin. North Am. — 2010. — Vol. 90, N 1. — P. 163–171.
20. Chen Y., Xu H., Li Y. et al. Laparoscopic resection of presacral teratomas //
J. Minim. Invasive Gynecol. — 2008. — Vol. 15, N 5. — P. 649–651.
21. Chirdan L.B., Uba A.F., Pam S.D. et al. Sacrococcygeal teratoma: clinical characteristics and longterm outcome in Nigerian children // Ann. Afr. Med. — 2009. — Vol. 8, N 2. — P. 105–109.
22. Cho S.H., Hong S.C., Lee J.H. et al. Total laparoscopic resection of primary large retroperitoneal teratoma resembling an ovarian tumor in an adult // J. Minim. Invasive Gynaecol. — 2008. — Vol. 15. — P. 384–386.
23. Chwalinski M., Nowacki M.P., Nasierowska-Guttmejer A. Anorectal teratoma
in an adult woman // Int. J. Colorectal Dis. — 2001. — Vol. 16, N 6. — P. 398–401.
24. Coco C., Manno A., Mattana C. et al. Congenital tumors of the retrorectal space in the adult: report of two cases and review of the literature // Tumori. — 2008. — Vol. 94, N 4. — P. 602–607.
25. Cody H.S., Marcove R.C., Quan S.H. Malignant retrorectal tumors: 28 years’ experience at Memorial Sloan-Kettering Cancer Center // Dis. Colon Rectum. — 1981. — Vol. 24, N 7. — P. 501–506.
26. Corman M.L. Colon and Rectal Surgery. — Philadelphia: Lippincott,
1984. — P. 129–134.
27. Du F., Jin K., Hu X., Dong X., Cao F. Surgical treatment of retrorectal tumors: a retrospective study of a ten-year experience in three institutions // Hepatogastroenterology. — 2012. — Vol. 59, N 117. — P. 1374–1377.
28. Fan M., Peng Q., Wang X.Y. et al. CT and MRI manifestations of pediatric presacral tumors // Ai Zheng. — 2009. — Vol. 28, N 4. — P. 420–424.
29. Freier D.T., Stanley J.C., Thompson N.W. Retrorectal tumors in adults // Surg. Gynecol. Obstet. — 1971. — Vol. 132, N 4. — P. 681–686.
30. Gabra H.O., Jesudason E.C., McDowell H.P. et al. Sacrococcygeal teratoma — a 25-year experience in a UK regional center // J. Pediatr. Surg. — 2006. — Vol. 41, N 9. — P. 1513–1516.
31. Ghosh J., Eglinton T., Frizelle F.A. et al. Presacral tumours in adults //
Surgeon. — 2007. — Vol. 5, N 1. — P. 13–18.
32. Glasgow S.C., Birnbaum E.H., Lowney J.K. et al. Retrorectal tumors: a diagnostic and therapeutic challenge // Dis. Colon Rectum. — 2005. — Vol. 48, N 8. — P. 1581–1587.
33. Golas M.M., Gunawan B., Raab B.W. et al. Malignant transformation of an untreated congenital sacrococcygeal teratoma: a amplification at 8q and 12p detected by comparative genomic hybrydyzation // Cancer Genet. Cytogenet. — 2010. — Vol. 197, N 1. — P. 95–98.
34. Graham D.F., McKenzie W.E. Adult pre-sacral teratoma // Postgrad.
Med. J. — 1979. — Vol. 55. — P. 52–53.
35. Grubor N., Krivokapic Z., Micev M. Presacral cysts, diagnosis, surgical treatment // Acta Chir. Iugosl. — 2000. — Vol. 47, N 4. — Suppl 1. — P. 53–59.
36. Guillem P., Ernst O., Herjean M. et al. Retrorectal tumors: an assessment of the abdominal approach // Ann. Chir. — 2001. — Vol. 126, N 2. — P. 138–142.
37. Hjermstad B.M., Helwig E.B. Tailgut cysts. Report of 53 cases // Am. J. Clin. Pathol. — 1988. — Vol. 89, N 2. — P. 139–147.
38. Ho K.O., Soundappan S.V., Walker K. et al. Sacrococcygeal teratoma: the 13-year experience of a tertiary paediatric centre // J. Paediatr. Child Health. — 2011. — Vol. 47, N 5. — P. 287–291.
39. Ho S.P. et al. Presacral teratocarcinoma presenting as anal fistula and rectal
adenocarcinoma: A Unique Case Presentation and Literature Review // Case Rep. Oncol. — 2012. — Vol. 5, N 1. — P. 84–90.
40. Hobson K.G., Ghaemmaghami V., Roe J.P. et al. Tumors of the retrorectal space // Dis. Colon Rectum. — 2005. — Vol. 48, N 10. — P. 1964–1974.
41. Isaacs H.Jr. Congenital and neonatal malignant tumors. A 28-year experience at Children’s Hospital of Los Angeles // Am. J. Pediatr. Hematol. Oncol. — 1987. — Vol. 9, N 2. — P. 121–129.
42. Isbister W.H., Al S.N. The cutting seton: an experience at King Faisal
Specialist Hospital // Dis. Colon Rectum. — 2001. — Vol. 44, N 5. — P. 722–727.
43. Jao S.W., Beart R.W.Jr., Spencer R.J. et al. Retrorectal tumors. Mayo Clinic experience, 1960–1979 // Dis. Colon Rectum. — 1985. — Vol. 28, N 9. — P. 644–652.
44. Johnson A.R., Ros P.R., Hjermstad B.M. Tailgut cyst: diagnosis with CT and sonography // Am. J. Roentgenol. — 1986. — Vol. 147, N 6. — P. 1309–1311.
45. Kanemitsu T., Kojima T., Jamamoto S. et al. The transspincteric and trans sacral approaches for the surgical excisions of rectal presacral lesions // Surg. Today. — 1993. — Vol. 23, N 10. — P. 860–866.
46. Keslar P., Buck J., Suarez E. From the archives of the AFIP //
Radiographics. — 1994. — Vol. 14. — P. 607–620.
47. Kocaoglu M., Frush D.P. Pediatric presacral masses // Radiographics. — 2006. — Vol. 26, N 3. — P. 833–857.
48. Szyllo K., Lesnik N. Sacrococcygeal teratoma — case report and review of the literature // Am. J. Case Rep. — 2013. — Vol. 14. — P. 1–5.
49. Lev-Chelouche D., Gutman M., Goldman G. et al. Presacral tumors: a practical classification and treatment of a unique and heterogeneous group of diseases // Surgery. — 2003. — Vol. 133, N 5. — P. 473–478.
50. Li G.D., Chen K., Fu D. et al. Surgical strategy for presacral tumors: analysis
of 33 cases // Chin. Med. J. (Engl.). — 2011. — Vol. 124, N 23. — P. 4086–4091.
51. Lin Y.H., Huang R.L, Lai H.C. Presacral teratoma in a Curarrino syndrome woman with an unreported insertion in MNX1 gene // Taiwan J. Obstet. Gynecol. — 2011. — Vol. 50, N 4. — P. 512–514.
52. Localio S.A., Eng K., Ranson J.H.C. Abdominosacral approach for retrorectal tumors // Ann. Surg. — 1980. — Vol. 191. — P. 555–560.
53. Ludwig K. Trans-sacral approaches for presacral cyst/rectal tumor // Operative Tech. Gen. Surg. — 2005. — Vol. 7. — P. 126–136.
54. Lukish J.R., Powell D.M. Laparoscopic ligation of the median sacral artery before resection of a sacrococcygeal teratoma // J. Pediatr. Surg. — 2004. — Vol. 39, N 8. — P. 1288–1290.
55. Lunniss P.J., Kamm M.A., Phillips R.K.S. Factors affecting continence after
surgery for anal fistula // Br. J. Surg. — 1994. — Vol. 81. — P. 1382–1385.
56. Marinello F.G., Targarona E.M., Luppi C.R. et al. Laparoscopic approach to retrorectal tumors: review of the literature and report of 4 cases // Surg. Laparosc. Endosc. Percutan. Tech. — 2011. — Vol. 21, N 1. — P. 10–13.
57. Mazreku A., Karaj A., Avdia I. et al. The presentation and management of presacral tumors // Acta Chir. Iugosl. — 2010. — Vol. 57, N 2. — P. 55–59.
58. Messick C.A., Londono J.M., Hull T. Presacral tumors: how do they compare in pediatric and adult patients? // Pol. Przegl. Chir. — 2013. — Vol. 85, N 5. — P. 253–261.
59. Miles R.M., Stewart G.S. Sacrococcygeal teratomas in adults // Ann. Surg. —
1974. — Vol. 179. — P. 676–683.
60. Negro F., Mercuri M., Ricciardi V. et al. Presacral epidermoid cyst. A case report // Ann. Ital. Chir. — 2006. — Vol. 77, N 1. — P. 75–77.
61. OCEBM Levels of Evidence Working Group. The Oxford 2011 Levels of Evidence. — Oxford Centre for Evidence-Based Medicine, 2011.
62. Pantoja E., Rodriguez-Ibanez I. Sacrococcygeal dermoids and ter-atomas: Historical review // Am J Surg. — 1976. — Vol. 132. — P. 377–383.
63. Pappalardo G., Frattaroli F.M., Casciani E. et al. Retrorectal tumors: the choice of surgical approach based on a new classification // Am. Surg. — 2009. — Vol. 75, N 3. — P. 240–248.
64. Paramythiotis D., Papavramidis T., Michalopoulos A. et al. Chronic
constipation due to presacral teratoma in a 36-year-old woman: a case report // J. Med. Case Rep. — 2010. — Vol. 4. — P. 23.
65. Park Y.J. Multiple presacral teratomas in an 18-year-old girl // J. Korean Soc. Coloproctol. — 2011. — Vol. 27, N 2. — P. 90–93.
66. Paul P.G., Pravinkumar T., Sheetal B. Sacrococcygeal neurofibroma: rare cause for chronic pelvic pain // J. Minim. Invasive Gynecol. — 2012. — Vol. 19, N 4. — P. 517–520.
67. Pidala M.J., Eisenstat T.E., Rubin R.J. et al. Presacral cysts: transrectal
excision in select patients // Am. Surg. — 1999. — Vol. 65, N 2. — P. 112–115.
68. Raney R.B.Jr., Chatten J., Littman P. et al. Treatment strategies for infants with malignant sacrococcygeal teratoma // J. Pediatr. Surg. — 1981. — Vol. 16, N 4. — Suppl. 1. — P. 573–577.
69. Rapport R.L., Ferguson G.S. Dorsal approach to presacral biopsy: technical case report // Neurosurgery. — 1997. — Vol. 40, N 5. — P. 1087–1088.
70. Rintala R., Lahdenne P., Lindahl H. et al. Anorectal function in adults operated for a benign sacrococcygeal teratoma // J. Pediatr. Surg. — 1993. — Vol. 28. — P. 1165–1167.
71. Roka Y.B., Koirala R., Bajracharya A. et al. Giant sacrococcygeal teratoma
in an adult: case report // Br. J. Neurosurg. — 2009. — Vol. 23, N 6. — P. 628–629.
72. Shapiro S.A. Malignant sacrococcygeal teratoma // Med. Pediatr. Oncol. — 1980. — Vol. 8, N 2. — P. 171–175.
73. Sharpe L.A., Van Oppen D.J. Laparoscopic removal of a benign pelvic retroperitoneal dermoid cyst // J. Am. Assoc. Gynecol. Laparosc. — 1995. — Vol. 2, N 2. — P. 223–226.
74. Singer M.A., Cintron J.R., Martz J.E. et al. Retrorectal cyst: a rare tumor
frequently misdiagnosed // J. Am. Coll. Surg. — 2003. — Vol. 196, N 6. — P. 880–886.
75. Stewart R.J., Humphreys W.G., Parks T.G. The presentation and management of presacral tumours // Br. J. Surg. — 1986. — Vol. 73, N 2. — P. 153–155.
76. Tsutsui A., Nakamura T., Mitomi H. et al. Successful laparoscopic resection of a sacrococcygeal teratoma in an adult. Report Case // Surg Today. — 2011. — Vol. 41. — P. 572–575.
77. Ueda K., Tsunoda A., Nakamura A. et al. Presacral epidermoid cyst: report of
a case. Review // Surg. Today. — 1998. — Vol. 28, N 6. — P. 665–668.
78. Uhlig B.E., Johnson R.L. Presacral tumors and cysts in adults // Dis. Colon Rectum 1975. — Vol. 18, N 7. — P. 581–589.
79. Urioste M., Garcia-Andrade Mdel C., Valle L. et al. Malignant degeneration of presacral teratoma in the Currarino anomaly // Am. J. Med. Genet. A. — 2004. — Vol. 128A, N 3. — P. 299–304.
80. Vega Menendez D., Quintans Rodriguez A., Hernandez Granados P. et al.
Tailgut cysts // Cir. Esp. — 2008. — Vol. 83, N 2. — P. 53–60.
81. Wagner M., Zastrow R., Reasa D.A. Presacral tumors: case report, review of the literature // Clin. Anat. — 1995. — Vol. 8, N 3. — P. 227–230.
82. Williams L.S., Rojiani A.M., Quisling R.G., Mickle J.P. Retrorectal cysthamartomas and sacral dysplasia: MR appearance // AJNR Am. J. Neuroradiol. — 1998. — Vol. 19, N 6. — P. 1043–1045.
83. Wolpert A., Beer-Gabel M., Lifschitz O. et al. The management of presacral masses in the adult // Tech. Coloproctol. — 2002. — Vol. 6, N 1. — P. 43–49.
84. Yang B.L., Gu Y.F., Shao W.J. et al. Retrorectal tumors in adults: magnetic resonance imaging findings // World J. Gastroenterol. — 2010. — Vol. 16, N 46. — P. 5822–5829.
85. Yang D.M., Kim H.C., Lee H.L. et al. Squamous cell carcinoma arising from a presacral epidermoid cyst: CT and MR findings // Abdom. Imaging. — 2008. — Vol. 33, N 4. — P. 498–500.
86. Yang D.M., Yoon M.H., Kim H.S. et al. Presacral epidermoid cyst: imaging findings with histopathologic correlation // Abdom. Imaging. — 2001. — Vol. 26, N 1. — P. 79–82.
87. Zoller S., Joos A., Dinter D. et al. Retrorectal tumors: excision by transanal endoscopic microsurgery // Rev. Esp. Enferm. Dig. — 2007. — Vol. 99, N 9. — P. 547–550.
РЕКТОЦЕЛЕ
Введение
Более 40% трудоспособного населения индустриально развитых стран страдает запором, при этом около 80% в этой категории больных составляют женщины. Развивающаяся в течение жизни слабость связочно-мышечного аппарата тазового дна, его повреждения во время осложненных родов приводят к опущению либо выпадению органов таза с нарушением их функции. Таким образом, возникает характерный симптомокомплекс, связанный с нарушением фиксации органов таза, — синдром опущения промежности. Наиболее часто повреждения тазового дна происходят в зоне ректовагинальной перегородки, что сопровождается развитием ректоцеле. Распространенность ректоцеле среди женщин, имеющих жалобы на нарушение опорожнения прямой кишки, по данным разных авторов, составляет от 7 до 56,5% [1–3].
Настоящие рекомендации по диагностике и лечению больных ректоцеле служат руководством для практических врачей, осуществляющих ведение и лечение таких пациентов. Рекомендации подлежат регулярному пересмотру в соответствии с новыми данными научных исследований в этой области.
Рекомендации включают следующие разделы: определение и классификация ректоцеле, диагностика, профилактика, консервативное и хирургическое лечение.
Для отдельных положений рекомендаций приведены уровни доказательности согласно общепринятой классификации Оксфордского центра доказательной медицины (табл. 8.1) [4].
ВАЛИДИЗАЦИЯ РЕКОМЕНДАЦИЙ
Настоящие рекомендации в предварительной версии были рецензированы независимыми экспертами, которых попросили прокомментировать прежде всего, насколько интерпретация доказательств, лежащих в основе рекомендаций, доступна для понимания. Получены комментарии со стороны врачей амбулаторного звена. Полученные комментарии тщательно систематизировались и обсуждались на совещаниях экспертной группы.
Последние изменения в настоящих рекомендациях были представлены для дискуссии на заседании профильной комиссии «Колопроктология»
Таблица 8.1. Уровни доказательности и степени рекомендаций на основании классификации Оксфордского центра доказательной медицины
|
Уровень |
Исследование методов диагностики |
Исследование методов лечения |
|
1а |
Систематический обзор гомогенных диагностических исследований 1-го уровня |
Систематический обзор гомогенных РКИ |
|
1b |
Валидизирующее когортное исследование с качественным «золотым стандартом» |
Отдельное РКИ (с узким доверительным интервалом) |
|
1с |
Специфичность или чувствительность столь высокие, что положительный или отрицательный результат позволяет исключить/установить диагноз |
Исследование «Всё или ничего» |
|
2а |
Систематический обзор гомогенных диагностических исследований >2-го уровня |
Систематический обзор (гомогенных) когортных исследований |
|
2b |
Разведочное когортное исследование с качественным «золотым стандартом» |
Отдельное когортное исследование (включая РКИ низкого качества; т.е. с <80% пациентов, прошедших контрольное наблюдение) |
|
2с |
Нет |
Исследование «исходов»; экологические исследования |
|
3а |
Систематический обзор гомогенных исследований уровня 3b и выше |
Систематический обзор гомогенных исследований «случай– контроль» |
|
3b |
Исследование с непоследовательным набором или без проведения исследования «золотого стандарта» у всех испытуемых |
Отдельное исследование «случай– контроль» |
|
4 |
Исследование «случай–контроль» или исследование с некачественным или зависимым «золотым стандартом» |
Серия случаев (и когортные исследования или исследования «случай–контроль» низкого качества) |
|
5 |
Мнение экспертов без тщательной критической оценки или основанное на физиологии, лабораторные исследования на животных или разработка «первых принципов» |
Мнение экспертов без тщательной критической оценки, лабораторные исследования на животных или разработка «первых принципов» |
|
Степени рекомендаций | ||
|
A |
Согласующиеся между собой исследования 1-го уровня | |
|
B |
Согласующиеся между собой исследования 2-го или 3-го уровня или экстраполяция на основе исследований 1-го уровня | |
|
C |
Исследования 4-го уровня или экстраполяция на основе уровня 2 или 3 | |
|
D |
Доказательства 4-го уровня или затруднительные для обобщения или некачественные исследования любого уровня | |
Экспертного совета Минздрава России 12 сентября 2013 г. Проект рекомендаций был повторно рецензирован независимыми экспертами и врачами амбулаторного звена. Для окончательной редакции и контроля качества рекомендации были проанализированы членами экспертной группы, которые пришли к заключению, что все замечания и комментарии приняты во внимание, риск систематических ошибок при разработке рекомендаций сведен к минимуму.
ОБЛАСТЬ ПРИМЕНЕНИЯ РЕКОМЕНДАЦИЙ
Данные клинические рекомендации применимы при осуществлении медицинской деятельности в рамках Порядка оказания медицинской помощи взрослому населению с заболеваниями толстой кишки, анального канала и промежности колопроктологического профиля.
Определение
Ректоцеле (rectocele: лат. rectum — прямая кишка; греч. kele — выпячивание, грыжа, припухлость) представляет собой дивертикулоподобное выпячивание стенки прямой кишки в сторону влагалища (переднее ректоцеле) и/или по задней полуокружности кишки (заднее ректоцеле). Переднее ректоцеле может быть представлено как изолированная форма или в сочетании с задним ректоцеле и внутренней инвагинацией прямой кишки [5–7].
Классификация
По уровню дефекта ректовагинальной перегородки различают:
n нижнее ректоцеле — локализовано в нижней трети влагалища;
n среднее ректоцеле — локализовано в средней трети влагалища;
n высокое ректоцеле — локализовано в верхней трети влагалища [2].
По выраженности анатомических изменений различают три степени ректоцеле:
n 1-я степень — ректоцеле определяется лишь при пальцевом исследовании прямой кишки как небольшой карман передней стенки прямой кишки;
n 2-я степень — выпячивание прямой кишки во влагалище доходит до его преддверия;
n 3-я степень — выпячивание передней стенки прямой кишки выходит за пределы влагалища [5].
Код по Международной классификации болезней 10-го пересмотра [8]
n Класс: Болезни мочеполовой системы (XIV).
n Блок: Невоспалительные болезни женских половых органов.
n Код: N81.6.
n Название: Ректоцеле.
Профилактика
Профилактика ректоцеле состоит в устранении факторов риска развития заболевания: повышенного внутрибрюшного давления, профилактика послеродовых осложнений, адекватное выполнение акушерских и гинекологических пособий (УД 2b, СР B [9, 10]).
Риск развития ректоцеле увеличивают:
n тяжелые физические нагрузки — современные исследования указывают на то, что ректоцеле чаще возникает в группе женщин, профессиональная деятельность которых связана с физическим трудом (УД 2b, СР B [9]);
n хронический запор, сопровождающийся частым и интенсивным натуживанием (УД 2b, СР B [11]);
n хронические заболевания дыхательной системы с интермиттирующими приступами кашля (УД 2b, СР B [12]);
n избыточный вес (по данным Women’s Health Initiative, увеличение индекса массы тела выше 30 кг/м2 повышает риск развития ректоцеле на 40–75%) (УД 2b, СР B [13]);
n изменение конфигурации позвоночника — отсутствие поясничного лордоза ведет к тому, что суммарный вектор сил внутрибрюшного давления направлен непосредственно на тазовое дно (УД 1b, СР A [14]);
n беременность (каждая беременность увеличивает риск развития ректоцеле на 31%) (УД 2а, СРB [15]);
n осложненное течение родов (хирургические пособия при родах, стремительные роды, разрывы промежности, роды крупным плодом) (УД 2а, СР B [16]);
n гистерэктомия (необходимо ставить строгие показания к удалению матки) (УД 3а, СР B [17, 18]).
Кесарево сечение снижает риск возникновения ректоцеле (УД 2а, СР B [10]).
Вследствие беременности и родов происходит растяжение мышц тазового дна с развитием нейромускулярной дисфункции, которая носит обратимый характер [19]. В связи с этим для профилактики развития синдрома опущения промежности и ректоцеле после родов показано проведение гимнастических упражнений, укрепляющих мышцы тазового дна — гимнастики Кегеля (УД 2а, СР B [20, 21]).
Клинические проявления
По данным литературы, ректоцеле обнаруживают у 40–80% женщин, не предъявляющих жалобы на свое состояние, т.е. без клинических проявлений (УД 2a, СР В [22–25]).
В других случаях ректоцеле отмечаются нарушением опорожнения прямой кишки с развитием синдрома обструктивной дефекации. Синдром выражается следующими признаками:
n затруднением дефекации, сопровождающимся длительным натуживанием;
n ощущением неполного опорожнения прямой кишки;
n применением ручного пособия для опорожнения прямой кишки (УД 2а, СР В [26–28]).
Кроме нарушения опорожнения прямой кишки, возникает диспареуния, что нарушает сексуальную функцию пациенток (УД 2c, СР В [15, 29]). В связи с этим важно определять выраженность диспареунии до и после операции, чтобы правильно оценить результат хирургического лечения в отношении сексуальной жизни пациенток [29]. Также женщины, имеющие ректоцеле, могут предъявлять жалобы на ощущение давления на влагалище и на наличие округлого образования в этой области, периодические боли в нижней половине живота и пояснице, недержание мочи и газов при физической нагрузке, кашле или при чиханье (УД 3a, СР В [30, 31]).
Диагностика
Диагностика ректоцеле начинается со сбора анамнеза, во время которого выясняют историю возникновения запора и особенности опорожнения прямой кишки (УД 3b, СР В [26, 32]).
Тщательный опрос пациентки позволяет установить длительность запора, изменение его характера с течением времени, наличие симптомов обструктивной дефекации, таких как затруднение опорожнения прямой кишки, ощущение неполного опорожнения и ручное вспоможение при дефекации [33]. Кроме этого, обращают внимание на выявление тревожных симптомов: выделение крови из ануса, потерю массы тела, вздутие живота, примеси крови в кале, также выясняют семейную историю в отношении рака или воспалительных заболеваний толстой кишки. Указания на перечисленные симптомы предполагает более полное обследование c использованием эндоскопических и рентгенологических
методов (УД 3b, СР В [26, 32]).
Из анамнеза можно получить сведения об особенностях жизни, указывающих на вероятную причину запора: малоподвижный образ жизни, психические расстройства, длительный прием лекарственных препаратов, заболевания эндокринной системы, такие как сахарный диабет или гипотиреоидизм, признаки синдрома раздраженного кишечника (СРК) с преобладанием запора (УД 3b, СР В [34–40]).
Объективный осмотр, включающий пальцевое обследование прямой кишки, влагалища и аноскопию, позволяет обнаружить выпячивание передней стенки прямой кишки во влагалище, внутреннюю инвагинацию или полное выпадение прямой кишки, парадоксальную реакцию пуборектальной петли, не расслабляющейся во время натуживания. При пальцевом осмотре также можно определить каловые камни, стриктуру или опухоль прямой кишки (УД 3b, СР В [32, 34, 36, 41]).
Однако только по анамнестическим данным и осмотру невозможно определенно диагностировать медленно-транзитный запор или эвакуа-
торные нарушения, которые служат этиопатогенетическими факторами развития ректоцеле (УД 3a, СР В [26, 35]).
Инструментальное обследование с использованием рентгенологических и физиологических методов позволяет определить степень выраженности синдрома опущения промежности, наличие сопутствующих ректоцеле признаков синдрома опущения промежности (внутреннюю инвагинацию, сигмоцеле, диссинергию тазовых мышц), а также функциональное состояние толстой кишки (УД 3а, СР В [42, 43]).
При дефекографии определяют положение прямой кишки относительно лобково-копчиковой линии в покое, при волевом сокращении, время ее опорожнения и остаточный объем (табл. 8.2).
Таблица 8.2. Нормальные показатели дефекографии [44]
|
|
Положение кишки относительно лобково-копчиковой линии, см |
Время опорожнения прямой кишки, с |
Остаточный объем |
|
Покой |
–2,9+0,9 |
12,6+4,2 |
16,5%±5,3 |
|
Волевое сокращение |
–1,7±1,2 | ||
|
Натуживание |
–5,6+1 |
Данные дефекографии позволяют сделать заключение о степени выраженности синдрома опущения промежности, а также определить размер ректоцеле и выявить такие сопутствующие изменения, как внутренняя инвагинация прямой кишки, сигмоцеле и диссинергия тазовых мышц (УД 3а, СР В [44, 42]).
Диагностика ректоцеле может осуществляться с помощью трансректального УЗИ. Смещение мочевого пузыря, матки и стенок влагалища в дистальном направлении при натуживании указывает на наличие у пациентки синдрома опущения промежности. Пролабирование стенки кишки в просвет влагалища служит признаком ректоцеле (УД 3а, СР В [43]).
Эвакуаторная проба — исследование, которое позволяет подтвердить наличие нарушения эвакуации из прямой кишки. Для выполнения данного теста в прямую кишку вводится латексный баллончик, который заполняется 100–120 мл жидкости. После этого в положении сидя на унитазе пациентку просят потужиться. Если баллончик выталкивается из прямой кишки, проба считается положительной, что соответствует норме. Если баллончик остается в кишке, проба отрицательная, что свидетельствует о наличии нарушения эвакуаторной функции прямой кишки и определяет консервативную тактику лечения (УД 3b, СР В [45, 46]).
Профилометрия определяет исходное состояние ЗАПК, которое может изменяться после хирургического лечения ректоцеле, особенно с при-
менением трансанального доступа (УД 3b, СР С [1, 47]). Исследование осуществляют с помощью катетера, введенного в прямую кишку, по которому устанавливают скорость перфузии жидкости, равную 1 мл/мин. Затем катетер вытягивается из прямой кишки со скоростью 5 мм/с, при этом регистрируют давление на всем протяжении его перемещения (табл. 8.3). Анализ данных проводится компьютерной программой с построением графика, на котором отражается распределение давления в анальном канале (УД 3b, СР C [47]).
Таблица 8.3. Показатели профилометрии в норме (мм рт.ст.) [47]
|
Показатель профилометрии |
Покой |
Волевое сокращение |
|
Анальный канал в целом | ||
|
Максимальное давление |
100,8±11,4 |
137,1±12,6 |
|
Среднее давление |
52,2±8,2 |
76,6±8,9 |
|
Коэффициент асимметрии, ЕД |
19,8±2,3 |
19,2±2,6 |
|
Зона высокого давления* | ||
|
Длина зоны, см |
2,2±0,5 |
2,7±0,65 |
|
Среднее давление |
72,1±9,7 |
100,1±12,5 |
|
Коэффициент асимметрии |
15,5±2,1 |
13,9±2,2 |
* Зона высокого давления соответствует проекции внутреннего сфинктера и глубокой порции наружного сфинктера.
Исследование пассажа по толстой кишке имеет значение для выявления медленно-транзитных запоров, которые могут быть одним из пусковых механизмов развития ректоцеле. Существуют разные методики данного исследования, включая использование радиоизотопных маркеров. Однако все они проводятся по одинаковой схеме: после приема контрастного вещества через рот осуществляют ежедневный рентгенологический контроль над его продвижением по толстой кишке, что позволяет оценить моторно-эвакуаторную функцию различных ее отделов. Исследование проводят на фоне обычного для пациента режима питания, а также обращают внимание на наличие или отсутствие стула во время диагностической процедуры. В норме кишка полностью опорожняется от контрастной взвеси в течение 48–72 ч. Время транзита свыше 72 ч говорит о нарушении функции кишки. В функционально скомпрометированных отделах стаз контрастного вещества может превышать 96 ч, что определяется при прочтении рентгенологических снимков (УД 3b, СР В [48–51]).
Интерпретацию данных пассажа по толстой кишке производят с уче-
том показателей дефекографии. Это позволяет определить функциональные особенности толстой кишки — преобладание медленно-транзитного запора или эвакуаторных нарушений [52].
КОНСЕРВАТИВНОЕ ЛЕЧЕНИЕ
Лечение
Пациенткам с ректоцеле без клинических проявлений специального лечения не требуется. Для них целесообразны контрольные осмотры для динамического наблюдения, а также назначение гимнастических упражнений, укрепляющих мышцы тазового дна (гимнастика Кегеля) (УД 3а, СР В [13, 21]).
У женщин с ректоцеле в сочетании с клиническими признаками нарушения опорожнения прямой кишки лечение следует начинать с консервативных мероприятий, заключающихся в подборе режима питания с включением в рацион высоковолокнистых продуктов и большого количества жидкости (УД 2а, СР В [38, 53]).
Ежедневный прием 25 г волокон увеличивает частоту стула у пациентов с хроническим запором (УД 1b, СР A [38]). Доказано, что употребление жидкости до 1,5–2,0 л в день увеличивает частоту стула и снижает необходимость в приеме слабительных средств у пациентов, соблюдающих высокошлаковую диету (УД 2а, СР В [53]).
Консервативное лечение функциональных нарушений толстой кишки всегда должно предварять хирургические мероприятия по поводу ректоцеле (УД 3b, СР В [54]).
В тех случаях, когда функцию кишки не удается улучшить с помощью режима питания, следует использовать слабительные средства и прокинетики.
Макрогол образует водородные связи с молекулами воды в просвете кишки, увеличивает содержание жидкости в химусе, стимулирует механорецепторы и улучшает перистальтику кишечника. Рекомендуется ежедневный прием 20 г макрогола (УД 2а, СР А [55]).
Прукалоприд — прокинетик, селективный антагонист 5-НТ4серотониновых рецепторов, что объясняет его действие на моторику кишечника. Рекомендуемая доза — 2 мг в день. В результате семи плацебо-контролируемых исследований установлено, что прокинетики увеличивают частоту опорожнения толстой кишки по сравнению с группой, принимавшей плацебо (УД 2а, СР А [57]).
Сочетание препаратов, увеличивающих объем кишечного содержимого (макрогол) и усиливающих кишечную перистальтику (прукалоприд), часто дает эффект в лечении хронического запора (УД 2а, СР А [55, 56]). Оправданно также применение биологических добавок на основе се-
мян подорожника и лактулозы (УД 2а, СР В [56]).
Мукофальк♠ — препарат растительного происхождения, состоящий из оболочек семян подорожника, увеличивает объем химуса, что стимулирует перистальтику. Доза мукофалька♠ подбирается в зависимости от выраженности запора — от 3 до 6 саше в день в 2–3 приема (максимальная доза соответствует 20 г псилиума).
Лактулоза оказывает осмотическое, слабительное действие, стимулирует размножение молочно-кислых бактерий и усиливает перистальтику толстой кишки. Максимальная доза для взрослых — 60 мл/сут. Кратность приема может составлять 12 (реже 3) раз в день. Курс лактулозы назначают на 1–2 мес, а при необходимости и на более длительный срок. Отменяют препарат постепенно под контролем частоты и консистенции стула.
Сравнительная оценка действия мукофалька♠ (фитомуцила♠) и лактулозы в рамках проспективного нерандомизированного исследования показала, что мукофальк♠ — более эффективное средство, которое обеспечивает лучшую консистенцию стула и дает меньше побочных реакций по сравнению с лактулозой и другими слабительными (УД 1a, СР A [58]). Кроме указанных препаратов, для улучшения функции толстой кишки могут применяться другие слабительные средства, такие как магния гидроксид, бисакодил и т.д. (УД 3в, СР С [56, 59]). По результатам метаанализа, включавшего 11 контролируемых исследований, отмечено учащение стула и увеличение объема каловых масс после приема слабительных, однако эти данные не отличались от плацебо-эффекта по ис-
течении 4 нед [59].
Пациенткам, у которых ректоцеле выявляется на фоне диссинергии мышц тазового дна, назначается проведение биофидбек-терапии (УД 2а, СР В [60]).
Методика. Пациентке в положении на боку в задний проход вводится датчик. При выполнении волевых сокращений сфинктера показатели давления в анальном канале трансформируются в акустические или визуальные сигналы, отраженные на мониторе. Анализируя эти сигналы, пациентка учится контролировать мышечные сокращения и изменять их с помощью волевых усилий, тем самым улучшая функцию опорожнения прямой кишки. Упражнения выполняются 15–30 раз. Курс 10–15 сеансов.
Положительный эффект от проведения биофидбек-терапии, по разным данным, составляет 35–90% (УД 2а, СР В [61–63]). Отмечается также стойкость достигнутого эффекта. Сообщается о пациентах, способных с помощью волевых усилий эвакуировать баллончик объемом 50 мл через 6 и 12 мес после лечения [60].
ПОКАЗАНИЯ К ХИРУРГИЧЕСКОМУ ЛЕЧЕНИЮ
Даже после проведенного консервативного лечения, не давшего положительного эффекта, у хирурга должны оставаться сомнения в необходимости хирургического лечения ректоцеле. Эти сомнения обусловлены тем, что синдром обструктивной дефекации, который диагностируется наряду с ректоцеле, может быть результатом различных проблем, разрешение которых невозможно только хирургическим путем (УД 2а, СР В [64, 65]).
В рамках проспективного исследования, проведенного в Италии, были обследованы 100 пациенток с выраженными эвакуаторными нарушениями из прямой кишки. У 2/3 из них был обнаружен тревожный или депрессивный синдром, что является негативным предиктором отдаленных результатов лечения, предполагаемого у этих больных. Кроме этого, у пациенток были выявлены такие патологические изменения, как энтероцеле (17%), диссинергия мышц тазового дна (44%), снижение ректальной чувствительности (33%) и замедление транзита по ободочной кишке (28%) [66]. Перечисленные состояния могут сопутствовать ректоцеле и определять неблагоприятные функциональные результаты после хирургической коррекции дефекта ректовагинальной перегородки (УД 2a, СР B [67–70]). Эти же патологические изменения с течением времени могут ухудшить до 50% хорошие результаты хирургического лечения ректоцеле, полученные в ранние сроки после операции (УД 2a, СР B [64, 67, 70–72]).
Следует также учитывать вероятность развития такого осложнения хирургического лечения ректоцеле, как диспареуния, что значительно нарушает интимную жизнь пациенток. В связи с этим нужно с осторожностью прибегать к оперативному лечению у молодых женщин, ведущих активную половую жизнь (УД 3d, СР B [73]).
Таким образом, показания к хирургическому лечению устанавливаются в тех случаях, когда:
n пациентку субъективно беспокоят ощущения давления на влагалище и присутствие «мешка» во влагалище;
n опорожнение прямой кишки производят только с помощью ручного вспоможения, и даже это не приносит удовлетворения от дефекации;
n все проводимые мероприятия, направленные на улучшение опорожнения прямой кишки (соблюдение режима питания, применение слабительных препаратов, биофидбек-терапия), не дали положительного результата;
n по данным дефекографии, вектор движения каловых масс направлен в сторону ректоцеле, и остаточный объем контраста в кишке превышает 30%;
n по данным обследования, ректоцеле сочетается с внутренней инвагинацией прямой кишки с клинической картиной недостаточности анального сфинктера (УД 2c, СР В [74, 75]).
Крайне важное значение имеет проведение перед операцией подробной беседы о предстоящем лечении. Пациентке следует объяснить, что цель операции — устранение анатомического дефекта ректовагинальной перегородки, что может улучшить функцию прямой кишки и опорожнение. Нужно также сообщить об имеющихся у нее других признаках опущения промежности, которые могут отрицательно повлиять на результат лечения, о рисках развития послеоперационных осложнений и необходимости соблюдения предписанного режима в послеоперационном периоде. И только после усвоения пациенткой ин-
формации о предстоящем лечении, вероятных его результатах и после ее согласия на хирургическое вмешательство можно начинать подготовку к операции [73].
ХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕ
Для лечения ректоцеле предложено более 30 способов операций и их модификаций. Все вмешательства направлены на укрепление передней стенки прямой кишки и ликвидацию дивертикулоподобного выпячивания и отличаются друг от друга хирургическими доступами (УД 2а, СР В [68, 76–79]).
Трансвагинальный доступ (УД 2а, СР В [74, 30])
Принцип операции, выполняемой трансвагинальным доступом, заключается в восстановлении ректовагинальной фасции и укреплении ректовагинальной перегородки с помощью передней леваторопластики [80, 81].
Методика. После гидравлической препаровки ректовагинальной перегородки раствором натрия хлорида с эпинефрином (1 мл эпинефрина на 400 мл раствора натрия хлорида) производят продольный разрез задней стенки влагалища в проекции ректоцеле. Стенку влагалища отделяют от ректовагинальной фасции в латеральных направлениях, мобилизуют переднюю стенку прямой кишки. На ректовагинальную фасцию накладывают несколько швов из синтетического, длительно рассасывающегося материала (викрил, полисорб). Острым путем мобилизуют края леваторов и сшиваются над ранее ушитой фасцией. Заднюю стенку влагалища ушивают непрерывным швом (викрил, полисорб).
С помощью этого метода удается добиться ликвидации дивертикулоподобного выпячивания во влагалище у 80% пациенток и необходимости ручного вспоможения при дефекации у 67% оперированных (УД 2а, СР В [74, 80]). Однако у 33% больных не отмечается улучшения опорожнения прямой кишки, послеоперационная диспареуния возникает у 25%, проблемы с анальным держанием появляются у 36% оперированных, и по крайней мере 10% пациенток нуждаются в повторной оперативной коррекции (УД 2а, СР В [76, 82, 83, 30]).
Для укрепления ректовагинальной перегородки используются также синтетические (полипропилен, пролен) и биологические материалы (пермакол) (УД 2а, СР В [84, 85]).
Методика. Таким же образом, как при типичной леваторопластике, обнажают переднюю стенку прямой кишки, покрытую ректовагинальной фасцией. После ушивания последней на переднюю стенку прямой кишки помещают ромбовидный имплантат, размер которого адаптируют к размеру раны. Латеральные края имплантата подшивают к надкостнице нисходящей ветви лобковой кости (викрил, полисорб), затем ушивают стенку влагалища. Данный метод позволяет укрепить ректовагинальную перегородку без натяжения тканей, которое создается при леваторопластике.
По результатам проспективного исследования было зарегистрировано улучшение опорожнения кишки после пластики ректовагинальной перегородки биологическим имплантатом, однако признаки синдрома обструктивной дефекации были отмечены почти у половины оперированных через 3 года после операции (УД 2а, СР В [85]). Другое рандомизированное исследование дало схожие показатели положительных результатов лечения после леваторопластики как самостоятельной операции и леваторопластики с использованием биологического имплантата — 89 и 76% соответственно (УД 1b СР A [86]).
Трансректальный доступ (УД 2а, СР В [87, 88])
Использование данного метода позволяет иссечь избыточную слизистую оболочку и ликвидировать дефект ректовагинальной перегородки через прямую кишку (УД 2а, СР В [88–91]).
В начале 1990-х г. А. Лонго была предложена степлерная трансанальная резекция прямой кишки (STARR) с помощью циркулярного аппарата РРН-01, которая стала применяться для лечения ректоцеле и с недавних пор практически вытеснила традиционный трансректальный метод лечения (УД 2а, СР В [92, 93]).
Методика. С помощью окончатого аноскопа накладывают два слизи-
сто-мышечных полукисетных шва на переднюю полуокружность прямой кишки (викрил на игле 5/8) — первый шов на 2 см от зубчатой линии, второй — на 2 см проксимальнее первого. В прямую кишку вводят рабочую часть циркулярного степлера РРН-01 с максимально выдвинутой головкой. Швы, подтягивающие стенку прямой кишки, завязывают на стержне аппарата и головку смыкают с основной частью. При нажатии на ручку аппарата происходит резекция участка стенки прямой кишки, вовлеченной в аппарат, с формированием двухрядного скрепочного шва. Наложенный механический шов создает соединительнотканно-мышечный каркас передней стенки кишки, тем самым укрепляя ректовагинальную перегородку. Таким же образом производят резекцию кишечной стенки по задней полуокружности.
Операция Лонго эффективна при сочетании ректоцеле с внутренней инвагинацией прямой кишки [94]. Однако есть сообщения, что она ненадежна при ректоцеле при диаметре более 3 см, так как недостаточно ликвидирует дефект ректовагинальной перегородки (УД 2а, СР В [94]).
По данным литературы, результаты лечения ректоцеле методом Лонго варьируют от 90% хороших результатов в первые месяцы после вмешательства до снижения эффекта от лечения и возврате симптомов у 52% пациенток через 18 мес после операции (УД 2а, СР В [96]).
Трансперинеальный доступ (УД 3в, СР D [97])
Данный доступ был предложен для хирургической коррекции ректоцеле, сочетающегося с анальной инконтиненцией, обусловленной дефектом анального сфинктера. Во время операции производят восстановление ректовагинальной фасции и переднюю сфинктеролеваторопластику.
Методика. Выполняют гидравлическую препаровку ректовагинальной перегородки раствором натрия хлорида с эпинефрином (1 мл эпинефрина на 400 мл раствора натрия хлорида). Разрез выполняют в поперечном направлении на границе слизистой оболочки влагалища и кожи промежности. Затем производят расщепление ректовагинальной перегородки, мобилизацию передней стенки прямой кишки, передних порций мышц леваторов. Затем выполняют восстановление ректовагинальной фасции и переднюю леваторопластику. При наличии дефекта анального сфинктера после иссечения замещающих его рубцовых тканей сшивают края сфинктера. Рану промежности ушивают в продольном направлении.
Улучшение эвакуаторной функции прямой кишки и анального держания наблюдается у 75% пациенток [97].
Трансперинеальный доступ используется также для пластики ректовагинальной перегородки сетчатыми (полипропилен, пролен) или биологическими (пермакол) имплантатами (УД 3в, СР D [98–101]). Методика пластики такая же, как при трансвагинальном доступе.
По данным ретроспективного исследования, субъективное улучшение состояния было отмечено у 77% женщин после трансперинеальной пластики ректовагинальной перегородки с использованием полипропиленового и полиглактин-полипропиленового имплантатов. Однако менее удовлетворительные результаты в этой группе отмечались у пациенток с нарушением транзита по толстой кишке и у тех, кто нуждался в ручном пособии для опорожнения кишки (УД 3a, СР D [99]).
Сообщается также об улучшении состояния по таким показателям, как необходимость длительного натуживания при дефекации и ощущение неполного опорожнения прямой кишки в 80 и 70% случаев соответственно, у пациенток, которым выполнялась пластика ректовагинальной перегородки с использованием коллагенового имплантата (пермакол) (УД 3a, СР D [100]).
Следует отметить, что операции с использованием синтетических имплантатов для укрепления ректовагинальной перегородки в 6% случаев осложняются эрозией влагалища в области сетки, а у 1,5% пациенток в послеоперационном периоде может возникнуть ректовагинальный свищ (УД 3a, СР D [102]).
Трансабдоминальный доступ (УД 3а, СР B [103, 104])
Чрезбрюшинный доступ для коррекции ректоцеле используют в тех случаях, когда дефект ректовагинальной перегородки сочетается с внутренней инвагинацией прямой кишки или энтероцеле. С помощью ректокольпосакропексии сетчатым имплантатом удается произвести коррекцию комплексных проявлений синдрома опущения промежности с низким показателем рецидивов [103].
Методика. Выполняют нижнесрединную лапаротомию. Справа
от прямой кишки на уровне мыса крестца вскрывается тазовая брюши-
на. Разрез продлевают вниз с переходом на маточно-прямокишечную складку. При этом производят мобилизацию прямой кишки по правой полуокружности до боковой связки и спереди до анального сфинктера. На этом уровне к передней стенке прямой кишки тремя швами (полисорб) фиксируют край полипропиленового имплантата, который имеет вид ленты размером 3×10 см. К этому же имплантату двумя-тремя швами с использованием аналогичного шовного материала фиксируют задний свод влагалища. Противоположный конец полипропиленовой ленты подшивают к мысу крестца (полисорб). Брюшина ушивается непрерывным швом с вовлечением в него края имплантата (полисорб). Таким образом уменьшается глубина дугласова кармана.
Этот метод позволяет одновременно выполнить коррекцию ректоцеле, фиксацию кишки к крестцу и укрепление тазовой брюшины (УД 3a, СР B [104, 105]).
Трансабдоминальную коррекцию ректоцеле производят как открытым, так и лапароскопическим способом. Это позволяет добиться ликвидации анатомических дефектов ректовагинальной перегородки и улучшения функции прямой кишки более чем в 80% случаев (УД 4, СР С [106–108]).
Прогноз
В результате хирургического лечения ректоцеле ликвидации или уменьшения размера дивертикулоподобного выпячивания передней стенки прямой кишки удается достигнуть у 90% пациенток (УД 2a, СР A [75, 76, 83, 98]). Однако почти у половины оперированных не отмечается прямой корреляционной зависимости между анатомическими и функциональными результатами хирургического лечения (УД 2a, СР A [67–70]). Независимо от метода оперативного лечения, улучшение функциональных результатов в течение первого года после хирургической коррекции ректоцеле регистрируется почти у 90% пациенток, однако с течением времени этот показатель снижается и достигает 50% в отдаленном послеоперационном периоде (УД 2a, СР A [64, 67, 70–72]).
Критерии оценки качества помощи в стационаре представлены в таблице 8.4. Для оценки качества медицинской помощи используют временные, процессуальные и профилактирующие критерии. Временные характеризуют своевременность оказания определенных этапов медицинской помощи. Выполнение пациенту ряда медицинских манипуляций, инструментальных и лабораторных исследований, необходимых для качественного оказания медицинской помощи, оценивают в процессуальных критериях. Для анализа мероприятий, направленных на предотвращение развития осложнений, используют профилактирующие критерии.
Таблица 8.4. Критерии оценки качества медицинской помощи в стационаре больным синдромом опущения промежности (ректоцеле) (0 — нет, 1 — да)
|
Клинические рекомендации |
Временные |
Процессуальные |
Профилактирующие |
|
Клинические рекомендации по диагностике и лечению взрослых пациентов с ректоцеле (код МКБ — N81.6) |
Установка клинического диагноза в течение 72 ч: 0/1 |
Оценка анального рефлекса: 0/1. Пальцевое исследование прямой кишки: 0/1. Аноскопия: 0/1. Ректороманоскопия: 0/1. Определение группы крови: 0/1. Исследование крови на сифилис, вирусный гепатит В, вирусный гепатит С: 0/1. Клинический анализ крови; биохимический анализ крови; клинический анализ мочи; коагулограмма: 0/1. Сфинктерометрия: 0/1. Проктография с натуживанием (дефекография): 0/1. Биопсия из края язвы с патоморфологическим исследованием при ее наличии: 0/1. Метод оперативного лечения в соответствии с клиническими рекомендациями: 0/1. Метод анестезии в соответствии с объемом оперативного лечения: 0/1 |
Отсутствие осложнений: • кровотечение: 0/1; • абсцесс: 0/1; • флегмона: 0/1; • пневмония: 0/1; • тромбоэмболия: 0/1; • летальный исход: 0/1 |
Литература
1. Шелыгин Ю.А., Титов А.Ю., Джанаев Ю.А. и др. Особенности клинической картины и характер нейрофункциональных нарушений у больных ректоцеле // Колопроктология. — 2012. — Т. 42, № 4. — С. 27–32.
2. Block I.R. Transrectal repair of rectocele using obliterative suture // Dis. Colon Rectum. — 1986. — Vol. 29. — P. 707–711.
3. Savoye-Collet C., Savoye G., Koning E. et al. Defecography in symptomatic older women living at home // Age Ageing. — 2003. — Vol. 32. — P. 347–350.
4. OCEBM Levels of Evidence Working Group. The Oxford 2011 Levels of Evidence. — Oxford Centre for Evidence-Based Medicine, 2011.
5. Воробьев Г.И. Основы колопроктологии. — М.: МИА, 2006. — С. 193–208.
6. Краснопольский В.Н., Иоселиани М.Н., Рижинашвили И.Д., Слободянюк А.И. Современные аспекты хирургического лечения опущения и выпадения внутренних половых органов у женщин // Акуш. и гин. — 1990. — № 8. — С. 58–61.
7. Попов А.А., Славутская О.С, Рамазанов М.Р. Современные аспекты диагностики и хирургического лечения опущения и выпадения половых органов у женщин // Эндоскоп. хир. — 2002. — № 6. — С. 13–15.
8. Международная классификация болезней 10-го пересмотра. Доступен с сайта: www.10mkb.ru.
9. Nygaard I., Bradley C., Brandt D. Women’s Health Initiative. Pelvic organ prolapse in older women: prevalence and risk factors // Obstet. Gynecol. — 2004. — Vol. 104. — P. 489–497.
10. Lukacz E.S., Lawrence J.M., Contreras R. et al. Parity, mode of delivery, and
pelvic floor disorders // Obstet. Gynecol. — 2006. — Vol. 107. — P. 1253–1260.
11. Soares F.A., Regadas F.S., Murad-Regadas S.M. et al. Role of age, bowel function and parity on anorectocele pathogenesis according to cinedefecography and anal manometry evaluation // Colorectal Dis. — 2009. — Vol. 11, N 9. —
P. 947–950. (УD-III cross-sectional study).
12. Blandon R.E., Bharucha A.E., Melton L.J. et al. Risk factors for pelvic floor repair after hysterectomy // Obstet. Gynecol. — 2009. — Vol. 113, N 3. — P. 601– 608.
13. Hendrix S.L., Clarc A., Nygaard I. et al. Pelvic organ prolapse in Women’s Health Initiative: gravity and gravidity // Am. J. Obstet. Gynecol. — 2002. — Vol. 186. — P. 1160–1166.
14. Mattbox T.F., Lucente V., McIntyre P. Abdominal spinal curvature and
its relationship to pelvic organ prolapsed // Am. J. Obstet. Gynecol. — 2000. — Vol. 183. — P. 1381–1384.
15. Handa V.L., Harvey L., Cundiff G.W. et al. Sexual function among women with urinary incontinence and pelvic organ prolapse // Am. J. Obstet. Gynecol. — 2004. — Vol. 191. — P. 751–756.
16. Fritel X., Ringa V., Varnoux N. et al. Mode of delivery and fecal incontinence
at midlife: a study of 2640 women in the Gazel cohort // Obstet. Gynecol. — 2007. — Vol. 110, N 1. — P. 31–38.
17. Moalli P.A., Jones I.S., Meyn L.A., Zyczynsky H.M. Risk factors associated with pelvic floor disorders in women undergoing surgical repair // Obstet. Gynecol. — 2003. — Vol. 101. — P. 869–874.
18. Swift S.E., Pound T., Dias J.K. Case-control study of etiologic factors in the
development of severe pelvic organ prolapse // Int. Urogynecol. J. Pelvic Floor Dysfunct. — 2001. — Vol. 12. — P. 187–192.
19. Weidner A.C., Jamison M.G., Branham V. et al. Neuropathic injury to the levator ani occurs in 1in 4 primaparous women // Am. J. Obstet. Gynecol. — 2006. — Vol. 195. — P. 1851–1856.
20. Marques A., Stothers L., Macnab A. The status of pelvic floor muscle training
for women // Can. Urol. Assoc. J. — 2010, Dec. — Vol. 4, N 6. — P. 419–424.
21. Harvey M.A. Pelvic floor exercises during and after pregnancy: a systematic review of their role in preventing pelvic floor dysfunction // J. Obstet. Gynaecol. Can. — 2003. — Vol. 25, N 6. — P. 487–498.
22. Bartolo D.C., Bartram C.I., Ekberg O. et al. Simposium proctography // Int.
J. Colorectal Dis. — 1988. — Vol. 3. — P. 67–89.
23. Shovron P.G., McHugh S., Diamant N.E. et al. Defecography in normal volunteers: Results and implications // Gut. — 1989. — Vol. 30. — P. 1737–1749.
24. Freimanis M.G., Wald A., Caruana B., Bauman D.H. Evacuation proctography in normal volunteers // Invest. Radiol. — 1999. — Vol. 26. — P. 581–585.
25. Selvaggy F., Pesce G., Scotto Di Carlo E. et al. Evaluation of normal subjects by defecographic techniques // Dis. Colon Rectum. — 1990. — Vol. 33. — P. 698–702.
26. Brandt L.J., Schoenfeld P., Prather C.M. et al. An evidence-based approach to the management of chronic constipation in North America. American College of Gastroenterology Task Force // Am. J. Gastroenterol. — 2005. — Vol. 100. —
P. S1–S4.
27. Keighley M.R.B. Stipsy // Chirurgia di Ano-Retto e Colon / Eds M.R.B. Keighley, N.S. Williams. — Italy: Piccin Padova, 2000. — P. 615–644.
28. Weber A.M., Walters M.D., Ballard L.A. et al. Posterior vaginal prolapse and urinary incontinence // Obstet. Gynecol. — 1995. — Vol. 85. — P. 483–487.
29. Weber A.M., Walters M.D., Piedmonte M.R. Sexual function and vaginal anatomy in women before and after surgery for pelvic organ prolapse and urinary incontinence // Am. J. Obstet. Gynecol. — 2000. — Vol. 182. — P. 1610–1615.
30. Kahn M.A., Stanton S.L. Techniques of rectocele repair and their effects on
bowel function // Int. Urogynecol. J. — 1998. — Vol. 9. — P. 37–47.
31. Felt-Bersma R.J.F., Cuesta M.A. Rectal prolapse, rectal intussusception, rectocele and solitary rectal ulcer syndrome // Gastroenterol. Clin. North Am. — 2001. — Vol. 30. — P. 199–222.
32. Drossman D.A., Corraziari E., Talley N.J. et al. Functional bowel disorders // Rome II: the Functional Gastrointestinal Disorders: Diagnosis, Pathophisiology, and Treatment: a Multinational Consensus. — 2nd ed. / McLean V.A. — Degnon Associates, 2000. — P. 352–397.
33. Mellgren A.F., Zetterstorm J., Lopez A. Rectocele // Complex Anorectal Disorders: Investigation and Management / Eds S.D. Wexner, A.P. Zbar,
M. Pescatori. — London: Spinger-Verlag, 2005. — P. 446–460.
34. Longstreth G.F., Thompson W.G., Chey W.D. et al. Functional bowel disorders // Gastroenterology. — 2006. — Vol. 130. — P. 1480–1491.
35. Beck D.E. Initial evaluation of constipation // Constipation evaluation and management / Eds S.D. Wexner, D.C. Bartolo. — Oxford: ButterworthHeinemann, 1995. — P. 31–38.
36. Thornton M.J., Lubowski D.Z. An overview // Complex Anorectal Disorders:
Investigation and Management / Eds S.D. Wexner, A.P. Zbar, M. Pescatori. — London: Spinger-Verlag, 2005. — P. 412–428.
37. Pfifer J. Managing slow-transit constipation // Complex Anorectal Disorders: Investigation and Management / Eds S.D. Wexner, A.P. Zbar, M. Pescatori. — London: Spinger-Verlag, 2005. — P. 429–445.
38. Griffenberg L., Morris M., Atkinson N., Levenback C. The effect of dietary fiber
on bowel function following radical hysterectomy: a randomized trial // Gynecol. Oncol. — 1997. — Vol. 66. — P. 417–424.
39. Preston D.M., Lennard-Jones J.E. Severe chronic constipation of young women: idiopathic slow-transit constipation // Gut. — 1986. — Vol. 27. — P. 41–48.
40. Walsh P.V., Peebles-Brown D.A., Watkinson G. Colectomy for slow-transit constipation // Ann. R. Coll. Surg. Engl. — 1987. — Vol. 69. — P. 71–75.
41. Rantis P.C., Vernava A.M., Daniel G.L., Longo W.E. Chronic constipation: is the workup worth the cost? // Dis. Colon Rectum. — 1997. — Vol. 40. — P. 280–286.
42. Dobben A.C., Wiersma T.G., Janssen L.W. et al. Prospective assessment of interobserver agreement for defecography in fecal incontinence // Am. J. Roentgenol. — 2005. — Vol. 185. — P. 1166–1172.
43. Regadas F.S.P., Murad-Regadas S.M., Wexner S.D. et al. Three-dimensional
endosonography and anal manometry in assessment anterior rectocele in women.
A new pathogenesis concept and the basic surgical principle // Colorectal Dis. — 2006. — Vol. 9. — P. 80–85.
44. Зароднюк И.В. Рентгенологическая дефекография в обследовании колопроктологических больных // Радиология-практика. — 2004. — № 2. — С. 26–30.
45. Beck D.E. Simplified balloon expulsion test // Dis. Colon Rectum. —
1992. — Vol. 35. — P. 597–598.
46. Fleshman J.W., Dreznik Z., Cohen E. et al. Balloon expulsion test facilitates diagnosis of pelvic floor outlet obstruction due to nonrelaxing puborectalis muscle // Dis. Colon Rectum. — 1992. — Vol. 35. — P. 1019–1025.
47. Подмаренкова Л.Ф., Алиева Э.И., Полетов Н.Н. и др. Роль функциональных методов исследования запирательного аппарата прямой кишки в выявлении патогенетических механизмов анальной инконтиненции // Колопроктология. — 2006. — Т. 16, № 2. — С. 24–30.
48. Metcalf A.M., Phillips S.F., Zinsmeister A.R. et al. Simplified assessment of
colonic transit // Gastroenterology. — 1987. — Vol. 92. — P. 40–47.
49. Hutchinson R., Kumar D. Colonic and small-bowel transit studies // Constipation: Etiology, Evaluation and Management / Eds S.D. Wexner,
D.C. Bartolo. — Oxford: Butterworth-Heinemann, 1995. — P. 52–62.
50. Van der Sijp J.R., Kamm M.A., Nightingale J.M. et al. Radioisotope determination of regional colonic transit in severe constipation: comparison with radiopaque marcers // Gut. — 1993. — Vol. 34. — P. 402–408.
51. McLean R.G., Smart R.C., Gaston-Parry D. et al. Colon transit scintigraphy in health and constipation using oral iodine-131-cellulose // J. Nucl. Med. — 1990. — Vol. 31. — P. 985–959.
52. Schmitt B., Wexner S.D., Bartolo D.C. Surgical treatment of colonic inertia //
Complex Anorectal Disorders: Investigation and Management / Eds S.D. Wexner,
A.P. Zbar, M. Pescatori. — London: Spinger-Verlag, 2005. — P. 153–159.
53. Anti M., Pignataro G., Armuzzi A. et al. Water supplementation enhances the effect of high-fiber diet on stool frequency and laxative consumption in adult patients with functional constipation // Hepatogastroenterology. — 1998. — Vol. 45. — P. 727–732.
54. Voderholzen W.A., Schatke W., Mudldorfer B.E. et al. Clinical response to dietary fiber treatment of chronic constipation // Am. J. Gastroenterol. — 1997. — Vol. 92. — P. 95–98.
55. Cleveland M.V., Flavin D.P., Ruben R.A. et al. New polyethylene glycol
laxative for treatment of constipation in adults: a randomized, doble-blind, placebo controlled study // South. Med. J. — 2001. — Vol. 94. — P. 478–481.
56. Ramkumar D., Rao S.S. Efficacy and safety of traditional medical therapies for chronic constipation: systematic review // Am. J. Gastroenterol. — 2005. — Vol. 100. — P. 936–971.
57. Evans B.W., Clarc W.K. et al. Tegaserod for the treatment of irritable bowel
syndrome // Cochrane Database Syst. Rev. — 2006. — Is. 2.
58. Dettmar P.W., Sykes J. A multi-centre, general practice comparison of ispaghula husk with lactulose and other laxatives in the treatment of simple constipation // Curr. Med. Res. Opin. — 1998. — Vol. 14. — P. 227–233.
59. Jones M.P., Talley N.J., Nuyts G., Dubois D. Lack of objective of efficacy of laxatives in chronic constipation // Dig. Dis. Sci. — 2002. — Vol. 47. — P. 2222–2230.
60. Chiaroni G., Whitehead W.E., Pezza V. et al. Biofeedback is superior to laxatives for normal transit constipation due to pelvic floor dissynergia // Gastroenterology. — 2006. — Vol. 130. — P. 657–664.
61. Wang J., Luo M.H., Qi Q.H., Dong Z.L. Prospective study of biofeedback retraning in patients with chronic idiopathic functional constipation // World J. Gastroenterol. — 2003. — Vol. 9. — P. 2109–2113.
62. Wexner S.D., Cheape J.D., Jorge J.M. et al. A prospective assessment of
biofeedback for treatment of paradoxical puborectalis contraction // Dis. Colon Rectum. — 1992. — Vol. 35. — P. 145–50.
63. Battaglia E., Serra A.M., Buonafede G. et al. Biofeedback for dyssynergia // Dis. Colon Rectum. — 2004. — Vol. 47. — P. 90–95.
64. Pescatori M., Boffi F., Russo A., Zbar A.P. Complications and recurrence after excision of rectal internal mucosal prolapse for obstructed defecation // Int. J. Colorectal Dis. — 2006. — Vol. 21. — P. 160–165.
65. Pescatori M., Spyrou M., Pulvurenti d’Urso A. A prospective evaluation of
occult disorders in obstructed defecation using the «iceberg diagram» // Colorectal Dis. — 2007. — Vol. 9. — P. 452–56.
66. Pescatori M., Zbar A.P. Reinterventions after complicated or failed STARR procedure // Int. J. Colorectal Dis. — 2009. — Vol. 24. — P. 87–95.
67. Christiansen J., Zhu B.W., Ramussen O.O., Sorensen M. Internal rectal intisusseption: Results of surgical repair // Dis. Colon Rectum. — 1992. — Vol. 35. — P. 1026–1028.
68. Boccasanta P., Venturi M., Calabro G. et al. Which surgical approach for rectocele? A multicentric report from Italian coloproctologists // Tech. Coloproctol. — 2001. — Vol. 5. — P. 149–56.
69. Vermeulen J., Lange J.F., Sikkenk A.C., van der Harst E. Anterolateral rectopexy for correction of rectocele leads to good anatomical but poor functional results // Tech. Coloproctol. — 2005. — Vol. 9. — P. 35–41.
70. Roman H., Michot F. Long-term outcomes of transanal rectocele repair //
Dis. Colon Rectum. — 2005. — Vol. 48. — P. 510–517.
71. Schultz I., Mellgren A. Dolk A. et al. Long-term results and functional outcome after Ripstein rectopexy // Dis. Colon Rectum. — 2000. — Vol. 43. — P. 35–43.
72. Brown A.J., Anderson J.H., McKee R.F., Finlay I.G. Surgery for occult rectal prolapse // Colorectal Dis. — 2004. — Vol. 6. — P. 176–179.
73. Weber A.M., Richter H.E. Pelvic organ prolapse // Obstet. Gynecol. — 2005. — Vol. 106, N 3. — P. 615–634.
74. Mellgren A., Anzen B., Nilsson B.Y. et al. Results of rectocele repair. A prospective study // Dis. Colon Rectum. — 1995. — Vol. 38. — P. 7–13.
75. Singh K., Cortes E., Reid W.M.N. Evaluation of the fascial technique for surgical repair of isolated posterior vaginal wall prolapse // Obstet. Gynecol. — 2003. — Vol. 101, N 2. — P. 320–324.
76. Arnold M.W., Stewart W.R., Aguilar P.S. Rectocele repair. Four years’
experience // Dis. Colon Rectum. — 1990. — Vol. 33, N 8. — P. 684–687.
77. Watson S.J., Loder P.B., Halligan S. et al. Transperineal repair of symptomatic rectocele with Marlex mesh: a clinical, physiological and radiologic assessment of treatment // J. Am. Coll. Surg. — 1996. — Vol. 183, N 3. — P. 257–261.
78. Van Laarhoven C.J., Kamm M.A., Bartram C.I. et al. Relationship between anatomic and symptomatic long-term results after rectocele repair for impaired
defecation // Dis. Colon Rectum. — 1999. — Vol. 42, N 2. — P. 204–10; discussion 210–1.
79. Arezzo A., Pescatori M. Surgical procedures for evacuatory disorders // Ann. Ital. Chir. — 2009. — Vol. 80. — P. 261–266.
80. Jeffcoat T.N. Posterior colpoperineorraphy // Am. J. Obstet. Gynecol. — 1959. — Vol. 77. — P. 490–502.
81. Zbar A.P., Leineman A., Fritsch H. et al. Rectocele: patogenesis and surgical management // Int. J. Colorectal Dis. — 2003. — Vol. 18. — P. 369–84.
82. Kahn M.A., Stanton S.L. Posterior colporrhaphy: its effects on bowel and sexual function // Br. J. Obstet. Gynecol. — 1997. — Vol. 104. — P. 882–886.
83. Yamada T., Takahashi T., Iwadare J. Clinical and physiologic outcomes after transvaginal rectocele repair // Dis. Colon Rectum. — 2006. — Vol. 49. — P. 661–667.
84. Parker M.C., Phillips R.K. Repair of rectocele using Marlex mesh // Ann. R. Coll. Surg. Engl. — 1993. — Vol. 75. — P. 193–194.
85. Altman D., Zetterstorm J., Mellgren A. et al. A three-year prospective assessment of rectocele repair using porcine xenograft // Obstet. Gynecol. — 2006. — Vol. 107. — P. 59–65.
86. Gandhi S., Know G., Goldberg R. et al. Does fascia lata graft decrease recurrent
posterior vaginal wall prolapsed? (abstract 86) // Int. Urogynecol. J. Pelvic Floor Dysfunct. — 2003. — Vol. 14. — P. S26.
87. Pichford C.A. Rectocele: a cause of anorectal pathological changes in women // Dis. Colon Rectum. — 1967. — Vol. 10. — P. 464–466.
88. Sullivan E.S., Leaverton G.H., Hardwick C.E. Transrectal perineal repair: an ajunct to improved function after anorectal surgery // Dis. Colon Rectum. — 1968. — Vol. 11. — P. 106–114.
89. Marks M.M. The rectal side of the rectocele // Dis. Colon Rectum. —
1967. — Vol. 10. — P. 387–388.
90. Arnold M.W., Steward W.R., Aguilar P.S. Rectocele repair: four years’ experience // Dis. Colon Rectum. — 1990. — Vol. 33. — P. 684–687.
91. Sehapayak S. Transrectal repair of rectocele: an extended armamentrarium of colorectal surgeons. A report of 355 cases // Dis. Colon Rectum. — 1985. — Vol. 28. — P. 422–433.
92. Longo A. Treatment of hemorrhoidal disease by reduction of mucosa and of
hemorrhoidal prolapsed with circular suturing device: a new procedure // Proceedings of the 6th World Congress of Endoscopic Surgery. — Rome, 1998. — P. 777–784.
93. Altomare D.F., Rinaldi M., Veglia A. et al. Combined perineal and endorectal repair of rectocele by circular stepler: a novel surgical technicue // Dis. Colon Rectum. — 2002. — Vol. 45, N 11. — P. 1549–1552.
94. Renzi A., Izzo D., Di Sarno G. et al. Stapled transanal rectal resection to
treat obstructed defecation caused by rectal intossusception and rectocele // Int. J. Colorectal Dis. — 2006. — Vol. 21, N 7. — P.661–667.
95. Gagliardi G., Pescotori M., Altomare D.F. et al. Italian Society of Colo-Rectal Surgery (SICCR). Results, outcome predictors, and complications after stapler transanal rectal resection for obstructed defecation // Dis. Colon Rectum. — 2008. — Vol. 51. — P. 186–189.
96. Boccasanta P., Venturi M., Calabro G. et al. Stapled transanal rectal resection
in solitary rectal ulcer associated with prolapse of the rectum: A prospective study // Dis. Colon Rectum. — 2008. — Vol. 51. — P. 348–354.
97. Ayabaca S.M., Zbar A.P., Pescatori M. Anal continence after rectocele repair // Dis. Colon Rectum. — 2002. — Vol. 45. — P. 63–69.
98. Watson S.J., Loder P.B., Halligan S. et al. Transperineal repair of symptomatic rectocele with Marlex mesh: a clinical, physiological, and radiological assessment of treatment // J. Am. Coll. Surg. — 1996. — Vol. 183. — P. 257–261.
99. Mercer-Jones M., Sprowson A., Varma J. Outcome after transperineal mesh repair of rectocele: A case series // Dis. Colon Rectum. — 2004. — Vol. 47. — P. 864–868.
100. Smart N.J., Mercer-Jones M.A. Functional outcome after transperineal rectocele repair with porcine dermal collagen implant // Dis. Colon Rectum. — 2007. — Vol. 50. — P. 1422–1427.
101. Milito G., Cadeddu F., Grande M. et al. Advances in treatment of obstructed defecation: Biomesh transperineal repair // Dis. Colon Rectum. — 2009. — Vol. 52. — P. 2051.
102. Goh J.T.W., Dwyer P.L. Effectiveness and safety of polypropylene mesh in vaginal prolapsed surgery // Int. Urogynecol. J. — 2001. — Vol. 12. — P. S90.
103. D’Hoore A., Vanbeckevoort D., Penninckx F. Clinical, phisiological and radiological assessment of rectovaginal septum reinforsment with mesh for complex rectocele // Br. J. Surg. — 2008. — Vol. 95. — P. 1264–1272.
104. Lyons T.L., Winer W.K. Laparoscopic rectocele repair using polyglactin mesh // J. Am. Assoc. Gynecol. Laparosc. — 1997. — Vol. 4. — P. 381–334.
105. Addison W.A., Cundiff G.W., Bump R.C., Harris R.L. Sacral colpopexy is the preferred treatment for vaginal vault prolapse // J. Gynecol. Tech. — 1996. — Vol. 2. — P. 69–74.
106. Xynos E. Functional results after surgery for obstructed defecation // Acta Chir. Iugosl. — 2012. — Vol. 59, N 2. — P. 25–29.
107. Oindiff G.W., Harris R.L., Coates K. et al. Abdominal sacral colpoperineopexy: a new approach for correction of posterior compartment defects and perineal descent associates with vaginal vault prolapse // Am. J. Obstet. Gynecol. — 1997. — Vol. 177. — P. 1345–1355.
108. Sullivan E.S., Longaker C.C.J., Lee P.Y. Total pelvic mesh repair: ten-year experience // Dis. Colon Rectum. — 2001. — Vol. 44. — P. 857–863.
ВЫПАДЕНИЕ ПРЯМОЙ КИШКИ, ВНУТРЕННЯЯ РЕКТАЛЬНАЯ
ИНВАГИНАЦИЯ И СОЛИТАРНАЯ ЯЗВА ПРЯМОЙ КИШКИ
Введение
Ректальный пролапс подразделяют на наружное выпадение прямой кишки и внутреннюю прямокишечную инвагинацию. Под наружным выпадением понимают выход наружу всех слоев кишечной стенки через заднепроходное отверстие. Внутренняя инвагинация — внедрение вышележащих отделов прямой кишки в просвет нижележащих без выхода из анального канала. Это заболевание приносит пациентам изнурительные мучения от пролабирующей ткани, выделений слизи и крови, запора либо анальной инконтиненции, которые сопровождают прямокишечное выпадение. Чаще всего заболеванию сопутствуют такие анатомические дефекты, как диастаз мышц леваторов, глубокий дугласов карман, избыточная подвижность сигмовидной кишки, недостаточность анального сфинктера, нарушение фиксации прямой кишки к крестцу [1–3]. Несмотря на наличие большого числа оперативных пособий, рецидивы заболевания достигают 30%, что не позволяет считать проблему ректального пролапса до конца решенной (УД 1a, СР A [4–6]).
Женщины в возрасте старше 50 лет в 6 раз чаще мужчин страдают выпадением прямой кишки [7–9]. Традиционно считается, что ректальный пролапс является следствием тяжелых многократных родов, однако около 1/3 пациенток с данным заболеванием нерожавшие. Пик заболеваемости приходится на седьмое десятилетие у женщин, однако у мужчин эта проблема может развиться в возрасте 40 лет и ранее. Ректальный пролапс, возникающий в молодом возрасте, чаще всего диагностируется на фоне аутизма, задержки психомоторного развития, а также различных психических заболеваний, требующих длительного приема нейролептиков [10]. У 31% больных заболевание развивается на фоне тяжелого физического труда [11].
Настоящие рекомендации по диагностике и лечению больных с выпадением прямой кишки, внутренней ректальной инвагинацией и солитар-
ной язвой прямой кишки служат руководством для практических врачей, осуществляющих ведение и лечение таких пациентов. Рекомендации подлежат регулярному пересмотру в соответствии с новыми данными научных исследований в этой области.
Рекомендации включают следующие разделы: определение, классификация, клинические проявления, диагностика, консервативное и хирургическое лечение.
Для отдельных положений рекомендаций приведены уровни доказательности согласно общепринятой классификации Оксфордского центра доказательной медицины (табл. 9.1) [12].
Таблица 9.1. Уровни доказательности и степени рекомендаций на основании классификации Оксфордского центра доказательной медицины
|
Уровень |
Исследование диагностических методов |
Исследование лечебных методов |
|
1а |
Систематический обзор гомогенных диагностических исследований 1-го уровня |
Систематический обзор гомогенных РКИ |
|
1b |
Валидизирующее когортное исследование с качественным «золотым стандартом» |
Отдельное РКИ (с узким доверительным интервалом) |
|
1с |
Специфичность или чувствительность столь высокие, что положительный или отрицательный результат позволяет исключить/установить диагноз |
Исследование «Всё или ничего» |
|
2а |
Систематический обзор гомогенных диагностических исследований >2-го уровня |
Систематический обзор (гомогенных) когортных исследований |
|
2b |
Разведочное когортное исследование с качественным «золотым стандартом» |
Отдельное когортное исследование (включая РКИ низкого качества; т.е. с <80% пациентов, прошедших контрольное наблюдение) |
|
2с |
Нет |
Исследование «исходов»; экологические исследования |
|
3а |
Систематический обзор гомогенных исследований уровня 3b и выше |
Систематический обзор гомогенных исследований «случай–контроль» |
|
3b |
Исследование с непоследовательным набором или без проведения исследования «золотого стандарта» у всех испытуемых |
Отдельное исследование «случай– контроль» |
|
4 |
Исследование «случай–контроль» или исследование с некачественным или зависимым «золотым стандартом» |
Серия случаев (и когортные исследования или исследования «случай– контроль» низкого качества) |
Табл. 9.1. Окончание
|
Уровень |
Исследование диагностических методов |
Исследование лечебных методов |
|
5 |
Мнение экспертов без тщательной критической оценки или основанное на физиологии, лабораторные исследования на животных или разработка «первых принципов» |
Мнение экспертов без тщательной критической оценки, лабораторные исследования на животных или разработка «первых принципов» |
|
Степени рекомендаций | ||
|
A |
Согласующиеся между собой исследования 1-го уровня | |
|
B |
Согласующиеся между собой исследования 2-го или 3-го уровня или экстраполяция на основе исследований 1-го уровня | |
|
C |
Исследования 4-го уровня или экстраполяция на основе уровня 2 или 3 | |
|
D |
Доказательства 4-го уровня или затруднительные для обобщения или некачественные исследования любого уровня | |
ВАЛИДИЗАЦИЯ РЕКОМЕНДАЦИЙ
Настоящие рекомендации в предварительной версии были рецензированы независимыми экспертами, которых попросили прокомментировать прежде всего, насколько интерпретация доказательств, лежащих в основе рекомендаций, доступна для понимания. Получены комментарии со стороны врачей амбулаторного звена. Полученные комментарии тщательно систематизировались и обсуждались на совещаниях экспертной группы. Последние изменения в настоящих рекомендациях были представлены для дискуссии на заседании профильной комиссии «Колопроктология» Экспертного совета Минздрава России 12 сентября 2013 г. Проект рекомендаций был повторно рецензирован независимыми экспертами и врачами амбулаторного звена. Для окончательной редакции и контроля качества рекомендации были проанализированы членами экспертной группы, которые пришли к заключению, что все замечания и комментарии приняты во внимание, риск систематических ошибок при разработ-
ке рекомендаций сведен к минимуму.
ОБЛАСТЬ ПРИМЕНЕНИЯ РЕКОМЕНДАЦИЙ
Данные клинические рекомендации применимы при осуществлении медицинской деятельности в рамках Порядка оказания медицинской помощи взрослому населению с заболеваниями толстой кишки, анального канала и промежности колопроктологического профиля.
Определение
Выпадение прямой кишки — выпячивание или выход всех слоев прямой кишки через заднепроходное отверстие [13–18].
В основе внутреннего выпадения лежит интраректальная инвагинация прямой и/или сигмовидной кишки без выхода наружу, т.е. стенка прямой кишки пролабирует, но не выпадает через задний проход [19, 20].
Код по Международной классификации болезней [21]
n Класс: Болезни органов пищеварения (XI).
n Блок: Другие болезни кишечника (К62).
n Код:
v K62.2 Выпадение заднего прохода
v K62.3 Выпадение прямой кишки
v K62.6 Язва заднего прохода и прямой кишки
Классификация
Оксфордская рентгенологическая классификация:
1) высокая ректоректальная инвагинация (выпадение остается выше пуборектальной линии);
2) низкая ректоректальная инвагинация (пролапс на уровне пуборектальной линии);
3) высокая ректоанальная инвагинация (пролапс доходит до анального канала);
4) низкая ректоанальная инвагинация (пролапс в анальном канале, но не выходит за анальную складку);
5) наружное выпадение прямой кишки [22].
Среди отечественных специалистов общепризнана классификация ректального пролапса, разработанная в 1972 г. в ГНЦ колопроктологии.
Стадии выпадения прямой кишки:
n 1-я стадия — прямая кишка выпадает только при акте дефекации;
n 2-я стадия — прямая кишка выпадает при дефекации и физической нагрузке;
n 3-я стадия — прямая кишка выпадает при ходьбе.
Фазы компенсации функции мышц тазового дна:
n фаза компенсации — выпавшая кишка вправляется за счет сокращения мышц тазового дна;
n фаза декомпенсации — вправление кишки осуществляется только с помощью руки.
Степени недостаточности анального сфинктера:
n 1-я степень — недержание газов;
n 2-я степень — недержание клизменных вод и жидкого кала;
n 3-я степень — недержание всех компонентов кишечного содержимого [23, 24].
Профилактика
В развитии выпадения прямой кишки и внутреннего ректального пролапса участвуют некорригируемые факторы, такие как наслед-
ственность, особенности конституции организма и строения прямой кишки, и корригируемые — приобретенные дегенеративные изменения в мышцах ЗАПК и стенке прямой кишки (УД 5, СР D [23]). Выпадение прямой кишки возможно предотвратить, воздействуя лишь на корригируемые факторы. В развитии ректального пролапса особое значение имеют:
n тяжелый физический труд — современные исследования указывают на то, что выпадение прямой кишки чаще возникает у женщин с низким уровнем образования, занимающихся тяжелым физическим трудом (УД 2b, СР B [11]);
n дисфункции кишечника (особенно запор) (УД 3b, СР С [4]);
n неврологические нарушения, изменения конфигурации позвоночника (повреждение конского хвоста, травма спинного мозга, старческие изменения) (УД 3b, СР С [25]);
n хронические обструктивные заболевания легких, сопровождающиеся длительными периодами кашля (УД 2b, СР B [26]);
n гинекологические факторы (беременность, осложненное течение родов, гистерэктомия) (УД 2b, СР B [27–29]).
В связи с этим для профилактики развития ректального пролапса необходимо избегать запора, длительных дисфункций кишечника, вызванных кишечными инфекциями, тяжелого изнуряющего физического труда. При беременности крупным плодом, угрозе разрыва промежности или развития других осложнений в родах необходимо выполнять кесарево сечение (УД 3b, СР С [29]).
Клинические проявления
Основное клиническое проявление заболевания — наличие выпадения, выворачивания прямой кишки через задний проход, вправляемого самостоятельно или требующего ручного пособия. Выпавшая часть прямой кишки может иметь разную форму, размеры и длину (УД 3b, СР C [30]). При этом во время ее пальпации помимо слизистого слоя определяется и мышечный слой кишечной стенки. Если пациент предъявляет жалобы на выпадение, а при осмотре его не обнаруживают, то необходимо попросить его натужиться, как при дефекации (для этой цели может быть полезным положение сидя или на корточках). Распространенным заблуждением служит ошибочное выявление ректального пролапса при выпадении геморроидальных узлов. Как правило, эти состояния легко дифференцировать при клиническом осмотре. Направление складок на выпадающих тканях показывает, что в случае полнослойного выпадения они всегда ориентированы концентрически, в то время как при выпадении геморроидальных узлов или слизистой оболочки прямой кишки наблюдается их радиальное расположение (УД 4, СР D [17, 23]). Если при осмотре пациент не может продемонстрировать выпадение, то его можно попросить сфотографировать пролапс дома.
При внутреннем ректальном пролапсе у пациентов отмечаются следующие симптомы:
n затруднение опорожнения прямой кишки;
n ощущение неполного опорожнения;
n необходимость давления рукой на промежность или введения пальца в просвет кишки для опорожнения;
n выделение крови при дефекации (при наличии повреждения слизистой оболочки прямой кишки или солитарной язвы) (УД 4, СР D [17, 23, 24]). Примерно 50–75% пациентов с ректальным пролапсом страдают недержанием кала, а 25–50% — запором (УД 2b, СР C [31–34]). Инконтиненция может быть объяснена механическим растяжением и травмой анального сфинктера выпадающими тканями, а также нейропатией тазового дна [35]. Патология половых нервов, выявляемая примерно у половины пациентов, может приводить к атрофии мышц наружного сфинктера [32, 35]. Запор, сопровождающий ректальный пролапс, может быть обусловлен снижением моторики толстой кишки, а также инвагинацией кишки при натуживании, которая создает препятствие
для движения каловых масс [33].
У 20–35% больных ректальным пролапсом отмечается недержание мочи, а в 15–30% случаев имеется выпадение стенок влагалища (УД 2b, СР B [9, 36, 37]). Эти симптомы требуют мультидисциплинарного подхода для выбора лечебной тактики с привлечением гинеколога и уролога.
Диагностика
Такие инструментальные методы исследования, как ректороманоскопия, дефекография, колоноскопия, ирригоскопия, урофлоуметрия и МРТ, могут быть использованы для уточнения диагноза и выявления сопутствующих заболеваний.
Важным методом диагностики внутреннего выпадения является ректороманоскопия, которая позволяет определить избыточную складчатость слизистой оболочки прямой кишки, а также ее внедрение в просвет трубки ректоскопа при натуживании больного, что служит характерным признаком внутренней инвагинации. Кроме этого, при ректороманоскопии можно обнаружить солитарную язву, уточнить ее расположение и произвести биопсию для морфологического подтверждения диагноза (УД 4, СР D [17, 23]).
Макроскопически в большинстве случаев она представляет собой участок гиперемированной слизистой оболочки небольшого размера с белым налетом. Приблизительно у 57% пациентов с солитарной язвой встречается изъязвление дефекта, а полиповидные разрастания в области язвы выявляются в 25% (УД 3b, СР C [38–40]).
Дефекография — основной метод диагностики ректального пролапса. Исследование проводят с помощью бариевой взвеси, введенной в прямую кишку. Оценивают положение кишки относительно лонно-коп-
чиковой линии в покое, при волевом сокращении и при натуживании, а также время и полноценность опорожнения (остаточный объем) прямой кишки (табл. 9.2).
Таблица 9.2. Нормальные показатели дефекографии
|
Показатель |
Положение кишки относительно лоннокопчиковой линии, см |
Время опорожнения прямой кишки, с |
Остаточный объем, % |
|
Покой |
2,9±0,9 |
12,6±4,2 |
16,5±5,3 |
|
Волевое сокращение |
1,7±1,2 |
|
|
|
Натуживание |
5,6±1 |
|
|
Метод позволяет определить степень опущения тазового дна, наличие интраректальной инвагинации, сопутствующих ректоцеле, энтерои сигмоцеле (УД 3b, СР C [41, 42]).
В качестве альтернативы дефекографии возможно применение МРТ. Исследование целесообразно у женщин репродуктивного возраста, беременных, а также у пациентов с риском развития побочных реакций на контрастное вещество (УД 4, СР D [43]).
Определение времени транзита по желудочно-кишечному тракту позволяет оценить пассаж рентгеноконтрастного вещества по различным отделам ободочной кишки. Исследование выполняют с использованием бариевой взвеси или специальных маркеров. После перорального приема контраста ежедневно выполняются рентгеновское исследование брюшной полости и контроль над его продвижением по различным отделам желудочно-кишечного тракта. В норме время транзита по ЖКТ составляет 48–72 ч. Замедление продвижения по левым отделам ободочной кишки служит основанием для постановки вопроса о резекционных методах лечения (УД 1a, СР A [5, 44]).
В редких случаях внутреннюю инвагинацию вызывает опухоль толстой кишки. Для исключения таких состояний и обследования всей толстой кишки необходимо проведение колоноскопии или ирригоскопии на основе существующих принципов скрининга колоректального рака (УД 4, СР D [45]).
Из физиологических методов исследования у пациентов с выпадением прямой кишки выполняют профилометрию, исследование латентности половых нервов и электромиографию мышц тазового дна (УД 2b, СР B [23, 46–48]).
Профилометрию проводят для оценки состояния ЗАПК путем определения давления в анальном канале [23].
Методика. Специальный перфузионный катетер вводят в прямую кишку. При вытягивании катетера производят перфузию жидкости через отверстия, расположенные по его окружности. Давление в анальном канале оценивают с помощью измерения сопротивления току жидкости.
Замеры выполняют в покое, при волевом сокращении и при натуживании (табл. 9.3).
Таблица 9.3. Показатели профилометрии в норме (мм рт.ст.)
|
Показатель профилометрии |
Покой |
Волевое сокращение |
|
Анальный канал в целом | ||
|
Максимальное давление |
100,8±11,4 |
137,1±12,6 |
|
Среднее давление |
52,2±8,2 |
76,6±8,9 |
|
Коэффициент асимметрии, ед |
19,8±2,3 |
19,2±2,6 |
|
Зона высокого давления* | ||
|
Длина зоны, см |
2,2±0,5 |
2,7±0,65 |
|
Среднее давление |
72,1±9,7 |
100,1±12,5 |
|
Коэффициент асимметрии |
15,5±2,1 |
13,9±2,2 |
* Зона высокого давления соответствует проекции внутреннего сфинктера и глубокой порции наружного сфинктера.
В покое оценивают внутрианальное давление для изучения состояния внутреннего сфинктера, при волевом усилии — сократительную способность наружного сфинктера. При натуживании возможно обнаружить диссинергию мышц таза, проявляющуюся в повышении внутрианального давления, которое в норме не должно превышать давление покоя.
Исследование латентности половых нервов производят для оценки соматической иннервации мышц тазового дна.
Методика. Исследование выполняют с помощью стимуляции специальным электродом св. Марка дистальных ветвей половых нервов в точке их входа в седалищно-прямокишечную ямку у седалищных остей. С электродом соединен датчик, который регистрирует вызванный моторный ответ. Время проведения импульса оценивают как латентность полового нерва. В норме она составляет 2,0±0,2 мс.
Больные с увеличением латентности половых нервов, т.е. с признаками их повреждения, могут иметь более высокую степень недержания кала после хирургической коррекции пролапса, хотя прямой корреляционной зависимости этих состояний не обнаружено (УД 2b, СР B [46–48]).
Электромиография мышц тазового дна. Метод важен для оценки функционального состояния мышц тазового дна, нарушение которого может быть причиной синдрома обструктивной дефекации (УД 2b, СР B [46]).
Методика. Электромиографический датчик вводят в анальный канал в проекции наружного сфинктера и мышц таза. В начале исследования регистрируют суммарную электрическую активность сфинктера в покое и при волевом сокращении. Затем выполняют пробы с изменением внутрибрюшного давления (напряжение брюшной стенки, покашливание и натуживание) [23] (табл. 9.4).
Таблица 9.4. Показатели электромиографии в норме
|
Показатель |
Норма |
|
Фоновая электрическая активность, мкВ |
15,2±2,1 |
|
Произвольная электрическая активность, мкВ |
74,3±13,7 |
|
Рефлекторные реакции на пробы с повышением внутрибрюшного давления (кашель, напряжение мышц передней брюшной стенки) |
++ |
При электромиографии в покое оценивают тонус наружного сфинктера. При волевом усилии — сократительную способность наружного сфинктера. При натуживании возможно обнаружение диссинергии мышц таза, проявляющееся не в снижении, а в повышении их биоэлектрической активности, что может служить причиной обструктивной дефекации.
Лечение
КОНСЕРВАТИВНОЕ ЛЕЧЕНИЕ
Основной метод лечения выпадения прямой кишки — хирургический. Однако при выявлении признаков хронического толстокишечного стаза и обструктивной дефекации начинать лечение необходимо с консервативных мероприятий, направленных на нормализацию стула и координирование моторики прямой кишки и мышц тазового дна, и лишь на этом фоне выполнять оперативное вмешательство.
Первый шаг, направленный на нормализацию стула у пациентов с дисфункцией толстой кишки, — прием растительных волокон (клетчатки). Ежедневное употребление 25 г волокон позволяет увеличить частоту стула у пациентов с хроническим запором (УД 1b, СР В [49]). Ежедневный прием 1,5–2 л жидкости усиливает данный эффект, при этом потребность в слабительных препаратах снижается (УД 1b, СР В [50]). Следует отметить, что увеличение физической активности ускоряет перистальтику кишечника (УД 3b, СР С [51]).
При неэффективности мероприятий по коррекции режима питания следует применять слабительные средства. Для усиления эффекта можно использовать комбинацию препаратов, увеличивающих объем кишечного содержимого (макрогол) и усиливающих кишечную перистальтику (прукалоприд) (УД 1b, СР B [52, 53]).
Макрогол является осмотическим слабительным, увеличивающим содержание жидкости в химусе и стимулирующим механорецепторы, ускоряя, таким образом, перистальтику кишечника. Рекомендуется ежедневный прием 20 г макрогола в течение 2 нед (УД 1b, СР B [52]).
Прукалоприд является селективным, высокоаффинным агонистом 5-HT4-серотониновых рецепторов. Прием препарата ведет к стимуля-
ции рецепторов в стенке кишки и активации моторики кишечника. Его назначают по 2 мг 1 раз в сутки. По данным многочисленных плацебоконтролируемых исследований, это позволяет увеличить частоту опорожнения толстой кишки по сравнению с контрольной группой (УД 1a, СР A [54]).
Препараты на основе семян подорожника или лактулозы достоверно улучшают функцию кишки при синдроме обструктивной дефекации и хроническом толстокишечном стазе (УД 1а, СР A [53]). Мукофальк♠ назначают по 1 саше 2–6 раз в сутки, лактулозу по 10–25 мл 1 раз в сутки. В результате проспективного рандомизированного исследования по сравнению эффективности препаратов семян подорожника и лактулозы установлено, что первые обладают более выраженным эффектом. Препараты семян подорожника обеспечивают лучшую консистенцию стула и дают меньше побочных реакций по сравнению с лактулозой
и другими слабительными (УД 1b, СР B [55]).
Для консервативного лечения функциональных нарушений толстой кишки возможно применение таких слабительных, как магния гидроксид, бисакодил, препараты сенны. Однако их эффективность сомнительна. Так, при проведении метаанализа 11 рандомизированных контролируемых исследований выявлено, что учащение стула и увеличение объема каловых масс после 4 нед приема указанных слабительных препаратов полностью соответствует эффекту плацебо (УД 1a, СР A [56]).
Метод биологической обратной связи
При выявлении признаков диссинергии мышц тазового дна, внутреннего выпадения прямой кишки, солитарной язвы возможно применение метода биологической обратной связи (БОС-терапии) (УД 3b, СР C [57, 58]). Цель терапии — моделирование режима работы мышц тазового дна, необходимого для осуществления эффективного акта дефекации. Метод основан на принципе обратной связи, который заключается в предоставлении пациенту аудиовизуальной информации о состоянии и изменении некоторых собственных физиологических процессов. На практике это реализуется в виде установки датчиков в анальный канал, на кожу промежности или брюшного пресса и выведения с них данных о состоянии мышц на экран, находящийся перед глазами пациента. В зависимости от полученных сигналов пациент может изменять мышечные сокращения с помощью волевых усилий и улучшать функцию мышц тазового дна. Упражнения выполняются 15–30 раз. Курс 10–15 сеансов [59].
По данным рандомизированных контролируемых исследований, у 70% пациентов с диссинергией мышц тазового дна БОС-терапия оказывается эффективной (УД 1a, СР A [60]), а у 50% этот эффект сохраняется в отдаленном периоде (УД 1b, СР B [61]). По сравнению с приемом слабительных для лечения тазовой диссинергии БОС-терапия является
более эффективной (УД 1b, СР В [62]). Ее действие не зависит от выраженности синдрома опущения промежности (наличия сопутствующих внутренней инвагинации ректоцеле, сигмоцеле) (УД 4, СР С [63]). Однако значительные анатомические дефекты, тяжелые психические или неврологические заболевания, недостаточный контакт между пациентом и врачом, а также плохое следование врачебным рекомендациям отрицательно сказываются на результатах лечения методом БОС (УД 3b, СР С [62, 64]).
ХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕ
Хирургический метод — основной для лечения выпадения прямой кишки. В литературе описано большое количество методик, применяемых при ректальном пролапсе. В зависимости от доступа их подразделяют на промежностные и трансабдоминальные вмешательства. Выбор вмешательства зависит от возраста пациента, наличия тяжелых сопутствующих заболеваний, состояния моторно-эвакуаторной функции кишечника, предпочтений хирурга и его опыта (УД 1a, СР A [5]).
Несмотря на множество предложенных методов, лишь немногие из них используются в настоящее время, а большинство представляют лишь исторический интерес.
Трансабдоминальные операции
Трансабдоминальные вмешательства имеют лучшие функциональные результаты и меньшую частоту рецидивов по сравнению с трансперинеальными, что делает их операциями выбора при лечении ректального пролапса (УД 1a, СР A [5, 65, 66]). Однако, несмотря на указанные преимущества, частота послеоперационных осложнений после них несколько выше, чем при промежностных методиках. В связи с этим данный доступ чаще применяется у молодых пациентов и у больных, не имеющих тяжелых сопутствующих заболеваний (УД 2b, СР B [66]). Практически все трансабдоминальные операции могут выполняться как открытым, так и лапароскопическим способом (УД 1а, СР А [5, 67–69]).
Шовная ректопексия (операция Зеренина–Кюммеля в модификации НИИ проктологии МЗ РСФСР)
Показания. Наружное или внутреннее выпадение прямой кишки.
Методика. Справа от прямой кишки на уровне мыса крестца вскрывают тазовую брюшину. Разрез продлевают вниз до дна дугласова кармана, огибая кишку спереди. Производят мобилизацию прямой кишки по задней и правой боковой полуокружностям до леваторов. Затем, начиная от мыса крестца, в дистальном направлении накладывают 3–4 шва нерассасывающимся материалом (полиамид), захватывая продольную связку крестца. Этими же швами, начиная с нижнего, прошивают переднюю стенку прямой кишки. При завязывании швов происходит ротация кишки на 180° с ее фиксацией к крестцу. Тазовую брюшину ушивают
над кишкой с созданием дубликатуры для того, чтобы ликвидировать глубокий дугласов карман.
По данным литературы, частота рецидивов после шовной ректопексии составляет от 3 до 9% (УД 1b, СР B [70, 71]). Эта методика может вызвать возникновение запора или усиление уже существующих нарушений транзита в отдаленные сроки после операции у 50% оперированных больных (УД 2a, СР B [72]).
Ректо (кольпо) сакропексия
Показания. Наружный или внутренний пролапс, сочетание выпадения кишки с ректоцеле и сигмоцеле.
Методика. После рассечения тазовой брюшины справа от прямой кишки производят ее мобилизацию по передней и правой боковой полуокружностям до латеральной связки. У мужчин по передней полуокружности кишку мобилизуют до границы среднеи нижнеампулярного отделов. У женщин при сопутствующем ректоцеле операция выполняется с расщеплением ректовагинальной перегородки и мобилизацией передней стенки кишки до анального сфинктера. Синтетический имплантат (полипропиленовая сетка размером 10×3 см) подшивают тремячетырьмя нерассасывающимися швами (полиамид) ко всей поверхности мобилизованной передней стенки прямой кишки. У женщин двумя дополнительными швами к сетке фиксируют задний свод влагалища. Затем свободный конец сетки крепится к надкостнице I крестцового позвонка двумя нерассасывающимися швами (полиамид), операцию завершают ушиванием тазовой брюшины над сеткой.
Систематический обзор 12 нерандомизированных серий из 728 пациентов установил, что частота рецидивов после ректо (кольпо) сакропексии составляет 3,4%, а средняя частота послеоперационных осложнений — 23%. Однако возникновение запора в послеоперационном периоде было отмечено лишь у 14,4% пациентов (УД 1a, СР A [73]).
Заднепетлевая ректопексия (операция Уэллса)
Показания. Наружное или внутреннее выпадение прямой кишки.
Методика. Рассекают тазовую брюшину с обеих сторон от прямой кишки, обнажая мыс крестца. Кишку мобилизуют по задней и боковым полуокружностям до уровня леваторов. К крестцу двумя швами с использованием нерассасывающегося материала (полиамид) подшивают в поперечном к оси крестца направлении сетчатый имплантат (полипропиленовая сетка) размером 8×3 см. Мобилизованную кишку без избыточного натяжения помещают на аллотрансплантат, и свободные края сетки фиксируют нерассасывающимся материалом (полиамид) к боковым стенкам кишки (2 шва с каждой стороны). Тазовую брюшину ушивают над сеткой. Частота рецидивов после заднепетлевой ректопексии составляет 3–6%, а улучшение держания в послеоперационном периоде происходит у 3–40% пациентов (УД 1b, СР B [72, 74–77]). Вероятность запора со-
ставляет 19% (УД 1a, СР A [5]).
Ректопексия с резекцией толстой кишки
Показания. Наружное или внутреннее выпадение прямой кишки в сочетании с хроническим толстокишечным стазом (время транзита более 96 ч за счет задержки в левых отделах).
Методика. Выполняют стандартную резекцию левых отделов ободочной кишки с наложением анастомоза конец в конец. Затем прямую кишку фиксируют к крестцу с помощью одного из описанных выше методов таким образом, что сигмо-сигмоидный анастомоз находится на 2–3 см выше мыса крестца.
Процент рецидивов после использования данного метода колеблется от 2 до 5%, а частота осложнений достигает 20% (УД 1a, СР A [5, 6]). По данным некоторых авторов, у пациентов с нарушением транзита по толстой кишке после выполнения резекции кишки с ректопексией происходит нормализация стула (УД 1a, СР A [5, 44, 78]). Другие авторы утверждают, что удаление левых отделов является неадекватным объемом резекции, и у пациентов с хроническим толстокишечным стазом должна выполняться ректопексия с субтотальной колэктомией. Отмечено, что выполнение резекции кишки в сочетании с ректопексией у пациентов с признаками анальной инконтиненции снижает вероятность улучшения анального держания в послеоперационном периоде по сравнению с изолированной ректопексией (УД 1a, СР A [5]). В литературе появляется все больше доказательств того, что резекцию левых отделов ободочной кишки можно выполнять только в случаях нарушения транзита по левым отделам ободочной кишки, а при преобладании симптомов недержания выполнение данного оперативного вмешательства противопоказано (УД 2b, СР B [79, 80]).
Передняя резекция прямой кишки
Показания. Внутреннее выпадение прямой кишки, осложненное солитарной язвой с рубцовой деформацией стенки кишки, нарушающей кишечную проходимость.
Методика. Производят разрез брюшины в области корня брыжейки сигмовидной кишки. Затем разрез продлевают на тазовую брюшину, огибая прямую кишку в виде лиры. Выполняют мобилизацию сигмовидной и прямой кишки до нижнеампулярного отдела. Граница резекции прямой кишки проходит ниже края солитарной язвы, сигмовидную кишку резецируют на уровне дистальной трети. Анастомоз накладывают конец в конец с использованием циркулярного сшивающего аппарата.
По результатам ретроспективных исследований установлено, что частота рецидивов выпадения прямой кишки после передней резекции растет с течением времени и через 2, 5 и 10 лет после операции составляет до 3, 6 и 12% соответственно (УД 2b, СР B [81]). Послеоперационные осложнения развиваются в 29% случаев (УД 2b, СР B [81]). Важно отметить, что низкое наложение анастомоза у больных с недержанием может привести к полной потере контроля над дефекацией (УД 2b, СР B [82]).
Промежностные операции
Выполнение хирургических вмешательств промежностным доступом менее травматично для пациента. Однако высокая частота рецидивов и плохие функциональные результаты определяют их применение лишь у пожилых пациентов или у больных с тяжелыми сопутствующими заболеваниями (УД 2b, СР B [23, 65, 66]).
Операция Делорма
Показания. Наружное выпадение прямой кишки у пожилых пациентов с наличием тяжелых сопутствующих заболеваний, повышающих риск трансабдоминальных вмешательств.
Методика. Трансанально, отступив 2 см от зубчатой линии, циркулярно рассекают слизистую оболочку прямой кишки. Последнюю отпрепаровывают от мышечного слоя выпавшей части кишки и отсекают. На мышечную стенку прямой кишки накладывают 4–5 вертикальных швов для создания мышечного валика, затем восстанавливают целостность слизистой оболочки.
Положительная сторона данного вмешательства — это малая травматичность. Кроме того, есть данные, что давление покоя и волевого сокращения анального сфинктера достоверно возрастают после операции Делорма, в результате чего улучшается держание кишечного содержимого (УД 3b, СР С [83]). Однако вероятность развития рецидива пролапса после этого метода выше, чем при трансабдоминальных операциях, и составляет 10–15% (УД 2b, СР B [83–86]). Воспалительные осложнения, задержка мочеиспускания, кровотечение и запор встречаются в послеоперационном периоде в 4–12% случаев (УД 2b, СР B [84, 86]).
Промежностная ректосигмоидэктомия (операция Альтмеера)
Показания. Наружное выпадение прямой кишки у пациентов, страдающих тяжелыми заболеваниями сердечно-сосудистой и дыхательной систем.
Методика. На 2 см выше зубчатой линии производят циркулярный разрез всей толщи кишечной стенки. Трансанально мобилизуют прямую кишку и дистальный отдел сигмовидной кишки с перевязкой кровеносных сосудов в максимальной близости от кишечной стенки до уровня, когда дальнейший пролапс кишки невозможен. После пересечения ободочной кишки и удаления препарата накладывают анастомоз ручным швом или с помощью сшивающего аппарата.
Преимущество данной операции заключается в низкой частоте осложнений (до 10%), которые включают кровотечение из линии швов, тазовые абсцессы и несостоятельность анастомоза. Частота рецидивов колеблется от 16 до 30% (УД 3b, СР C [65, 87–90]). Ряд хирургов дополнительно к ректосигмоидэктомии выполняют леваторопластику. В литературе есть сообщения, что применение леваторопластики уменьшает частоту рецидивов до 7% (УД 3b, СР С [91, 92]). Опубликованы резуль-
таты рандомизированного контролируемого исследования по сравнению с промежностной ректосигмодэктомии с трансабдоминальными операциями. По их данным, частота рецидивов после промежностных операций составила 10%, после трансабдоминальных вмешательств рецидивы не отмечены (УД 3b, СР С [66]).
Трансанальная проктопластика по Лонго
Показания. Внутреннее выпадение прямой кишки, не осложненное солитарной язвой.
Методика. При выполнении данной операции используются два циркулярных сшивающих аппарата (PPH-01, PPH-03). В анальный канал вводят окончатый аноскоп, идентифицируют инвагинированную стенку прямой кишки. Затем накладываются два слизисто-мышечных полукисетных шва на переднюю полуокружность прямой кишки (викрил на игле 5/8), захватывая инвагинат. Расстояние между швами 1–2 см в зависимости от выраженности пролапса. После введения в прямую кишку головки аппарата на ней завязывают наложенные швы и производят резекцию избыточных тканей с помощью циркулярного степлера. Аналогичным образом поступают и с задней стенкой.
Частота осложнений после данной операции варьирует от 15 до 47% (УД 1a, СР A [93–96]). Чаще всего встречается императивный позыв на дефекацию (40%), однако спустя год он сохраняется лишь у 10% пациентов (УД 2b, СР B [97]). Преимуществом данной методики является достижение улучшения эвакуаторной функции прямой кишки в послеоперационном периоде, что подтверждено многочисленными исследованиями (УД 1b, СР B [94, 98–100]).
Прогноз
При хирургическом лечении выпадения прямой кишки вероятность развития рецидивов, независимо от способа вмешательства, достигает 30%, и наиболее часто они возникают после выполнения промежностных операций (УД 1a, СР A [5, 66]). Нарушение моторно-эвакуаторной функции толстой кишки в послеоперационном периоде развивается, по разным данным, от 10 до 29% (УД 1a, СР A [5, 65, 73]).
Критерии оценки качества помощи в стационаре представлены в таблице 9.5. Для оценки качества медицинской помощи используют временные, процессуальные и профилактирующие критерии. Временные характеризуют своевременность оказания определенных этапов медицинской помощи. Выполнение пациенту ряда медицинских манипуляций, инструментальных и лабораторных исследований, необходимых для качественного оказания медицинской помощи, оценивают в процессуальных критериях. Для анализа мероприятий, направленных на предотвращение развития осложнений, используют профилактирующие критерии.
Таблица 9.5. Критерии оценки качества медицинской помощи в стационаре больным с синдромом опущения промежности (выпадение прямой кишки, внутренняя ректальная инвагинация, солитарная язва прямой кишки) (0 — нет, 1 — да)
|
Клинические рекомендации |
Временные |
Процессуальные |
Профилактирующие |
|
Клинические рекомендации по диагностике и лечению взрослых пациентов с выпадением прямой кишки, внутренней ректальной инвагинацией и солитарной язвой прямой кишки (код МКБ — К62.3, К62.6) |
Установка клинического диагноза в течение 72 ч: 0/1 |
Оценка анального рефлекса: 0/1. Пальцевое исследование прямой кишки: 0/1. Аноскопия: 0/1. Ректороманоскопия: 0/1. Определение группы крови: 0/1. Исследование крови на сифилис, вирусный гепатит В, вирусный гепатит С: 0/1. Клинический анализ крови; биохимический анализ крови; клинический анализ мочи; коагулограмма: 0/1. Сфинктерометрия: 0/1. Проктография с натуживанием (дефекография): 0/1. Биопсия из края язвы с патоморфологическим исследованием при ее наличии: 0/1. Метод оперативного лечения в соответствии с клиническими рекомендациями: 0/1. Метод анестезии в соответствии с объемом оперативного лечения: 0/1 |
Отсутствие осложнений: • кровотечение: 0/1; • абсцесс: 0/1; • флегмона: 0/1; • пневмония: 0/1; • тромбоэмболия: 0/1; • летальный исход: 0/1 |
Литература
1. Broden B., Snellman B. Procidentia of the rectum studied with cineradiography: a contribution to the discussion of causativemechanism // Dis. Colon Rectum. — 1968. — Vol. 11. — P. 330–347.
2. Kuijpers H.C. Treatment of complete rectal prolapse: to narrow, to wrap, to suspend, to fix, to encircle, to plicate or to resect? // World J. Surg. — 1992. — Vol. 16, N 5. — P. 826–830.
3. Nicholls R.J. Rectal prolapse and the solitary ulcer syndrome // Ann. Ital.
Chir. — 1994. — Vol. 65, N 2. — P. 157–162.
4. Soares F.A., Regadas F.S., Murad-Regadas S.M. et al. Role of age, bowel function and parity on anorectocele pathogenesis according to cinedefecography and anal manometry evaluation // Colorectal Dis. — 2009. — Vol. 11, N 9. — P. 947–950.
5. Tou S., Brown S.R., Malik A.I., Nelson R.L. Surgery for complete rectal prolapse in adults // Cochrane Database Syst. Rev. — 2008. — Is. 4. — CD001758.
6. Мусин А.И., Благодарный Л.А., Фролов С.А. Выпадение прямой кишки. Современное состояние проблемы (обзор литературы) // Колопроктология. — 2011. — № 3. — С. 41–47.
7. Gourgiotis S., Baratsis S. Rectal prolapse // Int. J. Colorectal Dis. — 2007. — Vol. 22, N 3. — P. 231–243.
8. Kairaluoma M.V., Kellokumpu I.H. Epidemiologic aspects of complete rectal prolapse // Scand. J. Surg. — 2005. — Vol. 94, N 3. — P. 207–210.
9. Madiba T.E., Baig M.K., Wexner S.D. Surgical management of rectal prolapse // Arch. Surg. —2005. — Vol. 140, N 1. — P. 63–73.
10. Marceau C., Parc Y., Debroux E. et al. Complete rectal prolapse in young patients: psychiatric disease a risk factor of poor outcome // Colorectal Dis. — 2005. — Vol. 7, N 4. — P. 360–365.
11. Nygaard I., Shaw J., Egger M.J. Exploring the association between lifetime
physical activity and pelvic floor disorders: study and design challenges // Contemp. Clin. Trials. — 2012. — Vol. 33, N 4. — P. 819–827.
12. OCEBM Levels of Evidence Working Group. The Oxford 2011 Levels of Evidence. — Oxford Centre for Evidence-Based Medicine, 2011.
13. Аведисов С.С. Выпадение прямой кишки. — М.: Медгиз, 1963. — С. 1–216.
14. Аминев А.М. Руководство по проктологии. — Куйбышев, 1971. — Вып. 2.
15. Рыжих А.Н., Вишневский А.А. Атлас операций на прямой и толстой кишках. — М.: Медучебпособие, 1960. — 283 с.
16. Федоров В.Д., Дульцев Ю.В. Проктология. — М.: Медицина, 1984. — 384 с.
17. Corman M.L. Colon and Rectal Surgery. — Philadelphia: Lippincott, 2004.
18. Pemberton J.H., Swash M., Henry M.M. The Pelvic Floor: Its Function and Disorders. — Philadelphia: Harcourt Publisher Limited and Mayo Foundation for Medical Education and Research, 2002. — P. 265–285.
19. Roig J.V., Buch E., Alos R. et al. Anorectal function in patients with complete rectal prolapse. Differences between continent and incontinent individuals // Rev. Esp. Enferm Dig. — 1998. — Vol. 90, N 11. — P. 794–805.
20. Felt-Bersma R.J., Luth W.J., Janssen J.J., Meuwissen S.G. Defecography in
patients with anorectal disorders. Which findings are clinically relevant? // Dis. Colon Rectum. — 1990. — Vol. 33, N 4. — P. 277–284.
21. Международная классификация болезней 10-го пересмотра. Доступен с сайта: www.10mkb.ru.
22. Collinson R., Cunningham C., D’Costa H., Lindsey I. Rectal intussusception and unexplained faecal incontinence: findings of a proctographic study // Colorectal Dis. — 2009. — Vol. 11, N 1. — P. 77–83.
23. Воробьев Г.И. Основы колопроктологии. — М.: МИА, 2006. — 432 с.
24. Воробьев Г.И., Шелыгин Ю.А., Орлова Л.П. и др. Клиника, диагностика и лечение больных с выпадением прямой кишки // Рос. журн. гастроэнтерол., гепатол., колопроктол. — 1996. — Т. 6. — С. 78–82.
25. Mattbox T.F., Lucente V., McIntyre P. Abnormal spinal curvature and its relationship to pelvic organ prolapsed // Obstet. Gynecol. — 2000. — Vol. 183. — P. 1381–1384.
26. Blandon R.E., Bharucha A.E., Melton L.J. et al. Risk factors for pelvic
floor repair after hysterectomy // Obstet. Gynecol. — 2009. — Vol. 113, N 3. — P. 601–608.
27. Moalli P.A., Jones Ivy.S., Meyn L.A., Zyczynski H.M. Risk factors associated with pelvic floor disorders in women undergoing surgical repair // Obstet. Gynecol. — 2003. — Vol. 101, N 5. — Pt 1. — P. 869–874.
28. Fritel X. [Pelvic floor and pregnancy] // Gynecol. Obstet. Fertil. — 2010. — Vol. 38, N 5. — P. 332–346.
29. Lukacz E.S., Lawrence J.M., Contreras R. et al. Parity, mode of delivery, and pelvic floor disorders // Obstet. Gynecol. — 2006. — Vol. 107, N 6. — P. 1253–1260.
30. Shin E.J. Surgical treatment of rectal prolapse // J. Korean Soc. Coloproctol. — 2011. — Vol. 27, N 1. — P. 5–12.
31. Madoff R.D., Mellgren A. One hundred years of rectal prolapse surgery // Dis. Colon Rectum. — 1999. — Vol. 42, N 4. — P. 441–450.
32. Schultz I., Mellgren A., Oberg M. et al. Whole gut transit is prolonged after Ripstein rectopexy // Eur. J. Surg. — 1999. — Vol. 165, N 3. — P. 242–247.
33. Senagore A.J. Management of rectal prolapse: the role of laparoscopic approaches // Semin. Laparosc. Surg. — 2003. — Vol. 10, N 4. — P. 197–202.
34. Glasgow S.C., Birnbaum E.H., Kodner I.J. et al. Preoperative anal manometry predicts continence after perineal proctectomy for rectal prolapse // Dis. Colon Rectum. — 2006. — Vol. 49, N 7. — P. 1052–1058.
35. Snooks S.J., Henry M.M., Swash M. Anorectal incontinence and rectal
prolapse: differential assessment of the innervation to puborectalis and external anal sphincter muscles // Gut. — 1985. — Vol. 26, N 5. — P. 470–476.
36. Gonzalez-Argente F.X., Jain A., Nogueras J.J. et al. Prevalence and severity of urinary incontinence and pelvic genital prolapse in females with anal incontinence or rectal prolapse // Dis. Colon Rectum. — 2001. — Vol. 44, N 7. — P. 920–926.
37. Шелыгин Ю.А., Титов А.Ю., Шехтер А.Б. и др. Характер гормонального
и морфологического статуса у женщин с синдромом опущения промежности // Колопроктология. — 2011. — № 3. — С. 3–13.
38. Haray P.N., Morris-Stiff G.J., Foster M.E. Solitary rectal ulcer syndrome — an underdiagnosed condition // Int. J. Colorectal Dis. — 1997. — Vol. 12, N 5. — P. 313–315.
39. Mahieu P.H. Barium enema and defaecography in the diagnosis and
evaluation of the solitary rectal ulcer syndrome // Int. J. Colorectal Dis. — 1986. — Vol. 1, N 2. — P. 85–90.
40. Tjandra J.J., Fazio V.W., Church J.M. et al. Clinical conundrum of solitary rectal ulcer // Dis. Colon Rectum. — 1992. — Vol. 35, N 3. — P. 227–234.
41. Pescatori M., Spyrou M., Pulvirenti d’Urso A. A prospective evaluation of occult disorders in obstructed defecation using the «iceberg diagram» // Colorectal Dis. — 2006. — Vol. 8, N 9. — P. 785–789.
42. Renzi A., Izzo D., Di Sarno G. et al. Cinedefecographic findings in patients
with obstructed defecation syndrome. A study in 420 cases // Minerva Chir. — 2006. — Vol. 61, N 6. — P. 493–499.
43. Healy J.C., Halligan S., Bartram C.I. et al. Dynamic magnetic resonance imaging evaluation of the structural and functional results of postanal repair for neuropathic fecal incontinence // Dis. Colon Rectum. — 2002. — Vol. 45, N 12. — P. 1629–1634.
44. Sayfan J., Pinho M., Alexander-Williams J., Keighley M.R. Sutured posterior
abdominal rectopexy with sigmoidectomy compared with Marlex rectopexy for rectal prolapse // Br. J. Surg. — 1990. — Vol. 77, N 2. — P. 143–145.
45. Bounovas A., Polychronidis A., Laftsidis P., Simopoulos C. Sigmoid colon cancer presenting as complete rectal prolapse // Colorectal Dis. — 2007. — Vol. 9, N 7. — P. 665–666.
46. Schultz I., Mellgren A., Nilsson B.Y. et al. Preoperative electrophysiologic assessment cannot predict continence after rectopexy // Dis. Colon Rectum. — 1998. — Vol. 41, N 11. — P. 1392–1398.
47. Johansen O.B., Wexner S.D., Daniel N. et al. Perineal rectosigmoidectomy in
the elderly // Dis. Colon Rectum. — 1993. — Vol. 36, N 8. — P. 767–772.
48. Birnbaum E.H., Stamm L., Rafferty J.F. et al. Pudendal nerve terminal motor latency influences surgical outcome in treatment of rectal prolapse // Dis. Colon Rectum. — 1996. — Vol. 39, N 11. — P. 1215–1221.
49. Griffenberg L., Morris M., Atkinson N., Levenback C. The effect of dietary fiber on bowel function following radical hysterectomy: a randomized trial // Gynecol. Oncol. — 1997. — Vol. 66, N 3. — P. 417–424.
50. Anti M., Pignataro G., Armuzzi A. et al. Water supplementation enhances
the effect of high-fiber diet on stool frequency and laxative consumption in adult patients with functional constipation // Hepatogastroenterology. — 1998. — Vol. 45, N 21. — P. 727–732.
51. De Schryver A.M., Keulemans Y.C., Peters H.P. et al. Effects of regular physical activity on defecation pattern in middle-aged patients complaining of chronic constipation // Scand. J. Gastroenterol. — 2005. — Vol. 40, N 4. — P. 422–429.
52. Cleveland M.V., Flavin D.P., Ruben R.A. et al. New polyethylene glycol
laxative for treatment of constipation in adults: a randomized, double-blind, placebo-controlled study // South. Med. J. — 2001. — Vol. 94, N 5. — P. 478–481.
53. Ramkumar D., Rao S.S. Efficacy and safety of traditional medical therapies for chronic constipation: systematic review // Am. J. Gastroenterol. — 2005. — Vol. 100, N 4. — P. 936–971.
54. Evans B.W., Clark W.K., Moore D.J., Whorwell P.J. Tegaserod for the
treatment of irritable bowel syndrome and chronic constipation // Cochrane Database Syst. Rev. — 2007. — Is. 4. — CD003960.
55. Dettmar P.W., Sykes J. A multi-centre, general practice comparison of ispaghula husk with lactulose and other laxatives in the treatment of simple constipation // Curr. Med. Res. Opin. — 1998. — Vol. 14, N 4. — P. 227–233.
56. Jones M.P., Talley N.J., Nuyts G., Dubois D. Lack of objective evidence of
efficacy of laxatives in chronic constipation // Dig. Dis. Sci. — 2002. — Vol. 47, N 10. — P. 2222–2230.
57. Khaikin M., Wexner S.D. Treatment strategies in obstructed defecation and fecal incontinence // World J. Gastroenterol. — 2006. — Vol. 12, N 20. — P. 3168–3173.
58. Andromanakos N., Skandalakis P., Troupis T., Filippou D. Constipation of
anorectal outlet obstruction: pathophysiology, evaluation and management //
J. Gastroenterol. Hepatol. — 2006. — Vol. 21, N 4. — P. 638–646.
59. Engel B.T., Nikoomanesh P., Schuster M.M. Operant conditioning of rectosphincteric responses in the treatment of fecal incontinence // N. Engl. J. Med. — 1974. — Vol. 290, N 12. — P. 646–649.
60. Foxx-Orenstein A.E., Camilleri M., Szarka L.A. et al. Does co-administration of a non-selective opiate antagonist enhance acceleration of transit by a 5-HT4 agonist
in constipation-predominant irritable bowel syndrome? A randomized controlled trial // Neurogastroenterol. Motil. — 2007. — Vol. 19, N 10. — P. 821–830.
61. Rao S.S., Seaton K., Miller M. et al. Randomized controlled trial of biofeedback, sham feedback, and standard therapy for dyssynergic defecation // Clin. Gastroenterol. Hepatol. — 2007. — Vol. 5, N 3. — P. 331–338.
62. Chiarioni G., Heymen S., Whitehead W.E. Biofeedback therapy for dyssynergic
defecation // World J. Gastroenterol. — 2006. — Vol. 12, N 44. — P. 7069–7074.
63. Lau C.W., Heymen S., Alabaz O. et al. Prognostic significance of rectocele, intussusception, and abnormal perineal descent in biofeedback treatment for constipated patients with paradoxical puborectalis contraction // Dis. Colon Rectum. — 2000. — Vol. 43, N 4. — P. 478–482.
64. Bassotti G., Chistolini F., Sietchiping-Nzepa F. et al. Biofeedback for pelvic floor dysfunction in constipation // BMJ. — 2004. — Vol. 328, N 7436. — P. 393– 396.
65. Kim D.S., Tsang C.B., Wong W.D. et al. Complete rectal prolapse: evolution
of management and results // Dis. Colon Rectum. — 1999. — Vol. 42, N 4. — P. 460–466; discussion 466–9.
66. Deen K.I., Grant E., Billingham C., Keighley M.R. Abdominal resection rectopexy with pelvic floor repair versus perineal rectosigmoidectomy and pelvic floor repair for full-thickness rectal prolapse // Br. J. Surg. — 1994. — Vol. 81, N 2. — P. 302–304.
67. Boccasanta P., Venturi M., Reitano M.C. et al. Laparotomic vs. laparoscopic
rectopexy in complete rectal prolapse // Dig. Surg. — 1999. — Vol. 16, N 5. — P. 415–419.
68. Purkayastha S., Tekkis P., Athanasiou T. et al. A comparison of open vs. laparoscopic abdominal rectopexy for full-thickness rectal prolapse: a metaanalysis // Dis. Colon Rectum. — 2005. — Vol. 48, N 10. — P. 1930–1940.
69. Solomon M.J., Young C.J., Eyers A.A., Roberts R.A. Randomized clinical
trial of laparoscopic versus open abdominal rectopexy for rectal prolapse // Br. J. Surg. — 2002. — Vol. 89, N 1. — P. 35–39.
70. Briel J.W., Schouten W.R., Boerma M.O. Long-term results of suture rectopexy in patients with fecal incontinence associated with incomplete rectal prolapse // Dis. Colon Rectum. — 1997. — Vol. 40, N 10. — P. 1228–1232.
71. Graf W., Karlbom U., Pahlman L. et al. Functional results after abdominal
suture rectopexy for rectal prolapse or intussusception // Eur. J. Surg. — 1996. — Vol. 162, N 11. — P. 905–911.
72. Aitola P.T., Hiltunen K.M., Matikainen M.J. Functional results of operative treatment of rectal prolapse over an 11-year period: emphasis on transabdominal approach // Dis. Colon Rectum. — 1999. — Vol. 42, N 5. — P. 655–660.
73. Samaranayake C.B., Luo C., Plank A.W. et al. Systematic review on ventral
rectopexy for rectal prolapse and intussusception // Colorectal Dis. — 2010. — Vol. 12, N 6. — P. 504–512.
74. Penfold J.C., Hawley P.R. Experiences of Ivalon-sponge implant for complete rectal prolapse at St. Mark’s Hospital, 1960–70 // Br. J. Surg. — 1972. — Vol. 59, N 11. — P. 846–848.
75. Morgan C.N., Porter N.H., Klugman D.J. Ivalon (polyvinyl alcohol) sponge
in the repair of complete rectal prolapse // Br. J. Surg. — 1972. — Vol. 59, N 11. — P. 841–846.
76. Keighley M.R., Fielding J.W., Alexander-Williams J. Results of Marlex mesh abdominal rectopexy for rectal prolapse in 100 consecutive patients // Br. J. Surg. — 1983. — Vol. 70, N 4. — P. 229–232.
77. Yakut M., Kaymakcioglu N., Simsek A. et al. Surgical treatment of rectal prolapse. A retrospective analysis of 94 cases // Int. Surg. — 1998. — Vol. 83, N 1. — P. 53–55.
78. McKee R.F., Lauder J.C., Poon F.W. et al. A prospective randomized study
of abdominal rectopexy with and without sigmoidectomy in rectal prolapse // Surg. Gynecol. Obstet. — 1992. — Vol. 174, N 2. — P. 145–148.
79. Hsu A., Brand M.I., Saclarides T.J. Laparoscopic rectopexy without resection: a worthwhile treatment for rectal prolapse in patients without prior constipation // Am. Surg. — 2007. — Vol. 73, N 9. — P. 858–861.
80. Дурлештер В.М., Корочанская Н.В., Котелевский Е.В. и др. Современная
технология хирургического лечения хронического колостаза // Колопроктология. — 2012. — № 3. — С. 15–19.
81. Schlinkert R.T., Beart R.W.Jr., Wolff B.G., Pemberton J.H. Anterior resection for complete rectal prolapse // Dis. Colon Rectum. — 1985. — Vol. 28, N 6. — P. 409–412.
82. Cirocco W.C., Brown A.C. Anterior resection for the treatment of rectal
prolapse: a 20-year experience // Am. Surg. — 1993. — Vol. 59, N 4. — P. 265–269.
83. Tsunoda A., Yasuda N., Yokoyama N. et al. Delorme’s procedure for rectal prolapse: clinical and physiological analysis // Dis. Colon Rectum. — 2003. — Vol. 46, N 9. — P. 1260–1265.
84. Lieberth M., Kondylis L.A., Reilly J.C., Kondylis P.D. The Delorme repair for full-thickness rectal prolapse: a retrospective review // Am. J. Surg. — 2009. — Vol. 197, N 3. — P. 418–423.
85. Senapati A., Nicholls R.J., Thomson J.P., Phillips R.K. Results of Delorme’s
procedure for rectal prolapse // Dis. Colon Rectum. — 1994. — Vol. 37, N 5. — P. 456–460.
86. Watkins B.P., Landercasper J., Belzer G.E. et al. Long-term follow-up of the modified Delorme procedure for rectal prolapse // Arch. Surg. — 2003. — Vol. 138, N 5. — P. 498–502; discussion 502–3.
87. Riansuwan W., Hull T.L., Bast J. et al. Comparison of perineal operations
with abdominal operations for full-thickness rectal prolapse // World J. Surg. — 2010. — Vol. 34, N 5. — P. 1116–1122.
88. Azimuddin K., Khubchandani I.T., Rosen L. et al. Rectal prolapse: a search for the «best» operation // Am. Surg. — 2001. — Vol. 67, N 7. — P. 622–627.
89. Pescatori M., Zbar A.P. Tailored surgery for internal and external rectal prolapse: functional results of 268 patients operated upon by a single surgeon over a 21-year period // Colorectal Dis. 2009. — Vol. 11, N 4. — P. 410–419.
90. Altomare D.F., Binda G., Ganio E. et al. Rectal Prolapse Study G. Long-term
outcome of Altemeier’s procedure for rectal prolapse // Dis. Colon Rectum. — 2009. — Vol. 52, N 4. — P. 698–703.
91. Chun S.W., Pikarsky A.J., You S.Y. et al. Perineal rectosigmoidectomy for rectal prolapse: role of levatorplasty // Tech. Coloproctol. — 2004. — Vol. 8, N 1. —
P. 3–8; discussion 8–9.
92. Habr-Gama A., Jacob C.E., Jorge J.M. et al. Rectal procidentia treatment by perineal rectosigmoidectomy combined with levator ani repair // Hepatogastroenterology. — 2006. — Vol. 53, N 68. — P. 213–217.
93. Lenisa L., Schwandner O., Stuto A. et al. STARR with Contour Transtar: prospective multicentre European study // Colorectal Dis. — 2009. — Vol. 11, N 8. — P. 821–827.
94. Boccasanta P., Venturi M., Salamina G. et al. New trends in the surgical treatment of outlet obstruction: clinical and functional results of two novel transanal stapled techniques from a randomised controlled trial // Int. J. Colorectal Dis. — 2004. — Vol. 19, N 4. — P. 359–369.
95. Reboa G., Gipponi M., Ligorio M. et al. The impact of stapled transanal rectal resection on anorectal function in patients with obstructed defecation syndrome // Dis. Colon Rectum. — 2009. — Vol. 52, N 9. — P. 1598–1604.
96 Titu L.V., Riyad K., Carter H., Dixon A.R. Stapled transanal rectal resection for obstructed defecation: a cautionary tale // Dis. Colon Rectum. — 2009. — Vol. 52, N 10. — P. 1716–1722.
97. Gagliardi G., Pescatori M., Altomare D.F. et al. Italian Society of Colo-Rectal Surgery. Results, outcome predictors, and complications after stapled transanal rectal resection for obstructed defecation // Dis. Colon Rectum. — 2008. — Vol. 51, N 2. — P. 186–195; discussion 195.
98. Petersen S., Hellmich G., Schuster A. et al. Stapled transanal rectal resection under laparoscopic surveillance for rectocele and concomitant enterocele // Dis. Colon Rectum. — 2006. — Vol. 49, N 5. — P. 685–659.
99. Corman M.L., Carriero A., Hager T. et al. Consensus conference on the stapled transanal rectal resection for disordered defaecation // Colorectal Dis. — 2006. — Vol. 8, N 2. — P. 98–101.
100. Binda G.A., Pescatori M., Romano G. The dark side of double-stapled transanal rectal resection // Dis. Colon Rectum. — 2005. — Vol. 48, N 9. — P. 1830–1831.
НЕДОСТАТОЧНОСТЬ АНАЛЬНОГО СФИНКТЕРА
Введение
На протяжении многих лет в центре внимания отечественных и зарубежных колопроктологов остается проблема лечения больных с недостаточностью анального сфинктера. Актуальность этой проблемы связана с увеличением количества пациентов с анальной инконтиненцией как в нашей стране, так и за рубежом [2, 60]. Вопросы реабилитации данного контингента пациентов остаются нерешенными до настоящего времени [1, 98]. К тому же недержание кишечного содержимого представляет огромную социальную проблему как для самих больных, так и для окружающих [16].
Функция держания обусловлена рядом факторов: функциональным состоянием ЗАПК, консистенцией стула, состоянием центральной и периферической нервной системы, ответственной за иннервацию органов малого таза и мышц тазового дна. Патологические процессы, структурно-функциональные нарушения любого из перечисленных факторов могут способствовать развитию недержания кишечного содержимого. Во многих случаях этиология недержания кала является многофакторной, поэтому необходимо рассматривать это заболевание в комплексном аспекте [1, 2, 13, 27].
Рекомендации по диагностике и лечению пациентов с недостаточностью анального сфинктера служат руководством для практических врачей, осуществляющих ведение и лечение таких больных, и подлежат регулярному пересмотру в соответствии с новыми данными научных исследований в этой области.
Рекомендации включают следующие разделы: определение заболевания, классификация, профилактика, диагностика, консервативное и оперативное лечение, правила ведения периоперационного периода, а также прогноз у больных с недостаточностью анального сфинктера.
Для отдельных положений рекомендаций приведены уровни доказательности согласно общепринятой классификации Оксфордского центра доказательной медицины [72] (табл. 10.1).
Таблица 10.1. Уровни доказательности и степени рекомендаций на основании руководства Оксфордского центра доказательной медицины
|
Уровень |
Исследования методов диагностики |
Исследования методов лечения |
|
1а |
Систематический обзор гомогенных диагностических исследований 1-го уровня |
Систематический обзор гомогенных РКИ |
|
1b |
Валидизирующее когортное исследование с качественным «золотым стандартом» |
Отдельное РКИ (с узким доверительным интервалом) |
|
1с |
Специфичность или чувствительность столь высокие, что положительный или отрицательный результат позволяет исключить/ установить диагноз |
Исследование «Всё или ничего» |
|
2а |
Систематический обзор гомогенных диагностических исследований >2-го уровня |
Систематический обзор (гомогенных) когортных исследований |
|
2b |
Разведочное когортное исследование с качественным «золотым стандартом» |
Отдельное когортное исследование (включая РКИ низкого качества; т.е. с <80% пациентов, прошедших контрольное наблюдение) |
|
2с |
Нет |
Исследование «исходов»; экологические исследования |
|
3а |
Систематический обзор гомогенных исследований уровня 3b и выше |
Систематический обзор гомогенных исследований «случай–контроль» |
|
3b |
Исследование с непоследовательным набором или без проведения исследования «золотого стандарта» у всех испытуемых |
Отдельное исследование «случай–контроль» |
|
4 |
Исследование «случай–контроль» или исследование с некачественным или независимым «золотым стандартом» |
Серия случаев (и когортные исследования или исследования «случай–контроль» низкого качества) |
|
5 |
Мнение экспертов без тщательной критической оценки или основанное на физиологии, лабораторных исследованиях на животных или разработка «первых принципов» |
Мнение экспертов без тщательной критической оценки, лабораторные исследования на животных или разработка «первых принципов» |
|
Степени рекомендаций | ||
|
A |
Согласующиеся между собой исследования 1-го уровня | |
|
B |
Согласующиеся между собой исследования 2-го или 3-го уровня или экстраполяция на основе исследований 1-го уровня | |
|
C |
Исследования 4-го уровня или экстраполяция на основе уровня 2 или 3 | |
|
D |
Доказательства 5-го уровня или затруднительные для обобщения или некачественные исследования любого уровня | |
ВАЛИДИЗАЦИЯ РЕКОМЕНДАЦИЙ
Настоящие рекомендации в предварительной версии были рецензированы независимыми экспертами, которых попросили прокомментировать прежде всего, насколько интерпретация доказательств, лежащих в основе рекомендаций, доступна для понимания. Получены комментарии со стороны врачей амбулаторного звена, комментарии тщательно систематизировались и обсуждались на совещаниях экспертной группы. Последние изменения в настоящих рекомендациях были представлены для дискуссии на заседании профильной комиссии «Колопроктология» Экспертного совета Минздрава России 12 сентября 2013 г. Проект рекомендаций был повторно рецензирован независимыми экспертами и врачами амбулаторного звена. Для окончательной редакции и контроля качества рекомендации были повторно проанализированы членами экспертной группы, которые пришли к заключению, что все замечания и комментарии приняты во внимание, риск систематических ошибок
при разработке рекомендаций сведен к минимуму.
ОБЛАСТЬ ПРИМЕНЕНИЯ РЕКОМЕНДАЦИЙ
Данные методические рекомендации применимы при осуществлении медицинской деятельности в рамках Порядка оказания медицинской помощи взрослому населению с заболеваниями толстой кишки, анального канала и промежности колопроктологического профиля.
Определение
Недостаточность анального сфинктера — это частичное или полное нарушение произвольного и непроизвольного удержания кишечного содержимого [1, 13, 76]. По данным литературы, недержание кала — это повторяющееся неконтролируемое отхождение фекалий по крайней мере в течение 1-го месяца, включая детей с 4 лет [76, 100]. Недержание газов также может привести к существенному ухудшению качества жизни и должно также рассматриваться в определении.
Код по Международной классификации болезней 10-го пересмотра
n Класс: Болезни органов пищеварения (XI).
n Блок: Другие болезни кишечника (К62).
n Код: К62.8.
n Название: Другие уточненные болезни заднего прохода и прямой кишки.
Классификация
Существуют различные классификации недостаточности анального сфинктера, с помощью которых можно оценить тяжесть инконтинен-
ции. Самой распространенной является шкала Кливлендской клиники (Wexner) [98], по которой пациентом самостоятельно оцениваются степень и частота эпизодов инконтиненции, необходимость использования специальных гигиенических средств, степень влияния анальной инконтиненции на качество жизни (табл. 10.2).
Таблица 10.2. Шкала оценки недержания по Wexner [98]
|
Факторы |
Частота | ||||
|
Тип недержания |
Никогда |
Редко (меньше 1 раза в месяц) |
Иногда (меньше 1 раза в неделю, но больше 1 раза в месяц) |
Обычно (меньше 1 раза в день, но больше 1 раза в неделю) |
Всегда (больше 1 раза в день) |
|
Твердый стул |
0 |
1 |
2 |
3 |
4 |
|
Жидкий стул |
0 |
1 |
2 |
3 |
4 |
|
Газы |
0 |
1 |
2 |
3 |
4 |
|
Ношение прокладок |
0 |
1 |
2 |
3 |
4 |
|
Изменение образа жизни |
0 |
1 |
2 |
3 |
4 |
Оценка результатов после суммирования баллов:
n 0 баллов — полное держание;
n 20 баллов — полное анальное недержание.
Преимущества — простота и практичность, легко использовать и интерпретировать.
Недостатки:
n система основана только на оценке субъективных данных, отсутствие объективных параметров;
n не учитывает психологическое состояние пациента.
В настоящее время в клинической практике используют классификацию, подразделяющую недостаточность анального сфинктера по форме, этиологии и степени недержания кишечного содержимого, по клинико-функциональным и морфологическим изменениям анального сфинктера. Классификацию применяют для определения тяжести инконтиненции и выбора метода лечения [12, 13]. Однако эта классификация достаточно громоздкая и в клинической практике чаще всего используется в таком виде.
КЛАССИФИКАЦИЯ НЕДОСТАТОЧНОСТИ СФИНКТЕРА ЗАДНЕГО ПРОХОДА [13]
По форме:
n органическая;
n неорганическая (функциональная);
n смешанная.
По локализации дефекта мышц по окружности заднепроходного канала:
n на передней стенке;
n задней стенке;
n боковой стенке;
n нескольких стенках (сочетание дефектов);
n по всей окружности.
По степени недержания кишечного содержимого (нарушения функции держания):
n 1-я степень — недержание газов;
n 2-я степень — недержание газов и жидкого кала;
n 3-я степень — недержание газов, жидкого и твердого кала.
По морфологическим изменениям ЗАПК и протяженности мышечного дефекта по окружности заднепроходного канала:
n до 1/4 окружности;
n 1/4 окружности;
n до 1/2 окружности;
n 1/2 окружности;
n 3/4 окружности;
n отсутствие сфинктера.
Формулировка диагноза
При формулировании диагноза следует отразить форму и этиологию заболевания, степень недержания кишечного содержимого и характер нарушения анального сфинктера (см. раздел «Диагностика»). Ниже приведены примеры формулировок диагноза.
n Послеродовая недостаточность анального сфинктера 1–3-й степени (дефект сфинктера по передней полуокружности).
n Посттравматическая недостаточность анального сфинктера 1–3-й степени (дефект сфинктера по боковой полуокружности).
n Врожденная недостаточность анального сфинктера 1–3-й степени (дефект или полное отсутствие сфинктера).
n Функциональная недостаточность анального сфинктера 1–3-й степени.
Диагностика
Диагностика недостаточности анального сфинктера основана на жалобах больного, степени их выраженности, длительности болезни, анализе результатов клинического и объективного обследования пациента (УД 3b, СР C [1, 3, 13, 27, 33, 76]).
Сбор анамнеза. Выявляют следующие этиологические факторы возникновения заболевания: врожденные заболевания, желудочно-кишечные или неврологические расстройства, акушерский анамнез, историю предыдущих аноректальных или промежностных оперативных вмешательств, а также травм промежности и прямой кишки (УД 3b, СР C [13, 27, 33,76]).
Осмотр больного проводят на гинекологическом кресле в положении, как для литотомии. При этом оценивают расположение и сомкнутость заднепроходного отверстия, наличие рубцовой деформации промежности и заднего прохода, состояние кожных покровов перианальной, крестцово-копчиковой области и ягодиц. При осмотре промежности и заднего прохода выявляют сопутствующие заболевания в этой области — анальную трещину, геморрой, свищи или выпадение прямой кишки. При пальпации определяют наличие рубцового и воспалительного процесса перианальной области, состояние подкожной порции наружного сфинктера (УД 3b, СР C [3, 13, 27, 33, 98]).
Оценка анального рефлекса. Используют для изучения сократительной способности мышц сфинктера. Нормальный рефлекс — при штриховом раздражении перианальной кожи происходит полноценное сокращение наружного сфинктера; повышенный — когда одновременно со сфинктером происходит сокращение мышц промежности; ослабленный — реакция наружного сфинктера малозаметна (УД 5, СР D [1, 2, 13, 98]).
Пальцевое обследование прямой кишки. Определяют наличие и протяженность рубцового процесса, распространение его в пределах стенки анального канала. Оцениваются эластичность и протяженность сфинктера, сохранность и состояние мышц тазового дна. Определяются также анатомические соотношения мышечных и костных структур тазового кольца. Во время обследования оцениваются тонус и волевые усилия сфинктера заднего прохода, характер его сокращений, наличие зияния заднего прохода после извлечения пальца (УД 3b, СР C [3, 13, 27, 33, 76]). Ректороманоскопия. Осматривают слизистую оболочку прямой и дистального отдела сигмовидной кишки. Оценивают характер сосудистого рисунка, наличие воспалительных изменений в дистальном отделе тол-
стой кишки (УД 5, СР D [1, 2, 3, 27]).
Проктография с ирригоскопией. Определяет рельеф слизистой оболочки прямой кишки, величину ректоанального угла, состояние тазового дна, наличие суженных и расширенных участков, каловых камней, аномальное расположение отделов толстой кишки (УД 5, СР D [3, 13, 27]).
Исследование кишечной и влагалищной микрофлоры. У больных с неустойчивым стулом исследуют кишечную микрофлору для выявления дисбактериоза. У пациенток с послеродовой травмой, ректовагинальным свищом производится исследование степени чистоты влагалища (УД 5, СР D [2]).
ФУНКЦИОНАЛЬНЫЕ ИССЛЕДОВАНИЯ ЗАПИРАТЕЛЬНОГО АППАРАТА ПРЯМОЙ КИШКИ
Профилометрия — метод оценки давления в просвете полого органа при протягивании измерительного катетера. Аноректальная профилометрия обеспечивает регистрацию давления в разных плоскостях по всей длине анального канала. С помощью компьютерной программы строится
график распределения величин давления и проводится подсчет максимальных, средних величин давления, а также коэффициента асимметрии. Программа обработки предусматривает анализ данных давления на любом уровне поперечного сечения анального канала (УД 3b, СР C [7, 33]). Методика. Исследование проводят в положении больного на боку.
После предварительной калибровки катетер вводят в прямую кишку
больного на глубину 6 см. Устанавливают скорость перфузии жидкости по катетеру, равную 1 мл/мин. С помощью специального устройства — пулера — катетер вытягивают из прямой кишки со скоростью 5 мм/с, при этом регистрируют давление на всем протяжении его перемещения (табл. 10.3).
Анализ данных проводится с помощью компьютерной программы с построением графика, на котором отражается распределение давления в анальном канале (УД 3b, СР C [7, 33, 62]).
Таблица 10.3. Показатели профилометрии в норме (мм рт.ст.)
|
Показатель профилометрии |
Покой |
Волевое сокращение |
|
Анальный канал в целом | ||
|
Максимальное давление |
100,8±11,4 |
137,1±12,6 |
|
Среднее давление |
52,2±8,2 |
76,6±8,9 |
|
Коэффициент асимметрии, ЕД |
19,8±2,3 |
19,2±2,6 |
|
Зона высокого давления* | ||
|
Длина зоны, см |
2,2±0,5 |
2,7±0,65 |
|
Среднее давление |
72,±9,7 |
100,1±12,5 |
|
Коэффициент асимметрии |
15,5±2,1 |
13,9±2,2 |
* Зона высокого давления соответствует проекции внутреннего сфинктера и глубокой порции наружного сфинктера.
Аноректальная профилометрия является простым, неинвазивным способом измерения тонуса внутреннего и наружного анального сфинктера и длины зоны высокого давления в анальном канале, что доказано несколькими крупными исследованиями (УД 1c, СР A [3, 9, 33, 77, 93]).
Электромиография наружного сфинктера и мышц тазового дна — метод, позволяющий оценить жизнеспособность и функциональную активность мышечных волокон и определить состояние периферических нервных путей иннервирующих мышцы ЗАПК. Результат исследования играет важную роль в прогнозировании эффекта от пластических операций (УД Зb, СР C [3, 33]).
Для оценки произвольной и рефлекторной деятельности наружного сфинктера и мышц, поднимающих задний проход, используют анальный биполярный электрод, позволяющий оценить общую биоэлектрическую активность сфинктера и мышц тазового дна (табл. 10.4), сегментарный
анальный электрод, позволяющий оценить биоэлектрическую активность сфинктера по сегментам, и игольчатый электрод, с помощью которого возможно оценить как состояние мышц тазового дна, так и жизнеспособность перемещенных мышечных лоскутов.
Таблица 10.4. Показатели электромиографии в норме (мкВ)
|
Фоновая электрическая активность |
31–50 |
|
Произвольная электрическая активность |
154–212 |
Методика. Запись электромиографии осуществляют в положении больного на боку. В прямую кишку вводится катетер с баллончиком на глубину 6–8 см. В анальный канал в проекции наружного сфинктера устанавливается электрод на глубину 1 см. В течение 2–3 с регистрируется суммарная электрическая активность наружного сфинктера, затем осуществляется запись волевого сокращения сфинктера, и проводятся пробы с изменением внутрибрюшного давления (покашливание, напряжение брюшной стенки и натуживание) (УД 5, СР D [1, 7, 13]).
ЭНДОРЕКТАЛЬНОЕ УЛЬТРАЗВУКОВОЕ ИССЛЕДОВАНИЕ
УЗИ позволяет выявить локальные структурные изменения в мышечных структурах ЗАПК, наличие и протяженность его дефектов, состояние мышц тазового дна (УД 2b, СР B [3, 6, 18, 33, 53, 55, 88–90]). Эффективность трансанального УЗИ в определении дефектов внутреннего и наружного сфинктера приближается к 100% (УД 2b, СР B [13, 18, 33, 88, 89]). Методика. Исследование выполняется на ультразвуковых диагностических приборах с использованием радиального и линейного ректальных датчиков частотой 10 МГц. Больному, находящемуся в коленно-локтевом положении или на боку, в анальный канал вводят ректальный датчик на расстояние 8 см с предварительно надетым на него резиновым баллончиком и откачанным из него воздухом. Через переходник баллончик заполняют дистиллированной водой 30–50 мл, что обеспечивает хорошую проводимость УЗ-луча. Датчиком проводят вращательные движения по часовой стрелке и линейное УЗ-сканирование путем проведения продольных сечений анального канала, вращая датчик (УД 4, СР C [6]).
Лечение
Лечебные мероприятия при недостаточности анального сфинктера подразделяются на два основных способа — консервативный и хирургический. Включают назначение лекарственных препаратов, БОСтерапию, электростимуляцию анального сфинктера, лечебно-физкультурный комплекс, хирургическое лечение, психосоциальную поддержку (УД 2b, СР B [1–3, 13, 61]).
Цель — улучшение функции держания.
Показания к госпитализации: невозможность улучшения функции держания в амбулаторных условиях, неэффективность консервативной терапии.
КОНСЕРВАТИВНОЕ ЛЕЧЕНИЕ
Консервативное лечение направлено на усиление сократительной способности анального сфинктера, поддержание и улучшение деятельности нервно-рефлекторного аппарата, обеспечивающего нормальную функциональную активность ЗАПК. Терапия состоит из специальной диеты, приема антидиарейных препаратов, лечения по принципу БОСтерапии, анальной электростимуляции, тибиальной нейромодуляции, лечебно-физкультурного комплекса.
Консервативное лечение применяется у больных с 1-й степенью недостаточности анального сфинктера, реже при 2-й степени, наличии линейного дефекта сфинктера, не превышающего 1/4 окружности, при отсутствии деформации заднего прохода (УД 5, СР D [1, 3, 13]).
Диета
n Увеличенное потребление клетчатки
Цель: достижение нормальной консистенции стула, уменьшение риска появления жидкого стула, уменьшение частоты дефекаций. По данным литературы, нормализующее влияние на консистенцию стула оказывает диета, богатая клетчаткой, продукты, содержащие подорожник и пищевые волокна (УД 3a, СР C [19]). Рекомендуемая доза пищевых волокон составляет 25–30 г в день. Употребление любых продуктов, способных вызвать диарею, противопоказано (УД 3b, СР C [19, 26, 27]).
n Очистительные клизмы, слабительные средства и свечи
Используются при лечении пациентов с эпизодами многомоментной дефекации, у пациентов с повреждениями спинного мозга и тяжелым запором, приводящими к проблемам с удержанием стула в результате постоянного перенаполнения кишечным содержимым прямой кишки (УД 1a, СР A [24, 56, 57, 101)].
МЕДИКАМЕНТОЗНОЕ ЛЕЧЕНИЕ (АНТИДИАРЕЙНЫЕ ВЕЩЕСТВА)
Аттапулгит в дозе 2 столовые ложки суспензии или по 2 таблетки после каждой дефекации, не более 12 таблеток в сутки, действуют, поглощая избыток жидкости в стуле (УД 3a, СР C [75]).
Лоперамид способствует замедлению моторики кишечника и увеличению поглощения жидкости. Дозировка лоперамида составляет от 2 до 4 мг с последующим титрованием доз в общей совокупности до 24 мг в течение 24 ч в разделенных дозах (УД 3а, СР C [75]).
БИОЛОГИЧЕСКАЯ ОБРАТНАЯ СВЯЗЬ
БОС-терапия рекомендуется на начальном этапе лечения пациентов с нарушением произвольного сокращения анального сфинктера, у ко-
торых не удалось добиться положительного эффекта с помощью диеты и медикаментозной терапии (УД 1b, СР B [48, 51, 67, 69]). Также терапия по принципу БОС может применяться при хирургическом лечении недостаточности анального сфинктера и в комплексе процедур послеоперационной реабилитации больных (УД 1b, СР В [29, 52]).
При лечении недостаточности анального сфинктера БОС-терапия направлена на развитие саморегуляции функциональной деятельности мышечных структур промежности, развитие правильного восприятия ощущений, способных улучшить контроль за функцией держания кишечного содержимого (УД 2b, СР B [15]). Метод подразделяется на силовой и координационный.
Силовой метод БОС направлен на повышение сократительной способности мышц сфинктера.
Методика. Больному, лежащему на боку перед экраном монитора, в задний проход вводят электромиографический датчик. Под контролем врача-методиста пациент выполняет волевые сокращения сфинктера, наблюдая на экране за эффективностью своих упражнений. Упражнения повторяются 15–30 раз. Курс 10–15 сеансов.
Координационный метод БОС направлен на выработку условного ректоанального рефлекса.
Методика. Больному, лежащему на боку перед экраном монитора, в задний проход в ампулу прямой кишки вводится латексный баллончик, который заполняется воздухом объемом 20–50 мл. Со сфинктера снимаются биопотенциалы с помощью электромиографического датчика. При наполнении баллона больной производит сокращения сфинктера и по экрану контролирует правильность выполнения упражнений. Упражнения повторяются 10–15 раз. Курс 10–15 сеансов.
Информация о функциональной активности мышечных структур промежности, силе мышечных сокращений предоставляется пациенту в виде доступной, наглядной формы электромиограммы в виде столбиков, графиков на дисплее или в виде мультимедийного варианта.
БОС-терапия дает возможность пациентам учиться самостоятельно, осознанно управлять мышцами заднего прохода, ориентируясь на ощущения, получаемые вследствие проводимого курса лечения. По данным различных авторов, эффективность БОС-терапии составляет 50–89% (УД 3a, СP C [3, 70, 74 78]).
ЭЛЕКТРОСТИМУЛЯЦИЯ АНАЛЬНОГО СФИНКТЕРА И МЫШЦ ПРОМЕЖНОСТИ
Электростимуляцию анального сфинктера применяют как самостоятельный вид лечения для больных с неорганической формой недержания 1-й степени, при линейных дефектах жома, не превышающих 1/4 окружности, при отсутствии деформации заднего прохода, а также в предоперационном периоде (УД ЗЬ, СР C [1, 2, 13]).
Методика. Электростимуляцию мышц анального сфинктера и промежности выполняют на различных аппаратах (стационарных и портативных) специальными внутрианальными электродами с частотой импульсов от 10 до 100 Гц в прерывистом и непрерывном режиме.
Курс внутрианальной электростимуляции составляет 14 дней. Длительность сеанса 10–20 мин (непрерывный режим — частота пачек импульсов 100 Гц, длительность сеанса 10 мин; прерывистый режим — частота пачек импульсов 10–100 Гц, длительность сеанса 20 мин). При необходимости проведения повторного курса стимуляции интервал между курсами составляет 3 мес (УД 4, СР C [20, 78]).
ТИБИАЛЬНАЯ НЕЙРОМОДУЛЯЦИЯ
Метод заключается в воздействии на тазово-крестцовое нервное сплетение (S2–S4) путем электростимуляции заднего большеберцового нерва на нижних конечностях. За счет стимуляции вегетативных, чувствительных и двигательных нервов методика улучшает тонус, сократительную способность и нервно-рефлекторную деятельность мышц ЗАПК.
Тибиальную нейромодуляцию применяют при лечении функциональной недостаточности анального сфинктера, а также в преди послеоперационном периоде при хирургической коррекции анальной инконтиненции (УД 2b, СР B [38]).
Методика. Стимуляция проводится с помощью игольчатого электрода или накожных поверхностных электродов, накладываемых в проекции заднего большеберцового нерва (частота тока 20 Гц, длительность 200 мс, импульсный режим — 5 с стимуляции, 10 с отдых). Длительность процедуры 30 мин. Курс лечения игольчатыми электродами длится 12 сеансов: по 2 сеанса в неделю; накожными электродами — 1 раз в день в течение 1 мес, затем 1 раз в 3 дня в течение 3 мес (УД 4, СР C [97]).
Улучшение функции держания после проведения тибиальной нейромодуляции отмечается в 65–85% наблюдений (УД 1b, СР B [14, 34, 38,
42, 45, 49]).
САКРАЛЬНАЯ СТИМУЛЯЦИЯ НЕРВОВ
Сакральная стимуляция нервов — метод, заключающийся в длительной электростимуляции тазово-крестцового нервного сплетения с помощью электрода, установленного через одно из наружных крестцовых отверстий к крестцовому нерву данной локализации.
Проведение сакральной стимуляции показано у больных с функциональной недостаточностью анального сфинктера при отсутствии грубых органических повреждений наружного и внутреннего сфинктера. Также метод может быть эффективен у больных с небольшими дефектами анального сфинктера (УД 2a, СР В [82, 83]).
Методика. Метод сакральной стимуляции включает три фазы. Во время 1-й фазы с помощью игольчатого электрода, который чрескожно
последовательно вводится к наружным крестцовым отверстиям слева и справа в проекции S2–S4, производится поиск крестцовых нервов, при электростимуляции которых происходит наиболее выраженное сокращение наружного сфинктера и мышц промежности. При получении выраженного ответа на раздражение переходят ко 2-й фазе. При этом игольчатый электрод заменяется на гибкий, который соединяется с внешним переносным электростимулятором. Во время 2-й фазы проводится пробный курс сакральной стимуляции продолжительностью от 1 до 3 нед до получения клинического эффекта. Пациенты с положительной динамикой, уменьшением симптоматики анальной инконтиненции переходят к 3-й фазе лечения — хирургической имплантации постоянного электрода и электростимулятора. Как правило, блок электростимулятора имплантируется в верхнюю часть ягодичной области слева или справа. Интенсивность и режим стимуляции контролируется пациентом с помощью внешнего устройства. На фоне сакральной стимуляции улучшение функции держания колеблется от 44 до 73% (УД 3a, СР B [42, 55, 63, 65, 82, 83, 94]).
Частота осложнений при сакральной стимуляции колеблется от 5 до 26% (УД 2a, СР B [41, 54, 82, 93]). Осложнения, требующие удаления имплантированного стимулятора, развиваются достаточно редко (УД 2a, СР B [41, 54, 64, 83, 93]). Наиболее частым осложнением является боль в области установленного электростимулятора. Гнойно-воспалительные осложнения в области имплантата отмечаются в 5% (УД 2a, СР B [83]).
КОМПЛЕКС ЛЕЧЕБНОЙ ФИЗКУЛЬТУРЫ
Лечебно-физкультурный комплекс проводится для укрепления сфинктера, увеличения силы, скорости сокращений и работоспособности мышц тазового дна. Комплекс лечебной физкультуры при недостаточности анального сфинктера разработан и предложен ГНЦ колопроктологии (УД 5, СР D [2, 12]).
Показания. Функциональная и органическая формы недостаточности анального сфинктера, компонент комплексной реабилитации пациентов после пластических операций по поводу недостаточности анального сфинктера. Курс занимает 13–15 дней и может проводиться в комплексе с электростимуляцией и медикаментозным лечением (УД 3b, СР C [2, 78]).
Комплекс упражнений. (См. приложение)
ГЕРМЕТИЗИРУЮЩИЙ АНАЛЬНЫЙ ТАМПОН
Применение герметизирующего анального тампона основано на механической герметизации заднего прохода специальным мягким тампоном, вводимым в анальный канал. Тампон имеет два размера — большой
(L) и маленький (S). Средняя длительность использования одного тампона составляет 12 ч (УД 1a, СР A [32]).
Показания. Недостаточность анального сфинктера 2–3-й степени. Анальный тампон применяется как временная мера или как вариант постоянного лечения при невозможности хирургической коррекции анальной инконтиненции.
Противопоказаниями к использованию служат выраженная диарея, кишечные инфекции и воспалительные заболевания толстой кишки и анального канала. У ряда пациентов использование анального тампона вызывает дискомфорт, что является препятствием к его применению (УД 1a, СР A [32]).
При тяжелой степени недостаточности анального сфинктера использование анального тампона позволяет снизить частоту развития мацерации и воспалительных изменений кожи перианальной области (УД 1a, СР A [56, 71]).
Согласно приказу Минздравсоцразвития, анальный тампон относится к перечню специальных средств при нарушениях функции выделения [8].
ХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕ
Вид оперативного вмешательства зависит от величины и локализации дефекта сфинктера, распространенности рубцового процесса. Современная тактика хирургического лечения направлена на восстановление сфинктера заднего прохода местными тканями при невозможности их использования близлежащими мышцами. В зависимости от степени поражения ЗАПК, величины дефекта анального сфинктера применяются следующие операции: сфинктеропластика, сфинктеролеватеропластика, сфинктероглютеопластика, глютеопластика, грацилопластика (УД 2b, СР B [1, 2, 13, 60]).
ПОКАЗАНИЯ К ХИРУРГИЧЕСКОМУ ЛЕЧЕНИЮ
Показаниями к хирургическому лечению пациентов с недостаточностью анального сфинктера служат невозможность радикального излечения пациентов с недостаточностью анального сфинктера консервативными методами, недостаточность анального сфинктера 2-й и 3-й степени, с дефектом сфинктера размером 1/4 окружности и более, при наличии рубцовой деформации стенок анального канала, нарушении анатомических взаимоотношений мышц запирательного аппарата (УД 4, СР С [1, 2, 13]).
Противопоказанием к хирургической коррекции является поражение
отделов центральной и периферической нервной системы, участвующих в иннервации органов малого таза и мышечных структур промежности (УД 5, СР D [2]).
СФИНКТЕРОПЛАСТИКА
Показания. Выполняется пациентам с локальными дефектами наружного сфинктера размером до 1/4 окружности (УД 3a, СР B [1, 3, 13, 60, 102]).
Методика. Из рубцовой ткани выделяются концы сфинктера и без натяжения ушиваются конец в конец. Хорошие результаты лечения возможны только при адекватной мобилизации обоих концов сфинктера.
Хорошие результаты лечения в раннем периоде после операции отмечаются в 31–83% случаев (УД 2a, СР A [3, 35, 37, 39, 43, 50, 68, 73, 81, 87,
92]). С течением времени при наблюдении за пациентами в отдаленном периоде результаты сфинктеропластики ухудшаются (УД 2a, СР A [3, 21, 37, 47, 60, 62]).
СФИНКТЕРОЛЕВАТОРОПЛАСТИКА
Показания. Производится при величине дефекта сфинктера от 1/4 до 1/2 окружности с локализацией по передней или задней полуокружности сфинктера (УД 2a, СР B [1, 9, 13, 44]).
Методика. При расположении дефекта по передней окружности иссекают рубцовые ткани, выделяют концы сфинктера и передние порции леваторов, которые сшивают, с ушиванием раны в продольном направлении.
При расположении дефекта по задней полуокружности также производится сшивание концов сфинктера и леваторов. Рана ушивается в продольном направлении. Важной задачей при задней сфинктеролеваторопластике является уменьшение аноректального угла (УД 2a, СР B [76, 80]).
Хорошие отдаленные результаты сохраняются у 33–55% пациентов (УД 2a, СР B [44, 1, 9, 13]).
СФИНКТЕРОГЛЮТЕОПЛАСТИКА (ЗАМЕЩЕНИЕ ДЕФЕКТА КОРОТКИМ ЛОСКУТОМ БОЛЬШОЙ ЯГОДИЧНОЙ МЫШЦЫ)
Показания. Сфинктероглютеопластика производится при величине дефекта сфинктера 1/2 окружности с локализацией его по боковым полуокружностям (УД b, СР C [2, 5]).
Методика. Производят мобилизацию концов сфинктера из рубцовой ткани. Из ягодичной мышцы выкраивают мышечный лоскут длиной 7–8 см. Свободную и проксимальную часть выделенного мышечного лоскута подшивают к мобилизованным краям анального сфинктера (УД 3b, СР C [12]).
Хорошие и удовлетворительные результаты отмечаются у 61,1% пациентов (УД 3b, СР C [2]).
ГЛЮТЕОПЛАСТИКА (ФОРМИРОВАНИЕ СФИНКТЕРА ЗАДНЕГО ПРОХОДА ДЛИННЫМИ ЛОСКУТАМИ БОЛЬШОЙ ЯГОДИЧНОЙ МЫШЦЫ)
Показания. Глютеопластика выполняется при дефекте более 1/2 окружности сфинктера при тяжелых травматических повреждениях и врожденных аномалиях развития ЗАПК в один или несколько этапов. В первом случае одновременно используют мышечные лоскуты обеих
ягодичных мышц, во втором — поочередно через 4–6 мес (УД 3b, СР C [2, 12]).
Методика. Производится выделение длинных мышечных лоскутов вдоль хода мышечных волокон из средней и нижней трети большой ягодичной мышцы. Обязательно сохранение сосудисто-нервного пучка. Концы мышечных лоскутов проводятся вокруг прямой кишки через подкожный тоннель, фиксируются к лонным костям либо сшиваются между собой.
Улучшение функции держания при глютеопластике отмечается в 43–60% случаев (УД 3b, СР C [25, 40, 59, 61]).
ГРАЦИЛОПЛАСТИКА (ФОРМИРОВАНИЕ СФИНКТЕРА ЗАДНЕГО ПРОХОДА НЕЖНОЙ МЫШЦЕЙ БЕДРА)
Показания. Грацилопластика производится при обширных дефектах сфинктера более 1/2 окружности, при тяжелых травматических повреждениях и врожденных аномалиях развития ЗАПК (УД 3a, СР B [9, 10, 11, 13, 23, 27, 58, 79]).
Методика. Нежную мышцу мобилизуют от проксимальной трети бедра до ее сухожильного конца, отсекают от надмыщелка большеберцовой кости. Обязательно сохранение сосудисто-нервного пучка. Мышцу поворачивают на 180° и проводят через подкожный тоннель вокруг заднего прохода, создавая вокруг него мышечное кольцо. Сухожильный конец нежной мышцы фиксируется к бугру седалищной кости.
Хорошие результаты отмечаются в 50–60% наблюдений (УД 3a, СР B [25, 40, 86]).
ИСКУССТВЕННЫЙ СФИНКТЕР
Имплантация искусственного анального сфинктера — вариант хирургической коррекции недостаточности анального сфинктера у больных с рефрактерной инконтиненцией при неэффективности пластики сфинктера другими методами (УД 3b, СР B [51]).
Противопоказания. Абсолютными противопоказаниями для этой процедуры являются наличие гнойных очагов в промежности, болезнь Крона, радиационный проктит, выраженная рубцовая деформация промежности.
Методика. Искусственный сфинктер представляет собой циркуляр-
ную емкость, сделанную из силикона, которая увеличивается в объеме за счет заполнения жидким гелем. Через отдельные разрезы имплантат устанавливается вокруг дистального отдела прямой кишки, отдельно в мягкие ткани имплантируется баллончик с гелем, который с помощью помпы перекачивается между искусственным сфинктером и баллончиком. Методика позволяет пациенту произвольно опорожнять кишечник и задерживать дефекацию. Недостатком метода является высокая частота нагноения раны в области установленного искусственного сфинктера, в результате чего устройство приходится удалять. Частота эксплантации
колеблется от 20 до 80% (УД 3a, СР B [3, 17, 22, 66, 100, 101]). При долгосрочных наблюдениях (38 мес) положительный результат наблюдается лишь в 19% случаев (УД 4, СР C [28]).
ИНЪЕКЦИОННЫЙ МЕТОД
Инъекционный метод применяется для лечения недержания, связанного с недостаточностью наружного или внутреннего сфинктеров (УД 5, СР D [4]).
Методика. Инъекция проводится силиконовыми биоматериалами, которые вводятся в проекции дефектов сфинктера или вокруг них в интерсфинктерное пространство либо в подслизистый слой нижнеампулярного отдела прямой кишки. При функциональной недостаточности инъекции выполняются в 3–4 точки с целью циркулярной эластичной герметизации заднего прохода. Точность введения достигается с помощью ультразвукового контроля (УД 3b, СР C [93]). Гель, расположенный в тканях дистального отдела прямой кишки, способствует увеличению внутрианального давления в покое. Эффект терапии обеспечивается за счет улучшения функции «пассивного» держания. Инъекционная терапия позволяет улучшить функцию держания в течение 12–24 мес после процедуры (УД 3b, СР C [93]). Данный метод способствует улучшению функции держания примерно у 50–56% пациентов (УД 1b, СР C [4, 30, 31, 64, 91, 96]).
Чего нельзя делать
n Выполнять оперативное вмешательство без тщательного объективного обследования больного.
n Выполнять сфинктеропластику при дефекте более 1/4 окружности сфинктера.
n Выполнять сфинктеролеваторопластику при дефекте более 1/2 окружности сфинктера.
n Выполнять операцию без достаточных знаний анатомических и функциональных особенностей ЗАПК.
n Выполнять пластические операции вне специализированных центров, хирургами с недостаточным опытом (УД 4, СР C [1,2,13]).
Дальнейшее ведение
Послеоперационный период складывается из двух этапов.
n Первый этап — 10–15 дней после операции, направлен на профилактику воспалительных явлений в операционной ране, лечение воспалительных осложнений. Следует применять раннее комплексное лечение недостаточности анального сфинктера и обучение пациента лечебной физкультуре во время нахождения в стационаре (УД 5, СР D [1, 13]).
n Второй этап — с 15–17-го дня после операции. Проводятся лечебнофизкультурный комплекс, электростимуляция сфинктера, БОС-терапия ЗАПК в течение 10–12 дней.
Адъювантная БОС-терапия после операции улучшает качество жизни оперированных пациентов (УД 3a, СР B [29]). Данный комплекс лечения показан больным с отсутствием или нарушением ректоанального рефлекса, пациентам с периодическими симптомами недержания кала, сохраняющимися после оперативного лечения (УД 3a, СР B [36, 46, 74, 85]). Лечебно-физкультурный комплекс назначают через 3–4 нед после операции. Общая дозированная нагрузка не должна вызывать чувства
болезненности и утомляемости.
Повторное обследование и проведение профилактических курсов лечения проводят 1 раз в год на протяжении 3 лет с момента операции. При нестабильном эффекте комплекс консервативных мероприятий повторяют каждые 6 мес на протяжении 4–5 лет. Как правило, к 3–4-му курсу лечения отмечается стабилизация эффекта лечения. Показано наблюдение за больными, перенесшими сфинктеропластику в течение года, сфинктеролеваторопластику — 2–3 лет, создание ЗАПК из мышц бедра и ягодичной области — 5 лет (УД 5, СР D [13]).
Прогноз
Применение консервативного лечения у больных с 1-й степенью недержания дает возможность добиться улучшения функции держания у большинства пациентов при условии повторения курсов лечения. Применение различных видов оперативного лечения в зависимости от степени недостаточности и выраженности рубцовых изменений ЗАПК и тканей промежности приводит к улучшению функции держания в среднем у 30–85% пациентов при условии регулярного проведения консервативного лечения (УД 2a, СР A [1, 3, 13, 35, 37, 39, 43, 50, 68, 73, 81, 87, 92]).
Прогностически неблагоприятными факторами хирургического лечения недостаточности анального сфинктера являются выраженные рубцовые изменения промежности и дистального отдела прямой кишки (УД 4, СР C [2]), нейропатии (УД 3a, СРB [61]).
Профилактика
Профилактика недостаточности анального сфинктера заключается в следующем.
n Улучшение качества акушерских пособий, сокращение послеродовых осложнений. При возникающих акушерских осложнениях показаны правильное и своевременное их лечение (ушивание разрывов) и адекватное послеродовое и послеоперационное ведение (УД 3a, СР B [88]).
n Улучшение качества хирургической помощи больным с заболеваниями анального канала и дистальной части прямой кишки (правильный выбор оперативного лечения; правильная техника выполнения операций; УД 5, СР D [1, 2, 13]).
n Улучшение качества периоперационного ведения пациентов (УД 5, СР D [2]).
Критерии оценки качества помощи в стационаре представлены в таблице 10.5. Для оценки качества медицинской помощи используют временные, процессуальные и профилактирующие критерии. Временные характеризуют своевременность оказания определенных этапов медицинской помощи. Выполнение пациенту ряда медицинских манипуляций, инструментальных и лабораторных исследований, необходимых для качественного оказания медицинской помощи, оценивают в процессуальных критериях. Для анализа мероприятий, направленных на предотвращение развития осложнений, используют профилактирующие критерии.
Таблица 10.5. Критерии оценки качества медицинской помощи в стационаре больным с недостаточностью анального сфинктера (0 — нет, 1 — да)
|
Клинические рекомендации |
Временные |
Процессуальные |
Профилактирующие |
|
1. Клинические рекомендации по диагностике и лечению взрослых пациентов c недостаточностью анального сфинктера (код МКБ — К62.8) |
Установка клинического диагноза в течение 72 ч: 0/1 |
Оценка анального рефлекса: 0/1. Пальцевое исследование прямой кишки: 0/1. Аноскопия: 0/1. Ректороманоскопия: 0/1. Определение группы крови: 0/1. Исследование крови на сифилис, вирусный гепатит В, вирусный гепатит С: 0/1. Клинический анализ крови; биохимический анализ крови; клинический анализ мочи; коагулограмма: 0/1. Объективизация степени недостаточности с помощью шкалы Векснера или сфинктерометрии: 0/1. Ультразвуковое исследование запирательного аппарата прямой кишки ректальным датчиком: 0/1. Метод оперативного лечения в соответствии с клиническими рекомендациями: 0/1. Метод анестезии в соответствии с объемом оперативного лечения: 0/1 |
Отсутствие осложнений: • кровотечение: 0/1; • абсцесс: 0/1; • флегмона: 0/1; • пневмония: 0/1; • тромбоэмболия: 0/1; • летальный исход: 0/1 |
Литература
1. Воробьев Г.И. Основы колопроктологии. — М.: МИА, 2006. — 430 с.
2. Дульцев Ю.В., Саламов К.Н. Анальное недержание. — М.: Медицина, 1993. — 208 с.
3. Кайзер А.М. Колоректальная хирургия. — М.: БИНОМ, 2011. — 737 с.
4. Комиссаров И.А., Колесников А.Г. Использование гелевой пластики анального канала у детей с недержанием кала // Рос. вестн. дет. хир., анестезиол. и реаниматол. — 2011. — Т. 7, № 4. — С. 33–37.
5. Махов Н.И. Восстановление наружного жома прямой кишки и укрепление промежности лоскутами большой ягодичной мышцы // Хирургия. — 1976. — № 7. — С. 107–116.
6. Орлова Л.П. УЗ-диагностика заболеваний толстой кишки // Практическое руководство по УЗ-диагностике / Под ред. В.В. Митькова. — М.: Видар-М, 2011. — С. 331–342.
7. Подмаренкова Л.Ф., Алиева Э.И., Полетов Н.Н. и др. Роль функцио-
нальных методов исследования запирательного аппарата прямой кишки в выявлении патогенетических механизмов анальной инконтиненции // Колопроктология. — 2006. — Т. 16, № 2. — С. 24–30.
8. Приказ Минздравсоцразвития России от 28.07.2011 № 823н «Об утверждении классификации технических средств реабилитации (изделия) в рамках федерального перечня реабилитационных мероприятий, технических средств реабилитации и услуг, предоставляемых инвалиду, в целях определения размера компенсации за технические средства реабилитации (изделия), приобретенные инвалидами (ветеранами) за собственный счет, и (или) оплаченные за счет собственных средств услуги по их ремонту».
9. Саидов А.С. Выбор метода хирургической коррекции недостаточности анального сфинктера: Сб. науч. работ // Проблемы проктологии. — М., 2002. — Вып. 18. — С. 216–219.
10. Татьянченко В.К., Шурыгин К.В., Гаербеков А.Ш. Принципы построения программы послеоперационной реабилитации больных с замыкательным аппаратом кишки, созданным из тонкой мышцы бедра // Актуальные вопросы колопроктологии. 1 съезд колопроктологов России. — Самара, 2003. — С. 370–371.
11. Темелков Т.Д. Пластические и реконструктивные операции на аналь-
ном сфинктерном аппарате // Хирургия. — 1990. — № 3. — С. 73–75.
12. Федоров В.Д., Дульцев Ю.В. Проктология. — М.: Медицина, 1984. — 384 с.
13. Шелыгин Ю.А., Благодарный Л.А. Справочник по колопроктологии. — М.: Литтерра, 2012. — 596 с.
14. Agrò E., Campagna A., Sciobica F. et al. Posterior tibial nerve stimulation: is the once-a-week protocol the best option // Finazzi Urol. Nefrol. — 2005. — Vol. 57, N 2. — P. 119–123.
15. Bartlett L.M., Hoots K., Nowak M., Ho Y.H. Biofeedback therapy for faecal
incontinence: a rural and regional perspective // Rural Remote Health. — 2011. — Vol. 11, N 2. — P. 1630.
16. Barucha A.F., Zinsmeister A.R., Locke G.R. et al. Symptoms and quality of life in community women with fecal incontinence // Clin. Gastroenterol. Hepatol. — 2006. — Vol. 4. — P. 1004–1009.
17. Baumgartner U. The artificial sphincter: therapy for faecal incontinence //
Zentralbl. Chir. — 2012. — Vol. 137, N 4. — P. 340–344.
18. Berger N., Tjandra J.J., Solomon M. Endoanal and endorectal ultrasound: applications in colorectal surgery // Aust. N.Z. J. Surg. — 2004. — Vol. 74. — P. 71–75.
19. Bliss D. Z., Jung H.J., Savik K. et al. Supplementation with dietary fiber improves fecal incontinence // Nurs. Res. — 2001. — Vol. 50. — P. 203–213.
20. Boselli A.S., Pinni F., Cecchini S. et al. Biofeedback therapy plus anal electrostimulation for fecal incontinence: Prognostic factors and effects on anorectal physiology // World J. Surg. — 2010. — Vol. 34. — P. 815–821.
21. Bravo Gutierrez A., Madoff R.D., Lowry A.C. et al. Long-term results of anterior sphincteroplasty // Dis. Colon Rectum. — 2004. — Vol. 47. — P. 727–731.
22. Casal E., San Ildefonso A., Carracedo R. et al. Artificial bowel sphincter in severe anal incontinence // Colorectal Dis. — 2004. — Vol. 6. — P. 180–184.
23. Chapman A.E., Geerdes B., Hewett P. et al. Dynamic graciloplasty in the treatment of faecal incontinence // Br. J. Surg. — 2002. — Vol. 89. — P. 138–153.
24. Cheetham M., Brazzelli M., Norton C., Glazener C.M. Drug treatment for faecal incontinence in adults // Cochrane Database Syst. Rev. — 2003. — URL: http://www.uptodate.com/contents/fecal-incontinence-in-adults/abstract/56.
25. Christiansen J., Hansen C.R., Rasmussen O.O. Bilateral gluteus maximus
transposition for anal incontinence // Br. J. Surg. — 1995. — Vol. 82, N 7. — P. 903–905.
26. Congilosi Parker S., Thorsen A. Fecal incontinence // Surg. Clin. North Am. — 2003. — Vol. 82. — P. 1273–1290.
27. Corman M.L. Colon and Rectal Surgery. — Philadelphia: Lippincott, 1984. — P. 129–134.
28. Darnis B., Faucheron J.L., Damon H., Barth H. Technical and functional results of the artificial bowel sphincter for treatment of severe fecal incontinence: is there any benefit for the patient? // Des. Colon Rectum. — 2013. — Vol. 56, N 4. — P. 505–510.
29. Davis K.J., Kumar D., Poloniecki J. Adjuvant biofeedback following anal
sphincter repair: a randomized study // Aliment. Pharmacol. Ther. — 2004. — Vol. 20. — P. 539–549.
30. De la Portilla F., Vega J., Rada R. et al. Evaluaton by Three-dimensional anal endosonography of injectable silicone biomaterial (PTQ) implants to treat fecal incontinence: long-term localization and relation with the deterioration of the continence // Tech. Coloproctol. — 2009. — Vol. 13, N 3. — P. 195–199.
31. Deli T., Stordal, Vatten G.G. et al. Sphincter training or anal injections of
dextranomer for treatment of anal incontinence: a randomized trial // Scand. J. Gastroenterol. — 2013. — Vol. 48, N 3. — P. 302–310.
32. Deutekom M., Dobben. Plugs for containing faecal incontinence // Cochrane Database Syst. Rev. — 2012. — URL: http://www.nice.org.uk/nicemedia/pdf/ CG49FullGuideline.pdf.
33. Dobben A.C., Terra M.P., Deutekom M. et al. Diagnostic work-up for faecal
incontinence in daily clinical practice in the Netherlands // Neth. J. Med. — 2005. — Vol. 63, N 7. — P. 265–269.
34. Eléouet M., Siproudhis L., Guillou N. et al. Chronic posterior tibial nerve transcutaneous electrical nerve stimulation to treat fecal incontinence // Int. J. Colorectal Dis. — 2010. — Vol. 25, N 9. — P. 1127–1132.
35. Elton C., Stoodley B.J. Anterior anal sphincter repair: results in a district
general hospital // Ann. R. Coll. Surg. Engl. — 2002. — Vol. 84. P. 321–324.
36. Enck P., Daublin G., Heinrich J. et al. Long-term efficacy of biofeedback training for fecal incontinence // Dis. Colon Rectum. — 1994. — Vol. 37. — P. 997–1001.
37. Engel A.F., Kamm M.A., Sultan A.H. et al. Anterior anal sphincter repair in patients with obstetric trauma // Br. J. Surg. — 1994. — Vol. 81. — P. 1231–1234.
38. Findlay J.M., Maxwell-Armstrong C. Posterior tibial nerve stimulation and faecal incontinence: a review // Int. J. Colorectal Dis. — 2011. — Vol. 26, N 3. — P. 265–273.
39. Fleshman J.W., Peters W.R., Shemesh E.I. et al. Anal sphincter reconstruction anterior overlappingmuscle repair // Dis. Colon Rectum. — 1991. — Vol. 34. — P. 739–743.
40. Fleshner P.R., Roberts P.L. Encirclement procedures for fecal incjntinence // Perspect. Colon Rectal Surg. — 1991. — Vol. 4. — P. 280–297.
41. Ganio E., Ratto C., Masin A. et al. Neuromodulation for fecal incontinence: outcome in 16 patients with definitive implant. The initial Italian Sacral Neurostimulation Group experience // Dis. Colon Rectum. — 2001. — Vol. 44. — P. 965–970.
42. George A.T., Kalmar K., Sala S. et al. Randomized controlled trial of
percutaneous versus transcutaneous posterior tibial nerve stimulation in faecal incontinence // Br. J. Surg. — 2013. — Vol. 100, N 3. — P. 330–338.
43. Giordano P., Renzi A., Efron J. et al. Previous sphincter repair does not affect the outcome of repeat repair // Dis. Colon Rectum. — 2002. — Vol. 45. — P. 635–640.
44. Glasgo S.C, Lowry A. Long-term outcomes of anal sphincter repair for fecal
incontinence: a systematic review // Dis. Colon Rectum. — 2012. — Vol. 55, N 4. — P. 482–490.
45. Govaert B., Pares D., Delgado-Aros S. et al. A prospective multicentre study to investigate percutaneous tibial nerve stimulation for the treatment of faecal incontinence // Colorectal Dis. — 2010. — Vol. 12, N 12. — P. 1236–1241.
46. Guillemot F., Bouche B., Gower-Rousseau C. et al. Biofeedback for the
treatment of fecal incontinence. Long-term clinical results // Dis. Colon Rectum. — 1995. — Vol. 38. — P. 393–397.
47. Halverson A.L., Hull T.L. Long-term outcome of overlapping anal sphincter repair // Dis. Colon Rectum. — 2002. — Vol. 45. — P. 345–348.
48. Heymen S., Jones K.R., Ringel Y. et al. Biofeedback treatment of fecal incontinence: a critical review // Dis. Colon Rectum. — 2001. — Vol. 44. — P. 728–736.
49. Thaha M.A., Allison M.E., Scott M., Chan C.L. Percutaneous tibial nerve stimulation in females with faecal incontinence: the impact of sphincter morphology and rectal sensation on the clinical outcome // Int. J. Colorectal Dis. — 2012. — Vol. 27, N 7. — P. 927–930.
50. Jacobs P.P., Scheuer M., Kuijpers J.H., Vingerhotts M.H. Obstetric fecal
incontinence. Role of pelvic floor denervation and results of delayed sphincter repair // Dis. Colon Rectum. — 1990. — Vol. 33. — P. 494–497.
51. Melenhorst J., Koch S.M., Wim G. et al. The artificial bowel sphincter for faecal incontinence: a single centre study // Int. J. Colorectal Dis. — 2008. — Vol. 23, N 1. — P. 107–111.
52. Jensen L., Lowry A. Biofeedback improves functional outcome after
sphincteroplasty // Dis. Colon Rectum. — 1997. — Vol. 40. — P. 197–200.
53. Karoui S., Savoye-Collet C., Koning E. et al. Prevalence of anal sphincter defects revealed by sonography in 335 incontinent patients and 115 continent patients // AJR Am. J. Roentgenol. — 1999. — Vol. 173. — P. 389–392.
54. Kenefick N.J., Vaizey C.J., Cohen R.C. et al. Medium-term results of permanent sacral nerve stimulation for faecal incontinence // Br. J. Surg. — 2002. — Vol. 89. — P. 896–901.
55. Kim J., Shim M.C., Choi B.Y. et al. Clinical application of continent anal plug
in bedridden patients with intractable diarrhea // Dis. Colon Rectum. — 2001. — Vol. 44. — P. 1162–1167.
56. King J.C, Currie D.M., Wright E. Bowel training in spina bifida: importance of education, patient compliance, age and anal reflexes // Arch. Phys. Med. Rehabil. — 1994. — Vol. 75. — P. 243–247.
57. Kirk P.M., King R.B., Temple R. et al. Long-term follow-up of bowel management after spinal cord injury // SCI Nurs. — 1997. — Vol. 14. — P. 56–63.
58. Koch S.M., Uludag O., Rongen M. et al. Dynamic graciloplasty in patients 5 with an anorectal malformation // Dis. Colon Rectum. — 2004. — Vol. 47. — P. 1711–1719.
59. Kong F., Li F., Liu J. et al. Gluteus maximus transplantation for fecal
incontinence after surgery of high anal atresia // Zhorgguo Xiu Fu Chong Jian Nai Ke Za Zhi. — 2012. — Vol. 26, N 5. — P. 571–575.
60. Laalim S.A., Hrora A., Raiss M. et al. La réparation sphinctérienne directe: points techniques, indications et résultats // Pan Afr. Med. J. — 2013. — Vol. 14. — P. 11.
61. Madoff R.D., Rosen H.R., Baeten C.G. et al. Safety and efficacy of dynamic
muscle plasty for anal incontinence: lessons from a prospective, multicenter trial // Gastroenterology. — 1999. — Vol. 116, N 3. — P. 549–556.
62. Malouf A.J., Norton C.S., Engel A.F. et al. Long-term results of overlapping anterior anal sphincter repair for obstetric trauma // Lancet. — 2000. — Vol. 355. — P. 260–265.
63. Malouf A.J., Vaizey C.J., Nicholls R.J., Kamm M.A. Permanent sacral nerve
stimulation for faecal incontinence // Ann. Surg. — 2000. — Vol. 232. — P. 143– 148.
64. Maslekar S., Smith K., Harji D. et al. Injectable collagen for the treatment of fecal incontinence: long-term results // Dis. Colon Rectum. — 2013. — Vol. 56, N 3. — P. 354–359.
65. Matzel K., Kamm M.A., Stösser M. et al. MDT 301 StudyGroup. Sacral nerve
stimulation for faecal incontinence: a multicenter study // Lancet. — 2004. — Vol. 363. — P. 1270–1276.
66. Michot F., Costaglioli B., Leroi A.M., Denis P. Artificial anal sphincter in severe fecal incontinence: outcome of prospective experience with 37 patients in one institution // Ann. Surg. — 2003. — Vol. 237, N 1. — P. 52–56.
67. Musial F., Hinninghofen H., Frieling T., Enck P. Therapy of fecal incontinence
in elderly patients: study of a home biofeedback training program // Z. Gerontol. Geriatr. — 2000. — Vol. 33. — P. 447–453.
68. Norderval S., Oian P., Revhaug A., Vonen B. Anal incontinence after obstetric sphincter tears: outcome of anatomic primary repairs // Dis. Colon Rectum. — 2005. — Vol. 48. — P. 1055–1061.
69. Norton C., Chelvanayagam S., Wilson-Barnett J. et al. Randomized controlled
trial of biofeedback for fecal incontinence // Gastroenterology. — 2003. — Vol. 125. — P. 1320–1329.
70. Norton C., Codi J.D. Biofeedback and/or sphincter exercises for the treatment of faecal incontinence in adults // Cochrane Database Syst. Rev. — 2012. — URL: http://www.nice.org.uk/nicemedia/pdf/CG49FullGuideline.pdf.
71. Norton C., Kamm M.A. Anal plug for fecal incontinence // Colorectal Dis. —
2001. — Vol. 3. — P. 323–327.
72. OCEBM Levels of Evidence Working Group. The Oxford 2011 Levels of Evidence. — Oxford Centre for Evidence-Based Medicine, 2011.
73. Osterberg A., Eeg-Olofsson E.K., Graf W. Results of surgical treatment for faecal incontinence // Br. J. Surg. — 2000. — Vol. 87. — P. 1546–1552.
74. Pager C.K., Solomon M.J., Rex J., Roberts R.A. Long-term outcomes of pelvic floor exercise and biofeedback treatment for patients with fecal incontinence // Dis. Colon Rectum. — 2002. — Vol. 45. — P. 997–1003.
75. Palmer K.R., Corbett C.L., Holdsworth C.D. Double-blind cross-over study
comparing loperamide, codeine and diphenoxylate in the treatment of chronic diarrhea // Gastroenterology. — 1980. — Vol. 79. — P. 1272–1275.
76. Parks A.G. Anorectal incontinence // Proc. R. Soc. Med. — 1975. — Vol. 68. — P. 683–687.
77. Pecl C., Seidl H., Scalercio N. et al. Accuracy of anorectal manometry in patients with fecal incontinence // Digestion. — 2012. — Vol. 86, N 2. — P. 78–85.
78. Peticca L., Pietroletti R., Ayabaca S.M., Pescatori M. Combined biofeedback, physiotherapy and electrostimulation for fecal incontinence // Tech. Coloproctol. — 2000. — Vol. 4. — P. 157–161.
79. Pickrell K.L., Georgiade N., Richard E.F., Morris F. Gracilis muscle transplant
for the correction of neurogenic rectal incontinence // Surg. Clin. North Am. — 1959. — Vol. 39. — P. 1405–1415.
80. Pinho M., Ortiz J., Oya M. et al. Total pelvic floor repair for treatment of neuropathic faecal incontinence // Am. J. Surg. — 1992. — Vol. 163. — P. 340–343.
81. Pinta T., Kylanpaa-Back M.L., Salmi T. et al. Delayed sphincter repair for obstetric ruptures: analysis of failure // Colorectal Dis. — 2003. — Vol. 5. — P. 73–78.
82. Rasmussen O.O., Buntzen S., Sorensen M. et al. Sacral nerve stimulation in
fecal incontinence // Dis. Colon Rectum. — 2004. — Vol. 47. — P. 1158–1162.
83. Ratto C., Grillo E., Parello A. et al. Sacral neuromodulation in treatment of fecal incontinence following anterior resection and chemoradiation for rectal cancer // Dis. Colon Rectum. — 2005. — Vol. 48. — P. 1027–1036.
84. Rosen H., Urbarz C., Holzer B. et al. Sacral nerve stimulation as a treatment for faecal incontinence // Gastroenterology. — 2001. — Vol. 121. — P. 536–541.
85. Ryn A.K., Morren G.L., Hallbook O., Sjodahl R. Long-term results of electromyographic biofeedback training for fecal incontinence // Dis. Colon Rectum. — 2000. — Vol. 43. — P. 1262–1266.
86. Sielezneff F., Bauer S., Bulgare J.C., Sarles J.C. Gracilis muscle transposition
in the treatment of fecal incontinence // Int. J. Colorectal Dis. — 1996. — Vol. 11. — P. 15–18.
87. Sitzler P.J., Thompson J.P. Overlap repair of damaged anal sphincter. A single surgeons series // Dis. Colon Rectum. — 1996. — Vol. 39. — P. 1356–1360.
88. Staff A., Laine K. Many sphincter injuries are preventable // Tidsskr. Nor. Laegeforen. — 2012. — Vol. 132, N 21. — P. 2364–2365.
89. Sultan A.H., Kamm M.A., Talbot I.C. et al. Anal endosonography for identifying external sphincter defects confirmed histologically // Br. J. Surg. — 1994. — Vol. 81. — P. 463–465.
90. Sultan A.H., Nicholls R.J., Kamm M.A. et al. Anal endosonography and
correlation with in vitro and in vivo anatomy // Br. J. Surg. — 1993. — Vol. 80. — P. 508–511.
91. Tjandra J.J., Chan M.K., Yeh H.C. Injectable silicone biomaterial (PTQ) is more effective than carbon-coated beads (Durasphere) in treating passive faecal
incontinence-a randomized trial // Colorectal Dis. — 2009. — Vol. 11, N 4. — P. 382–389.
92. Tjandra J.J., Han W.R., Goh J. et al. Direct repair vs. overlapping sphincter repair: A randomized controlled trial // Dis. Colon Rectum. — 2003. — Vol. 46. — P. 937–943.
93. Tjandra J.J., Lim J.F., Hiscock R., Rajendra P. Injectable silicone biomaterial for fecal incontinence due to internal anal sphincter dysfunction is effective // Dis. Colon Rectum. — 2004. — Vol. 47. — P. 2138–2146.
94. Tjandra J.J., Lim J.F., Matzel K. Sacral nerve stimulation: an emerging treatment for faecal incontinence // Aust. N. Z. Surg. J. — 2004. — Vol. 74. — P. 1098–1106.
95. Vaizey C.J., Norton C., Thornton M.J. et al. Long-term results of repeat anterior anal sphincter repair // Dis. Colon Rectum. — 2004. — Vol. 47. — P. 858– 863.
96. Vergara-Fernandes O., Valdovinos-Diaz M.A., Hagerman-Ruis G. et al. Improvement of fecal incontinence with silicone implants in patients with internal anal sphincter injury: First report in North America // Rev. Gastroenterol. Mex. — 2011. — Vol. 76, N 4. — P. 384–388.
97. Vitton V., Damon H., Roman S., Mion F. Transcutaneous electrical posterior tibial nerve stimulation for faecal incontinence: effects on symptoms and quality of life // Int. J. Colorectal Dis. — 2010. — Vol. 25, N 8. — P. 1017–1020.
98. Wexner S.D., Jorge J.M. Etiology and management of fecal incontinence // Dis. Colon Rectum. — 1993. — Vol. 36, N 1. — P. 77–97.
99. Whitehead W.E., Wald A., Norton N.J. Treatment options for fecal incontinence // Dis. Colon Rectum. — 2001. — Vol. 44, N 1. — P. 131–144.
100. Wong M.T., Meurette G., Wyart V. et al. The artificial bowel sphincter: a single institution experience over a decade // Ann. Surg. — 2011. — Vol. 254, N 6. — P. 951–956.
101. Wong W.D., Congliosi S.M., Spencer M.P. et al. The safety and efficacy of the artificial bowel sphincter for fecal incontinence: results from a multicenter cohort study // Dis. Colon Rectum. — 2002. — Vol. 45. — P. 1139–1153.
102. Zorcolo L., Covotta L., Bartolo D.C. Outcome of anterior sphincter repair for obstetric injury: comparison of early and late results // Dis. Colon Rectum. — 2005. — Vol. 48. — P. 524–531.
Приложение к рекомендациям по диагностике и лечению взрослых с недостаточностью анального сфинктера
Таблица 10.6. Комплекс упражнений лечебно-физкультурного комплекса
|
I. Исходное положение: лежа на спине, руки вдоль туловища | ||
|
|
Сжимание ягодиц с одновременным втягиванием сфинктера |
30 раз |
|
|
Поочередное втягивание прямых ног в тазобедренные суставы |
По 15 раз каждую ногу |
|
|
Дыхательное упражнение: вдох выдох |
2–3 раза |
|
|
Положение «полумост» (в верхней точке максимально сжать ягодицы и втянуть сфинктер) |
10–15 раз |
|
|
Сжимание мяча |
2 раза по 15 с. Отдых 1 мин |
|
|
Дыхательное упражнение: вдох выдох |
2–3 раза |
|
II. Исходное положение: лежа на боку, нижняя рука под головой, нижняя нога согнута в колене, верхняя рука в упоре перед грудью | ||
|
|
Поднимание ноги |
10–15 раз |
|
|
Сгибание ноги вперед с последующим отведением ее назад |
10–15 раз |
|
|
Дыхательное упражнение: вдох выдох |
2–3 раза |
![]()
![]()
![]() Табл. 10.6. Окончание
Табл. 10.6. Окончание
|
|
Одновременное поднимание двух ног |
10–15 раз |
|
III. Исходное положение: лежа на другом боку. Повторение упражнений | ||
|
IV. Исходное положение: лежа на животе, руки под подбородок, ноги прямые | ||
|
|
Поочередное поднимание прямых ног |
По 15 раз каждой ногой |
|
|
Поочередное сгибание ног к животу «по-пластунски» (колено не касается мата) |
По 10–15 раз каждой ногой |
|
|
Дыхательное упражнение: вдох выдох |
2–3 раза |
|
|
Одновременное поднимание двух ног |
10–15 раз |
ОСТРОКОНЕЧНЫЕ КОНДИЛОМЫ ПЕРИАНАЛЬНОЙ ОБЛАСТИ
И АНАЛЬНОГО КАНАЛА
Введение
По данным ВОЗ, аногенитальная папилломавирусная инфекция человека в настоящее время является одним из наиболее распространенных вирусных заболеваний, передаваемых половым путем (УД 3а, СР В [2, 13, 19, 21, 22, 24, 28, 39, 49, 67, 75, 86, 112]). Вирусом папилломы человека (ВПЧ) инфицировано 9–15% населения (~630 млн человек), при этом распространенность папилломавирусной инфекции в мире продолжает неуклонно расти — ежегодно в мире выявляется до 30 млн новых случаев болезни (УД 3а, СР В [1, 4, 17, 20, 30, 75]). Принципы лечения и особенно дальнейшего наблюдения пациентов, страдающих ВПЧ, отличаются от принципов лечения и наблюдения остальных инфекций, передаваемых половым путем, так как ВПЧ относится к вирусам, способным инициировать развитие злокачественных процессов (УД 3а, СР В [16, 19, 26, 41, 42, 44, 51, 52, 55, 56, 62, 77, 90, 100, 105]).
В Российской Федерации также отмечается устойчивый рост заболеваемости. При этом наиболее уязвимой категорией населения являются молодые люди от 18 до 19 лет, среди которых регистрируются высокие интенсивные показатели заболеваемости аногенитальными бородавками, составляющие в общей структуре инфекции, передаваемой половым путем, 55–65% (УД 3а, СР В [17, 30, 75]).
Рекомендации по диагностике и лечению пациентов с остроконечными кондиломами служат руководством для практических врачей, осуществляющих ведение и лечение таких больных, и подлежат регулярному пересмотру в соответствии с новыми данными научных исследований в этой области.
Рекомендации включают следующие разделы: определение заболевания, классификация по МКБ-10, профилактика, диагностика, консервативное и оперативное лечение, правила ведения периоперационного периода, а также прогноз у оперированных больных.
Данные рекомендации составлены на основании анализа литературы из базы данных PubMed, MEDLINE, Cochrane Collaboration, the
Standards Practice Task Force of the American Society of Colon and Rectal Surgeon, Oxford Center for Evidence-based Medicine — Levels of Evidence. Рекомендации сопровождаются пояснениями об уровне доказательности отдельных положений согласно рекомендациям Оксфордского центра доказательной медицины (табл. 11.1) [73, 88]. В зависимости от достоверности приводимых данных рекомендации разделены на степени A, B, C, D.
Таблица 11.1. Уровни доказательности и степени рекомендаций на основании руководства Оксфордского центра доказательной медицины
|
Уровень |
Исследования методов диагностики |
Исследования методов лечения |
|
1а |
Систематический обзор гомогенных диагностических исследований 1-го уровня |
Систематический обзор гомогенных РКИ |
|
1b |
Валидизирующее когортное исследование с качественным «золотым стандартом» |
Отдельное РКИ (с узким доверительным интервалом) |
|
1с |
Специфичность или чувствительность столь высокие, что положительный или отрицательный результат позволяет исключить/ установить диагноз |
Исследование «Всё или ничего» |
|
2а |
Систематический обзор гомогенных диагностических исследований >2-го уровня |
Систематический обзор (гомогенных) когортных исследований |
|
2b |
Разведочное когортное исследование с качественным «золотым стандартом» |
Отдельное когортное исследование (включая РКИ низкого качества; т.е. с <80% пациентов, прошедших контрольное наблюдение) |
|
2с |
Нет |
Исследование «исходов»; экологические исследования |
|
За |
Систематический обзор гомогенных исследований уровня 3b и выше |
Систематический обзор гомогенных исследований «случай– контроль» |
|
3b |
Исследование с непоследовательным набором или без проведения исследования «золотого стандарта» у всех испытуемых |
Отдельное исследование «случай–контроль» |
|
4 |
Исследование «случай–контроль» или исследование с некачественным или независимым «золотым стандартом» |
Серия случаев (и когортные исследования или исследования «случай–контроль» низкого качества) |
|
5 |
Мнение экспертов без тщательной критической оценки или основанное на физиологии, лабораторных исследованиях на животных или разработка «первых принципов» |
Мнение экспертов без тщательной критической оценки, лабораторные исследования на животных или разработка «первых принципов» |
Табл. 11.1. Окончание
|
Уровень |
Исследования методов диагностики |
Исследования методов лечения |
|
Степени рекомендаций | ||
|
A |
Согласующиеся между собой исследования 1-го уровня | |
|
B |
Согласующиеся между собой исследования 2-го или 3-го уровня или экстраполяция на основе исследований 1-го уровня | |
|
C |
Исследования 4-го уровня или экстраполяция на основе уровня 2 или 3 | |
|
D |
Доказательства 5-го уровня или затруднительные для обобщения или некачественные исследования любого уровня | |
ВАЛИДИЗАЦИЯ РЕКОМЕНДАЦИЙ
Настоящие рекомендации в предварительной версии были рецензированы независимыми экспертами, которых попросили прокомментировать прежде всего, насколько интерпретация доказательств, лежащих в основе рекомендаций, доступна для понимания. Получены комментарии со стороны врачей амбулаторного звена. Полученные комментарии тщательно систематизировались и обсуждались на совещаниях экспертной группы.
Последние изменения в настоящих рекомендациях были представлены для дискуссии на заседании профильной комиссии «Колопроктология» Экспертного совета Минздрава России 12 сентября 2013 г. Проект рекомендаций был повторно рецензирован независимыми экспертами и врачами амбулаторного звена. Для окончательной редакции и контроля качества рекомендации были повторно проанализированы членами экспертной группы, которые пришли к заключению, что все замечания и комментарии приняты во внимание, риск систематических ошибок при разработке рекомендаций сведен к минимуму.
ОБЛАСТЬ ПРИМЕНЕНИЯ РЕКОМЕНДАЦИЙ
Данные клинические рекомендации применимы при осуществлении медицинской деятельности в рамках Порядка оказания медицинской помощи взрослому населению с заболеваниями толстой кишки, анального канала и промежности колопроктологического профиля.
Определение [1–4, 13, 17, 24]
Аногенитальные бородавки — вирусное заболевание, обусловленное ВПЧ и характеризуемое появлением экзофитных и эндофитных фиброэпителиальных разрастаний на коже и слизистых оболочках наружных половых органов, уретры, шейки матки, перианальной области и анального канала.
Возбудитель — ВПЧ, мелкий вирус, содержащий двунитевую ДНК (УД la, СР А [3, 24, 53, 81, 89]). Типы ВПЧ высокого онкогенного риска —
16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59, 68: вирусы низкого онкогенного
риска — 6, 11, 42–44 (УД 1a, СР A [2, 14, 20, 24, 31, 53, 80, 81, 108, 114]).
Пути инфицирования: половой контакт (УД 1а, СР А [1, 2, 6, 19, 24, 26,
51, 59, 62, 81, 83, 99, 111]); трансплацентарный (УД 1b, СР A [54, 104]); перинатальный; контактно-бытовой (при этом возможность аутоинокуляции и передачи ВПЧ через бытовые предметы остается недостаточно изученной) (УД 3b, СР C [1, 5, 13, 28, 97, 98]).
Код по Международной классификации болезней 10-го пересмотра
n Класс: Некоторые инфекционные и паразитарные болезни.
n Блок: Инфекции, передаваемые преимущественно половым путем.
n Код: A63.0.
n Название: Аногенитальные (венерические) бородавки.
Классификация (УД 3b, СР C [2, 4, 14, 25, 28,
66, 80, 91, 94, 95, 109, 112])
n Остроконечные кондиломы.
n Бородавки в виде папул.
n Поражения в виде пятен.
n Внутриэпителиальная неоплазия.
n Бовеноидный папулез и болезнь Боуэна.
n Гигантская кондилома Бушке–Левенштейна.
Профилактика
Профилактика (УД 3а, СР А [1, 3, 13, 24, 28, 39]) ВПЧ включает ряд общих для всех инфекций, передаваемых половым путем, мероприятий. Современные профилактические мероприятия включают как обучение, так и изменение мотиваций и поведения. В целом профилактическую работу подразделяют на первичную и вторичную.
Первичная профилактика предполагает осуществление теоретически обоснованных вмешательств, направленных на изменение моделей поведения в популяциях высокого риска для предотвращения заражения. В настоящее время профилактические мероприятия, проводимые в обществе, включают в основном медико-санитарную пропаганду сексуального здоровья и информирование населения на страницах периодической печати, в средствах массовой информации, школах и других учебных заведениях, а также в лечебных учреждениях. Население должно знать особенности ранних и поздних клинических проявлений инфекций, пути заражения, способы их профилактики. Немаловажно информирование о местах приобретения средств индивидуальной про-
филактики. Кроме того, профилактические программы должны предусматривать отказ от самолечения и непрофессионального лечения в случаях подозрения заражения.
Вторичная профилактика направлена на пациентов с диагностированными инфекциями, передаваемыми половым путем, для снижения вероятности передачи инфекции партнерам во время «заразного» периода при половом контакте. Вторичная профилактика должна быть нацелена на снижение риска повторного заражения среди больных и уже переболевших людей.
Вакцинация. В настоящее время имеется информация о результатах испытаний двух вакцин: бивалентной (вакцина против вируса папилломы человека, направленная против типов 16 и 18 ВПЧ), и квадривалентной [(вакцина против вируса папилломы человека квадривалентная рекомбинантная, направленная против четырех типов ВПЧ (6, 11, 16, 18)], которая в 2006 г. зарегистрирована и разрешена к применению в Российской Федерации у девочек и мальчиков до начала половой жизни, начиная с 9 лет. Эта вакцина внесена в Национальные календари вакцинации подростков США, Австралии и большинства стран Евросоюза. В конце 2007 г. на международных конгрессах были впервые представлены данные о том, что гардасил♠ обладает не только 99% эффективностью в отношении четырех типов ВПЧ, но и перекрестной защитой в отношении еще 10 онкогенных типов ВПЧ, не входящих в состав вакцины. В исследованиях подтверждена ее эффективность на протяжении уже более 5 лет (УД 1 а, СР А [27, 57, 60, 65, 68, 69, 76, 96]).
Скрининг
Женщины с патологией шейки матки (УД 3b, СР C [28, 31–34, 51, 54, 95]). Лица с выявленными инфекциями, передаваемыми половым путем (УД 3b, СР C [13, 19, 24, 28, 67]).
Формулировка диагноза
При формулировании диагноза следует отразить форму заболевания и пораженную анатомическую область. Ниже приведены примеры формулировок диагноза.
n Остроконечные кондиломы перианальной области и анального канала.
n Гигантская кондилома Бушке–Левенштейна перианальной области.
Диагностика
КЛИНИЧЕСКИЕ ДИАГНОСТИЧЕСКИЕ КРИТЕРИИ
К основным клиническим симптомам остроконечных кондилом относится наличие патологических разрастаний в перианальной области,
области промежности и половых органах. Также часто наблюдается клиническая симптоматика поражения анального канала (зуд, боль при дефекации, патологические выделения из анального канала).
УСТАНОВЛЕНИЕ ДИАГНОЗА
Диагноз выставляется на основании сочетания данных анамнеза, клинической картины и данных инструментальных методов обследования.
Обязательные методы исследования при выявлении остроконечных кондилом перианальной области
Клинические методы
При сборе анамнеза определяются:
n факторы риска развития заболевания: проституция; многочисленные и случайные сексуальные связи; гомосексуализм; редкое использование барьерных методов контрацепции и спермицидов;
n давность возникновения образований, выявление тенденции к прогрессированию и клинической трансформации образований;
n при первичном эпизоде аногенитальных бородавок — предполагаемый источник инфицирования пациента и время, прошедшее с момента сексуального контакта с предполагаемым источником инфицирования до появления субъективных симптомов;
n при рецидиве заболевания — частота рецидивов, время последнего рецидива заболевания, методы деструкции высыпаний в анамнезе;
n результаты обследования половых партнеров;
n данные акушерско-гинекологического, урологического и полового анамнеза;
n наличие инфекций, передаваемых половым путем, в анамнезе и настоящее время.
Субъективные симптомы (жалобы):
n наличие фиброэпителиальных одиночных или множественных образований с тонкой ножкой или широким основанием в виде папул, папиллом, образований в виде «цветной капусты», «петушиного гребня» или пятен, локализующихся в перианальной области и анальном канале, на кожных покровах паховой области, промежности, а также:
v у мужчин — на головке полового члена, венечной борозде, уздечке полового члена, внутреннем листке крайней плоти, теле полового члена, коже мошонки;
v у женщин — на уздечке половых губ, клиторе, наружном отверстии уретры, в преддверии влагалища, на больших и малых половых губах, слизистой оболочке влагалища, шейке матки, девственной плеве;
n зуд, парестезии в области поражения;
n дискомфорт и боль при дефекации;
n мокнутие и кровоточивость кожных покровов и слизистых оболочек в местах поражения;
n диспареуния (болезненность во время полового акта);
n при локализации высыпаний в области уретры — дизурия (зуд, жжение, болезненность при мочеиспускании).
Осмотр больного. Проводят на гинекологическом кресле в положении, как для литотомии. При этом оценивают состояние наружных половых органов, области промежности и перианальной области. Оценивают площадь поражения, состояние и площадь здоровых тканей между очагами поражения. При пальпации определяют консистенцию образований и состояние их основания. При осмотре могут выявляться следующие типы поражений слизистой оболочки и кожных покровов аногенитальной области (УД 3а, СР А [1–4, 12, 13, 21, 22, 29, 31, 44, 45, 49, 52, 63, 74,
91, 101, 106]).
n Остроконечные кондиломы — пальцеобразные выпячивания с хорошо васкуляризованными участками на поверхности кожных покровов и слизистых оболочек, имеющие типичный «пестрый» и/или
«петлеобразный» рисунок и локализующиеся на коже паховой области, промежности, перианальной области, слизистой оболочке анального канала, наружного отверстия мочеиспускательного канала, малых и больших половых губ, входа во влагалище, влагалища, шейки матки.
n Бородавки в виде папул — папулезные высыпания без пальцеобразных выпячиваний, локализуемые на кератинизированном эпителии (наружный листок крайней плоти, тело полового члена, мошонка, латеральная область вульвы, лобок, промежность и перианальная область).
n Поражения в виде пятен — серовато-белые, розовато-красные или красновато-коричневые пятна на слизистой оболочке половых органов.
n Бовеноидный папулез и болезнь Боуэна — папулы и пятна с гладкой бархатистой поверхностью; цвет элементов в местах поражения слизистой оболочки — бурый или оранжево-красный, а поражений на коже — пепельно-серый или коричневато-черный.
n Гигантская кондилома Бушке–Левенштейна — бородавчатоподобные элементы типа папиллом, сливающиеся между собой и образующие очаг поражения с широким основанием, инфильтрирующим подлежащие ткани.
У женщин обязательны вагинальное исследование и осмотр шейки матки. Определяется наличие образований во влагалище и шейке матки, заинтересованность окружающих тканей.
Пальцевое исследование прямой кишки. Определяются наличие и площадь поражения стенок анального канала, вовлеченность в процесс окружающих тканей и мышц анального сфинктера, оценивается состояние зубчатой линии.
Обязательные инструментальные методы
Аноскопия. Осматривают зону аноректальной линии, нижнеампулярный отдел прямой кишки, оценивают состояние стенок анального канала, визуализируют площадь и характер поражения.
Ректороманоскопия. Осматривают слизистую оболочку прямой кишки и дистального отдела сигмовидной кишки. Оценивают характер сосудистого рисунка, наличие воспалительных изменений в дистальном отделе толстой кишки.
Кольпоскопия (у женщин). Оценивается состояние стенок влагалища, шейки матки.
Лабораторные исследования
n Постановка комплекса серологических реакций на сифилис.
n Определение антител к вирусу иммунодефицита человека (ВИЧ), гепатиту В и С.
n Молекулярно-биологические методы диагностики: полимеразная цепная реакция (ПЦР в реальном времени, ПЦР с использованием гибридной ловушки) или ВПЧ Digene-тест с типированием онкогенных и неонкогенных типов (УД 1a, СР A [2, 8, 16, 17, 22, 34, 60, 64, 78, 81, 91, 84]).
n Цитологическое исследование цервикальных мазков (УД 3a, СР B [22, 24, 30, 81]).
n Цитологическое исследование мазков-отпечатков (УД 3a, СР B [17, 22, 35, 37, 81]).
n Гистологическое исследование биопсийного материала (при подозрении на малигнизацию) (УД 3a, СР B [28, 39, 64, 81, 82, 93]).
n Гистологическое исследование удаленных образований (УД 3a, СР B [28, 39, 60]).
Дополнительные исследования
n Определение иммунного статуса при наличии иммунодефицитных состояний и частом рецидивировании заболевания (УД 1a, СР A [3, 4, 6, 8, 10, 17, 22, 28, 29, 31, 32, 38, 40, 46–48]).
n Колоноскопия при кровянистых выделениях из заднего прохода и подозрении на малигнизацию процесса (УД 4, СР D [6, 8, 12, 22, 49]).
n Ультразвуковое обследование ректальным и вагинальным датчиками при клинических признаках инвазии образований в окружающие ткани, больших размерах образований, подозрении на малигнизацию (УД a, СР B [8, 21, 22, 42, 45, 51]).
n Ультразвуковое обследование брюшной полости и малого таза при подозрении на малигнизацию и генерализацию процесса (УД 4, СР D [6, 8, 12, 22, 49]).
n Консультация гинеколога, вагиноскопия и кольпоскопия (УД 4, СР D [2, 3, 4, 6, 13, 21, 22, 24, 26, 30, 37]).
n Консультация уролога, уретроскопия при поражении уретры (УД 4, СР D [1, 4, 5, 21, 23]).
n Консультация онколога и радиолога при малигнизации процесса (УД 4, СР D [8, 16, 19, 22, 51, 52, 55, 56, 62, 64, 77, 90, 100, 105]).
n Исследования на другие инфекции, передаваемые половым путем (УД 4, СР D [1, 3, 4, 13, 24]).
ДИФФЕРЕНЦИАЛЬНАЯ ДИАГНОСТИКА (УД 4, СР D [1, 4, 8, 13, 21, 24, 28])
n Сифилис.
n Контагиозный моллюск.
n Жемчужные папулы полового члена.
n Себорейный кератоз.
n Интрадермальный невус.
n Микропапилломатоз половых губ и вульвы (физиологический вариант, представляющий собой несливающиеся папулы правильной формы,
расположенные симметрично на внутренней поверхности малых половых губ и в области преддверия влагалища).
Для визуальной дифференциации аногенитальных бородавок возможно проведение пробы с уксусной кислотой или распыление жидкого азота. После обработки 5% раствором уксусной кислоты или распыления жидкого азота поражения, вызванные ВПЧ, на несколько минут становятся серовато-белыми с характерным капиллярным рисунком.
Лечение
Цели лечения:
n коррекция иммунного статуса;
n удаление кондиломатозных разрастаний;
n предупреждение развития осложнений и малигнизации образований;
n улучшение качества жизни пациентов.
Показания к проведению лечения и госпитализации:
n показание к проведению лечения — наличие аногенитальных бородавок;
n показание к госпитализации — неэффективность консервативной терапии, невозможность деструкции образований в амбулаторных условиях, подозрение на малигнизацию.
МЕДИКАМЕНТОЗНОЕ ЛЕЧЕНИЕ
У всех больных кондиломами анального канала и перианальной области имеется нарушение интерферонового статуса (УД 3a, СР С [3, 8, 11, 22, 24, 29, 32, 38, 46, 61, 63, 70, 82, 87, 92, 108, 113]. Соответственно
лечение больных должно начинаться с коррекции иммунных нарушений (УД 3a, СР С [32, 36, 38, 48, 70, 92, 114]). После проведения местной иммуномодулирующей терапии выздоровление больных при небольших размерах и единичном характере образований отмечается в 72–84% наблюдений (УД, СР B [8, 10, 22, 23, 49, 66, 70, 112]).
Ниже приведены схемы иммуномодулирующего лечения.
n Ректальные суппозитории генферон по 1 млн ЕД 2 раза в день в течение 10 дней.
n Мазь панавир (полисахариды побегов Solanum Tuberosum) местно 5 раз в день в течение 10 дней.
ХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕ
Показания. Наличие остроконечных кондилом и неэффективность медикаментозного лечения служат показанием к их деструкции.
Методы деструкции
Химические методы. Препараты для химической деструкции: комбинированный кислотный препарат солкодерм, фенол (ферезол♠), трихлоруксусная кислота.
Препарат солкодерм является кератолитическим средством, состоящим из азотной (70%) и других неорганических и органических кислот.
Применяют его с помощью специальных аппликаторов. Солкодерм быстро проникает в пораженную ткань и мумифицирует ее. Препарат эффективен при единичных кондиломах небольших размеров, частота рецидивов после его применения составляет 12,5% (УД 5; СР D [9, 15,
22, 24]).
Ферезол♠ представляет собой смесь фенола (60%) и трикрезола (40%) и предназначен для поражений, локализующихся только на коже, его применение в анальном канале недопустимо. Применение препарата целесообразно при единичных образованиях небольших размеров (УД 5; СР D [30]).
Трихлоруксусная кислота является слабым деструктивным химическим препаратом, вызывающим образование локального коагуляционного некроза, применяется в концентрации 80–90%. Она используется при поражениях любой локализации, однако эффективна в отношении единичных кондилом небольших размеров (УД 5; СР D [22, 39, 49, 66]).
Цитотоксические методы. Цитотоксические препараты — подофиллинà и подофиллотоксин, выделенные из корней растения мандрагора или подофила щитовидного. Для лечения больных экзофитными кондиломами применяют раствор или мазь подофиллинаÃ, которую наносят на поверхность патологического элемента, защищая неповрежденную кожу, а затем через 4–6 ч смывают. Подофиллинà не разрешен для самостоятельного применения пациентом, кроме того, является тератогенным. Возврат заболевания после его применения отмечен в 30–70% случаев (УД 3b, СР C [2, 28, 49, 66, 112]). Подофиллотоксин представляет собой наиболее активную в терапевтическом отношении фракцию в составе подофиллинаÃ. Подофиллотоксин в Российской Федерации разрешен к медицинскому применению под торговым названием кондилин♠. Препарат более безопасен, чем подофиллинÃ, и может самостоятельно использоваться пациентами при нанесении его в доступных для больного зонах. Частота рецидивов после применения подофиллотоксина составляет 31–68% (УД 3b, СР C [13, 14, 28, 39]).
При применении подофиллинаà и подофиллотоксина в 20% наблюдений развиваются местные воспалительные реакции, эритема, жжение, болезненность, зуд, незначительное мокнутие и эрозии в области аппликации, поэтому эти препараты не рекомендованы для деструкции кондилом, локализующихся в анальном канале и во влагалище (УД 3b; СР C [22, 24, 66]). Также препараты не предназначены для обработки большой площади поражения (УД 3b; СР C [2, 14, 22, 49, 112]).
Методика нанесения препаратов для цитотоксической и химической деструкции на пораженную область. Больного укладывают на гинекологическое кресло. При локализации патологического процесса на пери-
анальной коже дополнительного оборудования не требуется. Используются специальные аппликаторы, поставляющиеся вместе с препаратом.
При поражении анального канала1 в прямую кишку вводят операционный аноскоп с осветителем. Постепенно выводя аноскоп из кишки, останавливаются при появлении в его просвете патологического участка. Препарат наносят на этот участок с помощью специального аппликатора после обработки спиртом. Для исключения побочных эффектов одномоментно обрабатывается площадь патологического участка, не превышающая 1 см. При использовании препарата солкодерм♠ экспозицию проводят до возникновения равномерного желтого окрашивания патологического очага. Через 3–4 мин после нанесения солкодерма♠ папилломатозные образования приобретают беловато-серое окрашивание и постепенно превращаются в серо-желтую аморфную массу, представляющую собой тканевый детрит, безболезненно и бескровно отторгающийся на 3–5-й день. Контрольный осмотр и следующий этап лечения препаратами для цитотоксической и химической деструкции показаны через 6–8 дней.
Физические методы (хирургическое иссечение (острым путем, электрокоагуляция, радиохирургия), лазерная вапоризация, криодеструкция). Основной метод лечения кондилом различных локализаций — хирургическое иссечение (острым путем, электрокоагуляция, радиоволновая хирургия). Метод может использоваться при любой локализации образований и площади поражения.
Методика. При аногенитальной локализации операция выполняется под спинальной анестезией. Используется стандартный набор хирургических инструментов, монополярный электрокоагулятор со стандартными насадками либо аппарат «Сургитрон». Частота возникновения рецидивов заболевания после иссечения кондилом составляет 28–51% (УД 3b, СР C [1, 6, 8, 12, 22, 80, 112]). Использование углеводородного лазера по эффективности приближается к иссечению кондилом с помощью электрокоагуляции (УД 3b, СР С [7, 23, 80]). В связи с высокой температурой происходит чрезвычайно быстрое испарение тканевой и внутриклеточной жидкости, а затем сгорание сухого остатка. Отрицательным моментом является отсутствие материала для гистологического исследования (УД 5, СР D [30, 49]).
Криодеструкция используется при любых локализациях кондилом (УД 5, СР D [4, 8, 13]). При этом происходит гибель опухолевых клеток путем образования внеи внутриклеточных кристалликов льда, стаза крови, приводящих к некрозу ткани, а также к гуморальному и клеточному иммунному ответу организма на криовоздействие. Метод наиболее эффективен при единичных, небольших размерах образований (УД 3b, СР C [22, 80, 112]. Возврат заболевания после применения криодеструкции отмечается у 31–40% пациентов (УД 3b, СР C [1, 2, 30, 49, 112].
 |
1 Используются только препараты, разрешенные для применения на слизистых оболочках.
Особенности хирургического иссечения кондилом перианальной области и анального канала (УД 3b, СР C [1, 8, 12, 91, 106])
n Для обеспечения радикальности оперативного вмешательства пора-
женные ткани должны иссекаться с собственной пластиной дермы. При расположении кондилом в анальном канале дном раны должен быть внутренний сфинктер, при расположении на перианальной коже — подкожная клетчатка.
n У больных с опухолью Бушке–Левенштейна необходимо иссекать вовлеченные в процесс ткани, отступив не менее 1 см от основания образования.
n После удаления образований необходимо морфологическое исследование. При наличии данных за малигнизацию процесса показано проведение консилиума с участием онколога и радиолога.
n Пациентам с верифицированным плоскоклеточным раком показано проведение лучевой терапии в специализированном стационаре.
Чего нельзя делать (УД 3b, СР C [1–4, 8, 13, 22,
34, 55, 56, 72, 91])
n Проведение иммуномоделирующей терапии при подозрении на малигнизацию процесса.
n Любые виды деструкции больших образований с плотным основанием без консультации онколога и радиолога.
Послеоперационное ведение (УД 3b, СР C [1–4, 8, 13, 22])
n Все пациенты, оперированные по поводу кондилом перианальной области и анального канала, нуждаются в ежемесячном осмотре в течение 1 года.
n В случае выявления рецидива заболевания: при размерах образований менее 1 см — химическая деструкция; при размерах образований более 1 см — иссечение в пределах здоровых тканей.
n У женщин, инфицированных вирусами высокого онкогенного риска, рекомендуются консультация гинеколога и проведение кольпоскопии и цитологического исследования цервикальных мазков 2 раза в год.
n Половых партнеров пациентов, инфицированных ВПЧ, рекомендуется обследовать, и при обнаружении у них клинических проявлений заболевания провести лечение по схеме.
Прогноз
У пациентов, перенесших только хирургическое лечение, возврат заболевания отмечается до 39% случаев. Проведение комплексного лечения, включающего иммунотерапию и удаление кондилом в сравнении только с хирургическим иссечением, снижает частоту развития рециди-
вов заболевания до 10% (УД 2a, СР B [3, 8, 22, 24, 29, 32, 46, 61, 63, 69, 82,
87, 108, 113].
Критерии оценки качества помощи в стационаре представлены в таблице 11.2. Для оценки качества медицинской помощи используют временные, процессуальные и профилактирующие критерии. Временные характеризуют своевременность оказания определенных этапов медицинской помощи. Выполнение пациенту ряда медицинских манипуляций, инструментальных и лабораторных исследований, необходимых для качественного оказания медицинской помощи, оценивают в процессуальных критериях. Для анализа мероприятий, направленных на предотвращение развития осложнений, используют профилактирующие критерии.
Таблица 11.2. Критерии оценки качества медицинской помощи в стационаре больным с доброкачественными заболеваниями промежности, прямой кишки и анального канала (остроконечные кондиломы) (0 — нет, 1 — да)
|
Клинические рекомендации |
Временные |
Процессуальные |
Профилактирующие |
|
Клинические рекомендации по диагностике и лечению взрослых пациентов с остроконечными кондиломами перианальной области и анального канала (код МКБ — K62.8) |
Установка клинического диагноза в течение 72 ч: 0/1 |
Оценка анального рефлекса: 0/1. Пальцевое обследование прямой кишки: 0/1. Аноскопия: 0/1. Ректороманоскопия: 0/1. Определение группы крови: 0/1. Исследование крови на сифилис, вирусный гепатит В, вирусный гепатит С: 0/1. Клинический анализ крови; биохимический анализ крови; клинический анализ мочи; коагулограмма: 0/1. Метод оперативного лечения в соответствии с клиническими рекомендациями: 0/1. Метод анестезии в соответствии с объемом оперативного лечения: 0/1 |
Отсутствие осложнений: • кровотечение: 0/1; • абсцесс: 0/1; • флегмона: 0/1; • пневмония: 0/1; • тромбоэмболия: 0/1; • летальный исход: 0/1 |
Литература
1. Адаскевич В.П. Инфекции, передаваемые половым путем. — М.: Медицинская книга, 2001. — С. 219–231.
2. Аполихина И.А. Папилломавирусная инфеция гениталий у женщин. — М.: ГЭОТАР-Медиа, 2002. — 112 с.
3. Борисов Л.Б. Медицинская микробиология, вирусология, иммунология. — М.: МИА, 2002. 734 с.
4. Ван Крог Г., Лейси Д., Гросс Г. Европейский курс по заболеваниям, ассоциированным с ВПЧ: рекомендации для врачей общей практики по диагностике и лечению аногенитальных бородавок // Инфекции, передаваемые половым путем. — 2001. — № 1. — С. 5–12.
5. Васильев В.В., Богатырева И.И., Котова Л.К., Белавин А.С. Современные аспекты папилломавирусной инфекции урогенитального тракта (клиника, диагностика, лечение) // Инфекции, передаваемые половым путем. — 1999. — № 5. — С. 20–26.
6. Вишневская А.С., Сафронникова Н.Р. Дискуссионные вопросы лечения
папилломавирусной инфекции шейки матки // Практ. онкология. — 2002. — Т. 3, № 3. — С. 166–174.
7. Волков В.Г., Захарова Т.В. Опыт применения СО2-лазерной хирургии в комплексном лечении патологии шейки матки, ассоциированной с вирусом папилломы человека // Вестн. новых мед. технологий. — 2000. — Т. 1,
№ 7. — С. 95–97.
8. Воробьев Г.И., Шелыгин Ю.А., Капуллер Л.Л. и др. Лечение папилломавирусной инфекции перианальной области и анального канала // Анналы хир. — 2007. — № 4. — С. 66–70.
9. Гомберг М.А., Соловьев A.M. Опыт применения солкодерма♠ в дерматовенерологической практике // Вестн. дерматол. — 1999. — № 1. — С. 60–62.
10. Дубенский В.В., Кузнецов В.П., Беляев Д.Л., Слюсарь Н.Н. Эффективность иммунокоррекции цитокинами при лечении папилломавирусной инфекции // Журн. микробиол. — 2001. — № 5. — С. 54–58.
11. Ершов Ф.И. Система интерферона в норме и при патологии. — М.:
Медицина, 1996. — 239 с.
12. Кныш В.И., Тимофеев Ю.М. Злокачественные опухоли анального канала. — М.: Медицина, 1997. — 303 с.
13. Кожные и венерические болезни: Руководство для врачей / Под ред. Ю.К. Скрипкина, В.Н. Мордовцева. — М.: Медицина, 1999. — 880 с.
14. Козлова В.И., Пухнер А.Д. Вирусные, хламидийные и микоплазменные заболевания гениталий: Руководство для врачей. — СПб.: Ольга, 2000. — 572 с.
15. Кривошеев Б.Н., Криницина Ю.М. Терапевтическая эффективность солкодерма♠ у больных с папилломавирусными поражениями кожи и слизистых оболочек // Рос. журн. кож. и вен. бол. — 2001. — № 6. — С. 10–15.
16. Кузнецова Ю.Н. Латентная папилломавирусная инфекция урогениталь-
ного тракта женщин, обусловленная ВПЧ 16-го и 18-го типов. Варианты течения, тактика ведения: Автореф. дис. … канд. мед. наук. — М., 2003. — 16 с.
17. Кулаков В.И. Современные подходы к диагностике папилломавирусной инфекции гениталий женщин и их значение для скрининга рака шейки матки // Гинекология. — 2000. — Т. 2, № 1. — С. 4–8.
18. Логинова Н.С., Аполихина И.А., Сухих Г.Т. Эффективность вобэнзи-
ма при папилломавирусной инфекции гениталий с комплексном лечении с циклофероном // Рус. журн. ВИЧ/СПИД и родств. пробл. — 1999. — Т. 1,
№ 3. — С. 87–88.
19. Мазуренко Н.Н. Роль вирусов папиллом в канцерогенезе шейки матки // Соврем. онкол. — 2003. — № 1 (5). — С. 7–10.
20. Максимов С.Я., Савичева A.M., Башмакова М.А. Роль опухоль-ассоциированных типов папилломавирусной инфекции гениталий в генезе фоновых
заболеваний эктоцервикса, дисплазии и преинвазивного рака шейки матки // Вопр. онкол. — 1999. — Т. 6, № 45. — С. 627–629.
21. Манухин И.Б., Кондриков Н.И., Крапошина Т.П. Заболевания наружных половых органов у женщин. — М.: МИА, 2002. — 303 с.
22. Мартьянова В.И. Результаты лечения папилломавирусной инфекции перианальной области и анального канала // Актуальные вопросы колопроктологии. — Уфа, 2007. — С. 72–75.
23. Михайлов И.Г., Максимов С.Я., Новик В.И. Сравнительная оценка
некоторых способов лечения генитальной папилломавирусной инфекции у женщин с различными генотипами вируса // Вопр. онкол. — 2000. — Т. 3,
№ 46. — С. 340–343.
24. Молочков В.А., Киселев В.И., Рудых И.В., Щербо С.Н. Папилломавирусная инфекция. Клиника. Диагностика. Лечение. — М.: Русский врач, 2004. — 44 с.
25. Морсон Б.К., Собин Л.Г. Международная гистологическая классификация опухолей № 15 // Гистологическая классификация опухолей кишечника ВОЗ. — Женева, 1981. — С. 69.
26. Подистов Ю.И. Роль вируса папилломы в развитии предрака и рака
шейки матки // Клин. лаб. диагностика. — 2003. — № 5. — С. 44–50.
27. Прилепская В.Н. Профилактика рака шейки матки // Гинекология. — 2007. — Т. 9, № 1. — С. 12–15.
28. Прилепская В.Н., Роговская С.И., Кондриков Н.И., Сухих Г.Т. Папилломавирусная инфекция: диагностика, лечение и профилактика. — М.: МЕДпресс-информ, 2007. — 32 с.
29. Роговская С.И. Папилломавирусная инфекция гениталий: роль ин-
терферонов в патогенезе и лечении (обзор литературы) // Гинекология. — 2003. — Т. 5, № 5. — С. 73–81.
30. Роговская С.И. Папилломавирусная инфекция у женщин и патология шейки матки. — М.: ГЭОТАР-Медиа, 2008. — 192 с.
31. Роговская С.И., Ежова Л.С., Прилепская В.Н. Клинико-морфологические особенности папилломавирусной инфекции у женщин // Гинекология. — 2004. — Т. 6, № 2. — С. 20–25.
32. Роговская С.И., Логинова Н.С., Файззулин Л.З., Сухих Г.Т. Препараты ин-
терферона и интерфероногены в лечении заболеваний половых органов, вызванных папилломавирусной инфекцией // 3ППП. — 1998. — № 5. — С. 27–30.
33. Самойлова Э.В. Молекулярные маркеры рака шейки матки: Автореф. дис. … канд. мед. наук. — М., 1997. — 26 с.
34. Сафронникова Н.Р., Зарайский М.И., Чухловин А.Б. Факторы онкологического риска при папилломавирусной инфекции // Вопр. онкол. — 2003. — Т. 4, № 49. — С. 450–454.
35. Сидорова Н.А., Минкина Г.Н. Цитологический метод в выявлении па-
пилломавирусной инфекции // Рос. онкол. журн. — 1996. — № 2. — С. 25–28.
36. Соловьев A.M. Консервативная терапия поражений, вызванных папилломавирусной инфекцией // Леч. врач. — 2003. — № 7. — С. 18–23.
37. Цитологический атлас. Диагностика заболеваний шейки матки / Под ред. И.П. Шабаловой. — М.: Триада, 2006. — С. 162.
38. Abcarian H., Smith D., Sharon N. The immunotherapy of anal condyloma acuminatum // Dis. Colon Rectum. — 1976. — Vol. 19. — P. 237–241.
39. Ault K.A. Human papillomavirus infections: diagnosis, treatment, and hope for a vaccine // Obstet. Gynecol. Clin. North Am. — 2003. — Vol. 30, N l. — P. 809–817.
40. Beutner K.R., Spruance S.L., Hougham A.J. et al. Treatment of genital warts with an immune-response modifier (imiquimod) // J. Am. Acad. Dermatol. — 1998. — Vol. 38. — P. 230–239.
41. Butler T.W., Gefter J., Kleto D. et al. Squamous-cell carcinoma of the anus in
condyloma acuminatum. Successful treatment with preoperative chemotherapy and radiation // Dis. Colon Rectum. — 1987. — Vol. 30, N 4. — P. 293–295.
42. Byars R.W., Poole G.V. Anal carcinoma arising from condyloma acuminate // Am. J. Surg. — 2001. — Vol. 67, N 5. — P. 469–472.
43. Canadas M.P., Bosch F.X., Junquera M.L. et al. Concordance of prevalence of human papillomavirus DNA in anogenital and oral infections in high-risk populations // J. Clin. Microbiol. — 2004. — Vol. 42. — P. 1330–1332.
44. Chu Q.D., Vezeridis M.P., Libbey N.P., Wanebo H.J. Giant condyloma
acuminatum (Buschke-Lowenstein tumor) of the anorectal and perianal regions: analysis of 42 cases // Dis. Colon Rectum. — 1994. — Vol. 37. — P. 950–957.
45. Cleary R.K., Schaldenbrand J.D., Fowler J.J. Perianal Bowen’s disease and anal intraepithelial neoplasia: review of the literature // Dis. Colon Rectum. — 1999. — Vol. 42, N 7. — P. 945–951.
46. Clerici M., Merola M., Ferrario E. Cytokine production patterns in cervical
intraepithelial neoplasia: association with human papillomavirus infection // J. Natl Cancer Inst. — 1997. — Vol. 89, N 3. — P. 245–250.
47. Coleman N., Birley H.D., Renton A.M. et al. Immunological events in regressing genital warts // Am. J. Clin. Pathol. — 1994. — Vol. 102. — P. 768–774.
48. Conant M.A. Immunomodulatory therapy in the management of viral infections in patients with HIV infection // J. Am. Acad. Dermatol. — 2000. — Vol. 43. — P. 27–30.
49. Corman M.L. Colon and Rectal Surgery. — Philadelphia: Lippincot, 1998. —
P. 527–533.
50. Cox J.T. Clinical role of HPV testing // Obstet. Gynecol. Clin. North Am. — 1996. — Vol. 23, N 4. — P. 811–851.
51. Daling J.R., Madeleine M.M., Johnson L.G. et al. Human papillomavirus, smoking, and sexual practices in the etiology of anal cancer // Cancer. — 2004. — Vol. 101. — P. 270–280.
52. Dawson D., Duckworth J., Bernhardt H.,Young J. Giant condyloma and verrucous
carcinoma of the genital area // Arch. Pathol. — 1965. — Vol. 79. — P. 225–230.
53. De Villiers E.M., Fauquet C., Broker T.R. et al. Classification of papillomaviruses // Virology. — 2004. — Vol. 324. — P. 17–27.
54. Dell D.L., Chen H., Ahmad F., Stewart D.E. Knowledge about human papillomavirus among adolescents // Obstet. Gynecol. — 2000. — Vol. 96. — P. 653–656.
55. de Oliveira C.M., Fregnani J.H., Carvalho J.P. et al. Human papillomavirus
genotypes distribution in 175 invasive cervical cancer cases from Brazil // BMC Cancer. — 2013. — Vol. 13, N 1. — P. 357.
56. Depuydt C.E., Criel A.M., Benoy I.H. et al. Changes in type-specific human papillomavirus load predict progression to cervical cancer // J. Cell. Mol. Med. — 2012. — Vol. 16, N 12. — P. 3096–3104.
57. Ezeneva B.M. Mothers’ human papilloma virus knowledge and willingness to vaccinate their adolescent daughters in Lagos, Nigeria // Int. J. Womens Health. — 2013. — Vol. 8, N 5. — P. 371–377.
58. Edwards L., Ferenczy A., Eron L. et al. Self-administered topical 5% imiquimod cream for external anogenital warts // Arch. Dermatol. — 1998. — Vol. 134. — P. 25–30.
59. Evander M., Edland K., Gustaafsson A. Human papillomavirus infection is
transient in young woman: a population-based cohort study // J. Infect. Dis. — 1995. — Vol. 171. — P. 1026–1030.
60. Favato G., Baio G., Capone A. et al. Novel health economic evaluation of a vaccination strategy to prevent HPV-related diseases: the BEST study // Med. Care. — 2012. — Vol. 50, N 12. — P. 1076–1085.
61. Foldvari M., Kumar P. Recent progress in the application of nanotechnology
for prevention and treatment of human papillomavirus infection // Ther. Deliv. — 2012. — Vol. 3, N 8. — P. 1005–1017.
62. Frisch M., Glimelius B., Brule J.C. Sexually transmitted infection as a cause of anal cancer // N. Engl. J. Med. — 1997. — Vol. 337. — P. 1350–1358.
63. Geusau A., Heinz-Peer G., Volc-Platzer B. et al. Regression of deeply infiltrating giant condyloma (Buschke-Lowenstein tumor) following long-term intralesional interferon alfa therapy // Arch. Dermatol. — 2000. — Vol. 136, N 6. — P. 707–710.
64. Hall J.S., Iype R., Armenoult L.S. et al. Poor prognosis associated with human
papillomavirus α7 genotypes in cervical carcinoma cannot be explained by intrinsic radiosensitivity // Int. J. Radiat. Oncol. Biol. Phys. — 2013. — Vol. 85, N 5. — P. 223–229.
65. Hammarlund K., Nyström M., Jomeen J. Young women’s experiences of managing self-treatment for anogenital warts // Sex. Reprod. Healthc. — 2012. — Vol. 3, N 3. — P. 117–121.
66. Handley J., Dinsmore W. Treatment of anogenital warts. Review // J. Acad.
Dermatol. Venerol. — 1994. — Vol. 3. — P. 251–265.
67. Handsfield H.H. Clinical presentation and natural course of anogenital warts // Am. J. Med. — 1997. — Vol. 102. — P. 16–20.
68. Harper D.M., Franco E.L., Wheeler C. et al. Efficacy of a bivalent L1 viruslike particle vaccine in prevention of infection with human papillomavirus types 16 and 18 in young women: a randomised controlled trial // Lancet. — 2004. — Vol. 364. — P. 1757–1765.
69. Hechter R.C., Chao C., Sy L.S. et al. Quadrivalent human papillomavirus
vaccine uptake in adolescent boys and maternal utilization of preventive care and history of sexually transmitted infections // Am. J. Public Health. — 2013. — Vol. 103, N 9. — P. 63–68.
70. Hengge U.R., Benninghoff B., Ruzicka T., Goos M. Topical immunomodulators — progress towards treating inflammation, infection, and cancer // Lancet Infect. Dis. — 2001. — Vol. 1. — P. 189–198.
71. Hernandez B.Y., McDuffie K., Zhu X. et al. Anal human papillomavirus
infection in women and its relationship with cervical infection // Cancer Epidemiol. Biomarkers Prev. — 2005. — Vol. 14, N 11. — P. 2550–2556.
72. Hope E., Johanna C. Anal cancer: an overview // Oncologist. — 2007. — Vol. 12. — P. 524–534.
73. Hoffmann J.C., Fischer I., Höhne W. et al. Methodische Grundlagen für die Ableitung von Konsensusempfehlungen [Methodological basis for the development of consensus recommendations] // Z. Gastroenterol. — 2004. — Vol. 42, N 9. — P. 984–986.
74. Ilkay A.K., Chodak G.W., Vogelzang N.J., Gerber G.S. Buschke-Lowenstein tumor: therapeutic options including systemic chemotherapy // Urology. — 1993. — Vol. 42, N 5. — P. 599–602.
75. Koutsky L. Epidemiology of genital human papillomavirus infection // Am.
J. Med. — 1997. — Vol. 102. — P. 3–8.
76. Koutsky L.A., Ault K.A., Wheeler C.M. A controlled trial of a human papillomavirus type 16 vaccine // N. Engl. J. Med. — 2002. — Vol. 347. — P. 1645– 1651.
77. Kreimer A.R., Clifford G.M., Boyle P., Franceschi S. Human papillomavirus types in head and neck squamous cell carcinomas worldwide: a systematic review // Cancer Epidemiol. Biomarkers Prev. — 2005. — Vol. 14. — P. 467–475.
78. Lorincz A. Hybrid Capture method for detection of human papillomavirus
DNA in clinical specimens // Papillomavirus Rep. — 1996. — Vol. 7. — P. 1–5.
79. Martin F., Bower M. Anal intraepithelial neoplasia in HIV positive people // Sex. Transm. Infect. — 2001. — Vol. 77, N 5. — P. 327–331.
80. Mathijs H., Kimberly A. Human papillomavirus: a review // Dermatol. Clin. — 2002. — Vol. 20. — P. 315–331.
81. Maglennon G.A., Doorbar J. The biology of papillomavirus latency // Open Virol. J. — 2012. — Vol. 6. — P. 190–197.
82. Muller M., Demeret C. The HPV E2-host protein-protein interactions: A complex hijacking of the cellular network // Open Virol. J. — 2012. — Vol. 6. — P. 173–189.
83. Noffsinger A.E., Witte D., Fenoglio-Preiser C.M. The relationship of human
papillomaviruses to anorectal neoplasia // Cancer. — 1992. — Vol. 70. — P. 1276– 1287.
84. Palefsky J.M., Holly E.A., Gonzales J. et al. Detection of human papillomavirus DNA in anal intraepithelial neoplasia and anal cancer // Cancer Res. — 1991. — Vol. 51. — P. 1014–1019.
85. Palmer J.G., Scholefield J.H., Coates P.J. et al. Anal cancer and human
papillomaviruses // Dis. Colon Rectum. — 1989. — Vol. 32. — P. 1016–1022.
86. Paba P., Morosetti G., Criscuolo A.A. et al. Prevalence of human papillomavirus infection in Italian and immigrant women // Int. J. Immunopathol. Pharmacol. — 2012. — Vol. 25, N 4. — P. 1055–1062.
87. Peter V., Palefsky J.M. Natural history and clinical management of anal human papillomavirus disease in men and women infected with human immunodeficiency virus // Clin. Infect. Dis. — 2002. — Vol. 35. — P. 1127–1134.
88. Phillips B., Ball C., Sackett D. et al. Oxford Centre for Evidence-Based
medicine — Levels of Evidence. — 2009. — Available from: http://www.cebm.net/ oxford-centre-evidence-based-medicine-levels-evidence-march-2009.
89. Prasad C.J. Pathobiology of human papillomavirus // Clin. Lab. Med. — 1995. — Vol. 15, N 3. — P. 685–704.
90. Rabkin C.S., Biggar R.J., Melbye M., Curtis R.E. Second primary cancers following anal and cervical carcinoma: evidence of shared etiologic factors // Am. J. Epidemiol. — 1992. — Vol. 136. — P. 54–58.
91. Radovanovic Z., Radovanovic D., Semnic R. et al. Highly aggressive Buschkelöwenstein tumor of the perineal region with fatal outcome. // Indian J. Dermatol. Venereol. Leprol. — 2012. — Vol. 78, N 5. — P. 648–650.
92. Rockley P.F., Tyring S.K. Interferons alpha, beta, and gamma therapy of anogenital human papillomavirus infections // Pharmacol. Ther. — 1995. — Vol. 65. — P. 265–287.
93. Roberts J.M., Thurloe J.K. Comparison of the performance of anal cytology
and cervical cytology as screening tests // Sex Health. — 2012. — Vol. 9, N 6. — P. 568–573.
94. Sarmiento J.M., Wolff B.G. Perianal Bowen’s disease: associated tumors, human papillomavirus, surgery, and other controversies // Dis. Colon Rectum. — 1997. — Vol. 40, N 8. — P. 912–918.
95. Schiffman M., Kjaer S.K. Natural history of anogenital human papillomavirus
infection and neoplasia // J. Natl Cancer Inst. Monogr. — 2003. — Vol. 31. — P. 14–19.
96. Schiller J.T., Lowy D.R. Understanding and learning from the success of prophylactic human papillomavirus vaccines // Nat. Rev. Microbiol. — 2012. — Vol. 10, N 10. — P. 681–692.
97. Schneider A. Natural history of genital papillomavirus infections //
Intervirology. — 1994. — Vol. 37. — P. 201–214.
98. Siegel J.F., Mellinger B.C. Human papillomavirus in the male patient // Urol. Clin. North Am. — 1992. — Vol. 19, N 1. — P. 83–91.
99. Silins I., Kallings I., Dillner J. Correlates of the spread of human papillomavirus infection // Cancer Epidemiol. Biomarkers Prev. — 2000. — Vol. 9. — P. 953–959.
100. Smith Y.R., Haefner H.K., Lieberman R.W., Quint E.H. Comparison of microscopic examination and human papillomavirus DNA subtyping in vulvar lesions of premenarchal girls // J. Pediatr. Adolesc. Gynecol. — 2001. — Vol. 14, N 2. — P. 81–84.
101. Sobhani I., Vuagnat A. Prevalence of high-grade dysplasia and cancer in the
anal canal in human papillomavirus-infected individuals // Gastroenterology. — 2001. — Vol. 120, N 4. — P. 857–866.
102. Sobrado C.W., Mester M., Nadalin W. et al. Radiation-induced total regression of a highly recurrent giant perianal condyloma // Dis. Colon Rectum. — 2000. — Vol. 43. — P. 257–260.
103. Stoler M.H. Human papillomavirus and cervical neoplasia: a model for
carcinogenesis // Int. J. Gynecol. Pathol. — 2000. — Vol. 19. — P. 16–28.
104. Syrjanen K.J. HPV infections and oesophageal cancer // J. Clin. Pathol. — 2002. — Vol. 55. — P. 721–728.
105. Syrjanen S., Puranen M. Human papillomavirus infections in children: the potential role of maternal transmission // Crit. Rev. Oral Biol. Med. — 2000. — Vol. 11. — P. 259–274.
106. Tilston P. Anal human papillomavirus and anal cancer // J. Clin. Pathol. —
1997. — Vol. 50. — P. 625–634.
107. Trombetta L.J., Place R.J. Giant condyloma acuminatum of the anorectum: trends in epidemiology and management: report of a case and review of the literature // Dis. Colon Rectum. — 2001. — Vol. 44, N 12. — P. 1878–1886.
108. Tyring S.K. Imiquimod applied topically: a novel immune response modifier // Skin Ther. Lett. — 2001. — Vol. 6, N 6. — P. 1–4.
109. Tyring S.K. Human papillomavirus infections: epidemiology, pathogenesis, and host immune response // J. Am. Acad. Dermatol. — 2000. — Vol. 43. — P. 18–26.
110. Varnai A.D., Bollmann M., Griefingholt H. et al. HPV in anal squamous cell carcinoma and anal intraepithelial neoplasia // Int. J. Colorectal Dis. — 2006. — Vol. 21. — P. 135–142.
111. Villa L.L., Costa R.L., Petta C.A. Prophylactic quadrivalent human papillomavirus (types 6, 11, 16, and 18) L1 virus-like particle vaccine in young women: a randomised double-blind placebo-controlled multicentre phase II efficacy trial // Lancet Oncol. — 2005. — Vol. 6. — P. 271–278.
112. Vukasin P. Anal condyloma and HIV-associated anal disease // Surg. Clin. North Am. — 2002. — Vol. 82. — P. 1199–1211.
113. Wiley D., Douglas J., Beutner K., Cox T. et al. External genital warts: diagnosis, treatment and prevention // Clin. Infect. Dis. — 2002. — Vol. 35, N 5. — P. 210–224.
114. Yuhan R., Orsay C. et al. Anorectal disease in HIV-infected patients // Dis. Colon Rectum. — 1998. — Vol. 41, N 11. — P. 1367–1370.
115. Zur Hauzen H., De Villiers E.M. Human papillomaviruses // Ann. Rev. Microbiol. — 1994. — Vol. 48. — P. 427–447.
АНАЛЬНЫЕ ПОЛИПЫ
Введение
Данные рекомендации посвящены диагностике и лечению доброкачественных новообразований анального канала.
Настоящие рекомендации по диагностике и лечению больных с анальными полипами служат руководством для практических врачей, осуществляющих ведение и лечение таких пациентов. Рекомендации подлежат регулярному пересмотру в соответствии с новыми данными научных исследований в этой области. Настоящие рекомендации составлены на основании данных литературы.
Рекомендации включают следующие разделы: определение и классификация анальных полипов, диагностика, лечение и прогноз.
Для отдельных положений рекомендаций приведены уровни доказательности согласно общепринятой классификации Оксфордского центра доказательной медицины (табл. 12.1).
Таблица 12.1. Уровни доказательности и степени рекомендаций на основании руководства Оксфордского центра доказательной медицины
|
Уровень |
Диагностическое исследование |
Терапевтическое исследование |
|
1а |
Систематический обзор гомогенных диагностических исследований 1-го уровня |
Систематический обзор гомогенных РКИ |
|
1b |
Валидизирующее когортное исследование с качественным «золотым стандартом» |
Отдельное РКИ (с узким доверительным интервалом) |
|
1с |
Специфичность или чувствительность столь высокие, что положительный или отрицательный результат позволяет исключить/установить диагноз |
Исследование «Всё или ничего» |
|
2а |
Систематический обзор гомогенных диагностических исследований >2-го уровня |
Систематический обзор (гомогенных) когортных исследований |
|
2b |
Разведочное когортное исследование с качественным «золотым стандартом» |
Отдельное когортное исследование (включая РКИ низкого качества; т.е. с <80% пациентов, прошедших контрольное наблюдение) |
Табл. 12.1. Окончание
|
Уровень |
Диагностическое исследование |
Терапевтическое исследование |
|
2с |
Нет |
Исследование «исходов»; экологические исследования |
|
3а |
Систематический обзор гомогенных исследований уровня 3b и выше |
Систематический обзор гомогенных исследований «случай–контроль» |
|
3b |
Исследование с непоследовательным набором или без проведения исследования «золотого стандарта» у всех испытуемых |
Отдельное исследование «случай– контроль» |
|
4 |
Исследование «случай–контроль» или исследование с некачественным или зависимым «золотым стандартом» |
Серия случаев (и когортные исследования или исследования «случай–контроль» низкого качества) |
|
5 |
Мнение экспертов без тщательной критической оценки или основанное на физиологии, лабораторные исследования на животных или разработка «первых принципов» |
Мнение экспертов без тщательной критической оценки, лабораторные исследования на животных или разработка «первых принципов» |
|
Степени рекомендаций | ||
|
A |
Согласующиеся между собой исследования 1-го уровня | |
|
B |
Согласующиеся между собой исследования 2-го или 3-го уровня или экстраполяция на основе исследований 1-го уровня | |
|
C |
Исследования 4-го уровня или экстраполяция на основе уровня 2 или 3 | |
|
D |
Доказательства 4-го уровня или затруднительные для обобщения или некачественные исследования любого уровня | |
ВАЛИДИЗАЦИЯ РЕКОМЕНДАЦИЙ
Настоящие рекомендации в предварительной версии были рецензированы независимыми экспертами, которых попросили прокомментировать прежде всего, насколько интерпретация доказательств, лежащих в основе рекомендаций, доступна для понимания. Получены комментарии со стороны врачей амбулаторного звена. Полученные комментарии тщательно систематизировались и обсуждались на совещаниях экспертной группы.
Последние изменения в настоящих рекомендациях были представлены для дискуссии на заседании профильной комиссии «Колопроктология» Экспертного совета Минздрава России 12 сентября 2013 г. Проект рекомендаций был повторно рецензирован независимыми экспертами и врачами амбулаторного звена. Для окончательной редакции и контроля качества рекомендации были повторно проанализированы членами экспертной группы, которые пришли к заключению, что все замечания и комментарии приняты во внимание, риск систематических ошибок при разработке рекомендаций сведен к минимуму.
ОБЛАСТЬ ПРИМЕНЕНИЯ РЕКОМЕНДАЦИЙ
Данные клинические рекомендации применимы при осуществлении медицинской деятельности в рамках Порядка оказания медицинской помощи взрослому населению с заболеваниями толстой кишки, анального канала и промежности колопроктологического профиля.
Определение
Термин «анальный канал», предложенный J. Symington [17] в 1888 г., был распространен лишь среди клиницистов, пока в 1955 г. не был официально признан и рекомендован к применению Международной анатомической номенклатурой в Париже [5]. Однако до настоящего времени отсутствует единое понимание границ анального канала, в результате чего появились термины «хирургический анальный канал», «анатомический», «гистологический» и т.д.
В ГНЦ колопроктологии придерживаются следующего определения:
«Анальный канал — это терминальная часть пищеварительного тракта, начинающаяся от места аноректального соединения у верхней границы тазового дна и заканчивающаяся наружным отверстием — анусом, границей которого является место перехода непигментированной анодермы в пигментированную (истинную) кожу» [4].
Анальные полипы, или полипы анального канала (anal polyp, anal papilla) — описательный, клинический термин, обозначающий любое внутрипросветное образование в границах анального канала.
Код по Международной классификации болезней 10-го пересмотра [3]
n Класс: Болезни органов пищеварительной системы.
n Блок: Другие болезни кишечника (K55–K63).
n Другие болезни заднего прохода и прямой кишки (K62).
n Код: К62.0.
n Название: Полип анального канала.
Классификация
Существуют разные классификации полипов (УД 1а СР А [1]), основанные на их различных характеристиках:
n характер роста (доброкачественный, злокачественный);
n особенности прикрепления к переходной зоне анального канала (полип на ножке, плоский);
n морфологические данные (аденома, гиперпластический полип и т.д.);
n гистологическое строение (тубулярный, ворсинчатый и т.д.).
По классификации З. Маржатка (1996) все полипы делятся на «истинные» и неопухолевой природы. К «истинным» полипам автор относит эпителиальные (аденома, карциноид) и неэпителиальные (лейомиома, липома, гемангиома и др.). К полипам второго типа относятся гиперпластические, гамартома, воспалительные полипы и гиперплазия анальных сосочков.
Однако, на наш взгляд, особое значение, определяющее тактику лечения и последующего наблюдения пациента, имеют морфогистологические данные.
Учитывая, что абсолютное большинство доброкачественных новообразований анального канала — случайные находки, вполне понятно отсутствие рандомизированных исследований, в связи с чем при анализе литературы сложно определить уровни доказательности согласно общепринятой классификации Оксфордского центра доказательной медицины.
ГИПЕРПЛАСТИЧЕСКИЕ ПОЛИПЫ
Гиперпластические полипы встречаются наиболее часто, являются результатом хронических воспалительных процессов анального канала и не представляют собой истинную опухоль. Чаще всего имеют строение на ножке, в связи с чем могут выпадать из анального канала при дефекации, что обычно и становится причиной обращения пациента к колопроктологу. В отличие от истинных аденом, как правило, имеют гладкую поверхность и выявляются при достижении размеров до нескольких сантиметров.
ГИПЕРТРОФИРОВАННЫЙ АНАЛЬНЫЙ СОСОЧЕК
В нижней части ампулярного отдела прямой кишки располагаются морганиевы столбики и крипты, окаймленные полулунными клапанами. На этих клапанах нередко можно наблюдать возвышения — анальные сосочки. Иногда они могут гипертрофироваться и нередко достигают диаметра 3–4 см. Описывается много причин гипертрофии анальных сосочков, однако большинство авторов указывают на наличие хронического воспалительного процесса в анальном канале. Часто гипертрофированные анальные сосочки принимают за анальные полипы.
КЛОАКОГЕННЫЕ ПОЛИПЫ
В последнее время в литературе все чаще появляются термины «клоакогенный полип», «клоакогенный рак». Так авторы обозначают новообразования, располагающиеся в переходной зоне, месте перехода железистого эпителия в плоскоклеточный. Наиболее частой жалобой таких пациентов является наличие ректальных кровотечений. Также отмечено сочетание данных новообразований с солитарной язвой прямой кишки (УД 1а, СР А [8, 10, 11, 12, 13, 15, 16]).
АДЕНОМЫ АНАЛЬНОГО КАНАЛА
Аденома — доброкачественная опухоль железистого эпителия, имеющая различную степень клеточной дисплазии. Длительное время среди клиницистов существовало мнение, что истинные аденомы не могут располагаться в анальном канале, учитывая плоскоклеточное строение его слизистой оболочки. Однако в последующем было выявлено, что 10–15% злокачественных опухолей анального канала составляют аденокарциномы. Таким образом была доказана возможность роста в анальном канале истинных аденом (УД 2а, СР В [4]).
Они могут иметь грибовидную форму (на ножке) или быть на широком основании. Аденоматозные полипы могут быть как одиночными, так и множественными и иметь размеры от нескольких миллиметров до нескольких сантиметров. Поверхность может быть как гладкой, так и бугристой. Данный тип полипов часто протекает бессимптомно и выявляется случайно при пальцевом обследовании или при выпадении наружу полипа на ножке при дефекации. Также иногда пациенты предъявляют жалобы на выделение слизи (при наличии ворсинчатой аденомы).
ФИБРОЗНЫЙ ПОЛИП
Фиброзный полип (син.: фиброэпителиальный полип) — одно из самых частых поражений переходной зоны. Макроскопически узел имеет сферическую или вытянутую форму и диаметр от нескольких миллиметров до 4 см. Его поверхность белого или серого цвета, часто бывает изъязвлена. При гистологическом исследовании строма коллагенизирована и выстлана многослойным плоским эпителием. В ней видны фибробласты с двумя ядрами и более, а также большое количество тучных клеток, иногда гранулемы [18].
РАЗНОЕ
В литературе также описаны единичные случаи, когда в новообразованиях анального канала и прямой кишки были обнаружены яйца шистосомы (УД 1а, СР А [6, 9, 14])
P. Raso и соавт. (2013) описали случай удаления полипа анального канала, где при исследовании были выявлены яйца Schistosoma mansoni, в связи с чем пациенту с клиническим эффектом был проведен курс лечения празиквантелом.
Диагностика
Диагностика анальных полипов основана на оценке жалоб, длительности заболевания, результатов пальцевого исследования и инструментальных методов обследования (УД 2b, СР В [8, 9]).
К основным клиническим симптомам полипа анального канала относят выпадение их из заднего прохода при дефекации, примесь крови
к стулу, дискомфорт, зуд, жжение и даже болезненность в области ануса. К более редким симптомам относятся влажность перианальной области, выделения слизи из прямой кишки. Болевые ощущения при полипе анального канала, как правило, не выражены, встречаются не часто и связаны с их травматизацией при выпадении.
Сбор анамнеза. Выявляются этиологические факторы возникновения заболевания: желудочно-кишечные расстройства, погрешности в диете, злоупотребление алкоголем, кишечные инфекции, воспалительные заболевания дистальных отделов толстой кишки, наличие родственников, страдавших доброкачественными и злокачественными новообразованиями ЖКТ (УД 1с, СР В [20]).
Осмотр врачом-колопроктологом. Пациента осматривают на гинекологическом кресле в положении на спине с максимально приведенными к животу ногами или в коленно-локтевом положении.
При наружном осмотре области промежности и заднего прохода обращают внимание на форму ануса, его зияния, наличия рубцовых изменений и деформации, состояние кожных покровов.
Пальцевое обследование прямой кишки. Определяют тоническое состояние анального сфинктера и силу волевых сокращений, болезненность при исследовании, наличие дефектов слизистой оболочки анального канала, объемных образований анального канала и прямой кишки (УД 5, СР Д [21, 24]).
Аноскопия. Осматривают анальный канал и дистальную часть прямой кишки. Оценивают расположение, размеры и внешний вид анальных полипов, состояние переходной зоны анального канала и зубчатой линии с анальными криптами, а также слизистой оболочки нижнеампулярного отдела прямой кишки.
Ректороманоскопия. Диагностика сопутствующих воспалительных заболеваний прямой и сигмовидной кишки (проктит, проктосигмоидит, внутреннее выпадение, болезнь Крона, язвенный колит).
Колоноскопия. Диагностика сопутствующих изменений толстой кишки, исключение воспалительных изменений, характерных для язвенного колита и болезни Крона (УД 1с, СР А [22, 23]).
ДИФФЕРЕНЦИАЛЬНАЯ ДИАГНОСТИКА
Дифференциальная диагностика полипа анального канала проводится с другими заболеваниями толстой кишки и анального канала (табл. 12.2) (УД 5, СР Д [25, 26]).
Таблица 12.2. Дифференциальная диагностика полипа анального канала
|
Жалобы |
Возможные заболевания |
|
Выпадение полипа анального канала |
Выпадение слизистой оболочки прямой кишки |
|
Выпадение прямой кишки | |
|
Выпадение геморроидальных узлов |
Табл. 12.2. Окончание
|
Жалобы |
Возможные заболевания |
|
Выделение крови из заднего прохода |
Анальная трещина |
|
Злокачественная опухоль прямой кишки и анального канала | |
|
Выпадение слизистой оболочки прямой кишки | |
|
Выпадение прямой кишки | |
|
Язвенный колит | |
|
Болезнь Крона | |
|
Гемангиома | |
|
Эндометриоз | |
|
Травма прямой кишки | |
|
Солитарная язва прямой кишки | |
|
Болевой синдром в анальном канале |
Трещина анального канала |
|
Острый и хронический парапроктит | |
|
Опухоли анального канала | |
|
Осложненные каудальные тератомы | |
|
Болезнь Крона с перианальным поражением | |
|
Идиопатический анокопчиковый болевой синдром | |
|
Эндометриоз | |
|
Прокталгия | |
|
Слизистые выделения из анального канала |
Выпадение прямой кишки |
|
Солитарная язва прямой кишки | |
|
Остроконечные кондиломы | |
|
Анальная трещина | |
|
Злокачественная опухоль анального канала и прямой кишки | |
|
Ворсинчатая опухоль прямой кишки | |
|
Синдром раздраженной толстой кишки | |
|
Воспалительные заболевания толстой кишки (болезнь Крона, язвенный колит) |
Лечение
ГИПЕРПЛАСТИЧЕСКИЕ ПОЛИПЫ
При наличии полипов на ножке или размерами более 5 мм рекомендовано их удаление с обязательным гистологическим исследованием удаленного препарата с целью исключения наличия истинной аденомы.
Пациента укладывают на столе в положение, как для промежностной литотомии: на спине с уложенными на специальные подставки ногами, согнутыми в коленных и тазобедренных суставах. После анестезии производится обработка анального канала. Специальной дивульсии анальных сфинктеров не производится. В анальный канал вводится ректальное зеркало. Верхушка полипа захватывается клеммой Алиса и слегка подтягивается кнаружи. Полип иссекается скальпелем или электроножом в пределах здоровых тканей. Производится ревизия анального канала с целью гемостаза. В прямую кишку вводят гемостатическую губку и газоотводную трубку до утра следующего дня. Удаленный препарат направляют на гистологическое исследование.
На следующий день в условиях перевязочной удаляется газоотводная трубка. Пациент выписывается из стационара после первого самостоятельного стула.
ГИПЕРТРОФИРОВАННЫЙ АНАЛЬНЫЙ СОСОЧЕК
Наличие неувеличенных анальных сосочков считается нормой. В то же время при их гипертрофии и, как следствие, выпадении из анального канала, что причиняет определенные неудобства пациенту, показано их удаление. В отличие от других новообразований анального канала в данной ситуации также обязательно иссечение воспаленной крипты и полулунной заслонки. Техника операции аналогична удалению гиперпластических полипов.
КЛОАКОГЕННЫЕ ПОЛИПЫ
При клоакогенных полипах рекомендовано их удаление в пределах здоровых тканей с обязательным гистологическим исследованием.
Техника операции аналогична удалению гиперпластических полипов.
АДЕНОМЫ АНАЛЬНОГО КАНАЛА
Данные новообразования подлежат обязательному удалению через аноскоп или трансанальному иссечению с гистологическим исследованием удаленного препарата. Техника операции аналогична удалению гиперпластических полипов.
ФИБРОЗНЫЙ ПОЛИП
После удаления требуется обязательное гистологическое исследование, так как необходимо дифференцировать фиброзные полипы от клоакогенных, учитывая их расположение также в переходной зоне. Техника операции аналогична удалению гиперпластических полипов.
Чего нельзя делать
n Не следует выполнять удаление полипов без обследования толстой кишки.
n Не следует выполнять удаление крупных полипов анального канала (более 3 см) без предварительной его биопсии с целью гистологического исследования (УД 1с, СР В [19]).
n Не следует выполнять удаление полипов анального канала на широком основании без предварительного ультразвукового обследования с помощью ректального датчика.
n Не следует удалять гипертрофированные анальные сосочки размером менее 5 мм при отсутствии клинических проявлений.
Дальнейшее ведение
n В послеоперационном периоде до момента полного заживления раны в анальном канале необходима ежедневная санация анального канала с использованием мазевых основ с противовоспалительным и ранозаживляющим действием (левомеколь♠, метилурацил♠).
n В период заживления раны рекомендуется соблюдение диеты, богатой растительной клетчаткой, а также исключение пищи раздражающего характера (прием алкоголя, острой пищи).
n После выписки пациента необходимы еженедельные контрольные осмотры до полного заживления раны анального канала.
Профилактика
При всех перечисленных новообразованиях анального канала, а именно: гиперпластических, клоакогенных, фиброзных полипах и гипертрофированных анальных сосочков — необходима профилактика и лечение воспалительных заболеваний толстой кишки (проктосигмоидит) и анального канала (криптит).
При наличии у пациентов истинных аденом анального канала необходимо следующее.
n Всем лицам, достигшим 50 лет, следует проводить эндоскопическое исследование толстой кишки не реже 1 раза в 3 года.
n Наиболее пристальное внимание следует уделять пациентам, имеющим отягощенный семейный анамнез (наличие полипов у близких родственников, опухолей ЖКТ).
n Эндоскопический контроль состояния толстой кишки в первый год после эндоскопического вмешательства необходимо проводить не реже 2 раз.
n При отсутствии патологических образований в толстой кишке в течение 5 лет после удаления полипов диспансерное наблюдение данной категории пациентов проводится 1 раз в 3 года (УД 1с, СР В [19]).
Прогноз
ГИПЕРПЛАСТИЧЕСКИЕ ПОЛИПЫ
Учитывая «ложный» характер полипа, прогноз, как правило, благоприятный. Однако обязательный ежегодный осмотр рекомендован.
ГИПЕРТРОФИРОВАННЫЙ АНАЛЬНЫЙ СОСОЧЕК
Прогноз благоприятный. Однако, учитывая, что развитие гипертрофии анальных сосочков, как правило, является следствием воспали-
тельного процесса в анальном канале, необходимо установить причину воспаления.
КЛОАКОГЕННЫЕ ПОЛИПЫ
Учитывая возможную взаимосвязь между клоакогенными полипами и развитием клоакогенного рака, при гистологически подтвержденном диагнозе рекомендовано регулярное динамическое наблюдение (не реже 1 раза в год).
АДЕНОМЫ АНАЛЬНОГО КАНАЛА
Из-за возможности повторного роста полипов при наличии гистологически подтвержденной тубулярной, тубулярно-ворсинчатой или ворсинчатой аденомы пациентам рекомендовано постоянное диспансерное наблюдение колопроктолога: в первый год — каждые 3 мес, во второй — каждые 6 мес и далее ежегодно. Также рекомендуется ежегодное проведение колоноскопии.
ФИБРОЗНЫЙ ПОЛИП
Прогноз благоприятный. Постоянного динамического наблюдения данные пациенты не требуют.
Критерии оценки качества помощи в стационаре представлены в таблице 12.3. Для оценки качества медицинской помощи используют временные, процессуальные и профилактирующие критерии. Временные характеризуют своевременность оказания определенных этапов медицинской помощи. Выполнение пациенту ряда медицинских манипуляций, инструментальных и лабораторных исследований, необходимых для качественного оказания медицинской помощи, оценивают в процессуальных критериях. Для анализа мероприятий, направленных на предотвращение развития осложнений, используют профилактирующие критерии.
Таблица 12.3. Критерии оценки качества медицинской помощи в стационаре больным с доброкачественными заболеваниями промежности, прямой кишки и анального канала (анальные полипы) (0 — нет, 1 — да)
|
Клинические рекомендации |
Временные |
Процессуальные |
Профилактирующие |
|
Клинические рекомендации по диагностике и лечению взрослых пациентов с анальными полипами (код МКБ — D12.9) |
Установка клинического диагноза в течение 72 ч: 0/1 |
Оценка анального рефлекса: 0/1. Пальцевое обследование прямой кишки: 0/1. Аноскопия: 0/1. Ректороманоскопия: 0/1. Определение группы крови: 0/1. Исследование крови на сифилис, вирусный гепатит В, вирусный гепатит С: 0/1. Клинический анализ крови; |
Отсутствие осложнений: • кровотечение: 0/1; • абсцесс: 0/1; • флегмона: 0/1; • пневмония: 0/1; • тромбоэмболия: 0/1; • летальный исход: 0/1 |
Табл. 12.3. Окончание
|
Клинические рекомендации |
Временные |
Процессуальные |
Профилактирующие |
|
|
|
биохимический анализ крови; клинический анализ мочи; коагулограмма: 0/1. Метод оперативного лечения в соответствии с клиническими рекомендациями: 0/1. Метод анестезии в соответствии с объемом оперативного лечения: 0/1 |
|
Литература
1. Кайзер А.М. Колоректальная хирургия: Пер. с англ. / Под ред. Ю.А. Шелыгина, С.Е. Урядова. — М.: Изд-во Панфилова, 2011. — 751 с.
2. Маржатка З. Эндоскопия пищеварительного тракта. — М., 1996.
3. МКБ-10 (Международная статистическая классификация болезней и проблем, связанных со здоровьем). — 1999.
4. Шелыгин Ю.А., Нечушкин М.И., Рыбаков Е.Г. Опухоли анального канала и перианальной кожи. — М.: Практическая Медицина, 2011.
5. Nomina anatomica. Международная анатомическая номенклатура. — 3-е изд. / Под ред. Д.А. Жданова. — М., 1970.
6. Abe Y., Inamori M., Fujita K. et al. Gastrointestinal rectal polyp associated with schistosomiasis // J. Gastroenterol. Hepatol. — 2006. — Vol. 21, N 7. — P. 1216.
7. Ali M., Akhtar R., Mirza T.I. Chronic anal fissure; comparison of lateral anal sphincterotomy (closed method) versus anal dilatation // Professional Med. J. — 2011. — Vol. 18, N 2. — P. 215–221.
8. Ewertsen C., Svendsen C.B., Svendsen L.B., Mogensen A.M. Inflammatory
cloacogenic polyp // Ugeskr. Laeger. — 2008. — Vol. 170, N 35. — P. 2708.
9. Gholam P., Autschbach F., Hartschuh W. Schistosomiasis in an HIV-positive patient presenting as an anal fissure and giant anal polyp // Arch. Dermatol. — 2008. — Vol. 144, N 7. — P. 950–952.
10. Hanson I.M., Armstrong G.R. Anal intraepithelial neoplasia in an inflammatory cloacogenic polyp // J. Clin. Pathol. — 1999. — Vol. 52, N 5. — P. 393–394.
11. Levey J.M., Banner B., Darrah J., Bonkovsky H.L. Inflammatory cloacogenic polyp: three cases and literature review // Am. J. Gastroenterol. — 1994. — Vol. 89, N 3. — P. 438–441.
12. Lobert P.F., Appelman H.D. Inflammatory cloacogenic polyP. A unique
inflammatory lesion of the anal transitional zone // Am. J. Surg. Pathol. — 1981. — Vol. 5, N 8. — P. 761–766.
13. Mathialagan R., Turner M.J., Gorard D.A. Inflammatory cloacogenic polyp mimicking anorectal malignancy // Eur. J. Gastroenterol. Hepatol. — 2000. — Vol. 12, N 2. — P. 247–250.
14. Raso P., Sander E.M., Raso L.A., Andrade J.D. Anal polyp caused by
Schistosoma mansoni // Rev. Soc. Bras. Med. Trop. — 2013. — Vol. 46, N 2. — P. 252–254.
15. Saul S.H. Inflammatory cloacogenic polyp: relationship to solitary rectal ulcer syndrome/mucosal prolapse and other bowel disorders // Hum. Pathol. — 1987. — Vol. 18, N 11. — P. 1120–1125.
16. Shih C.M., Tseng H.H., Tu U.C. Inflammatory cloacogenic polyp of anus: report of three cases // Zhonghua Yi Xue Za Zhi (Taipei). — 1990. — Vol. 45, N 1. — P. 69–74.
17. Symington J. http://www.ncbi.nlm.nih.gov/pmc/articles/PMC1288776/ // J. Anat. Physiol. — 1888, Oct 23. — Pt 1. — P. 106–115.
18. Abdullgaffar B., Abdulrahim M., Ghazi E. Benign fibrous polyp presenting in anal canal // Ann. Diagn. Pathol. — 2012, Sep 18. — pii: S1092–9134 (12) 00106–2.
19. Ванин А.И. Результаты активного выявления, хирургического лечения и динамического наблюдения пациентов с колоректальными полипами: Дис. … канд. мед. наук. — М., 2003.
20. Gupta P.J. Hypertrophied anal papillae and fibrous anal polyps, should they be removed during analfissure surgery? // World J. Gastroenterol. — 2004. — Vol. 10, N 16. — P. 2412–2414.
21. Шелыгин Ю.А., Благодарный Л.А. Справочник колопроктолога. — М.: Литтерра, 2012.
22. Church J.M. Analysis of the colonoscopic findings in patients with rectal bleeding according to the pattern of their presenting symptoms // Dis. Colon Rectum. — 1991. — Vol. 34. —P. 391–395.
23. Rex D.K., Bond J.H., Winawer S. et al. Quality in the technical performance of colonoscopy and the continuous quality improvement process for colonoscopy: recommendations of the U.S. Multi-Society Task Force on colorectal cancer // Am. J. Gastroenterol. — 2002. — Vol. 97 —P. 1296–1308.
24. Воробьев Г.И. Основы колопроктологии. — М.: МИА, 2006. — С. 79–82, 94.
25. Laurence R., Dana R. Ambulatory Colorectal Surgery. — N.Y.: Informa, 2009 —P. 79–85.
26. Marvin L., Corman M.D. Colon and Rectal Surgery. — Phiadelphia: Lippincott, 2005. — P. 177–255.
ДИВЕРТИКУЛЯРНАЯ БОЛЕЗНЬ ОБОДОЧНОЙ КИШКИ
Введение
До начала XX в. дивертикулы ободочной кишки и связанные с ними осложнения относились к области казуистики, и лишь в 1916 г. дивертикулярная болезнь впервые упоминается в англоязычном руководстве по заболеваниям желудочно-кишечного тракта. В 1930 г. в странах западной цивилизации частота встречаемости дивертикулов, по данным аутопсий, колебалась в пределах 2–10%, а в 1969 г. уже составляла 35–50%. В США к концу 1960-х гг. ХХ в. ежегодно по поводу дивертикулярной болезни госпитализировались 130 тыс. человек [43].
В настоящее время это число утроилось и составляет 71–126 госпитализаций на 100 тыс. населения в год. Аналогичная картина наблюдается в Канаде, Великобритании, Германии и Финляндии. В 2006 г. затраты на лечение дивертикулярной болезни в США превысили 2,6 млрд долларов [24].
Заболеваемость дивертикулезом в СССР в 1970 г. составляла 2–3 случая на 100 тыс. населения, в 1979 г. — уже 17 случаев на 100 тыс. По данным рентгеноэндоскопических исследований в ГНЦ колопроктологии в 2002 г. среди больных частота обнаружения дивертикулов ободочной кишки составляла 14,2%, а в 2012 г. — 28,8%.
В странах Азии и Африки заболевание встречается редко. Среди потомков иммигрантов из этих стран частота дивертикулярной болезни не отличается от таковой у коренных групп населения.
Частота дивертикулеза увеличивается с возрастом. Так, до 40 лет это заболевание выявляется менее чем у 5% населения, в возрасте 40– 50 лет — 5–10%, в возрасте 50–60 лет — 14%, у лиц старше 60 лет — 30%, старше 80 лет — 60–65%. Среди мужчин и женщин распространенность заболевания приблизительно одинаковая. Вероятность перехода дивертикулеза в состояние дивертикулярной болезни составляет 5–20%. При этом у 75% больных развивается острый дивертикулит, а у 25% — все другие осложнения. Перфорация дивертикула является 4-й по частоте среди причин экстренного хирургического вмешательства после острого аппендицита, перфоративной гастродуоденальной язвы и кишечной не-
проходимости, а также 3-й по частоте среди причин формирования кишечных стом. При дивертикулярной болезни частота формирования внутрибрюшного абсцесса или развития перитонита составляет 3,5–4 случая на 100 тыс. человек в год [19, 24, 35].
Толстокишечные кровотечения как осложнения дивертикулярной болезни развиваются у 3–15% пациентов. Доля дивертикулярной болезни среди других причин толстокишечных кровотечений колеблется от 20 до 40% [58].
30-дневная смертность при дивертикулярной болезни составляет 4,7%, в течение 1 года от осложнений умирают 9,8% больных [35, 44].
Рекомендации по диагностике и лечению пациентов с дивертикулярной болезнью служат руководством для практических врачей, осуществляющих ведение и лечение таких больных, и подлежат регулярному пересмотру в соответствии с новыми данными научных исследований в этой области.
Рекомендации включают следующие разделы: общая часть, классификация, клиническая картина и диагностика, лечение, профилактика и скрининг. Настоящие рекомендации составлены на основании анализа литературы из базы данных PubMed, MEDLINE, Cochrane Collaboration, the Standards Practice Task Force of the American Society of Colon and Rectal Surgeon, Oxford Center for Evidencebased Medicine — Levels of Evidence.
Рекомендации сопровождаются пояснениями об уровне доказательности отдельных положений согласно рекомендациям Оксфордского центра доказательной медицины (табл. 13.1) [64].
Таблица 13.1. Уровни доказательности и степени рекомендаций на основании руководства Оксфордского центра доказательной медицины
|
Уровень |
Исследования методов диагностики |
Исследования методов лечения |
|
1а |
Систематический обзор гомогенных диагностических исследований 1-го уровня |
Систематический обзор гомогенных РКИ |
|
1b |
Валидизирующее когортное исследование с качественным «золотым стандартом» |
Отдельное РКИ (с узким доверительным интервалом) |
|
1с |
Специфичность или чувствительность столь высокие, что положительный или отрицательный результат позволяет исключить/установить диагноз |
Исследование «Всё или ничего» |
|
2а |
Систематический обзор гомогенных диагностических исследований >2-го уровня |
Систематический обзор (гомогенных) когортных исследований |
Табл. 13.1. Окончание
|
Уровень |
Исследования методов диагностики |
Исследования методов лечения |
|
2b |
Разведочное когортное исследование с качественным «золотым стандартом» |
Отдельное когортное исследование (включая РКИ низкого качества; т.е. с <80% пациентов, прошедших контрольное наблюдение) |
|
2с |
Нет |
Исследование «исходов»; экологические исследования |
|
3а |
Систематический обзор гомогенных исследований уровня 3b и выше |
Систематический обзор гомогенных исследований «случай–контроль» |
|
3b |
Исследование с непоследовательным набором или без проведения исследования «золотого стандарта» у всех испытуемых |
Отдельное исследование «случай– контроль» |
|
4 |
Исследование «случай–контроль» или исследование с некачественным или зависимым «золотым стандартом» |
Серия случаев (и когортные исследования или исследования «случай– контроль» низкого качества) |
|
5 |
Мнение экспертов без тщательной критической оценки или основанное на физиологии, лабораторные исследования на животных или разработка «первых принципов» |
Мнение экспертов без тщательной критической оценки, лабораторные исследования на животных или разработка «первых принципов» |
|
Степени рекомендаций | ||
|
A |
Согласующиеся между собой исследования 1-го уровня | |
|
B |
Согласующиеся между собой исследования 2-го или 3-го уровня или экстраполяция на основе исследований 1-го уровня | |
|
C |
Исследования 4-го уровня или экстраполяция на основе уровня 2 или 3 | |
|
D |
Доказательства 4-го уровня или затруднительные для обобщения или некачественные исследования любого уровня | |
ВАЛИДИЗАЦИЯ РЕКОМЕНДАЦИЙ
Настоящие рекомендации составлены общероссийской общественной организацией «Ассоциация колопроктологов России», в предварительной версии были рецензированы независимыми экспертами, которых попросили прокомментировать прежде всего, насколько интерпретация доказательств, лежащих в основе рекомендаций, доступна для понимания. Получены комментарии со стороны врачей амбулаторного звена. Полученные комментарии тщательно систематизировались и обсуждались на совещаниях экспертной группы.
Последние изменения в настоящих рекомендациях были представлены для дискуссии на заседании профильной комиссии «Колопроктоло-
гия» Экспертного совета Минздрава России 12 сентября 2013 г. Проект рекомендаций был повторно рецензирован независимыми экспертами и врачами амбулаторного звена. Для окончательной редакции и контроля качества рекомендации были повторно проанализированы членами экспертной группы, которые пришли к заключению, что все замечания и комментарии приняты во внимание, риск систематических ошибок при разработке рекомендаций сведен к минимуму.
ОБЛАСТЬ ПРИМЕНЕНИЯ РЕКОМЕНДАЦИЙ
Данные рекомендации применимы при осуществлении медицинской деятельности в рамках Порядка оказания медицинской помощи взрослому населению с заболеваниями толстой кишки, анального канала и промежности колопроктологического профиля.
Определение
Дивертикул — это грыжевидное выпячивание стенки полого органа. По строению дивертикулы разделяют на истинные, в которых просле-
живаются все слои полого органа, и ложные, в стенке которых отсутствует мышечный и подслизистый слой. По происхождению дивертикулы разделяют на врожденные и приобретенные. Истинные дивертикулы по преимуществу врожденные, ложные — приобретенные. По морфофункциональным особенностям выделяют пульсионные дивертикулы, возникающие в результате действия внутрипросветного давления на стенку полого органа, и тракционные дивертикулы, формирующиеся в результате фиксации органа и деформации его стенки.
Дивертикулез — это наличие множественных дивертикулов полого
органа.
Дивертикулез ободочной кишки — это состояние, при котором в толстой кишке имеется хотя бы один дивертикул.
При дивертикулезе ободочной кишки дивертикулы по происхождению приобретенные, по строению — ложные, по морфофункциональным особенностям — пульсионные. Преимущественная локализация дивертикулов — ободочная кишка, в прямой кишке дивертикулы образуются крайне редко.
Выделяют два типа дивертикулеза — «западный» и «восточный». При «западном» типе дивертикулеза в первую очередь поражаются левые отделы ободочной кишки. В 95% дивертикулы располагаются в сигмовидной или сигмовидной и нисходящей ободочной кишке. Наибольшее количество дивертикулов и высокая плотность их расположения находятся в сигмовидной кишке. Эти показатели снижаются в проксимальном направлении, однако нередким бывает сегментарное поражение ободочной кишки дивертикулами, например, они определяются в сигмовидной и поперечной ободочной кишке, а в других отделах их нет.
Преимущественная географическая распространенность «западного» типа дивертикулеза — США, Канада, Европа, Россия, Австралия.
«Восточный» тип дивертикулеза характерен для стран Дальнего Востока и Юго-Восточной Азии. При этом дивертикулы локализуются в слепой и восходящей кишке. Распространенность его в десятки и сотни раз ниже, чем его «западный» вариант, в данных клинических рекомендациях «восточный» тип не рассматривается.
Дивертикулярная болезнь — это заболевание, клинические, морфологические и функциональные проявления которого определяются патологическими изменениями как минимум одного из дивертикулов [3, 6].
Патогенез
Стенка дивертикула представлена слизистой оболочкой, тонким соединительнотканным слоем, образующимся из дегенерировавших мышечного и подслизистого слоев. В дивертикуле различают устье, шейку, тело и дно.
Дивертикул может быть окружен жировой тканью, если располагается в жировом подвеске или брыжейке ободочной кишки, или же поверхностный слой дивертикула может быть представлен серозной оболочкой, если он располагается в интраперитонеальной части ободочной кишки. Если дно дивертикула не выходит за пределы стенки, то такой дивертикул называют неполным, или интрамуральным.
Размеры дивертикулов колеблются в пределах от 1 до 150 мм, в сред-
нем составляя 3–8 мм. Устья дивертикулов располагаются вблизи мышечных тений. В этих местах конечные ветви прямых сосудов проходят сквозь циркулярный мышечный слой в подслизистое сосудистое сплетение. Кровоснабжение дивертикула осуществляется за счет сосудов подслизистого слоя, плотно расположенных в области шейки дивертикула. От этих сосудов отходит конечная ветвь, которая достигает дна дивертикула.
Возникновение дивертикулов в стенке ободочной кишки в первую очередь обусловлено изменением эластических свойств соединительной ткани. При повышении внутрипросветного давления это приводит к пролапсу слизистой оболочки через «слабые» участки кишечной стенки — места прохождения сквозь нее сосудов.
Развитию «слабости» соединительной ткани способствуют преобладание в рационе рафинированной пищи животного происхождения и недостаток нутриентов растительного происхождения, в том числе грубой волокнистой клетчатки. Экспериментально было доказано, что при таком рационе существенно увеличивается количество поперечных сшивок в коллагеновых волокнах, достоверно растет доля III типа коллагена и возрастает концентрация эластина. Это снижает растяжимость и вязкоупругие свойства соединительной ткани, делает ее более плотной
и хрупкой. Помимо дивертикулеза, эти изменения характерны также для процессов старения. Совокупное действие обоих факторов приводит к значительному росту заболеваемости дивертикулезом от 10% в возрасте 40 лет до 60% в возрасте 70 лет. В 3 раза реже дивертикулы выявляют у вегетарианцев и чаще у лиц с ожирением, сниженной двигательной активностью, а также при врожденных дефектах структуры соединительной ткани (синдром Марфана, Энлоса–Данлоса, поликистоз почек) [19]. Дефицит растительной клетчатки, кроме того, приводит к уменьшению объема и повышению плотности каловых масс, что инициирует нарушения двигательной активности ободочной кишки: даже на незначительное раздражение кишка реагирует в виде хаотичных сокращений перемешивающего типа. Как следствие, формируются короткие замкнутые сегменты с повышенным внутрипросветным давлением. Параллельно с этим в стенке кишки снижается число клеток Кахаля (основных пейсмекеров моторики) и уменьшается количество нейронов в интрамуральных ганглиях, что, в свою очередь, усиливает выраженность на-
рушений двигательной активности, образуя порочный круг [3, 43, 56].
В основе развития дивертикулярной болезни, в отличие от дивертикулеза, лежат воспалительные изменения в стенке дивертикулов. Задержка эвакуации содержимого из тела дивертикула через его узкую шейку приводит к образованию плотного комка, называемого фекалитом. При полной обструкции шейки дивертикула в его теле развиваются процессы воспаления, а в просвете накапливается экссудат. Если в результате размягчения фекалита воспалительным экссудатом не происходит его эвакуации через шейку в просвет кишки, то развивается реактивное воспаление окружающих дивертикул тканей, а затем пропитывание окружающих тканей воспалительным экссудатом. В зависимости от реактивных свойств организма и вирулентности инфекционного агента воспаление может варьировать от незначительного отека окружающей кишку жировой клетчатки до перфорации дивертикула с развитием перитонита [3, 46, 53].
После стихания процессов острого воспаления полного восстановления структурной целостности стенки дивертикула не происходит. Дефекты стенки при этом заполняются грануляционной тканью, которая находится в постоянном контакте с агрессивным содержимым толстой кишки с высокой концентрацией микроорганизмов. Поскольку мышечный и подслизистый слои в дивертикуле отсутствуют, при разрушении базальной мембраны и собственной пластики слизистой оболочки содержимое кишки контактирует не со стенкой кишки, а околокишечной клетчаткой, создавая условия для перехода процесса в хроническую форму и развития рецидивов дивертикулита.
При дивертикулярной болезни в стенке ободочной кишки развиваются специфические изменения мышечного слоя в виде его разволокнения и утолщения, но не за счет гипертрофии, а вследствие деформации
по типу синусоиды. Эти изменения максимально выражены в области воспаленного дивертикула и постепенно убывают по мере удаления от источника воспаления.
Механизм развития кровотечения из дивертикула состоит в том, что при эвакуации фекалита через шейку в ее узкой части происходит повреждение рыхлой отечной слизистой оболочки. Именно в этом месте шейку дивертикула обвивают конечные ветви vasarecta.
Код по Международной классификации болезней 10-го пересмотра
n Класс: Болезни органов пищеварения (XI).
n Блок: Другие болезни кишечника K55–K63.
n Код:
v K57.2.
v К57.3.
n Название:
v Дивертикулярная болезнь толстой кишки с прободением и абсцессом.
v Дивертикулярная болезнь толстой кишки без прободения и абсцесса.
Классификация
СОВРЕМЕННЫЕ КЛАССИФИКАЦИИ ДИВЕРТИКУЛЯРНОЙ БОЛЕЗНИ
Универсальной классификации дивертикулярной болезни ободочной кишки не существует. Большинство современных специалистов придерживаются следующей принципиальной иерархии (табл. 13.2):
Таблица 13.2. Определение и классификационные признаки состояний, связанных с дивертикулами ободочной кишки
|
Определение |
Классификационные признаки |
|
A. Дивертикулез ободочной кишки |
1. Наличие дивертикулов. 2. Отсутствие каких-либо симптомов, причиной которых могут быть дивертикулы |
|
Б. Клинически выраженный дивертикулез |
1. Наличие дивертикулов. 2. Наличие клинической симптоматики, происхождение которой может быть связано с наличием дивертикулов в кишке. 3. Отсутствие признаков воспалительного процесса или кровотечения, источником которых является один из дивертикулов |
|
B. Дивертикулярная болезнь |
1. Наличие дивертикулов. 2. Наличие воспалительного процесса или кровотечения, источником которых является один или несколько дивертикулов ободочной кишки |
Одна из наименее дифференцируемых форм заболевания — клинически выраженный дивертикулез. К этой категории относят лиц с дивертикулами ободочной кишки, предъявляющими какие-либо жалобы (чаще функционального характера), источником которых нельзя не считать толстую кишку, но без каких-либо прямых или косвенных признаков существующего или ранее перенесенного воспаления.
Для определения распространенности воспалительного процесса при острых осложнениях широко применяется классификация
E.J. Hinchey (1978) [31]:
n I стадия — периколический абсцесс или инфильтрат;
n II стадия — тазовый, внутрибрюшной или ретроперитонеальный абсцесс;
n III стадия — генерализованный гнойный перитонит;
n IV стадия — генерализованный каловый перитонит.
В Германии и Центральной Европе распространена классификация
O. Hansen, W. Stock (1999) [30]:
n стадия 0 — дивертикулез;
n стадия 1 — острый неосложненный дивертикулит;
n стадия 2 — острый осложненный дивертикулит:
v перидивертикулит / флегмонозный дивертикулит;
v дивертикулярный абсцесс (прикрытая перфорация дивертикула);
v свободная перфорация дивертикула;
n стадия 3 — хронический дивертикулит.
Классификации Хинчи и Хансена–Штока имеют эмпирическое происхождение. Классификацию Хинчи, созданную для определения выраженности и распространенности острых осложнений, часто и ошибочно
применяют для диагностики хронических осложнений. В классификации Хансена и Штока нет места большинству вариантов хронических осложнений.
Осложнения дивертикулярной болезни целесообразно разделять на острые и хронические (табл. 13.3).
Таблица 13.3. Классификация дивертикулярной болезни Государственного научного центра колопроктологии
|
Острые осложнения |
Хронические осложнения |
|
I. Острый дивертикулит |
I. Хронический дивертикулит: • рецидивирующее течение; • непрерывное течение; • латентное течение |
|
II. Острый паракишечный инфильтрат (периколическая флегмона) |
II. Стеноз |
|
III. Перфоративный дивертикулит: • абсцесс; • гнойный перитонит; • каловый перитонит |
III. Хронический паракишечный инфильтрат: • рецидивирующее течение; • непрерывное течение |
|
IV. Толстокишечное кровотечение |
IV. Свищи ободочной кишки: • внутренние; • наружные |
|
|
V. Рецидивирующее толстокишечное кровотечение |
К острым осложнениям относят воспалительные осложнения или кровотечения, впервые возникшие в жизни. При остром воспалении наблюдается каскад типовых реакций, направленных на ликвидацию повреждающего агента. Если же повреждающий агент продолжает действовать, то происходит наслоение разных фаз воспаления друг на друга и заболевание становится хроническим.
К хроническим формам следует относить ситуации, если добиться ликвидации воспалительного процесса не удается в течение более чем 6 нед или же в этот срок и позже развивается рецидив воспаления.
Под дивертикулитом следует понимать ситуацию, когда воспаление локализуется в самом дивертикуле и распространяется на прилежащую клетчатку и стенку кишки на расстояние менее чем на 7 см без вовлечения в воспалительный процесс брюшной стенки или других органов брюшной полости.
Острый паракишечный инфильтрат (периколическая флегмона) — это острый воспалительный процесс, при котором воспалительный экссудат пропитывает соседние ткани и близлежащие органы, формируя пальпируемое опухолевидное образование размером ≥7 см без четких границ.
Хронический паракишечный инфильтрат — это хронический воспалительный процесс, при котором образуется опухолевидный инфильтрат
в брюшной полости и малом тазу размером ≥7 см или же распространяется на соседние органы.
Перфоративный дивертикулит — это разрушение стенок дивертикула воспалительным экссудатом с формированием гнойной полости (абсцесс) или развитием перитонита.
Абсцесс может быть периколическим, тазовым и отдаленным. Периколический абсцесс может локализоваться на месте разрушенного дивертикула, в брыжейке кишки или же прикрыт ею и стенкой живота. Тазовый абсцесс формируется, если его стенками, помимо кишки и стенки таза, является как минимум один из тазовых органов. К отдаленным абсцессам относят межпетельные гнойники вне полости малого таза, а также при локализации в других анатомических областях брюшной полости.
Перитонит, как и при других гнойно-воспалительных заболеваниях брюшной полости, дифференцируют по характеру экссудата (серозный, фибринозный, гнойный, каловый) и распространенности (местный, диффузный, разлитой).
Выделены три варианта клинического течения хронических осложнений.
Непрерывное течение — это: а) сохранение признаков воспаления (по данным объективных и дополнительных методов обследования) без тенденции к их стиханию в течение не менее 6 нед с начала лечения острого осложнения; б) возврат клинической симптоматики в течение 6 нед после проведенного лечения. Непрерывное клиническое течение всегда наблюдается при свищах ободочной кишки и стенозе, возможно при хроническом дивертикулите и хроническом паракишечном инфильтрате (≤30%).
Рецидивирующее течение — это вариант клинического течения хронических осложнений, когда после полной ликвидации клинических проявлений осложнения развивается его повторное развитие.
В интервалах между обострениями пациенты жалоб не предъявляют, а данные объективного и дополнительного обследования свидетельствуют об отсутствии классифицирующих признаков осложнений. Рецидивирующее течение наблюдается при хроническом дивертикулите, хроническом паракишечном инфильтрате, толстокишечных кровотечениях. Латентное течение — наличие признаков хронических осложнений без клинической манифестации. К латентному варианту относят ситуацию, когда при эндоскопическом обследовании выявляют дивертикул с гнойным отделяемым без каких-либо клинических проявлений и без признаков перехода воспаления на окружающую клетчатку. Кроме того, латентное течение констатируют в ситуации, когда имеет место разрушение дивертикула с формированием паракишечной полости («неполный внутренний свищ») без соответствующей клинической симптоматики в виде эпизодов болей, лихорадки или же наличия опухолевидного образования в брюшной полости или тазу. Латентное течение
характерно также для стеноза ободочной кишки, ведущим клиническим признаком которого является нарушение проходимости по кишке. Образование рубцово-воспалительной стриктуры в такой ситуации протекает в течение длительного периода времени (≥2 лет) и не сопровождается яркими клиническими проявлениями, а незначительная коррекция диеты приводит к разрешению симптомов осложнения. При этом хронический воспалительный процесс локализуется преимущественно интрамурально, а не в окружающих тканях, как при хроническом паракишечном инфильтрате.
Свищи ободочной кишки разделяют на внутренние и наружные. К вну-
тренним относят коловезикальные, коловагинальные, колоцервикальные, илеоколические. Другие варианты внутренних свищей, например образование свища с тощей кишкой, маточной трубой, уретрой, мочеточником, крайне редки, но описаны в специальной литературе. К редким также относятся случаи, когда гнойная полость имеет патологическое сообщение с внешней средой как через переднюю брюшную стенку, так и органы брюшной полости и/или таза.
Формулировка диагноза
При формулировании диагноза необходимо указать клинический вариант состояния пациента, связанного с диагностированными дивертикулами ободочной кишки, согласно приведенным в таблице 13.2 классификационным признакам, например:
n Дивертикулез ободочной кишки.
n Клинически выраженный дивертикулез.
n Дивертикулярная болезнь.
При дивертикулярной болезни должно быть указание характера осложнения (см. табл. 13.3), например:
n Дивертикулярная болезнь. Острый паракишечный инфильтрат.
n Дивертикулярная болезнь. Перфоративный дивертикулит, разлитой гнойный перитонит.
n Дивертикулярная болезнь. Сигмовезикальный свищ.
n Дивертикулярная болезнь. Хронический дивертикулит, непрерывное течение.
Клиническая картина и диагностика
ДИВЕРТИКУЛЕЗ
Дивертикулезу как таковому свойственно бессимптомное лечение. Цель обследования пациента с дивертикулезом — исключение осложнений при их латентном клиническом течении. Для этого необходимы трансабдоминальное УЗИ, ирригоскопия и колоноскопия. В ходе выполнения диагностической программы оценивают локализацию дивертикулов, их размеры, число, а также толщину и эластичность кишечной стенки.
КЛИНИЧЕСКИ ВЫРАЖЕННЫЙ ДИВЕРТИКУЛЕЗ
Клиническая картина данного варианта заболевания схожа с таковой при СРК. Более того, в настоящее время остается неизвестным, является ли клинически выраженный дивертикулез самостоятельной формой заболевания или же так протекает СРК на фоне дивертикулеза. Пациенты при этом предъявляют жалобы на периодические боли в животе, чаще в левых и нижних отделах. Выраженность болей значительно варьирует от незначительной до интенсивной. Больные также могут отмечать периодически возникающие запоры и поносы, вздутия живота. Диагноз устанавливают при наличии дивертикулов, отсутствии прямых или косвенных признаков воспаления, эпизодов осложнений в анамнезе. Диагностическая программа включает трансабдоминальное УЗИ, у женщин дополнительно — трансвагинальное УЗИ, ирригоскопию и колоноскопию.
ОСТРЫЕ ВОСПАЛИТЕЛЬНЫЕ ОСЛОЖНЕНИЯ
Клиническая картина острых осложнений находится в прямой зависимости от выраженности и распространенности воспалительного процесса.
Так, острый дивертикулит в первую очередь проявляет себя болями, которые локализуются в левой подвздошной области. Наряду с этим, в зависимости от анатомического расположения в брюшной полости воспаленного сегмента, пациенты могут предъявлять жалобы на боли в левой боковой, правой подвздошной и гипогастральной областях. Боли могут быть приступообразными или постоянными, умеренными, не требующими назначения анальгетиков, или выраженными. Боли в большинстве наблюдений сопровождаются лихорадкой и лейкоцитозом. Другие симптомы, такие как вздутие, задержка стула, частый жидкий стул, тошнота, нарушение мочеиспускания и рвота, встречаются реже. При пальпации живота и/или бимануальном (влагалищном или ректальном) исследовании определяется болезненный, относительно подвижный сегмент сигмовидной кишки тестоватой или плотной консистенции. Общее состояние больных при остром дивертикулите удовлетворительное [2, 3, 6].
При остром паракишечном инфильтрате (периколическая флегмона) клиническая симптоматика более выражена, что обусловлено большей интенсивностью и распространенностью воспалительного процесса. Закономерности локализации болей такие же, как и при остром дивертикуле, однако интенсивность их значительнее, и практически всегда возникает необходимость в назначении анальгетиков. Отличительный признак данного варианта острого осложнения — наличие опухолевидного образования в брюшной полости или полости таза, не имеющего четких границ. Возможны умеренное напряжение мышц передней брюшной стенки и слабо выраженные симптомы раздражения брюшины. Пальпация
живота в области инфильтрата достаточно болезненная, а подвижность его ограничена за счет фиксации к передней брюшной стенке, стенкам таза или другим органам. Постоянным признаком периколической флегмоны является лихорадка: у 2/3 пациентов температура тела поднимается выше 38 °С. В зависимости от выраженности интоксикации бывают тахикардия, сухость во рту, тошнота и рвота. Более 2/3 пациентов отмечают также вздутие живота и нарушения стула. Выраженные нарушения кишечной проходимости при периколической флегмоне встречаются редко. Механизм развития этого симптома связан со сдавлением кишки воспалительным инфильтратом извне, внутристеночный компонент воспаления здесь малозначимый. Функция кишечника достаточно быстро восстанавливается после начала антибактериальной терапии на фоне ограничений в диете и назначения масляных слабительных. Общее состояние больных при периколической флегмоне удовлетворительное или реже среднетяжелое.
Клиническая картина при перфоративном дивертикулите (абсцесс
брюшной полости, гнойный или каловый перитонит) не имеет специфических особенностей, указывающих на дивертикулярную болезнь.
При остром периколическом абсцессе гнойная полость локализуется либо в брыжейке сигмовидной кишки, либо в тазу, либо прилежит к передней брюшной стенке. Больные в такой ситуации предъявляют жалобы на достаточно четко локализованные боли в левых и нижних отделах живота постоянного характера, признаки интоксикации выражены умеренно. Усиление болей и распространение их на прилежащие анатомические области, нарастание признаков интоксикации, лихорадка выше 37,5 °С, сухость во рту, тошнота, рвота, тахикардия более 100 в минуту и наличие симптомов раздражения брюшины характерны для вскрытия гнойника в брюшную полость с развитием перитонита.
Перфорация дивертикула в свободную брюшную полость с развитием калового перитонита имеет внезапное начало в виде острых интенсивных болей, быстро принимающих разлитой характер и сопровождающихся клинической картиной интоксикации с присоединением симптомов раздражения брюшины и лихорадки [2, 3, 6, 53].
Лабораторные исследования включают общий и биохимический анализ крови, общий анализ мочи для верификации и определения выраженности воспалительных реакций. При перфоративном дивертикулите, по сравнению с острым дивертикулитом и острым паракишечным инфильтратом, снижен уровень натрия в крови (<136 ммоль/л), уровень С-реактивного белка повышен (>50 мг/л) [61].
Диагностические задачи при острых воспалительных осложнениях дивертикулярной болезни включают:
а) верификацию дивертикула ободочной кишки как источника осложнений (отек и уплотнение прилежащей к воспаленному дивертикулу клетчатки, разрушение стенок дивертикула с формированием параки-
шечной полости, выход воздуха или контрастного вещества через устье одного из дивертикулов);
б) определение клинического варианта острых осложнений (острый дивертикулит, периколическую флегмону, абсцесс, гнойный перитонит, каловый перитонит);
в) оценку распространенности воспалительного процесса (вовлечение брюшной стенки, забрюшинного пространства при периколической флегмоне, локализацию и размер гнойной полости при абсцессе, при перитоните — распространенность поражения брюшины и определение характера экссудата);
г) оценку выраженности интоксикации.
Помимо клинического обследования, первостепенное значение имеют УЗИ брюшной полости и КТ (УД 2a–3a, СР В [40]). Трансабдоминальное УЗИ у женщин целесообразно дополнять трансвагинальным исследованием. Информативность компьютерной томографии повышается при использовании внутривенного контрастирования. Диагностическая ценность УЗИ, КТ и МРТ одинакова. При этом УЗИ имеет преимущество как метод, исключающий дополнительную лучевую нагрузку, поэтому рекомендуется для контроля эффективности лечения. Внутрипросветное контрастирование при КТ следует проводить осторожно, так как высока вероятность перфорации воспаленного дивертикула. Кроме того, при наличии прикрытой перфорации проведение такого исследования может спровоцировать ее трансформацию в перфорацию дивертикула в свободную брюшную полость. Из этих же соображений ограничено и применение колоноскопии, которую целесообразно выполнять после стихания явлений острого воспаления. Ирригоскопия с использованием сульфата бария при острых осложнениях должна быть ограничена. Предпочтение при данном методе исследования следует отдавать водорастворимым контрастным веществам. Информативная ценность ирригоскопии при острых осложнениях достоверно ниже УЗИ и КТ.
Эндоскопические исследования необходимы только для решения
задач дифференциальной диагностики, в первую очередь в отношении рака и воспалительных заболеваний кишечника. При невозможности исключить опухолевый процесс проведение колоноскопии в острой фазе воспаления показано, если по данным КТ нет выхода воздуха за пределы кишечной стенки (УД 1b, СР В [39]).
Дифференциальная диагностика при острых воспалительных осложнениях требует исключения таких заболеваний, как аппендицит, опухоле-
вые заболевания органов брюшной полости и полости таза, острый колит вирусного или бактериального происхождения, острые воспалительные заболевания мочеполовой сферы, болезнь Крона, язвенный колит, острые заболевания жировых подвесок ободочной кишки (заворот, воспаление, некроз).
ХРОНИЧЕСКИЕ ВОСПАЛИТЕЛЬНЫЕ ОСЛОЖНЕНИЯ
При хроническом дивертикулите клинические проявления варьируют в зависимости от характера и выраженности воспалительного процесса. Основным проявлением заболевания бывают боли незначительной или умеренной интенсивности в левых и нижних отделах живота.
При латентном течении хронического дивертикулита клинических проявлений заболевания нет, а диагноз устанавливают по данным до-
полнительных методов обследования.
При непрерывном течении хронического дивертикулита в течение суток боли то периодически усиливаются, то ослабевают. Возможна иррадиация болей в поясничную область, в правую подвздошную область и эпигастральную область. Прием спазмолитических препаратов и анальгетиков позволяет купировать болевой синдром в течение 15–40 мин. Потребность ежедневного приема спазмолитиков и анальгетиков отмечают небольшое количество пациентов.
Пациенты с рецидивирующим течением хронического дивертикулита
вне периодов обострения не предъявляют каких-либо жалоб, или же они минимально выражены. При обострении развивается клиническая картина, как при острых воспалительных осложнениях. Частота обострений колеблется от 1 раза в 3 нед до 1 раза в 1,5 года.
При клиническом исследовании у большинства больных при пальпации в левой подвздошной области определяется плотная болезненная сигмовидная кишка. У части женщин она определяется при влагалищном обследовании.
Стеноз ободочной кишки при дивертикулярной болезни имеет скудную клиническую симптоматику при наличии основного классифицирующего признака — нарушения кишечной проходимости в виде эпизодов вздутия живота, ощущения тяжести в левой подвздошной области и гипогастрии, задержки стула до 3 сут, метеоризм. Симптомы, как правило, разрешаются после ограничения в питании и приема слабительных. У большей части больных в анамнезе можно было проследить эпизоды обострения воспалительного процесса без яркой симптоматики. В течение длительного периода времени, до появления клинических признаков нарушения кишечной проходимости, больные отмечают незначительные локализованные боли в левых отделах живота. Длительность этого периода составляет от 2 до 10 лет (в среднем 5,5 лет). Длительность существования симптомов нарушения кишечной проходимости колеблется от 4 мес до 3 лет [3, 4, 6].
При пальпации у больных в левой подвздошной или левой боковой об-
ласти живота определяется плотный умеренно болезненный сегмент сигмовидной кишки, фиксированный к стенке таза или брюшной стенке. Выше обнаруженного плотного тяжа выявляется умеренное расширение кишки, над которым при перкуссии может отмечаться тимпанический звук. На фоне консервативных мероприятий нарушение кишечной про-
ходимости удается ликвидировать в течение 12–24 ч, однако стойкого длительного эффекта достичь не удается. Расширение же диеты приводит к повторному развитию вздутия живота и задержке стула.
При хроническом паракишечном инфильтрате клиническая картина, характерная для хронического дивертикулита, дополняется наличием опухолевидного образования в брюшной полости, в основном фиксированного к брюшной стенке или другим органам. Как правило, это образование определяется пальпаторно через переднюю брюшную стенку и/или при бимануальном (влагалищном, ректальном) исследовании.
Клиническая картина при свищах ободочной кишки полиморфная и зависит от локализации наружного отверстия, выраженности парафистулярной инфильтрации, направления хода свища, наличия дополнительных гнойных затеков и полостей.
При наружных свищах наружное отверстие, как правило, располагается на передней брюшной стенке в послеоперационных рубцах, но может располагаться в ягодичной и поясничной областях, промежности, бедре. В большинстве наблюдений свищ образуется после экстренного хирургического вмешательства, при котором не была выполнена резекция воспаленного сегмента сигмовидной кишки, а вмешательство было завершено дренированием брюшной полости. Значительно реже наружные свищи образуются после пункции и/или пункции и дренирования абсцесса под контролем УЗИ. Редко свищ формируется после вскрытия абсцесса передней брюшной стенки и поясничной области и крайне редко промежности и бедра.
При внутренних свищах клиническая картина не соответствует тяжести развившегося осложнения, имеет стертый характер. При сигмовезикальных свищах — это выделение газов при мочеиспускании, мутный цвет мочи и примесь в ней кала, незначительные боли в нижних отделах живота без четкой локализации, недомогание, утомляемость и редкие подъемы температуры тела. До развития клинической манифестации кишечно-пузырного свища у этих больных периодически возникают боли в нижних отделах живота, сопровождающиеся лихорадкой. Большинство пациентов отмечают один эпизод резкого усиления болей с подъемом температуры тела, после чего у них начинают выделяться газы при мочеиспускании и/или появляется мутный цвет мочи. В последующем боли значительно ослабевают или же полностью исчезают, а температура тела нормализуется. Менее чем у 1/3 пациентов осложнение проявляется лишь стойкой бактериурией, пневматурией и невыраженной фекалурией, а первыми жалобами бывают выделение газов при мочеиспускании и жалобы на мутный характер мочи. Кишечно-генитальные свищи манифестируют болями незначительной и умеренной интенсивности, гнойно-каловыми выделениями из влагалища. В преобладающем большинстве наблюдений при сигмовагинальных и сигмоцервикальных свищах в анамнезе отмечаются либо экстирпация матки с придатками,
либо надвлагалищная ампутация матки. У 2/3 пациенток возникают периодические боли, которые становятся интенсивными, появляется лихорадка, а затем обильные гнойно-каловые выделения из влагалища, после чего явления интоксикации исчезают [3, 4, 6].
При кишечно-мочепузырных и кишечно-генитальных свищах при сомнениях в наличии патологического соустья проводят пробу Швайбольда (УД 3a–3b; СР В). Проба предполагает прием пациентом семян мака, используемых в кулинарии, в течение 2 сут по 1 чайной ложке семян, запивая их 1 стаканом воды. Общее количество семян мака должно составлять 250 г, необходимо принимать не менее 1,5 л жидкости в сутки. При подозрении на кишечно-мочепузырный свищ наличие семян мака исследуют во всех порциях мочи в проходящем свете, при кишечно-генитальных свищах у женщин — на влагалищных тампонах. Пробу проводят в течение 2 сут [41, 51].
При тонкокишечно-толстокишечных свищах клинические проявления неспецифичны. Они включают умеренные периодические боли, недомогание с субфебрильной лихорадкой, иногда неустойчивый либо учащенный жидкий стул.
При свищах в области внутреннего отверстия в стенке кишки возникает рубцово-воспалительный процесс, более чем в половине наблюдений приводящий к образованию стриктуры. При этом нарушения кишечной проходимости развиваются крайне редко вследствие особенностей строения свища.
Диагностические задачи при хронических воспалительных осложнениях дивертикулярной болезни включают:
n верификацию дивертикула ободочной кишки как источника осложнений;
n определение клинического варианта хронического воспалительного осложнения (хронический дивертикулит, хронический паракишечный инфильтрат, свищ, стеноз);
n оценку распространенности воспалительного процесса (утолщение кишечной стенки за счет деформации ≥3 мм, вовлечение в воспалительный процесс периколической клетчатки, брюшной стенки, забрюшинного пространства, других органов брюшной полости и таза, при свищах — их топографо-анатомическую характеристику).
Диагностическая программа включает основные, дополнительные (уточняющие) и интраоперационные методы диагностики.
Основные методы:
n клиническое обследование и изучение анамнеза;
n лабораторные исследования крови и мочи;
n рентгенологические методы (КТ с внутривенным и внутрипросветным контрастированием, ирригоскопия, при свищах — фистулография, цистография, вагинография, рентгенография тонкой кишки);
n колоноскопия;
n УЗИ (трансабдоминальное, трансвагинальное, трансректальное).
Уточняющие методы исследования:
n ультразвуковая колоноскопия;
n исследование двигательной активности толстой кишки и внутрипросветного давления.
Интраоперационные методы:
n УЗИ толстой кишки с целью определения границ резекции.
Дифференциальная диагностика при хронических воспалительных осложнениях требует исключения таких заболеваний, как рак толстой кишки, иные опухолевые заболевания органов брюшной полости и полости таза, СРК, болезнь Крона, язвенный колит, ишемический колит.
ТОЛСТОКИШЕЧНЫЕ КРОВОТЕЧЕНИЯ
Кровотечение как осложнение дивертикулярной болезни проявляется выделениями крови, которая может быть алого цвета, темного цвета, может быть со сгустками. Кровотечение возникает на фоне общего благополучия и не сопровождается никакими иными симптомами дивертикулярной болезни. Приблизительно в 1/3 наблюдений объем кровопотери превышает 500 мл.
Первичное диагностическое мероприятие при этом — колоноскопия, при которой в устье одного из дивертикулов можно обнаружить либо кровоточащий сосуд, либо фиксированный к стенке сгусток. Диагностическая эффективность колоноскопии составляет 69–80% при остром кровотечении. Возможность обнаружения кровоточащего дивертикула при этом составляет 10–20%, причем в случае выявления описанного симптома высока вероятность неэффективности консервативных мероприятий или рецидива кровотечения. К другим методам диагностики относятся КТ-ангиография, сцинтиграфия с эритроцитами, меченными изотопом технеция 99m (99mTc). Эффективность этих методов достигает 90%, а необходимость их применения возникает при малой информативности колоноскопии. Наряду с этим диагностическая программа должна включать обследование верхних отделов ЖКТ [29, 58].
Дифференциальная диагностика требует исключения в качестве при-
чины кровотечения опухоли или полипа толстой кишки, язвенного колита, болезни Крона, ишемического колита, инфекционного колита, ангиодисплазии, ятрогенных причин (предшествующая биопсия или полипэктомия), геморроя.
Лечение
КЛИНИЧЕСКИ ВЫРАЖЕННЫЙ ДИВЕРТИКУЛЕЗ
Лечение данной формы заболевания не отличается от лечения СРК, проводится в течение длительного времени с обязательным учетом индивидуальных особенностей и включает коррекцию диеты и назначение селективных спазмолитиков. Как правило, рекомендуется высокошла-
ковая диета с дополнительным введением в рацион нерастворимых растительных волокон (пшеничные отруби в дозе 20–32 г/сут, мукофальк♠, микрокристаллическая целлюлоза-200) (А, В). Возможно применение способа лечения, при котором в дополнении к высокошлаковой диете назначают рифаксимин (УД 1b, СР А [13]). Препарат назначают по 400 мг 2 раза в день в течение недели 1 раз в месяц в течение года, эффективность лечения увеличивается в 2 раза.
Эффективная ликвидация клинической симптоматики также достигается путем назначения месалазина в дозе 400 мг 2 раза в сутки в течение 10 дней. Курс лечения повторяют ежемесячно в течение 1 года (УД 2b, СР B [27]).
В зависимости от индивидуальных особенностей при комплексном лечении клинически выраженного дивертикулеза назначают слабительные при запоре и пробиотики.
При отсутствии эффекта от проводимого лечения необходимо повторить диагностические исследования, направленные на исключение маловыраженного воспалительного процесса.
ОСТРЫЕ ОСЛОЖНЕНИЯ
При остром дивертикулите и остром паракишечном инфильтрате (периколической флегмоне) показано консервативное лечение [2, 16, 52].
Отсутствие эффекта от проводимого лечения, прогрессирование выраженности явлений воспаления или ранний рецидив указывают на недиагностированное разрушение дивертикула и наличие более тяжелых осложнений.
Цели консервативного лечения состоят в предотвращении дальнейшего распространения острого воспаления и создании оптимальных условий для эвакуации воспалительного экссудата из дивертикула в просвет кишки.
Исходя из этих целей, консервативное лечение включает бесшлаковую диету (молочные продукты, отварное мясо, рыба, яйцо, омлет), прием вазелинового масла по 1–4 столовые ложки в сутки, назначение селективных спазмолитиков и антибиотиков широкого спектра действия.
При лечении острого дивертикулита предпочтительно назначение пероральных антибиотиков (УД 1а, СР А [49]).
Существует также обоснованная точка зрения, что при невыраженной клинической симптоматике, а также достаточной уверенности в отсутствии более тяжелых осложнений антибактериальные препараты можно не назначать (УД 1b, СР A [17, 32]).
Лечение острого дивертикулита, в зависимости от выраженности клинических проявлений, а также с учетом индивидуальных особенностей, возможно как в амбулаторных условиях, так и в условиях стационара. Длительность пребывания в стационаре определяется лечебными и диагностическими задачами в каждом отдельном клиническом случае.
При наличии уверенности в том, что воспалительный процесс локализован и имеется выраженный эффект от проводимого лечения, возможно проведение лечения или его продолжение в амбулаторных условиях. Риск развития рецидивного эпизода воспаления у лиц, перенесших атаку острого дивертикулита или переход в хроническую форму, не превышает 30% [2–4, 6].
При периколической флегмоне имеет место более выраженный и распространенный воспалительный процесс, что требует парентерального назначения антибиотиков, а также проведения детоксикационных мероприятий. Лечение должно проводиться в условиях стационара. Риск развития рецидивного эпизода воспаления у лиц, перенесших атаку острого паракишечного инфильтрата (периколической флегмоны) или же переход заболевания в хроническую форму, составляет более 50% [2, 4, 37].
При остром абсцессе возможны несколько вариантов лечения. При размере периколического абсцесса до 3 см предпочтение следует отдавать консервативному лечению. При размере абсцесса ≥3 см или отсутствии эффекта от проводимого консервативного лечения показаны пункция и дренирование абсцесса под контролем УЗИ или КТ и дальнейшее проведение консервативного лечения вплоть до максимально возможной ликвидации воспалительного процесса (УД 3a, СР C). Такая тактика позволяет избежать хирургического вмешательства у 30–40% пациентов. При отсутствии выраженного лечебного эффекта от малоинвазивного лечения показано хирургическое вмешательство. При остром абсцессе имеет место разрушение стенок одного из дивертикулов, поэтому переход воспаления в хроническую форму, а также вероятность формирования свищей толстой кишки весьма высока (УД 2b, СР C). У большинства пациентов в последующем возникает необходимость в плановом хирургическом лечении [4, 11, 22, 54].
При других формах перфоративного дивертикулита показано экстренное хирургическое лечение (УД 3а, СР В). Цель хирургического вмешательства — удаление сегмента толстой кишки с разрушенным дивертикулом из брюшной полости, так как борьба с абдоминальным сепсисом наиболее эффективна в условиях ликвидации источника инфекции. При этом наиболее эффективной является резекция сегмента с перфорацией (УД 1а, СР В). Ушивание дивертикула при его перфорации противопоказано вследствие крайне высокой летальности (УД 2b, СР B [2, 23, 27, 38, 55]).
Если имеет место перфорация сегмента ободочной кишки с длинной брыжейкой, то возможно выполнение операции экстериоризации — выведение перфорированного сегмента на переднюю брюшную стенку в виде двуствольной колостомы. Однако стремление к выполнению такого варианта вмешательства часто связано с высоким риском развития тяжелых перистомальных осложнений, поэтому необходимо отдавать предпочтение резекции перфорированного сегмента.
При хирургическом лечении перфоративного дивертикулита не следует пытаться решить при экстренной операции задачи, стоящие перед плановыми вмешательствами. Не следует пытаться иссекать и удалять все воспаленные участки, дополнительно мобилизовать левый изгиб и входить в пресакральное пространство, тем самым открывая новые пути для гнойно-воспалительного процесса. Кроме того, нет необходимости удалять дистальную часть сигмовидной кишки при экстренной операции, если в этом сегменте нет участка с перфорацией. Крайне важно хирургу до ушивания передней брюшной стенки вскрыть удаленный препарат, чтобы убедиться в отсутствии опухоли. При невозможности исключения злокачественного процесса необходимо выполнение ререзекции кишки по онкологическим принципам.
Операцией выбора при перфоративном дивертикулите является опе-
рация Гартмана или Микулича [2, 3, 12, 46, 53].
В тщательно отобранных клинических случаях, при локализованном абсцессе, начальных стадиях перитонита у больных без выраженных сопутствующих заболеваний возможно выполнение резекции толстой кишки с формированием толстокишечного анастомоза (УД 2b, СР B [12, 20, 28, 47, 48, 50, 63]). Операцию при этом целесообразно дополнять превентивной двуствольной илеоили колостомой.
Лечение перитонита при дивертикулярной болезни ободочной кишки должно проводиться согласно общим принципам лечения абдоминального сепсиса без какой-либо специфики.
ХРОНИЧЕСКИЕ ОСЛОЖНЕНИЯ
В лечении хронических воспалительных осложнений консервативный подход играет ведущую роль.
При рецидивирующем течении хронического дивертикулита или хронического паракишечного инфильтрата в стадию обострения воспалительного процесса лечение проводят так же, как и при острых осложнениях [4, 16].
При непрерывном варианте клинического течения хронического дивертикулита или хронического паракишечного инфильтрата лечение должно проводиться до достижения клинического эффекта не менее 1 мес. При этом возможна смена антибактериальных препаратов и спазмолитиков, включение в схему лечения не всасывающихся в просвете кишки антибиотиков [13]. После ликвидации воспалительных явлений необходимы постепенный переход на высокошлаковую диету, периодический прием спазмолитиков [9].
Неэффективность консервативных мероприятий констатируют в случае сохранения клинической картины заболевания после как минимум двух проведенных курсов комплексной консервативной терапии, сохранения или же прогрессирования признаков воспалительного процесса по данным дополнительных методов исследования, развития раннего или частого рецидивирования (2 раза в год и более) [4].
Показания к плановому хирургическому лечению при дивертикулярной болезни относительные, их устанавливают индивидуально на основании выраженности перенесенных воспалительных осложнений, оценки эффективности проводимых консервативных мероприятий и прогноза дальнейшего течения заболевания [4, 11, 26, 46, 50].
Факт наличия воспалительного процесса должен быть подтвержден хотя бы одним из соответствующих этой цели методов исследования (УЗИ, КТ или МРТ).
Основной предиктор неэффективности консервативного лечения — наличие признаков разрушения одного из дивертикулов, что должно быть подтверждено хотя бы одним из методов исследований: УЗИ, КТ, МРТ, ультразвуковой колоноскопией (УД 2b–3a, СР C [4, 22, 26, 37]). При наличии признаков разрушения одного из дивертикулов во время или после первой атаки острого воспаления, вне зависимости от результатов проведенного лечения, показано плановое хирургическое лечение [2, 4].
Кроме того, показанием к плановой операции служит невозможность исключения опухолевого процесса в толстой кишке.
Остальные факторы должны рассматриваться в качестве дополнительных: возраст до 50 лет, количество рецидивных атак, длительный системный прием нестероидных противовоспалительных средств, иммуносупрессивная терапия, коллагеновые и сосудистые заболевания, выраженность сопутствующих заболеваний [37].
Наличие свища ободочной кишки как осложнения дивертикулярной болезни считается показанием к плановому хирургическому лечению. Свищи ободочной кишки при дивертикулярной болезни не имеют тенденции к спонтанному закрытию, так как внутреннее отверстие свища представляет собой устье дивертикула с сохранной слизистой оболочкой. Консервативные мероприятия при свищах следует рассматривать как подготовку к хирургическому вмешательству. Они позволяют достичь лишь кратковременного снижения интенсивности и распространенности парафистулярного воспаления и проводятся с целью создания оптимальных условий для выполнения хирургического вмешательства, а не в качестве самостоятельного метода лечения [4, 6, 41, 46].
При стенозе консервативные мероприятия также малоэффективны вследствие выраженности рубцово-воспалительных изменений в стенке кишки и должны быть направлены на ликвидацию явлений нарушений кишечной проходимости с целью создания оптимальных условий для выполнения хирургического вмешательства и формирования первичного анастомоза.
Противовоспалительные мероприятия в качестве предоперационной подготовки при этом нецелесообразны. Основной метод лечения стеноза — хирургический [4, 26, 37].
Правильный выбор объема резекции толстой кишки при дивертикулярной болезни — ведущий фактор достижения хороших результатов
лечения. При плановом хирургическом лечении хронических осложнений дивертикулярной болезни необходимо придерживаться следующих принципов [1, 7, 46].
1. Не следует стремиться к удалению всех отделов толстой кишки, имеющих дивертикулы.
2. В границы резекции обязательно должны быть включены отделы с признаками воспаления.
3. При определении границ резекции необходимо удалить сегменты с утолщенной и деформированной кишечной стенкой. Ведущим и наиболее точным методом диагностики степени изменения кишечной стенки при этом является интраоперационное УЗИ.
4. Формирование анастомоза желательно между отделами с неутолщенной эластичной стенкой, не содержащей дивертикулы в непосредственной близости к линии кишечного шва.
5. При невозможности выполнить условия 3 и 4 формирование первичного анастомоза целесообразно сочетать с наложением проксимальной кишечной стомы.
При выполнении перечисленных условий риск осложнений со стороны анастомоза и риск рецидива дивертикулярной болезни минимальные (УД 2b–3b, CР С [7, 46, 53, 59, 60]).
При хирургическом лечении хронических осложнений дивертикулярной болезни следует стремиться к выполнению операций с применением лапароскопических технологий (УД 1b, СР A [26, 36, 45, 46]).
При выполнении реконструктивно-восстановительных вмешательств у лиц, перенесших операции с формированием кишечной стомы, необходимо учитывать особенности дивертикулярной болезни [1].
При этом, как правило, формирование толстокишечного анастомоза должно дополняться резекцией отключенных и/или функционирующих отделов по перечисленным выше принципам. В противном случае риск развития несостоятельности толстокишечных анастомозов многократно увеличивается (УД 4, СР C [1, 5, 26, 46]).
ТОЛСТОКИШЕЧНЫЕ КРОВОТЕЧЕНИЯ
При дивертикулярной болезни в большинстве наблюдений острые толстокишечные кровотечения останавливаются самостоятельно (~86% наблюдений). В любом случае необходимо выполнить колоноскопию для верификации этого факта. При толстокишечном кровотечении проводят гемостатическую терапию, как и при других вариантах желудочно-кишечного кровотечения, а также отменяют прием антиагрегантных, антикоагулянтных и нестероидных противовоспалительных средств. При эндоскопической верификации источника кровотечения необходимо выполнить остановку кровотечения путем инъекции эпинефрина, электрокоагуляции, клиппирования кровоточащего сосуда. При неэффективности эндоскопической остановки кровотечения жела-
тельно выполнить селективную артериографию с эмболизацией, эффективность которой составляет 76–100% с риском рецидива кровотечения менее 20% (УД 4, СР D [10, 15, 21, 25, 34]).
Хирургическое вмешательство при остром толстокишечном кровотечении показано в следующих ситуациях.
n Рецидивирующее или продолжающееся кровотечение при неэффективности других методов остановки кровотечения.
n Необходимость большого объема гемотрансфузии (не менее 4 доз в течение 24 ч).
n Нестабильная гемодинамика, некорригируемая при проведении интенсивной терапии.
Среди пациентов, требующих неотложного хирургического вмешательства, летальность составляет 10–20%.
Методом выбора хирургического лечения при остром толстокишечном кровотечении является сегментарная резекция при условии точной дооперационной топической диагностики источника кровотечения (УД 3а, СР С [18]). Вероятность рецидива толстокишечного кровотечения в течение 1 года после такого вмешательства составляет 14%. При отсутствии точной верификации источника кровотечения вероятность рецидива кровотечения после сегментарной резекции увеличивается до 42%.
Субтотальная колэктомия показана при отсутствии точной верификации источника кровотечения. В такой ситуации частота осложнений увеличивается до 37%, а летальность — до 33%. Вероятность рецидива толстокишечного кровотечения в течение 1 года после такого вмешательства составляет 0%.
При рецидивирующих кровотечениях показания к плановому хирургическому лечению устанавливают в зависимости от количества эпизодов кровотечения (≥2), объема кровопотери при каждом из эпизодов, необходимости приема пациентами антикоагулянтов [10, 15, 18].
Профилактика
Профилактика как самого дивертикулеза, так и перехода его в состояние дивертикулярной болезни однотипная. Она включает преимущественное содержание в рационе растительной клетчатки в количестве не менее 25 г/сут, контроль частоты стула и консистенции кала, профилактику ожирения. Такой режим питания достоверно снижает риск развития осложнений дивертикулярной болезни (УД 1b, СР В [9, 19, 57]).
Курение незначительно увеличивает риск развития перфоративного дивертикулита [33].
Преобладание в рационе содержания красного мяса и жиров незначительно увеличивает риск дивертикулярной болезни [19].
Роль приема алкоголя, кофеина, орехов не доказана [8,33]. Достоверно чаще дивертикулез и дивертикулярная болезнь разви-
ваются в группах пациентов с индексом массы тела ≥30 кг/м2, низкой
физической активностью, при уровне систематического ежедневного приема пищи с содержанием растительной клетчатки в дозе ≤15 г/сут, а также при генетически детерминированных заболеваниях соединительной ткани (синдром Марфана, Элерса–Данлоса, поликистоз почек) [8, 9, 19, 56, 57].
Наибольший риск развития осложнений дивертикулеза отмечается в группах пациентов, с нарушениями обычного течения воспалительных реакций. Это наблюдается при приеме нестероидных противовоспалительных средств, глюкокортикоидов и опиатов [37]. Дополнительное внимание необходимо уделять пациентам с гигантскими дивертикулами ободочной кишки размером более 3 см. Риск развития кровотечений высок при приеме антиагрегантов, нестероидных противовоспалительных средств, антикоагулянтов [15].
Скрининг
Скрининг необходим в группе пациентов, перенесших эпизод острых воспалительных осложнений, особенно в группах с высокой вероятностью развития повторных и более выраженных осложнений.
Критерии оценки качества помощи в стационаре представлены в таблице 13.4. Для оценки качества медицинской помощи используют временные, процессуальные и профилактирующие критерии. Временные характеризуют своевременность оказания определенных этапов медицинской помощи. Выполнение пациенту ряда медицинских манипуляций, инструментальных и лабораторных исследований, необходимых для качественного оказания медицинской помощи, оценивают в процессуальных критериях. Для анализа мероприятий, направленных на предотвращение развития осложнений, используют профилактирующие критерии.
Таблица 13.4. Критерии оценки качества медицинской помощи в стационаре больным с дивертикулярной болезнью ободочной кишки (0 — нет, 1 — да)
|
Клинические рекомендации |
Временные |
Процессуальные |
Профилактирующие |
|
Клинические рекомендации по диагностике и лечению взрослых пациентов с дивертикулярной болезнью (код МКБ — К57.0–57.9) |
Установка клинического диагноза в течение 72 ч: 0/1 |
Пальцевое исследование прямой кишки: 0/1. Клинический анализ крови; биохимический анализ крови; клинический анализ мочи; коагулограмма: 0/1. Трансабдоминальное УЗИ: 0/1. Колоноскопия: 0/1. Лучевая диагностика состояния толстой кишки (КТ и/или ирригоскопия): 0/1. |
Отсутствие осложнений • кровотечение: 0/1; • пневмония: 0/1; • тромбоэмболия: 0/1; • перитонит: 0/1; • летальный исход: 0/1 |
Табл. 13.4. Окончание
|
Клинические рекомендации |
Временные |
Процессуальные |
Профилактирующие |
|
|
|
Метод консервативного лечения в соответствии с установленным диагнозом и клиническими рекомендациями: 0/1. Метод оперативного лечения в соответствии с клиническими рекомендациями: 0/1 |
|
Литература
1. Ачкасов С.И. Хирургическая тактика при восстановительном лечении осложненного дивертикулеза ободочной кишки: Автореф. дис. … канд. мед. наук. — М., 1992. — 24 с.
2. Болихов К.В. Острые воспалительные осложнения дивертикулярной болезни ободочной кишки (клиника, диагностика, лечение): Автореф. дис. … канд. мед. наук. — М., 2006. — 30 с.
3. Воробьев Г.И. Основы колопроктологии. — М., 2006. — 432 с.
4. Москалев А.И. Клинико-морфофункциональные параллели при хронических осложнениях дивертикулярной болезни: Автореф. дис. … канд. мед. наук. — М., 2007. — 29 с.
5. Саламов К.Н., Ачкасов С.И., Солтанов Б.Ц. Место проксимальной колостомии в многоэтапном лечении осложненного дивертикулеза ободочной кишки // Рос. журн. гастроэнтерол., гепатол., колопроктол. — 1995. — № 1. — С. 77–80.
6. Шелыгин Ю.А., Благодарный Л.А. Справочник по колопроктологии. —
М.: Литтерра, 2012. — 608 с.
7. Саламов К.Н., Воробьев Г.И., Ачкасов С.И. и др. Определение границ резекции ободочной кишки при дивертикулезе // Хирургия. — 2001. — № 1.— С. 80–86.
8. Aldoori W.H., Giovannucci E.L., Rimm E.B. et al. A prospective study of alcohol, smoking, caffeine, and the risk of symptomatic diverticular disease in men // Ann. Epidemiol. — 1995. — Vol. 5. — P. 221–228.
9. Aldoori W.H., Giovannucci E.L., Rockett H.R.H. et al. A prospective study of
dietary fiber and symptomatic diverticular disease in men // J. Nutr. — 1998. — Vol. 128. — P. 714–719.
10. Andress H.J., Mewes A., Lange V. Endoscopic hemostasis of a bleeding diverticulum of the sigma with fibrin sealant // Endoscopy. — 1993. — Vol. 25, N 2. — P. 193.
11. Bahadursingh A.M. et al. Spectrum of disease and outcome of complicated
diverticular disease // Am. J. Surg. — 2003. — Vol. 186. — P. 696–701.
12. Belmonte C., Klas J.V., Perez J.J. et al. The Hartmann procedure. First choice or last resort in diverticular disease? // Arch. Surg. — 1996. — Vol. 131. — P. 612–615.
13. Bianchi M., Festa V., Moretti A. et al. Meta-analysis: longterm therapy with rifaximin in the management of uncomplicated diverticular disease // Aliment. Pharmacol. Ther. — 2011. — Vol. 33. — P. 902–910.
14. Broderick-Villa G., Burchette R.J., Collins J.C. et al. Hospitalization for acute diverticulitis does not mandate routine elective colectomy // Arch. Surg. — 2005. — Vol. 140. — P. 576–581.
15. Browder W., Cerise E.J., Litwin M.S. Impact of emergency angiography in massive lower gastrointestinal bleeding // Ann. Surg. — 1986. — Vol. 204, N 5. — P. 530–536.
16. Byrnes M.C., Mazuski J.E. Antimicrobial therapy for acute colonic diverticulitis // Surg. Infect. (Larchmt.). — 2009. — Vol. 10, N 2. — P. 143–154.
17. Chabok A., Påhlman L., Hjern F. et al. Randomized clinical trial of antibiotics in acute uncomplicated diverticulitis // Br. J. Surg. — 2012, Jan 30. — doi: 10.1002/ bjs.8688.
18. Chen C.Y., Wu C.C., Jao S.W. et al. Colonic diverticular bleeding with comorbid diseases may need elective colectomy // J. Gastrointest. Surg. — 2009. — Vol. 13, N 3. — P. 516–520.
19. Commane D.M., Arasaradnam R.P., Mills S. et al. Diet, ageing and genetic factors in the pathogenesis of diverticular disease // World J. Gastroenterol. — 2009. — Vol. 15, N 20. — P. 2479–2488.
20. Constantinides V.A., Tekkis P.P., Athanasiou T. et al. Primary resection with anastomosis vs. Hartmann procedure in nonelective surgery for acute colonic diverticulitis: a systematic review // Dis. Colon Rectum. — 2006. — Vol. 49, N 7. — P. 966–981.
21. DeBarros J., Rosas L., Cohen J. et al. The changing paradigm for the treatment of colonic hemorrhage: superselective angiographic embolization // Dis. Colon Rectum. — 2002. — Vol. 45, N 6. — P. 802–808.
22. Durmishi Y., Gervaz P., Brandt D. et al. Results from percutaneous drainage of Hinchey stage II diverticulitis guided by computer tomography scan // Surg. Endosc. — 2006. — Vol. 20. — P. 1129–1133.
23. Eng K., Ranson J.C.H., Localio S.A. Resection of the perforated segment. A significant advance in treatment of diverticulitis with free perforation or abscess // Am. J. Surg. — 1977. — Vol. 133. — P. 67–72.
24. Etzioni D.A., Mack T.M., Beart R.W. et al. Diverticulitis in the United States: 1998–2005. Changing patterns of disease and treatment // Ann. Surg. — 2009. — Vol. 249. — P. 210–217.
25. Farrell J.J., Graeme-Cook F., Kelsey P.B. Treatment of bleeding colonic diverticula by endoscopic band ligation: an in-vivo and ex-vivo pilot study // Endoscopy. — 2003. — Vol. 35, N 10. — P. 823–829.
26. Fozard J.B.J., Armitage N.C., Schofield J.B. et al. ACPGBI position statement on elective resection for diverticulitis // Colorectal Dis. — 2011. — Vol. 13. — Suppl. 3. — P. 1–11.
27. Giffin J.M., Butcher H.R., Ackerman L.V. Surgical management of colonic diverticulitis // Arch. Surg. — 1967. — Vol. 94. — P. 619–626.
28. Gooszen A.W., Tollenaar R.A., Geelkerken R.H. et al. Prospective study of primary anastomosis following sigmoid resection for suspected acute complicated diverticular disease // Br. J. Surg. — 2001. — Vol. 88. — P. 693–697.
29. Green B.T., Rockey D.C., Portwood G. et al. Urgent colonoscopy for evaluation and management of acute lower gastrointestinal hemorrhage: a randomized controlled trial // Am. J. Gastroenterol. — 2005. — Vol. 100, N 11. — P. 2395–2402.
30. Hansen O., Stock W. Prophylaktische Operation bei der Divertikelkrankheit des Kolons — Stufenkonzept durch exakte Stadieinteilung // Langenbecks Arch. Chir. — 1999. — Suppl. II. — P. 1257–1260.
31. Hinchey E.J., Schaal P.G.H., Richards G.K. Treatment of perforated diverticular disease of the colon // Adv. Surg. — 1978. — Vol. 12. — P. 85–109.
32. Hjern F., Josephson T., Altman D. et al. Conservative treatment of acute diverticulitis: are antibiotics always mandatory? // Scand. J. Gastroenterol. — 2007. — Vol. 42, N 1. — P. 41–47.
33. Hjern F., Wolk A., Hakansson N. Smoking and the risk of diverticular disease in women // Br. J. Surg. — 2011. — Vol. 98, N 7. — P. 997–1002.
34. Hokama A., Uehara T., Nakayoshi T. et al. Utility of endoscopic hemoclipping for colonic diverticular bleeding // Am. J. Gastroenterol. — 1997. — Vol. 92, N 3. — P. 543–546.
35. Humes D.J. Changing epidemiology: does it increase our understanding? // Dig. Dis. — 2012. — Vol. 30. — P. 6–11.
36. Jones O.M., Stevenson A.R.L., Clark D. et al. Laparo, Dec. — Vol. 248, N 6. — P. 1092–1097.
37. Klarenbeek B.R., Samuels M., van der Wal M.A. et al. Indications for elective sigmoid resection in diverticular disease // Ann. Surg. — 2010. — Vol. 251, N 4. — P. 670–674.
38. Kronborg O. Treatment of perforated sigmoid diverticulitis: a prospective randomized trial // Br. J. Surg. — 1993. — Vol. 80. — P. 505–507.
39. Lahat A., Yanai H., Menachem Y. et al. The feasibility and risk of early colonoscopy in acute diverticulitis: a prospective controlled study // Endoscopy. — 2007. — Vol. 39, N 6. — P. 521–524.
40. Liljegren G., Chabok A., Wickbom M. et al. Acute colonic diverticulitis: a systematic review of diagnostic accuracy // Colorectal Dis. — 2007. — Vol. 9, N 6. — P. 480–488.
41. Melchior S., Cudovic D., Jones J. et al. Diagnosis and surgical management of colovesical fistulas due to sigmoid diverticulitis // J. Urol. — 2009. — Vol. 182, N 3. — P. 978–982.
42. Nguyen G.C., Steinhart A.H. Nationwide patterns of hospitalizations to centers with high volume of admissions for inflammatory bowel disease and their impact on mortality // Inflamm. Bowel Dis. — 2008. — Vol. 14. — P. 1688–1694.
43. Painter N.S., Burkitt D.P. Diverticular disease of the colon, a 20th century problem // Clin. Gastroenterol. — 1975. — Vol. 4, N 1. — P. 3–21.
44. Pittet O., Kotzampassakis N., Schmidt S. et al. Recurrent left colonic episodes: more severe than the initial diverticulitis? // World J. Surg. — 2009. — Vol. 33, N 3. — P. 547–552.
45. Purkayastha S., Constantinides V.A., Tekkis P.P. et al. Laparoscopic vs. open resection for diverticular disease: A metaanalysis of non-randomized studies // Dis. Colon Rectum. — 2006. — Vol. 49. — P. 446–463.
46. Rafferty J., Shellito P., Hyman N.H., Buie W.D. Standards Committee of the American Society of Colon and Rectal Surgeons. Practice parameters for sigmoid diverticulitis // Dis. Colon Rectum. — 2006. — Vol. 49. — P. 939–944.
47. Regenet N., Pessaux P., Hennekinne S. et al. Primary anastomosis after intraoperative colonic lavage vs. Hartmann’s procedure in generalized peritonitis
complicating diverticular disease of the colon // Int. J. Colorectal Dis. — 2003. — Vol. 18. — P. 503–507.
48. Richter S., Lindemann W., Kollmar O. et al. One stage sigmoid colon resection for perforated diverticulitis (Hinchey stages III and IV) // World J. Surg. — 2006. — Vol. 30. — P. 1027–1032.
49. Ridgway P.F., Latif A., Shabbir J. et al. Randomized controlled trial of oral vs
intravenous therapy for the clinically diagnosed acute uncomplicated diverticulitis // Colorectal Dis. — 2008. — Vol. 11. — P. 941–946.
50. Salem L., Flum D.R. Primary anastomosis or Hartmann’s procedure for patients with diverticular peritonitis? A systematic review // Dis. Colon Rectum. — 2004. — Vol. 47. — P. 1953–1964.
51. Schwaibold H., Popiel C., Geist E. et al. Oral intake of poppy seed: a reliable
and simple method for diagnosing vesico-enteric fistula // J. Urol. —2001. — Vol. 166, N 2. — P. 530–531.
52. Schug-Pass C., Geers P., Hügel O. et al. Prospective randomized trial comparing short-term antibiotic therapy versus standard therapy for acute uncomplicated sigmoid diverticulitis // Int. J. Colorectal Dis. — 2010. — Vol. 25, N 6. — P. 751–759.
53. Schoetz D.J. Diverticular disease of the colon: a century old problem // Dis.
Colon Rectum 1999. — Vol. 42. — P. 703–709.
54. Siewert B., Tye G., Kruskal J. et al. Impact of CT-guided drainage in the treatment of diverticular abscesses: size matters // AJR Am. J. Roentgenol. — 2006. — Vol. 186. — P. 680–686.
55. Smiley D.F. Perforated sigmoid diverticulitis with spreading peritonitis // Am. J. Surg. — 1966. — Vol. 111. — P. 431–435.
56. Strate L.L., Liu Y.L., Aldoori W.H. et al. Physical activity decreases diverticular complications // Am. J. Gastroenterol. — 2009. — Vol. 104. — P. 1221–1230.
57. Strate L.L., Liu M.S., Aldoori W.H. et al. Obesity increases the risk of diverticulitis and diverticular bleeding // Gastroenterology. — 2009. — Vol. 136, N 1. — P. 115–122.
58. Suzuki K., Uchiyama S., Imajyo K. et al. Risk factors for colonic diverticular hemorrhage: Japanese multicenter study // Digestion. — 2012. — Vol. 85. — P. 261–265.
59. Thaler K., Baig M.K., Berho M. et al. Determinants of recurrence after
sigmoid resection for uncomplicated diverticulitis // Dis. Colon Rectum. — 2003. — Vol. 46. — P. 385–388.
60. Tocchi A., Mazzoni G., Fornasari V. et al. Preservation of the inferior mesenteric artery in colorectal resection for complicated diverticular disease // Am. J. Surg. — 2001. — Vol. 182, N 2. — P. 162–167.
61. Tursi A. Biomarkers in diverticular diseases of the colon // Dig Dis. —
2012. — Vol. 30. — P. 12–18.
62. Tursi A., Brandimarte G., Giorgetti G.M., Elisei V. Mesalazine and or Lactobacillus casei in preventing recurrence of symptomatic uncomplicated diverticular disease of the colon: a prospective, randomized, open-label study //
J. Clin. Gastroenterol. — 2006. — Vol. 40. — P. 312–316.
63. Umbach T.V., Dorzio R.A. Primary resection and anastomosis for perforated left colon lesions // Am. Surg. — 1999. — Vol. 65. — P. 931–933.
64. Willie-Jørgensen P., Renehan A.G. Systematic reviews and meta-analyses in coloproctology: interpretation and potential pitfalls // Colorectal Dis. — 2007. — Vol. 10. — P. 21–32.
БОЛЕЗНЬ ГИРШПРУНГА
Введение
Реабилитация пациентов с аномалиями развития и положения толстой кишки остается одной из наиболее сложных проблем в колопроктологии. Болезнь Гиршпрунга является достаточно распространенной аномалией развития. Частота возникновения болезни Гиршпрунга на протяжении нескольких десятилетий колеблется от 1:30 тыс. до 1:2000 к общему числу новорожденных (СР 4, УД D [12, 27, 45]).
Установлено, что во всех исследованиях преобладали пациенты мужского пола. У мальчиков заболевание встречается в 5 раз чаще, чем у девочек (СР 4, УД D [8, 15, 21]).
Распространенность аганглиоза толстой кишки значительно варьирует среди этнических групп. Данное заболевание встречается в Европе у 1 из 4500 новорожденных, а в Японии — у 1 из 4697 родившихся детей. Болезнь Гиршпрунга регистрируется у 1,5 из 10 тыс. человек, родившихся в кавказском регионе, у 2,1 из 10 тыс. новорожденных афроамериканцев и у 2,8 из 10 тыс. детей азиатского происхождения (СР 4, УД D [6, 26]).
Существует разница в частоте различных форм заболевания в зависимости от протяженности зоны аганглиоза. Случаи с коротким сегментом встречаются гораздо чаще и составляют до 80% общего числа. Остальные 20% наблюдений приходятся на пациентов, у которых аганглионарный сегмент распространяется проксимальнее прямой кишки (СР 4, УД D [18, 31, 38]).
Болезнь Гиршпрунга часто является семейным заболеванием. Риск возникновения этого заболевания у родственников значительно выше по сравнению с остальным населением. Из всех регистрируемых семейные случаи аганглиоза составляют 20% (СР 4, УД D [6, 40]).
В настоящее время болезнь Гиршпрунга считается полиэтиологичным заболеванием.
На 7–12-й неделе беременности происходит нарушение формирования нервных структур на определенном участке прямой кишки. Происходят значительные изменения в нервных сплетениях Ауэрбаха (мышечный слой) и Мейснера (подслизистый слой), а иногда и полное их отсутствие (СР 4, УД D [5, 18]).
Доказан генетический гетерогенный характер аномалии. Исследования в области молекулярной генетики указывают на ведущую роль в развитии
болезни Гиршпрунга 4 генов: RET (рецептор тирозинкиназы), GDNF (нейтрофический фактор глиальных клеток), ENDRB (ген рецептора эндотелина-В), EDN3 (эндотелин-3) и их определяющее влияние на процесс миграции нейробластов (СР 4, УД D [17, 34, 37]). Таким образом, в настоящее время основная теория, объясняющая отсутствие ганглиев в толстой кишке, — нарушение миграции нейробластов из вагусного нервного гребешка в процессе эмбриогенеза, и чем раньше прекращается миграция, тем длиннее аганглионарный сегмент (СР 4, УД D [13, 29, 30]). Кроме этого, существует гипотеза, согласно которой аганглиоз развивается вследствие нарушения дифференцировки нервных клеток, уже достигших кишечной стенки. Влиять на созревание клеток могут различные факторы, такие как гипоксия, воздействие химических агентов,
повышенная радиация, вирусная инфекция (СР 4, УД D [8, 15]).
Сочетание генетических нарушений с патологическим влиянием внешней и внутренней среды определяет характер поражения не только интрамурального нервного аппарата. По данным разных авторов, сочетание болезни Гиршпрунга с другими пороками развития происходит в 29–32,7% случаев (СР 4, УД D [12, 15, 24]).
Один из основных элементов в патогенезе болезни Гиршпрунга — изменение в гистологической структуре интрамурального нервного аппарата на определенном отрезке толстой кишки. Эти изменения состоят главным образом в отсутствии ганглиев мышечно-кишечного и подслизистого сплетений. На месте ганглиев определяются лишь нервные волокна и мелкие глиальные клетки (СР 4, УД D [1, 25]). Накопление ацетилхолинэстеразы в слизистой оболочке наряду с отсутствием медиаторов, обеспечивающих тормозящий эффект в кишечной стенке, вызывает стойкий спазм, который служит патогенетическим признаком болезни Гиршпрунга (СР 4, УД D [4, 22]).
Настоящие рекомендации по диагностике и лечению болезни Гиршпрунга у взрослых являются руководством для практических врачей, осуществляющих ведение и лечение таких пациентов. Рекомендации подлежат регулярному пересмотру в соответствии с новыми данными научных исследований в этой области. Представленные рекомендации составлены на основании данных литературы. Они включают следующие разделы: определение и классификация болезни Гиршпрунга, диагностика, хирургическое лечение. Ниже приведены уровни доказательности согласно общепринятой классификации Оксфордского центра доказательной медицины (табл. 14.1).
ВАЛИДИЗАЦИЯ РЕКОМЕНДАЦИЙ
Настоящие рекомендации в предварительной версии были рецензированы независимыми экспертами, которых попросили прокомментировать прежде всего, насколько интерпретация доказательств, лежащих в основе рекомендаций, доступна для понимания. Получены комментарии со стороны врачей амбулаторного звена. Полученные комментарии
Таблица 14.1. Уровни доказательности и степени рекомендаций на основании руководства Оксфордского центра доказательной медицины
|
Уровень |
Диагностическое исследование |
Терапевтическое исследование |
|
1а |
Систематический обзор гомогенных диагностических исследований 1-го уровня |
Систематический обзор гомогенных РКИ |
|
1b |
Валидизирующее когортное исследование с качественным «золотым стандартом» |
Отдельное РКИ (с узким доверительным интервалом) |
|
1с |
Специфичность или чувствительность столь высокие, что положительный или отрицательный результат позволяет исключить/установить диагноз |
Исследование «Всё или ничего» |
|
2а |
Систематический обзор гомогенных диагностических исследований >2-го уровня |
Систематический обзор (гомогенных) когортных исследований |
|
2b |
Разведочное когортное исследование с качественным «золотым стандартом» |
Отдельное когортное исследование (включая РКИ низкого качества; т.е. с <80% пациентов, прошедших контрольное наблюдение) |
|
2с |
Нет |
Исследование «исходов»; экологические исследования |
|
3а |
Систематический обзор гомогенных исследований уровня 3b и выше |
Систематический обзор гомогенных исследований «случай–контроль» |
|
3b |
Исследование с непоследовательным набором или без проведения исследования «золотого стандарта» у всех испытуемых |
Отдельное исследование «случай–контроль» |
|
4 |
Исследование «случай–контроль» или исследование с некачественным или зависимым «золотым стандартом» |
Серия случаев (и когортные исследования или исследования «случай–контроль» низкого качества) |
|
5 |
Мнение экспертов без тщательной критической оценки или основанное на физиологии, лабораторные исследования на животных или разработка «первых принципов» |
Мнение экспертов без тщательной критической оценки, лабораторные исследования на животных или разработка «первых принципов» |
|
Степени рекомендаций | ||
|
А |
Согласующиеся между собой исследования 1-го уровня | |
|
В |
Согласующиеся между собой исследования 2-го или 3-го уровня или экстраполяция на основе исследований 1-го уровня | |
|
С |
Исследования 4-го уровня или экстраполяция на основе уровня 2 или 3 | |
|
D |
Доказательства 4-го уровня или затруднительные для обобщения или некачественные исследования любого уровня | |
тщательно систематизировались и обсуждались на совещаниях экспертной группы.
Последние изменения в настоящих рекомендациях были представлены для дискуссии на заседании профильной комиссии «Колопроктология» Экспертного совета Минздрава России 12 сентября 2013 г. Проект рекомендаций был повторно рецензирован независимыми экспертами и врачами амбулаторного звена. Для окончательной редакции и контроля качества рекомендации были повторно проанализированы членами экспертной группы, которые пришли к заключению, что все замечания и комментарии приняты во внимание, риск систематических ошибок при разработке рекомендаций сведен к минимуму.
ОБЛАСТЬ ПРИМЕНЕНИЯ РЕКОМЕНДАЦИЙ
Данные клинические рекомендации применимы при осуществлении медицинской деятельности в рамках Порядка оказания медицинской помощи взрослому населению с заболеваниями толстой кишки, анального канала и промежности колопроктологического профиля.
Определение
Болезнь Гиршпрунга — это аномалия развития, характеризуемая врожденным отсутствием ганглиев интрамуральных и подслизистых нервных сплетений кишечной стенки всей толстой кишки или ее части (СР 4, УД D [6, 31]).
Существуют варианты заболевания с минимальной выраженностью симптомов, что позволяет части пациентов доживать до зрелого возраста, даже не подозревая о наличии у них порока развития толстой кишки. Такие пациенты представляют собой особую категорию больных, требующую нестандартной оценки и индивидуального подхода. Это позволяет рассматривать болезнь Гиршпрунга у взрослых в качестве отдельной формы заболевания (СР 4, УД D [3, 8]).
Код по Международной классификации болезней 10-го пересмотра
n Класс XVII — врожденные аномалии, деформации и хромосомные нарушения.
n Блок (Q38–Q45) — другие врожденные аномалии (пороки развития) органов пищеварения.
n Код: Q43.1.
Классификация
Классификация болезни Гиршпрунга основывается на анатомической локализации аганглиоза, распространенности мегаколон и выраженности клинических проявлений заболевания. Классификация заболе-
вания у взрослых пациентов построена на основании тех же критериев, что и у детей, однако по ряду параметров имеются различия (СР 4, УД D [5, 31]). Анатомические формы заболевания у взрослых подразделяются следующим образом.
n Наданальная форма — зона поражения локализуется в нижнеампулярном отделе прямой кишки.
n Ректальная форма — недоразвитие интрамурального нервного аппарата распространяется на всю прямую кишку.
n Ректосигмоидная форма — аганглиоз занимает всю прямую кишку и часть или всю сигмовидную кишку.
n Субтотальная форма — в аганглионарный сегмент включена поперечная ободочная кишка.
n Тотальная форма — поражение всей толстой кишки.
Мегаколон при болезни Гиршпрунга может ограничиваться одним отделом толстой кишки или распространяться на несколько ее участков. При тотальной форме аганглиоза выявляется расширение подвздошной кишки. Определяется следующая локализация расширения кишечника.
n Мегаректум.
n Мегасигма.
n Левосторонний мегаколон.
n Субтотальный мегаколон.
n Тотальный мегаколон.
n Мегаилеум.
Функциональное состояние мегаколон может быть компенсированным, субкомпенсированным и декомпенсированным.
n Компенсированное состояние кишки — на протяжении многих лет у больного отмечается редкий, но самостоятельный стул или имеется запор от 3 до 7 дней, которые легко разрешаются с помощью слабительных препаратов и клизм.
n Субкомпенсированное состояние, в отличие от предыдущего, требует интенсивных мероприятий по опорожнению кишки. В таких случаях без применения слабительных препаратов и клизм самостоятельный стул может отсутствовать свыше 7 дней.
n Декомпенсированное состояние характеризуется отсутствием позыва на дефекацию и самостоятельного стула. У многих пациентов толстая кишка бывает заполнена плотным кишечным содержимым или каловыми камнями. Зачастую даже интенсивные мероприятия не позволяют адекватно опорожнить толстую кишку. В подобных случаях показано срочное хирургическое лечение.
По клиническому течению у взрослых различают три варианта развития заболевания.
1. Типичный («детский») вариант — интенсивный запор развивается достаточно быстро, практически отсутствует самостоятельный стул, быстро нарастают явления кишечной непроходимости.
2. Пролонгированный вариант — медленное течение заболевания, когда с запором удается длительное время справляться с помощью консервативных мероприятий.
3. Латентный вариант — впервые запор появляется после 14 лет, и, как правило, быстро развивается хроническая толстокишечная непроходимость. Появившейся запор нарастает, слабительные средства совершенно неэффективны, и для опорожнения кишки приходится прибегать к ежедневным клизмам.
Формулировка диагноза
При формулировании диагноза следует отразить протяженность аганглионарной зоны, распространенность расширения толстой кишки и степень ее компенсации, а также наличие осложнений болезни Гиршпрунга. Ниже приведены примеры формулировок диагноза.
n Болезнь Гиршпрунга, наданальная форма, мегаректум, мегасигма, субкомпенсированная.
n Болезнь Гиршпрунга, ректальная форма, субтотальный мегаколон, осложненная нарушением кишечной проходимости.
Диагностика
КЛИНИЧЕСКАЯ КАРТИНА
Симптомы болезни Гиршпрунга обычно возникают в раннем детстве. Однако ее клинические проявления могут иметь стертую картину у детей и развиться в зрелом возрасте. Главной причиной обращения в клинику является запор, который отмечают все пациенты. При этом у большинства больных наблюдается отсутствие самостоятельного стула. Этот симптом всегда сочетается с отсутствием позыва на дефекацию. У ряда пациентов может быть позыв на дефекацию и самостоятельный стул, однако остается ощущение неполного опорожнения толстой кишки. Наличие самостоятельного стула у этих пациентов обусловлено сохранившейся пропульсивной способностью тех отделов толстой кишки, которые располагаются проксимальнее аганглионарной зоны (СР 4, УД D [3, 38]).
Вздутие живота регистрируется у половины пациентов. Этот симптом отмечается на фоне длительного отсутствия самостоятельного стула и исчезает после опорожнения толстой кишки. Боли в животе носят, как правило, приступообразный характер и возникают на высоте запора, который купируется применением очистительных клизм (СР 4, УД D [5, 10, 43]).
Тошнота и рвота появляются, как правило, при декомпенсированном состоянии, сопровождаются болями в животе, длительным отсутствием самостоятельного стула. У ряда пациентов могут отмечаться слабость и недомогание как проявление общей интоксикации (СР 4, УД D [35]).
У взрослых пациентов практически не развиваются явления энтероколита, столь характерного для детей, страдающих болезнью Гиршпрунга (СР 4, УД D [6]).
При объективном осмотре у многих пациентов отмечается развернутый реберный угол. На фоне вздутия, увеличения в размерах толстой кишки заметны асимметрия живота, увеличение его в размерах, с растянутой передней брюшной стенкой и видимой на глаз перистальтикой. В то же время при адекватно проводимых консервативных мероприятиях мегаколон развивается медленно, что позволяет сохранить нормальную форму живота (СР 4, УД D [5, 31]).
При компенсированном состоянии пальпация живота у пациентов с болезнью Гиршпрунга может быть малоинформативной. При субкомпенсированном и декомпенсированном мегаколоне пальпаторно определяется раздутая газами или заполненная каловыми массами ободочная кишка, наиболее часто сигмовидная кишка. Она имеет форму баллонообразного цилиндра, располагающегося, как правило, в левой половине живота. В случае переполнения кишки содержимым на ней остаются пальцевые вдавления. У ряда пациентов могут пальпироваться каловые камни, которые в некоторых наблюдениях смещаются в просвете кишки (СР 4, УД D [3, 38]). Осмотр промежности, перианальной области неинформативен. Ректальное исследование у больных наданальной формой заболевания позволяет выявить наличие каловых масс или копролитов в ампуле прямой
кишки (СР 4, УД D [10, 31]).
ИНСТРУМЕНТАЛЬНЫЕ ИССЛЕДОВАНИЯ
Рентгенологические методы исследования
Эти методы дают возможность оценить функциональное и морфологическое состояние толстой кишки, что существенно влияет на выбор дальнейшей диагностической и лечебной тактики (СР 4, УД D [2, 5, 10]). Обзорная рентгенография брюшной полости без предварительной подготовки позволяет определить наличие признаков кишечной непроходимости, выявить каловые камни. Ирригоскопия дает возможность установить наличие или отсутствие зоны сужения, ее протяженность, а также распространенность мегаколона и состояние нерасширенных отделов ободочной кишки. При этом оценивается сократительная способность кишечной стенки, выраженность гаустрации ободочной кишки, полноценность ее опорожнения и наличие продольной складчатости слизистой оболочки в расширенных отделах. При ирригоскопии контролируются уровень и степень заполнения толстой кишки, выбирается проекция для наилучшего выявления зоны сужения, которая обычно соответствует аганглионарному сегменту. Рельеф слизистой оболочки изучается после опорожнения толстой кишки от контрастных сред (СР 4, УД D [3, 8, 31]). Поскольку при болезни Гиршпрунга имеется очевидная причина нарушения пассажа кишечного содержимого – аганглионарный сегмент, у большинства пациентов нет необходимости в изучении моторно-эва-
куаторной функции толстой кишки. (СР 4, УД D [3, 16]).
Эндоскопические методы исследования
Наиболее простым и доступным методом является ректороманоскопия, которая дает возможность осмотреть прямую и дистальную часть сигмовидной кишки. При подозрении на болезнь Гиршпрунга это исследование проводится без специальной подготовки. При наличии аганглиоза выраженный спазм стенки дистального отдела толстой кишки не позволяет каловым массам проникать в суженный участок, что является патогномоничным признаком заболевания. Проксимальнее суженного участка обнаруживается расширенная часть кишки, содержащая каловые массы. В этом отделе определяются сглаженность и продольная направленность складок слизистой оболочки, иногда ее атрофия или гиперемия (СР 4, УД D [8, 31]).
Колоноскопия считается вспомогательным методом исследования при болезни Гиршпрунга, так как полноценная подготовка толстой кишки затруднена и большие размеры кишки создают значительные трудности проведения аппарата в связи с отсутствием достаточной площади фиксации колоноскопа [6].
Физиологические методы исследования
У больных с подозрением на болезнь Гиршпрунга важным диагностическим тестом является аноректальная манометрия, в частности, исследование ректоанального ингибиторного рефлекса (рефлекторного расслабления внутреннего сфинктера в ответ на повышение давления в прямой кишке). Отсутствие ректоанального ингибиторного рефлекса является надежным диагностическим критерием болезни Гиршпрунга с чувствительностью 70–95%.
Ректоанальный рефлекс вызывается путем раздражения прямой кишки баллоном, в который нагнетается воздух. Объем наполнения прямой кишки — 10–70 мл. Каждое последующее раздражение проводится через 40–60 с. При этом определяется порог и латентный период ректоанального рефлекса внутреннего сфинктера, а также амплитудно-временные характеристики рефлекторных ответов, которые подсчитываются при объеме раздражения прямой кишки в 50 мл. Эта величина раздражения прямой кишки в норме у всех вызывает устойчивый ректоанальный рефлекс — расслабление внутреннего сфинктера. Отсутствие расслабления внутреннего сфинктера или значительное уменьшение амплитуды и длительности его сокращений свидетельствуют о нарушении внутристеночной нервной передачи, характерной для аномалии развития интрамуральной нервной системы прямой кишки (СР 4, УД D [9, 23]).
Гистохимическая и морфологическая диагностика
Гистохимическая и морфологическая диагностика основана на выявлении ацетилхолинэстеразы в собственной пластинке слизистой оболочки аганглионарного сегмента толстой кишки. Установлено, что на-
копление ацетилхолинэстеразы в аганглионарной зоне значительно больше, чем в нормально иннервированном участке толстой кишки. Это обстоятельство послужило для разработки гистохимического метода диагностики аганглиоза [4, 22]. Материал для определения уровня ацетилхолинэстеразы берется с уровня 5, 10 и 15 см от края анального канала.
В последние годы наиболее активно используется иммуногистохимическая диагностика, направленная на выявление нервных волокон, содержащих оксид азота (NO). Он является нейротрансмиттером, осуществляющим передачу импульсов, расслабляющих внутренний сфинктер. Специфическая качественная реакция демонстрирует отсутствие оксида азота в аганглионарной зоне. Это исследование наиболее ценно для определения диагноза болезни Гиршпрунга с ультракоротким аганглионарным сегментом, когда нет характерной рентгенологической картины и при отсутствии ректоанального рефлекса обнаруживаются ганглии в биоптате стенки прямой кишки (СР 4, УД D [20, 32, 33]). Решающее значение в диагностике болезни Гиршпрунга имеет биопсия стенки прямой кишки. Методика предложена O. Swenson (1955) и заключается в иссечении полнослойного фрагмента стенки прямой кишки на расстоянии 3 см от зубчатой линии с последующим исследованием этого участка на наличие интрамуральных ганглиев. Необходимость в этой инвазивной процедуре возникает при дифференциальной диагностике идиопатического мегаколона и болезни Гиршпрунга, когда имеются противоречия между данными аноректальной манометрии, результатами пробы на ацетилхолинэстеразу и рентгенологической картиной. Выявление аганглиоза межмышечного и подслизистого нервных сплетений является надежным подтверждением болезни Гиршпрунга. Следует помнить, что зона физиологического гипои аганглиоза может распространяться до 5 см проксимальнее зубчатой линии [3]. Во избежание ложноположительного результата исследования рекомендуется выполнение биопсии путем иссечения полнослойного лоскута шириной 1 см по задней стенке прямой кишки от зубчатой линии протяженностью не менее 6 см (СР 4, УД D [4, 36]).
ДИАГНОСТИЧЕСКИЕ КРИТЕРИИ
В настоящее время разработаны клинико-диагностические критерии болезни Гиршпрунга у взрослых, которые включают:
n запор в анамнезе с детского возраста;
n наличие зоны относительного сужения в дистальных отделах толстой кишки с супрастенотическим расширением на ирригограммах;
n отсутствие ректоанального ингибиторного рефлекса при аноректальной манометрии;
n положительную реакцию слизистой оболочки прямой кишки на ацетилхолинэстеразу. При совокупности указанных признаков можно установить болезнь Гиршпрунга.
В сомнительных случаях при отсутствии характерного анамнеза, наличии нечеткой рентгенологической картины, ослабленной реакции внутреннего сфинктера на растяжение прямой кишки, слабоположительной реакции на ацетилхолинэстеразу необходимо проводить трансанальную биопсию стенки прямой кишки по Свенсону в предложенной модификации для оценки состояния интрамурального нервного сплетения. Данный метод позволяет установить диагноз заболевания практически у всех пациентов (СР 4, УД D [3, 10, 38]).
Лечение
ОБЩИЕ ПОЛОЖЕНИЯ
Лечение болезни Гиршпрунга у взрослых, как и у детей, в настоящее время возможно только хирургическим путем (СР 4, УД D [2, 39]). Задача лечения — нормализация пассажа кишечного содержимого по толстой кишке и беспрепятственная его эвакуация через анальный канал. Этой цели можно добиться с помощью исключения аганглионарной зоны из кишечного транзита и восстановления эвакуаторной способности лежащих выше отделов толстой кишки (СР 4, УД D [5, 11, 45]). Успех хирургического лечения болезни Гиршпрунга у взрослых зависит от следующих обстоятельств:
n Радикальности удаления аганглионарной зоны.
n Объема резекции декомпенсированных отделов ободочной кишки.
n Адекватной подготовки к операции.
ПЛАНОВОЕ ХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕ
Для хирургического лечения болезни Гиршпрунга предложены различные оперативные вмешательства (операции Соаве, Ребейна, Свенсона, Дюамеля), однако они применяются главным образом у детей, и их выполнение у взрослых пациентов значительно ухудшает функциональные результаты лечения (СР 4, УД D [14, 19, 41]). В настоящее время методом выбора хирургического лечения болезни Гиршпрунга у взрослых является операция Дюамеля в модификации Государственного научного центра колопроктологии (ГНЦК) (СР 4, УД D [3, 7, 8]). Данное оперативное вмешательство преследует следующие цели:
n Максимальное удаление аганглионарной зоны без излишней травматизации тазовых органов.
n Исключение возможности повреждения внутреннего сфинктера.
n Безопасность и асептичность формирования колоректального анастомоза.
n Профилактику несостоятельности колоректального анастомоза.
n Предотвращение формирования слепого мешка в культе прямой кишки.
n Создание условий для хорошей функции анастомоза.
n Уменьшение количества послеоперационных осложнений.
ОПЕРАЦИЯ ДЮАМЕЛЯ В МОДИФИКАЦИИ ГОСУДАРСТВЕННОГО НАУЧНОГО ЦЕНТРА КОЛОПРОКТОЛОГИИ
Техника операции Дюамеля в модификации Государственного научного центра колопроктологии
Операцию Дюамеля в модификации ГНЦК проводят в два этапа.
Первый этап выполняется двумя бригадами хирургов. Выполняются резекция ободочной и прямой кишки с резекцией аганглионарной зоны и формирование колоректального концебокового ретроректального анастомоза с избытком по Дюамелю.
Лапаротомия выполняется только срединным разрезом. Задача интраоперационной ревизии состоит в определении проксимальной границы аганглионарной зоны, степени изменений лежащих выше отделов на уровне функционирующей части толстой кишки. Аганглионарная зона у взрослых по внешнему виду мало чем отличается от здоровой кишки. В ряде случаев удается визуализировать участок явного сужения, однако его можно принять и за участок спазма кишечной стенки.
Расширенная декомпенсированная часть толстой кишки при болезни Гиршпрунга имеет очень характерный внешний вид. Степень расширения может быть различной и по величине, и по протяженности, но всегда отмечается выраженная гипертрофия стенки с перестройкой наружного мышечного слоя. Этот отдел кишки обычно имеет серовато-белый цвет, наружный мышечный слой сплошным плотным футляром окружает кишечную стенку, которая в виде грубого полуспавшегося баллона занимает значительную часть брюшной полости. Гаустры в этом отделе кишки отсутствуют, кровеносные сосуды крупные, с множественными разветвлениями. Переходная зона от расширенной части к аганглионарной зоне определяется довольно четко: появляются хорошо выраженные тении и гаустры, а диаметр кишки приближается к нормальному.
Мобилизация начинается с расширенного участка, при этом обязательно пересекается краевой сосуд в самой дистальной части отдела, предполагаемого для низведения. Затем выполняется мобилизация аганглионарной зоны. Ее производят как можно ближе к стенке кишки для уменьшения травматизации тазовых нервных сплетений.
Мобилизацию низводимых отделов производят путем перевязки основных сосудов: сигмовидных — при низведении сигмовидной кишки, нижнебрыжеечный — при низведении левых отделов, нижнебрыжеечных и средних ободочных сосудов — при низведении правой половины ободочной кишки. Мобилизация прямой кишки производится циркулярно до уровня 7–8 см, а по задней стенке до тазового дна. На высоте 7–8 см от края анального канала кишка пересекается. Низводимая кишка фиксируется к специальному проводнику, с его помощью выпячивают заднюю стенку прямой кишки сразу над верхним краем анального канала.
Промежностной бригадой после дивульсии ануса рассекают заднюю стенку прямой кишки на 1–2 см выше аноректальной линии над проводником. Через эту рану в подготовленный тоннель проводится низведенная кишка на проводнике. Перед этим накладывают провизорные швы, которыми затем сшивают низведенную кишку и прямую кишку по ранее намеченной линии анастомоза. Затем проводник снимают, а избыток низведенной кишки фиксируют к перианальной коже. Производится дренирование культи прямой кишки.
Второй этап операции — отсечение избытка низведенной кишки. Операция проводится под эпидуральной анестезией. Производят циркулярное отсечение избытка низведенной кишки на уровне ранее наложенных узловых швов. Затем формируется анастомоз с помощью сшивания задней стенки прямой кишки с передней стенкой, низведенной узловыми швами. Операция отсечения избытка низведенной кишки и формирование отсроченного колоректального анастомоза выполняются через 12–15 дней после проведения первого этапа операции.
Варианты выполнения операции Дюамеля в модификации Государственного научного центра колопроктологии
У ряда пациентов предпринимается многоэтапное плановое хирургическое лечение. Оно проводится в двух вариантах — с первичным или отсроченным удалением аганглионарной зоны.
Вариант 1
1- й этап — резекция прямой и ободочной кишки по типу операции Гартмана.
2- й этап — реконструктивно-восстановительное низведение ободочной кишки с формированием колоректального концебокового ретроректального анастомоза по Дюамелю.
3- й этап — отсечение избытка низведенной кишки и формирование отсроченного колоректального анастомоза через 12–15 дней после операции.
Вариант 2
Применяется при тяжелом состоянии пациентов, когда нецелесообразно расширять объем резекции и удалять прямую кишку.
1- й этап — резекция ободочной кишки по типу операции Гартмана.
2- й этап — ререзекция толстой кишки с зоной аганглиоза и формирование колоректального концебокового ретроректального анастомоза по Дюамелю.
3- й этап — отсечение избытка низведенной кишки и формирование отсроченного колоректального анастомоза через 12–15 дней после операции.
ЛЕЧЕНИЕ ОСЛОЖНЕНИЙ
К тяжелым осложнениям болезни Гиршпрунга, требующим выполнения ургентного хирургического вмешательства, относятся острая ки-
шечная непроходимость, перфорация кишки, пролежень толстой кишки каловым камнем.
Экстренные и срочные операции, в зависимости от тяжести состояния пациентов, выраженности осложнений, могут быть произведены в нескольких вариантах:
Вариант 1
Резекция ободочной кишки по типу операции Гартмана (в зависимости от выраженности мегаколона выполняются резекция сигмовидной кишки, резекция левых отделов, левосторонняя гемиколэктомия).
Вариант 2
Резекция ободочной и прямой кишки с аганглионарной зоной по типу операции Гартмана.
Вариант 3
Колостомия, илеостомия.
В дальнейшем всем пациентам, перенесшим экстренные и срочные оперативные вмешательства по поводу осложнений болезни Гиршпрунга, проводится плановое хирургическое лечение по указанным выше методам.
Диспансерное наблюдение за больными после операции
Все пациенты, оперированные по поводу болезни Гиршпрунга, после хирургического лечения подлежат диспансерному наблюдению. Цель мониторинга больных — оценка функциональных результатов лечения, а также выявление и коррекция поздних послеоперационных осложнений. Учитывая вероятность формирования стриктуры колоректального анастомоза в ранние сроки после операции, рекомендовано проводить осмотр пациентов еженедельно после выписки из стационара в течение 1 мес. В дальнейшем больные обращаются для контрольного осмотра 1 раз в 3 мес в течение 1 года.
Через 1 год после операции, кроме клинического осмотра для определения функционального состояния толстой кишки и исключения рецидива мегаколона, необходимо проведение рентгенологического исследования желудочно-кишечного тракта. Оно должно включать ирригоскопию и проведение пассажа бария по ЖКТ. Кроме этого, при наличии показаний (признаков нарушения функции держания кишечного содержимого) нужно проводить физиологическое исследование ЗАПК. В дальнейшем при отсутствии поздних послеоперационных осложнений, требующих оперативной или консервативной коррекции, диспансерное наблюдение за пациентами осуществляется 1 раз в год.
Прогноз
Прогноз у взрослых пациентов, перенесших операцию Дюамеля в модификации ГНЦК по поводу болезни Гиршпрунга, является благопри-
ятным при двух условиях: отсутствии поздних осложнений со стороны колоректального анастомоза и нормальной функции запирательного аппарата прямой кишки. Поздние стриктуры колоректального анастомоза могут привести к развитию мегаколона, поэтому необходимо проведение строгого мониторинга у оперированных больных.
Критерии оценки качества помощи в стационаре представлены в таблице 14.2. Для оценки качества медицинской помощи используют временные, процессуальные и профилактирующие критерии. Временные характеризуют своевременность оказания определенных этапов медицинской помощи. Выполнение пациенту ряда медицинских манипуляций, инструментальных и лабораторных исследований, необходимых для качественного оказания медицинской помощи, оценивают в процессуальных критериях. Для анализа мероприятий, направленных на предотвращение развития осложнений, используют профилактирующие критерии.
Таблица 14.2. Критерии оценки качества медицинской помощи в стационаре больным с мегаколоном (0 — нет, 1 — да)
|
Клинические рекомендации |
Временные |
Процессуальные |
Профилактирующие |
|
1. Клинические рекомендации по диагностике и лечению взрослых больных идиопатическим мегаколоном (код МКБ — К59.3). 2. Клинические рекомендации по диагностике и лечению болезни Гиршпрунга у взрослых (код МКБ — Q43.1). 3. Клинические рекомендации по диагностике и лечению взрослых пациентов с долихоколоном (код МКБ — Q43.8) |
Установка клинического диагноза в течение 72 ч: 0/1 |
Пальцевое обследование прямой кишки: 0/1. Ректороманоскопия: 0/1. Ирригоскопия: 0/1. Исследование крови на сифилис, вирусный гепатит В, вирусный гепатит С: 0/1. Клинический анализ крови; биохимический анализ крови; клинический анализ мочи; коагулограмма: 0/1. При подозрении на болезнь Гиршпрунга определение активности ацетилхолинэстеразы в биоптате слизистой оболочки прямой кишки: 0/1. При подозрении на болезнь Гиршпрунга определение ректоанального ингибиторного рефлекса: 0/1. При дифференциальной диагностике болезни Гиршпрунга и идиопатического мегаколона проведение биопсии по Свенсону: 0/1. |
Отсутствие осложнений: • кровотечение: 0/1; • пневмония: 0/1; • тромбоэмболия: 0/1; • послеоперационная спаечная кишечная непроходимость: 0/1; • перитонит: 0/1; • летальный исход: 0/1 |
Табл. 14.2. Окончание
|
Клинические рекомендации |
Временные |
Процессуальные |
Профилактирующие |
|
|
|
Метод оперативного лечения в соответствии с установленным диагнозом и клиническими рекомендациями: 0/1. Метод анестезии в соответствии с объемом оперативного лечения: 0/1 |
|
Литература
1. Аруин Л.И., Капуллер Л.Л., Исаков В.А. Морфологическая диагностика болезней желудка и кишечника. — М., 1998. — 483 с.
2. Ачкасов С.И. Аномалии развития и положения толстой кишки. Клиника, диагностика, лечение: Дис. … д-ра мед. наук. — М., 2003. — 294 с.
3. Бирюков О.М. Клинико-морфологическая характеристика болезни Гиршпрунга у взрослых: Дис. … канд. мед. наук. — М., 2006. — 191 с.
4. Вавилова Т.И., Воробьев Г.И., Жученко А.П. Гистохимическая диагностика болезни Гиршпрунга // Хирургия. — 1986. — № 3. — С. 15–22.
5. Воробьев Г.И. Мегаколон у взрослых (клиника, диагностика и хирургическое лечение): Дис. … д-ра мед наук. — М., 1982. — 402 с.
6. Воробьев Г.И., Ачкасов С.И. Болезнь Гиршпрунга у взрослых. — М.: Литтерра, 2009. — С. 10–11.
7. Воробьев Г.И., Жученко А.П., Ефремов А.В. Поздние осложнения после операции Дюамеля по поводу болезни Гиршпрунга у взрослых // Пробл. проктологии. — 1991. — Вып. 12. — С. 58–62.
8. Воробьев Г.И., Жученко А.П., Ачкасов С.И., Бирюков О.М. Болезнь Гиршпрунга у взрослых: 25-летний опыт клиники. Актуальные вопросы колопроктологии. — Самара, 2003. — 414 с.
9. Загороднюк В.П. Исследование неадренергического торможения в гладких мышцах кишечника человека: Автореф. дис. … канд. мед наук. — Киев, 1989. — 28 с.
10. Красовская Т.В., Вавилова Т.И., Кобзева Т.Н., Муратов И.Д. Диагностическая и лечебная тактика при острых формах болезни Гиршпрунга // Пробл. проктологии. — 1990. — Вып. 11. — С. 55–60.
11. Чепурной Г.И., Кивва А.Н. Сравнительная оценка различных способов оперативной коррекции болезни Гиршпрунга // Вестн. хир. — 2001. — № 4. — С. 62–65.
12. Amiel J., Lyonnet S. Hirschsprung’s disease, associated syndromes, and genetics: a review // J. Med. Gen. — 2001. — Vol. 38. — Р. 729–739.
13. Aminoso C., García-Minaúr S., Martínez L. et al. Recurrence of Hirschsprung disease due to maternal mosaicism of a novel RET gene mutation // Clin. Genet. — 2013, May. — Vol. 13. — doi: 10.1111/cge.12163.
14. Baillie C.T., Kenny S.E., Rintala R.J. et al. Long-term outcome and colonic motility after the Duhamel procedure for Hirschsprung’s disease // J. Pediatr. Surg. — 1999. — Vol. 34, N 2. — P. 325–329.
15. Baranyay F., Bogar G., Sebestyen M. Adult Hirschsprung’s disease with mental retardation and microcephaly // Orv. Hetil. — 2000. — Vol. 141, N 30. — P. 1673–1676.
16. Bjornland K., Diseth Т.Н., Emblem R. Long-term functional, manometric, and endosonographic evaluation of patients operated upon with Duhamel technique // Pediatr. Surg. Int. — 1998. — Vol. 13, N 1. — P. 24–28.
17. Borrego S., Ruiz-Ferrer M., Fernández R.M., Antinolo G. Hirschsprung’s disease as a model of complex genetic etiology // Histol. Histopathol. — 2013. — Vol. 28. — P. 1117–1136.
18. Butler Tjaden N.E., Trainor P.A. The developmental etiology and pathogenesis of Hirschsprung disease // Transl. Res. — 2013, Mar 22. — doi: pii: S1931–5244. — Vol. 13. — Р. 71–76.
19. Catto-Smitt A.G., Coffey C.M., Nolan T.M., Hutson J.M. Fecal incontinence after the surgical treatment of Hirschsprung’s disease // J. Pediatr. — 1995. — Vol. 127, N 6. — P. 954–957.
20. Chan G.L., Rand J.R. Nitric oxide and vasoactive intestinal polypeptide mediated non-adrenergic, non-cholinergic inhibitory transmission to smooth muscle of the rat gastric fundus // Eur. J. Pharmacol. — 1990. — Vol. 191. — P. 303–309.
21. Crocker N.L., Messmer J.M. Adult Hirschsprung’s disease // Clin. Radiol. — 1991. — Vol. 44, N 4. — P. 257–259.
22. de Arruda Lourencao P.L., Takegawa B.K., Ortolan E.V. et al. A useful panel for the diagnosis of Hirschsprung disease in rectal biopsies: calretinin immunostaining and acetylcholinesterase histochesmistry // Ann. Diagn. Pathol. — 2013, May 14. — Vol. 13. — Р. 26–29.
23. Emir H., Akman M., Sarimurat N. et al. Anorectal manometry during the ineonatal period: its specificity in the diagnosis of Hirschsprung‘s disease // Eur. J. Pediatr. Surg. — 1999. — Vol. 9. — Р. 101–103.
24. Fouquet V., De Lagausie P., Faure C. et al. Do prognostic factors exist for total colonic aganglionosis with ileal involvement? // J. Pediatr. Surg. — 2002. — Vol. 37, N 1. — P. 71–75.
25. Furness J.В., Costa M. Cytoarchitectonics of the enteric nervous system // The Enteric Nervous system. —N.Y.: Churchill Livingstone, 1987. — Р. 26, 54.
26. Gosemann J.H., Friedmacher F., Ure B., Lacher M. Open versus transanal pull-through for Hirschsprung disease: a systematic review of long-term outcome // Eur. J. Pediatr. Surg. — 2013. — Vol. 23, N 2. — P. 94–102.
27. Hanneman M.J., Sprangers M.A., Mik E.L., van Heurn L.W. Quality of life in patients with anorectal malformation or Hirschsprung’s disease // Dis. Colon Rectum. — 2001, Nov. — P. 1650–1660.
28. Jannot A.S., Pelet A., Henrion-Caude A. et al. Chromosome 21 sin Down syndrome reveals DSCAM as a predisposing locus in Hirschsprung disease // PLoS One. — 2013. — Vol. 8, N 5. — P. 6251–6259.
29. Lake J.I., Heuckeroth R.O. Enteric Nervous System Development: Migration, Differentiation, and Disease // Am. J. Physiol. Gastrointest, Liver Physiol. — 2013. — Vol. 305. — P. G1–G24.
30. Langer J.C. Hirschsprung disease // Curr. Opin. Pediatr. — 2013. — Vol. 25, N 3. — P. 368–374.
31. Jones O.M., Brading A.F., Mortensen N.J. Role of nitric oxide in anorectal function of normal and neuronal nitric oxide synthase knockout mice // Dis. Colon Rectum. — 2003. — Vol. 46, N 7. — P. 963–970.
32. Moore B.G., Singaram C., Eckhoff D.E. et al. Immunohistochemical evaluations of ultrashort-segment Hirschsprung’s disease // Dis. Colon Rectum. — 1996, July. — Vol. 39. — P. 817–822.
33. Puffenberger E.G., Hosoda K., Washington S.S. et al. A missense mutation of the endothelin-B receptor gene in multigenic Hirschsprung’s disease // Cell. — 1994. — Vol. 79. — Р. 1257–1266.
34. Sarsu S.B., Karakus S.C., Erdem A.U. Colon perforation caused by a foreign body in Hirschsprung disease // J. Pediatr. Surg. — 2012. — Vol. 47, N 10. — P. 15–17.
35. Sharp N.E., Pettiford-Cunningham J., Shah S.R. et al. The prevalence of Hirschsprung disease in premature infants after suction rectal biopsy // J. Surg. Res. — 2013, Apr 19. — Р. 480–484.
36. Solomon R., Attie Т., Pelet A. et. al. Germline mutations of the RET ligand GDNF are not sufficient to cause Hirschsprung’s disease // Nat. Genet. — 1996. — Vol. 14. — Р. 345–347.
37. Swenson O. Hirschsprung’s disease: a review // Pediatrics. — 2002. — Vol. 109, N 5. — P. 914 — 918.
38. Weber T.R., Fortuna R.S., Silen M.L., Dillon P.A. Reoperation for Hirschsprung’s disease // Pediatr. Surg. — 1999. — Vol. 34, N 1. — P. 153, 156–157.
39. Wedel Т., Gleiss J., Schiedeck Т. et al. Megacolon in adults the spectrum of underlying intestinal innervation disorders // Langenbecks Arch. Chir. Suppl. Kongressbd. — 1998. — Vol. 115. — Р. 979–981.
40. Wester Т., Hoehner J., Olsen L. Rehbein’s anterior resection in Hirschsprung’s disease, using a circular stapler // Eur. J. Pediatr. Surg. — 1995. — Vol. 5, N 6. — P. 358–362.
41. Wester Т., O’Briain D.S., Puri P. Notable postnatal alterations in the myenteric plexus of normal human bowel. — 1999. — Vol. 44. — Р. 666–674.
42. Wheatley M.J., Wesley J.R., Polley T.Z.Jr. Hirschsprung’s disease in adolescents and adults // Dis. Colon Rectum. — 1990. — Vol. 3. — Р. 662–669.
43. Wilkinson D., Kenny S. Anorectal function is not always normal after surgery in Hirschsprung’s disease // BMJ. — 2012. — Vol. 345. — Р. 81–92.
44. Wu J.S., Schoetz D.J., Coller J.A., Veidenheimer M.C. Treatment of Hirschsprung’s disease in the adult. Report of five cases // Dis. Colon Rectum. — 1995. — Vol. 38, N 6. — P. 655–659.
45. Yee L.M., Mulvihill S.J. Neuroendocrine disorders of the gut // West. J. Med. — 1995. — Vol. 163, N 5. — P. 454–462.
ДОЛИХОКОЛОН
Введение
Долихоколон — удлинение всей ободочной кишки или одного из ее отделов, представляет собой самую частую аномалию развития толстой кишки.
По данным А.И. Ленюшкина (1999), частота выявления данного состояния у новорожденных составляет более 30% [8]. Нет точных данных о частоте встречаемости долихоколона у взрослых, однако выявление удлинения толстой кишки у значительной части пациентов, страдающих запором, указывает на распространенность данного состояния и определяет актуальность проблемы. Так, удлинение ободочной кишки диагностируется у каждого 2 пациента, длительно страдающего запором [19], а одно из осложнений долихоколона —заворот сигмовидной кишки — прочно занимает 3-е место среди причин острой кишечной непроходимости [12, 24], и летальность при развитии этого осложнения достигает 15% [24], а в случае некроза — 46% [12]. Важным обстоятельством, затрудняющим диагностику и лечение долихоколона, является отсутствие четких объективных критериев диагноза. Так, например, до настоящего времени не определены числовые параметры нормальной длины ободочной кишки и каждого из ее отделов.
Кроме того, ряд исследователей допускает возможность приобретенного характера долихоколона [19, 40] вопреки общепринятым представлениям о врожденной природе этого состояния, причисляемого к аномалиям развития.
Следует подчеркнуть, что к долихоколону относят группу состояний, крайне разнородную по степени выраженности клинических проявлений — от случайно обнаруженного в ходе обследования удлинения ободочной кишки без каких-либо функциональных нарушений до угрожающего жизни пациента заболевания, характеризуемого рецидивирующими заворотами кишки и развитием кишечной непроходимости. Кроме того, несмотря на присутствие в МКБ (код Q43.8, МКБ-10) в качестве отдельной, самостоятельной нозологической формы, долихоколон, как правило, не рассматривается, а диагностика и лечение этого состояния обсуждаются в рамках других болезней — запора (код K59.0, МКБ-10), заворота кишок (код K56.2, МКБ-10). В настоящих рекомендациях вопросы диагностики
и лечения долихоколона рассматриваются в свете его клинических проявлений, которые являются определяющими в выборе лечебной тактики. Настоящие рекомендации по диагностике и лечению пациентов с долихоколоном служат руководством для практических врачей, осущест-
вляющих ведение и лечение таких больных.
Рекомендации включают следующие разделы: введение, определение и классификация, диагностика, лечение, профилактика, прогноз, раздел
«Чего нельзя делать» и литературу. Рекомендации составлены на основании анализа литературы из баз данных PubMed, MEDLINE, Cochrane Collaboration и подлежат регулярному пересмотру в соответствии с новыми данными научных исследований в этой области.
В настоящих клинических рекомендациях применяется общепринятая система оценки уровней доказательности и степеней рекомендации, основанная на разработках Оксфордского центра доказательной медицины (табл. 15.1) [37].
Таблица 15.1. Уровни доказательности и степени рекомендаций на основании руководства Оксфордского центра доказательной медицины
|
Уровень |
Диагностическое исследование |
Терапевтическое исследование |
|
1а |
Систематический обзор гомогенных диагностических исследований 1-го уровня |
Систематический обзор гомогенных РКИ |
|
1b |
Валидизирующее когортное исследование с качественным «золотым стандартом» |
Отдельное РКИ (с узким доверительным интервалом) |
|
1с |
Специфичность или чувствительность столь высокие, что положительный или отрицательный результат позволяет исключить/установить диагноз |
Исследование «Всё или ничего» |
|
2а |
Систематический обзор гомогенных диагностических исследований >2-го уровня |
Систематический обзор (гомогенных) когортных исследований |
|
2b |
Разведочное когортное исследование с качественным «золотым стандартом» |
Отдельное когортное исследование (включая РКИ низкого качества; т.е. с <80% пациентов, прошедших контрольное наблюдение) |
|
2с |
Нет |
Исследование «исходов»; экологические исследования |
|
3а |
Систематический обзор гомогенных исследований уровня 3b и выше |
Систематический обзор гомогенных исследований «случай– контроль» |
|
3b |
Исследование с непоследовательным набором или без проведения исследования «золотого стандарта» у всех испытуемых |
Отдельное исследование «случай– контроль» |
Табл. 15.1. Окончание
|
Уровень |
Диагностическое исследование |
Терапевтическое исследование |
|
4 |
Исследование «случай–контроль» или исследование с некачественным или зависимым «золотым стандартом» |
Серия случаев (и когортные исследования или исследования «случай–контроль» низкого качества) |
|
5 |
Мнение экспертов без тщательной критической оценки или основанное на физиологии, лабораторные исследования на животных или разработка «первых принципов» |
Мнение экспертов без тщательной критической оценки, лабораторные исследования на животных или разработка «первых принципов» |
|
Степени рекомендаций | ||
|
A |
Согласующиеся между собой исследования 1-го уровня | |
|
B |
Согласующиеся между собой исследования 2-го или 3-го уровня или экстраполяция на основе исследований 1-го уровня | |
|
C |
Исследования 4-го уровня или экстраполяция на основе уровня 2 или 3 | |
|
D |
Доказательства 4-го уровня или затруднительные для обобщения или некачественные исследования любого уровня | |
ВАЛИДИЗАЦИЯ РЕКОМЕНДАЦИЙ
Настоящие рекомендации составлены общероссийской общественной организацией «Ассоциация колопроктологов России», в предварительной версии были рецензированы независимыми экспертами, которых попросили прокомментировать, насколько интерпретация доказательств, лежащих в основе рекомендаций, доступна для понимания. Получены комментарии со стороны врачей амбулаторного звена. Полученные комментарии тщательно систематизировались и обсуждались на совещаниях экспертной группы.
Последние изменения в настоящих рекомендациях были представлены для дискуссии на заседании профильной комиссии «Колопроктология» Экспертного совета Минздрава России 12 сентября 2013 г. Проект рекомендаций был повторно рецензирован независимыми экспертами и врачами амбулаторного звена. Для окончательной редакции и контроля качества рекомендации были повторно проанализированы членами экспертной группы, которые пришли к заключению, что все замечания и комментарии приняты во внимание, риск систематических ошибок при разработке рекомендаций сведен к минимуму.
ОБЛАСТЬ ПРИМЕНЕНИЯ РЕКОМЕНДАЦИЙ
Данные рекомендации применимы при осуществлении медицинской деятельности в рамках Порядка оказания медицинской помощи взрослому населению с заболеваниями толстой кишки, анального канала и промежности колопроктологического профиля.
Определение
В настоящее время не существует общепринятого точного определения долихоколона.
В энциклопедическом словаре медицинских терминов под редакцией Б.В. Петровского (1982) приводится следующее определение: долихоколон — аномалия развития: необычно большая длина ободочной кишки (УД 5, СР D [18]).
При этом не уточняется, какая длина ободочной кишки считается нормальной.
В различных анатомических и клинических учебниках и монографиях приводятся различные значения верхней границы нормы для длины ободочной кишки и ее отделов (УД 5, СР D [2, 11, 20, 41]).
Необходимо отметить, что для взрослых пациентов отсутствует корреляция между ростом, полом, возрастом, типом телосложения и длиной толстой кишки (УД 4, СР C [2]).
Код по Международной классификации болезней 10-го пересмотра
n Класс: XVII. Врожденные аномалии [пороки развития], деформации и хромосомные нарушения (Q00–Q99).
n Блок: Другие врожденные аномалии [пороки развития] органов пищеварения (Q38–Q45).
n Код: Q43.8 Другие уточненные врожденные аномалии кишечника. Долихоколон.
Классификация
Для долихоколона не разработано универсальной классификации. Вместе с тем для уточнения диагноза может быть использован анатомический и клинический принципы классификации.
По анатомическому принципу долихоколон классифицируется исходя из отдела ободочной кишки, длина которого превышает среднестатистические значения. Выделяют следующие виды долихоколона (УД 5, СР D [4]).
n Долихосигма.
n Левосторонний долихоколон.
n Долихотрансверзум.
n Правосторонний долихоколон.
n Субтотальный долихоколон.
n Тотальный долихоколон.
В практическом здравоохранении большее значение имеет клинический принцип классификации, на основании которого долихоколон подразделяется на следующие формы (УД 5, СР D [2]).
n Долихоколон без клинических проявлений (бессимптомный долихоколон).
n Долихоколон с нарушением транзита по толстой кишке.
n Осложненный долихоколон. Осложнениями являются заворот кишки, инвагинация и узлообразование (УД 5, СР D [2, 4, 7, 12, 17, 24, 33, 35, 40]).
Формулировка диагноза
При формулировании диагноза следует отразить, длина каких отделов ободочной кишки превышает среднестатистические значения, а также указать наличие клинических проявлений или их отсутствие. В случае осложненного долихоколона необходимо указать осложнение, а также его рецидивирующий характер при повторном развитии и характер ранее перенесенных вмешательств. Ниже приведены примеры формулировок диагноза.
n Долихосигма без клинических проявлений.
n Субтотальный долихоколон с нарушением транзита по толстой кишке.
n Левосторонний долихоколон, осложненный рецидивирующим заворотом сигмовидной кишки. Состояние после эндоскопической деторсии заворота сигмовидной кишки.
Диагностика
КЛИНИЧЕСКАЯ ХАРАКТЕРИСТИКА
При бессимптомном долихоколоне у пациентов отсутствуют специфические жалобы.
Ведущее клиническое проявление долихоколона — картина запора (УД 5, СР D [1, 3, 5, 11, 16, 40]). При этом задержка стула до 3 дней часто не сопровождается другими жалобами, тогда как более длительный и выраженный запор сочетается с дискомфортом в животе, болями, метеоризмом вплоть до ухудшения общего самочувствия, социальной дезадаптации, развития приступов кишечной непроходимости (УД 5, СР D [2]). Большинство таких пациентов нуждается в соблюдении диеты, постоянном приеме слабительных средств, выполнении очистительных клизм.
Осложненный долихоколон характеризуется периодическим развитием заворота кишки, инвагинацией или узлообразованием, что проявляется клинической картиной острой странгуляционной кишечной непроходимости [2, 7, 22, 24, 35, 40, 41]. Наиболее часто в клинической практике встречаются завороты сигмовидной кишки, реже поперечной ободочной и слепой кишки. Завороты других отделов ободочной кишки описываются как казуистические случаи.
ДИАГНОСТИЧЕСКИЕ КРИТЕРИИ
В настоящее время не разработаны диагностические критерии долихоколон.
Факт превышения длины всей ободочной кишки или какого-либо из ее отделов среднестатистических показателей может быть установлен одним из следующих методов (УД 5, СР D [2]):
n Ирригоскопия.
n Виртуальная колонография.
n Интраоперационное морфометрическое исследование.
В 2003 г. в Государственном научном центре колопроктологии С.И. Ачкасов провел исследование, в котором были определены нормальные параметрические характеристики длины различных отделов ободочной кишки (УД 5, СР D [2]) на основании анализа данных 160 наблюдений (табл. 15.2).
Таблица 15.2. Нормальные показатели длины отделов ободочной кишки
|
Отдел ободочной кишки |
Границы колебания длины, см |
Средняя длина, см |
|
Слепая кишка |
4,0–10,0 |
6,2+1,6 |
|
Восходящая кишка |
8,0–34,0 |
23,4+4,1 |
|
Поперечная ободочная кишка |
20,0–51,0 |
32,8+9,5 |
|
Нисходящая кишка |
11,0–30,0 |
20,9+4,5 |
|
Сигмовидная кишка |
20,0–86,0 |
45,0+14,5 |
Сопутствующее долихоколону нарушение транзита по толстой кишке выявляется с помощью пассажа бариевой взвеси, рентгеноконтрастных маркеров или радиофармпрепарата по ЖКТ (УД 5, СР D [2, 10, 17]).
Диагноз «осложненный долихоколон» может быть установлен при удлиненной ободочной кишке и развитии по меньшей мере одного подтвержденного эпизода заворота кишки, инвагинации или узлообразования.
УСТАНОВЛЕНИЕ ДИАГНОЗА
Для уточнения диагноза и проведения дифференциальной диагностики применяют следующие методы обследования.
Сбор жалоб и изучение анамнеза заболевания (УД 5, СР D [2, 17]). Выяснение жалоб и анамнеза заболевания пациента позволяет определить клиническую форму долихоколона, что принципиально важно для выбора тактики лечения. Бессимптомный долихоколон не сопровождается жалобами, возможна задержка стула до 3 дней. Нарушение транзита по толстой кишке проявляется клинической картиной запора, которая может быть подтверждена соответствием Римским критериям запоров 3-го пересмотра [25] (табл. 15.3).
Следует выяснить, есть ли у пациента опыт приема слабительных средств, выполнения очистительных клизм и какова их эффективность. Кроме того, в беседе с больным выясняют наличие сопутствующих заболеваний и признаки болезней, с которыми проводится дифференци-
альная диагностика. Эпизоды кишечной непроходимости в анамнезе позволяют заподозрить осложненный долихоколон.
Таблица 15.3. Римские критерии запоров 3-го пересмотра
|
Симптомы |
Характерные особенности симптомов |
|
1. Натуживание, занимающее >1/4 времени дефекации. 2. Стул в виде твердого кала или комочков. 3. Ощущение неполного опорожнения (>1/4 времени дефекации). 4. Ощущение препятствия в аноректальной области (>1/4 времени дефекации). 5. Необходимость мануальных приемов для освобождения кишечника (эвакуация каловых масс пальцем, поддержка рукой тазового дна), занимающее >1/4 времени дефекации. 6. Стул <3 раз в неделю |
Симптомы должны наблюдаться в течение 12 нед (необязательно последовательных) на протяжении предыдущего года. Симптомокомплекс должен включать два или более перечисленных в данной таблице симптома |
Физикальное обследование (УД 5, СР D [2, 17]). При осмотре больного оцениваются общее состояние, тип телосложения, наличие признаков врожденных аномалий и сопутствующих заболеваний. При осмотре живота может определяться вздутие, при перкуссии — звук тимпанита, а при пальпации — умеренная болезненность в околопупочной области, левых и нижних отделах живота. При развитии осложнения долихоколон могут определяться асимметричное вздутие живота, ограничение участия живота в акте дыхания, симптомы раздражения брюшины. В случае инвагинации может пальпироваться головка инвагината. Вагинальное и ректальное исследования позволяют выявить наличие факторов, предрасполагающих к проктогенному запору, такие как выпадение матки и стенок влагалища, ректоцеле, выпадение прямой кишки, анальная трещина.
Ирригоскопия (УД 5, СР D [2, 17]). Исследование проводится по методике двойного контрастирования — бариевой взвесью и воздухом. Ирригоскопия — наиболее информативный диагностический метод, позволяющий определить форму, размеры и положение всех отделов толстой кишки, оценить их подвижность в брюшной полости.
Пассаж бариевой взвеси, рентгеноконтрастных маркеров или радиофармпрепарата по ЖКТ (УД 5, СР D [2, 17]). Контроль продвижения контраста проводится в течение 5 сут после его приема внутрь, позволяя оценить время прохождения кишечного содержимого по разным отделам тонкой и толстой кишки. В норме общее время транзита по ЖКТ не превышает 48 ч. При сохранении контраста в толстой кишке через 72 ч после приема внутрь констатируют задержку пассажа по ЖКТ.
Проктография с натуживанием/сцинтидефекография (УД 5, СР D [2, 17]). Методики позволяют определить положение промежности, изменение
ректоанального угла, состояние пуборектальной петли, наличие переднего или заднего ректоцеле, внутренней инвагинации прямой кишки при моделировании акта дефекации, что способствует выявлению проктогенного характера запора в рамках дифференциальной диагностики.
Колоноскопия (УД 5, СР D [2, 17]). В ходе эндоскопического исследования толстой кишки определяют тонус, складчатость, выраженность сосудистого рисунка, цвет и контактную кровоточивость слизистой оболочки, а кроме того, оценивают длину и ширину различных отделов толстой кишки, их петлистость, фиксацию и число гаустр. Колоноскопия имеет большое значение в дифференциальной диагностике долихоколона.
Гастроскопия (УД 5, СР D [2, 17]). Эзофагогастродуоденоскопия позволяет выявить сопутствующие заболевания верхних отделов пищеварительного тракта, а также определить наличие гастроптоза у больных с множественными аномалиями ЖКТ.
Ультразвуковое и томографическое исследование (компьютерная рентгеновская/магнитно-резонансная томография) органов брюшной полости и малого таза (УД 5, СР D [2, 17]). Методы лучевой диагностики позволяют выявить сопутствующие заболевания, а также получить дополнительную информацию о состоянии стенки толстой кишки. Виртуальная компьютерная колонография может быть альтернативой выполнению ирригоскопии, с ее помощью измеряют длину и ширину отделов толстой кишки, определяют их положение в брюшной полости.
Функциональное исследование состояния мышц ЗАПК, тазового дна (УД 5, СР D [2, 17]). Комплекс функциональных исследований позволяет исключить заболевания, обусловливающие проктогенный характер запора, а также болезнь Гиршпрунга.
Профилометрическое исследование позволяет исключить спазм внутреннего анального сфинктера. Электромиография способствует оценке функции пуборектальной мышцы — сравнивается исходная электрическая активность ее в состоянии покоя и в момент натуживания. В норме при натуживании регистрируется различная степень угнетения биоэлектрической активности исследуемой мышечной структуры. Сохранение или подъем биоэлектрической активности расценивается как парадоксальная реакция пуборектальной мышцы, что является одной из причин проктогенного запора.
При необходимости дифференциальной диагностики с болезнью Гиршпрунга проводится аноректальная манометрия — исследование ректоанального ингибиторного рефлекса (рефлекторного расслабления внутреннего сфинктера в ответ на повышение давления в прямой кишке). При болезни Гиршпрунга в 70–95% случаев ректоанальный ингибиторный рефлекс не определяется.
Определение уровня тканевой ацетилхолинэстеразы (УД 5, СР D [2, 17]). При необходимости дифференциальной диагностики с болезнью Гиршпрунга выполняется исследование биоптатов слизистой оболочки прямой кишки с уровня 5, 10 и 15 см от наружного края анального канала для определения активности ацетилхолинэстеразы. При болезни Гиршпрунга проба положительная.
Консультации смежных специалистов (УД 5, СР D [2, 17]). Консультации специалистов (эндокринолога, невропатолога, психиатра, медицинского генетика, уролога, гинеколога) позволяют оценить вклад сопутствующих заболеваний в состояние пациента.
ДИФФЕРЕНЦИАЛЬНАЯ ДИАГНОСТИКА
При подозрении на долихоколон необходимо исключить следующие заболевания.
n Болезнь Гиршпрунга.
n Идиопатический мегаколон.
n Воспалительные заболевания кишечника (ВЗК).
n Ишемический колит.
n Новообразования толстой кишки.
n Медикаментозный запор.
Лечение
Выбор тактики лечения долихоколона основывается на клинической форме болезни.
Бессимптомный долихоколон не требует консервативного или хирургического лечения, однако пациенты должны быть предупреждены о возможном развитии в дальнейшем медленно-транзитного запора и о потенциальной угрозе осложнений (УД 5, СР D [2]). У таких пациентов необходима первичная профилактика запора (см. раздел
«Профилактика»).
ЛЕЧЕНИЕ НЕОСЛОЖНЕННОГО ДОЛИХОКОЛОНА
Лечение долихоколона с нарушением транзита по толстой кишке должно проводиться в соответствии с принципами лечения медленнотранзитных запоров.
Консервативное лечение долихоколон с нарушением транзита по толстой кишке
При установлении диагноза «долихоколон», сопровождающегося нарушением транзита по толстой кишке, должно быть назначено консервативное лечение. Принципы лечения не отличаются от таковых при медленно-транзитном запоре без удлинения толстой кишки и включают (УД 5, СР D [2, 17]):
n добавление в рацион питания пищевых волокон;
n соблюдение водно-питьевого режима;
n проведение лечебной физкультуры;
n физиотерапевтическое лечение (электростимуляцию толстой кишки, иглорефлексотерапию);
n медикаментозную терапию.
![]()
![]()
![]() Предпочтение отдается комплексному поэтапному лечению (УД 4, СР С [10]) (рис. 15.1).
Предпочтение отдается комплексному поэтапному лечению (УД 4, СР С [10]) (рис. 15.1).
Рис. 15.1. Алгоритм комплексного поэтапного консервативного лечения запора
Медикаментозная терапия включает назначение средств, увеличивающих объем кишечного содержимого (препараты семян подорожника, мелкокристаллическая целлюлоза), осмотических слабительных препаратов (лактулоза, магния сульфат, полиэтиленгликоль), прокинетиков (цизаприд, тримебутин).
Назначение препаратов пищевых волокон не всегда приводит к улучшению. Более того, состояние пациентов с долихоколоном на фоне высокошлаковой диеты может ухудшаться за счет усиления метеоризма и тяжести в животе. Таким больным рекомендуется назначать препараты полиэтиленгликоля (макрогол).
При неэффективности осмотических слабительных оправдано назначение стимулирующих (контактных) слабительных. Основными представителями этой группы лекарств являются препараты, содержащие антрахиноны, преимущественно растительного происхождения (сена, алоэ, ревень), и соединения дифенилметана (бисакодил, натрия пикосульфат). Они обладают прокинетическим действием, повышают интестинальную секрецию и снижают абсорбцию. Следует отметить, что современные исследования не подтвердили ранее существовавшие опасения о потенциальном канцерогенном действии препаратов этой группы [34]. Также
опровергнута гипотеза о нейродегенеративных изменениях в результате длительного приема контактных слабительных средств [21, 30]. Таким образом, представляется оправданным длительное использование слабительных, в том числе и стимулирующих, если они позволяют пациентам с долихоколоном добиваться удовлетворительного самочувствия и сохранять социальную и профессиональную активность (УД 5, СР D).
При сопутствующем дисбактериозе назначают эубактериальные препараты.
При болевом синдроме показано добавление к терапии селективных спазмолитических препаратов (пинаверия бромид, мебеверин), ненаркотических анальгетиков.
При выраженном метеоризме назначают пеногасители (симетикон). По согласованию с неврологом могут быть назначены седативные,
снотворные препараты, антидепрессанты.
Помимо медикаментозной терапии, возможно использование различных физиотерапевтических методов — накожной и ректальной электростимуляции кишечника, иглорефлексотерапии, лазеротерапии [13, 14,
15] (УД 5, СР D).
В случае неэффективности консервативной терапии долихоколона, сопровождающегося нарушением транзита по толстой кишке, может быть рассмотрена возможность хирургического лечения.
Альтернативой хирургическому лечению рефрактерных к терапии запоров является сакральная нейромодуляция (УД 3b, СР C [25, 28, 42]), роль которой изучена недостаточно. Метод подразумевает имплантацию подкожного программируемого стимулятора, обеспечивающего постоянное воздействие низкочастотного электрического тока на крестцовые нервы посредством электрода, проведенного, как правило, через III крестцовое отверстие. Механизм действия сакральной нейромодуляции достоверно неизвестен, однако в ряде исследований отмечено учащение числа дефекаций и снижение потребности в слабительных средствах у больных с медленно-транзитным запором на фоне применения данного метода лечения (УД 3b, СР C [25, 28, 42]).
Хирургическое лечение долихоколона с нарушением транзита по толстой кишке
Принципы хирургического лечения долихоколона с нарушением транзита по толстой кишке соответствуют таковым при лечении медленнотранзитного запора.
Лечение должно быть максимально консервативным, поскольку хирургическое лечение запора имеет неоднозначные функциональные результаты и сопровождается относительно высоким риском осложнений, свойственных для операций на толстой кишке. В частности, общая частота послеоперационных осложнений составляет в среднем 20% (2–71%), при этом летальность достигает 2,6% (0–15%) (УД 3b [22, 29, 36, 38, 43]).
Показанием к хирургическому вмешательству является неэффективность консервативной терапии при выраженном нарушении качества жизни.
Хирургическое лечение долихоколона подразумевает резекцию толстой кишки в объеме субтотальной резекции или колэктомии с формированием илеоректального анастомоза.
Субтотальная резекция ободочной кишки характеризуется лучшими функциональными результатами, по сравнению с колэктомией, но вместе с тем более высокой частотой рецидивов запора (УД 3a [39]).
В качестве альтернативы резекции ободочной кишки может быть сформирована постоянная кишечная стома.
ЛЕЧЕНИЕ ОСЛОЖНЕННОГО ДОЛИХОКОЛОНА
Пациентам с осложненным долихоколоном должно быть предложено плановое хирургическое вмешательство, учитывая риск повторного развития угрожающего жизни осложнения.
При развитии осложнения долихоколона (заворот, инвагинация, узлообразование) лечение проводят в соответствии с принципами терапии странгуляционной кишечной непроходимости. Консервативное лечение включает введение спазмолитических средств, обезболивающих препаратов, внутривенные вливания, применение клизм.
При завороте кишки методом выбора является эндоскопическая деторсия.
В случае невозможности разрешения осложнения с помощью консервативных мероприятий должна быть предпринята срочная операция. При сохранении жизнеспособности участка кишки, вовлеченного в заворот, инвагинат или образование узла, объем операции может быть ограничен деторсией заворота (расправлением инвагината или узла). В случае стойкого нарушения кровоснабжения ободочной кишки, в том числе с развитием некроза, производят ее резекцию (УД 5, СР D [12]). Объем резекции и способ завершения операции определяют на основании протяженности поражения, тяжести состояния больного и степени вы-
раженности кишечной непроходимости и сопутствующих заболеваний. Выполнение фиксирующих операций (мезосигмопликации, сигмо-
пексии, цекопексии) нецелесообразно, так как последние сопровождаются неудовлетворительными функциональными результатами и не исключают рецидива осложнения (УД 5, СР D [2]).
Пациенты, перенесшие срочные вмешательства по поводу осложненного долихоколона, должны подвергнуться полноценному комплексному обследованию, после чего может быть предложена плановая операция (УД 5, СР D [2]).
В случае отсутствия признаков нарушения транзита по толстой кишке у больных с осложненным долихоколоном, возможно выполнение сегментарной резекции удлиненного отдела ободочной кишки (УД 5, СР D [2, 22]).
При сочетании осложненного долихоколона с запором должна быть предложена субтотальная резекция ободочной кишки или колэктомия (УД 5, СР D [2, 22]).
Послеоперационное ведение
Ведение пациентов, перенесших резекцию ободочной кишки по поводу долихоколона, в раннем послеоперационном периоде не имеет особенностей, не требуется специфического лечения или выполнения специальных диагностических процедур.
Все больные долихоколоном после хирургического лечения подлежат диспансерному наблюдению (УД 5, СР D [2]). Периодичность осмотра оперированных больных — 1 раз в 6 мес в течение 1 года с последующим ежегодным обследованием. Цель таких периодических врачебных осмотров — оценка эффективности проведенного хирургического лечения. Выявление пациентов с ухудшением результатов лечения определяет группу лиц для проведения противорецидивных мероприятий.
Изучение общего времени транзита является минимальным диагностическим алгоритмом, который необходим и достаточен для проведения диспансерного наблюдения за моторно-эвакуаторной функцией толстой кишки (УД 5, СР D [2]). Если на этом этапе обследования возникают какие-либо новые сведения об изменении функционального состояния толстой кишки, диагностическая программа должна быть расширена.
Профилактика
Учитывая врожденный характер долихоколона, первичной профилактики этого состояния не существует. Вторичная профилактика подразумевает комплекс мероприятий по предотвращению развития запора (УД 3a, СР B [10]).
n Употреблять хорошо сбалансированную пищу, которая должна включать отруби, цельные зерна пшеницы, свежие фрукты и овощи и не возлагать чрезмерные надежды на прием слабительных средств.
n Употреблять достаточное количество жидкости.
n Регулярно выполнять физические упражнения.
n Уделять достаточное время для спокойного посещения туалета и не подавлять позывы к дефекации. Нет убедительных данных о возможности эффективной профилактики осложнений (заворота, инвагинации, узлообразования) у больных долихоколоном.
При отсутствии противопоказаний к хирургическому лечению пациентам с осложненным долихоколоном должна быть предложена резекция ободочной кишки (см. раздел «Лечение осложненного долихоколон»).
Прогноз
В настоящее время не получено данных, однозначно указывающих на прогрессирующий характер клинических проявлений долихоколона.
Общеизвестен факт большей частоты запоров у пожилых пациентов, однако нет достоверных данных о роли долихоколона в увеличении частоты запора с возрастом. Независимыми факторами, предрасполагающими к запору у пожилых лиц, являются диета, снижение физической активности, прием лекарственных средств.
Хирургическое лечение долихоколона с нарушением транзита по толстой кишке до настоящего времени характеризуется неоднозначными результатами — частота рецидивов запора после колэктомии достигает 10% (УД 2a, СР B [38]).
Нет достаточных данных об отдаленных результатах хирургического лечения долихоколона.
Чего нельзя делать
n Проводить медикаментозное или хирургическое лечение бессимптомного долихоколона.
n Ставить целью хирургического вмешательства коррекцию длины толстой кишки.
n Начинать лечение долихоколона, сопровождающегося запором, без полноценного обследования, исключающего другие возможные причины нарушения транзита по толстой кишке.
n Необоснованно назначать слабительные средства.
Критерии оценки качества помощи в стационаре представлены в таблице 15.4. Для оценки качества медицинской помощи используют временные, процессуальные и профилактирующие критерии. Временные характеризуют своевременность оказания определенных этапов медицинской помощи. Выполнение пациенту ряда медицинских манипуляций, инструментальных и лабораторных исследований, необходимых для качественного оказания медицинской помощи, оценивают в процессуальных критериях. Для анализа мероприятий, направленных на предотвращение развития осложнений, используют профилактирующие критерии.
Таблица 15.4. Критерии оценки качества медицинской помощи в стационаре больным с долихоколоном (0 — нет, 1 — да)
|
Клинические рекомендации |
Временные |
Процессуальные |
Профилактирующие |
|
1. Клинические рекомендации по диагностике и лечению взрослых больных с идиопатическим мегаколоном (код МКБ — К59.3). |
Установка клинического диагноза в течение 72 ч: 0/1 |
Пальцевое обследование прямой кишки: 0/1. Ректороманоскопия: 0/1. Ирригоскопия: 0/1. Исследование крови на сифилис, вирусный гепатит В, вирусный гепатит С: 0/1. Клинический анализ крови; биохимический анализ крови; клинический анализ мочи; коагулограмма: 0/1. |
Отсутствие осложнений: • кровотечение: 0/1; • пневмония: 0/1; • тромбоэмболия: 0/1; • послеоперационная спаечная кишечная непроходимость: 0/1; • перитонит: 0/1; • летальный исход 0/1 |
Табл. 15.4. Окончание
|
Клинические рекомендации |
Временные |
Процессуальные |
Профилактирующие |
|
2. Клинические |
|
При подозрении на болезнь |
|
|
рекомендации |
Гиршпрунга определение | ||
|
по диагностике |
активности ацетилхолинэсте- | ||
|
и лечению болез- |
разы в биоптате слизистой | ||
|
ни Гиршпрунга |
оболочки прямой кишки: 0/1. | ||
|
у взрослых (код |
При подозрении на болезнь | ||
|
МКБ — Q43.1). |
Гиршпрунга определение рек- | ||
|
3. Клинические |
тоанального ингибиторного | ||
|
рекомендации |
рефлекса: 0/1. | ||
|
по диагностике |
При дифференциальной диа- | ||
|
и лечению взрос- |
гностике болезни Гиршпрунга | ||
|
лых пациентов |
и идиопатического мегако- | ||
|
с долихоколоном |
лона проведение биопсии | ||
|
(код МКБ — |
по Свенсону: 0/1. | ||
|
Q43.8) |
Метод оперативного лечения | ||
|
|
в соответствии с установлен- | ||
|
|
ным диагнозом и клинически- | ||
|
|
ми рекомендациями: 0/1. | ||
|
|
Метод анестезии в соответ- | ||
|
|
ствии с объемом оперативно- | ||
|
|
го лечения: 0/1 |
Литература
1. Анистратенко И.К. Клиника и лечение аномалий развития толстого кишечника. — Киев, 1969. — 128 с.
2. Ачкасов С.И. Аномалии развития и положения толстой кишки (клиника, диагностика, лечение): Дис. … д-ра мед. наук. — М., 2003. — 297 с.
3. Ачкасов С.И., Саламов К.Н., Капуллер Л.Л. и др. Запоры при аномалиях развития и положения толстой кишки у взрослых // Рос. журн. гастроэнтерол., гепатол., колопроктологии. — 2000. — № 2. — С. 58–62.
4. Воробьев Г.И., Саламов К.Н., Минц Я.В., Мушникова В.Н. Аномалии толстой кишки // Хирургия. — 1989. — № 10. — С. 154–155.
5. Иванов А.И. Этиопатогенез, классификация, клиника, диагностика и лечение хронического толстокишечного стаза, обусловленного аномалиями развития и фиксации ободочной кишки. Методические рекомендации. — Якутск, 1997. — 44 с.
6. Колопроктология и тазовое дно / Под ред. М.М. Генри, М. Своша. — М.: Медицина, 1988. — С. 415–416.
7. Королев Л.Ф. Узлообразования кишечника // Хирургия. — 1966. —
№ 3. — С. 45–48.
8. Ленюшкин А.И. Хирургическая колопроктология детского возраста: Руководство для врачей. — М.: Медицина, 1999. — 368 с.
9. Малоинвазивная колопроктология / Под ред. М.Е. Аррегви, Дж.М. Саккиера. — М., 1999. — 280 с.
10. Практическое руководство по диагностике и лечению запоров Всемирной организации гастроэнтерологов (2007). http://www.worldgastroenterology. org/assets/downloads/ru/pdf/guidelines/g_data4_ru.pdf.
11. Романов П.А. Клиническая анатомия вариантов и аномалий толстой кишки. — М., 1987. — 192 c.
12. Руководство по неотложной хирургии органов брюшной полости / Под ред. В.С. Савельева. — М., 1986. — 608 с.
13. Самсонюк В.Г., Захарченко А.А., Штоппель А.Э. Комплексное консервативное лечение нарушений моторно-эвакуаторной функции толстой кишки // Проблемы колопроктологии: Сборник. — М.: МНПИ, 2000. — Вып. 17. — С. 530–535.
14. Тупикова А.П., Подмаренкова Л.Ф., Елисеева М.В., Румянцев В.Г. Функ-
циональное обоснование применения физических факторов воздействия в лечении нарушений моторно-эвакуаторной функции толстой кишки // Рос. журн. гастроэнтерол., гепатол. и колопроктол. — 1995. — Т. 5, № 3. — С. 71–76.
15. Хаммад Е.В. Хронический запор (тактика совершенствования диагностики и лечения): Дис. … канд. мед. наук. — М., 1997. — 134 с.
16. Царев Н.И. Удлиненная толстая кишка как хроническое заболевание // Вестн. хир. — 1981. — Т. 127, № 9. — С. 58–63.
17. Шелыгин Ю.А., Благодарный Л.А. Справочник по колопроктологии. — М.: Литтерра, 2012. — 596 с.
18. Энциклопедический словарь медицинских терминов / Под ред. Б.В. Петровского. — М.: Советская энциклопедия, 1982. — 464 с.
19. Brummer P., Seppala P., Wegelius U. Redundant colon as a cause of constipation // Gut. — 1962. — Vol. 3. — P. 140–141.
20. Corman M.L. Colon and Rectal Surgery. — Philadelphia: Lippincott, 1984. — P. 129–134.
21. Dufour P., Gendre P. Ultrastructure of mouse intestinal mucosa and changes observed after long term anthraquinone administration // Gut. — 1984. — Vol. 25. — P. 1358–1363.
22. Feng Y, Jianjiang L. Functional outcomes of two types of subtotal
colectomy for slow-transit constipation: ileosigmoidal anastomosis and cecorectal anastomosis // Am. J. Surg. — 2008. — Vol. 195. — P. 73–77.
23. Gray E.J., Marteinsson B.T.H. Dolichocolon: Indication for operation // Am. Surg. — 1971. — Vol. 37, N 8. — P. 509–511.
24. Grossman E.M., Longo E.W., Stratton M.D. et al. Sigmoid volvulus in department of veterans affairs medical centers // Dis. Colon Rectum. — 2000. — Vol. 43. — P. 414–418.
25. Kamm M.A., Dudding T.C., Melenhorst J. et al. Sacral nerve stimulation for
intractable constipation // Gut. — 2010. — Vol. 59. — P. 333–340.
26. Kamm M.A., Van der Sijp J.R.M., Hawley P.R. et al. Left hemicolectomy with rectal excision for severe idiopathic constipation // Int. J. Colorectal Dis. — 1991. — Vol. 6. — P. 49–51.
27. Kamm M.A., Hawley P.R., Lennard-Jones J.E. Outcome of colectomy for severe idiopathic constipation // Gut. — 1988. — Vol. 29. — P. 969–973.
28. Kenefick N.J. Sacral nerve neuromodulation for the treatment of lower bowel motility disorders // Ann. R. Coll. Surg. Engl. — 2006. — Vol. 88. — P. 617–623.
29. Knowles C.H., Scott M., Lunniss P.J. Outcome of colectomy for slow transit constipation // Ann. Surg. — 1999. — Vol. 230. — P. 627–638.
30. Keuzenkamp-Jansen C.W., Fijnvandraat C.J., Kneepkens C.M., Douwes A.C. Diagnostic dilemmas and results of treatment for chronic constipation // Arch. Dis. Child. — 1996. — Vol. 75, N 1. — P. 36–41.
31. Longstreth G.F., Thompson W.G., Chey W.D. et al. Functional bowel disorders // Gastroenterology. — 2006. — Vol. 130, N 5. — P. 1480–1491.
32. Lubowski D.Z., Chen F.C., Kennedy M.L., King D.W. Results of colectomy for severe slow transit constipation // Dis. Colon Rectum. — 1996. — Vol. 39. — P. 23–29.
33. Mellor S.G., Phillips R.K.S. The aetiology and management of sigmoid volvulus in the UK: how much colon need be excised? // Ann. R. Coll. Surg. Engl. — 1990. — Vol. 72. — P. 193–195.
34. Muller-Lissner S.A., Kamm M.A., Scarpignato C., Wald A. Myths and misconceptions about chronic constipation // Am. J. Gastroenterol. — 2004. — Vol. 99. — P. 1–11.
35. Northeast A.D.R., Dennison A.R., Lee E.G. Sigmoid volvulus: new thoughts on the epidemiology // Dis. Colon. Rectum. — 1984. — Vol. 27, N 4. — P. 260–261.
36. Nylund G., Oresland T., Fasth S., Nordgren S. Long-term outcome after colectomy in severe idiopathic constipation // Colorectal Dis. — 2001. — Vol. 3. — P. 253–258.
37. OCEBM Levels of Evidence Working Group. The Oxford 2011 Levels of Evidence. — Oxford Centre for Evidence-Based Medicine, 2011.
38. Riss S., Herbst F., Birsan T., Stift A. Postoperative course and long term follow up after colectomy for slow transit constipationis surgery an appropriate approach? // Colorectal Dis. — 2009. — Vol. 11. — P. 302–307.
39. Pfeifer J., Agachan F., Wexner S.D. Surgery for constipation. A review // Dis. Colon Rectum. — 1996. — Vol. 39. — P. 444–460.
40. Schagen van Leeuwen J.H. Sigmoid volvulus in a West African population // Dis. Colon Rectum. — 1985. — Vol. 28, N 10. — P. 712–716.
41. The Large Intestine: Physiology, Pathophysiology, and Disease / Eds S.F. Phillips, J.H. Pemberton, P.G. Shorter. — N.Y.: Mayo Foundation, 1991. — P. 10.
42. Thomas G.P., Dudding T.C., Rahbour G. et al. Sacral nerve stimulation for constipation // Br. J. Surg. — 2013. — Vol. 100, N 2. — P. 174–181.
43. Zutshi M., Hull T.L., Trzcinski R. et al. Surgery for slow transit constipation: are we helping patients? // Int. J. Colorectal Dis. — 2007. — Vol. 22. — P. 265–269.
ИДИОПАТИЧЕСКИЙ МЕГАКОЛОН
Введение
Причиной остро развивающегося мегаколона могут быть механическое препятствие (опухоль, стриктура кишки воспалительной или ишемической природы), синдром псевдообструкции или тяжелое воспаление (токсический мегаколон как осложнение язвенного или псевдомембранозного колита). Хроническое расширение толстой кишки может быть обусловлено органическим поражением центральной нервной системы, в том числе спинальными травмами, а также рядом эндокринологических расстройств. Кроме того, хронический мегаколон наблюдается при болезни Гиршпрунга у взрослых, аноректальных пороках развития (атрезии, стеноз) и некоторых инфекционных процессах (болезнь Чагаса). Диагноз идиопатического мегаколона устанавливается путем исключения как кишечных, так и внекишечных известных причин расширения толстой кишки.
Расширение правых отделов более характерно для синдрома псевдообструкции и токсической дилатации. Идиопатический мегаколон наблюдается в виде изолированного расширения ободочной кишки (чаще левых отделов, реже тотального) при нормальном размере прямой кишки или же охватывает дистальные отделы толстой кишки — мегаректум в сочетании с более или менее протяженным расширением сигмовидной кишки. Расширенной может оказаться и вся толстая кишка.
Распространенность идиопатического мегаколона неизвестна, но в целом это редко встречающееся состояние. При ретроспективном анализе из 1600 пациентов с запором, обратившихся в Лондонский Королевский госпиталь за 10-летний период, только у 20 были выявлены рентгенологические признаки мегаколона/мегаректума [28]. Однако, с другой стороны, умеренно выраженные формы этого состояния часто остаются нераспознанными, и, по некоторым данным, до 11% пациентов с рефрактерным запором могут иметь мегаколон [44, 48]. Кроме того, оценка распространенности мегаколона затруднена отсутствием общепринятых диагностических критериев этого состояния.
Настоящие рекомендации по диагностике и лечению пациентов с идиопатическим мегаколоном служат руководством для практических врачей, осуществляющих ведение и лечение таких больных.
Рекомендации включают следующие разделы: определение, классификация, код по МКБ-10, диагностика, консервативное и оперативное лечение, правила ведения периоперационного периода, а также прогноз.
Рекомендации подлежат регулярному пересмотру в соответствии с новыми данными научных исследований в этой области. Данные рекомендации составлены на основе метаанализов M.A. Gladman и соавт., выполненных в 2005 и 2008 гг. [19, 22], и данных литературы из базы данных PubMed, MEDLINE, Cochrane Collaboration.
В настоящих клинических рекомендациях применяется общепринятая система оценки уровней доказательности и степеней рекомендации, основанная на разработках Оксфордского центра доказательной медицины (табл. 16.1) (Phillips Bob, 1998).
Таблица 16.1. Уровни доказательности и степени рекомендаций на основании руководства Оксфордского центра доказательной медицины
|
Уровень |
Исследования методов диагностики |
Исследования методов лечения |
|
1а |
Систематический обзор гомогенных диагностических исследований 1-го уровня |
Систематический обзор гомогенных РКИ |
|
1b |
Валидизирующее когортное исследование с качественным «золотым стандартом» |
Отдельное РКИ (с узким доверительным интервалом) |
|
1с |
Специфичность или чувствительность столь высокие, что положительный или отрицательный результат позволяет исключить/установить диагноз |
Исследование «Всё или ничего» |
|
2а |
Систематический обзор гомогенных диагностических исследований >2-го уровня |
Систематический обзор (гомогенных) когортных исследований |
|
2b |
Разведочное когортное исследование с качественным «золотым стандартом» |
Отдельное когортное исследование (включая РКИ низкого качества; т.е. с <80% пациентов, прошедших контрольное наблюдение) |
|
2с |
Нет |
Исследование «исходов»; экологические исследования |
|
3а |
Систематический обзор гомогенных исследований уровня 3b и выше |
Систематический обзор гомогенных исследований «случай–контроль» |
|
3b |
Исследование с непоследовательным набором или без проведения исследования «золотого стандарта» у всех испытуемых |
Отдельное исследование «случай– контроль» |
|
4 |
Исследование «случай–контроль» или исследование с некачественным или зависимым «золотым стандартом» |
Серия случаев (и когортные исследования или исследования «случай–контроль» низкого качества) |
Табл. 16.1. Окончание
|
5 |
Мнение экспертов без тщательной критической оценки или основанное на физиологии, лабораторные исследования на животных или разработка «первых принципов» |
Мнение экспертов без тщательной критической оценки, лабораторные исследования на животных или разработка «первых принципов» |
|
Степени рекомендаций | ||
|
A |
Согласующиеся между собой исследования 1-го уровня | |
|
B |
Согласующиеся между собой исследования 2-го или 3-го уровня или экстраполяция на основе исследований 1-го уровня | |
|
C |
Исследования 4-го уровня или экстраполяция на основе уровня 2 или 3 | |
|
D |
Доказательства 4-го уровня или затруднительные для обобщения или некачественные исследования любого уровня | |
Следует отметить, что в силу невысокой распространенности идиопатического мегаколона и противоречий в диагностических критериях большинство публикаций по этой проблеме являются по существу сообщениями о серии случаев с низким уровнем доказательности. Таким образом, большинство рекомендаций по диагностике и лечению соответствуют степени D или С, что необходимо учитывать при принятии решения в каждой конкретной клинической ситуации.
ВАЛИДИЗАЦИЯ РЕКОМЕНДАЦИЙ
Настоящие рекомендации составлены общероссийской общественной организацией «Ассоциация колопроктологов России», в предварительной версии были рецензированы независимыми экспертами, которых попросили прокомментировать, насколько интерпретация доказательств, лежащих в основе рекомендаций, доступна для понимания. Получены комментарии со стороны врачей амбулаторного звена, которые тщательно систематизировались и обсуждались на совещаниях экспертной группы. Последние изменения в настоящих рекомендациях были представлены для дискуссии на заседании профильной комиссии «Колопроктология» Экспертного совета Минздрава России 12 сентября 2013 г. Проект рекомендаций был повторно рецензирован независимыми экспертами и врачами амбулаторного звена. Для окончательной редакции и контроля качества рекомендации были повторно проанализированы членами экспертной группы, которые пришли к заключению, что все замечания и комментарии приняты во внимание, риск систематических ошибок
при разработке рекомендаций сведен к минимуму.
ОБЛАСТЬ ПРИМЕНЕНИЯ РЕКОМЕНДАЦИЙ
Данные рекомендации применимы при осуществлении медицинской деятельности в рамках Порядка оказания медицинской помощи взросло-
му населению с заболеваниями толстой кишки, анального канала и промежности колопроктологического профиля.
Определение
Идиопатический мегаколон — это хроническое расширение толстой кишки, для которого не удается выявить четкий этиологический фактор.
Код по Международной классификации болезней 10-го пересмотра
n Класс: Болезни органов пищеварения (XI).
n Блок: Другие болезни кишечника (K55–K63).
n Раздел: Другие функциональные кишечные нарушения (К59).
n Код: К59.3 Мегаколон, не классифицированный в других рубриках.
Классификация
Общепринятой классификации идиопатического мегаколона не существует. В англоязычной литературе обычно описывается 3 вида мегаколона в зависимости от локализации патологически расширенного отдела:
n Idiopathic megacolon — расширение ободочной кишки или ее отдела;
n Idiopathic megarectum — расширение прямой кишки;
n Idiopathic megabowel — расширение всей толстой кишки, т.е. сочетание мегаколона с мегаректумом.
Согласно классификации мегаколона у взрослых, предложенной Г.И. Воробьевым (1982), выделяется 3 анатомические формы идиопатического мегаколона:
1) мегаректум;
2) мегаколон;
3) долихомегаколон [4].
В зависимости от протяженности пораженного сегмента ободочной кишки выделяют:
n мегасигму — расширение сигмовидной кишки;
n левосторонний мегаколон — расширение сигмовидной и нисходящей ободочных кишок;
n субтотальный мегаколон — распространение поражения до правого изгиба;
n тотальный мегаколон — расширение всей ободочной кишки и слепой кишки.
Формулировка диагноза
При формулировании диагноза следует отразить форму мегаколона, протяженность поражения для ободочной кишки и наличие осложнений (СР D). Примеры формулировок диагноза:
n Идиопатический мегаректум.
n Идиопатический левосторонний мегаколон, осложненный рецидивирующими заворотами сигмовидной кишки.
n Идиопатический мегаректум, мегасигма, осложненный формированием калового камня прямой и сигмовидной кишки с нарушением кишечной проходимости. Стеркоральная язва сигмовидной кишки, рецидивирующие кишечные кровотечения. Вторичная анемия.
Диагностика
Диагностическая программа преследует две цели:
1) выявление мегаколона и его осложнений, определение протяженности поражения;
2) исключение известных кишечных и внекишечных причин его возникновения.
ДИАГНОСТИЧЕСКИЕ КРИТЕРИИ
Единых общепринятых критериев мегаколона не существует. Расширение кишки может быть столь выраженным, что выявляется уже при клиническом осмотре, лапаротомии или обзорной рентгенографии органов брюшной полости. Однако расширение кишки может быть не столь демонстративным, и постановка диагноза на основании таких признаков в значительной степени субъективна и не всегда возможна. Основной метод выявления мегаколона — рентгенологический: измерение ширины просвета кишки при тугом ее наполнении, обычно бариевой взвесью, в условиях двойного контрастирования. Параметры «нормы» были получены в двух основных рентгеноморфометрических исследованиях и оказались сопоставимы за исключением ширины прямой кишки [2, 36] (табл. 16.2).
Таблица 16.2. Ширина просвета различных отделов толстой кишки в норме
|
Отдел кишки |
Ширина просвета, см | |
|
Ачкасов С.И., 2003 (n=160) |
Preston D.M., Lennard-Jones J.E. et al., 1985 (n=50) | |
|
Слепая |
4,0–9,0 |
– |
|
Восходящая |
2,5–9,0 |
5,0–9,3 |
|
Поперечная |
2,5–8,5 |
4,5–8,3 |
|
Нисходящая |
1,5–6,0 |
3,7–7,1 |
|
Сигмовидная |
1,5–6,0 |
3,3–6,3 |
|
Прямая |
4,5–8,5 |
2,2–6,5 |
Несоответствие в нормальных показателях диаметра прямой кишки между двумя исследованиями, вероятно, объясняется различиями в методике проведения теста. Косвенным подтверждением этого явля-
ется тот факт, что верхний предел ширины прямой кишки у здоровых добровольцев, по данным эвакуаторной проктографии, составил 8,3 см [21]. Учитывая стандартизацию методики двойного контрастирования на территории Российской Федерации, рекомендуется использовать параметры, полученные отечественными авторами (СР D). Диагноз
«мегаколон» устанавливается, если ширина просвета какого-либо отдела толстой кишки превышает указанные значения. Таким образом, если наибольший диаметр прямой кишки в любой проекции превышает 8,5 см, диагностируется мегаректум. Ширина сигмовидной кишки более 6 см служит основанием для постановки диагноза мегасигмы.
Альтернативным диагностическим критерием мегаректума является повышение МПО воздуха, вводимого в ректальный латексный баллон при аноректальном физиологическом исследовании [39, 49]. У данного критерия существует ряд недостатков: проникновение ректального баллона в сигмовидную кишку за счет осевого растяжения, снижение чувствительности прямой кишки к наполнению могут привести к гипердиагностике мегаректума. С другой стороны, неполное опорожнение кишки перед исследованием может быть причиной ложноотрицательного результата и соответственно недооценки ее размеров. А для пациентов с мегаректумом как раз характерны трудности с подготовкой к исследованиям. Кроме того, величина МПО сильно зависит от методики проведения теста (скорость инсуффляции воздуха, ее дискретность или непрерывность и т.д). В результате нормальные значения МПО, превышение которых свидетельствует о наличии мегаректума, существенно отличаются в разных лабораториях. Тем не менее, если ирригоскопия еще не была выполнена, данный метод может быть использован в качестве скрининг-теста у пациентов с запором. Поскольку большинство из них не имеют мегаректума, это позволит избежать контрастного исследования и снизить радиационную нагрузку (УД 5, СР D [22]).
Методом диагностики мегаректума, позволяющим частично преодо-
леть описанные выше трудности, является исследование резервуарной функции прямой кишки. Оно заключается в постепенном ступенчатом заполнении латексного ректального баллона воздухом с шагом в 20 мл и интервалом в 20 с. Одновременно записывается манометрическая кривая, отражающая изменение давления в прямой кишке соответственно изменению объема вводимого в баллон воздуха. Интегральным
показателем адаптационной способности прямой кишки является индекс максимально переносимого объема (IМПО) — отношение максимально переносимого объема к величине создаваемого им остаточного ректального давления: VМПО/PМПО, где VМПО и PМПО — объем и остаточное давление, соответствующие максимально переносимому объему. Увеличение IМПО свыше 15 мл/мм рт.ст., т.е. больше максимального значения, зарегистри-
рованного у добровольцев, служит диагностическим критерием идиопа-
тического мегаректума [1].
Недавно была предложена еще одна методика диагностики мегаректума. Она заключается в рентгеноскопической оценке ширины просвета прямой кишки во время изобарического ее растяжения с помощью баростата. О мегаректуме свидетельствует максимальный ректальный диаметр более 6,3 см при минимальном ректальном давлении (давлении при инсуффляции такого количества воздуха, которое предотвращает спадание стенок, но не вызывает активного растяжения прямой кишки) [21]. Нормальные показатели, как и для предыдущей методики, были получены при изучении здоровых добровольцев.
Выбор способа диагностики мегаректума определяется диагностическими ресурсами конкретного колопроктологического центра. Если есть техническая возможность, в качестве первого шага предпочтительно использовать физиологические методы исследования с целью снижения лучевой нагрузки на пациентов (УД 5, СР D).
ДИФФЕРЕНЦИАЛЬНАЯ ДИАГНОСТИКА
С целью подтверждения идиопатического характера мегаколона следует исключить все известные причины его возникновения. Для этого необходимо провести комплексное обследование.
Подробный опрос пациента. Для большинства пациентов с идиопатическим мегаколоном характерен длительный анамнез запора. В случае идиопатического расширения дистальных отделов толстой кишки (изолированный мегаректум или в сочетании с мегасигмой) симптомы обычно наблюдаются с раннего детства. При этом очень характерно сочетание запора с каломазанием, в отличие от болезни Гиршпрунга, при которой запор также отмечается с детства, но каломазания не бывает. У пациентов с идиопатическим мегаколоном при нормальном размере прямой кишки обычно удается выявить склонность к запору в детстве и юности, однако манифестация симптоматики чаще приходится на более поздний возраст.
У части больных с течением времени запор сменяется неустойчивым стулом и поносом в сочетании с прогрессирующим вздутием живота, похудением, приступами затрудненного отхождения газов. Такое
«острое» ухудшение состояния подчас и служит поводом для обращения к врачу. Другой причиной острого развития симптоматики может быть осложненное течение идиопатического мегаколона — заворот кишки, чаще всего сигмовидной. При этом характерно появление острой боли в животе, обычно первоначально схваткообразной, в сочетании со вздутием живота и прекращением отхождения газов и кишечного содержимого.
Однако чаще короткий анамнез заболевания позволяет предположить вторичный характер мегаколона. В таком случае необходимо, прежде всего, исключить опухоль кишки или воспалительную стриктуру, а также токсический мегаколон как осложнение язвенного или псев-
домембранозного колита и синдром псевдообструкции (синдром Огилви). В пользу последнего может указывать анамнез приема наркотиков или лекарственных препаратов (анестетики, миорелаксанты, антидепрессанты и др.), а также перенесенная травма, в том числе хирургические вмешательства.
При сборе анамнеза необходимо помнить, что причиной развития мегаколона могут быть органические поражения центральной нервной системы и эндокринологические расстройства. А указание на пребывание в южно-американских странах, особенно при наличии связи между поездкой и возникновением симптомов, позволит заподозрить паразитарный характер заболевания (болезнь Чагаса).
Физикальный осмотр. Общее состояние пациентов с неосложненным идиопатическим мегаколоном обычно не страдает. В случае выраженного мегаколона при осмотре и пальпации часто выявляются вздутие живота, тупой реберный угол, истончение передней брюшной стенки. Характерно уменьшение/исчезновение печеночной тупости за счет оттеснения печени кзади расширенной ободочной кишкой. У пациентов с дистальным расширением кишки над лоном нередко пальпируется верхний полюс опухолевидного образования полости таза — калового комка/камня в просвете прямой кишки. Каловые камни могут определяться через переднюю брюшную стенку и в лежащих выше отделах ободочной кишки. Наличие лихорадки, тахикардии, озноба, тошноты, рвоты, перитонеальных симптомов свидетельствует о вторичном мегаколоне или же осложненном течении идиопатического.
Осмотр перианальной области, пальцевое исследование прямой кишки и ректороманоскопия позволяют прежде всего исключить опухолевую природу мегаколона или обструктивную при аноректальных атрезиях и стенозах. Наличие следов кала на перианальной коже является подтверждением каломазания, характерного для идиопатического мегаректума. Тонус анального жома и волевые сокращения обычно при этом сохранены. Также для идиопатического мегаректума типично выявляемое при пальцевом исследовании расширение прямой кишки сразу за анальным каналом и наличие в ней большого количества замазкообразного содержимого или калового камня. При болезни Гиршпрунга, в отличие от идиопатического мегаректума, ампула прямой кишки чаще всего пуста, и перианальная область не изменена. Однако в случае идиопатического мегаколона без мегаректума при осмотре и пальцевом обследовании прямой кишки существенные изменения также не выявляются. Но при ректоскопии для болезни Гиршпрунга характерно затрудненное проведение ректоскопа через прямую кишку, несмотря на активную инсуффляцию воздуха, и затем резкий переход в расширенную кишку, как правило, содержащую большое количество содержимого. При идиопатическом мегаколоне тонус даже нерасширенной прямой кишки снижен и переход в мегасигму постепенный (УД 5, СР D).
Исследования крови
n Общий анализ крови.
n Скорость оседания эритроцитов (СОЭ).
n Биохимический анализ крови.
n Уровень кальция, калия плазмы.
n Уровень тиреотропного гормона — ориентировочный тест для исключения гипотиреоза как причины мегаколона.
Рентгенологические методы исследования
n Обзорная рентгенография брюшной полости позволяет заподозрить наличие мегаколона или его осложнений: заворота кишки или калового камня, являющихся причиной нарушения кишечной проходимости, перфорации кишки при токсическом мегаколоне или синдроме псевдообструкции. При плановом обследовании пациента с мегаколоном используется редко.
n Ирригоскопия — основной метод диагностики мегаколона (см. раздел
«Диагностические критерии мегаколона»). Кроме того, контрастное исследование необходимо для дифференциальной диагностики идиопатического мегаколона и болезни Гиршпрунга. Для болезни Гиршпрунга характерна резкая граница между расширенной ободочной кишкой и относительно суженным дистальным аганглионарным сегментом различной протяженности (чаще прямая кишка, возможно, с частью сигмовидной). При идиопатическом мегаколоне или прямая кишка расширяется сразу от анального канала, или же имеется постепенный переход нормального размера прямой кишки в расширенную сигмовидную.
n Исследование транзита по ЖКТ бариевой взвеси, рентгеноконтрастных маркеров или радиофармпрепарата у пациентов с идиопатическим мегаколоном используется для оценки пропульсивной активности нерасширенных отделов толстой кишки при определении границ резекции во время планового хирургического вмешательства (см. раздел «Хирургическое лечение»).
Колоноскопия используется для исключения обструктивного мегаколона различной этиологии (прежде всего опухолевой). В случае заворота кишки, помимо диагностики (выявление спирально суженного сегмента кишки), колоноскопия преследует лечебную цель — попытку деторсии заворота и декомпрессии кишки.
Аноректальные физиологические тесты
n Аноректальная манометрия — исследование ректоанального ингибиторного рефлекса (рефлекторного расслабления внутреннего сфинктера в ответ на повышение давления в прямой кишке). Отсутствие ректоанального ингибиторного рефлекса является надежным диагностическим критерием болезни Гиршпрунга с чувствительностью 70–95%. При идиопатическом мегаколоне/мегаректуме ректоанальный ингибиторный рефлекс сохранен, хотя порог его может быть существенно повышен за счет увеличения объема прямой кишки.
n Исследование резервуарной функции прямой кишки позволяет диагностировать и количественно оценить выраженность мегаректума. Увеличение индекса максимально переносимого объема IМПО свыше 15 мл/мм рт.ст. является диагностическим критерием идиопатического мегаректума (см. раздел «Диагностические критерии мегаколона»).
Исследование ацетилхолинэстеразной активности в биоптатах слизистой оболочки прямой кишки — еще один качественный тест, необходимый для дифференциальной диагностики идиопатического мегаколона и болезни Гиршпрунга. Проба на ацетилхолинэстеразу положительная при болезни Гиршпрунга и отрицательная при идиопатическом мегаколоне. Биоптаты берутся в прямой кишке, обычно с 5, 10 и 15 см.
Биопсия стенки прямой кишки по Свенсону — иссечение полнослойного участка стенки прямой кишки с последующим морфологическим исследованием. Необходимость в этой инвазивной процедуре возникает при дифференциальной диагностике идиопатического мегаколона и болезни Гиршпрунга, когда имеются противоречия между данными аноректальной манометрии, результатами пробы на ацетилхолинэстеразу и рентгенологической картиной. Выявление аганглиоза межмышечного и подслизистого нервных сплетений является надежным подтверждением болезни Гиршпрунга. Следует помнить, что зона физиологического гипои аганглиоза может распространяться до 5 см проксимальнее зубчатой линии [5]. Во избежание ложноположительного результата исследования рекомендуется выполнение биопсии путем иссечения полнослойного лоскута шириной 1 см по задней стенке прямой кишки от зубчатой линии протяженностью не менее 6 см (УД 5, СР D [3]).
Для исключения внекишечных причин развития вторичного мегаколона может понадобиться консультация следующих специалистов:
n эндокринолога (исключение гипотиреоза, гиперпаратиреоза, феохромоцитомы, множественной эндокринной неоплазии);
n невролога (исключение органического поражения центральной нервной системы);
n психиатра (исключение психогенного мегаколона, оценка психического статуса пациентов с сочетанием идиопатического мегаколона и ипохондрии, астеноневротического синдрома и пр.);
n ревматолога (исключение системных заболеваний соединительной ткани как причины мегаколона).
Может также возникнуть необходимость в дополнительных обследованиях:
n УЗИ брюшной полости, малого таза, щитовидной железы;
n КТ или МРТ брюшной полости, малого таза;
n эзофагогастродуоденоскопии;
n анализе кала на токсины Cl. difficile (исключение псевдомембранозного колита как причины токсического мегаколона).
Лечение
ЛЕЧЕБНАЯ ТАКТИКА
При неосложненном течении идиопатического мегаколона лечение в большинстве случаев консервативное. В настоящее время не существует лекарственных препаратов или иных терапевтических методов,
позволяющих добиться исчезновения идиопатического мегаколона. Даже при полном купировании симптоматики ширина просвета кишки существенно не меняется. Цель лечения заключается в подборе эффективного и удобного для пациента режима опорожнения кишечника и купировании или облегчении симптомов абдоминального дискомфорта. Необходимость в хирургическом вмешательстве возникает при развитии осложнений или высоком их риске и неэффективности или непереносимости пациентом консервативных методов лечения (УД 5, СР D).
КОНСЕРВАТИВНОЕ ЛЕЧЕНИЕ
Неосложненный мегаколон
Консервативное лечение пациентов с идиопатическим мегаколоном принципиально не отличается от терапии хронического медленно-транзитного запора. В качестве первого этапа назначаются высокошлаковая диета и препараты пищевых волокон, микрокристаллическая целлюлоза, морские водоросли, пищевые отруби и т.д. в сочетании с увеличением количества потребляемой жидкости и усилением физической активности. При этом пациенты должны быть предупреждены, что пищевые волокна не обладают немедленным слабительным действием. Эффект от лечения проявляется в течение 3–4 нед. Подчас неплохой результат дает дополнительное назначение желчегонных препаратов, так как желчные кислоты обладают естественным слабительным эффектом. Боли и вздутие живота помогают облегчить спазмолитики [мебеверин (дюспаталин♠), пинаверия бромид (дицетел♠)] и препараты симетикона (эспумизан♠) (УД 5, СР D).
Назначение препаратов пищевых волокон не всегда приводит к улучшению. Более того, состояние пациентов с мегаколоном на фоне высокошлаковой диеты может даже ухудшаться за счет усиления метеоризма и тяжести в животе. Таким больным рекомендуется назначать препараты полиэтиленгликоля (макрогол).
Следующий этап консервативного лечения при неэффективности предыдущих — назначение стимулирующих слабительных. Основными представителями этой группы лекарств являются препараты, содержащие антрахиноны, преимущественно растительного происхождения (сена, алоэ, ревень), и соединения дифенилметана (бисакодил, натрия пикосульфат). Они обладают прокинетическим действием, повышают интестинальную секрецию и снижают абсорбцию. Следует отметить, что значительное число как отечественных, так и зарубежных авторов считают длительный прием препаратов этой группы опасным из-за повреждающего их действия на интрамуральный нервный аппарат и предполагаемого канцерогенного эффекта [7, 9, 11, 13, 14, 37, 38, 40, 41]. Однако дегенеративные изменения в нервных сплетениях, выявленные авторами у пациентов со стойким запором, могли быть не следствием
длительного применения слабительных, а изначальной причиной замедления транзита. А результаты, полученные в экспериментах на животных, не были подтверждены позднее другими исследователями, использовавшими более современные методы и оборудование [17, 27]. Также в экспериментах in vitro и на животных было показано, что стимулирующие слабительные обладают канцерогенным эффектом [47]. Однако в этом исследовании применялись сверхвысокие дозы слабительных. S.A. Muller-Lissner и соавт. (2004) на основании широкого анализа литературы, включая контролируемые исследования, делают вывод, что применяемые в настоящее время слабительные не увеличивают риск колоректального рака даже при многолетнем применении [35]. Таким образом, представляется вполне оправданным длительное использование слабительных, в том числе и стимулирующих, если они позволяют пациентам добиваться удовлетворительного самочувствия и сохранять социальную и профессиональную активность (УД 5, СР D).
У пациентов с расширением дистальных отделов толстой кишки слабительные лучше сочетать с регулярными клизмами объемом 200–600 мл для облегчения опорожнения прямой кишки. Периодичность клизм определяется индивидуально — от 2–3 раз в неделю до 1–2 раз в месяц (УД 5, СР D).
Помимо слабительных и клизм, возможно использование различных физиотерапевтических методов — электростимуляции кишечника, накожной и ректальной, иглорефлексотерапии, лазеротерапии [6, 8, 10] (УД 5, СР D). При наличии технической возможности у пациентов с идиопатическим мегаректумом рекомендуется применение терапии с использованием БОС-терапии, хотя данные о ее эффективности ограничены (УД 4, СР D [33]).
Консервативное лечение осложненного мегаколона
Заворот кишки на фоне мегаколона или нарушение кишечной проходимости, обусловленное каловым камнем или завалом, служит показанием для срочной госпитализации пациента. Методом выбора лечения заворота являются эндоскопическая деторсия и декомпрессия кишки с помощью колоноскопа (УД 5, CP D).
Разрешения кишечной непроходимости, обусловленной каловым завалом, в большинстве случаев удается добиться с помощью многократных клизм и пальцевого опорожнения прямой кишки под местным или регионарным обезболиванием (УД 5, СР D).
ХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕ
Плановое хирургическое лечение пациентов с идиопатическим мегаколоном должно осуществляться в специализированных колопроктологических центрах, где есть возможность проведения всего спектра необходимых диагностических исследований (УД 5, СР D).
Мегаколон
У пациентов с мегаколоном и нормальным диаметром и функцией прямой кишки операцией выбора является колэктомия с илеоректальным, цекоректальным, асцендоректальным или илеосигмоидным анастомозом (УД 3а, СР С [19, 22]). Наиболее надежным в смысле риска рецидива запора является формирование илеоректального анастомоза. Расширение остающихся слепой кишки при асцендо/цекоректальном или сигмовидной при илеосигмоидном анастомозах может приводить к рецидиву вздутия живота, нарушению опорожнения при дефекации, запоре и к необходимости дополнительных более агрессивных резекций [15, 16, 42]. С другой стороны, оставление слепой кишки делает менее вероятным развитие поноса и инконтиненции (УД 5, СР D [29]).
Альтернативным подходом являются резекция расширенной кишки и оставление анатомически и функционально сохранных проксимальных отделов. По сравнению с колэктомией, частота рецидива запора и повторных операций после сегментарных резекций (резекция сигмовидной кишки, левосторонняя гемиколэктомия) выше [19]. Хотя при тщательном отборе пациентов и оценке функции нерасширенных отделов ободочной кишки на основании исследования транзита возможно получение хороших функциональных результатов и при ограниченных резекциях (УД 4, СР D [26, 31]).
Расширение дистальных отделов толстой кишки
При расширении только дистальных отделов толстой кишки (изолированный мегаректум или в сочетании с мегасигмой) показаны проктэктомия с колоанальным анастомозом или вертикальная редукционная ректопластика. Вертикальная редукционная ректопластика — это предложенная относительно недавно хирургическая процедура, направленная на уменьшение объема прямой кишки с целью уменьшения количества кишечного содержимого, вызывающего возникновение позывов к дефекации [45]. Она предполагает удаление расширенной сигмовидной кишки с пересечением ее на уровне дистальной трети, затем мобилизацию прямой кишки до тазового дна. После этого прямая кишка прошивается и рассекается в вертикальном направлении и фронтальной плоскости 100 мм сшивающе-режущим аппаратом. Таким образом, кишка делится на переднюю и заднюю половины. Передняя половина затем отсекается с помощью 60 мм линейного аппарата. Аппаратные швы укрывают непрерывным ручным швом. Далее формируется анастомоз между суженной прямой кишкой и проксимальной частью нисходящей кишки циркулярным сшивающим аппаратом. Операция заканчивается формированием превентивной илеостомы. При сопоставимом с проктэктомией уровне успеха (70–80%) вертикальная редукционная ректопластика кажется менее травматичной и более благоприятной с функциональной точки зрения операцией [20, 45]. Однако в настоящее время опубликован
опыт применения вертикальной редукционной ректопластики только в одной клинике, и необходимы дальнейшие исследования ее эффективности и безопасности (УД 5, СР D).
Тотальный мегаколон в сочетании с мегаректумом
У пациентов с тотальным мегаколоном и мегаректумом наиболее подходящей операцией кажется проктоколэктомия с тонкокишечным резервуаром и илеоанальным анастомозом (УД 5, СР D [19]). Частота удовлетворительных результатов при этом более 70%, однако пациент должен быть предупрежден о риске нарушения функции резервуара, что может проявляться частыми дефекациями и ночным недержанием. По данным Hosie et al., средняя частота дефекации у 5 оперированных пациентов составила 5 раз в день, и 3 пациента (60%) отмечали ночное недержание [25]. Stewart et al. выполнили проктоколэктомию с J-образным резервуаром у 14 пациентов без осложнений. 12 (86%) из них имели частоту стула менее 7 раз в день и не страдали недержанием, 1 пациент отмечал «небольшое подтекание» и еще у 1 потребовалась грацилопластика по поводу явной инконтиненции. Однако в последующем 4 пациентам (28,6%) были выполнены удаление резервуара, илеостомия в связи с персистирующими абдоминальными болями и вздутием [43].
Не рекомендуется использование операции Дюамеля или низведения
у пациентов с мегаколоном из-за неудовлетворительных функциональных исходов, неприемлемо высокого уровня летальности и большого числа осложнений, требующих дополнительных операций (УД 4, СР D [19]).
Промежностные операции — сфинктеротомия, рассечение пуборектальной мышцы у пациентов с мегаколоном/мегаректумом, неэффективны и сопровождаются риском развития инконтиненции (УД 3а, СР B [19]).
Формирование стомы
У части пациентов с тяжелым соматическим состоянием или желающих избежать риска осложнений, связанных с большими операциями, альтернативой является формирование стомы. Она также может оказаться актуальной в случае, когда другие операции не увенчались успехом. В любом случае стома должна быть сформирована проксимальнее расширенных отделов, а пациент должен быть предупрежден, что она может не избавить его от болей в животе и вздутия (УД 5, СР D).
Хирургическое лечение осложненного мегаколона
При неэффективности попыток ликвидации заворота кишки консервативными методами пациенту показано срочное хирургическое вмешательство. Если кишка, формирующая заворот, жизнеспособна, выполняется деторсия. В последующем больной обследуется и в плановом порядке оперируется в соответствии с изложенными выше принципами (см. разделы «Мегаколон», «Расширение дистальных отделов толстой
кишки», «Тотальный мегаколон в сочетании с мегаректумом»). В случае нарушения кровоснабжения кишки, наличия перфорации и/или перитонита выполняется резекция пораженного участка без первичного анастомоза. В дальнейшем, после обследования и уточнения функционального состояния оставшихся отделов, возможна восстановительная операция.
Послеоперационное ведение
Послеоперационное ведение пациентов с идиопатическим мегаколоном не имеет специфических особенностей и не требует проведения специальных диагностических или лечебных процедур.
Прогноз
В целом прогноз благоприятный. С одной стороны, даже эффективное консервативное лечение, проводимое в течение нескольких лет, не приводит к нормализации диаметра кишки. С другой — нет оснований ожидать обязательного прогрессирования идиопатического мегаколона или ухудшения симптоматики. Поэтому, если лечение эффективно, его следует продолжать, пока сохраняется эффект или не исчерпаны все терапевтические возможности. Что касается хирургического лечения, то благоприятного исхода можно ожидать в зависимости от ситуации и объема операции в 50–90% случаев. Однако необходимо иметь в виду, что операция направлена прежде всего на профилактику жизненно опасных осложнений и купирование нарушений опорожнения кишечника. В отношении симптомов абдоминального дискомфорта прогноз значительно менее определен. Кроме того, сама операция связана с риском потенциально опасных для здоровья осложнений как в ближайшем периоде, так и в отдаленном. Пациент должен быть предупрежден, что частота спаечной непроходимости при длительном наблюдении достигает 40–50%, а череда послеоперационных осложнений или безуспешность предпринятых вмешательств могут привести к необходимости формирования постоянной стомы.
Критерии оценки качества помощи в стационаре представлены в та-
блице 16.3. Для оценки качества медицинской помощи используют временные, процессуальные и профилактирующие критерии. Временные характеризуют своевременность оказания определенных этапов медицинской помощи. Выполнение пациенту ряда медицинских манипуляций, инструментальных и лабораторных исследований, необходимых для качественного оказания медицинской помощи, оценивают в процессуальных критериях. Для анализа мероприятий, направленных на предотвращение развития осложнений, используют профилактирующие критерии.
Таблица 16.3. Критерии оценки качества медицинской помощи в стационаре больным с мегаколоном (0 — нет, 1 — да)
|
Клинические рекомендации |
Временные |
Процессуальные |
Профилактирующие |
|
1. Клинические рекомендации по диагностике и лечению взрослых больных с идиопатическим мегаколоном (код МКБ — К59.3). 2. Клинические рекомендации по диагностике и лечению болезни Гиршпрунга у взрослых (код МКБ — Q43.1). 3. Клинические рекомендации по диагностике и лечению взрослых пациентов с долихоколоном (код МКБ — Q43.8). |
Установка клинического диагноза в течение 72 ч: 0/1 |
Пальцевое обследование прямой кишки: 0/1. Ректороманоскопия: 0/1. Ирригоскопия: 0/1. Исследование крови на сифилис, вирусный гепатит В, вирусный гепатит С: 0/1. Клинический анализ крови; биохимический анализ крови; клинический анализ мочи; коагулограмма: 0/1. При подозрении на болезнь Гиршпрунга определение активности ацетилхолинэстеразы в биоптате слизистой оболочки прямой кишки: 0/1. При подозрении на болезнь Гиршпрунга определение ректоанального ингибиторного рефлекса: 0/1. При дифференциальной диагностике болезни Гиршпрунга и идиопатического мегаколон проведение биопсии по Свенсону: 0/1. Метод оперативного лечения в соответствии с установлен- ным диагнозом и клиническими рекомендациями: 0/1. Метод анестезии в соответствии с объемом оперативного лечения: 0/1 |
Отсутствие осложнений: • кровотечение: 0/1; • пневмония: 0/1; • тромбоэмболия: 0/1; • послеоперационная спаечная кишечная непроходимость: 0/1; • перитонит: 0/1; • летальный исход: 0/1 |
Литература
1. Алешин Д.В., Ачкасов С.И., Жученко А.П. и др. Клинико-функциональные критерии идиопатического мегаректум // Колопроктология. — 2012. — Т. 39, № 1. — С. 11–18.
2. Ачкасов С.И. Аномалии развития и положения толстой кишки. Клиника, диагностика, лечение: Дис. … д-ра мед. наук. — М., 2003. — 294 с.
3. Воробьев Г.И., Жученко А.П., Ачкасов С.И. и др. Возможности модификации биопсии стенки прямой кишки по Свенсону в диагностике пороков развития интрамуральной нервной системы у взрослых // Хирургия. — 2005. — № 10. — С. 4–7.
4. Воробьев Г.И. Мегаколон у взрослых (клиника, диагностика и хирургическое лечение): Дис. … д-ра мед. наук. — М., 1982. — 402 с.
5. Капуллер Л.Л., Жученко А.П., Ачкасов С.И., Бирюков О.М. Протяженность зоны физиологического гипоганглиоза у взрослых и ее значение в диагностике болезни Гиршпрунга // Арх. пат. — 2008. — Т. 70. — С. 46–49.
6. Самсонюк В.Г., Захарченко А.А., Штоппель А.Э. Комплексное консер-
вативное лечение нарушений моторно-эвакуаторной функции толстой кишки // Проблемы колопроктологии: Сборник. — М.: МНПИ, 2000. — Вып. 17. — С. 530–535.
7. Румянцев В.Г., Косачева Т.А., Коровкина Е.А. Дифференцированное лечение запоров // Фарматека. — 2004. — Т. 90, № 13. — С. 1–6.
8. Туликова А.П., Подмаренкова Л.Ф., Елисеева М.В., Румянцев В.Г. Функциональное обоснование применения физических факторов воздействия в лечении нарушений моторно-эвакуаторной функции толстой кишки // Рос. журн. гастроэнтерол., гепатол. и колопроктол. — 1995. — Т. 5, № 3. — С. 71–76.
9. Фролькис А.В. Функциональные заболевания желудочно-кишечного
тракта. — Л.: Медицина, 1991. — 224 с.
10. Хаммад Е.В. Хронический запор (тактика совершенствования диагностики и лечения): Дис. … канд. мед. наук. — М., 1997. — 134 с.
11. Шульпекова Ю.О., Ивашкин В.Т. Патогенез и лечение запоров // Болезни органов пищеварения. — 2004. — Т. 6, № 1 — С. 49–52.
12. Яковенко Э.П., Агафонова Н.А. Механизмы развития запоров и методы их лечения // Клин. перспективы гастроэнтерол., гепатол. — 2003. — № 3. — С. 25–32.
13. Яремчук А.Я. Хирургическое лечение хронических колостазов: Дис. …
д-ра мед. наук. — Киев, 1990. — 199 с.
14. Allescher H.D. Laxatives and prokinetics — good or bad? // Constipation and Anorectal Insufficiency: Falk Symposium 95. — Kluwer Academic Publishers, 1997. — P. 121–129.
15. Belliveau P., Goldberg S.M., Rothenberger D.A. et al. Idiopathic acquired megacolon: the value of subtotal colectomy // Dis. Colon Rectum. — 1982. — Vol. 25. — P. 118–121.
16. Coremans G.E. Surgical aspects of severe chronic non-Hirschsprung
constipation // Hepatogastroenterology. — 1990. — Vol. 37. — P. 588–595.
17. Dufour P., Gendre P. Ultrastructure of mouse intestinal mucosa and changes observed after long term anthraquinone administration // Gut. — 1984. — Vol. 25. — P. 1358–1363.
18. Gattuso J.M., Kamm M.A., Talbot I.C. Pathology of idiopathic megarectum and megacolon // Gut. — 1997. — Vol. 41. — P. 252–257.
19. Gladman M.A., Scott S.M., Lunniss P.J., Williams N.S. Systematic review of surgical options for idiopathic megarectum and megacolon // Ann. Surg. —2005. — Vol. 241. — P. 562–574.
20. Gladman M.A., Williams N.S., Ogunbiyi O.A. et al. Medium-term results of
vertical reduction rectoplasty and sigmoid colectomy for idiopathic megarectum // Br. J. Surg. —2005. — Vol. 92. — P. 624–630.
21. Gladman M.A., Dvorkin L.S., Scott S.M. et al. A novel technique to identify patients with megarectum // Dis. Colon Rectum. —2007. — Vol. 50. — P. 621–629.
22. Gladman M.A., Knowles C.H. Novel concepts in the diagnosis, pathophysiology and management of idiopathic megabowel // Colorectal Dis. — 2008. — Vol. 10, N 6. — P. 531–538.
23. Gladman M.A., Lunniss P.J., Williams N.S., Scott S.M. Rectal hyposensitivity: pathophysiological mechanisms // Neurogastroenterol. Motil. — 2005. — Vol. 17. — Suppl. 2. — P. 18.
24. Goligher J.C. Discussion on megacolon and megarectum // Proc. R. Soc.
Med. — 1961. — Vol. 54. — P. 1053–1056.
25. Hosie K.B., Kmiot W.A., Keighley M.R. Constipation: another indication for restorative proctocolectomy // Br. J. Surg. — 1990. — Vol. 77. — P. 801–802.
26. Hughes E.S., McDermott F.T., Johnson W.R. et al. Surgery for constipation // Aust. N.Z. J. Surg. — 1981. — Vol. 51. — P. 144–148.
27. Keuzenkamp-Jansen C.W., Fijnvandraat C.J., Kneepkens C.M., Douwes A.C. Diagnostic dilemmas and results of treatment for chronic constipation // Arch. Dis. Child. — 1996. — Vol. 75, N 1. — P. 36–41.
28. Knowles C.H., Scott S.M., Rayner C. et al. Idiopathic slow-transit constipation:
an almost exclusively female disorder // Dis. Colon Rectum. — 2003. — Vol. 46. — P. 1716–1717.
29. Lane R.H., Todd I.P. Idiopathic megacolon: a review of 42 cases // Br. J. Surg. — 1977. — Vol. 64. — P. 307–310.
30. Loening-Baucke V., Yamada T. Is the afferent pathway from the rectum impaired in children with chronic constipation and encopresis? // Gastroenterology. — 1995. — Vol. 109. — P. 397–403.
31. McCready R.A., Beart R.W.Jr. The surgical treatment of incapacitating
constipation associated with idiopathic megacolon // Mayo Clin. Proc. — 1979. — Vol. 54. — P. 779–783.
32. Meunier P., Louis D., Jaubert de Beaujeu M. Physiologic investigation of primary chronic constipation in children: comparison with the barium enema study // Gastroenterology. — 1984. — Vol. 87. — P. 1351–1357.
33. Mimura T., Nicholls T., Storrie J.B., Kamm M.A. Treatment of constipation
in adults associated with idiopathic megarectum by behavioural retraining including biofeedback // Colorectal Dis. — 2002. — Vol. 4. — P. 477–482.
34. Molnar D., Taitz L.S., Urwin O.M., Wales J.K. Anorectal manometry results in defecation disorders // Arch. Dis. Child. — 1983. — Vol. 58. — P. 257–261.
35. Muller-Lissner S.A., Kamm M.A., Scarpignato C., Wald A. Myths and misconceptions about chronic constipation // Am. J. Gastroenterol. — 2004. — Vol. 99. — P. 1–11.
36. Preston D.M., Lennard-Jones J.E., Thomas B.M. Towards a radiologic
definition of idiopathic megacolon // Gastrointest. Radiol. — 1985. — Vol. 10. — P. 167–169.
37. Riemann J.F., Schmidt H., Zimmermann W. The fine structure of colonic submucosal nerves in patients with chronic laxative abuse // Scand. J. Gastroenterol. — 1980. — Vol. 15. — P. 761–768.
38. Riemann J.F., Schmidt H. Ultrastructural changes in the gut autonomic
nervous system following laxative abuse and in other conditions // Scand. J. Gastroenterol. — 1982. — Suppl. 71. — P. 11–24.
39. Siproudhis L., Le Gall R., Ropert A. et al. Does manometric megarectum have a symptomatic role in patients complaining of dyschezia? // Gastroenterol. Clin. Biol. — 1993. — Vol. 17. — P. 162–167.
40. Smith B. Effect of irritant purgatives on the myenteric plexus in man and the mouse // Gut. — 1968. — Vol. 9. — P. 139–145.
41. Smith B. Pathologic changes in the colon produced by anthraquinone laxatives // Dis. Colon Rectum. — 1973. — Vol. 16. — P. 455–458.
42. Stabile G., Kamm M.A., Hawley P.R. et al. Colectomy for idiopathic megarectum and megacolon // Gut. — 1991. — Vol. 32. — P. 1538–1540.
43. Stewart J., Kumar D., Keighley M.R. Results of anal or low rectal anastomosis and pouch construction for megarectum and megacolon // Br. J. Surg. — 1994. — Vol. 81. — P. 1051–1053.
44. Waldron D., Bowes K.L., Kingma Y.J., Cote K.R. Colonic and anorectal motility in young women with severe idiopathic constipation // Gastroenterology. — 1988. — Vol. 95. — P. 1388–1394.
45. Williams N.S., Fajobi O.A., Lunniss P.J. et al. Vertical reduction rectoplasty: a new treatment for idiopathic megarectum // Br. J. Surg. — 2000. — Vol. 87. — P. 1203–1208.
46. Van der Plas R.N., Benninga M.A., Staalman C.R. et al. Megarectum in constipation // Arch. Dis. Child. — 2000. — Vol. 83. — P. 52–58.
47. Van Gorkom B.A., de Vries E.G., Karrenbeld A. et al. Review article: Anthranoid laxatives and their potential carcinogenic effects // Aliment. Pharmacol. Ther. — 1999. — Vol. 13. — P. 443–452.
48. Varma J.S., Smith A.N. Neurophysiological dysfunction in young women with intractable constipation // Gut. — 1988. — Vol. 29. — P. 963–968.
49. Verduron A., Devroede G., Bouchoucha M. et al. Megarectum // Dig. Dis. Sci. — 1988. — Vol. 33. — P. 1164–1174.
АНГИОДИСПЛАЗИЯ КИШЕЧНИКА
Введение
Исследования конца 1980-х гг. показали, что причиной кровотечений из нижних отделов ЖКТ в 15–27% случаев служит ангиодисплазия [9, 17, 21, 29].
Более поздние и крупные исследования показали меньший удельный вес ангиодисплазий среди кровотечений из нижних отделов ЖКТ. Так, в крупном исследовании, в котором участвовало 1112 пациентов с кровотечениями, частота ангиодисплазий составила 4,76% в период с 1988 по 1997 г. и 2,3% в 1998–2006 гг. [13]. Подобные результаты (3%) были получены еще в одном крупном исследовании [35].
Настоящие рекомендации по диагностике и лечению больных ангиодисплазией кишечника являются руководством для практических врачей, осуществляющих ведение и лечение таких пациентов. Рекомендации подлежат регулярному пересмотру в соответствии с новыми данными научных исследований в этой области.
Настоящие рекомендации включают следующие разделы: определение и классификация ангиодисплазии кишечника, диагностика, консервативное и хирургическое лечение. Для отдельных положений рекомендаций приведены уровни доказательности согласно общепринятой классификации Оксфордского центра доказательной медицины (табл. 17.1).
Таблица 17.1. Уровни доказательности и степени рекомендаций на основании руководства Оксфордского центра доказательной медицины
|
Уровень |
Исследование методов диагностики |
Исследование методов лечения |
|
1а |
Систематический обзор гомогенных диагностических исследований 1-го уровня |
Систематический обзор гомогенных РКИ |
|
1b |
Валидизирующее когортное исследование с качественным «золотым стандартом» |
Отдельное РКИ (с узким доверительным интервалом) |
|
1с |
Специфичность или чувствительность столь высокие, что положительный или отрицательный результат позволяет исключить/установить диагноз |
Исследование «Всё или ничего» |
Табл. 17.1. Окончание
|
Уровень |
Исследование методов диагностики |
Исследование методов лечения |
|
2а |
Систематический обзор гомогенных диагностических исследований >2-го уровня |
Систематический обзор (гомогенных) когортных исследований |
|
2b |
Разведочное когортное исследование с качественным «золотым стандартом» |
Отдельное когортное исследование (включая РКИ низкого качества; т.е. с <80% пациентов, прошедших контрольное наблюдение) |
|
2с |
Нет |
Исследование «исходов»; экологические исследования |
|
3а |
Систематический обзор гомогенных исследований уровня 3b и выше |
Систематический обзор гомогенных исследований «случай–контроль» |
|
3b |
Исследование с непоследовательным набором или без проведения исследования «золотого стандарта» у всех испытуемых |
Отдельное исследование «случай– контроль» |
|
4 |
Исследование «случай–контроль» или исследование с некачественным или зависимым «золотым стандартом» |
Серия случаев (и когортные исследования или исследования «случай– контроль» низкого качества) |
|
5 |
Мнение экспертов без тщательной критической оценки или основанное на физиологии, лабораторные исследования на животных или разработка «первых принципов» |
Мнение экспертов без тщательной критической оценки, лабораторные исследования на животных или разработка «первых принципов» |
|
Степени рекомендаций | ||
|
A |
Согласующиеся между собой исследования 1-го уровня | |
|
B |
Согласующиеся между собой исследования 2-го или 3-го уровня или экстраполяция на основе исследований 1-го уровня | |
|
C |
Исследования 4-го уровня или экстраполяция на основе уровня 2 или 3 | |
|
D |
Доказательства 4-го уровня или затруднительные для обобщения или некачественные исследования любого уровня | |
ВАЛИДИЗАЦИЯ РЕКОМЕНДАЦИЙ
Настоящие рекомендации в предварительной версии были рецензированы независимыми экспертами, которых попросили прокомментировать прежде всего, насколько интерпретация доказательств, лежащих в основе рекомендаций, доступна для понимания. Получены комментарии со стороны врачей амбулаторного звена. Полученные комментарии тщательно систематизировались и обсуждались на совещаниях экспертной группы.
Последние изменения в настоящих рекомендациях были представлены для дискуссии на заседании профильной комиссии «Колопроктология» Экспертного совета Минздрава России 12 сентября 2013 г. Проект рекомендаций был повторно рецензирован независимыми экспертами и врачами амбулаторного звена. Для окончательной редакции и контроля качества рекомендации были повторно проанализированы членами экспертной группы, которые пришли к заключению, что все замечания и комментарии приняты во внимание, риск систематических ошибок при разработке рекомендаций сведен к минимуму.
ОБЛАСТЬ ПРИМЕНЕНИЯ РЕКОМЕНДАЦИЙ
Данные клинические рекомендации применимы при осуществлении медицинской деятельности в рамках Порядка оказания медицинской помощи взрослому населению с заболеваниями толстой кишки, анального канала и промежности колопроктологического профиля.
Определение
Наименее изученным среди многочисленных факторов, приводящих к кишечным кровотечениям различной степени интенсивности, является ангиодисплазия. Этот термин обозначает патологическое состояние, при котором имеются порочное (патологическое) развитие и строение сосудов кишечной стенки.
Код по Международной классификации болезней 10-го пересмотра
n Класс: XI Болезни органов пищеварения.
n Блок: K55 Сосудистые болезни кишечника.
n Код:
v K55.2 Ангиодисплазия ободочной кишки.
v K55.8 Другие сосудистые болезни кишечника.
Классификация
Трудность исчерпывающей классификации ангиодисплазий кишечника объясняется многообразием форм заболевания, локализацией и обширностью поражения, наличием сочетанных форм с поражением других органов и систем организма.
С момента появления интереса ученых, опубликования первых статей в конце XIX в. и появления термина «ангиодисплазия кишечника» было предложено большое количество классификаций этого состояния. Однако ни одна из них не является универсальной. Стоит отметить, что в силу относительной редкости этой патологии опыт отдельных клиник чаще
всего представлен единичными (редко более 15–20) наблюдениями. Это может также объясняться тем фактом, что большинство больных получают лечение не в специализированных стационарах, где кумулируется данный опыт, а в стационарах общего профиля, куда поступают больные с клинической картиной кишечного кровотечения. В ГНЦК была предложена собственная классификация с учетом происхождения, морфологического строения ангиодисплазий, распространенности и локализации поражения, а также клинического течения (УД 4, СР D [1–3]).
По происхождению:
n I тип — врожденная ангиодисплазия:
v ненаследственная форма;
v наследственная форма (болезнь Рендю–Ослера);
n II тип — приобретенная ангиодисплазия.
По морфологическому строению:
n венозная ангиодисплазия:
v капиллярный тип;
v кавернозный тип;
n артериовенозная ангиодисплазия;
n артериальная ангиодисплазия.
По распространенности:
n ограниченная ангиодисплазия (поражение одного отдела толстой кишки протяженностью не более 5 см);
n диффузная ангиодисплазия (поражение одного или нескольких отделов толстой кишки протяженностью более 5–10 см);
n генерализованная ангиодисплазия (системный ангиоматоз с сочетанным поражением других органов и систем, синдром Клиппеля–Треноне).
По локализации:
n толстая кишка;
n тонкая кишка;
n смешанная форма с поражением толстой и тонкой кишки.
По клиническому течению:
n неосложненное (в том числе бессимптомное);
n осложненное.
Основополагающим моментом является необходимость систематизировать обнаруженные изменения по происхождению. Важен также признак распространенности. Если патологический процесс локализуется в одном отделе толстой кишки, площадь поражения не более 5 см, — это ограниченный процесс. Если изменения захватывают несколько анатомических областей, процесс считается диффузным. Изменения, обнаруженные в нескольких органах или областях, называют генерализованными. Такие изменения характерны для синдрома Клиппеля–Треноне. Данная классификация охватывает все основные, наиболее часто встречающиеся типы ангиодисплазий, учитывает их происхождение, гистологическую структуру, обширность патологического процесса, варианты клинической картины заболевания, что позволяет максимально
полно сформулировать клинический диагноз, разработать тактику лечения, определить объем операции.
Врожденная ангиодисплазия кишечника
ОПРЕДЕЛЕНИЕ
Врожденная форма ангиодисплазии кишечника — это сосудистое образование, локализующееся в ЖКТ (чаще всего в прямой кишке). В зарубежной литературе используется термин «сосудистая мальформация». Впервые подобные изменения были описаны в 1839 г. B. Phillips, который сообщил о трех случаях массивного кровотечения из опухоли, величиной с грецкий орех, располагающейся в прямой кишке. В последующем авторы опубликовали в основном информацию об отдельных случаях ангиодисплазии кишечника. Стоит подчеркнуть, что опыт отдельных клиник колеблется от 1 до 48 наблюдений за продолжительные сроки наблюдения, что свидетельствует о небольшом распространении данного вида дисплазии, который является редким заболеванием.
КЛИНИЧЕСКАЯ КАРТИНА
Клиническая картина врожденной ангиодисплазии характеризуется появлением первых симптомов в раннем детстве или с рождения. В клинической картине превалируют часто повторяющиеся кишечные кровотечения. Иногда выделение крови происходит с каждой дефекацией. Характерным признаком подобных кровотечений являются их безболезненность, связь только с дефекацией, тенденция к более массивным кровопотерям с каждым последующим кровотечением.
Возраст, в котором манифестирует заболевание, тип кровотечений, частота и тяжесть зависят от распространенности поражения толстой кишки. Несмотря на доступность диагностики, яркую картину заболевания, зачастую диагноз устанавливается неправильно, что нередко может привести к неадекватному лечению, необоснованным операциям.
ДИАГНОСТИКА
Основные методы диагностики врожденной ангиодисплазии толстой кишки — эндоскопические и рентгенологические. Однако практически у половины (54,2%) пациентов с сочетанными внекишечными проявлениями системного ангиоматоза и жалобами на кишечные кровотечения уже при наружном осмотре с большой степенью уверенности можно было диагностировать ангиодисплазию толстой кишки (УД 4, СР D [3]). Наличие пигментных (сосудистых) пятен, варикозного расширения поверхностных вен и гипертрофия пораженной конечности известны в литературе под названием «синдром Клиппеля–Треноне». Такой вариант заболевания встречается тоже достаточно часто (до 1/3 наблюдений, по данным отдельных авторов).
Эндоскопические методы диагностики
Колоноскопия. Высокая разрешающая диагностическая способность колоноскопии позволяет установить распространенность патологического процесса. Эндоскопическая картина врожденной ангиодисплазии толстой кишки достаточно характерна. Сосудистые образования выступают над слизистой оболочкой в виде неровных бугристых возвышений и выпячиваний разной формы и величины, наполненных кровью. Они мягкой консистенции, легко сдавливаются и быстро вновь наполняются кровью. Цвет их багровый, с более густым синюшным оттенком, чем у кожных форм, благодаря большей прозрачности слизистой оболочки. Эти образования могут иметь гроздевидный (узловатый) вид от глубокого синего до ярко-красного цвета. Такая выраженная эндоскопическая картина обнаруживается у 58,3%. В остальных наблюдениях она не так ярко манифестирует, сосудистые образования меньших размеров, цвет их более синюшный, но все характерные симптомы непременно присутствуют и у них. При анализе результатов эндоскопических исследований установлены типичные для врожденной ангиодисплазии толстой кишки симптомы: относительное сужение просвета кишки за счет сосудистых образований, расправление и спадание их при инсуфляции воздухом, отсутствие изъязвления слизистой оболочки и четкая граница между пораженными отделами и нормальной толстой кишкой. При колоноскопии устанавливается протяженность поражения патологическим процессом.
Рентгенологические методы диагностики
Обзорная рентгенография органов брюшной полости. При обзорной рентгенографии брюшной полости может быть установлен характерный для этого заболевания признак — наличие атипично расположенных разнокалиберных флеболитов, локализующихся чаще всего по ходу пораженной прямой кишки и в параректальной клетчатке, что может свидетельствовать о сочетанном поражении в полости таза. Встречаемость этого признака до 40% (УД 4, СР D [3]).
Ирригоскопия. Метод, определяющий не только наличие ангиодисплазии, но и устанавливающий распространенность ее по различным отделам толстой кишки, функциональное состояние последней, подвижность, ширину просвета и состояние окружающих тканей. Рентгеносемиотика врожденной ангиодисплазии толстой кишки не менее характерна, чем эндоскопическая картина. Достоверными признаками наличия ангиодисплазии являются множественные центральные и краевые дефекты наполнения и деформация контуров пораженной кишки. Сам контур зазубрен, иногда меняется по мере наполнения кишки бариевой взвесью. При тугом наполнении контуры кишки несколько выпрямляются и представлены в виде симптома «пальцевых вдавлений». После опорожнения в этих местах формируется крупноячеистый рельеф, напоминающий симптом «булыжной мостовой». Относительно сужен-
ная пораженная прямая кишка расправляется при тугом наполнении. При двойном контрастировании определяется множество внутрипросветных образований различной формы и величины, в виде полуколец, что указывает на сосудистое их происхождение.
Мезентериальная ангиография. Чувствительность метода достигает 86%, специфичность приближается к 100% (УД 4, СР D [12, 36, 38]). Данный метод позволяет диагностировать скрытое кровотечение при объеме 0,5 мл/мин и более (УД 4, СР D [4, 23]). При анализе полученных ангиограмм выявлены характерные симптомы: наличие
«контрастных» пятен в проекции поражения, длительная задержка контраста в артериальном русле (до 15 с), замедление венозной фазы, ранний венозный сброс, наличие артериовенозных шунтов и расширение магистральных артерий и вен. Наиболее часто эти симптомы выявляются у больных с синдромом Клиппеля–Треноне. При положительном результате ангиографии достаточно эффективной считается суперселективная эмболизация в качестве кровеостанавливающего мероприятия. Проведенные исследования демонстрируют хорошую эффективность метода в 60–90% наблюдений. Рецидив кровотечения возникает в 0–33% случаев. Клинически значимая ишемия возникает менее чем в 7% случаев. Однако приведенные цифры имеют отношение ко всем случаям кровотечения из тонкой и толстой кишки, не только ангиодиспластической природы (УД 4, СР D [20, 37]).
Радионуклидная сцинтиграфия. Наиболее чувствительным методом диагностики кровотечения из нижних отделов ЖКТ является радионуклидная сцинтиграфия. В отличие от эндоскопических методов, ангиографии, данная методика не подразумевает терапевтического воздействия на источник кровотечения. Она не требует подготовки кишечника и позволяет выявить источник кровотечения с кровопотерей менее 0,1 мл/мин.
УСТАНОВЛЕНИЕ ДИАГНОЗА
Локализация патологического процесса в преобладающем числе наблюдений в прямой кишке, раннее начало ректальных безболезненных, упорных кровотечений, перенесенные многократные операции на дистальном отделе прямой кишки и возможное наличие внекишечных проявлений заболевания делает диагностику врожденной ангиодисплазии толстой кишки несложной. Ректальное исследование прямой кишки с правильной оценкой полученных данных оказывается эффективным у 90% больных. Яркая специфическая эндои рентгенологическая картина подтверждает диагноз и устанавливает распространенность поражения. Дифференциальную диагностику необходимо проводить с другими заболеваниями и состояниями, сопровождающимися кишечными кровотечениями (опухолевые заболевания толстой кишки и анального канала, осложненный дивертикулез, кровоточащий геморрой и др.).
ЛЕЧЕНИЕ
Единственным методом радикального излечения больных с врожденной ангиодисплазией большинство авторов признает оперативное вмешательство, направленное на резекцию пораженного сегмента. В некоторых ситуациях, когда имеется слабо выраженная аноректальная мальформация, возможно применение склеротерапии в качестве лечебной меры с неплохими результатами.
Однако в литературе имеются сведения о неэффективности предпринимаемых попыток местного воздействия на кровоточащий сосуд. Склеротерапия, лигирование и пересечение часто приводили к рецидиву кишечного кровотечения, что, скорее всего, было связано как с техникой, так и с характером склерозирующего препарата (УД 4, СР D [15]).
В настоящее время показанием к хирургическому лечению считается наличие у больного врожденной ангиодисплазии с большой площадью распространения, с вовлечением нескольких отделов толстой кишки, ежедневными стойкими прямокишечными кровотечениями со среднесуточной кровопотерей 30–50 мл и более, приводящими к выраженной и стойкой анемии, значительным нарушениям гомеостаза и ухудшению общего состояния (УД 4, СР D [1–3]). В преобладающем большинстве случаев операций выбора является брюшно-анальная резекция прямой кишки.
Оперативные вмешательства, предпринимаемые у больных с врожденной ангиодисплазией толстой кишки, сопряжены со значительными трудностями, обусловленными, прежде всего, распространенностью патологического процесса на соседние органы и ткани в полости таза, сосудистым характером поражения и техническими трудностями при проведении гемостаза. Так зачастую пораженная кишечная стенка сплошь покрыта извитыми и расширенными сосудами, сливающимися в большие кавернозные конгломераты, и нередко представлена в виде единой «сосудистой опухоли». В таких вариантах поражаются брыжейка и окружающая клетчатка, значительно увеличивая в размерах пораженный орган. Мобилизация и удаление такой прямой кишки, диаметром достигающей порой 20 см и более, занимающей практически всю полость таза, представляет значительные технические трудности. Кавернозные сосудистые образования настолько тонкостенны, что малейшая их травматизация вызывает плохо контролируемое кровотечение (УД 4, СР D [1–3]).
Другая важная особенность, которую надо учитывать, выполняя операцию по поводу данного заболевания, — это сочетанное «поражение» передней стенки прямой кишки и задней стенки влагалища. В таких ситуациях необходимо знать, что патологически измененные сосуды не обладают инвазивным ростом, а существует взаимное внедрение сосудистых конгломератов пораженных органов по извилистой траектории. Ранение соседних органов на этом этапе операции (предстательная железа у мужчин и влагалище у женщин) могут привести к трудноостанавливаемому кровотечению из них.
Принципы мобилизации и резекции прямой кишки при различных заболеваниях достаточно широко известны, но у больных с врожденной ангиодисплазией они приобретают главенствующее значение ввиду технических особенностей, определяющихся во время операции и присущих только для этой категории больных.
Основные правила при выполнении хирургических пособий у больных врожденной ангиодисплазией толстой кишки: соблюдение принципа футлярности при мобилизации прямой кишки, выполняемой визуально и острым путем, бережное отношение к тканям, в том числе удаляемым, и наименьшая их травматизация, щадящая техника и тщательный гемостаз на всех этапах операции.
Таким образом, наиболее грозным и частым интраоперационным осложнением при удалении прямой кишки является трудноостанавливаемое кровотечение, которое может носить массивный характер и представлять непосредственную угрозу для жизни больного.
Указанные выше особенности и дооперационные нарушения определяют уровень интраоперационной кровопотери. Так, в одном из исследований было установлено, что у каждого 4 больного отмечалась достаточно выраженная степень интраоперационной кровопотери (более 30 мл/кг) [3]. При имеющихся признаках фибринолитического кровотечения в конце операции и уровня кровопотери более 30 мл на 1 кг массы тела операцию необходимо заканчивать формированием одноствольной колостомы без попытки низведения проксимальных отделов ободочной кишки и тампонадой малого таза. Этим больным возможно выполнение отсроченного
низведения ободочной кишки в анальный канал в сроки от 6 до 12 мес.
Некоторые авторы считают, что больные с врожденной ангиодисплазией имеют более высокий риск развития тромбоэмболических осложнений. Объясняется это наличием у этих больных целого ряда факторов риска: большого количества варикозно измененных вен при синдроме Клиппеля–Треноне (нередко с явлениями хронического флебита), патологических сосудистых образований в полости таза с замедленным кровотоком в них, продолжительных операций на органах малого таза и высокой частотой развития пресакральных абсцессов. Необходимо также учитывать роль исходных коагулопатических нарушений у этих больных. Из поздних осложнений стоит обратить внимание на возможность формирования стриктуры колоанального анастомоза, частота развития которой, по данным литературы, доходит до 18,6%. Одной из возможных предпосылок к тому может быть низведение ободочной кишки в анальный канал с избытком. Поэтому следует отдавать предпочтение операциям с первичным формированием колоанального анастомоза с формированием превентивной колоили илеостомы. В случае формирования стриктуры и неэффективности многократного бужирования анастомоза показано выполнение иссечения рубцовых тканей с восстановлением
нормальной проходимости в зоне соустья.
Приобретенная ангиодисплазия кишечника
ОПРЕДЕЛЕНИЕ
В понятие приобретенной ангиодисплазии мы вкладываем заболевание, причиной которого является приобретенное патологическое (аномальное) строение правильно сформированных расширенных сосудов кишечника. В литературе подобные изменения также называют сосудистыми аномалиями, сосудистыми эктазиями, телеангиэктазиями. Гистологическое исследование этих сосудистых нарушений показывает, что они состоят из расширенных полнокровных сосудов, в основном выстланных эндотелием и значительно реже небольшим количеством гладкой мускулатуры. Большинство исследователей придерживаются теории, по которой периодически наступающая обструкция вен подслизистого слоя (функциональная венозная недостаточность) вследствие спазма гладкой мускулатуры с годами приводит к обязательному их расширению и ретроградно к расширению капилляров. Так происходит формирование приобретенной ангиодисплазии. Ишемия слизистой оболочки усугубляет это состояние. По данным трех крупных исследований, установлено, что в восточной популяции ангиэктазии распределены почти поровну между проксимальными и дистальными отделами тонкой кишки (44–69 и 31–56%
соответственно) (УД 4, СР D [10, 19, 32]).
Напротив, в США преобладающее большинство изменений (93%) локализовалось в тощей кишке и лишь 7% — в подвздошной кишке (УД 4, СР D [7, 14]).
По данным одного из отечественных исследований, наиболее часто (66,7%) приобретенные ангиодиспластические изменения локализовались в правой половине ободочной кишки и в терминальном отделе подвздошной кишки, у 25% — в сигмовидной кишке, и лишь у 8,3% больных имелось множественное поражение правых и левых отделов ободочной кишки (УД 4, СР D [1–3]).
Несмотря на малочисленность группы больных с приобретенной ангиодисплазией кишечника, изучение клинической картины, диагностики и лечения у пациентов с этим заболеванием является не менее актуальным, чем у больных с врожденной формой заболевания.
КЛИНИЧЕСКАЯ КАРТИНА
Характерным признаком приобретенной ангиодисплазии является ее развитие у лиц старшего возраста (старше 60 лет).
Основное клиническое проявление заболевания у пациентов — выделения крови из заднего прохода различной степени интенсивности, возникающие без видимых причин или после физической нагрузки на фоне удовлетворительного самочувствия.
В литературе встречаются описания остро возникших массивных кровотечений, с нарушением гемодинамических показателей, которые
потребовали интенсивной кровезамещающей терапии параллельно с проведением обследования. Следует отметить, что, по данным некоторых авторов, до 50% больных с этой патологией, учитывая рецидивный интенсивный характер кишечного кровотечения, были неоднократно оперированы в экстренном порядке. Однако данные интраоперационной ревизии с множественными гастро-, энтерои колотомиями не позволили выявить причину геморрагии. Иногда во время этих операций выполнялись необоснованные резекции различных отделов кишечника. Редкое установление причины кровотечения во время операции, по мнению исследователей, является другим характерным признаком приобретенной ангиодисплазии (УД 4, СР D [1–3]).
ДИАГНОСТИКА
Эндоскопические методы
Колоноскопия. При эндоскопическом исследовании приобретенная ангиодисплазия может выглядеть как участок слизистой оболочки округлой формы, ярко-красного или вишневого цвета, не выступающий в просвет кишечной стенки. От него радиально расходятся умеренно расширенные извитые сосуды на протяжении 7–10 мм. Размер этих патологических образований от 0,3 до 0,7 см. Образования легко травмируются, с появлением капелек крови. Небольшой размер сосудистого патологического образования также можно отнести к характерным признакам приобретенной ангиодисплазии. По данным самого крупного в нашей стране исследования, у большинства больных ангиодисплазии локализуются в правых отделах ободочной и терминальном отделе подвздошной кишки, что является еще одним характерным признаком этого заболевания (УД 4, СР D [1–3]).
Учитывая эти особенности клинических проявлений, следует подчеркнуть особую важность дифференциальной диагностики у больных приобретенной ангиодисплазией кишечника.
Капсульная эндоскопия. Говоря об эндоскопических методах диагностики, нельзя не упомянуть о капсульной эндоскопии, которая применяется для установления источника скрытого кровотечения. Достаточно информативна двухбаллонная энтероскопия с осмотром всей тонкой кишки (УД 4 СР D [14, 18, 22]). Оба метода могут применяться, когда все остальные способы обнаружения источника кровотечения уже исчерпаны. Диагностическая ценность капсульной эндоскопии и двухбаллонной энтероскопии в установлении источника тонкокишечного кровотечения составляют 38–83 и 58% соответственно (УД 4 СР D [24, 26, 28]). Два других сравнительных метаанализа подтверждают полученные данные (УД 4, СР D [11, 25]). В двух независимых исследованиях было высказано мнение, что капсульная эндоскопия и двухбаллонная энтероскопия являются взаимодополняющими методами и должны использоваться
совместно для поиска источника тонкокишечного кровотечения (УД 4, СР D [2, 5, 18]).
Рентгенологические методы
Мезентерикография. В настоящее время эффективными методами диагностики можно считать две объективные и взаимодополняющие методики: мезентерикография и эндоскопическое исследование (колоноскопия, энтероскопия).
При этом решающее значение в диагностике, в выборе способа и объема резекции у больных приобретенной ангиодисплазией кишечника имеет селективная мезентерикография.
Основные ангиографические признаки приобретенной ангиодисплазии: расширение магистральной артерии (подвздошно-ободочной), контрастирование дренирующей вены на ранней стадии исследования (на 3–4-й секунде), наличие четких и интенсивных сосудистых сплетений в кишечной стенке, указывающих на наличие артериовенозных шунтов, и медленная венозная разгрузка.
УСТАНОВЛЕНИЕ ДИАГНОЗА
Диагноз приобретенной ангиодисплазии устанавливается на основании характерной эндоскопической картины, данных мезентерикографии. Дифференциальную диагностику необходимо проводить с заболеваниями, сопровождающимися кровотечениями из желудка и тонкой кишки (язвенная болезнь желудка и двенадцатиперстной кишки, опухолевые заболевания желудка, двенадцатиперстной и тонкой кишки, дивертикул Меккеля и др.).
ЛЕЧЕНИЕ
Стоит отметить, что диагностическая двухбаллонная энтероскопия может трансформироваться в лечебную, если признано целесообразным, например, выполнение склерозирующего лечения.
Лечебная тактика при приобретенных ангиодисплазиях кишечника определяется величиной кровопотери, периодичностью кровотечений и наличием положительных ангиографических симптомов.
Так, известны попытки фармакологического воздействия на кровотечение, причиной которого являются ангиодиспластические изменения в кишечнике (УД 4, СР D [2, 6]). Эффективные, по данным одних исследований, гормоны талидомид или октреотид оказались не столь эффективными, по данным других исследований. Возможными механизмами воздействия авторы называют уменьшение мезентериального кровотока и блокирование вазодилататорных пептидов. Лечение с использованием эстрогена и прогестерона является наиболее распространенной фармакологической терапией, хотя недавние исследования показали меньшую эффективность, чем в ранее выполненных исследованиях (УД 4, СР D [27, 33, 34]).
При незначительных периодических кишечных кровотечениях возможно выполнение эндоскопической абляции, фотокоагуляции или склерозирующего лечения.
Так, в одном британском исследовании эндоскопическая абляция в ходе энтероскопии была применена у 23 пациентов. Методика признана весьма эффективной, несмотря на необходимость в повторной абляции у 30% больных (УД 4, СР D [16]).
Достаточно эффективна методика фотокоагуляции с использованием неодимового лазера, который, в отличие от аргонового, вызывает в 3–4 раза более глубокий и протяженный фиброз ткани (УД 4, СР D [8]). Эти данные были подтверждены двумя независимыми исследованиями (УД 4, СР D [30, 31]). При этом авторы отметили необходимость осторожного использования подобной технологии в тонкой кишке.
Несмотря на то что были предложены различные способы остановки кровотечения, причиной которого являются ангиодиспластические изменения в кишечнике, зачастую они рецидивируют спустя какое-то время. Это основная причина трудности оценки влияния примененных методик на любое повторное кровотечение. В связи с этим часто необходимо сочетать медикаментозную и эндоскопическую терапию. В случае выраженных сопутствующих заболеваний предпочтение целесообразно отдавать медикаментозной терапии как первой линии (УД 4, СР D [27]). Профузные рецидивирующие кишечные кровотечения с выраженной анемизацией и ухудшением общего состояния больных являются показанием к хирургическому лечению и резекции соответствующего отдела
кишечника.
Операцией выбора в большинстве случаев считается правосторонняя гемиколэктомия с формированием илеотрансверзоанастомоза. Использование лапароскопических технологий при выполнении операции существенно снижает инвазивность, обеспечивает хорошие непосредственные результаты операции.
Многообразие причин ангиодисплазии кишечника требует применения разных видов лечения, адекватных для каждой из форм заболевания и для каждого конкретного клинического наблюдения.
Критерии оценки качества помощи в стационаре представлены в таблице 17.2. Для оценки качества медицинской помощи используют временные, процессуальные и профилактирующие критерии. Временные характеризуют своевременность оказания определенных этапов медицинской помощи. Выполнение пациенту ряда медицинских манипуляций, инструментальных и лабораторных исследований, необходимых для качественного оказания медицинской помощи, оценивают в процессуальных критериях. Для анализа мероприятий, направленных на предотвращение развития осложнений, используют профилактирующие критерии.
Таблица 17.2. Критерии оценки качества медицинской помощи в стационаре больным с сосудистыми заболеваниями толстой кишки (ангиодисплазии) (0 — нет, 1 — да)
|
Клинические рекомендации |
Временные |
Процессуальные |
Профилактирующие |
|
Клинические рекомендации по диагностике и лечению взрослых больных ангиодисплазией кишечника (код МКБ — K55.2) |
Установка клинического диагноза: 72 ч |
Осмотр больного: 0/1. Ректороманоскопия: 0/1. Определение группы крови: 0/1. Клинический анализ крови; биохимический анализ крови; клинический анализ мочи; коагулограмма: 0/1. Исследование крови на сифилис, вирусный гепатит В, вирусный гепатит С: 0/1. Эзофагогастродуоденоскопия: 0/1. Колоноскопия: 0/1. Интестиноскопия: 0/1. Изучение ангиоархитектоники ЖКТ: 0/1. Метод оперативного лечения в соответствии с клиническими рекомендациями: 0/1. Метод анестезии в соответствии с объемом оперативного лечения: 0/1 |
Отсутствие осложнений: • кровотечение: 0/1; • абсцесс: 0/1; • пневмония: 0/1; • тромбоэмболия: 0/1; • перитонит: 0/1; • летальный исход: 0/1 |
Литература
1. Воробьев Г.И., Саламов К.Н., Кузьминов А.М. Ангиодисплазии кишечника. — М., 2001. — 160 с.
2. Кузьминов А.М., Саламов К.Н. Хирургическое лечение врожденных ангиодисплазий толстой кишки. Актуальные проблемы проктологии. — СПб., 1993. — 31 с.
3. Кузьминов А.М. Ангиодисплазии кишечника: Дис. … д-ра мед. наук. — М., 1997. — 297 с.
4. Abbas S.M., Bissett I.P., Holden A. et al. Clinical variables associated with positive angiographic localization of lower gastrointestinal bleeding // Aust. N.Z. J. Surg. — 2005. — Vol. 75. — P. 953–957.
5. Alexander J.A., Leighton J.A. Capsule endoscopy and balloon-assisted endoscopy: competing or complementary technologies in the evaluation of small bowel disease? // Curr. Opin. Gastroenterol. — 2009. — Vol. 25. — P. 433–437.
6. Barkin J.S., Ross B.S. Medical therapy for chronic gastrointestinal bleeding of obscure origin // Am. J. Gastroenterol. — 1998. — Vol. 93. — P. 1250–1254.
7. Bollinger E., Raines D., Saitta P. Distribution of bleeding gastrointestinal angioectasias in a Western population // World J. Gastroenterol. — 2012. — Vol. 18, N 43. — P. 6235–6239.
8. Bown S.G., Swain C.P., Storey D.W. et al. Endoscopic laser treatment of vascular anomalies of the upper gastrointestinal tract // Gut. — 1985. — Vol. 26. — P. 1338–1348.
9. Caos A., Benner K.D., Manier J. et al. Colonoscopy after Golytely preparation in acute rectal bleeding // J. Clin. Gastroenterol. — 1986. — Vol. 8. — P. 46–49.
10. Chen L.H., Chen W.G., Cao H.J. et al. Double-balloon enteroscopy for obscure gastrointestinal bleeding: a single center experience in China // World J. Gastroenterol. — 2010. — Vol. 16. — P. 1655–1659.
11. Chen X., Ran Z.H., Tong J.L. et al. A meta-analysis of the yield of capsule endoscopy compared to double-balloon enteroscopy in patients with small bowel diseases // World J. Gastroenterol. — 2007. — Vol. 13. — P. 4372–4378.
12. Fiorito J.J., Brandt L.J., Kozicky O. et al. The diagnostic yield of superior mesenteric angiography: correlation with the pattern of gastrointestinal bleeding // Am. J. Gastroenterol. — 1988. — Vol. 84. — P. 878–881.
13. Gayer C., Chino A., Lucas C. et al. Acute lower gastrointestinal bleeding in 1, 112 patients admitted to an urban emergency medical center // Surgery. — 2009. — Vol. 146. — P. 600–607.
14. Gerson L., Tokar J., Decker A. et al. Complications associated with double balloon enteroscopy: the U.S. experience // Am. J. Gastroenterol. — 2008. — Vol. 103. — S. 109.
15. Ghahremani G., Kangarloo H., Volberg F. Diffuse cavernous hemangioma of the colon in the Klippel-Trenaunay syndrome // Radiology. — 1976. — Vol. 18. — P. 673–678.
16. Hayat M., Axon A.T., O’Mahony S. Diagnostic yield and effect on clinical outcomes of push enteroscopy in suspected small-bowel bleeding // Endoscopy. — 2000. — Vol. 32. — P. 369–372.
17. Jenson D.M., Machicado G.A. Diagnosis and treatment of severe hematochezia: the role of urgent colonoscopy after purge // Gastroenterology. — 1988. — Vol. 95. — P. 1569–1574.
18. Kamalaporum P., Cho S., Basset N. et al. Double-balloon enteroscopy following capsule endoscopy in the management of obscure gastrointestinal bleeding: outcome of combined approach // Can. J. Gastroenterol. — 2008. — Vol. 22, N 5. — P. 491–495.
19. Kameda N., Higuchi K., Shiba M. et al. A prospective, single-blind trial comparing wireless capsule endoscopy and double-balloon enteroscopy in patients with obscure BMC // Gastroenterology. — 2012. — Vol. 18. — Is. 43. — P. 6235–6239.
20. Khanna A., Ognibene S.J., Koniaris L.G. Embolization as first line therapy for diverticulosis-related massive lower gastrointestinal bleeding: evidence from a metaanalysis // J. Gastrointest Surg. — 2005. — Vol. 9. — P. 343–352.
21. Leitman I.M., Paull D.E., Shires G.T. Evaluation and management of massive lower gastrointestinal hemorrhage // Ann. Surg. — 1989. — Vol. 209. — P. 175–180.
22. Mensink P.B., Haringsma J., Kucharzik T. et al. Complications of double balloon enteroscopy: a multicenter survey // Endoscopy. — 2007. — Vol. 39. — P. 613–615.
23. Ng D.A., Opelka F.G., Beck D.E. et al. Predictive value of technetium Tc99m-labeled red blood cell scintigraphy for positive angiogram in massive lower gastrointestinal hemorrhage // Dis. Colon Rectum. — 1997. — Vol. 40. — P. 471–477.
24. Ohmiya N., Yano T., Yamamoto H. et al. Diagnosis and treatment of obscure GI bleeding at double balloon endoscopy // Gastrointest. Endosc. — 2007. — Vol. 66, N 3. — P. 72–77.
25. Pasha S.F, Leighton J.A., Das A. et al. Double-balloon enteroscopy and capsule endoscopy have comparable diagnostic yield in small-bowel disease: a metaanalysis // Clin. Gastroenterol. Hepatol. — 2008. — Vol. 6. — P. 671–676.
26. Pennazio M., Santucci R., Rondonotti E. et al. Outcome of patients with obscure gastrointestinal bleeding after capsule endoscopy: report of 100 consecutive patients // Gastroenterology. — 2004. — Vol. 126. — P. 643–653.
27. Regula J., Wronska E., Pachlewski J. Vascular lesions of the gastrointestinal tract // Best Pract. Res. Clin. Gastroenterol. — 2008. — Vol. 22. — P. 313–328.
28. Rondonotti E., Villa F., Mulder C.J.J. et al. Small bowel capsule endoscopy in 2007: indications, risks and limitations // World J. Gastroenterol. — 2007. — Vol. 14. — P. 6140–6149.
29. Rossini F.P., Ferrari A., Spandre M. et al. Emergency colonoscopy // World J. Surg. — 1989. — Vol. 13. — P. 190–192.
30. Rutgeerts P., Van Gompel F., Geboes K. et al. Long term results of treatment of vascular malformations of the gastrointestinal tract by neodymium Yag laser photocoagulation // Gut. — 1985. — Vol. 26. — P. 586–593.
31. Sargeant I.R., Loizou L.A., Rampton D. et al. Laser ablation of upper gastrointestinal vascular ectasias: long term results // Gut. — 1993. — Vol. 34. — P. 470–475.
32. Sun B., Rajan E., Cheng S. et al. Diagnostic yield and therapeutic impact of double-balloon enteroscopy in a large cohort of patients with obscure gastrointestinal bleeding // Am. J. Gastroenterol. — 2006. — Vol. 101. — P. 2011–2015.
33. Szilagyi A., Ghali M.P. Pharmacological therapy of vascular malformations of the gastrointestinal tract // Can. J. Gastroenterol. — 2006. — Vol. 20. — P. 171–178.
34. Van Cutsem E., Rutgeerts P., Vantrappen G. Treatment of bleeding gastrointestinal vascular malformations with oestrogen-progesterone // Lancet. — 1990. — Vol. 335. — P. 953–955.
35. Vernava A.M., Longo W.E., Virgo K.S., Johnson F.E. A nationwide study of the incidence and etiology of lower gastrointestinal bleeding // Surg. Res. Commun. — 1996. — Vol. 18. — P. 113–120.
36. Vernava A.M., Moore B.A., Longo W.E., Johnson F.E. Lower gastrointestinal bleeding // Dis. Colon Rectum. — 1997. — Vol. 40. — P. 846–858.
37. Weldon D.T., Burke S.J., Sun S. et al. Interventional management of lower gastrointestinal bleeding // Eur. Radiol. — 2008. — Vol. 18. — P. 857–867.
38. Zuckerman G.R., Prakash C. Acute lower intestinal bleeding. Part I: clinical presentation and diagnosis // Gastrointest. Endosc. — 1998. — Vol. 48. — P. 606–616.
СЕМЕЙНЫЙ АДЕНОМАТОЗ ТОЛСТОЙ КИШКИ
Введение
На протяжении многих лет в центре внимания отечественных и зарубежных колопроктологов остается проблема лечения больных семейным аденоматозом толстой кишки. Актуальность этой проблемы связана с увеличением количества пациентов с семейным аденоматозом толстой кишки (САТК) как в нашей стране, так и за рубежом [12, 19, 33]. Вопросы реабилитации данного контингента пациентов, а также выбора оперативного вмешательства остаются нерешенными до настоящего времени [57]. К тому же наличие постоянной или временной илеостомы после хирургического лечения САТК представляет огромную социальную проблему как для самих больных, так и для окружающих [57].
Рекомендации по диагностике и лечению пациентов с САТК служат руководством для практических врачей, осуществляющих ведение и лечение таких больных, и подлежат регулярному пересмотру в соответствии с новыми данными научных исследований в этой области.
Рекомендации включают следующие разделы: определение заболевания, классификация, профилактика, диагностика, консервативное и оперативное лечение, правила ведения периоперационного периода, а также прогноз у больных с недостаточностью анального сфинктера.
Для отдельных положений рекомендаций приведены уровни доказательности согласно общепринятой классификации Оксфордского центра доказательной медицины [47] (табл. 18.1).
Таблица 18.1. Уровни доказательности и степени рекомендаций на основании руководства Оксфордского центра доказательной медицины
|
Уровень |
Исследования методов диагностики |
Исследования методов лечения |
|
1а |
Систематический обзор гомогенных диагностических исследований 1-го уровня |
Систематический обзор гомогенных РКИ |
|
1b |
Валидизирующее когортное исследование с качественным «золотым стандартом» |
Отдельное РКИ (с узким доверительным интервалом) |
Табл. 18.1. Окончание
|
Уровень |
Исследования методов диагностики |
Исследования методов лечения |
|
1с |
Специфичность или чувствительность столь высокие, что положительный или отрицательный результат позволяет исключить/установить диагноз |
Исследование «Всё или ничего» |
|
2а |
Систематический обзор гомогенных диагностических исследований >2-го уровня |
Систематический обзор (гомогенных) когортных исследований |
|
2b |
Разведочное когортное исследование с качественным «золотым стандартом» |
Отдельное когортное исследование (включая РКИ низкого качества; т.е. с <80% пациентов, прошедших контрольное наблюдение) |
|
2с |
Нет |
Исследование «исходов»; экологические исследования |
|
3а |
Систематический обзор гомогенных исследований уровня 3b и выше |
Систематический обзор гомогенных исследований «случай–контроль» |
|
3b |
Исследование с непоследовательным набором или без проведения исследования «золотого стандарта» у всех испытуемых |
Отдельное исследование «случай– контроль» |
|
4 |
Исследование «случай–контроль» или исследование с некачественным или зависимым «золотым стандартом» |
Серия случаев (и когортные исследования или исследования «случай–контроль» низкого качества) |
|
5 |
Мнение экспертов без тщательной критической оценки или основанное на физиологии, лабораторных исследованиях на животных или разработка «первых принципов» |
Мнение экспертов без тщательной критической оценки, лабораторные исследования на животных или разработка «первых принципов» |
|
Степени рекомендаций | ||
|
A |
Согласующиеся между собой исследования 1-го уровня | |
|
B |
Согласующиеся между собой исследования 2-го или 3-го уровня или экстраполяция на основе исследований 1-го уровня | |
|
C |
Исследования 4-го уровня или экстраполяция на основе уровня 2 или 3 | |
|
D |
Доказательства 5-го уровня или затруднительные для обобщения или некачественные исследования любого уровня | |
ВАЛИДИЗАЦИЯ РЕКОМЕНДАЦИЙ
Настоящие рекомендации составлены Общероссийской общественной организацией «Ассоциация колопроктологов России» и в предварительной версии были рецензированы независимыми экспертами,
которых попросили прокомментировать прежде всего, насколько интерпретация доказательств, лежащих в основе рекомендаций, доступна для понимания. Получены комментарии со стороны врачей амбулаторного звена, комментарии тщательно систематизировались и обсуждались на совещаниях экспертной группы.
Последние изменения в настоящих рекомендациях были представлены для дискуссии на заседании профильной комиссии «Колопроктология» Экспертного совета Минздрава России 12 сентября 2013 г. Проект рекомендаций был повторно рецензирован независимыми экспертами и врачами амбулаторного звена. Для окончательной редакции и контроля качества рекомендации были повторно проанализированы членами экспертной группы, которые пришли к заключению, что все замечания и комментарии приняты во внимание, риск систематических ошибок при разработке рекомендаций сведен к минимуму.
ОБЛАСТЬ ПРИМЕНЕНИЯ РЕКОМЕНДАЦИЙ
Данные клинические рекомендации применимы при осуществлении медицинской деятельности в рамках Порядка оказания медицинской помощи взрослому населению с заболеваниями толстой кишки, анального канала и промежности колопроктологического профиля.
Определение
Семейный аденоматоз (полипоз) толстой кишки (САТК) — это аутосомно-доминантный наследственный синдром, характеризующийся развитием большого количества полипов (аденом), от 100 до нескольких тысяч, на слизистой оболочке толстой кишки с прогрессивным ростом и обязательной малигнизацией при отсутствии своевременного лечения [20, 22].
Код по Международной классификации болезней 10-го пересмотра
n Класс: Новообразования (C00–D48) (II).
n Блок: Доброкачественные новообразования (D10–D36).
n Код:
v D12 Доброкачественное новообразование ободочной кишки, прямой кишки, заднего прохода [ануса] и анального канала:
- D12.0 Слепой кишки.
- D12.2 Восходящей ободочной кишки.
- D12.3 Поперечной ободочной кишки.
- D12.4 Нисходящей ободочной кишки.
- D12.5 Сигмовидной кишки.
- D12.6 Ободочной кишки неуточненной части.
- D12.7 Ректосигмоидного соединения.
- D12.8 Прямой кишки.
Классификация
В настоящее время в клинической практике используется классификация, подразделяющая САТК по клиническому течению. Классификация применяется для определения тяжести САТК и выбора тактики оперативного лечения [1, 3, 4].
По клиническому течению [3]
1. Классическая форма. Эта форма заболевания встречается наиболее часто. Первые симптомы появляются в возрасте 14–16 лет, злокачественное перерождение полипов наступает в возрасте 30–40 лет.
2. Тяжелая форма. Клинические проявления отмечаются уже в детском возрасте. При эндоскопическом обследовании определяются сотни или тысячи полипов, и их злокачественная трансформация наступает к 18–25 годам. Рано развиваются выраженные метаболические нарушения, вызывающие нередко отставание в физическом развитии.
3. Ослабленная (аттенуированная) форма. Для ослабленной формы аденоматоза характерно наличие в толстой кишке менее 100 полипов, которые расположены преимущественно в правых отделах. Характерен скудный семейный анамнез. Клинические проявления возникают в возрасте 40–45 лет, а малигнизация полипов происходит в возрасте старше 50 лет.
4. Полипозные синдромы. При САТК встречаются различные внекишечные проявления заболевания, которые можно определить уже при внешнем осмотре пациента. Сочетание полипоза толстой кишки с другими проявлениями заболевания обозначается как синдром.
n Синдром Гарднера — сочетание САТК с опухолями мягких тканей, остеома-
ми костей черепа. Чаще всего встречаются десмоиды — высокодифференцированные соединительнотканные опухоли, локализующиеся в передней брюшной стенке, брыжейке тонкой или толстой кишки, иногда в межмышечных слоях спины и плечевого пояса. Эти опухоли микроскопически лишены злокачественности, не дают метастазов, но склонны к агрессивному местно-деструктивному росту и частому рецидивированию.
n Синдром Тюрко — САТК в сочетании со злокачественными опухолями центральной нервной системы.
n Синдром Золингера–Эллисона — сочетание САТК с опухолями эндокринных желез.
n Синдром Пейтца–Егерса — сочетание полипоза ЖКТ с характерной меланиновой пигментацией слизистой оболочки губ и кожи лица. По-
липы при этом синдроме не являются аденомами. Это — гамартомы. Они крупные, с хорошо выраженной ножкой и крупнодольчатым телом. Количество полипов меньше, чем при других формах полипоза. Этот порок развития обусловлен генетическими повреждениями. Гамартомы чаще всего локализуются в тонкой кишке, несколько реже в толстой кишке и желудке. Малигнизация полипов при синдроме Пейтца–Егерса наблюдается очень редко.
n Ювенильный полипоз. Полипоз с преобладанием в полипах секреции эпителия желез.
Формулировка диагноза
При формулировании диагноза следует отразить клиническое течение заболевания (см. раздел «Диагностика»). Ниже приведены примеры формулировок диагноза.
n Семейный аденоматоз толстой кишки, тяжелая форма.
n Семейный аденоматоз толстой кишки, ослабленная форма.
Диагностика
Диагностика САТК основана на жалобах больного, степени их выраженности, анамнезе, анализе результатов обследования пациента (УД 3b, СР C [1, 4, 22, 65]).
Сбор анамнеза. Выясняется характер и интенсивность клинических проявлений (боли в животе, наличие патологических примесей в кале, кишечные расстройства), длительность заболевания, узнают семейный анамнез (УД 3b, СР C [1, 4, 65]).
Осмотр больного. Оценивается общее состояние больного (снижение массы тела, бледность и сухость кожных покровов и др.). Проводят пальпацию живота с целью выявления возможных опухолей брюшной полости (возможно, уже развившийся рак толстой кишки или желудка), выявляют десмоидные опухоли (УД 3b, СР B [23, 42, 56]). Отмечают внекишечные проявления полипоза (пигментация слизистой оболочки губ, кожи лица, опухоли мягких тканей, остеомы) (УД 3b, СР C [3]).
Пальцевое исследование прямой кишки. Оценивают наличие или отсутствие полипов в прямой кишке, их размеры, а также наличие или отсутствие их ракового превращения, тонус и волевые сокращения анального сфинктера (УД 3b, СР C [1, 4, 14]).
Ректороманоскопия. Осматривается слизистая оболочка прямой и дистальной части сигмовидной кишки: визуально оценивают распространенность и степень поражения полипами, наличие малигнизации (УД 2a, СР A [14]).
Колоноскопия с множественной биопсией. Основной и наиболее точный метод диагностики САТК. При данном исследовании определяют степень поражения различных отделов толстой кишки, количество и размеры полипов, что прямым образом влияет на выбор характера хирургического лечения. С помощью биопсии получают данные о злокачественной трансформации полипов в различных участках кишки (УД 2a, СР A [1, 4, 8]).
Гастроскопия. Определяют сопутствующие патологические изменения желудка, характерные для САТК, — наличие полипов с возможной их малигнизацией (УД 2a, СР B [12, 18, 30, 31, 67]).
Рентгенологическое исследование
Показания. Наличие циркулярной опухоли толстой кишки, не позволяющей исследовать проксимальные ее отделы.
Методика. Исследование проводят методом бариевой клизмы с двойным контрастированием.
При невозможности эндоскопического исследования данный метод — единственная возможность получить представление о характере поражения ободочной кишки (УД 4, СР C [1, 3, 4]).
Генетическое исследование. Проводится не только у больных с клиническими и эндоскопическими признаками заболевания, но также и для диагностики ранних (доклинических) стадий болезни у ближайших кровных родственников пациента. Поскольку установлено, что развитие САТК обусловлено мутацией APC-гена (Adenomatous Polyposis Coli), расположенного в длинном плече хромосомы 5 (локус 5q21), отвечающей за дифференцировку клеток кишечного эпителия. До 70% случаев классической и тяжелой форм САТК связаны именно с мутациями в этом гене. Основными типами мутаций в гене APC являются делеции и нонсенс-мутации, ведущие к возникновению укороченного нефункционального белка. Мутации в гене APC приводят почти к 100% риску возникновения заболевания. Мутации в интервалах между кодонами 437–1249 и 1465–1596 чаще всего определяются при классическом варианте течения САТК. В интервале 1250–1464 и в кодоне 1309 при тяжелом фенотипическом проявлении САТК. А в интервалах между кодонами 0–436 и 1597–2843, т.е. по обоим концам APC-гена, при ослабленной форме САТК.
Небольшая часть случаев классической формы САТК (менее 10%) может быть обусловлена мутациями в гене MYH (MutYH). Этот ген (OMIM 604933), расположенный на первой хромосоме в регионе 1р34, был картирован в 2002 г. САТК вызывают, как правило, биаллельные (расположенные на обеих хромосомах) мутации данного гена, однако некоторые исследователи указывают значимость для возникновения заболевания и гетерозиготных (на одной хромосоме) мутаций.
Таким образом, у всех пациентов с классической (или тяжелой) формой заболевания необходимо проводить ДНК-диагностику гена APC, а при отрицательном результате исследовать первичную структуру гена MYH. У 30–40% пациентов с ослабленной формой САТК выявляются мутации в гене MYH, еще у 10–15% встречаются мутации в гене APC (в основном миссенс-варианты). Поэтому молекулярно-генетический анализ у пациентов с ослабленной формой необходимо начинать именно с гена MYH, а в случае отрицательного результата исследовать ген APC.
В случае обнаружения мутации при любой форме САТК крайне важно
обследование всех кровных родственников данного пациента, так как если данная мутация будет выявлена у здоровых родственников, они автоматически включаются в группу риска, и им проводится пожизненный клинический мониторинг с целью выявления заболевания на ранней стадии. Родственники пациента, у которых мутация не будет выявлена, считаются здоровыми людьми с риском развития рака толстой кишки,
который не превышает общепопуляционный. Эти люди не нуждаются в пожизненном мониторинге.
В случае отсутствия мутаций в генах АРС и MYH у больных с клинической картиной полипоза толстой кишки отпадает целесообразность генетического тестирования всех его кровных родственников. Однако все эти родственники потенциально находятся в группе риска развития рака толстой кишки и нуждаются в пожизненном мониторинге.
Методика: производят забор крови больного САТК и его кровных родственников. Учитывая, что мутации, сходные по типу, локализуются в одних и тех же участках гена, наиболее точно удается определить вариант клинического течения и вероятность развития заболевания у родственников больного (УД 2a, СР B [9, 20, 70]).
Дополнительные исследования. Помимо указанных методов исследования, во время комплексной диагностики САТК и наследственных полипозных синдромов, при подозрении на малигнизацию полипов и наличие десмоидных опухолей дополнительно применяют УЗИ, КТ, МРТ (УД 4, СР C [24]).
ДИФФЕРЕНЦИАЛЬНАЯ ДИАГНОСТИКА
САТК дифференцируют от семейного рака толстой кишки без идентификации мутантного гена, ненаследственного неполипозного рака толстой кишки (синдром Линча), диффузной лимфоидной гиперплазии, неспецифического колита (неспецифический язвенный колит, гранулематозный и др.) (УД 4, СР C [2, 92]).
Лечение
Лечение САТК в настоящее время только хирургическое (УД 2b, СР B [40, 51]). Несмотря на успехи генетиков в изучении этого наследственного заболевания, методов профилактики и нехирургического лечения не существует (УД 2b, СР B [20, 22, 28, 70]).
Цель — эндоскопическое удаление одиночных полипов (паллиативное лечение), хирургическое удаление всей толстой кишки.
Показания к госпитализации — верифицированный диагноз САТК.
ХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕ
В настоящее время основным методом лечения САТК является хирургический. Способов консервативного лечения не существует. Химиотерапия проводится по определенным показаниям при развитии рака на фоне САТК (УД 4, СР C [29, 58, 60]). Наиболее широко применяются следующие операции.
n Эндоскопическая полипэктомия.
n Колэктомия с формированием илеоректального анастомоза.
n Колэктомия c брюшно-анальной резекцией прямой кишки, илеостомия по Бруку.
n Колопроктэктомия, илеостомия по Бруку.
n Колэктомия, резекция прямой кишки с формированием J-образного тонкокишечного резервуара, илеостомия по Торнболлу, мукозэктомия слизистой оболочки оставшейся части прямой кишки (УД 2b, СР B [40, 51, 53, 54]).
Эндоскопическая полипэктомия
Показания. При количестве полипов менее 20 при ослабленной форме полипоза (УД 3a, СР B [50]).
Методика. Производится электроэксцизия полипов через колоноскоп (УД 3a, СР B [50]).
Хорошие результаты лечения в раннем периоде после операции отмечаются в 31–83% случаев (УД 2a, СР B [5, 55]). Пациентам требуется регулярное динамическое наблюдение, так как данный метод являет ся исключительно поддерживающим и не может заменить операцию (УД 2a, СР A [2, 45, 54]).
Колэктомия с формированием илеоректального анастомоза
Показания. Не более 20 полипов в прямой кишке и отсутствие признаков рака (УД 3b, СР C [2, 10, 46]).
Методика. Положение больного на спине или модифицированное положение для литотомии. Производят среднесрединную лапаротомию, мобилизуют ободочную кишку от илеоцекального угла до прямой кишки, раздельно перевязывают питающие сосуды. Линейным степлером пересекают терминальную часть подвздошной кишки и прямую кишку на уровне первого крестцового позвонка. Далее формируют илеоректальный анастомоз «конец в конец» циркулярным сшивающим аппаратом (УД 3b, СР C [2, 21, 44, 53]).
Частота развития рака в сохраненной части прямой кишки после подобной операции через 10 лет составляет 3,9%, а через 25 лет — 25,8%
(УД 3b, СР C [15, 38, 69]).
Колэктомия c брюшно-анальной резекцией прямой кишки, илеостомия по Бруку
Показания. САТК с развитием рака прямой кишки выше уровня 6 см от края анального канала, противопоказано наложение тонкокишечного резервуара (УД 3a, СР B [36, 66]).
Методика. Положение больного на спине или модифицированное положение для литотомии. Производят среднесрединную лапаротомию, мобилизуют ободочную кишку от илеоцекального угла до прямой кишки, раздельно перевязывают питающие сосуды. Линейным степлером пересекают терминальную часть подвздошной кишки. Далее выделяют прямую кишку. Промежностная бригада рассекает все слои кишечной стенки на уровне зубчатой линии до соединения с абдоминальной бригадой хирургов. После удаления толстой кишки накладывают концевую илеостому по Бруку (УД 3b, СР B [2, 21, 53, 66]).
Хорошие и удовлетворительные результаты отмечаются у 61,1% пациентов (УД 3b, СР C [25, 53, 66]).
Были описаны случаи развития полипов на илеостоме (УД 5, СР D [41]).
Колопроктэктомия, илеостомия по Бруку
Показания. САТК с развитием рака нижнеампулярного отдела прямой кишки ниже уровня 6 см от края анального канала, противопоказано наложение тонкокишечного резервуара (УД 3a, СР B [36, 66]).
Методика. Положение больного на спине или модифицированное положение для литотомии. Производят среднесрединную лапаротомию, мобилизуют ободочную кишку от илеоцекального угла до прямой кишки, раздельно перевязывают питающие сосуды. Линейным степлером пересекают терминальную часть подвздошной кишки. Далее синхронно двумя бригадами выделяют прямую кишку, широко иссекая клетчатку. Со стороны промежности кисетным швом ушивается наружное отверстие заднего прохода. Отступив не менее 6 см от наложенного шва на заднем проходе, рассекают кожу промежности. Сзади по средней линии выделяют и пересекают копчиково-анальную связку. Пересекают мышцы, поднимающие задний проход. Мобилизуют переднюю полуокружность прямой кишки и соединяются с абдоминальной бригадой хирургов. После удаления толстой кишки накладывают концевую илеостому по Бруку (УД 3b, СР B [2, 21, 53, 66]).
Колопроктэктомия с формированием J-образного тонкокишечного резервуара, илеоанального анастомоза, илеостомия по Торнболлу. Мукозэктомия слизистой оболочки прямой кишки
Показания. Наличие множественных полипов во всех отделах толстой кишки (УД 2a, СР B [13, 38, 39, 62]).
Методика. Положение больного на спине или модифицированное положение для литотомии. Производят среднесрединную лапаротомию, мобилизуют ободочную кишку от илеоцекального угла до прямой кишки, раздельно перевязывают питающие сосуды. Линейным степлером пересекают терминальную часть подвздошной кишки. Далее выделяют прямую кишку. Следущим этапом операции промежностная бригада выполняет мукозэктомию прямой кишки со стороны промежности. При первом варианте мукозэктомия выполняется трансанально через операционный аноскоп или ректоскоп. При втором варианте мукозэктомия выполняется после эвагинации прямой кишки на промежность. Для этого с помощью специального окончатого аноскопа производят циркулярный разрез слизистой оболочки и отсепаровывают слизистую оболочку на 3–4 см в проксимальном направлении. После этого производят эвагинацию прямой кишки. Для этого вводят булавовидный инструмент, на котором на границе среднеи верхнеампулярного отдела завязывают тесьму и эвагинируют прямую кишку через анальный канал на промежность.
Далее удаляют оставшуюся часть слизистой оболочки. В настоящее время осуществляется научная программа, направленная на разработку технологии по созданию реконструированной слизистой оболочки прямой кишки с использованием методов клеточной трансплантации. С этой целью применяется клеточная аллотрансплантация клеток кишечного эпителия и мезенхимы различного происхождения. Получены успешные результаты этой научной работы. И, несмотря на то что эта методика в настоящее время пока не может быть рекомендована для широкого применения, перспективы этого направления представляются очевидными. Прямую кишку отсекают, культю прошивают линейным сшивающим аппаратом и инвагинируют в полость таза. Терминальный отдел подвздошной кишки складывают в виде буквы J, и с помощью аппаратов формируют тонкокишечный резервуар, а затем илеоректальный анастомоз. Операцию заканчивают наложением превентивной илеостомы по Торнболлу (УД 2a, СР B [2, 26, 37, 38, 52, 68, 71]).
Хорошие отдаленные результаты прослеживаются у 58–95% пациентов (УД 2a, СР B [6, 7, 38, 48, 59, 61–63]).
Развитие аденом и рака в анальном канале наблюдается в 10–31%, в тонкокишечном резервуаре в 8–62% случаев (УД 4, СР С [34, 35, 38,
49, 64]).
ЛЕЧЕНИЕ ДЕСМОИДНЫХ ОПУХОЛЕЙ
Лечение десмоидных опухолей комплексное.
Хирургическое лечение
Наиболее частой локализацией десмоидной опухоли в брюшной полости является брыжейка тонкой кишки. Удаление такой опухоли требует пересечения кровеносных сосудов брыжейки и резекции тонкой кишки. Поэтому при абдоминальной локализации десмоида после лапаротомии необходимо точно оценить резектабельность опухоли и предполагаемый объем резекции тонкой кишки. При локализации десмоидной опухоли в передней брюшной стенке выполняется ее широкое иссечение. Поскольку опухоль часто не имеет четких границ, обязательна тщательная ревизия послеоперационной раны во избежание оставления отростков опухоли. Выполняется пластическое закрытие дефектов передней брюшной стенки местными тканями или с использованием синтетической сетки.
Нехирургическое лечение
При нерезектабельных опухолях проводятся лекарственная терапия (винбластин, метотрексат) и химиолучевая терапия.
Дальнейшее ведение
Тяжесть состояния больного в раннем послеоперационном периоде обусловлена объемом хирургического вмешательства и исходными метаболическими нарушениями. Учитывая это, в течение первых 18–24 ч
после операции лечение пациента проводится в условиях отделения интенсивной терапии. Активизацию больного можно начинать со 2–3-го дня после операции. Прием жидкости и белковой пищи возможен со 2-го дня операции. У больных, перенесших мукозэктомию части прямой кишки и формирование тонкокишечного резервуара, орошение демукозированной прямой кишки и тонкокишечного резервуара растворами антисептиков проводится с 3–4-го дня после операции. Рентгенологическое и эндоскопическое обследование демукозированной прямой кишки и тонкокишечного резервуара проводится не ранее 1 мес после операции.
При отсутствии послеоперационных осложнений закрытие илеостомы может быть осуществлено через 2–3 мес после первой операции.
Чего нельзя делать
n Отказываться от проведения генетического тестирования кровных родственников пациента с клинически подтвержденным диагнозом САТК (родственников пробанда).
n Отказываться от проведения инструментального обследования толстой кишки родственникам пробанда, начиная с 14–15 лет, даже при отсутствии клинических проявлений аденоматоза и данных генетического тестирования.
n Отказываться от мониторинга кровных родственников пациентов, унаследовавших мутацию в АРС-гене от своих родителей, даже при отсутствии у них в момент первого обследования полипов толстой кишки.
n Не следует прибегать к пожизненному мониторингу родственников пробанда-носителя мутации в АРС-гене, не унаследовавших эту мутацию и, по сути, являющихся здоровыми людьми.
n Отказываться от мониторинга кровных родственников пробандов в семьях с невыявленной мутацией в АРС-гене.
n Не следует при хирургическом лечении САТК выполнять сегментарные резекции толстой кишки.
n Не следует отказываться от диспансерного наблюдения за больными с удаленной толстой кишкой в связи с пожизненно сохраняющейся угрозой развития полипов и рака верхних отделов ЖКТ, а также десмоидных фибром и возможностью возникновения метаболических расстройств у больных с илеостомой в случае ее дисфункции (УД 4, СР С [95]).
Прогноз
Если не лечить больного САТК, то неизбежно развитие рака из одного или нескольких полипов. Выполнение сфинктеросохраняющих операций возможно у 85% пациентов, обратившихся до малигнизации полипов, в то время как при развитии рака в прямой кишке процент успешных операций снижается до 30% (УД 3a, СР B [1, 4, 32]).
Профилактика
Поскольку САТК является наследственным заболеванием, профилактики его не существует (УД 5, СР D [28, 70]). Всем пациентам, перенесшим хирургическое лечение САТК, необходимо пожизненное медицинское наблюдение.
Критерии оценки качества помощи в стационаре представлены в таблице 18.2. Для оценки качества медицинской помощи используют временные, процессуальные и профилактирующие критерии. Временные характеризуют своевременность оказания определенных этапов медицинской помощи. Выполнение пациенту ряда медицинских манипуляций, инструментальных и лабораторных исследований, необходимых для качественного оказания медицинской помощи, оценивают в процессуальных критериях. Для анализа мероприятий, направленных на предотвращение развития осложнений, используют профилактирующие критерии.
Таблица 18.2. Критерии оценки качества медицинской помощи в стационаре больным семейным аденоматозом толстой кишки (0 — нет, 1 — да)
|
Клинические рекомендации |
Временные |
Процессуальные |
Профилактирующие |
|
Клинические рекомендации по диагностике и лечению взрослых пациентов с семейным аденоматозом толстой кишки (код по МКБ — D 12.6) |
Установка клинического диагноза в течение 72 ч: 0/1 |
Оценка анального рефлекса: 0/1. Пальцевое обследование прямой кишки: 0/1. Аноскопия: 0/1. Ректороманоскопия: 0/1. Определение группы крови: 0/1. Исследование крови на сифилис, вирусный гепатит В, вирусный гепатит С: 0/1. Клинический анализ крови; биохимический анализ крови; клинический анализ мочи; коагулограмма: 0/1. Колоноскопия: 0/1. Гастроскопия: 0/1. Генетические исследования: 0/1. Метод оперативного лечения в соответствии с клиническими рекомендациями: 0/1. Метод анестезии в соответствии с объемом оперативного лечения: 0/1 |
Отсутствие осложнений: • кровотечение: 0/1; • пневмония: 0/1; • тромбоэмболия: 0/1; • перитонит: 0/1; • летальный исход: 0/1 |
Литература
1. Воробьев Г.И. Основы колопроктологии. — М.: МИА, 2006. — 430 с.
2. Кайзер А.М. Колоректальная хирургия. — М.: БИНОМ, 2011. — 737 с.
3. Федоров В.Д., Дульцев Ю.В. Проктология. — М.: Медицина, 1984. — 384 с.
4. Шелыгин Ю.А., Благодарный Л.А. Справочник по колопроктологии. — М.: Литтерра, 2012. — 596 с.
5. Alarcon F.J., Burke C.A., Church J.M., van Stolk R.U. Familial adenomatous polyposis: efficacy of endoscopic and surgical treatment for advanced duodenal adenomas // Dis. Colon Rectum. — 1999. — Vol. 42. — P. 1533–1536.
6. Al-Sanea N., Alfaifi J., Homoud S.A. et al. Outcome after ileal pouch-anal
anastomosis for familial adenomatous polyposis compared to mucosal ulcerative colitis in a Middle Eastern population // Ann. Saudi Med. — 2013. — Vol. 33, N 3. — P. 268–272. doi: 10.5144/0256–4947.2013.268.
7. Ambroze W.L.Jr., Dozois R.R., Pemberton J.H. et al. Familial adenomatous polyposis: results following ileal pouch-anal anastomosis and ileorectostomy // Dis. Colon Rectum. — 1992. — Vol. 35. — P. 12–15.
8. Baron T.H., Smyrk T.C., Rex D.K. Recommended intervals between screening
and surveillance colonoscopies // Mayo Clin. Proc. — 2013. — Vol. 88, N 8. — P. 854–858.
9. Bertario L., Russo A., Radice P. et al. Genotype and phenotype factors as determinants for rectal stump cancer in patients with familial adenomatous polyposis. Hereditary Colorectal Tumors Registry // Ann. Surg. — 2000. — Vol. 231. — P. 538–543.
10. Browning S.M., Nivatvongs S. Intraoperative abandonment of ileal pouch
to anal anastomosis-the Mayo Clinic experience // J. Am. Coll. Surg. — 1998. — Vol. 186. — P. 441–445.
11. Bulow C., Vasen H., Jarvinen H. et al. Ileorectal anastomosis is appropriate for a subset of patients with familial adenomatous polyposis // Gastroenterology. — 2000. — Vol. 119. — P. 1454–1460.
12. Burke C., Church J., Beck G. The natural history of upper gastrointestinal
adenomas in untreated patients with familial polyposis // Gastrointest. Endosc. — 1999. — Vol. 49. — P. 358–642.
13. Chun H., Smith L.E., Orkin B.A. Intraoperative reasons for abandoning ileal pouch-anal anastomosis procedures // Dis. Colon Rectum. — 1995. — Vol. 38. — P. 273–275.
14. Church J., Burke C., McGannon E. et al. Predicting polyposis severity by
proctoscopy: how reliable is it? // Dis. Colon Rectum. — 2001. — Vol. 44. — P. 1249–1254.
15. Church J., McGannon E., Pastean O. et al. Rectal cancer risk after ileorectal anastomosis for familial polyposis is lower than you think // Dis. Colon Rectum. — 2000. — Vol. 43. — P. A27.
16. Church J.M., Fazio V.W., Lavery I.C. et al. Quality of life after prophylactic
colectomy and ileorectal anastomosis in patients with familial adenomatous polyposis // Dis. Colon Rectum. — 1996. — Vol. 39. — P. 1404–1408.
17. Church J.M., McGannon E., Burke C., Clark B. Teenagers with familial adenomatous polyposis: what is their risk for colorectal cancer? // Dis. Colon Rectum. — 2002. — Vol. 45. — P. 887–889.
18. Church J.M., McGannon E., Hull-Boiner S. et al. Gastroduodenal polyps in patients with familial adenomatous polyposis // Dis. Colon Rectum. — 1992. — Vol. 35. — P. 1170–1173.
19. Church J.M., McGannon E. A polyposis registry; how to set one up and make it work // Semin. Colon Rectal Surg. — 1995. — Vol. 6. — P. 48–54.
20. Church J.M. Anatomy of a gene: functional correlations of APC mutation // Semin. Colon Rectum Surg. — 1998. — Vol. 9. — P. 49–52.
21. Corman M.L. Colon and Rectal Surgery. — 4th ed. — Philadelphia, 1998. — 800 р.
22. Church J.M. Familial adenomatous polyposis: a review // Perspect. Colon Rectal Surg. — 1995. — Vol. 8. — P. 203–225.
23. Clark S.K., Neale K.F., Landgrebe J.C., Phillips R.K. Desmoid tumours complicating familial adenomatous polyposis // Br. J. Surg. — 1999. — Vol. 86. — P. 1185–1189.
24. Debinski H., Love S., Spigelman A.D., Phillips R.K. Colorectal polyp counts
and cancer in familial adenomatous polyposis // Gastroenterology. — 1996. — Vol. 110. — P. 1028–1030.
25. Fazio V.W., Church J.M. Complications and function of the continent ileostomy at the Cleveland Clinic // World J. Surg. — 1988. — Vol. 12. — P. 148–154.
26. Fazio V.W., Tjandra J.J. Transanal mucosectomy: ileal pouch advancement for anorectal dysplasia or inflammation after restorative proctocolectomy // Dis. Colon Rectum. — 1994. — Vol. 37. — P. 1008–1011.
27. Feinberg S.M., Jagelman D.G., Sarre R.G. et al. Spontaneous resolution of
rectal polyps in patients with familial polyposis following abdominal colectomy and ileorectal anastomosis // Dis. Colon Rectum. — 1988. — Vol. 31. — P. 169–175.
28. Friedl W., Caspari R., Sengteller M. et al. Can APC mutation analysis contribute to therapeutic decisions in familial adenomatous polyposis? Experience from 680 FAP families // Gut. — 2001. — Vol. 48. — P. 515–521.
29. Giardiello F.M., Yang V.W., Hylind L.M. et al. Primary chemoprevention
of familial adenomatous polyposis with sulindac // N. Engl. J. Med. — 2002. — Vol. 346. — P. 1054–1059.
30. Groves C.J., Saunders B.P., Spigelman A.D., Phillips R.K. Duodenal cancer in patients with familial adenomatous polyposis: results of a 10 year prospective study // Gut. — 2002. — Vol. 50. — P. 636–634.
31. Guillem J.G., Smith A., Puig-La Calle J., Ruo L. Gastrointestinal polyposis
syndromes // Curr. Probl. Surg. — 1999. — Vol. 36. — P. 217–323.
32. Heiskanen I., Luostarinen T., Jarvinen H.J. Impact of screening examinations on survival in familial adenomatous polyposis // Scand. J. Gastroenterol. — 2000. — Vol. 35. — P. 1284–1287.
33. Hernegger G.S., Moore H.G., Guillem J.G. Attenuated familial adenomatous polyposis: an evolving and poorly understood entity // Dis. Colon Rectum. — 2002. — Vol. 45. — P. 127–136.
34. Heuschen U.A., Heuschen G., Autschbach F. et al. Adenocarcinoma in the
ileal pouch: late risk of cancer after restorative proctocolectomy // Int. J. Colorectal Dis. — 2001. — Vol. 16. — P. 126–130.
35. Iwama T., Kamikawa J., Higuchi T. et al. Development of invasive adenocarcinoma in a long-standing diverted ileal J-pouch for ulcerative colitis: report of a case // Dis. Colon Rectum. — 2000. — Vol. 43. — P. 101–104.
36. Jirásek V. Digestive tract polyposis // Vnitr. Lek. — 2013. — Vol. 59, N 7. — P. 559–565.
37. Kaiser A.M., Stein J.P., Beart R.W.Jr. T-pouch: a new valve design for a continent ileostomy // Dis. Colon Rectum. — 2002. — Vol. 45. — P. 411–415.
38. Kartheuser A., Stangherlin H., Brandt L. et al. Restorative proctocolectomy and ileal pouch — anal anastomosis for familial adenomatous polyposis revisited // Fam. Cancer. — 2006. — Vol. 5. — P. 241–260.
39. Kartheuser A.H., Parc R., Penna C.P. et al. Ileal pouch-anal anastomosis as the first choice operation in patients with familial adenomatous polyposis: a ten year experience // Surgery. — 1996. — Vol. 119. — P. 615–623.
40. Komori K., Kanemitsu Y., Kimura K. et al. Efforts to advance surgical treatments for patients with familial adenomatous polyposis for 40 years in a cancer hospital // Hepatogastroenterology. — 2013. — Vol. 9, N 60. — P. 125.
41. Lux N., Wedell J., Busch M., van Calker H. Adenocarcinoma of the ileostomy after total proctocolectomy in familial polyposis. A case report and synthesis of previously published cases // Chirurg. — 1993. — Vol. 64. — P. 416–418.
42. Ma J.H., Ma Z.H., Dong X.F. et al. Abdominal wall desmoid tumors: A case report // Oncol. Lett. — 2013. — Vol. 5, N 6. — P. 1976–1978.
43. Madden M.V., Neale K.F., Nicholls R.J. et al. Comparison of the morbidity and function after colectomy and ileorectal anastomosis or restorative proctectomy for familial adenomatous polyposis // Br. J. Surg. — 1991. — Vol. 78. — P. 789–792.
44. Milsom J.W., Ludwig K.A., Church J.M., Garcia-Ruiz A. Laparoscopic total abdominal colectomy with ileorectal anastomosis for familial adenomatous polyposis // Dis. Colon Rectum. — 1997. — Vol. 40. — P. 675–678.
45. Norton I.D., Geller A., Petersen B.T. et al. Endoscopic surveillance and ablative therapy for periampullary adenomas // Am. J. Gastroenterol. — 2001. — Vol. 96. — P. 101–106.
46. Nugent K.P., Phillips R.K. Rectal cancer risk in older patients with familial adenomatous polyposis and an ileorectal anastomosis: a cause for concern // Br. J. Surg. — 1992. — Vol. 79. — P. 1204–1206.
47. OCEBM Levels of Evidence Working Group. The Oxford 2011 Levels of Evidence. — Oxford Centre for Evidence-Based Medicine, 2011.
48. Ozdemir Y., Kalady M.F., Aytac E. et al. Anal transitional zone neoplasia in patients with familial adenomatous polyposis after restorative proctocolectomy and IPAA: incidence, management, and oncologic and functional outcomes // Dis. Colon Rectum. — 2013. — Vol. 56, N 7. — P. 808–814.
49. Parc Y.R., Olschwang S., Desaint B. et al. Familial adenomatous polyposis: prevalence of adenomas in the ileal pouch after restorative proctocolectomy // Ann. Surg. — 2001. — Vol. 233. — P. 360–364.
50. Penna C., Phillips R.K., Tiret E., Spigelman A.D. Surgical polypectomy of duodenal adenomas in familial adenomatous polyposis: experience of two European centres // Br. J. Surg. — 1993. — Vol. 80. — P. 1027–1029.
51. Phillips R.K. Familial adenomatous polyposis: the surgical treatment of the colorectum // Semin. Colon Rectal Surg. — 1995. — Vol. 6. — P. 33–37.
52. Remzi F.H., Church J.M., Bast J. et al. Mucosectomy vs stapled ileal pouchanal anastomosis in patients with familial adenomatous polyposis: functional outcome and neoplasia control // Dis. Colon Rectum. — 2001. — Vol. 44. — P. 1590–1596.
53. Setti-Carraro P., Nicholls R.J. Choice of prophylactic surgery for the large bowel component of familial adenomatous polyposis // Br. J. Surg. — 1996. — Vol. 83. — P. 885–892.
54. Smith J.C., Schäffer M.W., Ballard B.R. et al. Adenocarcinomas after prophylactic surgery for familial adenomatous polyposis // J. Cancer Ther. — 2013. — Vol. 4, N 1. — P. 260–270.
55. Soravia C., Berk T., Haber G. et al. Management of advanced duodenal polyposis in familial adenomatous polyposis // J. Gastrointest. Surg. — 1997. — Vol. 1. — P. 474–478.
56. Soravia C., Berk T., McLeod R.S., Cohen Z. Desmoid disease in patients with familial adenomatous polyposis // Dis. Colon Rectum. — 2000. — Vol. 43. — P. 363–369.
57. Phillips R.K., Spigelman A.D., Thomson J.P. Introduction, history and registries // Familial Adenomatous Polyposis and other Polyposis Syndromes. — London: Edward Arnold, 1995.
58. Stoner G.D., Budd G.T., Ganapathi R. et al. Sulindac sulfone induced regression of rectal polyps in patients with familial adenomatous polyposis // Adv. Exp. Med. Biol. — 1999. — Vol. 470. — P. 45–53.
59. Thompson-Fawcett M.W., Marcus V.A., Redston M. et al. Adenomatous polyps develop commonly in the ileal pouch of patients with familial adenomatous polyposis // Dis. Colon Rectum. — 2001. — Vol. 44. — P. 347–353.
60. Tonelli F., Valanzano R., Messerini L., Ficari F. Long-term treatment with sulindac in familial adenomatous polyposis: is there an actual efficacy in prevention of rectal cancer? // J. Surg. Oncol. — 2000. — Vol. 74. — P. 15–20.
61. Tuckson W., Lavery I., Fazio V. et al. Manometric and functional comparison of ileal pouch anal anastomosis with and without anal manipulation // Am. J. Surg. — 1991. — Vol. 161. — P. 90–95.
62. Uyeda J.W., Lebedis C.A., Penn D.R. et al. Ileal pouch-anal anastomosis surgery: anatomy, postoperative complications, and image-guided intervention // Semin. Ultrasound CT MR. — 2013. — Vol. 34, N 4. — P. 299–310.
63. Van Duijvendijk P., Slors J.F., Taat C.W. et al. Quality of life after total colectomy with ileorectal anastomosis or proctocolectomy and ileal pouch-anal anastomosis for familial adenomatous polyposis // Br. J. Surg. — 2000. — Vol. 87. — P. 590–596.
64. Van Duijvendijk P., Vasen H.F., Bertario L. et al. Cumulative risk of developing polyps or malignancy at the ileal pouch-anal anastomosis in patients with familial adenomatous polyposis // J. Gastrointest. Surg. — 1999. — Vol. 3. — P. 325–330.
65. Vasen H.F. Clinical diagnosis and management of hereditary colorectal cancer syndromes // J. Clin. Oncol. — 2000. — Vol. 1. — N. 18. — P. 81–92.
66. Wallace M.H., Phillips R.K. Preventative strategies for periampullary tumours in FAP // Ann. Oncol. — 1999. — Vol. 10. — Suppl. 4. — P. 201–203.
67. Wallace M.H., Phillips R.K. Upper gastrointestinal disease in patients with familial adenomatous polyposis // Br. J. Surg. — 1998. — Vol. 85. — P. 742–750.
68. Wasmuth H.H., Trano G., Myrvold H.E. et al. Adenoma formation and malignancy after restorative proctocolectomy with or without mucosectomy in patients with familial adenomatous polyposis // Dis. Colon Rectum. — 2013. — Vol. 56, N 3. — P. 288–294.
69. Wu J.S., McGannon E.A., Church J.M. Incidence of neoplastic polyps in the ileal pouch of patients with familial adenomatous polyposis after restorative proctocolectomy // Dis. Colon Rectum. — 1998. — Vol. 41. — P. 552–527.
70. Wu J.S., Paul P., McGannon E.A., Church J.M. APC genotype, polyp number and surgical options in familial adenomatous polyposis // Ann. Surg. — 1998. — Vol. 227. — P. 57–62.
71. Ziv Y., Fazio V.W., Church J.M. et al. Stapled ileal pouch anal anastomoses are safer than hand-sewn anastomoses in patients with ulcerative colitis // Am. J. Surg. — 1996. — Vol. 171. — P. 320–323.
БОЛЕЗНЬ КРОНА
Введение
Болезнь Крона названа в честь американского гастроэнтеролога B.B. Crohn, который вместе со своими коллегами I. Ginzburg и G.D. Oppenheimer в 1932 г. опубликовали 14 случаев этого заболевания с локализацией в терминальном отделе подвздошной кишки.
При болезни Крона могут поражаться любые отделы желудочно-кишечного тракта (ЖКТ) — от полости рта до ануса. Тем не менее в преобладающем большинстве случаев болезнь Крона поражает илеоцекальный отдел, поэтому клиническая картина в острых случаях имеет сходство с острым аппендицитом. Болезнь Крона, в отличие от язвенного колита, не может быть излечена ни терапевтическими, ни хирургическими методами лечения [1].
Настоящие рекомендации по диагностике и лечению больных болезнью Крона являются руководством для практических врачей, осуществляющих ведение и лечение таких пациентов. Рекомендации подлежат регулярному пересмотру в соответствии с новыми данными научных исследований в этой области. Настоящие рекомендации составлены на основании анализа литературы, Европейского доказательного консенсуса по диагностике и лечению болезни Крона, представленного Европейским обществом по изучению язвенного колита и болезни Крона [2]. Рекомендации включают следующие разделы: определение, класси-
фикация, диагностика, консервативное и хирургическое лечение.
Для отдельных положений рекомендаций приведены уровни доказательности согласно общепринятой классификации Оксфордского центра доказательной медицины (табл. 19.1) [3].
Таблица 19.1. Уровни доказательности и степени рекомендаций на основании руководства Оксфордского центра доказательной медицины
|
Уровень |
Диагностическое исследование |
Терапевтическое исследование |
|
1а |
Систематический обзор гомогенных диагностических исследований 1-го уровня |
Систематический обзор гомогенных РКИ |
|
1b |
Валидизирующее когортное исследование с качественным «золотым стандартом» |
Отдельное РКИ (с узким доверительным интервалом) |
Табл. 19.1. Окончание
|
Уровень |
Диагностическое исследование |
Терапевтическое исследование |
|
1с |
Специфичность или чувствительность столь высокие, что положительный или отрицательный результат позволяет исключить/установить диагноз |
Исследование «Всё или ничего» |
|
2а |
Систематический обзор гомогенных диагностических исследований >2-го уровня |
Систематический обзор (гомогенных) когортных исследований |
|
2b |
Разведочное когортное исследование с качественным «золотым стандартом» |
Отдельное когортное исследование (включая РКИ низкого качества; т.е. с <80% пациентов, прошедших контрольное наблюдение) |
|
2с |
Нет |
Исследование «исходов»; экологические исследования |
|
За |
Систематический обзор гомогенных исследований уровня 3b и выше |
Систематический обзор гомогенных исследований «случай–контроль» |
|
3b |
Исследование с непоследовательным набором или без проведения исследования «золотого стандарта» у всех испытуемых |
Отдельное исследование «случай– контроль» |
|
4 |
Исследование «случай–контроль» или исследование с некачественным или зависимым «золотым стандартом» |
Серия случаев (и когортные исследования или исследования «случай–контроль» низкого качества) |
|
5 |
Мнение экспертов без тщательной критической оценки или основанное на физиологии, лабораторные исследования на животных или разработка «первых принципов» |
Мнение экспертов без тщательной критической оценки, лабораторные исследования на животных или разработка «первых принципов» |
|
Степени рекомендаций | ||
|
A |
Согласующиеся между собой исследования 1-го уровня | |
|
B |
Согласующиеся между собой исследования 2-го или 3-го уровня или экстраполяция на основе исследований 1-го уровня | |
|
C |
Исследования 4-го уровня или экстраполяция на основе уровня 2 или 3 | |
|
D |
Доказательства 4-го уровня или затруднительные для обобщения или некачественные исследования любого уровня | |
ВАЛИДИЗАЦИЯ РЕКОМЕНДАЦИЙ
Настоящие рекомендации в предварительной версии были рецензированы независимыми экспертами, которых попросили прокомментировать прежде всего, насколько интерпретация доказательств, лежащих
в основе рекомендаций, доступна для понимания. Получены комментарии со стороны врачей амбулаторного звена. Полученные комментарии тщательно систематизировались и обсуждались на совещаниях экспертной группы.
Последние изменения в настоящих рекомендациях были представлены для дискуссии на заседании профильной комиссии «Колопроктология» Экспертного совета Минздрава России 17 декабря 2012 г. Проект рекомендаций был повторно рецензирован независимыми экспертами и врачами амбулаторного звена. Для окончательной редакции и контроля качества рекомендации были повторно проанализированы членами экспертной группы, которые пришли к заключению, что все замечания и комментарии приняты во внимание, риск систематических ошибок при разработке рекомендаций сведен к минимуму.
ОБЛАСТЬ ПРИМЕНЕНИЯ РЕКОМЕНДАЦИЙ
Данные клинические рекомендации применимы при осуществлении медицинской деятельности в рамках Порядка оказания медицинской помощи взрослому населению с заболеваниями толстой кишки, анального канала и промежности колопроктологического профиля, а также в рамках Порядка оказания медицинской помощи населению при заболеваниях гастроэнтерологического профиля.
Определения
Болезнь Крона — хроническое, рецидивирующее заболевание желудочно-кишечного тракта неясной этиологии, характеризуемое трансмуральным, сегментарным, гранулематозным воспалением с развитием местных и системных осложнений [4].
Под обострением (рецидивом, атакой) болезни Крона понимают появление типичных симптомов заболевания у больных болезнью Крона в стадии клинической ремиссии, спонтанной или медикаментозно поддерживаемой. Ремиссия болезни Крона — исчезновение типичных проявлений заболевания (УД 5, СР D [5]). Выделяют:
n клиническую ремиссию — отсутствие симптомов болезни Крона [соответствует значению индекса активности болезни Крона <150 (см. ниже)];
n эндоскопическую ремиссию — отсутствие видимых макроскопических признаков воспаления при эндоскопическом исследовании;
n гистологическую ремиссию — отсутствие микроскопических признаков воспаления.
Код по Международной классификации болезней 10-го пересмотра
n К50 Болезнь Крона
Классификация
Для описания локализации поражения применяется Монреальская классификация (табл. 19.2) [6]. Поражение верхних отделов ЖКТ редко встречается в изолированном виде и, как правило, дополняет терминальный илеит, колит или илеоколит.
Таблица 19.2. Монреальская классификация болезни Крона по локализации поражения
|
Терминальный илеит |
± Поражение верхних отделов ЖКТ |
|
Колит | |
|
Илеоколит |
По распространенности поражения выделяют следующие виды болезни Крона:
n локализованную:
v поражение протяженностью менее 30 см. Обычно используется для описания изолированного поражения илеоцекальной зоны (<30 см подвздошной кишки + правый отдел толстой кишки);
v возможно изолированное поражение небольшого участка толстой кишки;
n распространенную:
v поражение протяженностью более 100 см (сумма всех пораженных участков).
По характеру течения выделяют [7]:
n острое течение (менее 6 мес от дебюта заболевания):
v с фульминантным началом;
v с постепенным началом;
n хроническое непрерывное течение (отсутствие более чем 6-месячных периодов ремиссии на фоне адекватной терапии);
n хроническое рецидивирующее течение (наличие более чем 6-месячных периодов ремиссии):
v редко рецидивирующее (1 раз в год или реже);
v часто рецидивирующее (2 раза и более в год).
Тяжесть заболевания в целом определяется тяжестью текущей атаки, наличием внекишечных проявлений и осложнений, рефрактерностью к лечению, в частности развитием гормональной зависимости и резистентности. Однако для формулирования диагноза и определения тактики лечения следует определять тяжесть текущего обострения (атаки) (УД 1b, СР В), для чего используются простые критерии, разработанные Обществом по изучению ВЗК при Ассоциации колопроктологов России, и индекс активности болезни Крона (индекс Беста; CDAI), как правило, применяемый в клинических испытаниях в виду сложности его расчета. Выделяют легкую, среднетяжелую и тяжелую атаки болезни Крона (табл. 19.3, 19.4).
Таблица 19.3. Тяжесть атаки по критериям Общества по изучению воспалительных заболеваний кишечника при Ассоциации колопроктологов России [8]
|
Критерий |
Степень тяжести атаки | ||
|
легкая |
среднетяжелая |
тяжелая | |
|
Средняя частота стула в сутки за последние 3 дня |
Менее 4 |
4–6 |
7 и более |
|
Боль в животе |
Отсутствует или незначительная |
Умеренная |
Сильная |
|
Лихорадка, °С |
Отсутствует |
<38 |
>38 |
|
Тахикардия, в минуту |
Отсутствует |
<90 |
>90 |
|
Снижение массы тела |
Отсутствует |
<5% |
5% и более |
|
Гемоглобин, г/л |
>100 |
90–100 |
<90 |
|
СОЭ, мм/ч |
Норма |
<30 |
>30 |
|
Лейкоцитоз |
Отсутствует |
Умеренный |
Высокий с изменением формулы |
|
СРБ, г/л |
Норма |
<10 |
>10 |
|
Гипопротеинемия |
Отсутствует |
Незначительная |
Выраженная |
|
Внекишечные проявления (любые) |
Нет |
Есть |
Есть |
|
Кишечные осложнения (любые) |
Нет |
Есть |
Есть |
Таблица 19.4. Тяжесть атаки болезни Крона по индексу активности болезни Крона (CDAI; индекс Беста) [9]
|
Критерий |
Система подсчета |
Коэффициент |
Сумма баллов |
|
Частота жидкого или кашицеобразного стула |
Учитывается сумма дефекаций за последние 7 дней |
×2 |
= |
|
Боль в животе: 0 — отсутствие; 1 — слабая; 2 — умеренная; 3 — сильная |
Учитывается сумма баллов за 7 дней |
×5 |
= |
|
Общее самочувствие: 0 — хорошее; 1 — удовлетворительное; 2 — плохое; 3 — очень плохое; 4 — ужасное |
Учитывается сумма баллов за 7 дней |
×7 |
= |
Табл. 19.4. Окончание
|
Критерий |
Система подсчета |
Коэффициент |
Сумма баллов |
|
Другие симптомы (внекишечные или кишечные осложнения): артрит или атралгия; ирит или увеит; узловая эритема; гангренозная пиодермия; афтозный стоматит; анальные поражения (трещины, свищи, абсцессы); другие свищи |
Каждый из существующих пунктов умножается на коэффициент |
×20 |
= |
|
Лихорадка >37,5 |
Учитывается сумма эпизодов лихорадки за 7 дней |
×20 |
= |
|
Применение лоперамида (других опиатов) для купирования диареи: 0 — нет; 1 — да |
|
×30 |
= |
|
Напряжение мышц живота (или пальпируемый инфильтрат): 0 — отсутствует; 2 — сомнительно; 5 — отчетливо |
Оценка производится однократно в момент осмотра |
×10 |
= |
|
Гематокрит: 47 минус показатель больного (М); 42 минус показатель больного (Ж) |
Учитывается разница между нормальным уровнем и показателем больного (с учетом знака «+» или «–») |
×6 |
= |
|
Масса тела, кг |
1 – (фактическая масса: идеальная масса) |
×100 |
= |
|
Итого |
|
|
Общее число баллов |
Примечание: <150 баллов — неактивная болезнь Крона (клиническая ремиссия); 150–300 баллов — легкая атака; 301–450 баллов — среднетяжелая атака; >450 — тяжелая атака.
Болезнь Крона также классифицируется в зависимости от фенотипического варианта, как:
n нестриктурирующий, непенетрирующий тип;
n стриктурующий тип;
n пенетрирующий тип.
Перианальные поражения (свищи, анальные трещины, перианальные абсцессы) могут дополнять любой из указанных фенотипических вариантов.
Классификация болезни Крона, в зависимости от ответа на гормональную терапию, совпадает с таковой для язвенного колита. Выделяют:
n гормональную резистентность:
v в случае тяжелой атаки — сохранение активности заболевания, несмотря на в/в введение глюкокортикостероидов (ГКС) в дозе, эквивалентной 2 мг/кг в сутки, в течение более чем 7 дней;
v в случае среднетяжелого обострения — сохранение активности заболевания при пероральном приеме ГКС в дозе, эквивалентной преднизолона 0,75 мг/кг в сутки в течение 4 нед;
n гормональная зависимость:
v увеличение активности болезни при уменьшении дозы ГКС ниже дозы, эквивалентной 10–15 мг преднизолона в сутки в течение 3 мес от начала лечения;
v возникновение рецидива болезни в течение 3 мес после окончания лечения ГКС.
Формулировка диагноза
При формулировании диагноза следует отразить локализацию поражения с перечислением пораженных сегментов желудочно-кишечного тракта, характер течения заболевания, фазу течения (ремиссия или обострение), тяжесть текущей атаки или наличие ремиссии, наличие гормональной зависимости или резистентности, а также наличие внекишечных или кишечных и перианальных осложнений (см. раздел «Диагностика»). Ниже приведены примеры формулировок диагноза.
n Болезнь Крона в форме илеоколита с поражением терминального отдела подвздошной кишки, слепой и восходящей кишки, хроническое рецидивирующее течение, среднетяжелая форма, осложненная инфильтратом брюшной полости, наружным кишечным свищом и перианальными поражениями (передняя и задняя анальные трещины).
n Болезнь Крона в форме терминального илеита, хроническое рецидивирующее течение, ремиссия. Стриктура терминального отдела подвздошной кишки без нарушения кишечной проходимости.
n Болезнь Крона в форме колита с поражением восходящей, сигмовидной и прямой кишки, хроническое непрерывное течение, тяжелая форма. Перианальные проявления в виде заднего экстрасфинктерного свища прямой кишки, осложненного параректальным затеком. Гормональная зависимость.
n Болезнь Крона с поражением подвздошной, тощей и двенадцатиперстной кишки, хроническое рецидивирующее течение, тяжелая форма, осложненная инфильтратом брюшной полости и стриктурой тощей кишки с нарушением кишечной проходимости. Состояние после резекции илеоцекального отдела в 1999 г. по поводу стриктуры терминального отдела подвздошной кишки.
Диагностика
КЛИНИЧЕСКИЕ ДИАГНОСТИЧЕСКИЕ КРИТЕРИИ
К наиболее частым клиническим симптомам болезни Крона относятся хроническая диарея (более 6 нед), боль в животе, лихорадка и анемия неясного генеза, кишечная непроходимость, а также перианальные осложнения (хронические анальные трещины, рецидивирующие после хирургического лечения; парапроктит; свищи прямой кишки) (табл. 19.5).
Кроме того, болезнь Крона может сопровождаться различными внекишечными проявлениями [10], схожими с таковыми при язвенном колите, и кишечными осложнениями.
Таблица 19.5. Основные клинико-лабораторные проявления болезни Крона
Таблица 19.6. Внекишечные проявления болезни Крона
|
Аутоиммунные, связанные с активностью заболевания |
Аутоиммунные, не связанные с активностью заболевания |
Обусловленные длительным воспалением и метаболическими нарушениями |
|
• Артропатии (артралгии, артриты). • Поражение кожи (узловатая эритема, гангренозная пиодермия). • Поражение слизистых оболочек (афтозный стоматит). • Поражение глаз (увеит, ирит, иридоциклит, эписклерит) |
• Ревматоидный артрит (серонегативный). • Анкилозирующий спондилоартрит, сакроилеит. • Первичный склерозирующий холангит. • Остеопороз, остеомаляция. • Псориаз |
• Холелитиаз. • Стеатоз печени, стеатогепатит. • Тромбоз периферических вен, тромбоэмболия легочной артерии. • Амилоидоз |
К осложнениям болезни Крона относятся:
n наружные свищи (кишечно-кожные);
n внутренние свищи (межкишечные, кишечно пузырные, ректовагинальные);
n инфильтрат брюшной полости;
n межкишечные или интраабдоминальные абсцессы;
n стриктуры ЖКТ;
n кишечная непроходимость;
n анальные трещины;
n парапроктит (при аноректальном поражении);
n кишечное кровотечение.
УСТАНОВЛЕНИЕ ДИАГНОЗА
Как и в случае язвенного колита, однозначных диагностических критериев болезни Крона не существует, и диагноз выставляется на основании сочетания данных анамнеза, клинической картины и типичных эндоскопических и гистологических изменений [11, 12]. Для подтверждения диагноза необходимы следующие мероприятия:
n подробный опрос пациента со сбором информации о характере начала заболевания, поездках в южные страны, непереносимости пищевых продуктов, приеме лекарственных препаратов (включая антибиотики и нестероидные противовоспалительные средства), о наличии аппендэктомии в анамнезе, курении и семейном анамнезе;
n подробный физикальный осмотр (УД 1b, СР B);
n осмотр перианальной области, пальцевое обследование прямой кишки, ректороманоскопия (УД 5, СР D);
n обзорная рентгенография брюшной полости (при симптомах кишечной непроходимости) (УД 5, СР D);
n тотальная колоноскопия с илеоскопией (УД 5, СР D);
n фиброгастродуоденоскопия (УД 3a, СР C);
n рентгенологическое исследование пассажа бариевой взвеси по тонкой кишке (после исключения признаков непроходимости) (УД 5, СР D);
n биопсия слизистой оболочки кишки в зоне поражения (УД 5, СР D);
n УЗИ органов брюшной полости, забрюшинного пространства, малого таза (УД 5, СР D) [13];
n трансректальное УЗИ прямой кишки и анального канала (при перианальных поражениях) (УД 5, СР D);
n анализ кала для исключения острой кишечной инфекции (при остром начале), исключение паразитарного колита (при остром начале), исследование токсинов А и В Cl. difficile (при недавно проведенном курсе антибиотикотерапии или пребывании в стационаре для исключения псевдомембранозного колита. Для выявления инфекции в 90% случаев требуется минимум 4 образца кала) (УД 2b, СР B [14, 15]);
n исследование крови (общий анализ крови, СОЭ, С-реактивный белок, гемокоагулограмма, биохимический анализ крови, группа крови и резус-фактор) (УД 2b, СР B);
n общий анализ мочи.
Диагноз должен быть подтвержден:
n эндоскопическим и морфологическим методом
и/или
n эндоскопическим и рентгенологическим методом.
При необходимости проводят следующие дополнительные исследования:
n магнитно-резонансную томографию, компьютерную томографию (диагностика свищей, абсцессов, инфильтратов);
n фистулографию (при наличии наружных свищей);
n капсульную эндоскопию (при подозрении на поражение тонкой кишки и при отсутствии стриктур). Следует помнить, что задержка капсулы в кишечнике наблюдается у 13% пациентов [16]. В настоящее время
у больных болезнью Крона до проведения капсульной эндоскопии рекомендуется выполнять рентгенологические исследования (пассаж бария по кишечнику, КТ-энтерография) или МР-энтерографию для оценки наличия стриктур тонкой кишки [17, 18];
n баллонную энтероскопию (при подозрении на поражение тонкой кишки).
Общепринятыми являются критерии достоверного диагноза болезни Крона по Lennard–Jones, включающие определение семи ключевых признаков заболевания [19].
1. Поражение от полости рта до анального канала: хроническое гранулематозное поражение слизистой оболочки губ или щек; пилородуоденальное поражение, поражение тонкой кишки, хроническое перианальное поражение.
2. Прерывистый характер поражения.
3. Трансмуральный характер поражения: язвы-трещины, абсцессы, свищи.
4. Фиброз: стриктуры.
5. Лимфоидная ткань (гистология): афтоидные язвы или трансмуральные лимфоидные скопления.
6. Муцин (гистология): нормальное содержание муцина в зоне активного воспаления слизистой оболочки толстой кишки.
7. Наличие саркоидной гранулемы.
Диагноз болезни Крона считается достоверным при наличии 3 любых признаков или при обнаружении гранулемы в сочетании с любым другим признаком.
Эндоскопическими критериями диагностики болезни Крона являются регионарное (прерывистое) поражение слизистой оболочки, симптом
«булыжной мостовой» (сочетание глубоких, продольно ориентированных язв и поперечно направленных язв c островками отечной гиперемированной слизистой оболочки), линейные язвы (язвы-трещины), афты, а в некоторых случаях стриктуры и устья свищей.
Рентгенологические проявления болезни Крона включают регионарное, прерывистое поражение, стриктуры, «булыжную мостовую», свищи и межкишечные или интраабдоминальные абсцессы.
Морфологическими признаками болезни Крона служат:
n глубокие щелевидные язвы, проникающие в подслизистую основу или мышечный слой;
n саркоидные гранулемы (скопления эпителиоидных гистиоцитов без очагов некроза и гигантских клеток), которые обычно обнаруживаются в стенке резецированного участка и только в 15–36% случаев — при биопсии слизистой оболочки;
n фокальная (дискретная) лимфоплазмоцитарная инфильтрация собственной пластинки слизистой оболочки;
n трансмуральная воспалительная инфильтрация с лимфоидной гиперплазией во всех слоях кишечной стенки;
n поражение подвздошной кишки со структурными изменениями ворсин, мукоидной или псевдопилорической метаплазией крипт и хроническим активным воспалением [20];
n прерывистое поражение — чередование пораженных и здоровых участков кишки (при исследовании резецированного участка кишки).
В отличие от язвенного колита, крипт-абсцессы при болезни Крона формируются редко, а секреция слизи остается нормальной.
ДИФФЕРЕНЦИАЛЬНАЯ ДИАГНОСТИКА
Дифференциальную диагностику [21] болезни Крона проводят с:
n язвенным колитом;
n острыми кишечными инфекциями:
v дизентерией;
v сальмонеллезом;
v кампилобактериозом;
v иерсиниозом;
v амебиазом;
n глистными инвазиями;
n паразитозами;
n антибиотико-ассоциированными поражениями кишечника (Cl. difficile) [22];
n туберкулезом кишечника;
n системным васкулитом;
n неоплазиями толстой и тонкой кишки;
n дивертикулитом;
n аппендицитом;
n эндометриозом;
n солитарной язвой прямой кишки;
n ишемическим колитом;
n актиномикозом;
n лучевыми поражениями кишечника;
n синдромом раздраженного кишечника (СРК).
Лечение
КОНСЕРВАТИВНОЕ ЛЕЧЕНИЕ [23]
Принципы терапии
Лечебные мероприятия при болезни Крона включают назначение лекарственных препаратов, хирургическое лечение, психосоциальную поддержку и диетотерапию [24].
Выбор вида консервативного или хирургического лечения определяется тяжестью атаки, протяженностью и локализацией поражения ЖКТ, наличием внекишечных проявлений и кишечных осложнений (стриктуры, абсцесса, инфильтрата), длительностью анамнеза, эффективностью и безопасностью ранее проводившейся терапии, а также риском развития осложнений болезни Крона [25, 26].
Целями терапии болезни Крона являются индукция ремиссии и ее поддержание без постоянного приема ГКС, профилактика осложнений болезни Крона, предупреждение операции, а при прогрессировании процесса и развитии опасных для жизни осложнений — своевременное назначение хирургического лечения. Поскольку хирургическое лечение не приводит к полному излечению пациентов с болезнью Крона даже при радикальном удалении всех пораженных сегментов кишечника, необходимо проведение противорецидивной терапии, которую следует начать не позднее 2 нед после перенесенного оперативного вмешательства. Лекарственные препараты, назначаемые пациентам с болезнью Крона, условно подразделяются:
n на средства для индукции ремиссии:
v глюкокортикостероиды (ГКС) [системные (преднизолон и метилпреднизолон) и топические (будесонид)];
v биологические препараты: инфликсимаб, адалимумаб и цертолизумаб пэгол, а также антибиотики и 5-аминосалициловая кислота (5-АСК);
n средства для поддержания ремиссии (противорецидивные средства): 5-АСК и ее производные, иммуносупрессоры (азатиоприн, 6-меркаптопурин (6-МП) и метотрексат), инфликсимаб, адалимумаб и цертолизумаб пэгол;
n вспомогательные средства для профилактики осложнений заболевания и нежелательного действия лекарственных препаратов (омепразол, препараты кальция, железа и т.п.).
Следует особо отметить, что ГКС не могут применяться в качестве поддерживающей терапии [28].
Болезнь Крона илеоцекальной локализации (терминальный илеит, илеоколит). Легкая атака
Терапия первой линии заключается в назначении будесонида (9 мг/сут в течение 8 нед, затем снижение по 3 мг в неделю до полной отмены) (УД 2a, СР B [29, 30]). Возможно назначение месалазина (4 г/сут), однако, хотя метаанализ 3 крупных исследований, посвященных эффективности месалазина в дозе 4 г/сут, продемонстрировал статистически значимое превосходство препарата над плацебо, эти различия не имеют существенного значения для клинической практики, поскольку составили всего 18 баллов при оценке по шкале индекса активности болезни Крона [31]. Таким образом, убедительных доказательств применения препаратов 5-АСК в качестве терапии первой линии не получено.
Терапевтический эффект (наличие клинической ремиссии, индекс активности болезни Крона <150) следует оценить через 2–4 нед. При наличии ремиссии на фоне монотерапии месалазином лечение пролонгируется до 8 нед. При индукции ремиссии с помощью будесонида терапия проводится по схеме: прием 9 мг/сут в течение 8 нед, затем снижение по 3 мг в неделю. Поддерживающая терапия проводится месалазином
4 г/сут (УД 5, СР D [32]). При отсутствии терапевтического ответа лечение проводится как при среднетяжелой атаке болезни Крона.
Болезнь Крона илеоцекальной локализации (терминальный илеит, илеоколит). Среднетяжелая атака
Показана терапия ГКС в сочетании с иммуносупрессорами: для индукции ремиссии применяются будесонид (9 мг/сут) (УД 1a, СР A) или пероральные ГКС (преднизолон 1 мг/кг или метилпреднизолон 0,8 мг/кг) (УД 1a, СР A [33]). Решение о применении системных ГКС (а не топического ГКС будесонида) принимается с учетом выраженности системных проявлений болезни Крона. Наличие внекишечных проявлений и/или инфильтрата брюшной полости диктует выбор системных ГКС. Одновременно назначаются иммуносупрессоры: азатиоприн (2 мг/кг), 6-МП (1,5 мг/кг), а при непереносимости тиопуринов — метотрексат (25 мг/нед п/к или в/м). Эффект от терапии ГКС оценивается в течение 1–3 нед. Терапию полной дозой ГКС не следует проводить более 1–3 нед. При достижении клинической ремиссии (индекс активности болезни Крона <150) на фоне продолжения терапии иммуносупрессорами проводится снижение дозы ГКС до полной отмены: преднизолон — снижение по 5–10 мг в неделю, метилпреднизолон — по 4–8 мг в неделю, будесонид прием 9 мг/сут в течение 8 нед, затем снижение по 3 мг в неделю. Суммарная продолжительность терапии ГКС не должна превышать 12 нед [34]. Поддерживающая терапия иммуносупрессорами проводится не менее 4 лет (УД 1a, СР A [35, 36]).
При отсутствии эффекта от кортикостероидов или обострении болезни Крона после отмены/снижения дозы стероидов (гормонозависимая форма) или неэффективности терапии иммуносупрессорами (рецидив через 3–6 мес после отмены кортикостероидов) показаны биологическая терапия (инфликсимаб, адалимумаб или цертолизумаб пэгол) или хирургическое лечение (УД 1b, СР A).
Поддерживающая терапия после достижения ремиссии с помощью биологической терапии проводится инфликсимабом/адалимумабом в комбинации с иммуносупрессорами [40, 41]. Тактика противорецидивной терапии после хирургического лечения описана в разделе «Противорецидивная терапия после хирургического лечения болезни Крона».
Болезнь Крона толстой кишки. Легкая атака
Лечение легкой атаки болезни Крона толстой кишки может эффективно проводиться с помощью перорального сульфасалазина в дозе 4 г или перорального месалазина 4 г (УД 1b, СР A). Оценка терапевтического эффекта выполняется через 2–4 нед. При достижении клинической ремиссии (индекс активности болезни Крона <150) поддерживающая терапия проводится также сульфасалазином или месалазином 4 г (не менее 4 лет) [42]. При отсутствии терапевтического ответа лечение проводится как при среднетяжелой атаке болезни Крона (УД 1a, СР B).
Болезнь Крона толстой кишки. Среднетяжелая атака
Показана терапия системными ГКС в сочетании с иммуносупрессорами: для индукции ремиссии применяются преднизолон 1 мг/кг или метилпреднизолон 0,8 мг/кг (УД 1a, СР A [43]). Одновременно назначаются иммуносупрессоры: азатиоприн (2 мг/кг), 6-МП (1,5 мг/кг), а при непереносимости тиопуринов — метотрексат (25 мг/нед п/к или в/м). Эффект от терапии ГКС оценивается в течение 1–3 нед. Терапию полной дозой ГКС не следует проводить более 1–3 нед. При достижении клинической ремиссии (индекс активности болезни Крона <150) на фоне продолжения терапии иммуносупрессорами проводится снижение дозы ГКС до полной отмены: преднизолон — снижение по 5–10 мг в неделю, метилпреднизолон — по 4–8 мг в неделю. Суммарная продолжительность терапии ГКС не должна превышать 12 нед [44]. Поддерживающая терапия иммуносупрессорами проводится не менее 4 лет (УД a, СР A [45]).
При отсутствии эффекта от кортикостероидов или обострении болезни Крона после отмены/снижения дозы стероидов (гормонозависимая форма) или неэффективности терапии иммуносупрессорами (рецидив через 3–6 мес после отмены кортикостероидов) показана биологическая терапия (инфликсимаб, адалимумаб или цертолизумаб [46, 47]) или хирургическое лечение (УД 1b, СР A [48, 49]).
Поддерживающая терапия после достижения ремиссии с помощью биологической терапии проводится инфликсимабом/адалимумабом/ цертолизумабом в комбинации с иммуносупрессорами [50, 51]. Тактика противорецидивной терапии после хирургического лечения описана в разделе «Противорецидивная терапия после хирургического лечения болезни Крона».
Тяжелая атака болезни Крона (любая локализация)
Тяжелая атака болезни Крона требует проведения интенсивной противовоспалительной терапии системными ГКС.
n Внутривенное введение ГКС: преднизолон 2 мг/кг в сутки (например, по 25 мг 4 раза в сутки) в течение 7–10 дней с последующим переходом на пероральный прием ГКС (преднизолон 1 мг на 1 кг массы тела или метилпреднизолон 0,8 мг/кг). В первые 5–7 дней целесообразно комбинировать пероральные ГКС с дополнительным в/в введением преднизолона по 50 мг/сут.
n Назначение иммуносупрессоров: азатиоприн (2–2,5 мг/кг), 6-МП (1,5 мг/кг), а при непереносимости тиопуринов — метотрексат (25 мг/нед п/к или в/м).
n Антибактериальная терапия (УД 5, СР D):
v 1-я линия — метронидазол 1,5 г/сут + фторхинолоны (ципрофлоксацин, офлоксацин) в/в 10–14 дней;
v 2-я линия — цефалоспорины в/в 7–10 дней [52, 53].
Данные, полученные при проведении систематических обзоров и метаанализов, диктуют необходимость дальнейших исследований для оцен-
ки целесообразности применения антибиотиков в лечении болезни Крона [54].
n Инфузионная терапия: коррекция белково-электролитных нарушений, дезинтоксикация.
n Коррекция анемии (гемотрансфузии при анемии ниже 80 г/л, далее — терапия препаратами железа, предпочтительно парентерально).
n Энтеральное питание у истощенных пациентов.
При достижении клинической ремиссии дальнейшее лечение (поддерживающая терапия иммуносупрессорами/биологическая терапия, снижение дозы пероральных ГКС) проводится так же, как и при среднетяжелой атаке. При отсутствии эффекта от 7–10-дневной терапии в/в ГКС показаны проведение биологической терапии (адалимумаб/ инфликсимаб/цертолизумаб пэгол) или хирургическое лечение.
Болезнь Крона с перианальными поражениями
Перианальные проявления при болезни Крона часто требуют хирургического лечения, поэтому рассматриваются в разделе «Хирургическое лечение перианальной болезни Крона».
Болезнь Крона тонкой кишки (кроме терминального илеита)
При легкой атаке показано назначение месалазина 4 г/сут, прием которого в этой же дозе продолжается и в качестве поддерживающей терапии не менее 2 лет (УД 2b, СР B). Следует отдавать предпочтение препаратам с оболочкой, обеспечивающей создание достаточной концентрации месалазина в зоне поражения (оболочка из этилцеллюлозы).
Среднетяжелая атака требует проведения системной гормональной терапии в сочетании с иммуносупрессорами: назначаются преднизолон 1 мг/кг или метилпреднизолон 0,8 мг/кг (УД 1a, СР A) в комбинации с иммуносупрессорами: азатиоприн (2,0–2,5 мг/кг), 6-МП (1,5 мг/кг), а при непереносимости тиопуринов — метотрексат (25 мг/нед п/к или в/м). При наличии инфильтрата брюшной полости назначаются антибиотики: метронидазол в/в + фторхинолоны (преимущественно) парентерально 10–14 дней (УД 1a, СР A [55]). При необходимости назначают нутритивную поддержку (энтеральное питание).
При достижении ремиссии поддерживающая терапия проводится иммуносупрессорами в течение не менее чем 4 лет [56]. Неэффективность терапии ГКС или развитие гормональной зависимости является показанием к назначению биологической терапии: инфликсимаба/адалимумаба или цертолизумаба пэгол. Лечение тяжелой атаки описано в разделе «Тяжелая атака болезни Крона (любая локализация)», но обязательным дополнением является нутритивная поддержка (энтеральное питание) [57].
Отдельные аспекты терапии
При проведении гормональной терапии постепенное снижение дозы стероидов до полной отмены строго обязательно. Суммарная продолжи-
тельность гормональной терапии не должна превышать 12 нед. В период терапии ГКС показан сопутствующий прием препаратов кальция, витамина D (профилактика остеопороза), ингибиторов протонной помпы, контроль уровня глюкозы в крови.
При назначении иммуносупрессоров (азатиоприн, 6-МП, метотрексат) следует помнить, что их действие, обусловленное терапевтической концентрацией препарата в организме, развивается в среднем в течение 3 мес для тиопуринов и 1 мес для метотрексата [58]. В период терапии рекомендуется ежемесячный контроль уровня лейкоцитов.
Перед проведением биологической (антицитокиновой) терапии обязательным являются консультация врача-фтизиатра и скрининг на туберкулез (квантифероновый тест, а при невозможности проведения — проба Манту, диаскин-тест). Строгое соблюдение доз и графика введения [59] является обязательным. Нерегулярное введение биологических препаратов повышает риск аллергических реакций и неэффективности лечения.
Терапия инфликсимабом (ремикейд♠) проводится в стартовой дозе 5 мг/кг и включает индукционный курс из трех инфузий по схеме
«0–2–6», т.е. со вторым введением препарата через 2 нед и третьим введением через 6 нед после первой инфузии. Инфузии в рамках дальнейшей поддерживающей терапии проводятся каждые 8 нед. У некоторых пациентов могут потребоваться увеличение дозы до 10 мг/кг и сокращение срока введения до 6 нед для достижения эффекта.
Индукционный курс адалимумаба (хумир♠) включает подкожные введения в дозе 160 мг, а затем в дозе 80 мг через 2 нед. Дальнейшие введения (в рамках поддерживающей терапии) выполняются с 4 нед от начала лечения по 40 мг подкожно каждые 2 нед.
Схема применения цертолизумаба пэгол (симзия) включает введение препарата в дозе 400 мг на неделях 0, 2 и 6 и далее каждые 4 недели.
Биологическую (антицитокиновую) терапию для большей эффективности необходимо сочетать с иммуносупрессивной (азатиоприн) терапией [60]. Проведение хирургического вмешательства на фоне терапии иммуносупрессорами и биологическими препаратами, как правило, не требует изменения противорецидивной терапии.
Профилактика оппортунистических инфекций [61]
К факторам риска развития оппортунистических инфекций относятся:
n прием лекарственных средств: азатиоприн, внутривенная гормональная терапия 2 мг/кг или перорально более 20 мг в день в течение более 2 нед, биологическая терапия;
n возраст старше 50 лет;
n сопутствующие заболевания: хронические заболевания легких, алкоголизм, органические заболевания головного мозга, сахарный диабет.
В соответствии с Европейским консенсусом по профилактике, диагностике и лечению оппортунистических инфекций при ВЗК такие
пациенты подлежат обязательной вакцинопрофилактике. Необходимым минимумом вакцинопрофилактики является:
n рекомбинантная вакцина против HBV;
n поливалентная инактивированная пневмококковая вакцина;
n трехвалентная инактивированная вакцина против вируса гриппа.
Для женщин до 26 лет при отсутствии вируса на момент скрининга рекомендуется вакцинация от вируса папилломы человека.
ХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕ
Большинство пациентов с болезнью Крона в течение жизни переносят хотя бы одно оперативное вмешательство на ЖКТ. Невозможность радикального излечения пациентов с болезнью Крона нередко приводит к повторным резекциям, увеличивая риск синдрома короткой кишки. Современная тактика хирургического лечения болезни Крона направлена на выполнение ограниченных резекций, а при возможности — проведение органосохраняющих вмешательств (стриктуропластика, дилатация стриктур) [62].
Показания к хирургическому лечению
Показаниями к оперативному вмешательству при болезни Крона служат острые и хронические осложнения, а также неэффективность консервативной терапии и задержка физического развития [63].
Острые осложнения болезни Крона включают кишечное кровотечение, перфорацию кишки и токсическую дилатацию ободочной кишки.
При кишечном кровотечении экстренное хирургическое вмешательство показано при невозможности стабилизировать гемодинамику пациента, несмотря на переливания эритроцитарной массы и проведение интенсивной гемостатической терапии [64]. Кишечное кровотечение констатируют при потере более 100 мл крови в сутки по данным объективных лабораторных методов (сцинтиграфия, определение гемоглобина в каловых массах гемоглобинцианидным методом) или при объеме каловых масс с визуально определяемой примесью крови более 800 мл/сут. В подобных случаях выполняется резекция пораженного участка кишечника (с наложением анастомоза или без такового) с обязательной интраоперационной энтероили колоноскопией [65].
Перфорация тонкой кишки в свободную брюшную полость является достаточно редким осложнением и обычно возникает либо дистальнее, либо проксимальнее участка кишки с наличием стриктуры. При выявлении угрожающих симптомов (перитонеальные симптомы, свободный газ в брюшной полости по данным обзорной рентгенографии) показано экстренное хирургическое вмешательство, которое в подобной ситуации может быть ограничено резекцией пораженного отдела с формированием анастомоза или стомы [66]. В случае экстренной операции следует избегать формирования первичного анастомоза без протекции с помощью двуствольной илеостомы.
Перфорация толстой кишки при болезни Крона встречается крайне редко. Операцией выбора является субтотальная резекция ободочной кишки с формированием илеостомы.
Токсическая дилатация ободочной кишки — редкое осложнение при БК, представляет собой не связанное с обструкцией расширение ободочной кишки до 6 см и более с явлениями интоксикации. К факторам риска токсической дилатации относятся гипокалиемия, гипомагниемия, подготовка кишки к колоноскопии с помощью осмотических слабительных и прием антидиарейных препаратов. О развитии токсической дилатации свидетельствуют внезапное сокращение частоты стула на фоне имевшейся диареи, вздутие живота, а также внезапное уменьшение или исчезновение болевого синдрома и нарастание симптомов интоксикации (нарастание тахикардии, снижение АД). Операцией выбора является субтотальная резекция ободочной кишки с одноствольной илеостомией.
Хронические осложнения включают стриктуры, инфильтрат брюшной полости, внутренние или наружные кишечные свищи и наличие неоплазии [68].
Неэффективность консервативной терапии и задержка физического развития. О неэффективности консервативной терапии свидетельствует наличие гормональной зависимости и резистентности (см. раздел
«Классификация»). Проявлением неадекватной лекарственной терапии считается также задержка физического развития, чаще всего возникающая при поражении верхних отделов ЖКТ.
Хирургическое лечение болезни Крона тонкой кишки и илеоцекальной зоны
Подобная локализация имеется приблизительно у 1/3 всех пациентов с болезнью Крона и часто осложняется формированием стриктуры подвздошной кишки или илеоцекального клапана. Операцией выбора является резекция илеоцекального отдела с формированием илеоасцендоанастомоза [69, 70].
При выявлении стриктуры после первого курса консервативного лечения (т.е. применения ГКС) в качестве первого этапа лечения показана резекция пораженного участка кишки, а не повторный курс консервативной (гормональной) терапии.
При наличии активной болезни Крона с формированием абсцесса брюшной полости требуется назначение антибиотиков, а также дренирование абсцесса или резекции пораженного участка. Дренирование может осуществляться хирургическим путем или в специализированных центрах и при наличии достаточной квалификации путем чрескожного дренирования. Последний вариант может применяться только при отсутствии стриктуры пораженного участка, что определяет необходимость резекции пораженного отдела.
При наличии непротяженных стриктур тощей или подвздошной кишки, включая стриктуры анастомоза после предшествовавшей резекции, альтернативой резекции становится выполнение стриктуропластики, позволяющей избежать обширных резекций тонкой кишки. Выполнение данного вмешательства возможно при длине стриктуры не более 10 см. Противопоказаниями к стриктуропластике служат наличие инфильтрата, абсцесса, злокачественных образований в стенке кишки или активное кровотечение и выраженное воспаление пораженного участка.
При отсутствии инфильтрата и абсцесса предпочтительно выполнение хирургического вмешательства на тонкой кишке и илеоцекальной зоне лапароскопическим способом [71, 72]. Одномоментное формирование двух анастомозов не приводит к увеличению частоты послеоперационных осложнений и частоты рецидива заболевания [73]. Предпочтительной методикой формирования анастомоза на тонкой кишке является наложение аппаратного анастомоза по типу «бок в бок», что уменьшает вероятность его несостоятельности [74] и последующего развития стриктуры.
Хирургическое лечение болезни Крона толстой кишки
Ограниченное поражение толстой кишки при болезни Крона (менее трети толстой кишки) не требует колэктомии. В этом случае можно ограничиться резекцией пораженного сегмента с формированием кишечного анастомоза в пределах здоровых тканей [75, 76]. При наличии поражения в восходящем отделе ободочной кишки проксимальная граница резекции должна располагаться на уровне средних ободочных сосудов с сохранением последних. Правосторонняя гемиколэктомия показана при выявлении необратимых воспалительных процессов в восходящей и/ или поперечной ободочной кишке. В этой ситуации также возможно выполнение расширенной правосторонней гемиколэктомии. При левостороннем поражении выполняется резекция левых отделов с формированием колоректального анастомоза, а при вовлечении в воспалительный процесс также и поперечной ободочной кишки возможно формирование асцендоректального анастомоза.
При протяженной болезни Крона толстой кишки с тяжелыми клиническим проявлениями операцией выбора служит субтотальная резекция ободочной кишки с наложением одноствольной илеостомы. Дистальную часть толстой кишки возможно не резецировать при условии отсутствия в ней выраженного воспаления и вывести на переднюю брюшную стенку в виде одноствольной сигмостомы либо погрузить ушитый конец под тазовую брюшину.
Альтернативная операция — колопроктэктомия с формированием концевой одноствольной илеостомы. Данное вмешательство выполняется только у пациентов с выраженной активностью воспалительного процесса в прямой кишке или тяжелыми перианальными проявлениями,
поскольку делает невозможным дальнейшее восстановление анальной дефекации. При этом по возможности следует избегать брюшно-промежностной экстирпации в связи с крайне низкими репарационными возможностями и риском формирования обширных промежностных ран, которые в дальнейшем длительно заживают вторичным натяжением, что делает больных инвалидами и ограничивает их социальную активность.
При отсутствии тяжелых клинических проявлений у пациентов с тотальным поражением толстой кишки при минимальной активности воспалительных изменений в прямой кишке, адекватной функции держания кишечного содержимого и отсутствии перианальных поражений
операцией выбора является колэктомия с формированием илеоректального анастомоза [77].
Возможность формирования илеоанального резервуарного анастомоза
при болезни Крона толстой кишки считается спорной в связи с высокой частотой осложнений и частым возникновением показаний к удалению резервуара. В то же время средняя продолжительность жизни пациентов после формирования илеоанального резервуарного анастомоза без постоянной илеостомы достигает 10 лет, что имеет значение для молодых работоспособных пациентов [78]. Основные проблемы, угрожающие пациенту с илеоанальным резервуарным анастомозом на фоне болезни Крона, — это развитие перианальных поражений и болезни Крона тонкокишечного резервуара.
Операция «отключения» транзита кишечного содержимого по толстой
кишке путем формирования двуствольной илеостомы или колостомы показана только крайне истощенным пациентам и беременным. Данный вид хирургического лечения является временным. Учитывая, что при язвенном колите отключение пассажа по толстой кишки неэффективно, необходимо проведение точной дифференциальной диагностики между болезнью Крона толстой кишки и язвенным колитом.
Все перечисленные хирургические вмешательства возможно безопасно выполнить с использованием лапароскопических технологий [79].
При выявлении непротяженной стриктуры толстой кишки возможно выполнение эндоскопической дилатации [80], однако данная манипуляция связана с более высоким риском рецидива заболевания по сравнению с резекцией пораженного участка кишечника [81, 82]. Выполнение стриктуропластики при стриктурах толстой кишки не рекомендуется.
Хирургическое лечение болезни Крона с поражением верхних отделов желудочно-кишечного тракта
Вовлечение в воспалительный процесс участка кишечника проксимальнее терминального отдела подвздошной кишки часто приводит к формированию множественных стриктур и межкишечных свищей, что обусловливает неблагоприятный прогноз болезни Крона. В качестве
хирургического лечения возможны формирование обходного анастомоза, стриктуропластика и резекция пораженного участка. Прибегать к формированию обходного тонкокишечного анастомоза следует лишь в исключительных случаях из-за высокого риска развития синдрома избыточного бактериального роста в отключенной части тонкой кишки и малигнизации. Обширные резекции способствуют формированию синдрома короткой тонкой кишки [83]. При наличии единичных или множественных непротяженных стриктур операцией выбора может быть стриктуропластика в различных вариантах. Стриктуры гастродуоденальной зоны (как правило, двенадцатиперстной кишки) поддаются баллонной дилатации. Также эффективным является выполнение стриктуропластики.
Лечение болезни Крона с перианальными поражениями [85]
Перианальные проявления развиваются у 26–54% больных, страдающих болезнью Крона [86, 87], и чаще встречаются при поражении толстой кишки. Наиболее точными методами диагностики являются МРТ малого таза, местный осмотр под обезболиванием и в условиях специализированного центра УЗИ ректальным датчиком. Фистулография обладает меньшей точностью при диагностике перианальных свищей, чем МРТ.
Цель обследования при перианальных проявлениях болезни Крона — в первую очередь исключение острого гнойного процесса в параректальной области, требующего срочного хирургического лечения.
Подход к хирургическому вмешательству на перианальной области должен быть индивидуален для каждого пациента [88, 89].
Перианальные проявления при болезни Крона исключают возможность применения салицилатов для поддержания ремиссии и требуют назначения иммуносупрессоров (азатиоприн, 6-МП, метотрексат) и/или биологических препаратов (инфликсимаб, адалимумаб, цертолизумаб пэгол) в стандартных дозах.
Перианальные проявления болезни Крона также требуют назначения метронидазола 0,75 г/сут и/или ципрофлоксацина 1 г/сут [90]. Антибиотики назначаются длительно (до 6 мес или до появления побочных эффектов). Местное применение стероидных препаратов и аминосалицилатов при параректальных свищах неэффективно. Эффективно подключение к терапии препаратов метронидазола в виде свечей и мазей.
При наличии трещин анального канала хирургическое вмешательство не рекомендуется, а отдается предпочтение описанной выше консервативной терапии.
Простые свищи, не сопровождающиеся какими-либо симптомами, не требуют хирургического вмешательства. Показано динамическое наблюдение на фоне описанной выше консервативной терапии. При наличии симптомов возможны ликвидация свища с помощью фистулотомии
[91] или его адекватное дренирование с помощью установки латексных
дренажей-сетонов. Показанием к установке сетонов в большинстве случаев является вовлечение части сфинктера в свищевой ход. При отсутствии воспаления слизистой оболочки прямой кишки возможно выполнение низведения слизисто-мышечного лоскута прямой кишки с пластикой внутреннего свищевого отверстия [92].
Лечение сложных свищей включает установку латексных дренажейсетонов в комбинации с агрессивной медикаментозной терапией. Учитывая высокую эффективность биологической терапии при надлежащем дренировании сложных свищей оправдано раннее назначение инфликсимаба или адалимумаба или цертолизумаба пэгол. Тем не менее сложные перианальные свищи, с высокой частотой приводящие к развитию гнойных осложнений, часто служат показанием к отключению пассажа по толстой кишке путем формирования двуствольной илеостомы.
Ректовагинальные свищи в большинстве случаев требуют хирургиче-
ского вмешательства. Лишь в отдельных ситуациях при наличии низкого свища между прямой кишкой и преддверием влагалища возможно проведение только консервативного лечения. В остальных случаях показано оперативное лечение под прикрытием илеостомы. При наличии активного поражения прямой кишки адекватная противовоспалительная терапия до операции увеличивает эффективность вмешательства.
Наиболее неблагоприятным фактором, повышающим вероятность постоянной илеостомы или колостомы, является наличие стриктуры нижнеампулярного отдела прямой кишки или стеноза анального канала. В большинстве случаев данные осложнения требуют выполнения проктэктомии или брюшно-промежностной экстирпации прямой кишки. В отдельных ситуациях, при отсутствии активного воспаления в лежащих выше отделах кишечника, возможно бужирование стриктуры.
Противорецидивная терапия после хирургического лечения болезни Крона
Даже при полном удалении всех макроскопически измененных отделов кишечника хирургическое вмешательство не приводит к полному исцелению: в течение 5 лет клинически значимый рецидив отмечается у 28–45% пациентов, а в течение 10 лет — у 36–61%, что диктует необходимость продолжения противорецидивной терапии после операции по поводу болезни Крона [93, 94]. К факторам, достоверно повышающим риск послеоперационного рецидива, относятся курение, две и более резекции кишки в анамнезе, протяженные резекции тонкой кишки в анамнезе (>50 см), перианальные поражения, пенетрирующий фенотип [95].
В зависимости от сочетания факторов риска, а также от эффективности ранее проводившейся противорецидивной терапии пациенты после операции должны быть стратифицированы на группы с различным риском послеоперационного рецидива. В группе низкого риска рецидива болезни Крона целесообразно назначение месалазина
(4 г) или сульфасалазина (4 г). Пациенты из группы промежуточного риска являются кандидатами на проведение терапии азатиоприном (2,5 мг/кг в сутки) или 6-МП (1,5 мг/кг в сутки) [96]. Пациентам с высоким риском рецидива целесообразно еще до проведения контрольного эндоскопического исследования начать курс биологической терапии анти-ФНО-препаратами (инфликсимаб, адалимумаб, цертолизумаб пегол) [97].
Противорецидивную терапию рекомендуется начинать через 2 нед после оперативного вмешательства. Спустя 6–12 мес всем оперированным пациентам с болезнью Крона показано проведение контрольного обследования, в первую очередь эндоскопического. При невозможности визуализировать зону анастомоза следует констатировать наличие или отсутствие рецидива, основываясь на сочетании данных рентгенологического обследования (как правило, КТ) и неинвазивных маркеров воспаления — С-реактивного белка, фекального кальпротектина и др.
При отсутствии признаков воспаления или обнаружении минимальных (i1 по шкале Rutgeerts) (табл. 19.7) воспалительных изменений проводимая терапия должна быть продолжена. Наличие более выраженных воспалительных изменений (i2–i4) указывает на неэффективность проводимой терапии и должно служить показанием к усилению терапии: подключению иммуносупрессоров у пациентов, ранее их не получавших, или к проведению биологической терапии адалимумабом [99], инфликсимабом [100] или церотлизумабом пэгол у пациентов, находящихся на поддерживающей терапии азатиоприном/6-МП. В дальнейшем вне зависимости от характера течения заболевания и клинической манифестации болезни Крона следует не реже 1 раза в 1–3 года выполнять контрольное эндоскопическое исследование, следуя этому же алгоритму выбора противорецидивного средства (рис. 19.1) [101].
Таблица 19.7. Шкала эндоскопической активности послеоперационного рецидива болезни Крона по Rutgeerts [98]
|
Оценка |
Определение |
|
i0 |
Нет признаков воспаления |
|
i1 |
≤5 афтозных язв |
|
i2 |
>5 афтозных язв с нормальной слизистой оболочкой между ними, или протяженные участки здоровой слизистой оболочки между более выраженными изъязвлениями, или поражения, ограниченные подвздошно-толстокишечным анастомозом |
|
i3 |
Диффузный афтозный илеит с диффузно воспаленной слизистой оболочкой |
|
i4 |
Диффузное воспаление с крупными язвами, «булыжной мостовой» и/или сужением просвета |
|
Оценка риска послеоперационного рецидива болезни Крона Курение Пенетрирующий фенотип Перианальные поражения Две и более резекции кишки в анамнезе Резекция протяженного сегмента тонкой кишки в анамнезе (>50 см) | ||
|
¯ |
¯ |
¯ |
|
Низкий риск |
Высокий риск |
Средний риск |
|
¯ |
¯ |
|
|
Месалазин или воздержаться от терапии |
АЗА или 6-МП в сочетании с метронидазолом |
Инфликсимаб / Адалимумаб |
|
¯ |
¯ |
¯ |
|
Контрольное эндоскопическое обследование через 6–12 мес | ||
|
¯ |
|
¯ |
|
Нет рецидива ® Колоноскопия через 1–3 года |
Нет рецидива ® Колоноскопия через 1–3 года |
Нет рецидива ® Колоноскопия через 1–3 года |
|
Рецидив ®азатиоприн/ 6-МП или инфликсимаб/ адалимумаб |
Рецидив ®азатиоприн/ 6-МП или инфликсимаб/ адалимумаб |
Рецидив ® смена биологического препарата или оптимизация дозы инфликсимаба/адалимумаба |
Рис. 19.1. Алгоритм профилактики послеоперационного рецидива болезни Крона
Прогноз
Болезнь Крона характеризуется прогрессирующим поражением кишечника. На момент установления диагноза осложнения (стриктуры, свищи) обнаруживаются лишь у 10–20% больных, в то время как в течение 10 лет подобные осложнения развиваются у >90% пациентов. В течение 10 лет хирургическое вмешательство в связи с осложнениями и/или неэффективностью консервативной терапии выполняется у половины пациентов с болезнью Крона, а у 35–60% в течение 10 лет после операции развивается рецидив заболевания. Гормональная зависимость при болезни Крона в течение 10 лет хотя бы раз констатируют у 30% больных [102]. Прогностически неблагоприятными факторами при болезни Крона являются курение, дебют заболевания в детском возрасте, перианальные поражения, пенетрирующий фенотип заболевания и распространенное
поражение тонкой кишки.
Критерии оценки качества помощи в стационаре представлены в таблице 19.8. Для оценки качества медицинской помощи используют временные, процессуальные и профилактирующие критерии. Временные характеризуют своевременность оказания определенных этапов
медицинской помощи. Выполнение пациенту ряда медицинских манипуляций, инструментальных и лабораторных исследований, необходимых для качественного оказания медицинской помощи, оценивают в процессуальных критериях. Для анализа мероприятий, направленных на предотвращение развития осложнений, используют профилактирующие критерии.
Таблица 19.8. Критерии оценки качества медицинской помощи в стационаре больным воспалительными заболеваниями кишечника (0 — нет, 1 — да)
|
Клинические рекомендации |
Временные |
Процессуальные |
Профилактирующие |
|
Клинические рекомендации по диагностике и лечению взрослых пациентов с болезнью Крона (код МКБ — К50) |
Установка клинического диагноза в течение 72 ч: 0/1 |
Пальцевое обследование прямой кишки: 0/1. Илеоколоноскопия в течение госпитализации или в течение 6 мес до госпитализации: 0/1. Исследование пассажа бариевой взвеси по кишечнику: 0/1. УЗИ кишечника: 0/1. Определение группы крови: 0/1. Исследование крови на сифилис, вирусный гепатит В, вирусный гепатит С: 0/1. Клинический анализ крови; биохимический анализ крови; клинический анализ мочи; коагулограмма: 0/1. Метод консервативного лечения в соответствии с установленным диагнозом и клиническими рекомендациями: 0/1. Метод оперативного лечения при неэффективности консервативной терапии в соответствии с клиническими рекомендациями: 0/1. Метод анестезии в соответствии с объемом оперативного лечения: 0/1 |
Отсутствие осложнений: • пневмония: 0/1; • тромбоэмболия: 0/1; • гипергликемическая кома: 0/1; • летальный исход: 0/1 |
Литература
1. Гастроэнтерология: Национальное руководство / Под ред. В.Т. Ивашкина, Т.Л. Лапиной. — ГЭОТАР-Медиа, 2008. — 754 c.
2. Assche G.Van, Dignass A., Panes J. et al. The second European evidence-based consensus on the diagnosis and management of Crohn’s disease: Definitions and diagnosis // J. Crohns Colitis. — 2010. — Vol. 4. — P. 7–27.
3. OCEBM Levels of Evidence Working Group. The Oxford 2011 Levels of Evidence. — Oxford Centre for Evidence-Based Medicine, 2011.
4. Воробьев Г.И., Халиф И.Л. Неспецифические воспалительные заболевания кишечника. — М.: Миклош, 2008.
5. Sandborn W.J., Feagan B.G., Hanauer S.B. et al. A review of activity indices and efficacy endpoints for clinical trials of medical therapy in adults with Crohn’s disease // Gastroenterology. — 2002. — Vol. 122. — P. 512–530.
6. Silverberg M.S., Satsangi J., Ahmad T. et al. Toward an integrated clinical, molecular and serological classification of inflammatory bowel disease: Report of a Working Party of the 2005 Montreal World Congress of Gastroenterology // Can.
J. Gastroenterol. — 2005. — Vol. 19. — Suppl. A. — P. 5–36.
7. Cosnes J., Cattan S., Blain A. et al. Long-term evolution of disease behavior of Crohn’s disease // Inflamm. Bowel Dis. — 2002. — Vol. 8. — P. 244–250.
8. Белоусова Е.А. Рекомендации по диагностике и лечению болезни Крона // Фарматека. — 2009. — № 13. — С. 38–44.
9. Best W.R., Becktel J.M., Singleton J.W., Kern F.Jr. Development of a Crohn’s disease activity index. National Cooperative Crohn’s Disease Study // Gastroenterology. — 1976. — Vol. 70, N 3. — P. 439–444.
10. Григорьева Г.А., Мешалкина Н.Ю. О проблеме системных проявлений воспалительных заболеваний кишечника // Фарматека. — 2011. — № 15. — С. 44–49.
11. Horsthuis K., Bipat S., Bennink R.J., Stoker J. Inflammatory bowel disease diagnosed with US, MR, scintigraphy, and CT: metaanalysis of prospective studies // Radiology. — 2008. — Vol. 247, N 1. — P. 64–79.
12. Чашкова Е.Ю., Владимирова А.А., Неустроев В.Г. и др. Воспалительные заболевания толстой кишки — аспекты диагностики // Бюл. Вост.-Сибир. науч. центра СО РАМН. — 2011. — № 4–2. — С. 209–221.
13. Воробьев Г.И., Орлова Л.П., Самсонова Т.В. и др. Возможности ультразвукового исследования в диагностике болезни крона // Ультразвук. и функциональная диагностика. — 2010. — № 1. — С. 29–36.
14. Issa M., Ananthakrishnan A.N., Binion D.G. Clostridium difficile and inflammatory bowel disease // Inflamm. Bowel Dis. — 2008. — Vol. 14. — P. 1432– 1442.
15. Nguyen G.C., Kaplan G.G., Harris M.L. et al. A national survey of the prevalence and impact of Clostridium difficile infection among hospitalized inflammatory bowel disease patients // Am. J. Gastroenterol. — 2008. — Vol. 103. — P. 1443–1450.
16. Cheifetz A.S., Kornbluth A.A., Legnani P. et al. the risk of retention of the capsule endoscope in patients with known or suspected Crohn’s disease // Am. J. Gastroenterol. — 2006. — Vol. 101. — P. 2218–2222.
17. Spada C., Riccioni M.E., Costamagna G. Patients with known small bowel stricture or with symptoms of small bowel obstruction secondary to Crohn’s disease should not perform video capsule endoscopy without previously tested for small bowel patency // Am. J. Gastroenterol. — 2007. — Vol. 102. — P. 1542–1543.
18. Spada C., Shah S.K., Riccioni M.E. et al. Video capsule endoscopy in patients with known or suspected small bowel stricture previously tested with the dissolving patency capsule // J. Clin. Gastroenterol. — 2007. — Vol. 42. — P. 576–582.
19. Lennard-Jones J.E. Classification of inflammatory bowel disease // Scand. J. Gastroenterol. Suppl. — 1989. — Vol. 170. — P. 2–6.
20. Тертычный А.С., Андреев А.И., Гебоэс К. Современные подходы к морфологической диагностике воспалительных заболеваний кишечника на материале эндоскопических биопсий // Арх. пат. — 2011. — Т. 73, № 1. — P. 40–47.
21. American Gastroenterological Association medical position statement: guidelines for the evaluation and management of chronic diarrhea // Gastroenterology. — 1999. — Vol. 116, N 6. — P. 1461–1463.
22. Корнеева О.И., Ивашкин В.Т. Антибиотикоассоциированный колит: патоморфология, клиника, лечение // Рос. журн. гастроэнтерол., гепатол., колопроктол. — 2007. — Т. 17, № 3. — С. 65–71.
23. Голованчикова В.М., Шифрин О.С, Ивашкин В.Т. Современные подходы к лечению хронических воспалительных заболеваний кишечника // Рос. мед. вести. — 2009. — Т. 14, № 3. — С. 29–37.
24. Assche G.Van, Dignass A., Panes J. et al. The second European evidencebased consensus on the diagnosis and management of Crohn’s disease: Current management // J. Crohns Colitis. — 2010. — Vol. 4. — P. 28–58.
25. Carter M.J., Lobo A.J., Travis S.P. IBD Section, British Society of Gastroenterology. Guidelines for the management of inflammatory bowel disease in adults // Gut. — 2004. — Vol. 53. — Suppl. 5. — P. 1–16.
26. Simms L., Steinhart A.H. Budesonide for maintenance of remission in Crohn’s disease // Cochrane Database Syst. Rev. — 2001. — CD002913.
27. Tay G.S., Binion D.G., Eastwood D., Otterson M.F. Multivariate analysis suggests improved perioperative outcome in Crohn’s disease patients receiving immunomodulator therapy after segmental resection and/or strictureplasty // Surgery. — 2003. — Vol. 34. — P. 565–572; discussion 572–397.
28. Steinhart A.H., Ewe K., Griffiths A.M. et al. Corticosteroids for maintaining remission of Crohn’s disease // Cochrane Database Syst. Rev. — 2003. — Is. 4. — CD000301.
29. Otley A.R., Steinhart A.H. Budesonide for induction of remission in Crohn’s disease // Cochrane Database Syst. Rev. — 2008. — Is. 3. — CD000296.
30. Tromm A., Bunganic I., Tomsova E. et al. Double-blind, doubledummy, randomised, multicentre study to compare the efficacy and safety of oral budesonide (9 mg) and oral mesalazine (4.5 g) in moderately active Crohn’s disease patients // Gastroenterology. — 2009. — Vol. 139. — Suppl. 1. — P. 391.
31. Hanauer S.B., Stromberg U. Oral Pentasa in the treatment of active Crohn’s disease: a meta-analysis of double-blind, placebo-controlled trials // Clin. Gastroenterol. Hepatol. — 2004. — Vol. 2. — P. 379–388.
32. Camma C., Giunta M., Rosselli M., Cottone M. Mesalamine in the maintenance treatment of Crohn’s disease: a meta-analysis adjusted for confounding variables // Gastroenterology. — 1997. — Vol. 113. — P. 1465–1473.
33. Benchimol E.I., Seow C.H., Steinhart A.H., Griffiths A.M. Traditional corticosteroids for induction of remission in Crohn’s disease // Cochrane Database Syst. Rev. — 2008. — Is. 2. — CD006792.
34. Ho G.T., Chiam P., Drummond H. et al. The efficacy of corticosteroid therapy in inflammatory bowel disease: analysis of a 5-year UK inception cohort // Aliment. Pharmacol. Ther. — 2006. — Vol. 24. — P. 319–330.
35. Lémann M., Mary J.Y., Duclos B. et al. Infliximab plus azathioprine for steroid-dependent Crohn’s disease patients: a randomized placebo-controlled trial // Gastroenterology. — 2006. — Vol. 130. — P. 1054–1061.
36. Sandborn W., Sutherland L., Pearson D. et al. Azathioprine or 6-mercaptopurine for inducing remission of Crohn’s disease // Cochrane Database Syst. Rev. — 2000. — Is. 2. — CD000545.
37. Sandborn W.J., Feagan B., Radford-Smith G. et al. CDP571, a humanised monoclonal antibody to tumour necrosis factor alpha, for moderate to severe Crohn’s disease: a randomised, double blind, placebo controlled trial // Gut. — 2004. — Vol. 53. — P. 1485–1493.
38. Feagan B., Sandborn W.J., Baker J.P. et al. A randomized, double-blind, placebo-controlled trial of CDP571, a humanized monoclonal antibody to tumour necrosis factor-alpha, in patients with corticosteroid-dependent Crohn’s disease // Aliment. Pharmacol. Ther. — 2005. — Vol. 21. — P. 373–384.
39. D’Haens G., Panaccione R., Gassull M. et al. The London Position Statement of the World Congress of Gastroenterology on biological therapy for IBD with the European Crohn’s and Colitis Organisation: when to start, when to stop and what to do in between? // Am. J. Gastroenterol. — 2010.
40. Pearson D.C., May G.R., Fick G.R., Sutherland L.R. Azathioprine for maintaining remission of Crohn’s disease // Cochrane Database Syst. Rev. — 2000. — Is. 2. — CD000067.
41. Prefontaine E., Sutherland L.R., MacDonald J.K. et al. Azathioprine or 6-mercaptopurine formaintenance of remission in Crohn’s disease // Cochrane Database Syst. Rev. — 2009. — Is. 1. — CD000067.
42. Bresci G., Petrucci A., Banti S. 5-aminosalicylic acid in the prevention of relapses of Crohn’s disease in remission: a long-term study // Int. J. Clin. Pharmacol. Res. — 1991. — Vol. 11. — P. 200–202.
43. Lémann M., Mary J.Y., Duclos B. et al. Infliximab plus azathioprine for steroid-dependent Crohn’s disease patients: a randomized placebo-controlled trial // Gastroenterology. — 2006. — Vol. 130. — P. 1054–1061.
44. Ho G.T., Chiam P., Drummond H. et al. The efficacy of corticosteroid therapy in inflammatory bowel disease: analysis of a 5-year UK inception cohort // Aliment. Pharmacol. Ther. — 2006. — Vol. 24. — P. 319–330.
45. Malchow H., Ewe K., Brandes J.W. et al. European co-operative Crohn’s disease study (ECCDS): results of drug treatment // Gastroenterology. — 1984. — Vol. 86. — P. 249–266.
46. Sandborn W.J., Feagan B., Radford-Smith G. et al. CDP571, a humanised monoclonal antibody to tumour necrosis factor alpha, for moderate to severe Crohn’s disease: a randomised, double blind, placebo controlled trial // Gut. — 2004. — Vol. 53. — P. 1485–1493.
47. Feagan B., Sandborn W.J., Baker J.P. et al. A randomized, double-blind, placebo-controlled trial of CDP571, a humanized monoclonal antibody to tumour necrosis factor-alpha, in patients with corticosteroid-dependent Crohn’s disease // Aliment. Pharmacol. Ther. — 2005. — Vol. 21. — P. 373–384.
48. Colombel J.F., Rutgeerts P., Reinisch W. et al. SONIC: a randomized, double blind, controlled trial comparing infliximab and infliximab plus azathioprine to azathioprine in patients with Crohn’s disease naive to immunomodulators and biologic therapy // Gut. — 2008. — Vol. 57. — Suppl. II. — P. A1.
49. Behm B.W., Bickston S.J. Tumor necrosis factor-alpha antibody for maintenance of remission in Crohn’s disease // Cochrane Database Syst. Rev. — 2009. — Is. 1. — CD006893.
50. Pearson D.C., May G.R., Fick G.R., Sutherland L.R. Azathioprine for maintaining remission of Crohn’s disease // Cochrane Database Syst. Rev. — 2000. — Is. 2. — CD000067.
51. Prefontaine E., Sutherland L.R., MacDonald J.K. et al. Azathioprine or 6-mercaptopurine for maintenance of remission in Crohn’s disease // Cochrane Database Syst. Rev. — 2009. — Is. 1. — CD000067.
52. Khan K.J., Ullman T.A., Ford A.C. et al. Antibiotic therapy in inflammatory bowel disease: a systematic review and meta-analysis // Am. J. Gastroenterol. — 2011. — Vol. 106. — P. 661–673.
53. Ohkusa T., Kato K., Terao S. et al. Newly developed antibiotic combination therapy for ulcerative colitis: a double-blind placebo-controlled multicenter trial // Am. J. Gastroenterol. — 2010. — Vol. 105. — P. 1820–1829.
54. Khan K.J., Ullman T.A., Ford A.C. et al. Antibiotic therapy in inflammatory bowel disease: a systematic review and metaanalysis // Am. J. Gastroenterol. — 2011. — Vol. 106. — P. 661–673.
55. Alfadhli A.A., McDonald J.W., Feagan B.G. Methotrexate for induction of remission in refractory Crohn’s disease (Cochrane Review) // Cochrane Database Syst. Rev. — 2003. — Is. 1. — CD003459.
56. Candy S., Wright J., Gerber M. et al. A controlled double blind study of azathioprine in the management of Crohn’s disease // Gut. — 1995. — Vol. 37. — P. 674–679.
57. D’Haens G., Baert F., van Assche G. et al. Belgian Inflammatory Bowel Disease Research Group; North-Holland Gut Club. Early combined immunosuppression or conventional management in patients with newly diagnosed Crohn’s disease: an open randomized trial // Lancet. — 2008. — Vol. 371. — P. 660–677.
58. Sandborn W.J. Azathioprine: state of the art in inflammatory bowel disease // Gastroenterol. Suppl. — 1998. — Vol. 225. — P. 92–99.
59. Rutgeerts P., Feagan B.G., Lichtenstein G.R. et al. Comparison of scheduled and episodic treatment strategies of infliximab in Crohn’s disease // Gastroenterology. — 2004. — Vol. 126. — P. 402–413.
60. Rahier J.F. et al. European evidence-based Consensus on the prevention, diagnosis and management of opportunistic infections in inflammatory bowel disease // J Crohns. Colitis. — 2009. — Vol. 3, N 2. — P. 47–91.
61. Strong S.A., Koltun W.A., Hyman N.H., Buie W.D. Standards Practice Task Force of the American Society of Colon and Rectal Surgeons. Practice parameters for the surgical management of Crohn’s disease // Dis. Colon Rectum. — 2007. — Vol. 50. — P. 1735–1746.
62. Справочник по колопроктологии / Под ред. Ю.А. Шелыгина, Л.А. Благодарного. — М.: Литтерра, 2012. — C. 460–522.
63. Хачатурова Э.А., Ерошкина Т.Д., Блинова О.В. и др. Коррекция нарушений метаболизма в раннем послеоперационном периоде при тяжелых формах неспецифического язвенного колита и болезни Крона // Рос. журн. гастроэнтерол., гепатол., колопроктол. — 2003. — Т. 8, № 4. — С. 63–68.
64. Korzenik J.R. Massive lower gastrointestinal hemorrhage in Crohn’s disease // Curr. Treat. Options Gastroenterol. — 2000. — Vol. 3. — P. 211–216.
65. Bundred N.J., Dixon J.M., Lumsden A.B. et al. Free perforation in Crohn’s colitis. A ten-year review // Dis. Colon Rectum. — 1985. — Vol. 28. — P. 35–37.
66. Werbin N., Haddad R., Greenberg R. et al. Free perforation in Crohn’s disease // Isr. Med. Assoc. J. — 2003. — Vol. 5. — P. 175–177.
67. Papi C., Festa V., Fagnani C. et al. Evolution of clinical behaviour in Crohn’s disease: predictive factors of penetrating complications // Dig. Liver Dis. — 2005. — Vol. 37. — P. 247–253.
68. Poggioli G., Stocchi L., Laureti S. et al. Conservative surgical management of terminal ileitis: side-to-side enterocolic anastomosis // Dis. Colon Rectum. — 1997. — Vol. 40. — P. 234–237.
69. Melton G.B., Fazio V.W., Kiran R.P. et al. Long-term outcomes with ileal pouch-anal anastomosis and Crohn’s disease: pouch retention and implications of delayed diagnosis // Ann. Surg. — 2008. — Vol. 248. — P. 608–616.
70. Варданян А.В., Кашников В.Н., Болихов К.В., Халиф И.Л. Лапароскопическая илеостомия при болезни Крона // Колопроктология. — 2011. — Т. 37,
№ 3. — С. 20–23.
71. Воробьев Г.И., Болихов К.В., Варданян А.В. Место лапароскопической илеостомии в лечении болезни Крона толстой кишки (обзор литературы) // Колопроктология. — 2009. — Т. 29, № 3. — С. 52–58.
72. Sagar P.M., Dozois R.R., Wolff B.G. Long-term results of ileal pouch-anal anastomosis in patients with Crohn’s disease // Dis. Colon Rectum. — 1996. — Vol. 39. — P. 893–898.
73. Simillis C., Purkayastha S., Yamamoto T. et al. A meta-analysis comparing conventional end-to-end anastomosis vs. other anastomotic configurations after resection in Crohn’s disease // Dis. Colon Rectum. — 2007. — Vol. 50, N 10. — P. 1674–1687.
74. Stocchi L., Milsom J.W., Fazio V.W. Long-term outcomes of laparoscopic versus open ileocolic resection for Crohn’s disease: follow-up of a prospective randomized trial // Surgery. — 2008. — Vol. 144. — P. 622–627.
75. Tekkis P.P., Purkayastha S., Lanitis S. et al. A comparison of segmental vs. subtotal/total colectomy for colonic Crohn’s disease: a meta-analysis // Colorectal Dis. — 2006. — Vol. 8. — P. 82–90.
76. Vorobiev G.I, Bolikhov K.V., Romanov R.I., Vardanyan A.V. Laparoscopic ileostomy as the stage of surgical treatment complicated Crohn’s disease of the colon // Proktologia. — 2008. — Vol. 9. — P. 145.
77. Byrne C.M., Solomon M.J., Young J.M. et al. Patient preferences between surgical and medical treatment in Crohn’s disease // Dis. Colon Rectum. — 2007. — Vol. 50. — P. 586–897.
78. Воробьев Г.И., Михайлова Т.Л., Болихов К.В., Варданян А.В. Эффективность илеостомии в лечении пациентов с тяжелой формой болезни Крона толстой кишки // Материалы научно-практической конференции «Актуальные проблемы гастроэнтерологии» (Василенковские чтения). — М., 2010. — С. 34.
79. Tichansky D., Cagir B., Yoo E. et al. Strictureplasty for Crohn’s disease: metaanalysis // Dis. Colon Rectum. — 2000. — Vol. 43. — P. 911–919.
80. Reese G.E., Purkayastha S., Tilney H.S. et al. Strictureplasty vs resection in small bowel Crohn’s disease: an evaluation of short-term outcomes and recurrence // Colorectal Dis. — 2007. — Vol. 9. — P. 686–694.
81. Yamamoto T., Fazio V.W., Tekkis P.P. Safety and efficacy of strictureplasty for Crohn’s disease: a systematic review and metaanalysis // Dis. Colon Rectum. — 2007. — Vol. 50. — P. 1968–1986.
82. Caprilli R., Gassull M.A., Escher J.C. et al. European evidence based consensus on the diagnosis and management of Crohn’s disease: special situations // Gut. — 2006. — Vol. 5. — Suppl. 1. — P. i36–i58.
83. Dietz D.W., Laureti S., Strong S.A. et al. Safety and longterm efficacy of strictureplasty in 314 patients with obstructing small bowel Crohn’s disease // J. Am. Coll. Surg. — 2001. — Vol. 192. — P. 330–337.
84. Щукина О.Б. Перианальная болезнь Крона: диагностика и медикаментозная терапия // Фарматека. — 2008. — № 13. — С. 22–30.
85. Keighley M.R., Allan R.N. Current status and influence of operation on perianal Crohn’s disease // Int. J. Colorectal Dis. — 1986. — Vol. 1. — P. 104–107.
86. Tang L.Y., Rawsthorne P., Bernstein C.N. Are perineal and luminal fistulas associated in Crohn’s disease? A population-based study // Clin. Gastroenterol. Hepatol. — 2006. — Vol. 4. — P. 1130–1134.
87. Шелыгин Ю.А., Халиф И.Л., Кашников В.Н. и др. Илеостомия в лечении болезни Крона толстой кишки с перианальными поражениями // Колопроктология. — 2011. — Т. 37, № 3. — С. 133.
88. Vardanyan A.V., Khalif I.L., Kashnicov V.N. et al. Ileostomy effectiveness in the treatment of the patients with the severe form of perianal Crohn’s disease // Falk Symposium. — Brussel: Belgium, 2011, Sepr 30–Oct 1. — Vol. 179. — 56 p.
89. Prantera C., Zannoni F., Scribano M.L. et al. An antibiotic regimen for the treatment of active Crohn’s disease: a randomized, controlled clinical trial of metronidazole plus ciprofloxacin // Am. J. Gastroenterol. —1996. — Vol. 91. — P. 328–332.
90. Van Dongen L.M., Lubbers E.J.C. Perianal fistulas in patients with Crohn’s disease // Arch. Surg. — 1986. — Vol. 121. — P. 1187–1190.
91. Yamamoto T., Allan R.N., Keighley M.R. Effect of fecal diversion alone on perianal Crohn’s disease // World J. Surg. — 2000. — Vol. 24. — P. 1258–1262.
92. Rutgeerts P., Geboes K., Vantrappen G. et al. Predictability of the postoperative course of Crohn’s disease // Gastroenterology. — 1990. — Vol. 99. — P. 956–963.
93. Loftus Jr.E.V. Clinical epidemiology of inflammatory bowel disease: Incidence, prevalence, and environmental influences // Gastroenterology. — 2004. — Vol. 126, N 6. — P. 1504–1517.
94. Головенко А.О., Халиф И.Л., Головенко О.В. Профилактика послеоперационных рецидивов болезни Крона // Колопроктология. — 2012. — № 4. — С. 40–48.
95. Peyrin-Biroulet L. et al. Azathioprine and 6-mercaptopurine for the prevention of postoperative recurrence in Crohn’s disease: a meta-analysis // Am. J. Gastroenterol. — 2009. — Vol. 104, N 8. — P. 2089–2096.
96. Regueiro M., Schraut W., Baidoo L. et al. Infliximab prevents Crohn’s disease recurrence after ileal resection // Gastroenterology. — 2009. — Vol. 136. — P. 441–450.
97. Terdiman J.P. Prevention of postoperative recurrence in Crohn’s disease // Clin. Gastroenterol. Hepatol. — 2008. — Vol. 6, N 6. — P. 616–620.
98. Papamichael K. et al. Adalimumab for the prevention and/or treatment of post-operative recurrence of Crohn’s disease: a prospective, two-year, single center, pilot study // J. Crohns Colitis. — 2012. — Vol. 6, N 9. — P. 924–931.
99. Regueiro M. et al. Infliximab prevents Crohn’s disease recurrence after ileal resection // Gastroenterology. — 2009. — Vol. 136, N 2. — P. 441–450 e1; quiz 716.
100. Loly C., Belaiche J., Louis E. Predictors of severe Crohn’s disease // Scand. J. Gastroenterol. — 2008. — Vol. 43. — P. 948–954.
101. Froslie K.F., Jahnsen J., Moum B.A., Vatn M.H. Group I. Mucosal healing in inflammatory bowel disease: results from a Norwegian population-based cohort // Gastroenterology. — 2007. — Vol. 133. — P. 412–422.
ЯЗВЕННЫЙ КОЛИТ
Введение
Воспалительные заболевания кишечника (ВЗК), к которым относятся язвенный колит и болезнь Крона, были и остаются одной из наиболее серьезных проблем в современной гастроэнтерологии. Несмотря на то что по уровню заболеваемости ВЗК значительно уступают другим гастроэнтерологическим заболеваниям, по тяжести течения, частоте осложнений и летальности во всем мире они занимают одно из ведущих мест в структуре болезней желудочно-кишечного тракта (ЖКТ). Постоянный интерес к ВЗК обусловлен прежде всего тем, что, несмотря на многолетнюю историю изучения, их этиология остается неизвестной, а патогенез раскрыт недостаточно [1, 2].
Язвенный колит — хроническое заболевание, которое поражает только толстую кишку и никогда не распространяется на тонкую кишку. Исключение составляет состояние, обозначенное термином «ретроградный илеит», однако это воспаление носит временный характер и не является истинным проявлением язвенного колита.
Распространенность язвенного колита составляет от 21 до 268 случаев на 100 тыс. населения. Ежегодный прирост заболеваемости составляет 5–20 случаев на 100 тыс. населения, и этот показатель продолжает увеличиваться (приблизительно в 6 раз за последние 40 лет) [3].
Социальную значимость язвенного колита определяют преобладание заболевания среди лиц молодого трудоспособного возраста — пик заболеваемости язвенным колитом приходится на 20–30 лет, а также ухудшение качества жизни из-за хронизации процесса, а следовательно, частого стационарного лечения [4].
Настоящие рекомендации по диагностике и лечению больных язвенным колитом являются руководством для практических врачей, осуществляющих ведение и лечение таких пациентов. Рекомендации подлежат регулярному пересмотру в соответствии с новыми данными научных исследований в этой области. Настоящие рекомендации составлены на основании анализа литературы и Европейского доказательного консенсуса по диагностике и лечению язвенного колита, являющегося главенствующим руководством по лечению язвенного колита в странах Европейского союза.
Рекомендации включают следующие разделы: определение и классификация язвенного колита, диагностика, консервативное и хирургическое лечение. Для отдельных положений рекомендаций приведены уровни доказательности согласно общепринятой классификации Оксфордского центра доказательной медицины (табл. 20.1).
Таблица 20.1. Уровни доказательности и степени рекомендаций на основании руководства Оксфордского центра доказательной медицины [5]
|
Уровень |
Диагностическое исследование |
Терапевтическое исследование |
|
1а |
Систематический обзор гомогенных диагностических исследований 1-го уровня |
Систематический обзор гомогенных РКИ |
|
1b |
Валидизирующее когортное исследование с качественным «золотым стандартом» |
Отдельное РКИ (с узким доверительным интервалом) |
|
1с |
Специфичность или чувствительность столь высокие, что положительный или отрицательный результат позволяет исключить/установить диагноз |
Исследование «Всё или ничего» |
|
2а |
Систематический обзор гомогенных диагностических исследований >2 уровня |
Систематический обзор (гомогенных) когортных исследований |
|
2b |
Разведочное когортное исследование с качественным «золотым стандартом» |
Отдельное когортное исследование (включая РКИ низкого качества; т.е. с <80% пациентов, прошедших контрольное наблюдение) |
|
2с |
Нет |
Исследование «исходов»; экологические исследования |
|
За |
Систематический обзор гомогенных исследований 3b уровня и выше |
Систематический обзор гомогенных исследований «случай–контроль» |
|
3b |
Исследование с непоследовательным набором или без проведения исследования «золотого стандарта» у всех испытуемых |
Отдельное исследование «случай– контроль» |
|
4 |
Исследование «случай–контроль» или исследование с некачественным или зависимым «золотым стандартом» |
Серия случаев (и когортные исследования или исследования «случай–контроль» низкого качества) |
|
5 |
Мнение экспертов без тщательной критической оценки или основанное на физиологии, лабораторные исследования на животных или разработка «первых принципов» |
Мнение экспертов без тщательной критической оценки, лабораторные исследования на животных или разработка «первых принципов» |
|
Степени рекомендаций | ||
|
A |
Согласующиеся между собой исследования 1-го уровня | |
|
B |
Согласующиеся между собой исследования 2-го или 3-го уровня либо экстраполяция на основе исследований 1-го уровня | |
Табл. 20.1. Окончание
|
Уровень |
Диагностическое исследование |
Терапевтическое исследование |
|
C |
Исследования 4-го уровня или экстраполяция на основе уровня 2 или 3 | |
|
D |
Доказательства 4-го уровня или затруднительные для обобщения или некачественные исследования любого уровня | |
ВАЛИДИЗАЦИЯ РЕКОМЕНДАЦИЙ
Настоящие рекомендации в предварительной версии были рецензированы независимыми экспертами, которых попросили прокомментировать прежде всего, насколько интерпретация доказательств, лежащих в основе рекомендаций, доступна для понимания. Получены комментарии со стороны врачей амбулаторного звена. Полученные комментарии тщательно систематизировались и обсуждались на совещаниях экспертной группы.
Последние изменения в настоящих рекомендациях были представлены для дискуссии на заседании профильной комиссии «Колопроктология» Экспертного совета Минздрава России 17 декабря 2012 г. Проект рекомендаций был повторно рецензирован независимыми экспертами и врачами амбулаторного звена. Для окончательной редакции и контроля качества рекомендации были повторно проанализированы членами экспертной группы, которые пришли к заключению, что все замечания и комментарии приняты во внимание, риск систематических ошибок при разработке рекомендаций сведен к минимуму.
ОБЛАСТЬ ПРИМЕНЕНИЯ РЕКОМЕНДАЦИЙ
Данные клинические рекомендации применимы при осуществлении медицинской деятельности в рамках Порядка оказания медицинской помощи взрослому населению с заболеваниями толстой кишки, анального канала и промежности колопроктологического профиля, а также в рамках Порядка оказания медицинской помощи населению при заболеваниях гастроэнтерологического профиля.
Определения
Язвенный колит — хроническое заболевание толстой кишки, характеризуемое иммунным воспалением ее слизистой оболочки [6].
При язвенном колите поражается только толстая кишка (за исключением ретроградного илеита), в процесс обязательно вовлекается прямая кишка, воспаление чаще всего ограничивается слизистой оболочкой (за исключением фульминантного колита) и носит диффузный характер. Под обострением (рецидивом, атакой) язвенного колита понимают появление типичных симптомов заболевания у больных язвенным колитом в стадии клинической ремиссии, спонтанной или медикаментозно
поддерживаемой. Ранним рецидивом называют рецидив, возникший менее чем через 3 мес после медикаментозно достигнутой ремиссии. На практике признаками клинического обострения служат увеличение частоты дефекаций с выделением крови и/или характерные изменения, обнаруживаемые при эндоскопическом исследовании толстой кишки.
Ремиссией язвенного колита считают исчезновение основных клинических симптомов заболевания (УД 5, СР D [7]) и заживление слизистой оболочки толстой кишки [8]. Выделяют:
n клиническую ремиссию — отсутствие примеси крови в стуле, отсутствие императивных/ложных позывов при частоте дефекаций не более 3 раз в сутки;
n эндоскопическую ремиссию — отсутствие видимых макроскопических признаков воспаления при эндоскопическом исследовании толстой кишки;
n гистологическую ремиссию — отсутствие микроскопических признаков воспаления.
Код по Международной классификации болезней 10-го пересмотра
n К51 Язвенный колит
Классификация
Надлежащая классификация язвенного колита по протяженности поражения, характеру течения, тяжести атаки и наличию осложнений определяет вид и форму введения лекарственных препаратов (УД 1b, СР В), а также периодичность скрининга на колоректальный рак (УД 2, СР В [9]). Для описания протяженности поражения применяется Монреальская классификация (табл. 20.2), оценивающая протяженность макроскопических изменений при эндоскопическом исследовании толстой кишки
(УД 5, СР D).
Таблица 20.2. Монреальская классификация язвенного колита по протяженности поражения [10]
|
Проктит |
Поражение ограничено прямой кишкой |
|
Левосторонний колит |
Поражение распространяется до левого изгиба толстой кишки (включая проктосигмоидит) |
|
Тотальный колит |
Включая субтотальный колит, а также тотальный язвенный колит с ретроградным илеитом |
По характеру течения выделяют:
n острое (менее 6 мес от дебюта заболевания):
v с фульминантным началом;
v с постепенным началом;
n хроническое непрерывное (отсутствие более чем 6-месячных периодов ремиссии на фоне адекватной терапии);
n хроническое рецидивирующее (наличие более чем 6-месячных периодов ремиссии):
v редко рецидивирующее (1 раз в год или реже);
v часто рецидивирующее (2 раза и более в год).
Тяжесть заболевания в целом определяется тяжестью текущей атаки, наличием внекишечных проявлений и осложнений, рефрактерностью к лечению, в частности развитием гормональной зависимости и резистентности. Однако для формулирования диагноза и определения тактики лечения следует определять тяжесть текущего обострения (атаки) (УД 1b, СР В), для чего используются простые критерии Truelove–Witts, как правило, применяемые в повседневной клинической практике, и индекс активности язвенного колита (индекс Мейо; DAI), как правило, применяемый в клинических испытаниях. Выделяют легкую, среднетяжелую и тяжелую атаки язвенного колита (табл. 20.3, 20.4).
Таблица 20.3. Тяжесть атаки язвенного колита согласно критериям Truelove–Witts [11]
|
|
Легкая |
Среднетяжелая |
Тяжелая |
|
Частота дефекаций с кровью |
<4 |
≥4, если: |
≥6, если: |
|
Пульс, в минуту |
Нормальные значения |
≤90 |
>90 |
|
Температура, °С |
|
≤37, |
>37,5 °С |
|
Гемоглобин, г/л |
|
≥105 |
<105 г/л |
|
СОЭ, мм/ч |
|
≤30 |
>30 мм/ч |
|
Контактная ранимость слизистой оболочки толстой кишки |
Нет |
Есть |
Есть |
Таблица 20.4. Тяжесть атаки согласно индексу активности язвенного колита (индексу Мейо)
|
Значение индекса |
0 |
1 |
2 |
3 |
|
Частота стула |
Обычная |
На 1–2-й день больше обычной |
На 3–4-й день больше обычной |
На 5-й день больше обычной |
|
Примесь крови в стуле |
Нет |
Прожилки |
Видимая кровь |
Преимущественно кровь |
|
Состояние слизистой оболочки |
Норма |
Легкая ранимость (1 балл по шкале Schroeder) |
Умеренная ранимость (2 балла по шкале Schroeder) |
Выраженная ранимость (3 балла по шкале Schroeder) |
|
Общая оценка состояния врачом |
Норма |
Удовлетворительное состояние |
Состояние средней тяжести |
Тяжелое состояние |
Примечание. Среднетяжелая и тяжелая атака констатируются при значении индекса (сумма оценок по 4 параметрам) от 6 и выше.
Используемая в индексе Мейо шкала оценки состояния слизистой оболочки по Schroeder приведена в табл. 20.5 и применяется для оценки эндоскопической активности язвенного колита.
Таблица 20.5. Классификация язвенного колита в зависимости от эндоскопической активности (по Schroeder) [12]
|
0 |
1 (минимальная активность) |
2 (умеренная активность) |
3 (выраженная активность) |
|
Норма или неактивное заболевание |
Гиперемия, смазанный сосудистый рисунок. Контактная ранимость отсутствует |
Выраженная гиперемия, отсутствие сосудистого рисунка, контактная ранимость, эрозии |
Спонтанная ранимость, изъязвления |
Классификация язвенного колита в зависимости от ответа на гормональную терапию облегчает выбор рациональной лечебной тактики, поскольку целью консервативного лечения является достижение стойкой ремиссии с прекращением терапии глюкокортикостероидами (ГКС). Для этих целей выделяют следующее.
1. Гормональная резистентность
n В случае тяжелой атаки сохранение активности заболевания, несмотря на в/в введение ГКС в дозе, эквивалентной 2 мг/кг в сутки преднизолона, в течение более чем 7 дней
или
n в случае среднетяжелой атаки сохранение активности заболевания при пероральном приеме ГКС в дозе, эквивалентной 1 мг/кг в сутки преднизолона, в течение 4 нед.
2. Гормональная зависимость
n Увеличение активности болезни при уменьшении дозы ГКС ниже дозы, эквивалентной 10–15 мг преднизолона в сутки в течение 3 мес от начала лечения
или
n возникновение рецидива болезни в течение 3 мес после окончания лечения ГКС.
Формулировка диагноза
При формулировании диагноза следует отразить характер течения заболевания, протяженность поражения, тяжесть текущей атаки или наличие ремиссии, наличие гормональной зависимости или резистентности, а также наличие внекишечных или кишечных осложнений язвенного колита (см. раздел «Диагностика»). Ниже приведены примеры формулировок диагноза.
n Язвенный колит, хроническое рецидивирующее течение, проктит, среднетяжелая атака.
n Язвенный колит, хроническое непрерывное течение, левостороннее поражение, среднетяжелая атака. Гормональная зависимость. Внекишечные проявления (периферическая артропатия).
n Язвенный колит, хроническое рецидивирующее течение, тотальное поражение, тяжелая атака. Гормональная резистентность. Токсический мегаколон.
Диагностика [13]
КЛИНИЧЕСКИЕ ДИАГНОСТИЧЕСКИЕ КРИТЕРИИ
К основным клиническим симптомам язвенного колита относятся диарея и/или ложные позывы с кровью, тенезмы и императивные позывы на дефекацию, а также ночная дефекация. При тяжелой атаке язвенного колита возможно появление общих симптомов, таких как снижение массы тела, общая слабость, анорексия и лихорадка (табл. 20.6–20.8).
Таблица 20.6. Клинические проявления язвенного колита
|
Возможные симптомы болезни в анамнезе |
Типичные клинические симптомы в момент осмотра | ||
|
• Эпизоды диареи. • Примесь крови в кале. • Тенезмы |
• Внекишечные симптомы (поражение кожи, слизистых оболочек, суставов, глаз и др.) |
• Диарея. • Кровь в кале. • Ночная дефекация (чаще при выраженной активности процесса) |
• Тенезмы (чаще при проктитах и проктосигмоидитах). • Потеря массы тела. • Лихорадка. • Анемия. • Внекишечные симптомы |
Примечание. Для язвенного колита, в отличие от болезни Крона, боль в животе менее характерна и носит умеренный (спастический) характер, чаще перед стулом; при проктитах и проктосигмоидитах диарея отсутствует, а частые ложные позывы могут сочетаться с запором или оформленным стулом.
Таблица 20.7. Системные проявления язвенного колита
|
Системные признаки воспаления (синдром эндотоксемии) |
Метаболические расстройства |
|
• Лихорадка. • Лейкоцитоз. • Увеличение СОЭ. • Повышение уровня острофазных белков (С-реактивный белок, фибриноген, серомукоид) |
• Потеря массы тела. • Общая слабость. • Анемия. • Гипопротеинемия. • Дисбаланс электролитов |
Таблица 20.8. Внекишечные проявления язвенного колита [14]
|
Аутоиммунные, связанные с активностью заболевания |
Аутоиммунные, не связанные с активностью заболевания |
Обусловленные длительным воспалением и метаболическими нарушениями |
|
• Артропатии (артралгии, артриты). • Поражение кожи |
• Первичный склерозирующий холангит, перихолангит. |
• Холелитиаз. • Стеатоз печени, стеатогепатит |
Табл. 20.8. Окончание
|
Аутоиммунные, связанные с активностью заболевания |
Аутоиммунные, не связанные с активностью заболевания |
Обусловленные длительным воспалением и метаболическими нарушениями |
|
(узловатая эритема, гангренозная пиодермия). • Поражение слизистой оболочки ротовой полости (афтозный стоматит). • Поражение глаз (увеит, ирит, иридоциклит, эписклерит) |
• Анкилозирующий спондилоартрит, сакроилеит (редко). • Серонегативный ревматоидный артрит (редко). • Псориаз |
• Тромбоз периферических вен, тромбоэмболия легочной артерии. • Амилоидоз |
Кишечные осложнения язвенного колита включают кишечное кровотечение, токсическую дилатацию и перфорацию толстой кишки, а также колоректальный рак. Поскольку эти осложнения требуют хирургического лечения, подробно они рассматриваются в разделах «Кишечные осложнения язвенного колита» и «Колоректальный рак и рекомендации по скринингу».
УСТАНОВЛЕНИЕ ДИАГНОЗА
Однозначных диагностических критериев язвенного колита не существует. Диагноз выставляется на основании сочетания данных анамнеза, клинической картины и типичных эндоскопических и гистологических изменений (УД 5, СР D). Для этого врачу необходимо провести:
n подробный опрос пациента, включающий, в частности, сбор информации о поездках в южные страны, непереносимости каких-либо продуктов, о принимаемых лекарствах (в частности, антибиотиках и нестероидных противовоспалительных средствах), курении и наличии воспалительных и злокачественных заболеваний кишечника у родственников (УД 5, СР D);
n подробный физикальный осмотр, при котором следует оценить частоту пульса, температуру тела, артериальное давление, индекс массы тела, наличие перитонеальных симптомов и признаков токсической дилатации, осмотр ротовой полости (исключение афтозного стоматита), а также кожных покровов (исключение узловатой эритемы и гангренозной пиодермии), глаз (исключение увеита, иридоциклита и т.п.) и суставов (УД 5, СР D);
n осмотр перианальной области, пальцевое обследование прямой кишки, ректороманоскопию (УД 5, СР D);
n обзорную рентгенографию брюшной полости (при тяжелой атаке) (УД 5, СР D):
v исключение токсической дилатации и перфорации толстой кишки;
n тотальную колоноскопию с илеоскопией:
v обязательная процедура для установления диагноза язвенного колита, а также при решении вопроса о колэктомии в случае гормональной зависимости/резистентности; при невозможности ее выполнения —
ирригоскопия с двойным контрастированием (для оценки протяженности поражения толстой кишки);
n биопсию слизистой оболочки толстой кишки (УД 1b, СР B):
v при первичной постановке диагноза;
v при сомнениях в правильности ранее выставленного диагноза;
v при длительном анамнезе язвенного колита (более 7–10 лет) — ступенчатая биопсия (из каждого отдела толстой кишки) для исключения дисплазии эпителия (УД 3а, СР В); см. раздел «Колоректальный рак и рекомендации по скринингу»;
v рекомендуемым стандартом биопсии является взятие биоптатов слизистой оболочки прямой кишки и не менее чем из 4 других участков толстой кишки, а также слизистой оболочки подвздошной кишки (УД 1b, СР B);
n УЗИ органов брюшной полости, забрюшинного пространства, малого таза (УД 3, СР С);
n анализ кала (УД 2b, СР B):
v исключение острой инфекции при первичной диагностике язвенного колита;
v исключение паразитарного колита;
v исследование токсинов А и В Cl. difficile после проведенного курса антибиотикотерапии или пребывания в стационаре, а также при тяжелом обострении заболевания, резистентного к проводимой терапии [15, 16]. Для выявления инфекции в 90% случаев требуется минимум 4 образца кала [17, 18];
v исследование уровня фекального кальпротектина при первичной дифференциальной диагностике язвенного колита с функциональными заболеваниями кишечника, а также для неинвазивной оценки активности воспалительного процесса в кишечнике на фоне лечения (УД 2b, СР B [19, 20]);
n исследование крови:
v общий анализ крови, СОЭ (скорость оседания эритроцитов);
v С-реактивный белок;
v гемокоагулограмма;
v биохимический анализ крови (обязательно печеночные ферменты, креатинин, мочевина, электролиты);
v группа крови и резус фактор;
n общий анализ мочи.
При необходимости дифференциальной диагностики проводят следующие дополнительные исследования:
n магнитно-резонансную томографию (МРТ);
n компьютерную томографию (КТ);
n трансабдоминальное ультразвуковое сканирование тонкой и ободочной кишки;
n трансректальное УЗИ прямой кишки и анального канала;
n рентгеноконтрастное исследование тонкой кишки с бариевой взвесью;
n фиброгастродуоденоскопию;
n капсульную эндоскопию;
n одноили двухбаллонную энтероскопию.
С целью дифференциальной диагностики и подбора терапии внекишечных проявлений язвенного колита и сопутствующих заболеваний могут потребоваться консультации:
n психотерапевта, психолога (невроз, планируемая операция с наличием стомы и т.п.);
n эндокринолога (стероидный сахарный диабет, надпочечниковая недостаточность у больных на длительной гормональной терапии);
n дерматолога (дифференциальный диагноз узловатой эритемы, пиодермии и т.п.);
n ревматолога (артропатии, сакроилеит и т.п.);
n акушера-гинеколога (беременность).
Эндоскопическое исследование толстой кишки — основной метод диагностики язвенного колита, однако специфичные эндоскопические признаки отсутствуют. Наиболее характерными являются непрерывное воспаление, ограниченное слизистой оболочкой, начинающееся в прямой кишке и распространяющееся проксимальнее, с четкой границей воспаления. Эндоскопическую активность язвенного колита наилучшим образом отражают контактная ранимость (выделение крови при контакте с эндоскопом), отсутствие сосудистого рисунка и наличие или отсутствие эрозий и изъязвлений (УД 2b, СР В). Обнаружение стойкого сужения кишки на фоне язвенного колита требует обязательного исключения колоректального рака (УД 5, СР D).
К микроскопическим признакам язвенного колита относятся деформация крипт (разветвленность, разнонаправленность, появление крипт разного диаметра, уменьшение плотности крипт, «укорочение крипт», крипты не достигают подлежащего слоя мышечной пластинки слизистой оболочки), «неровная» поверхность в биоптате слизистой оболочки, уменьшение количества бокаловидных клеток, базальный плазмоцитоз, инфильтрация собственной пластинки слизистой оболочки, наличие крипт-абсцессов и базальных лимфоидных скоплений. Степень воспалительной инфильтрации обычно уменьшается по мере удаления от прямой кишки.
ДИФФЕРЕНЦИАЛЬНАЯ ДИАГНОСТИКА
ВЗК — это группа хронических воспалительных заболеваний кишечника с неизвестной этиологией. Язвенный колит входит в группу этих болезней.
При подозрении на язвенный колит дифференциальная диагностика начинается с исключения воспалительных заболеваний толстой кишки, которые не относятся к группе ВЗК. Это инфекционные, сосудистые, медикаментозные, токсические и радиационные поражения, а также дивертикулит и др. На следующем этапе дифференциальной диагностики проводится верификация клинических диагнозов язвенного колита и болезни Крона, относящихся к группе ВЗК.
Таким образом, дифференциальная диагностика язвенного колита проводится с:
n болезнью Крона толстой кишки;
n острыми кишечными инфекциями:
v дизентерией;
v сальмонеллезом;
v кампилобактериозом;
v иерсиниозом;
v амебиазом;
n глистными инвазиями, паразитозами;
n антибиотико-ассоциированными поражениями кишечника (псевдомембранозный колит, вызываемый Cl. difficile) [21];
n туберкулезом кишечника;
n системным васкулитом;
n раком толстой кишки;
n дивертикулитом;
n микроскопическими колитами (коллагеновым и лимфоцитарным) [22];
n радиационным проктитом.
Лечение
КОНСЕРВАТИВНОЕ ЛЕЧЕНИЕ [23]
Принципы терапии
Лечебные мероприятия при язвенном колите включают назначение лекарственных препаратов, хирургическое лечение, психосоциальную поддержку и диетические рекомендации.
Выбор вида консервативного или хирургического лечения определяется тяжестью атаки, протяженностью поражения толстой кишки, наличием внекишечных проявлений, длительностью анамнеза, эффективностью и безопасностью ранее проводившейся терапии, а также риском развития осложнений язвенного колита [24, 25].
Цель терапии — достижение и поддержание бесстероидной ремиссии
(прекращение приема глюкокортикостероидов (ГКС) в течение 12 нед после начала терапии) [26], профилактика осложнений язвенного колита, предупреждение операции, а при прогрессировании процесса, а также при развитии опасных для жизни осложнений — своевременное назначение хирургического лечения. Поскольку полное излечение больных язвенным колитом достигается только путем удаления субстрата заболевания (колопроктэктомия), при достижении ремиссии неоперированный больной должен оставаться на постоянной поддерживающей (противорецидивной) терапии.
Следует особо отметить, что глюкокортикостероиды не могут применяться в качестве поддерживающей терапии.
Ниже представлены рекомендации по выбору препаратов для индукции и поддержания ремиссии в зависимости от протяженности поражения и тяжести атаки [26].
Проктит
Легкая и среднетяжелая атака
Терапия заключается в назначении суппозиториев с месалазином (1–2 г/сут) или ректальной пены месалазина (1–2 г/сут) [27]. Оценка терапевтического ответа производится в течение 2 нед (УД 1b, СР А [28]).
При ответе терапия в указанных дозах пролонгируется до 6–8 нед.
При неэффективности лечения эффективно подключение ректальных форм ГКС (суппозиториев с преднизолоном 10 мг × 1–2 раза в сутки) (УД 5, СР D [30]). При достижении ремиссии проводится поддерживающая терапия — местное введение месалазина (свечи или ректальная пена) 1–2 г × 3 раза в неделю в виде монотерапии (не менее 2 лет) (УД 1b, СР А [30]).
При неэффективности лечения следует подключить пероральные формы месалазина в дозе 3–4 г/сут (УД 1b, СР B [31]). При отсутствии эффекта показано назначение системных кортикостероидов (преднизолон 0,75 мг/кг) в комбинации с азатиоприном 2 мг/кг или 6-меркаптопурином (6-МП) 1,5 мг/кг (УД 4, СР C).
Местная терапия (свечи с преднизолоном 10 мг × 1–2 раза в сутки) может быть продолжена.
При достижении ремиссии, индуцированной с помощью ГКС, поддерживающая терапия проводится с помощью азатиоприна 2 мг/кг или 6-МП 1,5 мг/кг не менее 2 лет.
Тяжелая атака (развивается крайне редко)
Лечение атаки заключается в назначении системных ГКС в дозе, эквивалентной 1 мг/кг преднизолона в комбинации с местной терапией месалазином или преднизолоном (суппозитории, ректальная пена) (УД 5, СР D). При достижении ремиссии поддерживающая терапия проводится местными препаратами месалазина (суппозитории, ректальная пена) 1–2 г × 3 раза в неделю в виде монотерапии или в комбинации с пероральным месалазином 1,5–2 г — не менее 2 лет (УД 1b, СР А). При рецидиве, требующем повторного назначения ГКС, дополнительно назначается азатиоприн 2 мг/кг (или 6-МП 1,5 мг/кг), и дальнейшая поддерживающая терапия проводится иммуносупрессорами (азатиоприн или 6-МП) не менее 2 лет (УД 5, СР D).
Левосторонний и тотальный колит. Легкая атака
Первая атака или рецидив требуют назначения месалазина внутрь 3 г/ сут (или сульфасалазин 4 г/сут) в комбинации с месалазином в клизмах 2–4 г/сут (в зависимости от эндоскопической активности) (УД 1а, СР А [32–34]). Терапевтический ответ оценивается в течение 2 нед. При ответе
терапия продолжается до 6–8 нед. При отсутствии эффекта от местных и пероральных препаратов 5-аминосалициловой кислоты (5-АСК) целесообразно подключение ректальных форм ГКС (клизмы с суспензией гидрокортизона 125 мг × 1–2 раза в сутки) (УД 1а, СР А). Отсутствие ответа на терапию пероральной 5-АСК в сочетании с местным лечением, как правило, является показанием к назначению системных ГКС (см. ниже).
При достижении ремиссии поддерживающая терапия проводится с помощью перорального месалазина 1,5 г/сут [33]. Дополнительное введение месалазина в клизмах по 2 г 2 раза в неделю (так называемая терапия выходного дня) увеличивает вероятность долгосрочной ремиссии (УД 1b, СР А). Допустимо назначение сульфасалазина (3 г) вместо месалазина (УД 1b, СР А).
Левосторонний и тотальный колит. Среднетяжелая атака
При первой атаке или рецидиве необходимо назначение месалазина в таблетках 4–5 г/сут в комбинации с месалазином в клизмах 2–4 г/ сут (в зависимости от эндоскопической активности) (УД 1а, СР А [33]). Терапевтический ответ оценивается в течение 2 нед. При ответе терапия пролонгируется до 6–8 нед. При достижении ремиссии проводится поддерживающая терапия месалазином 1,5–2 г/сут внутрь + месалазин в клизмах по 2 г 2 раза в неделю (УД 1b, СР A [34]). Допустимо назначение сульфасалазина 3 г/сут вместо месалазина (УД 1b, СРА [35]).
При отсутствии эффекта от 5-АСК показано назначение системных стероидов в дозе, эквивалентной 1 мг/кг преднизолона в сочетании с азатиоприном 2 мг/кг или 6-МП 1,5 мг/кг (УД 1b, СР C). При достижении ремиссии дальнейшая поддерживающая терапия проводится с помощью азатиоприна 2 мг/кг в сутки или 6-МП 1,5 мг/кг не менее 2 лет (УД 1a, СР А [36]).
При отсутствии эффекта от системных стероидов в течение 4 нед показано проведение биологической терапии (инфликсимаб 5 мг/кг на 0, 2, 6 нед, или голимумаб 200 мг на неделе 0, 100 мг на неделе 2, а далее по 50 или 100 мг в зависимости от массы тела ежемесячно) в сочетании с азатиоприном 2 мг/кг или 6-МП 1,5 мг/кг (УД 1a, СР А). Поддерживающая терапия проводится с помощью азатиоприна (или 6-МП) в сочетании с введениями инфликсимаба каждые 8 нед или голимумаба каждый месяц (УД 1b, СР А) в течение не менее 1 года [37]. При невозможности пролонгированного использования инфликсимаба/голимумаба поддерживающая терапия проводится только тиопуринами, в случае непереносимости тиопуринов — инфликсимабом/голимумабом в виде монотерапии (УД 5, СР D).
Левосторонний и тотальный колит. Тяжелая атака
При тяжелом обострении заболевания, сопровождающемся диареей более 5 раз в сутки, тахикардией свыше 90 в минуту, повышением
температуры тела свыше 37,8 °С, анемией менее 105 г/л, больной язвенным колитом должен быть госпитализирован в многопрофильный стационар с последующим обязательным наблюдением специалистомгастроэнтерологом и специалистом-колопроктологом (УД 5, СР D). При тяжелой атаке язвенного колита необходимо проведение следующих мероприятий:
n Внутривенное введение ГКС: преднизолон 2 мг/кг в сутки.
n Местная терапия клизмами с месалазином 2–4 г/сут или гидрокортизоном 125 мг/сут.
n Инфузионная терапия: коррекция белково-электролитных нарушений, дезинтоксикация (гипокалиемия и гипомагниемия повышают риск токсической дилатации ободочной кишки).
n Коррекция анемии (гемотрансфузии при анемии ниже 80 г/л, далее терапия препаратами железа, предпочтительно парентерально).
n Эндоскопическое исследование толстой кишки при поступлении больного следует выполнять без подготовки, поскольку ее проведение повышает риск токсической дилатации.
n Подключение дополнительного энтерального питания у истощенных пациентов. Полностью парентеральное питание и/или временное ограничение приема пищи внутрь нецелесообразно [38].
n При наличии лихорадки или подозрении на кишечную инфекцию — назначение антибиотиков (УД 5, СР D).
v 1-я линия — метронидазол 1,5 г/сут + фторхинолоны (ципрофлоксацин, офлоксацин) в/в 10–14 дней;
v 2-я линия — цефалоспорины в/в 7–10 дней [39, 40].
Продолжение гормональной терапии более 7 дней при отсутствии эффекта нецелесообразно.
При клиническом ответе через 7 дней показан перевод пациента на прием ГКС внутрь: преднизолон 1 мг/кг или метилпреднизолон 0,8 мг/кг с последующим снижением до полной отмены по 5–10 мг преднизолона или 4–8 мг метилпреднизолона в неделю (в течение первых 5–7 дней комбинировать с дополнительным в/в введением преднизолона 50 мг/сут) (УД 2b, СР B). Следует помнить, что суммарная продолжительность курса ГКС не должна превышать 12 нед. При снижении дозы стероидов до 30–40 мг в качестве поддерживающей терапии следует подключить месалазин в дозе 3 г. При достижении ремиссии поддерживающая терапия проводится с помощью 1,5–2 г перорального месалазина в течение 2 лет. Допустимо назначение сульфасалазина 3 г вместо месалазина (УД 1b, СР А).
При отсутствии эффекта от стероидной терапии через 7 дней показана терапия 2-й линии, которая включает следующие варианты лечения:
n биологическую терапию инфликсимабом 5 мг/кг (введения в рамках индукционного курса на 0, 2 и 6 нед) (УД 1a, СР А [41, 42]) или голимумабом в дозе 200 мг на неделе 0, затем 100 мг на неделе 2, а далее через месяц после второго введения (в дозе 100 мг при массе тела более 80 кг или 50 мг при массе тела менее 80 кг);
n введение циклоспорина А в/в или внутрь 2–4 мг/кг в течение 7 дней с мониторированием показателей функции почек и определением концентрации препарата в крови (УД 1a, СР А [43, 44]).
При ответе на индукционный курс инфликсимаба дальнейшая поддерживающая терапия проводится с инфузиями каждые 8 нед в течение не менее чем 1 года (УД 1b, СР А) в комбинации с азатиоприном 2 мг/кг (или 6-МП 1,5 мг/кг) (УД 2a, СРB [45, 46]).
При ответе на индукционный курс голимумаба дальнейшая поддержива-
ющая терапия проводится при помощи ежемесячных инъекций по 100 мг пациентам с массой тела более 80 мг и по 50 мг пациентам с массой тела менее 80 мг.
При эффекте от терапии циклоспорином А через 7 дней необходимо перейти на прием азатиоприна 2 мг/кг в комбинации с пероральным циклоспорином (на фоне терапевтической дозы стероидов) с постепенной отменой стероидов в течение 12 нед. Поддерживающая терапия проводится пероральным циклоспорином в течение 3 мес до момента достижения терапевтической концентрации азатиоприна. Дальнейшую поддерживающую терапию проводят с помощью азатиоприна 2 мг/кг в течение не менее чем 2 лет (УД 2b, СР В [47]).
При отсутствии ответа на 2-ю инфузию инфликсимаба 2-ю инъекцию голимумаба или 7-дневную терапию циклоспорином А необходимо рассмотреть варианты хирургического лечения.
Прогнозирование эффективности консервативной терапии при тяжелой атаке язвенного колита
Совместное наблюдение пациента опытными гастроэнтерологом и колопроктологом остаются ключевым условием безопасного ведения тяжелой атаки язвенного колита. Хотя медикаментозная терапия во многих случаях оказывается эффективной, имеются данные, указывающие, что задержка в проведении необходимого оперативного лечения пагубно сказывается на исходе лечения больного, в частности, увеличивая риск операционных осложнений [48]. Большинство исследований предикторов колэктомии проведены до широкого применения биологической терапии и циклоспорина и позволяют прогнозировать неэффективность ГКС, а не инфликсимаба и иммуносупрессоров.
n Частота стула >12 раз в сутки на 2-е сутки в/в гормональной терапии повышает риск колэктомии до 55% [49].
n Если на 3-й день гормональной терапии частота стула превышает 8 раз в сутки или составляет от 3 до 8 раз в сутки и при этом уровень С-реактивного белка превышает 45 мг/л, вероятность колэктомии составляет 85% (так называемый оксфордский индекс) [68].
n На 3-й день также можно определить шведский индекс по формуле: частота стула × 0,14 × уровень С-реактивный белок. Его значение 8 и более повышает вероятность колэктомии до 75% [50].
n Риск колэктомии также повышается в 5–9 раз при наличии гипоальбуминемии и лихорадки при поступлении, а также при отсутствии
более чем 40% уменьшения частоты стула за 5 дней в/в гормональной терапии [51].
n Наличие глубоких изъязвлений толстой кишки (на фоне которых остаточная слизистая оболочка определяется только в виде «островков») повышает риск колэктомии до 86–93% [52, 53].
Эффективность инфликсимаба при гормональной резистентности, по разным данным, колеблется от 25 до 80%, что может объясняться различиями в эффективности препарата у отдельных пациентов. Исследования, посвященные прогнозированию эффективности биологической терапии, остаются ограниченными, однако установлено:
n эффективность инфликсимаба при гормонорезистентной тяжелой атаке язвенного колита уменьшается с возрастом [54], при наличии тотального поражения толстой кишки [55], а также при выраженной гипоальбуминемии [56], уровне гемоглобина менее 95 г/л и уровне С-реактивного белка более 10 мг/л на момент первого введения инфликсимаба [57];
n эффективность инфликсимаба существенно ниже у пациентов, у которых показания к антицитокиновой терапии возникли уже при первой атаке язвенного колита [46];
n наличие обширных язвенных дефектов слизистой оболочки толстой кишки при колоноскопии до начала терапии инфликсимабом с 78% точностью прогнозирует ее дальнейшую неэффективность [58].
У пациентов с высоким риском колэктомии следует принимать индивидуальное решение о проведении терапии 2-й линии с помощью циклоспорина или инфликсимаба или о хирургическом лечении непосредственно после неэффективного курса в/в ГКС.
Профилактика осложнений терапии
При назначении гормональной терапии необходимо учитывать следующее:
n постепенное снижение дозы стероидов до полной отмены — строго обязательно;
n суммарная продолжительность гормональной терапии не должна превышать 12 нед;
n обязательным является сопутствующий прием препаратов кальция, витамина D, ингибиторов протонной помпы;
n в период лечения необходим регулярный контроль уровня глюкозы в крови.
При назначении иммуносупрессоров и биологической терапии необходимо следующее:
n перед началом биологической терапии консультация фтизиатра — скри-
нинг на туберкулез (рентгенография органов грудной клетки, квантифероновый тест, при невозможности его проведения — проба Манту, Диаскин-тест) [59];
n биологическая терапия требует строгого соблюдения доз и графика введения (нерегулярное введение повышает риск инфузионных реакций и неэффективности);
n на фоне терапии иммуносупрессорами обязательным является контроль уровня лейкоцитов (общий анализ крови ежемесячно).
Профилактика оппортунистических инфекций [60]
К факторам риска развития оппортунистических инфекций относятся:
n прием лекарственных средств: азатиоприн, внутривенная гормональная терапия 2 мг/кг или перорально более 20 мг в день в течение более 2 нед, биологическая терапия;
n возраст старше 50 лет;
n сопутствующие заболевания: хронические заболевания легких, алкоголизм, органические заболевания головного мозга, сахарный диабет.
В соответствии с Европейским консенсусом по профилактике, диагностике и лечению оппортунистических инфекций при ВЗК такие пациенты подлежат обязательной вакцинопрофилактике. Необходимый минимум вакцинопрофилактики:
n рекомбинантная вакцина против HBV;
n поливалентная инактивированная пневмококковая вакцина;
n трехвалентная инактивированная вакцина против вируса гриппа.
Для женщин до 26 лет при отсутствии вируса на момент скрининга рекомендуется вакцинация от вируса папилломы человека.
ХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕ
Показания для хирургического лечения
Показаниями к хирургическому лечению язвенного колита служат неэффективность консервативной терапии (гормональная резистентность, неэффективность биологической терапии) или невозможность ее продолжения (гормональная зависимость), кишечные осложнения язвенного колита (токсическая дилатация, перфорация кишки, кишечное кровотечение), а также рак толстой кишки или высокий риск его возникновения.
Неэффективность или невозможность продолжения консервативной терапии
О неэффективности консервативной терапии свидетельствуют (см. раздел «Классификация»):
n гормональная резистентность;
n гормональная зависимость.
Гормональную зависимость удается эффективно преодолеть с помощью биологических препаратов и/или иммуносупрессоров (азатиоприн, 6-МП) в 40–55% случаев [61, 62], а при гормональной резистентности назначение циклоспорина А или биологической терапии позволяет индуцировать ремиссию в 43–80% случаев [43]. Однако у части больных с высоким риском осложнений и неэффективности консервативной терапии при развитии гормональной резистентности или зависимости возможно проведение хирургического лечения без попытки применения биологических препаратов или иммуносупрессоров. Подробно этот вопрос описан в разделе «Прогнозирование эффективности консервативной терапии при тяжелой атаке язвенного колита».
Кишечные осложнения
К кишечным осложнениям язвенного колита, требующим хирургического лечения, относятся:
n кишечное кровотечение, наличие которого констатируют при потере более 100 мл крови в сутки, по данным объективных лабораторных методов (сцинтиграфия, определение гемоглобина в каловых массах гемоглобинцианидным методом), или при объеме каловых масс с визуально определяемой примесью крови более 800 мл/сут. Косвенно о кишечном кровотечении свидетельствует прогрессирующее снижение уровня гемоглобина на фоне адекватной терапии, однако четкие пороговые значения для снижения его уровня, свидетельствующие о кишечном кровотечении, не определены. При развитии данного осложнения показана экстренная операция;
n токсическая дилатация ободочной кишки (токсический мегаколон), представляющая собой не связанное с обструкцией расширение ободочной кишки до 6 см и более с явлениями интоксикации. К факторам риска токсической дилатации относятся гипокалиемия, гипомагниемия, подготовка кишки к колоноскопии с помощью осмотических слабительных (см. раздел «Диагностика») и прием антидиарейных препаратов. Косвенно о развитии токсической дилатации свидетельствуют внезапное сокращение частоты стула на фоне имевшейся диареи, вздутие живота, а также внезапное уменьшение или исчезновение болевого синдрома и нарастание симптомов интоксикации (нарастание тахикардии, снижение АД):
v при развитии токсической дилатации на фоне адекватной интенсивной терапии показана экстренная операция;
v если токсическая дилатация обнаруживается у пациента, ранее не получавшего полноценной лекарственной (в первую очередь гормональной) терапии, возможно консервативное лечение: в/в ГКС в дозе, эквивалентной 2 мг/кг преднизолона в сутки, инфузионная терапия (коррекция электролитных нарушений), метронидазол 1,5 г/сут в/в. При отсутствии положительной динамики (нормализации диаметра кишки) в течение суток показана колэктомия;
n перфорация толстой кишки — наиболее опасное осложнение язвенного колита почти с 50% смертностью. При выявлении угрожающих симптомов (перитонеальные симптомы, свободный газ в брюшной полости по данным обзорной рентгенографии) показана экстренная колэктомия.
Колоректальный рак и рекомендации по скринингу
У больных с длительным анамнезом язвенного колита существенно повышен риск колоректального рака, что обусловливает необходимость регулярного обследования для выявления дисплазии эпителия толстой кишки. На вероятность развития рака влияют следующие факторы.
n Длительность анамнеза язвенного колита: риск колоректального рака составляет 2% при 10-летнем, 8% при 20-летнем и 18% при 30-летнем анамнезе [63].
n Начало заболевания в детском и подростковом возрасте, хотя этот фактор может лишь отражать длительность анамнеза и не являться независимым предиктором колоректального рака [64].
n Протяженность поражения: риск наиболее повышен у пациентов с тотальным язвенным колитом, в то время как у пациентов с проктитом риск не отличается от среднего в популяции.
n Наличие первичного склерозирующего холангита [65].
n Семейный анамнез колоректального рака.
n Тяжелые обострения язвенного колита в анамнезе или непрерывное течение язвенного колита. Последствием высокой активности язвенного колита может стать воспалительный полипоз, также являющийся фактором риска развития колоректального рака [66].
В целом скрининг колоректального рака у больных язвенным колитом следует начинать после 6–8 лет от дебюта заболевания. У пациентов, страдающих первичным склерозирующим холангитом, регулярное контрольное обследование следует начать раньше в связи с высоким риском рака. Пациенты с поражением, ограниченным прямой кишкой, могут наблюдаться с той же периодичностью, что и здоровые люди, при условии, что прошедшее или активное воспаление проксимальнее прямой кишки исключено при эндоскопическом исследовании и биопсии остальных отделов кишки. Частота рутинных эндоскопических исследований диктуется степенью риска, оцениваемой при колоноскопии через 6–8 нед после начала язвенного колита (табл. 20.9)
Таблица 20.9. Определение риска колоректального рака у больных язвенным колитом (по данным колоноскопии через 6–8 лет от дебюта заболевания)
|
Тотальный язвенный колит |
Низкий риск — 0–2 фактора риска Высокий риск — 3–4 фактора риска |
|
Сохраняющееся воспаление (по данным эндоскопического / гистологического исследования) |
|
|
Семейный анамнез колоректального рака |
|
|
Воспалительный полипоз |
|
|
При высоком риске скрининговая колоноскопия проводится каждые 1–2 года, а при низком риске — каждые 3–4 года | |
Контрольная колоноскопия должна проводиться в условиях хорошей подготовки кишки и желательно в период ремиссии, поскольку активное воспаление затрудняет выявление дисплазии.
Для скрининга неопластических изменений слизистой оболочки используют два подхода.
1. Биопсия слизистой оболочки по 4 фрагмента из каждых 10 см ободочной и прямой кишки (при эндоскопии в белом свете). Такой подход не исключает обязательной биопсии всех подозрительных образований.
2. При надлежащей квалификации эндоскописта и наличии эндоскопа с высоким разрешением — хромоэндоскопия с прицельной биопсией участков, подозрительных на неоплазию.
Результаты скрининговой биопсии влияют на тактику дальнейшего лечения и наблюдения.
n Дисплазия высокой степени, обнаруживаемая в неизмененной слизистой оболочке (т.е. не в приподнятых образованиях), является абсолютным показанием к колэктомии. Наличие дисплазии должно быть подтверждено вторым независимым патоморфологом.
n При дисплазии легкой степени в неизмененной слизистой оболочке (не в приподнятых образованиях) решение принимается индивидуально: следует обсудить возможность колэктомии, но приемлемым может быть продолжение регулярного эндоскопического скрининга с сокращением интервала между исследованиями до 1 года.
n Если проксимальнее зоны поражения (которая определяется при эндоскопическом/гистологическом исследовании) обнаруживается аденоматозный полип, то может быть выполнена стандартная полипэктомия с последующим рутинным наблюдением.
n Наличие полипа с дисплазией в участке толстой кишки, пораженной язвенным колитом, не является показанием к колэктомии при условии, что его гистологическое строение соответствует аденоме, и признаки дисплазии отсутствуют в окружающей неизмененной слизистой оболочке или где-либо в кишке, а также в краях удаленного полипа.
Виды хирургических вмешательств
У большинства больных язвенным колитом современная консервативная терапия позволяет контролировать течение воспалительного процесса, однако у 10–30% больных в связи с неэффективностью медикаментозного лечения приходится прибегать к хирургическому вмешательству, направленному на удаление толстой кишки [67, 68]. До начала 1980-х гг. стандартом хирургического лечения была колопроктэктомия с илеостомией, несмотря на эпизодическое использование илеоректального анастомоза. За последние 20 лет новым «золотым стандартом» стала восстановительно-пластическая операция — колопроктэктомия с илеоанальным резервуарным анастомозом (ИАРА) [69, 70]. При успешном выполнении данная операция обеспечивает возможность контролируемой дефекации через задний проход с удовлетворительным качеством жизни: средняя частота дефекации после формирование ИАРА составляет от 4 до 8 раз в сутки [72–74], суточный объем полуоформленного/ жидкого стула составляет около 700 мл/сут (в сравнении с 200 мл/сут у здорового человека) (табл. 20.10).
Выбор вида хирургического лечения
Проведение восстановительно-пластической операции с формированием ИАРА, несмотря на очевидную привлекательность для пациента, возможно не во всех случаях, поскольку ряд факторов ухудшает функциональный исход операции и увеличивает риск осложнений, приводя к необходимости удаления резервуара у 3,5–10,0% больных [75–77].
Таблица 20.10. Методы хирургического лечения язвенного колита
|
С формированием постоянной илеостомы |
С восстановлением дефекации через задний проход | ||
|
1. Колопроктэктомия с фор- |
С формированием ИАРА, |
С формированием ИАРА, | |
|
мированием постоянной |
в 2 этапа: |
в 3 этапа: | |
|
илеостомы по Бруку | |||
|
1. Колопроктэктомия, |
1. Субтотальная резекция обо- | ||
|
|
формирование ИАРА, |
дочной кишки (субтотальная | |
|
|
петлевая илеостомия |
колэктомия), илеостомия | |
|
|
по Торболлу. |
по Торболлу. | |
|
|
2. Закрытие илеостомы |
2. Проктэктомия, формирова- | |
|
|
|
ние ИАРА. | |
|
|
|
3. Закрытие илеостомы | |
* Субтотальная резекция ободочной кишки с формированием илеоректального анастомоза (в исключительных случаях).
Факторы, влияющие на возможность формирования илеоанального резервуарного анастомоза
Несмотря на более высокую частоту сопутствующих заболеваний после 65 лет, само хирургическое вмешательство с формированием ИАРА у лиц старшего возраста безопасно и эффективно [78]. Однако функция анального держания, играющая ключевую роль для нормального функционирования ИАРА, очевидно, ухудшается в старшем возрасте [79]. Кроме того, у пожилых пациентов чаще развиваются осложнения, в частности резервуарит и стриктуры анастомоза [80, 81]. В то же время какой-либо определенный возрастной порог для отказа от формирования ИАРА не определен.
Формирование ИАРА на 30–70% [82–86] повышает риск бесплодия у женщин детородного возраста с язвенным колитом (УД 3b, СР В), вероятно, за счет спаечного процесса с вовлечением маточных труб. Планируемая беременность и молодой возраст женщины не являются противопоказаниями в формированию ИАРА, однако пациентка должна быть предупреждена о потенциальном риске бесплодия. В отдельных случаях возможно рассмотреть вопрос о формировании илеоректального анастомоза в качестве промежуточного этапа хирургического лечения (см. ниже).
Приблизительно у 10% пациентов с колитом даже при изучении операционного материала, полученного при колэктомии, не удается провести дифференциальную диагностику между болезнью Крона и язвенным колитом, в связи с чем им выставляется диагноз недифференцированного неспецифического колита. Решение о формировании ИАРА в таких случаях принимается индивидуально, при этом пациент должен быть предупрежден о рисках неэффективности восстановительно-пластической операции и иных осложнениях, связанных с болезнью Крона.
Очевидными противопоказаниями к формированию ИАРА служат рак толстой кишки и выраженная недостаточность анального сфинктера. Двухи трехэтапное хирургическое лечение с формированием илеоаналь-
ного резервуарного анастомоза
Трехэтапное лечение (с колэктомией на первом этапе) рекомендовано в случаях тяжелой атаки у пациентов, не ответивших на консервативное лечение (УР 4, СР С), или если пациент принимает 20 мг преднизолона в течение более чем 6 нед (УР 4, СР С). Субтотальная колэктомия с илеостомией купирует интоксикацию, обусловленную колитом, что позволяет улучшить общее состояние больного, восстановить метаболизм, а изучение операционного препарата также позволяет уточнить диагноз и исключить болезнь Крона. Субтотальная колэктомия является относительно безопасным вмешательством даже у пациентов в критическом состоянии [87–89], при этом при достаточной квалификации хирурга безопасным является и проведение минимально инвазивных или лапароскопических операций [90, 91].
Илеоректальный анастомоз
Формирование илеоректального анастомоза [92–94] не приводит к исцелению пациента и не исключает возможности рецидива воспаления в прямой кишке и развития рака. Данная операция при язвенном колите может выполняться только в исключительных случаях у женщин, планирующих беременность. Обязательным условием является согласие пациентки на регулярное обследование прямой кишки с биопсией слизистой оболочки [95, 96] (см. раздел «Скрининг колоректального рака»).
Особенности хирургического вмешательства при формировании илеоанального резервуарного анастомоза
Реконструктивно-пластические операции с формированием ИАРА при язвенном колите должны выполняться в специализированных стационарах, поскольку частота осложнений и функциональный исход таких операций существенно зависят от квалификации хирурга (в частности, от количества проведенных аналогичных вмешательств) (УР 4, СР С [96]).
Длина сохраняемой прямой и/или сигмовидной кишки
Если после колэктомии по срочным показаниям при язвенном колите планируется формирование ИАРА, следует сохранить всю прямую кишку и нижнебрыжеечные сосуды (УР 4, СР С). Прямую кишку целесообразно пересечь на уровне мыса (т.е. на уровне «ректосигмоидного перехода») или дополнительно сохранить дистальный отдел сигмовидной кишки (решение принимается оперирующим хирургом). При сохранении дистального отдела сигмовидной кишки она выводится на переднюю брюшную стенку в виде сигмостомы. Последний вариант наиболее безопасен, поскольку при этом в брюшной полости не остается культи
кишки. При пересечении прямой кишки на уровне мыса в течение нескольких дней рекомендуется дренирование культи через задний проход для профилактики несостоятельности швов в связи с накоплением в культе слизи.
В случае сохранения отключенной прямой или прямой и сигмовидной кишки возможно развитие вторичных воспалительных изменений слизистой оболочки по типу колита отключенной кишки. Контролируемые испытания лекарственных средств у больных после колэктомии не проводились, эмпирическое лечение заключается в применении местного месалазина [97], преднизолона, промывании отключенной прямой кишки растворами антисептиков.
Наложение анастомоза при формировании илеоанального резервуарного анастомоза
Сохранение протяженного участка прямой кишки (более 2 см над зубчатой линией) при использовании сшивающего аппарата для формирования ИАРА может быть причиной хронического воспаления в ней с дисфункцией резервуара, а также способствует сохранению риска дисплазии и (очень редко) рака [92]. Максимальная длина аноректальной слизистой оболочки между зубчатой линией и анастомозом не должна превышать 2 см (УР 4, СР С). При невозможности сформировать анастомоз с помощью сшивающего аппарата следует выполнить мукозэктомию и наложить ручной анастомоз. Несмотря на то что при использовании сшивающего аппарата сохраняется небольшой фрагмент слизистой оболочки, риск рака невысок и соответствует таковому при формировании ручного анастомоза (УД 4, СР С). Формирование ИАРА в преобладающем большинстве случаев проводится под прикрытием петлевой илеостомы (УД 3b, СР С).
Наблюдение пациентов с ИАРА
Морфологические изменения эпителиальной выстилки резервуара обычно развиваются через 12–18 мес после закрытия илеостомы и характеризуются уплощением и сокращением числа ворсинок, приводящим к их атрофии («толстокишечная метаплазия») [98, 99], что потенциально связано с риском развития злокачественной трансформации слизистой оболочки резервуара. Кроме того, при наложении аппаратного ИАРА сохраняется небольшой участок слизистой оболочки прямой кишки («манжетка»). Риск развития рака резервуара повышен у пациентов, оперированных по поводу рака или дисплазии на фоне язвенного колита (и при обнаружении дисплазии в операционном материале), и у больных первичным склерозирующим холангитом. Научное обоснование частоты контрольных обследований больных с ИАРА не выполнялось, однако у пациентов с наличием указанных выше факторов риска целесообразно проведение контрольных эндоскопических исследований (резервуароскопии) с биопсией слизистой оболочки не реже 1-го раза в 2 года.
Медикаментозная терапия в период хирургического лечения
Влияние лекарственной терапии на риск хирургических осложнений
Прием преднизолона в дозе более 20 мг в течение более чем 6 нед повышает риск хирургических осложнений [100, 101]. Предоперационный прием азатиоприна не ухудшает исход хирургического лечения [102], в то время как введение инфликсимаба и циклоспорина незадолго до операции может увеличивать частоту послеоперационных осложнений [103, 104], хотя данные по инфликсимабу остаются противоречивыми [105].
Гормональная терапия перед операцией и в раннем послеоперационном периоде
Резкое прекращение терапии ГКС может вызвать синдром отмены (острую недостаточность коры надпочечников, так называемый аддисонический криз), что обусловливает необходимость временного продолжения гормональной терапии после операции до полной отмены. На время оперативного вмешательства и в раннем послеоперационном периоде до возможности приема пациентом ГКС внутрь рекомендуется внутривенное введение ГКС в дозе, эквивалентной 2 мг/кг преднизолона (доза, таким образом, может превышать принимавшуюся до хирургического вмешательства).
На настоящий момент отсутствует надежная научная база для обоснования какой-либо схемы прекращения гормональной терапии после колэктомии по поводу язвенного колита. Доза ГКС для дальнейшего перорального приема в период отмены гормональной терапии определяется длительностью предшествовавшей терапии и величиной использованных доз. Согласно рекомендациям Европейского общества по изучению язвенного колита и болезни Крона (ECCO) [106], в случае если гормональная терапия перед операцией проводилась не более 1 мес, сразу после операции возможно прекращение приема ГКС.
Если перед операцией пациент более 1 мес получал ГКС, после хирургического вмешательства целесообразно перейти с описанной выше высокой парентеральной дозы ГКС (2 мг/кг) на пероральный прием ГКС внутрь в дозе не ниже верхней границы суточной продукции кортизола, т.е. не ниже 20 мг преднизолона. Дальнейшее снижение дозы и отмена ГКС проводятся под наблюдением врача-эндокринолога.
Калоприемники и средства ухода за стомой
Хирургическое лечение язвенного колита неразрывно связано с необходимостью формирования временной или постоянной илеостомы. Существует широкий спектр средств ухода за илеостомой, позволяющих пациенту практически реабилитироваться социально. К средствам медицинской реабилитации пациента с илеостомой (или колостомой) относятся клеящиеся (адгезивные) калоприемники и вспомогательные принадлежности к ним.
Все калоприемники можно разделить на два основных вида — однокомпонентные и двухкомпонентные. Наряду с ними для ухода за стомой используются вспомогательные средства (лечебная или адгезивная паста, порошок, дезодоранты, поглотители запаха, защитные пленки, уплотнительные кольца, стержни под двуствольную стому, ирригаторы, абсорбенты и др.) и средства ухода за кожей вокруг стомы. Стомированные пациенты нуждаются в комплексной медико-социальной программе реабилитации. Ее основой является индивидуальная программа реабилитации пациента — комплекс мероприятий, направленных на компенсацию нарушенных или утраченных функций организма и восстановление способностей к выполнению определенных видов деятельности.
Резервуарит и другие осложнения хирургического лечения с формированием тонкокишечного резервуара
Резервуарит представляет собой неспецифическое воспаление тонкокишечного резервуара и наиболее частое осложнение ИАРА. Частота его возникновения колеблется в широком диапазоне от 15 до 50% в течение 10 лет после формирования ИАРА в крупных специализированных центрах. Такие различия могут быть обусловлены существенно большим риском резервуарита при язвенном колите, превышающим частоту этого осложнения при формировании ИАРА по поводу других заболеваний (в частности, САТК [109, 110]).
Диагностика резервуарита
Диагноз устанавливается на основании клинических симптомов, а также характерных эндоскопических и гистологических изменений (УД 3а, СР B). Риск резервуарита, по-видимому, выше у некурящих и принимающих нестероидные противовоспалительные средства лиц, а также у пациентов с протяженным язвенным колитом и внекишечными проявлениями (первичный склерозирующий холангит) (УД 3b, СР D).
К симптомам резервуарита относятся учащение дефекаций, в том числе и жидкими каловыми массами, спастические боли в животе, недержание стула (может быть и самостоятельным симптомом) и тенезмы. В редких случаях возможно возникновение лихорадки и внекишечных проявлений. Выделение крови не является характерным и, как правило, возникает при воспалении сохраненной слизистой оболочки прямой кишки (УД 1с, СР В).
У пациентов с симптомами, соответствующими резервуариту, для подтверждения диагноза необходимо провести резервуароскопию с биопсией слизистой оболочки резервуара. У больных ИАРА нередко имеется стриктура резервуарно-анального анастомоза, поэтому для резервуароскопии предпочтительнее использовать фистулоскоп, а не колоноскоп. Всегда следует предпринять попытку провести аппарат в приводящую петлю подвздошной кишки. Следует отметить, что при достижении клинической ремиссии рутинной резервуароскопии не требуется (УД5, СР D).
Эндоскопические признаки, соответствующие резервуариту, включают диффузную эритему, которая может быть очаговой, в отличие от таковой при язвенном колите. Характерными эндоскопическими проявлениями также бывают отек и зернистость слизистой оболочки, спонтанная и контактная кровоточивость, эрозии и изъязвления. Эрозии и/или язвы по линии скобок не обязательно свидетельствуют о резервуарите. Биоптаты следует брать из слизистой оболочки резервуара и приводящей петли над резервуаром, но не из линии скобок.
Гистологические проявления резервуарита также неспецифичны и включают признаки острого воспаления с полиморфно-ядерной лейкоцитарной инфильтрацией, крипт-абсцессами и изъязвлениями на фоне хронической воспалительной инфильтрации.
Осложнения резервуарита включают абсцессы, свищи, стеноз резервуарно-анального анастомоза и аденокарциному резервуара. Последнее осложнение встречается исключительно редко и почти всегда при выявленной дисплазии или раке в операционном препарате, полученном при выполнении колэктомии.
Дифференциальную диагностику при подозрении на резервуарит проводят с синдромом раздраженного резервуара, ишемическими поражениями, болезнью Крона и другими редкими причинами дисфункции резервуара, такими как коллагенозный, цитомегаловирусный и Cl. difficileассоциированный резервуарит. Следует учитывать возможность развития неспецифического илеита, вызываемого приемом нестероидных противовоспалительных средств и синдрома избыточного бактериального роста.
Лечение резервуарита и поддержание ремиссии
Основными препаратами, применяемыми для лечения резервуарита, остаются антибиотики, что позволяет классифицировать резервуарит как антибиотикочувствительный, антибиотикозависимый и антибиотикорезистентный. Первая линия терапии включает 14-дневный курс перорального метронидазола (15–20 мг/кг в сутки) или ципрофлоксацина (1000 мг/сут). Нежелательные явления значительно чаще отмечаются при приеме метронидазола. При отсутствии эффекта или при развитии зависимости от приема указанных препаратов возможно назначение резервных препаратов — рифаксимина (2000 мг/сут), тинидазола, ректальных ГКС, ректальных препаратов месалазина, азатиоприна. В случаях антибиотикорезистентного резервуарита возможно назначение перорального будесонида (9 мг) в течение 8 нед.
Обязательное условие эффективной терапии резистентного резервуарита — надежное исключение альтернативных причин дисфункции резервуара.
Воспаление слизистой оболочки сохраненного участка прямой кишки и синдром раздраженного резервуара
Другим потенциальным осложнением ИАРА является воспаление слизистой оболочки прямой кишки, сохраняемой при наложении аппарат-
ного анастомоза. Лечение воспаления «манжетки» проводится свечами месалазина 500 мг 2 раза в сутки и/или ректальными ГКС.
Синдром раздраженного резервуара [111] представляет собой функциональное расстройство, симптомы которого совпадают с проявлениями резервуарита. Встречается у пациентов, принимавших анксиолитики или антидепрессанты до колэктомии, что косвенно свидетельствует о проявлениях у таких пациентов синдрома раздраженного кишечника (СРК) до операции. Методы лечения этих двух функциональных расстройств совпадают и включают психотерапевтическую помощь и назначение антидепрессантов, назначение пищевых волокон, противодиарейных препаратов, спазмолитиков, а также неабсорбируемых антибиотиков для коррекции синдрома избыточного бактериального роста.
Прогноз
Риск тяжелого обострения язвенного колита в течение жизни составляет 15%, при этом вероятность тяжелой атаки выше у больных с тотальным поражением толстой кишки. При проведении адекватной противорецидивной терапии в течение 5 лет обострений удается избежать у половины пациентов, а в течение 10 лет — у 20% больных. В течение 1 года после постановки диагноза вероятность колэктомии составляет 4–9% (при тяжелой атаке — около 50%), в дальнейшем с каждым годом заболевания риск колэктомии увеличивается на 1%. Факторами риска агрессивного течения язвенного колита являются прогрессирование поражения от дистального (проктита) к тотальному, первичный склерозирующий холангит, а также детский и подростковый возраст на момент начала заболевания.
Критерии оценки качества помощи в стационаре представлены в таблице 20.11. Для оценки качества медицинской помощи используют временные, процессуальные и профилактирующие критерии. Временные характеризуют своевременность оказания определенных этапов медицинской помощи. Выполнение пациенту ряда медицинских манипуляций, инструментальных и лабораторных исследований, необходимых для качественного оказания медицинской помощи, оценивают в процессуальных критериях. Для анализа мероприятий, направленных на предотвращение развития осложнений, используют профилактирующие критерии.
Таблица 20.11. Критерии оценки качества медицинской помощи в стационаре больным воспалительными заболеваниями кишечника (0 — нет, 1 — да)
|
Клинические рекомендации |
Временные |
Процессуальные |
Профилактирующие |
|
Клинические |
Установка |
Пальцевое обследование пря- |
Отсутствие осложне- |
|
рекомендации |
клинического |
мой кишки: 0/1. |
ний: |
|
по диагности- |
диагноза |
Илеоколоноскопия в течение |
• пневмония: 0/1; |
|
ке и лечению взрослых |
в течение 72 ч: 0/1 |
госпитализации или в течение 6 мес до госпитализации: 0/1. |
• тромбоэмболия: 0/1; |
Табл. 20.11. Окончание
|
Клинические рекомендации |
Временные |
Процессуальные |
Профилактирующие |
|
больных язвенным колитом (код по МКБ — К51) |
|
Исследование пассажа бариевой взвеси по кишечнику: 0/1. УЗИ кишечника: 0/1. Определение группы крови: 0/1. Исследование крови на сифилис, вирусный гепатит В, вирусный гепатит С: 0/1. Клинический анализ крови; биохимический анализ крови; клинический анализ мочи; коагулограмма: 0/1. Метод консервативного лечения в соответствии с установленным диагнозом и клиническими рекомендациями: 0/1. Метод оперативного лечения при неэффективности консервативной терапии в соответствии с клиническими рекомендациями: 0/1. Метод анестезии в соответствии с объемом оперативного лечения: 0/1 |
• гипергликемическая кома: 0/1; • летальный исход: 0/1 |
Литература
1. Гастроэнтерология: Национальное руководство / Под ред. В.Т. Ивашкина, Т.Л. Лапиной. — М.: ГЭОТАР-Медиа, 2008. — 754 c.
2. Воробьев Г.И., Халиф И.Л. Неспецифические воспалительные заболевания кишечника. — М.: Миклош, 2008.
3. Marchal J., Hilsden R. Environment and epidemiology of inflammatory bowel disease // Inflammatory Bowel Disease / Eds J. Satsangi., L. Sutherland — London: Churchill Livingstone, 2003. — P. 17–28.
4. Irvine E.J., Farrokhyar F., Swarbick E.T. Z critical review of epidemiological studies in inflammatory bowel disease // Scand. J. Gastroenterol. — 2001. — Vol. 36, N 1. — P. 2–15.
5. OCEBM Levels of Evidence Working Group. The Oxford 2011 Levels of Evidence. — Oxford Centre for Evidence-Based Medicine, 2011.
6. Dignass A. et al. Second EUROPEAN evidence-based Consensus on the diagnosis and management of ulcerative colitis: Definitions and diagnosis // J. Crohns Colitis. — 2012. — Vol. 6. — P. 965–990.
7. Travis S.P., Dinesen L. Remission in trials of ulcerative colitis: what does it mean? // Pract. Gastroenterol. — 2010. — Vol. 30. — P. 17–20.
8. D’Haens G. et al. A review of activity indices and efficacy end points for clinical trials of medical therapy in adults with ulcerative colitis // Gastroenterology. — 2007. — Vol. 132. — P. 763–786.
9. Katsanos K.H., Vermeire S., Christodoulou D.K. et al. Dysplasia and cancer in inflammatory bowel disease 10 years after diagnosis: results of a populationbased European collaborative follow-up study // Digestion. — 2007. — Vol. 75. — P. 113–121.
10. Silverberg M.S. et al. Toward an integrated clinical, molecular and serological
classification of inflammatory bowel disease: report of a working party of the 2005 Montreal World Congress of Gastroenterology // Can. J. Gastroenterol. — 2005. — Vol. 19. — Suppl. A. — P. 5–36.
11. Truelove S.C. et al. Cortisone in ulcerative colitis; final report on a therapeutic trial // Br. Med. J. — 1955. — Vol. 2. — P. 1041–1048.
12. Schroeder K.W., Tremaine W.J., Ilstrup D.M. Coated oral 5-aminosalicylic acid therapy for mildly to moderately active ulcerative colitis. A randomized study // N. Engl. J. Med. — 1987. — Vol. 317. — P. 1625–1629.
13. Чашкова Е.Ю., Владимирова А.А., Неустроев В.Г. и др. Воспалительные
заболевания толстой кишки — аспекты диагностики // Бюл. Вост.-Сибир. науч. центра СО РАМН. — 2011. — Т. 2, № 4. — С. 209–221.
14. Григорьева Г.А., Мешалкина Н.Ю. О проблеме системных проявлений воспалительных заболеваний кишечника // Фарматека. — 2011. — № 15. — С. 44–49.
15. Issa M., Vikayapal A., Gracham M.B. et al. Impact of Clostridium difficile in
inflammatory bowel disease patients // Clin. Gastroenterol. Hepatol. — 2007. — Vol. 5. — P. 345–351.
16. Rodeman J.F., Dubberke E.R., Reske K.A. et al. Incidence of Clostridium difficile in inflammatory bowel disease // Clin. Gastroenterol. Hepatol. — 2007. — Vol. 5. — P. 339–344.
17. Issa M., Ananthakrishnan A.N., Binion D.G. Clostridium difficile and
inflammatory bowel disease // Inflamm. Bowel Dis. — 2008. — Vol. 14. — P. 1432–1442.
18. Nguyen G.C., Kaplan G.G., Harris M.L. et al. A national survey of the prevalence and impact of Clostridium difficile infection among hospitalized inflammatory bowel disease patients // Am. J. Gastroenterol. — 2008. — Vol. 103. — P. 1443–1450.
19. Mindenmark M., Larsson A. Rulling out IBD estimation of the possible
economic effects of pre-endoscopic screening with F-calprotectin // Clin. Biochem. — 2012. — Vol. 45. — P. 552–555.
20. Costa F., Mumolo M.G., Bellini M. et al. Role of faecal calprotectin as noninvasive marker of intestinal inflammation // Dig. Liver Dis. — 2003. — Vol. 35. — P. 642–647.
21. Корнеева О.И., Ивашкин В.Т. Антибиотикоассоциированный колит:
патоморфология, клиника, лечение // Рос. журн. гастроэнтерол., гепатол., колопроктол. — 2007. — Т. 17, № 3. — С. 65–71.
22. Ивашкин В.Т., Шептулин А.А., Шифрин О.С. и др. Микроскопический колит: клинические формы, диагностика, лечение // Рос. журн. гастроэнтерол., гепатол., колопроктол. — 2006. — Т. 16, № 6. — С. 56–60.
23. Голованчикова В.М., Шифрин О.С., Ивашкин В.Т. Современные подходы к лечению хронических воспалительных заболеваний кишечника // Рос. мед. вести. — 2009. — Т. 14, № 3. — С. 29–37.
24. Белоусова Е.А., Никитина Н.В., Цодикова О.М. Лечение язвенного колита легкого и среднетяжелого течения // Фарматека. — 2013. — № 2. — С. 42–46.
25. Халиф И.Л. Лечебная тактика при язвенном колите // Рос. журн. гастроэнтерол., гепатол., колопроктол. — 2006. — Т. 16, № 3. — С. 58–62.
26. Халиф И.Л. Принципы лечения язвенного колита (рекомендации российской группы по изучению воспалительных заболеваний кишечника) // Колопроктология. — 2006. — № 2. — С. 31–33.
27. Su C., Lewis J.D., Goldberg B., Brensinger C., Lichtenstein G.R. A metaanalysis of the placebo rates of remission and response in clinical trials of active ulcerative colitis // Gastroenterology. — 2007. — Vol. 132. — P. 516–526.
28. Marshall J.K., Thabane M., Steinhart A.H. et al. Rectal 5-aminosalicylic acid for induction of remission in ulcerative colitis // Cochrane Database Syst. Rev. — 2010. — CD004115.
29. Marshall J.K., Irvine E.J. Rectal corticosteroids versus alternative treatments in ulcerative colitis: a meta-analysis // Gut. — 1997. — Vol. 40. — P. 775–781.
30. Lamet M. A multicenter, randomized study to evaluate the efficacy and safety of mesalamine suppositories 1 g at bedtime and 500 mg twice daily in patients with active mild-to-moderate ulcerative proctitis // Dig. Dis. Sci. — 2011. — Vol. 56. — P. 513–522.
31. Safdi M., DeMicco M, Sninsky C. et al. A double-blind comparison of oral versus rectal mesalamine versus combination therapy in the treatment of distal ulcerative colitis // Am. J. Gastroenterol. — 1997. — Vol. 92. — P. 1867–1871.
32. Regueiro M., Loftus Jr.E.V., Steinhart A.H., Cohen R.D. Medical management of left-sided ulcerative colitis and ulcerative proctitis: critical evaluation of therapeutic trials // Inflamm. Bowel Dis. — 2006. — Vol. 12. — P. 979–994.
33. Ford A.C., Achkar J.-P., Khan K.J. et al. Efficacy of 5-aminosalicylates in ulcerative colitis: systematic review and meta-analysis // Am. J. Gastroenterol. — 2011. — Vol. 106. — P. 601–616.
34. Kane S.V., Bjorkman D.J. The efficacy of oral 5-ASAs in the treatment of active ulcerative colitis: a systematic review // Rev. Gastroenterol. Disord. — 2003. — Vol. 3. — P. 210–218.
35. Sutherland L., Macdonald J.K. Oral 5-aminosalicylic acid for induction of remission in ulcerative colitis // Cochrane Database Syst. Rev. — 2006. — P. CD000543.
36. Gisbert J.P., Linares P.M., McNicholl A.G. et al. Meta-analysis: the efficacy of azathioprine and mercaptopurine in ulcerative colitis // Aliment. Pharmacol. Ther. — 2009. — Vol. 30. — P. 126–137.
37. Panaccione R., Ghosh S., Middleton S. et al. Infliximab, azathioprine or infliximab + azathioprine for treatment of moderate to severe ulcerative colitis. The UC SUCCESS trial // J. Crohns Colitis. — 2011. — Vol. 5. — P. 13.
38. Gonzalez-Huix F., Fernandez-Banares F., Esteve-Comas M. et al. Enteral versus parenteral nutrition as adjunct therapy in acute ulcerative colitis // Am. J. Gastroenterol. — 1993. — Vol. 88. — P. 227–232.
39. Khan K.J., Ullman T.A., Ford A.C. et al. Antibiotic therapy in inflammatory bowel disease: a systematic review and meta-analysis // Am. J. Gastroenterol. — 2011. — Vol. 106. — P. 661–673.
40. Ohkusa T., Kato K., Terao S. et al. Newly developed antibiotic combination therapy for ulcerative colitis: a double-blind placebo-controlled multicenter trial // Am. J. Gastroenterol. — 2010. — Vol. 105. — P. 1820–1829.
41. Järnerot G., Hertervig E., Friis-Liby I. et al. Infliximab as rescue therapy in severe to moderately severe ulcerative colitis: a randomized, placebo-controlled study // Gastroenterology. — 2005. — Vol. 128. — P. 1805–1811.
42. Lees C.W., Heys D., Ho G.T. et al. A retrospective analysis of the efficacy and safety of infliximab as rescue therapy in acute severe ulcerative colitis // Aliment. Pharmacol. Ther. — 2007. — Vol. 26. — P. 411–419.
43. Van Assche G., D’Haens G., Noman M. et al. Randomized, double-blind comparison of 4 mg/kg versus 2 mg/kg intravenous cyclosporine in severe ulcerative colitis // Gastroenterology. — 2003. — Vol. 125. — P. 1025–1031.
44. Sjoberg M., Walch A., Meshkat M. et al. Infliximab or cyclosporine as rescue therapy in hospitalized patients with steroid-refractory ulcerative colitis: a retrospective observational study // Inflamm. Bowel Dis. — 2012. — Vol. 18, N 2. — P. 212–218.
45. Sokol H., Seksik P., Carrat F. et al. Usefulness of co-treatment with immunomodulators in patients with inflammatory bowel disease treated with scheduled infliximab maintenance therapy // Gut. — 2010. — Vol. 59. — P. 1363–1368.
46. Reinisch W., Sandborn W.J., Rutgeerts P. et al. Long-term infliximab maintenance therapy for ulcerative colitis: the ACT-1 and -2 extension studies // Inflamm. Bowel Dis. — 2012. — Vol. 18. — P. 201–211.
47. Chebli L.A., LDdM Chaves, Pimentel F.F. et al. Azathioprine maintains longterm steroid-free remission through 3 years in patients with steroid-dependent ulcerative colitis // Inflamm. Bowel Dis. — 2010. — Vol. 16. — P. 613–619.
48. Randall J.S.B., Warren B.F., Travis S.P. et al. Delayed surgery for acute severe colitis is associated with increased risk of postoperative complications // Br. J. Surg. — 2010. — Vol. 97. — P. 404–409.
49. Lennard-Jones J.E., Ritchie J.K., Hilder W., Spicer C.C. Assessment of severity in colitis: a preliminary study // Gut. — 1975. — Vol. 16. — P. 579–584.
50. Lindgren S.C., Flood L.M., Kilander A.F. et al. Early predictors of glucocorticosteroid treatment failure in severe and moderately severe attacks of ulcerative colitis // Eur. J. Gastroenterol. Hepatol. — 1998. — Vol. 10. — P. 831– 835.
51. Benazzato L., D’Inca R, Grigoletto F. et al. Prognosis of severe attacks in ulcerative colitis: effect of intensive medical treatment // Dig. Liver Dis. — 2004. — Vol. 36. — P. 461–466.
52. Almer S., Bodemar G., Franzen L. et al. Use of air enema radiography to assess depth of ulceration during acute attacks of ulcerative colitis // Lancet. — 1996. — Vol. 347. — P. 1731–1735.
53. Carbonnel F., Lavergne A., Lemann M. et al. Colonoscopy of acute colitis. A safe and reliable tool for assessment of severity // Dig. Dis. Sci. — 1994. — Vol. 39. — P. 1550–1557.
54. Ferrante M., Vermeire S., Katsanos K.H. Predictors of early response to infliximab in patients with ulcerative colitis // Inflamm. Bowel Dis. — 2007. — Vol. 13, N 2. — P. 123–128.
55. Gonzalez-Lama Y., Fernandez-Blanco I., Lopez-SanRoman A. Open-label infliximab therapy in ulcerative colitis: a multicenter survey of results and predictors
of response // Hepatogastroenterology. — 2008. — Vol. 55, N 86–87. — P. 1609– 1614.
56. Fasanmade A.A., Adedokun O.J., Olson A. et al. Serum albumin concentration: a predictive factor of infliximab pharmacokinetics and clinical response in patients with ulcerative colitis // Int. J. Clin. Pharmacol. Ther. — 2010. — Vol. 48, N 5. — P. 297–308.
57. Oussalah A., Evesque L., Laharie D., Roblin X. A multicenter experience with infliximab for ulcerative colitis: outcomes and predictors of response, optimization, colectomy, and hospitalization // Am. J. Gastroenterol. — 2010. — Vol. 105, N 12. — P. 2617–2625.
58. Головенко A.O., Халиф И.Л., Головенко О.В., Веселов В.В. Предикторы эффективности инфликсимаба у больных с тяжелой атакой язвенного колита // Рос. журн. гастроэнтерол., гепатол., колопроктол. — 2013. — № 3. — С. 65–74.
59. American Thoracic Society/Centers for Disease Control and Prevention/ Infectious Diseases Society of America: controlling tuberculosis in the United States // Am. J. Respir. Crit. Care Med. — 2005. — Vol. 172, N 9. — P. 1169–1227.
60. Rahier J.F. et al. European evidence-based Consensus on the prevention, diagnosis and management of opportunistic infections inflammatory bowel disease // J. Crohns Colitis. — 2009. — Vol. 3, N 2. — P. 47–91.
61. Ardizzone S., Maconi G., Russo A. et al. Randomised controlled trial of azathioprine and 5-aminosalicylic acid for treatment of steroid dependent ulcerative colitis // Gut. — 2006. — Vol. 55.
62. Panaccione R., Ghosh S., Middleton S. et al. Infliximab, azathioprine or infliximab + azathioprine for treatment of moderate to severe ulcerative colitis. The UC SUCCESS trial // J. Crohns Colitis. — 2011. — Vol. 5. — abstract 13.
63. Eaden J.A., Abrams K.R., Mayberry J.F. The risk of colorectal cancer in ulcerative colitis: a meta-analysis // Gut. — 2001. — Vol. 48. — P. 526–535.
64. Jess T., Loftus E.V.Jr, Velayos F.S. et al. Risk of intestinal cancer in inflammatory bowel disease: a population-based study from olmsted county, Minnesota // Gastroenterology. — 2006. — Vol. 130. — P. 1039–1046.
65. Bergeron V., Vienne A., Sokol H. et al. Risk factors for neoplasia in inflammatory bowel disease patients with pancolitis // Am. J. Gastroenterol. — 2010 [advance online publication, 15 June 2010].
66. Rutter M., Saunders B., Wilkinson K. et al. Severity of inflammation is a risk factor for colorectal neoplasia in ulcerative colitis // Gastroenterology. — 2004. — Vol. 126. — P. 451–459.
67. Справочник по колопроктологии / Под ред. Ю.А. Шелыгина, Л.А. Благодарного. — М.: Литтерра, 2012. — С. 460–522.
68. Travis S.P.L., Farrant J.M., Ricketts C. et al. Predicting outcome in severe ulcerative colitis // Gut. — 1996. — Vol. 38. — P. 905–910.
69. Richards D.M., Hughes S.A., Irving M.H., Scott N.A. Patient quality of life after successful restorative proctocolectomy is normal // Colorectal Dis. — 2001. — Vol. 3. — P. 223–226.
70. McLaughlin S.D., Clark S.K., Thomas-Gibson S. et al. Guide to endoscopy of the ileo-anal pouch following restorative proctocolectomy with ileal pouch-anal anastomosis; indications, technique, and management of common findings // Inflamm. Bowel Dis. — 2009. — Vol. 15. — P. 1256–1263.
71. Berndtsson I., Oresland T. Quality of life before and after proctocolectomy and IPAA in patients with ulcerative proctocolitis — a prospective study // Colorectal Dis. — 2003. — Vol. 5. — P. 173–179.
72. Marcello P.W., Roberts P.L., Schoetz D.J.Jr et al. Long-term results of the ileoanal pouch procedure // Arch. Surg. — 1993. — Vol. 128. — P. 500–503; discussion 503–4.
73. Sagar P.M., Pemberton J.H. Ileo-anal pouch function and dysfunction // Dig. Dis. — 1997. — Vol. 15. — P. 172–188.
74. Meagher A.P., Farouk R., Dozois R.R. et al. J ileal pouch-anal anastomosis for chronic ulcerative colitis: complications and long-term outcome in 1310 patients // Br. J. Surg. — 1998. — Vol. 85. — P. 800–803.
75. Setti-Carraro P., Ritchie J.K., Wilkinson K.H. et al. The first 10 years’ experience of restorative proctocolectomy for ulcerative colitis // Gut. — 1994. — Vol. 35. — P. 1070–1075.
76. Fazio V.W., Ziv Y., Church J.M. et al. Ileal pouch-anal anastomoses complications and function in 1005 patients // Ann. Surg. — 1995. — Vol. 222. — P. 120–127.
77. Belliveau P., Trudel J., Vasilevsky C.A. et al. Ileoanal anastomosis with reservoirs: complications and long-term results // Can. J. Surg. — 1999. — Vol. 42. — P. 345–352.
78. Pinto R.A., Canedo J., Murad-Regadas S. et al. Ileal pouch-anal anastomosis in elderly patients: is there a difference in morbidity compared with younger patients? // Colorectal Dis. — 2011. — Vol. 13. — P. 177–183.
79. Church J.M. Functional outcome and quality of life in an elderly patient with an ileal pouch-anal anastomosis: a 10-year follow up // Aust. N.Z. J. Surg. — 2000. — Vol. 70. — P. 906–907.
80. Chapman J.R., Larson D.W., Wolff B.G. et al. Ileal pouch-anal anastomosis: does age at the time of surgery affect outcome? // Arch. Surg. — 2005. — Vol. 140. — P. 534–540.
81. Delaney C.P., Dadvand B., Remzi F.H. et al. Functional outcome, quality of life, and complications after ileal pouch-anal anastomosis in selected septuagenarians // Dis. Colon Rectum. — 2002. — Vol. 45. — P. 890–894.
82. Olsen K.O., Joelsson M., Laurberg S., Oresland T. Fertility after ileal pouchanal anastomosis in women with ulcerative colitis // Br. J. Surg. — 1999. — Vol. 86. — P. 493–495.
83. Ording O.K., Juul S., Berndtsson I. et al. Ulcerative colitis: female fecundity before diagnosis, during disease, and after surgery compared with a population sample // Gastroenterology. — 2002. — Vol. 122. — P. 15–19.
84. Gorgun E., Remzi F.H., Goldberg J.M. et al. Fertility is reduced after restorative proctocolectomy with ileal pouch anal anastomosis: a study of 300 patients // Surgery. — 2004. — Vol. 136. — P. 795–803.
85. Johnson P., Richard C., Ravid A. et al. Female infertility after ileal pouch-anal anastomosis for ulcerative colitis // Dis. Colon Rectum. — 2004. — Vol. 47. — P. 1119–1126.
86. Oresland T., Palmblad S., Ellstrom M. et al. Gynaecological and sexual function related to anatomical changes in the female pelvis after restorative proctocolectomy // Int. J. Colorectal Dis. — 1994. — Vol. 9. — P. 77–81.
87. Alves A., Panis Y., Bouhnik Y. et al. Subtotal colectomy for severe acute colitis: a 20-year experience of a tertiary care center with an aggressive and early surgical policy // J. Am. Coll. Surg. — 2003. — Vol. 197. — P. 379–385.
88. Berg D.F., Bahadursingh A.M., Kaminski D.L., Longo W.E. Acute surgical emergencies in inflammatory bowel disease // Am. J. Surg. — 2002. — Vol. 184. — P. 45–51.
89. Hyman N.H., Cataldo P., Osler T. Urgent subtotal colectomy for severe inflammatory bowel disease // Dis. Colon Rectum. — 2005. — Vol. 48. — P. 70–73.
90. Holubar S.D., Larson D.W., Dozois E.J. et al. Minimally invasive subtotal colectomy and ileal pouch-anal anastomosis for fulminant ulcerative colitis: a reasonable approach? // Dis. Colon Rectum. — 2009. — Vol. 52. — P. 187–192.
91. Marceau C., Alves A., Ouaissi M. et al. Laparoscopic subtotal colectomy for acute or severe colitis complicating inflammatory bowel disease: a case-matched study in 88 patients // Surgery. — 2007. — Vol. 141. — P. 640.
92. Annibali R., Oresland T., Hulten L. Does the level of stapled ileoanal anastomosis influence physiologic and functional outcome? // Dis. Colon Rectum. — 1994. — Vol. 37. — P. 321–329.
93. Bottle A., Aylin P., Clark S.K. A et al. Volume analysis of outcome following restorative proctocolectomy // Br. J. Surg. — 2011. — Vol. 98. — P. 408–417.
94. Tekkis P.P., Fazio V.W., Lavery I.C. et al. Evaluation of the learning curve in ileal pouch-anal anastomosis surgery // Ann. Surg. — 2005. — Vol. 241. — P. 262–268.
95. Lepisto A. Fate of the rectum after colectomy with ileorectal anastomosis in ulcerative colitis // Scand. J. Surg. — 2005. — Vol. 94. — P. 40–42.
96. Burns E.M., Bottle A., Aylin P. et al. Volume analysis of outcome following restorative proctocolectomy // Br. J. Surg. — 2011. — Vol. 98. — P. 408–417.
97. Edwards C.M., George B., Warren B.F. Diversion colitis: new light through old windows // Histopathology. — 1999. — Vol. 35, N 1. — P. 86–87.
98. Shepherd N.A., Jass J.R., Duval I. et al. Restorative proctocolectomy with ileal reservoir: pathological and histochemical study of mucosal biopsy specimens // J. Clin. Pathol. — 1987. — Vol. 40. — P. 601–607.
99. Setti Carraro P.G., Talbot I.C., Nicholls J.R. Patterns of distribution of endoscopic and histological changes in the ileal reservoir after restorative proctocolectomy for ulcerative colitis. A long-term follow-up study // Int. J. Colorectal Dis. — 1998. — Vol. 13. — P. 103–107.
100. Ferrante M., D’Hoore A., Vermeire S. et al. Corticosteroids but not infliximab increase short-term postoperative infectious complications in patients with ulcerative colitis // Inflamm. Bowel Dis. — 2009. — Vol. 15. — P. 1062–1070.
101. Lake J.P., Firoozmand E., Kang J.C. et al. Effect of high-dose steroids on anastomotic complications after proctocolectomy with ileal pouch-anal anastomosis // J. Gastrointest. Surg. — 2004. — Vol. 8. — P. 547–551.
102. Mahadevan U., Loftus E.V.Jr, Tremaine W.J. et al. Azathioprine or 6-mercaptopurine before colectomy for ulcerative colitis is not associated with increased postoperative complications // Inflamm. Bowel Dis. — 2002. — Vol. 8. — P. 311–316.
103. Pugliese D., Armuzzi A., Rizzo G. et al. Effect of anti-TNF-alpha treatment on short-term post-operative complications in patients with inflammatory bowel disease // Gut. — 2010. — Vol. 59. — Suppl. III. — P. A13.
104. Subramanian V., Pollok R.C., Kang J.Y., Kumar D. Systematic review of postoperative complications in patients with inflammatory bowel disease treated with immunomodulators // Br. J. Surg. — 2006. — Vol. 93. — P. 793–799.
105. Yang Z., Wu Q., Wang F. et al. Meta-analysis: effect of preoperative infliximab use on early postoperative complications in patients with ulcerative colitis undergoing abdominal surgery // Aliment. Pharmacol. Ther. — 2012. — Vol. 36, N 10. — P. 922–928. doi: 10.1111/apt.12060. Epub 2012, Sep 24.
106. Dignass A. et al. Second European evidence-based consensus on the diagnosis and management of ulcerative colitis part 2: current management // J. Crohns Colitis. — 2012. — Vol. 6, N 10. — P. 991–1030.116.
107. Simchuk E.J,, Thirlby R.C. Risk factors and true incidence of pouchitis in patients after ileal pouch-anal anastomoses // World J. Surg. — 2000. — Vol. 24. — P. 851–856.
108. Stahlberg D., Gullberg K., Liljeqvist L. et al. Pouchitis following pelvic pouch operation for ulcerative colitis. Incidence, cumulative risk, and risk factors // Dis. Colon Rectum. — 1996. — Vol. 39. — P. 1012–1018.
109. Penna C., Tiret E., Kartheuser A. et al. Function of ileal J pouch-anal anastomosis in patients with familial adenomatous polyposis // Br. J. Surg. — 1993. — Vol. 80. — P. 765–767.
110. Tjandra J.J., Fazio V.W., Church J.M. et al. Similar functional results after restorative proctocolectomy in patients with familial adenomatous polyposis and mucosal ulcerative colitis // Am. J. Surg. — 1993. — Vol. 165. — P. 322–325.
111. Shen B., Achkar J.P., Lashner B.A. Irritable pouch syndrome: a new category of diagnosis for symptomatic patients with ileal pouch-anal anastomosis // Am. J. Gastroenterol. — 2002. — Vol. 97, N 4. — P. 972–977.
СИНДРОМ РАЗДРАЖЕННОГО КИШЕЧНИКА
Введение
Синдром раздраженного кишечника (СРК) представляет собой функциональное расстройство кишечника, при котором боль или дискомфорт в животе связаны с актом дефекации или изменениями его частоты. Наиболее частыми симптомами также являются метеоризм и расстройства процесса дефекации.
Как и в случае других функциональных нарушений ЖКТ, диагноз СРК устанавливается на основании симптомов и при отсутствии выраженных органических причин. Для СРК невозможно определить однозначный набор симптомов, поскольку большинство проявлений могут эпизодически отмечаться и у здоровых лиц, поэтому для подтверждения диагноза обязательно наличие хронической симптоматики.
Наличие СРК не сопровождается повышением риска колоректального рака или ВЗК, а равно и увеличением смертности. В то же время возможен «перехлест» СРК с другими заболеваниями ЖКТ, в частности с гастроэзофагеальной рефлюксной болезнью, функциональной неязвенной диспепсией и функциональным запором.
Несмотря на то что СРК не оказывает влияния на смертность, заболевание может существенно ухудшать качество жизни пациентов [1] и приводит к значительным прямым и непрямым затратам на его лечение и диагностику [2].
Рекомендации по диагностике и лечению больных СРК служат руководством для практических врачей, осуществляющих ведение таких пациентов, и подлежат регулярному пересмотру в соответствии с новыми данными научных исследований.
При составлении настоящих рекомендаций использованные научные источники классифицировались в зависимости от их доказательной ценности согласно общепринятой классификации Оксфордского центра доказательной медицины (табл. 21.1).
ВАЛИДИЗАЦИЯ РЕКОМЕНДАЦИЙ
Данные рекомендации в предварительной версии были рецензированы независимыми экспертами, которых попросили прокомментировать,
Таблица 21.1. Уровни доказательности и степени рекомендаций на основании руководства Оксфордского центра доказательной медицины [3]
|
Уровень |
Диагностическое исследование |
Терапевтическое исследование |
|
1а |
Систематический обзор гомогенных диагностических исследований 1-го уровня |
Систематический обзор гомогенных РКИ |
|
1b |
Валидизирующее когортное исследование с качественным «золотым стандартом» |
Отдельное РКИ (с узким доверительным интервалом) |
|
1с |
Специфичность или чувствительность столь высокие, что положительный или отрицательный результат позволяет исключить/установить диагноз |
Исследование «Всё или ничего» |
|
2а |
Систематический обзор гомогенных диагностических исследований >2-го уровня |
Систематический обзор (гомогенных) когортных исследований |
|
2b |
Разведочное когортное исследование с качественным «золотым стандартом» |
Отдельное когортное исследование (включая РКИ низкого качества; т.е. с <80% пациентов, прошедших контрольное наблюдение) |
|
2с |
Нет |
Исследование «исходов»; экологические исследования |
|
За |
Систематический обзор гомогенных исследований уровня 3b и выше |
Систематический обзор гомогенных исследований «случай– контроль» |
|
3b |
Исследование с непоследовательным набором или без проведения исследования «золотого стандарта» у всех испытуемых |
Отдельное исследование «случай– контроль» |
|
4 |
Исследование «случай–контроль» или исследование с некачественным или зависимым «золотым стандартом» |
Серия случаев (и когортные исследования или исследования «случай– контроль» низкого качества) |
|
5 |
Мнение экспертов без тщательной критической оценки или основанное на физиологии, лабораторные исследования на животных или разработка «первых принципов» |
Мнение экспертов без тщательной критической оценки, лабораторные исследования на животных или разработка «первых принципов» |
|
Степени рекомендаций | ||
|
A |
Согласующиеся между собой исследования 1-го уровня | |
|
B |
Согласующиеся между собой исследования 2-го или 3-го уровня или экстраполяция на основе исследований 1-го уровня | |
|
C |
Исследования 4-го уровня или экстраполяция на основе уровня 2 или 3 | |
|
D |
Доказательства 4-го уровня или затруднительные для обобщения или некачественные исследования любого уровня | |
насколько интерпретация доказательных данных, лежащих в основе рекомендаций, доступна для понимания. Затем были получены комментарии со стороны врачей амбулаторного звена. Полученные комментарии тщательно систематизировались и обсуждались на совещаниях экспертной группы. Последние изменения в настоящих рекомендациях были представлены для дискуссии на заседании профильной комиссии
«Колопроктология» Экспертного совета Минздрава России 12 сентября 2013 г. Проект рекомендаций был повторно рецензирован независимыми экспертами и врачами амбулаторного звена. Для окончательной редакции и контроля качества рекомендации были повторно проанализированы членами экспертной группы, которые пришли к выводу, что все замечания и комментарии приняты во внимание, риск систематических ошибок при разработке рекомендаций сведен к минимуму.
ОБЛАСТЬ ПРИМЕНЕНИЯ РЕКОМЕНДАЦИЙ
Данные клинические рекомендации применимы при осуществлении медицинской деятельности в рамках Порядка оказания медицинской помощи взрослому населению с заболеваниями толстой кишки, анального канала и промежности колопроктологического профиля, а также в рамках Порядка оказания медицинской помощи населению при заболеваниях гастроэнтерологического профиля.
Определения
Согласно Римским критериям III [4, 5], СРК диагностируется при наличии следующих признаков: рецидивирующая боль или дискомфорт в животе, отмечавшиеся в течение не менее чем 3 дня в месяц за последние 3 мес с дебютом симптомов не менее чем 6 мес до постановки диагноза.
Обязательными также являются следующие характеристики боли в животе:
n Улучшение состояния после дефекации.
n Появление симптомов связано с изменением частоты стула.
n Появление симптомов связано с изменением консистенции стула.
Код по Международной классификации болезней 10-го пересмотра
n K58 Синдром раздраженного кишечника
Классификация
В зависимости от характера изменений стула выделяют:
n СРК с преобладанием диареи, для которого характерно присутствие жидкого стула более чем в 25% дефекаций и оформленного стула менее
чем в 25% дефекаций. Данный тип СРК встречается приблизительно у 1/3 всех пациентов, чаще обнаруживается у мужчин [4];
n СРК с преобладанием запора, для которого характерно присутствие плотного стула более чем в 25% дефекаций и жидкого стула менее чем в 25% дефекаций. Данный тип СРК также обнаруживают приблизительно в 1/3 всех случаев заболевания, чаще встречаясь у женщин;
n СРК со смешанным характером стула или его цикличным изменением, при котором более чем в 25% случаев присутствуют и плотный, и неоформленный стул. Данный тип СРК составляет от 1/3 до 1/2 всех случаев заболевания.
Следует тщательно оценить правильность понимания пациентами терминов «запор» и «понос». Так, многие больные СРК, жалующиеся на «диарею», имеют в виду частую дефекацию оформленным стулом, пациенты с «запором» могут предъявлять жалобы на дискомфорт в аноректальной области при дефекации, а не на редкое опорожнение кишечника или дефекацию плотными каловыми массами. Для описания консистенции стула может применяться бристольская шкала формы кала, согласно которой плотному стулу соответствуют типы 1 и 2, а жидкому — типы 6 и 7 (табл. 21.2).
Таблица 21.2. Бристольская шкала форм кала
|
Тип 1 |
Отдельные твердые комки, типа «орехов», трудно продвигаются |
|
Тип 2 |
В форме колбаски, но комковатый |
|
Тип 3 |
В форме колбаски, но с ребристой поверхностью |
|
Тип 4 |
В форме колбаски или змеи, гладкий и мягкий |
|
Тип 5 |
Мягкие маленькие шарики с ровными краями |
|
Тип 6 |
Рыхлые частицы с неровными краями, кашицеобразный стул |
|
Тип 7 |
Водянистый, без твердых частиц |
Кроме того, возможны следующие классификации СРК, однако они носят вспомогательный характер и в настоящих рекомендациях не используются для выбора тактики лечения, а также не используются при формулировании диагноза.
1. Классификация по основному симптому (симптомы, оцениваемые пациентом как причиняющие наибольший дискомфорт):
n СРК с преобладанием нарушения частоты стула;
n СРК с преобладанием болевого синдрома;
n СРК с преобладанием метеоризма.
2. Классификация по наличию отягощающих факторов:
n постинфекционный СРК;
n СРК, связанный с приемом определенных пищевых продуктов;
n СРК, связанный со стрессом.
Формулировка диагноза
При формулировании диагноза необходимо указать тип преобладающих нарушений стула. Возможны три формулировки диагноза.
n Синдром раздраженного кишечника с преобладанием диареи.
n Синдром раздраженного кишечника с преобладанием запора.
n Синдром раздраженного кишечника, смешанный тип.
Диагностика [6, 7]
КЛИНИЧЕСКИЕ ПРОЯВЛЕНИЯ
Диагноз СРК устанавливается при наличии хронических симптомов и после надлежащего исключения органа [8, 9].
При установлении диагноза СРК следует оценить наличие следующих характерных симптомов.
n Боль в животе, для которой при СРК характерны:
v хроническое течение (наличие боли в течение более чем 6 мес);
v уменьшение или купирование боли после дефекации/отхождения газов;
v связь боли с нервным стрессом, приемом пищи;
v преходящий чаще, чем постоянный, характер боли.
n Боль в животе у больных СРК может быть как локализованной (чаще всего в нижних отделах брюшной полости), так и нелокализованной. Появление болей в ночное время встречается редко и может быть признаком органической патологии [10].
n Нарушения стула в виде запора, поноса или их чередования, а также наличие примеси слизи в стуле.
n Ощущение вздутия живота, повышенное газообразование, урчание в животе.
n Нарушения акта дефекации в виде императивных позывов на дефекацию или ощущение неполного опорожнения кишечника.
Также наличие СРК могут сопровождать жалобы, не связанные с функционированием кишечника, а именно:
n диспепсия (отмечается у 42–87% пациентов с СРК), тошнота, изжога [11, 12];
n боли в поясничной области, другие мышечные и суставные боли;
n урологические симптомы (никтурия, учащенные и императивные позывы к мочеиспусканию, ощущение неполного опорожнения мочевого пузыря) [13];
n диспареуния (появление боли при половом сношении) у женщин [14];
n бессонница;
n низкая переносимость лекарственных препаратов.
Кроме того, у больных СРК следует оценить наличие следующих психических факторов [15]:
n тревожность;
n депрессия;
n соматизация;
n ипохондрия;
n страх, связанный с симптомами (в том числе канцерофобия).
СИМПТОМЫ ТРЕВОГИ
Приведенные ниже симптомы могут сопровождать органическую патологию желудочно-кишечного тракта (ЖКТ) и должны стать показаниями к углубленному обследованию, в большинстве случаев — к проведению эндоскопического исследования ЖКТ:
n необъяснимая потеря массы тела;
n наличие крови в стуле;
n лихорадка, сопровождающая боли в животе;
n необъяснимая анемия.
К особенностям анамнеза, указывающим на вероятное органическое поражение ЖКТ, относятся:
n семейный анамнез колоректального рака, целиакии, язвенного колита и болезни Крона;
n связь симптомов:
v с менструациями;
v лекарственной терапией;
v приемом молока, искусственных заменителей сахара, диетических продуктов, алкоголя;
n поездки в субтропики и тропики;
n нарушения питания:
v нерегулярный, неадекватный прием пищи; недостаточный прием жидкости;
v ожирение при соблюдении диеты.
ДИФФЕРЕНЦИАЛЬНАЯ ДИАГНОСТИКА
Дифференциальную диагностику СРК проводят со следующими заболеваниями [16, 17].
n Целиакия (глютеновая энтеропатия) [18], для которой характерно начало заболевания в детстве и которая может сопровождать замедленное развитие ребенка. Необходимым скрининговым исследованием для исключения целиакии является анализ уровня антител IgA к тканевой трансглутаминазе и эндомизию.
n Лактазная и дисахаридазная недостаточность, при которых прослеживается связь симптомов с приемом определенных продуктов. Диагностика проводится с помощью дыхательного водородного теста с нагрузкой лактозой или фруктозой.
n Внешнесекреторная недостаточность поджелудочной железы.
n Эндокринологические расстройства (гипертиреоз, гормонпродуцирующие опухоли ЖКТ).
n Воспалительные заболевания кишечника — ВЗК (болезнь Крона и язвенный колит), при которых возможно наличие ректального кровотечения, длительной постоянной диареи, инфильтрата в брюшной полости, необъяснимой потери массы тела, анемии, а также перианальные поражения (свищи, трещины). При подозрении на указанные патологии больной должен быть направлен на илеоколоноскопию.
n Лимфоцитарный или коллагенозный колит (микроскопические колиты), как правило, протекающий без боли и являющийся причиной
23–30% случаев хронической диареи у лиц старшего возраста [19]. Для подтверждения диагноза необходимо проведение колоноскопии с биопсией слизистой оболочки ободочной кишки.
n Радиационный (постлучевой) колит.
n Колит, ассоциированный с приемом нестероидных противовоспалительных средств.
n Ишемическая болезнь органов пищеварения.
n Рак толстой кишки.
n Острая инфекционная диарея, антибиотико-ассоциированная диарея и псевдомембранозный колит.
n Лямблиоз.
n Синдром избыточного бактериального роста в тонкой кишке, для которого характерны диарея, вздутие живота и мальабсорбция. Диагностика осуществляется путем проведения дыхательного водородного теста для подтверждения избыточной колонизации тонкой кишки.
n Дивертикулит, при котором может отмечаться лихорадка, определяться инфильтрат в виде пальпируемого мягкого образования в левой подвздошной области, а боль носит локализованный характер (как правило, в левой подвздошной области).
n Эндометриоз, сопровождающийся циклической болью в нижних отделах живота, увеличением яичников или наличием ретроцервикальных узлов.
n Воспалительные заболевания органов малого таза, для которых характерно наличие неострых болей в нижних отделах живота, необъяснимой лихорадки, давящей боли с иррадиацией вверх при влагалищном исследовании придатков, а также набухание придатков.
n Рак яичника, являющийся обязательным для исключения диагнозом у женщин старше 40 лет.
К редким причинам СРК-подобных симптомов, в первую очередь диареи, относятся болезнь Уиппла, амилоидоз с поражением кишечника, а также вирусные поражения толстой кишки (цитомегаловирус, вирус простого герпеса).
АЛГОРИТМ ДИАГНОСТИКИ [20–22]
В рутинной практике исключение всех потенциальных органических патологий не является обоснованным при отсутствии характерных симптомов (УД 5, СР D). Вероятность выявления различных видов органического поражения ЖКТ («предтестовая вероятность») у пациентов с симптомами СРК представлена ниже в таблице 21.3.
С учетом этих данных рутинное проведение УЗИ, эндоскопического исследования толстой кишки или ирригоскопии, исследования функции щитовидной железы, анализа кала на яйца глист и паразитов, а также дыхательный водородный тест для диагностики непереносимости лактозы и избыточного бактериального роста представляются нецелесообразными при отсутствии клинически обоснованного подозрения на эти патологии. Диагностическим минимумом при наличии симптоматики, соответствующей СРК, являются проведение общего анализа крови с определе-
нием СОЭ, определение уровня С-реактивного белка, общий анализ кала и тест на скрытую кровь, а также определение антител IgA к эндомизию и тканевой трансглутаминазе [24], а также общий анализ мочи (УД 5, СР D). Дополнительным подтверждением диагноза может служить определение висцеральной гиперчувствительности [25, 26].
Таблица 21.3. Предтестовая вероятность органического поражения желудочнокишечного тракта у пациентов с симптомами, соответствующими синдрому раздраженного кишечника [23]
|
Органическое поражение ЖКТ |
Пациенты с СРК, % |
Общая популяция, % |
|
Колит / ВЗК |
0,51–0,98 |
0,3–1,2 |
|
Колоректальный рак |
0–0,51 |
4,0–6,0 |
|
Целиакия |
4,67 |
0,25–0,5 |
|
Инфекция ЖКТ |
0–1,7 |
Нет данных |
|
Дисфункция щитовидной железы |
6,0 |
5,0–9,0 |
|
Непереносимость лактозы |
22,0–26,0 |
25,0 |
Ниже представлен алгоритм диагностических мероприятий при подозрении на СРК (рис. 21.1).
Лечение
Лечение СРК [28, 29] включает коррекцию диеты, образа жизни, прием фармакологических средства, а также психотерапевтические методы воздействия.
ДИЕТА И ОБРАЗ ЖИЗНИ [30]
Диета при СРК подбирается индивидуально путем исключения продуктов, вызывающих усиление симптомов заболевания (элиминационная диета). Несмотря на противоречивые данные исследований по оценке эффекта от назначения конкретной диеты, всем пациентам с СРК следует рекомендовать (УД 5, СР 5):
n принимать пищу регулярно в специально отведенное для этого время, избегать приема пищи в спешке, в процессе работы;
n не пропускать приемы пищи и не допускать длительных перерывов между приемами пищи;
n выпивать не менее 8 стаканов жидкости в течение дня, особенно воды или других не содержащих кофеин продуктов (например, травяного чая);
n ограничить прием черного чая и кофе тремя чашками в день;
n ограничить прием алкоголя и газированных напитков, курения;
n даже при наличии сопутствующего запора провести тест с исключением продуктов с повышенным содержанием нерастворимых пищевых волокон, в частности хлебо-булочных изделий, зерновых хлопьев и необработанного риса (УД 1b, СР B [31]). Уменьшению вздутия может
![]()
![]()
![]()
|
|
Наличие симптомов тревоги: – Возраст 50 лет и старше. – Кровь в стуле. – Необъяснимая потеря веса. – Отсутствие аппетита. – Возникновение симптомов в ночное время. – Лихорадка. – Объемные образования в брюшной полости. – Асцит | ||
|
Есть симптомы тревоги |
Нет симптомов тревоги | |
|
• Клинический анализ крови. • СОЭ, С-реактивный белок. • Общий анализ мочи. • Оценка функции щитовидной железы. • Анализ кала на скрытую кровь. • Общий анализ кала. • Определение антител к эндомизию и тканевой. трансглутаминазе | ||
|
Есть отклонения |
Нет отклонений | |
|
Дополнительные исследования с целью исключения органической патологии ЖКТ |
Исследование висцеральной чувствительности. Установление диагноза СРК. Проверка наличия симптомов тревоги на каждом визите | |
![]() Рис. 21.1. Алгоритм диагностики синдрома раздраженного кишечника [27].
Рис. 21.1. Алгоритм диагностики синдрома раздраженного кишечника [27].
способствовать прием овса в виде хлопьев и каш (растворимых пищевых волокон), а также семян льна (до 1 столовой ложки в день);
n провести тест с исключением лактозы из рациона. При этом следует помнить, что даже пациенты с подтвержденной непереносимостью лактозы нормально переносят прием 10–12 г лактозы в день [32], содержание которой наиболее велико в коровьем молоке (5 г в 100 мл), творожном сыре (1 г в столовой ложке), плавленом сыре (1 г в 18-граммовом ломтике) и йогуртах (4 г в 100 г);
n ограничить прием свежих фруктов тремя порциями в день (по 80 г каждая);
n при наличии сопутствующей диареи исключить прием сорбитола, входящего в состав подсластителей пищевых продуктов (например, жевательной резинки) и напитков, а также в продукты для похудения;
n при наличии сопутствующего вздутия — ограничение приема животных жиров и продуктов, приготовленных на нем, ограничение приема капусты, молока, мучных изделий.
Эффективность гипоаллергенной диеты в отношении уменьшения симптомов заболевания не доказана. При подозрении на непереносимость конкретного продукта питания следует рекомендовать консультацию диетолога, в том числе для проведения иммунологических тестов (выявление антител IgG к определенным пищевым белкам), хотя сведения об эффективности диеты, подобранной на основании анализа уровня антител, остаются противоречивыми [33].
Масштабные исследования эффективности увеличения физической активности при СРК не проводились. Тем не менее пациентам с СРК следует рекомендовать тратить не менее чем 30 мин в день в течение рабочей недели на умеренные физические нагрузки (бег, занятия на тренажерах, плавание) [34], а также планировать рабочий день таким образом, чтобы выделять время на необходимый отдых в течение дня (УД 2b, СР B [35]).
МЕДИКАМЕНТОЗНОЕ ЛЕЧЕНИЕ [36–39]
Пищевые волокна и слабительные препараты
В качестве 1-й линии терапии у пациентов с СРК с преобладанием запора рекомендуется назначение препаратов пищевых волокон. Подтверждена эффективность гидрофильного муциллоида псиллиума (экстракт шелухи семян подорожника яйцевидного), который назначается в дозе 4–5 г от 3 до 6 раз в сутки (УД 2а, СР В [40–43]). Проведение терапии псиллиумом требует адекватного приема жидкости (не менее 100–200 мл жидкости дополнительно на каждый прием препарата). Пшеничные и кукурузные отруби не эффективнее плацебо в отношении купирования основных симптомов СРК [44]. Нередко самостоятельно применяемые пациентами препараты алоэ вера неэффективны [45]. Несмотря на подтвержденный слабительный эффект, лактулоза неэффективна в лечении СРК в связи с высокой частотой нежелательных явлений, в первую очередь повышенного газообразования.
Эффект от назначения пищевых волокон следует оценивать не ранее чем через 2–4 нед от начала приема. При неэффективности терапии псиллиумом и диетотерапии (см. выше) целесообразно назначение препаратов полиэтиленгликоля по 10 мг 1–2 раза в день на 1–2 приема (предпочтителен однократный прием утром), эффективно нормализующего консистенцию стула, но не оказывающего статистически значимого влияния на остальные симптомы СРК (УД За, СР С [46]).
Цель назначения слабительных препаратов при СРК — поддержание нормальной консистенции стула, соответствующей типу 4 по бристольской шкале форм кала.
Следует учитывать, что эффективность слабительных средств при СРК с преобладанием запора может не совпадать с их эффективностью при хроническом запоре без болевого синдрома [47]. Тем не менее при подборе адекватной терапии слабительными следует руководствоваться алгоритмом диагностики и лечения хронического запора (рис. 21.2) [48].
Назначение пищевых волокон (пшеничные отруби и т.д.) ± осмотических слабительных (полиэтиленгликоль)
Беседа с пациентом, выполнение общего анализа крови, оценка симптомов тревоги
![]()
Недостаточный ответ
![]()
Проведение аноректальной манометрии, теста с выталкиванием баллончика.
При необходимости: рентгеновская или МР-дефекография
![]() Отклонения от нормы Отклонений нет
Отклонения от нормы Отклонений нет
![]()
![]()
Расстройства дефекации (проктогенный запор)
Исследование пассажа по ЖКТ
![]()
![]()
![]() Запор с нормальным или замедленным пассажем
Запор с нормальным или замедленным пассажем
Рис. 21.2. Алгоритм диагностики и лечения хронического запора.
Терапия по принципу «биологической обратной связи», при неэффективности — слабительные клизмы/свечи, подключение стимулирующих слабительных (натрия пикосульфат, при неэффективности бисакодил).
Пробиотики и антибиотики
Эффективность различных пробиотиков [49, 50] при СРК подтверждена РКИ и систематическим обзором Cochrane Database [51–54] (УД 1b,
СР А). Эффективность препаратов, содержащих исключительно лактобактерии, не подтверждена. Предпочтение следует отдавать мультиштаммовым препаратам, а также средствам, содержащим бифидобактерии (УД 2а, СР В). Эффект от терапии пробиотиками следует оценивать не ранее чем через 4 нед от начала приема препарата в дозе, рекомендованной производителем [55].
В трех рандомизированных клинических исследованиях подтверждена эффективность неабсорбируемого антибиотика рифаксимина при СРК с преобладанием диареи в отношении уменьшения вздутия живота и совокупности симптомов [56–58]. Препарат назначают в дозе от 800 до 1200 мг/ сут на 2–3 приема на 10–14 дней. Данные о долгосрочной эффективности отсутствуют.
Спазмолитики
Первой линией при купировании болевого компонента СРК является назначение [59, 60] спазмолитиков. Возможности применения М-холинолитиков и дротаверина ограничены их неселективностью и риском нежелательных явлений, в первую очередь за счет снижения тонуса гладкой мускулатуры сосудов. Предпочтительно назначение селективных миотропных спазмолитиков, к которым относятся пинаверия бромид, итоприд, гиосцина бутилбромид, мебеверин, тримебутин (УД 2а, СР В [61, 62]). Препараты принимаются за 30–45 мин до приема пищи. Эффект следует оценить не ранее чем через 1 мес после начала приема. Также в качестве средства купирования болей в животе может применяться масло перечной мяты [63].
Противодиарейные средства
Лоперамид — препарат 1-й линии для купирования диареи при СРК (УД 2b, СР В [64–66]). Лоперамид эффективно нормализует частоту дефекаций и консистенцию стула, а также повышает тонус анального сфинктера, но не более эффективен, чем плацебо, в уменьшении совокупности симптомов СРК. Доза подбирается индивидуально и составляет от 4 до 16 мг/сут. Не реже 1 раза в 3 мес рекомендуется оценка эффективности и целесообразности продолжения терапии.
Трициклические антидепрессанты и селективные ингибиторы обратного захвата серотонина
Эффективность антидепрессантов в лечении СРК подтверждена систематическим обзором Cochrane Database. Данные препараты должны рекомендоваться в качестве 2-й линии терапии при неэффективности комбинированной терапии слабительными/противодиарейными препаратами в сочетании со спазмолитиками (УД 1a, СР А [67, 68]). Для лечения СРК применяются трициклические антидепрессанты, включающие амитриптилин, кломипрамин, имипрамин, лофепраминÃ, нортриптилинÃ, тримипраминà и миансерин, а также селективные
ингибиторы обратного захвата серотонина, включающие циталопрам, эсциталопрам, флуоксетин, флувоксамин, пароксетин и сертралин. Доказательная база эффективности трициклических антидипрессантов больше, чем для селективных ингибиторов обратного захвата серотонина, поэтому трициклические антидепрессанты, несмотря на более высокий риск нежелательных явлений, применяются в качестве 1-й линии терапии антидепрессантами.
Стартовая терапия проводится малыми дозами препаратов: 10 мг для всех видов антидепрессантов. При отсутствии эффекта, не ранее чем через 2 нед от начала приема, возможно увеличение дозы на 10 мг в 2 нед. При отсутствии эффекта от приема максимальной дозы (30 мг для трициклических антидепрессантов и 20 мг для селективных ингибиторов обратного захвата серотонина) следует сменить препарат (трициклические антидепрессанты на селективные ингибиторы обратного захвата серотонина, и наоборот). Консультация для решения вопроса о целесообразности продолжения терапии проводится каждые 6 мес.
ПСИХОТЕРАПЕВТИЧЕСКИЕ МЕТОДЫ ЛЕЧЕНИЯ
При неэффективности медикаментозного лечения СРК, результат которого следует оценить через 9–12 мес, больным показана консультация психоневролога для определения целесообразности психотерапевтических методов лечения (УД 3а, СР С) [69, 70]. Согласно систематическому обзору, эффективны при СРК когнитивная поведенческая терапия [71–73], гипнотерапия [74] и психологическая поддержка [75–77]. Эффективность релаксационных методик не подтверждена. Двойное слепое исследование также не подтвердило эффективность акупунктуры у пациентов с СРК [78].
Прогноз
Имеющиеся данные о прогнозе [79] течения СРК неоднозначны. Согласно наиболее масштабному исследованию, у большинства пациентов с СРК симптомы, несмотря на проводимое лечение, сохраняются, но не усиливаются. Вероятность купирования симптомов СРК при наблюдении в течение 12–20 мес составляет 38%. К факторам, оказывающим негативное влияние на прогноз заболевания, относятся нежелание получать лечение, тревожность по поводу рисков, связанных с заболеванием, нарушение повседневных функций в результате СРК, длительный анамнез СРК, хронический стресс, а также наличие сопутствующих психиатрических заболеваний.
Критерии оценки качества помощи в стационаре представлены в таблице 21.4. Для оценки качества медицинской помощи используют временные, процессуальные и профилактирующие критерии. Временные характеризуют своевременность оказания определенных этапов медицин-
ской помощи. Выполнение пациенту ряда медицинских манипуляций, инструментальных и лабораторных исследований, необходимых для качественного оказания медицинской помощи, оценивают в процессуальных критериях. Для анализа мероприятий, направленных на предотвращение развития осложнений, используют профилактирующие критерии.
Таблица 21.4. Критерии оценки качества медицинской помощи в стационаре больным синдромом раздраженного кишечника (0 — нет, 1 — да)
|
Клинические рекомендации |
Временные |
Процессуальные |
Профилактирующие |
|
Клинические рекомендации по диагностике и лечению взрослых больных синдромом раздраженного кишечника (коды по МКБ — К58, К59) |
Установка клинического диагноза в течение 72 ч: 0/1 |
Пальцевое обследование прямой кишки: 0/1. Илеоколоноскопия в течение госпитализации или в течение 6 мес до госпитализации: 0/1. Клинический анализ крови; биохимический анализ крови; клинический анализ мочи: 0/1. Анализ кала на яйца глист и простейшие: 0/1. Метод консервативного лечения в соответствии с установленным диагнозом и клиническими рекомендациями: 0/1 |
Отсутствие осложнений: • пневмония: 0/1; • тромбоэмболия: 0/1; • летальный исход: 0/1 |
Литература
1. El Serag H.B., Olden K., Bjorkman D. et al. Health-related quality of life among persons with irritable bowel syndrome: a systematic review // Aliment. Pharmacol. Ther. — 2002. — Vol. 16, N 6. — P. 1171–1185.
2. Akehurst R.L., Brazier J.E., Mathers N. et al. Health-related quality of life and cost impact of irritable bowel syndrome in a UK primary care setting // Pharmacoeconomics. — 2002. — Vol. 20, N 7. — P. 455–462.
3. OCEBM Levels of Evidence Working Group. The Oxford 2011 Levels of Evidence. — Oxford Centre for Evidence-Based Medicine, 2011.
4. Парфенов А.И., Ручкина И.Н., Оробей Ю.А., Быкова С.В. Эффективность римских критериев II в диагностике синдрома раздраженного кишечника // Тер. арх. — 2004. — Т. 76, № 4. — С. 51–54.
5. Drossman D.A. The Functional Gastrointestinal Disorders and the Rome III Process // Gastroenterology. — 2006. — Vol. 130, N 5. — P. 1377–1390.
6. Agrawal A., Whorwell P.J. Irritable bowel syndrome: Diagnosis and management // Br. Med. J. — 2002. — Vol. 332, N 7536. — P. 280–283.
7. Cash B.D., Chey W.D. Diagnosis of irritable bowel syndrome // Gastroenterol. Clin. North Am. — 2005. — Vol. 34, N 2. — P. 205–220.
8. Bijkerk C.J., de Wit N.J., Stalman W.A.B. et al. Irritable bowel syndrome in primary care: The patient’s and doctors’ views on symptoms, etiology and management // Can. J. Gastroenterol. — 2003. — Vol. 17, N 6. — P. 363–368.
9. Лоранская И.Д. Синдром раздраженного кишечника — вопросы диагностики и эффективности лечения // Экспер. и клин. гастроэнтерол. — 2008. — № 1. — С. 90–95.
10. American Gastroenterology Association. American Gastroenterological Association medical position statement: irritable bowel syndrome // Gastroenterology. — 2002. — Vol. 123, N 6. — P. 2105–2107.
11. Ивашкин В.Т., Полуэктова Е.А. Сочетании синдрома функциональной диспепсии и синдрома раздраженного кишечника // Рос. журн. гастроэнтерол., гепатол., колопроктол. — 2011. — № 4. — С. 75–81.
12. Yarandi S.S., Christie J. Functional dyspepsia in review: Pathophysiology and challenges in the diagnosis and management due to coexisting gastroesophageal reflux disease and irritable bowel syndrome // Gastroenterol. Res. Pract. — 2013. — ID351086. — P. 1–8.
13. Francis C.Y., Duffy J.N., Whorwell P.J., Morris J. High prevalence of irritable bowel syndrome in patients attending urological outpatient departments // Dig. Dis. Sci. — 1997. — Vol. 42, N 2. — P. 404–407.
14. Jamieson D.J., Steege J.F. The prevalence of dysmenorrhea, dyspareunia, pelvic pain, and irritable bowel syndrome in primary care practices // Obstet. Gynecol. — 1996. — Vol. 87, N 1. — P. 55–58.
15. Cho H.S., Park J.M., Lim C.H. et al. Anxiety, depression and quality of life in patients with irritable bowel syndrome // Gut Liver. — 2011. — Vol. 5, N 1. — P. 29–36.
16. Макарова И.А., Новожилов Д.Г., Хадзегова Ф.Р., Лоранская И.Д. Синдром раздраженного кишечника // Леч. дело. — 2006. — № 1. — С. 4–12.
17. Осипенко М.Ф., Холин С.И., Рыжичкина А.Н. Хроническая абдоминальная боль и синдром раздраженного кишечника // Леч. врач. — 2011. —
№ 2. — С. 30–34.
18. Шульпекова Ю.О., Баранская Е.К. Дифференциальная диагностика синдрома раздраженного кишечника иглютеновой энтеропатии // Рос. журн. гастроэнтерол., гепатол., колопроктол. — 2009. — Т. 19, № 6. — С. 39–48.
19. Ивашкин В.Т., Шептулин А.А., Шифрин О.С. и др. Микроскопический колит: клинические формы, диагностика, лечение // Рос. журн. гастроэнтерол., гепатол., колопроктол. — 2006. — Т. 16, № 6. — С. 56–60.
20. Adeniji O.A., Barnett C.B., Di Palma J.A. Durability of the diagnosis of irritable bowel syndrome based on clinical criteria // Dig. Dis. Sci. — 2004. — Vol. 49, N 4. — P. 572–574.
21. Barnes J. When to investigate and treat IBS symptoms // Practitioner. — 1996. — Vol. 240, N 1560. — P. 184–187.
22. Bellini M., Tosetti C., Costa F. et al. The general practitioner’s approach to irritable bowel syndrome: from intention to practice // Dig. Liver Dis. — 2005. — Vol. 37, N 12. — P. 934–939.
23. Cash B.D., Schoenfeld P., Chey W.D. The utility of diagnostic tests in irritable bowel syndrome patients: a systematic review // Am. J. Gastroenterol. — 2002. — Vol. 97, N 11. — P. 2812–2819.
24. Mein S.M., Ladabaum U., Mein S.M., Ladabaum U. Serological testing for coeliac disease in patients with symptoms of irritable bowel syndrome: a costeffectiveness analysis // Aliment. Pharmacol. Ther. — 2004. — Vol. 19, N 11. — P. 1199–1210.
25. Макарчук П.А., Головенко О.В., Михайлова Т.Л., Подмаренкова Л.Ф. Динамика клинических симптомов и показателей висцеральной чувствительности у больных СРК при лечении Метеоспазмилом // Экспер. и клин. гастроэнтерол. — 2005. — № 1. — С. 25–28.
26. Головенко О.В., Михайлова Т.Л., Плдмаренкова Л.Ф., Макарчук П.А. Клиническое значение висцеральной гиперчувствительности при синдроме раздраженного кишечника // Колопроктология. — 2004. — Т. 9, № 3. — С. 27–30.
27. World Gastroenterology Organisation, 2009. Irritable bowel syndrome: the global perspective (Clinical guideline).
28. Jones J., Boorman J., Cann P. et al. British Society of Gastroenterology guidelines for the management of the irritable bowel syndrome // Gut. — 2000. — Vol. 47. — Suppl. 2. — P. 1–19.
29. National Collaborating Centre for Nursing and Supportive Care, National Institute for Health and Clinical Excellence. Diagnosis and Management of Irritable Bowel Syndrome in Primary Care. — London, 2008, Feb.
30. Burden S. Dietary treatment of irritable bowel syndrome: Current evidence and guidelines for future practice // J. Hum. Nutr. Diet. — 2001. — Vol. 14, N 3. — P. 231–241.
31. Aller R., de Luis D.A., Izaola O. et al. Effects of a high-fiber diet on symptoms of irritable bowel syndrome: a randomized clinical trial // Nutrition. — 2004. — Vol. 20, N 9. — P. 735–737.
32. Vesa T.H., Seppo L.M., Martea P.R. et al. Role of irritable bowel syndrome in subjective lactose intolerance // Am. J.Clin. Nutr. — 1998. — Vol. 67, N 4. — P. 710–715.
33. Atkinson W., Sheldon T.A., Shaath N., Whorwell P.J. Food elimination based on IgG antibodies in irritable bowel syndrome: a randomised controlled trial // Gut. — 2004. — Vol. 53, N 10. — P. 1459–1464.
34. De Schryver A.M., Keulemans Y.C., Peters H.P. et al. Effects of regular physical activity on defecation pattern in middle-aged patients complaining of chronic constipation // Scand. J. Gastroenterol. — 2005. — Vol. 40, N 4. — P. 422–429.
35. Bi L.,Triadafilopoulos G. Exercise and gastrointestinal function and disease: an evidence based review of risks and benefits // Clin. Gastroenterol. Hepatol. — 2003. — Vol. 1, N 5. — P. 345–355.
36. Cash B.D., Chey W.D. Irritable bowel syndrome: A systematic review // Clin. Fam. Pract. — 2004. — Vol. 6, N 3. — P. 647–669.
37. Ардатская М.Д., Минушкин О.Н. Патогенетическое лечение синдрома раздраженного кишечника // Фарматека. — 2012. — № 7. — С. 18–25.
38. Полуэктова Е.А., Кучумова С.Ю., Шептулин А.А., Ивашкин В.Т. Лечение синдрома раздраженного кишечника с позиций современных представлений о патогенезе заболевания // Рос. журн. гастроэнтерол., гепатол., колопроктол. — 2013. — № 1. — С. 57–65.
39. Осипенко М.Ф., Бикбулатова Е.А., Фролова Н.Н., Лосева Н.В. Комплексная терапия больных с синдромом раздраженного кишечника // Экспер. и клин. гастроэнтерол. —2004. — № 5. — С. 39–44.
40. Arthurs Y., Fielding J.F. Double blind trial of ispaghula/poloxamer in the irritable bowel syndrome // Ir. Med. J. — 1983. — Vol. 76, N 5. — P. 253.
41. Chapman N.D., Grillage M.G., Mazumder R., Atkinson S.N. A comparison of mebeverine with high-fibre dietary advice and mebeverine plus ispaghula in the treatment of irritable bowel syndrome: an open, prospectively randomised, parallel group study // Br. J. Clin. Pract. — 1990. — Vol. 44, N 11. — P. 461–466.
42. Golechha A.C., Chadda V.S., Chadda S. et al. Role of ispaghula husk in the management of irritable bowel syndrome (a randomized double-blind crossover study) // J. Assoc. Physicians India. — 1982. — Vol. 30, N 6. — P. 353–355.
43. Шульпекова Ю.О., Ивашкин В.Т., Денисов Н.Л. Фитомуцил♠ в лечении запора при синдроме раздраженного кишечника // Клин. перспективы гастроэнтерол., гепатол. — 2007. — № 4. — С. 35–43.
44. Snook J., Shepherd H.A. Bran supplementation in the treatment of irritable bowel syndrome // Aliment. Pharmacol. Ther. — 1994. — Vol. 8, N 5. — P. 511–514.
45. Davis K. Randomised double-blind placebo-controlled trial of aloe vera for irritable bowel syndrome // Int. J. Clin. Pract. — 2006. — Vol. 60, N 9. — P. 1080–1086.
46. Chaussade S., Minic M. Comparison of efficacy and safety of two doses of two different polyethylene glycolbased laxatives in the treatment of constipation // Aliment. Pharmacol. Ther. — 2003. — Vol. 17, N 1. — P. 165–172.
47. Парфенов А.И. Патогенетическое лечение хронического запора // Тер. арх. — 2012. — Т. 84, № 8. — С. 4–9.
48. Bharucha A.E., Spencer D., Lembo A., Pressman A. American Gastroenterological Association Medical Position Statement on Constipation // Gastroenterology. — 2013. — Vol. 144, N 1. — P. 211–217.
49. Ручкина И.Н., Парфенов А.И., Осипов Г.А. Роль дисбиотических нарушений в этиологии и патогенезе синдрома раздраженного кишечника // Экспер. и клин. гастроэнтерол. — 2003. — № 1. — С. 57.
50. Осипенко М.Ф., Бикбулатова Е.А., Холин С.И. Пробиотики в лечении диарейного синдрома // Фарматека. — 2008. — № 13. — С. 36–41.
51. Bittner A.C., Croffut R.M., Stranahan M.C. Prescript-assist probioticprebiotic treatment for irritable bowel syndrome: A methodologically oriented, 2-week, randomized, placebo-controlled, double-blind clinical study // Clin. Ther. — 2005. — Vol. 27, N 6. — P. 755–761.
52. Kim H.J., Camilleri M., McKinzie S. et al. A randomized controlled trial of a probiotic, VSL#3, on gut transit and symptoms in diarrhoeapredominant irritable bowel syndrome // Aliment. Pharmacol. Ther. — 2003. — Vol. 17, N 7. — P. 895–904.
53. Kim H.J., Vazquez Roque M.I., Camilleri M. et al. A randomized controlled trial of a probiotic combination VSL# 3 and placebo in irritable bowel syndrome with bloating // Neurogastroenterol. Motil. — 2005. — Vol. 17, N 5. — P. 687–696.
54. Niedzielin K., Kordecki H., Birkenfeld B. A controlled, double-blind, randomized study on the efficacy of Lactobacillus plantarum 299V in patients with irritable bowel syndrome // Eur. J. Gastroenterol. Hepatol. — 2001. — Vol. 13, N 10. — P. 1143–1147.
55. Ткаченко Е.И., Успенский Ю.П., Бапукова Е.В., Барышникова Н.В. Новые возможности пробиотической терапии в лечении синдрома раздраженного кишечника // Экспер. и клин. гастроэнтерол. — 2006. — № 3. — С. 26–30.
56. Pimentel M., Lembo A., Chey W.D. et al. TARGET Study Group. Rifaximin therapy for patients with irritable bowel syndrome without constipation // N. Engl. J. Med. — 2011. — Vol. 364, N 1. — P. 22–32.
57. Meyrat P., Safroneeva E., Schoepfer A.M. Rifaximin treatment for the irritable bowel syndrome with a positive lactulose hydrogen breath test improves symptoms for at least 3 months // Aliment. Pharmacol. Ther. — 2012. — Vol. 36, N 11–12. — P. 1084–1093.
58. Majewski M., Reddymasu S.C., Sostarich S. et al. Efficacy of rifaximin, a nonabsorbed oral antibiotic, in the treatment of small intestinal bacterial overgrowth // Am. J. Med. Sci. — 2007. — Vol. 333, N 5. — P. 266–270.
59. Ивашкин В.Т., Драпкина О.М. Возможности применения тримебутина в лечении больных с синдромом раздраженного кишечника // Рос. журн. гастроэнтерол., гепатол., колопроктол. — 2008. — Т. 18, № 5. — С. 12–16.
60. Ивашкин В.Т., Шептулин А.А., Трухманов А.С. Клинические аспекты функциональной диспепсии и эффективность ганатона (итоприда) в ее лечении // Рос. журн. гастроэнтерол., гепатол., колопроктол. — 2009. — Т. 19,
№ 6. — С. 17–22.
61. Gilbody J.S., Fletcher C.P., Hughes I.W., Kidman S.P. Comparison of two different formulations of mebeverine hydrochloride in irritable bowel syndrome // Int. J. Clin. Pract. — 2000. — Vol. 54, N 7. — P. 461–464.
62. Grillage M.G., Nankani J.N., Atkinson S.N., Prescott P. A randomised, double-blind study of mebeverine versus dicyclomine in the treatment of functional abdominal pain in young adults // Br. J. Clin. Pract. — 1990. — Vol. 44, N 5. — P. 176–179.
63. Carling L., Svedberg L.-E., Hulten S. Short term treatment of the irritable bowel syndrome: A placebocontrolled trial of peppermint oil against hyoscyamine // Opuscula Med. — 1989. — Vol. 34, N 3. — P. 55–57.
64. Amery W., Duyck F., Polak J., van den Bouwhuysen. G. A multicentre doubleblind study in acute diarrhoea comparing loperamide (R 18553) with two common antidiarrhoeal agents and a placebo // Curr. Ther. Res. Clin. Exp. — 1975. — Vol. 17, N 3. — P. 263–270.
65. Allison M.C., Sercombe J., Pounder R.E. A double-blind crossover comparison of lidamidine, loperamide and placebo for the control of chronic diarrhea // Aliment. Pharmacol. Ther. — 1998. — Vol. 2, N 4. — P. 347–351.
66. Efskind P.S., Bernklev T., Vatn M.H. A double-blind placebo-controlled trial with loperamide in irritable bowel syndrome. Scand. J. Gastroenterol. — 1996. — Vol. 31, N 5. — P. 463–468.
67. Quartero A.O., Meineche-Schmidt V., Muris J. et al. Bulking agents, antispasmodic and antidepressant medication for the treatment of irritable bowel syndrome // Cochrane Database Syst. Rev. — 2005. — Is. 2. — CD003460.
68. Myren J., Lovland B., Larssen S.E., Larsen S. A double-blind study of the effect of trimipramine in patients with the irritable bowel syndrome // Scand. J. Gastroenterol. — 1984. — Vol. 6. — P. 835–843.
69. Ивашкин В.Т., Полуэктова Е.А., Бениашвили А.Г. Взаимодействие гастроэнтеролога и психиатра при ведении пациентов с функциональным расстройством желудочно-кишечного тракта // Рос. журн. гастроэнтерол., гепатол., колопроктол. — 2011. — № 6. — С. 74–81.
70. Bennett P., Wilkinson S. A comparison of psychological and medical treatment of the irritable bowel syndrome // Br. J. Clin. Psychol. — 1985. — Vol. 24. — Pt 3. — P. 215–216.
71. Corney R.H., Stanton R., Newell R. et al. Behavioural psychotherapy in the treatment of irritable bowel syndrome // J. Psychosom. Res. — 1991. — Vol. 35, N 4–5. — P. 461–469.
72. Drossman D.A., Toner B.B., Whitehead W.E. et al. Cognitive-behavioral therapy versus education and desipramine versus placebo for moderate to severe functional bowel disorders // Gastroenterology. — 2003. — Vol. 125, N 1. — P. 19–31.
73. Heymann-Monnikes I., Arnold R., Florin I. et al. The combination of medical treatment plus multicomponent behavioral therapy is superior to medical treatment alone in the therapy of irritable bowel syndrome // Am. J. Gastroenterol. — 2000. — Vol. 95, N 4. — P. 981–994.
74. Forbes A., MacAuley S., Chiotakakou-Faliakou E. Hypnotherapy and therapeutic audiotape: effective in previously unsuccessfully treated irritable bowel syndrome? // Int. J. Colorectal Dis. — 2000. — Vol. 15, N 5–6. — P. 328–334.
75. Bergeron C.M. A comparison of cognitive stress management, progressive muscle relaxation, and biofeedback in the treatment of irritable bowel syndrome // Dissertation Abstracts Int. — 1984. — Vol. 44, N 10-B. — P. 3186.
76. Blanchard E.B., Schwarz S.P., Suls J.M. et al. Two controlled evaluations of multicomponent psychological treatment of irritable bowel syndrome // Behav. Res. Ther. — 1992. — Vol. 30, N 2. — P. 175–189.
77. Bogalo L, Moss-Morris R. The effectiveness of homework tasks in an irritable bowel syndrome cognitive behavioural self-management programme // N. Z. J. Psychol. — 2006. — Vol. 35, N 3. — P. 120–125.
78. Forbes A., Jackson S., Walter C. et al. Acupuncture for irritable bowel syndrome: a blinded placebo-controlled trial // World J. Gastroenterol. — 2005. — Vol. 11, N 26. — P. 4040–4044.
79. Harvey R.F., Mauad E.C., Brown A.M. Prognosis in the irritable bowel syndrome: a 5-year prospective study // Lancet. — 1987. — Vol. 1, N 8539. — P. 963–965.
ВЕДЕНИЕ ВЗРОСЛЫХ ПАЦИЕНТОВ С КИШЕЧНОЙ СТОМОЙ
Введение
В России, как и во всем мире, постоянно растет число людей, перенесших операции по наложению кишечной стомы в связи с различными заболеваниями, аномалиями или травмами кишечника. Преобладающее число таких пациентов (около 90%) имеет стому в связи с онкологическими заболеваниями толстой кишки. По данным ВОЗ, число стомированных пациентов на 100 тыс. населения составляет 100–150 человек [1]. Несмотря на высокий уровень хирургической реабилитации, число стомированных пациентов в России приближается к 180 тыс. человек.
Формирование противоестественного заднего прохода вносит существенные ограничения в жизнь человека и значительно снижает ее качество, что приводит к инвалидизации и высокому уровню социальной дезинтеграции [2, 3].
Стомированные пациенты нуждаются в комплексной медико-социальной программе реабилитации. Общими принципами реабилитации являются индивидуальность, последовательность, непрерывность и комплексность [4–7].
Настоящие рекомендации по ведению взрослых пациентов с кишечной стомой являются руководством для практических врачей, осуществляющих ведение и лечение таких пациентов. Рекомендации подлежат регулярному пересмотру в соответствии с новыми данными научных исследований в этой области. Настоящие рекомендации составлены с учетом имеющегося отечественного и зарубежного опыта по ведению стомированных пациентов, клинических руководств профессиональных ассоциаций [8–10], научных публикаций и действующих нормативных документов.
Рекомендации включают следующие разделы: определение и классификация кишечных стом, организация помощи стомированным пациентам, диагностика осложнений кишечных стом и выбор метода лечения, лечение осложнений кишечных стом, лечение перистомальных кожных осложнений, технические средства реабилитации для пациентов с кишечной стомой, некоторые аспекты помощи стомированным пациентам.
Для отдельных положений рекомендаций приведены уровни доказательности согласно общепринятой классификации Оксфордского центра доказательной медицины [11] (табл. 22.1).
Таблица 22.1. Уровни доказательности и степени рекомендаций на основании руководства Оксфордского центра доказательной медицины
|
Уровень |
Диагностическое исследование |
Терапевтическое исследование |
|
1а |
Систематический обзор гомогенных диагностических исследований 1-го уровня |
Систематический обзор гомогенных РКИ |
|
1b |
Валидизирующее когортное исследование с качественным «золотым стандартом» |
Отдельное РКИ (с узким доверительным интервалом) |
|
1с |
Специфичность или чувствительность столь высокие, что положительный или отрицательный результат позволяет исключить/установить диагноз |
Исследование «Всё или ничего» |
|
2а |
Систематический обзор гомогенных диагностических исследований >2-го уровня |
Систематический обзор (гомогенных) когортных исследований |
|
2b |
Разведочное когортное исследование с качественным «золотым стандартом» |
Отдельное когортное исследование (включая РКИ низкого качества; т.е. с <80% пациентов, прошедших контрольное наблюдение) |
|
2с |
Нет |
Исследование «исходов»; экологические исследования |
|
3а |
Систематический обзор гомогенных исследований уровня 3b и выше |
Систематический обзор гомогенных исследований «случай–контроль» |
|
3b |
Исследование с непоследовательным набором или без проведения исследования «золотого стандарта» у всех испытуемых |
Отдельное исследование «случай– контроль» |
|
4 |
Исследование «случай–контроль» или исследование с некачественным или зависимым «золотым стандартом» |
Серия случаев (и когортные исследования или исследования «случай–контроль» низкого качества) |
|
5 |
Мнение экспертов без тщательной критической оценки или основанное на физиологии, лабораторные исследования на животных или разработка «первых принципов» |
Мнение экспертов без тщательной критической оценки, лабораторные исследования на животных или разработка «первых принципов» |
|
Степени рекомендаций (убедительности доказательств) | ||
|
A |
Согласующиеся между собой исследования 1-го уровня | |
|
B |
Согласующиеся между собой исследования 2-го или 3-го уровня или экстраполяция на основе исследований 1-го уровня | |
|
C |
Исследования 4-го уровня или экстраполяция на основе уровня 2 или 3 | |
|
D |
Доказательства 4-го уровня или затруднительные для обобщения или некачественные исследования любого уровня | |
ВАЛИДИЗАЦИЯ РЕКОМЕНДАЦИЙ
Настоящие рекомендации в предварительной версии были рецензированы независимыми экспертами, которых попросили прокомментировать прежде всего, насколько интерпретация доказательств, лежащих в основе рекомендаций, доступна для понимания. Получены комментарии со стороны руководителей отделений (кабинетов) реабилитации стомированных пациентов и врачей амбулаторного звена лечебно-профилактического учреждения. Полученные комментарии тщательно систематизировались и обсуждались на совещаниях экспертной группы.
Последние изменения в настоящих рекомендациях были представлены для дискуссии на заседании профильной комиссии «Колопроктология» Экспертного совета Минздрава России 12 сентября 2013 г. Проект рекомендаций был повторно рецензирован независимыми экспертами и врачами амбулаторного звена. Для окончательной редакции и контроля качества рекомендации были повторно проанализированы членами экспертной группы, которые пришли к заключению, что все замечания и комментарии приняты во внимание, риск систематических ошибок при разработке рекомендаций сведен к минимуму.
ОБЛАСТЬ ПРИМЕНЕНИЯ РЕКОМЕНДАЦИЙ
Данные клинические рекомендации применимы при осуществлении медицинской деятельности в рамках Порядка оказания медицинской помощи взрослому населению с заболеваниями толстой кишки, анального канала и промежности колопроктологического профиля.
Определение
Стома — это противоестественное отверстие, искусственно созданное хирургическим путем. Вслед за удалением части кишечника на передней брюшной стенке формируется постоянный или временный свищ, через который происходит неконтролируемое отхождение газов, содержимого кишечника.
Код по Международной классификации болезней 10-го пересмотра
В МКБ-10 термины «колостома» и «илеостома» употребляются для обозначения следующих состояний:
n наличие илеостомы (Z93.2);
n наличие колостомы (Z93.3);
n дисфункция после колостомии и энтеротомии (K91.4);
n осложнения колои илеостом (K45, K56.6, K63.8).
Классификация
КЛИНИЧЕСКАЯ КЛАССИФИКАЦИЯ КИШЕЧНЫХ СТОМ [12, 13]
По локализации на кишечнике:
n еюностома;
n илеостома;
n колостома (асцендостома, трансверзостома, десцендостома, сигмостома);
n цекостома;
n аппендикостома.
По методу формирования:
n одноствольная;
n двуствольная: петлевая; раздельная;
n краевая (пристеночная).
По способу выведения на переднюю брюшную стенку:
n чрезбрюшная (внутрибрюшная);
n забрюшинная.
По технике формирования:
n «плоская»;
n «столбиком».
По прогнозу в плане хирургической реабилитации:
n постоянная;
n временная.
По месту наложения стомы на теле пациента:
n абдоминальная;
n промежностная.
По наличию осложнений:
n осложнения стомы;
n перистомальные кожные осложнения.
Организация помощи стомированным пациентам
СТРУКТУРА ПОМОЩИ
Первым звеном в структуре региональной службы реабилитации стомированных больных является кабинет реабилитации стомированных больных [13, 14]. В целях повышения доступности и качества колопроктологической помощи, оказываемой населению Российской Федерации, приказом Министерства здравоохранения и социального развития РФ от 2 апреля 2010 г. № 206-н утверждено Положение о кабинете реабилитации стомированных больных. Согласно этому положению, кабинет создается в структуре медицинской организации, оказывающей колопроктологическую помощь, и предназначен для проведения диагностических, лечебных, профилактических и реабилитационных мероприятий стомированным пациентам. В ряде регионов кабинеты реабилитации
стомированных больных организованы на базе онкологических диспансеров и/или крупных хирургических учреждений на основании региональных законодательных актов.
В хирургическом отделении обязанности по уходу за стомированными больными целесообразно возложить на перевязочных медицинских сестер. Для успешной работы они должны пройти базовое обучение по уходу за стомой в кабинете реабилитации стомированных больных, работать в тесном контакте с сотрудниками кабинета. Совместно с лечащим врачом медицинская сестра стационара осуществляет непосредственный послеоперационный уход и наблюдение стомированных пациентов, организует обучение больных и их родственников навыкам ухода за стомой; накануне выписки из стационара направляет больных в кабинет реабилитации стомированных больных для подбора средств ухода для постоянного использования, диспансерного наблюдения.
МЕРОПРИЯТИЯ ПО МЕДИЦИНСКОЙ РЕАБИЛИТАЦИИ ПАЦИЕНТОВ С КИШЕЧНОЙ СТОМОЙ
Стомированные пациенты нуждаются в комплексной медико-социальной программе реабилитации [15]. Общими принципами реабилитации являются индивидуальность, последовательность, непрерывность и комплексность.
Условно процесс медицинской реабилитации можно разделить на следующие этапы: предоперационный, послеоперационный, реконвалесцентный.
Каждый этап характеризуется мероприятиями медицинского, педагогического, психологического и социального характера, реализуемыми медицинскими и немедицинскими участниками, обеспечивающими условия для проведения комплексной реабилитации стомированных пациентов [16, 17].
Предоперационный этап включает:
n обследование и клиническую диагностику;
n психологическую подготовку;
n адекватное информирование пациента и его родственников;
n выбор тактики оперативного вмешательства;
n определение места наложения стомы на передней брюшной стенке;
n информационное обеспечение пациента соответствующими пособиями по уходу за стомой и образцами технических средств реабилитации Предоперационная подготовка осуществляется врачами (хирургами, колопроктологами, онкологами) и медицинскими работниками, специально обученными уходу за стомированными пациентами.
Послеоперационный этап включает:
n обследование и постоянное наблюдение за стомированным пациентом;
n выявление осложнений после операции;
n специализированный уход за стомированным пациентом; индивидуальный подбор и обеспечение средствами ухода за стомой в отделении стационара;
n обучение стомированного пациента и его родственников навыкам по уходу за стомой;
n обеспечение стомированного пациента и его родственников специальной литературой и пособиями по уходу за стомой;
n психологическую поддержку;
n информирование стомированного пациента и его родственников о его льготном праве бесплатного получения средств ухода за стомой и выдачей соответствующих документов, в том числе алгоритма по оформлению индивидуальной программы реабилитации;
n социальную помощь.
Послеоперационное ведение стомированных пациентов осуществляется хирургами, медицинским персоналом, имеющим стоматерапевтическую подготовку, психологами, работниками социальных служб, врачами клинико-экспертной комиссии, реабилитологами медико-социальной экспертизы.
Реконвалесцентный этап охватывает процесс реабилитации стомированного пациента после его выписки из стационара. К этому времени пациент и его родственники должны уметь пользоваться средствами ухода за стомой, обладать знаниями по уходу за стомой, о режиме и характере питания.
На данном этапе проводятся следующие мероприятия:
n амбулаторное диспансерное наблюдение стомированного пациента;
n окончательный индивидуальный подбор средств ухода за стомой;
n определение степени нетрудоспособности стомированного пациента;
n патронаж социальных служб, социальная помощь;
n психологические консультации;
n занятия в группах взаимопомощи стомированных пациентов;
n правовая помощь и юридические консультации;
n информационное обеспечение публикациями, учебными пособиями по уходу за стомой;
n проведение реконструктивно-восстановительных операций.
Ключевые мероприятия по реабилитации пациентов с кишечной стомой представлены в табл. 22.2.
Таблица 22.2. Программа мероприятий по реабилитации пациентов с кишечной стомой [14]
|
Мероприятия |
Ответственное лицо |
|
До проведения операции | |
|
1. На догоспитальном этапе: |
|
|
а) ознакомление пациентов с характером и целесообразностью предстоящей операции с формированием стомы (беседа) |
Колопроктолог, хирург, онколог |
|
б) разъяснение путей регуляции деятельности стомы, способов ухода за стомой, ознакомление с продукцией по уходу за стомой (беседа, буклет) |
Колопроктолог, хирург, онколог, медицинская сестра по уходу за стомой |
Табл. 22.2. Окончание
|
Мероприятия |
Ответственное лицо |
|
2. В стационаре: |
|
|
а) выбор способа формирования стомы |
Оперирующий хирург |
|
б) выбор места на передней брюшной стенке для стомы |
Оперирующий хирург, медицинская сестра по уходу за стомой |
|
После проведения операции | |
|
1. Использование калоприемников в раннем послеоперационном периоде: |
Лечащий врач, перевязочная медицинская сестра |
|
а) определение размера и типа калоприемника; б) обучение пациента уходу за стомой, формирование навыка ношения калоприемника |
Лечащий врач, медицинская сестра по уходу за стомой |
|
2. Консервативные мероприятия по уходу за стомой: |
|
|
а) рекомендации по диете и режиму питания |
Медицинская сестра по уходу за стомой, лечащий врач |
|
б) выбор типа калоприемника для постоянного использования |
Медицинская сестра по уходу за стомой |
|
в) обучение методу «ирригации» толстой кишки |
Лечащий врач, медицинская сестра по уходу за стомой |
|
г) использование медикаментозных средств при лечении перистомальных кожных осложнений и для регуляции функции толстой кишки |
Лечащий врач, медицинская сестра по уходу за стомой |
|
3. Систематическая диспансеризация стомированных больных в сроки 3–6–12 мес. после операции |
Колопроктолог, медицинская сестра по уходу за стомой |
|
4. Хирургическая реабилитация пациентов со стомой, определение показаний: а) к ликвидации осложнений стомы; б) к реконструктивно-восстановительному оперативному лечению |
Колопроктолог, оперирующий хирург |
ПРОТОКОЛЫ ВЕДЕНИЯ СТОМИРОВАННЫХ ПАЦИЕНТОВ
Протоколы ведения стомированных пациентов составлены согласно правилам, отраженным в Отраслевом стандарте ГОСТ Р 52600– 2006 «Протоколы ведения больных. Общие требования», от 1 октября 2007 г.
В протоколы включены ситуационные модели, наиболее полно описывающие типичные клинические ситуации при работе со стомированными пациентами.
Ситуационная модель определяется клинической ситуацией и связана с группой заболеваний, профильностью и функциональным назначением отделения, медицинского учреждения. Пример ситуационной модели представлен в табл. 22.3.
Таблица 22.3. Оценка пациента перед операцией с формированием кишечной стомы
|
Раздел |
Наименование |
|
Клиническая ситуация |
Оценка состояния пациента перед операцией с формированием стомы |
|
Группа заболеваний |
Заболевания толстой кишки С18–С21, К50–К63 |
|
Профильность подразделения |
Отделение колопроктологии, хирургии, онкологии. Кабинет реабилитации стомированных пациентов |
|
Функциональное назначение отделения |
Хирургическое лечение заболеваний толстой кишки. Проведение реабилитационных мероприятий у пациентов с кишечной стомой |
|
Критерии и признаки, определяющие модель пациента |
Все пациенты, подлежащие хирургическому лечению заболеваний толстой кишки с формированием кишечной стомы |
Ситуационная модель 1
Оценка состояния пациента перед операцией с формированием кишечной стомы (УД 3b, СP C [18, 19])
I. Цель
Для определения объема специализированной помощи необходимо получить всеобъемлющую объективную информацию о пациенте и его родственниках.
II. Процедура
1. Обеспечить приватность общения с пациентом.
2. Провести оценку состояния пациента по следующим параметрам.
2.1. Социальная, культурная и духовная среда.
2.2. Семейный анамнез/предшествующий опыт и имеющиеся представления о диагнозе/стоме.
2.3. Условия для реабилитации.
2.3.1. Домашняя обстановка/наличие санитарно-гигиенических условий.
2.3.2. Поддержка семьи.
2.4. Эмоциональное и психологическое состояние.
2.5. Род занятий и образ жизни.
2.6. История и последствия болезни, адаптация.
2.7. Наличие хронического заболевания/текущее лечение.
2.8. Возможные аллергические реакции.
2.9. Способность к общению.
2.10. Координация движений, острота зрения и ловкость рук.
3. Зафиксировать и обновить информацию о пациенте.
III. Результат
1. Точная информация о пациенте, готовящемся к операции с формированием стомы, задокументирована и подтверждена.
2. Потребности пациента выявлены и задокументированы.
3. План ухода за стомой разработан.
Ситуационная модель 2
Предоперационная подготовка и психологическая помощь пациенту
(УД 1а, СР А [20–24])
I. Цель
Пациент (и/или родственники) должен быть проинформирован о предстоящей операции, а также должен получить необходимую психологическую поддержку.
II. Процедура
1. Обеспечить приватность общения с пациентом (и/или родственниками).
2. Провести оценку состояния пациента по следующим параметрам.
2.1. Степень беспокойства.
2.2. Психологическая адаптация.
2.3. Имеющиеся знания и необходимость в обучении.
3. Помочь пациенту выразить свои чувства, страхи и опасения.
4. Предоставить необходимую информацию о функции стомы, средствах ухода за стомой.
5. Оказать пациенту индивидуальную поддержку и психологическую помощь.
6. Организовать, если необходимо, встречу с членами ассоциации стомированных больных.
7. Организовать, если необходимо, консультации с другими специалистами.
8. Составить и записать отчет на основании полученных данных, ответов пациента и сведений, полученных от других специалистов.
III. Результат
1. Пациент проявляет естественное (нормальное) беспокойство.
2. Пациент осознает необходимость хирургического вмешательства, понимает последствие операции — выведение стомы, знаком с основами ухода за стомой.
3. Вся полученная информация задокументирована. Учебные пособия / материалы:
Образовательные материалы по уходу за стомой.
Ситуационная модель 3
Маркировка местоположения стомы перед операцией (УД 1a, СР А [24–28])
I. Цель
Выбрать наиболее подходящее место расположения стомы.
II. Процедура
1. Обеспечить приватность общения с пациентом.
2. Обеспечить необходимые условия для проведения маркировки стомы (температура помещения, хорошее освещение).
3. Объяснить пациенту необходимость и процедуру проведения маркировки.
4. Оценить тип операции, физическое, психологическое состояние пациента, его социальный статус.
5. Определить конфигурацию передней брюшной стенки для определения наиболее подходящего места выведения стомы.
6. Сделать маркировку стомы.
6.1. Сделать предварительную маркировку.
6.2. Обсудить предварительную маркировку с пациентом.
6.3. Провести корректировку, если необходимо.
6.4. Отметить место выведения стомы на передней брюшной стенке.
7. Документировать полученные данные.
III. Результат
1. Разметка стомы отмечена на наиболее подходящем месте.
2. Выбор разметки и маркировка стомы сделаны при участии пациента.
3. Пациент удовлетворен выбранным местом наложения стомы. Необходимое оборудование и информация.
1. Пластина для маркировки стомы, маркер.
2. Предоперационная информация о пациенте.
Невыполнение маркировки местоположения часто приводит к затруднению в уходе за стомой, а впоследствии — к возникновению осложнений.
Стома должна быть расположена в проекции прямой мышцы живота, при этом избегать близости к линии запланированного разреза, линии талии, пупку, гребню подвздошной кости, нижнему краю реберной дуги, кожным складкам, паховым складкам, послеоперационным рубцам, участкам тела, невидимым пациентом (рис. 22.1). На передней брюшной стенке необходимо выбрать ровную площадку диаметром 10 см (обычный размер пластины современных калоприемников на адгезивной основе). Приложить пластину (или ее макет) таким образом, чтобы она не закрывала линии предполагаемого разреза, пупка; располагалась выше кожной жировой складки в пределах видимости для пациента. Через отверстие в центре сделать метку несмываемым маркером. Местами для формирования петлевой трансверзо-, реже десцендостомы являются правое, левое подреберье на расстояние менее 5 см от реберной дуги
и пупка. При формировании сигмостомы ее располагают в левом нижнем квадранте в точке, расположенной в средней трети линии, соединяющей пупок и передневерхнюю ость гребня подвздошной кости. Илеостому формируют в аналогичном месте справа. При одновременном наложении уростомы и колостомы уростому располагают выше кишечной стомы.
 |
Рис. 22.1. Схема местоположения кишечных стом.
Место расположения стомы должно быть определено в различных положениях больного (стоя, сидя, лежа), так как при переходе из горизонтального положения в вертикальное происходит смещение кожи и подкожной жировой клетчатки вниз, особенно у пациентов с ожирением или дряблой передней брюшной стенкой. Необходимо учитывать также предпочтения больного в одежде, особенно в ношении пояса, ремня. Стому располагают ниже линии талии и пояса, чтобы последний не травмировал кишку. При показаниях к абдоминальной радиотерапии следует избегать запланированного места облучения и располагать стому выше него, по краю прямых мышц живота.
Ситуационная модель 4
Послеоперационная оценка пациента с кишечной стомой (УД 2b, СР B [10, 29])
I. Цель
Получить необходимую информацию о пациенте (его родственниках) для планирования послеоперационного ухода за стомой.
II. Процедура
1. Обеспечить приватность общения с пациентом.
2. Обеспечить необходимые условия для проведения осмотра (температура помещения, хорошее освещение).
3. Объяснить пациенту смысл и необходимость процедуры.
4. Провести оценку состояния пациента по следующим параметрам:
4.1. Диагноз и тип хирургической операции.
4.2. Место расположения стомы и хирургический метод формирования стомы.
4.2.1. Тип стомы.
4.2.2. Размер стомы.
4.2.3 Расположение стомы.
4.3. Состояние и функционирование стомы.
4.3.1. Состояние стомы (форма, состояние кожно-кишечного шва).
4.3.2. Цвет стомы.
4.3.3. Оформленность и объем кишечного отделяемого.
4.4. Состояние кожи в перистомальной области.
4.4.2. Целостность кожи.
4.4.2. Тургор кожи.
4.5. Определить состояние перистомальной области для обеспечения герметичной фиксации калоприемника.
5. Документировать полученные данные.
III. Результат
1. Необходимая информация о прооперированном пациенте получена и задокументирована.
2. Потребности стомированного пациента определены и документально оформлены.
3. План ухода за стомой выработан.
Ситуационная модель 5
Уход за пациентом с илеостомой, колостомой (УД 3b, СР С [10, 30–32])
I. Цель
Обеспечение оптимального ухода за стомой и перистомальной кожей у пациента с илеостомой, колостомой.
II. Процедура
1. Обеспечить приватность общения с пациентом.
2. Обеспечить необходимые условия для проведения ухода за стомой (температура помещения, хорошее освещение).
3. Объяснить пациенту смысл и необходимость процедуры.
4. Подготовить необходимые калоприемники и аксессуары.
5. Разместить пациента максимально удобно для проведения процедуры.
6. Обеспечить надлежащий уход за илеостомой, основанный на оценке состояния пациента.
7. Уделить особое внимание следующим моментам:
7.1. Осмотреть стому и перистомальную кожу на предмет осложнений.
7.2. Определить точный размер и форму стомы.
7.3. Подобрать подходящий калоприемник и аксессуары (если они необходимы).
8. Задокументировать состояние стомы, кожи вокруг стомы, характер и объем кишечного отделяемого, а также дату смены калоприемника.
III. Результат
1. Пациент (и/или родственник) удовлетворен надежностью калоприемника.
2. Осложнения стомы выявлены.
3. Точные записи ведутся. Необходимое оборудование
1. Калоприемники и аксессуары.
2. Послеоперационная документация и записи о ходе проведения процедур.
Особенности ухода в раннем послеоперационном периоде
Для ухода за стомой в раннем послеоперационном периоде используется специальный послеоперационный калоприемник, который наклеивается сразу же по окончании операции. В пластине вырезается отверстие, соответствующее размеру стомы. После наложения пастыгерметик мешок одевают таким образом, чтобы удерживающий стержень располагался поверх пластины. Прозрачный мешок и снимающаяся крышка позволяют контролировать состояние стомы в раннем послеоперационном периоде. На 10–14-й день после операции удерживающий стержень удаляют.
Для дальнейшего ухода за стомой пациенту подбирают одноили двухкомпонентную систему с учетом функциональных особенностей стомы, рельефа перистомальной области, индивидуальных предпочтений пациента.
Послеоперационный эластичный бандаж накладывают поверх калоприемника.
Дренируемый конец мешка для обеспечения своевременного контроля его наполнения вытаскивают через щелевидный разрез на бандаже ниже уровня месторасположения стомы.
Ситуационная модель 6
Ирригация кишечника через стому1 (УД 2b, СР В [33, 34])
I. Цель
Проведение безопасной и эффективной ирригации кишечника.
II. Процедура
1.
1 Ирригация применяется только у пациентов с сигмостомой, строго по рекомендации специалиста и после обучения проведению процедуры.
Обеспечить приватность общения с пациентом.
2. Обеспечить необходимые условия для проведения ирригации кишечника (температура помещения, хорошее освещение).
3. Объяснить пациенту смысл и необходимость процедуры.
4. Подготовить ирригационную систему и необходимые калоприемники и аксессуары.
5. Разместить пациента максимально удобно для проведения процедуры.
6. С помощью пальцевого исследования определить направление кишки.
7. Уделить особое внимание следующим моментам.
7.1. Температура воды.
7.2. Скорость подачи воды в кишечник.
8. Промыть кишку полностью.
9. Проконтролировать, не жалуется ли пациент на боли в животе или на вздутие живота во время проведения процедуры.
10. Задокументировать результаты процедуры.
III. Результат
1. Ирригация проведена безопасным и эффективным способом.
2. Пациент (и/или родственники) удовлетворен проведенной процедурой и полученными объяснениями.
3. Возможные осложнения обнаружены, приняты соответствующие действия по их устранению.
4. Точные записи ведутся. Необходимое оборудование
1. Ирригационная система с регулятором подачи воды и ирригационная воронка.
2. Пластина, сливной рукав, ремень для пластины, зажим.
3. Смазочный гель.
4. Теплая вода.
5. Калоприемник.
6. Документация (карта) пациента.
Ситуационная модель 7
Подготовка к выписке из стационара (УД 2b, СР В [35–37])
I. Цель
Обеспечить преемственность в уходе за стомированными пациентами после выписки из стационара домой.
II. Процедура
1. Обеспечить приватность общения с пациентом.
2. Определить возможные потребности пациента при первом посещении врача (медицинской сестры) после выписки.
2.1. Способность самостоятельно ухаживать за стомой.
2.2. Адаптация пациента к жизни со стомой.
2.3. Финансовое положение.
2.4. Уход за стомой, психологическая и социальная поддержка пациента после выписки.
3. Обучить пациента самостоятельному уходу за стомой, проинформировать о возможных осложнениях, помогать адаптироваться к изменениям в привычном образе жизни.
4. Оценить общее состояние пациента, запланировать день визита к специалисту по реабилитации стомированных пациентов после выписки.
5. Сообщить пациенту адрес специалиста по уходу за стомой поликлинического звена, назначить день посещения.
6. Предоставить информацию о социальной поддержке и ассоциации стомированных пациентов.
7. Задокументировать беседу с пациентом.
III. Результат
1. Пациент доволен оказанной ему помощью и предоставленными рекомендациями.
2. После выписки из стационара пациент продолжает получать специализированную помощь и находится под наблюдением специалистов по уходу за стомой.
Дополнительные материалы
1. Информационные материалы.
2. Выписка (история болезни) пациента.
Ситуационная модель 8
Обучение пациента со стомой (УД 2b, СР В [38–41])
I. Цель
Обучение пациента (и/или родственников) уходу за стомой.
II. Процедура
1. Обеспечить приватность общения с пациентом.
2. Оценить способность пациента обучаться и определить объем необходимой информации.
3. Провести обучение в соответствии с индивидуальными потребностями.
4. Убедиться, что пациент знает и понимает следующее:
4.1. Диагноз и проведенную операцию.
4.2. Уход за стомой и кожей вокруг нее.
4.3. Дренаж и смена калоприемника.
4.4. Решение неожиданных проблем (протекание кишечного содержимого и др.).
4.5. Изменения в диете.
4.6. Изменения в одежде.
4.7. Ограничение физической активности.
4.8. Изменения в сексуальной жизни.
4.9. Подбор соответствующих средств ухода за стомой.
4.10. Обеспечение необходимыми средствами ухода за стомой и аксессуарами.
4.11. Ассоциация стомированных больных и другие группы поддержки.
5. Оценить реакцию пациента на проведенное обучение.
III. Результат
1. Пациент может продемонстрировать полученные навыки ухода за стомой и кожей вокруг стомы.
2. Пациент понимает изменения образа жизни.
3. Пациент доволен обучающей программой и полученными навыками.
Дополнительные материалы
1. Учебные пособия.
2. Образцы средств ухода за стомой и аксессуаров.
3. Информационные материалы о средствах ухода за стомой и аксессуарах.
4. Карта (история болезни) пациента после выписки.
Составление протоколов ведения пациентов с осложнениями кишечной стомы представляло собой трудную задачу ввиду наличия большого количества и разнообразия осложнений, а также возможного их сочетания. В связи с этим были разработаны алгоритмы выбора тактики лечения осложнений, которые включались в протоколы ведения стомированных пациентов в соответствии с конкретной клинической ситуацией.
Диагностика осложнений кишечных стом и выбор метода лечения
Осложнения после операций с формированием стомы являются значительной проблемой для многих пациентов. Исследования, проведенные в разных странах, показывают, что до 71% пациентов с илеостомой и 43% с колостомой имеют осложнения.
КЛАССИФИКАЦИЯ ОСЛОЖНЕНИЙ КИШЕЧНЫХ СТОМ
С точки зрения этиопатогенетических факторов, локализации процесса, клинических проявлений, тактики ведения и лечения стомированных больных целесообразно разделять осложнения кишечных стом на осложнения собственно стом и перистомальные кожные осложнения [42–44]. К осложнениям стомы относят кровотечение, некроз, эвентрацию, поверхностное нагноение (несостоятельность кожно-кишечного шва), парастомальный абсцесс, флегмону, ретракцию стомы, пролапс, парастомальные грыжи, стеноз, свищи, гиперплазию слизистой оболочки кишки, рецидив опухоли в области стомы. Осложнения стомы, как правило, описываются изменением самой кишки или ее отношением к пе-
редней брюшной стенке.
К перистомальным кожным осложнениям относят контактный перистомальный дерматит, аллергический дерматит, фолликулит, гангренозную пиодермию, гиперкератоз, гипергрануляции кожи, специфические поражения (грибковый дерматит, псориаз и др.). Перистомальные кожные осложнения характеризуются изменениями кожных покровов.
АЛГОРИТМ ДИАГНОСТИКИ ОСЛОЖНЕНИЙ КИШЕЧНЫХ СТОМ И ВЫБОРА МЕТОДА ЛЕЧЕНИЯ
![]()
![]() Для диагностики осложнений стомы используют алгоритм, изображенный на рисунке 22.2.
Для диагностики осложнений стомы используют алгоритм, изображенный на рисунке 22.2.
Рис. 22.2. Алгоритм диагностики осложнений кишечных стом.
После определения локализации осложнений (стома или кожа вокруг стомы) визуально устанавливают характер изменений в области стомы. Если изменения касаются самой выведенной на переднюю брюшную стенку кишки, оценивают их характер при внешнем осмотре (рис. 22.3).
При этом определяют расположение кишки по отношению к уровню брюшной стенки, конфигурацию брюшной стенки в парастомальной
Рис. 22.3. Определение характера изменений в области стомы с помощью внешнего осмотра.
области, оценивают диаметр кишки и состояние ее стенки, выявляют изменения парастомальной раны. При пальцевом исследовании стомы определяют размер стомы, наличие или отсутствие дефекта в апоневрозе, расположение петли кишки или сальника в клетчатке вокруг стомы, выявляют дефект стенки кишки или наличие инфильтрата в парастомальной области (рис. 22.4). Важно определить не только характер, но и уровень выявленных изменений (кожа, подкожная клетчатка, апоневроз), так как это имеет значение для выбора тактики лечения осложнений
![]()
![]() Рис. 22.4. Определение характера изменений в области стомы с помощью пальцевого исследования.
Рис. 22.4. Определение характера изменений в области стомы с помощью пальцевого исследования.
При необходимости уточнения диагноза применяют инструментальные и лабораторные методы диагностики:
n рентгенологические методы исследования: ирригоскопию, фистулографию;
n КТ (диагностика парастомальных грыж, свищей, стриктур, рецидива опухолевого процесса);
n УЗИ парастомальной области (диагностика парастомальных абсцессов, свищей);
n патоморфологические исследования (дифференциальная диагностика гипергрануляций слизистой оболочки, рецидива опухоли в стоме);
n микробиологические исследования раневого отделяемого (диагностика воспалительных осложнений).
Для диагностики перистомальных кожных осложнений применяют алгоритм, построенный с учетом особенностей клинических проявлений поражения кожи (рис. 22.5)
Рис. 22.5. Определение характера изменений кожи в области стомы.
При внешнем осмотре оценивают окраску кожных покровов, наличие и степень их повреждения. Устанавливают связь между появлением изменений в перистомальной области и воздействием различных факторов (протекание кишечного отделяемого под пластину, применение новых средств ухода за стомой, инфицирование кожи или волосяных фолликулов, наличие кожных болезней другой локализации). Для дифференциальной диагностики могут быть использованы патоморфологические и микробиологические исследования.
АЛГОРИТМ ВЫБОРА МЕТОДА ЛЕЧЕНИЯ ОСЛОЖНЕНИЙ СТОМЫ
После выявления осложнений, связанных с наличием стомы, в зависимости от их типа (осложнения стомы, перистомальные кожные осложнения или сочетание осложнений) определяют показания к проведению хирургического или консервативного лечения (рис. 22.6).
Рис. 22.6. Алгоритм выбора метода лечения осложнений кишечной стомы.
Показаниями к хирургическому лечению в экстренном или срочном порядке являются осложнения стомы, угрожающие жизни: эвентрация, кровотечение, глубокий некроз стомы, ретракция кишки ниже уровня апоневроза, высокие тонкокишечные свищи, абсцесс, флегмона в парастомальной области, острая кишечная непроходимость.
В плановом порядке хирургическому лечению подлежат осложнения, нарушающие нормальную функцию кишечника (стриктура, грыжа, пролапс), и осложнения, затрудняющие или делающие невозможным адекватный уход за стомой (ретракция, парастомальная грыжа, стриктура, пролапс). При определении показаний к оперативному лечению учитывают наличие или отсутствие рецидива основного заболевания, тяжелых сопутствующих болезней и степень их компенсации. С учетом всех перечисленных выше факторов избирают вид хирургического лечения:
n реконструкцию стомы с оставлением ее на прежнем месте;
n реконструкцию стомы с перемещением на новое место;
n устранение осложнения стомы в сочетании с реконструктивно-восстановительной операцией.
Консервативное лечение осложнений стомы предпринимается в случае невозможности проведения хирургической коррекции стомы из-за тяжелых сопутствующих заболеваний, рецидива основного заболевания. Этот вид лечения включает:
n этиопатогенетическое лечение;
n индивидуальный подбор технических средств реабилитации;
n использование дополнительных средств ухода за стомой;
n коррекцию нарушений функции организма, кишечника.
Лечение осложнений кишечных стом [46–50]
ХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕ
Лечение ранних осложнений
1. Кровотечение из кишечной стомы
Причины осложнения:
n выделение крови из краев кишки, подшитой к коже;
n кровотечение из сосудов брыжейки при соскальзывании лигатуры.
Способы остановки кровотечения:
n консервативные: холод на область раны, гемостатические материалы;
n хирургические: электрокоагуляция, прошивание кровоточащего участка, ререзекция петли кишки, несущей стому, и повторное формирование стомы.
Возможные осложнения: некроз, сквозное прошивание стенки кишки с последующим развитием гнойно-воспалительных осложнений.
2. Некроз стомы, нарушение кровообращения в кишечной стоме
Частота: 2,3–17,0%.
Причины осложнения:
n перевязка, травматизация, тромбоз краевого сосуда;
n венозный застой вследствие отека кишки;
n недостаточная мобилизация сегмента кишки, выводимого на переднюю брюшную стенку;
n сдавление кишки в тканях передней брюшной стенки (избыточное количество жировой клетчатки брыжейки, узкий канал в передней брюшной стенке);
n перекрут кишки, выводимой на переднюю брюшную стенку.
Лечение
Если признаки нарушения кровообращения в выведенной на переднюю брюшную стенку кишке наблюдаются уже на операционном столе, необходимо выполнить повторное формирование кишечной стомы.
При нарушении кровообращения кишки на уровне кожи возможно придерживаться консервативной тактики, тем более при общем тяжелом состоянии пациента, принимая во внимание тот факт, что у больных данной категории вероятность развития ретракции и гнойно-воспалительных осложнений, а в отдаленных сроках стриктуры стомы достоверно увеличивается.
При распространении нарушения кровообращения вплоть до уровня апоневроза и проксимальнее необходимо повторное хирургическое вмешательство, включающее ререзекцию сегмента кишки, несущего стому, и повторное формирование кишечной стомы.
Профилактические мероприятия:
n адекватная оценка кровообращения в сегменте кишки, планируемом к выведению на переднюю брюшную стенку в качестве стомы;
n полная подготовка к выведению кишки на внутрибрюшном этапе, а не после выведения на переднюю брюшную стенку;
n участок кишки, освобожденный от брыжейки, должен быть не более 5 см;
n при высокой перевязке нижней брыжеечной артерии необходимо сохранение восходящей ветви;
n при формировании петлевой превентивной стомы и совокупности неблагоприятных факторов отдать предпочтение илеостоме.
3. Эвентрация кишечной стомы
Частота: редкое осложнение.
Лечение: экстренное хирургическое вмешательство с ушиванием дефекта передней брюшной стенки и повторным формированием кишечной стомы.
4. Ретракция кишечной стомы
Ретракция стомы — расположение стенки кишки ниже уровня кожи, циркулярное или частичное.
Частота осложнения: 3–14% для колостом, 3–17% для илеостом. Достоверно чаще возникает у лиц с ожирением.
Факторы риска и причины развития осложнения:
n недостаточная длина сегмента кишки, выводимого на переднюю брюшную стенку, и его натяжение;
n нарушения кровообращения и некроз стомы;
n плохое приживление кишки вследствие истощения, длительной гормональной терапии, химиотерапии и лучевого лечения;
n неадекватная фиксация кишки к коже;
n вскрытие парастомальной патологической полости (гнойник, гематома, серома).
Лечение
n При образовании частичного дефекта — консервативное лечение.
n При достаточной подвижности стенки кишки возможно выполнить повторное подшивание кишки к коже передней брюшной стенки.
n При ретракции кишки до уровня апоневроза и/или постепенном прогрессировании гнойно-воспалительного процесса больному показано хирургическое лечение:
v ререзекция кишки, несущей стому, и перенос стомы в другое место (транспозиция стомы);
v при невозможности и повышенном риске такого вмешательства — формирование проксимальной двуствольной стомы с целью выключения осложненной стомы из пассажа.
Профилактические мероприятия:
n достаточная мобилизация сегмента кишки, выводимого на переднюю брюшную стенку. При необходимости выполняют мобилизацию левого или правого изгибов ободочной кишки;
n при невозможности сформировать двуствольную стому без натяжения следует сформировать одноствольную стому с дополнительным рассечением брыжейки;
n стома должна возвышаться над уровнем кожи приблизительно на 2,5 см. Если длина «кишечного столбика» менее 10 мм, то вероятность осложнений резко увеличивается (до 35%).
5. Гнойно-воспалительные осложнения
Варианты осложнений: нагноение раны, расхождение кожно-кишечного шва (полное или частичное, поверхностное или глубокое), парастомальный абсцесс, парастомальная флегмона передней брюшной стенки.
Частота: 2–14,8%.
Лечение
n При поверхностной локализации осложнений — снятие швов и дренирование через слизисто-кожную рану с использованием абсорбирующих и альгинатных повязок, 2-компонентных систем.
n При локализации гнойно-воспалительного очага в тканях брюшной стенки до уровня апоневроза — пункция, вскрытие и дренирование через кожу передней брюшной стенки вне области фиксации калоприемника.
n При высокой вероятности перехода гнойно-воспалительного процесса в жизненно опасные формы (сепсис, распространенная флегмона передней брюшной стенки, угроза прорыва гнойника в брюшную полость) — формирование проксимальной кишечной стомы или ликвидация осложненной стомы, ререзекция кишки, несущей стомы с формированием новой стомы в иной анатомической области передней брюшной стенки.
Профилактика:
n минимальная травматизация выводимой на переднюю брюшную стенку кишки;
n тщательный гемостаз и своевременная ликвидация гематом и сером в стомальной ране;
n антибактериальная терапия и эффективное лечение основного заболевания.
Лечение поздних осложнений
1. Эвагинация (пролапс, выпадение) кишечной стомы
Определение: выворачивание кишки, несущей стому, и отделов, располагающихся в брюшной полости, через стомальное отверстие.
Частота осложнения: 2–26%, в среднем для колостом — 11,8%, для илеостом — 11%.
Факторы риска и причины развития осложнения:
n ожирение;
n повышенное внутрибрюшное давление;
n избыточная длина выводимой на переднюю брюшную стенку кишки.
Показания к хирургическому лечению:
n развитие осложнений (нарушение кровообращения в кишке, нарушение кишечной проходимости);
n невозможность адекватного ухода за стомой.
Лечение эвагинации кишечной стомы
n Клинически значимая эвагинация, требующая хирургического лечения, в большинстве случаев сочетается с парастомальной грыжей, операции направлены на ликвидацию обоих осложнений. Резекцию несущей стому кишки выполняют при наличии выраженных изменений стенки.
n При выраженных сопутствующих заболеваниях и невыраженной сопутствующей парастомальной грыже показано выполнение ликвидации эвагинации стомы по типу операции Альтмайера: отсечение кишки на 1 см кнутри от слизисто-кожного рубца, резекция выпадающего сегмента кишки и формирование анастомоза ручным способом.
Профилактика
n Риск эвагинации и формирования парастомальной грыжи снижается при использовании синтетических сеток. Дополнительная фиксация брыжейки не снижает вероятности эвагинации кишечной стомы.
2. Парастомальная грыжа
Частота: в зависимости от критериев оценки частота развития грыж при двуствольных колостомах составляет 0–30,8%, при двуствольных илеостомах — 0–6,2%, при концевых колостомах — 4–45%, при концевых илеостомах — 1,8–28,3%.
Факторы риска и причины развития осложнений
Общие причины:
n возраст, ожирение;
n прием стероидов;
n парастомальные гнойно-воспалительные осложнения;
n хронический кашель и другие факторы резкого повышения внутрибрюшного давления.
Технические причины:
n выведение кишки за пределы прямой мышцы живота;
n избыточно широкое по отношению к ширине просвета кишки отверстие в передней брюшной стенке;
n наложение кишечной стомы при операциях, выполняемых по экстренным показаниям;
n формирование внутрибрюшной стомы.
Классификация парастомальных грыж:
n интерстициальные — грыжевой мешок располагается в пределах тканей передней брюшной стенки;
n подкожные — грыжевой мешок располагается под кожей перистомальной области;
n интрастомальные — грыжевой мешок достигает области слизисто-кожного рубца;
n парастомальные — грыжевой мешок располагается в выпадающей части стомы.
Возможные осложнения парастомальных грыж:
n ущемление;
n некроз, кровотечение;
n кишечная непроходимость.
Показания к хирургическому лечению:
n развитие осложнений;
n невозможность адекватного ухода за стомой и снижение качества жизни пациента.
Способы хирургического лечения:
n лапаротомия, перевод внутрибрюшной стомы в забрюшинную с пластикой дефекта передней брюшной стенки;
n лапаротомия, транспозиция стомы с дополнительным укреплением новой стомы синтетическим материалом;
n пластика синтетическим материалом (с расположением сетки над апоневрозом, под апоневрозом, пластика по Sugarbaker, применение 3D-сетки).
Ликвидация грыжи местным доступом и пластика дефекта местными тканями сопровождаются крайне высоким риском рецидива (46–100%) и целесообразны при ликвидации осложнений на фоне выраженных сопутствующих заболеваний, существенно увеличивающих риск более обширных вмешательств.
3. Стриктура кишечной стомы
Частота: 2–15%.
Факторы риска и причины возникновения:
n ретракция;
n неправильный выбор места для стомы;
n узкое отверстие на коже при формировании стомы;
n местные гнойно-воспалительные осложнения;
n травматизация при частых манипуляциях;
n пренебрежение формированием кожно-слизистого шва;
n рецидив заболевания (болезнь Крона, опухоль).
Лечение стриктуры кишечной стомы
n При короткой стриктуре, достаточной длине мобилизуемой в пределах передней брюшной стенки кишки, несущей стому, — реконструкция стомы местным доступом.
n При протяженной стриктуре, недостаточной длине кишки в тканях передней брюшной стенки, выраженном перистомальном рубцовом и/или воспалительном процессе — лапаротомия и транспозиция стомы.
КОНСЕРВАТИВНОЕ ЛЕЧЕНИЕ
Ретракция стомы:
n двухкомпонентная система с конвексными пластинами и поясом для дополнительной фиксации пластины;
n паста-герметик (в полосках) или адаптационное кольцо для выравнивания углубления + однокомпонентная система;
n рекомендации по снижению массы тела;
n обучение ирригации (при сигмостоме).
Парастомальная грыжа:
n переход на более гибкие калоприемники (однокомпонентные, двухкомпонентные с адгезивным фланцем);
n использование специального пояса или эластичного бандажа. Вырезание отверстия в бандаже в проекции стомы недопустимо из-за увеличения риска возникновения пролапса и парастомальной грыжи!
n прекращение ирригации.
Пролапс (эвагинация) стомы:
n вправление кишки вручную (для уменьшения отека используется лед или сахарная пудра) в положении пациента лежа;
n бандаж эластичный после вправления кишки, поверх калоприемника;
n калоприемники с большим вырезаемым отверстием, большого объема, прозрачные мешки (для наблюдения за цветом стомы).
Стриктура стомы:
n бужирование (при полноценном инструктаже пациентов позволяет в 52–60% избежать операции);
n двухкомпонентные калоприемники (для удобного ежедневного доступа к стоме), реже однокомпонентные с закрытыми (недренируемыми) мешками;
n расслабляющие средства (осмотические слабительные).
Парастомальные свищи:
n дренаж свища;
n тотальное парентеральное питание для уменьшения отделяемого из свища пастой-герметик, двухкомпонентная система, конвексная пластина (в случае пристеночного свища в области кожно-кишечного соединения);
n раневые (послеоперационные) мешки, позволяющие контролировать отхождение содержимого по свищу, при необходимости дренировать его, промывать;
n защитная пленка для профилактики повреждения перистомальной кожи.
Нагноение (несостоятельность кожно-слизистого шва):
n тщательный осмотр: определение глубины раны и наличия раневой полости;
n промывание и очищение раны антисептическими растворами;
n открытый дренаж или влажное заживление (ранозаживляющий порошок, альгинатные повязки, гидроколлоидные повязки) + паста-герметик, двухкомпонентные калоприемники.
СОВРЕМЕННЫЕ ПРИНЦИПЫ ЛЕЧЕНИЯ КОЖНЫХ ПОВРЕЖДЕНИЙ В ОБЛАСТИ СТОМЫ [42, 51–56]:
n защита окружающей стому кожи обеспечивается адекватным использованием современных адгезивных калоприемников и средств ухода за кожей;
n «влажное заживление» поврежденной кожи достигается использованием калоприемников и перевязочных средств на гидроколлоидной основе;
n двухкомпонентные системы калоприемников, благодаря смене 1 раз в 3–5 дней, обеспечивают щадящий уход и оптимальный лечебный эффект при поражении кожи вокруг стомы;
n для эффективного лечения и профилактики кожных осложнений больной или его родственники должны быть хорошо обучены использованию средств ухода.
Аллергический дерматит:
n замена на другую марку калоприемника;
n двухкомпонентная система;
n гидрокортизоновая мазь, эмульсия (аппликации), стероидный аэрозоль;
n защитный крем;
n защитная пленка;
n оральные и местные антигистаминные средства.
Контактный дерматит:
n исключение механического повреждения кожи (аккуратное отклеивание калоприемника, щадящий, с помощью мягких материалов, уход за стомой);
n исключение химического воздействия на кожу (предотвращение протекания кишечного отделяемого за счет обеспечения герметичного прилегания пластины к коже вокруг стомы, обеспечение ухода за кожей с помощью нейтральных средств);
n использование двухкомпонентных калоприемников.
Применение в зависимости от степени повреждения кожи следующих средств:
n эритема — защитный крем, защитная пленка;
n мацерация, эрозия — ранозаживляющий, абсорбирующий порошок для подсушивания кожи, возможно применение 0,5–1% раствора бриллиантового зеленого. При выраженном поражении рекомендуется 1–2-кратное использование гидрокортизоновой мази, эмульсии;
n язва — ранозаживляющий порошок, паста, гидроколлоидная пластина;
n регуляция стула (следует избегать неустойчивого стула, диареи).
Фолликулит:
n срезание волос на коже вокруг стомы, аккуратное отклеивание пластин (без выдергивания волосков), адекватный уход за кожей;
n использование двухкомпонентных калоприемников;
n использование местных антисептиков (0,5–1,0% раствор бриллиантового зеленого), при выраженных воспалительных явлениях рекомендуется пероральный прием антибиотиков;
n коррекция общего состояния (иммуностимулирующая терапия, витаминотерапия).
Гипергрануляции кожи:
n аккуратное вырезание отверстия в пластине, чтобы его края не травмировали слизистую оболочку и кожу вокруг стомы;
n использование двухкомпонентных калоприемников;
n удаление грануляций при выраженных симптомах (боль, кровотечение, протекание) прижиганием (ляписный карандаш, электрокоагуляция);
n использование пасты-герметик поверх грануляций.
Гангренозная пиодермия [прогрессивный некроз кожи неизвестной этиологии наблюдается при язвенном колите и болезни Крона с равной частотой (1,5–5,0%)]:
n хирургическая обработка раны (пустулы, язвы) под местной анестезией;
n локальное применение стероидных препаратов (обезжиренного состава) или иммунодепрессивных средств в сочетании с альгинатными повязками с серебром;
n использование гидроколлоидных повязок;
n двухкомпонентные системы калоприемников.
При неэффективности местного лечения в течение 2 нед используется комплексная лечебная терапия, включающая антибиотики, системные кортикостероиды и иммунодепрессанты. Биологическая терапия может быть полезной для улучшения заживления язв у пациентов, которые не отвечают или частично отвечают на предшествующую терапию. Перенос стомы в другое место применяют, если все другие варианты лечения были исчерпаны и только у больных со стабильным течением заболевания или при частичной ремиссии [57–59].
Сочетанные осложнения кишечной стомы. Тактику лечения выбирают в зависимости от преобладания осложнений самой стомы (хирургическое лечение) или кожных перистомальных изменений (консервативное лечение).
Технические средства реабилитации для стомированных пациентов
К техническим средствам реабилитации, включенным в Федеральный перечень реабилитационных мероприятий, относятся средства, используемые при нарушении функций выделения при противоестественных
отверстиях — стомах (калои мочеприемники и вспомогательные принадлежности к ним).
Калоприемники — это устройства, фиксирующиеся на теле больного, предназначенные для сбора кишечного содержимого и устранения его агрессивного воздействия на кожу. К калоприемникам предъявляется ряд требований: безопасность для кожных покровов, полная и надежная изоляция кишечного содержимого от внешней среды и элементов одежды пациента, герметичность, прочность прикрепления, а также незаметность под одеждой, простота использования.
ОБЩАЯ ХАРАКТЕРИСТИКА ТЕХНИЧЕСКИХ СРЕДСТВ РЕАБИЛИТАЦИИ ДЛЯ СТОМИРОВАННЫХ ПАЦИЕНТОВ
Калоприемники
Все клеящиеся (адгезивные) калоприемники можно разделить на два основных вида — однокомпонентные и двухкомпонентные [13].
Однокомпонентный калоприемник представляет собой стомный мешок со встроенной адгезивной (клеевой) пластиной.
Однокомпонентные калоприемники могут быть дренируемыми (открытыми) или недренируемыми (закрытыми). Однокомпонентные калоприемники (дренируемые) имеют конструкцию со специальным отверстием внизу мешка, закрывающимся зажимом, что позволяет опорожнять его по мере наполнения.
Двухкомпонентный калоприемник представляет собой комплект, состоящий из двух частей — адгезивной (клеевой) пластины и стомного мешка, он имеет специальное устройство для крепления мешка к пластине. Пластины и стомные мешки имеют специальные фланцы для соединения друг с другом. При подборе двухкомпонентной системы необходимо соответствие фланца мешка и фланца пластины. Производители предлагают различные системы фланцевых соединений: механическое (фланец мешка надевается на фланец пластины или мешок крепится на фланце пластины с помощью фланцевого кольца-защелки) и адгезивное (фланец мешка приклеивается к фланцу пластины).
Современные клеящиеся калоприемники изготовлены из полимерных материалов. Адгезивные пластины имеют гипоаллергенную гидроколлоидную основу, которая предохраняет кожу, обладает защитными, заживляющими и адгезивными свойствами. Пластины могут иметь различную форму: круглую, овальную, квадратную, а также они могут быть плоскими и конвексными (вогнутыми).
Конвексные пластины имеют различную величину вогнутости. Эти пластины предназначены для пациентов со втянутыми стомами, стомами, находящимися между кожными складками или на уровне кожи. Адгезивы пластин различны по своим функциональным характеристикам: адгезивы стандартные, для длительного ношения, для чувствительной кожи.
Стомные мешки изготавливаются из непрозрачного или прозрачного многослойного, не пропускающего запах биостабильного полиэтилена. Стомные мешки могут быть недренируемыми (закрытыми) или дренируемыми (открытыми).
Дренируемые калоприемники имеют специальное дренажное отверстие внизу мешка, дренажный конец мешка закрывается зажимом, что позволяет опорожнять мешок по мере его наполнения.
Недренируемые калоприемники должны быть обязательно оснащены фильтрами, которые не только нейтрализуют запах, но и позволяют удалить из мешка избыточный воздух, препятствуя надуванию мешка. Наличие фильтра в дренируемом мешке необязательно, так как избыток воздуха удаляется при дренировании мешка, кроме того, современные калоприемники отличаются высокой герметичностью и не пропускают запах.
Некоторые виды калоприемников имеют на пластине или мешке специальные крепления для пояса.
Наряду с калоприемниками на адгезивной основе используются калоприемники из пластмассы, крепящиеся к телу с помощью пояса. Однако они не обладают всеми перечисленными выше свойствами и не дают возможности проводить полноценную реабилитацию стомированных пациентов.
Послеоперационные дренируемые универсальные стомные мешки, прозрачные, со встроенной адгезивной пластиной без окошка или с окошком для инспекции стомы, со сливным клапаном или с клеящимся гибким зажимом, накладывают сразу после завершения операции по формированию стомы.
Вспомогательные средства для ухода за стомой
Вспомогательные средства для ухода за стомой (паста, порошок, дезодоранты, поглотители запаха, уплотнительные кольца, стержни под двуствольную стому, ирригаторы, абсорбенты и др.) и средства ухода за кожей вокруг стомы (очистители, защитные пленки, кремы).
Очиститель для кожи вокруг стомы используется для обработки кожи вокруг стомы или фистулы, служит эффективным средством, замещающим мыло и воду, растворители или другие агрессивные и высушивающие кожу вещества, которыми пользуются пациенты со стомами.
Защитная пленка для кожи вокруг стомы используется для защиты кожи от агрессивных выделений или от повреждений, вызываемых при удалении адгезива с кожи вокруг стомы.
Пленка не растворяется в воде и обеспечивает защиту даже при купании.
Защитный крем для кожи вокруг стомы используется для защиты кожи от воздействия вредных выделений из стомы. Обладает водоотталкивающими свойствами, смягчает кожу, восстанавливает нормальный уровень pH кожи, предохраняет ее от повреждения.
Паста-герметик используется для защиты кожи вокруг стомы от возможного раздражения, так как, засыхая, паста образует долговременный влагонепроницаемый барьер, предотвращая затекание содержимого под пластину. Паста также используется для заполнения неровностей на коже вокруг стомы (рубцы, впадины и другие деформации), образуя тем самым плоскую поверхность для наложения пластины. Паста обеспечивает герметичное крепление калоприемника на коже, остается мягкой и гибкой, отделяется от кожи вместе с калоприемником при его замене, продлевает срок ношения калоприемника.
Существуют варианты пасты в виде полоски, уплотняющих колец.
Абсорбирующий порошок используется для лечения мацерации и эрозирования кожи в перистомальной области, а также для лечения поверхностных ран при расхождении кожно-кишечного шва.
ПОДБОР ТЕХНИЧЕСКИХ СРЕДСТВ РЕАБИЛИТАЦИИ БОЛЬНЫХ С КИШЕЧНОЙ СТОМОЙ
Выбор модели калоприемника, дополнительных средств ухода за кожей вокруг стомы определяется индивидуально, с учетом места наложения стомы, ее типа и размера, наличия осложнений стомы, а также состояния кожи вокруг нее. Правильное использование продукции обеспечивает гарантированную надежность крепления к коже, максимально щадящее воздействие на нее, безболезненное удаление калоприемника, герметичность и незаметность для окружающих [60].
Алгоритм подбора технических средств реабилитации пациентов с кишечной стомой
n Определить вид стомы.
n Оценить размер, конфигурацию, месторасположение стомы.
n Выявить наличие или отсутствие осложнений стомы, перистомальных кожных осложнений.
n Установить психофизические особенности пациента.
n Определить размер и тип калоприемника.
n Определить норму выдачи технических средств реабилитации.
ПОКАЗАНИЯ И ПРОТИВОПОКАЗАНИЯ К ПРИМЕНЕНИЮ ТЕХНИЧЕСКИХ СРЕДСТВ РЕАБИЛИТАЦИИ У СТОМИРОВАННЫХ ПАЦИЕНТОВ
Показания и противопоказания к применению технических средств реабилитации у стомированных пациентов представлены в таблице 22.4.
СИСТЕМА ОБЕСПЕЧЕНИЯ СТОМИРОВАННЫХ ПАЦИЕНТОВ ТЕХНИЧЕСКИМИ СРЕДСТВАМИ РЕАБИЛИТАЦИИ
Порядок обеспечения стомированных пациентов специальными средствами реабилитации регулируется законодательными актами, предусматривающими финансирование расходов на технические средства реабилитации за счет региональных бюджетов. Пациенты с кишечной стомой — инвалиды по российскому законодательству имеют право на льготное обеспечение средствами ухода и лекарствами.
Таблица 22.4. Перечень показаний и противопоказаний к применению технических средств реабилитации
|
Пункт раздела «Технические средства реабилитации» Федерального перечня |
Номер вида технического средства реабилитации (изделий) |
Вид технического средства реабилитации (изделия)* |
Медицинские показания для обеспече- ния инвалидов техническими средствами реабилитации |
Медицинские противопоказания для обеспечения инвалидов техническими средствами реабилитации** |
|
21. Специальные средства при нарушениях функций выделения (мочеи калоприемники) |
21–01 |
Адгезивная пластина для двухкомпонентного калоприемника |
Наличие кишечной стомы (колостомы, или илеостомы, или еюностомы), кишечного свища на передней брюшной стенке |
Наличие изогнутых поверхностей в перистомальной области, парастомальной грыжи (для калоприемников с жестким фланцем) |
|
• плоская |
Кожные осложнения в перистомальной области | |||
|
• конвексная |
Ретракция (втянутость) кишечной стомы, стомы, находящейся между кожными складками или на уровне кожи | |||
|
21–02 |
Однокомпонентный дренируемый калоприемник |
Наличие кишечной стомы (колостомы, или илеостомы, или еюностомы), кишечного свища на передней брюшной стенке |
Наличие перистомального дерматита, стриктуры стомы при необходимости ее бужирования | |
|
21–03 |
Однокомпонентный недренируемый калоприемник |
Наличие колостомы (сигмостомы, десцендостомы) с оформленным кишечным отделяемым |
Наличие парастомальной грыжи, перистомального дерматита | |
|
21–04 |
Мешок, дренируемый для двухкомпонентного калоприемника |
Наличие илеостомы, или еюностомы, колостомы с жидким кишечным отделяемым |
Нет |
Табл. 22.4. Продолжение
|
Пункт раздела «Технические средства реабилитации» Федерального перечня |
Номер вида технического средства реабилитации (изделий) |
Вид технического средства реабилитации (изделия)* |
Медицинские показания для обеспече- ния инвалидов техническими средствами реабилитации |
Медицинские противопоказания для обеспечения инвалидов техническими средствами реабилитации** |
|
|
21–05 |
Мешок, недренируемый для двухкомпонентного калоприемника |
Наличие колостомы (сигмостомы, десцендостомы) с оформленным кишечным отделяемым |
Наличие илеостомы или еюностомы, колостомы с жидким кишечным отделяемым |
|
21–06 |
Пояс для калоприемников и уроприемников |
Необходимость дополнительной фиксации калоприемника или уроприемника |
Нет | |
|
21–07 |
Калоприемник из пластмассы на поясе в ком- плекте с мешками |
Наличие кишечной стомы. Аллергический перистомальный дерматит (непереносимость адгезивов) |
Наличие илеостомы или еюностомы, колостомы с жидким кишечным отделяемым | |
|
21–19 |
Паста-герметик (полоски, кольца) для защиты и выравнивания кожи вокруг стомы |
Наличие илеостомы или еюностомы, кишечного свища на передней брюшной стенке, уростомы. Неровности и кожные осложнения в перистомальной области |
Наличие перистомальных глубоких ран, гнойных осложнений | |
|
21–20 |
Крем защитный (тюбик) |
Для защиты и ухода за кожей вокруг кишечной стомы, кишечного свища или уростомы |
| |
|
21–21 |
Порошок (пудра) абсорбирующий |
Для защиты кожи вокруг кишечной стомы, кишечного свища |
Наличие перистомальных глубоких ран, гнойных осложнений |
Табл. 22.4. Окончание
|
Пункт раздела «Технические средства реабилитации» Федерального перечня |
Номер вида технического средства реабилитации (изделий) |
Вид технического средства реабилитации (изделия)* |
Медицинские показания для обеспече- ния инвалидов техническими средствами реабилитации |
Медицинские противопоказания для обеспечения инвалидов техническими средствами реабилитации** |
|
|
|
|
или уростомы при мацерации (мокнутии) кожи |
|
|
21–22 |
Защитная пленка |
Для защиты кожи вокруг кишечной стомы, кишечного свища или уростомы от контакта с кишечным отделяемым или мочой и механических повреждений при удалении адгезивных пластин |
Наличие перистомальных глубоких ран, гнойных осложнений | |
|
21–23 |
Очиститель для кожи |
Для очищения стомы кожи, вокруг стомы, удаления остатков пасты, адгезивов и других средств ухода за кожей |
| |
|
21–25 |
Средство для опорожнения колостомы |
Для промывания (опорожнения) кишечника только через колостому (сигмостому, десцендостому) |
Дивертикулез ободочной кишки, воспалительные заболевания тостой кишки. Сердечно-сосудистые заболевания в стадии декомпенсации |
* Вид технического средства реабилитации подбирается индивидуально с учетом физиологических особенностей человека и условий использования технического средства реабилитации.
** Медицинские противопоказания для обеспечения инвалидов техническими средствами реабилитации являются основанием для подбора иного показанного технического средства реабилитации.
На основании Федерального закона от 24 ноября 1995 г. № 181 «О социальной защите инвалидов в РФ» государство гарантирует инвалидам получение необходимых технических средств реабилитации, предусмотренных Федеральным перечнем технических средств реабилитации, утвержденным Правительством РФ. В этот Перечень включены технические средства реабилитации при нарушении функций выделения (п. 21 Перечня).
Согласно классификации технических средств реабилитации, утвержденной приказом Минтруда и соцзащиты России от 24 мая 2013 г.
№ 214н, п. 21, к специальным средствам при нарушении функции выделения относятся однои двухкомпонентные калоприемники и уроприемники, средства ухода за кожей вокруг стомы и аксессуары.
Нормы обеспечения (сроки пользования) вышеуказанными средствами утверждены в приказе Минтруда и соцзащиты России от 24 мая 2013 г.
№215н «Об утверждении сроков пользования техническими средствами реабилитации, протезами и протезно-ортопедическими изделиями до их замены»:
n однокомпонентные дренируемые калоприемники — 30 штук в месяц, однокомпонентные недренируемые калоприемники — 60 штук в месяц, однокомпонентные уроприемники — 30 штук в месяц;
n двухкомпонентные калоприемники и уроприемники: пластины — 10 штук в месяц, дренируемые стомные мешки — 30 штук в месяц, недренируемые стомные мешки — 60 штук в месяц, уростомные мешки — 30 штук в месяц.
Рекомендуемые нормы средств ухода за кожей: паста — 1 штука в месяц, защитный крем — 1 штука в месяц, порошок абсорбирующий — 1 штука в месяц, очиститель — 1 штука в месяц, защитная пленка — согласно рекомендации специалиста.
Обеспечение инвалидов техническими средствами осуществляется в соответствии с индивидуальными программами реабилитации инвалидов, разрабатываемыми федеральными государственными учреждениями медико-социальной экспертизы.
Путь пациента для льготного получения технических средств реабилитации
Необходимо:
1. Получить от лечащего врача выписной эпикриз или справку с рекомендацией о необходимости использования нужного технического средства реабилитации с указанием полного наименования (названия), размера, нужного количества в месяц.
2. Обратиться в поликлинику по месту жительства, чтобы пройти врачебную комиссию (ВК или КЭК) и получить направление на медикосоциальную экспертизу (МСЭ) по форме № 088/у. В п. 34 направления должна быть вписана полученная ранее рекомендация лечащего врача или специалиста по уходу за стомой.
3. Обратиться с направлением на МСЭ (форма 088/у) с рекомендацией в п. 34 в филиал учреждения государственной службы медико-социальной экспертизы (МСЭ) для:
а) оформления инвалидности;
б) разработки «Индивидуальной программы реабилитации» (ИПР).
4. С оформленной ИПР обратиться в отделение Фонда социального страхования (ФСС РФ) или в Центр социального обслуживания при Департаменте социальной защиты (в зависимости от условий региона). Предъявить ИПР и написать заявление о необходимости обеспечения нужными техническими средствам реабилитации (с указанием названия, размера, количества). Получить направление на бесплатное получение ТСР.
5. По направлению получить технические средства реабилитации в соответствии с региональными условиями.
НЕКОТОРЫЕ АСПЕКТЫ ПОМОЩИ СТОМИРОВАННЫМ ПАЦИЕНТАМ
Любая стома функционирует неуправляемо. Однако имеются некоторые мероприятия, позволяющие в определенной степени оказать влияние на работу стомы и сделать ее наиболее приемлемой. К их числу относится соблюдение диеты, применение некоторых лекарств, промывание (ирригация) кишки.
Регуляция стула с помощью диеты
Цель диеты заключается в выработке регулярного, самопроизвольного, по возможности менее частого стула. Если колостома наложена на левую половину толстой кишки, то обычно этой цели добиться нетрудно. При наличии илеостомы изменения частоты опорожнения кишечника добиться нельзя и поэтому необходимо стремиться к сгущению его содержимого.
С целью выработки правильного режима питания пациенту следует вести журнал, в который он записывает принимаемую им пищу, ее количество, когда и как часто происходило опорожнение кишки, качество стула, наличие газов, возможные боли после приема пищи, количество мочи. Обычно достаточно следить за приемом пищи на протяжении примерно 1-го месяца.
Ирригация — опорожнение кишечника с помощью промывания
n Ирригация используется при сигмостоме, десцендостоме.
n Противопоказания: дивертикулез, воспалительные заболевания.
n Необходимо использовать специальные наборы.
n После промывания пациент остается без стула на протяжении 24–48 ч.
n Пациент должен освоить ирригацию под руководством врача или медицинской сестры.
Проводить процедуру следует с предельной осторожностью, так как при введении наконечника в колостому он может перфорировать кишечную стенку.
Абсолютные противопоказания к применению ирригации: стриктура сигмостомы, парастомальная грыжа, грыжи передней брюшной стенки, дивертикулез ободочной кишки, воспалительные заболевания толстой
кишки. Относительные медицинские противопоказания: диарея, нарушения зрения, моторики кисти, препятствующие безопасному проведению ирригации.
Если больному наложена двухствольная колостома или проведена операция по типу Гартмана, то ежедневно необходимо промывать также и отключенные отделы, в которых накапливается сгущенная слизь и эпителий слизистой оболочки.
Критерии оценки качества помощи в стационаре представлены в таблице 22.5. Для оценки качества медицинской помощи используют временные, процессуальные и профилактирующие критерии. Временные характеризуют своевременность оказания определенных этапов медицинской помощи. Выполнение пациенту ряда медицинских манипуляций, инструментальных и лабораторных исследований, необходимых для качественного оказания медицинской помощи, оценивают в процессуальных критериях. Для анализа мероприятий, направленных на предотвращение развития осложнений, используют профилактирующие критерии.
Таблица 22.5. Критерии оценки качества медицинской помощи в стационаре больным с кишечными стомами (0 — нет, 1 — да)
|
Клинические рекомендации |
Временные |
Процессуальные |
Профилактирующие |
|
1. Клинические |
Установка |
Предоперацион- |
Пальцевое обследование стомы: |
|
рекомендации |
диагноза |
ная подготовка |
0/1. |
|
по ведению |
в течение |
и психологическая |
Оценка состояния перистомальной |
|
взрослых паци- |
72 ч: 0/1 |
помощь пациенту: |
кожи: 0/1. |
|
ентов с кишеч- |
|
0/1. |
Уход за пациентом с илеостомой, |
|
ной стомой (код |
|
Маркировка место- |
колостомой: 0/1. |
|
МКБ — Z93.2, |
|
положения стомы |
Подготовка к выписке из стацио- |
|
Z93.3, K 45, |
|
перед операцией: |
нара: 0/1. |
|
K 56.6, K 63.8, |
|
0/1. |
Обучение пациента со стомой: 0/1. |
|
K 91.4) |
|
Метод форми- |
Отсутствие осложнений: |
|
|
|
рования стомы |
• парастомальный абсцесс: 0/1; |
|
|
|
в соответствии |
• парастомальная флегмона: 0/1; |
|
|
|
с клиническими |
• некроз стомы: 0/1; |
|
|
|
рекомендациями: |
• ретракция стомы: 0/1; |
|
|
|
0/1 |
• выпадение стомы: 0/1 |
Литература
1. Программа ВОЗ «SINDI». — 2001. — 340 c.
2. Renzulli P., Candinas D. Intestinal stomas — indications, stoma types, surgical technique // Ther. Umsch. — 2007. — Vol. 64, N 9. — P. 517–527.
3. Суханов В.Г. Социальная реабилитация пациентов со стомой. — М.: Наука, 2006. — С. 12.
4. Лукьянова И.Е. Научное обоснование современной реабилитационной помощи лицам с ограничениями жизнедеятельности: Дис. … д-ра мед. наук. — М., 2009.
5. Pittman J., Kozell K., Gray M. Should WOC nurses measure health-related quality of life in patients undergoing intestinal ostomy surgery? // J. Wound Ostomy Continence Nurs. — 2009. — Vol. 36, N 3. — P. 254–265.
6. Breckman B. Stoma Care and Rehabilitation. — Edinburgh: Elsevier; Chruchill Livingstone, 2005. — P. 280–290.
7. Hong Kong Enterostomal Therapist Association. HKETA Standards in Stoma Care. ISBN 962-86486–2-4 Published by Hong Kong Enterostomal Therapists Association Limited. — 2004, Dec.
8. Olsen T., Alstad B., Thomsen L. et al. Postoperative Standards. Stoma Care. Skin Care. Nordic Stoma Cooperation. — Goteborg, 2001.
9. Registered Nurses’ Association of Ontario. Ostomy Care and Management. — Toronto (ON): Registered Nurses’ Association of Ontario, 2009, Aug. — 115 P. [101 references].
10. Wound, Ostomy, and Continence Nurses Society (WOCN). Management of the patient with a fecal ostomy: best practice guideline for clinicians. — Mount Laurel (NJ): Wound, Ostomy, and Continence Nurses Society, 2010, Jun 1. — 44
P. [95 references]
11. OCEBM Levels of Evidence Working Group. The Oxford 2011 Levels of Evidence. — Oxford Centre for Evidence-Based Medicine, 2011.
12. Воробьев Г.И., Царьков П.В. Основы хирургии кишечных стом. — М.: Стольный град, 2002.
13. Шелыгин Ю.А., Благодарный Л.А. Справочник по колопроктологии. — М.: Литтерра, 2012. — С. 538–596.
14. Воробьев Г.И., Царьков П.В., Суханов В.Г. и др. Вопросы организации службы реабилитации стомированных пациентов // Колопроктология. — 2005. — Т. 12, № 2. — С. 46–52.
15. Манихас Г.М. Амбулаторно-стационарная реабилитация больных с колостомой: Дис. … д-ра мед. наук. — М., 2006. — 215 с.
16. Stoia Davis J., Svavarsdóttir M.H., Pudlo M. et al. Factors impairing quality of life for people with an ostomy // Gastrointest. Nurs. — 2011. — Vol. 9, N 2. — P. 14–18.
17. Nichols T.R., Riemer M. The impact of stabilizing forces on postsurgical recovery in ostomy patients // J. Wound Ostomy Continence Nurs. — 2008. — Vol. 35, N 3. — P. 316–320.
18. Persson E., Gutavsson B., Hellstrom A.L. et al. Information to the relatives
of people with ostomies: Is it satisfactory and adequate? // J. Wound Ostomy Continence Nurs. — 2005. — Vol. 32, N 4. — P. 238–244.
19. Wu H.K.-M., Chau J.P.-C., Twinn S. Self-efficacy and quality of life among stoma patients in Hong Kong // Cancer Nurs. — 2007. — Vol. 30, N 3. — P. 186–193.
20. Chaudhri S., Brown L., Hassan I., Horgan A.F. Preoperative intensive, community-based vs. traditional stoma education: A randomized, controlled trial // Dis. Colon Rectum. — 2005. — Vol. 48, N 3. — P. 504–509.
21. Colwell J.C., Gray M. Does preoperative teaching and stoma site marking
affect surgical outcomes in patients undergoing ostomy surgery? // J. Wound Ostomy Continence Nurs. — 2007. — Vol. 34, N 5. — P. 492–496.
22. Marquis P., Marrel A., Jambon B. Quality of life in patients with stomas: The Montreux Study // Ostomy Wound Management. — 2003. — Vol. 49, N 2. — P. 48–55.
23. Haugen V., Bliss D.Z., Savik K. Perioperative factors that affect long-term adjustment to an incontinent ostomy // J. Wound Ostomy Continence Nurs. — 2006. — Vol. 33, N 5. — P. 525–535.
24. Colwell J.C., Gray M. Does preoperative teaching and stoma site marking affect surgical outcomes in patients undergoing ostomy surgery? // J. Wound Ostomy Continence Nurs. — 2007. — Vol. 34, N 5. — P. 492–496.
25. Pittman J., Rawl S.M., Schmidt C.M. et al. Demographic and clinical factors related to ostomy complications and quality of life in veterans with an ostomy // J. Wound Ostomy Continence Nurs. — 2008. — Vol. 35, N 5. — P. 493–503.
26. Mahjoubi B., Kiani Goodarzi K., Mohammad-Sadeghi H. Quality of life in stoma patients: appropriate and inappropriate stoma sites // World J. Surg. — 2010. — Vol. 34, N 1. — P. 147–152.
27. Bass E.M., Del P.A., Tan A. et al. Does preoperative stoma marking and education by the enterostomal therapist affect outcome? // Dis Colon Rectum. — 1997. — Vol. 40, N 4. — P. 440–442.
28. Park J.J., Del P.A., Orsay C.P. et al. Stoma complications: the Cook County Hospital experience // Dis Colon Rectum. — 1999. — Vol. 42, N 12. — P. 1575–1580.
29. Colwell J.C., Beitz J. Survey of Wound, Ostomy and Continence nurse clinicians on stomal and peristomal complications: A content validation study //
J. Wound Ostomy Continence Nurs. — 2007. — Vol. 34, N 1. — P. 57–69.
30. Cottam J., Richards K., Hasted A., Blackman A. Results of a nationwide prospective audit of stoma complications within 3 weeks of surgery // Colorectal Dis. — 2007. — Vol. 9, N 9. — P. 834–838.
31. Wound Ostomy and Continence Nurses Society. Colostomy and Ileostomy: Products and Tips. — Mt. Laurel (NJ): Wound Ostomy and Continence Nurses Society, 2008.
32. Richbourg L., Fellows J., Arroyave W.D. Ostomy pouch wear time in the United States // J. Wound Ostomy Continence Nurs. — 2008. — Vol. 35, N 5. — P. 504–508.
33. Cesaretti I.U., Santos V.L., Vianna L.A. Quality of life of the colostomized person with or without use of methods of bowel control // Rev. Bras. Enferm. — 2010. — Vol. 63, N 1. — P. 16–21.
34. Grant M., McMullen C.K., Altschuler A. et al. Irrigation practices in long-term survivors of colorectal cancer with colostomies // Clin. J. Oncol. Nurs. — 2012. — Vol. 16, N 5. — P. 514–519.
35. Addis G. The effect of home visits after discharge on patients who have had an ileostomy or a colostomy // World Council Enterostomal Therapists J. — 2003. — Vol. 23, N 1. — P. 26–33.
36. O’Connor G. Discharge planning in rehabilitation following surgery for a stoma // Br. J. Nurs. — 2003. — Vol. 12, N 13. — P. 800–807.
37. Richbourg L., Thorpe J.M., Rapp C.G. Difficulties experienced by the ostomate after hospital discharge // J. Wound Ostomy Continence Nurs. — 2007. — Vol. 34, N 1. — P. 70–79.
38. Chaudhri S., Brown L., Hassan I., Horgan A.F. Preoperative intensive, community-based vs. traditional stoma education: A randomized, controlled trial // Dis. Colon Rectum. — 2005. — Vol. 48, N 3. — P. 504–509.
39. Colwell J.C., Gray M. Does preoperative teaching and stoma site marking affect surgical outcomes in patients undergoing ostomy surgery? // J. Wound Ostomy Continence Nurs. — 2007. — Vol. 34, N 5. — P. 492–496.
40. Lo S.F., Wang Y.T., Wu L.Y. et al. Multimedia education programme for patients with a stoma: effectiveness evaluation // J. Adv. Nurs. — 2011. — Vol. 67, N 1. — P. 68–76.
41. O’Connor G. Discharge planning in rehabilitation following surgery for a stoma // Br. J. Nurs. — 2003. — Vol. 12, N 13. — P. 800–807.
42. Калашникова И.А., Ачкасов С.И. Алгоритм диагностики и лечения осложнений кишечной стомы // Колопроктология. — 2009. — Т. 29, № 3. — С. 8–14.
43. Beitz J., Gerlach M., Ginsburg P. et al. Content validation of a standardized algorithm for ostomy care // Ostomy Wound Manage. — 2010. — Vol. 56. — P. 22–38.
44. Salvadalena G. Incidence of complications of the stoma and peristomal skin among individuals with colostomy, ileostomy, and urostomy: a systematic review //
J. Wound Ostomy Continence Nurs. — 2008. — Vol. 35, N 6. — P. 596–607.
45. Kalashnikova I., Achkasov S., Fadeeva S., Vorobiev G. The development and use of algorithms for diagnosing and choosing treatment of ostomy complications: results of a prospective evaluation // Ostomy Wound Manage. — 2011. — Vol. 57, N 1. — P. 20–27.
46. Стойко Ю.М., Манихас Г.М., Ханевич М.Д., Коновалов С.В. Профилактика и лечение осложнений колостом. — СПб.: Аграф +, 2008. — С. 16–17, 40.
47. Vujnovich A. The management of stoma-related skin complications // Wounds UK. — 2006. — Vol. 2, N 3. — P. 36–47.
48. Butler D.L. Early postoperative complications following ostomy surgery: a review // J. Wound Ostomy Continence Nurs. — 2009. — Vol. 36, N 5. — P. 513– 519.
49. Husain S.G., Cataldo T.E. Late stomal complications // Clin. Colon Rectal Surg. — 2008. — Vol. 21, N 1. — P. 21–40.
50. Caricato M., Ausania F., Ripetti V. et al. Retrospective analysis of long-term defunctioning stoma complications after colorectal surgery // Colorectal Dis. — 2007. — Vol. 9, N 6. — P. 559–561.
51. Burch J., Sica J. Common peristomal skin problems and potential treatment options // Br. J. Nurs. — 2008. — Vol. 17, N 17. — P. 4–11.
52. Deitz D., Gate J. Basic ostomy management // Wound Skin Care. — 2010. — Vol. 20, N 2. — P. 61–62.
53. Herlufsen P., Olsen A.G., Carlsen B. et al. Study of peristomal skin disorders in patients with permanent stomas // Br. J. Nurs. — 2006. — Vol. 15, N 16. — P. 854–862.
54. Erwin-Toth P., Stricker L.J., van Rijswijk L. Peristomal skin complications // Am. J. Nurs. — 2010. — Vol. 110, N 2. — P. 43–48.
55. Jemec G.B., Martins L., Claessens I. et al. Ostomy Skin Tool Validation study: Assessing peristomal skin changes in ostomy patients: validation of the Ostomy Skin Tool // Br. J. Dermatol. — 2011. — Vol. 164. — P. 330–335.
56. Meisner S., Lehur P-A., Moran B. et al. Peristomal skin complications are common, expensive, and difficult to manage: A population based cost modelling study // PloS One. — 2012. — Vol. 7, N 5. — P. 1–8.
57. Uchino M., Ikeuchi H., Matsuoka H. et al. Clinical features and management of parastomal pyoderma gangrenosum in inflammatory bowel disease // Digestion. — 2012. — Vol. 85, N 4. — P. 295–301. doi: 10.1159/000336719. Epub 2012, May 12.
58. Funayama Y., Kumagai E., Takahashi K. et al. Early diagnosis and early corticosteroid administration improves healing of peristomal pyoderma gangrenosum in inflammatory bowel disease // Dis. Colon Rectum. — 2009. — Vol. 52. — P. 311–314.
59. Hanley J. Effective management of peristomal pyoderma gangrenosum // Br. J. Nurs. — 2011. — Vol. 20, N 7. — P. 12–14.
60. Калашникова И.А., Ачкасов С.И. Алгоритм индивидуального подбора технических средств реабилитации у больных с кишечной стомой // Менеджмент качества в сфере здравоохранения и социального развития. — 2007. —
№ 2. — С. 56–57.
ОСТРАЯ КИШЕЧНАЯ НЕПРОХОДИМОСТЬ ОПУХОЛЕВОЙ ЭТИОЛОГИИ
В данных клинических рекомендациях все сведения ранжированы по уровню достоверности (доказательности) в зависимости от количества и качества исследований по данной проблеме (табл. 23.1).
Таблица 23.1. Уровни доказательности и степени рекомендаций на основании руководства Оксфордского центра доказательной медицины [43]
|
Уровень |
Исследование методов диагностики |
Исследование методов лечения |
|
1а |
Систематический обзор гомогенных диагностических исследований 1-го уровня |
Систематический обзор гомогенных РКИ |
|
1b |
Валидизирующее когортное исследование с качественным «золотым стандартом» |
Отдельное РКИ (с узким доверительным интервалом) |
|
1с |
Специфичность или чувствительность столь высокие, что положительный или отрицательный результат позволяет исключить/установить диагноз |
Исследование «Всё или ничего» |
|
2а |
Систематический обзор гомогенных диагностических исследований >2-го уровня |
Систематический обзор (гомогенных) когортных исследований |
|
2b |
Разведочное когортное исследование с качественным «золотым стандартом» |
Отдельное когортное исследование (включая РКИ низкого качества; т.е. с <80% пациентов, прошедших контрольное наблюдение) |
|
2с |
Нет |
Исследование «исходов»; экологические исследования |
|
3а |
Систематический обзор гомогенных исследований уровня 3b и выше |
Систематический обзор гомогенных исследований «случай– контроль» |
|
3b |
Исследование с непоследовательным набором или без проведения исследования «золотого стандарта» у всех испытуемых |
Отдельное исследование «случай–контроль» |
Табл. 22.4. Окончание
|
Уровень |
Исследование методов диагностики |
Исследование методов лечения |
|
4 |
Исследование «случай–контроль» или исследование с некачественным или зависимым «золотым стандартом» |
Серия случаев (и когортные исследования или исследования «случай–контроль» низкого качества) |
|
5 |
Мнение экспертов без тщательной критической оценки или основанное на физиологии, лабораторные исследования на животных или разработка «первых принципов» |
Мнение экспертов без тщательной критической оценки, лабораторные исследования на животных или разработка «первых принципов» |
|
Степени рекомендаций | ||
|
A |
Согласующиеся между собой исследования 1-го уровня | |
|
B |
Согласующиеся между собой исследования 2-го или 3-го уровня или экстраполяция на основе исследований 1-го уровня | |
|
C |
Исследования 4-го уровня или экстраполяция на основе уровня 2 или 3 | |
|
D |
Доказательства 4-го уровня или затруднительные для обобщения или некачественные исследования любого уровня | |
Настоящие рекомендации в предварительной версии были рецензированы независимыми экспертами, которых попросили прокомментировать прежде всего, насколько интерпретация доказательств, лежащих в основе рекомендаций, доступна для понимания. Получены комментарии со стороны врачей амбулаторного звена. Данные комментарии тщательно систематизировались и обсуждались на совещаниях экспертной группы. 23 октября 2014 г. в рамках Всероссийской научно-практической конференции «Актуальные вопросы колопроктологии» (г. Смоленск) на заседании профильной комиссии «Колопроктология» Экспертного совета Минздрава России с участием представителей ассоциации колопроктологов России, ассоциации онкологов России, Российского общества хирургов были обсуждены наиболее спорные вопросы лечения больных острой кишечной непроходимостью, внесены последние изменения в настоящих рекомендациях. Для окончательной редакции и контроля качества рекомендации были повторно проанализированы членами экспертной группы, которые пришли к заключению, что все замечания и комментарии приняты во внимание, риск систематических ошибок при разработке рекомендаций сведен к минимуму.
Определение
Кишечная непроходимость опухолевого генеза — синдром, характеризующийся нарушением продвижения содержимого по пищеварительному тракту и обусловленный механическим препятствием, которым является злокачественное или доброкачественное новообразование кишечника.
Кишечная непроходимость опухолевой этиологии относится к обтурационной непроходимости и в преобладающем числе случаев является толстокишечной. К развитию данного синдрома прежде всего могут приводить злокачественные опухоли слепой кишки, ободочной кишки и злокачественные новообразования прямой кишки. Значительно реже кишечная непроходимость опухолевой природы бывает вызвана злокачественными новообразованиями тонкой кишки и доброкачественными опухолями кишечника.
Обтурация может возникнуть также вследствие перекрытия просвета кишечной трубки первичной или сдавления рецидивной опухолью извне, исходящей из соседних органов и тканей.
Распространенность
В преобладающем большинстве случаев острая кишечная непроходимость является осложнением колоректального рака, которое возникает у 15–20% больных, может наблюдаться во всех возрастных группах, но чаще у пациентов старше 50 лет [10, 38, 41]. Хирургия острой кишечной непроходимости сопряжена с высоким уровнем летальности, достигающим 25%, частым развитием послеоперационных осложнений [32].
Этиология и патогенез
Основная причина развития кишечной непроходимости опухолевого генеза — это рак толстой кишки. Значительно реже к развитию этого синдрома приводят аденомы и неэпителиальные опухоли толстой кишки, а также новообразования тонкой кишки. Кроме этого, к кишечной непроходимости может привести канцероматоз висцеральной брюшины с поражением тонкой кишки, развитием деформации и обструкции ее просвета. Патогенез кишечной непроходимости опухолевой природы отличается стадийностью. Наиболее характерно стертое, медленно прогрессирующее начало в виде нарушения транзита в связи с неполной окклюзией просвета кишки. Острое начало может быть обусловлено полной обтурацией суженного участка опухолью или плотными каловыми массами. Нарушения моторной и секреторно-резорбтивной функции кишечника.
В раннюю стадию непроходимости перистальтика усиливается, при этом кишечник своими сокращениями как бы стремится преодолеть появившееся препятствие. На этом этапе перистальтические движения в приводящей петле укорачиваются по протяженности, но становятся чаще. В дальнейшем в результате гипертонуса симпатической нервной системы, перерастяжения кишечника, резкого угнетения тканевой перфузии возникает фаза значительного угнетении моторной функции, а в поздних стадиях непроходимости развивается полный паралич кишечника. Расстройства метаболизма кишечных клеток усугубляет нарастающая эндогенная интоксикация, которая, в свою очередь, увеличивает тканевую гипоксию.
Водно-электролитные нарушения связаны с потерей большого количества воды, электролитов и белков. Жидкость теряется со рвотными массами, депонируется в приводящем отделе кишечника, скапливается в отечной кишечной стенке, ее брыжейке, а также в свободной брюшной полости. Потери жидкости в течение суток могут достигать 4 л и более. Происходит нарушение электролитного баланса, прежде всего потеря калия. Наряду с жидкостью и электролитами теряется значительное количество белков (до 300 г/сут) за счет голодания, рвоты, пропотевания в просвет кишки и брюшную полость. Особенно значимы потери альбумина плазмы. Белковые потери усугубляются превалированием процессов катаболизма.
Указанные выше изменения гуморального статуса обусловливают принципы предоперационной комплексной терапии, которая должна включать переливание кристаллоидных, коллоидных растворов, препаратов белков.
Эндотоксикоз — важное звено патофизиологических процессов при кишечной непроходимости. В условиях циркуляторной гипоксии кишка утрачивает функцию биологического барьера, и значительная часть токсических продуктов поступает в общий кровоток, что способствует нарастанию интоксикации.
Затем нарушается нормальная микробиологическая экосистема за счет застоя содержимого, что способствует бурному росту и размножению микроорганизмов. Происходит миграция микрофлоры, характерной для дистальных отделов кишечника, в проксимальные, для которых она чужеродна. Выделение экзои эндотоксинов, нарушение барьерной функции кишечной стенки приводят к транслокации бактерий в портальный кровоток, лимфу и перитонеальный экссудат. Эти процессы лежат в основе системной воспалительной реакции и абдоминального хирургического сепсиса, характерных для острой кишечной непроходимости. Некроз кишки и гнойный перитонит — второй источник эндотоксикоза. Исходом данного процесса являются усугубление нарушений тканевого метаболизма и возникновение полиорганной недостаточности.
В патогенезе кишечной непроходимости значительная роль отво-
дится внутрибрюшной гипертензии — так называемому компартментсиндрому. Этот синдром представляет собой комплекс отрицательного эффекта стремительного повышения внутрибрюшного давления. При этом нарушается кровоснабжение внутренних органов, понижается жизнеспособность тканей, что приводит к развитию полиорганной недостаточности. Основными принципами лечения компартмент-синдрома являются ранняя хирургическая декомпрессия и рациональная инфузионная терапия.
Инфекционно-воспалительные осложнения, как следствие перфорации (микроперфорации) опухоли или приводящих отделов толстой кишки,
а также транслокации микроорганизмов в перитонеальный транссудат, приводят к формированию:
n инфильтрата брюшной полости;
n абсцесса брюшной полости;
n абсцесса брыжейки кишки;
n абсцесса или флегмоны забрюшинного пространства;
n местного неотграниченного или распространенного перитонита.
Классификация
По уровню непроходимости:
n высокая (характерна для локализации опухолей в правых отделах ободочной кишки);
n низкая (характерна для локализации новообразований в левых отделах ободочной кишки и в прямой кишке).
По степени нарушения пассажа кишечного содержимого:
n полная;
n частичная.
По степени компенсации:
n компенсированная кишечная непроходимость: периодически возникающий запор, сопровождающийся задержкой стула и затруднением отхождения газов; на обзорной рентгенограмме брюшной полости может выявляться пневматизация ободочной кишки с единичными уровнями жидкости в ней;
n субкомпенсированная кишечная непроходимость: задержка стула и газов менее 3 сут, на обзорной рентгенограмме определяются тонкокишечные арки, пневматоз и чаши Клойбера в правой половине живота; отсутствуют признаки полиогранных дисфункций; эффективна консервативная терапия;
n декомпенсированная кишечная непроходимость: задержка стула и газов более 3 сут; рентгенологические признаки как толсто-, так и тонкокишечной непроходимости с локализацией тонкокишечных уровней и арок во всех отделах брюшной полости; рвота застойным содержимым; наличие органных дисфункций [1].
Код по Международной классификации болезней 10-го пересмотра
n К56.6 Другая и неуточненная кишечная непроходимость
n С18 Злокачественное новообразование ободочной кишки
n С19 Злокачественное новообразование ректосигмоидного соединения
n С20 Злокачественное новообразование прямой кишки
Клиническая картина
Особенность кишечной непроходимости при опухолях толстой кишки — стертость клинической симптоматики на ранних этапах развития
заболевания, большая возможность для проведения консервативных мероприятий.
Клинические проявления острой кишечной непроходимости опухолевой природы разнообразны и зависят от многих факторов. Наиболее распространенными из них являются следующие.
n Боль в животе — постоянный и ранний признак непроходимости,
обычно возникает внезапно, вне зависимости от приема пищи, в любое время суток, без предвестников; характер боли схваткообразный. Приступы боли связаны с перистальтической волной и повторяются через 10–15 мин. В период декомпенсации, истощения энергетических запасов мускулатуры кишечника боль начинает носить постоянный характер. При острой обтурационной непроходимости боль сразу постоянная, с периодами усиления во время волны перистальтики. При прогрессировании заболевания острые боли, как правило, стихают на 2–3-и сутки, когда перистальтическая активность кишечника прекращается, что служит плохим прогностическим признаком (симптом Мондора) — усиленная перистальтика кишечника сменяется на постепенное угасание перистальтики («Шум вначале, тишина в конце»). При дальнейшем прогрессировании кишечной непроходимости может определяться симптом «мертвой (могильной) тишины» — отсутствие звуков перистальтики; зловещий признак непроходимости кишечника. В этот период при резком вздутии живота над ним можно выслушать не перистальтику, а дыхательные шумы и сердечные тоны, которые в норме через живот не проводятся.
n Вздутие и асимметрия живота. Определяются патогномоничные симп-
томы кишечной непроходимости, такие как симптом Валя — относительно устойчивое асимметричное вздутие живота, заметное на глаз, определяемое на ощупь; симптом Шланге — видимая перистальтика кишок, особенно после пальпации; симптом Склярова — выслушивание
«шума плеска» над петлями кишечника; симптом Спасокукоцкого– Вильмса — «шум падающей капли», выявляющийся при аускультации; симптом Кивуля — усиленный тимпанический звук с металлическим оттенком над растянутой петлей кишки.
n Задержка стула и газов — патогномоничный признак непроходимости кишечника. Это ранний симптом низкой непроходимости. При вы-
соком ее характере, в начале заболевания, особенно под влиянием лечебных мероприятий, может быть стул, иногда многократный за счет опорожнения кишечника, расположенного ниже препятствия.
n Рвота вначале носит рефлекторный характер, при продолжающейся
непроходимости рвотные массы представлены застойным желудочным содержимым. В позднем периоде она становится неукротимой, рвотные массы приобретают вид и запах кишечного содержимого. Чем выше уровень непроходимости, тем более выражена рвота.
n Патологические выделения из заднего прохода имеют кровянистый, слизистый или смешанный характер. Их наличие может быть обусловлено
слизеобразованием, распадом опухоли, травматизацией ее каловыми массами, а также воспалительными явлениями в проксимально расположенных отделах кишечника. Кроме того, могут быть определены
следующие специфические симптомы: Обуховской больницы — признак низкой толстокишечной непроходимости, проявляющийся баллонообразным вздутием пустой ампулы прямой кишки на фоне зияния ануса; симптом Цеге–Мантейфеля — признак низкой толстокишечной непроходимости: малая вместимость (не более 500 мл воды) дистального отдела кишечника при постановке клизмы.
Кроме перечисленных выше симптомов, нередко наблюдаются другие клинические проявления опухоли. Это гипертермия, тахикардия, общая слабость, головокружение, снижение работоспособности, потеря массы тела, анемия.
Диагностика
При поступлении в стационар больного с подозрением на кишечную непроходимость в первую очередь проводят его осмотр, при котором оценивается состояние его кожного покрова, лица, рассчитывается индекс массы тела.
n Термометрия, измерение пульса и артериального давления.
n Аускультация, перкуссия и пальпация живота.
n Пальцевое ректальное исследование, у женщин дополнительно проводят вагинальное исследование.
n Выведение содержимого из желудка зондом, предпочтительно толстым.
n Лабораторные исследования: общий анализ крови, общий анализ мочи, биохимический анализ крови, группа крови и Rh-фактор, определяется кислотно-основный состав крови.
n Инструментальные исследования.
n Обязательный диагностический минимум инструментальных исследований: ЭКГ, обзорная рентгенография брюшной полости. Причина кишечной непроходимости может быть установлена при выполнении ректороманоскопии, ирригоскопии или колоноскопии. Кроме этого, в качестве предоперационного обследования онкологических больных показано проведение рентгенографии грудной клетки, УЗИ органов брюшной полости, таза, забрюшинного пространства, при возможности КТ или МРТ брюшной полости и малого таза, гастродуоденоскопии.
n Осмотр женщин гинекологом.
n Осмотр терапевтом и анестезиологом.
Дифференциальная диагностика кишечной непроходимости проводится со следующими заболеваниями и синдромами.
n Перфорация полого органа.
n Острый аппендицит.
n Острый холецистит.
n Острый панкреатит.
n Острое нарушение мезентериального кровообращения.
n Асцит.
n Перитонит.
n Спонтанный бактериальный перитонит.
n Острый синдром приводящей петли (с резекцией желудка по Бильрот-2 в анамнезе).
n Почечная колика.
n Мегаколон.
Главная задача дифференциальной диагностики при наличии признаков острой кишечной непроходимости — выделение больных со странгуляционными формами механической непроходимости, а также выявление осложнений, требующих экстренного хирургического вмешательства (СР D [29]). При выявлении странгуляционной непроходимости показано неотложное хирургическое лечение. Исключение составляют пациенты с признаками полиорганных дисфункций, нестабильной гемодинамикой, дыхательными расстройствами (ASA 4–5). Данной группе пациентов показано проведение интенсивной предоперационной подготовки
в условиях палаты интенсивной терапии.
Предельный срок пребывания пациента в приемном покое не должен превышать 2 ч. В случаях когда в течение этого времени не удается исключить острую кишечную непроходимость и отсутствуют показания к экстренной операции, пациента госпитализируют в хирургический стационар, где лечебно-диагностические мероприятия должны быть продолжены (СР D [17]).
ДИАГНОСТИЧЕСКИЕ КРИТЕРИИ
Диагностические критерии кишечной непроходимости опухолевого генеза основываются прежде всего на оценке жалоб больного, клиническом осмотре, пальпации, перкуссии, аускультации, пальцевом исследовании прямой кишки и влагалища у женщин, эндоскопическом, рентгенологическом и ультразвуковом методах исследования.
Клинические проявления: наиболее характерные симптомы — схваткообразные боли в животе высокой интенсивности, вздутие живота, отсутствие отхождения стула и газов, тошнота, рвота.
Рентгенологический метод: основной специальный метод исследования при подозрении на кишечную непроходимость:
n обзорная полипозиционная рентгенография органов брюшной полости по-
зволяет поставить диагноз острой кишечной непроходимости, опираясь на следующие специфические признаки:
v определение газа и уровней жидкости в расширенных петлях кишок (чаши Клойбера);
v поперечная исчерченность кишки;
n ирригоскопия (может быть выполнена после УЗИ и эндоскопических исследований) позволяет выявить специфические рентгенологические признаки непроходимости опухолевой природы:
v дефект наполнения в толстой кишке;
v циркулярный дефект наполнения на уровне стенозирующей просвет кишки опухоли, проксимальнее которой поступление контрастного вещества не происходит;
n пассаж бариевой взвеси по ЖКТ при кишечной непроходимости опухолевой этиологии затягивает время принятия решения, может быть не-
эффективным методом исследования.
Для подтверждения диагноза острой кишечной непроходимости и уточнения локализации препятствия, исключения псевдообструкции необходимо выполнять рентгеноконтрастные исследования (ирригография) (УД 3, СР B [11, 26, 43]).
Применение ирригографии имеет ограничения, связанные с невозможностью выполнения исследования у лежачих больных и у пациентов с нарушенной функцией держания анального сфинктера. Кроме того, это исследование не позволяет оценить состояние приводящего отдела кишки, степень первичного опухолевого поражения и наличие отдаленных метастазов. Оно сопряжено с риском диастатической перфорации супрастенотического отдела толстой кишки при декомпенсированной кишечной непроходимости.
КТ способна подтвердить диагноз острой кишечной непроходимости более чем в 90% случаев, позволяет определить точную локализацию и распространенность опухоли, выявить отдаленные метастазы.
КТ предоставляет дополнительную информацию о локализации и распространенности первичной опухоли, наличии отдаленных метастазов, позволяет отказаться от выполнения ирригоскопии. КТ должна применяться во всех случаях, когда есть такая возможность (УД 3, СР D [19, 30]).
Эндоскопический метод: ректороманоскопия, колоноскопия позволяют верифицировать диагноз новообразования прямой или ободочной кишки, определить уровень поражения, выраженность стеноза просвета кишки на уровне опухоли.
Колоноскопия может быть использована для выявления уровня обструкции и верификации диагноза путем выполнения биопсии опухоли. В некоторых случаях во время колоноскопии удается провести зонд через стенозирующую опухоль с целью декомпрессии проксимальных отделов кишки.
Колоноскопия позволяет определить причину кишечной непроходимости, дает возможность выполнения лечебных мероприятий, направленных на разрешение острой кишечной непроходимости (УД 3 [22]).
Противопоказанием к проведению колоноскопии является декомпенсированная кишечная непроходимость, сопровождаемая диастатической перфорацией кишки или высоким риском ее развития, перитонитом, крайне тяжелым общим состоянием больного.
Ультразвуковой метод диагностики — патогномоничные признаки:
n расширение просвета тонкой кишки более 2 см с наличием феномена
«секвестрации жидкости» в просвете кишки;
n утолщение стенки тонкой кишки более 4 мм;
n наличие возвратно-поступательных движений химуса по кишке;
n увеличение высоты керкринговых складок более 5 мм, увеличение расстояния между ними более 5 мм;
n гиперпневматизация кишечника в приводящем отделе;
n наличие свободной жидкости в брюшной полости.
УЗИ может иметь значение в диагностике кишечной непроходимости в связи со своей простотой выполнения, доступностью, неинвазивностью и отсутствием лучевой нагрузки, однако избыточное количество газа в петлях кишечника зачастую делают это исследование малоинформативным (СР D).
Лечение
Всех больных с подозрением на кишечную непроходимость необходимо срочно госпитализировать в хирургический стационар. Сроки поступления таких пациентов могут определять исход заболевания. Чем позже начинается лечение, тем выше уровень летальности.
КОНСЕРВАТИВНЫЕ МЕРОПРИЯТИЯ
При сомнении в диагнозе острой механической кишечной непроходимости, отсутствии перитонеальной симптоматики проводят консервативные лечебно-диагностические мероприятия по подтверждению или исключению острой кишечной непроходимости, определяют ее природу и уровень.
Проводится коррекция водно-электролитных нарушений, эндогенной интоксикации, при инфекционно-септических осложнениях начинается антибактериальная терапия.
Если кишечная непроходимость не разрешается, проведенное консервативное лечение становится предоперационной подготовкой.
Элементы консервативного лечения:
n обеспечение декомпрессии проксимальных отделов ЖКТ путем аспирации содержимого через назогастральный или назоинтестинальный зонд;
n очистительные и сифонные клизмы. Постановка клизм в ряде случаев позволяет добиться опорожнения отделов толстой кишки, расположенных выше препятствия. Постановка сифонных клизм при острой кишечной непроходимости является исключительно врачебной процедурой;
n инфузия кристаллоидных растворов с целью коррекции водно-электролитных нарушений, ликвидации гиповолемии. Объем инфузионной терапии следует проводить под контролем центрального венозного давления, что требует постановки центрального венозного катетера;
n коррекция белкового баланса путем переливания белковых препаратов;
n при компенсированной форме кишечной непроходимости лечение целесообразно дополнить назначением сбалансированных питательных смесей. Положительным клиническим эффектом от консервативной терапии и подтверждением правомерности продолжения консервативных мероприятий следует считать достижение совокупности следующих
критериев:
n общая положительная динамика при отсутствии перитонеальной симптоматики;
n прекращение рвоты и отделения застойного содержимого по назогастральному зонду;
n восстановление ритмичной непатологической перистальтики кишечника при аускультации живота;
n уменьшение вздутия живота;
n восстановление отхождения газов;
n купирование болевого синдрома;
n восстановление естественного опорожнения кишечника.
По данным рентгенологических методов исследования:
n уменьшение диаметра участка кишки, расположенного проксимальнее опухоли;
n исчезновение поперечной исчерченности стенки супрастенотического участка кишки;
n уменьшение количества и исчезновение «арок» и уровней жидкости (чаш Клойбера);
n продвижение контраста через опухолевый канал и в дистальные отделы кишки.
Декомпенсированная форма острой кишечной непроходимости подлежит оперативному лечению после короткой предоперационной подготовки. Характер и объем инфузионной терапии определяются совместно с анестезиологом-реаниматологом.
Консервативная терапия при субкомпенсированной форме острой кишечной непроходимости считается эффективной при достижении положительной динамики в течение первых 6–12 ч лечения. При явной положительной динамике, отсутствии перитонеальной симптоматики консервативное лечение может быть продолжено.
Компенсированная форма острой кишечной непроходимости подлежит оперативному лечению в плановом порядке.
В случае установления опухолевой этиологии кишечной непроходимости отсроченное оперативное вмешательство выполняется на фоне указанной консервативной терапии в течение не более 10 сут от установленного диагноза без выписки на амбулаторное лечение во избежание рецидива непроходимости либо после перевода в специализированное онкологическое или колопроктологическое отделение.
Стентирование опухоли
В настоящее время все большее распространение получают саморасширяющиеся сетчатые системы (так называемые стенты — self-expanding metallic stents — SEMS), вводимые в просвет кишки на уровень опухоли с помощью эндоскопа. После установки стента он расширяется, раздвигая ткань опухоли, и восстанавливает свободный просвет кишечника. Основные осложнения данного метода: перфорация кишки, возникающая в 3,0–6,7% случаев; миграция стента — в 10–11% наблюдений; рецидив непроходимости — у 7–10% пациентов (УД 3 [25, 37]).
Разрешение кишечной непроходимости позволяет избежать выполнения экстренного или срочного оперативного вмешательства, что дает возможность использовать дополнительные лечебно-диагностические
мероприятия для подготовки больного к плановому оперативному лечению. В некоторых случаях ликвидация острой кишечной непроходимости позволяет выполнить операцию с формированием первичного анастомоза, без наложения превентивной кишечной стомы (УД 3 [12]).
При отсутствии признаков перфорации, перитонита, кровотечения, полной окклюзии просвета кишки опухолью может быть рекомендована установка саморасширяющихся металлических стентов (СР В [17]).
При наличии множественных метастазов или поражения более 25% объема печени в сочетании с тяжелым общим состоянием больного, тяжелой анемией риск от проведения хирургического вмешательства может оказаться выше, чем возможный положительный эффект. В таких случаях систематический анализ эффективности использования колоректальных стентов позволяет предположить, что они являются относительно безопасным и действенным симптоматическим средством. Стентирование значительно снижает риск развития кишечной непроходимости в процессе роста опухоли и тем самым избавляет больного от наложения стомы (УД 3, 4 [25, 26, 31]).
ХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕ
При отсутствии положительного эффекта от пробного консервативного лечения, нарастании или сохранении симптомов кишечной непроходимости показано хирургическое лечение по срочным показаниям. В случае купирования симптомов кишечной непроходимости опухолевого генеза в результате проведения консервативных мероприятий или стентирования возможно выполнение отсроченных хирургических вмешательств, объем которых соответствует плановым операциям.
Предоперационная подготовка
Пациент с кишечной непроходимостью должен быть тщательно подготовлен к операции. Лечебные мероприятия направлены на ликвидацию водно-электролитных и белковых расстройств, купирование явлений эндотоксикоза, декомпрессию кишечника. Обязательно получение информированного согласия пациента на выполнение операции, маркировка места выведения стомы. Должна быть проведена антибиотикопрофилактика и профилактика тромбоэмболических осложнений.
Информированное согласие
В соответствии с Законом Российской Федерации от 21 ноября 2011 г.
№ 323-ФЗ «Об основах охраны здоровья граждан в Российской Федерации» получение добровольного информированного согласия — обязательная и необходимая процедура, которая отражает соблюдение юридических и этических прав человека принимать самостоятельное решение, касающееся его здоровья. Условиями возможности получения информированного согласия являются способность больного принимать обдуманные решения относительно лечебных мероприятий, доступное
предоставление всей необходимой для принятия решения информации. Основные вопросы: польза и риск предлагаемого лечения, предполагаемый объем лечебных мероприятий, последствия отказа от лечения.
Все пациенты, которым планируется провести хирургическую манипуляцию по поводу колоректального рака, должны дать информированное согласие. Оно подразумевает под собой то, что больному представлена информация о возможной пользе и гипотетических рисках лечения, а также о наличии каких-либо альтернативных методов лечения. По возможности информированное согласие должно быть получено непосредственно оперирующим хирургом (СР В).
Профилактика тромбоэмболических осложнений
Пациенты, которым выполняется оперативное вмешательство по поводу колоректального рака, относятся к группе высокого риска возникновения тромбоэмболических осложнений. При наличии кишечной непроходимости риск подобных осложнений расценивается как крайне высокий. Применение низкомолекулярных гепаринов может существенно снизить вероятность возникновения тромбоза глубоких вен нижних конечностей и тромбоэмболию легочной артерии. Использование обычных гепаринов не отличается по эффективности, однако сопряжено с большим числом геморрагических осложнений и развитием гепарин-индуцированной тромбоцитопении. Дополнительно используются компрессионные чулки, а также приборы прерывистой пневматической компрессии. В то же время раннее прекращение постельного режима является одним из условий успешной профилактики венозного тромбоза и практикуется во всех случаях, когда это возможно. У больных, перенесших обширные оперативные вмешательства по поводу онкологических операций, целесообразно проводить профилактические мероприятия, сочетающиеся с введением низкомолекулярных гепаринов как минимум в течение 4 нед (УД 1b [36, 14, 24]).
Пациентам, которым проведена операция по поводу колоректального рака, с целью профилактики тромбоэмболических осложнений следует назначать инъекции препаратов гепарина и использование компрессионных чулок (СР А [3]).
Антибиотикопрофилактика
Назначение антибактериальных препаратов может уменьшать частоту развития инфекционных осложнений, укорачивать сроки пребывания больного в стационаре, снижать затраты на лечение осложнений после хирургических операций. Приемлемым считается профилактическое интраоперационное внутривенное введение цефалоспоринов или фторхинолонов в сочетании с метронидазолом. Эффективность профилактики нагноения послеоперационной раны при однократном внутривенном введении цефалоспоринов в сочетании с метронидазолом не уступает таковой при троекратном их применении после операции (УД 1b [28]).
Все пациенты, оперированные по поводу колоректального рака, должны получать профилактическую антибактериальную терапию. В настоящее время нельзя сказать, какая схема наиболее оптимальная, однако достаточно эффективным считается однократное введение антибактериального препарата широкого спектра действия непосредственно перед операцией, а при длительности хирургического вмешательства более 3 ч — его повторное введение (СР А [15]).
Подготовка кишечника
Необходимость подготовки кишечника к оперативному вмешательству зависит от степени нарушения пассажа кишечного содержимого, уровня кишечной непроходимости, клинического течения (острое или хроническое).
При нарушении кишечной проходимости за счет частичного нарушения пассажа назначается бесшлаковая диета в сочетании с приемом вазелинового масла, 15% раствора сернокислой агнезии и механической очисткой толстой кишки.
При острой декомпенсированной кишечной непроходимости не рекомендуется применение слабительных препаратов, стимуляция перистальтики кишечника, постановка очистительных клизм (СР A [20]).
Подготовка к формированию стомы
Если пациенту предполагается формирование стомы, то ход самой процедуры и ее последствия должны быть тщательно разъяснены. Необходимо выполнить маркировку области, где предполагается сформировать стому. Наиболее оптимальным является направление больного перед выполнением операции на консультацию специалиста по реабилитации стомированных больных. В экстренных ситуациях не всегда возможно соблюдение указанных выше рекомендаций, в таких случаях разметка области предполагаемого выведения стомы должна проводиться оперирующим хирургом. Разметка производится в положении больного стоя, лежа и сидя с учетом его индивидуальных и конституциональных особенностей. Всем больным, у которых не исключена вероятность формирования стомы, перед операцией выполняется маркировка области предполагае-
мой стомы (СР С [2]).
ЭКСТРЕННОЕ/СРОЧНОЕ ХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕ
При развитии острой кишечной непроходимости опухолевого генеза, нарастании симптоматики и отсутствии эффекта от консервативных мероприятий, предпринимаемых в течение первых 12 ч лечения, первоочередной задачей хирургического лечения является ликвидация кишечной непроходимости и сохранение жизни пациенту.
Неотложные операции должны проводиться по мере возможности в дневное время хирургами и анестезиологами, имеющими опыт в лечении колоректального рака (СР D [17]).
При наличии распространенного перитонита, тяжелого абдоминального сепсиса хирургическое лечение должно соответствовать стандартам лечения перитонита и сепсиса (УД 3 [7]).
ОСНОВНЫЕ ПРАВИЛА ФОРМИРОВАНИЯ КИШЕЧНЫХ СТОМ
Место формирования будущей стомы должно быть выбрано до операции с учетом телосложения больного, толщины брюшной стенки, естественных складок живота, при осмотре больного лежа на спине, сидя и стоя. Колостому (илеостому) следует размещать на наиболее плоском участке передней брюшной стенки, сохраняющем свою форму при разных положениях больного. Выбранное место должно быть удобным для последующего ухода и использования калоприемника. Вблизи стомы не должно быть костных выступов, жировых складок, рубцов и грубых деформаций.
Существует два варианта выведения стомы.
1. Вблизи опухоли — при формировании временной стомы и предполагаемом удалении новообразования толстой кишки вторым этапом, когда стома войдет в зону резекции кишки с опухолью.
2. Вдали от опухоли, когда стома является постоянной, или второй этап хирургического лечения подразумевает сохранение имеющейся стомы в качестве превентивной. Мобилизация участка кишки должна производиться:
n на протяжении, достаточном для предотвращения возможного натяжения брыжейки в условиях послеоперационного пареза кишечника, поворотов больного на бок, при кашле и т.п.;
n с сохранением хорошего кровоснабжения выводимого участка кишки.
Диаметр отверстия в брюшной стенке должен соответствовать нормальному диаметру соответствующего отдела кишечника. При несоблюдении этого условия возможны осложнения в послеоперационном периоде в виде некроза, ретракции и последующих стриктур стом, эвагинаций кишки через стому, парастомальных грыж.
Выведенная петля толстой кишки при колостомии должна быть не ниже уровня кожного покрова. Наименьшее расстояние от места предполагаемой илеостомы до слепой кишки 15–20 см. Необходимое условие выбора петли — возможность подтянуть ее выше уровня кожи на 3–4 см. Целесообразна установка поддерживающих палочек под петлевую стому для профилактики ее ретракции. Этап формирования кишечной стомы завершается фиксацией серозно-мышечного слоя кишки к коже, для чего используется атравматическая игла с рассасывающейся нитью. Не рекомендуется фиксация брюшины к коже, а также прикрепление к швам марлевых шариков или турунд, введение в просвет кишки зондов [2]. После фиксации кишки к коже передней брюшной стенки и ушивания послеоперационных ран производится вскрытие просвета кишки и окончательное формирование стомы.
Формирование пристеночных колостом, в том числе цекостом, нецелесообразно, так как не происходит полного отключения пассажа кишечного содержимого и полноценного купирования осложнений опухолевого процесса.
ОСНОВНЫЕ ПРИНЦИПЫ ВЫПОЛНЕНИЯ ОПЕРАТИВНЫХ ВМЕШАТЕЛЬСТВ ПРИ КИШЕЧНОЙ НЕПРОХОДИМОСТИ ОПУХОЛЕВОГО ГЕНЕЗА
Эффективность консервативного лечения и предоперационной подготовки больных с кишечной непроходимостью опухолевого генеза служит фактором, в значительной степени определяющим хирургическую тактику.
При неэффективности консервативных мероприятий, нарастании явлений кишечной непроходимости объем хирургического вмешательства может быть минимизирован до дренирующей операции. Формирование проксимальной разгрузочной илеоили колостомы показано при отсутствии таких осложнений со стороны первичной опухоли, как перфорация, абсцедирование, кровотечение, а также диастатических разрывов и перфорации отделов ободочной кишки, расположенных проксимальнее злокачественного новообразования. Наличие таких осложнений диктует крайнюю необходимость выполнения первичной резекции без формирования анастомоза. После стабилизации состояния больного в условиях специализированного стационара показано выполнение резекции толстой кишки с соблюдением онкологических принципов. При этом возможно сохранение ранее наложенной стомы в качестве превентивной для протекции сформированного межкишечного анастомоза.
Отсутствие эффекта от предоперационного консервативного лечения у больных с кишечной непроходимостью и другими жизненно опасными осложнениями со стороны опухоли, такими как перфорация, абсцедирование, кровотечение, диастатические разрывы и перфорация проксимально расположенных отделов, является показанием к резекции толстой кишки. При расположении новообразований в правых отделах ободочной кишки выполняется операция по типу Лахея, при левосторонней локализации — резекция толстой кишки по типу операции Гартмана. При наличии ишемических и некротических изменений кишечной стенки, перфорации проксимально расположенных отделов ободочной кишки должна производиться ее резекция в пределах неизмененных тканей.
При эффективности консервативного лечения, стабилизации состояния пациента и наличии благоприятных условий (резектабельность, отсутствие диссеминированных форм канцероматоза, перитонита, переносимость операции, наличие хирурга соответствующей квалификации) следует стремиться к удалению первичной опухоли независимо от стадии заболевания.
Принципы абластичности:
n одномоментное удаление лимфатических коллекторов резецированных отделов толстой кишки путем высокой перевязки соответствующих сосудов;
n расширенная лимфаденэктомия с удалением парааортальных лимфатических узлов при их метастатическом поражении;
n при местном распространении опухоли на прилежащие органы и ткани — их резекция или удаление.
Метастазы в печень и легкие не являются противопоказанием к удалению первичной опухоли. Однако наличие кишечной непроходимости служит абсолютным противопоказанием к одномоментным резекциям печени или легких. Вторым этапом лечение этих пациентов должно быть продолжено в специализированных хирургических стационарах.
Предпочтительным способом завершения резекции толстой кишки, предпринимаемой по поводу опухолевой непроходимости, является формирование одноствольной колоили илеостомы. Одномоментное восстановление кишечной трубки допустимо лишь при формировании тонко-толстокишечного анастомоза в условиях специализированного стационара при наличии хирурга соответствующей квалификации и особо благоприятной клинической ситуации, когда кишечная непроходимость расценивается как компенсированная.
Завершить операцию целесообразно дренированием брюшной полости. Наиболее частый вариант дренирования брюшной полости после резекции толстой кишки по поводу острой кишечной непроходимости — малый таз, правое подпеченочное пространство, левый латеральный канал.
При радикальных операциях для гистологического исследования в обязательном порядке отправляется весь препарат, удаленный во время хирургического вмешательства.
При паллиативных резекциях необходима биопсия остающихся метастазов из доступных очагов с учетом риска осложнений (кровотечение, травма органа и сосудов), для верификации очаговых изменений и стадирования заболевания.
ТИПОВЫЕ ОБЪЕМЫ ОПЕРАТИВНЫХ ВМЕШАТЕЛЬСТВ
ПРИ ТОЛСТОКИШЕЧНОЙ НЕПРОХОДИМОСТИ ОПУХОЛЕВОЙ ЭТИОЛОГИИ
Толстокишечная непроходимость без инфекционно-воспалительных осложнений
Опухоли правых отделов ободочной кишки (слепая, восходящая ободочная кишка, правый изгиб, проксимальная часть поперечной ободочной кишки):
n петлевая илеостомия лапароскопическим, или минилапаротомным,
или открытым доступом;
n правосторонняя гемиколэктомия по Лахею;
n при отсутствии декомпенсированной кишечной непроходимости возможно выполнение правосторонней гемиколэктомии с формированием илеорансверзоанастомоза;
n при наличии отдаленных метастазов и/или тяжелом состоянии пациента — формирование проксимальной кишечной стомы.
Опухоль средней трети поперечной ободочной кишки:
n петлевая илеостомия лапароскопическим, или минилапаротомным, или открытым доступом;
n расширенная правосторонняя гемиколэктомия по Лахею;
n резекция поперечной ободочной кишки по типу операции Гартмана;
n субтотальная резекция ободочной кишки (по типу операции Гартмана или с формированием илеосигмоидного анастомоза);
n при наличии отдаленных метастазов и/или тяжелом состоянии пациента — формирование проксимальной кишечной стомы.
Опухоли левых отделов ободочной кишки (дистальная часть поперечной ободочной кишки, левый изгиб, нисходящая ободочная кишка, сигмовидная кишка):
n петлевая колостомия (сигмостомия, трансвезостомия в зависимо-
сти от локализации опухоли) предпочтительно лапароскопическая или из минилапаротомного доступа;
n левосторонняя гемиколэктомия по типу операции Гартмана;
n резекция левых отделов ободочной кишки по типу операции Гартмана;
n резекция сигмовидной кишки по типу операции Гартмана;
n при наличии неудалимых отдаленных метастазов в качестве окончательной операции, наряду со стентированием, может выполняться петлевая колостомия (УД 1b [18]).
Субтотальная резекция ободочной кишки может быть рекомендована:
n в общей сети стационаров — в исключительных случаях при выраженных ишемических изменениях отделов ободочной кишки, расположенных проксимальнее опухоли, а также в случае диастатической перфорации супрастенотически расширенных отделов толстой кишки;
n в условиях специализированного стационара при соответствующем анестезиологическом обеспечении, наличии квалифицированных хирургов и отсутствии технических трудностей — для сокращения этапов хирургического лечения, а также при синхронных опухолях ободочной кишки (СР D).
В условиях острой декомпенсированной кишечной непроходимости от формирования анастомоза следует отказаться.
Тактика лечения осложненного рака прямой кишки зависит, прежде всего, от характеристики опухоли, состояния больного, уровня лечебного учреждения и квалификации оперирующего хирурга.
В случае кишечной непроходимости, обусловленной наличием опухоли прямой кишки, от выполнения первичной резекции прямой кишки по Гартману целесообразно отказаться, так как это существенно затрудняет последующую реабилитацию больного. Трудности при формировании реконструктивно-восстановительного колоректального анастомоза обусловлены прежде всего наличием короткой культи прямой кишки,
а также изменениями топографо-анатомических взаимоотношений органов таза.
Помимо этого, при наличии у больного рака среднеили нижнеампулярного отделов прямой кишки, особенно в случае местно-распространенных опухолей, выполнение операции Гартмана лишает больного возможности проведения неоадъювантной химиолучевой терапии. Исключение предоперационного облучения из комплексного лечения больных раком прямой кишки низкой локализации дискредитирует принципы онкологического радикализма этой категории больных.
Большое значение имеет выбор места выведения разгрузочной стомы в ситуации, когда опухоль прямой кишки стала причиной кишечной непроходимости. Так, если в последующем высока вероятность выполнения резекции прямой кишки с формированием колоректального анастомоза без превентивной стомы, то разгрузочную стому целесообразно наложить ближе к опухоли на дистальную часть сигмовидной кишки для обеспечения возможности включения ее в зону резекции и удаления вместе с препаратом. В случае когда локализация и/или распространенность опухоли диктует в дальнейшем необходимость выполнения резекции прямой кишки с формированием защитной стомы, наиболее рационально в виде разгрузочной стомы вывести проксимальный отдел поперечной ободочной кишки. Эта стома в последующем будет выполнять роль превентивной (УД 3 [5]).
Толстокишечная непроходимость c инфекционно-воспалительными осложнениями
Основной принцип лечения данной категории больных — ликвидация непроходимости, санация и дренирование очагов гнойного воспаления. Абсцесс брыжейки. При локализации абсцесса в брыжейке ободочной кишки у больных с кишечной непроходимостью и резектабельной опухолью выполняется резекция ободочной кишки с абсцессом. При локализации опухоли в правых отделах выполняется правосторонняя гемиколэктомия по типу операции Лахея. При локализации опухоли в средней трети поперечной ободочной кишки производится ее резекция по типу операции Гартмана. При локализации опухоли в левых отделах и возможности удаления абсцесса без его вскрытия выполняется резекция
ободочной кишки по типу Гартмана (СР D).
При отсутствии возможности удаления опухоли и/или наличии отдаленных метастазов выполняются пункция полости абсцесса или его вскрытие и дренирование (желательно экстраперитонеально), затем формирование петлевой стомы проксимальнее основного процесса (СР D).
Абсцесс забрюшинного пространства. Наличие абсцесса забрюшинного пространства в сочетании с кишечной непроходимостью опухолевого генеза ставит перед хирургами две задачи: вскрытие и дренирова-
ние абсцесса (предпочтительно пункционным методом) и ликвидация непроходимости.
При локализации опухоли в правых отделах ободочной кишки производится пункция абсцесса или его вскрытие и дренирование. При резектабельных новообразованиях выполняется правосторонняя гемиколэктомия по типу операции Лахея. При невозможности удаления опухоли и/или наличии отдаленных метастазов производятся экстраперитонеальное вскрытие и дренирование абсцесса с формированием проксимальной стомы. При локализации опухоли в средней трети поперечной ободочной кишки производится ее резекция по типу операции Гартмана. При локализации опухоли в левых отделах ободочной кишки выполняются пункция или вскрытие и дренирование абсцесса, по возможности экстраперитонеально, резекция по типу операции Гартмана. При невозможности удаления опухоли и/или наличии отдаленных метастазов производятся экстраперитонеально вскрытие и дренирование абсцесса с наложением кишечной стомы.
При локализации опухоли в прямой кишке выполняют пункцию абсцесса или его экстраперитонеальное вскрытие и дренирование с формированием проксимальной петлевой колостомы (СР D [34]).
Перитонит. Кишечная непроходимость в сочетании с перитонитом является абсолютным показанием к экстренному хирургическому лечению (СР D [40]). В такой ситуации необходимо проведение предоперационной подготовки в максимально допустимом объеме в сжатые сроки. Основная задача лечения этой категории больных — ликвидация кишечной непроходимости и устранение причины перитонита, санация и дренирование брюшной полости.
Основными причинами развития перитонита при кишечной непроходимости опухолевого генеза служат перфорация опухоли, перфорация супрастенотического отдела толстой кишки (диастатическая перфорация), вскрытие абсцесса брыжейки или забрюшинного пространства в свободную брюшную полость. Еще одной причиной перитонита опухолевого генеза может стать инфицирование транссудата брюшной полости.
При перфорации опухоли наиболее предпочтительны резекция толстой кишки с формированием проксимальной одноствольной стомы, санация и дренирование брюшной полости. При невозможности удаления первичной опухоли необходимо выведение проксимальной стомы и дренирование брюшной полости.
При перфорации супрастенотического отдела толстой кишки оптимальным методом хирургического лечения является резекция кишки с опухолью и местом перфорации. При этом необходимо формирование проксимальной одноствольной стомы. При неудалимой первичной опухоли возможны выведение места перфорации кишки в качестве стомы, санация и дренирование брюшной полости.
В случае вскрытия абсцесса брыжейки кишки или забрюшинного пространства при резектабельной опухоли следует выполнить ее удаление, произвести санацию и дренирование брюшной полости, операцию завершить формированием одноствольной стомы. При невозможности удаления первичной опухоли необходимо провести санацию и дренирование брюшной полости и вывести проксимальную петлевую илеоили колостому.
Комплексное лечение перитонита при наличии явлений тяжелого абдоминального сепсиса и септического шока должно проводиться по стандартам лечения этих осложнений.
Плановое/отсроченное хирургическое лечение
Купирование явлений кишечной непроходимости в результате проведения консервативных мероприятий, стентирования или формирования проксимальной кишечной стомы позволяет выполнить оперативное вмешательство по поводу колоректального рака в плановом порядке.
Объем операции зависит от локализации новообразования, степени местного распространения опухоли, наличия отдаленных метастазов, тяжести соматического состояния пациента [6].
При удалении злокачественного новообразования обязательно соблюдение так называемых онкологических принципов: абластики, антибластики, зональности и футлярности. Футлярность достигается путем выполнения мезоколонэктомии при опухолях ободочной кишки и тотальной мезоректумэктомии при локализации рака в прямой кишки, с обязательной высокой перевязкой питающих сосудов. Принцип зональности подразумевает соблюдение адекватных границ резекций — дистальной, проксимальной и латеральной. Для опухолей ободочной кишки и верхнеампулярного отдела прямой кишки допустимой минимальной проксимальной границей резекции является 10 см от опухоли, дистальной — 5 см. Для рака среднеи нижнеампулярного отдела прямой кишки дистальная граница резекции должна составлять не менее 2 см, а латеральная не менее 1 мм.
При расположении опухоли в слепой, восходящей кишке, правом изгибе ободочной кишки стандартной операцией является правосторонняя гемиколэктомия с высокой перевязкой подвздошно-ободочной артерии, правой ободочной артерии и правой ветви средней ободочной артерии и формированием илеотрансверзоанастомоза (СР В [27, 21]). При локализации опухоли в проксимальной части поперечной ободочной кишки выполняется расширенная правосторонняя гемиколэктомия, при которой, помимо указанных выше сосудов, производят высокую перевязку средней ободочной артерии. При местно-распространенных новообразованиях этой локализации, а также при наличии отдаленных метастазов в печень, яичники выполняются комбинированные хирургические вмешательства. У пациентов с тяжелыми сопутствующими заболевани-
ями, с распространенным канцероматозом брюшины или массивным метастатическим поражением печени операция может быть ограничена формированием обходного илеотрансверзоанастомоза или выведением илеостомы.
У пациентов с новообразованиями средней трети поперечной ободочной кишки плановые оперативные вмешательства могут быть выполнены в объеме резекции поперечной ободочной кишки или субтотальной резекции ободочной кишки [33].
В качестве планового оперативного вмешательства при локализации злокачественного новообразования в дистальной трети поперечной ободочной кишки, левом изгибе, нисходящей кишке, проксимальной и средней трети сигмовидной кишки выполняется левосторонняя гемиколэктомия, при которой производят высокое лигирование нижнебрыжеечных сосудов и левой ветви средней ободочной артерии. Операцию завершают формированием трансверзосигмоидного или трансверзоректального анастомоза [23]. При раке дистальной трети сигмовидной кишки производится дистальная резекция сигмовидной кишки, при которой необходимо производить перевязку нижнебрыжеечной артерии у места отхождения от аорты. При местно-распространенных опухолях этих локализаций, а также при наличии отдаленных метастазов могут быть выполнены комбинированные операции. У больных тяжелыми сопутствующими заболеваниями, при распространенном метастатическим поражении брюшины или печени может быть также выполнена резекция ободочной кишки по типу операции Гартмана [13, 16]. Операция в этой ситуации может быть ограничена формированием колостомы или илеостомы (предпочтительно через лапароскопический или мини-доступ).
При раке прямой кишки в зависимости от локализации опухоли в плановом порядке могут быть выполнены следующие оперативные вмешательства: передняя резекция прямой кишки, низкая передняя резекция прямой кишки с превентивной илеоили колостомой, операция Гартмана, брюшно-анальная резекция прямой кишки, брюшно-промежностная экстирпация прямой кишки, комбинированные операции. У тяжелых больных при местно-распространенных новообразованиях прямой кишки и при массивном отдаленном распространении опухоли операция может быть ограничена колоили илеостомией (предпочтительно через лапароскопический или мини-доступ).
ЛЕЧЕБНАЯ ТАКТИКА ПРИ КИШЕЧНОЙ НЕПРОХОДИМОСТИ, ОБУСЛОВЛЕННОЙ МЕСТНЫМИ РЕЦИДИВАМИ РАКА ТОЛСТОЙ КИШКИ
Хирургическое лечение местных рецидивов рака ободочной и прямой кишки представляет собой наиболее сложную проблему в колоректальной хирургии. Это обусловлено местно-деструирующим характером роста опухолей, с глубоким прорастанием ее в окружающие ткани, нарушением анатомических соотношений, что требует выполнения
комбинированных экстрафасциальных хирургических вмешательств. Эти операции отличаются высоким травматизмом, большой интраоперационной кровопотерей и продолжительностью, а также значительным числом послеоперационных осложнений и летальности. Учитывая эти факторы, радикальные оперативные вмешательства по поводу местных рецидивов рака толстой кишки должны производиться только в специализированных клиниках наиболее опытными хирургами. Тактика лечения больных при поступлении в общехирургические стационары должна заключаться в выведении проксимальной стомы, стабилизации состояния пациента и направлении его в специализированные лечебные учреждения (УД D [4, 8]).
Кишечная непроходимость у больных с местными рецидивами рака толстой кишки может развиться как при внутрикишечном росте рецидивной опухоли, так и при внекишечной ее локализации при сдавлении кишки извне. Диагноз устанавливается на основании анамнестических данных, клинического и инструментального методов обследования, основными из которых являются обзорная рентгенография брюшной полости, КТ или УЗИ брюшной полости, малого таза и забрюшинного пространства, эндоскопические методы (ректороманоскопия, колоноскопия) (УД D [35]).
На хирургическую тактику при кишечной непроходимости у пациентов с местными рецидивами колоректального рака оказывают влияние следующие факторы.
n Локализация местного рецидива (в тазу или в брюшной полости; внутрипросветный или внекишечный).
n Местное распространение рецидивной опухоли.
n Наличие отдаленных метастазов и их локализация.
n Выраженность явлений кишечной непроходимости.
n Другие осложнения со стороны рецидивной опухоли (перифокальное воспаление, абсцедирование, кровотечение, формирование свищей).
n Общее состояние пациента и выраженность сопутствующих заболеваний. В общехирургическом стационаре операции при местных рецидивах рака толстой кишки с явлениями кишечной непроходимости должны носить симптоматический характер (в объеме проксимальной стомы или обходного анастомоза). В специализированной клинике аналогичный объем хирургического вмешательства производится при декомпенсированной кишечной непроходимости и ее осложнениях (перитонит, абсцесс), общем тяжелом состоянии больного, наличии у него выраженных сопутствующих заболеваний, метастатического поражения других органов, а также вовлечении в рецидивный опухолевый процесс крупных сосудов и костных структур. При отсутствии полной кишечной непроходимости, резектабельном местном рецидиве опухоли, отсутствии отдаленных метастазов и удовлетворительном состоянии пациента показано выполнение комбинированной операции — удаление местного рецидива опухоли,
органов и тканей, вовлеченных в опухолевый процесс (УД 4 [9, 42]).
КИШЕЧНАЯ НЕПРОХОДИМОСТЬ ПРИ РАКЕ ТОЛСТОЙ КИШКИ С КАНЦЕРОМАТОЗОМ БРЮШИНЫ
У больных раком ободочной кишки с канцероматозом брюшины явления кишечной непроходимости могут быть обусловлены не только первичной опухолью, но и имплантационными метастазами, которые деформируют и перекрывают просвет кишечника на том или ином уровне. Выбор хирургической тактики у этих пациентов представляет значительные трудности.
В хирургическом отделении общего профиля оперативное лечение этой категории пациентов носит исключительно симптоматический характер. В зависимости от локализации в тонкой кишке канцероматозного узла, вызвавшего кишечную непроходимость, могут быть выполнены следующие операции: проксимальная илеостомия (при расположении препятствия в дистальных отделах подвздошной кишки); формирование обходного энтеро-энтероанастомоза (при высоком уровне непроходимости).
В специализированном стационаре при наличии хирургов-онкологов высокой квалификации, обладающих опытом выполнения мультивисцеральных резекций и перитонэктомии при колоректальном раке с канцероматозом брюшины, объем операции зависит от различных факторов.
n Распространенность канцероматоза по брюшине.
n Локализация и степень местного распространения первичной опухоли.
n Осложнения со стороны первичной опухоли (перифокальное воспаление, абсцедирование).
n Наличие других отдаленных метастазов и их распространенность.
n Выраженность явлений кишечной непроходимости.
n Тяжесть состояния больного и выраженность сопутствующих заболеваний.
В зависимости от перечисленных выше обстоятельств объем хирургического пособия может варьировать от симптоматических операций до выполнения обширных циторедуктивных комбинированных мультивисцеральных резекций, включающих перитонэктомию, оментэктомию, в сочетании с проведением интраоперационной внутрибрюшной химиотерапией. При данном типе операций производится удаление первичной опухоли толстой кишки, всех по возможности имплантационных метастазов для достижения полной циторедукции, а хирургическое лечение дополняется внутрибрюшной химиотерапией для воздействия на свободные опухолевые комплексы. В настоящее время такая лечебная тактика является единственным методом, позволяющим увеличить продолжительность жизни этих больных и надеяться на их выздоровление.
Критерии оценки качества помощи в стационаре представлены в таблице 23.2. Для оценки качества медицинской помощи используют временные, процессуальные и профилактирующие критерии. Временные характеризуют своевременность оказания определенных этапов медицин-
ской помощи. Выполнение пациенту ряда медицинских манипуляций, инструментальных и лабораторных исследований, необходимых для качественного оказания медицинской помощи, оценивают в процессуальных критериях. Для анализа мероприятий, направленных на предотвращение развития осложнений, используют профилактирующие критерии.
Таблица 23.2. Критерии оценки качества медицинской помощи в стационаре больным острой кишечной непроходимостью (0 — нет, 1 — да)
|
Клинические рекомендации |
Временные |
Процессуальные |
Профилактирующие |
|
Клинические рекомендации по лечению больных кишечной непроходимостью опухолевой этиологии (код МКБ — К56.6, С18–С20) |
Установка клинического диагноза в течение 2 ч: 0/1. Оценка эффективности проводимой консервативной терапии не позднее 12 ч: 0/1. При разрешении острой кишечной непроходимости направление больного для плановой операции в онкологический или колопроктологический стационар: 0/1 |
Пальцевое ректальное обследование 0/1. Ректороманоскопия: 0/1. ЭКГ: 0/1. Обзорная рентгенография органов грудной клетки: 0/1. Лучевые методы обследования брюшной полости: 0/1. Определение группы крови: 0/1. Клинический анализ крови; биохимический анализ крови; клинический анализ мочи; коагулограмма: 0/1. Исследование крови на сифилис, вирусный гепатит В, вирусный гепатит С: 0/1. Метод оперативного лечения в соответствии с клиническими рекомендациями: 0/1. Метод анестезии в соответствии с объемом оперативного лечения: 0/1 |
Отсутствие осложнений: • внутрибрюшное кровотечение: 0/1; • абсцесс: 0/1; • пневмония: 0/1; • тромбоэмболия: 0/1; • парастомальные осложнения: 0/1; • эвентрация: 0/1; • несостоятельность анастомоза: 0/1; • послеоперационный перитонит: 0/1; • летальный исход: 0/1 |
Литература
1. Ачкасов Е.Е., Пугаев А.В., Алекперов С.Ф. и др. Классификация обтурационной толстокишечной непроходимости опухолевого генеза // Колопроктология. — 2009. — № 3. — C. 17–23.
2. Воробьев Г., Царьков П. Основы хирургии кишечных стом. — М.: Стольный град, 2002. — C. 54.
3. Савельев В., Чазов Е., Гусев Е. и др. Российские клинические рекомендации по диагностике, лечению и профилактике венозных тромбоэмболических осложнений // Флебология. — 2010. — № 2. — C. 37.
4. Akiyoshi T., Fujimoto Y., Konishi T. et al. Prognostic factors for survival after salvage surgery for locoregional recurrence of colon cancer // Am. J. Surg. — 2011. — Vol. 201, N 6. — P. 726–733.
5. Ansaloni L., Andersson R.E., Bazzoli F. et al. Guidelenines in the management of obstructing cancer of the left colon: consensus conference of the world society of emergency surgery and peritoneum and surgery society // World J. Emerg. Surg. — 2010. — Vol. 5. — P. 29.
6. Aslar A.K., Ozdemir S., Mahmoudi H. et al. Analysis of 230 cases of emergent surgery for obstructing colon cancer-lessons learned // J. Gastrointest. Surg. — 2011. — Vol. 15, N 1. — P. 110–119.
7. Biondo S., Jaurrieta E., Marti Rague J. et al. Role of resection and primary anastomosis of the left colon in the presence of peritonitis // Br. J. Surg. — 2000. — Vol. 87, N 11. — P. 1580–1584.
8. Bowne W.B., Lee B., Wong W.D. et al. Operative salvage for locoregional recurrent colon cancer after curative resection: an analysis of 100 cases // Dis. Colon Rectum. — 2005. — Vol. 48, N 5. — P. 897–909.
9. Carne P.W., Frye J.N., Kennedy-Smith A. et al. Local invasion of the bladder with colorectal cancers: surgical management and patterns of local recurrence // Dis. Colon Rectum. — 2004. — Vol. 47, N 1. — P. 44–47.
10. Carraro P.G., Segala M., Cesana B.M. et al. Obstructing colonic cancer: failure and survival patterns over a ten-year follow-up after one-stage curative surgery // Dis. Colon Rectum. — 2001. — Vol. 44, N 2. — P. 243–250.
11. Chapman A.H., McNamara M., Porter G. The acute contrast enema in suspected large bowel obstruction: value and technique // Clin. Radiol. — 1992. — Vol. 46, N 4. — P. 273–278.
12. Cirocchi R., Farinella E., Trastulli S. et al. Safety and efficacy of endoscopic colonic stenting as a bridge to surgery in the management of intestinal obstruction due to left colon and rectal cancer: a systematic review and meta-analysis // Surg. Oncol. — 2013. — Vol. 22, N 1. — P. 14–21.
13. Cirocchi R., Trastulli S., Farinella E. et al. High tie versus low tie of the inferior mesenteric artery in colorectal cancer: a RCT is needed // Surg. Oncol. — 2012. — Vol. 21, N 3. — P. 111–123.
14. Collins R., Scrimgeour A., Yusuf S., Peto R. Reduction in fatal pulmonary embolism and venous thrombosis by perioperative administration of subcutaneous heparin. Overview of results of randomized trials in general, orthopedic, and urologic surgery // N. Engl. J. Med. — 1988. — Vol. 318, N 18. — P. 1162–1173.
15. Deierhoi R.J., Dawes L.G., Vick C. et al. Choice of intravenous antibiotic prophylaxis for colorectal surgery does matter // J. Am. Coll. Surg. — 2013. — Vol. 217, N 5. — P. 763–769.
16. Duran Gimenez-Rico H., Abril Vega C., Herreros Rodriguez J. et al. Hartmann’s procedure for obstructive carcinoma of the left colon and rectum: a comparative study with one-stage surgery // Clin. Transl. Oncol. — 2005. — Vol. 7, N 7. — P. 306–313.
17. Finan P.J., Campbell S., Verma R. et al. The management of malignant large bowel obstruction: ACPGBI position statement // Colorectal Dis. — 2007. — Vol. 9, N 4. — P. 1–17.
18. Fiori E., Lamazza A., Schillaci A. et al. Palliative management for patients with subacute obstruction and stage IV unresectable rectosigmoid cancer: colostomy
versus endoscopic stenting: final results of a prospective randomized trial // Am. J. Surg. — 2012. — Vol. 204, N 3. — P. 321–326.
19. Frager D., Rovno H.D., Baer J.W. et al. Prospective evaluation of colonic obstruction with computed tomography // Abdom. Imaging. — 1998. — Vol. 23, N 2. — P. 141–146.
20. Hassan C., Bretthauer M., Kaminski M.F. et al. Bowel preparation for colonoscopy: European Society of Gastrointestinal Endoscopy guideline // Endoscopy. — 2013. — Vol. 45, N 2. — P. 142–150.
21. Hohenberger W., Weber K., Matzel K. et al. Standardized surgery for colonic cancer: complete mesocolic excision and central ligation--technical notes and outcome // Colorectal Dis. — 2009. — Vol. 11, N 4. — P. 354–364; discussion 364-5.
22. Horiuchi A., Nakayama Y., Tanaka N. et al. Acute colorectal obstruction treated by means of transanal drainage tube: effectiveness before surgery and stenting // Am. J. Gastroenterol. — 2005. — Vol. 100, N 12. — P. 2765–2770.
23. Jimenez Fuertes M., Costa Navarro D. Resection and primary anastomosis without diverting ileostomy for left colon emergencies: is it a safe procedure? // World J. Surg. — 2012. — Vol. 36, N 5. — P. 1148–1153.
24. Kakkar V.V., Cohen A.T., Edmonson R.A. et al. Low molecular weight versus standard heparin for prevention of venous thromboembolism after major abdominal surgery. The Thromboprophylaxis Collaborative Group // Lancet. — 1993. — Vol. 341, N 8840. — P. 259–265.
25. Khot U.P., Lang A.W., Murali K. et al. Systematic review of the efficacy and safety of colorectal stents // Br. J. Surg. — 2002. — Vol. 89, N 9. — P. 1096–1102.
26. Kuo L.J., Leu S.Y., Liu M.C. et al. How aggressive should we be in patients with stage IV colorectal cancer? // Dis. Colon Rectum. — 2003. — Vol. 46, N 12. — P. 1646–1652.
27. Lee Y.M., Law W.L., Chu K.W. et al. Emergency surgery for obstructing colorectal cancers: a comparison between right-sided and left-sided lesions // J. Am. Coll. Surg. — 2001. — Vol. 192, N 6. — P. 719–725.
28. Lyman G.H., Khorana A.A., Kuderer N.M. et al. Venous thromboembolism prophylaxis and treatment in patients with cancer: American Society of Clinical Oncology clinical practice guideline update // J. Clin. Oncol. — 2013. — Vol. 31, N 17. — P. 2189–2204.
29. Maung A.A., Johnson D.C., Piper G.L. et al. Evaluation and management of small-bowel obstruction: an Eastern Association for the Surgery of Trauma practice management guideline // J. Trauma Acute Care Surg. — 2012. — Vol. 73, N 5. — Suppl. 4. — P. 362–369.
30. Megibow A.J., Balthazar E.J., Cho K.C. et al. Bowel obstruction: evaluation with CT // Radiology. — 1991. — Vol. 180, N 2. — P. 313–318.
31. Meisner S., Gonzalez-Huix F., Vandervoort J.G. et al. Self-expandable metal stents for relieving malignant colorectal obstruction: short-term safety and efficacy within 30 days of stent procedure in 447 patients // Gastrointest. Endosc. — 2011. — Vol. 74, N 4. — P. 876–884.
32. Mella J., Biffin A., Radcliffe A.G. et al. Population-based audit of colorectal cancer management in two UK health regions. Colorectal Cancer Working Group, Royal College of Surgeons of England Clinical Epidemiology and Audit Unit // Br. J. Surg. — 1997. — Vol. 84, N 12. — P. 1731–1736.
33. Ortiz H., Biondo S., Ciga M.A. et al. Comparative study to determine the need for intraoperative colonic irrigation for primary anastomosis in left-sided colonic emergencies // Colorectal Dis. — 2009. — Vol. 11, N 6. — P. 648–652.
34. Park J., Charles H.W. Intra-abdominal abscess drainage: interval to surgery // Semin. Intervent. Radiol. — 2012. — Vol. 29, N 4. — P. 311–313.
35. Platell C., Ng S., O’Bichere A., Tebbutt N. Changing management and survival in patients with stage IV colorectal cancer // Dis. Colon Rectum. — 2011. — Vol. 54, N 2. — P. 214–219.
36. Salzman E.W., Davies G.C. Prophylaxis of venous thromboembolism: analysis of cost effectiveness // Ann. Surg. — 1980. — Vol. 191, N 2. — P. 207–218.
37. Sebastian S., Johnston S., Geoghegan T. Pooled analysis of the efficacy and safety of self-expanding metal stenting in malignant colorectal obstruction // Am. J. Gastroenterol. — 2004. — Vol. 99, N 10. — P. 2051–2057.
38. Serpell J.W., McDermott F.T., Katrivessis H. et al. Obstructing carcinomas of the colon // Br. J. Surg. — 1989. — Vol. 76, N 9. — P. 965–969.
39. Sjo O.H., Larsen S., Lunde O.C. et al. Short term outcome after emergency and elective surgery for colon cancer // Colorectal Dis. — 2009. — Vol. 11, N 7. — P. 733–739.
40. Uematsu D., Akiyama G., Magishi A. et al. Laparoscopic Hartmann’s procedure for fecal peritonitis resulting from perforation of the left-sided colon in elderly and severely ill patients // Tech. Coloproctol. — 2012. — Vol. 16, N 3. — P. 243–246.
41. Umpleby H.C., Williamson R.C. Survival in acute obstructing colorectal carcinoma // Dis. Colon Rectum. — 1984. — Vol. 27, N 5. — P. 299–304.
42. Zorcolo L., Covotta L., Carlomagno N. Toward lowering morbidity, mortality, and stoma formation in emergency colorectal surgery: the role of specialization // Dis. Colon Rectum. — 2003. — Vol. 46, N 11. — P. 1461–1467; discussion 1467-8.
43. OCEBM Levels of Evidence Working Group. The Oxford 2011 Levels of Evidence. — Oxford Centre for Evidence-Based Medicine, 2011.
КРИТЕРИИ ОЦЕНКИ КАЧЕСТВА ОКАЗАНИЯ МЕДИЦИНСКОЙ
ПОМОЩИ
ПО ПРОФИЛЮ ГАСТРОЭНТЕРОЛОГИЯ И КОЛОПРОКТОЛОГИЯ
В СТАЦИОНАРНЫХ И АМБУЛАТОРНЫХ УСЛОВИЯХ
1. Критерии оценки качества медицинской помощи по профилю гастроэнтерология1
1.1. В стационарных условиях.
1.1.1. Госпитализация пациента в медицинскую организацию, имеющую структурное подразделение, соответствующее стандарту оснащения и рекомендуемым штатным нормативам.
1.1.2. Установление предварительного диагноза в течение первых суток на основании данных клинического обследования, результатов инструментальных и лабораторных методов исследования. Установление/ подтверждение/ верификация обоснованного клинического диагноза в течение 96 часов.
1.1.3. Принятия решения о выборе метода лечения в срок не более 72 часов с учетом возраста, тяжести и стадии заболевания, наличия сопутствующих заболеваний и/или осложнений.
1.1.4. В случае затруднения установления обоснованного клинического диагноза и /или выбора метода лечения в течение сроков указанных в пп.3.1.2. и 3.1.3. – созыв консилиума врачей с целью принятия решения.
1.1.5. Ведение лечащим врачом унифицированных форм медицинской документации, в том числе в электронном виде.
1.1.6. В случае необходимости в целях диагностики и/или лечения применение ультразвуковых/рентгенологических/эндоскопических методов.
1 Критерии оценки качества медицинской помощи формируются на основе порядков, стандартов и клинических рекомендаций оказания медицинской помощи.
1.1.7. Выполнение в полном объеме диагностических исследований и процедур, имеющих частоту предоставления 1,0.
1.1.8. Выполнение в полном объеме лечебных медицинских услуг, имеющих частоту предоставления 1,0.
1.1.9. Назначение группы лекарственных препаратов в полном объеме по анатомо-терапевтическо-химической классификации, имеющих частоту предоставления 1,0.
1.1.10. Наличие консультации и осмотра специалиста при сопутствующей патологии у пациента.
1.1.11. Осуществление экспертизы временной нетрудоспособности.
1.1.12. При наличии осложнений — своевременная диагностика и лечение/ коррекция возникших осложнений.
1.1.12. Назначение лекарственной терапии в соответствии с предусмотренным алгоритмом и учетом инструкции по применению лекарственных препаратов, возраста пациента, тяжести заболевания, наличия осложнений и сопутствующей патологии, и осуществляется в стационарных условиях в соответствии с приказом Минздрава России от 20.12.2012 № 1175н.
1.1.13. Назначение лекарственных препаратов, не зарегистрированных на территории Российской Федерации, препаратов, не входящих в стандарты медицинской помощи, осуществляется по решению врачебной комиссии медицинской организации. Решение врачебной комиссии медицинской организации фиксируется в медицинских документах пациента и журнале врачебной комиссии.
1.1.14. Наличие отказа в госпитализации профильного пациента, зафиксированного в журнале отказов от госпитализации с указанием причины отказа.
1.1.15. Наличие выписного эпикриза из медицинской карты стационарного больного с результатами проведенного обследования и лечения и рекомендациями по дальнейшей тактике наблюдения и лечения по заболеванию.
1.2. Критерии оценки качества медицинской помощи по профилю гастроэнтерология в амбулаторных условиях
1.2.1. Наблюдение врача терапевта, участкового врача, врача общей практики (семейного врача), врача-гастроэнтеролога.
1.2.2. Ведение лечащим врачом унифицированных форм медицинской документации, в том числе в электронном виде.
1.2.3. При выявлении у пациента заболевания гастроэнтерологического профиля – направление на консультацию к врачу гастроэнтерологу, при необходимости направление на госпитализацию в профильное отделение
1.2.4. Осуществление экспертизы временной нетрудоспособности.
1.2.5. Наличие консультации и осмотра специалиста при сопутствующей патологии у пациента.
1.2.6. Диспансерное наблюдение пациента с хроническим заболеванием с рекомендациями по диетотерапии и осмотром (вызовом на осмотр) лечащего врача не менее 1 раз в год.
![]()
1.2.7. Выполнение в полном объеме диагностических исследований и процедур, имеющих частоту предоставления 1,0.
1.2.8. Назначение лекарственных препаратов в полном объеме по заболеванию (состоянию), имеющих частоту предоставления 1,0.
1.2.9. Проведение профилактических мероприятий, направленных на снижение риска обострения хронического заболевания, в том числе с рекомендациями по соблюдению диеты (при условии возможности получение санаторно-курортного лечения).
1.2.10. При наличии осложнений — своевременная диагностика и лечение/коррекция возникших осложнений.
1.2.11. При необходимости направление на госпитализацию в профильное отделение.
1.2.12. Проведение медицинской реабилитации после выписки из стационара с учетом рекомендаций, изложенных в выписки из медицинской карты стационарного больного.
2. Критерии оценки качества медицинской помощи по профилю колопроктология1
2.1. В стационарных условиях
2.1.1. Госпитализация пациента в медицинскую организацию, имеющую структурное подразделение, соответствующее стандарту оснащения и рекомендуемым штатным нормативам.
2.1.2. Наличие отказа в госпитализации пациента, зафиксированного в журнале отказов от госпитализации с указанием причины отказа.
2.1.3. Установление/подтверждение/верификация обоснованного клинического диагноза в течение 72 часов после госпитализации пациента в профильное отделение.
2.1.4. Принятия решения о выборе метода лечения в срок не более 48 часов (консервативное/оперативное) с учетом возраста, тяжести и стадии заболевания, наличия сопутствующих заболеваний и/или осложнений.
2.1.5. В случае госпитализации пациента с целью оказания медицинской помощи по экстренным и неотложным показаниям установление/ подтверждение/верификация клинического диагноза и принятия решения о выборе метода лечения с учетом состояния тяжести пациента осуществляется в срок не более 24–48 часов.
2.1.6. При выборе хирургического метода лечения – выбор анестезиологического пособия с учетом состояния тяжести пациента и объема планируемого оперативного вмешательства.
2.1.7. В случае затруднения установления обоснованного клинического диагноза и/или выбора метода лечения в течение указанных сроков — созыв консилиума врачей с целью принятия решения.
1 Критерии оценки формируются на основе порядков оказания медицинской помощи населению, стандартов медицинской помощи и клинических рекомендаций.
2.1.8. Назначение лекарственной терапии в соответствии с предусмотренным алгоритмом и учетом инструкции по применению лекарственных препаратов, пола, возраста пациента, тяжести заболевания, наличия осложнений и сопутствующей патологии.
2.1.9. Выполнение в полном объеме диагностических исследований и процедур, имеющих частоту предоставления 1,0.
2.1.10. Выполнение в полном объеме лечебных медицинских услуг, имеющих частоту предоставления 1,0.
2.1.11. Назначение группы лекарственных препаратов в полном объеме по анатомо-терапевтическо-химической классификации, имеющих частоту предоставления 1,0.
2.1.12. При наличии осложнений — своевременная диагностика и лечение/коррекция.
2.1.13. Наличие рекомендации по заболеванию (состоянию) в выписке из медицинской карты стационарного больного.
2.2. Критерии оценки качества медицинской помощи по профилю колопроктология в амбулаторных условиях
2.2.1. Наблюдение врача-терапевта, участкового врача, врача общей практики (семейного врача), врача – колопроктолога, хирурга.
2.2.2. Ведение унифицированных форм медицинской документации, в том числе в электронной форме.
2.2.3. При подозрении или выявлении у пациента заболевания колопроктологического профиля – направление на консультацию к врачу колопроктологу, при необходимости направление на госпитализацию в профильное отделение.
2.2.4. Осуществление экспертизы временной нетрудоспособности.
2.2.5. Наличие консультации и осмотра специалиста при сопутствующей патологии у пациента.
2.2.6. Диспансерное наблюдение пациента с установленным диагнозом колопроктологического профиля.
2.2.7. Выполнение в полном объеме диагностических исследований и процедур, имеющих частоту предоставления 1,0.
2.2.8. Выполнение в полном объеме лечебных медицинских услуг, имеющих частоту предоставления 1,0.
2.2.9. Назначение группы лекарственных препаратов в полном объеме по анатомо-терапевтическо-химической классификации, имеющих частоту предоставления 1,0.
2.2.10. Проведение профилактических мероприятий, направленных на снижение риска обострения хронического заболевания.
2.2.11. При наличии медицинских показаний направление на госпитализацию в профильное отделение.
2.2.12. Проведение медицинской реабилитации после выписки из стационара (при необходимости) с учетом рекомендаций, изложенных в выписке из медицинской карты стационарного больного.
Аденоматоз толстой кишки семейный 348 Ангиодисплазия
артериальная 333
артериовенозная 333
венозная 333
врожденная 333, 334
генерализованная 333
диффузная 333
ограниченная 333
приобретенная 333, 339 Болезнь
Боуэна 219, 222
Гиршпрунга 280
наданальная 281
ректальная 281
ректосигмоидная 281
субтотальная 281
тотальная 281
дивертикулярная 252
Крона 365
Рендю–Ослера 333
Уиппла 436
Чагаса 311
Бородавки аногенитальные 218 Бородавки в виде папул 222 Ведение взрослых пациентов
с кишечной стомой 449 Выпадение прямой кишки 170 Геморроидэктомия
аппаратом LigaSure 45
аппаратом UltraCision 45
закрытая 42
открытая 42
подслизистая 43
степлерная 43
внутренний 33
комбинированный 33
наружный 33
острый 33
хронический 33
Дивертикул 251
неполный 252
Дивертикулез 251
«восточный» 252
«западный» 251 Дивертикулез ободочной кишки 251
Дивертикулит 256
перфоративный 257
Долихоколон 297
бессимптомный 298
долихосигма 297
долихотрансверзум 297
левосторонний 297
осложненный 298
правосторонний 297
с нарушением транзита 298 субтотальный 297
тотальный 297 Инвагинация ректоанальная
высокая 171
низкая 171
Инвагинация ректоректальная высокая 171
низкая 171 Индекс
Беста 366
максимально переносимого объема 316
массы тела 150
Мейо 399
оксфордский 409
шведский 409 Инфильтрат паракишечный
острый 256
хронический 256
Калоприемник 478
двухкомпонентный 478
дренируемые 479
недренируемые 479
однокомпонентный 478 Кисты
пресакральные 128
внетазовые 129
внутритазовые 129
неосложненного течения 129
осложненного течения 129 тератоидные образования кистозного строения 129
солидного строения 129
эктодермальные 129
тератомы 129
Колит язвенный 395, 397
обострение 397
ремиссия 398 Кондилома(ы)
Бушке–Левенштейна гигантская 222
перианальной области и анального канала остроконечные 216
Криз
аддисонический 418 Мегаколон
декомпенсированный 281
идиопатический 314
компенсированный 281
левосторонний 314
субкомпенсированный 281
субтотальный 314
тотальный 314
Мегасигма 314 Недостаточность анального сфинктера 192
на боковой стенке 194 на задней стенке 194
на нескольких стенках 194 на передней стенке 194 неорганическая 193
органическая 193
па всей окружности 194 смешанная 193
Непроходимость кишечная высокая 495
декомпенсированная 495
компенсированная 495
низкая 495
опухолевого генеза 492
полная 495
субкомпенсированная 495
частичная 495
Парапроктит хронический 84
Парапроктит острый 69
анаэробный 70
клостридиальный 70
неклостридиальный 70
аэробный 70
боковой 70
задний 70
интрасфинктерный 70
ишеоанальный 70
межмышечный 70
передний 70
подкожный 70
подслизистый 70
тазово-прямокишечный 70
пельвиоректальный 70
подковообразный 70
ретроректальный 70
транссфинктерный 70
экстрасфинктерный 70
Пектеноз 20 Пластины
конвексные 478
адгезивные 478
Пневмодивульсия 21
Полипоз ювенильный 349
Полипы анальные 238
аденома 238
ворсинчатые 238
гиперпластические 238, 239
доброкачественные 238
злокачественные 238
«истинные» 239
клоакогенные 239
на ножке 238
неопухолевые 239
плоские 238
тубулярные 238
фиброзные 240 Поражения в виде пятен 222 Пролапс ректальный 168
внутренняя инвагинация. См. также Инвагинация
внутренняя 168
наружное выпадение прямой кишки 168
Профилометрия 16, 114, 195
Ректоцеле 149
высокое 149
нижнее 149
среднее 149 Свищ
заднего прохода и прямой кишки 84
боковой 86
задний 86
интрасфинктерный 86, 87
неполный внутренний 86
передний 86
полный 86
транссфинктерный 86, 88
экстрасфинктерный 86, 88 Свищи
ректовагинальные 110
перианальные 111
постлучевые 111
ишемические 112
посттравматические 111
послеоперационные 111
послеродовые 111 Синдром
Гарднера 349
Золингера–Эллисона 349 избыточного бактериального
роста 383
Клиппеля–Треноне 333
компартмент 494
короткой кишки 379
Линча 352
Марфана 253
обструктивной дефекации 150
Огилви 318
опущения промежности 147
Пейтца–Егерса 349
псевдообструкции 311
раздраженного кишечника 430 со смешанным
характером 433 с преобладанием
болевого синдрома 433
диареи 432
запоров 433
метеоризма 433 нарушения частоты
стула 433
раздраженного резервуара 421 тревожный или
депрессивный 156
Тюрко 349
эндотоксемии 401
Энлоса–Данлоса 253
Стома 451
классификация 452 Сфинктеротомия подкожная боковая 21
закрытая 21
открытая 21
Трещина анальная 14
без спазма 14
боковая 14
задняя 14
острая 14, 17
передняя 14
со спазмом 14
хроническая 14, 17 Ход копчиковый эпителиальный 55
воспаление острое 56
хроническое 56
неосложненный 56
ремиссия воспаления 56
![]()
Научно-практическое издание
КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ КОЛОПРОКТОЛОГИЯ
Под редакцией Ю.А. Шелыгина
Главный редактор издательства С.Ю. Кочетков
Зав. редакцией А.В. Андреева
Менеджер проекта И.О. Ксёндзова Выпускающий редактор И.В. Курдюкова Корректоры М.Ю. Никитина, Л.И. Базылевич Компьютерная верстка А.В. Вишневский Дизайн обложки И.Ю. Баранова
Технолог Ю.В. Дмитриева
Подписано в печать 19.03.2015. Формат 60×90 1/16.
Бумага офсетная. Печать офсетная.
Объем 33 усл. печ. л. Тираж 3000 экз. (I завод 1000 экз.). Заказ № ООО Издательская группа «ГЭОТАР-Медиа».
115035, Москва, ул. Садовническая, д. 9, стр. 4.
Тел.: 8 (495) 921-39-07.
E-mail: info@geotar.ru, http://www.geotar.ru.
Отпечатано в ППП «Типография “Наука”». 121099, Москва, Шубинский пер., д. 6.
.
Рекомендуемые статьи
При эндоскопическом исследовании в случае бронхоэктазов в стадии ремиссии выявляется
частично диффузный бронхит I степени воспаления
Активируйте PUSH уведомления в браузер
Отключите PUSH уведомления в браузер
Содержание
Интернет магазин
Популярное
- О нас
- Правовые вопросы
- Политика
обработки персональных
данных EndoExpert.ru - Связаться с нами
- Стать партнером
© 2016-2022 EndoExpert.ru

Вы находитесь в разделе предназначенном только для специалистов (раздел для пациентов по ссылке). Пожалуйста, внимательно прочитайте полные условия использования и подтвердите, что Вы являетесь медицинским или фармацевтическим работником или студентом медицинского образовательного учреждения и подтверждаете своё понимание и согласие с тем, что применение рецептурных препаратов, обращение за той или иной медицинской услугой, равно как и ее выполнение, использование медицинских изделий, выбор метода профилактики, диагностики, лечения, медицинской реабилитации, равно как и их применение, возможны только после предварительной консультации со специалистом. Мы используем файлы cookie, чтобы предложить Вам лучший опыт взаимодействия. Файлы cookie позволяют адаптировать веб-сайты к вашим интересам и предпочтениям.
Я прочитал и настоящим принимаю вышеизложенное, хочу продолжить ознакомление с размещенной на данном сайте информацией для специалистов.











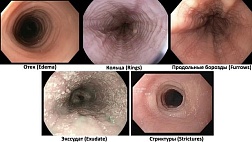


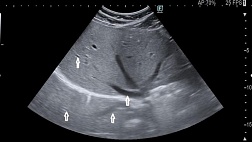


.jpg)




.png)














Комментарии