- Компании
- Takeda. О компании, буклеты, каталоги, контакты
- Olympus. О компании, буклеты, каталоги, контакты
- Boston Scientific. О компании, буклеты, каталоги, контакты
- Pentax. О компании, буклеты, каталоги, контакты
- Fujifilm & R-Farm. О компании, буклеты, каталоги, контакты
- Erbe. О компании, буклеты, каталоги, контакты
- Еще каталоги
- Мероприятия
- Информация
- Обучение
- Дайджест
- QuaCol
- Разделы
- Пациентy
QR-код этой страницы

Для продолжения изучения на мобильном устройстве ПРОСКАНИРУЙТЕ QR-код с помощью спец. программы или фотокамеры мобильного устройства
Статьи: Капсульная эндоскопия тонкой кишки и аппаратная энтероскопия для диагностики и лечения заболеваний тонкой кишки: Технический обзор Европейского общества желудочно-кишечной эндоскопии (ESGE)
| Авторы: | Emanuele Rondonotti , Cristiano Spada , Samuel Adler , Andrea May , Edward J. Despott , Anastasios Koulaouzidis , Simon Panter , Dirk Domagk , Ignacio Fernandez-Urien , Gabriel Rahmi , Maria Elena Riccioni , Jeanin E. van Hooft , Cesare Hassan , Marco Pennazio |

Полный текст статьи:
Капсульная эндоскопия тонкой кишки (SBCE)
1 ESGE рекомендует пациентам перед SBCE принять слабительное (2 л полиэтиленгликоля [PEG]) для лучшей визуализации.
Сильная рекомендация, высокое качество доказательств.
Однако оптимальные сроки приема слабительных еще не установлены.
2 ESGE рекомендует, чтобы SBCE выполнялась как амбулаторная процедура, если это возможно, поскольку показатели завершенности выше у амбулаторных пациентов, чем у стационарных.
Сильная рекомендация, доказательства среднего качества.
3 ESGE рекомендует пациентам с электрокардиостимуляторами безопасно проходить SBCE без особых мер предосторожности.
Сильная рекомендация, доказательства низкого качества.
4 ESGE предполагает, что SBCE также можно безопасно выполнять у пациентов с имплантируемыми кардиовертерами-дефибрилляторами и вспомогательными устройствами для левого желудочка.
Слабая рекомендация, низкое качество доказательств.
5 ESGE рекомендует допускать квалифицированных медсестер и обученных техников в качестве предварительных считывателей исследований капсульной эндоскопии, поскольку их компетентность в выявлении патологии аналогична компетенции считывателей с медицинской квалификацией. Однако ответственность за постановку диагноза должна лежать на лечащем враче.
Сильная рекомендация, доказательства среднего качества.
6 ESGE рекомендует наблюдение в случаях бессимптомной задержки капсулы.
Сильная рекомендация, доказательства среднего качества.
В тех случаях, когда показано извлечение капсулы, ESGE рекомендует использование аппаратной энтероскопии в качестве метода выбора.
Сильная рекомендация, доказательства среднего качества.
Аппаратная энтероскопия (DAE)
1 ESGE рекомендует проводить диагностическую ДАЭ в качестве амбулаторной процедуры у пациентов без существенных сопутствующих заболеваний; у пациентов с сопутствующими заболеваниями и/или находящихся на терапевтических процедурах рекомендуется пребывание в стационаре.
Сильная рекомендация, доказательства низкого качества
Выбор между различными настройками также зависит от протоколов седации.
Сильная рекомендация, доказательства низкого качества.
2 ESGE предполагает, что сознательная седация, глубокая седация и общая анестезия являются приемлемыми альтернативами: выбор между ними должен определяться сложностью процедуры, клиническими факторами и местными организационными протоколами.
Слабая рекомендация, низкое качество доказательств.
3 ESGE рекомендует, чтобы результаты предыдущих диагностических исследований определяли выбор пути введения.
Сильная рекомендация, доказательства среднего качества.
Если локализация поражения тонкой кишки неизвестна или неясна, ESGE рекомендует отдавать предпочтение антеградному доступу.
Сильная рекомендация, доказательства низкого качества.
В условиях массивного открытого кровотечения ESGE рекомендует первоначальный антеградный подход.
Сильная рекомендация, доказательства низкого качества.
4 ESGE рекомендует, чтобы для баллонной энтероскопии (т. е. однобаллонной энтероскопии [SBE] и двухбаллонной энтероскопии [DBE]) глубина введения тонкой кишки оценивалась путем подсчета чистого продвижения энтероскопа во время фазы введения, с подтверждением этой оценки при выводе.
Сильная рекомендация, доказательства низкого качества.
ESGE рекомендует при спиральной энтероскопии оценивать глубину введения во время извлечения.
Сильная рекомендация, доказательства среднего качества.
Поскольку расчетная глубина введения является лишь приблизительной оценкой, ESGE рекомендует наносить татуировку, чтобы отметить выявленное поражение и/или самую глубокую точку введения.
Сильная рекомендация, доказательства низкого качества.
5 ESGE рекомендует проводить все эндоскопические терапевтические процедуры во время DAE.
Сильная рекомендация, доказательства среднего качества.
Более того, при проведении терапевтических вмешательств необходимы дополнительные специфические меры безопасности для предотвращения осложнений.
Сильная рекомендация, высокое качество доказательств.
Этот технический обзор дополняет недавнее клиническое руководство Европейского общества гастроинтестинальной эндоскопии (ESGE) по капсульной эндоскопии тонкой кишки (SBCE) и аппаратной энтероскопии (DAE) для диагностики и лечения заболеваний тонкой кишки. Целью этого дополнительного технического обзора является обсуждение технических вопросов, связанных с использованием как SBCE, так и DAE, предоставление рекомендаций для клиницистов по оптимальному выполнению этих процедур в клинической практике.
ALICE: расширенный цветовой спектр изображения живого тела
APC: аргоноплазменная коагуляция
ASA: Американское общество анестезиологов
BAE: баллонная энтероскопия
BGE: эндоскопия с баллонным наведением
БИС: биспектральный
БМ: синий режим
ПЗС: устройство с зарядовой связью
CECDAI: Индекс активности болезни Крона при капсульной эндоскопии
КМОП: комплементарный полупроводник на основе оксида металла
СО 2 : двуокись углерода
КТ: компьютерная томография
DAE: аппаратная энтероскопия
ДБЭ: двухбаллонная энтероскопия
DPEJ: прямая чрескожная эндоскопическая еюностомия
EBD: эндоскопическая баллонная дилатация
ЭРХПГ: эндоскопическая ретроградная холангиопанкреатография
ESGE: Европейское общество желудочно-кишечной эндоскопии
FICE: гибкое улучшение цвета спектрального изображения
GRADE: классификация рекомендаций по оценке, разработке и оценке
ВЗК: воспалительное заболевание кишечника
ИКД: имплантируемый кардиовертер-дефибриллятор
Светодиод: светодиод
LVAD: вспомогательное устройство для левого желудочка
MAC: контролируемая анестезия
НПВП: нестероидный противовоспалительный препарат
ИЛИ: отношение шансов
ПЭГ: полиэтиленгликоль
РКИ: рандомизированное контролируемое исследование
ROC: рабочая характеристика приемника
SBCE: капсульная эндоскопия тонкой кишки
SBE: однобаллонная энтероскопия
SBFT: последующее обследование тонкой кишки
SPICE: Индекс гладкого выступающего поражения при капсульной эндоскопии
1. Введение и цель
Капсульная эндоскопия тонкой кишки (SBCE) и аппаратная энтероскопия (DAE) используются в клинической практике в западных странах с 2001 и 2005 гг. соответственно. Их комбинированное использование произвело революцию в подходе к исследованию и лечению патологии тонкой кишки, изменив хорошо зарекомендовавшие себя клинические модели (например, определение скрытого желудочно-кишечного кровотечения) [ 1 ] и приведя к разработке новых диагностических и терапевтических алгоритмов [ 1 ] . [ 2 ].
В 2015 году Европейское общество желудочно-кишечной эндоскопии (ESGE) выпустило Клинические рекомендации [ 2 ], в которых основное внимание уделялось роли SBCE и DAE в диагностике и лечении заболеваний тонкой кишки; технические и практические аспекты не обсуждались. Аналогичным образом, в других обзорах и руководствах [ 3 ] [ 4 ] [ 5 ] [ 6 ] [ 7 ] [ 8 ] технические вопросы, такие как график подготовки, протоколы чтения/отчетности, режимы седации и выбор пути введения ДАЭ (которые были показано влияние на диагностический и терапевтический эффект [ 9 ] [ 10 ]), рассматриваются лишь частично.
Чтобы дополнить Клинические рекомендации 2015 года, ESGE заказала и профинансировала этот всеобъемлющий технический обзор, основанный на фактических данных. Сама эндоскопическая техника уже была подробно описана в других источниках [ 3 ] [ 4 ] [ 5 ] [ 6 ] [ 7 ] [ 8 ] [ 11 ] [ 12 ]; поэтому в этом техническом обзоре основное внимание уделяется другим нерешенным техническим вопросам, связанным с SBCE и DAE, чтобы предоставить врачам рекомендации по оптимальному использованию этих технологий в клинической практике.
2. Методы
Определения процедуры, принятые в настоящем Техническом обзоре, соответствуют определениям Клинического руководства [ 2 ]. DAE включает двухбаллонную энтероскопию (DBE), однобаллонную энтероскопию (SBE), спиральную энтероскопию и баллонную эндоскопию (BGE). Доказательств, касающихся последнего метода, очень мало, поэтому настоящий Технический обзор сосредоточен на DBE, SBE и спиральной энтероскопии (DBE и SBE объединены в группу энтероскопии с использованием баллона [BAE]). Поскольку некоторые технические вопросы DAE полностью различаются у взрослых и детей [ 13 ] [ 14 ] [ 15 ], настоящий технический обзор посвящен ведению взрослых пациентов.
ESGE назначила координирующую группу (ER, CS и MP), которая сформировала две рабочие группы (одну для SBCE и одну для DAE) и определила двух руководителей групп (SA для SBCE и AM для DAE) ( Приложение e1 , см. только онлайн Дополнительный материал). Каждой рабочей группе было поручено ответить на ряд ключевых вопросов по конкретной теме ( Приложение e2 )., дополнительный онлайн-материал) и провел специальный систематический поиск литературы, включающий, как минимум, следующие ключевые слова: капсульная эндоскопия тонкой кишки, аппаратная энтероскопия, двухбаллонная энтероскопия, однобаллонная энтероскопия, спиральная энтероскопия, баллонная энтероскопия. вспомогательная энтероскопия, эндоскопия тонкой кишки, капсульная эндоскопия и энтероскопия, по мере необходимости. Все извлеченные статьи оценивались путем проверки заголовка, аннотации и полного текста. Систематический поиск литературы был проведен в июле 2016 г. Несистематический поиск литературы повторялся, при необходимости, до марта 2017 г. (эту дату следует учитывать для будущих обновлений).
Все отобранные статьи были ранжированы по уровню доказательности и силе рекомендации; заявления были предоставлены двумя рабочими группами в соответствии с системой оценки рекомендаций, разработки и оценки (GRADE) [ 16 ] [ 17 ]. Во время специальной встречи в октябре 2016 года заявления были представлены, обсуждены, изменены и, наконец, одобрены на основе консенсуса. Координационная группа подготовила рукопись, которая в конечном итоге была рассмотрена, изменена и одобрена руководителями рабочей группы. Документ был разослан всем членам ESGE на внутреннее рассмотрение в июле 2017 года. После учета их комментариев Совет управляющих ESGE одобрил его перед отправкой в Endoscopy для международной экспертной оценки.
Этот Технический обзор будет рассмотрен для рассмотрения в 2022 году или раньше, если появятся новые важные доказательства. Любые обновления в промежуточный период будут отмечены на веб-сайте ESGE: http://www.esge.com/esge-guidelines.html .
3. Положения и рекомендации по капсульной эндоскопии тонкой кишки (SBCE)
3.1 Имеющиеся в продаже устройства
Доступные устройства и их основные технологические характеристики перечислены в Таблице 1 в Приложении e3 (Дополнительный материал, доступный только онлайн).
3.2 Подготовка
ESGE рекомендует пациентам перед SBCE соблюдать модифицированную диету.
Сильная рекомендация, доказательства низкого качества.
ESGE рекомендует пациентам принимать слабительное (2 л полиэтиленгликоля [ПЭГ]) перед SBCE для лучшей визуализации.
Сильная рекомендация, высокое качество доказательств.
Оптимальное время для приема слабительных еще предстоит установить. Прокинетики не улучшают частоту завершения SBCE, и их рутинное введение не рекомендуется.
Сильная рекомендация, высокое качество доказательств.
ESGE рекомендует введение противовспенивающих средств перед приемом внутрь капсулы.
Сильная рекомендация, высокое качество доказательств.
Оптимальная подготовка пациента к SBCE была спорной. Компания Given Imaging (Yoqneam, Израиль), первый производитель капсульных эндоскопов, не рекомендовала применять слабительные перед процедурой для SBCE; единственными рекомендуемыми требованиями были диета с низким содержанием клетчатки за день до процедуры с прозрачными жидкостями только вечером и 12-часовое голодание. Действительно, этот протокол использовался в контролируемых исследованиях скрытых желудочно-кишечных кровотечений и подозреваемой или установленной болезни Крона. В 2007 г., после обзора ценности кишечного лаважа перед SBCE, в первом консенсусном документе экспертов по SBCE был сделан вывод: «текущие данные, в основном из полностью опубликованных статей, свидетельствуют о том, что ПЭГ-лаваж и симетикон положительно влияют на видимость слизистой оболочки и, возможно, также на диагностический результат» [4]. 18]. Восемь рандомизированных контролируемых исследований рассматривали вопрос о том, улучшают ли слабительные средства видимость слизистой оболочки, диагностическую ценность и скорость завершения лечения [ 12 ], [ 19 ], [ 20 ], [ 21 ], [ 22 ], [ 23 ], [ 24 ], [ 25 ]. На сегодняшний день четыре мета-анализа пришли к выводу, что прием 2 л раствора ПЭГ перед приемом внутрь капсул приводит к улучшению видимости слизистой оболочки тонкой кишки. Тем не менее, доказательства, касающиеся частоты завершения лечения и диагностического результата, все еще неубедительны, а оптимальные сроки для слабительного использования еще предстоит установить [ 26 ] [ 26].27 ] [ 28 ] [ 29 ].
Мета-анализ четырех рандомизированных контролируемых исследований (РКИ), оценивающих роль прокинетиков в SBCE, пришел к выводу, что использование прокинетиков само по себе неэффективно для увеличения показателей завершения SBCE [ 30 ]. И наоборот, пациенты с повышенным риском неполного исследования SBCE (например, у пациентов или пациентов с одним или несколькими из следующих состояний: предшествующая абдоминальная хирургия, замедленное опорожнение желудка, диабетическая невропатия, тяжелый гипотиреоз, прием психотропных препаратов и т. ) может помочь введение некоторых прокинетиков (метоклопрамид или домперидон), когда капсула остается в желудке более 30–60 минут, что подтверждается мониторингом в режиме реального времени [ 30 ]. В некоторых РКИ показано, что пеногасители улучшают качество визуализации слизистой оболочки.20 ] [ 31 ] [ 32 ] [ 33 ] и два мета-анализа пришли к выводу, что симетикон значительно уменьшает наличие пузырьков / пены в тонкой кишке [ 28 ] [ 34 ]. Оптимальная доза симетикона еще не определена и составляет от 80 до 200 мг [ 20 ] [ 31 ] [ 32 ] [ 33 ] [ 34 ].
3.3 Настройка
ESGE рекомендует, чтобы SBCE выполнялась как амбулаторная процедура, если это возможно, поскольку показатели завершения выше у амбулаторных пациентов, чем у стационарных.
Сильная рекомендация, доказательства среднего качества.
Имеющиеся в литературе данные подтверждают, что стационарное лечение чаще связано с незавершенной процедурой SBCE [ 35 ] [ 36 ]. Когортное исследование 334 последовательных пациентов, перенесших SBCE (264 амбулаторных и 70 стационарных процедур), было проанализировано ретроспективно [ 35 ]. Капсула не попала в тонкую кишку у 6 из 70 стационарных пациентов по сравнению с 8 из 264 амбулаторных пациентов ( р = 0,04). Капсула не достигала слепой кишки в 31,4 % стационарных исследований по сравнению с 9,5 % амбулаторных исследований ( P < 0,001). Среднее время транзита по желудку было увеличено у стационарных больных (98,5 мин) по сравнению с амбулаторными (60,4 мин, P = 0,008). Среди стационарных пациентов доля незавершенных обследований была выше в условиях отделения интенсивной терапии (7/13, 54 %), чем в условиях общей медицинской палаты (15/57, 26 %) ( P = 0,05). Хотя нет четких объяснений этим результатам, количество и тяжесть сопутствующих заболеваний, использование лекарств, которые могут повлиять на время прохождения по тонкой кишке, а также снижение физической активности стационарных пациентов были постулированы как потенциальные способствующие факторы. . В другом проспективном исследовании 76 пациентов, перенесших SBCE, были включены для оценки взаимосвязи физической активности с показателями завершения [ 37 ].]. Частота завершения SBCE составила 100 % (23/23) в амбулаторной группе, 85,7 % (30/35) в группе «мягкого постельного режима» и 72,2 % (13/18) в группе «строгого постельного режима». группа. Снижение физической активности было значительным фактором риска для неполного обследования SBCE (скорректированное отношение шансов [OR] 3,39) [ 37 ].
В некоторых клинических сценариях время SBCE является решающим вопросом. У пациентов с острым явным кровотечением клинические рекомендации [ 2 ] предлагают выполнять ЭКК как можно скорее после эпизода кровотечения (в идеале в течение 24–72 часов). При наличии клинических показаний обследование не следует откладывать только потому, что пациент находится в стационаре. В таких ситуациях, однако, следует ожидать более высокий уровень незавершенных обследований из-за длительного времени транзита у критически больных пациентов, которые, скорее всего, будут прикованы к постели; следовательно, все те методы, которые способствовали бы полному обследованию (см. раздел 3.4), должны быть реализованы.
3.4 Роль мониторинга в реальном времени
ESGE рекомендует использовать средство просмотра в реальном времени, особенно у пациентов с риском замедленного опорожнения желудка и у которых может наблюдаться задержка желудочной капсулы. В этих случаях наблюдатель в режиме реального времени может направить соответствующее вмешательство (введение прокинетического агента и/или доставку капсулы с помощью эндоскопа в двенадцатиперстную кишку) для оптимизации исследования SBCE.
Сильная рекомендация, доказательства низкого качества.
В настоящее время средства просмотра в реальном времени включены в несколько систем SBCE. Хотя неопубликованные данные по опыту сотен здоровых добровольцев показывают, что прохождение капсулы через желудок обычно происходит в течение 4 часов после приема капсулы (в 97 % – 100 %), у пациентов с риском замедленного опорожнения желудка может быть неудачное исследование SBCE из-за преходящая задержка капсулы в желудке. В эту подгруппу входят стационарные пациенты, пациенты с диабетической невропатией, тяжелым гипотиреозом или почечной недостаточностью и/или принимающие психотропные или наркотические препараты. Таким пациентам может быть полезно использование системы просмотра в реальном времени, чтобы направлять упреждающее вмешательство в случае задержки капсулы в желудке.
Проспективное исследование Hosono et al. [ 38 ] из Японии сравнили эффективность SBCE у 80 пациентов с просмотром в реальном времени или без него. В группе наблюдения в режиме реального времени вводили 10 мг метоклопрамида, а затем 500 мл ПЭГ, если капсула не прошла через желудок через 60 минут после приема. Уровень завершения в группе просмотра в реальном времени был значительно выше, чем в контрольной группе (90 % против 72,5 %). Шиотани и др. [ 39] недавно сравнили долю завершенных обследований и положительных результатов среди группы пациентов, обследованных до внедрения просмотра в реальном времени, и группы, в которой регулярно контролировалось прохождение капсулы через пищевод, желудок и тонкую кишку и принимались меры (например, введение воды или внутривенное введение метоклопрамида), если оно было отсрочено. Они обнаружили, что использование средства просмотра в реальном времени увеличило процент завершения SBCE с 66% до 86% ( P = 0,002). Огата и др. обнаружили, что средство просмотра в реальном времени было полезно для выявления пациентов с желудочным транзитом более 1 часа, и что пероральное введение 10 мг метоклопрамида было полезно в этих условиях [ 40 ].
3.5 Меры предосторожности, связанные с процедурами и особыми ситуациями
ESGE рекомендует пациентам голодать не менее 2 часов после приема капсул. Пациентам может быть разрешено пить прозрачные жидкости через 2 часа после приема капсулы и есть твердую пищу через 4 часа после приема капсулы.
Слабая рекомендация, доказательства очень низкого качества.
ESGE рекомендует пациентам с кардиостимулятором безопасно проходить SBCE без особых мер предосторожности.
Сильная рекомендация, доказательства низкого качества .
ESGE предполагает, что SBCE также можно безопасно выполнять у пациентов с имплантируемыми кардиовертерами-дефибрилляторами (ICD) и вспомогательными устройствами для левого желудочка (LVAD).
Слабая рекомендация, низкое качество доказательств.
Когда SBCE был введен в клиническую практику, производители рекомендовали пациентам пить воду через 2 часа после приема капсулы и принимать пищу через 4 часа после приема капсулы. В связи с отсутствием исследований, оценивающих влияние времени приема воды и/или пищи на качество изображения капсулы и/или время прохождения, в настоящее время мнение экспертов поддерживает соблюдение этого режима. Тем не менее, недавний опыт, в основном полученный в результате исследований, посвященных режимам подготовки к эндоскопии капсулы толстой кишки, позволяет предположить, что более ранний прием прозрачных жидкостей может улучшить качество обзора капсулы и двигательную активность.
3.5.2 Электромагнитные помехи другим устройствам
Технические характеристики капсул, которые используют радиочастоты для передачи данных, показывают, что максимальная мощность передачи обычно ниже допустимых пределов для кардиологических устройств [ 41 ] [ 42 ]. Следовательно, повреждение имплантированных сердечных устройств при SBCE маловероятно. Тем не менее, пользователи SBCE обеспокоены тем, что возможные помехи между капсулами и кардиологическими устройствами могут быть опасными для жизни пациентов. Таким образом, с момента введения SBCE несколько in vitro [ 43 ] [ 44 ] [ 45 ] и in vivo [ 45 ] [ 46 ] [ 47 ] [ 48 ]49 ][ 50 ] [ 51 ] [ 52 ] [ 53 ] [ 54 ] [ 55 ] [ 56 ] [ 57 ] [ 58 ] исследования проанализировали электромагнитные помехи между SBCE и имплантируемыми сердечными устройствами (например, кардиостимуляторами, имплантируемыми кардиовертерами-дефибрилляторами [ICDs]). ] и LVAD). Бандорски и др. [ 46] (данные 2010 г.) сообщили о ретроспективном исследовании 300 пациентов с кардиостимуляторами, перенесших SBCE, несмотря на формальные противопоказания, заявленные производителями; никаких нежелательных явлений не произошло. Впоследствии другие авторы исследовали потенциальное взаимодействие SBCE с кардиостимуляторами in vivo и подтвердили отсутствие клинически значимого вмешательства в любом случае [ 45 ], [ 46 ], [ 47 ], [ 48 ], [ 49 ], [ 50 ], [ 51 ], [ 52 ], [ 53 ]. ] [ 59 ].
В настоящее время имеется меньше данных о пациентах с SBCE с ИКД [ 45 ] [ 46 ] [ 48 ] [ 49 ] [ 55 ] [ 56 ] [ 57 ] [ 58 ] или LVAD [ 60 ] [ 61 ] [ 62 ] [ 63 ] [ 64 ] [ 65], в основном из-за относительной редкости клинических состояний, требующих их имплантации. Однако имеющиеся данные о безопасности SBCE у этой подгруппы пациентов кажутся обнадеживающими. Хотя Dubner et al. в исследовании in vitro [ 45 ] описали чрезмерную чувствительность ИКД и неадекватное проведение разряда, до сих пор в нескольких отчетах о случаях и сериях случаев (включающих в общей сложности более 100 пациентов) сообщалось, что у пациентов с ИКД. Точно так же в отчетах о случаях и сериях случаев, включающих в общей сложности около 90 пациентов с LVADs, перенесших SBCE [ 60 ] [ 61 ] [ 62 ] [ 63 ] [ 64 ] [ 65], никаких гемодинамических, электронных или механических отклонений или нарушений работы LVAD не наблюдалось, тогда как были описаны короткие помехи (потеря изображений) при получении изображения SBCE. Что касается капсул без радиочастотной передачи данных, то в одном исследовании, посвященном капсуле, которая использует человеческое тело для передачи данных (включая 3 пациентов с кардиостимуляторами и 3 пациентов с ИКД), не сообщалось о каких-либо помехах в любом направлении [ 66 ]; для капсул с бортовым хранением изображений без передачи невозможны помехи для кардиологических устройств [ 41 ].
В свете всех этих данных наличие имплантированных кардиологических устройств больше не должно рассматриваться как противопоказание для СБКЭ, если оно клинически показано. Во время записи SBCE пациентам с имплантированными кардиологическими устройствами следует избегать мест, содержащих инструменты/устройства, генерирующие сильные электромагнитные поля (например, кардиологических отделений, использующих телеметрический мониторинг, рентгенологических отделений и т. д.), поскольку они могут мешать записи данных капсулы [ 46 ] [ 49 ] [ 52 ]. Таким образом, систематический телеметрический мониторинг не рекомендуется у пациентов с имплантированными кардиостимуляторами, которым проводится SBCE; если необходим кардиомониторинг во время SBCE, следует использовать проводные системы [ 41 ].
Недавно сообщалось о помехах между капсульной эндоскопией и патч-помпой OmniPod второго поколения, которая использует ту же радиочастоту [ 67 ], тогда как мобильные телефоны, по-видимому, не мешают визуализации SBCE.
3.5.3 Беременность
Сообщалось лишь о нескольких случаях капсульной эндоскопии во время беременности [ 68 ] [ 69 ]. Хотя зарегистрированные случаи привели к благоприятным исходам для матери и плода, текущих данных недостаточно, чтобы давать какие-либо конкретные рекомендации. Специалисты предполагают, что в настоящее время капсульная эндоскопия считается противопоказанной при беременности, но может быть рассмотрена в случае жизнеугрожающих состояний, таких как массивное угрожающее жизни кровотечение, после всестороннего обсуждения с пациенткой и своевременного рассмотрение возможных рисков и преимуществ.
3.6 Меры предосторожности после процедуры
ESGE рекомендует выполнять обзорную рентгенографию брюшной полости пациентам с незавершенным исследованием капсулы (капсула не достигает толстой кишки или мешка стомы), если они не замечают выделения капсулы через 15 дней.
Сильная рекомендация, доказательства среднего качества.
Задержка капсулы произвольно определяется как идентификация эндоскопа капсулы на рентгенологическом изображении брюшной полости через ≥ 14 дней после приема капсулы [ 70 ]. Пациенты, перенесшие SBCE, должны быть проинструктированы о необходимости проверки на предмет выпячивания капсулы эндоскопа и сообщать о любых соответствующих симптомах, которые потенциально могут свидетельствовать о задержке капсулы. У бессимптомных пациентов, которые не замечают выделения капсулы в течение 2 недель после приема внутрь, как правило, следует выполнить рентгенографию брюшной полости, чтобы исключить задержку капсулы. Абдоминальной рентгенографии можно избежать, если запись капсулы подтверждает попадание в толстую кишку, поскольку риск задержки капсулы у этих пациентов кажется незначительным [ 70 ] [ 71 ].
Относительно ведения пациентов с задержкой капсулы см. раздел 3.10.
3.7 Капсульные эндоскопические ридеры
ESGE рекомендует допускать квалифицированных медсестер и обученных техников в качестве предварительных считывателей исследований капсульной эндоскопии, поскольку их компетентность в выявлении патологии аналогична компетенции считывателей с медицинской квалификацией. Однако ответственность за постановку диагноза должна лежать на лечащем враче.
Сильная рекомендация, доказательства среднего качества.
Имеющиеся данные подтверждают, что после соответствующей подготовки медсестры и/или другой технический персонал способны выявлять патологию так же, как и врачи [ 72 ] [ 73 ] [ 74 ] [ 75 ] [ 76 ]. Поэтому для врачей приемлемо полагаться на адекватно обученных и квалифицированных специалистов по предварительному чтению. Однако окончательная диагностическая ответственность и интерпретация результатов исследования капсулы в конкретном клиническом контексте должны оставаться за лечащим врачом.
3.8 Протоколы чтения капсульной эндоскопии тонкой кишки
ESGE рекомендует считывать записи SBCE с максимальной скоростью 10 кадров в секунду в режиме одиночного просмотра. Режимы двойного и множественного просмотра, если они доступны, с максимальной скоростью 20 кадров в секунду также являются жизнеспособными альтернативами.
Слабая рекомендация, низкое качество доказательств.
ESGE предлагает снизить частоту кадров до пороговых значений, рекомендованных выше, при оценке проксимального отдела тонкой кишки.
Сильная рекомендация, доказательства низкого качества.
ESGE предполагает, что автоматизированное программное обеспечение для быстрого чтения может использоваться при состояниях, затрагивающих диффузно слизистую оболочку тонкой кишки, но оно никогда не должно заменять обычное чтение.
Слабая рекомендация, доказательства среднего качества.
ESGE не рекомендует рутинное использование виртуальной хромоэндоскопии во время считывания записи капсулы, поскольку она, по-видимому, не улучшает обнаружение или характеристику поражения.
Сильная рекомендация, высокое качество доказательств.
Нет основанных на фактических данных рекомендаций относительно оптимальной частоты кадров для чтения записей SBCE. Однако, поскольку чтение SBCE является трудоемким процессом, было оценено несколько вариантов с целью экономии времени без ущерба для скорости обнаружения поражений. К ним относятся режим просмотра (автоматический или ручной), частота кадров (количество изображений, просматриваемых в секунду), однокадровые и многокадровые представления, а также автоматические приложения для просмотра. Автоматический режим, который устраняет похожие изображения, приводит к значительному сокращению времени считывания (до 50 %) с очень низким уровнем диагностических ошибок по сравнению с ручным режимом [ 77 ] [ 78 ].]. С другой стороны, влияние частоты кадров при просмотре на обнаружение повреждений неясно. В то время как некоторые авторы продемонстрировали низкую частоту диагностических ошибок независимо от частоты кадров при просмотре [ 77 ] [ 79 ], другие пришли к выводу, что увеличение частоты кадров при просмотре может привести к пропуску поражений [ 80 ] [ 81 ]. В большинстве исследований в качестве «эталонного стандарта» выбрана частота кадров при просмотре 10 кадров в секунду в режиме одиночного просмотра. Хотя прямые доказательства отсутствуют, в нескольких исследованиях сообщалось, что частота пропущенных поражений SBCE выше в проксимальном отделе тонкой кишки [ 82 ] [ 83 ] [ 84 ].]. Факторы, которые могут способствовать более высокой частоте пропущенных поражений в этой области, включают более быстрое продвижение капсулы через сегменты с острыми углами, а также наличие желчи и пены, которые могут затемнять слизистую оболочку. Таким образом, по мнению экспертов, при оценке проксимального отдела тонкой кишки следует уменьшать частоту кадров при просмотре [ 85 ] [ 86 ] [ 87 ] [ 88 ].]. Кроме того, другими факторами, потенциально влияющими на скорость просмотра, являются опыт читателя (опытный читатель может читать видео SBCE с более высокой частотой кадров по сравнению с новичком), скорость продвижения капсулы SBCE и качество подготовки тонкой кишки (если капсула проходит очень быстро или качество просмотра низкое, читатель должен уменьшить частоту кадров).
В четырех исследованиях оценивалось влияние многокадрового и однокадрового просмотра на время чтения и обнаружение повреждений [ 77 ], [ 79 ], [ 80 ], [ 81 ].]. Многокадровые режимы, по-видимому, экономят время без ущерба для обнаружения поражений (особенно для диффузной патологии, такой как обнаруженная при воспалительном заболевании кишечника [ВЗК]), по сравнению с однокадровым режимом просмотра. Большая часть доказательств, касающихся автоматических приложений для быстрого просмотра, получена из исследований, связанных с режимом QuickView, автоматическим режимом быстрого чтения, доступным в программном обеспечении Rapid (Medtronic, Дублин, Ирландия). Хотя было продемонстрировано, что это определенно экономит время, это потенциальное преимущество компенсируется неприемлемой частотой пропущенных поражений, варьирующейся от 6,5% до 12% [ 78 ] [ 89 ] [ 90 ].]. Большинство пропущенных поражений были одиночными изолированными поражениями (такими как полипы, сосудистые или изолированные воспалительные поражения). Несмотря на этот недостаток, он все еще может играть роль при состояниях, связанных с диффузной патологией тонкой кишки, такой как ВЗК. На самом деле согласие между автоматическим быстрым чтением и обычным просмотром было выше, когда показанием к процедуре было подозрение на ВЗК.
В свете того факта, что в настоящее время изображения, полученные в SBCE, не имеют высокого разрешения, потенциальные роли любого инструмента улучшения изображения заключаются в следующем: (а) повысить скорость обнаружения клинически значимых поражений; (b) для более точной характеристики/определения наблюдаемых поражений; и/или (c) предоставить новую систему классификации поражений, чтобы повлиять на результаты лечения пациентов (например, для выявления тех поражений, которые требуют лечения) [ 91 ]. В 2005 г. была разработана гибкая технология улучшения цвета спектральной визуализации (FICE) (Fujifilm, Сайтама, Япония) как новый тип эндоскопии с усилением изображения [ 92 ].]; он также был дополнен модальностью «синий режим» («BM»). Эта система теперь встроена в программное обеспечение для быстрого чтения. Другое программное обеспечение (например, расширенное улучшение цветового спектра изображения живого тела [ALICE]) также доступно и встроено в другие платформы капсульной эндоскопии (MiroView; Intromedic, Сеул, Корея) [ 93 ]. Большинство доказательств в литературе относится к клинической достоверности FICE при капсульной эндоскопии. В нескольких исследованиях оценивалась роль капсульной эндоскопии с усилением изображения в улучшении характеристики (то есть визуализации и/или очерчивания) поражений [ 94 ], [ 95 ], [ 96 ], [ 97 ], [ 98 ], [ 99 ].] [ 100 ] [ 101 ]. Влияние FICE на частоту обнаружения повреждений было тщательно оценено [ 94 ] [ 95 ] [ 96 ] [ 97 ] [ 98 ] [ 99 ] [ 102 ] [ 103 ] [ 104 ] [ 105 ] [ 106 ] [ 107 ] [ 108 ]. ] [ 109]. В недавнем метаанализе объединенных результатов 13 исследований (10 были посвящены обнаружению поражений и 3 — определению контуров поражений) была изучена возможная роль различных параметров FICE. Авторы отдельно оценили три доступных параметра FICE для каждого подтипа поражения тонкой кишки (сосудистое, воспалительное и протрузионное). Интересно, что в этом мета-анализе все три метода FICE не показали каких-либо значительных улучшений ни в обнаружении, ни в определении границ любого подтипа поражения тонкой кишки [ 110 ].
Модальность «синего режима», отдельно или в сочетании с FICE, также была исследована [ 98 ] [ 99 ] [ 100 ] [ 101 ] [ 102 ] [ 104 ] [ 109 ] [ 111 ], и результаты для этой дополнительной модальности неоднородны. . Недавние исследования не показали каких-либо преимуществ синего режима по сравнению с обычной капсульной эндоскопией с белым светом при очерчивании поражений тонкой кишки [ 104 ]. Что касается обнаружения повреждений [ 94 ] [ 102 ] [ 103 ] [ 104 ] [108 ] [ 112 ], в одном исследовании было показано, что синий режим улучшает скорость обнаружения [ 109 ], в то время как в другом исследовании не наблюдалось никакой разницы в скорости обнаружения [ 104 ]. Что касается ALICE, немногочисленные доступные данные не позволяют давать рекомендации.
3.9 Отчетность
ESGE признает, что данных о том, какую информацию следует включать в отчет SBCE, недостаточно. ESGE предлагает использовать стандартизированные баллы, когда это применимо, для описания соответствующих результатов. О местонахождении поражения также следует сообщать с помощью соответствующего индекса времени прохождения.
Слабая рекомендация, низкое качество доказательств.
Существует мало доказательств, на которых можно основывать рекомендации о том, что следует включить в отчет SBCE. Однако существует четкая информация, которая должна быть включена в каждый отчет об эндоскопии (т. е. имя пациента, демографические и контактные данные, данные направления, показания к процедуре, краткая история предыдущих исследований и соответствующие медицинские данные). Отчет SBCE также должен включать: (а) данные, относящиеся к процедуре (некоторые из которых предоставляются соответствующим проприетарным программным обеспечением, т. е. время прохождения по желудку, время прохождения по тонкой кишке и общее время регистрации); (b) использованная подготовка кишечника, если таковая имеется; (c) качество подготовки кишечника (возможно, оцениваемое с использованием опубликованной оценочной шкалы [ 113] даже если, как в настоящее время, отсутствуют надежные проверенные весы, а компьютерные автоматизированные системы все еще находятся в стадии оценки); (d) завершение/объем экзамена; (e) клинические данные; и f) совет.
Учитывая внутренние ограничения SBCE, отчет должен включать (если применимо):
· предполагаемый размер поражения и предполагаемое местоположение;
· объективное сообщение о любых визуализируемых воспалительных изменениях с помощью шкалы Льюиса или индекса активности болезни Крона при капсульной эндоскопии (CECDAI) [ 114 ] [ 115 ], в зависимости от обстоятельств;
· точное описание с помощью индекса гладких выступающих поражений при капсульной эндоскопии (SPICE) и/или шкалы Shyung [ 116 ] [ 117 ] (для выступающих поражений, которые могут представлять новообразования или безобидные выпячивания слизистой оболочки); а также
· клиническая значимость результатов (т. е. прогнозируемая значимость наблюдаемых поражений, особенно при подозрении на тонкокишечное кровотечение) [ 118 ].
Оценка местоположения поражения, основанная на индексе времени прохождения (например, время от привратника до поражения, деленное на время от привратника до илеоцекального клапана [ 119 ]), всегда должна быть включена для каждого идентифицированного поражения в чтобы облегчить выбор соответствующего доступа для последующей процедуры DAE (т. е. антеградный или ретроградный путь) [ 119 ] [ 120]; см. также раздел 4.5). Стандартизированные баллы вместе с предполагаемой локализацией поражения помогают сократить отчет SBCE, что позволяет избежать длинных, произвольных и иногда двусмысленных описаний. Тем не менее, читатель должен резюмировать результаты в ясной и клинически значимой форме, которая позволит лечащему врачу спланировать будущее терапевтическое/диагностическое лечение пациента.
3.10 Частота осложнений и профилактика осложнений (см. также раздел 3.11: Использование капсулы проходимости)
ESGE рекомендует наблюдение в случаях бессимптомной задержки капсулы.
Сильная рекомендация, доказательства среднего качества.
При наличии клинических показаний (например, у пациентов с ВЗК) следует рассмотреть возможность целенаправленного лечения стероидами для облегчения выведения капсул из организма.
Сильная рекомендация, доказательства низкого качества.
В случаях, когда показано извлечение капсулы, ESGE рекомендует использовать аппаратную энтероскопию (DAE) в качестве метода выбора. При наличии клинических показаний или при неэффективности ЭПР показано хирургическое вмешательство для извлечения капсулы и/или лечения основного заболевания
Сильная рекомендация, доказательства среднего качества.
ESGE рекомендует использовать эндоскопическую установку капсулы у пациентов с подозрением или установленным необструктивным расстройством глотания, чтобы предотвратить аспирацию капсулы.
Сильная рекомендация, доказательства низкого качества.
Хорошо известно, что определенные основные состояния предрасполагают к задержке капсулы. Недавно опубликованный мета-анализ показал, что показатель ретенции капсулы составил 2,1 % у пациентов с подозрением на тонкокишечное кровотечение (95 % ДИ 1,5–2,8 %) и 2,2 % (95 % ДИ 0,9–5,0 %) у пациентов, которым проводилась оценка из-за болей в животе и/или диареи. Частота удержания пациентов с подозрением на ВЗК составила 3,6% (95% ДИ 1,7–8,6%), а у пациентов с установленным ВЗК — 8,2% (95% ДИ 6,0–11,0%) [ 121 ]. Задержка капсулы обычно протекает бессимптомно [ 122 ] [ 123 ], и капсула может оставаться в тонкой кишке без каких-либо симптомов в течение нескольких месяцев или даже выводиться естественным путем при последующем наблюдении [ 122 ].] [ 123 ] [ 124 ] [ 125 ] [ 126 ] [ 127 ] [ 128 ] [ 129 ] [ 130 ] [ 131 ] [ 132 ] [ 133 ] [ 134 ]. В недавнем исследовании только 2 из 104 задержек капсулы (1,9%) развились в симптоматическую кишечную непроходимость [ 121 ] [ 123 ].]. Таким образом, если нет сильного подозрения на злокачественное новообразование, консервативное наблюдение является оправданным терапевтическим вариантом лечения задержки капсулы в большинстве случаев. В течение этого периода целевое лечение лекарствами (в том числе кортикостероидами по мере необходимости) может способствовать экскреции капсулы у 20–30 % пациентов с задержкой капсулы [ 119 ] [ 128 ] [ 129 ].
Когда требуется извлечение капсулы, и DAE, и операция кажутся жизнеспособными альтернативами. В ранних исследованиях капсул хирургия была методом выбора даже в бессимптомных случаях [ 123 , 128 , 130 , 131 , 132 , 133 ] . В современной практике растущая доступность DAE снизила потребность в хирургическом вмешательстве. Если капсула остается в тонкой кишке и раннее хирургическое лечение не требуется, DAE оказалась чрезвычайно эффективной (90–100 % случаев) для извлечения капсулы [ 135 ] [ 136 ] [ 137 ].]. Тем не менее хирургическое вмешательство остается первым выбором во всех случаях, когда исследования однозначно указывают на наличие опухолевого заболевания. В этих случаях операция в первую очередь направлена на лечение заболевания тонкой кишки, одновременно позволяя извлечь капсулу.
Другие осложнения, о которых сообщалось в литературе, такие как перфорация кишечника и распад капсулы, носят эпизодический характер и были опубликованы только в виде сообщений о клинических случаях [ 123 ] [ 124 ] [ 125 ] [ 126 ]. Возможные осложнения, которые постулировались во время введения капсульной эндоскопии в клиническую практику (например, удержание капсул в дивертикулах тощей или толстой кишки, взаимодействие с кардиостимуляторами и т. д.), оказались очень редкими и/или не имели клинически значимых последствий [ 138 ] . . И наоборот, аспирация капсулы стала потенциально серьезным, хотя и нечастым побочным эффектом [ 139 ].]. В недавнем систематическом обзоре литературы сообщается, что общая частота аспирации составляет 0,1% [ 140 ]. Хотя было показано, что капсульная эндоскопия безопасна у пожилых пациентов, большинство капсульных трахеобронхиальных аспираций (около 90 %) было зарегистрировано у этой подгруппы пациентов [ 134 ] [ 138 ] [ 139 ] [ 140 ].]. Недиагностированные до сих пор бесшумные расстройства глотания могут быть основной причиной этих находок. Поэтому перед введением капсул настоятельно рекомендуется собрать полный анамнез; особое внимание следует уделять выявлению потенциальной дисфункции глотания у пациентов пожилого возраста. В ситуации, когда у пациента есть нарушения или трудности с глотанием, врач должен эндоскопически ввести капсулу в двенадцатиперстную кишку (предпочтительно с помощью специального эндоскопического устройства для доставки капсулы или, если оно недоступно, с помощью других принадлежностей, таких как сетка Roth). Было продемонстрировано, что такие методы осуществимы и безопасны [ 141 ], [ 142 ], [ 143 ].
3.11 Использование капсулы проходимости
ESGE рекомендует собирать полный медицинский анамнез (например, предшествующие абдоминальные операции, принимаемые лекарства, отпускаемые по рецепту и без рецепта, обструктивные симптомы и т. д.) у всех пациентов, перенесших SBCE.
Сильная рекомендация, доказательства низкого качества.
ESGE не рекомендует предлагать процедуру капсульной эндоскопии без разбора всем пациентам, которым проводится капсульная эндоскопия.
Сильная рекомендация, доказательства низкого качества.
ESGE рекомендует предлагать процедуру с капсулой проходимости пациентам с повышенным риском задержки капсулы.
Сильная рекомендация, доказательства среднего качества.
Как отмечалось выше, общая частота задержки капсулы низкая и связана с клиническими показаниями [ 121 ]. Таким образом, рутинное использование техники, направленной на предотвращение ретенции капсулы, не является необходимым для каждого пациента, направленного на SBCE. Однако было показано, что наличие комбинации симптомов боли в животе, вздутия живота и тошноты/рвоты перед капсульной эндоскопией связано со значительно более высокой частотой удержания капсулы [ 122 ] [ 130 ] [ 144 ] [ 145 ].]. Кроме того, было показано, что резекция тонкой кишки в анамнезе, лучевая терапия органов брюшной полости/таза и длительное применение высоких доз нестероидных противовоспалительных препаратов (НПВП) повышают риск задержки капсулы [ 131 ] [ 132 ] [ 145 ] [ 146 ]. ] [ 147 ] [ 148 ]. Поэтому перед выполнением капсульной эндоскопии крайне важно тщательно изучить анамнез пациента, чтобы выявить те, которые требуют специального предварительного обследования, направленного на предотвращение ретенции капсулы.
В этих условиях динамическое обследование тонкой кишки (SBFT) и компьютерная томография (КТ) брюшной полости ненадежны, в то время как тестирование капсулы проходимости и специальные методы визуализации поперечного сечения тонкой кишки оказались эффективными [ 149 ]. Недавно опубликованный метаанализ (включая 5 исследований и 203 пациента) подтвердил точность капсульного теста проходимости с чувствительностью 97 % (95 % ДИ 93 % – 99 %), специфичностью 83 % (95 % ДИ 65 % – 94 %) и площадь под рабочей характеристикой приемника (ROC) 0,9557 [ 150]. К сожалению, исследования, сравнивающие тестирование проходимости капсулы и специальные методы визуализации поперечного сечения тонкой кишки у пациентов с повышенным риском задержки капсулы, ограничены, а результаты противоречивы. Ядав и др. показали существенную эквивалентность между использованием капсулы проходимости и специальными методами визуализации поперечного сечения [ 151 ], тогда как многоцентровое итальянское исследование показало, что показатель ретенции был значительно ниже (0,7%) у пациентов с высоким риском с отрицательными результатами капсулы проходимости, чем у тех, кто с отрицательными результатами специальной предшествующей визуализации поперечного сечения тонкой кишки (8,3 %) [ 152 ].]. Кроме того, процедура с капсулой проходимости не требует значительного воздействия ионизирующего излучения; он также удобен для пользователя и имеет очень высокую отрицательную прогностическую ценность. С другой стороны, сообщалось о некоторых случаях обструкции из-за проглатывания капсулы проходимости [ 153 ].
4. Положения и рекомендации по аппаратной энтероскопии (DAE)
4.1. Имеющиеся в продаже устройства
Имеющиеся в продаже энтероскопы и специальные наружные тубусы для DAE перечислены в таблице 2 (см. Приложение e3 , дополнительный материал, доступный только онлайн).
4.2 Подготовка
ESGE рекомендует 8-12-часовое голодание от твердой пищи, а также 4-6-часовое голодание от жидкостей перед процедурой для пациентов, перенесших антеградную ДАЭ. ESGE рекомендует оптимальную схему подготовки к колоноскопии для пациентов, перенесших ретроградную ДАЭ.
Сильная рекомендация, доказательства среднего качества.
Как и при других эндоскопических процедурах [ 154 ], качество подготовки кишечника и отсутствие остатка имеют первостепенное значение для обнаружения поражения при DAE. Кроме того, остатки пищи или фекалии могут помешать процедуре DAE из-за чрезмерного трения между энтероскопом и наружной трубкой.
Сравнительных исследований по подготовке к антеградному (пероральному) ДАЭ не проводилось. Более того, все авторы сообщают об аналогичном режиме, который основан на физиологии тонкой кишки [ 155 ] [ 156 ] [ 157 ]: обычно рекомендуется 8-12-часовое голодание с приемом твердой пищи и 4-6-часовое голодание с приемом жидкости. [ 158 ] [ 159 ] [ 160 ] [ 161 ]. Оптимальный режим подготовки к колоноскопии для ретроградного (перанального) ДАЭ [ 158 ] [ 159 ] [ 160 ] [ 161 ]] обычно рекомендуется. Его расписание отличается от учебы к учебе. Поскольку субоптимальное очищение толстой кишки может значительно замедлить прогрессирование ДАЭ и предотвратить интубацию илеоцекального клапана, ESGE рекомендует современный режим подготовки к колоноскопии [ 162 ] [ 163 ].
При наличии основного клинического состояния, которое может увеличить риск образования просвета в просвете (например, в контексте стеноза тонкой кишки или симптомов обструкции), следует рассмотреть более продолжительное голодание и использование подготовки кишечника даже у пациентов, перенесших антеградную терапию. ДАЭ. В этих случаях оптимальный график подготовки следует выбирать в каждом конкретном случае с учетом нескольких факторов, таких как сроки проведения процедуры, клинические показания, режим седации, предполагаемое расположение поражения, путь введения энтероскопа и т. д. -объемное кровотечение должно выполняться антеградным путем (см. также раздел 4.5) [ 164 ] [ 165 ], и в этом контексте также следует следовать вышеупомянутым рекомендациям для плановой антеградной ДАЭ.
4.3 Настройка
ESGE рекомендует выполнять диагностическую ДАЭ в качестве амбулаторной процедуры у пациентов без существенных сопутствующих заболеваний; у пациентов с сопутствующими заболеваниями и/или находящихся на терапевтических процедурах рекомендуется пребывание в стационаре.
Сильная рекомендация, доказательства низкого качества.
Выбор между различными настройками также зависит от протоколов седации.
Сильная рекомендация, доказательства низкого качества.
Выбор между стационарным лечением и дневным стационаром в основном зависит от необходимости перипроцедурного клинического мониторинга. При повышенном риске нежелательных явлений обязателен тщательный клинический мониторинг. Опубликованные данные о побочных эффектах DAE в основном получены из исследований DBE. Общая частота осложнений, связанных с ДАЭ, составляет около 1% [ 166 ] [ 167 ] [ 168 ] [ 169 ] [ 170 ] [ 171 ] [ 172 ]. Частота осложнений диагностических процедур составляет до 0,8 % [ 166 ] [ 167 ] [ 168 ] [ 169 ].] [ 170 ] [ 171 ], в то время как терапевтические процедуры могут достигать 8 % [ 173 ] [ 174 ] [ 175 ]. Наиболее частыми осложнениями ДАЭ являются перфорация, кровотечение и панкреатит. Кровотечение и перфорация чаще связаны с терапевтическими вмешательствами, такими как полипэктомия (до 10 % при резекции крупных полипов единым блоком) [ 175 ] и расширение стриктур (до 8 %) [ 173 ].]. Сообщалось, что панкреатит возникает в 0,3 % процедур DAE (в подавляющем большинстве случаев во время антеградной DAE). Механизм острого панкреатита, связанного с DAE, возможно, связан с ишемическим/травматическим повреждением поджелудочной железы во время маневров «тяни-толкай» [ 171 ]. Было обнаружено, что острый панкреатит после DAE связан с продолжительностью процедуры и глубиной введения эндоскопа [ 176 ] [ 177 ] [ 178 ] [ 179 ] [ 180 ]. Риск панкреатита можно снизить с помощью осторожной, атравматичной техники, сводящей к минимуму механическую нагрузку и избегающей раздувания баллонов в проксимальном отделе двенадцатиперстной кишки [ 175 ].]. Другие превентивные меры освещены в разделе 4.10 настоящего документа.
Хотя, как подробно описано выше, осложнения, связанные с процедурой, были зарегистрированы у пациентов, которым проводилась эндоскопическая терапия с высоким риском (например, баллонная дилатация, резекция большого полипа и стентирование), тяжелые осложнения (например, перфорация) также были зарегистрированы у пациентов, получавших кровоостанавливающие методы лечения (например, аргоноплазменная коагуляция), которые обычно считаются эндоскопическими методами лечения с низким риском в других сегментах желудочно-кишечного тракта. Таким образом, для всех пациентов, подвергающихся терапевтическим процедурам, ESGE рекомендует длительное наблюдение за пациентом после процедуры; это лучше всего выполнять в стационарных условиях. Пациенты со значительными сопутствующими заболеваниями подвергаются более высокому риску нежелательных явлений (в основном осложнений, связанных с седацией; см. раздел 4.4), и, как правило, им также следует предлагать стационарное наблюдение после ДАЭ.
Было показано, что частота нежелательных явлений для различных типов ДАЭ одинакова [ 181 ] [ 182 ] [ 183 ] [ 184 ] [ 185 ] [ 186 ] [ 187 ] независимо от возраста пациентов [ 188 ] [ 189 ]. Таким образом, возраст пациента и тип используемого оборудования DAE не должны влиять на выбор настройки процедуры. Хотя частота острого панкреатита выше у пациентов, прошедших антеградное обследование [ 166 ] [ 167 ].], сам по себе другой путь введения (антеградный или ретроградный) не должен влиять на выбор настройки.
Эти рекомендации должны выполняться на местном уровне с учетом местных организационных моделей и политики возмещения расходов.
4.4 Седация
ESGE рекомендует адекватную и безопасную седацию при ДАЭ.
Сильная рекомендация, доказательства низкого качества.
ESGE предполагает, что сознательная седация, глубокая седация и общая анестезия являются приемлемыми альтернативами: выбор между ними должен определяться сложностью процедуры, клиническими факторами и местными организационными протоколами.
Слабая рекомендация, низкое качество доказательств.
Процедуры DAE длительны и требуют адекватного растяжения тонкой кишки для эффективной визуализации поражения и лечения. Кроме того, и энтероскоп, и наружную трубку необходимо неоднократно продвигать и извлекать в ходе процедуры; эта манипуляция с тонкой кишкой, ее брыжейкой и прилегающими внутренними органами может вызывать дискомфорт/боль. Это может повлиять на соблюдение пациентом режима лечения и общую эффективность процедуры. Кроме того, движение пациента во время DAE может сделать процедуру более сложной с технической точки зрения. Адекватная, безопасная седация во время DAE очень полезна. Тем не менее, безопасность седации должна оставаться первостепенной, поскольку осложнения, связанные с седацией, были зарегистрированы у 0,5% из 2245 пациентов, собранных в проспективной немецкой базе данных [ 168 ].
В литературе описан широкий спектр протоколов седации при ДАЭ, и все они признаны безопасными. Несколько крупных недавно опубликованных серий клинических случаев [ 190 ] [ 191 ] [ 192 ] [ 193 ] [ 194 ], включающих как ретроградные, так и антеградные процедуры, показали, что энтероскопия может безопасно выполняться под комбинированной седацией бензодиазепинов и опиатов, даже у пациентов с сопутствующими сопутствующими заболеваниями. -заболевания. Тем не менее, это в основном ретроспективные серии случаев, не сфокусированные на осложнениях, связанных с седацией. Поэтому, как недавно предполагалось [ 195], частота осложнений, связанных с седацией, может быть недооценена у пациентов, перенесших DAE с седацией в сознании.
Ретроспективное исследование Zubek et al. [ 196 ] показали, что у пациентов, перенесших DBE, общая анестезия с эндотрахеальной интубацией предотвращает риск аспирации и также может быть безопасно применена. При надлежащем обучении побочные эффекты, связанные с седацией, такие как гипотензия, десатурация и апноэ, могут быть быстро и эффективно устранены. В 2014 году Сети и соавт. [ 197 ] показали, что для пациентов, перенесших однобаллонную энтероскопию, контролируемая анестезия (MAC) без эндотрахеальной интубации безопасна; то же самое относится к проводимой медсестрой прерывистой глубокой седации пропофолом для расширенной эндоскопии (включая DBE) [ 198 ]. Недавно Кавано и соавт. [ 199] предложили новый режим седации для антеградных процедур DBE, основанный на контролируемой инфузионной анестезии пропофолом, плюс внутривенное болюсное введение пентазоцина при необходимости под биспектральным (BIS) мониторингом. В этом исследовании ни у одного пациента не было серьезных нежелательных явлений, а протокол седации был оценен как удовлетворительный всеми пациентами и 80 % эндоскопистов.
Насколько нам известно, существует только одно сравнительное исследование, посвященное седативному эффекту DAE [ 200 ]. В этой проспективной нерандомизированной серии случаев сравнивается седация в сознании под руководством гастроэнтеролога и медсестра (комбинация бензодиазепинов и опиатов) с седацией, проводимой анестезиологом (MAC или общая анестезия), у пациентов, перенесших спиральную энтероскопию. Не было выявлено никаких различий ни в процедурных результатах, ни в частоте осложнений, что побудило авторов отдать предпочтение использованию седации в сознании. Тем не менее, из-за отсутствия рандомизации (показатель Американского общества анестезиологов [ASA] [ 201 ], а также распространенность кишечных спаек различается между двумя группами), сделанные выводы остаются сомнительными.
К сожалению, имеется мало доступных данных о влиянии седации на успех DAE или расчетную глубину введения в тонкую кишку. Мурино и др. [ 202 ], анализируя факторы, влияющие на глубину введения во время DBE, показали, что это не было связано с типом используемой седации (седация в сознании или общая анестезия). Танака и др. [ 203 ] сообщили, что ретроградное DBE может быть эффективно выполнено под седацией в сознании, тогда как антеградный путь требует более глубокой седации. Интересно, что Сидху и др. подтвердили это наблюдение только у молодых пациентов (средний возраст 54 года, диапазон 18–70 лет), в то время как у пожилых пациентов, перенесших ДБЭ (средний возраст 77 лет, диапазон 70–83 лет), средние дозы седативных средств (бензодиазепинов и опиатов) были сопоставимы независимо от маршрута вставки [189 ]. Однако на сегодняшний день ни одно крупное рандомизированное проспективное исследование не оценивало успешность ДАЭ в зависимости от используемого типа седации/анестезии.
Несмотря на это ограничение, имеющиеся в настоящее время данные свидетельствуют о том, что режим седации, по-видимому, не приводит к различиям в глубине введения тонкой кишки и общих показателях успешности процедуры DAE. В настоящее время недостаточно данных, относящихся к различным методам ДАЭ или различным путям введения в зависимости от режима седации. Точно так же отсутствуют конкретные данные об удовлетворенности пациентов седацией или различными устройствами. Поэтому в настоящее время нельзя рекомендовать конкретный режим седации. Что касается других передовых эндоскопических процедур, выбор режима седации будет зависеть от связанных с пациентом и других клинических факторов (например, сопутствующих заболеваний, баллов по шкале ASA, текущей терапии и т. терапия и др.), а также по локальным организационным протоколам. Поэтому этот выбор часто включает в себя разных специалистов (например, гастроэнтерологов, анестезиологов, медсестер и т. д.) и может повлиять на несколько практических вопросов, таких как условия (процедура дневного стационара или стационарная процедура)
4.5 Выбор пути введения (антеградный или ретроградный)
ESGE рекомендует, чтобы результаты предыдущих диагностических исследований определяли выбор пути введения.
Сильная рекомендация, доказательства среднего качества.
Если локализация поражения тонкой кишки неизвестна или неясна, ESGE рекомендует отдавать предпочтение антеградному доступу.
Сильная рекомендация, доказательства низкого качества.
В условиях массивного открытого кровотечения ESGE рекомендует первоначальный антеградный подход.
Сильная рекомендация, доказательства низкого качества.
ESGE не рекомендует выполнять антеградную и ретроградную ЭПР в одном и том же сеансе.
Сильная рекомендация, доказательства низкого качества.
ДАЭ обычно предшествуют менее инвазивные исследования, такие как SBCE или специализированная визуализация поперечного сечения тонкой кишки (например, компьютерная томография или магнитно-резонансная энтерография или энтероклизис). Эти исследования могут позволить оценить локализацию поражения тонкой кишки и должны использоваться для определения пути введения ДАЭ.
В 2006 г. Гей и соавт. [ 204 ] провели исследование, в котором для определения маршрута введения DBE использовался индекс, основанный на времени прохождения SBCE. В этом исследовании ретроградная DBE выполнялась, если время прохождения капсулы от момента проглатывания до обнаружения поражения составляло > 75 % от общего времени от проглатывания до визуализации слепой кишки. Авторы обнаружили, что положительные и отрицательные прогностические значения этого индекса, основанного на времени прохождения SBCE, составили 94,7% и 96,7% соответственно. Следовательно, оказалось, что он надежно предсказывает правильный маршрут приближения DAE; только примерно в 12 % случаев потребовалась вторая ППД альтернативным путем.
Впоследствии Ли и соавт. предложил основанный на времени индекс местоположения, определяемый как время от привратника до поражения в процентах от времени от привратника до илеоцекального клапана [ 119 ]. В исследовании 60 пациентов, перенесших как SBCE, так и DAE, пороговое значение 60 % было очень точным при выборе пути введения DAE. Эти результаты были недавно подтверждены Mandaliya et al. [ 205 ].
В ретроспективном исследовании 250 процедур DAE, выполненных по нескольким клиническим показаниям, Sanaka et al. [ 206 ] продемонстрировали, что антеградный путь был связан с более высокой диагностической ценностью, чем ретроградный. Это также показали Akyuz et al. [ 207 ], которые обнаружили, что выявление значимой патологии тонкой кишки было выше при антеградном введении в подгруппе пациентов с тонкокишечным кровотечением. Это наблюдение, а именно то, что патологические поражения у пациентов с тонкокишечными кровотечениями чаще выявлялись в проксимальном отделе тонкой кишки, также было продемонстрировано в нескольких других исследованиях [ 161 ], [ 206 ], [ 207 ], [ 208 ].] [ 209 ] [ 210 ] [ 211 ]. Эти данные поддерживают метод антеградного доступа, когда предыдущие исследования до DAE не могут предоставить данные о локализации поражения, по крайней мере, у пациентов, направленных с подозрением на тонкокишечное кровотечение. Напротив, при болезни Крона или нейроэндокринных опухолях в первую очередь следует рассматривать ретроградный подход, учитывая склонность этих состояний к поражению дистальных отделов тонкой кишки [ 212 ] [ 213 ].
В условиях массивного явного желудочно-кишечного кровотечения антеградный путь обычно предпочтительнее как по техническим, так и по клиническим причинам. С технической точки зрения, если в этих условиях выполняется ретроградная ДАЭ, кровь и сгустки крови, стекающие по направлению к энтероскопу, ухудшают видимость и могут создавать дополнительные помехи из-за чрезмерного трения между энтероскопом и наружной трубкой; транспортировка крови и сгустков проксимально во время самой процедуры также может затруднить идентификацию действительного источника кровотечения. Кроме того, как упоминалось выше, было показано, что антеградный путь имеет более высокую диагностическую ценность в контексте тонкокишечного кровотечения [ 164 ] [ 170 ].
Когда целевое поражение не достигнуто, самую глубокую точку введения в тонкую кишку всегда следует маркировать подслизистой татуировкой. Затем можно попытаться выполнить еще один DAE, выполненный обратным путем, чтобы достичь целевого поражения или татуировки [ 168 ] [ 174 ] [ 214 ]. Ретроспективный анализ 290 процедур DBE, проведенный Teshima et al. [ 215] продемонстрировали увеличение глубины введения при ретроградном доступе, если это выполнялось в отдельном случае, а не сразу после антеградного введения, что означает, что достижение панэнтероскопии может быть более вероятным, если антеградный и ретроградный доступы выполняются в разные дни. Таким образом, комбинированный антеградный и ретроградный подходы во время одного и того же сеанса обычно не рекомендуются.
4.6 Оценка глубины введения
ESGE рекомендует, чтобы для баллонной энтероскопии (т. е. SBE и DBE) глубина введения тонкой кишки оценивалась путем подсчета чистого продвижения энтероскопа во время фазы введения с подтверждением этой оценки во время извлечения.
Сильная рекомендация, доказательства низкого качества.
ESGE рекомендует при спиральной энтероскопии оценивать глубину введения во время извлечения.
Сильная рекомендация, доказательства среднего качества.
Поскольку расчетная глубина введения является лишь приблизительной оценкой, ESGE рекомендует наносить татуировку, чтобы отметить выявленное поражение и/или самую глубокую точку введения.
Сильная рекомендация, доказательства низкого качества.
Метод измерения глубины введения был впервые описан для DBE [ 216 ] [ 217 ]. Во время процедуры DBE глубину введения энтероскопа в тонкую кишку следует оценивать путем записи в одну стандартную форму чистого продвижения эндоскопа для каждого маневра «тяни-толкай»; эти чистые оценки затем добавляются для получения общей оценочной глубины вставки. Первоначально этот метод был разработан с использованием модели животных ex vivo [ 216 ], а затем был протестирован на моделях свиней in vivo [ 218 ].]. В последнем исследовании глубина введения оценивалась во время введения и извлечения. Хотя обе эти оценки были аналогичны эталонному стандарту вскрытия, оценки, полученные на этапе введения, были более точными. Впоследствии были предложены два других альтернативных метода: один основан на подсчете складок во время отдергивания [ 219 ], а другой основан на измерении продвижения наружной трубки [ 220 ].]. Однако обе эти альтернативы имеют некоторые ограничения: первый метод трудно применим в клинической практике, тогда как второй основан на гипотезе о том, что 5 см продвижения наружной трубки неизменно соответствуют 40 см продвижения энтероскопа. К сожалению, тонкая кишка не всегда укладывается на наружную трубку одинаково, она не постоянно заполняется одним и тем же объемом инсуффляционного газа, и не все сегменты тонкой кишки могут быть растянуты одинаково. Более того, баллон с наружной трубкой может соскальзывать назад при наличии спаек или узких углов.
Поскольку все методы баллонной энтероскопии основаны на принципе «тяни-толкай», метод оценки глубины введения, предложенный для DBE, также применялся к SBE. Тем не менее, есть некоторые специфические проблемы, связанные с SBE, которые могут сделать оценку глубины вставки еще более сложной. Во время SBE угол наклона кончика энтероскопа, используемый для маневра натяжения [ 221 ], частично затрудняет обзор, и это может затруднить оценку глубины. Хотя это потенциальное ограничение может быть преодолено за счет использования аспирации вместо наклона кончика, соскальзывание тонкой кишки с кончика энтероскопа и/или наружной трубки во время отвода может затруднить оценку введения, особенно когда энтероскоп расположен глубоко в тонкой кишке. или в случаях технически сложной анатомии.
В отличие от BAE, при котором глубина введения оценивается поэтапно во время интубации, при спиральной энтероскопии глубина тонкой кишки оценивается при извлечении [ 222 ]; эндоскопист пытается оценить длину тонкой кишки, «освободившейся» от наружной трубки по мере ее постепенного извлечения.
Независимо от типа используемого DAE, энтероскописты должны пройти специальное обучение, в идеале с использованием специальных моделей тонкой кишки [ 222 ], а расчетная глубина введения должна быть задокументирована в одной структурированной стандартной форме [ 222 ]. Кроме того, следует иметь в виду, что глубина введения часто является лишь приблизительной оценкой и, даже если она надежна, не должна отменять требование маркировки на основе татуировки локализации поражения и/или самой глубокой точки введения.
В нескольких исследованиях сравнивались различные методы DAE, чтобы определить, какой из них способствует более обширной оценке тонкой кишки. К сожалению, большинство этих исследований являются ретроспективными, нерандомизированными, одноцентровыми и выполняются только опытными эндоскопистами. Из-за этих методологических ограничений в сочетании с субъективным характером оценки введения тонкой кишки эти исследования показали противоречивые результаты. Проведено три рандомизированных контролируемых исследования, сравнивающих ЭБЭ с ДБЭ [ 219 ] [ 223 ] [ 224 ]. Два из них [ 219 ] [ 223 ] сообщили о сопоставимой глубине введения, тогда как третий [ 224] показали, что DBE был связан с более глубокой вставкой. В свете этих несоответствий было проведено два метаанализа РКИ [ 225 ] [ 226 ]. Оба этих метаанализа показали, что DBE и SBE были сходны с точки зрения расчетной глубины введения, диагностической эффективности, терапевтической эффективности и осложнений. Этот результат соответствует предыдущему систематическому обзору по той же теме (который включал 68 исследований, в основном ретроспективных исследований и серий случаев) [ 227 ]. Когда антеградный DBE сравнивали со спиральной энтероскопией, два параллельных исследования [ 228 ] [ 229 ] последовательно показали, что DBE позволяет проводить более глубокое введение.
Полная энтероскопия также была предложена в качестве показателя для сравнения различных методов DAE. Хотя проспективные РКИ, сравнивающие DBE и SBE [ 214 ] [ 223 ] [ 224 ] [ 230 ], показали противоречивые результаты, оба недавно опубликованных метаанализа подтвердили, что общая частота энтероскопии была значительно выше для DBE по сравнению с SBE [ 225 ] . [ 226]. Тем не менее, хотя тотальная энтероскопия остается полезным достижением, диагностический и терапевтический эффект DBE и SBE остается одинаковым. Кроме того, хотя отрицательный результат полной энтероскопии тонкой кишки является клинически обнадеживающим, диагностика и терапия часто могут быть выполнены за один сеанс, а выполнение полной энтероскопии требуется лишь у меньшинства пациентов. Таким образом, в настоящее время DBE и SBE (два метода, для которых имеются существенные доказательства) одинаково подходят для рутинной клинической практики; меньше данных доступно для спиральной энтероскопии. Кроме того, проходят испытания новые энтероскопы (например, автоматический спиральный энтероскоп, новые прототипы DBE), которые могут увеличить наши возможности для осмотра всей тонкой кишки за один сеанс, сократить время операции,
Что ясно видно из всех текущих исследований, независимо от конкретной техники DAE, так это то, что как предполагаемая глубина введения, так и частота полной энтероскопии увеличиваются с опытом [ 4 ] [ 216 ] [ 231 ] [ 232 ] [ 233 ] [ 234 ]. Соответствующее обучение, а также большой объем процедур являются важными факторами для освоения DAE и обеспечения технического успеха и клинической эффективности.
4.7 Использование рентгеноскопии
ESGE предполагает, что рутинное использование рентгеноскопии не обязательно. Тем не менее, он может быть полезен в определенных обстоятельствах (например, во время обучения, у пациентов с измененной анатомией или у пациентов со стриктурами тонкой кишки и т. д.).
Слабая рекомендация, низкое качество доказательств.
Только в одном проспективном рандомизированном исследовании оценивалось влияние рутинного использования рентгеноскопии на антеградную ДБЭ [ 235 ]. В этом исследовании рентгеноскопический контроль не влиял на глубину введения или время процедуры. Однако следует иметь в виду, что в данном исследовании все процедуры выполнял высококвалифицированный эндоскопист, и этот факт мог оказать влияние на результат.
В больших ретроспективных сериях случаев рентгеноскопия в основном применялась по требованию, в зависимости от опыта эндоскописта и анатомии тонкой кишки пациента [ 234 ] [ 235 ]. Сообщается, что рентгеноскопия особенно полезна в начале кривой обучения и при наличии послеоперационных спаек [ 234 ] [ 236 ]. Хотя большинство исследований было выполнено с DBE, мы, по всей вероятности, можем распространить настоящие рекомендации по рентгеноскопии на SBE из-за сходства эндоскопической техники [ 221 ]. Что касается спиральной энтероскопии, то в настоящее время нет данных или исследований, посвященных этой конкретной теме.
В контексте подозрения на стриктуры тонкой кишки (например, у пациентов с болезнью Крона) рекомендуется использование рентгеноскопии, особенно для оценки сложности любого стеноза (например, длины, угла наклона и калибра) с использованием рентгенологического контраста. СМИ [ 237 ]. Использование рентгеноскопического контроля является обязательным для эффективного и безопасного расширения стриктур тонкой кишки (см. также раздел 4.10).
4.8 Использование углекислого газа для инсуффляции
ESGE рекомендует диоксид углерода (CO 2 ) для инсуффляции всем пациентам, перенесшим DAE.
Сильная рекомендация, высокое качество доказательств.
Процедуры DAE обычно занимают более 1 часа и требуют инсуффляции больших объемов газа [ 238 ]. В то время как инсуффляция с использованием воздуха может привести к значительному растяжению тонкой кишки во время и после процедуры, CO 2 быстро абсорбируется из желудочно-кишечного тракта и в результате приводит к меньшему растяжению. В нескольких РКИ оценивалось использование СО 2 в ДАЭ и его влияние на комфорт пациента и глубину введения [ 239 ] [ 240 ] [ 241 ] [ 242 ]. Систематический обзор с метаанализом Nishizawa et al. [ 243] недавно проанализировал 4 РКИ (2 по DBE и 2 по SBE; всего 461 пациент, 235 рандомизированных для прохождения энтероскопии с воздухом и 226 с инсуффляцией CO 2 ), целью которых было оценить влияние CO 2 на процедуры DAE. По сравнению с воздухом использование инсуффляции CO 2 значительно увеличивает глубину введения при антеградной энтероскопии, но не при ретроградном подходе. Использование инсуффляции CO 2 значительно уменьшило боль в животе после процедуры как при ретроградном, так и при антеградном DAE. Интересно, что Ленц и соавт. [ 241 ] сообщили, что в подгруппе пациентов с абдоминальной хирургией в анамнезе CO 2инсуффляция оказалась особенно полезной, так как глубина введения для антеградных процедур, выполняемых в этих случаях, была значительно больше при использовании CO 2 (на ~ 60 см глубже, чем при использовании воздуха в качестве инсуффляционного газа).
Различные исследования [ 9 ] [ 244 ] [ 245 ] [ 246 ] [ 247 ] [ 248 ] показали, что использование CO 2 безопасно даже во время длительных эндоскопических процедур (включая ДАЭ [ 9 ] [ 239 ] [ 240 ] [ 241 ]. ] [ 242 ] [ 243 ] [ 248 ]) и что стандартного мониторинга пациента достаточно для его использования.
Основываясь на результатах исследований колоноскопии с использованием воды [ 249 ] [ 250 ] [ 251 ], некоторые авторы недавно предложили использовать воду вместо CO 2 для расширения просвета при DAE. Лян и др. [ 252 ] недавно случайным образом распределили 110 последовательных пациентов для выполнения SBE со стандартной инсуффляцией CO 2 или методом водообмена. Они обнаружили, что метод водообмена улучшает показатели полной энтероскопии и глубину введения тонкой кишки во время СБЭ. Побочные эффекты водообменной энтероскопии были аналогичны тем, которые наблюдались при методе инсуффляции CO 2 . Эти предварительные результаты требуют дальнейших исследований.
4.9 Как оптимизировать оценку слизистой оболочки тонкой кишки
ESGE рекомендует осматривать слизистую оболочку тонкой кишки с адекватной инсуффляцией, предпочтительно во время фазы отмены.
Сильная рекомендация, доказательства низкого качества.
Нет исследований, сравнивающих частоту обнаружения поражений тонкой кишки при введении и извлечении энтероскопа. Минимальная инсуффляция во время фазы введения обеспечивает пликацию тонкой кишки на наружную трубку, что, в свою очередь, способствует более глубокому введению. Однако субоптимальное растяжение может затруднить идентификацию поражений слизистой оболочки, особенно когда они небольшие или расположены между нерастянутыми складками. Таким образом, слизистую оболочку тонкой кишки следует оценивать с адекватным растяжением просвета, главным образом, в фазе отмены.
Как и при других эндоскопических процедурах [ 253 ], эксперты предложили использовать специальный короткий прозрачный пластиковый колпачок (дистальное крепление) для улучшения визуализации небольших поражений за складками, а также для облегчения терапевтических процедур путем обнажения поражения [ 254 ]. ]. Дюфо и др. [ 255 ] недавно сообщили о серии случаев из 36 пациентов, у которых рутинное использование прозрачного колпачка позволило успешно провести терминальную интубацию подвздошной кишки во время ретроградной ТКЭ в 97 % случаев.
Мисра и др. [ 256 ] показали, что введение спазмолитика гиосцин-N-бутилбромида облегчает терминальную интубацию подвздошной кишки и визуализацию во время колоноскопии. Однако на сегодняшний день нет исследований, оценивающих влияние введения спазмолитиков на частоту выявления поражений ДАЭ.
4.10 Терапевтические маневры
ESGE рекомендует, чтобы при патологии тонкой кишки ДАЭ был предпочтительным вариантом для обследования и терапевтического вмешательства перед более инвазивными методами, если иное не показано клинически.
Сильная рекомендация, доказательства низкого качества.
ESGE рекомендует проводить все эндоскопические терапевтические процедуры во время DAE.
Сильная рекомендация, доказательства среднего качества.
ESGE рекомендует, чтобы при проведении терапевтических вмешательств были необходимы дополнительные специальные меры безопасности для предотвращения осложнений.
Сильная рекомендация, высокое качество доказательств.
ESGE предполагает, что эндоскопическую терапию во время DAE обычно следует проводить на этапе отмены процедуры.
Слабая рекомендация, низкое качество доказательств.
DAE облегчает все эндотерапевтические методы, включая гемостатическое лечение (с помощью аргоноплазменной коагуляции [APC], инъекционной терапии и установки клипсы), резекцию полиповидных образований, расширение стриктур, установку стента, извлечение инородных тел, прямое введение тощекишечных зондов для кормления. прямая чрескожная эндоскопическая еюностомия [DPEJ]) и эндоскопическая ретроградная холангиопанкреатография (ERCP) после операции на желудке [ 160 ] [ 161 ] [ 174 ] [ 217 ] [ 237 ] [ 257 ] [ 258 ] [ 259 ] [ 260 ] [ 261] [ 262 ] [ 263 ] [ 264 ] [ 265 ] [ 266 ] [ 267 ] [ 268 ] [ 269 ].
Учитывая положение поражений, выявленных и леченных с помощью ДАЭ (глубоко в тонкой кишке), хирургическое вмешательство было единственным жизнеспособным терапевтическим вариантом до того, как ДАЭ был введен в клиническую практику. Эндотерапия ДАЭ в настоящее время представляет собой безопасную и эффективную альтернативу обширному хирургическому вмешательству (см. также раздел 4.3) и часто представляет собой предпочтительный вариант лечения патологии тонкой кишки. Однако, особенно при работе с пациентами со сложными заболеваниями тонкой кишки, оценка вариантов лечения и планирование лечения являются совместными процессами: таких пациентов лучше всего лечить с помощью междисциплинарного подхода с участием различных медицинских работников, таких как гастроэнтерологи, радиологи, хирурги, анестезиологи, и патологоанатомов.
Однако терапевтические вмешательства во время DAE технически сложны, учитывая длинный (2 м) энтероскоп. Кроме того, терапия DAE часто осложняется атипичным образованием петель тонкой кишки и относительно нестабильным положением энтероскопа [ 270 ]. Кроме того, учитывая, что стенка тонкой кишки очень тонкая (всего до 3 мм в толщину) [ 271 ], следует быть особенно осторожным, чтобы избежать перфорации при применении эндотерапии в пределах тонкой кишки. Хотя нет опубликованных исследований, сравнивающих различные виды эндотерапии, эксперты рекомендуют соблюдать особые меры предосторожности при их проведении в тонкой кишке. Эти рекомендации по безопасности, в зависимости от терапевтического метода, следующие:
· АПК сосудистых поражений . Принимая во внимание как уменьшенную толщину стенки тонкой кишки, так и рекомендации производителей, следует использовать настройки низкой мощности; предварительное введение физиологического раствора в подслизистую оболочку перед применением АПК также следует проводить, особенно при больших (> 0,5–0,7 см) сосудистых поражениях.
· Эндоскопическая резекция поражений слизистой оболочки.Для снижения риска перфорации и кровотечения в основание ножки поражений на ножке можно ввести разведенный раствор адреналина в физиологическом растворе (1 на 100 000). Поражения на широком основании, а также большие поражения лучше всего удалять по частям после инъекции под слизистую оболочку. Однако из-за малого диаметра просвета тонкой кишки следует избегать введения большого объема лифтингового раствора. (Например, 1–2 мл на основание полипов на ножке или 5–10 мл на плоские образования обычно достаточно для обеспечения безопасной резекции, оставляя достаточно места для простого и эффективного размещения петли.) Для резекции гамартомных полипов на ножке. (например, при синдроме Пейтца-Егерса) ножку следует резецировать близко к головке полипа,272 ] [ 273 ].
· Расширение стриктур тонкой кишки. Перед эндоскопической баллонной дилатацией (EBD) необходимо провести тщательную оценку количества, местоположения, характеристик и длины стриктур с помощью специальной диагностической визуализации тонкой кишки [ 173 ] [ 266 ] [ 274 ] [ 275 ]. Короткие стриктуры (< 5 см) с большей вероятностью будут иметь благоприятный долгосрочный ответ, чем более длинные [ 173 ] [ 266 ] [ 276 ]. Активное воспаление, такое как глубокая язва в стриктуре, связано с более высоким риском перфорации и должно лечиться путем эскалации медикаментозной терапии, прежде чем будет пересмотрено решение о ДЭБ.173 ] [ 266 ] [ 274 ] [ 275 ] [ 276 ]. Другим фактором, который может увеличить риск перфорации, является острая ангуляция; поэтому прямые стриктуры считаются более подходящими для EBD [ 173 ] [ 266 ]. Сквозной подход с использованием системы дилатации с прозрачным баллоном в настоящее время является наиболее часто используемой техникой, связанной с благоприятными результатами [ 173 ] [ 266 ]. Общепризнанной практикой является постепенное надувание баллона водой под прямым эндоскопическим контролем до максимального диаметра 18–20 мм в течение 1–2 минут.173 ] [ 266 ]. Рентгеноскопия может дать дополнительную характеристику во время EBD, и ее использование настоятельно рекомендуется [ 173 ] [ 274 ] [ 275 ]. Долгосрочный успех может потребовать повторения EBD в отдельных случаях [ 266 ].
· Прямая чрескожная эндоскопическая еюностомия (DPEJ) с размещением питательного зонда. Подобно размещению чрескожной эндоскопической гастростомической трубки, адекватная трансиллюминация и пальцевое углубление являются предпосылками для безопасности и успеха [ 267 ]. Использование иглы 21-G «искатель» и ее закрепление петлей для фиксации положения петли тощей кишки во время введения троакара DPEJ также считается важной мерой безопасности [ 267 ].
Хотя нет опубликованных сравнительных исследований по этому вопросу, большинство экспертов рекомендуют проводить эндотерапию при отмене. Улучшенная визуализация поражений для терапии при отмене может быть достигнута путем частичного надувания баллона энтероскопа, поскольку это позволяет выпрямить и осторожно растянуть любые складчатые складки тонкой кишки. Небольшие одиночные поражения, такие как крошечные сосудистые поражения, которые может быть трудно снова обнаружить при отмене, лучше всего лечить на этапе введения энтероскопии.
4.11 Отчетность
В этом разделе перечислены конкретные данные, связанные с ДАЭ, которые должны быть включены в отчет об энтероскопии. Эти данные, показанные в Таблице 3 (см. Дополнительный материал, доступный только в Интернете, Приложение e3 ), не заменяют, а дополняют стандартный отчет об эндоскопии [ 277 ] [ 278 ] [ 279 ].
4.12 Частота осложнений и профилактика осложнений
Спектр и частота осложнений ДАЭ подробно обсуждаются в разделах 4.3 и 4.4. В этих разделах сообщается информация о профилактике осложнений. Осложнения, связанные с лечебными маневрами, и их предотвращение см. в разделе 4.10. Как и у пациентов, перенесших другие эндоскопические процедуры, перед ДАЭ следует тщательно и подробно собрать анамнез, уделяя особое внимание лекарственным препаратам (например, антиагрегантам и антикоагулянтам), которые потенциально могут увеличить риск кровотечения. Лечение пациентов, использующих такие препараты, должно осуществляться в соответствии со специальными рекомендациями [ 280 ], в которых диагностический ДАЭ и ДАЭ без полипэктомии рассматривается как процедура с низким риском.
4.13 Ведение пациента после осмотра
ESGE предполагает, что пациенты могут пить через 1 час и есть через 2 часа после диагностической энтероскопии. После терапевтических вмешательств ESGE предлагает более осторожный подход к пероральному приему, в зависимости от типа проведенной эндоскопической терапии и клинических обстоятельств.
Слабая рекомендация, доказательства очень низкого качества.
ESGE рекомендует не проводить рутинное тестирование уровней амилазы/липазы после процедур DAE.
Сильная рекомендация, доказательства низкого качества.
Нет исследований, специально посвященных постпроцедурному ведению пациентов; поэтому рекомендации в основном основаны на мнении экспертов. Пациентов, подвергающихся диагностическим процедурам, обычно лечат в дневном стационаре (см. также раздел 4.3); после удовлетворительного восстановления после седации пациентам можно разрешить пить через 1 час и есть легкую пищу через 2 часа после процедуры. Из-за повышенного риска потенциальных осложнений пациенты, подвергающиеся терапевтическому вмешательству, должны вести себя более осторожно, а точное время начала перорального приема должно определяться индивидуально для каждого пациента, в зависимости от конкретной проводимой эндоскопической терапии, клинических обстоятельств, продолжительности процедуры. и сопутствующие заболевания.
Острый панкреатит представляет собой тяжелое осложнение, связанное с процедурой, у пациентов, подвергающихся как диагностическому, так и терапевтическому DAE (см. также раздел 4.3). Раннее распознавание этого потенциального осложнения может повлиять на окончательный результат. Несколько исследований [ 175 ] [ 176 ] [ 177 ] [ 178 ] [ 179 ] [ 281 ] [ 282 ] [ 283 ] [ 284 ] [ 285 ]] показали, что, хотя повышение уровня амилазы и/или липазы может быть задокументировано в 30–40 % процедур DAE, острый панкреатит возникает только у 0,3 % пациентов. Следовательно, рутинное измерение этих ферментов после ДАЭ потенциально может привести к дальнейшим ненужным исследованиям, длительному клиническому наблюдению и, в конечном счете, к неоправданной трате ресурсов. ESGE рекомендует проверять уровни амилазы и/или липазы только в случаях сильной стойкой или рецидивирующей боли в животе после процедуры или по клиническим показаниям.
5. Обсуждение
Рекомендации ESGE представляют собой консенсус передового опыта, основанный на имеющихся данных на момент их написания. Однако появляющиеся технические и технологические инновации могут потребовать критической оценки этих заявлений в ближайшем будущем. Например, в области капсульной эндоскопии внедрение новых капсул с программным обеспечением, предназначенным для конкретных условий, может привести к значительным изменениям в клинической практике. Точно так же и для DAE, на момент написания, в ближайшее время ожидаются технологические инновации. В некоторых странах спиральные наружные трубки больше не доступны для покупки, и недавно был представлен новый прототип автоматизированного спирального энтероскопа, который может помочь сделать процедуру проще и быстрее.
Кроме того, несмотря на многочисленные статьи, касающиеся как SBCE, так и DAE, они часто характеризуются важными методологическими ограничениями: РКИ, сравнительных и крупных популяционных исследований немного. Поэтому предлагаемые утверждения часто основаны на мнении экспертов, а не на методологически надежных доказательствах.
В настоящем техническом обзоре мы не затрагивали вопросы, связанные с обучением. На самом деле уже есть конкретные документы на эту тему, устанавливающие пороги достижения компетентности [ 286 ] [ 287 ] [ 288]. Тем не менее, как часто упоминается в настоящем обзоре, мы хотели бы подчеркнуть первостепенную важность адекватного обучения, чтобы обеспечить пациентам безопасные и эффективные процедуры с оптимальным опытом и клиническим результатом. Кроме того, учитывая непрерывную технологическую эволюцию в этой области, мы также хотели бы подчеркнуть, что гастроэнтерологи, занимающиеся энтероскопией, будь то SBCE или DAE, должны не только соответствовать требованиям, которые предоставляют практику привилегии там, где они работают, но также должны участвовать в процессе энтероскопии. постоянное профессиональное развитие, особенно связанное с энтероскопией. Рекомендации ESGE предназначены для обучения и предоставления информации, которая может помочь гастроэнтерологам обеспечить оптимальный уход за пациентами. Однако предлагаемые утверждения могут не применяться ко всем обстоятельствам,
Отказ от ответственности
Правовая оговорка для Руководящих принципов ESGE [ 17 ] применяется к этому Руководству.
Конкурирующие интересы
С. Адлер получает гонорары за проведение семинаров по капсульной эндоскопии, спонсируемых компанией Medtronic. Э. Дж. Деспотт получил образовательные и туристические гранты, а также гонорары спикеров от Fujifilm, Aquilant, Diagmed и Medtronic (с 2007 г. по настоящее время); его отдел получил образовательные и туристические гранты, а также гонорары спикеров от Olympus (с 2012 г. по настоящее время). И. Фернандес-Уриен получал гонорары за консультационные услуги от Medtronic (с 2016 по 2017 год). А. Кулаузидис получает материальную поддержку для исследований от SynMed UK и IntroMedic (постоянно); его отдел получает материальную поддержку от Aquilant/OMOM (постоянно); он получил исследовательский грант от Given Imaging (с 2011 по 2012 год). А. Мэй получает гонорары спикеров от FALK и Fujifilm; ее отдел получает исследовательскую поддержку от Fujifilm (с 2014 по 2018 год), Olympus (с 2014 по 2018 год), и Interscope (с 2017 по 2019 год). С. Пантер получил спонсорскую поддержку от Diagmed и Given для участия в конференциях и образовательных мероприятиях (с 2005 г. по настоящее время); его отдел получил финансирование исследовательской стипендии от Aquilant и Fuji (с 2013 по 2015 год) и поддержку для покрытия расходов на инфраструктуру капсульного курса (с 2005 года по настоящее время); в настоящее время он является неоплачиваемым председателем группы пользователей капсульной эндоскопии в Великобритании. Г. Рахми проводит учебные курсы, организованные Medtronic, по капсуле для тонкой кишки (с 2017 по 2018 год). C. Spada получает вознаграждение за консультационные услуги от Medtronic. Отделение Дж. ван Хофта в настоящее время получает исследовательские гранты от Cook Medical, Boston Scientific, Olympus и Medtronic. Д. Домагк, К. Хассан, М. Пеннацио, М. Е. Риччони и Э. Рондонотти не имеют конкурирующих интересов. Panter получил спонсорскую поддержку от Diagmed и Given для участия в конференциях и образовательных мероприятиях (с 2005 г. по настоящее время); его отдел получил финансирование исследовательской стипендии от Aquilant и Fuji (с 2013 по 2015 год) и поддержку для покрытия расходов на инфраструктуру капсульного курса (с 2005 года по настоящее время); в настоящее время он является неоплачиваемым председателем группы пользователей капсульной эндоскопии в Великобритании. Г. Рахми проводит учебные курсы, организованные Medtronic, по капсуле для тонкой кишки (с 2017 по 2018 год). C. Spada получает вознаграждение за консультационные услуги от Medtronic. Отделение Дж. ван Хофта в настоящее время получает исследовательские гранты от Cook Medical, Boston Scientific, Olympus и Medtronic. Д. Домагк, К. Хассан, М. Пеннацио, М. Е. Риччони и Э. Рондонотти не имеют конкурирующих интересов. Panter получил спонсорскую поддержку от Diagmed и Given для участия в конференциях и образовательных мероприятиях (с 2005 г. по настоящее время); его отдел получил финансирование исследовательской стипендии от Aquilant и Fuji (с 2013 по 2015 год) и поддержку для покрытия расходов на инфраструктуру капсульного курса (с 2005 года по настоящее время); в настоящее время он является неоплачиваемым председателем группы пользователей капсульной эндоскопии в Великобритании. Г. Рахми проводит учебные курсы, организованные Medtronic, по капсуле для тонкой кишки (с 2017 по 2018 год). C. Spada получает вознаграждение за консультационные услуги от Medtronic. Отделение Дж. ван Хофта в настоящее время получает исследовательские гранты от Cook Medical, Boston Scientific, Olympus и Medtronic. Д. Домагк, К. Хассан, М. Пеннацио, М. Е. Риччони и Э. Рондонотти не имеют конкурирующих интересов. его отдел получил финансирование исследовательской стипендии от Aquilant и Fuji (с 2013 по 2015 год) и поддержку для покрытия расходов на инфраструктуру капсульного курса (с 2005 года по настоящее время); в настоящее время он является неоплачиваемым председателем группы пользователей капсульной эндоскопии в Великобритании. Г. Рахми проводит учебные курсы, организованные Medtronic, по капсуле для тонкой кишки (с 2017 по 2018 год). C. Spada получает вознаграждение за консультационные услуги от Medtronic. Отделение Дж. ван Хофта в настоящее время получает исследовательские гранты от Cook Medical, Boston Scientific, Olympus и Medtronic. Д. Домагк, К. Хассан, М. Пеннацио, М. Е. Риччони и Э. Рондонотти не имеют конкурирующих интересов. его отдел получил финансирование исследовательской стипендии от Aquilant и Fuji (с 2013 по 2015 год) и поддержку для покрытия расходов на инфраструктуру капсульного курса (с 2005 года по настоящее время); в настоящее время он является неоплачиваемым председателем группы пользователей капсульной эндоскопии в Великобритании. Г. Рахми проводит учебные курсы, организованные Medtronic, по капсуле для тонкой кишки (с 2017 по 2018 год). C. Spada получает вознаграждение за консультационные услуги от Medtronic. Отделение Дж. ван Хофта в настоящее время получает исследовательские гранты от Cook Medical, Boston Scientific, Olympus и Medtronic. Д. Домагк, К. Хассан, М. Пеннацио, М. Е. Риччони и Э. Рондонотти не имеют конкурирующих интересов. в настоящее время он является неоплачиваемым председателем группы пользователей капсульной эндоскопии в Великобритании. Г. Рахми проводит учебные курсы, организованные Medtronic, по капсуле для тонкой кишки (с 2017 по 2018 год). C. Spada получает вознаграждение за консультационные услуги от Medtronic. Отделение Дж. ван Хофта в настоящее время получает исследовательские гранты от Cook Medical, Boston Scientific, Olympus и Medtronic. Д. Домагк, К. Хассан, М. Пеннацио, М. Е. Риччони и Э. Рондонотти не имеют конкурирующих интересов. в настоящее время он является неоплачиваемым председателем группы пользователей капсульной эндоскопии в Великобритании. Г. Рахми проводит учебные курсы, организованные Medtronic, по капсуле для тонкой кишки (с 2017 по 2018 год). C. Spada получает вознаграждение за консультационные услуги от Medtronic. Отделение Дж. ван Хофта в настоящее время получает исследовательские гранты от Cook Medical, Boston Scientific, Olympus и Medtronic. Д. Домагк, К. Хассан, М. Пеннацио, М. Е. Риччони и Э. Рондонотти не имеют конкурирующих интересов.
Мы искренне благодарим всех авторов Клинических рекомендаций ESGE по видеокапсульной эндоскопии и аппаратной энтероскопии: Р. Элиакима, М. Койхеля, С. Дж. Малдера, Дж. Альберта, П. Балтеса, Ф. Барбаро, К. Селье, Дж. П. Чартона. , M. Delvaux, A. Klein, M. McAlindon, B. Rosa, G. Rowse, DS Sanders, JC Saurin, R. Sidhu, JM Dumonceau, C. Hassan и IM Gralnek. В процессе редактирования Клинического руководства они обсуждали и поднимали вопросы о технических проблемах капсульной эндоскопии и аппаратной энтероскопии. Поэтому настоящий Технический обзор в основном вдохновлен и основан на их работе.
Мы также благодарим Д. Юнга, А. Тортору, Р. Мармо и Э. Валчоу, которые внесли свой вклад в поиск литературы и процесс редактирования.
Мы также благодарим рецензентов, Дж. Плевриса и К. Триантафиллоу: статья была значительно улучшена благодаря их детальному и тщательному процессу редактирования.
Наконец, мы также благодарим Франсуазу Хайденрайх и Мартину Берц из Секретариата ESGE за их неоценимую помощь в решении всех логистических и организационных вопросов.
.
По теме:
- ЭКСПЕРТНЫЙ ОБРАЗОВАТЕЛЬНЫЙ СЕМИНАР «ENTEROPRO». КАПСУЛЬНАЯ ЭНДОСКОПИЯ
- РЕТРОГРАДНЫЙ ОСМОТР ТОЛСТОЙ КИШКИ С ПОМОЩЬЮ УПРАВЛЯЕМОЙ ЭНДОСКОПИЧЕСКОЙ КАПСУЛЫ
- ЮБИЛЕЙНЫЙ КОНГРЕСС «20 ЛЕТ НЕИНВАЗИВНОЙ ЭНДОСКОПИИ»
- ВИДЕОКАПСУЛЬНАЯ ЭНДОСКОПИЯ В ДИАГНОСТИКЕ МЕЛАНОМЫ ТОНКОЙ КИШКИ
- Сергей Собянин вручил премии Москвы в области медицины. Лечебно-диагностическая интестиноскопия – новые решения сложных клинических проблем
- МЕСТО ВИДЕОКАПСУЛЬНОЙ ЭНДОСКОПИИ В АЛГОРИТМЕ ДИАГНОСТИКИ БОЛЕЗНИ КРОНА ТОНКОЙ КИШКИ
- Кавернозная гемангиома тощей кишки как источник рецидивирующего кишечного кровотечения у ребёнка 11 лет
- Классификация по Саурин (Saurin) для оценки значимости поражений при капсульной эндоскопии для пациентов с подозрением на желудочно-кишечное кровотечение
Список литературы:
2 Pennazio M, Spada C, Eliakim R. et al. Small-bowel capsule endoscopy and device-assisted enteroscopy for diagnosis and treatment of small-bowel disorders: European Society of Gastrointestinal Endoscopy (ESGE) Clinical Guideline. Endoscopy 2015; 47: 352-376
3 Buscaglia JM, Okolo 3rd PI . Deep enteroscopy: training, indications, and the endoscopic technique. Gastrointest Endosc 2011; 73: 1023-1028
4 ASGE Technology Committee Chauhan SS, Manfredi MA. et al. Enteroscopy. Gastrointest Endosc 2015; 82: 975-990
5 Ladas SD, Triantafyllou K, Spada C. et al. European Society of Gastrointestinal Endoscopy (ESGE): recommendations (2009) on clinical use of video capsule endoscopy to investigate small-bowel, esophageal and colonic diseases. Endoscopy 2010; 42: 220-227
6 ASGE Technology Committee Wang A, Banerjee S. et al. Wireless capsule endoscopy. Gastrointest Endosc 2013; 78: 805-815
7 Yamamoto H, Ogata H, Matsumoto T. et al. Clinical practice guideline for enteroscopy. Dig Endosc 2017; 29: 519-546
8 Shim KN, Jeon SR, Jang HJ. et al. Quality indicators for small bowel capsule endoscopy. Clin Endosc 2017; 50: 148-160
9 Wang WL, Wu ZH, Sun Q. et al. Meta-analysis: the use of carbon dioxide insufflation vs. room air insufflation for gastrointestinal endoscopy. Aliment Pharmacol Ther 2012; 35: 1145-1154
10 ASGE Technology Committee Barth BA, Banerjee S. et al. Equipment for pediatric endoscopy. Gastrointest Endosc 2012; 76: 8-17
11 Mishkin DS, Chuttani R, Croffie J. et al. ASGE Technology Status Evaluation report: wireless capsule endoscopy. Gastrointest Endosc 2006; 63: 539-545
12 Viazis N, Sgouros S, Papaxoinis K. et al. Bowel preparation increases the diagnostic yield of capsule endoscopy: a prospective, randomized, controlled study. Gastrointest Endosc 2004; 60: 534-538
13 ASGE Standards of Practice Committee Lee KK, Anderson MA. et al. Modifications in endoscopic practice for pediatric patients. Gastrointest Endosc 2008; 67: 1-9
14 Friedlander JA, Liu QY, Sahn B. et al. NASPGHAN capsule endoscopy clinical report. J Pediatr Gastroenterol Nutr 2017; 64: 485-494
15 Arguelles-Arias F, Donat E, Fernandez-Urien I. et al. Guidelines for wireless capsule endoscopy in children and adolescents: a consensus document by the SEGHNP (Spanish Society for Pediatric Gastroenterology, Hepatology and Nutrition) and SEOD (Spanish Society for Digestive Disease. Rev Esp Enferm Dig 2015; 107: 714-731
16 Atkins D, Best D, Briss PA. et al. Grading quality of evidence and strength of recommendations. BMJ 2004; 328: 74541490
17 Dumonceau JM, Hassan C, Riphaus A. et al. European Society of Gastrointestinal Endoscopy (ESGE) Guideline Development Policy. Endoscopy 2012; 44: 626-629
18 Mergener K, Ponchon T, Gralnek I. et al. Literature review and recommendations for clinical application of small-bowel capsule endoscopy, based on a panel discussion by international experts. Consensus statements for small-bowel capsule endoscopy, 2006/2007. Endoscopy 2007; 39: 895-909
19 Van Tuyl SA, den Ouden H, Stolk MF. et al. Optimal preparation for video capsule endoscopy: a prospective, randomized, single-blind study. Endoscopy 2007; 39: 1037-1040
20 Wei W, Ge ZZ, Lu H. et al. Purgative bowel cleansing combined with simethicone improves capsule endoscopy imaging. Am J Gastroenterol 2008; 103: 77-82
21 Wi JH, Moon JS, Choi MG. et al. Bowel preparation for capsule endoscopy: a prospective randomized multicenter study. Gut Liver 2009; 3: 180-185
22 Pons Beltran V, Gonzalez Suarez B, Gonzalez Asanza C. et al. Evaluation of different bowel preparations for small bowel capsule endoscopy: a prospective, randomized, controlled study. Dig Dis Sci 2011; 56: 2900-2905
23 Lapalus MG, Ben Soussan E, Saurin JC. et al. Capsule endoscopy and bowel preparation with oral sodium phosphate: a prospective randomized controlled trial. Gastrointest Endosc 2008; 67: 1091-1096
24 Park SC, Keum B, Seo YS. et al. Effect of bowel preparation with polyethylene glycol on quality of capsule endoscopy. Dig Dis Sci 2011; 56: 1769-1775
25 Oliva S, Cucchiara S, Spada C. et al. Small bowel cleansing for capsule endoscopy in paediatric patients: a prospective randomized single-blind study. Dig Liver Dis 2014; 46: 51-55
26 Niv Y. Efficiency of bowel preparation for capsule endoscopy examination: a meta-analysis. World J Gastroenterol 2008; 14: 1313-1317
27 Rokkas T, Papaxoinis K, Triantafyllou K. et al. Does purgative preparation influence the diagnostic yield of small bowel video capsule endoscopy?: A meta-analysis. Am J Gastroenterol 2009; 104: 219-227
28 Kotwal VS, Attar BM, Gupta S. et al. Should bowel preparation, antifoaming agents, or prokinetics be used before video capsule endoscopy? A systematic review and meta-analysis. Eur J Gastroenterol Hepatol 2014; 26: 137-145
29 Wu S, Gao YJ, Ge ZZ. Optimal use of polyethylene glycol for preparation of small bowel video capsule endoscopy: a network meta-analysis. Curr Med Res Opin 2017; 33: 1149-1154
30 Koulaouzidis A, Giannakou A, Yung DE. et al. Do prokinetics influence the completion rate in small bowel capsule endoscopy? A systematic review and meta-analysis. Curr Med Res Opin 2013; 29: 1171-1185
31 Nouda S, Morita E, Murano M. et al. Usefulness of polyethylene glycol solution with imethylpolysiloxanes for bowel preparation before capsule endoscopy. J Gastroenterol Hepatol 2010; 25: 70-74
32 Fang YH, Chen CX, Zhang BL. Effect of small bowel preparation with simethicone on capsule endoscopy. J Zhejiang Univ Sci B 2009; 10: 46-51
33 Albert J, Gobel CM, Lesske J. et al. Simethicone for small bowel preparation for capsule endoscopy: a systematic, single-blinded, controlled study. Gastrointest Endosc 2004; 59: 487-491
34 Wu L, Cao Y, Liao C. et al. Systematic review and meta-analysis of randomized controlled trials of simethicone for gastrointestinal endoscopic visibility. Scand J Gastroenterol 2011; 46: 227-235
35 Yazici C, Losurdo J, Brown MD. et al. In-patient capsule endoscopy leads to frequent incomplete small bowel examinations. World J Gastroenterol 2012; 18: 5051-5057
36 Robinson CA, Jackson C, Condon D. et al. Impact of in-patient status and gender on small bowel capsule endoscopy findings. Gastrointest Endosc 2011; 74: 1061-1066
37 Shibuya T, Mori H, Takeda T. et al. The relationship between physical activity level and completion rate of small bowel examination in patients undergoing capsule endoscopy. Intern Med 2012; 51: 997-1001
38 Hosono K, Endo H, Sakai E. et al. Optimal approach for small bowel capsule endoscopy using polyethylene glycol and metoclopramide with the assistance of a real-time viewer. Digestion 2011; 84: 119-125
39 Shiotani A, Honda K, Kawakami M. et al. Use of an external real-time image viewer coupled with prespecified actions enhanced the complete examinations for capsule endoscopy. J Gastroenterol Hepatol 2011; 26: 1270-1274
40 Ogata H, Kumai K, Imaeda H. et al. Clinical impact of a newly developed capsule endoscope: usefulness of a real-time image viewer for gastric transit abnormality. J Gastroenterol 2008; 43: 186-192
41 Bandorski D, Kurniawan N, Baltes P. et al. Contraindications for video capsule endoscopy. World J Gastroenterol 2016; 22: 9898-9908
42 Bandorski D, Höltgen R, Stunder D. et al. Capsule endoscopy in patients with cardiac pacemakers, implantable cardioverter defibrillators and left heart assist devices. Ann Gastroenterol 2014; 27: 3-8
43 Bandorski D, Irnich W, Brück M. et al. Capsule endoscopy and cardiac pacemakers: investigation for possible interference. Endoscopy 2008; 40: 36-39
44 Bandorski D, Irnich W, Brück M. et al. Do endoscopy capsules interfere with implantable cardioverter-defibrillators?. Endoscopy 2009; 41: 457-461
45 Dubner S, Dubner Y, Rubio H. et al. Electromagnetic interference from wireless video-capsule endoscopy on implantable cardioverter-defibrillators. Pacing Clin Electrophysiol 2007; 30: 472-475
46 Bandorski D, Jakobs R, Bruck M. et al. Capsule endoscopy in patients with cardiac pacemakers and implantable cardioverter defibrillators: (re)evaluation of the current state in Germany, Austria, and Switzerland 2010. Gastroenterol Res Pract 2012; 2012: 717408
47 Payeras G, Piqueras J, Moreno VJ. et al. Effects of capsule endoscopy on cardiac pacemakers. Endoscopy 2005; 37: 1181-1185
48 Bandorski D, Diehl KL, Jaspersen D. Capsule endoscopy in patients with cardiac pacemakers: current situation in Germany. Z Gastroenterol 2005; 43: 715-718
49 Bandorski D, Lotterer E, Hartmann D. et al. Capsule endoscopy in patients with cardiac pacemakers and implantable cardioverter-defibrillators – a retrospective multicenter investigation. J Gastrointestin Liver Dis 2011; 20: 33-37
50 Dirks MH, Costea F, Seidman EG. Successful videocapsule endoscopy in patients with an abdominal cardiac pacemaker. Endoscopy 2008; 40: 73-75
51 Dubner S, Dubner Y, Gallino S. et al. Electromagnetic interference with implantable cardiac pacemakers by video capsule. Gastrointest Endosc 2005; 61: 250-254
52 Guyomar Y, Vandeville L, Heuls S. et al. Interference between pacemaker and video capsule endoscopy. Pacing Clin Electrophysiol 2004; 27: 1329-1330
53 Harris LA, Hansel SL, Rajan E. et al. Capsule endoscopy in patients with implantable electromedical devices is safe. Gastroenterol Res Pract 2013; 2013: 959234
54 Stanich PP, Kleinman B, Betkerur K. et al. Video capsule endoscopy is successful and effective in outpatients with implantable cardiac devices. Dig Endosc 2014; 26: 726-730
55 Leighton JA, Srivathsan K, Carey EJ. et al. Safety of wireless capsule endoscopy in patients with implantable cardiac defibrillators. Am J Gastroenterol 2005; 100: 1728-1731
56 Moneghini D, Lipari A, Missale G. et al. Lack of interference between small bowel capsule endoscopy and implantable cardiac defibrillators: an ‘in vivo’ electrophysiological study. United European Gastroenterol J 2016; 4: 216-220
57 Pelargonio G, Dello Russo A, Pace M. et al. Use of video capsule endoscopy in a patient with an implantable cardiac defibrillator. Europace 2006; 8: 1062-1063
58 Cuschieri JR, Osman MN, Wong RC. et al. Small bowel capsule endoscopy in patients with cardiac pacemakers and implantable cardioverter defibrillators: Outcome analysis using telemetry review. World J Gastrointest Endosc 2012; 4: 87-93
59 Leighton JA, Sharma VK, Srivathsan K. et al. Safety of capsule endoscopy in patients with pacemakers. Gastrointest Endosc 2004; 59: 567-569
60 Zikos TA, Pan J, Limketkai B. et al. Efficacy of video capsule endoscopy in the management of suspected small bowel bleeding in patients with continuous flow left ventricular assist devices. Gastroenterology Res 2017; 10: 280-287
61 Amornsawadwattana S, Nassif M, Raymer D. et al. Video capsule endoscopy in left ventricular assist device recipients with obscure gastrointestinal bleeding. World J Gastroenterol 2016; 22: 4559-4566
62 Elmunzer BJ, Padhya KT, Lewis JJ. et al. Endoscopic findings and clinical outcomes in ventricular assist device recipients with gastrointestinal bleeding. Dig Dis Sci 2011; 56: 3241-3246
63 Meyer MM, Young SD, Sun B. et al. Endoscopic evaluation and management of gastrointestinal bleeding in patients with ventricular assist devices. Gastroenterol Res Pract 2012; 2012: 630483
64 Hanson BJ, Koene RJ, Roy SS. et al. Safety and outcomes of capsule endoscopy in patients with left ventricular assist device: a single-center retrospective case series. J Cardiovasc Transl Res 2016; 9: 402-404
65 Truss WD, Weber F, Pamboukian SV. et al. Early implementation of video capsule enteroscopy in patients with left ventricular assist devices and obscure gastrointestinal bleeding. ASAIO J 2016; 62: 40-45
66 Chung JW, Hwang HJ, Chung MJ. et al. Safety of capsule endoscopy using human body communication in patients with cardiac devices. Dig Dis Sci 2012; 57: 1719-1723
67 Pitocco D, Rizzi A, Tortora A. et al. Possible radio interference between video capsule endoscopy and second-generation omnipod patch pump. Diabetes Technol Ther 2016; 18: 444-445
68 Hogan RB, Ahmad N, Hogan RB. et al. Video capsule endoscopy detection of jejunal carcinoid in life-threatening hemorrhage, first trimester pregnancy. Gastrointest Endosc 2007; 66: 205-207
69 Wax JR, Pinette MG, Cartin A. et al. Cavernous transformation of the portal vein complicating pregnancy. Obstet Gynecol 2006; 108: 782-784
70 Cave D, Legnani P, de Franchis R. et al. ICCE consensus for capsule retention. Endoscopy 2005; 37: 1065-1067
71 Sachdev MS, Leighton JA, Fleischer DE. et al. A prospective study of the utility of abdominal radiographs after capsule endoscopy for the diagnosis of capsule retention. Gastrointest Endosc 2007; 66: 894-900
72 Dokoutsidou H, Karagiannis S, Giannakoulopoulou E. et al. A study comparing an endoscopy nurse and an endoscopy physician in capsule endoscopy interpretation. Eur J Gastroenterol Hepatol 2011; 23: 166-170
73 Niv Y, Niv G. Capsule endoscopy examination – preliminary review by a nurse. Dig Dis Sci 2005; 50: 2121-2124
74 Bossa F, Cocomazzi G, Valvano MR. et al. Detection of abnormal lesions recorded by capsule endoscopy. A prospective study comparing endoscopist’s and nurse’s accuracy. Dig Liver Dis 2006; 38: 599-602
75 Levinthal GN, Burke CA, Santisi JM. The accuracy of an endoscopy nurse in interpreting capsule endoscopy. Am J Gastroenterol 2003; 98: 2669-2671
76 Sidhu R, Sanders DS, Kapur K. et al. Capsule endoscopy: is there a role for nurses as physician extenders?. Gastroenterol Nurs 2007; 30: 45-48
77 Kyriakos N, Karagiannis S, Galanis P. et al. Evaluation of four time-saving methods of reading capsule endoscopy videos. Eur J Gastroenterol Hepatol 2012; 24: 1276-1280
78 Hosoe N, Rey JF, Imaeda H. et al. Evaluations of capsule endoscopy software in reducing the reading time and the rate of false negatives by inexperienced endoscopists. Clin Res Hepatol Gastroenterol 2012; 36: 66-71
79 Günther U, Daum S, Zeitz M. et al. Capsule endoscopy: comparison of two different reading modes. Int J Colorectal Dis 2012; 27: 521-525
80 Nakamura M, Murino A, O’Rourke A. et al. A critical analysis of the effect of view mode and frame rate on reading time and lesion detection during capsule endoscopy. Dig Dis Sci 2015; 60: 1743-1747
81 Zheng Y, Hawkins L, Wolff J. et al. Detection of lesions during capsule endoscopy: physician performance is disappointing. Am J Gastroenterol 2012; 107: 554-560
82 Zagorowicz ES, Pietrzak AM, Wronska E. et al. Small bowel tumors detected and missed during capsule endoscopy: single center experience. World J Gastroenterol 2013; 19: 9043-9048
83 Lewis BS, Eisen GM, Friedman S. A pooled analysis to evaluate results of capsule endoscopy trials. Endoscopy 2005; 37: 960-965
84 Honda W, Ohmiya N, Hirooka Y. et al. Enteroscopic and radiologic diagnoses, treatment, and prognoses of small bowel tumors. Gastrointest Endosc 2012; 76: 344-354
85 Worsoe J, Fynne L, Gregersen T. et al. Gastric transit and small intestinal transit time and motility assessed by a magnet tracking system. BMC Gastroenterol 2011; 11: 145
86 Koulaouzidis A, Plevris JN. Detection of the ampulla of Vater in small bowel capsule endoscopy: experience with two different systems. J Dig Dis 2012; 13: 621-627
87 Selby WS, Prakoso E. The inability to visualize the ampulla of Vater is an inherent limitation of capsule endoscopy. Eur J Gastroenterol Hepatol 2011; 23: 101-103
88 Clarke JO, Giday SA, Magno P. et al. How good is capsule endoscopy for detection of periampullary lesions? Results of a tertiary-referral center. Gastrointest Endosc 2008; 68: 267-272
89 Saurin JC, Lapalus MG, Cholet F. et al. Can we shorten the small bowel capsule reading time with the “Quick-view” image detection system?. Dig Liver Dis 2012; 44: 477-481
90 Westerhof J, Koornstra JJ, Weersma RK. Can we reduce capsule endoscopy reading times?. Gastrointest Endosc 2009; 69: 497-502
91 Spada C, Hassan C, Costamagna G. Virtual chromoendoscopy: will it play a role in capsule endoscopy?. Dig Liver Dis 2011; 43: 927-928
92 Osawa H, Yamamoto H. Present and future status of flexible spectral imaging color enhancement and blue laser imaging technology. Dig Endosc 2014; 26: 105-115
93 Ryu CB, Song J, Lee MS. et al. Does capsule endoscopy with Alice improves visibility of small bowel lesions?. Gastrointest Endosc 2013; 77: AB466
94 Imagawa H, Oka S, Tanaka S. et al. Improved visibility of lesions of the small intestine via capsule endoscopy with computed virtual chromoendoscopy. Gastrointest Endosc 2011; 73: 299-306
95 Dias de Castro F, Magalhães J, Boal Carvalho P. et al. Improving diagnostic yield in obscure gastrointestinal bleeding – how virtual chromoendoscopy may be the answer. Eur J Gastroenterol Hepatol 2015; 27: 735-740
96 Duque G, Almeida N, Figueiredo P. et al. Virtual chromoendoscopy can be a useful software tool in capsule endoscopy. Rev Esp Enferm Dig 2012; 104: 231-236
97 Koulaouzidis A, Smirnidis A, Douglas S. et al. QuickView in small bowel capsule endoscopy is useful in certain clinical settings, but QuickView with Blue Mode is of no additional benefit. Eur J Gastroenterol Hepatol 2012; 24: 1099-1104
98 Nogales Rincon O, Merino Rodríguez B, González Asanza C. et al. Utility of capsule endoscopy with flexible spectral imaging color enhancement in the diagnosis of small bowel lesions. Gastroenterol Hepatol 2013; 36: 63-68
99 Sato Y, Sagawa T, Hirakawa M. et al. Clinical utility of capsule endoscopy with flexible spectral imaging color enhancement for diagnosis of small bowel lesions. Endosc Int Open 2014; 2: 80-87
100 Cotter J, Magalhaes J, de Castro FD. et al. Virtual chromoendoscopy in small bowel capsule endoscopy: new light or a cast of shadow?. World J Gastrointest Endosc 2014; 6: 359-365
101 Rimbas M, Negreanu L, Ciobanu L. et al. Is virtual chromoendoscopy useful in the evaluation of subtle ulcerative small bowel lesions detected by video capsule endoscopy?. Endosc Int Open 2015; 3: 615-620
102 Gupta T, Ibrahim M, Deviere J. et al. Evaluation of Fujinon intelligent chromo endoscopy-assisted capsule endoscopy in patients with obscure gastroenterology bleeding. World J Gastroenterol 2011; 17: 4590-4595
103 Matsumura T, Arai M, Sato T. et al. Efficacy of computed image modification of capsule endoscopy in patients with obscure gastrointestinal bleeding. World J Gastrointest Endosc 2012; 4: 421-428
104 Koulaouzidis A, Douglas S, Plevris JN. Blue mode does not offer any benefit over white light when calculating Lewis score in small bowel capsule endoscopy. World J Gastrointest Endosc 2012; 4: 33-37
105 Kobayashi Y, Watabe H, Yamada A. et al. Efficacy of flexible spectral imaging color enhancement on the detection of small intestinal diseases by capsule endoscopy. J Dig Dis 2012; 13: 614-620
106 Maeda M, Hiraishi H. Efficacy of video capsule endoscopy with flexible spectral imaging color enhancement at setting 3 for differential diagnosis of red spots in the small bowel. Dig Endosc 2014; 26: 228-231
107 Konishi M, Shibuya T, Mori H. et al. Usefulness of flexible spectral imaging color enhancement for the detection and diagnosis of small intestinal lesions found by capsule endoscopy. Scand J Gastroenterol 2014; 49: 501-505
108 Boal Carvalho P, Magalhães J, Dias de Castro F. et al. Virtual chromoendoscopy improves the diagnostic yield of small bowel capsule endoscopy in obscure gastrointestinal bleeding. Dig Liver Dis 2016; 48: 172-175
109 Abdelaal UM, Morita E, Nouda S. et al. Blue mode imaging may improve the detection and visualization of small bowel lesions: A capsule endoscopy study. Saudi J Gastroenterol 2015; 21: 418-422
110 Yung DE, Boal Carvalho P, Giannakou A. et al. Clinical validity of flexible spectral imaging color enhancement (FICE) in small bowel capsule endoscopy: a systematic review and meta-analysis. Endoscopy 2017; 49: 258-269
111 Krystallis C, Koulaouzidis A, Douglas S. et al. Chromoendoscopy in small bowel capsule endoscopy: Blue mode or Fuji Intelligent Colour Enhancement?. Dig Liver Dis 2011; 43: 953-957
112 Sakai E, Endo H, Kato S. et al. Capsule endoscopy with flexible spectral imaging color enhancement reduces the bile pigment effect and improves the detectability of small bowel lesions. BMC Gastroenterol 2012; 12: 83
113 Ponte A, Pinho R, Rodrigues A. et al. Review of small bowel cleansing scales in capsule endoscopy: a panoply of choices. World J Gastrointest Endosc 2016; 16: 600-609
114 Gralnek IM, de Franchis R, Seidman E. et al. Development of a capsule endoscopy scoring index for small bowel mucosal inflammatory change. Aliment Pharmacol Ther 2008; 27: 146-154
115 Niv Y, Ilani S, Levi Z. et al. Validation of the Capsule Endoscopy Crohn's Disease Activity Index (CECDAI or Niv score): a multicenter prospective study. Endoscopy 2012; 44: 21-26
116 Girelli CM, Porta P, Colombo E. et al. Development of a novel index to discriminate bulge from mass on small bowel capsule endoscopy. Gastrointest Endosc 2011; 74: 1067-1074
117 Shyung LR, Lin SC, Shih SC. et al. Proposed scoring system to determine small bowel mass lesions using capsule endoscopy. J Formos Med Assoc 2009; 108: 533-538
118 Saurin JC, Pioche M. Why should we systematically specify the clinical relevance of images observed at capsule endoscopy?. Endosc Int Open 2014; 2: 88-89
119 Li X, Chen H, Dai J. et al. Predictive role of capsule endoscopy on the insertion route of double-balloon enteroscopy. Endoscopy 2009; 41: 762-766
120 Delvaux M, Fassler I, Gay G. Clinical usefulness of the endoscopic video capsule as the initial intestinal investigation in patients with obscure digestive bleeding: validation of a diagnostic strategy based on the patient outcome after 12 months. Endoscopy 2004; 36: 1067-1073
121 Rezapour M, Amadi C, Gerson L. Retention associated with video capsule endoscopy: systematic review and meta-analysis. Gastrointest Endosc 2017; 85: 1157-1168.e2
122 Liao Z, Gao R, Xu C. et al. Indications and detection, completion and retention rates of small bowel capsule endoscopy: a systematic review. Gastrointest Endosc 2010; 71: 280-286
123 Fernandez-Urien I, Carretero C, González B. et al. Incidence, clinical outcomes, and therapeutic approaches of capsule endoscopy-related adverse events in a large study population. Rev Esp Enferm Dig 2015; 107: 745-752
124 Um S, Poblete H, Zavotsky J. Small bowel perforation caused by an impacted endocapsule. Endoscopy 2008; 40: 122-123
125 Skovsen AP, Burchart J, Burgdorf SK. Capsule endoscopy: a cause of late small bowel obstruction and perforation. Case Rep Surg 2013; 2013: 458108
126 Royall NA, Fiscina CD. Report of video-capsule endoscopy disruption producing episodic small bowel obstruction after prolonged retention. Int J Surg Case Rep 2014; 5: 1001-1004
127 Cheifetz AS, Lewis BS. Capsule endoscopy retention: is it a complication?. J Clin Gastroenterol 2006; 40: 688-691
128 Cheon JH, Kim YS, Lee IS. et al. Can we predict spontaneous capsule passage after retention? A nationwide study to evaluate the incidence and clinical outcomes of capsule retention. Endoscopy 2007; 39: 1046-1052
129 Vanfleteren L, van der Schaar P, Goedhard J. Ileus related to wireless capsule retention in suspected Crohn’s disease: emergency surgery obviated by early pharmacological treatment. Endoscopy 2009; 41: 134-135
130 Li F, Gurudu SR, De Petris G. et al. Retention of the capsule endoscope: a single-center experience of 1000 capsule endoscopy procedures. Gastrointest Endosc 2008; 68: 174-180
131 Rondonotti E, Herrerias JM, Pennazio M. et al. Complications, limitations and failures of capsule endoscopy: a review of 733 cases. Gastrointest Endosc 2005; 62: 712-716
132 Hoog CM, Bark LA, Arkani J. et al. Capsule retentions and incomplete capsule endoscopy examinations: an analysis of 2300 examinations. Gastroenterol Res Pract 2012; 2012: 518718
133 Sears DM, Avots-Avontins A, Culp K. et al. Frequency and clinical outcome of capsule retention during capsule endoscopy for GI bleeding of obscure origin. Gastrointest Endosc 2004; 60: 822-827
134 Harrington C, Rodgers C. The longest duration of retention of a video capsule. BMJ Case Rep 2014; DOI: 10.1136/bcr-2013-203241.
135 Van Weyenberg SJ, Van Turenhout ST, Bouma G. et al. Double-balloon endoscopy as the primary method for small bowel video capsule endoscope retrieval. Gastrointest Endosc 2010; 71: 535-541
136 Makipour K, Modiri AN, Ehrlich A. et al. Double balloon enteroscopy: effective and minimally invasive method for removal of retained video capsules. Dig Endosc 2014; 26: 646-649
137 Mitsui K, Fujimori S, Tanaka S. et al. Retrieval of retained capsule endoscopy at small bowel stricture by double-balloon endoscopy significantly decreases surgical treatment. J Clin Gastroenterol 2016; 50: 141-146
138 Koulaouzidis A, Rondonotti E, Karargyris A. Small bowel capsule endoscopy: a ten-point contemporary review. World J Gastroenterol 2013; 19: 3726-3746
139 Despott EJ, O'Rourke A, Anikin V. et al. Tracheal aspiration of capsule endoscopes: detection, management, and susceptibility. Dig Dis Sci 2012; 57: 1973-1974
140 Yung DE, Plevris JN, Koulaouzidis A. Short article: Aspiration of capsule endoscopes: a comprehensive review of the existing literature. Eur J Gastroenterol Hepatol 2017; 29: 428-434
141 Holden JP, Dureja P, Pfau PR. et al. Endoscopic placement of the small bowel video capsule by using a capsule endoscope delivery device. Gastrointest Endosc 2007; 65: 842-847
142 Almeida N, Figueiredo P, Lopes S. et al. Capsule endoscopy assisted by traditional upper endoscopy. Rev Esp Enferm Dig 2008; 100: 758-763
143 Carey EJ, Heigh RI, Fleischer DE. Endoscopic capsule endoscope delivery for patients with dysphagia, anatomical abnormalities, or gastroparesis. Gastrointest Endosc 2004; 59: 423-426
144 Rondonotti E, Soncini M, Girelli C. et al. Small bowel capsule endoscopy in clinical practice: a multicentre 7-years survey. Eur J Gastroenterol 2010; 22: 1380-1386
145 Postgate AJ, Burling D, Gupta A. et al. Safety, reliability and limitations of the given patency capsule in patients at risk of capsule retention: a 3-year technical review. Dig Dis Sci 2008; 53: 2732-2738
146 Al-Bawardy B, Locke G, Huprich JE. et al. Retained capsule endoscopy in a large tertiary care academic practice and radiologic predictors of retention. Inflamm Bowel Dis 2015; 21: 2158-2164
147 Signorelli C, Rondonotti E, Villa F. et al. Use of the Given Patency System for the screening of patients at high risk for capsule retention. Dig Liver Dis 2006; 38: 326-330
148 Du J, Pan D, Ma P. et al. The clinical characteristic and risk of capsule incomplete and retention in Crohn’s disease. Int J Clin Exp Med 2015; 5: 13482-90
149 Spada C, Spera G, Riccioni M. et al. A novel diagnostic tool for detecting functional patency of the small bowel: the Given patency capsule. Endoscopy 2005; 37: 793-800
150 Zhang W, Han ZL, Cheng Y. et al. Value of the patency capsule in pre-evaluation for capsule endoscopy in cases of intestinal obstruction. J Dig Dis 2014; 15: 345-351
151 Yadav A, Heigh RI, Hara AK. et al. Performance of the patency capsule compared with nonenteroclysis radiologic examinations in patients with known or suspected intestinal strictures. Gastrointest Endosc 2011; 74: 834-839
152 Rondonotti E, Soncini M, Girelli CM. et al. Short article: Negative small bowel cross-sectional imaging does not exclude capsule retention in high-risk patients. Eur J Gastroenterol Hepatol 2016; 28: 871-875
153 Kopylov U, Nemeth A, Cebrian A. et al. Symptomatic retention of the patency capsule: a multicenter real life case series. Endosc Int Open 2016; 4: 964-969
154 Chokshi RV, Hovis CE, Hollander T. et al. Prevalence of missed adenomas in patients with inadequate bowel preparation on screening colonoscopy. Gastrointest Endosc 2012; 75: 1197-1203
155 Phillips SF. Functions of the large bowel: an overview. Scand J Gastroenterol Suppl 1984; 93: 1-12
156 Spiller RC. Intestinal absorptive function. Gut 1994; 35: S5-S9
157 Volk N, Lacy B. Anatomy and physiology of the small bowel. Gastrointest Endosc Clin N Am 2017; 27: 1-13
158 Lin MC, Chen PJ, Shih YL. et al. Outcome and safety of anterograde and retrograde single-balloon enteroscopy: clinical experience at a tertiary medical center in Taiwan. PLoS One 2016; 11: e0161188
159 Lenz P, Roggel M, Domagk D. Double- vs. single-balloon enteroscopy: single center experience with emphasis on procedural performance. Int J Colorectal Dis 2013; 28: 1239-1246
160 May A, Nachbar L, Ell C. Double-balloon enteroscopy (push-and-pull enteroscopy) of the small bowel: feasibility and diagnostic and therapeutic yield in patients with suspected small bowel disease. Gastrointest Endosc 2005; 62: 62-70
161 Yamamoto H, Kita H, Sunada K. et al. Clinical outcomes of double-balloon endoscopy for the diagnosis and treatment of small-intestinal diseases. Clin Gastroenterol Hepatol 2004; 2: 1010-1016
162 Hassan C, Bretthauer M, Kaminski MF. et al. Bowel preparation for colonoscopy: European Society of Gastrointestinal Endoscopy (ESGE) guideline. Endoscopy 2013; 45: 142-150
163 Johnson DA, Barkun AN, Cohen LB. et al. Optimizing adequacy of bowel cleansing for colonoscopy: recommendations from the US multi-society task force on colorectal cancer. Gastroenterology 2014; 147: 903-924
164 Aniwan S, Viriyautsahakul V, Angsuwatcharakon P. et al. Comparison of urgent video capsule endoscopy and urgent double-balloon endoscopy in massive obscure gastrointestinal bleeding. Hepatogastroenterology 2014; 61: 1990-1994
165 Monkemuller K, Neumann H, Meyer F. et al. A retrospective analysis of emergency double-balloon enteroscopy for small-bowel bleeding. Endoscopy 2009; 41: 715-717
166 Mensink PB, Haringsma J, Kucharzik T. et al. Complications of double balloon enteroscopy: A multicenter survey. Endoscopy 2007; 39: 613-615
167 Gerson LB, Tokar J, Chiorean M. et al. Complications associated with double balloon enteroscopy at nine US centers. Clin. Gastroenterol Hepatol 2009; 7: 1177-1182
168 Möschler O, May A, Muller MK. et al. Complications in and performance of double-balloon enteroscopy (DBE): Results from a large prospective DBE database in Germany. Endoscopy 2011; 43: 484-489
169 Despott EJ, Murino A, Hughes S. et al. Second report of the UK multi-centre DBE registry: furthering the international DBE experience. Gastrointest Endosc 2011; 73: AB394
170 Rondonotti E, Sunada K, Yano T. et al. Double-balloon endoscopy in clinical practice: where are we now?. Dig Endosc 2012; 24: 209-219
171 Moeschler O, Mueller MK. Deep enteroscopy – indications, diagnostic yield and complications. World J Gastroenterol 2015; 21: 1385-1393
172 Cotton PB, Eisen GM, Aabakken L. et al. A lexicon for endoscopic adverse events: report of an ASGE workshop. Gastrointest Endosc 2010; 71: 446-454
173 Hirai F, Beppu T, Sou S. et al. Endoscopic balloon dilatation using double-balloon endoscopy is a useful and safe treatment for small intestinal strictures in Crohn’s disease. Dig Endosc 2010; 22: 200-204
174 Xin L, Liao Z, Jiang YP. et al. Indications, detectability, positive findings, total enteroscopy and complications of diagnostic double-balloon endoscopy: a systematic review of data over the first decade of use. Gastrointest Endosc 2011; 74: 563-570
175 Möschler O, May AD, Müller MK. et al. Complications in double-balloon-enteroscopy: results of the German DBE register. DBE-Studiengruppe Deutschland. Z Gastroenterol 2008; 46: 266-270
176 Teshima CW, Aktas H, Kuipers EJ. et al. Hyperamylasemia and pancreatitis following spiral enteroscopy. Can J Gastroenterol 2012; 26: 603-606
177 Zepeda-Gomez S, Barreto-Zuniga R. et al. Risk of hyperamylasemia and acute pancreatitis after double-balloon enteroscopy: a prospective study. Endoscopy 201 43: 766-770
178 Tsujikawa T, Bamba S, Inatomi O. et al. Factors affecting pancreatic hyperamylasemia in patients undergoing peroral single-balloon enteroscopy. Dig Endosc 2015; 27: 674-678
179 Kopacova M, Tacheci I, Rejchrt S. et al. Double balloon enteroscopy and acute pancreatitis. World J Gastroenterol 2010 21 16: 2331-2340
180 Pata C, Akyuz U, Rzin Y. et al. Post-procedure elevated amylase and lipase levels after double-balloon enteroscopy: relations with the double-balloon technique. Dig Dis Sci 2010; 55: 1982-1988
181 Judah JR, Draganov PV, Lam Y. et al. Spiral enteroscopy is safe and effective for an elderly United States population of patients with numerous comorbidities. Clin Gastroenterol Hepatol 2010; 8: 572-576
182 Akerman PA, Cantero D. Spiral enteroscopy and push enteroscopy. Gastrointest Endosc Clin N Am 2009; 19: 357-369
183 Chavalitdhamrong D, Adler DG, Draganov PV. Complications of enteroscopy: how to avoid them and manage them when they arise. Gastrointest Endosc Clin N Am 2015; 25: 83-95
184 Khashab MA, Lennon AM, Dunbar KB. et al. A comparative evaluation of single-balloon enteroscopy and spiral enteroscopy for patients with mid-gut disorders. Gastrointest Endosc 2010; 72: 766-772
185 Davis-Yadley AH, Lipka S, Rodriguez AC. et al. The safety and efficacy of single balloon enteroscopy in the elderly. Therap Adv Gastroenterol 2016; 9: 169-179
186 Manno M, Riccioni ME, Cannizzaro R. et al. Diagnostic and therapeutic yield of single balloon enteroscopy in patients with suspected small-bowel disease: results of the Italian multicentre study. Dig Liver Dis 2013; 45: 211-215
187 Shinozaki S, Yamamoto H, Yano T. et al. Long-term outcome of patients with obscure gastrointestinal bleeding investigated by double-balloon endoscopy. Clin Gastroenterol Hepatol 2010; 8: 151-158
188 Byeon J-S, Mann NK, Jamil LH. et al. Double balloon enteroscopy can be safely done in elderly patients with significant co-morbidities. J Gastroenterol Hepatol 2012; 27: 1831-1836
189 Sidhu R, Sanders DS. Double-balloon enteroscopy in the elderly with obscure gastrointestinal bleeding: safety and feasibility. Eur J Gastroenterol Hepatol 2013; 25: 1230-1234
190 Akarsu M, Akkaya Ozdinç S, Celtik A. et al. Diagnostic and therapeutic efficacy of double-balloon endoscopy in patients with small intestinal diseases: single-center experience in 513 procedures. Turk J Gastroenterol 2014; 25: 374-380
191 Lahat A, Nadler M, Simon C. et al. Double balloon enteroscopy: a 2 year experience. Isr Med Assoc J 2009; 11: 456-459
192 Disibeyaz S, Suna N, Kuzu UB. et al. Double balloon enteroscopy: A 7-year experience at a tertiary care Centre. Eur J Intern Med 2016; 33: 108-111
193 Choi DH, Jeon SR, Kim JO. et al. Double-balloon enteroscopy in elderly patients: is it safe and useful?. Intest Res 2014; 12: 313-319
194 Cazzato IA, Cammarota G, Nista EC. et al. Diagnostic and therapeutic impact of double-balloon enteroscopy (DBE) in a series of 100 patients with suspected small bowel diseases. Dig Liver Dis 2007; 39: 483-487
195 Yang DH. Questions about sedation protocols for double-balloon enteroscopy. Intest Res 2015; 13: 97-98
196 Zubek L, Szabo L, Lakatos PL. et al. Double balloon enteroscopy examinations in general anesthesia. World J Gastroenterol 2010; 16: 3418-3422
197 Sethi S, Thaker AM, Cohen J. et al. Monitored anesthesia care without endotracheal intubation is safe and efficacious for single-balloon enteroscopy. Dig Dis Sci 2014; 59: 2184-2190
198 Jensen JT, Hornslet P, Konge L. et al. High efficacy with deep nurse-administered propofol sedation for advanced gastroenterologic endoscopic procedures. Endosc Int Open 2016; 4: E107-E111
199 Kawano S, Okada H, Iwamuro M. et al. An effective and safe sedation technique combining target-controlled infusion pump with propofol, intravenous pentazocine, and bispectral index monitoring for peroral double-balloon endoscopy. Digestion 2015; 91: 112-116
200 Judah JR, Collins D, Gaidos JK. et al. Prospective evaluation of gastroenterologist-guided, nurse-administered standard sedation for spiral deep small bowel enteroscopy. Dig Dis Sci 2010; 55: 2584-2591
201 American Society of Anesthesiologists. ASA Physical Status Classification System. Available at: https://www.asahq.org/resources/clinical-information/asa-physical-status-classification-system Accessed March 2017
202 Murino A, Nakamura M, Despott EJ. et al. Factors associated with reduced insertion depth at double balloon enteroscopy: a retrospective, multivariate analysis. Dig Liver Dis 2014; 46: 956-958
203 Tanaka S, Mitsui K, Tatsuguchi A. et al. Current status of double balloon endoscopy–indications, insertion route, sedation, complications, technical matters. Gastrointest Endosc 2007; 66: S30-S33
204 Gay G, Delvaux M, Fassler I. Outcome of capsule endoscopy in determining indication and route for push-and-pull enteroscopy. Endoscopy 2006; 38: 49-58
205 Mandaliya R, Korenblit J, O’Hare B. et al. Spiral enteroscopy utilizing capsule location index for achieving high diagnostic and therapeutic yield. Diagn Ther Endosc 2015; 793516
206 Sanaka M, Navaneethan U, Kosuru B. et al. Antegrade is more effective than retrograde enteroscopy for evaluation and management of suspected small bowel disease. Clin Gastroenterol Hepatol 2012; 910-916
207 Akyuz U, Pata C, Kalayci M. et al. Route selection for double balloon enteroscopy in patients with obscure gastrointestinal bleeding: experience from a single center. Turk J Gastroenterol 2012; 23: 670-675
208 Kaufman D, Leslie G, Marya N. et al. Small intestinal angioectasia: characterization, risk factors, and rebleeding. J Clin Gastroenterol 2016; 51: 720-727
209 Plotkin E, Imaeda A. Small intestinal angioectasias are not randomly distributed in the small bowel and most may be reached by push enteroscopy. J Clin Gastroenterol 2016; 50: 561-565
210 Bollinger E, Raines D, Saitta P. Distribution of bleeding gastrointestinal angioectasias in Western population. World J Gastroenterol 2012; 18: 6235-6239
211 Jackson C, Strong R. Gastrointestinal angiodysplasia: diagnosis and management. Gastrointest Endosc Clin N Am 2017; 27: 51-62
212 Despott EJ, Fraser C. Small bowel endoscopy in inflammatory bowel disease. Best Pract Res Clin Gastroenterol 2012; 26: 279-291
213 Pape UF, Perren A, Niederle B. et al. ENETS consensus guidelines for the management of patients with neuroendocrine neoplasms from the jejuno-ileum and the appendix including goblet cell carcinomas. Neuroendocrinology 2012; 95: 135-156
214 Messer I, May A, Manner H. et al. Prospective, randomized, single-center trial comparing double-balloon enteroscopy and spiral enteroscopy in patients with suspected small bowel disorders. Gastrointest Endosc 2013; 77: 241-249
215 Teshima CW, Aktas H, van Buuren HR. et al. Retrograde double balloon enteroscopy: comparing performance of solely vs. combined same-day anterograde and retrograde procedure. Scand J Gastroenterol 2011; 36: 220-226
216 May A, Nachbar L, Schneider M. et al. Push-and-pull enteroscopy using the double-balloon technique: method of assessing depth of insertion and training of the enteroscopy. Endoscopy 2005; 37: 66-70
217 Zhong J, Ma T, Zhang C. et al. A retrospective study of the application on double-balloon enteroscopy in 378 patients with suspected small-bowel diseases. Endoscopy 2007; 39: 208-215
218 Lopez AO, Soria F, Perez Cuadrado E. et al. Validity of insertion depth measurement in double-balloon endoscopy. Endoscopy 2012; 44: 1045-1050
219 Efthymiou M, Desmond PV, Brown G. et al. SINGLE-01: a randomized, controlled trial comparing the efficacy and depth of insertion of single- and double-balloon enteroscopy by using a novel method to determine insertion depth. Gastrointest Endosc 2012; 76: 972-980
220 Li XB, Chen HM, Zhuang J. et al. A novel modality for the estimation of the enteroscope insertion depth during double-balloon enteroscopy. Gastrointest Endosc 2010; 72: 999-1005
221 Manno M, Barbera C, Bertani H. et al. Single balloon enteroscopy: technical aspects and clinical applications. World J Gastrointest Endosc 2012; 4: 28-32
222 Akerman P, Agrawal D, Cantero D. et al. Spiral enteroscopy with the new DSB overtube: a novel technique for deep peroral small bowel intubation. Endoscopy 2008; 40: 974-978
223 Domagk D, Mensink P, Aktas H. et al. Single- vs. double-balloon enteroscopy in small bowel diagnostics: a randomized multicenter trial. Endoscopy 2011; 43: 472-476
224 Takano N, Yamada A, Watabe H. et al. Single-balloon vs. double-balloon endoscopy for achieving total enteroscopy: a randomized, controlled trial. Gastrointest Endosc 2011; 73: 734-739
225 Wadhwa V, Sethi S, Tewani S. et al. A meta-analysis on efficacy and safety: single-balloon vs. double-balloon enteroscopy. Gastroenterol Rep 2015; 3: 148-155
226 Lipka S, Rabbanifard R, Kumar A. et al. Single vs. double balloon enteroscopy for small bowel diagnostics: a systematic review and meta-analysis. J Clin Gastroenterol 2015; 49: 177-184
227 Lenz P, Domagk D. Double- vs. single-balloon vs. spiral enteroscopy. Best Pract Res Clin Gastroenterol 2012; 26: 303-313
228 Despott EJ, Murino A, Bourikas L. et al. A prospective comparison of performance during back-to-back, anterograde manual spiral enteroscopy and double-balloon enteroscopy. Dig Liver Dis 2015; 47: 395-400
229 May A, Manner H, Aschmoneit I. et al. Prospective, cross-over, single-center trial comparing oral double-balloon enteroscopy and oral spiral enteroscopy in patients with suspected small bowel vascular malformations. Endoscopy 2011; 43: 477-483
230 May A, Farber M, Aschmoneit I. et al. Prospective multicenter trial comparing push-and-pull enteroscopy with the single- and double-balloon techniques in patients with small bowel disorders. Am J Gastroenterol 2010; 105: 575-581
231 May A. Double-balloon enteroscopy. Gastrointest Endosc Clin N Am 2017; 27: 113-122
232 Lenz P, Domagk D. Single-balloon enteroscopy. Gastrointest Endosc Clin N Am 27: 123-131
233 Tee HP, How SH, Kaffes AJ. Learning curve for double-balloon enteroscopy: findings from an analysis of 282 procedures. World J Gastrointest Endosc 2012; 4: 368-372
234 Mehdizadeh S, Ross A, Gerson L. et al. What is the learning curve associated with double-balloon enteroscopy? Technical details and early experience in 6 U.S. tertiary care centers. Gastrointest Endosc 2006; 64: 740-750
235 Manner H, May A, Pohl J. et al. The impact of fluoroscopy on the outcome of oral double-balloon enteroscopy: results of a randomized trial in 156 patients. Endoscopy 2010; 42: 820-826
236 Lo SK. Technical matters in double balloon enteroscopy. Gastrointest Endosc 2007; 66: S15-S18
237 May A, Nachbar L, Pohl J. et al. Endoscopic interventions in the small bowel using double-balloon enteroscopy: feasibility and limitations. Am J Gastroenterol 2007; 102: 527-535
238 ASGE Technology Committee, Lo SK, Fujii-Lau LL et al. The use of carbon dioxide in gastrointestinal endoscopy. Gastrointest Endosc 2016; 83: 857-865
239 Domagk D, Bretthauer M, Lenz P. et al. Carbon dioxide insufflation improves intubation depth in double-balloon enteroscopy: a randomized, controlled, double-blind trial. Endoscopy 2007; 39: 1064-1067
240 Hirai F, Beppu T, Nishimura T. et al. Carbon dioxide insufflation compared with air insufflation in double balloon enteroscopy: a prospective, randomized, double-blind trial. Gastrointest Endosc 2011; 73: 743-749
241 Lenz P, Meister T, Manno M. et al. CO2 insufflation during single-balloon enteroscopy: A multicenter randomized controlled trial. Endoscopy 2014; 46: 53-58
242 Li X, Zhao YJ, Dai J. et al. Carbon dioxide insufflation improves the intubation depth and total enteroscopy rate in single-balloon enteroscopy: A randomised, controlled, double-blind trial. Gut 2014; 63: 1560-1565
243 Nishizawa T, Suzuki H, Fujimoto A. et al. Effects of carbon dioxide insufflation in balloon-assisted enteroscopy: A systematic review and meta-analysis. United European Gastroenterol J 2016; 4: 11-7
244 Bretthauer M, Thiis-Evensen E, Huppertz-Hauss G. et al. NORCCAP (Norwegian colorectal cancer prevention): a randomised trial to assess the safety and efficacy of carbon dioxide vs. air insufflation in colonoscopy. Gut 2002; 50: 604-607
245 Saito Y, Uraoka T, Matsuda T. et al. A pilot study to assess the safety and efficacy of carbon dioxide insufflation during colorectal endoscopic submucosal dissection with the patient under conscious sedation. Gastrointest Endosc 2007; 65: 537-542
246 Sumanac K, Zealley I, Fox BM. et al. Minimizing postcolonoscopy abdominal pain by using CO2 insufflation: a prospective, randomized, double blind, controlled trial evaluating a new commercially available CO2 delivery system. Gastrointest Endosc 2002; 56: 190-194
247 Bretthauer M, Lynge AB, Thiis-Evensen E. et al. Carbon dioxide insufflation in colonoscopy: safe and effective in sedated patients. Endoscopy 2005; 37: 706-709
248 Soria F, Lopez-Albors O, Morcillo E. et al. Carbon dioxide insufflation safety in double-balloon enteroscopy: an experimental animal study. Dig Endosc 2013; 25: 39-46
249 Anderson JC. Water-aided colonoscopy. Gastrointest Endosc Clin N Am 2015; 25: 211-226
250 Hafner S, Zolk K, Radaelli F. et al. Water infusion vs. air insufflation for colonoscopy. Cochrane Database Syst Rev 2015; 26: CD009863
251 Cadoni S, Falt P, Rondonotti E. et al. Water exchange for screening colonoscopy increases adenoma detection rate: a multicenter, double-blinded, randomized controlled trial. Endoscopy 2017; 49: 456-467
252 Liang S, Pan Y, Wang B. et al. Water exchange method improves the total examination rate of single balloon enteroscopy: a prospective, randomized, controlled trial. Gastrointest Endosc 2016; 83: AB161-AB162
253 Westwood DA, Alexakis N, Connor SJ. Transparent cap-assisted colonoscopy vs. standard adult colonoscopy: a systematic review and meta-analysis. Dis Colon Rectum 2012; 55: 218-225
254 Sanchez-Yague A, Kaltenbach T, Yamamoto H. et al. The endoscopic cap that can (with videos). Gastrointest Endosc 2012; 76: 169-178
255 Dufault DL, Brock AS. Cap-assisted retrograde single-balloon enteroscopy results in high terminal ileal intubation rate. Endosc Int Open 2016; 4: E202-E204
256 Misra SP, Dwivedi M. Role of intravenously administered hyoscine butyl bromide in retrograde terminal ileoscopy: a randomized, double-blinded, placebo-controlled trial. World J Gastroenterol 2007; 13: 1820-1823
257 Ell C, May A, Nachbar L. et al. Push-and-pull enteroscopy in the small bowel using the double-balloon technique: results of a prospective European multicenter study. Endoscopy 2005; 37: 613-616
258 Heine GD, Hadithi M, Groenen MJ. et al. Double-balloon enteroscopy: indications, diagnostic yield, and complications in a series of 275 patients with suspected small-bowel disease. Endoscopy 2006; 38: 42-48
259 Sun B, Rajan E, Cheng S. et al. Diagnostic yield and therapeutic impact of double-balloon enteroscopy in a large cohort of patients with obscure gastrointestinal bleeding. Am J Gastroenterol 2006; 101: 2011-2015
260 Ramchandani M, Reddy DN, Gupta R. et al. Diagnostic yield and therapeutic impact of single-balloon enteroscopy: series of 106 cases. J Gastroenterol Hepatol 2009; 24: 1631-1638
261 Aktas H, de Ridder L, Haringsma J. et al. Complications of single-balloon enteroscopy: a prospective evaluation of 166 procedures. Endoscopy 2010; 42: 365-368
262 Frantz DJ, Dellon ES, Grimm I. et al. Single-balloon enteroscopy: results from an initial experience at a U.S. tertiary-care center. Gastrointest Endosc 2010; 72: 422-426
263 Upchurch BR, Sanaka MR, Lopez AR. et al. The clinical utility of single-balloon enteroscopy: a single-center experience of 172 procedures. Gastrointest Endosc 2010; 71: 1218-1223
264 Morgan D, Upchurch BR, Draganov PV. et al. Spiral enteroscopy: prospective multicenter U.S. trial in patients with small bowel disorders. Gastrointest Endosc 2010; 72: 992-998
265 Hartmann D, Schmidt H, Bolz G. et al. A prospective two-center study comparing wireless capsule endoscopy with intraoperative enteroscopy in patients with obscure GI bleeding. Gastrointest Endosc 2005; 61: 826-832
266 Despott EJ, Gupta A, Burling D. et al. Effective dilation of small bowel strictures by double-balloon enteroscopy in patients with symptomatic Crohn’s disease (with video). Gastrointest Endosc 2009; 70: 1030-1036
267 Despott EJ, Gabe S, Tripoli E. et al. Enteral access by double-balloon enteroscopy: an alternative method of direct percutaneous endoscopic jejunostomy placement. Dig Dis Sci 2011; 56: 494-498
268 Gómez V, Petersen BT. Endoscopic retrograde cholangiopancreatography in surgically altered anatomy. Gastrointest Endosc Clin N Am 2015; 25: 631-656
269 Ishii K, Itoi T, Tonozuka R. Balloon enteroscopy-assisted ERCP in patients with Roux-en-Y gastrectomy and intact papillae (with videos). Gastrointest Endosc 2016; 83: 377-386
270 May A. How to approach the small bowel with flexible enteroscopy. Gastroenterol Clin North Am 2010; 39: 797-806
271 Finkelstone L, Wolf E, Stein MW. Etiology of small bowel thickening on computed tomography. Can J Gastroenterol 2012; 26: 897-901
272 Fraser C, Despott EJ. Peutz–Jeghers syndrome. In: Keuchel M, Hagenmüller F, Hisao T. , eds. Video capsule endoscopy: a reference guide and atlas. Dordrecht: Springer Science and Business Media; 2014
273 Despott EJ, Fraser C. Capsule endoscopy in polyposis syndromes. In: Zhao-Shen L, Zhuan L, McAlindon M. , eds. Handbook of capsule endoscopy. Dordrecht: Springer Science and Business Media; 2014
274 Pohl J, May A, Nachbar L. et al. Diagnostic and therapeutic yield of push-and-pull enteroscopy for symptomatic small bowel Crohn’s disease strictures. Eur J Gastroenterol Hepatol 2007; 19: 529-534
275 Sunada K, Yamamoto H, Yano T. et al. Advances in the diagnosis and treatment of small bowel lesions with Crohn’s disease using double-balloon endoscopy. Therap Adv Gastroenterol 2009; 2: 357-366
276 Thienpont C, D’Hoore A, Vermeire S. et al. Long-term outcome of endoscopic dilatation in patients with Crohn’s disease is not affected by disease activity or medical therapy. Gut 2010; 59: 320-324
277 Beaulieu D, Barkun AN, Dubé C. et al. Endoscopy reporting standards. Can J Gastroenterol 2013; 27: 286-292
278 Rizk MK, Sawhney MS, Cohen J. et al. Quality indicators common to all GI endoscopic procedures. Gastrointest Endosc 2015; 81: 3-16
279 Bretthauer M, Aabakken L, Dekker E. et al. Requirements and standards facilitating quality improvement for reporting systems in gastrointestinal endoscopy: European Society of Gastrointestinal Endoscopy (ESGE) Position Statement. Endoscopy 2016; 48: 291-294
280 Veitch AM, Vanbiervliet G, Gershlick AH. et al. Endoscopy in patients on antiplatelet or anticoagulant therapy, including direct oral anticoagulants: British Society of Gastroenterology (BSG) and European Society of Gastrointestinal Endoscopy (ESGE) guidelines. Endoscopy 2016; 48: 385-402
281 Itaba S, Nakamura K, Aso A. et al. Prospective, randomized, double-blind, placebo-controlled trial of ulinastatin for prevention of hyperenzymemia after double balloon endoscopy via the antegrade approach. Dig Endosc 2013; 25: 421-427
282 Groenen MJ, Moreels TG, Orlent H. et al. Acute pancreatitis after double-balloon enteroscopy: an old pathogenetic theory revisited as a result of using a new endoscopic tool. Endoscopy 2006; 38: 82-85
283 Matsushita M, Shimatani M, Uchida K. et al. Mechanism of acute pancreatitis after peroral double-balloon enteroscopy. Endoscopy 2007; 39: 480
284 Latorre R, Soria F, Lopez-Albors O. et al. Effect of double-balloon enteroscopy on pancreas: an experimental porcine model. World J Gastroenterol 2012; 18: 5181-5187
285 Honda K, Itaba S, Mizutani T. et al. An increase in the serum amylase level in patients after peroral double-balloon enteroscopy: an association with the development of pancreatitis. Endoscopy 2006; 38: 1040-1043
286 European Section and Board of Gastroenterology and Hepatology. The Blue Book. Available at: http://www.eubogh.org/blue-book/ Accessed: March 2017
287 ASGE Training Committee 2011–2012, Rajan EA, Pais SA et al. Small-bowel endoscopy core curriculum. Gastrointest Endosc 2013; 77: 1-6
288 Sidhu R, Sanders DS, Morris AJ. et al. Guidelines on small bowel enteroscopy and capsule endoscopy in adults. Gut 2008; 57: 125-136
Статьи по теме
Рекомендуемые статьи
Синдром Ахенбаха-Линча-Двайта
проявление неспецифического язвенного колита в виде идиопатического ульцерозного эзофагита.
При эндоскопическом исследовании в случае бронхоэктазов в стадии ремиссии выявляется
частично диффузный бронхит I степени воспаления
Активируйте PUSH уведомления в браузер
Отключите PUSH уведомления в браузер
Содержание
Интернет магазин
Популярное
- О нас
- Правовые вопросы
- Политика
обработки персональных
данных EndoExpert.ru - Связаться с нами
- Стать партнером
© 2016-2022 EndoExpert.ru

Вы находитесь в разделе предназначенном только для специалистов (раздел для пациентов по ссылке). Пожалуйста, внимательно прочитайте полные условия использования и подтвердите, что Вы являетесь медицинским или фармацевтическим работником или студентом медицинского образовательного учреждения и подтверждаете своё понимание и согласие с тем, что применение рецептурных препаратов, обращение за той или иной медицинской услугой, равно как и ее выполнение, использование медицинских изделий, выбор метода профилактики, диагностики, лечения, медицинской реабилитации, равно как и их применение, возможны только после предварительной консультации со специалистом. Мы используем файлы cookie, чтобы предложить Вам лучший опыт взаимодействия. Файлы cookie позволяют адаптировать веб-сайты к вашим интересам и предпочтениям.
Я прочитал и настоящим принимаю вышеизложенное, хочу продолжить ознакомление с размещенной на данном сайте информацией для специалистов.


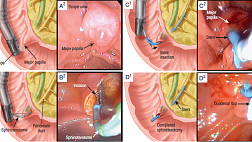






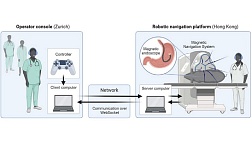
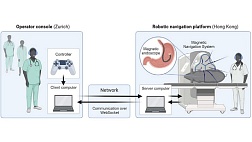



.jpg)





.png)


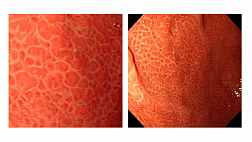

















Комментарии