- Компании
- Takeda. О компании, буклеты, каталоги, контакты
- Olympus. О компании, буклеты, каталоги, контакты
- Boston Scientific. О компании, буклеты, каталоги, контакты
- Pentax. О компании, буклеты, каталоги, контакты
- Fujifilm & R-Farm. О компании, буклеты, каталоги, контакты
- Erbe. О компании, буклеты, каталоги, контакты
- Еще каталоги
- Мероприятия
- Информация
- Обучение
- Классификации
- Атлас
- Quiz
- Разделы
- Пациенту
QR-код этой страницы
Для продолжения изучения на мобильном устройстве ПРОСКАНИРУЙТЕ QR-код с помощью спец. программы или фотокамеры мобильного устройства
Статьи: ПРИОБРЕТЕННЫЕ АНГИОДИСПЛАЗИИ ТОЛСТОЙ КИШКИ
| Авторы: | Аникина М.С. 1 2019г. |
| Об авторах: |
1. Врач-эндоскопист ГБУЗ НСО «Государственная Новосибирская областная клиническая больница» |
Анонс:
Ангиодисплазия (АД) — наименее изученный среди многочисленных факторов, приводящих к кишечным кровотечениям различной степени интенсивности. Этот термин обозначает патологическое состояние, при котором имеется порочное развитие и строение сосудов кишечной стенки [1].
КОД ПО МКБ-10:
КЛАСС XI: Болезни органов пищеварения.
БЛОК K55: Сосудистые болезни кишечника.
КОД K55.2: Ангиодисплазия ободочной кишки.
K55.8: Другие сосудистые болезни кишечника.
Полный текст статьи:
Первый случай ангиодисплазии был описан в литературе в 1839 году, но термин в обиход ввел J.J. Caldabini в 1974-м — он назвал так аномально расширенные вены подслизистой основы слепой и восходящей ободочной кишок, которые стали причиной кишечного кровотечения у больного старческого возраста. С тех пор в литературе возникали споры о точной этиологии данных поражений, что привело к множеству синонимичных терминов, таких как ангиэктазии, телеангиэктазии, артериовенозные мальформации и т. д. [1, 5].
В настоящее время АД желудочно-кишечного тракта (ЖКТ) — заболевание, характеризующееся эктазией сосудов любого типа с преимущественной локализацией в подслизистой основе. Ангиодисплазия проявляется аномальными расширенными и извитыми эктопированными сосудами в слизистой или подслизистом слое кишки (рис. 1). При морфологическом исследовании сосуды выстланы только эндотелием, гладкомышечные волокна присутствуют в небольшом количестве или не определяются [5].
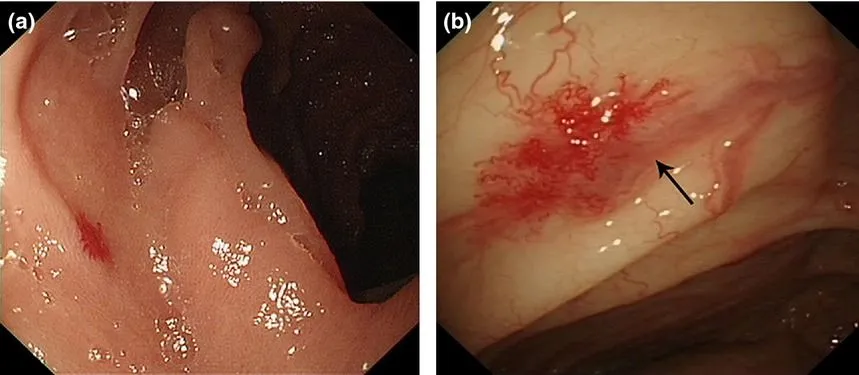
Рис. 1. Эндоскопическая картина ангиодисплазии тонкой и толстой кишки [5].
A. АД в тонкой кишке, выявленная при однобаллонной энтероскопии.
B. АД восходящей ободочной кишки, выявленная при колоноскопии (стрелка показывает питающий сосуд).
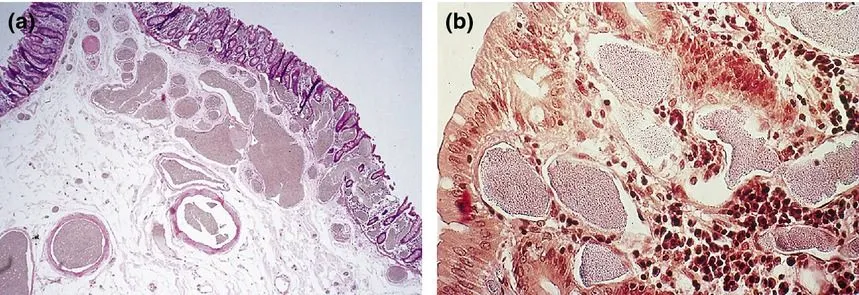
Рис. 2. Гистологическая картина ангиодисплазии [5].
А. Гистологическая картина АД с преимущественно подслизистой локализацией с расширенными толстостенными артериями и тонкостенными венами.
B. Гистологическая картина АД слепой кишки: видны расширенные внутрислизистые сосуды за слоем эпителиальных клеток.
Многообразие форм, локализаций и связь с другими поражениями различных органов и систем затрудняют классификацию данного заболевания.
Существует множество классификаций. В 1993 году в Государственном научном центре колопроктологии (ГНЦК) Кузьминым А.М. с соавторами была предложена классификация с учетом происхождения, морфологического строения АД, распространенности и локализации поражения, а также клинического течения [1].
Классификация ангиодисплазий по Кузьмину А.М.
А. По происхождению.
I тип – врожденная АД:
а) ненаследственная форма;
б) наследственная форма (болезнь Рандю — Ослера).
II тип – приобретенная АД.
Б. По морфологическому строению.
1. Венозная АД:
а) капиллярный тип;
б) кавернозный тип.
2. Артериовенозная АД.
3. Артериальная АД.
В. По распространенности.
1. Ограниченная АД (поражение одного отдела толстой кишки протяженностью не более 5 см).
2. Диффузная АД (поражение одного или нескольких отделов толстой кишки протяженностью более 5–10 см).
3. Генерализованная АД (системный ангиоматоз с сочетанным поражением других органов и систем, синдром Клиппеля — Треноне).
Г. По локализации.
1. Толстая кишка.
2. Тонкая кишка.
3. Смешанная форма с поражением толстой и тонкой кишок.
Д. По клиническому течению.
1. Неосложненное (в том числе бессимптомное).
2. Осложненное.
Основополагающий момент — необходимость систематизировать обнаруженные изменения по происхождению. Кроме того, важен также признак распространенности. Если патологический процесс локализуется в одном отделе толстой кишки и площадь поражения не более 5 см — это ограниченный процесс. Если изменения захватывают несколько анатомических областей — процесс считается диффузным. Изменения, обнаруженные в нескольких органах или областях, называют генерализованными. Такие изменения характерны для синдрома Клиппеля — Треноне.
Данная классификация охватывает все основные, наиболее часто встречающиеся типы ангиодисплазий, учитывает их происхождение, гистологическую структуру, обширность патологического процесса, варианты клинической картины заболевания, что позволяет максимально полно сформулировать клинический диагноз, разработать тактику лечения, определить объем операции [1].
Толстая кишка — наиболее частая локализация приобретенной АД. У западных пациентов ангиодисплазии располагаются преимущественно в слепой и восходящей ободочной кишке (54–93%), при этом по данным трех крупных исследований было установлено, что в восточной популяции АД распределены почти поровну между проксимальными и дистальными отделами тонкой кишки (44–69% и 31–56%, соответственно). Российские исследователи сообщают, что наиболее часто (66,7%) приобретенные ангиодиспластические изменения локализовались в правой половине ободочной и терминальном отделе подвздошной кишки, у 25% — в сигмовидной кишке и лишь у 8,3% больных имелось множественное поражение правых и левых отделов ободочной кишки. При этом ряд зарубежных авторов сообщает, что у 40–60% пациентов с ангиодисплазиями имеется более одного поражения, 27% больных с толстокишечной локализацией АД имеют множественные поражения, затрагивающие два сегмента или более. Кроме того, одновременные поражения других отделов ЖКТ выявляется примерно у 20% пациентов. Таким образом, при обнаружении ангиодисплазии в любом отделе ЖКТ требуется тщательное обследование для исключения множественного поражения [1, 5].
Клиническая картина
Характерный признак приобретенной ангиодисплазии — ее развитие у лиц старшего возраста (старше 60 лет).
Основное клиническое проявление заболевания — кровотечения различной интенсивности, от скрытых до массивных, возникающие без видимых причин или после физической нагрузки на фоне удовлетворительного самочувствия. Данные о частоте кровотечений из нижних отделов ЖКТ, причиной которых была АД, широко варьируют (3–40%). В литературе встречаются описания остро возникших массивных кровотечений с нарушением гемодинамических показателей, которые потребовали интенсивной кровезамещающей терапии с параллельным проведением обследования. Следует отметить, что, по данным некоторых авторов, до 50% больных с этой патологией, учитывая рецидивный интенсивный характер кишечного кровотечения, были неоднократно прооперированы в экстренном порядке. Однако данные интраоперационной ревизии с множественными гастро-, энтеро- и колотомиями не позволили выявить причину геморрагии. Иногда во время этих операций выполнялись необоснованные резекции различных отделов кишечника. Редкое установление причины кровотечения во время операции, по мнению исследователей, — другой характерный признак приобретенной ангиодисплазии [1].
Патогенез
Этиология и патогенез развития АД выяснены не до конца. На сегодняшний день наиболее цитируемой является гипотеза, предложенная Boley с соавторами, по которой периодически наступающая обструкция вен подслизистого слоя (функциональная венозная недостаточность) вследствие спазма гладкой мускулатуры толстой кишки с годами приводит к обязательному их расширению и к спазму прекапилляров, из-за чего формируются мелкие артериовенозные коллатерали. Так происходит формирование приобретенной ангиодисплазии. Ишемия слизистой оболочки усугубляет это состояние (рис. 3). К предрасполагающим факторам развития приобретенной АД относят аортальный стеноз, болезнь Виллебранда и хроническую почечную недостаточность.
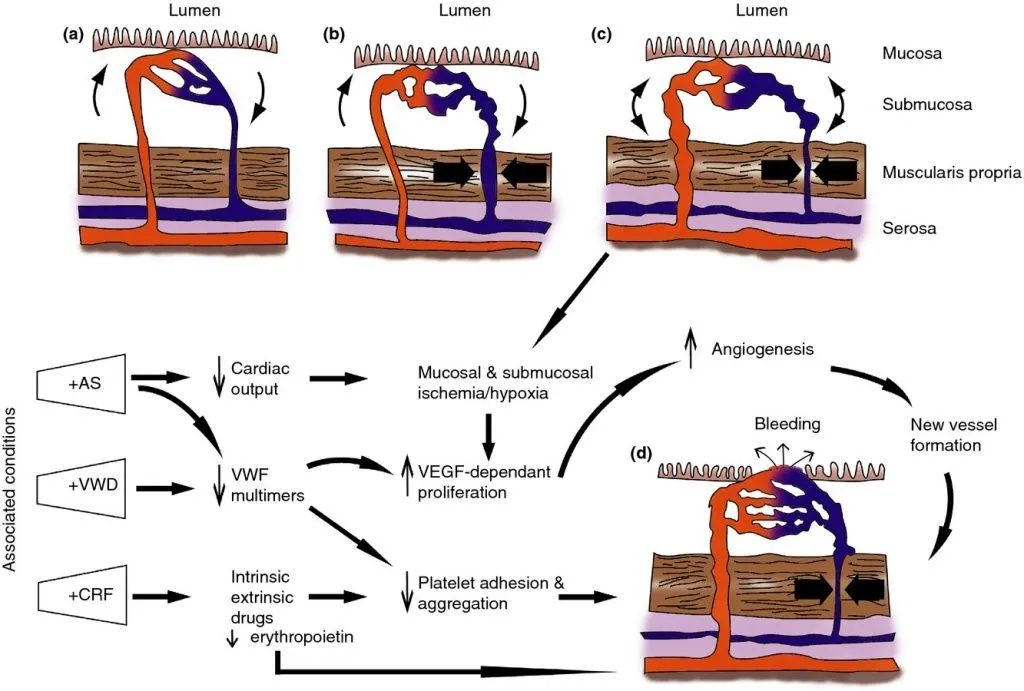
Рис. 3. Патогенез приобретенной АД [5].
Диагностика
В настоящее время наиболее эффективными методами диагностики можно считать две объективные и взаимодополняющие методики: мезентерикография и эндоскопическое исследование (колоноскопия, энтероскопия).
Эндоскопические методы — основной инструмент для диагностики АД. Это в значительной степени связано с развитием эндоскопической техники и улучшением качества изображения. Ангиодисплазии верхних отделов ЖКТ и толстой кишки обычно диагностируются при выполнении стандартной эзофагогастродуоденоскопии и колоноскопии [1, 5].
Качественная подготовка к колоноскопии необходима для выявления ангиодисплазий. Действенная альтернатива полнообъемным препаратам ПЭГ — применение малообъемного препарата ПЭГ с аскорбатным комплексом (МОВИПРЕП®) в разделенном режиме или по утренней одноэтапной схеме. Применение МОВИПРЕП® связано с достоверно меньшим количеством таких нежелательных явлений, как тошнота и рвота [8]. Использование МОВИПРЕП® эффективно и безопасно у пациентов с нарушением функции почек, при этом характеризуется большей приверженностью пациентов к подготовке и готовностью повторить прием препарата по сравнению с ПЭГ в стандартном объеме [6, 7].
Колоноскопия
При эндоскопическом исследовании приобретенная АД может выглядеть как участок слизистой оболочки округлой формы ярко-красного или вишневого цвета, не выступающий в просвет кишечной стенки. От него радиально расходятся умеренно расширенные извитые сосуды на протяжении 7–10 мм. Размер этих патологических образований — от 0,3 до 0,7 см. Образования легко травмируются, появляются капельки крови. Небольшой размер сосудистого патологического образования также можно отнести к характерным признакам приобретенной ангиодисплазии [1]. В некоторых случаях слизистая вокруг зоны поражения имеет более светлый оттенок, так называемый бледный ободок [1, 5].
Энтероскопия
Для диагностики АД тонкой кишки широко используются капсульная и баллон-ассистированная энтероскопия. Эти методы дополняют друг друга и должны совместно использоваться для поиска источника тонкокишечного кровотечения. Также одно- и двухбаллонная энтероскопия обладают возможностями терапевтического воздействия на АД тонкой кишки. Интраоперационная энтероскопия облегчает полное обследование тонкой кишки и выполняется совместно хирургом и эндоскопистом. Эта процедура связана с потенциально серьезными осложнениями и показана только тем пациентам, у которых менее инвазивные методы не позволили выявить или вылечить источник кровотечения [1, 5].
Рентгенологические методы обследования
Наиболее информативный рентгенологический метод диагностики АД — мезентерикография. Этот метод может быть использован для выбора способа и объема хирургического вмешательства у больных с ангиодисплазией. Эффективность использования селективной мезентерикографии сопоставима с результатами колоноскопии. Также метод полезен при отрицательных результатах колоноскопии или неполных осмотрах. Основные ангиографические признаки приобретенной АД:
· расширение магистральной артерии (подвздошно-ободочной);
· контрастирование дренирующей вены на ранней стадии исследования (на 3–4 секунде);
· наличие четких и интенсивных сосудистых сплетений в кишечной стенке, говорящих о наличии артериовенозных шунтов;
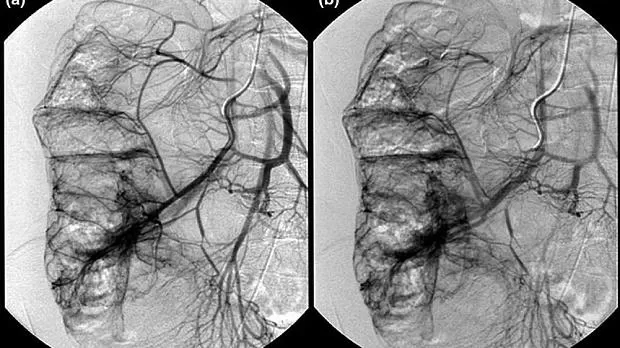
· медленная венозная разгрузка (рис. 4) [1, 5].
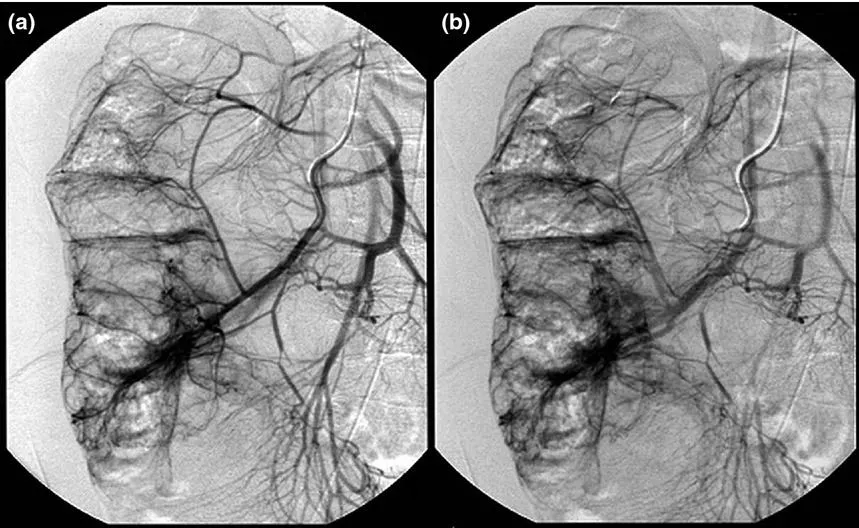
Рис. 4. Мезентерикография для диагностики АД [5].
А. Артериальная фаза селективной верхней брыжеечной ангиограммы, показывающая одновременное раннее венозное заполнение (быстрое шунтирование) с расширенными участками сосудистой системы в стенке слепой кишки.
B. Венозная фаза той же ангиограммы.
Лечение ангиодисплазии
Лечебная тактика при АД ЖКТ зависит от степени кровопотери, периодичности кровотечений и наличия положительных ангиографических симптомов. При незначительных периодических кишечных кровотечениях возможно применение эндоскопических методов [1].
Аргоноплазменная коагуляция
По своей сути аргоноплазменная коагуляция (АПК) — электрохирургический монополярный бесконтактный метод воздействия на биологические ткани высокочастотным током с помощью ионизированного и, как следствие, электропроводящего аргона, аргоновой плазмы. На сегодняшний день АПК — наиболее распространенный метод лечения приобретенной ангиодисплазии, применяющийся как для остановки кровотечения, так и в безрецидивный период. К преимуществам метода относятся лимитированная глубина поражения тканей и возможность воздействия на большую площадь поражения, а также отсутствие контакта между зондом и поверхностью слизистой. К недостаткам АПК относят большое количество рецидивов кровотечения — до 19%, которые при этом часто возникают из других поражений слизистой (и возможно повторное проведение АПК для их терапии). При этом выделены независимые предикторы рецидивов кровотечения у больных с АД ЖКТ. Это пожилой возраст, сопутствующие заболевания сердечно-сосудистой системы, терапия антикоагулянтами, множественные поражения, размер поражений ≤5 мм [5].
Также применение АПК связано с рядом осложнений, в первую очередь с перфорацией, вызванной как непосредственным повреждением стенки, так и баротравмой. Поэтому при воздействии на поражения в правой половине толстой кишки, где стенка тоньше, следует проводить гидролифтинг ангиодисплазии с применением адреналина или без него. Это позволяет снизить частоту перфораций стенки кишки в зоне АПК (рис. 5) [1, 4, 5].
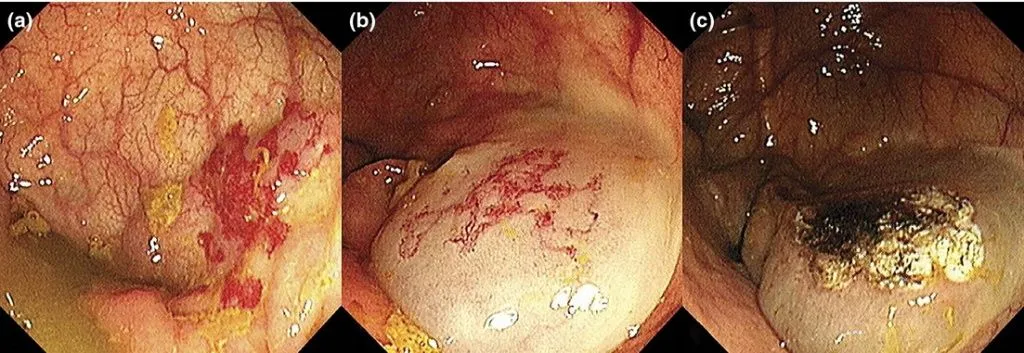
Рис. 5. АПК приобретенной АД в толстой кишке с введением в подслизистый слой раствора адреналина [5].
A. Ангиодисплазия.
B. После введения раствора адреналина (1:200 000) отмечается сужение сосудов и бледность слизистой.
C. Струп в зоне АД после применения АПК (50 Вт).
Электрокоагуляция
Коагуляция АД щипцами для «горячей» биопсии (монополярная электрокоагуляция) стала первой электрохирургической методикой, используемой для лечения АД в начале 1980-х годов. На сегодняшний день этот метод не рекомендуется из-за относительно высокой степени риска серьезных осложнений, включая перфорацию, в том числе и отсроченную, и из-за высоких показателей повторного кровотечения (53% на 3 года). Зонды для контактной коагуляции были введены в практику в конце 1980-х и используются до сих пор — правда, на сегодняшний день в продаже сохранилось мало таких устройств. Наиболее распространены зонд HeatProbe (Olympus, Япония), относящийся к монополярным устройствам, и зонд GoldProbe (Boston Scientific), являющийся биполярным устройством, что ограничивает его максимальную температуру и площадь воздействия. Эффективность применения зондов подобного типа сравнима с АПК, оба метода сопряжены с опасностью перфорации и кровотечения. С особой осторожностью следует их применять в правых отделах толстой и в двенадцатиперстной кишке. В качестве первой линии терапии рекомендуется применение АПК или биполярного зонда, если в клинике имеется опыт его применения [4, 5].
Фотокоагуляция
Для фотокоагуляции приобретенных АД желудочно-кишечного тракта возможно применение неодимового и аргонового лазеров. Оба метода являются бесконтактными и с контролируемой глубиной поражения, что обеспечивает небольшое число (2,4%) осложнений в виде перфорации стенки кишки. Воздействие неодимового (Nd: YAG) лазера по сравнению с аргоновым дает в 3–4 раза более глубокий и протяженный фиброз. Также неодимовый лазер более распространен. При этом доказана эффективность применения аргонового лазера при ангиодисплазиях, однако обе методики дорогостоящие и на сегодняшний день не имеют широкого распространения [5].
Эндоскопическое клипирование
Этот подход показал эффективность и безопасность в нескольких случаях кровотечения из толстой кишки при использовании в качестве монотерапии или в сочетании с другими методиками абляции (аргоноплазменной или термической). Клипирование особенно эффективно в случае изолированных и относительно крупных АД. Также возможно использование данного метода у пациентов с высоким риском кровотечения при приеме антикоагулянтов или обширных коагуляционных дефектов после абляции [3, 5].
Эндоскопическое лигирование
Данная методика продемонстрировала эффективность в небольшой серии случаев, сравнимую с применением биполярной коагуляции, серьезных осложнений отмечено не было. Однако в другом исследовании (Ljubicic и соавторов) было описано кровотечение после перевязки АД в двенадцатиперстной кишке, которое потребовало эндоскопического лечения. Также отмечается высокий риск рецидивных кровотечений при наблюдении на протяжении полутора лет, поэтому долгосрочные результаты данного метода сомнительны [5].
Эндоваскулярные методики лечения ангиодисплазий
При неэффективности эндоскопических методов терапии приобретенных АД ЖКТ возможно применение эндоваскулярных вмешательств.
Суперселективная транскатетерная эмболизация — современный ангиографический метод лечения кровотечения при АД. Эффективность метода может достигать 80–90% при относительно низких показателях рецидивных кровотечений, которые также могут быть остановлены повторной эмболизацией. Частота осложнений — около 5–9%. Серьезные осложнения, такие как гематомы, тромбозы, формирование псевдоаневризмы и инфаркт кишечника, встречаются менее чем в 2% случаев. Таким образом, транскатетерная эмболизация мезентериальных сосудов — перспективный, эффективный и безопасный метод лечения кровотечений из АД, к его недостаткам следует отнести низкую доступность и дороговизну [1, 5].
Медикаментозная терапия
Медикаментозная терапия АД применяется при неэффективности других методов лечения или для профилактики рецидивов у пациентов с хроническими кровотечениями. На сегодняшний день в практике используются талидомид и октреотид благодаря их угнетающему действию на ангиогенез. В связи с высоким процентом побочных явлений талидомида его максимальная рекомендуемая доза составляет 100 мг в сутки, у женщин детородного возраста должен использоваться надежный метод контрацепции во время лечения из-за тератогенности. Данный препарат должен быть зарезервирован для пациентов, зависимых от переливания крови. Считается, что влияние октреотида на кровотечение из АД должно быть связано с несколькими механизмами, включая ингибирование ангиогенеза, увеличение резистентности сосудов, уменьшение висцерального кровотока и увеличение агрегации тромбоцитов [2, 5].
Хирургическое лечение
Профузные рецидивирующие кишечные кровотечения с выраженной анемизацией и ухудшением общего состояния больных — показание к хирургическому лечению и резекции соответствующего отдела кишечника.
Операцией выбора в большинстве случаев является правосторонняя гемиколэктомия с формированием илеотрансверзоанастомоза. Использование лапароскопических технологий в ходе операции существенно снижает инвазивность, обеспечивает хорошие непосредственные результаты операции [1, 5].
Выводы
Приобретенная ангиодисплазия слизистой нижних отделов ЖКТ — распространенная причина кровотечений у лиц старшего возраста. У жителей Российской Федерации АД в толстой кишке чаще расположены в правых отделах, что требует тщательной подготовки толстой кишки к исследованию. В диагностике и лечении данной патологии ведущее место отведено эндоскопическим методам. Рутинным методом гемостаза из АД и профилактики рецидивов является аргоноплазменная коагуляция. Также возможно применение других методов эндоскопического воздействия, выбор которых во многом зависит от оснащенности и опыта клиники. Препарат октреотид используется для медикаментозного лечения пациентов с приобретенной ангиодисплазией; у больных, зависимых от переливания крови, возможно (с осторожностью!) применение талидомида. Альтернативные методы диагностики и малоинвазивного лечения — мезентерикография с суперселективной транскатетерной эмболизацией. В случае неэффективности или недоступности данных методик применяется открытое хирургическое лечение в объеме резекции соответствующего отдела кишечника.
Список литературы:
Рекомендуемые статьи
При эндоскопическом исследовании в случае бронхоэктазов в стадии ремиссии выявляется
частично диффузный бронхит I степени воспаления
Активируйте PUSH уведомления в браузер
Отключите PUSH уведомления в браузер
Содержание
Интернет магазин
Популярное
- О нас
- Правовые вопросы
- Политика
обработки персональных
данных EndoExpert.ru - Связаться с нами
- Стать партнером
© 2016-2022 EndoExpert.ru

Вы находитесь в разделе предназначенном только для специалистов (раздел для пациентов по ссылке). Пожалуйста, внимательно прочитайте полные условия использования и подтвердите, что Вы являетесь медицинским или фармацевтическим работником или студентом медицинского образовательного учреждения и подтверждаете своё понимание и согласие с тем, что применение рецептурных препаратов, обращение за той или иной медицинской услугой, равно как и ее выполнение, использование медицинских изделий, выбор метода профилактики, диагностики, лечения, медицинской реабилитации, равно как и их применение, возможны только после предварительной консультации со специалистом. Мы используем файлы cookie, чтобы предложить Вам лучший опыт взаимодействия. Файлы cookie позволяют адаптировать веб-сайты к вашим интересам и предпочтениям.
Я прочитал и настоящим принимаю вышеизложенное, хочу продолжить ознакомление с размещенной на данном сайте информацией для специалистов.











.jpg)




.png)

















Комментарии 1