- Компании
- Takeda. О компании, буклеты, каталоги, контакты
- Olympus. О компании, буклеты, каталоги, контакты
- Boston Scientific. О компании, буклеты, каталоги, контакты
- Pentax. О компании, буклеты, каталоги, контакты
- Fujifilm & R-Farm. О компании, буклеты, каталоги, контакты
- Erbe. О компании, буклеты, каталоги, контакты
- Еще каталоги
- Мероприятия
- Информация
- Обучение
- Классификации
- Атлас
- Quiz
- Разделы
- Пациенту
QR-код этой страницы
Для продолжения изучения на мобильном устройстве ПРОСКАНИРУЙТЕ QR-код с помощью спец. программы или фотокамеры мобильного устройства
Статьи: Шкала эндоскопической активности послеоперационного рецидива болезни Крона по Rutgeerts
Анонс:
Спустя 6-12 месяцев всем оперированным пациентам с болезнью Крона показано проведение контрольного обследования, в первую очередь, эндоскопического. Область послеоперационного анастомоза должна быть тщательно осмотрена и оценена в соответствии со шкалой эндоскопической активности послеоперационного рецидива болезни Крона по Rutgeerts (при резекции терминального отдела подвздошной кишки или илеоцекальной резекции).

Полный текст статьи:
|
Оценка |
Определение |
|
i0 |
Нет признаков воспаления |
|
i1 |
≤5 афтозных язв |
|
i2 |
>5 афтозных язв с нормальной слизистой оболочкой между ними ИЛИ протяженные участки здоровой слизистой оболочки между более выраженными изъязвлениями ИЛИ поражения, ограниченные подвздошно-толстокишечным анастомозом |
|
i3 |
Диффузный афтозный илеит с диффузно-воспаленной слизистой оболочкой |
|
i4 |
Диффузное воспаление с крупными язвами, «булыжной мостовой» И/ИЛИ сужением просвета |
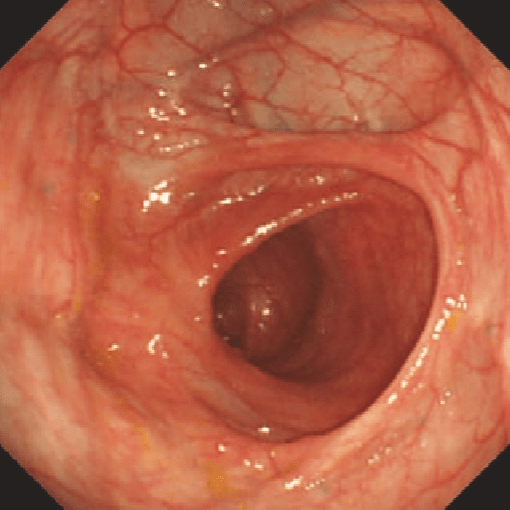
Rutgeerts i0 | 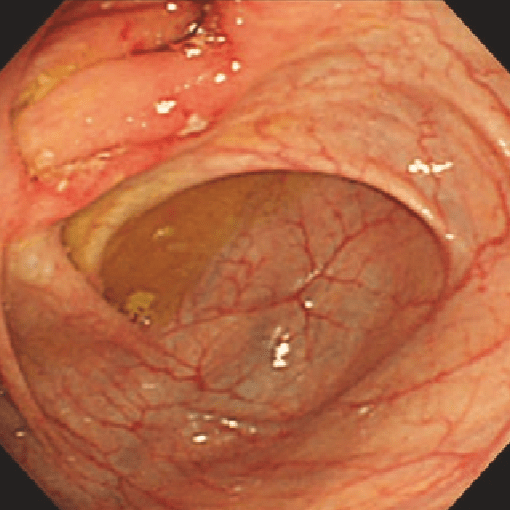
Rutgeerts i1 |
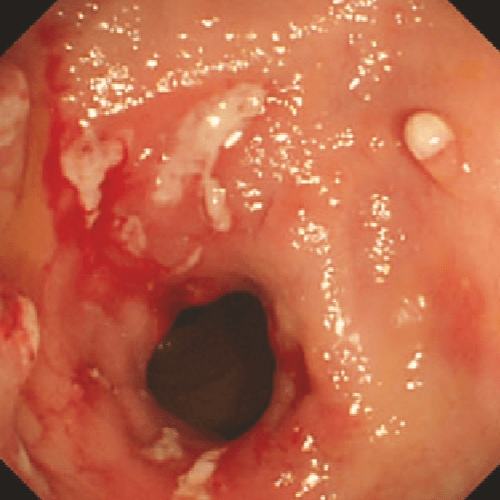
Rutgeerts i2 | 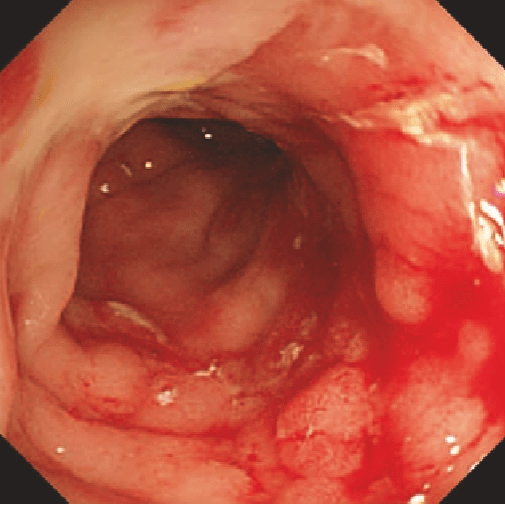
Rutgeerts i3 |
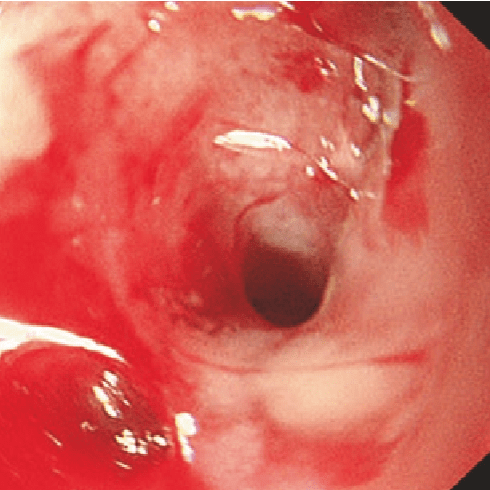
Rutgeerts i4 |
Даже при полном удалении всех макроскопически измененных отделов кишечника, хирургическое вмешательство не приводит к полному исцелению: в течение 5 лет клинически значимый рецидив отмечается у 28-45% пациентов, а в течение 10 лет – у 36-61%, что диктует необходимость продолжения противорецидивной терапии после операции по поводу БК [83,84].
К факторам, достоверно повышающим риск послеоперационного рецидива, относятся:
- · курение,
- · две и более резекции кишки в анамнезе,
- · протяженные резекции тонкой кишки в анамнезе (>50 см),
- · перианальные поражения,
- · пенетрирующий фенотип [85].
В зависимости от сочетания факторов риска, а также от эффективности, ранее проводившейся противорецидивной терапии, пациенты после операции должны быть стратифицированы на группы с различным риском послеоперационного рецидива.
- · В группе низкого риска рецидива БК целесообразно назначение месалазина (4 г) или сульфасалазина (4 г).
- · Пациенты из группы промежуточного риска являются кандидатами на проведение терапии азатиоприном (2,0-2,5 мг/кг/сут) или 6-меркаптопурином (1,5 мг/кг/сут.) [86].
- · Пациентам с высоким риском рецидива целесообразно еще до проведения контрольного эндоскопического исследования начать курс биологической терапии (инфликсимаб, адалимумаб, цертолизумаба пэгол, ведолизумаб) [87].
Противорецидивную терапию рекомендуется начинать через 2 недели после оперативного вмешательства.
Спустя 6-12 месяцев всем оперированным пациентам с БК показано проведение контрольного обследования, в первую очередь, эндоскопического. При невозможности визуализировать зону анастомоза следует констатировать наличие или отсутствие рецидива, основываясь на сочетании данных рентгенологического обследования (как правило, КТ) и неинвазивных маркеров воспаления – С-реактивного белка, фекального кальпротектина и др.
- · При отсутствии признаков воспаления или обнаружении минимальных (i1 по шкале Rutgeerts) воспалительных изменений проводимая терапия должна быть продолжена.
- · Наличие более выраженных воспалительных изменений (i2-i4) указывает на неэффективность проводимой терапии и должно служить показанием к усилению терапии: подключению иммуносупрессоров у пациентов, ранее их не получавших или к проведению биологической терапии (адалимумабом [89], инфликсимабом [90], цертолизумаба пэголом, ведолизумабом) у пациентов, находящихся на поддерживающей терапии азатиоприном/6-меркаптопурином.
В дальнейшем, вне зависимости от характера течения заболевания и клинической манифестации БК, следует не реже 1 раза в 1-3 года выполнять контрольное эндоскопическое исследование, следуя этому же алгоритму выбора противорецидивного средства [91].
 Вам может быть интересно:
Вам может быть интересно:
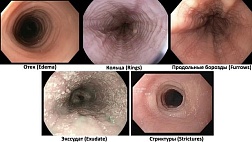
- Статьи: SES-CD (Simple Endoscopic Score for Crohn's Disease) - простая эндоскопическая шкала болезни Крона - 2004 год (балл по шкале SES-CD)
- Рекомендации Болезнь Крона 2017
- Образовательный модуль "Воспалительные заболевания кишечника" с Веселовым В.В.
Список литературы:
Статьи по теме
Рекомендуемые статьи
Синдром Бурхаве
Спонтанный разрыв пищевода - характеризуется спонтанным разрывом всех слоев стенки пищевода. Первое описание данного состояния дано голландским врачом Германом Бурхаве (Hermann Boerhaave) в 1724 г.
При эндоскопическом исследовании в случае бронхоэктазов в стадии ремиссии выявляется
частично диффузный бронхит I степени воспаления
Активируйте PUSH уведомления в браузер
Отключите PUSH уведомления в браузер
Содержание
Интернет магазин
Популярное
- О нас
- Правовые вопросы
- Политика
обработки персональных
данных EndoExpert.ru - Связаться с нами
- Стать партнером
© 2016-2022 EndoExpert.ru

Вы находитесь в разделе предназначенном только для специалистов (раздел для пациентов по ссылке). Пожалуйста, внимательно прочитайте полные условия использования и подтвердите, что Вы являетесь медицинским или фармацевтическим работником или студентом медицинского образовательного учреждения и подтверждаете своё понимание и согласие с тем, что применение рецептурных препаратов, обращение за той или иной медицинской услугой, равно как и ее выполнение, использование медицинских изделий, выбор метода профилактики, диагностики, лечения, медицинской реабилитации, равно как и их применение, возможны только после предварительной консультации со специалистом. Мы используем файлы cookie, чтобы предложить Вам лучший опыт взаимодействия. Файлы cookie позволяют адаптировать веб-сайты к вашим интересам и предпочтениям.
Я прочитал и настоящим принимаю вышеизложенное, хочу продолжить ознакомление с размещенной на данном сайте информацией для специалистов.















.jpg)




.png)














Комментарии