- Компании
- Takeda. О компании, буклеты, каталоги, контакты
- Olympus. О компании, буклеты, каталоги, контакты
- Boston Scientific. О компании, буклеты, каталоги, контакты
- Pentax. О компании, буклеты, каталоги, контакты
- Fujifilm & R-Farm. О компании, буклеты, каталоги, контакты
- Erbe. О компании, буклеты, каталоги, контакты
- Еще каталоги
- Мероприятия
- Информация
- Обучение
- Классификации
- Атлас
- Quiz
- Разделы
- Пациенту
QR-код этой страницы
Для продолжения изучения на мобильном устройстве ПРОСКАНИРУЙТЕ QR-код с помощью спец. программы или фотокамеры мобильного устройства
Статьи: Современное лечение гастроэзофагеальной рефлюксной болезни
| Авторы: | Ренев Е.Н. 2002г. |
Введение:


Полный текст статьи:
Гастроэзофагиальная рефлюксная болезнь – это патологическое состояние, характеризующееся наличием симптомов и/или наличием морфологического субстрата воспалительного поражения нижних отделов пищевода, возникающих вследствие желудочно-пищеводного рефлюкса [1].
Международная рабочая группа считает, что о ГЭРБ следует говорить тогда, когда гастроэзофагеальный рефлюкс приводит к риску возникновения соматических осложнений или симптомы рефлюкса значительно ухудшают качество жизни пациента [6].
Существует вариант эндоскопически негативной рефлюксной болезни. В этом случае, несмотря на наличие симптомов, у пациента во время эзофагоскопии не обнаруживаются эрозивные повреждения, язвы или пищевод Барретта [6].
Патогенез
Для развития ГЭРБ необходимо сочетание нескольких патологических факторов:
- Заброс желудочного содержимого в пищевод (рефлюкс);
- Нарушение эзофагеального клиренса;
- Достаточная кислотность желудочного сока.
Соблюдение первого условия связано с кардиальным сфинктером пищевода. Атония или гипотония мускулатуры кардии, увеличение количества спонтанных расслаблений сфинктера, его структурные дефекты – основные причины возникновения желудочно-пищеводного заброса.
Эзофагеальный клиренс – это процесс продвижения содержимого пищевода в желудок. Для этого должно быть достаточно слюны в просвете пищевода и сохраняться нормальная его перестальтика. При несоблюдении этих условий, клиренс нарушается.
Кислотность желудочного сока – немаловажный фактор возникновения ГЭРБ. У людей с гипоацидными состояниями рефлюкс протекает бессимптомно и не приводит к ГЭРБ. Чем ниже рН желудочного сока, тем агрессивнее его влияние на пищевод.
При сочетании вышеуказанных факторов, происходит заброс пепсина и соляной кислоты вместе с содержимым желудка в просвет пищевода. Ферменты и кислота повреждают слизистую пищевода, приводят к эзофагиту и другим осложнениям.
Эпидемиология
Отдельные симптомы ГЭРБ такие, как изжога, наблюдаются примерно у половины взрослого населения планеты. При этом морфологические изменения выявляются не более, чем у 10% обследованных [1].
ГЭРБ не всегда ассоциируется с эзофагитом. Более, чем у половины пациентов, имеющих симптомы рефлюкса, во время эндоскопического исследования никаких изменений не обнаруживается [8]. Однако это не говорит о более легком течении заболевания.
Снижение качества жизни пациентов с ГЭРБ зависит от симптомов, но не зависит от морфологических проявлений[29]. Эндоскопически негативная рефлюксная болезнь реже приводит к эзофагиту и другим осложнениям [7,8].
Диагностика
Диагностика ГЭРБ складывается из клинических данных, инструментальных и лабораторных исследований. У большинства пациентов основным симптомом рефлюкса является изжога [6]. Дополнительно могут встречаться отрыжка и чувство жжения за грудиной. Все эти признаки ассоциированы с приемом пищи.
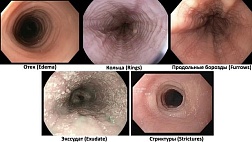
Золотым стандартом диагностики является эзофагоскопия. Эндоскопическое обследование с микроскопией биоптата позволяет диагностировать пищевод Барретта. По эндоскопической классификации выделяют 4 степени эзофагита в зависимости от морфологической картины.
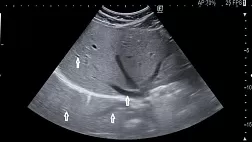
Рентгенография с пассажем бария не является высокочувствительным тестом. Она информативна при тяжелом эзофагите и эзофагите средней тяжести, но малоинформативная при легких изменениях [12, 22, 23].
Для диагностики эндоскопически негативного рефлюкса используют рН-метрию. Согласно критериям МКБ, для диагностики необходимо как минимум 50 эпизодов снижения рН менее 4 [1]. В случае, если ГЭРБ диагностируется клинически, но не удовлетворяет эндоскопическим критериям и критериям рН-метрии говорят о гиперчувствительном пищеводе.
Лечение
Основной целью лечения является уменьшение и полное исчезновение симптомов заболевания. Отсутствие симптомов коррелирует с морфологическим излечением [6].
Изменение образа жизни
Имеются данные о том, что стиль жизни не влияет на возникновение рефлюкса [6]. Однако пациентам с хроническим рефлюксом следует давать ряд рекомендаций:
- Нормализация питания. Диета предполагает исключения жирной, жареной и острой пищи, газированных напитков, лука и чеснока – всего, что способствует снижению рН.
- Дробное питание маленькими порциями.
- Последний прием пищи не менее, чем за 3 часа до сна.
- Отказ от вредных привычек. Есть доказательства того, что курение способствует развитию рефлюкса [7], но нет достоверных доказательств того, что отказ от курения способствует излечению заболевания [6] .
- Исключение ношения корсетов, обтягивающей одежды и тугих поясов.
- Подъем головного конца кровати в случаях, когда симптомы возникают в ночное время.
Антациды
Антациды – препараты, которые нейтрализуют уже имеющуюся в желудке соляную кислоту. К ним относится маалокс, альмагель, фосфалюгель. На самом деле, с их помощью невозможно лечить ГЭРБ. Антациды способны только уменьшать симптомы заболевания. Рекомендуется использовать это лекарство только тогда, когда проявления болезни единичные или имеет место однократное нарушение диеты.
Н2-блокаторы
Это первые антисекреторные препараты, изобретенные раньше блокаторов протонной помпы. Они влияют только на один путь регуляции секреции соляной кислоты – гистаминовый. При этом два других – гастриновый и ацетилхолиновый – продолжают работать. Для ранних стадий заболевания этого эффекта может быть достаточно.
Наиболее часто использует фамотидин и ранитидин, реже – циметидин и низатидин. Механизм их влияния на ГЭРБ связан не с воздействием на рефлюкс, а со снижением агрессивности желудочной среды. Таким образом, заброс желудочного содержимого будет продолжаться, но само содержимое перестанет негативно влиять на стенки пищевода.
С тех пор, как изобрели блокаторы протонной помпы, от гистаминовых блокаторов стали отказываться многие врачи. На самом деле, Н2-блокаторы доказали хорошую эффективность в сравнении с плацебо [7]. Более того, их рекомендуют в качестве терапии ночных симптомов [21] даже пациентам на PPI-терапии [25].
Блокаторы протонной помпы
PPI-препараты по механизму действия похожи на Н2-блокаторы. С тем лишь отличием, что ингибиторы протонной помпы выключают все пути регуляции секреции соляной кислоты. Как следствие, они более эффективно повышают кислотно-основное равновесие. Минус этих препаратов заключается в том, что максимальный их эффект достигается только на 2-3 сутки приема, как терапия «по требованию» они не используются.
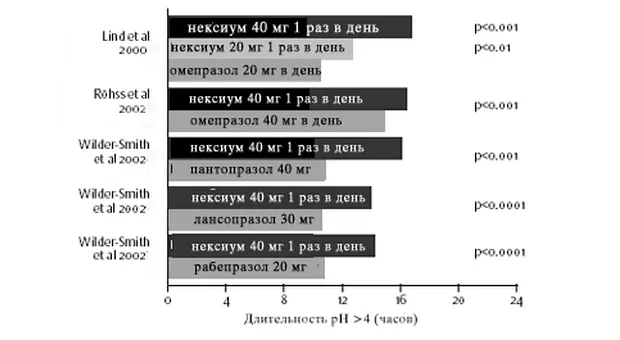
К представителям PPI относятся омепразол, пантопразол, рабепразол. Эти препараты имеют примерно одинаковую эффективность и короткий период полувыведения. Более эффективным и длительно действующим их аналогом является эзомепразол. Его рекомендуется применять при более тяжелых формах эзофагита [4].
Прокинетики
Эти лекарственные средства способствуют нормализации перистальтики пищевода и повышению тонуса нижнего пищеводного сфинктера. К ним относится домперидон, метаклопрамид, цизаприд. Они способствуют уменьшению рефлюкса и показывают хорошую эффективность в сравнении с плацебо [9, 18, 24]. Более того, последние исследования показали их хорошую эффективность и в сравнении с Н2-блокаторами. Сочетание же этих двух групп препаратов приводит к усилению действия обоих, но оно менее эффективно, чем PPI-терапия [31].
Проблемой прокинетиков является большое количество побочных эффектов. Это ограничивает применение этой группы препаратов. Кроме того, они не эффективны при тяжелых степенях эзофагита.
Helicobacter pylori и ГЭРБ
Вопрос о взаимосвязи хеликобактерной инфекции и рефлюкс эзофагита до сих пор остается открытым. ГЭРБ не является показанием к назначению эрадикационной терапии. Ряд исследователей утверждают, что НР оказывает протективную роль для пищевода [10, 28, 30]. Другие же исследования выявили увеличение числа атрофического эзофагита и метаплазии, ассоциированное с хеликобактерной инфекцией и лечением PPI [3, 13, 16]. Целесообразность эрадикационной терапии при ГЭРБ не доказана [15].
Новые препараты
Миорелаксант центрального действия баклофен в исследованиях показал положительное влияние на тонус нижнего пищеводного сфинктера. Он повышает базальное давление и уменьшает количество спонтанных расслаблений кардии [11]. Препарат оказался более эффективным в сравнении с плацебо для лечения ГЭРБ [5], но опыта его применения недостаточно для того, чтобы делать окончательные выводы.
Терапевтическая тактика
Существуют два подхода к терапии ГЭРБ: step-up и step-down. Первый предусматривает назначение щадящих методов вначале, а затем применение более эффективных способов терапии. Второй – начало лечения с наиболее эффективных препаратов и дозировок с последующем уменьшением до поддерживающего режима. Более предпочтителен второй вариант.
Терапевтическая тактика выглядит следующим образом:
- PPI в стандартной дозировке до 4 недель или в тяжелых случаях до 8 недель;
- При неэффективности – переход на максимальную дозу PPI или замена на эзомепразол до 10 дней;
- При неэффективности – высокие дозы Н2-блокаторов [17] в сочетании с прокинетиками под контролем рН-метрии;
- При неэффективности – хирургические методы лечения;
- При эффективности терапии – снижение дозировок до минимальных.
Поддерживающее лечение
Поддерживающая терапия включает в себя длительное применение минимально эффективных доз PPI [2]. В тех случаях, когда эти препараты были изначально неэффектитвны, рекомендуется поддерживающее лечение с помощью гистаминовых блокаторов. Также важно помнить о диете и коррекции стиля жизни.
Таким образом, ГЭРБ – часто встречающееся заболевание. Золотым стандартом его диагностики является эзофагоскопия, но нормальная эндоскопическая картина не исключает диагноз. Важное значение имеет наличие симптомов заболевания. Для лечения ГЭРБ используют разные группы препаратов, но наиболее эффективными и безопасными на данный момент являются блокаторы протонной помпы.
Вывод:
Список литературы:
- Пиманов И.С. Эзофагит, гастрит и язвенная болезнь. Н. Новгород 2000.
- Antonson CW, Robinson MG, Hawkins TM, et al. High doses of histamine antagonists do not prevent relapses of peptic esophagitis following therapy with a proton pump inhibitor. Gastroenterology 1990;98:A16.
- Berstad AE, Hatlebakk FG, Maartmann-Moe H, et al. Helicobacter pylori, gastritis and epithelial cell proliferation in patients with reflux oesophagitis after treatment with omeprazole. Gut 1997;41:735-739
- Castell DO, Kahrilas PJ, Richter JE, Vakil NB, Johnson DA, Zuckerman S et al. Esomeprazole (40 mg) compared with lansoprazole (30 mg) on the treatment of erosive esophagitis. Am J Gastroenterol 2002;97:575-83.
- Ciccaglione AF, Bartolacci S, Marzio L. Effects of one month treatment with GABA agonist baclofen on gastro-esophageal reflux and symptoms in patients with gastro-esophageal reflux disease. Gastroenterology. 2002;122:A-196.
- Dent J, et al. An evidence-based appraisal of reflux disease management the Genval Workshop Report. Gut 1998;44(Suppl 2):S1-S16 ( April ).
- DeVault K, Castell D and The Practice Parameters Committee of the American College of Gastroenterology. Updated Guidelines for the Diagnosis and Treatment of Gastroesophageal Reflux Disease. Am J Gastroenterol 1999;94:1434-1442.
- Fass R. Epidemiology and pathophysiology of symptomatic gastroesophageal reflux disease. Am J Gastroenterol.
- Galmiche JP, Fraitag B, Filoche B, et al. Double-blind comparison of cisapride and cimetidine in treatment of reflux esophagitis. Dig Dis Sci 1990;35:649-55.
- Haruma K, Mihara M, Kawaguchi H, et al. Low prevalence of Helicobacter pylori infection in patients with reflux oesophagitis [abstract]. Gastroenterology 1996;110:A130.
- Holloway RH. GABA-B receptors and control of gastrointestinal motility. In: AGA Research Symposium: GABA-B receptor agonists as novel treatments of reflux disorders. Program and abstracts of Digestive Disease Week 2002; May 19-22, 2002; San Francisco, California.
- Koehler RE, Weymean PJ, Oakley HF. Single- and double-contrast techniques in esophagitis. AJR 1980;135:15-9.
- Kuipers EJ, Lundell L, Klinkenberg-Knoll EC, et al. Atrophic gastritis and Helicobacter pylori infection in patients with reflux oesophagitis treated with omeprazole or fundoplication. N Engl J Med 1996;334:1018-1022.
- Labenz J, Malfertheiner P. Helicobacter pylori in gastro-oesophageal reflux disease: causal agent, independent or protective factor? Gut 1997;41:277-280.
- Laine L; Sugg J Effect of Helicobacter pylori eradication on development of erosive esophagitis and gastroesophageal reflux disease symptoms: a post hoc analysis of eight double blind prospective studies. Am J Gastroenterol 2002 Dec;97(12):2992-7 (ISSN: 0002-9270).
- Lamberts R, Creutzfeldt W, Struber HG, et al. Long term omeprazole therapy in peptic ulcer disease: gastrin, endocrine cell growth and gastritis. Gastroenterology 1993;104:1356-1370.
- Leite LP, Just RJ, Castell DO, et al. Control of gastric acid with high dose H2-receptor antagonists after omeprazole failure: Report of two cases. Am J Gastroenterol 195;90:1874-7.
- Lepoutre L, Van der Spek P, Vanderlinden I, et al. Healing of grade-II and III oesophagitis through motility stimulation with cisapride. Digestion 1990;45:109-14.
- Lind T, Rydberg L, Kylebдck A, Jonsson A, Andersson T, Hasselgren G et al. Esomeprazole provides improved acid control vs. omeprazole in patients with symptoms of gastro-oesophageal reflux disease. Aliment Pharmacol Ther 2000;14:861-7.
- Lundell L, Havu N, Andersson A, et al. Gastric atrophy development and acid supression therapy revisited. Result of a randomised clinical study with long term follow up [abstract]. Gastroenterology 1997;112:A28.
- Mann SG, Murakami A, McCarroll K, et al. Low dose famotidine in the prevention of sleep disturbance caused by heartburn after an evening meal. Aliment Pharmacol Ther 1995;9:395-401.
- Ott DJ, Wu WC, Gelfand DW. Reflux esophagitis revisited: Prospective analysis of radiological accuracy. Gastrointest Radiol 1981;6:1-7. Koehler RE, Weymean PJ, Oakley HF. Single- and double-contrast techniques in esophagitis. AJR 1980;135:15-9.
- Ott DJ, Chen YM, Gelfand DW, et al. Analysis of a multiphasic radiographic examination for detecting reflux esophagitis. Gastrointest Radiol 1986;11:1-6.
- Richter JE, Long JF. Cisapride for gastroesophageal reflux disease: A placebo-controlled, double-blind study. Am J Gastroenterol 1995;90:423-30.
- Robinson M, Yale J Biol Med 1999 Mar-Jun;72(2-3):169-72 (ISSN: 0044-0086).
- Rоhss K, Hasselgren G, Hedenstrцm H. Effect of esomeprazole 40 mg vs omeprazole 40 mg on 24-hour intragastric pH in patients with symptoms of gastroesophageal reflux disease. Dig Dis Sci 2002;47:954-8.
- Saco LS, Orlando RC, Levinson SL, et al. Double-blind controlled trial of bethanecol and antacid versus placebo and antacid in the treatment of erosive esophagitis. Gastroenterology 1982;82:1369-73.
- Sehiguchi T, Shirota T, Horikoshi T, et al. Helicobacter pylori infection and severity of reflux oesophagitis [abstract]. Gastroenterology 1996;110:A755.
- Tew S, Jamieson GG, Pilowski I, et al. The illness behavior of patients with gastroesophageal reflux disease with and without endoscopic esophagitis. Dis Esophagus 1997;10:9-15.
- Vicari JJ, Peek RM, Falk GW, et al. The seroprevalence of cag A-positive Helicobacter pylori strains in the spectrum of gastro-oesophageal reflux disease. Gastroenterology 1998;115:50-57.
- Vigneri S, Termini R, Leandro G, et al. A comparison of five maintenance therapies for reflux esophagitis. N Engl J Med 1995;333:1106-10.
- Werdmuller BFM, Loffeld RJLF. Helicobacter pylori infection has no role in the pathogenesis of reflux esophagitis. Dig Dis Sci 1997;42:103-105. 135.
- Wilder-Smith C, Rцhss K, Lundin C, Rydholm H. Esomeprazole 40 mg provides more effective acid control than pantoprazole 40 mg. J Gastroenterol Hepatol 2002;17 Suppl:A784.
- Wilder-Smith C, Rоhss K, Claar-Nilsson C, Lundin C. Esomeprazole 40 mg provides faster and more effective acid control than lansoprazole 30 mg in patients with symptoms of gastroesophageal reflux disease. Gastroenterology 2002;122 4 Suppl 1:A200.
- Wilder-Smith C, Claar-Nilsson C, Hasselgren G,Rоhss K. Esomeprazole 40 mg provides faster and more effective acid control than rabeprazole 20 mg in patients with symptoms of GERD. J Gastroenterol Hepatol 2002;17 Suppl:A612.
Статьи по теме
Рекомендуемые статьи
При эндоскопическом исследовании в случае бронхоэктазов в стадии ремиссии выявляется
частично диффузный бронхит I степени воспаления
Активируйте PUSH уведомления в браузер
Отключите PUSH уведомления в браузер
Содержание
Интернет магазин
Популярное
- О нас
- Правовые вопросы
- Политика
обработки персональных
данных EndoExpert.ru - Связаться с нами
- Стать партнером
© 2016-2022 EndoExpert.ru

Вы находитесь в разделе предназначенном только для специалистов (раздел для пациентов по ссылке). Пожалуйста, внимательно прочитайте полные условия использования и подтвердите, что Вы являетесь медицинским или фармацевтическим работником или студентом медицинского образовательного учреждения и подтверждаете своё понимание и согласие с тем, что применение рецептурных препаратов, обращение за той или иной медицинской услугой, равно как и ее выполнение, использование медицинских изделий, выбор метода профилактики, диагностики, лечения, медицинской реабилитации, равно как и их применение, возможны только после предварительной консультации со специалистом. Мы используем файлы cookie, чтобы предложить Вам лучший опыт взаимодействия. Файлы cookie позволяют адаптировать веб-сайты к вашим интересам и предпочтениям.
Я прочитал и настоящим принимаю вышеизложенное, хочу продолжить ознакомление с размещенной на данном сайте информацией для специалистов.















.jpg)




.png)














Комментарии